Область, к которой относится изобретение
Настоящее изобретение относится к новым пиридазинам, к способам их получения, к содержащим их фармацевтическим композициям и к их применению в терапии, в частности, при лечении и/или профилактике заболеваний и нарушений, опосредованных аутотаксином.
Предпосылки создания изобретения
Аутотаксин (ATX; ENPP2) представляет собой секретируемый фермент, ответственный за гидролиз лизофосфатидилхолина (LPC) до биоактивного липида лизофосфатидовой кислоты (LPA) за счет его активности лизофосфолипазы D. В свою очередь, LPA проявляет свои эффекты посредством взаимодействия с шестью GPCR (рецепторы LPA 1-6, LPAR1-6) (Houben AJ, 2011). Передача сигналов ATX-LPA была задействована, например, в ангиогенезе, хроническом воспалении, аутоиммунных заболеваниях, фиброзных заболеваниях, прогрессировании рака и метастазировании опухолей. Например, LPA, действуя на LPAR1, индуцирует миграцию, пролиферацию и дифференцировку фибробластов легких; модулирует функцию эпителиального и эндотелиального барьеров; и способствует апоптозу эпителиальных клеток легких (Budd, 2013). Было показано, что ингибирование АТХ, делеция гена LPAR1 и селективные антагонисты LPAR1 эффективны на доклинических моделях фиброза легких и кожи (Tager AM, 2008; Swaney J, 2010, Casetelino FV, 2016).
У пациентов с идиопатическим фиброзом легких (ИФЛ) уровни LPA в жидкости бронхоальвеолярного лаважа повышены (Tager и соавт., 2008, Nat. Med.), а в фиброзной ткани легких человека были обнаружены повышенные концентрации ATX. (Oikonomou и соавт., 2012, AJRCMB). Уровни LPA повышены в конденсате выдыхаемого воздуха у субъектов с ИФЛ (Montesi и соавт., 2014_ВМСРМ), а уровень LPC повышен в 2 раза в сыворотке у стабильных пациентов с ИЛФ (Rindlisbacher и соавт., 2018, Resp. Res.).
Следовательно, повышенные уровни АТХ и/или повышенные уровни LPA, измененная экспрессия рецептора LPA и измененные ответы на LPA могут влиять на ряд патофизиологических состояний, связанных с передачей сигналов ATX-LPA.
Интерстициальные заболевания легких (ILD) характеризуются воспалением и фиброзом интерстиция, ткани и пространства между воздушными мешочками легкого (du Bois, Nat. Rev. Drug Discov. 2010, 9, 129-140). ILD может возникнуть, когда повреждение легких вызывает ненормальную реакцию на заживление. Таким образом, ILD также включают в себя прогрессирующие фиброзирующие интерстициальные заболевания легких (PFILD), при которых реакция на повреждение легких становится прогрессирующей, самоподдерживающейся и независимой от исходной клинической ассоциации или триггера. Наиболее заметными PF-ILD являются идиопатический легочный фиброз (IPF) и системный склероз-ILD (SSc-ILD).
IPF представляет собой хроническое фиброзное необратимое и в конечном итоге смертельное заболевание легких, характеризующееся прогрессирующим фиброзом интерстиция легких, который приводит к уменьшению объема легких и прогрессирующей легочной недостаточности. IPF также характеризуется специфическим гистопатологическим паттерном, известным как обычная интерстициальная пневмония (UIP) (Raghu и соавт, Am. J. Respir. Crit. Care Med. 183: 788-824).
Системный склероз (SSc), также называемый склеродермией, представляет собой иммуноопосредованное ревматическое заболевание сложной этиологии. Это мультиорганное гетерогенное заболевание, характеризующееся обширным фиброзом, васкулопатией и аутоантителами против различных клеточных антигенов с высокой смертностью. Оно представляет собой редкое заболевание, орфанное заболевание со значительной неудовлетворенной медицинской потребностью. Ранние клинические признаки SSc могут быть разными. На ранних стадиях заболевания часто проявляются синдром Рейно и гастроэзофагеальный рефлюкс (Rongioletti F, и соавт., J Eur Acad Dermatol Venereol 2015; 29: 2399-404). У некоторых пациентов наблюдаются воспалительные заболевания кожи, отекшие и опухшие пальцы рук, скелетно-мышечное воспаление или такие конституциональные проявления, как утомляемость. Избыточное отложение коллагена в коже пациентов делает кожу толстой и жесткой. У некоторых пациентов наблюдаются органные проявления заболевания, такие как фиброз легких, легочная артериальная гипертензия, почечная недостаточность или желудочно-кишечные осложнения. Кроме того, одним из наиболее распространенных проявлений иммунного вовлечения является наличие аномальных уровней аутоиммунных антител к ядру собственных клеток (антиядерных антител или ANA), которые наблюдаются почти у всех с SSc (Guiducci S и соавт., Isr Med Assoc J 2016; 18: 141-43). ILD и легочная артериальная гипертензия (РАН) являются наиболее частыми причинами смерти пациентов с SSc (Tyndall AJ и соавт. Ann Rheum Dis 2010; 69: 1809-15).
Пациентов с SSc подразделяют на две основные подгруппы заболеваний: диффузный кожный системный склероз и ограниченный кожный системный склероз (LeRoy ЕС, и соавт., J Rheumatol 1988; 15:202-5). Три клинических признака - чрезмерный фиброз (рубцевание), васкулопатия и аутоиммунитет - по-видимому, лежат в основе процессов, которые приводят к различным проявлениям, характерным для SSc. В настоящее время SSc рассматривают как проявление нерегулируемого или дисфункционального восстановления соединительной ткани до повреждения (Denton CP и соавт., Lancet 2017; 390: 1685-99).
Поэтому желательно обеспечить сильнодействующие ингибиторы АТХ.
Обзор ингибиторов АТХ различных структурных классов приведен у D. Castagna и соавт. (J. Med. Chem. 2016, 59, 5604-5621). В заявке WO 2014/139882 раскрыты соединения, которые являются ингибиторами АТХ, имеющие обобщенную структурную формулу:
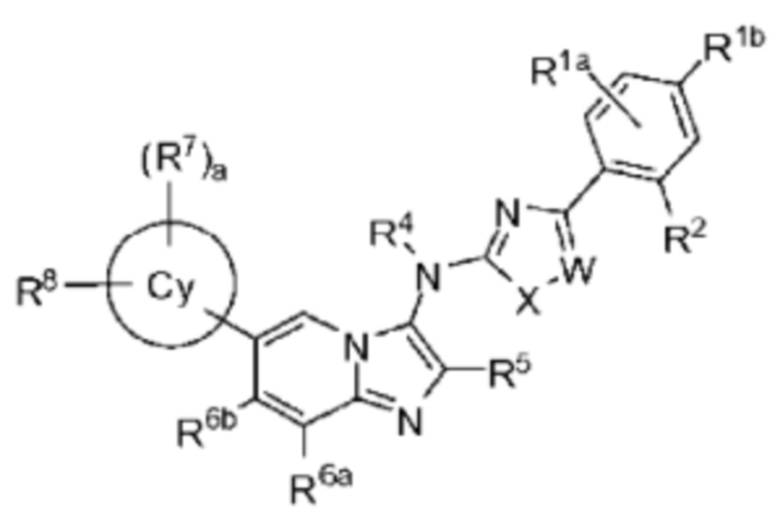 .
.
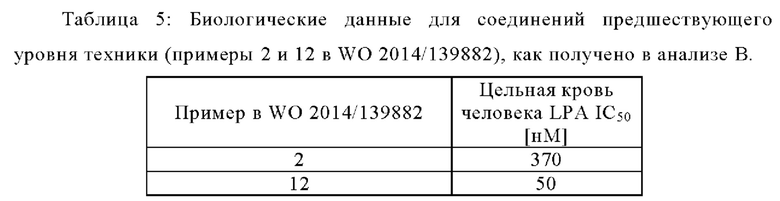
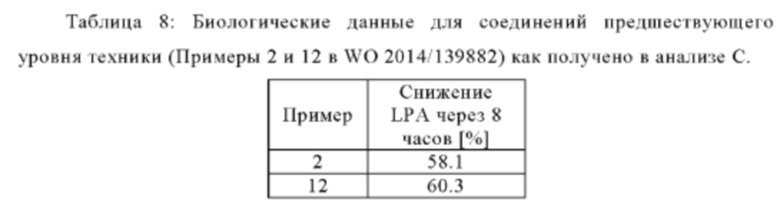
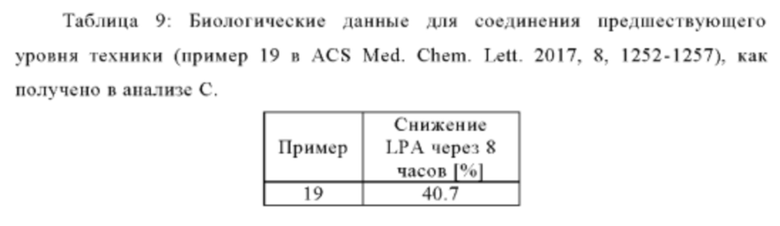
Пример 2 там дополнительно описан у N. Desroy, и соавт. (J. Med. Chem. 2017, 60, 3580-3590 как пример 11) в качестве первого в своем классе ингибитора АТХ, проходящего клиническую оценку для лечения идиопатического легочного фиброза. У С. Kutruff, и соавт. (ACS Med. Chem. Lett. 2017, 8, 1252-1257) раскрыт ингибитор ATX BI-2545 (пример 19), который значительно снижает уровни LPA in vivo.
Подробное описание изобретения
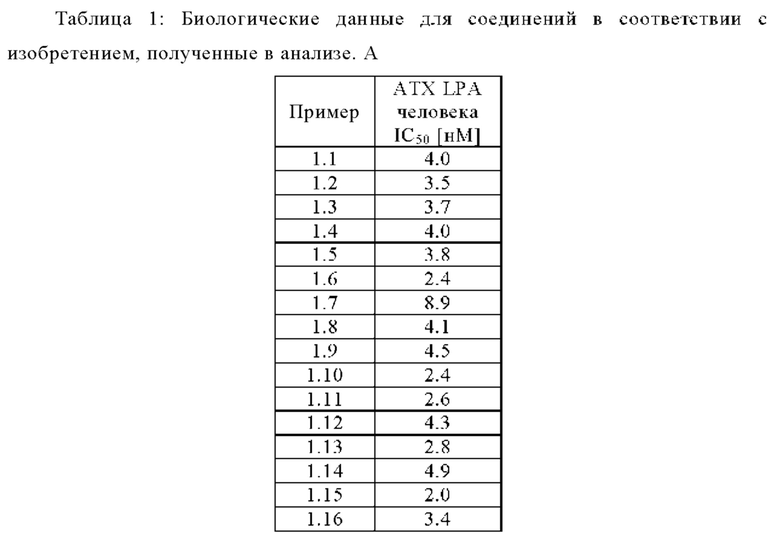
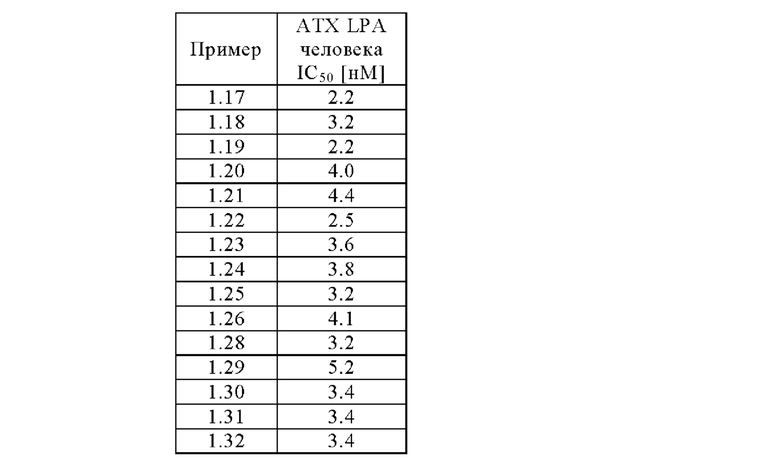
Настоящее изобретение относится к новым пиридазинам, которые неожиданно являются сильными ингибиторами аутотаксина (Анализ А), которые дополнительно характеризуются:
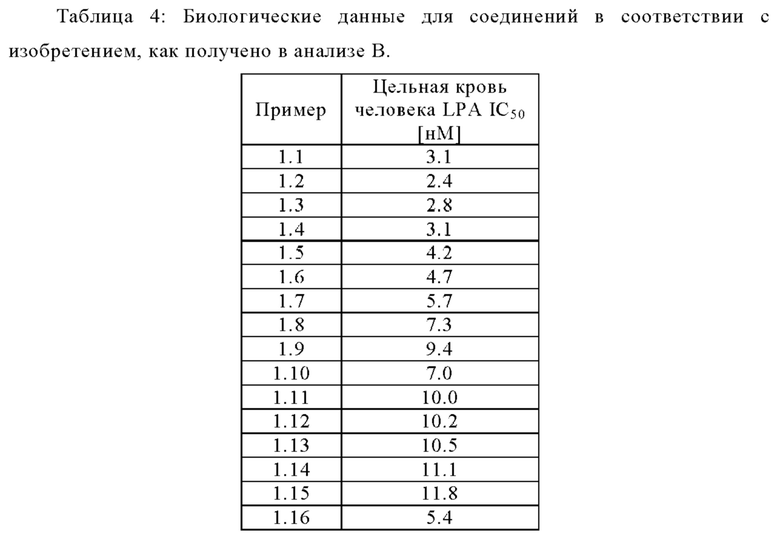
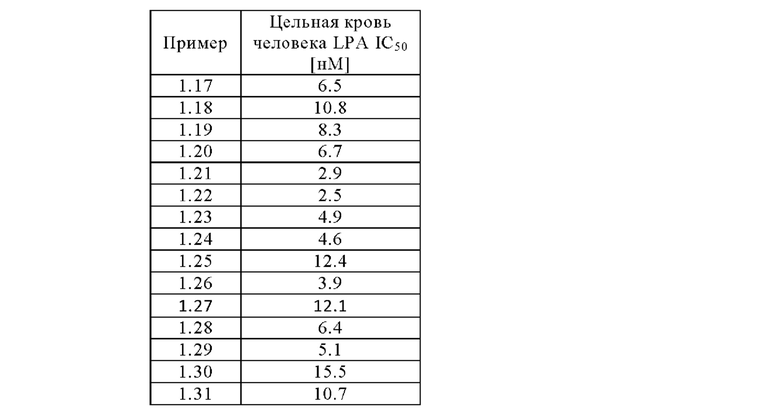
- высокой эффективностью в цельной крови человека (Анализ В) и
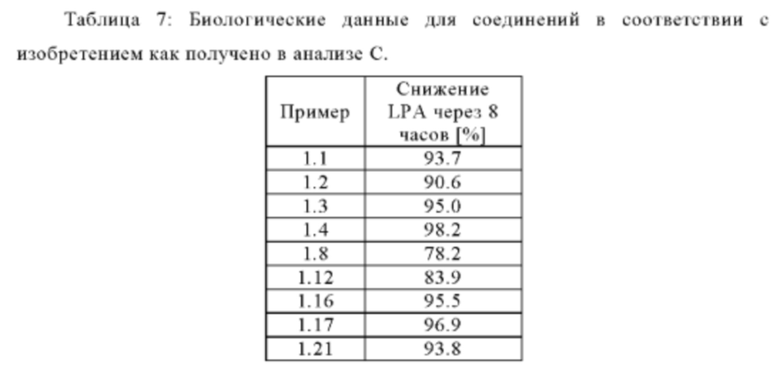
- существенным снижением уровней концентрации LPA в плазме in vivo в течение нескольких часов (Анализ С).
Соединения в соответствии с настоящим изобретением пригодны в качестве средств для лечения или профилактики заболеваний или состояний, в которых участвует активность АТХ и/или передача сигналов LPA, вовлечены в этиологию или патологию заболевания или иным образом связаны по меньшей мере с одним симптом болезни. Передача сигналов ATX-LPA задействована, например, в ангиогенезе, хроническом воспалении, аутоиммунных заболеваниях, фиброзных заболеваниях, прогрессировании рака и метастазировании опухоли.
Соединения в соответствии с изобретением превосходят соединения, раскрытые в предшествующем уровне техники, с точки зрения комбинации следующих параметров:
- активность в качестве ингибиторов АТХ,
- активность в качестве ингибиторов АТХ в цельной крови человека,
- снижение уровней концентрации LPA в плазме in vivo в течение нескольких часов.
АТХ представляет собой растворимый белок плазмы, который активен в гепаринизированной цельной крови. Его субстрат LPC имеет высокую избыточность, его концентрация находится в диапазоне мкм. Таким образом, анализ цельной крови при физиологических концентрациях субстрата является весьма актуальным анализом, позволяющим прогнозировать эффективность ингибиторов АТХ in vivo.
Снижение LPA in vivo определяют путем измерения концентрации LPA в плазме после перорального введения соединений в соответствии с настоящим изобретением. LPA представляет собой очень сильный биоактивный липид, который эффективно активирует нисходящие пути через LPA-рецепторы 1-6 в зависимости от концентрации. Выраженную и стойкую блокировку образования LPA посредством ингибирования АТХ оценивают путем измерения степени уменьшения LPA через 8 часов после введения дозировки соединения. Таким образом, сильное снижение уровня LPA в плазме через 8 часов свидетельствует об эффективности и устойчивой продолжительности действия in vivo, а также об устойчивом целевом воздействии на рецепторы LPA.
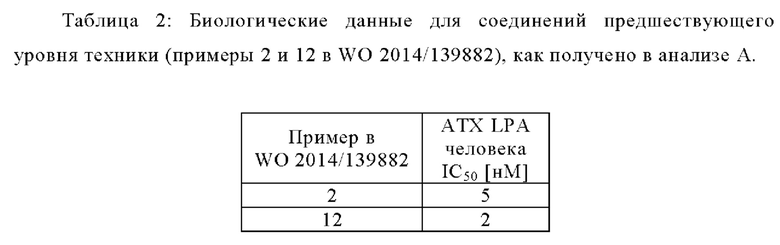
Соединения в соответствии с настоящим изобретением структурно отличаются от примеров 2 и 12 в заявке WO 2014/139882 и примера 19 в ACS Med. Chem. Lett. 2017, 8, 1252-1257 тем, что они содержат центральное пиридазиновое ядро с заместителями в 3- и 6-положениях. Это структурное различие неожиданно приводит к превосходной комбинации (i) ингибирования АТХ, (ii) ингибирования АТХ в цельной крови человека и (iii) снижения уровней концентрации LPA в плазме in vivo в течение нескольких часов.
Следовательно, соединения в соответствии с настоящим изобретением демонстрируют высокое взаимодействие с мишенью in vivo, и можно ожидать, что они будут иметь более высокую эффективность у людей.
Настоящее изобретение обеспечивает новые соединения в соответствии с формулой (I)
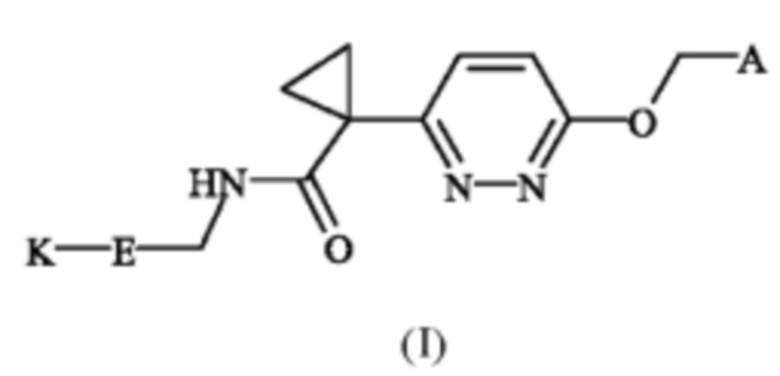
в которой
А представляет собой пиридил, замещенный одним или двумя членами группы, включающей в себя фтор и F1-7-фтор-С1-3-алкил;
Е выбран из группы, включающей в себя фенил и пиридил, необязательно выбранный из одного или двух членов группы, включающей в себя фтор и F1-7-фтор-С1-3-алкил;
K выбран из группы, включающей в себя
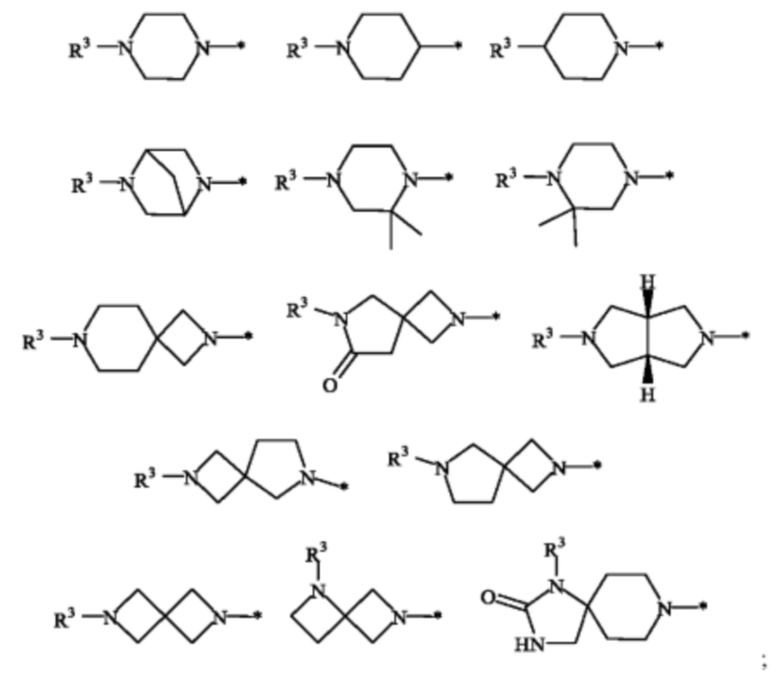
R3 выбран из группы, включающей в себя R4(O)C-, метил и
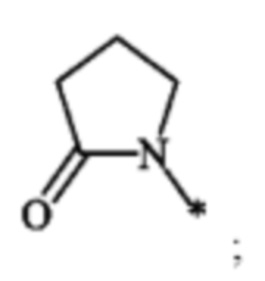
R4 представляет собой метил.
Другой вариант осуществления настоящего изобретения относится к соединению формулы (I), в которой А представляет собой пиридил, замещенный одним или двумя из F1-3-фтор-С1-алкила; и заместители Е и K определены как в предыдущем варианте осуществления.
Другой вариант осуществления настоящего изобретения относится к соединению формулы (I), в которой А представляет собой пиридил, замещенный одним или двумя членами группы, включающей в себя F2HC и F3C; и заместители Е и K определены как в предыдущем варианте осуществления.
Другой вариант осуществления настоящего изобретения относится к соединению формулы (I), в которой А выбран из группы, включающей в себя
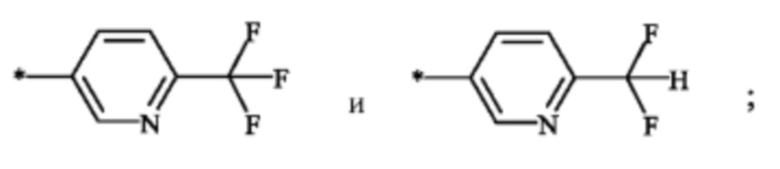
и заместители Е и K определены как в любом из предыдущих вариантов осуществления.
Другой вариант осуществления настоящего изобретения относится к соединению формулы (I), в которой Е выбран из группы, включающей в себя фенил и пиридил, необязательно выбранный из одного или двух членов группы, включающей в себя F и F3C;
и заместители А и K определены как в любом из предыдущих вариантов осуществления.
Другой вариант осуществления настоящего изобретения относится к соединению формулы (I), в которой Е выбран из группы, включающей в себя
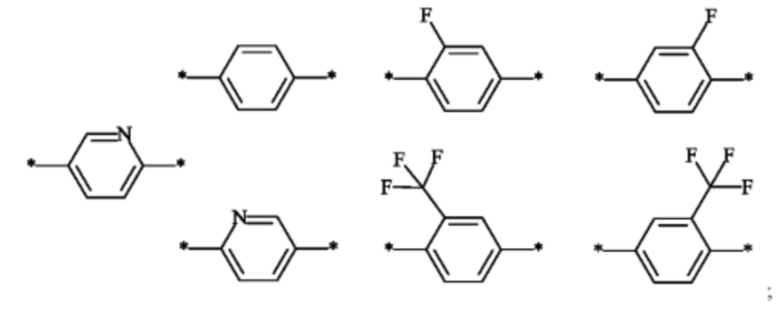
и заместители А и K определены как в любом из предыдущих вариантов осуществления.
Предпочтительным является соединение формулы (I), в соответствии с настоящим изобретением, выбранное из группы, включающей в себя
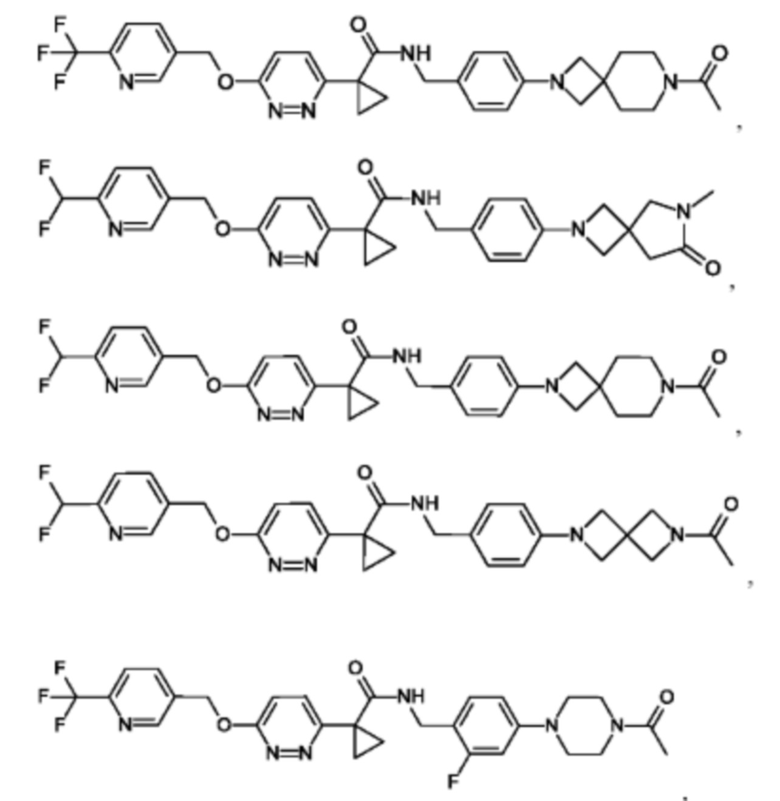
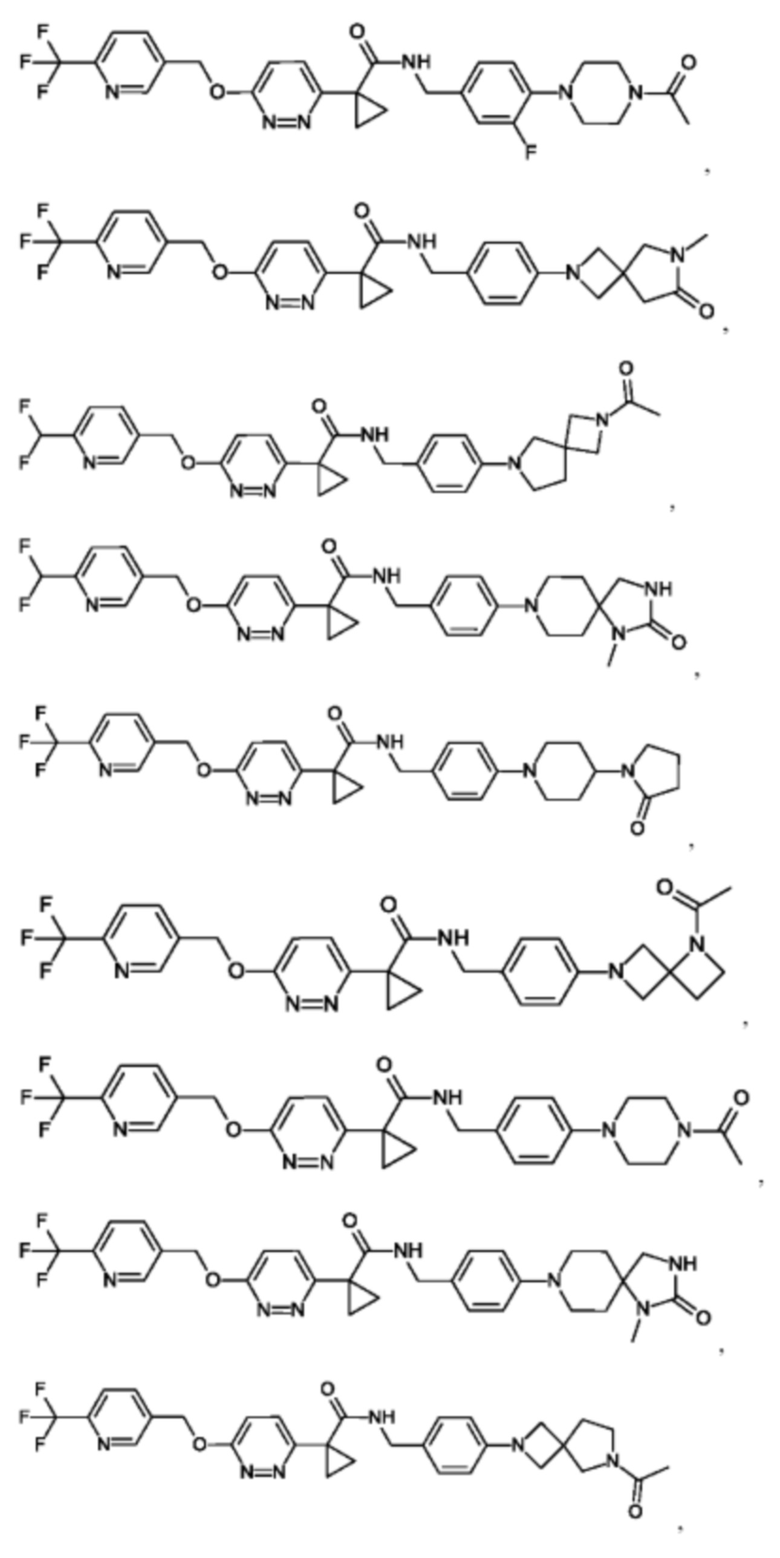
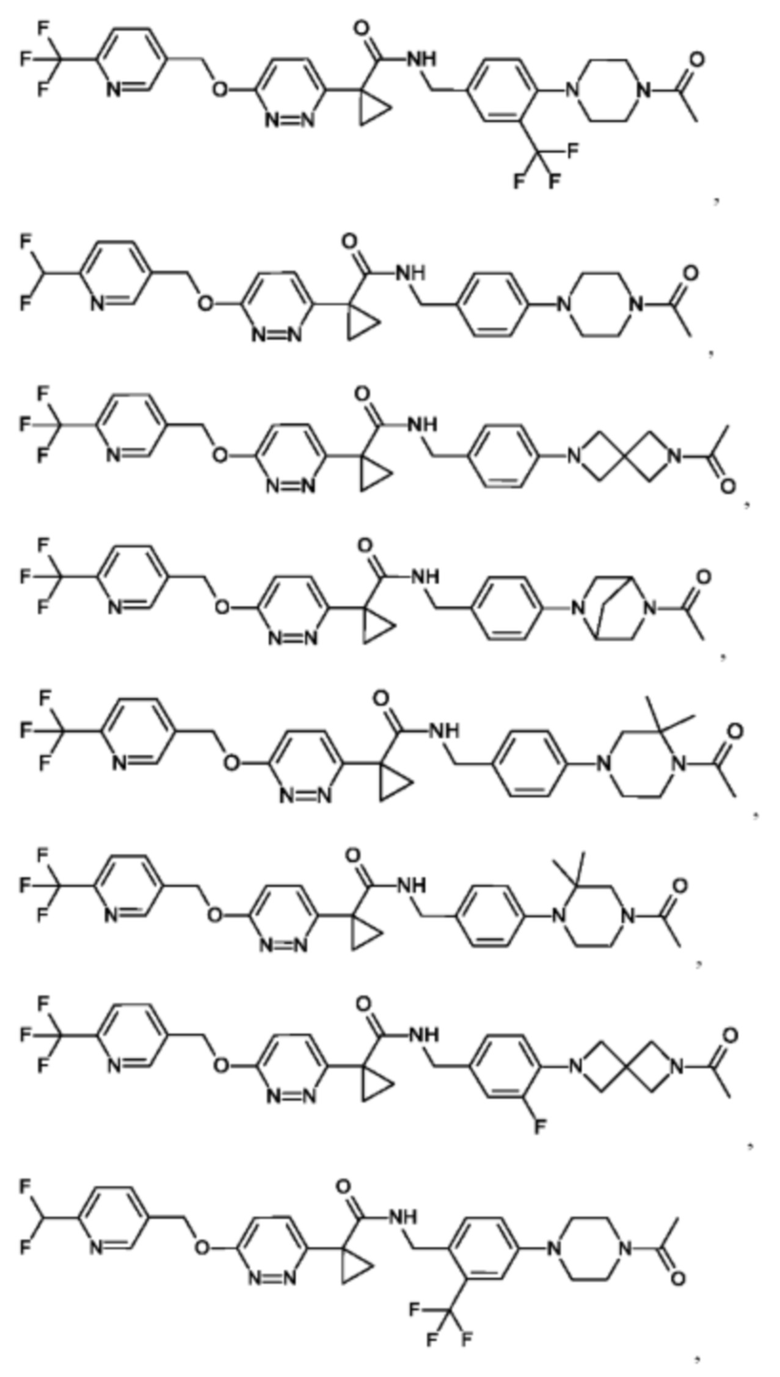
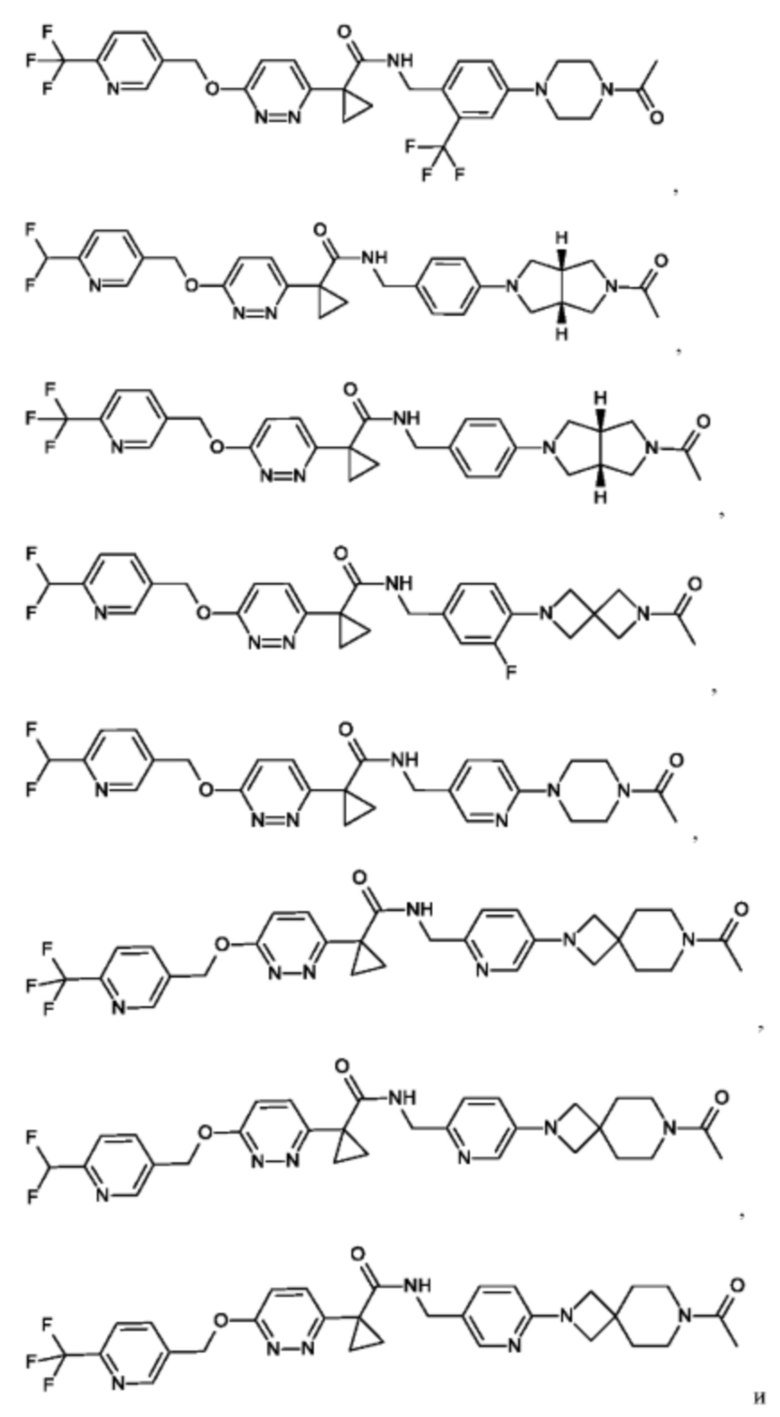
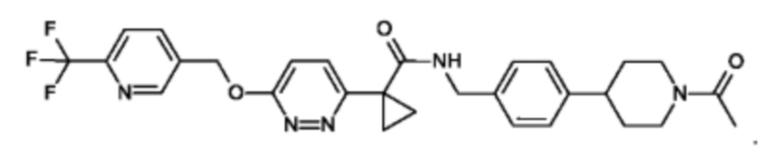
Другой вариант осуществления относится к фармацевтической композиции, содержащей по меньшей мере одно соединение формулы I в соответствии с настоящим изобретением или его фармацевтически приемлемую соль и одно или несколько фармацевтически приемлемых вспомогательных веществ.
Другой вариант осуществления относится к соединению формулы (I) в соответствии с настоящим изобретением, для применения в качестве лекарственного средства.
Используемые термины и определения
Терминам, не определенным в настоящей заявке конкретно, следует придавать значения, которые им придавал бы специалист в данной области в свете раскрытия и контекста. Однако при использовании в описании, если не указано иное, следующие термины имеют указанное значение, и соблюдаются следующие соглашения.
В группах, радикалах или фрагментах, определенных ниже, количество атомов углерода часто указано перед группой, например, С1-6-алкил означает алкильную группу или радикал, имеющий от 1 до 6 атомов углерода. Как правило, в таких группах, как НО, H2N, (O)S, (O)2S, NC (циано), HOOC, F3C или т.п., специалист в данной области техники может увидеть точку (точки) присоединения радикала к молекуле по свободным валентностям самой группы. Для комбинированных групп, содержащих две или большее количество подгрупп, последняя названная подгруппа представляет собой точку присоединения радикала, например, заместитель «арил-С1-3-алкил» означает арильную группу, которая связана с С1-3-алкильной группой, последний из которых связан с ядром или с группой, к которой присоединен заместитель.
В случае, если соединение в соответствии с настоящим изобретением представлено в форме химического названия и в виде формулы, в случае любого расхождения преимущественную силу имеет формула. Звездочка может быть использована в подформулах для обозначения связи, которая связана с основной молекулой, как определено.
Нумерация атомов заместителя начинается с атома, ближайшего к ядру или группе, к которой присоединен заместитель.
Например, термин «3-карбоксипропильная группа» представляет собой следующий заместитель:
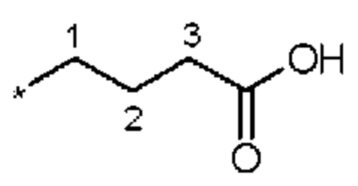
где карбокси-группа присоединена к третьему атому углерода пропильной группы. Термины «1-метилпропильная», «2,2-диметилпропильная» или «циклопропилметильная» группа представляют собой следующие группы:
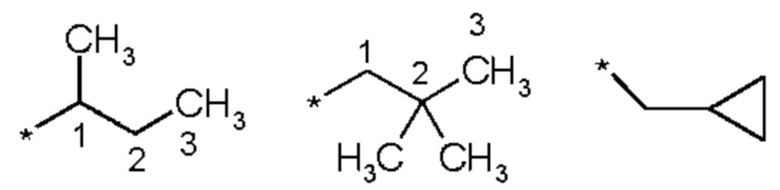
Звездочка может быть использована в подформулах для обозначения связи, которая связана с основной молекулой, как определено.
Используемый в настоящей заявке термин «замещенный» означает, что любой один или несколько атомов водорода в указанном атоме замещены атомами, выбранными из указанной группы, при условии, что нормальная валентность указанного атома не превышена, и что замещение приводит к стабильному соединению.
Термин «C1-n-алкил», где n представляет собой целое число, выбранное из 2, 3, 4, 5 или 6, предпочтительно 4 или 6, либо отдельно, либо в сочетании с другим радикалом означает ациклический, насыщенный, разветвленный или линейный углеводородный радикал с от 1 до n атомов С. Например термин С1-5-алкил охватывает радикалы Н3С-, Н3С-СН2-, Н3С-СН2-СН2-, Н3С-CH(СН3)-, Н3С-СН2-СН2-СН2-, Н3С-СН2-СН(СН3)-, Н3С-СН(СН3)-СН2-, Н3С-С(СН3)2-, Н3С-СН2-СН2-СН2-СН2-, Н3С-СН2-СН2-СН(СН3)-, Н3С-СН2-СН(СН3)-СН2-, Н3С-СН(СН3)-СН2-СН2-, Н3С-СН2-С(СН3)2-, Н3С-С(СН3)2-СН2-, Н3С-СН(СН3)-СН(СН3)- и Н3С-СН2-СН(СН2СН3)-.
Термин «галоген» означает хлор, бром, йод и фтор. Под термином «галоген», добавленным к «алкильной», «алкиленовой» или «циклоалкильной» группе (насыщенной или ненасыщенной), понимается такая алкильная или циклоалкильная группа, в которой один или несколько атомов водорода заменены атомом галогена, выбранным из числа фтора, хлора или брома, предпочтительно фтора и хлора, особенно предпочтительным является фтор. Примеры включают в себя: H2FC-, HF2C-, F3C-.
Термин фенил относится к радикалу следующего кольца
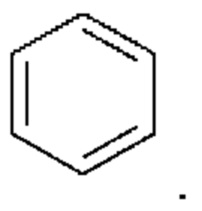
Термин пиридинил относится к радикалу следующего кольца
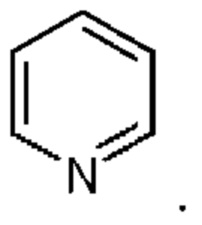
Термин пиридазин относится к следующему кольцу
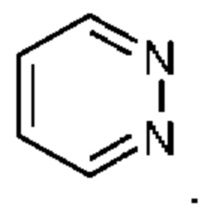
Если конкретно не указано, то в описании и прилагаемой формуле изобретения, приведенная химическая формула или название должны охватывать таутомеры и все стерео-, оптические и геометрические изомеры (например, энантиомеры, диастереомеры, E/Z-изомеры и т.д.) и их рацематы, а также их смеси в различных пропорциях отдельных энантиомеров, смеси диастереомеров или смеси любых из вышеуказанных форм, где такие изомеры и энантиомеры существуют, а также соли, включая их фармацевтически приемлемые соли и их сольваты, такие как, например, гидраты, включая сольваты свободных соединений или сольваты соли соединения.
Как правило, по существу чистые стереоизомеры могут быть получены в соответствии с принципами синтеза, известными специалисту в данной области, например, разделением соответствующих смесей, используя стереохимически чистые исходные вещества и/или путем стереоселективного синтеза. Из уровня техники известно, как получить оптически активные формы, например, путем разделения рацемических форм или путем синтеза, например, исходя из оптически активных исходных веществ и/или с использованием хиральных реагентов.
Энантиомерно чистые соединения в соответствии с настоящим изобретением или промежуточные соединения могут быть получены посредством асимметричного синтеза, например, путем получения и последующего разделения соответствующих диастереомерных соединений или промежуточных соединений, которые могут быть разделены известными способами (например, хроматографическим разделением или кристаллизацией) и/или путем использования хиральных реагентов, таких как хиральные исходные вещества, хиральные катализаторы или хиральные вспомогательные вещества.
Кроме того, специалисту в данной области известно, как получить энантиомерно чистые соединения из соответствующих рацемических смесей, например, путем хроматографического разделения соответствующих рацемических смесей на хиральных неподвижных фазах; или путем разделения рацемической смеси с использованием подходящего разделяющего агента, например, посредством образования диастереомерной соли рацемического соединения с оптически активными кислотами или основаниями, последующим разделением солей и высвобождением желаемого соединения из соли; или путем дериватизации соответствующих рацемических соединений оптически активными хиральными вспомогательными реагентами с последующим разделением диастереомеров и удалением хиральной вспомогательной группы; или путем кинетического разделения рацемата (например, путем ферментативного разделения); энантиоселективной кристаллизацией из конгломерата энантиоморфных кристаллов в подходящих условиях; или путем (фракционной) кристаллизации из подходящего растворителя в присутствии оптически активного хирального вспомогательного вещества.
Фраза «фармацевтически приемлемый» использована в настоящей заявке для обозначения тех соединений, материалов, композиций и/или дозированных форм, которые, в рамках здравого медицинского заключения, подходят для использования в контакте с тканями людей и животных без чрезмерной токсичности, раздражения, аллергической реакции или других проблем или осложнений и соизмеримы с разумным соотношением польза/риск.
Используемый в настоящей заявке термин «фармацевтически приемлемая соль» относится к производным описанных соединений, в которых исходное соединение образует соль или комплекс с кислотой или основанием.
Примеры кислот, образующих фармацевтически приемлемую соль с исходным соединением, содержащим основную группу, включают в себя минеральные или органические кислоты, такие как бензолсульфоновая кислота, бензойная кислота, лимонная кислота, этансульфоновая кислота, фумаровая кислота, гентизиновая кислота, бромистоводородная кислота, соляная кислота, малеиновая кислота, яблочная кислота, малоновая кислота, миндальная кислота, метансульфоновая кислота, 4-метилбензолсульфоновая кислота, фосфорная кислота, салициловая кислота, янтарная кислота, серная кислота и винная кислота.
Примеры катионов и оснований, образующих фармацевтически приемлемую соль с исходным соединением, содержащим кислотный фрагмент, включают в себя Na+, K+, Са2+, Mg2+, NH4+, L-аргинин, 2,2'-иминобисэтанол, L-лизин, N-метил-D-глюкамин или трис(гидроскиметил)-аминометан.
Фармацевтически приемлемые соли в соответствии с настоящим изобретением можно синтезировать из исходного соединения, которое содержит основной или кислотный фрагмент, обычными химическими способами. Как правило, такие соли могут быть получены взаимодействием свободных кислотных или основных форм этих соединений с достаточным количеством подходящего основания или кислоты в воде или в органическом разбавителе, таком как эфир, этилацетат, этанол, изопропанол или ацетонитрил, или их смесь.
Соли других кислот, кроме упомянутых выше, которые, например, применимы для очистки или выделения соединений в соответствии с настоящим изобретением (например, трифторацетатных солей), также составляют часть настоящего изобретения.
Биологические анализы
Биологическую активность соединений определяли следующими методами:
Анализ А: биохимический анализ АТХ
5 нМ рекомбинантного АТХ (Cayman Chemicals) добавляли к 50 мМ буфера Tris (рН 8.0), содержащего 3 мМ KCl, 1 мМ CaCl2, 1 мМ MgCl2 0,14 мМ NaCl, и 0,1% бычий сывороточный альбумин. Исследуемые соединения растворяли в ДМСО и тестировали в диапазоне от 0,1 нМ до 10 мкМ. Ферментативную реакцию (22,5 мкл) запускали добавлением 2,5 мкл 10 мкМ 18:1 LPC (Avanti Lipids, Алабастер, Алабама, США). После 2-часовой инкубации при комнатной температуре реакцию останавливали добавлением 20 мкл воды, содержащей 500 нМ 20:4 LPA в качестве внутреннего стандарта и 100 мкл 1-бутанола для экстракции LPA. Затем планшеты центрифугировали при 4000 об/мин, 4°С, в течение 2 мин. Полученную верхнюю бутанольную фазу непосредственно использовали для впрыска в систему RapidFire (Agilent).
Автоматический пробоотборник RapidFire был соединен с бинарным насосом (Agilent 1290) и Triple Quad 6500 (ABSciex, Торонто, Канада). Эта система была оборудована петлей на 10 мкл, 5-мкл картриджем Waters Atlantis HILIC (Waters, Elstree, UK), 90% ацетонитрилом, содержащим 10 мМ цетата аммония в качестве элюента А и 40% ацетонитрила, содержащего 10 мМ цетата аммония в качестве элюента В. Подробнее см. (Bretschneider и соавт., SLAS Discovery, 2017). МС работала в отрицательном режиме с температурой источника 550°С, завесным газом=35, газом 1=65, и газом 2=80. Были определены следующие переходы и параметры МС (DP: потенциал декластеризации и СЕ: столкновение энергии) для соответствующих LPA: 18:1 LPA при 435.2/152.8, DP=-40, СЕ=-28 и 20:4 LPA при 457.2/152.8, DP=-100, СЕ=-27).
За образованием 18:1 LPA наблюдали и оценивали как отношение к 20:4 LPA.

Анализ В: анализ АТХ цельной крови
К 45 мкл цельной крови человека добавляли 5 мкл исследуемого соединения, растворенного в фосфатно-солевом буфере (диапазон концентраций 0,12 нМ-100 мкМ). Эту смесь инкубировали в течение 1 ч при 37°С и останавливали добавлением 100 мкл 40 мМ динатрий гидрофосфатного буфера, содержащего 30 мМ лимонной кислоты (рН 4) и 1 мкМ 17:0 LPA (внутренний стандарт). LPA экстрагировали добавлением 500 мкл 1-бутанола с последующим 10-минутным центрифугированием при 4000 об/мин, 4°С. Из полученного органического супернатанта аликвоту 200 мкл переносили в 96-луночный планшет и переносили на измерение МС/МС на основе RapidFire.
Автоматический пробоотборник RapidFire был соединен с бинарным насосом (Agilent 1290) и Triple Quad 6500 (ABSciex, Торонто, Канада). Эта система была оснащена петлей на 10 мкл, 5-мкл картриджем Waters Atlantis HILIC (Waters, Elstree, UK), 90% ацетонитрилом, содержащим 10 мМ ацетата аммония в качестве элюента А и 40% ацетонитрилом, содержащим 10 мМ ацетата аммония в качестве элюента В. Подробнее см. (Bretschneider и соавт., SLAS Discovery, 2017, 22, 425-432). МС работала в отрицательном режиме с температурой источника 550°С, завесным газом=35, газом 1=65 и газом 2=80. Были определены следующие переходы и параметры МС (DP: потенциал декластеризации и СЕ: энергия столкновения) для соответствующих LPA: 18:2 LPA при 433.2/152.8, DP=-150, СЕ=-27 и 17:0 LPA при 423.5/152.8, DP=100.
За образованием 18:2 LPA наблюдали и оценивали как отношение к 17:0 LPA.

Анализ С: in vivo
Исследуемое вещество растворяли в 0,5% натрозоле с добавлением 0,015% Tween 80 для перорального применения крысам в дозе 5 мг/кг. Образцы крови собирали перед введением соединения и через 8 часов после нанесения на лед с использованием EDTA в качестве коагулирующего средства. Затем плазму готовили центрифугированием и хранили до анализа при -20°С.
LPA из образцов плазмы экстрагировали с использованием процедуры, описанной у Scherer и соавт. (Clinical chemistry 2009, 55, 1218-22). 35 мкл гепаринизированной плазмы смешивали с 200 мкл 40 мМ динатрий гидрофосфатного буфера, содержащего 30 мМ лимонной кислоты (рН 4) и 1 мкМ 17:0 LPA (внутренний стандарт). Затем добавляли 500 мкл бутанола и энергично встряхивали в течение 10 мин. После этого образцы центрифугировали при 4000 об/мин, 4°С, в течение 10 мин. 500 мкл органической верхней фазы переносили в свежий 96-луночный планшет и упаривали в слабом потоке азота 15 фунтов на квадратный дюйм в течение 45 минут. Полученный остаток растворяли в 100 мкл этанола перед анализом ЖХ-МС.
Метод ЖХ-МС для анализа образцов in vivo
Triple Quad 6500 (ABSciex, Торонто, Канада) был оснащен системой ЖХ Agilent 1290 (Agilent, Санта-Клара, Калифорния), автоматическим пробоотборником СТС и ЖХ колонкой Atlantis 50×2.1-мм, 3-мкМ HILIC (Waters, Elstree, UK). Элюент А содержал 0,2% муравьиной кислоты и 50 мМ формиата аммония в воде, тогда как элюент В состоял из 0,2% муравьиной кислоты в ацетонитриле. Градиент ЖХ начинался с 95% растворителя В и снижался в течение 1,5 мин до 75% и в течение 0,2 мин. до 50% растворителя В с дальнейшим увеличением скорости потока с 500 до 700 мкл⋅мин-1. На 1,8 мин концентрация растворителя В снова устанавливалась на 95% и оставалась постоянной в течение 0,7 мин для повторного уравновешивания колонки. Наблюдали следующие виды LPA (DP: потенциал декластеризации и СЕ: энергия столкновения): 16:0 LPA при 409.2/152.8, DP=150, СЕ=28; 18:0 LPA при 437.3/152.8, DP=-60, СЕ=-28; 18:1 LPA при 435.2/152.8, DP=-40, СЕ=-28; 18:2 LPA при 433.2/152.8, DP=-150, СЕ=-28; 20:4 LPA при 457.2/152.8, DP=-100, СЕ=-29 и 17:0 LPA при 423.5/152.8, DP=-100, СЕ=-36.
Истощение LPA в процентах рассчитывали на основе базовых уровней LPA до применения исследуемого соединения. Сумма LPA относится к видам 16:0; 18:0; 18:1; 18:2 и 20:4
Способ лечения
Настоящее изобретение относится к соединениям общей формулы (I), которые пригодны для предупреждения и/или лечения заболевания и/или состояния, связанного с или модулируемого посредством АТХ и/или биологической активностью LPA, включая, но не ограничиваясь лечением и/или предупреждением воспалительных состояний, фиброзных заболеваний, заболеваний дыхательной системы, почек, печени, сосудов и сердечнососудистых заболеваний, рака, глазных состояний, метаболических состояний, холестатического и других форм хронического зуда, острого и хронического отторжения трансплантата органов и заболеваний нервной системы.
Соединения общей формулы (I) пригодны для предупреждения и/или лечения воспалительных состояний, включая, помимо прочего, синдром Шегрена, артрит, остеоартрит, рассеянный склероз, системную красную волчанку, воспалительное заболевание кишечника, воспалительные заболевания дыхательных путей, такие как хроническая обструктивная болезнь легких (ХОБЛ) и хроническая астма; фиброзные заболевания, включая, помимо прочего, интерстициальные заболевания легких (ILD), включая прогрессирующие фиброзирующие интерстициальные заболевания легких (PFILD), такие как идиопатический фиброз легких (IPF) и SSC-ILD, семейные интерстициальные заболевания легких, фиброз миокарда и сосудов, фиброз почек, фиброз печени, фиброз легких, фиброз кожи, коллагеновые сосудистые заболевания, включая системный склероз (SSc) и инкапсулирующий перитонит; заболевания дыхательной системы, включая, помимо прочего, диффузные паренхиматозные заболевания легких различной этиологии, включая ятрогенный фиброз, вызванный лекарственными средствами, профессиональный фиброз и/или фиброз, вызванный окружающей средой, системные заболевания и васкулиты, гранулематозные заболевания (саркоидоз, гиперчувствительная пневмония), почечные заболевания, включая, но не ограничиваясь острым повреждением почек и хроническим заболеванием почек с протеинурией и без нее, включая терминальную стадию почечной недостаточности (ESRD, фокальный сегментарный гломерулярный склероз, IgA нефропатию, васкулиты/системные заболевания, а также острое и хроническое отторжение трансплантата почки; заболевания печени, включая, помимо прочего, цирроз печени, застой в печени, холестатическое заболевание печени, включая зуд, первичный билиарный холангит, неалкогольный стеатогепатит и острое и хроническое отторжение трансплантата печени; сосудистые заболевания, включая, помимо прочего, атеросклероз, тромботические сосудистые заболевания, а также тромботические микроангиопатии, пролиферативную артериопатию (как например, набухшие миоинтимальные клетки, окруженные слизистым внеклеточным матриксом и узелковое утолщение), эндотелиальную дисфункцию; сердечно-сосудистые заболевания, включая, помимо прочего, острый коронарный синдром, ишемическую болезнь сердца, инфаркт миокарда, артериальную и легочную гипертензию, сердечную аритмию, такую как фибрилляция предсердий, инсульт и другие сосудистые поражения; рак и метастазы рака, включая, помимо прочего, рак молочной железы, рак яичников, рак легких, рак предстательной железы, мезотелиому, глиому, карциному печени, рак желудочно-кишечного тракта и их прогрессирование и метастатическую агрессивность; глазные заболевания, включая, но не ограничиваясь ими, пролиферативную и непролиферативную (диабетическую) ретинопатию, сухую и влажную форму возрастной макулярной дегенерации сетчатки (AMD), макулярный отек сетчатки, окклюзия центральной артерии/вен, травматическое повреждение, глаукома; метаболические состояния, включая, помимо прочего, ожирение, дислипидемию и диабет; состояния нервной системы, включая, помимо прочего нейропатическую боль, болезнь Альцгеймера, шизофрению, нейровоспаление (например, астроглиоз), периферические и/или вегетативные (диабетические) невропатии.
Соответственно, настоящее изобретение относится к соединению общей формулы (I) для применения в качестве лекарственного средства.
Кроме того, настоящее изобретение относится к применению соединения общей формулы (I) для лечения и/или предотвращения заболевания и/или состояния, связанного с или модулируемого посредством АТХ и/или биологической активностью LPA.
Помимо этого, настоящее изобретение относится к применению соединения общей формулы (I) для лечения и/или предотвращения заболевания и/или состояния, связанного с или модулируемого посредством АТХ и/или биологической активностью LPA, включая, но не ограничиваясь воспалительными состояниями, фиброзными заболеваниями, состояниями дыхательной системы, состояниями почек, состояниями печени, сосудистыми и сердечно-сосудистыми состояниями, раком, заболеваниями глаз, метаболическими состояниями, холестатическими и другими формами хронического зуда, а также острыми и хроническими отторжениями трансплантата и состояниями нервной системы.
Кроме того, настоящее изобретение относится к применению соединения общей формулы (I) для лечения и/или предотвращения воспалительных состояний, включая, но не ограничиваясь этим, синдром Шегрена, артрит, остеоартрит, множественный склероз, системную красную волчанку, воспалительное заболевание кишечника, воспалительные заболевания дыхательных путей, такие как хроническая обструктивная болезнь легких (ХОБЛ) и хроническая астма; фиброзные заболевания, включая, но не ограничиваясь этим но не ограничиваясь этим (ILD), включая прогрессирующие фиброзирующие интерстициальные заболевания легких (PFILD), такие как идиопатический фиброз легких (IPF) и SSC-ILD, семейное интерстициальное заболевание легких, фиброз миокарда и сосудов, почечный фиброз, фиброз печени, легочный фиброз, фиброз кожи, коллагеновые сосудистые заболевания, включая системный склероз (SSc) и инкапсулирующий перитонит; состояния дыхательной системы, включая, помимо прочего, диффузные паренхиматозные заболевания легких различной этиологии, включая ятрогенный фиброз, вызванный лекарственными средствами, профессиональный фиброз и/или фиброз, вызванный окружающей средой, системные заболевания и васкулиты, гранулематозные заболевания (саркоидоз, гиперчувствительная пневмония), почечные заболевания, включая, помимо прочего, острое повреждение почек и хроническое заболевание почек с протеинурией и без нее, включая терминальную стадию почечной недостаточности (ESRD, очаговый сегментарный гломерулярный склероз, IgA-нефропатию, васкулиты/системные заболевания, а также острое и хроническое отторжение трансплантата почки; состояния печени, включая, но не ограничиваясь ими, цирроз печени, застой в печени, холестатическое заболевание печени, включая зуд, первичный билиарный холангит, неалкогольный стеатогепатит и острое и хроническое отторжение трансплантата печени; сосудистые состояния, включая, помимо прочего, атеросклероз, тромботическое сосудистое заболевание, а также тромботические микроангиопатии, пролиферативную артериопатию (как например, набухшие миоинтимальные клетки, окруженные муцинозным внеклеточным матриксом и узловым утолщением), эндотелиальную дисфункцию; сердечно-сосудистые состояния, включая, помимо прочего, острый коронарный синдром, ишемическую болезнь сердца, инфаркт миокарда, артериальную и легочную гипертензию, сердечную аритмию, такую как фибрилляция предсердий, инсульт и другие сосудистые поражения; рак и метастазы рака, включая, помимо прочего, рак молочной железы, рак яичников, рак легких, рак предстательной железы, мезотелиому, глиому, карциному печени, рак желудочно-кишечного тракта и их прогрессирование и метастатическую агрессивность; глазные заболевания, включая, но не ограничиваясь ими, пролиферативную и непролиферативную (диабетическую) ретинопатию, сухую и влажную форму возрастной макулярной дегенерации сетчатки (AMD), макулярный отек сетчатки, окклюзия центральной артерии/вен, травматическое повреждение, глаукома; метаболические состояния, включая, помимо прочего, ожирение, дислипидемию и диабет; состояния нервной системы, включая, помимо прочего нейропатическую боль, болезнь Альцгеймера, шизофрению, нейровоспаление, (например, астроглиоз), периферические и/или вегетативные (диабетические) невропатии.
В дополнительном аспекте настоящее изобретение относится к соединению общей формулы (I) для применения при лечении и/или предупреждении вышеупомянутых заболеваний и состояний.
В дополнительном аспекте настоящее изобретение относится к применению соединения общей формулы (I) для приготовления лекарственного средства для лечения и/или предупреждения вышеупомянутых заболеваний и состояний.
В дополнительном аспекте настоящего изобретения данное изобретение относится к способам лечения или предупреждения вышеупомянутых заболеваний и состояний, причем способ включает в себя введение эффективного количества соединения общей формулы (I) человеку.
Фармацевтические композиции
Пригодные препараты для введения соединений формулы (I) будут очевидны для специалистов в данной области и включают в себя, например, таблетки, пилюли, капсулы, суппозитории, таблетки для рассасывания, пастилки, растворы, сиропы, эликсиры, саше, инъекции, ингаляционные средства, порошки и т.д.
Пригодные таблетки могут быть получены, например, путем смешивания одного или нескольких соединений в соответствии с формулой I с известными вспомогательными веществами, например, инертными разбавителями, носителями, разрыхлителями, адъювантами, поверхностно-активными веществами, связующими веществами и/или смазывающими веществами.
Комбинированная терапия
Соединения в соответствии с настоящим изобретением можно комбинировать с другими вариантами лечения, которые, как известно, используют в данной области, так что для лечения показания, при котором настоящее изобретение применимо одновременно используют по меньшей мере два активных соединения в эффективных количествах. Хотя комбинированная терапия предпочтительно включает введение пациенту двух активных соединений одновременно, нет необходимости, чтобы эти соединения вводились пациенту в одно и то же время, хотя эффективные количества отдельных соединений будут присутствовать в организме пациента в одно и то же время. Соединения в соответствии с настоящим изобретением можно вводить с одним или несколькими составляющими комбинации, как иначе описано в настоящей заявке.
Соответственно, настоящее изобретение обеспечивает соединение формулы (I) в соответствии с любым из предыдущих вариантов осуществления, отличающееся тем, что соединение формулы (I) вводят в дополнение к лечению одной или несколькими противовоспалительными молекулами из списка, включающего в себя модуляторы IL6, модуляторы против IL6R и модуляторы IL13/IL-4 JAKi.
В соответствии с другим аспектом изобретение обеспечивает соединение формулы (I) в соответствии с любым из предыдущих вариантов осуществления, отличающееся тем, что соединение формулы (I) вводят в дополнение к лечению одной или несколькими антифиброзными молекулами из перечня, включающего в себя агонисты СВ2, модуляторы TGF, модуляторы FGFR, ингибиторы VEGFR, ингибиторы PDGFR, модуляторы FGF, модуляторы интегрина αvβ6, антитела против CTGF, ингибиторы ROCK2, rhPTX-2 (пентраксин-2), ингибиторы JNK1, ингибиторы LOXL2, ингибиторы галектина3, ингибиторы MK2, ингибиторы пути Wnt, ингибиторы TGFR, модуляторы PDE4, ингибиторы TRPA1 и модуляторы микроРНК.
В соответствии с другим аспектом настоящее изобретение относится к соединению формулы (I) в соответствии с любым из предыдущих вариантов осуществления, отличающемуся тем, что соединение формулы (I) вводят в дополнение к нинтеданибу.
В соответствии с другим аспектом настоящее изобретение относится к соединению формулы (I) в соответствии с любым из предыдущих вариантов осуществления, отличающемуся тем, что соединение формулы (I) вводят в дополнение к пирфенидону.
Получение
Соединения в соответствии с настоящим изобретением могут быть получены с использованием способов синтеза, которые известны специалисту в данной области и описаны в литературных источниках по органическому синтезу. Предпочтительно соединения получают аналогично способам получения, более подробно поясненным ниже, в частности, как описано в экспериментальном разделе.
Общие способы получения соединений по изобретению станут очевидны специалисту в данной области при изучении следующих схем. Исходные вещества могут быть получены способами, описанными в литературных источниках или в настоящей заявке, или могут быть получены аналогичным или сходным способом. Любые функциональные группы в исходных веществах или промежуточных соединениях могут быть защищены с использованием обычных защитных групп. Эти защитные группы могут быть снова отщеплены на подходящей стадии последовательности реакций с использованием методов, известных специалисту в данной области.
Соединения общей формулы (I) могут быть получены амидным сочетанием амина (VII) с кислотой (VI).
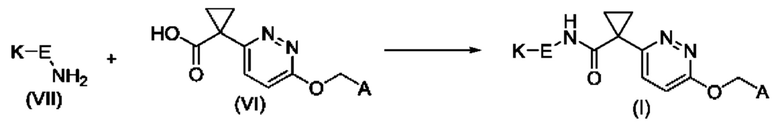
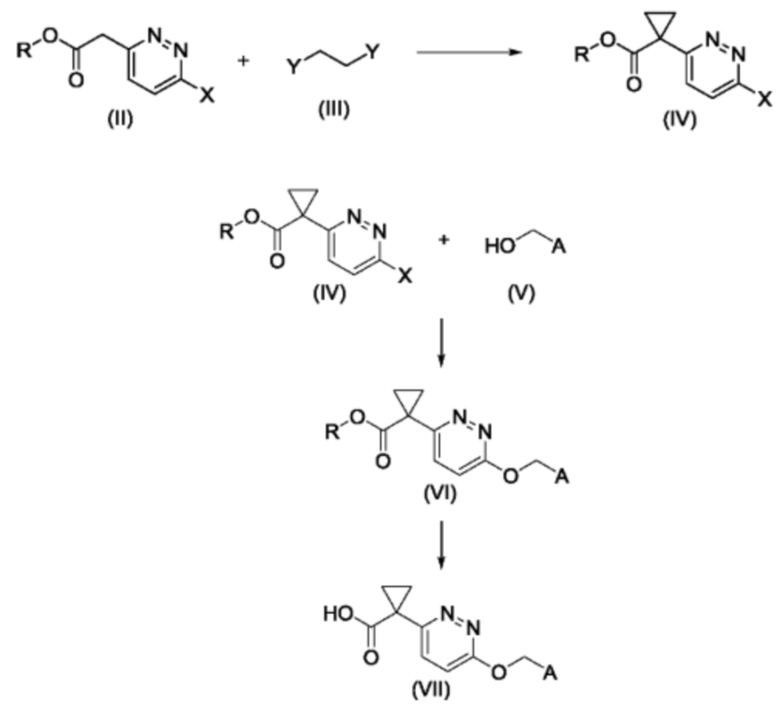
Кислоты (VII) получают путем омыления сложных эфиров (VI) (где R представляет собой пригодную кислотозащитную группу, такую как метил или этил). Сложные эфиры (VI) получают путем сочетания бензиловых спиртов (V) до получения галогенидов (IV) с использованием основания, где X представляет собой галоген, такой как Cl, Br или I. Сложные эфиры (IV) могут быть синтезированы путем алкилирования галогенпиридазинов (II) с алкилгалогенидами (III), где Y представляет собой галоген, такой как Cl, Br или йод.
Примеры
Экспериментальная часть
Приведенные ниже примеры предназначены для пояснения настоящего изобретения, не ограничивая его. Термины «температура окружающей среды» и «комнатная температура» используют взаимозаменяемо и обозначают температуру около 20°С.
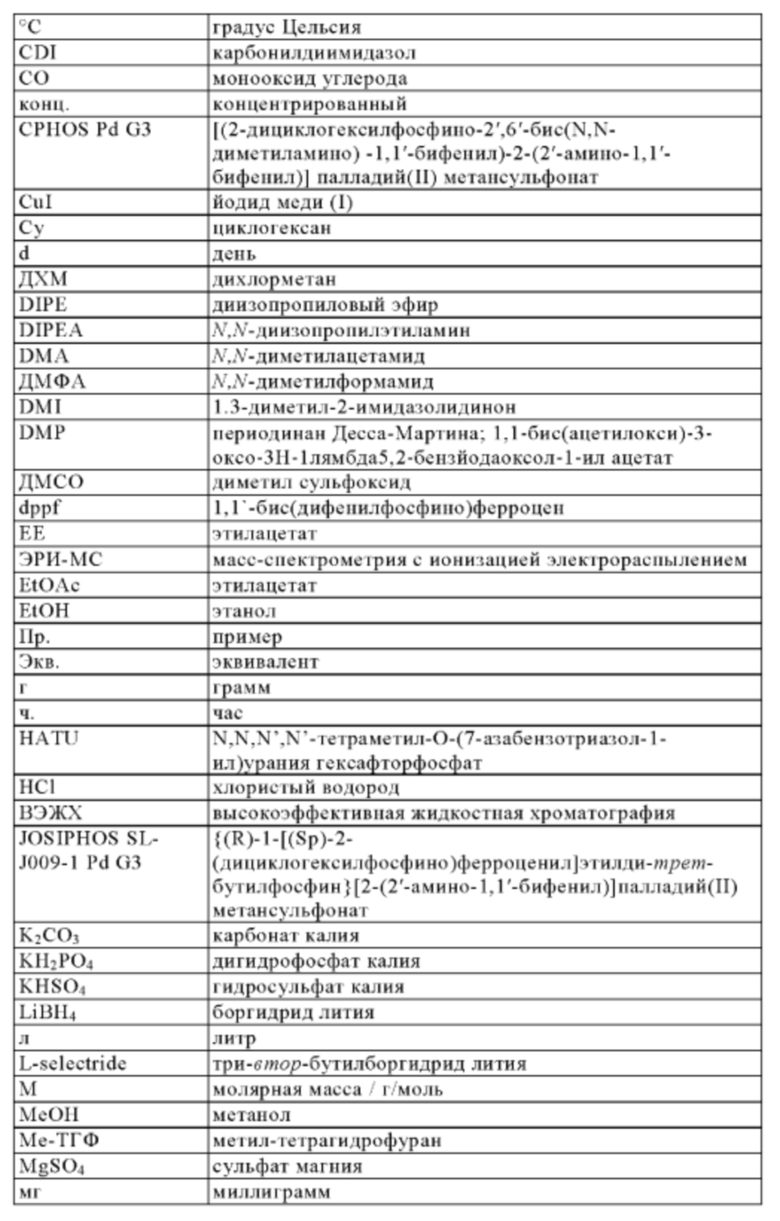
Сокращения:

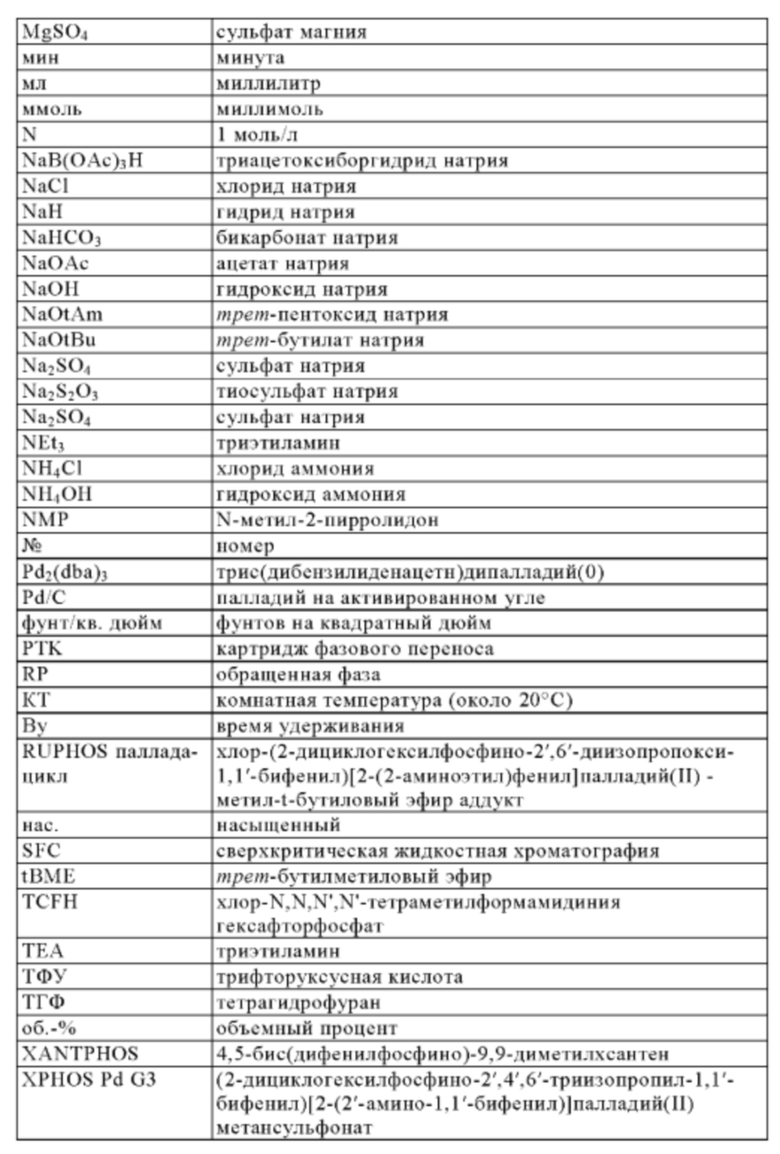
Получение исходных соединений
Пример I
Пример I.1
4-(4-Ацетилпиперазин-1-ил)-3-фторбензонитрил
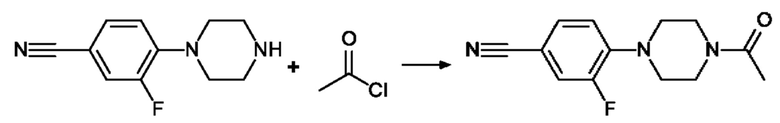
К раствору 0.40 г (1.95 ммоль) 3-фтор-4-пиперазин-1-ил-бензонитрила (CAS-№182181-38-0) и 0.60 мл (4.30 ммоль) триэтиламина в 7 мл ДХМ добавляют 0.14 мл (1.95 ммоль) ацетилхлорида, и смесь перемешивают при КТ в течение ночи. Реакционную смесь обрабатывают с помощью 0.09 мл (1.25 ммоль) триэтиламина и перемешивают при КТ в течение 2 ч. Органический слой промывают водой, сушат посредством PTK и растворитель выпаривают под сниженным давлением с получением 500 мг неочищенного продукта.
Следующие соединения получают по общей методике (пример I.1), описанной выше:
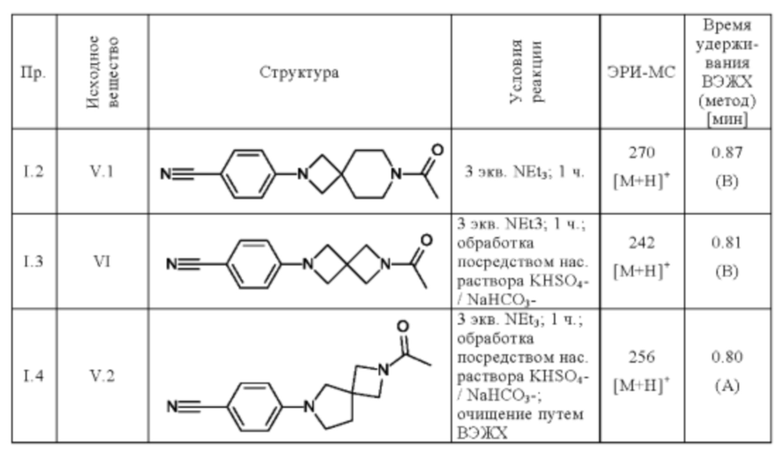
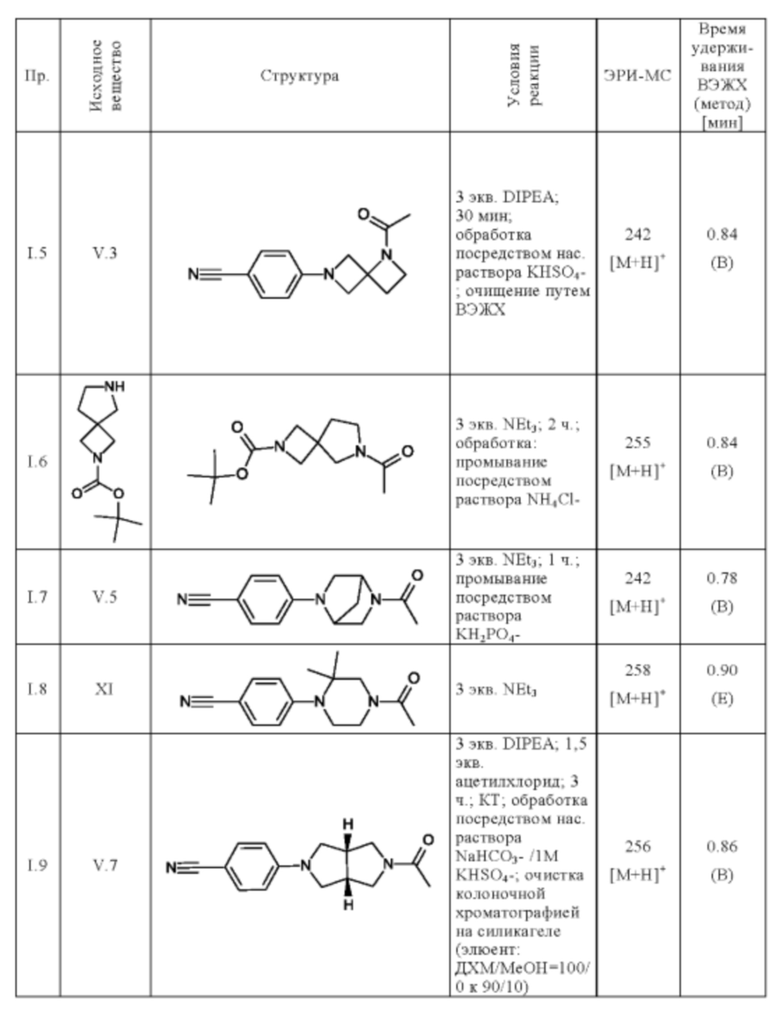
Пример 34
Пример II.1
1-{4-[4-(Аминометил)-2-фторфенил]пиперазин-1-ил}этан-1-он
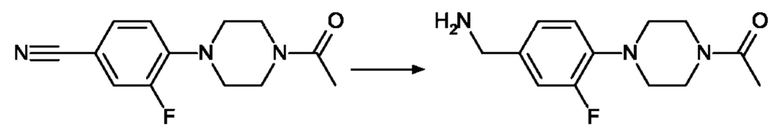
Смесь из 550 мг (2.22 ммоль) 4-(4-ацетилпиперазин-1-ил)-3-фторбензонитрила (пример I.1), 55.0 мг никеля Ренея, и 15 мл 7 N аммиака в МеОН перемешивают в атмосфере водорода (50 фунт/кв. дюйм) при 50°С в течение ночи, фильтруют и упаривают в вакууме с получением 510 мг продукта.
Следующие соединения получают по общей методике (пример II.1), описанной выше:
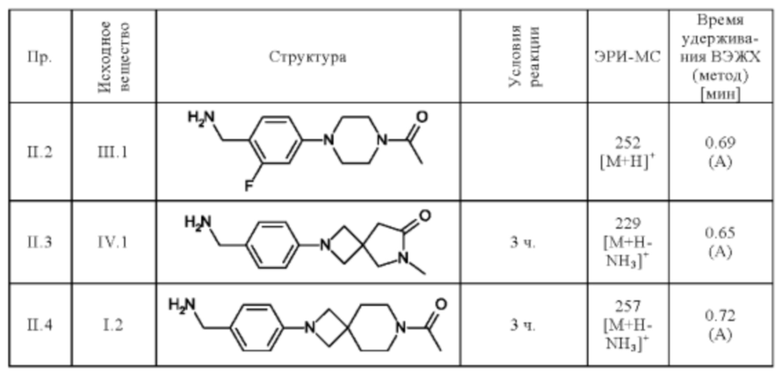
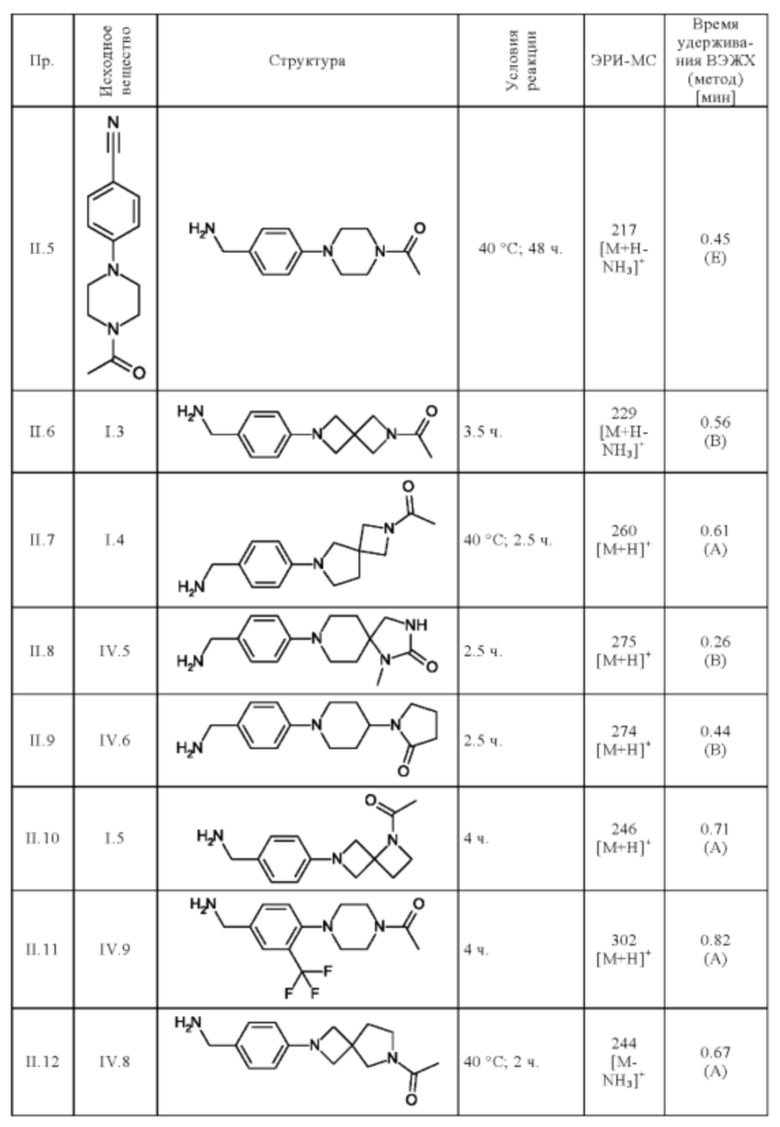
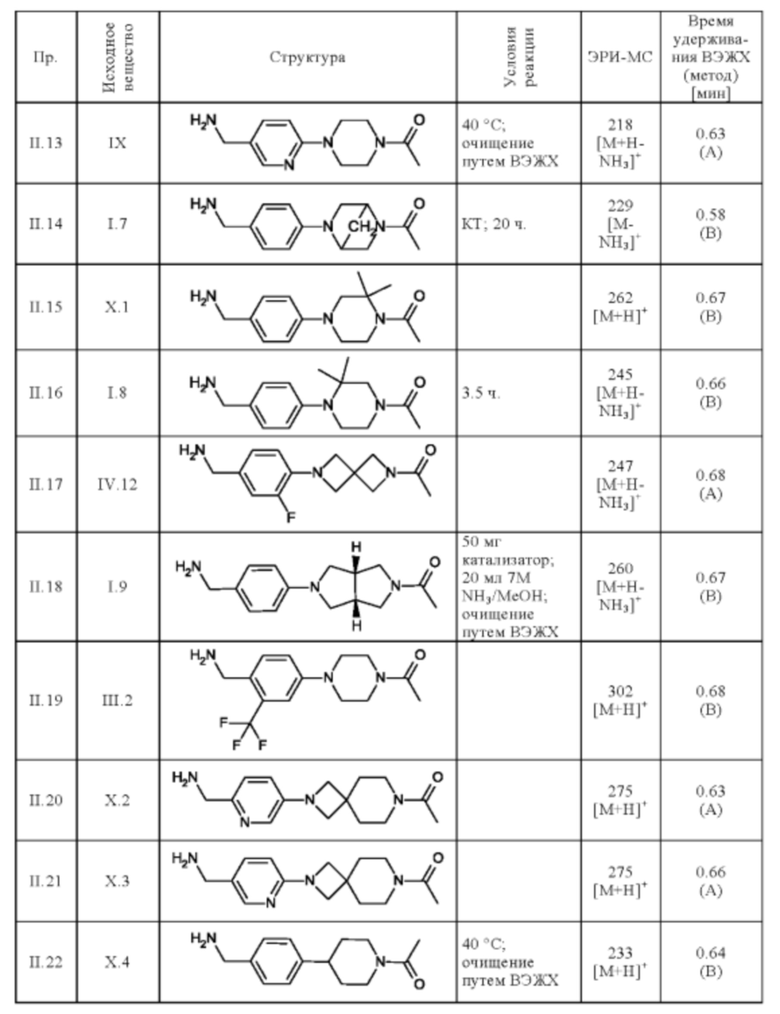
Пример 37
Пример III.1
4-(4-Ацетилпиперазин-1-ил)-2-фторбензонитрил
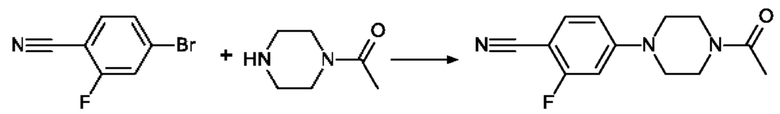
Смесь из 0,50 г (2.50 ммоль) 4-бром-2-фторбензонитрила (CAS-№105942-08-3), 0.32 г (2.50 ммоль) 1-(пиперазин-1-ил)этан-1-она (CAS №13889-98-0), 1.63 г (5.00 ммоль) карбоната цезия и 0,05 г (0.06 ммоль) XPhos Pd G3 (CAS-№1445085-55-1) в 2 мл 1,4-диоксана перемешивают при 80°С в течение ночи. Ее разбавляют с водой. Оставшееся твердое вещество фильтруют, промывают водой и сушат в атмосфере воздуха с получением 570 мг продукта.
Следующее соединение получают по общей методике (пример III.1), описанной выше:
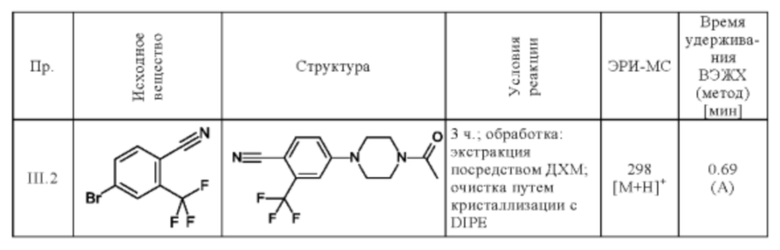
Пример 38
Пример IV.1
4-{6-Метил-7-оксо-2,6-диазаспиро[3.4]октан-2-ил}бензонитрил
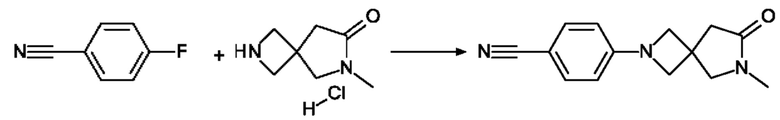
222 мг (1,81 ммоль) 4-Фторбензонитрила (CAS №1194-02-1) и 320 мг (1.81 ммоль) 6-метил-2,6-диазаспиро[3.4]октан-7-она гидрохлорида (CAS №2097951-61-4), разбавленного с 1,6 мл ДМСО, обрабатывают с помощью 790 мг (5,62 ммоль) K2CO3 и перемешивают при 120°С в течение 3 ч. и при КТ в течение ночи. Реакционную смесь охлаждают и разбавляют с водой. Осадок отфильтровывают, промывают водой и сушат в вакууме при 50°С с получением 340 мг продукта.
Следующие соединения получают по общей методике (пример IV.1), описанной выше:
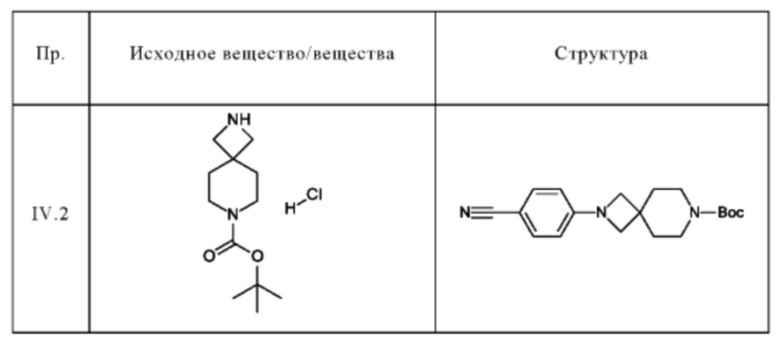
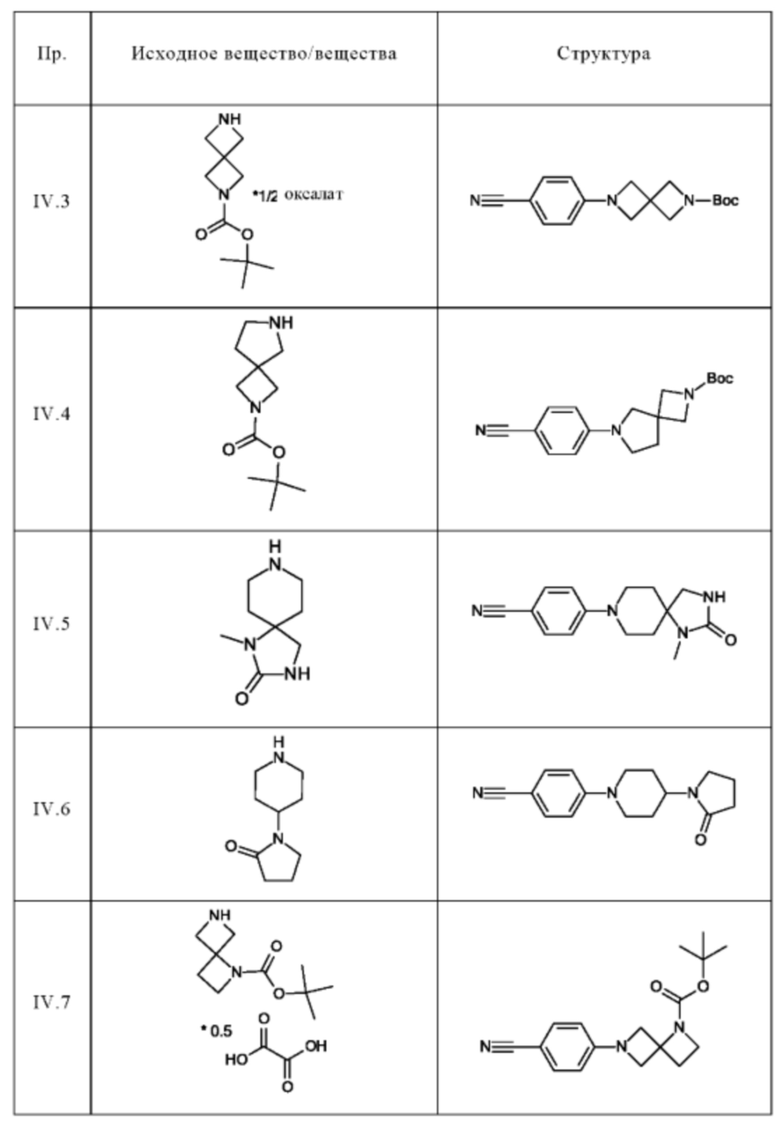
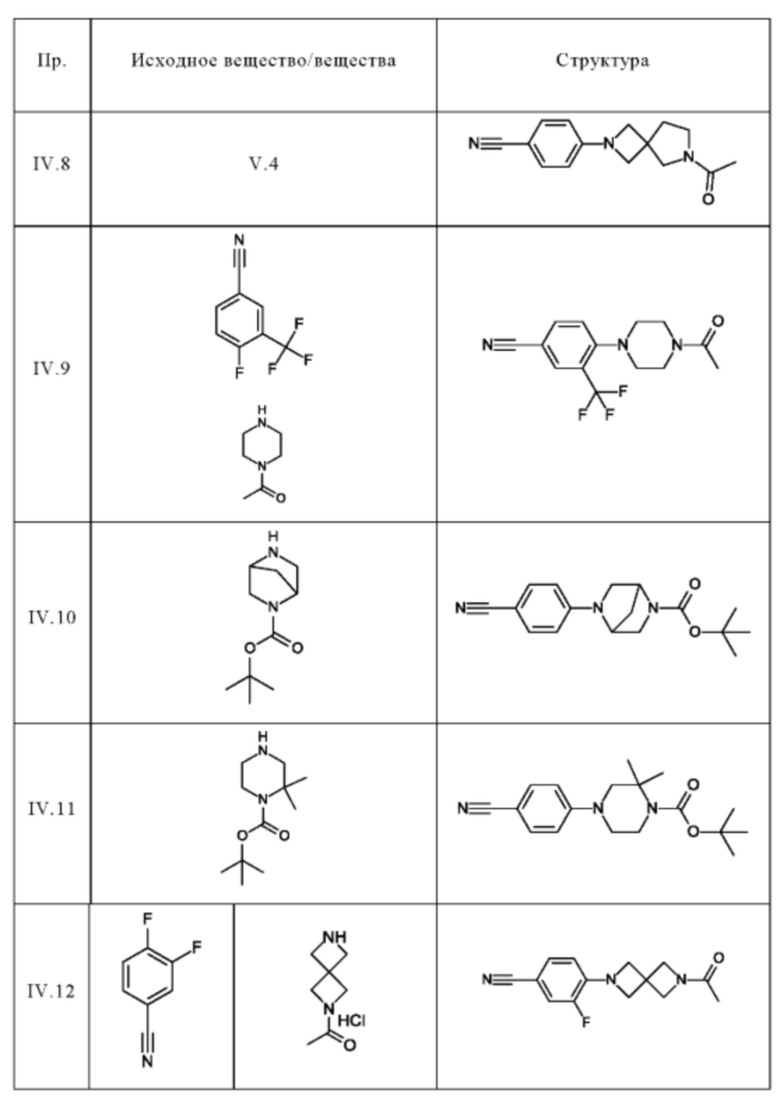
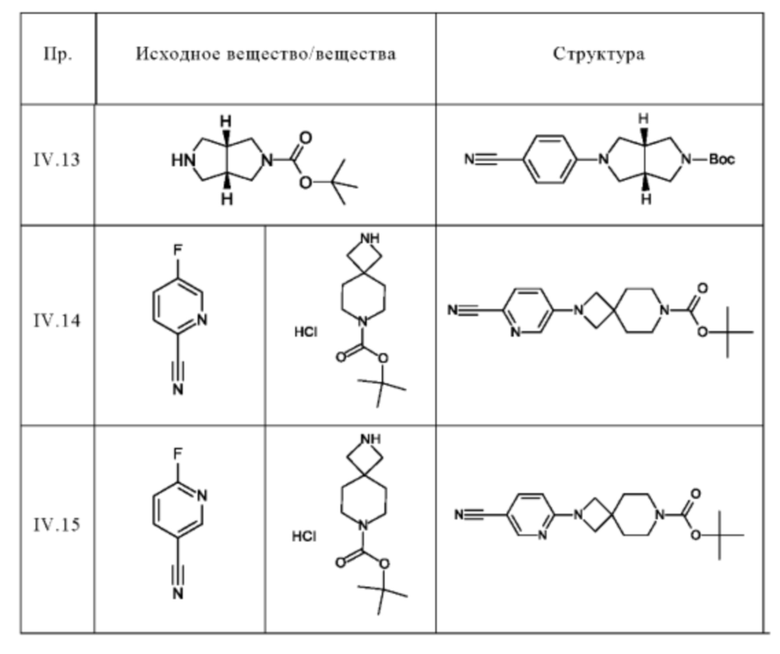

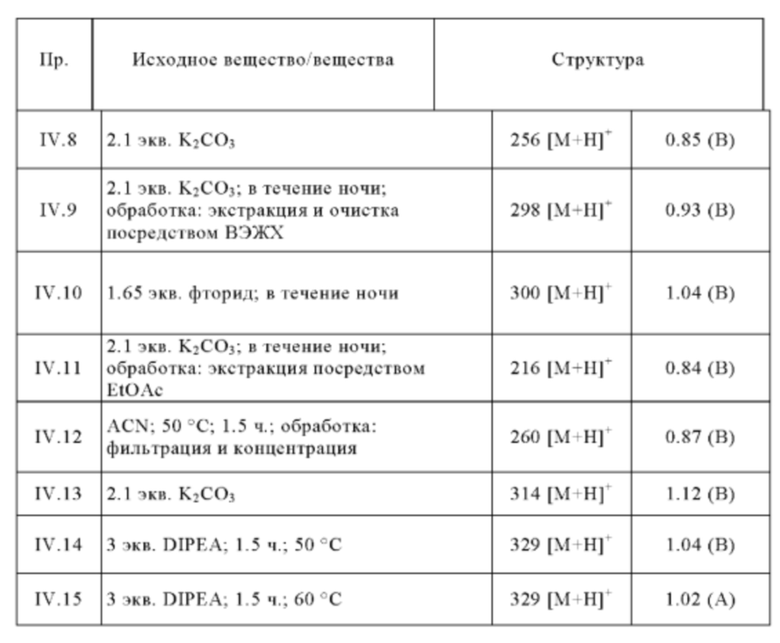
Пример V
Пример V.1
4-{2,7-Диазаспиро[3.5]нонан-2-ил}бензонитрил; трифторуксусная кислота
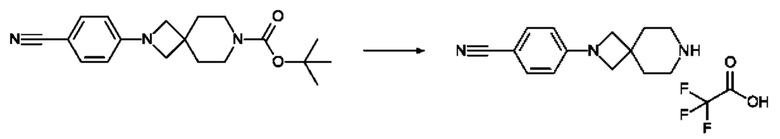
255 мг (0.780 ммоль) трет-Бутил 2-(4-цианофенил)-2,7-диазаспиро[3.5]нонан-7-карбоксилата (пример IV.2) разбавляют с 5 мл ДХМ и добавляют 300 мкл (3,89 ммоль) ТФУ. Реакционную смесь перемешивают при КТ в течение 2 ч и концентрируют под сниженным давлением с получением 260 мг продукта.
ЭРИ-МС: 228 [М+Н]+
Следующие соединения получают по общей методике (пример V.1), описанной выше:
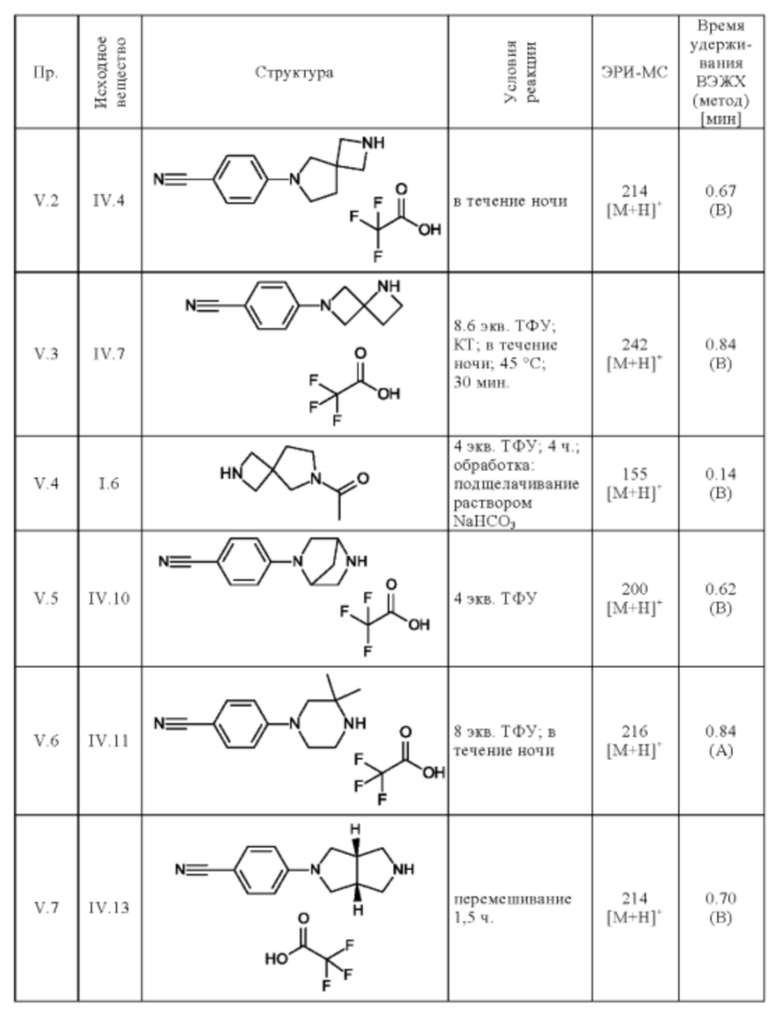
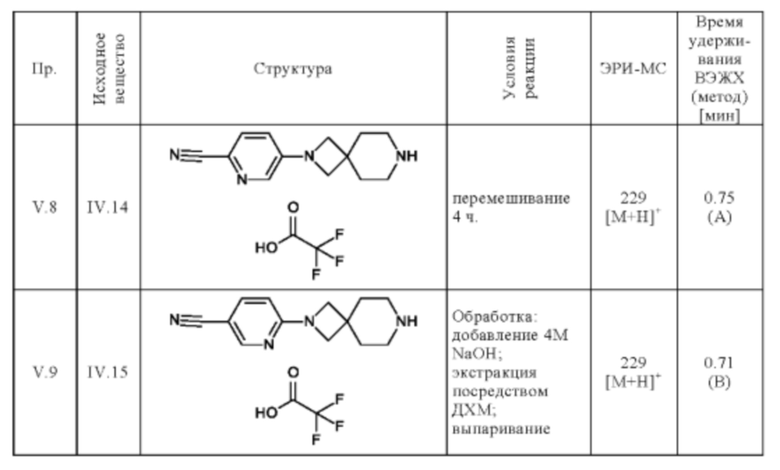
Пример VI
4-{2,6-Диазаспиро[3.3]гептан-2-ил}бензонитрил
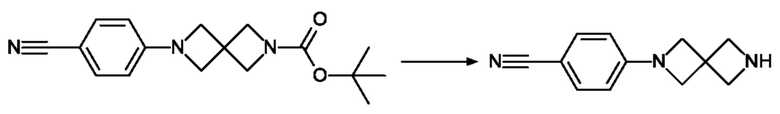
Раствор 0.90 г (3.01 ммоль) трет-бутил 6-(4-цианофенил)-2,6-диазаспиро[3.3]гептан-2-карбоксилата (пример IV.3) в 8 мл ACN обрабатывают с помощью 1.14 г (6.01 ммоль) моногидрата n-толуолсульфоновой кислоты и перемешивают при КТ в течение 24 ч. Реакционную смесь разбавляют с ДХМ и экстрагируют посредством нас. раствора NaHCO3. Объединенные органические слои сушат с помощью MgSO4 и концентрируют под сниженным давлением с получением 600 мг продукта.
Пример 45
Этил 1-(6-хлорпиридазин-3-ил)циклопропан-1-карбоксилат
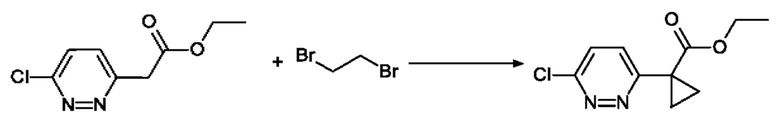
Раствор 13.8 г (68.8 ммоль) этил 2-(6-хлорпиридазин-3-ил)ацетата (CAS №1023817-10-8) в 100 мл ДМСО охлаждают на ледяной бане и обрабатывают посредством 8.25 г (206.4 ммоль) гидрида натрия (60% дисперсия). Реакционную смесь перемешивают в течение 20 мин 8.89 мл (103.2 ммоль). К реакционной смеси добавляют дибромэтан и перемешивают при температурном контроле (максимум 38°С) в течение 45 мин. Реакционную смесь охлаждают льдом и разбавляют с раствором NH4Cl. Водную фазу экстрагируют посредством EtOAc. Объединенные органические слои сушат с помощью MgSO4 и концентрируют под сниженным давлением. Остаток очищают посредством колоночной хроматографии (силикагель; элюент: Су/EtOAc=90/10 к 65/35) с получением 11.4 г продукта.
Пример VIII
Пример VIII.1
1-(6-{[6-(Дифторметил)пиридин-3-ил]метокси}пиридазин-3-ил)циклопропан-1-карбоновая кислота
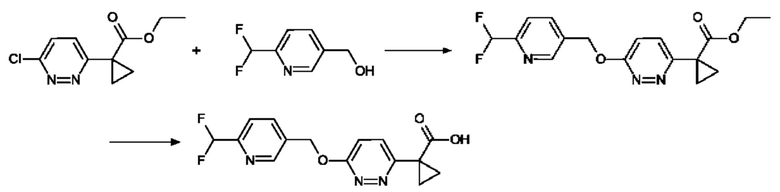
843 мг (5,29 ммоль) [6-(Дифторметил)пиридин-3-ил]метанола (CAS №946578-33-2) в 8 мл ДМФА охлаждают на ледяной бане и добавляют 385 мг (8.82 ммоль) гидрид натрия (55% чистота). Смесь перемешивают при КТ в течение 10 мин. К реакционной смеси добавляют 1.00 г (4.41 ммоль) этил 1-(6-хлорпиридазин-3-ил)циклопропан-1-карбоксилата (пример VII) в 5 мл ДМФА и перемешивают при КТ в течение 1 ч. Реакционную смесь разбавляют с охлажденным раствором NH4Cl и экстрагируют ее с помощью EtOAc три раза. Органическую фазу сушат с помощью MgSO4 и концентрируют в вакууме с получением промежуточного этилового эфира.
Остаток обрабатывают с помощью МеОН и добавляют 200 мг (8.35 ммоль) гидроксида лития и 3 мл воды. Реакционную смесь перемешивают при КТ в течение ночи и обрабатывают посредством 2 мл (8.00 ммоль) раствора 4 N гидроксида натрия. Ее перемешивают при 45°С в течение 1 ч., а тем временем ТГФ испаряется под сниженным давлением. Медленно добавляют DIPE к реакционной смеси и отделяют. Водную фазу разбавляют с раствором NH4Cl, подкисляют путем добавления лимонной кислоты и экстрагируют посредством EtOAc. Органическую фазу сушат с помощью MgSO4, фильтруют через силикагель и выпаривают досуха в вакууме. Остаток очищают посредством колоночной хроматографии (силикагель; элюент: ДХМ/МеОН=100/0 к 85/15) с получением 845 мг продукта.
Следующее соединение получают по общей методике (пример VIII.1), описанной выше:
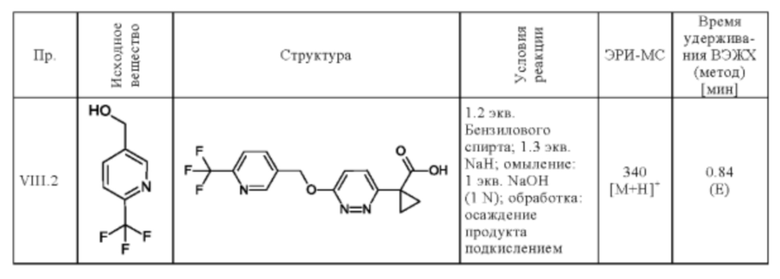
Пример 47
6-(4-Ацетилпиперазин-1-ил)пиридин-3-карбонитрил
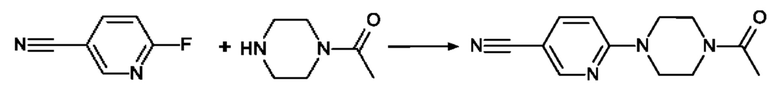
Смесь из 250 мг (2.05 ммоль) 6-фторпиридин-3-карбонитрила, 315 мг (2.46 ммоль) 1-ацетилпиперазина и 705 мкл (4.10 ммоль) DIPEA в 3 мл ДМСО перемешивают при 80°С в течение 45 мин и гасят посредством раствора полуконц. NaCl. Водную фазу экстрагируют посредством EtOAc. Объединенные органические фазы сушат посредством PTK и концентрируют в вакууме с получением 420 мг продукта.
Пример X
Пример X.1
4-(4-Ацетил-3,3-диметилпиперазин-1-ил)бензонитрил
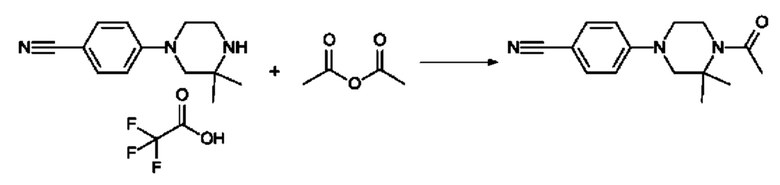
800 мг (1.21 ммоль) 4-(3,3-Диметилпиперазин-1-ил)бензонитрил-трифторуксусной кислоты (пример V.6) растворяют в 3 мл пиридина и добавляют 2.00 мл (21.2 ммоль) уксусного ангидрида. Реакционную смесь кипятят с обратным холодильником в течение ночи и выпаривают при пониженном давлении. Остаток ресуспендируют в нас. растворе NaHCO3 и экстрагируют с EtOAc. Органический слой сушат, концентрируют в вакууме и очищают посредством колоночной хроматографии (силикагель; элюент: ДХМ/МеОН=98/2 к 9/1) с получением 80 мг продукта.
Следующее соединение получают по общей методике (пример Х.1), описанной выше:
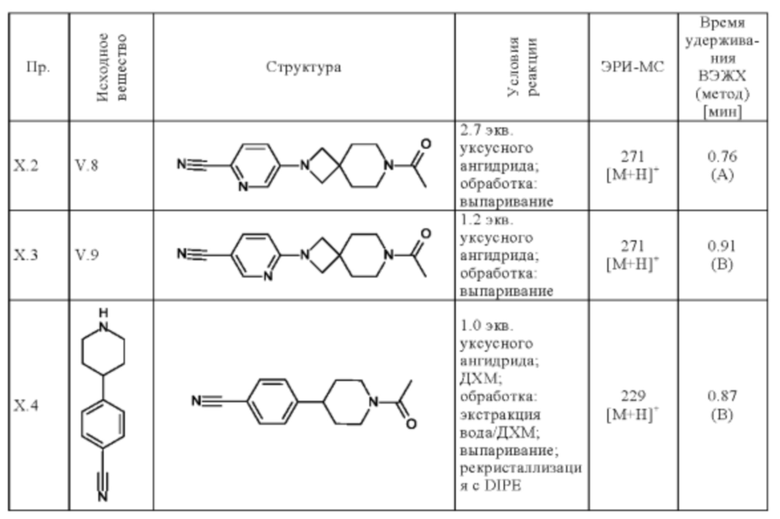
Пример XI
4-(2,2-Диметилпиперазин-1-ил)бензонитрил
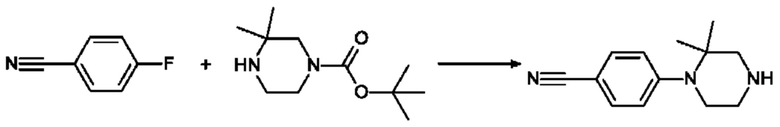
Раствор 56,5 мг (0.47 ммоль) 4-фторбензонитрила (CAS №1194-02-1) и 100 мг (0.47 ммоль) трет-бутил-3,3-диметилпиперазин-1-карбоксилат (CAS №259808-67-8) в 3 мл NMP обрабатывают со 120 мкл (0.71 ммоль) DIPEA и перемешивают при 190°С в течение 7 ч. под микроволновым облучением. Реакционную смесь разбавляют с водой и EtOAc, органический слой отделяют и промывают нас. раствором NaHCO3. Органический слой сушат, фильтруют и концентрируют при пониженном давлении, чтобы получить 120 мг продукта.
Получение конечных соединений
Пример 1.1
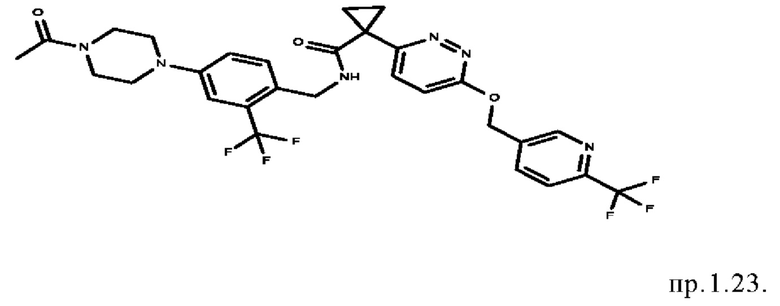
N-(4-(7-ацетил-2,7-диазаспиро[3.5]нонан-2-ил)бензил)-1-(6-((6-(трифтрметил)пиридин-3-ил)метокси)пиридазин-3-ил)циклопропан-1-карбоксамид
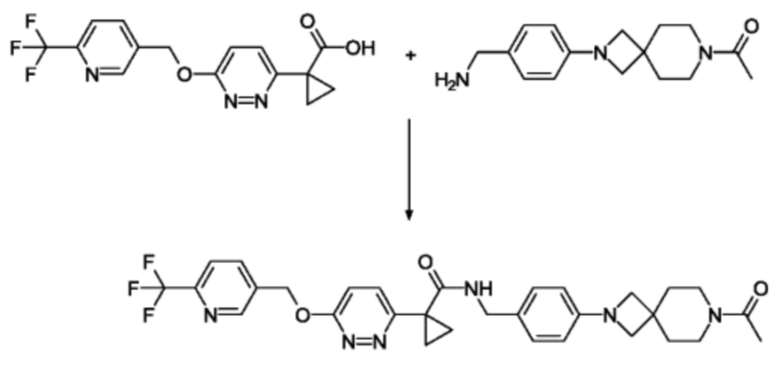
300 мг (0,88 ммоль) 1-(6-((6-(трифтрметил)пиридин-3-ил)метокси)пиридазин-3-ил)циклопропан-1-карбоновой кислоты (пример VIII.2) и 0.45 мл (2.65 ммоль) DIPEA разбавляют с 3 мл ДМФА и добавляют 370 мг (0.97 ммоль) HATU. Смесь перемешивают при КТ в течение 5 мин, затем добавляют 242 мг (0,88 ммоль) 1-(2-(4-(аминометил)фенил)-2,7-диазаспиро[3.5]нонан-7-ил)этан-1-она (пример II.4). Реакционную смесь перемешивают в течение 30 мин при КТ, разбавляют с МеОН и очищают посредством ВЭЖХ с получением продукта.
1H ЯМР (400 МГц, ДМСО-d6) δ 8.90 (d, J=1.39 Гц, 1Н), 8.20 (dd, J=1.46, 8.05 Гц, 1H), 7.91-7.99 (m, 2Н), 7.61 (d, J=9.13 Гц, 1H), 7.27 (d, J=9.13 Гц, 1Н), 7.02 (d, J=8.49 Гц, 2Н), 6.35 (d, J=8.49 Гц, 2Н), 5.67 (s, 2Н), 4.13 (d, J=5.83 Гц, 2Н), 3.54 (d, J=1.77 Гц, 4H), 3.40 (td, J=5.61, 14.38 Гц, 4Н), 1.99 (s, 3Н), 1.61-1.78 (m, 4Н), 1.22-1.46 (m, 4Н)
Следующие соединения получают в соответствии с общей методикой (пример 1.1), описанной выше:
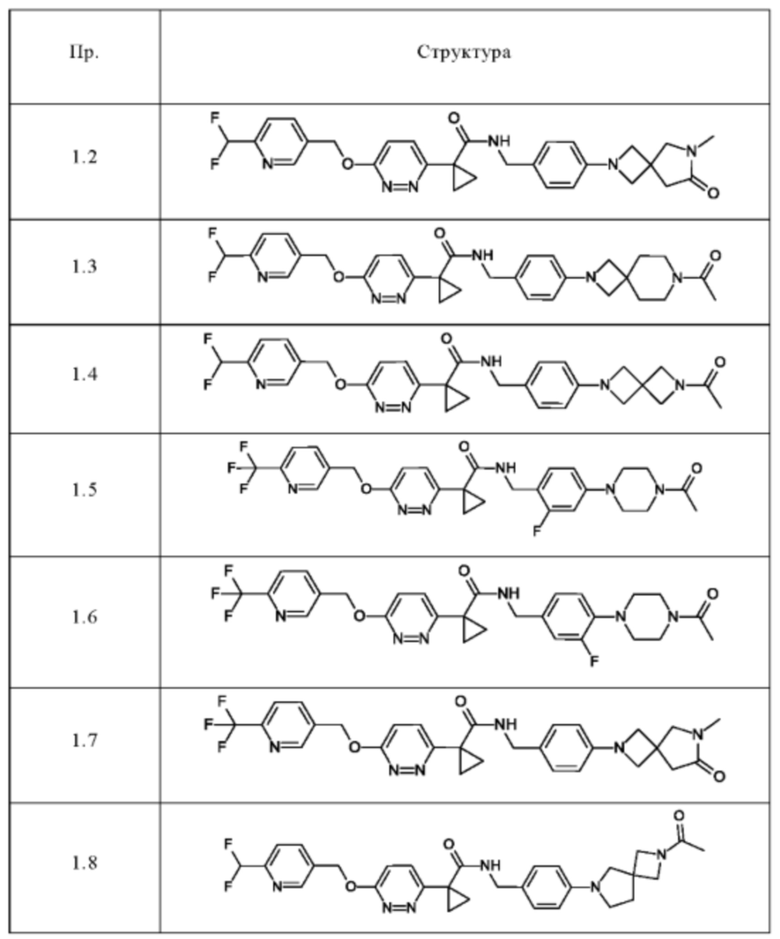
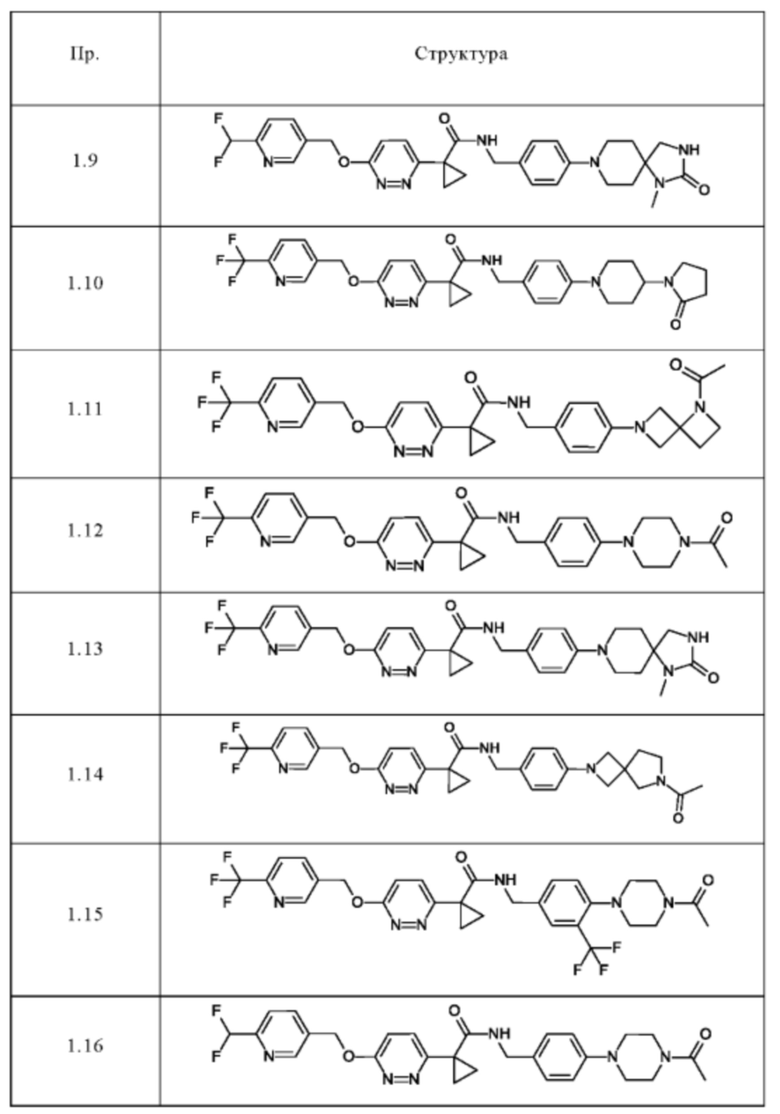
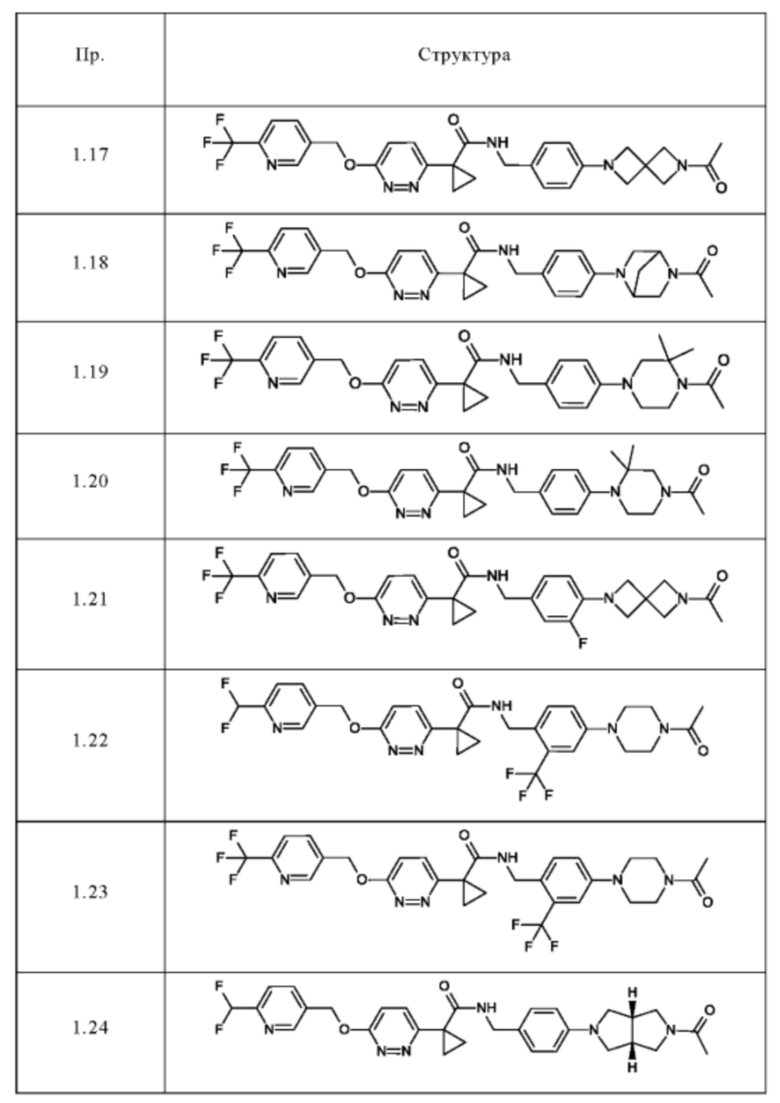
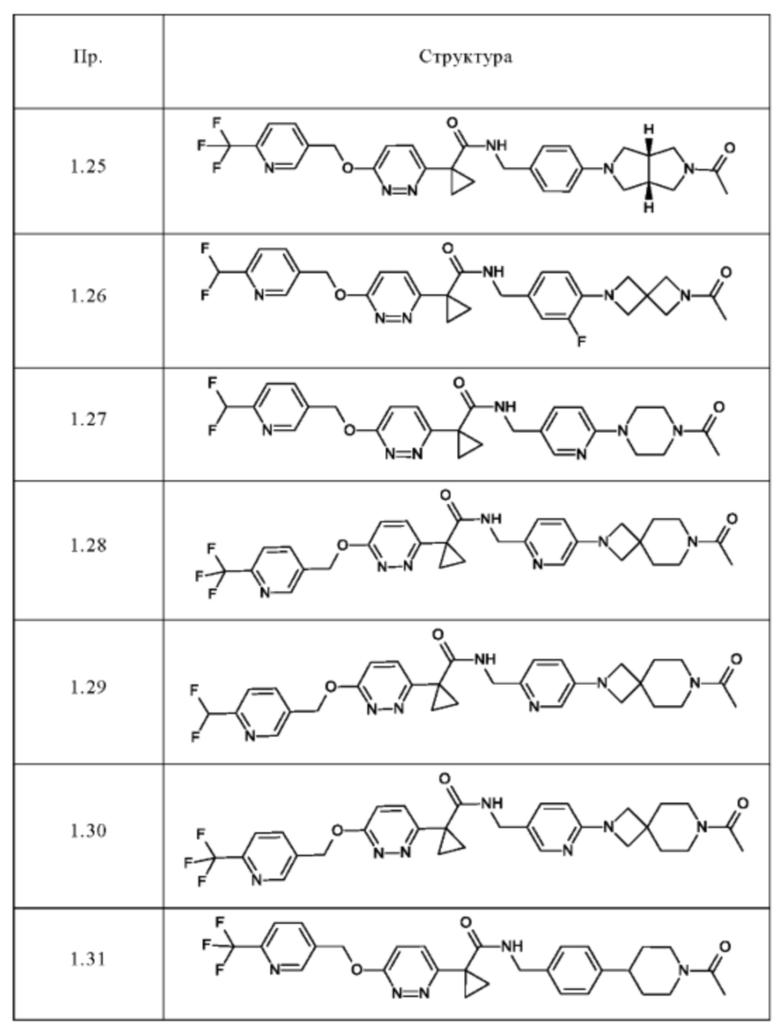
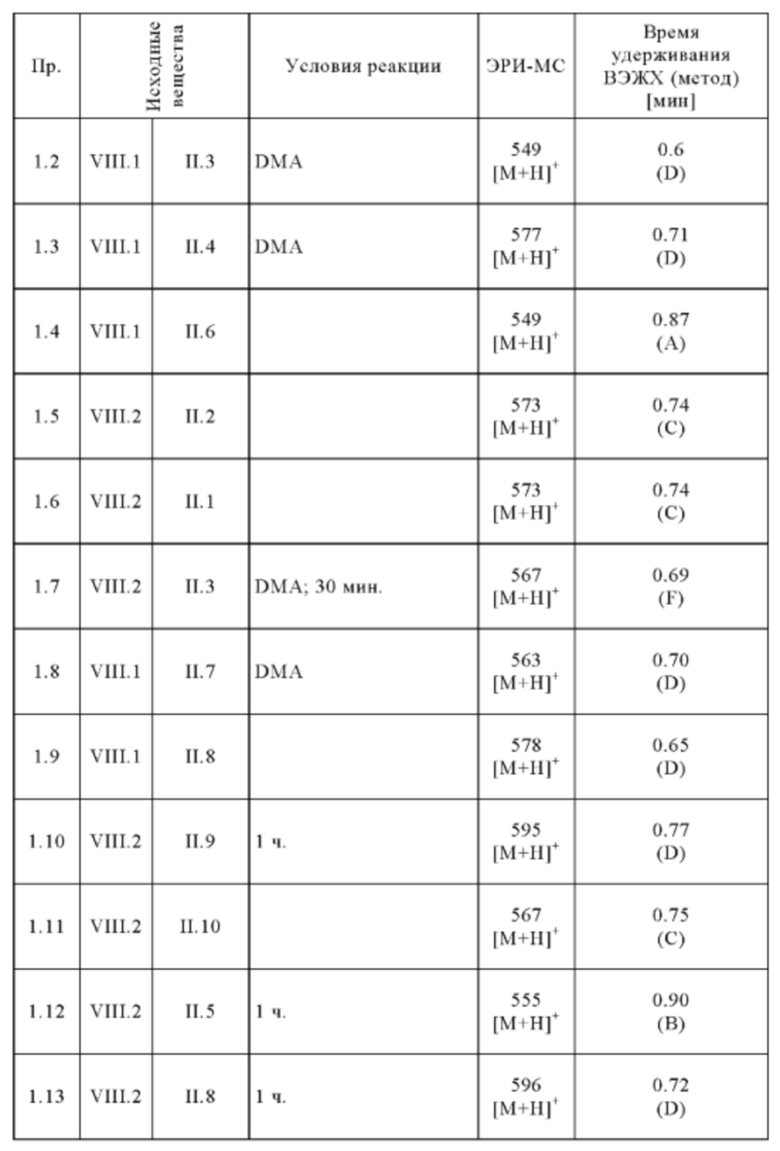
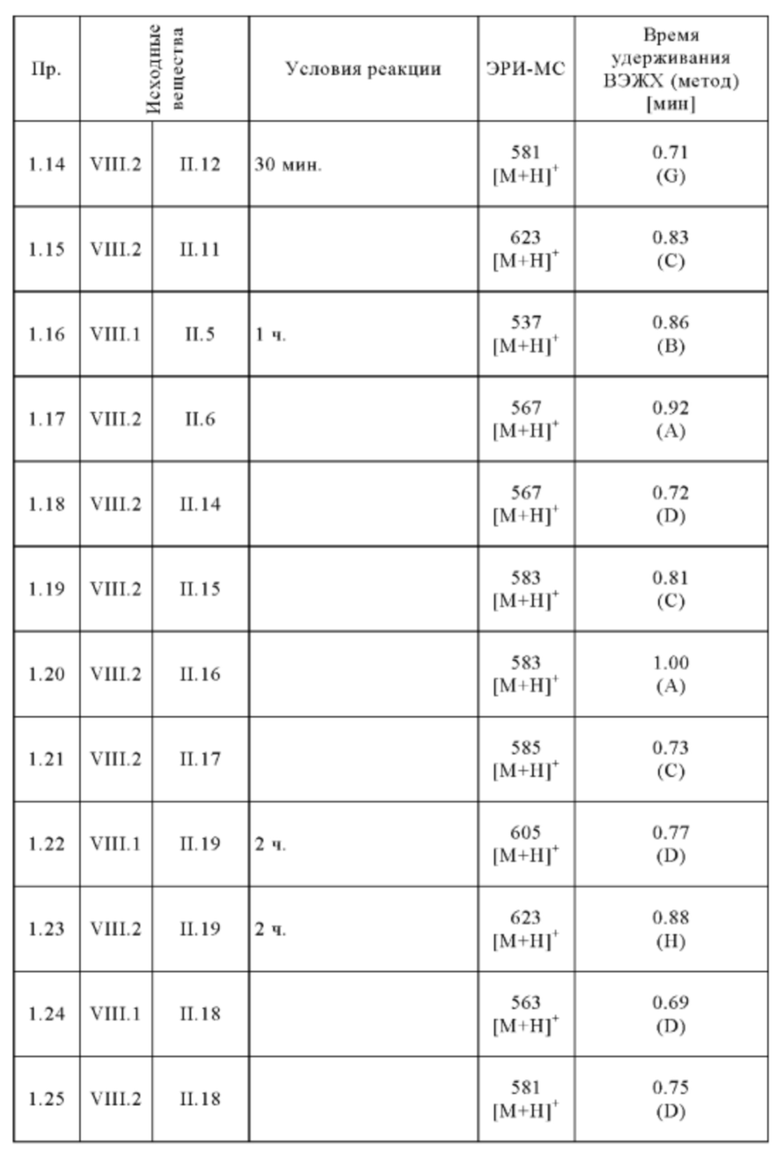
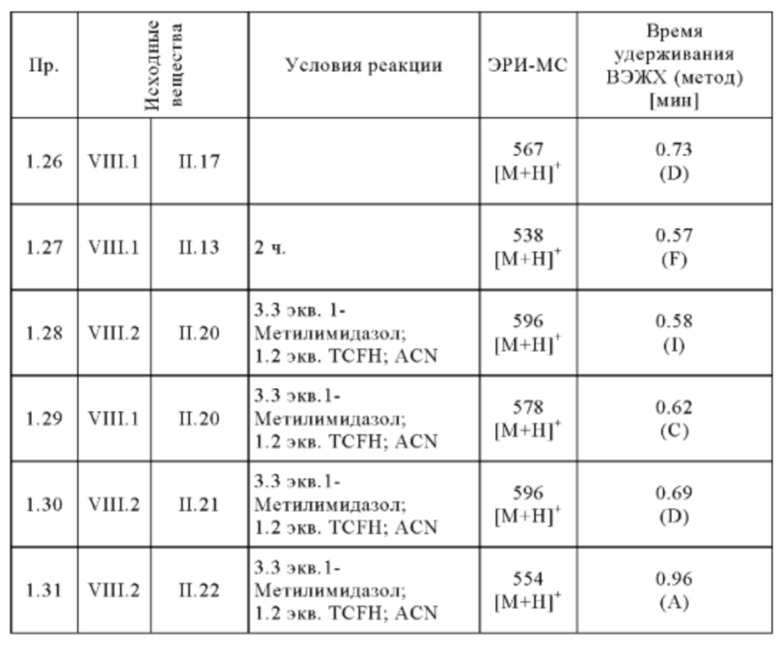


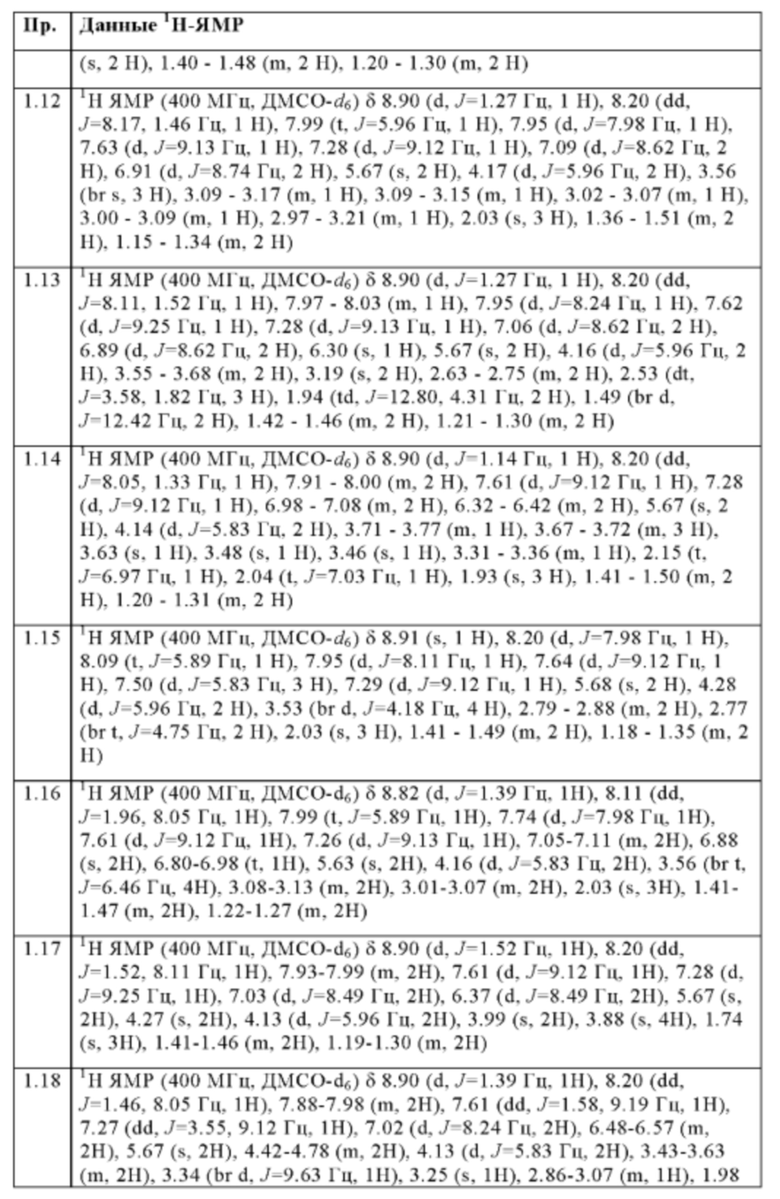
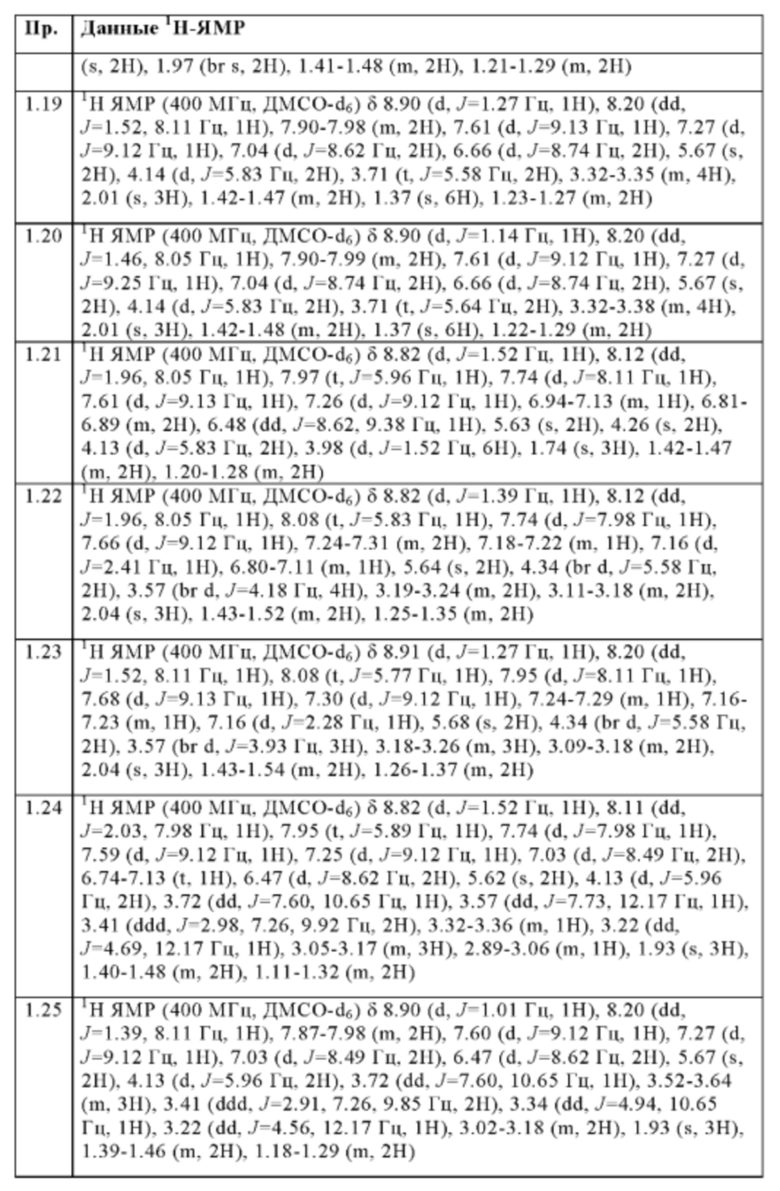
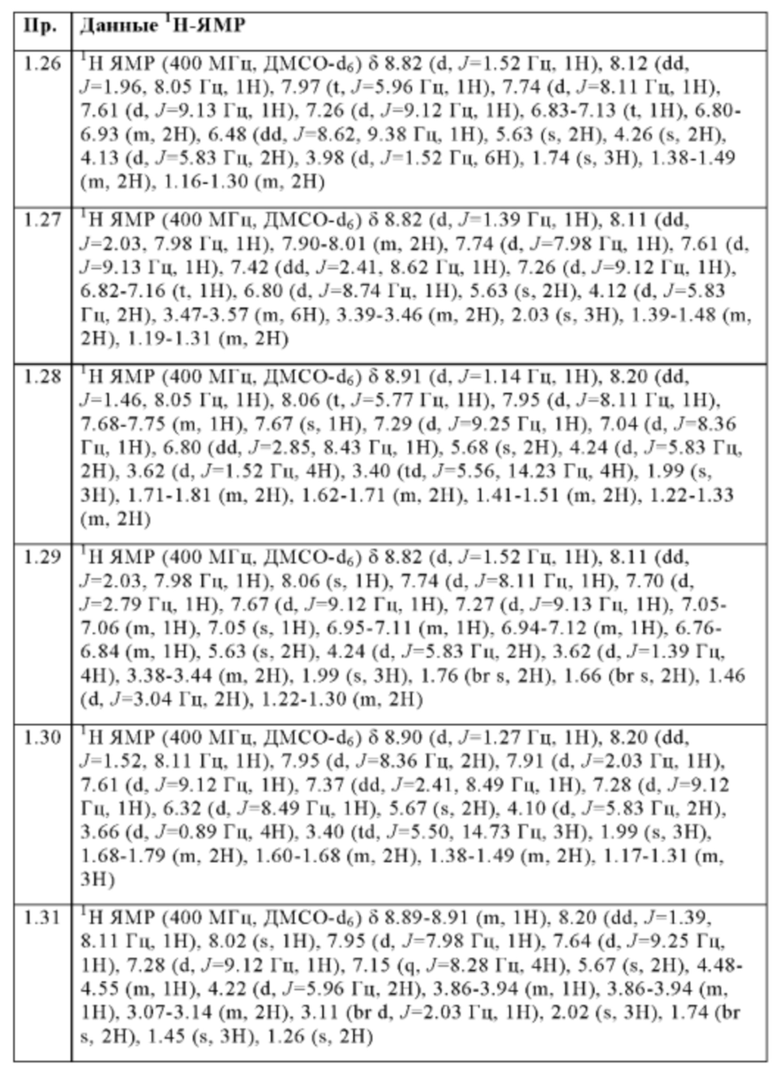
Методы аналитической ВЭЖХ
Метод А
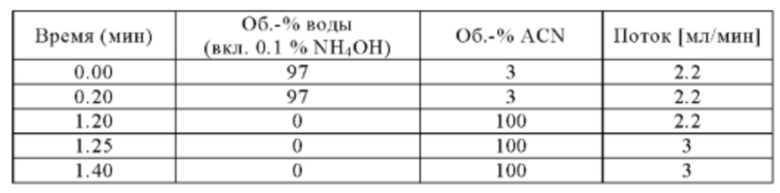
Аналитическая колонка: XBridge С18 (Waters) 2.5 мкм; 3.0×30 мм; температура колонки: 60°С
Метод В
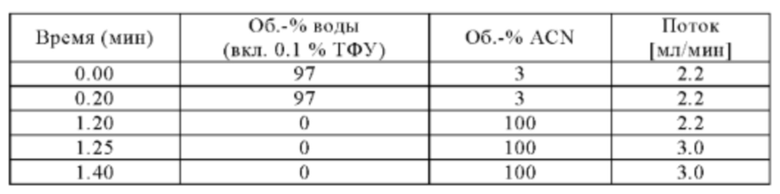
Аналитическая колонка: Stable Bond (Agilent) 1.8 мкм; 3.0×30 мм; температура колонки: 60°С
Метод С
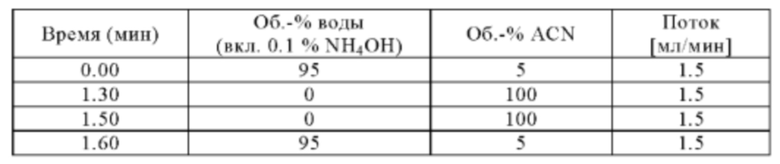
Аналитическая колонка: XBridge (Waters) С18_3.0×30 мм_2.5 мкм; температура колонки: 60°С
Метод D
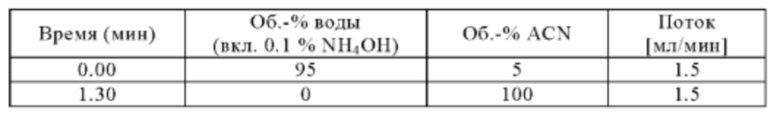
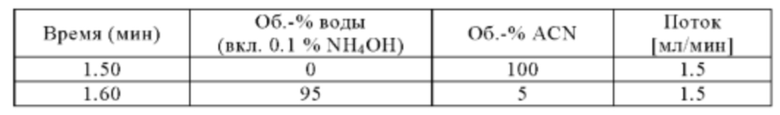
Аналитическая колонка: XBridge С18_3.0×30 мм_2.5 мкм (Waters); температура колонки: 60°С
Метод Е
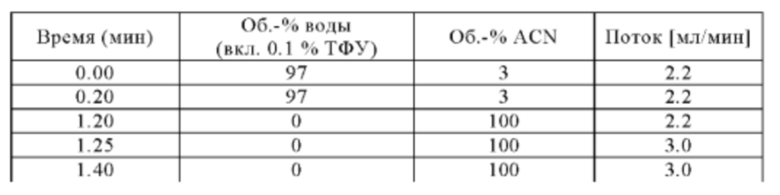
Аналитическая колонка: Sunfire (Waters) 2.5 мкм; 3.0×30 мм; температура колонки: 60°С
Метод F
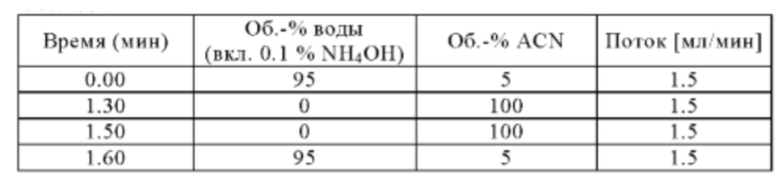
Аналитическая колонка: XBridge С18 (Waters) 2.5 мкм; 3.0×30 мм; температура колонки: 60°С
Метод G
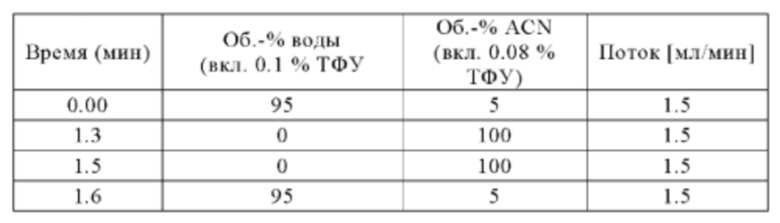
Аналитическая колонка: Sunfire С18 (Waters) 2.5 мкм; 3.0×30 мм; температура колонки: 60°С
Метод Н
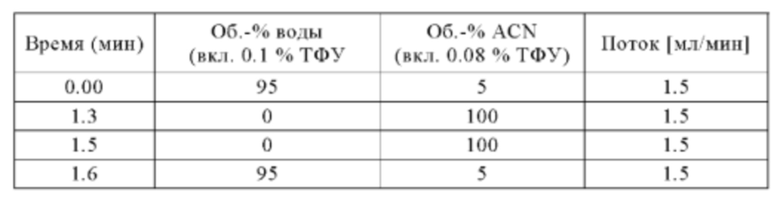
Аналитическая колонка: Sunfire С18 (Waters) 2.5 мкм; 3.0×30 мм; температура колонки: 60°С
Метод I
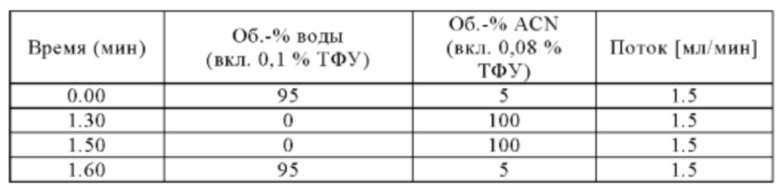
Аналитическая колонка: Sunfire С18 (Waters) 2.5 мкм; 3.0×30 мм; температура колонки: 60°С
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНОЕ ПИРРОЛОПИРИМИДИНА И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2780254C1 |
| ПИРИМИДИНОВОЕ СОЕДИНЕНИЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2790017C1 |
| НОВЫЕ ПРОИЗВОДНЫЕ 3,5-ДИЗАМЕЩЕННОГО ПИРИДИНА И 3,5-ДИЗАМЕЩЕННОГО ПИРИДАЗИНА И ИХ ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2799544C2 |
| ИНГИБИРУЮЩИЕ ASK1 ПРОИЗВОДНЫЕ ПИРРОЛОПИРИМИДИНА И ПИРРОЛОПИРИДИНА | 2018 |
|
RU2772422C2 |
| 3-АРИЛ-5-ЗАМЕЩЕННЫЕ СОЕДИНЕНИЯ ИЗОХИНОЛИН-1-ОНА И ИХ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2013 |
|
RU2696572C2 |
| Фармацевтическая композиция для предупреждения или лечения фиброза | 2022 |
|
RU2829908C2 |
| НОВЫЕ БИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ДВОЙНЫХ ИНГИБИТОРОВ АУТОТАКСИНА (ATX)/КАРБОАНГИДРАЗЫ (CA) | 2016 |
|
RU2725138C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ИЛИ ЛЕЧЕНИЯ СИСТЕМНОГО СКЛЕРОЗА | 2022 |
|
RU2834641C2 |
| НОВЫЕ СПИРО[ИМИДАЗОЛИДИН-4,3'-ИНДОЛ]-2,2',5(1'Н)-ТРИОНЫ ДЛЯ ЛЕЧЕНИЯ СОСТОЯНИЙ, АССОЦИИРОВАННЫХ С ВАНИЛЛОИДНЫМ РЕЦЕПТОРОМ 1 | 2007 |
|
RU2421457C2 |
| 1-((3S,4R)-4-(3-ФТОРФЕНИЛ)-1-(2-МЕТОКСИЭТИЛ)ПИРРОЛИДИН-3-ИЛ)-3-(4-МЕТИЛ-3-(2-МЕТИЛПИРИМИДИН-5-ИЛ)-1-ФЕНИЛ-1Н-ПИРАЗОЛ-5-ИЛ)МОЧЕВИНА В КАЧЕСТВЕ ИНГИБИТОРА TrkA КИНАЗЫ | 2015 |
|
RU2719489C2 |
Изобретение относится к производным 1-(6-(метокси)пиридазин-3-ил)-циклопропан-1-карбоксамида формулы (I), где A, E, K определены в формуле изобретения, в качестве модуляторов аутотаксина (АТХ) для лечения воспалительных заболеваний дыхательных путей или фиброзных заболеваний, таких как, например, идиопатическое заболевание легких (IPF) или системный склероз (SSc). 13 н. и 8 з.п. ф-лы, 9 табл., 31 пр.
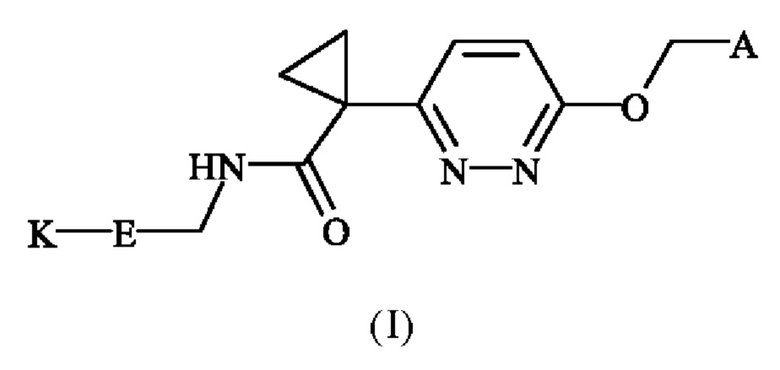
1. Соединение формулы (I)
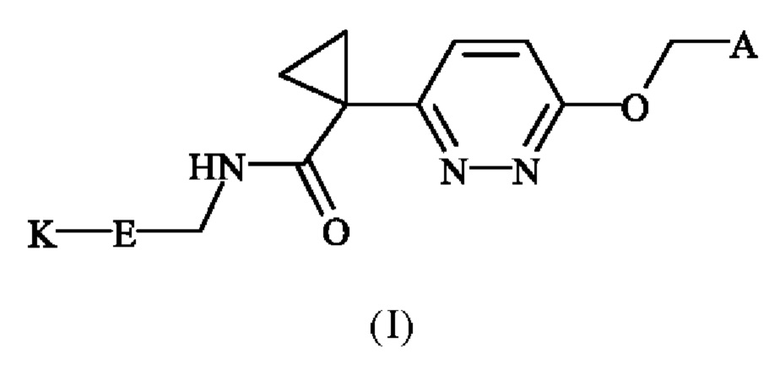 ,
,
в которой
А представляет собой пиридил, замещенный одним или двумя членами группы, включающей F1-7-фтор-С1-3-алкил;
Е выбран из группы, состоящей из фенила и пиридила, необязательно замещенного одним или двумя членами группы, состоящей из фтора и F1-7-фтор-С1-3-алкила;
K выбран из группы, состоящей из
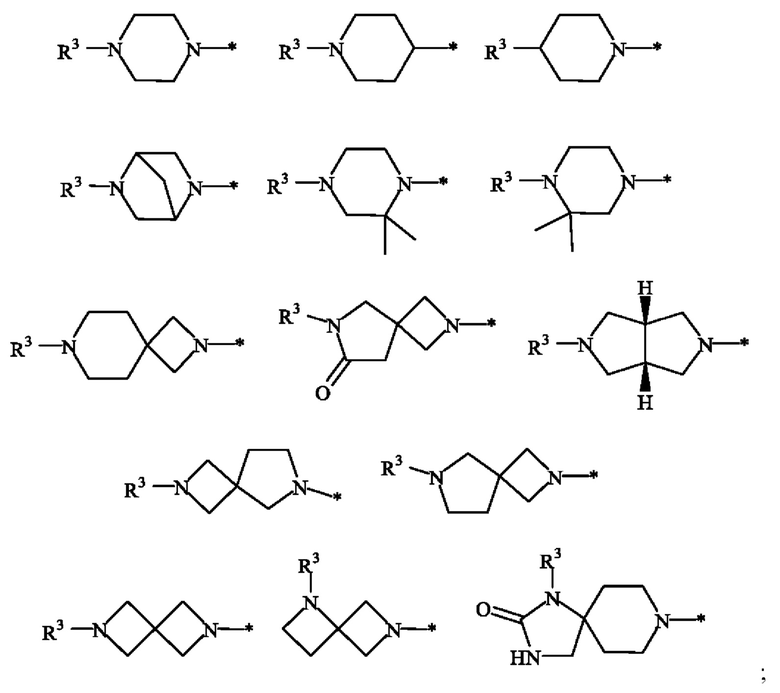
R3 выбран из группы, состоящей из R4(O)C-, метила и
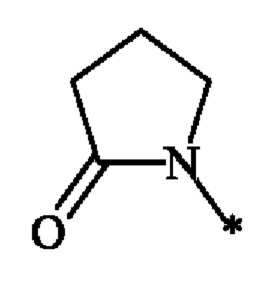 ;
;
R4 представляет собой метил.
2. Соединение формулы (I) по п. 1, где А представляет собой пиридил, замещенный одним или двумя из Е1-3-фтор-С1-алкила.
3. Соединение формулы (I) по п. 1, где А выбран из группы, состоящей из
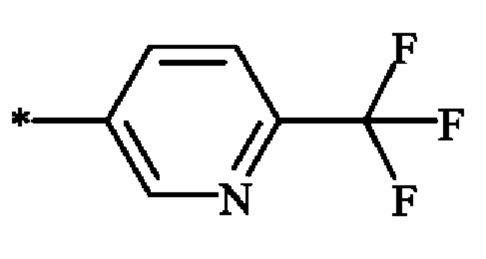 и
и 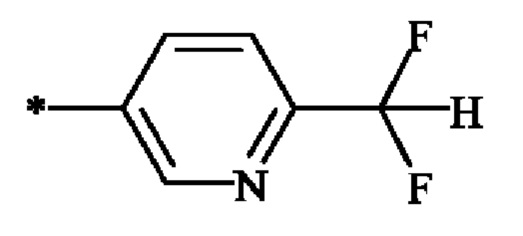 .
.
4. Соединение формулы (I) по любому из пп. 1-3, где Е выбран из группы, состоящей из фенила и пиридила, необязательно замещенного одним или двумя членами группы, состоящей из F и F3C.
5. Соединение формулы (I) по любому из пп. 1-3, где Е выбран из группы, состоящей из
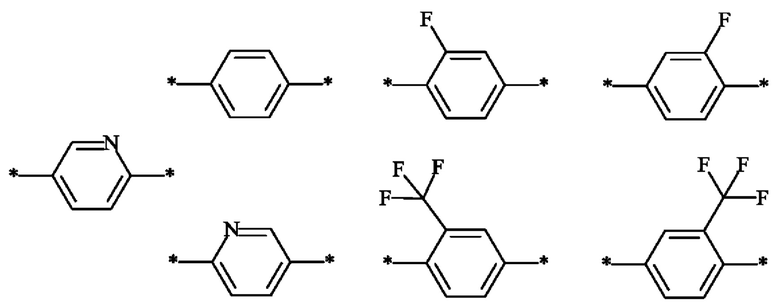
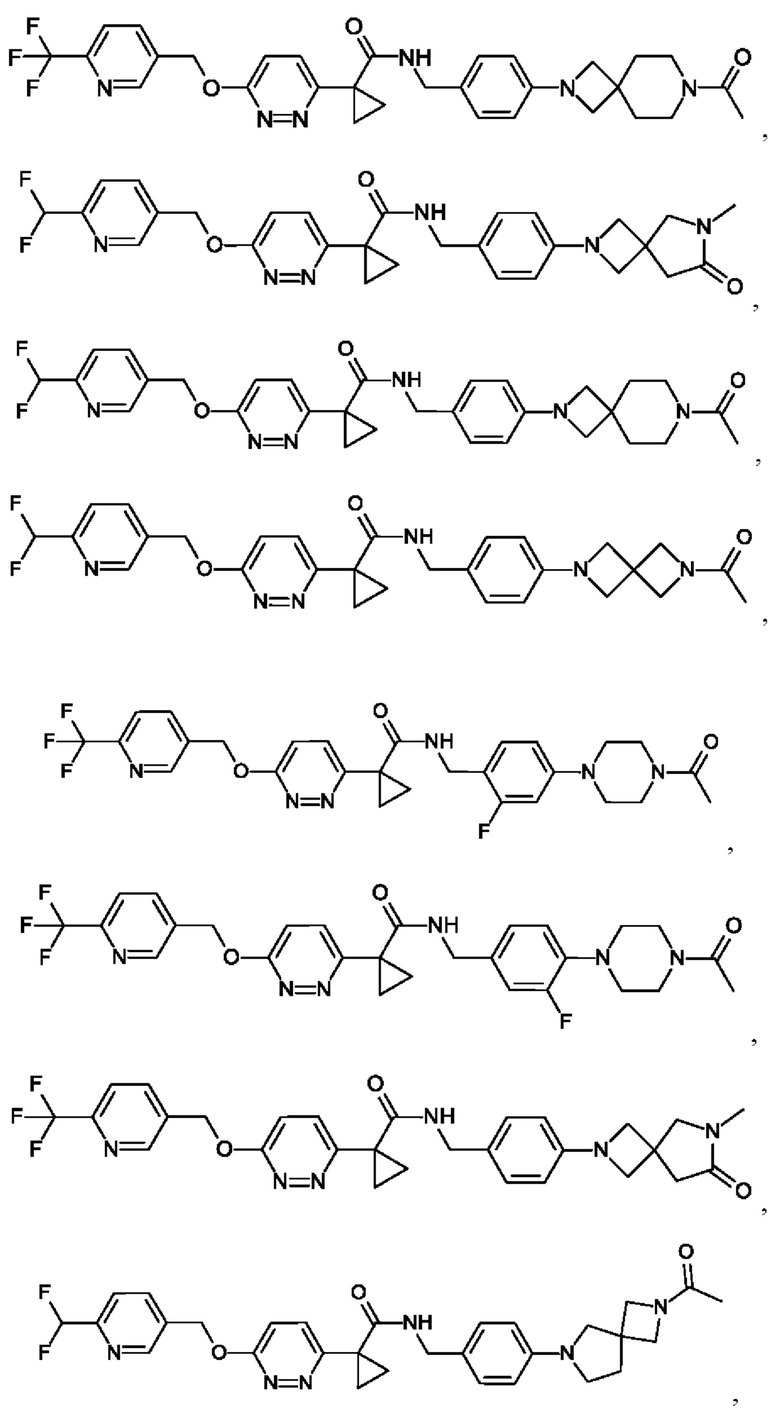
6. Соединение формулы (I) по п. 1, выбранное из группы, состоящей из
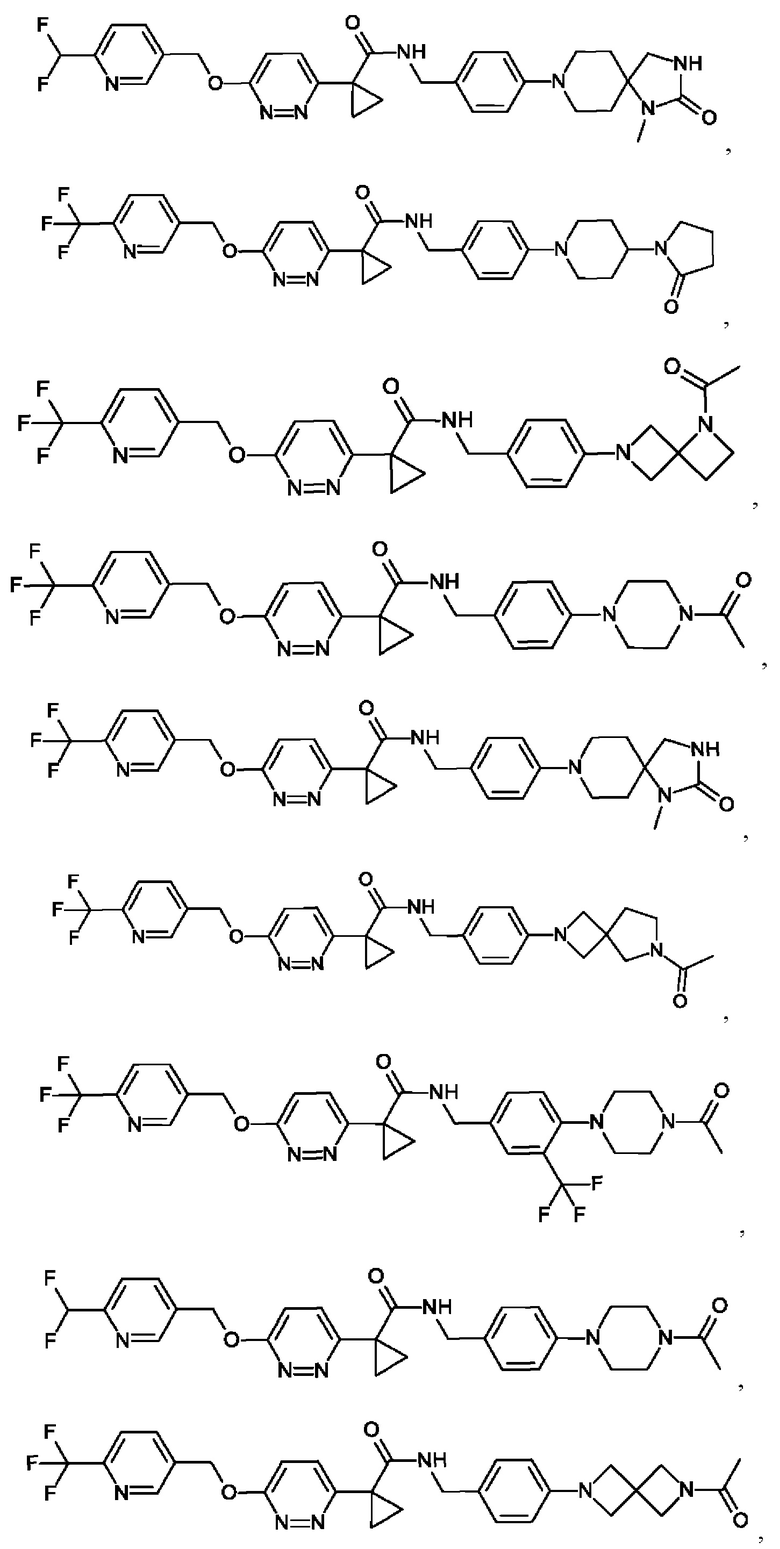
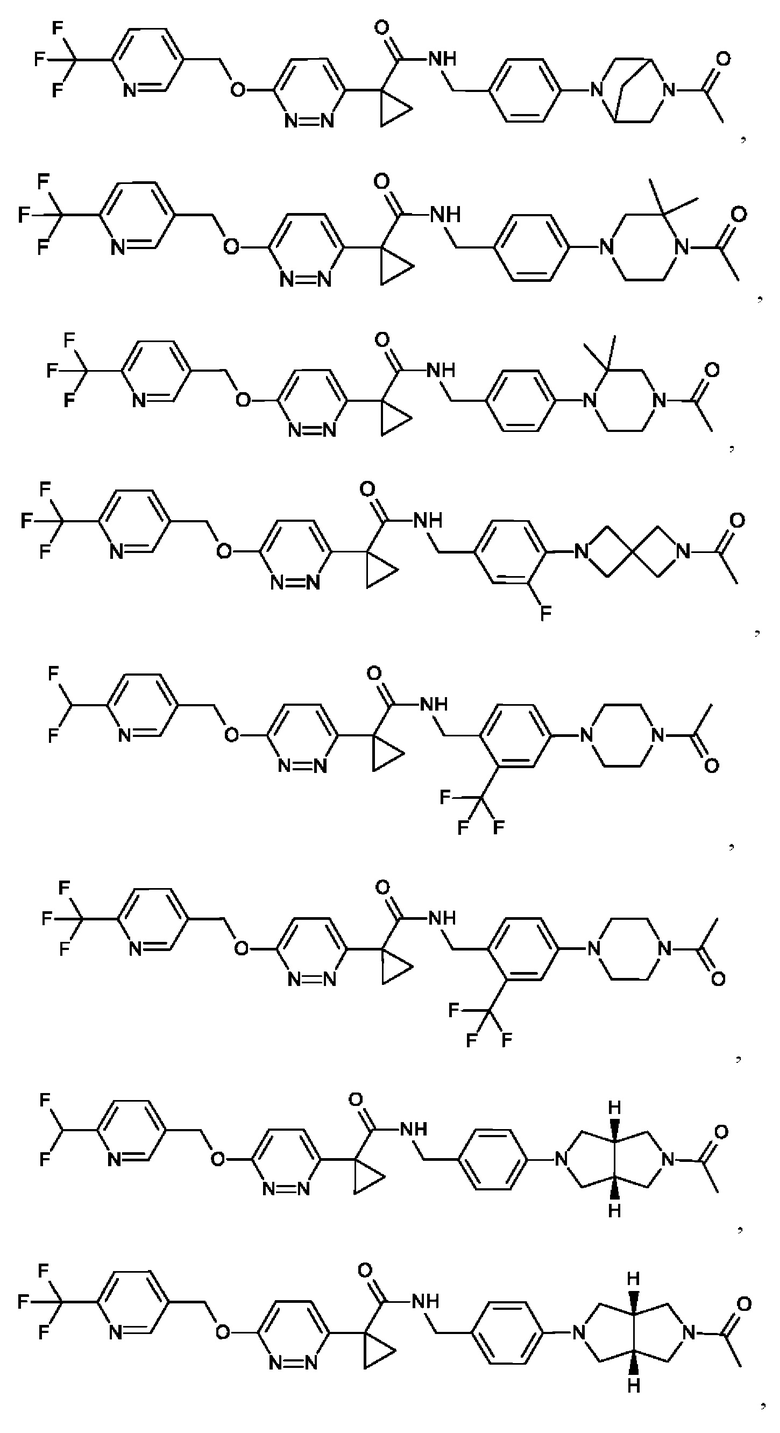
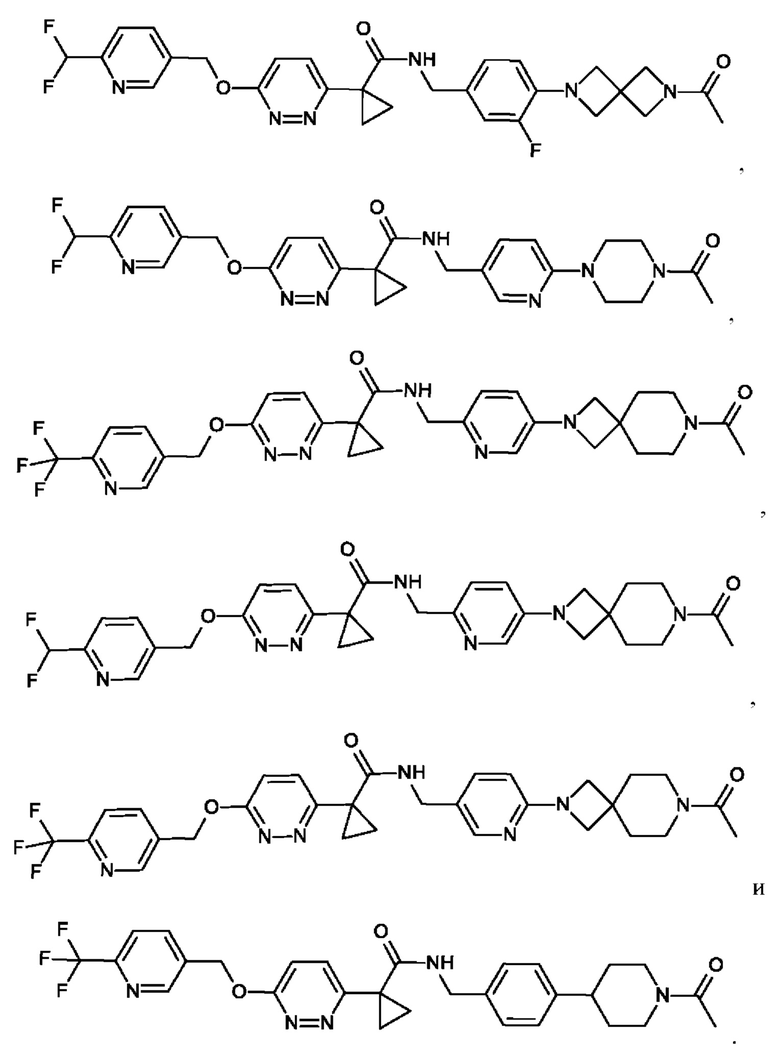
7. Соединение формулы
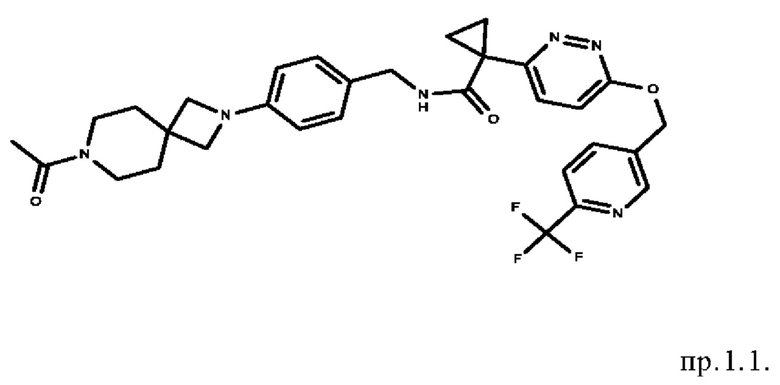
8. Соединение формулы
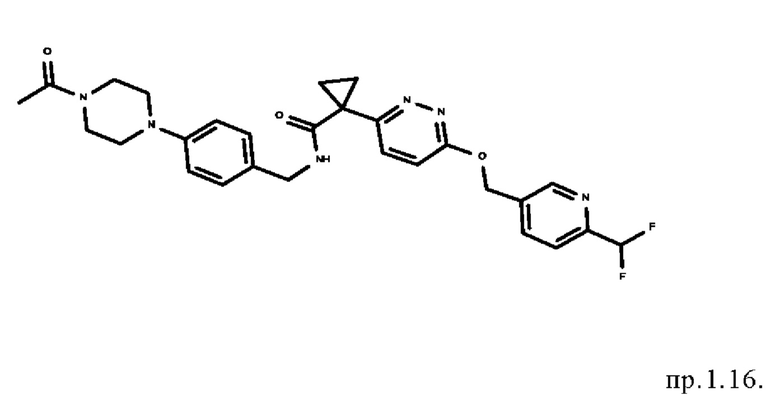
9. Соединение формулы
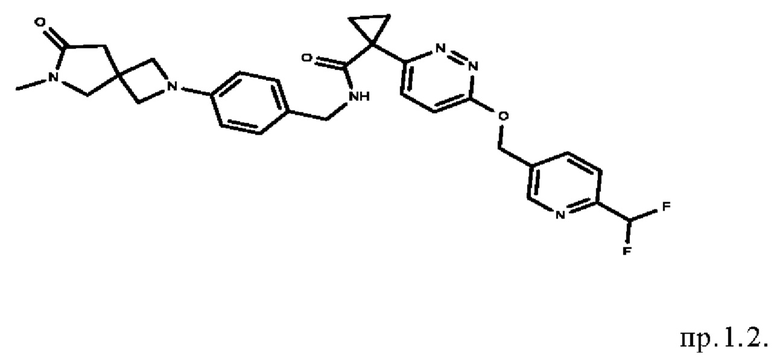
10. Соединение формулы
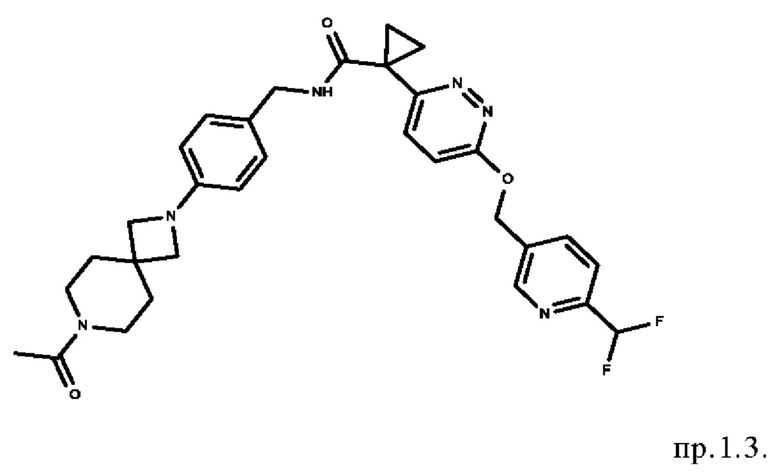
11. Соединение формулы
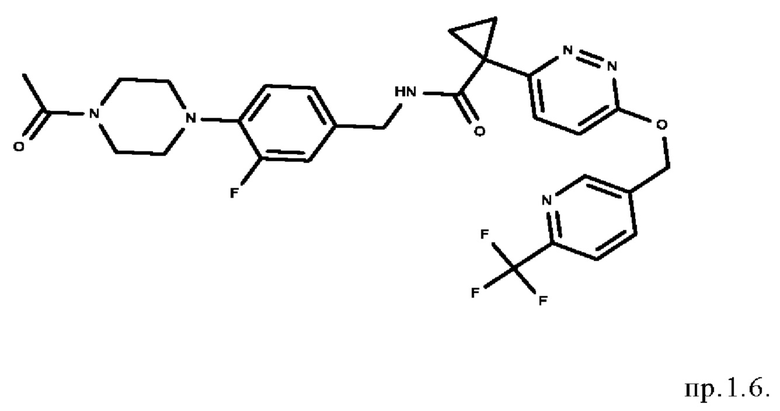
12. Соединение формулы
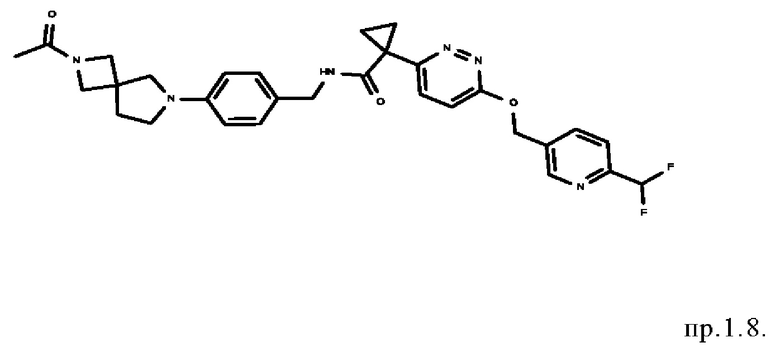
13. Соединение формулы
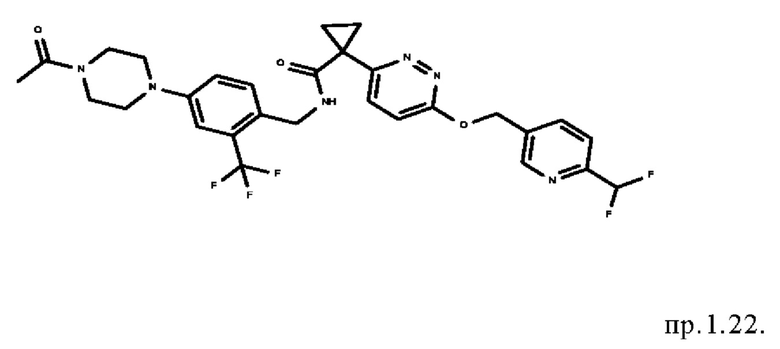
14. Соединение формулы
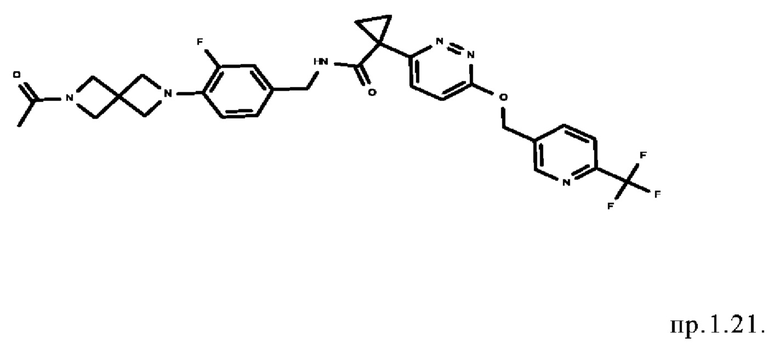
15. Соединение формулы
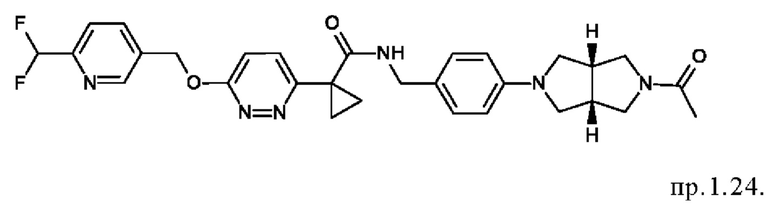
16. Соединение формулы
17. Фармацевтически приемлемая соль соединения по одному из пп. 7-16.
18. Фармацевтическая композиция для ингибирования активности аутотаксина (АТХ), содержащая эффективное количество по меньшей мере одного соединения формулы I по одному из пп. 1-16 или его фармацевтически приемлемую соль и одно или несколько фармацевтически приемлемых вспомогательных веществ.
19. Соединение формулы (I) по одному или нескольким пп. 1-16, для применения в качестве лекарственного средства.
20. Соединение по любому из пп. 1-16 или его фармацевтически приемлемая соль для лечения или профилактики воспалительных заболеваний дыхательных путей или фиброзных заболеваний.
21. Соединение по любому из пп. 1-16, или его фармацевтически приемлемая соль для лечения или профилактики идиопатического заболевания легких (IPF) или системной склеродермии (SSc).
| WO 2013061297 A1, 02.05.2013 | |||
| WO 2017148787 A1, 08.09.2017 | |||
| EA 201990045 A1, 31.05.2019 | |||
| WO 2017050747 A1, 30.03.2017 | |||
| Приспособление для профилирования дорожного полотна | 1932 |
|
SU28509A1 |
Авторы
Даты
2024-11-13—Публикация
2020-07-21—Подача