Область изобретения
Настоящее изобретение относится к фармацевтической композиции для предупреждения или лечения фиброза.
Уровень техники
Фиброз относится к явлению, при котором часть органа теряет эластичность по определенной причине, и в качестве типичного заболевания рассматривают фиброз легких или фиброз печени. В случае фиброза легких почти в подавляющем большинстве случаев легкие теряют эластичность вследствие воздействия излучения или наполнения легких водой. Однако фиброз легких может возникать только у некоторых людей. В настоящее время практически не существует полноценного способа терапии симптомов фиброза, и терапевтические способы находятся в стадии разработки и изучения. Типы фиброза включают интерстициальное легочное заболевание (ILD), склеродерму, келоид, гипертрофический рубец, неалкогольную жировую болезнь печени, первичный склерозирующий холангит (PSC), первичный билиарный холангит (РВС), диабетическую ретинопатию, возрастную макулодистрофию (AMD), гипертрофическую кардиомиопатию, инфаркт миокарда, мышечную дистрофию, диабетическую болезнь почек, фокально-сегментарный гломерулосклероз (FSGS), воспалительное заболевание кишечника (IBD) и им подобные. Интерстициальное легочное заболевание включает идиопатический фиброз легких (IPF), интерстициальное легочное заболевание, ассоциированное с системным склерозом, (SSc-ILD) и хроническое фиброзирующее интерстициальное легочное заболевание с прогрессирующим фенотипом (PF-ILD) и им подобные.
Идиопатический фиброз легких (IPF) представляет собой одно из хронически прогрессирующих интерстициальных заболеваний легких, попадающих в категорию редких заболеваний, и известно, что течение заболевания не является благоприятным, и утвержденного способа терапии не существует. До настоящего времени причина точно не установлена, и уровень 5-летней выживаемости после установления диагноза составляет 43%, и уровень 10-летней выживаемости составляет примерно 15%, что неблагоприятно. Несмотря на многочисленные проведенные исследования до сих пор не разработан способ терапии, улучшающий уровень выживаемости. Принимая во внимание то, что другие интерстициальные легочные заболевания, такие как неспецифическая интерстициальная пневмония (NSIP) и идиопатическая организующаяся пневмония (СОР), имеют относительно благоприятный прогноз при правильном лечении, можно сказать, что течение заболевания является неблагоприятным в сравнении с другими интерстициальными легочными заболеваниями. Наиболее частой причиной смерти является дыхательная недостаточность (39%) и порок сердца (27%), и другие включают рак легкого, легочную эмболию и пневмонию. Прогноз более неблагоприятный, если пациент является пожилым или малообеспеченным мужчиной, или если функция легких является недостаточной ко времени диагностики или обнаружено много скоплений фибробластов при биопсии.
Как и для неспецифической интерстициальной пневмонии (NSIP), в способе терапии идиопатического фиброза легких применяют стероиды и цитотоксические лекарственные средства. В последнее время противофиброзные агенты представляют собой главное средство терапии, и с ними проводили различные исследования. В настоящее время утвержденные лекарственные средства при идиопатическом легочном фиброзе включают Пирфенидон и Нинтеданиб, и эти лекарственные средства представляют собой не полноценный терапевтический агент, а они оказывают действие по замедлению фиброза легких и облегчению симптомов. Следовательно, необходимо разработать более эффективные лекарственные средства, которые могут улучшать качество жизни пациентов.
Интерстициальное легочное заболевание, ассоциированное с системным склерозом, (SSc-ILD) представляет собой заболевание, осложнением которого является интерстициальное легочное заболевание (ILD), у пациентов с системным склерозом (SSc), и ухудшение функции легких является ведущей причиной смерти при системном склерозе. В качестве терапевтического агента, одобренного при этом заболевании в Соединенных Штатах, используют Нинтеданиб и Тоцилизумаб, для которых подтверждено действие по уменьшению ухудшения легочной функции, но существует потребность в разработке более эффективных лекарственных средств, способных улучшать качество жизни пациента, как и для идиопатического фиброза легких.
Термин "хронические фиброзирующие интерстициальные легочные заболевания с прогрессирующим фенотипом (PF-ILD)" относится к различным прогрессирующим фиброзирующим интерстициальным легочным заболеваниям за исключением идиопатического фиброза легких, включая аутоиммунную интерстициальное легочное заболевание, идиопатическую интерстициальную пневмонию и им подобные. Было подтверждено, что Нинтеданиб обладает действием по уменьшению ухудшения легочной функции у пациентов с различными фиброзными заболеваниями легких, и он одобрен в качестве терапевтического агента в Соединенных Штатах. Поскольку фиброзирующие интерстициальные легочные заболевания могут приводить к развитию прогрессирующего фенотипа, такого как фиброз легких, ухудшение функции легких и плохому качеству жизни, действия по уменьшению ухудшения функции легкого можно ожидать даже при других интерстициальных легочных заболеваниях, когда действие по уменьшению ухудшения функции легких при определенном интерстициальном легочном заболевании проявляется независимо от классификации и основного заболевания.
Между тем, PRS (пролил-тРНК-синтетаза) относится к семейству аминоацил-тРНК-синтетаз (ARS) и служит для активации аминокислот в синтезе белка. То есть, ARS выполняет функцию по образованию аминоацил-аденилата (АА-АМР) и последующему переносу активированной аминокислоты к 3'-концу соответствующей тРНК при трансляции. Поскольку ARS играет ключевую роль в синтезе белка, ингибирование ARS подавляет рост всех клеток. Поэтому ARS признана перспективной мишенью для антибиотиков или терапевтических агентов, которые должны подавлять сверхэкспрессию в клетках при заболеваниях (Nature, 2013, 494: 121-125).
PRS присутствует в мультисинтетазном комплексе (MSC) в форме глутамил-пролил-тРНК-синтетазы (EPRS) или функционирует в составе такого комплекса. В частности, среди различных MSC EPRS функционирует как сайленсер транскрипции, который подавляет продукцию васкулярно-эндотелиального фактора роста A (VEGF А), представляющего собой ключевой фактор ангиогенеза. Дополнительно сообщалось, что EPRS тесно связан с различными злокачественными солидными опухолями (Nat. Rev. Cancer, 2011, 11, 708-718).
Соответственно, автор настоящего изобретения интенсивно изучал способы предупреждения или лечения фиброза, и подтвердил, что эффективное предупреждение или лечение фиброза возможно путем использования специфического ингибитора PRS, описанного далее, по определенной схеме лечения и в определенной дозировке, тем самым выполняя настоящее изобретение.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Техническая задача
Задачей данного изобретения является предложение фармацевтической композиции для предупреждения или лечения фиброза.
Техническое решение
Для решения вышеизложенной задачи предложена следующая фармацевтическая композиция для предупреждения или лечения фиброза: фармацевтическая композиция для предупреждения или лечения фиброза, содержащая соединение, представленное следующей Химической Формулой 1, или его фармацевтически приемлемую соль для введения от 100 до 150 мг два раза в сутки (BID)
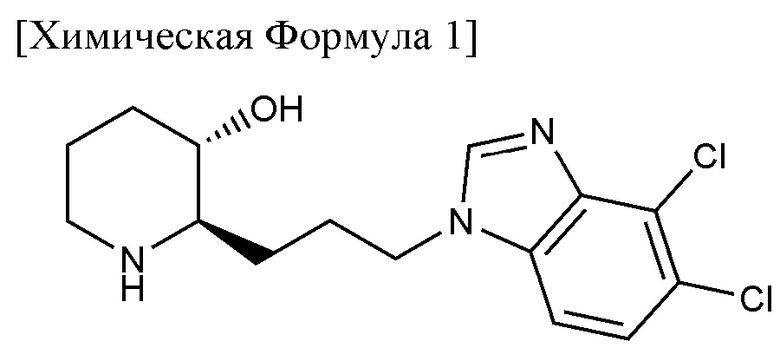
Соединение, представленное Химической Формулой 1, или его фармацевтически приемлемая соль представляет собой соединение, описанное в Патенте Кореи, зарегистрированном под №10-2084772, и в частности соединение, описанное в Примере 40 описания. Это вещество можно использовать в качестве ингибитора PRS для предупреждения или лечения фиброза.
В частности, при введении 100-150 мг два раза в сутки (BID), как в настоящем изобретении, возможно эффективное предупреждение или лечение фиброза. Указанная выше дозировка представляет собой дозировку, которая может предупреждать потенциальные риски в максимальной степени, в то же время увеличивая превентивный или терапевтический эффект соединения, представленного Химической Формулой 1, или его фармацевтически приемлемой соли в отношении фиброза. Далее, площадь под кривой зависимости концентрации лекарственного средства в плазме от времени (AUCinf) после введения соединения, представленного Химической Формулой 1, или его фармацевтически приемлемой соли, то есть времени воздействия на организм, может демонстрировать оптимальные результаты в плане предупреждения или лечения фиброза в зависимости от дозировки.
Между тем, соединение, представленное Химической Формулой 1, можно использовать в форме фармацевтически приемлемой соли. В качестве соли полезна соль присоединения кислоты, образованная фармацевтически приемлемой свободной кислотой. В качестве свободной кислоты можно использовать неорганическую кислоту и органическую кислоту. Примеры неорганической кислоты могут включать соляную кислоту, бромноватую кислоту, серную кислоту, фосфорную кислоту и им подобные. Примеры органической кислоты могут включать лимонную кислоту, уксусную кислоту, молочную кислоту, малеиновую кислоту, глюконовую кислоту, метансульфоновую кислоту, янтарную кислоту, 4-толуолсульфоновую кислоту, глутаминовую кислоту, аспарагиновую кислоту или им подобные. Предпочтительно фармацевтически приемлемая соль соединения, представленного Химической Формулой 1, представляет собой гидрохлорид.
Далее, соединение, представленное Химической Формулой 1, можно получить в кристаллической форме или некристаллической форме. Когда соединение, представленное Химической Формулой 1, получено в кристаллической форме, оно возможно может быть гидратированным или сольватированным. Настоящее изобретение может включать не только стехиометрические гидраты соединения, представленного Химической Формулой 1, но также соединения, содержащие различное количество воды. Сольваты соединения, представленного Химической Формулой 1, включают как стехиометрические сольваты, так и нестехиометрические сольваты.
Между тем, примеры фиброза включают интерстициальное легочное заболевание (ILD), склеродерму, келоид, гипертрофический рубец, неалкогольную жировую болезнь печени, первичный склерозирующий холангит (PSC), первичный билиарный холангит (РВС), диабетическую ретинопатию, возрастную макулодистрофию (AMD), гипертрофическую кардиомиопатию, инфаркт миокарда, мышечную дисрофию, диабетическую болезнь почек, фокально-сегментарный гломерулосклероз (FSGS) или воспалительное заболевание кишечника (IBD). Интерстициальное легочное заболевание (ILD) включает идиопатический фиброз легких (IPF), интерстициальное легочное заболевание, ассоциированное с системным склерозом, (SSc-ILD) или хроническое фиброзирующее интерстициальное легочное заболевание с прогрессирующим фенотипом (PF-ILD).
Термин "предупреждение", как его используют здесь, относится к любому действию по замедлению или ингибированию возникновения, распространения или рецидивирования рака, воспалительного заболевания, аутоиммунного заболевания или фиброза путем введения композиции по настоящему изобретению, и термин "лечение" относится к любому действию по улучшению или изменению в лучшую сторону симптомов вышеупомянутого заболевания путем введения композиции по настоящему изобретению.
Фармацевтическую композицию по настоящему изобретению можно изготавливать в форме препаратов для перорального или парентерального введения в соответствии со стандартной фармацевтической практикой. Дополнительно к активному компоненту эти композиции могут содержать добавки, такие как фармацевтически приемлемый носитель, адьювант или разбавитель.
Подходящие носители включают, например, физиологический раствор, полиэтиленгликоль, этанол, растительное масло и изопропилмиристат и тому подобное. Разбавители включают, например, лактозу, декстрозу, сахарозу, маннит, сорбит, целлюлозу и/или глицин и тому подобное, но не ограничиваясь ими. Далее, соединения по настоящему изобретению можно растворять в маслах, пропиленгликоле или других растворителях, обычно используемых при изготовлении инъецируемых растворов. Более того, соединения по настоящему изобретению можно изготавливать в форме мазей или кремов для местного нанесения.
В фармацевтических дозированных формах соединений по настоящему изобретению их также можно использовать в форме их фармацевтически приемлемой соли или сольвата, и их можно использовать по отдельности или в комбинации с другими фармацевтически активными соединениями, а также в подходящих комбинациях. В одном примере фармацевтическая композиция по настоящему изобретению может дополнительно включать другие активные компоненты, используемые для предупреждения или лечения фиброза. Примеры таких других активных компонентов включают Пирфенидон или Нинтеданиб. Кроме того, когда фармацевтическая композиция по настоящему изобретению дополнительно содержит другой активный компонент, массовое соотношение соединения, представленного Химической Формулой 1, или его фармацевтически приемлемой соли, и другого активного компонента составляет предпочтительно от 1:0,1 до 1:10.
Соединения по настоящему изобретению можно изготавливать в форме инъекций путем растворения, ресуспендирования или эмульгирования соединений в водных растворителях, таких как обычный физиологический раствор или 5%-ный декстрин, или в неводных растворителях, таких как синтетические глицериды жирных кислот, сложные эфиры высших жирных кислот или пропиленгликоль. Композиция по настоящему изобретению может включать традиционные добавки, такие как солюбилизаторы, изотонические агенты, суспендирующие агенты, эмульгирующие агенты, стабилизаторы и консерванты.
Фармацевтическую композицию по настоящему изобретению можно вводить пероральным или парентеральным путем. В зависимости от способа введения композиция по настоящему изобретению может содержать от 0,001 до 99% по массе, предпочтительно от 0,01 до 60% по массе соединения, представленного Химической Формулой 1, или его фармацевтически приемлемой соли.
Фармацевтическую композицию по настоящему изобретению можно вводить млекопитающим, таким как крыса, мышь, домашнее животное, человек, различными путями. Введение можно выполнять любыми возможными способами, например путем перорального, ректального, внутривенного, внутримышечного, подкожного, внутриматочного, интрацеребровентрикулярного введения.
Полезные эффекты изобретения
Как описано выше, фармацевтическую композицию по настоящему изобретению используют в определенной схеме лечения и дозировке, и ее можно с пользой применять для предупреждения или лечения фиброза.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг. 1 представлены результаты оценки функции легких из Экспериментального Примера 1-1.
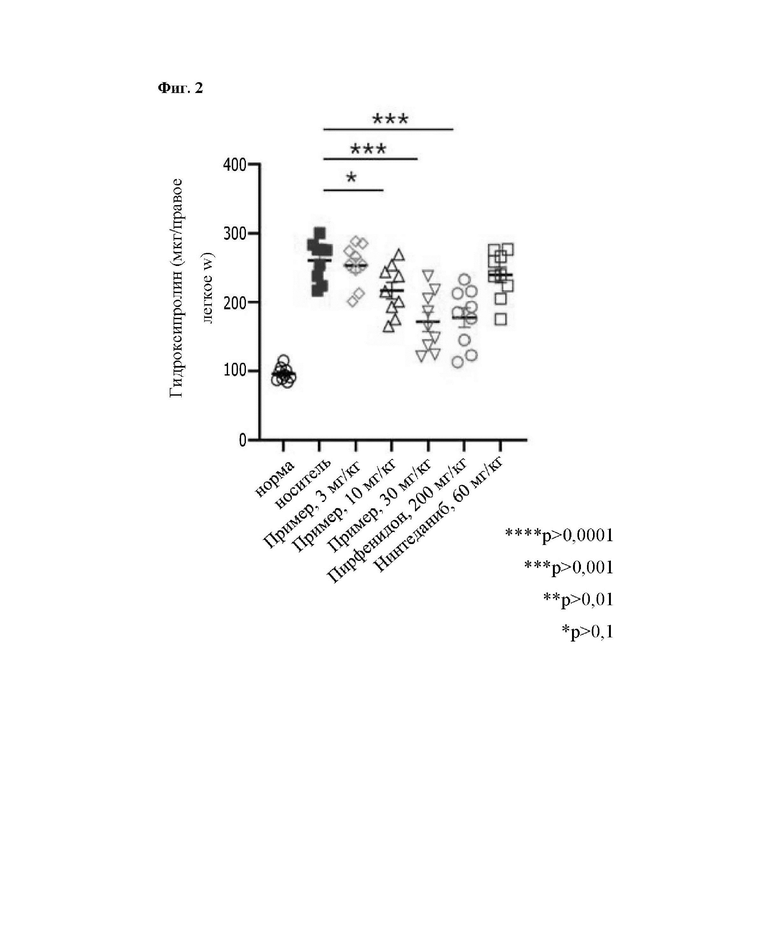
На Фиг. 2 представлены результаты измерения содержания коллагена в легких из Экспериментального Примера 1-2.
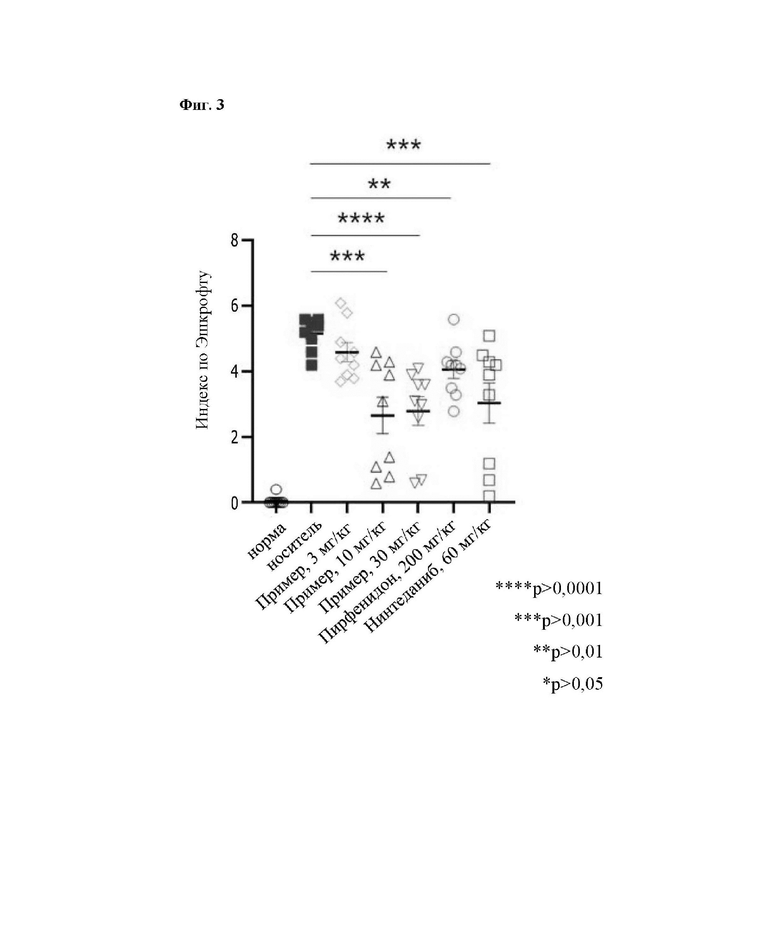
На Фиг. 3 представлены результаты гистопатологического анализа из Экспериментальных Примеров 1-3.
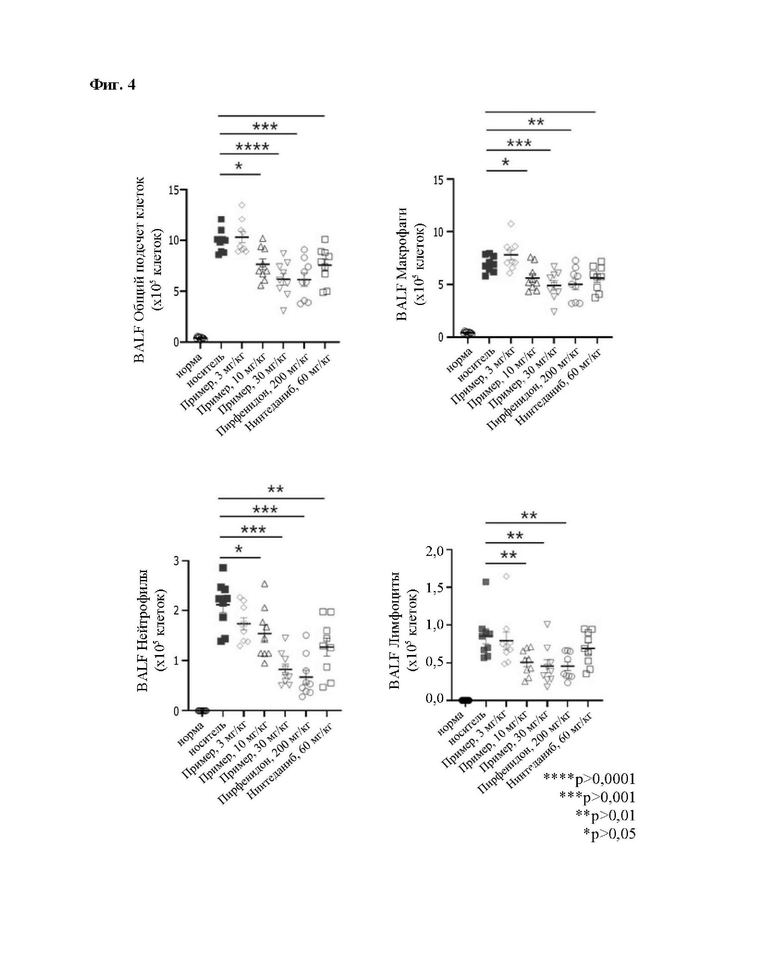
На Фиг. 4 представлены результаты анализа инфильтрации клетками воспаления из Экспериментального Примера 1-4.
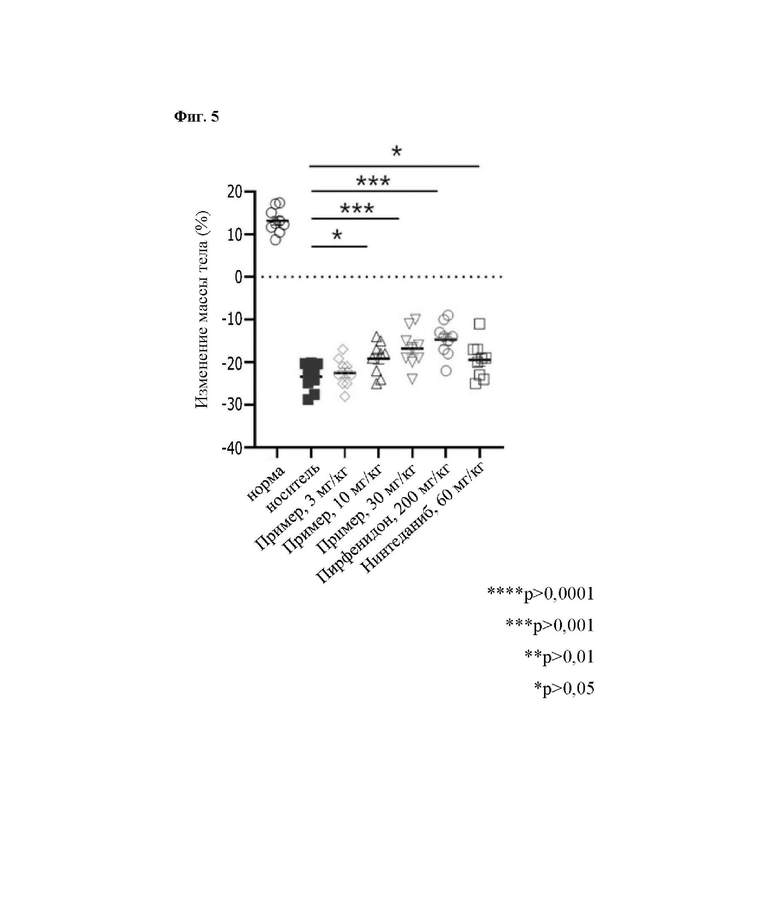
На Фиг. 5 представлены результаты измерений изменения массы из Экспериментальных Примеров 1-5.
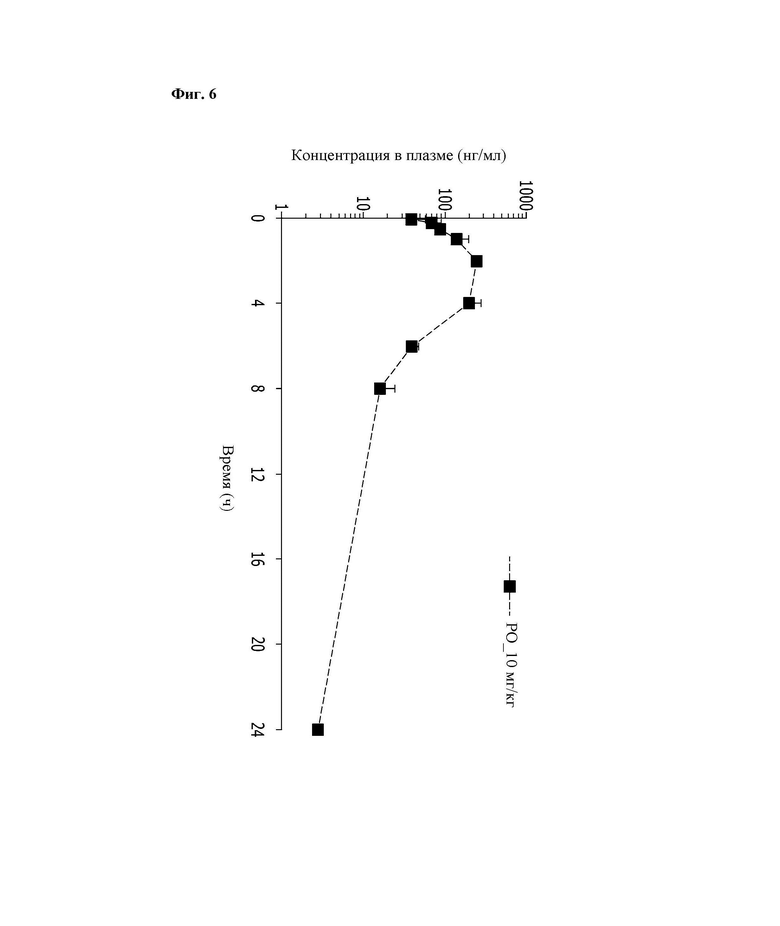
На Фиг. 6 показано изменение концентрации активного компонента в крови из Экспериментального Примера 3.
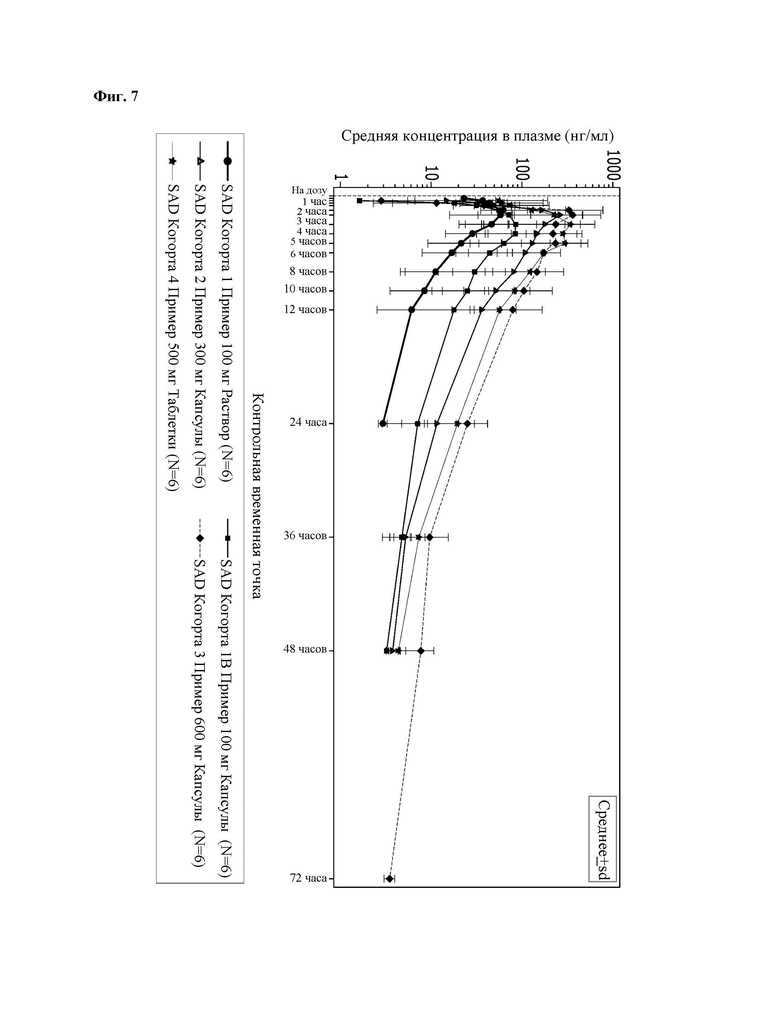
На Фиг. 7 показано изменение концентрации в плазме для однократного введения из Экспериментального Примера 4.
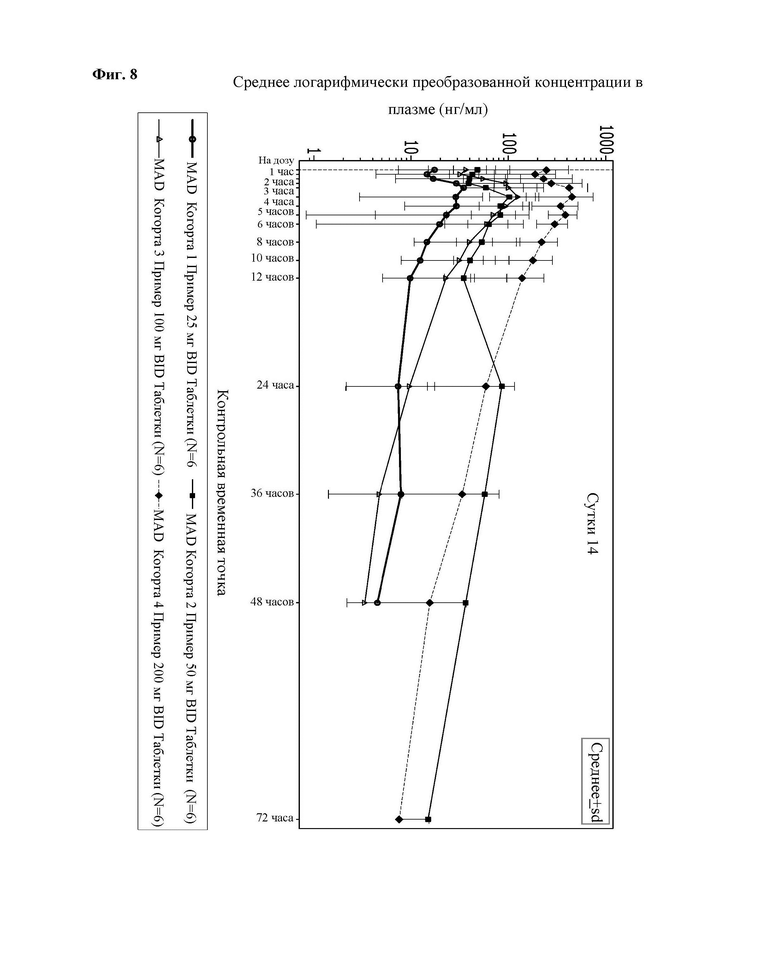
На Фиг. 8 показаны изменения концентрации в плазме для множественных введений из Экспериментального Примера 4.
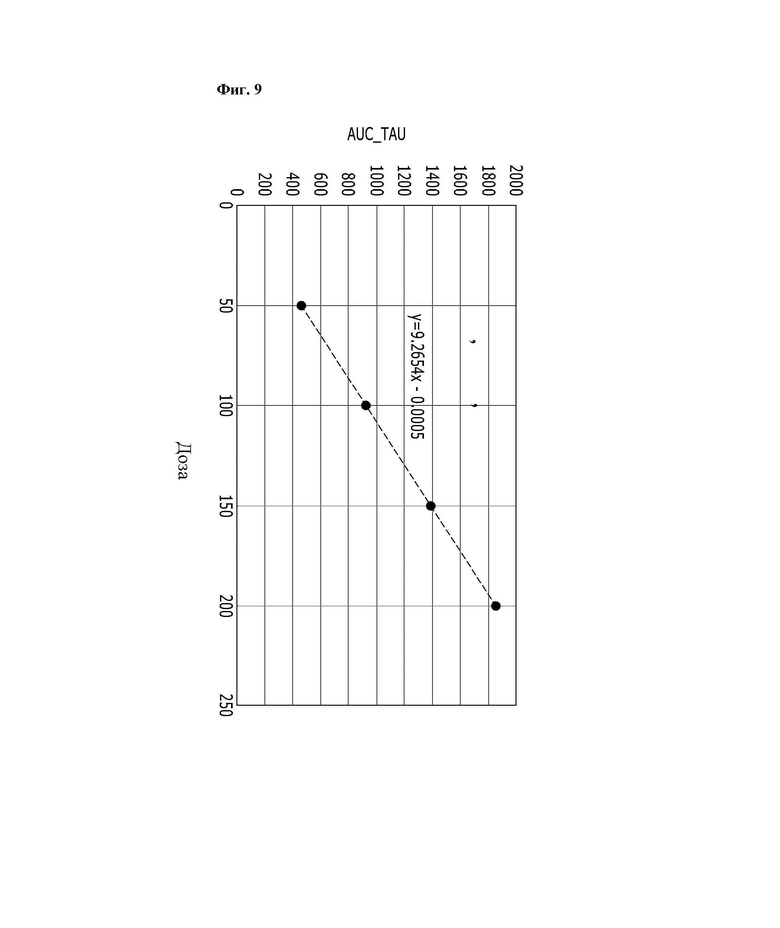
На Фиг. 9 представлен график, показывающий зависимость AUC от дозы, введенной в Экспериментальном Примере 4.
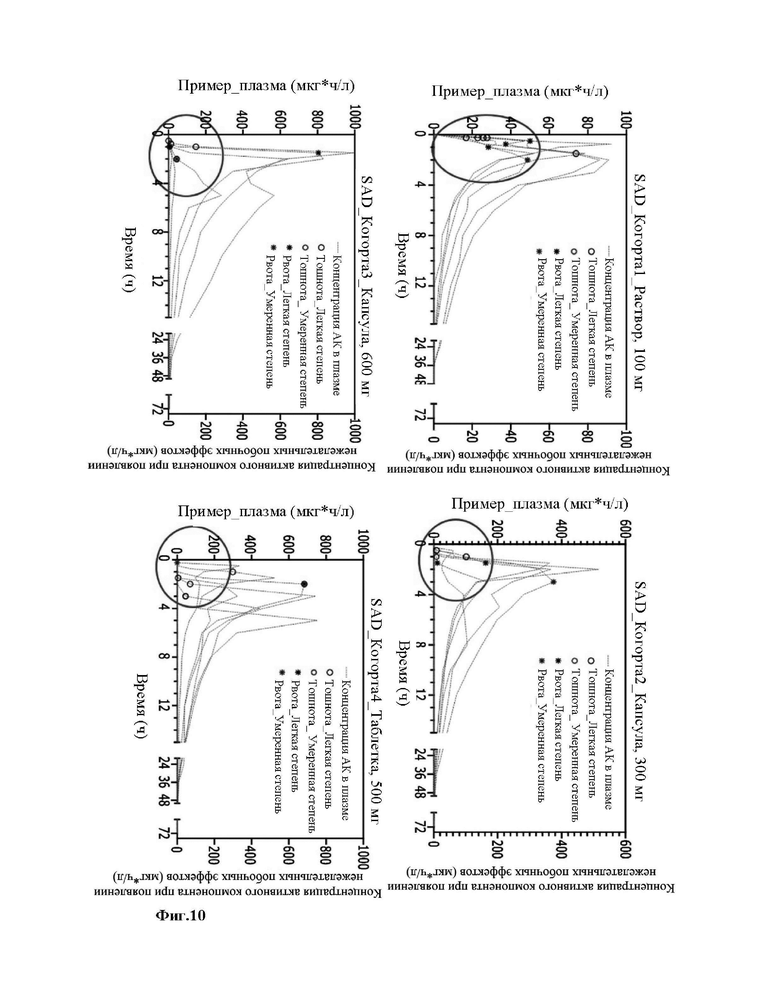
На Фиг. 10 показано соотношение между временем появления побочных эффектов, тошноты и рвоты, и временем воздействия на организм в Экспериментальном Примере 5.
ПОДРОБНОЕ ОПИСАНИЕ ВОПЛОЩЕНИЙ
Далее настоящее изобретение будет описано более подробно посредством примеров. Однако эти примеры предназначены исключительно для иллюстративных целей, и их не следует рассматривать как ограничивающие объем настоящего изобретения каким-либо образом.
ПРИМЕР
Следующее соединение было получено таким же способом как в Примере 40 Патента Кореи, зарегистрированного под №10-2084772, и здесь и далее оно обозначено как "активный компонент" или "Пример"
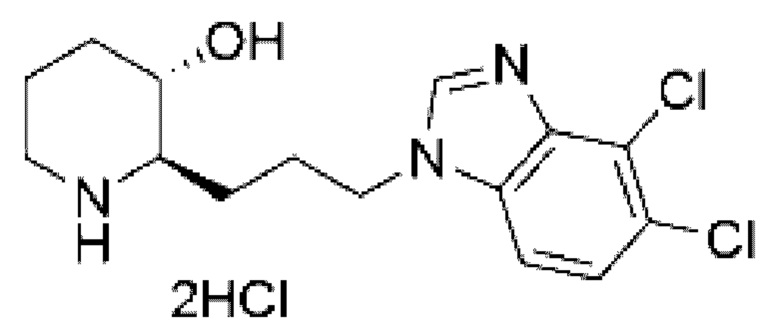
1Н NMR (500 MHz, MeOD): δ 9.67 (s, 1H). 8.02 (d, 1H), 7.82 (d, 1H), 4.62 (m, 2H), 3.60 (m, 1H), 3.28 (m, 1H), 2.99 (m, 2H), 2.25 (m, 2H), 2.08 (m, 2H), 1.99 (m, 1H), 1.78 (m, 2H), 1.54 (m, 1H).
Экспериментальный Пример 1: Эксперимент на животных по противофиброзной эффективности при введении дозы
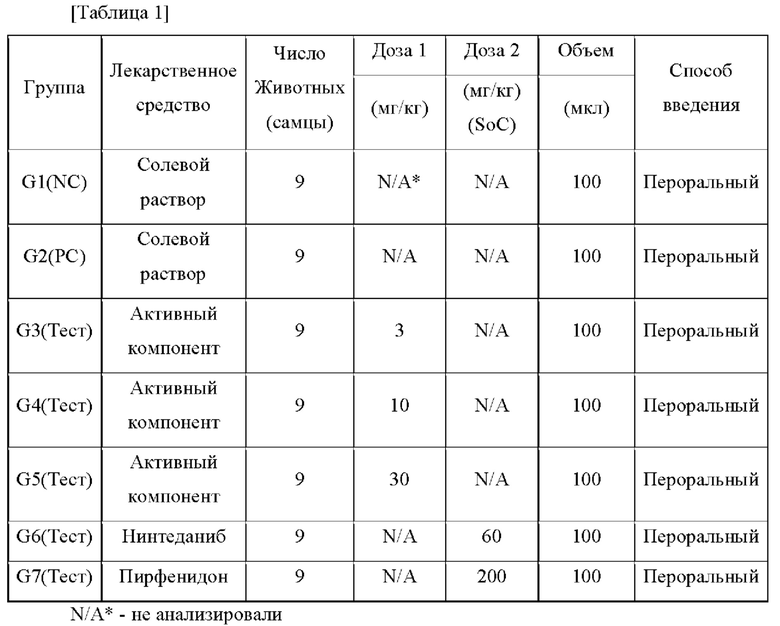
70-100 мкл раствора BLM (блеомицин 1-3 мг/кг) вводили в легкое акклиматизированных экспериментальных животных с помощью катетера в течение 5 суток или дольше. В соответствии с задачей теста тестируемое лекарственное средство вводили в течение 7 суток после введения BLM, и лекарственное средство вводили перорально в течение 2 недель до 21-ых суток от введения BLM. Состав экспериментальной группы показан в Таблице 1 ниже. Массу тела, SpO2, гидроксипролин и число клеток воспаления измеряли для определения противофиброзной эффективности активного компонента.
В контрольной группе использовали Нинтеданиб (здесь и далее 'NIN') и Пирфенидон (здесь и далее 'PID'), представляющие собой стандартные лекарственные средства (здесь и далее 'SoC') для лечения идиопатического фиброза легких. Используемая эффективная доза NIN подтверждена данными литературы по эффективности in vivo, опубликованными Boehringer Ingelheim, представляющей собой компанию по разработке NIN, и эффективная доза PID для мышей была установлена на основе данных по эффективности (на крысах) и токсичности 2-недельной повторной дозы (для крыс) из "FDA Pharmacology Review".
Экспериментальный Пример 1-1: Оценка функции легких
Оценка функции легких представляет собой самый прямой и важный оценочный показатель, который оказывает самое большое влияние на симптомы и качество жизни пациентов с фиброзом легких, и представляет собой исследование, которое может наиболее прямо показать действие по улучшению функции легких на животной модели фиброза легких путем измерения концентрации кислорода в организме.
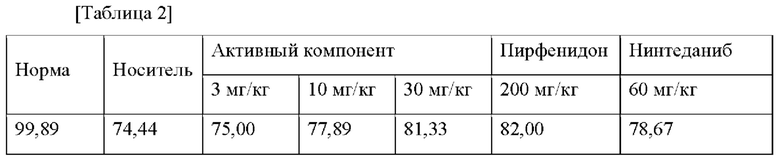
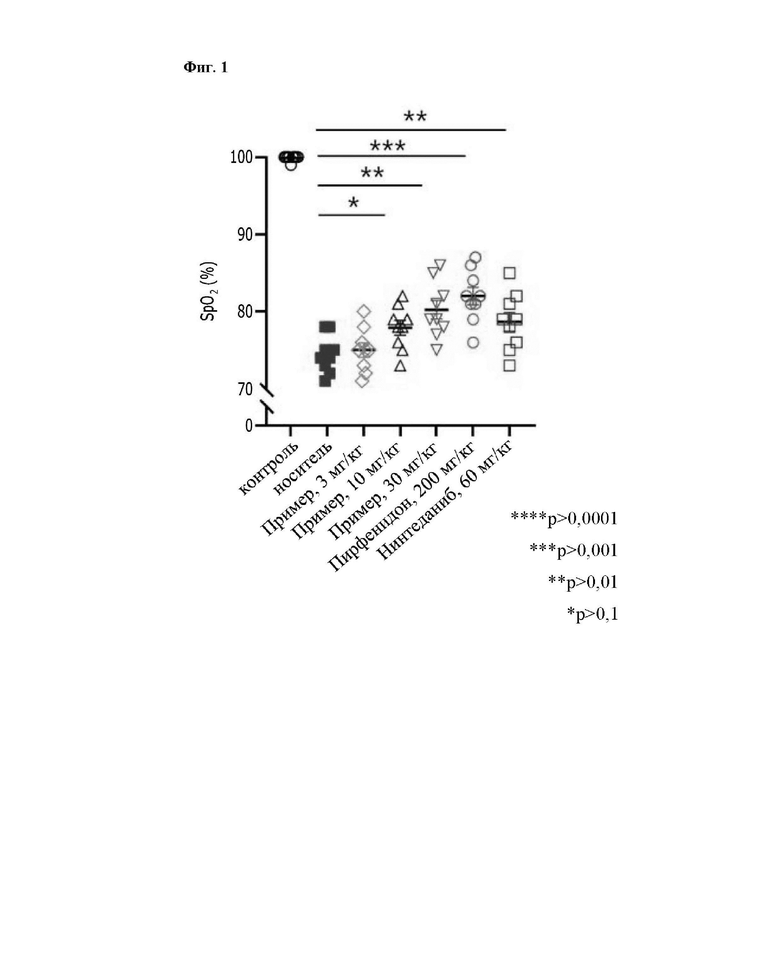
На 21-е сутки проводили измерения с помощью устройства для измерения SpO2 (Berry, Ветеринарный пульсоксиметр) через брюшную сторону мыши, и результаты показаны в Таблице 2 и на Фиг. 1.
Было проведено исследование для подтверждения функции по проникновению кислорода в легкие путем измерения SpO2 в животе мышей. Было подтверждено, что по сравнению с группой носителя эта функция улучшилась на 18% или более в группе обработки 10 мг/кг "активного компонента" и на 28% или более в группе обработки 30 мг/кг. Было подтверждено, что это составляет такую же степень улучшения функции проникновения кислорода, как для имеющегося в наличии вещества SoC. Этот результат подтверждает, что при введении "активного компонента" имеет место прямое действие по улучшению функции легких через увеличение проникновения кислорода, которое было снижено в процессе фиброза легких.
Экспериментальный Пример 1-2: Измерение общего содержания коллагена в легком
Фиброз легких представляет собой накопление коллагена в легких, которое делает их неэластичными. Основная причина фиброза легких заключается в накоплении коллагена, и степень развития фиброза можно предсказать путем измерения содержания коллагена в ткани легкого.
В этом экспериментальном примере выполняли анализ с использованием "INSOLUBLE Collagen Assay" (Biocolor, S2000). После умерщвления на 21-ые сутки криоконсервированную ткань легкого измельчали путем добавления 100 мкл Реагента Фрагментации и затем добавляли 100 мкл 37%-ной HCl и инкубировали при 65°С в течение 3 часов. Содержимое пробирки встряхивали через 30-минутные интервалы для облегчения разрушения ткани. После центрифугирования концентрацию доводили до 100 мкл и проводили окрашивание коллагена для получения образца. Поглощение измеряли при 560 нм. Величину соотношения измеряли путем сравнения значения для гидроксипролина с таковым в группе нормы, и результаты показаны в Таблице 3 и на Фиг.2.
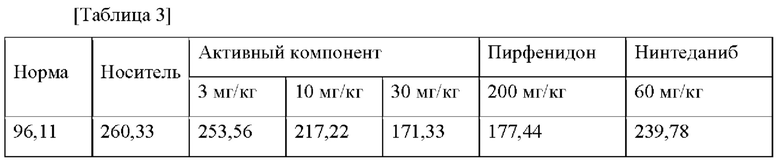
Результаты этого эксперимента подтверждают, что содержание коллагена в легких было значительно снижено в группах обработки 10 и 30 мг/кг "активного компонента" по сравнению с группой носителя, что представляет собой результат, сходный с таковым для PID, представляющим собой имеющееся в наличии вещество SoC. Из результатов этого эксперимента видно, что степень фиброза легких во время введения активного компонента снижалась.
Экспериментальный Пример 1-3: Гистопатологический анализ (шкала Эшкрофта)
Степень фиброза и воспаления ткани легкого визуально наблюдали в микроскоп, и степень фиброза ткани легкого измеряли с помощью индекса фиброза в соответствии с нормализованными критериями. Чем выше значение индекса фиброза, тем тяжелее степень и симптомы фиброза. Можно интерпретировать так, что чем ниже значение, тем легче симптомы.
На 21-ые сутки ткань легкого отделяли и окрашивали красителями Н&Е и МТ и исследовали при 200-кратном увеличении. Наблюдаемые результаты оценивали по Эшкрофту (Hubner et al., 2008). Индекс фиброза рассчитывали путем деления суммы скорректированных баллов полей Эшкрофта на число протестированных полей, и он показан в Таблице 4 и на Фиг. 3.
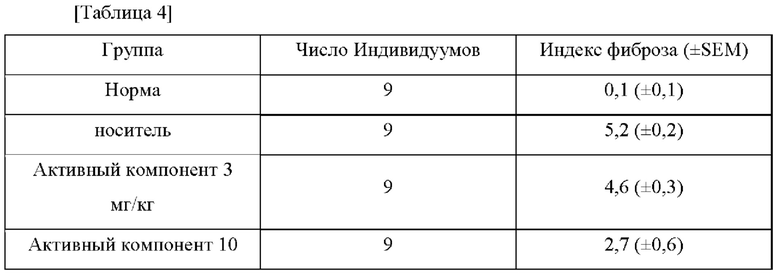
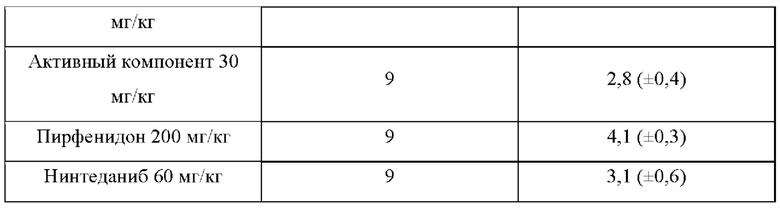
В группах 10 и 30 мг/кг "активного компонента" было подтверждено действие по улучшению ткани эквивалентное или более чем эквивалентное, чем для NIN, и было подтверждено превосходное действие по улучшению ткани по сравнению с PID.
Экспериментальный Пример 1-4: Анализ по подсчету клеток воспаления
Поскольку фиброз представляет собой хроническое воспалительное заболевание, характеризуемое избыточным отложением коллагена, инфильтрацию клетками воспаления анализировали для определения степени воспаления в ткани легкого.
После умерщвления на 21-ые сутки введения клетки BALF (жидкость бронхоальвеолярного лаважа), полученные путем промывания воздухоносных путей мышей, разводили в 1,05 X PBS (забуференный фосфатом физиологический раствор) и наносили на предметное стекло, и затем это стекло окрашивали красителями Дифф-квик в порядке 1, 2, 3 следующим образом: смачивали красителем и удаляли его через 30 секунд. Подсчет вели на 500 клеток. Макрофаги являются самыми крупными клетками, мононуклеарными и окрашиваются синим. Нейтрофилы и эозинофилы представляют собой многоядерные клетки, но эозинофилы окрашиваются красным эозином и отличаются от нейтрофилов. Лимфоциты имеют очень мало цитоплазмы и являются такими же маленькими по размеру как моноциты. Подсчитывали общее число клеток и переводили в %, и результат показан в Таблице 5 и на Фиг. 4.
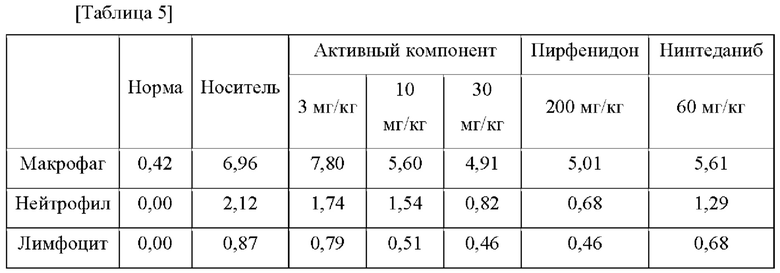

По результатам этого эксперимента можно видеть, что по сравнению с группой носителя общее число клеток было улучшено на 20% или более при использовании 10 мг/кг "активного компонента" и на 30% или более при использовании 30 мг/кг такового, что свидетельствует об уменьшении воспаления ткани легкого. В частности, было подтверждено, что клетки нейтрофилы представляют собой клетки воспаления, которые показывают высокий уровень фибротического воспаления легкого, и число этих клеток было снижено на 20% или более при использовании 10 мг/кг "активного компонента" и на 60% или более при использовании 30 мг/кг по сравнению с группой носителя, так что соотношение основных клеток воспаления было значительно улучшено. Можно видеть, что этот уровень эквивалентен уровню в группе PID, представляющего собой имеющееся в наличии вещество SoC, и является действием, превосходящее таковое NIN.
Экспериментальный Пример 1-5: Измерение изменения массы тела
Масса тела является непрямым показателем, по которому можно судить о степени улучшения общего физического состояния животной модели. Когда степень потери массы является небольшой, можно считать, что общее физическое состояние или симптомы заболевания улучшены.
Массу тела измеряли с помощью весов на 21-ые сутки при завершении введения, и результаты представлены в Таблице 6 ниже и на Фиг. 5.
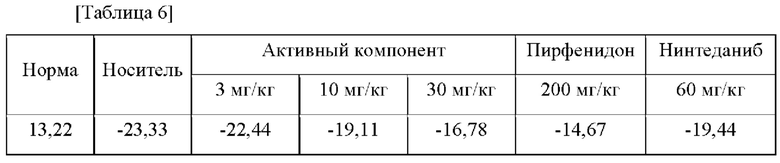
Подтверждено, что степень потери массы тела улучшена в группах 10 мг/кг и 30 мг/кг по сравнению с группой носителя. Подтверждено, что уровень этого улучшения близок к таковому для вещества SoC или больше него, и в целом симптомы улучшены при введении "активного компонента".
На основании результатов описанной выше серии экспериментов можно подтвердить, что при введении мышам "активного компонента" в количестве 10 мг/кг массы организма два раза в сутки уровень терапевтического действия эквивалентен имеющемуся в наличии стандартному лечению IPF.
Экспериментальный Пример 2: 2-недельный тест на токсичность повторяющейся дозы у мышей
Активный компонент вводили перорально акклиматизированным мышам ICR в течение 7 суток или более в течение 2 недель. Состав экспериментальной группы был таким, как показано в Таблице 7 ниже, и выполняли измерение массы тела, наблюдение общих симптомов, гематологический/биохимический анализ крови, измерение массы органа и гистопатологические тесты.
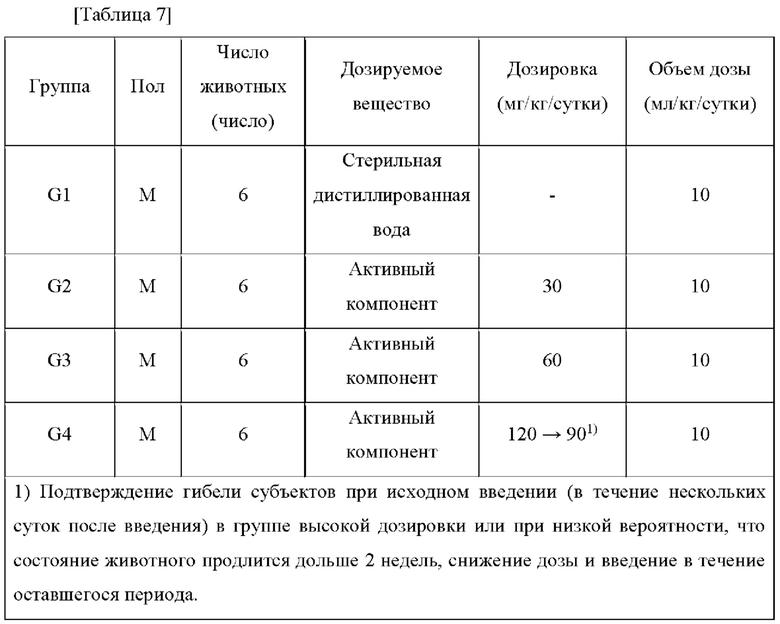
После введения в течение 2 недель проводили аутопсию для всех животных. При аутопсии измеряли массу каждого органа. Никакой токсичности или существенных патологических симптомов не было обнаружено во всех результатах, измеренных после введения, повторяющегося в течение 2 недель. Однако, как показано в Таблице 8 ниже, при введении группе 30 мг/кг/сутки или более наблюдали небольшую тенденцию к потере массы только для селезенки и тимуса из всех органов.
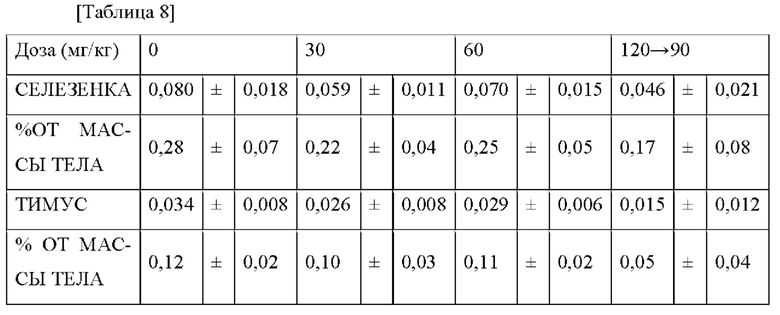
Такие результаты считают не связанными с токсичностью, но на основании тенденции к потере массы селезенки и тимуса активную дозу активного компонента устанавливали на 10 мг/кг для предупреждения потенциального риска токсичности при длительном введении.
Экспериментальный Пример 3: Анализ фармакокинетики/фармакодинамики у животных
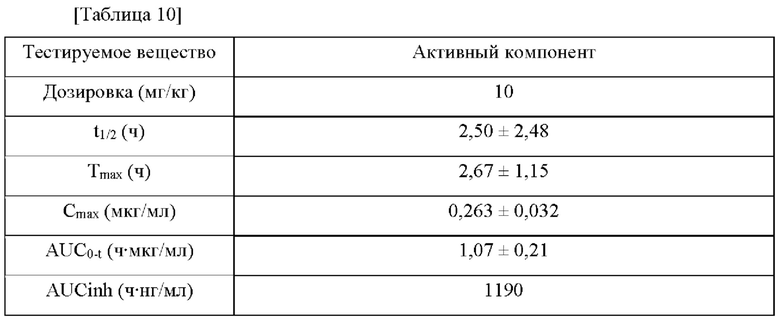
Фармакокинетический тест после однократного перорального введения активного компонента мышам ICR проводили как показано в Таблице 9 ниже. Фармакокинетические параметры рассчитывали с использованием программного обеспечения Excel® и WinNonlin6.1 для концентрации лекарственного средства в крови с учетом изменения с течением времени, измеренной методом LC-MS/MS (жидкостная хроматография-масс-спектрометрия/масс-спектрометрия), и изменения концентрации активного компонента в крови показаны в Таблице 9 и на Фиг. 6.
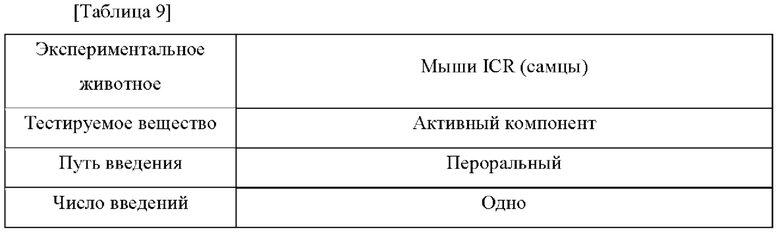

Пример получения 1: Получение капсул с энтеросолюбильным покрытием, содержащих активные компоненты
Дозу только основных компонентов без каких-либо дополнительных эксципиентов помещали в капсулы к активному компоненту в форме гидрохлорида, при этом использовали капсулы Vcaps® с энтеросолюбильным покрытием.
Пример получения 2: Получение таблеток с энтеросолюбильным покрытием, содержащих активный компонент
Микрокристаллическую целлюлозу, гидрат лактозы, кросповидон и стеарат магния смешивали с активным компонентом в форме гидрохлорида, формовали в прессованный продукт в форме пластинки с помощью сухого гранулятора и измельчали в осцилляторе для получения сухих гранул. Микрокристаллическую целлюлозу, гидрат лактозы и стеарат магния дополнительно смешивали с гранулированным материалом, подвергали формованию под давлением для получения таблеток и покрывали энтеросолюбильным покрытием для завершения процесса.
Экспериментальный Пример 4: Анализ фармакокинетики/фармакодинамики у человека
Для подтверждения безопасности/переносимости/pK в организме человека было разработано рандомизированное двойное слепое плацебо-контролируемое исследование с однократным введением и постепенным увеличением дозы для 72 здоровых взрослых, как показано в Таблице 11. Композиция, используемая в этом клиническом испытании, была получена таким же способом как в Примерах Получения 1 и 2.
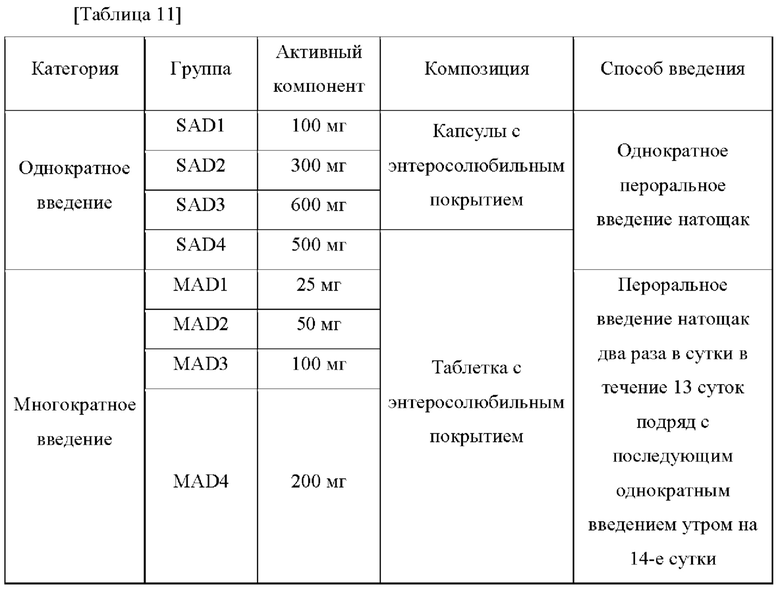
В результате описанного выше клинического испытания никакие серьезные патологические признаки или побочные эффекты не были подтверждены.
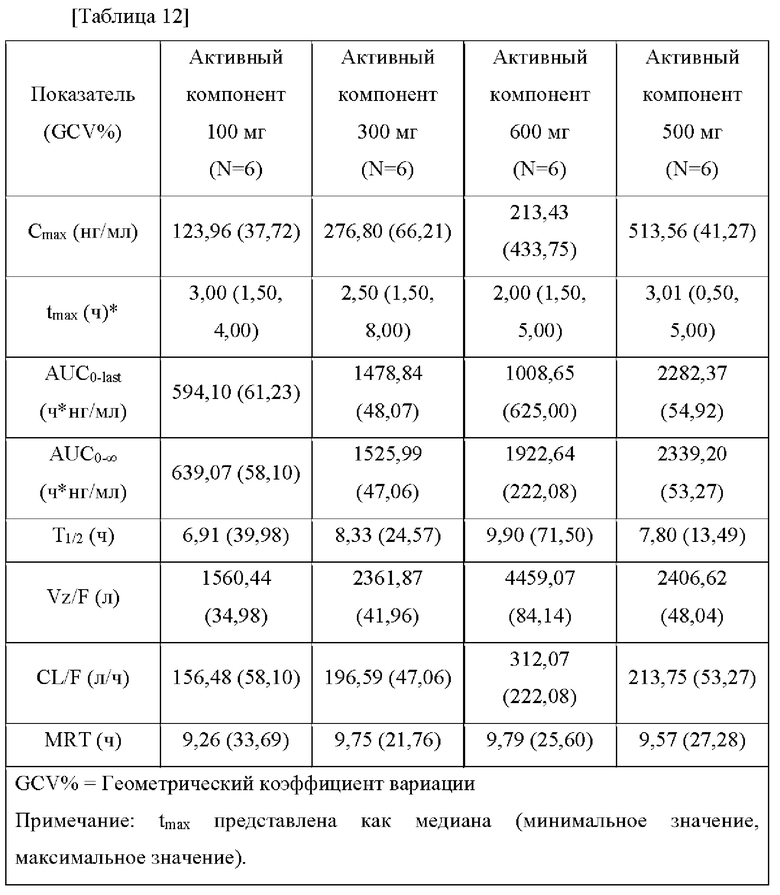
В результате подтверждения pK для однократного введения, как можно видеть из Таблицы 12 ниже и Фиг. 7, максимальные концентрации в плазме зарегистрированы в промежутке от 1,5 до 8 часов после введения, и геометрическое среднее периода полувыведения находилось в диапазоне от 6,91 часов до 9,90 часов, и концентрации в плазме увеличивались прямо пропорционально дозе.
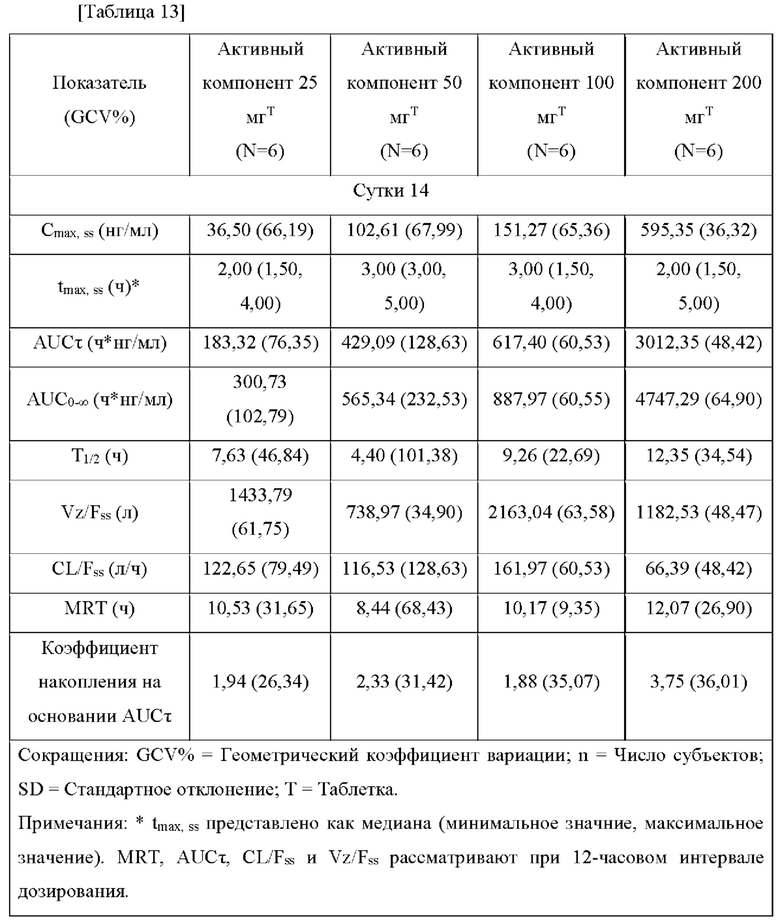
Дополнительно, как можно видеть в Таблице 13 и на Фиг. 8, на 14-ые сутки результаты по подтверждению pK для многократного введения подтвердили, что максимальная концентрация в плазме была зарегистрирована в промежутке от 1,5 до 5 часов в стационарном состоянии после введения, геометрическое среднее периода полувыведения варьировало в диапазоне от 4,4 часов до 12,35 часов, и среднее геометрическое интервала дозы экспозиции in vivo (AUCτ) варьировало от 183,32 до 3012,35 ч нг/мл. Было подтверждено, что концентрации в плазме находятся в линейной зависимости от дозы в диапазоне доз от 25 мг до 200 мг активного компонента.
Следовательно, оптимальные фармакокинетические параметры модели, которые могут объяснить изменения в концентрациях всех доз, наблюдаемых с использованием программного обеспечения Excel® и WinNonlin8.1 оценивали для концентрации лекарственного средства в крови, полученной в многодозовом клиническом испытании на человеке. Уровень воздействия у людей был предсказан при различных перорально вводимых дозах, и основные результаты показаны в Таблице 14 ниже.
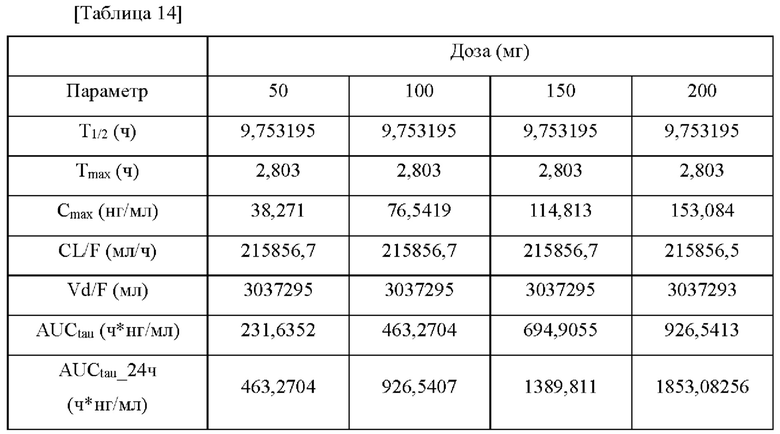
Результаты эксперимента на экспериментальной модели фиброза легких у мышей из Экспериментального Примера 2 подтвердили, что введение 10 мг/кг один раз в сутки представляет собой эффективную дозу для крыс, и в Экспериментальном Примере 3 значение AUCinf в плазме при эффективной дозе составило 1190 ч⋅нг/мл. Следовательно для предсказания дозы, которая, как ожидается, обеспечит значение AUCinf в организме человека на таком же уровне, как эффективная доза у крыс, была рассмотрена корреляция AUC с введенной дозой, как показано на Фиг. 9, и в результате было подтверждено, что введение 150 мг является необходимым при намерении вводить человеку дозу два раза в сутки.
Экспериментальный Пример 5: Анализ безопасности/переносимости лекарственного средства при введении человеку
Безопасность и устойчивость к лекарственному средству для соединения по настоящему изобретению при введении человеку были подтверждены таким же образом как в Экспериментальном Примере 4.
В результате исследования безопасности и переносимости при однократном введении было выявлено, что наиболее частыми побочными реакциями были желудочно-кишечные нежелательные побочные эффекты (АЕ), включая тошноту, рвоту, диарею и боль в животе. Среди них тошноту и рвоту оценивали как вносящие существенный вклад в безопасность и устойчивость к лекарственному средству. Было подтверждено, что эти эффекты вызваны самим активным компонентом (АК). В результате исследования зависимости между временем появления этих побочных эффектов в виде тошноты и рвоты и временем воздействия на организм, как показано на Фиг. 10, было подтверждено, что большинство эпизодов происходит до того, как повышается концентрация в крови. Было обнаружено, что тошнота и рвота, возникающие при введении активного компонента, оказывают воздействие на желудочно-кишечный тракт, раздражая блуждающий нерв и, следовательно, активируя рвотный центр, а не вызывают активацию рвотного центра через стимуляцию хеморецептор-индуцируемого сайта в организме при контакте с кровью.
Следовательно, можно видеть, что способ введения эффективной дозы, разделенной на два приема в сутки для уменьшения уровня стимуляции блуждающего нерва, действующего на желудочно-кишечный тракт, является более приемлемым для активного компонента.
Экспериментальный Пример 6: Подтверждение терапевтического действия на человека
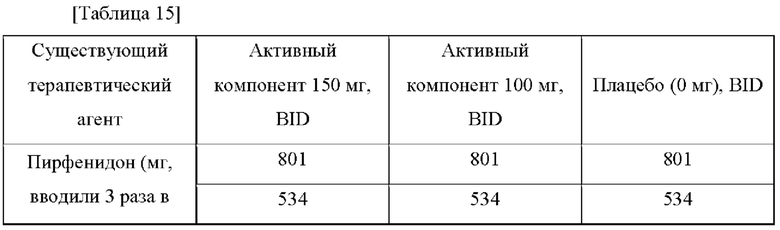
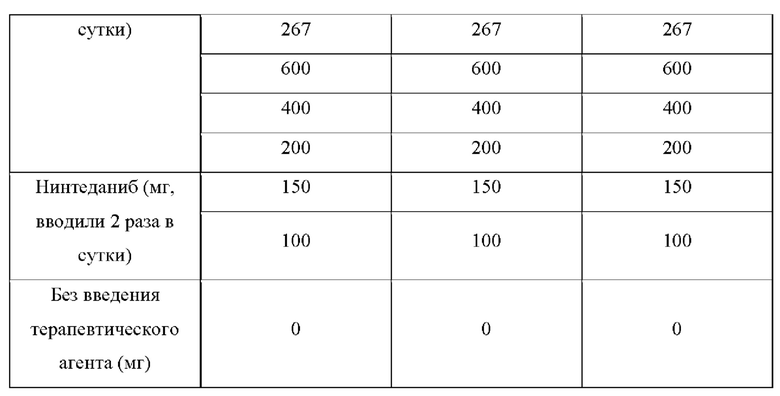
Для подтверждения безопасности и эффективности активного компонента у пациентов с идиопатический фиброзом легких было разработано рандомизированное двойное слепое плацебо-контролируемое исследование для группы обработки стандартного лечения или группы без обработки, как показано в Таблице 15. Для подтверждения безопасности и переносимости активного компонента после лечения активным компонентом в течение 24 недель его оценивали в сравнении с плацебо. Для подтверждения терапевтического эффекта активного компонента в отношении идиопатического фиброза легких после лечения активным компонентом в течение 24 недель уровень уменьшения форсированной жизненной емкости легких (FVC) относительно базового значения через 24 недели оценивали как первичную переменную оценки эффективности после введения активного компонента в течение 24 недель. В качестве вторичной переменной валидации оценивали: 1) смертность или госпитализацию, связанные с ремпираторными заболеваниями, острое ухудшение IPF, относительное уменьшение значения FVC на 10% или более относительно нормального значения и время до развития заболевания IPF, включая абсолютное уменьшение величины Hgb-скорректированной диффузионной способности минооксида углерода (DLCO) на 15% или более от нормального предсказанного уровня; 2) время, необходимое для незапланированной первой госпитализации во всех случаях в течение 24 недель; 3) изменения функциональной двигательной способности по сравнению с базовым уровнем по оценке расстояния, зарегистрированного в 6-минутном тесте ходьбы (6MWT) на неделе 24; 4) изменение уровней DLCO (с поправкой на Hgb) относительно базового значения на неделе 24; 5) категориальная оценка абсолютного изменения прогностической ценности FVC в процентах относительно базового уровня на неделе 24; 6) изменение количественных значений при компьютерной томографии грудной клетки высокого разрешения (HRCT) относительно базового уровня на неделе 24; 7) изменения по оценке результатов пациентами (PRO) относительно базового уровня по опроснику для больных с респираторными заболеваниями больницы Святого Георгия, SGRQ, и живущих с идиопатический фиброзом легких (L-IPF) на неделе 24, и тому подобное. В качестве экспериментальной переменной оценки валидности оценивали: 1) изменение IPF-специфических биомаркеров по сравнению с базовым уровнем на неделе 24; 2) изменения биомаркеров в крови по сравнению с базовым уровнем через 24 недели. В качестве переменных оценки безопасности оценивали: 1) появление патологических реакций, возникающих после введения активного компонента; 2) данные медицинского осмотра; 3) электрокардиограмму в 12 отведениях; 4) проявления жизненной силы; 5) результаты клинических лабораторных тестов, и тому подобное.
Целевую группу разделяли на пациентов, получающих Пирфенидон в качестве существующего стандарта лечения, пациентов, получающих Нинтеданиб, и пациентов, не получающих никакого лечения, и эффект, возникающий в результате введения активного компонента или плацебо каждой группе пациентов, был подтвержден. Если возникала нежелательная реакция, связанная с активным компонентом, ответ пациента внимательно контролировали и рассматривали уменьшение дозы.
Изобретение относится к фармацевтической промышленности, а именно к применению фармацевтической композиции для предупреждения или лечения фиброза. Применение фармацевтической композиции, содержащей соединение, представленное следующей Химической Формулой 1
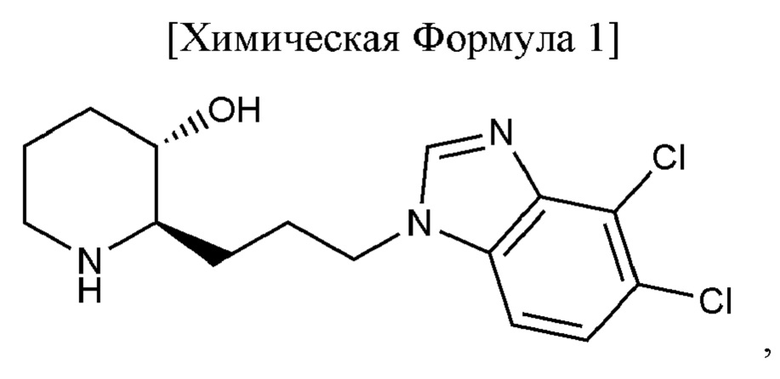
или его фармацевтически приемлемую соль, для предупреждения или лечения фиброза путем введения от 100 до 150 мг два раза в сутки (BID). Вышеописанная применяемая композиция эффективна для предупреждения или лечения фиброза. 5 з.п. ф-лы, 10 ил, 15 табл., 6 пр.
1. Применение фармацевтической композиции, содержащей соединение, представленное следующей Химической Формулой 1
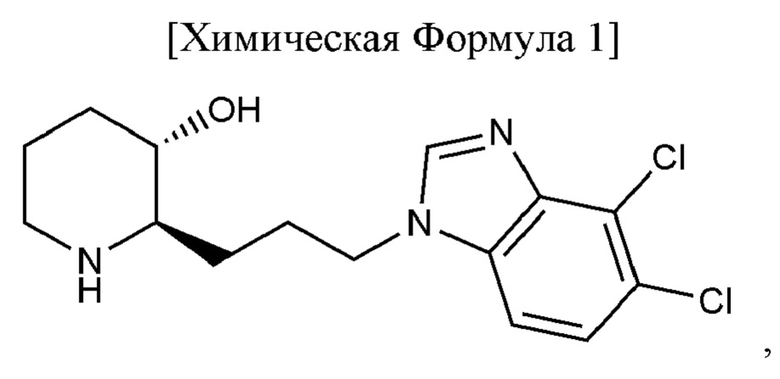
или его фармацевтически приемлемую соль, для предупреждения или лечения фиброза путем введения от 100 до 150 мг два раза в сутки (BID).
2. Применение по п. 1, где фиброз представляет собой интерстициальное легочное заболевание (ILD), склеродерму, келоид, гипертрофический рубец, неалкогольную жировую болезнь печени, первичный склерозирующий холангит (PSC), первичный билиарный холангит (РВС), диабетическую ретинопатию, возрастную макулодистрофию (AMD), гипертрофическую кардиомиопатию, инфаркт миокарда, мышечную дистрофию, диабетическую болезнь почек, фокально-сегментарный гломерулосклероз (FSGS) или воспалительное заболевание кишечника (IBD).
3. Применение по п. 2, где интерстициальное легочное заболевание (ILD) представляет собой идиопатический фиброз легких (IPF), интерстициальное легочное заболевание, ассоциированное с системным склерозом (SSc-ILD), или хронические фиброзирующие интерстициальные легочные заболевания с прогрессирующим фенотипом (PF-ILD).
4. Применение по п. 1, где фармацевтически приемлемая соль представляет собой гидрохлорид.
5. Применение по п. 1, где фармацевтическая композиция дополнительно содержит другой активный компонент, используемый для предупреждения или лечения фиброза.
6. Применение по п. 5, где указанный другой активный компонент, используемый для предупреждения или лечения фиброза, представляет собой Пирфенидон или Нинтеданиб.
| WO 2018147626 A1, 16.08.2018 | |||
| LEE C.H | |||
| et all | |||
| A first-in Class PRS inhibitor, DWN12088, as a novel therapeutic agent for idiopathic pulmonary fibrosis //Am J Respir Crit Med 2020, 201:А2786 | |||
| WO2019231281 A1, 05.12.2019 | |||
| US 20190282565 A1, 19.09.2019 | |||
| KEVIN R | |||
| et all | |||
| Safety of Nintedanib Added to Pirfenidone Treatment for Idiopathic Pulmonary |
Авторы
Даты
2024-11-08—Публикация
2022-05-02—Подача