ОБЛАСТЬ ТЕХНИКИ
[001] Настоящее изобретение относится к терапии для лечения рака; лечение включает внутривенное или внутриопухолевое введение рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего нуклеиновую кислоту, кодирующую 4-1BBL (CD137L). Рекомбинантный модифицированный вирус осповакцины Анкара (MVA) в контексте настоящего описания (также «рекомбинантный MVA» или «rMVA») относится к MVA, содержащему по меньшей мере один полинуклеотид, кодирующий опухолеассоциированный антиген (TAA). В более конкретном аспекте настоящее изобретение включает внутривенное или внутриопухолевое введенное рекомбинантного MVA, содержащего нуклеиновую кислоту, кодирующую TAA, и нуклеиновую кислоту, кодирующую 4-1BBL. В дополнительных аспектах настоящее изобретение включает внутривенное или внутриопухолевое введение рекомбинантного MVA, содержащего нуклеиновую кислоту, кодирующую TAA, и нуклеиновую кислоту, кодирующую CD40L. В дополнительных аспектах настоящее изобретение включает внутривенное и/или внутриопухолевое введение рекомбинантного MVA, содержащего нуклеиновые кислоты, кодирующие TAA, 4-1BBL (CD137L) и CD40L.
УРОВЕНЬ ТЕХНИКИ
[002] Рекомбинантные поксвирусы использовали в качестве иммунотерапевтических вакцин против инфекционных организмов и, позже, против опухолей (Mastrangelo et al. (2000) J Clin Invest. 105(8):1031-1034).
[003] Одним из штаммов поксвируса, применимость которых в качестве иммунотерапевтической вакцины против инфекционных заболеваний и рака была доказана, является модифицированный вирус осповакцины Анкара (MVA) (иногда называемый просто «MVA»). MVA был создан путем 516 серийных пассажей в куриных эмбриональных фибробластах штамма Анкара вируса осповакцины (CVA) (обзор смотрите в Mayr et al. (1975) Infection 3: 6-14). Вследствие этих длительных пассажей в геноме полученного вируса MVA было удалено около 31 тысячи пар нуклеотидов в его геномной последовательности, и следовательно, он очень ограничен по репликации в отношении клеток-хозяев клетками птиц (Meyer et al. (1991) J. Gen. Virol. 72: 1031-1038). В ряде животных моделей было показано, что полученный MVA является по существу авирулентным (Mayr & Danner (1978) Dev. Biol. Stand. 41: 225-34). Были описаны штаммы MVA, имеющие улучшенные профили безопасности, для разработки более безопасных продуктов, таких как вакцины или фармацевтические средства (см. публикацию международной заявки на патент PCT WO2002042480; также см., например, патенты США №№ 6 761 893 и 6 913 752, все из которых включены в настоящий документ посредством ссылки). Такие варианты способны к репродуктивной репликации в нечеловеческих клетках и клеточных линиях, в особенности в куриных эмбриональных фибробластах (CEF), но не способны к репликации в человеческих клеточных линиях, в частности, включая клеточные линии HeLa, HaCat и 143B. Такие штаммы также не способны к репродуктивной репликации in vivo, например, в некоторых мышиных штаммах, таких как трансгенная мышиная модель AGR 129, которая имеет очень ослабленный иммунитет и высокую восприимчивость к реплицирующимся вирусам (см. патент США № 6 761 893). Были описаны такие варианты MVA и его производные, включая рекомбинантные варианты, называемые «MVA-BN» (см. публикацию международной заявки на патент PCT WO2002/042480; также см., например, патенты США №№ 6 761 893 и 6 913 752).
[004] Было показано, что использование поксвирусных векторов, которые кодируют опухолеассоциированные антигены (TAA), успешно уменьшает размер опухоли, а также повышает общий уровень выживаемости онкологических пациентов (см., например, WO 2014/062778). Было продемонстрировано, что когда онкологическому пациенту вводят поксвирусный вектор, кодирующий TAA, такой как HER2, CEA, MUC1 и/или Brachyury, в организме пациента генерируется устойчивый и специфический Т-клеточный ответ для борьбы с раком (Id.; также см. Guardino et al. ((2009) Cancer Res. 69 (24), doi 10.1158/0008-5472.SABCS-09-5089), Heery et al. (2015) JAMA Oncol. 1: 1087-95).
[005] Одним из типов TAA, который экспрессируется на многих раковых и опухолевых клетках, являются эндогенные ретровирусные белки (ERV). ERV представляют собой остатки последних экзогенных форм, которые проникли в зародышевую линию хозяина и с тех пор передаются вертикально через генетическую популяцию (см. Bannert et al. (2018) Frontiers in Microbiology, Volume 9, Article 178). Было документально подтверждено, что явления геномной рекомбинации, вызванные ERV, и нарушение регуляции нормальных клеточных генов способствуют образованию опухолей (Id.). Кроме того, есть указания на то, что некоторые белки ERV обладают онкогенными свойствами (Id.). Было обнаружено, что ERV экспрессируются в большом числе видов рака, включая, например, рак молочной железы, яичников, меланому, рак предстательной железы, рак поджелудочной железы и лимфому. (См., например, Bannert et al. (2018) Front. Microbiol. 9: 178; Cegolon et al. (2013) BMC Cancer 13: 4; Wang-Johanning et al. (2003) Oncogene 22: 1528-35; Wang-Johanning et al. (2007) Int. J. Cancer 120: 81-90; Wang-Johanning et al. (2008) Cancer Res. 68: 5869-77; Wang-Johanning et al. (2018) Cancer Res. 78 (13 Suppl.), AACR Annual Meeting April 2018, Abstract 1257; Contreras-Galindo et al. (2008) J. Virol. 82: 9329-36; Schiavetti et al. (2002) Cancer Res. 62: 5510-16; Maliniemi et al. (2013) PLoS One 8: e76281; Fava et al. (2017) Genes Dev. 31: 34-45, Muster et al. (2003) Cancer Res. 63: 8735-41; Buscher et al. (2005) Cancer Res. 65: 4172-80; Serafino et al. (2009) Expt’l. Cell Res. 315: 849-62; Iramaneerat et al. (2011) Int. J. Gynecol. Cancer 21: 51-7; Ishida et al. (2006) Cancer Sci. 97: 1139-46; Goering et al. (2011) Carcinogenesis 32: 1484-92; Agoni et al. (2013) Front. Oncol. 9: 180; Li et al. (2017) J. Mol. Diagn. 19: 4-23).
[006] Помимо их эффективности в комбинации с TAA, было показано, что поксвирусы, такие как MVA, имеют повышенную эффективность в комбинации с агонистом CD40, таким как лиганд CD40 (CD40L) (см. WO 2014/037124) или с агонистом 4-1BB, таким как лиганд 4-1BB (4-1BBL) (Spencer et al. (2014) PLoS One 9: e105520).
[007] CD40/CD40L является представителем суперсемейства рецепторов факторов некроза опухоли/факторов некроза опухоли («TNFR/TNF»). Несмотря на то, что CD40 конститутивно экспрессируется на многих типах клеток, включая B-клетки, макрофаги и ДК, его лиганд CD40L преимущественно экспрессируется на активированных CD4+ T-клетках (Lee et al. (2002) J. Immunol. 171(11): 5707-5717; Ma and Clark (2009) Semin. Immunol. 21(5): 265-272). Родственное взаимодействие между ДК и CD4+ Т-клетками на ранней стадии после инфицирования или иммунизации «лицензирует» ДК для прайминга CD8+ T-клеточных ответов (Ridge et al. (1998) Nature 393: 474-478). Лицензирование ДК приводит к повышению экспрессии костимулирующих молекул, повышению выживаемости и лучшей способности к перекрестной презентации ДК. Данный процесс опосредован в основном за счет взаимодействия CD40/CD40L (Bennet et al. (1998) Nature 393: 478-480; Schoenberger et al. (1998) Nature 393: 480-483), но также существуют независимые от CD40/CD40L механизмы (CD70, LT.beta.R). Интересно, что также было предложено прямое взаимодействие между CD40L, экспрессируемым на ДК, и CD40, экспрессируемым на CD8+ T-клетках, обеспечивая возможное объяснение образования хелпер-независимых ответов CTL (Johnson et al. (2009) Immunity 30: 218-227).
[008] 4-1BB/4-1BBL является членом суперсемейства TNFR/TNF. 4-1BBL представляет собой костимулирующий лиганд, экспрессируемый в активированных В-клетках, моноцитах и ДК. 4-1BB конститутивно экспрессируется естественными клетками-киллерами (NK) и естественными киллерными T-клетками (NKT), Treg и несколькими популяциями клеток врожденного иммунитета, включая ДК, моноциты и нейтрофилы. Интересно, что 4-1BB экспрессируется на активированных, но не на Т-клетках в состоянии покоя (Wang et al. (2009) Immunol. Rev. 229: 192-215). Лигирование 4-1BB индуцирует пролиферацию и продукцию интерферона гамма (IFN-γ) и интерлейкина 2 (IL-2), а также повышает выживаемость Т-клеток за счет активации антиапоптозных молекул, таких как Bcl-xL (Snell et al. (2011) Immunol. Rev. 244: 197-217). Важно отметить, что стимуляция 4-1BB усиливает пролиферацию NK-клеток, продукцию IFN-γ и цитолитическую активность за счет усиления антителозависимой клеточноопосредованной цитотоксичности (АЗКЦ) (Kohrt et al. (2011) Blood 117: 2423-32).
[009] Ось иммунитета 4-1BB/4-1BBL в настоящее время исследуют посредством различных иммунотерапевтических стратегий. Например, аутологичный перенос Т-клеток химерного антигенного рецептора (CAR) демонстрирует клиническую пользу при В-крепноклеточных лимфомах, что было одобрено FDA в 2017 году. Аутологичные Т-клетки пациента трансдуцируются CAR, которые объединяют внеклеточный домен, полученный из опухолеспецифичного антитела, внутриклеточный сигнальный домен CD3ζ и костимулирующий мотив 4-1BB. Добавление 4-1BB иметь решающее значение для устойчивости in vivo и противоопухолевой токсичности Т-клеток CAR (Song et al. (2011) Cancer Res. 71: 4617e27). В настоящее время исследуются антитела, нацеленные на 4-1BB.
[010] Несколько исследований показали, что агонистические антитела, нацеленные на 4-1BB/путь 4-1BBL, проявляют противоопухолевую активность при использовании в качестве монотерапии ( et al. (2012) Cancer Discovery 2: 608-23). Агонистические антитела, нацеленные на 4-1BB (урелумаб, BMS; утолимумаб, Pfizer), в настоящее время находятся на стадии клинической разработки. В последние годы переменный успех показали исследования, в которых 4-1BBL комбинировали с другими способами лечения. Например, когда мышам с ранее существующими опухолями MC38 (мышиная аденокарцинома), отличными от опухолей меланомы B16, вводили антитела к CTLA-4 и к 4-1BB, наблюдалась значительная CD8+ T-клеточная регрессия опухоли вместе с длительным стойким иммунитетом к данным опухолям. В другом примере лечение посредством антител к 4-1BB (Bristol-Myers Squibb (BMS)-469492) привело только к умеренной регрессии опухолей M109, но значительно задержало рост опухолей EMT6.
et al. (2012) Cancer Discovery 2: 608-23). Агонистические антитела, нацеленные на 4-1BB (урелумаб, BMS; утолимумаб, Pfizer), в настоящее время находятся на стадии клинической разработки. В последние годы переменный успех показали исследования, в которых 4-1BBL комбинировали с другими способами лечения. Например, когда мышам с ранее существующими опухолями MC38 (мышиная аденокарцинома), отличными от опухолей меланомы B16, вводили антитела к CTLA-4 и к 4-1BB, наблюдалась значительная CD8+ T-клеточная регрессия опухоли вместе с длительным стойким иммунитетом к данным опухолям. В другом примере лечение посредством антител к 4-1BB (Bristol-Myers Squibb (BMS)-469492) привело только к умеренной регрессии опухолей M109, но значительно задержало рост опухолей EMT6.
[011] Микроокружение опухоли состоит из большого количества типов клеток, от инфильтратов иммунных клеток до раковых клеток, внеклеточного матрикса, эндотелиальных клеток и других клеточных участников, которые влияют на прогрессирование опухоли. Данное сложное и запутанное равновесие варьируется не только от пациента к пациенту, но и внутри поражений одного и того же субъекта ( et al. (2017) Cell 170(5): 927-938). Стратификация опухолей на основе экспрессии инфильтрирующих опухоль лимфоцитов (TIL) и лиганда запрограммированной смерти 1 (PD-L1), подчеркивает важность воспалительной среды для достижения объективных ответов против рака (Teng et al. (2015) рак Res. 75(11): 2139-45). Пан-раковый анализ профилей экспрессии генов из Атласа генома рака (TCGA) подтверждает, что отличительная черта опухолевого воспаления коррелирует с объективными ответами на иммунотерапию (Danaher et al. (2018) J. Immunother. Cancer 6(1): 63).
et al. (2017) Cell 170(5): 927-938). Стратификация опухолей на основе экспрессии инфильтрирующих опухоль лимфоцитов (TIL) и лиганда запрограммированной смерти 1 (PD-L1), подчеркивает важность воспалительной среды для достижения объективных ответов против рака (Teng et al. (2015) рак Res. 75(11): 2139-45). Пан-раковый анализ профилей экспрессии генов из Атласа генома рака (TCGA) подтверждает, что отличительная черта опухолевого воспаления коррелирует с объективными ответами на иммунотерапию (Danaher et al. (2018) J. Immunother. Cancer 6(1): 63).
[012] В последние годы попытки улучшить терапевтические пути введения вакцин расширились с подкожной инъекции до внутривенного пути введения. Например, было продемонстрировано, что внутривенное введение вакцины MVA, кодирующей гетерологичный антиген, способно индуцировать сильный специфический иммунный ответ на антиген (см. WO 2014/037124). Кроме того, усиленный иммунный генерировался, если вакцина MVA включала CD40L.
[013] Уже давно сообщалось об инокуляции материала бактериального происхождения (токсина Коули) в опухолевые поражения, обеспечивающего лечебный эффект, что подчеркивает роль местной инфекции в стимулировании противоопухолевых ответов (Coley (1906) Proc. R. Soc. Med. 3 (Surg Sect): 1-48). Местное введение патоген-ассоциированных молекулярных паттернов (PAMP - англ.: Pathogen Associated Molecular Patterns), бактериальных продуктов и вирусов в опухолевые поражения вызывает противомикробную программу, которая приводит к каскаду явлений после введения, в том числе: i) секрецию провоспалительных цитокинов, таких как интерфероны типа I, II и III и фактор некроза опухоли альфа (TNF-альфа); ii) сигналы опасности, такие как алармины и белки теплового шока; и iii) высвобождение опухолевых антигенов (Aznar et al. (2017) J. Immunol. 198: 31-39). Местное введение иммунотерапии в опухоль вызывает системные иммунные ответы, поскольку регрессия определялась в необработанных опухолевых поражениях ((2018) Cancer Discov. 8(6): 67).
[014] Сообщалось о внутриопухолевом введении вакцин MVA в последние несколько лет. Было обнаружено, что внутриопухолевые инъекции MVA, экспрессирующей ГМ-КСФ, и иммунизация ДНК-вакциной повышали выживаемость мышей с опухолями ВПЧ16 E7 (Nemeckova et al. (2007) Neoplasma 54: 4). Другие исследования внутриопухолевой инъекции MVA не смогли продемонстрировать ингибирование роста опухоли поджелудочной железы (White et al. (2018) PLoS One 13(2): e0193131). Внутриопухолевая инъекция инактивированной нагреванием MVA индуцировала противоопухолевые иммунные ответы, зависящие от генерации сигналов опасности, интерферона I типа и перекрестной презентации антигена дендритными клетками (Dai et al. (2017) Sci. Immunol. 2(11): eaal1713).
[015] Очевидно, что существует значительная неудовлетворенная медицинская потребность в дополнительных видах лечения рака, включая активные иммунотерапевтические препараты и противораковые вакцины. Кроме того, существует потребность в способах лечения, которые могут вызывать усиленные иммунные ответы в нескольких областях иммунного ответа пациента. Во многих аспектах варианты осуществления настоящего раскрытия удовлетворяют данные потребности, обеспечивая вакцины, терапию и комбинированную терапию, которые увеличивают и улучшают доступные в настоящее время способы лечения рака.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[016] В различных вариантах осуществления настоящего изобретения было определено, что рекомбинантный MVA, кодирующий опухолеассоциированный антиген (TAA) и лиганд 4-1BB (также называемый 41BBL, 4-1BBL или CD137L) при внутриопухолевом или внутривенном введении повышает эффективность и/или усиливает лечение онкологического пациента. Более конкретно, было определено, что различные варианты осуществления настоящего раскрытия обеспечивали повышенное воспаление в опухоли, снижение регуляторных Т-клеток (Treg) и истощение Т-клеток в опухоли, экспансию опухолеспецифичных Т-клеток и активацию NK-клеток, усиление уменьшения объема опухоли и/или повышение выживаемости субъекта с раком по сравнению с введением рекомбинантного MVA отдельно.
[017] В различных вариантах осуществления настоящего изобретения было определено, что рекомбинантный MVA, кодирующий опухолеассоциированный антиген (TAA) и лиганд CD40 (CD40L) при внутриопухолевом или внутривенном введении усиливает лечение онкологического пациента. Более конкретно, было определено, что различные варианты осуществления настоящего раскрытия обеспечивали повышенное воспаление в опухоли, снижение регуляторных Т-клеток (Treg) и истощение Т-клеток в опухоли, экспансию опухолеспецифичных Т-клеток и активацию NK-клеток, усиление уменьшения объема опухоли и/или повышение выживаемости субъекта с раком по сравнению с введением рекомбинантного MVA отдельно.
[018] В дополнительных вариантах осуществления настоящее изобретение включает рекомбинантный модифицированный вирус осповакцины Анкара (MVA), содержащий нуклеиновую кислоту, кодирующую 4-1BBL (CD137L), и нуклеиновую кислоту, кодирующую CD40L, который при внутривенном и/или внутриопухолевом введении усиливает лечение онкологического пациента.
[019] Соответственно, в одном варианте осуществления настоящее изобретение включает способ уменьшения размера опухоли и/или повышения выживаемости субъекта с раковой опухолью, включающий внутриопухолевое введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA), и вторую нуклеиновую кислоту, кодирующую 4-1BBL, причем внутриопухолевое введение рекомбинантного MVA усиливает воспалительный ответ в раковой опухоли, усиливает уменьшение опухоли и/или повышает общую выживаемость субъекта по сравнению с отличной от внутриопухолевой инъекции рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую TAA и антиген 4-1BBL.
[020] В дополнительном варианте осуществления настоящее изобретение включает способ уменьшения размера опухоли и/или повышения выживаемости субъекта с раковой опухолью, включающий внутриопухолевое введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA), и вторую нуклеиновую кислоту, кодирующую CD40L, причем внутриопухолевое введение рекомбинантный MVA усиливает воспалительный ответ в раковой опухоли, усиливает уменьшение опухоли и/или повышает общую выживаемость субъекта по сравнению с отличной от внутриопухолевой инъекции рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую антиген TAA и CD40L.
[021] В дополнительном варианте осуществления настоящее изобретение включает способ уменьшения размера опухоли и/или повышения выживаемости у субъекта с раковой опухолью, включающий внутриопухолевое и/или внутривенное введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA), вторую нуклеиновую кислоту, кодирующую CD40L, и третью нуклеиновую кислоту, кодирующую 4-1BBL (CD137L), причем введение рекомбинантного MVA повышает воспалительный ответ в раковой опухоли, усиливает уменьшение опухоли, и/или повышает общую выживаемость субъекта по сравнению с инъекцией рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую TAA, антиген CD40L и антиген 4-1BBL, посредством различных путей инъекции (т.e. отличной от внутриопухолевой или отличной от внутривенной инъекции).
[022] В дополнительном варианте осуществления настоящее изобретение включает способ уменьшения размера опухоли и/или повышение выживаемости у субъекта с раковой опухолью, включающий внутривенное введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA) и вторую нуклеиновую кислоту, кодирующую 4-1BBL, причем внутривенное введение рекомбинантного MVA усиливает ответ естественных клеток-киллеров (NK) и усиливает ответы CD8 T-клеток, специфичных к TAA по сравнению с отличной от внутривенной инъекцией рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую TAA и антиген 4-1BBL.
[023] В дополнительном варианте осуществления настоящее изобретение включает способ уменьшения размера опухоли и/или повышения выживаемости у субъекта с раковой опухолью, включающий внутривенное введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA), и вторую нуклеиновую кислоту, кодирующую CD40L, причем внутривенное введение рекомбинантного MVA повышает ответ естественных клеток-киллеров (NK) и повышает ответы CD8 T-клеток, специфичных к TAA по сравнению с отличной от внутривенной инъекции рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую TAA и антиген CD40L.
[024] В дополнительном варианте осуществления настоящее изобретение включает способ уменьшения размера опухоли и/или повышения выживаемости у субъекта с раковой опухолью, включающий внутривенное и/или внутриопухолевое введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA), вторую нуклеиновую кислоту, кодирующую CD40L, и третью нуклеиновую кислоту, кодирующую 4-1BBL, причем внутривенное и/или внутриопухолевое введение рекомбинантного MVA усиливает ответ естественных клеток-киллеров (NK) и усиливает ответы CD8 T-клеток, специфичных к TAA по сравнению с отличной от внутривенной или отличной от внутриопухолевой инъекции рекомбинантного вируса MVA, содержащего первую нуклеиновую кислоту, кодирующую TAA, вторую нуклеиновую кислоту, кодирующую антиген CD40L, и третью нуклеиновую кислоту, кодирующую антиген 4-1BBL.
[025] В еще одном варианте осуществления настоящее изобретение включает способ индукции усиленного воспалительного ответа в раковой опухоли субъекта, включающий внутриопухолевое введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую первый гетерологичный опухолеассоциированный антиген (TAA), и вторую нуклеиновую кислоту, кодирующую антиген 4-1BBL, причем внутриопухолевое введение рекомбинантного MVA генерирует усиленный воспалительный ответ в опухоли по сравнению с воспалительным ответом, сгенирированным посредством отличной от внутриопухолевой инъекции рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую гетерологичный опухолеассоциированный антиген и антиген 4-1BBL.
[026] В еще одном варианте осуществления настоящее изобретение включает способ индукции усиленного воспалительного ответа в раковой опухоли субъекта, включающий внутриопухолевое введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую первый гетерологичный опухолеассоциированный антиген (TAA), и вторую нуклеиновую кислоту, кодирующую антиген CD40L, причем внутриопухолевое введение рекомбинантного MVA генерирует усиленный воспалительный ответ в опухоли по сравнению с воспалительным ответом, сгенирированным посредством отличной от внутриопухолевой инъекции рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую гетерологичный опухолеассоциированный антиген и антиген CD40L.
[027] В еще одном варианте осуществления настоящее изобретение включает способ индукции усиленного воспалительного ответа в раковой опухоли субъекта, включающий внутриопухолевое и/или внутривенное введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую первый гетерологичный опухолеассоциированный антиген (TAA), вторую нуклеиновую кислоту, кодирующую антиген CD40L, и третью нуклеиновую кислоту, кодирующую антиген 4-1BBL, причем внутриопухолевое и/или внутривенное введение рекомбинантного MVA генерирует усиленный воспалительный ответ в опухоли по сравнению с воспалительным ответом, сгенирированным посредством отличной от внутриопухолевой или отличной от внутривенной инъекции рекомбинантного вируса MVA, содержащего первую нуклеиновую кислоту, кодирующую гетерологичный опухолеассоциированный антиген, вторую нуклеиновую кислоту, кодирующую антиген CD40L, и третью нуклеиновую кислоту, кодирующую антиген 4-1BBL.
[028] В различных дополнительных вариантах осуществления настоящее изобретение относится к рекомбинантному модифицированному вирусу осповакцины Анкара (MVA) для лечения субъекта с раком, причем рекомбинантный MVA содержит (a) первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA) и (b) вторую нуклеиновую кислоту, кодирующую 4-1BBL.
[029] В различных дополнительных вариантах осуществления настоящее изобретение относится к рекомбинантному модифицированному вирусу осповакцины Анкара (MVA) для лечения субъекта с раком, причем рекомбинантный MVA содержит a) первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA) и b) вторую нуклеиновую кислоту, кодирующую CD40L.
[030] В различных дополнительных вариантах осуществления настоящее изобретение включает рекомбинантный модифицированный вирус осповакцины Анкара (MVA) для лечения субъекта с раком, при этом рекомбинантный MVA содержит a) первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA) и b) вторую нуклеиновую кислоту, кодирующую CD40L, и с) третью нуклеиновую кислоту, кодирующую 4-1BBL.
[031] В еще одном варианте осуществления рекомбинантный MVA, кодирующий антиген 4-1BBL, при внутриопухолевом введении пациенту в комбинации с введением антагониста ингибитора иммунных контрольных точек усиливает лечение онкологического пациента, более конкретно повышает уменьшение объема опухоли и/или повышает выживаемость онкологического пациента.
[032] В еще одном варианте осуществления рекомбинантный MVA, кодирующий антиген CD40L, при внутриопухолевом введении пациенту в комбинации с введением антагониста ингибитора иммунных контрольных точек усиливает лечение онкологического пациента, более конкретно повышает уменьшение объема опухоли и/или повышает выживаемость онкологического пациента.
[033] В еще одном варианте осуществления рекомбинантный MVA, кодирующий антиген CD40L и 4-1BBL, при внутриопухолевом и/или внутривенном введении пациенту в комбинации с введением антагониста ингибитора иммунных контрольных точек усиливает лечение онкологического пациента, более конкретно усиливает уменьшение объема опухоли и/или повышает выживаемость онкологического пациента.
[034] В другом варианте осуществления рекомбинантный MVA по настоящему изобретению вводят одновременно или после введения антитела. В более предпочтительном варианте осуществления рекомбинантный MVA вводят после антитела.
[035] В другом варианте осуществления рекомбинантный MVA по настоящему изобретению вводят посредством тех же путей введения и одновременно или после введения антитела. В другом варианте осуществления рекомбинантный MVA вводят посредством отличного пути или способов введения или после введения антитела.
[036] В другом варианте осуществления настоящее изобретение включает способ усиления противораковой терапии у онкологического пациента, включающий введение онкологическому пациенту фармацевтической комбинации по настоящему изобретению, причем введение фармацевтической комбинации усиливает антителозависимую клеточноопосредованную цитотоксичность (АЗКЦ), индуцированную терапией на основе антитела, по сравнению с применением только терапии на основе антитела.
[037] В предпочтительных вариантах осуществления первая нуклеиновая кислота кодирует TAA, который представляет собой эндогенный ретровирусный белок (ERV). В более предпочтительных вариантах осуществления белок ERV происходит из семейства человеческих эндогенных ретровирусных белков K (HERV-K). В более предпочтительных вариантах осуществления белок ERV выбран из оболочечного белка HERV-K и белка HERV-K gag.
[038] В предпочтительных вариантах осуществления первая нуклеиновая кислота кодирует TAA, который представляет собой эндогенный ретровирусный пептид (ERV). В более предпочтительных вариантах осуществления пептид ERV происходит из семейства человеческих эндогенных ретровирусных белков K (HERV-K). В более предпочтительных вариантах осуществления пептид ERV выбран из псевдогена оболочечного белка HERV-K (HERV-K-MEL).
[039] В других предпочтительных вариантах осуществления первая нуклеиновая кислота кодирует TAA, выбранный из группы, включающей карциноэмбриональный антиген (CEA), ассоциированный с клеточной поверхностью муцин-1 (MUC-1), простатическую кислую фосфатазу (PAP), простатспецифический антиген (PSA), рецептор человеческого эпидермального фактора роста 2-го типа (HER-2), сурвивин, связанный с тирозином белок 1 (TRP1), связанный с тирозином белок 1 (TRP2), Brachyury, предпочтительно экспрессируемый антиген меланомы (PRAME), фолатный рецептор 1 (FOLR1) и их комбинации.
[040] В одном или более предпочтительных вариантах осуществления рекомбинантный MVA представляет собой MVA-BN или его производное.
[041] В различных дополнительных вариантах осуществления рекомбинантные MVA и способы, описанные в настоящем изобретении, вводят субъекту с раком в комбинации либо с антагонистом, либо с агонистом молекул иммунных контрольных точек. В дополнительных вариантах осуществления рекомбинантные MVA и способы, описанные в настоящем изобретении, вводят субъекту с раком в комбинации с антителом, специфичным к TAA, для лечения субъекта с раком. В более предпочтительном варианте осуществления рекомбинантные MVA и способы, описанные в настоящем изобретении, вводят в комбинации с антагонистом или агонистом молекул иммунных контрольных точек, выбранным из CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 и ICOS. В наиболее предпочтительных вариантах осуществления антагонист или агонист молекул иммунных контрольных точек содержит антитело. В наиболее предпочтительном варианте осуществления антагонист или агонист молекул иммунных контрольных точек содержит антитело к PD-1 или PD-L1.
[042] Дополнительные цели и преимущества этого изобретения будут изложены частично в нижеприведенном описании, а частично станут очевидны из описания, или же они могут быть выявлены при практической реализации этого изобретения. Цели и преимущества этого изобретения будут реализованы и достигнуты посредством элементов и комбинаций, конкретно указанных в прилагаемой формуле изобретения.
[043] Сопроводительные графические материалы, которые включены и составляют часть этого описания, иллюстрируют один или более вариантов осуществления этого изобретения и вместе с описанием служат для пояснения принципов этого изобретения.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[044] На фиг. 1A, 1B, 1C и 1D проиллюстрировано, что 4-1BBL-опосредованная костимуляция CD8 Т-клеток посредством инфицированных MVA-OVA-4-1BBL опухолевых клеток влияет на выработку цитокинов без потребности в ДК. Напротив, MVA-OVA-CD40L усиливает выработку цитокинов только в присутствии ДК. Как описано в примере 2, дендритные клетки (ДК) были получены после культивирования клеток костного мозга мышей C57BL/6 в присутствии рекомбинантного Flt3L в течение 14 дней. Клетки B16.F10 инфицировали MVA-OVA, MVA-OVA-CD40L или MVA-OVA-4-1BBL, и инфицированные опухолевые клетки собирали и совместно культивировали, если указано, в присутствии ДК. Интактные OVA (257-264)-специфичные CD8+ Т-клетки очищали посредством магнитного способа от OT-I мышей и добавляли в совместную культуру. Клетки культивировали и супернатант собирали для анализа концентрации цитокинов с помощью Luminex. Показана концентрация в супернатанте IL-6 (фиг. 1A), ГМ-КСФ (фиг. 1B), IL-2 (фиг. 1C) и IFN-γ (фиг. 1D). Данные представлены в виде среднего значения ± СОС.
[045] На фиг. 2A и фиг. 2B показано, что инфицированные MVA-OVA-4-1BBL опухолевые клетки непосредственно, т.е. без потребности в ДК, запускают дифференцировку антигенспецифичных Т-клеток CD8 до активированных эффекторных Т-клеток, тогда как CD40L-опосредованная костимуляция инфицированных MVA-OVA-CD40L опухолевых клеток зависит от наличия ДК. Как описано в примере 3, дендритные клетки (ДК) были получены после культивирования клеток костного мозга мышей C57BL/6 в присутствии рекомбинантного Flt3L в течение 14 дней. Клетки B16.F10 (модель меланомы) инфицировали посредством MVA-OVA, MVA-OVA-CD40L или MVA-OVA-4-1BBL. На следующий день инфицированные опухолевые клетки собирали и совместно культивировали (если указано) в присутствии ДК. Интактные OVA (257-264)-специфичные CD8+ Т-клетки очищали посредством магнитного способа от мышей OT-I и добавляли в совместную культуру в соотношении 1:5. Клетки культивировали при 37°C и 5% CO2 в течение 48 часов. Затем клетки окрашивали и анализировали посредством проточной цитометрии. На фиг. 2A показано GMFI T-bet на OT-I CD8+ Т-клетках (отмеченных на фигуре как «CD8+»); на фиг. 2B показано процентное отношение CD44+гранзим B+ IFNγ+ TNFα+ OT-I CD8+ Т-клеток. Данные представлены в виде среднего значения ± СОС.
[046] На фиг. 3A, 3B, 3C, 3D и 3E проиллюстрировано, что инфицирование посредством MVA, кодирующего либо CD40L, либо 4-1BBL, индуцирует гибель опухолевых клеток в опухолевых клеточных линиях и макрофагах. Как описано в примере 4, линии опухолевых клеток B16.OVA (фиг. 3A и 3B), MC38 (фиг. 3C) и B16.F10 (фиг. 3D) инфицировали векторами с указанной MOI в течение 20 часов. Клетки анализировали на их жизнеспособность посредством проточной цитометрии; на фиг. 3A, 3C, 3D и 3E показан процент мертвых клеток («Live/Dead+»). Фиг. 3B: HMGB1 в супернатантах с фиг. 3A количественно оценивали посредством ELISA. Фиг. 3E: Макрофаги, происходящие из костного мозга (BMDM), инфицировали при указанной MOI в течение 20 часов. Клетки анализировали на их жизнеспособность посредством проточной цитометрии. Данные представлены виде среднего значения ± СОС.
[047] На фиг. 4A и 4B показано, что rMVA-4-1BBL включает активацию NK-клеток in vivo. Как описано в примере 5, мышей C57BL/6 (n=5/группа) внутривенно иммунизировали либо физиологическим раствором, либо 5×107 TCID50 «rMVA» (=MVA-OVA), «rMVA-4-1BBL» (=MVA-OVA-4-1BBL) или 5×107 TCID50 rMVA в комбинации с 200 мкг антитела к 4-1BBL (клон TKS-1). Через 24 часа мышей умерщвляли и селезенки обрабатывали для анализа посредством проточной цитометрии. Показана среднее геометрическое интенсивности флуоресценции (GMFI) CD69 (A) и CD70 (B). Данные представлены в виде среднего значения ± СОС.
[048] На фиг. 5A и 5B показано, что внутривенная иммунизация посредством rMVA-4-1BBL способствует секреции сывороточного IFN-γ in vivo. Как описано в примере 6, мышей C57BL/6 (n=5/группа) внутривенно иммунизировали либо физиологическим раствором, либо 5×107 TCID50 «rMVA» (=MVA-OVA), «rMVA-4-1BBL» (=MVA-OVA-4-1BBL), либо 5×107 TCID50 rMVA в комбинации с 200 мкг антитела к 4-1BBL (клон TKS-1). Фиг. 5A: через 6 часов у мышей отбирали кровь, сыворотку отделяли от цельной крови и концентрацию IFN-γ в сыворотке определяли посредством Luminex. Фиг. 5B: через 3, 21 и 45 часов мышам внутривенно инъецировали брефельдин A для окончания секреции белка. Мышей умерщвляли через 6, 24 и 48 часов после иммунизации и спленоциты анализировали посредством проточной цитометрии. Данные представлены в виде среднего значения ± СОС.
[049] На фиг. 6 показано, что внутривенная иммунизация «rMVA-4-1BBL» (=MVA-OVA-4-1BBL) способствует секреции IFN-γ у мышей с опухолью B16.OVA. Как описано в примере 7, мышей C57BL/6 с опухолью B16.OVA (n=5/группа) группировали, и они в/в (внутривенно) получали ФСБ или 5×107 TCID50 rMVA (= MVA-OVA) или rMVA-4-1BBL на 7 день после инокуляции опухоли. Через 6 часов у мышей отбирали кровь, сыворотку отделяли от цельной крови и определяли концентрацию IFN-γ в сыворотке посредством Luminex. Данные представлены в виде среднего значения ± СОС.
[050] На фиг. 7A, 7B, 7C и 7D показаны антиген- и вектор-специфичная CD8+ T-клеточная экспансия после внутривенной первичной и бустерной иммунизации «rMVA-4-1BBL» (=MVA-OVA-4-1BBL). Как описано в примере 8, мыши C57BL/6 (n=4/группа) получали внутривенную первичную иммунизацию физиологическим раствором или 5×107 TCID50 «rMVA» (= MVA-OVA), rMVA-4-1BBL или 5×107 TCID50 rMVA в комбинации с 200 мкг антитела к 4-1BBL (клон TKS-1) в день 0 и бустерную иммунизацию в день 41. У мышей отбирали кровь в дни 6, 21, 35, 48 и 64 дни после первичной иммунизации и выполняли анализ посредством проточной цитометрии периферической крови. На фиг. 7A показано процентное содержание антиген-(OVA)-специфичных CD8+ Т-клеток среди лейкоцитов периферической крови (PBL); на фиг. 7В показано процентное содержание вектор(B8R)-специфичных CD8+ Т-клеток среди PBL. Мышей умерщвляли на 70 день после первичной иммунизации. Селезенки собирали и проводили анализ посредством проточной цитометрии. На фиг. 7C показано процентное содержание антиген-(OVA)-специфичных CD8+ Т-клеток среди живых клеток; и на фиг. 7D показано процентное соотношение вектор (B8R)-специфичных CD8+Т-клеток среди живых клеток. Данные представлены в виде среднего значения ± СОС.
[051] На фиг. 8 показано усиление противоопухолевого эффекта внутривенной инъекции вируса MVA, кодирующего 4-1BBL, по сравнению с рекомбинантным MVA без 4-1BBL. Как описано в примере 9, мышей C57BL/6 с опухолью B16.OVA (n=5/группа) группировали, и они получили внутривенное введение ФСБ или 5×107 TCID50 MVA-OVA («rMVA» на рисунке) или MVA-OVA-4-1BBL («rMVA-4-1BBL» на фигуре) в день 7 (черная пунктирная линия) после инокуляции опухоли. Рост опухоли измеряли через равные интервалы.
[052] На фиг. 9A, 9B, 9C и 9D показан усиленный противоопухолевый эффект внутриопухолевой инъекции вируса MVA, кодирующего 4-1BBL или CD40L. Как описано в примере 10, мышей C57BL/6 с опухолью B16.OVA (n=4-5/группа) группировали, и они получали внутриопухолевое введение ФСБ или 5×107 TCID50 MVA-OVA (обозначено на рисунке «rMVA»), MVA -OVA-CD40L (обозначен как «rMVA-CD40L» на фиг.) или MVA-OVA-4-1BBL (обозначен «rMVA-4-1BBL» на фиг.) в дни 7 (черная пунктирная линия), 12 и 15 (серые пунктирные линии) после инокуляции опухоли. Рост опухоли измеряли через равные интервалы.
[053] На фиг. 10A, 10B и 10C показан противоопухолевый эффект внутриопухолевой инъекции вируса MVA, кодирующего CD40L, против установленного рака толстой кишки. Как описано в примере 11, мышей C57BL/6 с опухолью MC38 (n=5/группа) группировали, и они получали внутриопухолевое (it) введение ФСБ или 5×107 TCID50 MVA-TAA (обозначено на фигуре «rMVA») или MVA. -TAA-CD40L (обозначенный на фигуре «rMVA-CD40L») в день 14 (черная пунктирная линия), 19 и 22 (черные пунктирные линии) после инокуляции опухоли. Рост опухоли измеряли через равные интервалы. В данных экспериментах TAA, кодируемый рекомбинантными MVA, включал антигены AH1A5, p15E и TRP2.
[054] На фиг. 11 показано, что блокада контрольной точки и нацеленные на опухоль антитела действуют синергически с внутриопухолевым (в/о) введением rMVA-4-1BBL (также называемого в настоящем изобретении «MVA-OVA-4-1BBL»). Как описано в примере 12, мышей C57BL/6 с опухолью B16.OVA (n=5/группа) группировали, и они получали 200 мкг IgG2a, антитела к TRP-1 или к PD-1 внутрибрюшинно по показаниям (галочки). Мышей иммунизировали посредством внутриопухолевого (в/о) введения либо ФСБ, либо 5×107 TCID50 MVA-OVA-4-1BBL в дни 13 (черная пунктирная линия), 18 и 21 (серые пунктирные линии) после инокуляции опухоли. Рост опухоли измеряли через равные интервалы.
[055] На фиг. 12 показано, что внутриопухолевая инъекция MVA-OVA-4-1BBL приводит к более сильному противоопухолевому эффекту по сравнению с лечением антителами к CD137. Как описано в примере 13, мыши C57BL/6 получали 5×105 клеток B16.OVA п/к (подкожно). Через семь дней, если размер опухолей превышал 5×5 мм, мышей группировали и осуществляли внутриопухолевую инъекцию либо ФСБ, 5×107 TCID50 MVA-OVA-4-1BBL, либо 10 мкг антитела к 4-1BB (3H3). Рост опухоли измеряли через равные интервалы. На фиг. 12A показан средний объем опухоли. Фиг. 12В: в день 12 после первичной иммунизации лимфоциты периферической крови окрашивали OVA-декстрамером и анализировали посредством FACS. Показано процентное содержание декстрамера OVA+CD44+Т-клеток среди CD8+Т-клеток.
[056] На фиг. 13 показан противоопухолевый эффект внутривенной инъекции вируса MVA, кодирующего эндогенный ретровирусный антиген Gp70. Как описано в примере 14, мыши Balb/c получали 5×105 клеток CT26.wt п/к (подкожно). Когда размер опухолей превышал 5×5 мм, мышей с опухолью CT26.wt (n=5/группа) группировали, и они получали в/в (внутривенно) ФСБ или 5×107 TCID50 MVA, rMVA-Gp70 или rMVA-Gp70-CD40L на 12 день после инокуляции опухоли. Рост опухоли измеряли через равные интервалы. Показаны средний диаметр опухоли (фиг. 13A) и средний объем опухоли (фиг. 13B). Фиг. 13C: через 7 дней после иммунизации клетки крови рестимулировали, и показан процент клеток CD8+CD44+IFN-γ+в крови после стимуляции.
[057] На фиг. 14 показан противоопухолевый эффект внутривенной инъекции вируса MVA, кодирующего эндогенный ретровирусный антиген Gp70 плюс CD40L. Как описано в примере 15, мыши C57BL/6 получали 5×105 клеток B16.F10 п/к (подкожно). Через семь дней, когда размер опухолей превышал 5×5 мм, мышей C57BL/6 с опухолью B16.F10 (n=5/группа) группировали, и они получали в/в (внутривенно) ФСБ или 5×107 TCID50 MVA, rMVA-Gp70 или rMVA-Gp70-CD40L. Рост опухоли измеряли через равные интервалы. Показаны средний объем опухоли (фиг. 14A) и процентное содержание клеток CD8+ CD44+ IFN-γ+ в крови после стимуляции пептидом p15e через 7 дней после иммунизации (фиг. 14B).
[058] Фиг. 15: Ответы основной цепи цитокинов/хемокинов MVA-BN на IT-иммунизацию могут быть увеличены посредством адъювантации 4-1BBL. Под «адъювантацией» в настоящем изобретении подразумевается, что конкретный кодируемый белок или компонент рекомбинантного MVA увеличивает иммунный ответ, продуцируемый другим кодируемым(-ыми) белком(-ами) или компонентом(-ами) рекомбинантного MVA. В данном случае, 5 × 105 клеток B16.OVA подкожно (п/к) имплантировали мышам C57BL/6 (см. пример 23). Мышей иммунизировали на 10-й день внутриопухолево (в/о) с помощью ФСБ или 2 × 108 TCID50 MVA-BN, MVA-OVA или MVA-OVA-4-1BBL (n=6 мышей/группа). Через 6 часов опухоли извлекали и лизаты опухолей обрабатывали. Профили цитокинов/хемокинов анализировали посредством Luminex. На фиг. 15 показана повышенная регуляция цитокинов/хемокинов у иммунизированных мышей.
[059] Фиг. 16: Цитокиновые/хемокиновые провоспалительные ответы на внутриопухолевую (в/о) иммунизацию усиливаются посредством MVA-OVA-4-1BBL. 5×105 клеток B16.OVA подкожно имплантировали мышам C57BL/6 (см. примеры 23 и 24). Мышей иммунизировали на 10-й день внутриопухолевого (в/о) с помощью ФСБ или 2×108 TCID50 MVA-BN, MVA-OVA или MVA-OVA-4-1BBL (n=6 мышей/группа). Через 6 часов опухоли извлекали и лизаты опухолей обрабатывали. Профили цитокинов/хемокинов анализировали посредством Luminex. На фиг. 16 показаны те цитокины/хемокины, которые имеют повышенную регуляцию у мышей, иммунизированных MVA-OVA-4-1BBL, по сравнению с MVA-BN.
[060] Фиг. 17: Количественный и качественный анализ Т-клеток микроокружения опухоли (TME) и лимфатического узла, дренирующего опухоль (TdLN) после внутриопухолевой инъекции MVA-OVA-4-1BBL. Мыши C57BL/6 подкожно (п/к) получали 5×105 клеток B16.OVA. Спустя девять-тринадцать дней, когда размер опухолей превышал 5×5 мм, мышей группировали и осуществляли внутриопухолевую инъекцию либо ФСБ, 2×108 TCID50 MVA-OVA, либо MVA-OVA-4-1BBL (см. пример 25). Через один, три и семь дней после иммунизации мышей умерщвляли и опухоли, а также лимфатические узлы, дренирующие опухоль (TdLN), обрабатывали коллагеназой/ДНКазой и анализировали посредством проточной цитометрии. Показано количество CD45+ клеток, CD8+ Т-клеток, CD4+ Т-клеток и OVA-специфичных CD8+ Т-клеток на мг опухоли и на TdLN.
[061] Фиг. 18: Количественный и качественный Т-клеточный анализ TME и дренирующего ЛУ после внутриопухолевой инъекции MVA-OVA-4-1BBL. Мыши C57BL/6 подкожно (п/к) получали 5×105 клеток B16.OVA. Спустя девять-тринадцать дней, когда размер опухолей превышал 5,5×5,5 мм, мышей группировали и осуществляли внутриопухолевую инъекцию либо ФСБ, либо 2×108 TCID50 MVA-OVA, либо MVA-OVA-4-1BBL (см. пример 26). Через один, три и семь дней после иммунизации мышей умерщвляли и опухоли, а также TdLN (лимфатические узлы, дренирующие опухоль), обрабатывали коллагеназой/ДНКазой и анализировали посредством проточной цитометрии. Фиг. 18А: Показано процентное содержание клеток Ki67+ среди OVA-специфичных CD8+ Т-клеток в опухоли (левая панель) и TdLN (правая панель). Фиг. 18B: Показаны GMFI PD1 среди OVA-специфичных CD8+ Т-клеток в опухоли через семь дней после в/о иммунизации. Фиг. 18C: Показано OVA-специфичное отношение Teff/Treg в опухоли через семь дней после в/о иммунизации.
[062] Фиг. 19: Количественный и качественный анализ NK-клеток TME и лимфатического узла, дренирующего опухоль (TdLN) после внутриопухолевой инъекции MVA-OVA-4-1BBL. Мыши C57BL/6 подкожно (п/к) получали 5×105 клеток B16.OVA. Спустя девять-тринадцать дней, когда размер опухолей превышал 5,5×5,5 мм, мышей группировали и осуществляли внутриопухолевую инъекцию либо ФСБ, либо 2×108 TCID50 MVA-OVA, либо MVA-OVA-4-1BBL (см. пример 27). Мышей умерщвляли через один, три и семь дней после иммунизации, и опухоли, а также лимфатические узлы, дренирующие опухоль (TdLN), обрабатывали коллагеназой/ДНКазой и анализировали посредством проточной цитометрии. Показано количество NK-клеток на мг опухоли и TdLN и GMFI CD69, гранзим B и Ki67, поверхностные маркеры NK-клеток в опухоли и T dLN.
[063] Фиг. 20: Зависимость от CD8 Т-лимфоцитов противоопухолевых эффектов, опосредованных MVA-OVA-4-1BBL. Мыши C57BL/6 подкожно (п/к) получали 5×105 клеток B16.OVA. Через семь дней мышей группировали и осуществляли внутриопухолевую инъекцию ФСБ или 2 × 108 TCID50 MVA-OVA-4-1BBL (см. пример 28). В дни 5 и 8 после данной первой инъекции данные внутриопухолевые (в/о) инъекции повторяли (вертикальные пунктирные линии). Дополнительно, контрольное антитело изотипа IgG2b (левая и средняя панели) или антитело к CD8 (2,43; правая панель) вводили внутрибрюшинно (в/б) в день -1 до и день 1, 4, 7, 11 после первой иммунизации (100 мкг/мышь). Рост опухоли измеряли через равные промежутки времени, и показан средний диаметр опухоли.
[064] Фиг. 21: Зависимость от Batf3+ДК противоопухолевых эффектов, опосредованных MVA-OVA и MVA-OVA-4-1BBL. Мыши C57BL/6 или мыши Batf3-/- подкожно (п/к) получали клетки 5×105 B16.OVA. Через семь дней (вертикальная пунктирная линия) мышей группировали и осуществляли внутриопухолевую инъекцию ФСБ или 2×108 TCID50 MVA, MVA-OVA или MVA-OVA-4-1BBL (см. пример 29). В день 5 и день 8 после первой внутриопухолевой инъекции в/о инъекцию повторяли (вертикальные пунктирные линии). Рост опухоли измеряли через равные интервалы. Фиг. 21A: показан средний объем опухоли. Фиг. 21B: Через 11 дней после первой иммунизации кровь отбирали и анализировали на наличие антигенспецифичных Т-клеток (т.е. OVA 257-264-специфичные Т-клетки). Показан процент OVA-специфичных Т-клеток среди CD8+ Т-клеток.
[065] Фиг. 22: Роль NK-клеток при внутриопухолевом введении MVA-OVA-4-1BBL у мышей с меланомой B16.OVA. Мыши C57BL/6 или мыши IL15Rα-/- подкожно (п/к) получали 5×105 клеток B16.OVA. Через семь дней мышей группировали и осуществляли внутриопухолевую инъекцию ФСБ или 2×108 TCID50 MVA-OVA или MVA-OVA-4-1BBL (см. пример 30). Обработку повторяли в день 5 и 8 после первой инъекции. Рост опухоли измеряли через равные интервалы. Показан средний диаметр опухоли (фиг. 22A) и процент выживаемости (фиг. 22B). Через 11 дней после первой иммунизации кровь отбирали и анализировали на наличие антигенспецифичных Т-клеток (фиг. 22С). Показано процентное содержание OVA 257-264-декстрамер + (SIINFEKL +) CD44+ Т-клетки в CD8+ Т-клеток.
[066] На фиг. 23 показан профиль цитокинов/хемокинов, зависимый от NK-клеток, в ответ на IT-иммунизацию MVA-OVA-4-1BBL. 5×105 клеток B16.OVA подкожно имплантировали мышам C57BL/6 и IL15Rα-/- (см. пример 31). Мышей иммунизировали внутриопухолево (в/о) в день 7 посредством ФСБ или 2×108 TCID50 MVA-OVA или MVA-OVA-4-1BBL (n=2-3 мыши/группа). Через 6 часов опухоли извлекали и лизаты опухолей обрабатывали. Профили цитокинов/хемокинов анализировали посредством Luminex. На фиг. 23 показаны те цитокины/хемокины, которые уменьшаются в отсутствие IL15Rα после внутриопухолевой (в/о) иммунизации MVA-OVA-4-1BBL.
[067] На фиг. 24 показана противоопухолевая эффективность внутриопухолевой иммунизации MVA-gp70-CD40L по сравнению с MVA-gp70-4-1BBL у мышей с меланомой B16.F10. Мыши C57BL/6 подкожно (п/к) получали 5×105 клеток B16.F10. Через семь дней мышей группировали и осуществляли внутриопухолевую инъекцию ФСБ или 5×107 TCID50 MVA-gp70, MVA-gp70-4-1BBL, MVA-gp70-CD40L, MVA-4-1BBL или MVA-CD40L (см. пример 32). Обработку повторяли в день 5 и 8 после первой инъекции. Рост опухоли измеряли через равные интервалы. На фиг. 24A показан средний диаметр опухоли, а на фиг. 24B показано появление витилиго у мышей, получавших MVA-gp70-4-1BBL. Через 11 дней после первой иммунизации кровь отбирали и анализировали на наличие антигенспецифичных Т-клеток. Процент IFNγ, продуцирующего CD44+ Т-клетки в CD8+ Т-клетках после рестимуляции p15E, показан на фиг. 24C.
[068] Фиг. 25: Противоопухолевая эффективность внутриопухолевого введения MVA-gp70-4-1BBL-CD40L у мышей с меланомой B16.F10. Мыши C57BL/6 подкожно (п/к) получали 5×105 клеток B16.F10. Через семь дней мышей группировали и осуществляли внутриопухолевую инъекцию ФСБ или 5×107 TCID50: MVA-gp70, MVA-gp70-4-1BBL, MVA-gp70-CD40L, MVA-gp70-4-1BBL-CD40L, MVA-4-1BBL, MVA-CD40L или MVA-4-1BBL-CD40L (см. пример 33). Обработку повторяли в день 5 и 8 после первой инъекции. Рост опухоли измеряли через равные интервалы. Средний диаметр опухоли показан на фиг. 25А. Через одиннадцать дней после первой иммунизации кровь отбирали и рестимулировали пептидом p15e. Процент IFNγ+ CD44+ Т-клеток в CD8+ Т-клетках показан на фиг. 25B.
[069] Фиг. 26: Противоопухолевая эффективность MVA-gp70 с адъювантом CD40L или 4-1BBL у мышей с опухолью CT26. Мыши Balb/c подкожно (п/к) получали 5×105 клеток Ct26wТ. Через семь дней мышей группировали и осуществляли внутриопухолевую инъекцию ФСБ или 5×107 TCID50: MVA-gp70, MVA-gp70-4-1BBL, MVA-gp70-CD40L, MVA-gp70-4-1BBL-CD40L, MVA-4-1BBL, MVA-CD40L и MVA-4-1BBL-CD40L (см. пример 34). Обработку повторяли в день 5 и 8 после первой инъекции. Рост опухоли измеряли через равные интервалы. На фиг. 26A показан средний диаметр опухоли, а на фиг. 26B показан процент выживаемости. Фиг. 26.C: Через одиннадцать дней после первой иммунизации кровь отбирали и рестимулировали пептидом AH1; показано процентное содержание IFNγ+ CD44+ Т-клеток в составе CD8+ Т-клеток.
[070] Фиг. 27: Количественный и качественный анализ Т-клеток микроокружения опухоли (TME) и лимфатического узла, дренирующего опухоль (TdLN) после внутриопухолевой инъекции MVA-gp70, дополнительно содержащего 4-1BBL, и/или CD40L. Мыши C57BL/6 подкожно (п/к) получали 5×105 клеток B16.F10. Спустя девять дней, когда размер опухолей превышал 5×5 мм, мышей группировали и осуществляли внутриопухолевую инъекцию ФСБ или 5×107 TCID50 of MVA-gp70, MVA-gp70-4-1BBL, MVA-gp70-CD40L или MVA-gp70-4-1BBL-CD40L (см. пример 35). Через один, три и семь дней после иммунизации мышей умерщвляли, и опухоли, а также лимфатические узлы, дренирующие опухоль (TdLN), собирали, обрабатывали коллагеназой/ДНКазой и анализировали посредством проточной цитометрии. На фиг. 27 показано количество CD8+ Т-клеток, p15E-специфичных CD8+ Т-клеток, и Ki67+ p15E-специфичных CD8+ Т-клеток на мг опухоли и на TdLN. Данные представлены в виде среднего значения ± СОС.
[071] На фиг. 28 показан количественный и качественный анализ Т-клеток микроокружения опухоли (TME) и лимфатического узла, дренирующего опухоль (TdLN) после внутриопухолевой инъекции MVA-gp70, дополнительно экспрессирующего 4-1BBL, и/или CD40L. Мыши C57BL/6 подкожно (п/к) получали 5×105 B16.F10 (см. пример 36). Спустя девять дней, когда размер опухолей превышал 5,5×5,5 мм, мышей группировали и осуществляли внутриопухолевую инъекцию ФСБ или 5×107 TCID50: MVA-Gp70, MVA-gp70-4-1BBL, MVA-gp70-CD40L и MVA-gp70-4-1BBL-CD40L. Через три дня после иммунизации мышей умерщвляли, и опухоли, а также TdLN, собирали и обрабатывали коллагеназой/ДНКазой, и полученные отдельные клетки анализировали посредством проточной цитометрии. Показано количество NK-клеток, Ki67+ NK-клеток и гранзима B+ NK-клеток на мг опухоли и TdLN. Данные представлены в виде среднего значения ± СОС.
[072] Фиг. 29: Противоопухолевая эффективность внутривенного введения MVA-gp70 с адъювантом 4-1BBL и/или CD40L у мышей с опухолью CT26.WT. Мыши Balb/c подкожно (п/к) получали 5×105 клеток CT26.WТ. Спустя двенадцать дней мышей группировали и внутривенно вводили ФСБ или 5×107 TCID50 MVA-Gp70, MVA-Gp70-4-1BBL, MVA-Gp70-CD40L, MVA-Gp70-4-1BBL-CD40L и MVA-4-1BBL-CD40L (см. пример 37). На фиг. 29A показан средний диаметр опухоли, а на фиг. 29B показан процент выживаемости. Через семь дней после первой иммунизации кровь отбирали и рестимулировали пептидом AH1; на фиг. 29C показано процентное содержание IFNγ+CD44+Т-клеток в CD8+Т-клетках в виде среднего значения ± СОС.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[073] Следует понимать, что как приведенное выше краткое описание сущности изобретения, так и приведенное ниже подробное описание являются просто иллюстративными и пояснительными и не ограничивают заявляемое изобретение.
[074] Описанные и проиллюстрированные в настоящей заявке рекомбинантный MVA и способы по настоящему изобретению усиливают несколько аспектов онкологического иммунного ответа пациента. В различных аспектах в настоящем изобретении показано, что если рекомбинантный MVA, содержащий опухолеассоциированный антиген (TAA) и антиген 4-1BBL, вводят посредством внутриопухолевой или внутривенной инъекции субъекту с раком, то у субъекта реализуется усиленный противоопухолевый эффект. Как более подробно описано в настоящем изобретении, данный усиленный противоопухолевый эффект включает более высокое уменьшение объема опухоли, повышение общей выживаемости, усиленный ответ Т-лимфоцитов CD8 на TAA и усиление воспалительных реакций, таких как повышенная активность NK-клеток, увеличение продукции цитокинов, и т.д.
[075] Описанные и проиллюстрированные в настоящей заявке рекомбинантный MVA и способы по настоящему изобретению усиливают несколько аспектов онкологического иммунного ответа пациента. В различных аспектах в настоящем изобретении показано, что если рекомбинантный MVA, содержащий опухолеассоциированный антиген (TAA) и антиген CD40L, вводят посредством внутриопухолевой или внутривенной инъекции субъекту с раком, то у субъекта реализуется усиленный противоопухолевый эффект. Как более подробно описано в настоящем изобретении, данный усиленный противоопухолевый эффект включает более высокое уменьшение объема опухоли, повышение общей выживаемости, усиленный ответ Т-лимфоцитов CD8 на TAA и усиление воспалительных реакций, таких как повышенная активность NK-клеток, увеличение продукции цитокинов, и т.д.
[076] В дополнительных аспектах в различных вариантах осуществления настоящего изобретения показано, что если рекомбинантный MVA, содержащий опухолеассоциированный антиген (TAA) и антиген 4-1BBL, вводят посредством внутриопухолевой инъекции в комбинации по меньшей мере с одним антагонистом/агонистом молекул иммунных контрольных точек, наблюдается усиленное уменьшение опухоли и повышение общей выживаемости у субъектов с раком.
[077] В дополнительных аспектах в различных вариантах осуществления настоящего изобретения продемонстрировано, что если рекомбинантный MVA, содержащий опухолеассоциированный антиген (TAA) и антиген 4-1BBL, вводят внутриопухолево в комбинации с опухолеспецифичным антителом, происходит усиление уменьшения опухоли и повышение общей выживаемости у субъекта с раком.
[078] Хотя рекомбинантные вирусы MVA ранее кодировали антиген 4-1BBL, иммуногенные преимущества MVA, кодирующего 4-1BBL, были неясны (см., например, Spencer et al. (2014) PLoS One 9(8): e105520). Согласно Spencer, совместная экспрессия 4-1BBL и трансгенного антигена либо в векторе MVA, либо в векторе аденовируса приводила к увеличению Т-клеточных ответов CD8 мыши; тем не менее, после внутримышечного введения аденовирусного вектора, кодирующего 4-1BBL, не наблюдалось никакого увеличения ответов IFN-γ у отличных от человеческих приматов (Id. на страницах 2, 6). Кроме того, иммуногенные преимущества применения MVA, кодирующего 4-1BBL, в качестве части лечения рака и разрушения опухоли и/или опухолевых клеток были неизвестны.
[079] В различных вариантах осуществления настоящего раскрытия показано, что MVA, кодирующий 4-1BBL и TAA (называемые в настоящем изобретении MVA-TAA-4-1BBL), могут быть эффективными при лечении рака у субъекта, такого как человек. Как показано и описано в настоящем изобретении, введение MVA-TAA-4-1BBL может усиливать несколько аспектов иммунной реакции субъекта с раком и может эффективно уменьшать и уничтожать опухолевые клетки. Один или более из усиленных противоопухолевых эффектов в различных вариантах осуществления настоящего раскрытия кратко изложены следующим образом.
[080] Внутривенное введение рекомбинантного MVA, кодирующего 4-1BBL, обеспечивает усиленный противоопухолевый эффект. По меньшей мере в одном аспекте настоящее изобретение включает рекомбинантный MVA, кодирующий TAA и антиген 4-1BBL (rMVA-TAA-4-1BBL), который вводят внутривенно, причем внутривенное введение усиливает противоопухолевый эффект, по сравнению с внутривенным введением рекомбинантного MVA без 4-1BBL, или по сравнению с отличным от внутривенного введения рекомбинантного MVA, кодирующего 4-1BBL (например, такого как подкожное введение рекомбинантного MVA, кодирующего 4-1BBL). Данные усиленные противоопухолевые эффекты включают усиленный ответ NK-клеток (показан на фиг. 4), усиленный воспалительный ответ, что показано увеличением секреции IFN-γ (показано на фиг. 5 и 6), усиление экспансии антиген- и вектор-специфичных Т-клеток CD8 (показано на фиг. 7) и усиление уменьшения опухоли (показано на фиг. 8).
[081] Внутриопухолевое введение рекомбинантного MVA, кодирующего 4-1BBL, усиливает воспаление в опухоли. В другом аспекте настоящего изобретения было определено, что инфицирование опухолевых клеток с использованием MVA-OVA-4-1BBL, но не MVA-OVA-CD40L, активировало антигенспецифичесные CD8+ Т-клетки с образованием цитокинов, происходящих из Т-клеток, таких как ГМ-КСФ, IL-2 и IFN-γ в отсутствие ДК, перекрестно презентующих антиген (фиг. 1A-1D). Это было неожиданно в случае GM-CSF, фактора роста, продуцируемого интектными Т-клетками при активации, которая индуцирует созревание дендритных клеток и субпопуляций миелоидных клеток (Min et al. (2010) J. Immunol. 184: 4625-4629). В присутствии перекрестно презентующих антиген ДК антигенспецифичные CD8+ Т-клетки, стимулированные инфицированными опухолевыми клетками rMVA-CD40L, продуцировали IFN-γ, но не IL-2 или ГМ-КСФ, как rMVA-4-1BBL (фиг. 1A-1D). Интересно, что были обнаружены большие количества IL-6, ключевого цитокина, продуцируемого ДК (фиг. 1A).
[082] В одном преимущественном аспекте усиление воспаления в опухоли может привести к наличию большого количества TIL (инфильтрирующих опухоль лимфоцитов), уничтожающих опухолевые клетки в месте опухоли (см., например, Lanitis et al. (2017) Annals Oncol. 28 (suppl 12): xii18-xii32). Данные опухоли с воспалением, также известные как «горячие» опухоли, обеспечивают усиленное разрушение опухолевых клеток ввиду увеличения количества TIL, цитокинов и других воспалительных молекул.
[083] Внутриопухолевое введение рекомбинантного MVA, кодирующего 4-1BBL, снижает объем опухоли и повышает общую выживаемость. В одном аспекте настоящее изобретение включает рекомбинантный MVA, кодирующий антиген 4-1BBL (MVA-4-1BBL), который вводят посредством внутриопухолевой инъекции, причем внутриопухолевое введение усиливает противоопухолевые эффекты у субъекта с раком по сравнению с внутриопухолевым введением рекомбинантного MVA без 4-1BBL.
[084] В то время как рекомбинантные вирусы MVA ранее вводили посредством внутриопухолевой инъекции (см., например, White et al. (2018) PLoS One 13: e0193131, и Nemeckova et al. (2007) Neoplasma 54: 326-33), исследования обеспечивали разные результаты. Например, согласно Nemeckova, было обнаружено, что внутриопухолевые инъекции вируса осповакцины MVA, экспрессирующего ГМ-КСФ, и иммунизация ДНК-вакциной повышали выживаемость мышей с опухолями, индуцированными ВПЧ16 (см. Nemeckova в разделе Реферат). В качестве альтернативы, White et al. не смогли продемонстрировать ингибирование роста опухоли поджелудочной железы после внутриопухолевой инъекции MVA (см. White в разделе Реферат).
[085] В рамках настоящего изобретения рекомбинантный MVA, содержащий одну или несколько нуклеиновых кислот, кодирующих TAA и 4-1BBL, вводили субъекту посредством внутриопухолевой инъекции. На фиг. 9 показано, что внутриопухолевое введение MVA-TAA-4-1BBL продемонстрировало значительное уменьшение объема опухоли по сравнению с TAA рекомбинантного MVA.
[086] Внутриопухолевое введение рекомбинантного MVA, кодирующего 4-1BBL, введенного в комбинации с антагонистом или агонистом иммунных контрольных точек обеспечивает усиленный противоопухолевый эффект. В различных вариантах осуществления настоящее изобретение включает введение MVA-TAA-4-1BBL в комбинации с антагонистом или агонистом иммунных контрольных точек. Предпочтительно введение MVA-TAA-4-1BBL является внутривенным или внутриопухолевым путем. MVA по настоящему изобретению в комбинации с антагонистом или агонистом иммунных контрольных точек являются преимущественными поскольку комбинация обеспечивает более эффективное лечение рака. Например, комбинация и/или комбинированная терапия по настоящему изобретению усиливает многие аспекты иммунного ответа онкологического пациента. По меньшей мере в одном аспекте комбинация синергетическим образом повышает как врожденный, так и адаптивный иммунные ответы и, при соединении с антагонистом или агонистом молекулы иммунных контрольных точек, снижает объем опухоли и повышает выживаемость онкологического пациента.
[087] Данные, представленные в настоящей заявке, демонстрируют, что MVA-TAA-4-1BBL в комбинации с антагонистом или агонистом иммунных контрольных точек вызывает усиленный противоопухолевый эффект. Действительно, как показано на фиг. 11, если внутриопухолевое введение MVA-OVA-4-1BBL объединяли с антителом к PD-1 внутрибрюшинно, наблюдали снижение объема опухоли по сравнению с PD-1.
[088] Внутриопухолевое введение рекомбинантного MVA, кодирующего 4-1BBL, в комбинации с антителом, специфичным к опухолеассоциированному антигеному (TAA), обеспечивает повышенный противоопухолевый эффект. В различных вариантах осуществления настоящее изобретение включает введение MVA-TAA-4-1BBL в комбинации с антителом, специфичным к TAA. Предпочтительно введение MVA-TAA-4-1BBL является внутривенным или внутриопухолевым. MVA по настоящему изобретению в комбинации с антителами, специфичными к TAA, являются предпочтительными и могут работать вместе, обеспечивая более эффективное лечение рака.
[089] В одном иллюстративном аспекте усиленный ответ NK-клеток, индуцированный введением MVA-TAA-4-1BBL, работает синергетическим образом с антителом, специфичным к TAA, усиливая зависимую от антител цитотоксичность (АЗКЦ) у субъекта. Данное усиление АЗКЦ у субъекта с раком приводит к повышению уничтожения опухолевых клеток и разрушения опухоли.
[090] Данные, представленные в настоящей заявке, демонстрируют, что MVA-TAA-4-1BBL в комбинации с антителом, специфичным к TAA, обеспечивает усиленный противоопухолевый эффект. Действительно, как показано на фиг. 11, если внутриопухолевое введение MVA-OVA-4-1BBL объединяли с антителом к TRP-1 внутрибрюшинно, наблюдали снижение объема опухоли по сравнению с антителом TRP-1.
[091] Введение MVA-TAA-4-1BBL в качестве части первичной и бустерной иммунизации согласно настоящему изобретению повышает экспансию антиген- и вектор-специфичных CD8+ Т-клеток. В других аспектах настоящее изобретение относится к способу, в котором MVA-TAA-4-1BBL вводят в качестве части гомологичной и/или гетерологичной схемы прайм-буст вакцинации. Предпочтительно введение MVA-TAA-4-1BBL является внутривенным или внутриопухолевым. Как показано на фиг. 7, экспансия антиген- и вектор-специфичных CD8+ Т-клеток повышалась в ходе первичной и бустерной иммунизации посредством внутривенного введения MVA-TAA-4-1BBL.
Определения
[092] В контексте настоящего изобретения формы единственного числа включают ссылки на формы множественного числа, если из контекста явно следует иное. Так, например, ссылка на «нуклеиновую кислоту» включает одну или более нуклеиновых кислот, а ссылка на «способ» включает ссылку на эквивалентные этапы и способы, известные специалистам в данной области техники, которыми могут быть модифицированы или замещены способы, описанные в настоящем изобретении.
[093] Если не указано иное, термин «по меньшей мере», предшествующий ряду элементов, следует понимать как относящийся к каждому элементу ряда. Специалистам в данной области будет понятно или они смогут установить, используя не более чем рутинные эксперименты, существование многочисленных эквивалентов конкретных вариантов осуществления изобретения, описанных в настоящем изобретении. Подразумевается, что такие эквиваленты охвачены объемом настоящего изобретения.
[094] В тексте этого описания и следующей за ним формулы изобретения, если из контекста не следует иное, слово «содержать», и его вариации, такие как «содержит» и «содержащий», следует понимать как включение указанного целого числа или этапа или группы целых чисел или этапов, но не исключение какого-либо другого целого числа или этапа или группы целых чисел или этапов. В контексте настоящего изобретения термин «содержащий» может быть заменен термином «включающий» или иногда, в контексте настоящего изобретения, термином «имеющий». Любой из вышеуказанных терминов (содержащий, включающий, имеющий), хотя это и менее предпочтительно, в каждом случае, когда он употреблен в настоящем изобретении в контексте аспекта варианта осуществления настоящего изобретения, может быть заменен термином «состоящий из». В контексте настоящего изобретения термин «состоящий из» исключает любой элемент, этап или ингредиент, не указанные в элементе пункта формулы изобретения. В контексте настоящего изобретения термин «состоящий преимущественно из» не исключает материалы или этапы, которые не оказывают существенное влияние на основные и новые характеристики пункта формулы изобретения.
[095] В контексте настоящего изобретения соединительный термин «и/или» между множеством перечисляемых элементов следует понимать как включающий, как отдельные, так и комбинированные варианты. Например, если два элемента соединены «и/или», первый вариант относится к применению первого элемента без второго. Второй вариант относится к применению второго элемента без первого. Третий вариант относится к применению первого и второго элементов вместе. Подразумевается, что любой из этих вариантов соответствует значению и, соответственно, удовлетворяет требованию термина «и/или» в контексте настоящего изобретения. Также подразумевается, что одновременное применение более чем одного из этих вариантов соответствует значению и, соответственно, удовлетворяет требованию термина «и/или».
[096] Описанный в настоящем изобретении «мутированный» или «модифицированный» белок или антиген означает любую модификацию нуклеиновой кислоты или аминокислоты, такую как делеции, добавления, вставки и/или замещения.
[097] «Процент (%) гомологии или идентичности последовательности» в отношении последовательностей нуклеиновых кислот, описанных в настоящем изобретении, определяется как процентное содержание нуклеотидов в кандидатной последовательности, которые являются идентичными с нуклеотидами в референсной последовательности (т.е. последовательности нуклеиновой кислоты, из которой она получена), после выравнивания последовательностей и введения в случае необходимости гэпов для достижения максимального процента идентичности последовательности и не считая любые консервативные замены частью идентичности последовательности. Выравнивание в целях определения процента идентичности или гомологии нуклеотидной последовательности можно осуществлять различными способами, находящимися в компетенции специалиста в данной области техники, например, с помощью общедоступного компьютерного программного обеспечения, такого как BLAST, ALIGN или Megalign (DNASTAR). Специалисты в данной области техники могут определить соответствующие параметры для определения выравнивания, включая любые алгоритмы, необходимые для достижения максимального выравнивания по всей длине сравниваемых последовательностей.
[098] Например, соответствующее выравнивание для последовательностей нуклеиновых кислот обеспечивает алгоритм локальной гомологии Смита и Уотермана (Smith and Waterman, (1981) Advances in Applied Mathematics 2:482- 489). Данный алгоритм можно использовать к аминокислотным последовательностям, используя весовую матрицу, разработанную Dayhoff, Atlas of Protein Sequences and Structure, M. O. Dayhoff ed., 5 suppl. 3:353-358, National Biomedical Research Foundation, Washington, D.C., USA, и нормализованную Gribskov ((1986) Nucl. Acids Res. 14(6): 6745-6763) Пример осуществления этого алгоритма для определения процента идентичности последовательности приведен в Genetics Computer Group (Madison, Wisconsin, USA) в приложении «BestFit». Параметры по умолчанию для этого метода описаны в Wisconsin Sequence Analysis Package Program Manual, версия 8 (1995) (доступная от Genetics Computer Group, г. Мэдисон, штат Висконсин). Предпочтительный способ определения процента идентичности в контексте настоящего изобретения заключается в использовании пакета программ MPSRCH, защищенного авторским правом Эдинбургского университета, разработанного Collins и Sturrok и распространяемого IntelliGenetics, Inc. (Mountain View, California, USA). Из этого набора пакетов может быть использован алгоритм Смита-Уотермана, если для оценочной таблицы используются параметры по умолчанию (например, штраф за открытие гэпа, равный 12, штраф за продление гэпа, равный одному и гэп, равный шести). Из сгенерированных данных значение «соответствие» (англ. - «Match») отражает «идентичность последовательности». Другие подходящие программы для вычисления процента идентичности или сходства между последовательностями в целом известны в данной области техники, например, другой программой выравнивания является BLAST, используемая с параметрами по умолчанию. Например, BLASTN и BLASTP можно использовать со следующими параметрами по умолчанию: генетический код=стандарт; фильтр=отсутствует; цепь=обе; отсечение=60; ожидание=10; матрица=BLOSUM62; описания=50 последовательностей; сортировать по=НАИБОЛЬШЕЙ ОЦЕНКЕ; базы данных=не дублирующиеся, GenBank+EMBL+DDBJ+PDB+переводы GenBank CDS+Swiss protein+Spupdate+PIR. Подробную информацию по этим программам можно найти по следующему интернет-адресу: blast.ncbi.nlm.nih.gov/.
[099] Термин «прайм-буст вакцинация» или «схема прайм-буст» относится к стратегии или схеме вакцинации с использованием первой первичной инъекции вакцины, нацеленной на конкретный антиген, с последующими через определенные промежутки времени одной или более бустерными инъекциями той же вакцины. Прайм-буст вакцинация может быть гомологичной или гетерологичной. В гомологичной прайм-буст вакцинации используют вакцину, содержащую одинаковые антиген и вектор как для первичной инъекции, так и для одной или более бустерных инъекций. В гетерологичной прайм-буст вакцинации используют вакцину, содержащую одинаковый антиген как для первичной инъекции, так и для одной или более бустерных инъекций, но разные векторы для первичной инъекции и для одной или более бустерных инъекций. Например, в гомологичной прайм-буст вакцинации можно использовать рекомбинантный поксвирус, содержащий нуклеиновые кислоты, экспрессирующие один или более антигенов, для первичной инъекции, и такой же рекомбинантный поксвирус, экспрессирующий один или более антигенов, для одной или более бустерных инъекций. В противоположность этому, в гетерологичной прайм-буст вакцинации можно использовать рекомбинантный поксвирус, содержащий нуклеиновые кислоты, экспрессирующие один или более антигенов, для первичной инъекции, и другой рекомбинантный поксвирус, экспрессирующий один или более антигенов, для одной или более бустерных инъекций.
[0100] Термин «рекомбинантный» означает полинуклеотид, вирус или вектор полусинтетического или синтетического происхождения, который либо не существует в природе, либо связан с другим полинуклеотидом в порядке, не встречающемся в природе. Под «рекомбинантным MVA» или «rMVA» в контексте настоящего описания обычно подразумевается модифицированный вирус осповакцины Анкара (MVA), который содержит по меньшей мере один полинуклеотид, кодирующий антиген, связанный с опухолью (TAA).
[0101] В рамках изобретения уменьшение объема опухоли или уменьшение объема опухоли можно охарактеризовать как уменьшение объема и/или размера опухоли, но также можно охарактеризовать с точки зрения конечных точек клинических испытаний, понятных в данной области. Некоторые иллюстративные конечные результаты клинического исследования, связанные со снижением объема и/или размера опухоли, могут включать без ограничения частоту ответов (ЧО), частоту объективных ответов (ЧОО) и т.д.
[0102] В контексте настоящего изобретения повышение уровня выживаемости можно охарактеризовать как повышение выживаемости онкологического пациента, но также можно охарактеризовать в терминах конечных результатов клинического исследования, известных в данной области техники. Некоторые иллюстративные конечные результаты клинического исследования, связанные со снижением объема и/или размера опухоли, могут включать без ограничения частоту ответов (ЧО), частоту объективных ответов (ЧОО) и т.д.
[0103] В контексте настоящего изобретения «трансген» или «гетерологичный» ген следует понимать как нуклеотидную или аминокислотную последовательность, которая не присутствует в геноме поксвируса дикого типа (например, вируса осповакцины, вируса оспы кур или MVA). Специалисту в данной области понятно, что «трансген» или «гетерологичный ген», если он присутствует в поксвирусе, таком как вирус осповакцины, должен быть включен в геном поксвируса так, чтобы после введения рекомбинантного поксвируса в клетку-хозяина он экспрессировался в виде соответствующего гетерологичного генного продукта, т.е. в виде «гетерологичного антигена» и/или «гетерологичного белка». Экспрессию обычно обеспечивают посредством функционального связывания гетерологичного гена с регуляторными элементами, которые делают возможной экспрессию в инфицированной поксвирусом клетке. Предпочтительно регуляторные элементы включают природный и синтетический поксвирусный промотор.
[0104] «Вектор» относится к рекомбинантным ДНК- или РНК-плазмиде или вирусу, которые могут содержать гетерологичный полинуклеотид. Гетерологичный полинуклеотид может содержать представляющую интерес последовательность в целях предотвращения или терапии и может, необязательно, иметь форму экспрессионной кассеты. В контексте настоящего изобретения вектор не обязательно должен быть способен к репликации в конечной целевой клетке или организме субъекта. Этот термин включает клонирующие векторы и вирусные векторы.
Комбинации и способы
[0105] В различных вариантах осуществления настоящее изобретение включает рекомбинантный MVA, содержащий первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA), и вторую нуклеиновую кислоту, кодирующую 4-1BBL, который при внутриопухолевом введении индуцирует как воспалительный ответ, так и усиленный Т-клеточный ответ по сравнению с воспалительным ответом и Т-клеточным ответом, индуцированным отличным от внутриопухолевого введением рекомбинантного вируса MVA, содержащего первую нуклеиновую кислоту, кодирующую TAA, и вторую нуклеиновую кислоту, кодирующую 4-1BBL.
[0106] В различных дополнительных вариантах осуществления настоящее изобретение включает первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA), и вторую нуклеиновую кислоту, кодирующую 4-1BBL, который при внутриопухолевом введении индуцирует как усиленный внутриопухолевый воспалительный ответ, так и усиленный T-клеточный ответ по сравнению с внутриопухолевым воспалительным ответом и T-клеточным ответом, индуцированным посредством внутриопухолевого введения рекомбинантного вируса MVA, содержащего первую нуклеиновую кислоту, кодирующую TAA.
[0107] Усиленный воспалительный ответ в опухоли. В различных аспектах настоящего раскрытия было определено, что внутриопухолевое введение рекомбинантного MVA, кодирующего TAA и 4-1BBL, вызывает усиленный воспалительный ответ в опухоли по сравнению с введением рекомбинантного MVA отдельно. По меньшей мере в одном аспекте «усиленный воспалительный ответ» в опухоли согласно настоящему раскрытию характеризуется одним или несколькими из следующих: 1) увеличением экспрессии IFN-γ и/или 2) увеличением экспрессии гранзима B (GraB) в опухоли и/или опухолевых клетках. Таким образом, усиливается ли воспалительный ответ в опухоли и/или опухолевых клетках в соответствии с настоящим описанием, можно определить посредством измерения для определения того, наблюдается ли повышение экспрессии одной или нескольких молекул, которые указывают на усиление воспалительного ответа, включая секрецию хемокинов и цитокинов, как известно в данной области. Иллюстративные маркеры воспалительного ответа включают один или более маркеров, которые применяют для измерения частоты и/или активности NK-клеток, включая один или более из следующих: IFN-γ и/или гранзим B (GraB). Эти молекулы и их измерения относятся к валидированным методам анализа, известным в данной области техники, которые можно проводить в соответствии с известными методиками. См., например, Borrego et al. ((1999) Immunology 7(1): 159-165).
[0108] Усиленный ответ NK-клеток. В различных дополнительных аспектах настоящего раскрытия было определено, что внутриопухолевое введение или внутривенное введение рекомбинантного MVA, кодирующего TAA и 4-1BBL, вызывает усиленный ответ NK-клеток в опухоли или опухолевой среде по сравнению с введением рекомбинантного MVA отдельно. В одном аспекте «усиленный ответ NK-клеток» согласно настоящему раскрытию характеризуется одним или несколькими из следующих: 1) повышением частоты NK-клеток, 2) повышением активации NK-клеток и/или 3) повышением пролиферации NK-клеток. Таким образом, то, усилен ли ответ NK-клеток в соответствии с настоящим описанием, можно определить, измеряя экспрессию одного или более молекул, показательных для повышения частоты NK-клеток, повышения активации NK-клеток и/или повышения пролиферации NK-клеток. Примеры маркеров, которые можно использовать для измерения частоты и/или активности NK-клеток, включают один или более из следующих: NKp46, IFN-γ, CD69, CD70, NKG2D, FasL, гранзим B, CD56 и/или Bcl-XL. Типовые маркеры, применимые при определении активации NK-клеток, включают один или более из IFN-γ, CD69, CD70, NKG2D, FasL, гранзима B и/или Bcl- XL. Типовые маркеры, применимые при определении пролиферации NK-клеток, включают Ki67. Эти молекулы и их измерения относятся к валидированным методам анализа, известным в данной области техники, которые можно проводить в соответствии с известными методиками (см., например, Borrego et al. (1999) Immunology 7(1): 159-165). Помимо этого, способы анализа для измерения молекул можно найти в примерах 5 и 6 настоящего описания. По меньшей мере в одном аспекте 1) повышение частоты NK-клеток можно определить как по меньшей мере 2-кратное повышение количества CD3-NKp46+ клеток по сравнению с количеством до обработки/исходным уровнем; 2) повышение активации NK-клеток можно определить как по меньшей мере 2-кратное повышение экспрессии IFN-γ, CD69, CD70, NKG2D, FasL, гранзима B и/или Bcl-XL по сравнению с экспрессией до обработки/на исходном уровне; и/или 3) повышение пролиферации NK-клеток можно определить как по меньшей мере 1,5-кратное повышение экспрессии Ki67 по сравнению с экспрессией до обработки/на исходном уровне.
[0109] Усиленный ответ Т-клеток. В соответствии с настоящей заявкой «усиленный Т-клеточный ответ» характеризуется одним или несколькими из следующего: 1) повышением частоты CD8 T-клеток; 2) повышением активации CD8 T-клеток; и/или 3) повышением пролиферации CD8 T-клеток. Таким образом, то, усилен ли ответ T-клеток в соответствии с настоящей заявкой, можно определить, измеряя экспрессию одного или более молекул, показательных для 1) повышения частоты CD8 T-клеток, 2) повышения активации CD8 T-клеток и/или 3) повышения пролиферации CD8 T-клеток. Типовые маркеры, применимые для определения частоты, активации и пролиферации CD8 T-клеток, включают CD3, CD8, IFN-γ, TNF-α, IL-2, CD69 и/или CD44 и Ki67, соответственно. Измерение частоты антигенспецифичных Т-клеток также можно измерить с использованием мультимеров MHC, таких как пентамеры или декстрамеры, как показано в настоящей заявке. Такие измерения и анализы, а также другие подходящие для применения при оценке способов и композиций по настоящему изобретению подтверждены и понятны в данной области.
[0110] В одном аспекте повышение частоты CD8 T-клеток характеризуется по меньшей мере 2-кратным повышением количества IFN-γ и/или декстрамер+ CD8 T-клеток по сравнению с количеством до обработки/на исходном уровне. Повышение активации CD8 T-клеток характеризуется как по меньшей мере 2-кратное повышение экспрессии CD69 и/или CD44 по сравнению с экспрессией до обработки/на исходном уровне. Повышение пролиферации CD8 T-клеток характеризуется как по меньшей мере 2-кратное повышение экспрессии Ki67 по сравнению с экспрессией до обработки/на исходном уровне.
[0111] В альтернативном аспекте усиленный ответ Т-клеток характеризуется повышением экспрессии CD8 T-клетками эффекторных цитокинов и/или повышением цитотоксических эффекторных функций. Повышение экспрессии эффекторных цитокинов можно определить по экспрессии одного или более из IFN-γ, TNF-α и/или IL-2 по сравнению с экспрессией до обработки/на исходном уровне. Повышение цитотоксических эффекторных функций можно определить по экспрессии одного или более из CD107a, гранзима B и/или перфорина и/или антиген-специфичному уничтожению клеток-мишеней.
[0112] Описанные в настоящем изобретении методы анализа, цитокины, маркеры и молекулы, а также их измерения валидированы и известны в данной области техники, и их можно проводить в соответствии с известными методиками. Кроме того, анализы для измерения ответов Т-клеток можно найти в рабочих примерах, в которых анализировали ответы Т-клеток, включая без ограничения примеры 2, 3, 8, 13 и 14.
[0113] Усиленный ответ Т-клеток, реализуемый посредством настоящего изобретения, обеспечивает исключительное преимущество в комбинации с усиленным ответом Nk-клеток и усиленный воспалительный ответ, так как усиленный ответ Т-клеток эффективно нацеливается и уничтожает те опухолевые клетки, которые уклонились и/или выжили после начальных ответов врожденного иммунитета у онкологического пациента.
[0114] В других дополнительных вариантах осуществления комбинации и способы, описанные в настоящем изобретении, предназначены для лечения онкологического пациента-человека. В предпочтительных вариантах осуществления онкологический пациент страдает раком и/или имеет установленный диагноз рак, выбранный из группы, включающей следующее: рак молочной железы, рак легкого, рак головы и шеи, рак щитовидной железы, меланома, рак пищевода, рак мочевого пузыря, рак почки, рак печени, меланома, рак поджелудочной железы, рак предстательной железы, рак яичника, рак уротелия, рак шейки матки или колоректальный рак. В других дополнительных вариантах осуществления комбинации и способы, описанные в настоящем изобретении, предназначены для лечения онкологического пациента-человека, страдающего раком и/или имеющий установленный диагноз рак молочной железы, колоректальный рак или меланома, предпочтительно меланома, более предпочтительно колоректальный рак или наиболее предпочтительно колоректальный рак.
[0115] Некоторые иллюстративные опухолеассоциированные антигены. В некоторых вариантах осуществления у субъекта возникает иммунный ответ против ассоциированного с клеткой полипептидного антигена. В некоторых подобных вариантах осуществления ассоциированный с клеткой полипептидный антиген представляет собой опухолеассоциированный антиген (TAA).
[0116] Термин «полипептид» относится к полимеру из двух или более аминокислот, соединенных друг с другом пептидными связями или модифицированными пептидными связями. Аминокислоты могут быть встречающимися в природе, а также не встречающимися в природе, или химическими аналогами встречающейся в природе аминокислоты. Термин также относится к белкам, то есть функциональным биомолекулам, содержащим по меньшей мере один полипептид; если они включают по меньшей мере два полипептида, они могут образовывать комплексы, быть ковалентно связанными или могут быть нековалентно связанными. Полипептиды в белке могут быть гликозилированным и/или липидированным, и/или содержать простетические группы.
[0117] Эндогенные ретровирусные белки (ERV). Предпочтительно ТАА воплощен в эндогенных ретровирусных белках (ERV). Более предпочтительно ERV представляет собой ERV из семейства белков HERV-K человека. Наиболее предпочтительно белок HERV-K выбран из оболочечного белка (env) HERV-K, белка HERV-K-группоспецифичного антигена (gag) и белка HERV-K «маркера риска меланомы» (mel) (см., например, Cegolon et al. (2013) BMC Cancer 13:4).
[0118] ERV составляют 8% генома человека и произошли от инфекций зародышевой линии миллионы лет назад. Большинство данных элементов, вставленных в наш геном, сильно мутированы и, следовательно, не транскрибируются и не транслируются. Тем не менее, небольшая, относительно недавно приобретенная фракция ERV все еще функционирует и транслируется, а в некоторых случаях даже производит вирусные частицы. Транскрипция ERV очень ограничена, поскольку локус обычно сильно метилирован и, следовательно, не транскрибируется в соматических клетках (Kassiotis (2016) Nat. Rev. Immunol. 16: 207-19). Только при некоторых обстоятельствах, таких как клеточный стресс (химические вещества, УФ-излучение, гормоны, цитокины), ERV могут быть реактивированы. Важно отметить, что ERV также экспрессируются во многих различных типах рака, но не в нормальных тканях (Cegolon et al. (2013) BMC Cancer 13: 4; Wang-Johanning et al. (2003) Oncogene 22: 1528-35). Данный очень ограниченный паттерн экспрессии гарантирует, что ERV не подвергаются или редко подвергаются воздействию механизмов иммунологической толерантности, что предположительно приводит к компетентному репертуару ERV-специфичных Т-клеток. Таким образом, ERV можно использовать в MVA в качестве опухолевых антигенов («TAA»).
[0119] В различных вариантах осуществления TAA включает без ограничения HER2, PSA, PAP, CEA, MUC-1, FOLR1, PRAME, сурвивин, TRP1, TRP2 или Brachyury отдельно или в комбинациях. Такая иллюстративная комбинация может включать CEA и MUC-1, например, в MVA, также известном как CV301. Другие иллюстративные комбинации могут включать PAP и PSA.
[0120] В следующих дополнительных вариантах осуществления дополнительные TAA включают без ограничения 5-альфа-редуктазу, альфа-фетопротеин, AM-1, APC, April, BAGE, бета-катенин, Bcl12, bcr-abl, CA-125, CASP-8/FLICE, катепсины, CD19, CD20, CD21, CD23, CD22, CD33 CD35, CD44, CD45, CD46, CD5, CD52, CD55, CD59, CDC27, CDK4, CEA, c-myc, Cox-2, DCC, DcR3, E6/E7, CGFR, EMBP, Dna78, фарнезилтрансферазу, FGF8b, FGF8a, FLK-1/KDR, рецептор фолиевой кислоты, G250, GAGE-семейство, гастрин 17, гастрин-высвобождающий гормон, GD2/GD3/GM2, GnRH, GnTV, GP1, gp100/Pmel17, gp-100-in4, gp15, gp75/TRP1, hCG, гепараназу, Her2/neu, HMTV, Hsp70, hTERT, IGFR1, IL-13R, iNOS, Ki67, KIAA0205, K-ras, H-ras, N-ras, KSA, LKLR-FUT, MAGE-семейство, маммаглобин, MAP17, мелан-A/MART-1, мезотелин, MIC A/B, MT-MMPs, муцин, NY-ESO-1, остеонектин, p15, P170/MDR1, p53, p97/меланотрансферрин, PAI-1, PDGF, uPA, PRAME, пробазин, прогенипоиентин, PSA, PSM, RAGE-1, Rb, RCAS1, SART-1, SSX-семейство, STAT3, STn, TAG-72, TGF-альфа, TGF-бета, тимозин-бета-15, TNF-альфа, TRP1, TRP2, тирозиназу, VEGF, ZAG, p16INK4 и глутатион-S-трансферазу.
[0121] Предпочтительный антиген PSA содержит аминокислотную замену изолейцина на лейцин в позиции 155 (см. Патент США 7,247,615, включенный в настоящий документ посредством ссылки).
[0122] В одном или более предпочтительных вариантах осуществления настоящего изобретения гетерологичный TAA выбран из HER2 и/или Brachyury.
[0123] Любой ТАА можно использовать при условии, что он выполняет по меньшей мере одну цель или необходимое окончание настоящего изобретения, такое как, например, стимуляция иммунного ответа после введения MVA, содержащего его. Иллюстративные последовательности TAA, включая TAA, указанные в настоящем изобретении, известны в данной области и пригодны для применения в композициях и способах по настоящему изобретению. Последовательности TAA для применения в композициях и способах по настоящему изобретению могут быть идентичны последовательностям, известных в данной области или раскрытых в настоящем изобретении, или они могут быть идентичны менее чем на 100%, например, по меньшей мере на 90%, 91%, 92%, 95%, 97%, 98% или 99% или более идентичны последовательности либо нуклеотида, или аминокислоты, известной в данной области или раскрытой в настоящем изобретении. Таким образом, последовательность TAA для применения в композиции или способе по настоящему изобретению может отличаться от эталонной последовательности, известной в данной области и/или раскрытой в настоящем изобретении, менее чем на 20 или менее чем на 19, 18, 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 нуклеотидов или аминокислот, при условии, что он выполняет по крайней мере одну цель или необходимое окончание настоящего изобретения. Специалист в данной области знаком со способами и анализами для оценки TAA для гарантии их пригодности для применения в MVA или способе по настоящему изобретению.
[0124] Модифицированные опухолеассоциированные антигены. В некоторых вариантах осуществления ассоциированный с клеткой полипептидный антиген модифицирован таким образом, что CTL-ответ индуцируется против клетки, которая представляет эпитопы, полученные из полипептидного антигена, на своей поверхности, если они представлены в ассоциации с молекулой MHC I класса на поверхности APC. В некоторых таких вариантах осуществления по меньшей мере один первый чужеродный эпитоп TH, если он присутствует, связан с молекулой MHC II класса на поверхности APC. В некоторых подобных вариантах осуществления ассоциированный с клеткой антиген представляет собой опухолеассоциированный антиген.
[0125] Примеры APC, способных представлять эпитопы, включают дендритные клетки и макрофаги. Дополнительные иллюстративные APC включают любые пино- или фагоцитирующие APC, которые способны одновременно презентовать: 1) эпитопы CTL, связанные с молекулами MHC I класса; и 2) эпитопы TH, связанные с молекулами MHC II класса.
[0126] В некоторых вариантах осуществления модификации одного или более TAA, таких как, помимо прочего, HERV-K env, HERV-K gag, HERV-K mel, CEA, MUC-1, PAP, PSA, PRAME, FOLR1, HER2, сурвивин, TRP1, TRP2 или Brachyury получают таким образом, что после введения субъекту вырабатываются поликлональные антитела, которые преимущественно реагируют с одним или несколькими TAA, описанными в настоящем изобретении. Такие антитела могут атаковать и уничтожать опухолевые клетки, а также предотвращать превращение метастатических клеток в метастазы. Эффекторный механизм данного противоопухолевого эффекта опосредуется через комплемент и антитело-зависимую клеточную цитотоксичность. Кроме того, индуцированные антитела могут также ингибировать рост раковых клеток посредством ингибирования зависимой от фактора роста олигодимеризации и интернализации рецепторов. В некоторых вариантах осуществления такие модифицированные ТАА могут индуцировать ответы CTL, направленные против известных и/или предсказанных эпитопов ТАА, отображаемых опухолевыми клетками.
[0127] В некоторых вариантах осуществления модифицированный полипептидный антиген ТАА содержит эпитоп CTL ассоциированного с клеткой полипептидного антигена и вариацию, причем вариация содержит по меньшей мере один эпитоп CTL или чужеродный эпитоп TH. Некоторые такие модифицированные TAA могут включать в одном неограничивающем примере один или более полипептидных антигенов HER2, содержащих по меньшей мере один эпитоп CTL, и вариацию, содержащую по меньшей мере один эпитоп CTL чужеродного эпитопа TH, и способы их получения описаны в Патенте США №7005498 и патентных публикациях США №№ 2004/0141958 и 2006/0008465.
[0128] Некоторые такие модифицированные TAA могут включать в одном неограничивающем примере один или более полипептидных антигенов MUC-1, содержащих по меньшей мере один эпитоп CTL, и вариацию, содержащую по меньшей мере один эпитоп CTL чужеродного эпитопа, и способы их получения описаны в патентных публикациях США № и 2014/0363495.
[0129] Дополнительные беспорядочные Т-клеточные эпитопы включают пептиды, способные связывать большую часть молекул HLA-DR, кодируемых разными HLA-DR. См., например, WO 98/23635 (Frazer I.H. et al., назначенный The University of Queensland); Southwood et. al. (1998) J. Immunol. 160: 3363 3373; Sinigaglia et al. (1988) Nature 336: 778 780; Rammensee et al. (1995) Immunogenetics 41: 178 228; Chicz et al. (1993) J. Exp. Med. 178: 27 47; Hammer et al. (1993) Cell 74: 197 203; и Falk et al. (1994) Immunogenetics 39: 230 242. Последняя ссылка также касается лигандов HLA-DQ и -DP. Все эпитопы, перечисленные в данных ссылках, являются подходящими в качестве возможных природных эпитопов, как описано в настоящем изобретении, как и эпитопы, которые имеют общие с ними мотивы.
[0130] В определенных других вариантах осуществления беспорядочный Т-клеточный эпитоп представляет собой искусственный Т-клеточный эпитоп, который способен связывать большую часть гаплотипов. В некоторых таких вариантах осуществления искусственный Т-клеточный эпитоп представляет собой пептид-эпитоп pan DR («PADRE»), как описано в WO 95/07707 и в соответствующей статье Alexander et al. (1994) Immunity 1: 751 761.
[0131] 4-1BBL (также называемый в настоящем изобретении «41BBL» или «лиганд 4-1BB»). Как показано в настоящем раскрытии, включение 4-1BBL в качестве части рекомбинантный MVA и сопутствующие способы индуцируют повышенные и усиленные противоопухолевые эффекты при внутриопухолевом или внутривенном введении субъекту с раком. Таким образом, в различных вариантах осуществления помимо кодирования TAA, существует рекомбинантный MVA, кодирующий антиген 4-1BBL.
[0132] 4-1BB/4-1BBL является членом суперсемейства TNFR/TNF. 4-1BBL представляет собой костимулирующий лиганд, экспрессируемый в активированных В-клетках, моноцитах и ДК. 4-1BB конститутивно экспрессируется естественными клетками-киллерами (NK) и естественными киллерными T-клетками (NKT), Treg и несколькими популяциями клеток врожденного иммунитета, включая ДК, моноциты и нейтрофилы. Интересно, что 4-1BB экспрессируется на активированных, но не на Т-клетках в состоянии покоя (Wang et al. (2009) Immunol. Rev. 229: 192-215). Лигирование 4-1BB индуцирует пролиферацию и продукцию интерферона гамма (IFN-γ) и интерлейкина 2 (IL-2), а также повышает выживаемость Т-клеток за счет активации антиапоптозных молекул, таких как Bcl-xL (Snell et al. (2011) Immunol. Rev. 244: 197-217). Важно отметить, что стимуляция 4-1BB усиливает пролиферацию NK-клеток, продукцию IFN-γ и цитолитическую активность за счет усиления антителозависимой клеточноопосредованной цитотоксичности (АЗКЦ) (Kohrt et al. (2011) Blood 117: 2423-32).
[0133] В одном или более предпочтительных вариантах осуществления 4-1BBL кодируется MVA по настоящему изобретению. В одном или более других предпочтительных вариантах осуществления 4-1BBL представляет собой 4-1BBL человека. В еще более предпочтительных вариантах осуществления 4-1BBL содержит нуклеиновую кислоту, кодирующую аминокислотную последовательность, имеющую последовательность, идентичную SEQ ID NO: 3 по меньшей мере на 90%, 95%, 97%, 98% или 99%, т.е. из аминокислотной последовательности, указанной в SEQ ID NO: 3, менее чем на 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 аминокислоту. В еще более предпочтительных вариантах осуществления 4-1BBL содержит нуклеиновую кислоту, кодирующую аминокислотную последовательность, содержащую SEQ ID NO: 3. В других вариантах осуществления нуклеиновая кислота, кодирующая 4-1BBL, содержит последовательность нуклеиновой кислоты, по меньшей мере на 90%, 95%, 97% 98% или 99% идентичную SEQ ID NO: 4, т.е. отличаются от нуклеиновой кислоты, указанной в SEQ ID NO: 4, менее чем на 20, 10, 5, 4, 3, 2 или 1 нуклеиновую кислоту в последовательности. В более предпочтительных вариантах осуществления 4-1BBL содержит нуклеиновую кислоту, включающую SEQ ID NO: 4.
[0134] CD40L. Как проиллюстрировано в настоящем описании, включение CD40L в качестве части комбинации и связанный с этим способ дополнительно усиливают снижение объема опухоли, повышают выживаемость без прогрессирования и повышают уровень выживаемости, реализуемые посредством настоящего изобретения. Таким образом, в различных вариантах осуществления комбинация дополнительно включает введение CD40L онкологическому пациенту. В предпочтительных вариантах осуществления CD40L кодируется в качестве части рекомбинантного MVA, как описано в настоящем изобретении.
[0135] Хотя CD40 конститутивно экспрессируется во многих типах клеток, включая В-клетки, макрофаги и дендритные клетки, его лиганд CD40L экспрессируется преимущественно на активированных хелперных Т-клетках. Когнатное взаимодействие между дендритными клетками и хелперными Т-клетками в ранние моменты времени после инфицирования или иммунизации «дает лицензию» дендритным клеткам примировать ответы ЦТЛ. Лицензирование дендритных клеток приводит к повышению экспрессии костимулирующих молекул, повышению выживаемости и лучшей способности к перекрестной презентации. Этот процесс опосредован в основном за счет взаимодействия CD40/CD40L. При этом описаны различные конфигурации CD40L, от мембраносвязанной до растворимой (мономерной или тримерной), которые индуцируют разнообразные стимулы, индуцирующие или подавляющие активацию, пролиферацию и дифференцировку АПК.
[0136] В одном или более предпочтительных вариантах осуществления CD40L кодируется MVA по настоящему изобретению. В одном или более других предпочтительных вариантах осуществления CD40L представляет собой CD40L человека. В еще более предпочтительных вариантах осуществления CD40L содержит нуклеиновую кислоту, кодирующую аминокислоту, имеющую последовательность, идентичную SEQ ID NO: 1 по меньшей мере на 90%, 95%, 97%, 98% или 99%, т.е. из аминокислотной последовательности, указанной в SEQ ID NO: 1, менее чем на 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 аминокислоту. В еще более предпочтительных вариантах осуществления CD40L содержит нуклеиновую кислоту, кодирующую аминокислотную содержащую SEQ ID NO: 1. В других вариантах осуществления нуклеиновая кислота, кодирующая CD40L, содержит последовательность нуклеиновой кислоты, по меньшей мере на 90%, 95%, 97% 98% или 99% идентичную SEQ ID NO: 2, т.е. отличаются от нуклеиновой кислоты, указанной в SEQ ID NO: 2, менее чем на 20, 10, 5, 4, 3, 2 или 1 нуклеиновую кислоту в последовательности. В более предпочтительных вариантах осуществления CD40L содержит нуклеиновую кислоту, включающую SEQ ID NO: 2.
[0137] Антагонисты молекул иммунных контрольных точек. Как описано в настоящем изобретении по меньшей мере в одном аспекте, настоящее изобретение охватывает применение антагонистов иммунных контрольных точек. Такие антагонисты иммунных контрольных точек действуют для препятствования и/или блокирования функции молекулы иммунных контрольных точек. Некоторые предпочтительные антагонисты иммунных контрольных точек включают цитотоксический антиген Т-лимфоцитов 4 (CTLA-4), белок запрограммированной смерти клетки 1 (PD-1), лиганд запрограммированной смерти 1 (PD-L1), ген активации лимфоцитов 3 (LAG-3) и Т-клеточный иммуноглобулин и муциновый домен 3 (TIM-3).
[0138] Кроме того, иллюстративные антагонисты иммунных контрольных точек могут включать без ограничения CTLA-4, PD-1, PD-L1, PD-L2, LAG-3, TIM-3, Т-клеточный иммунорецептор с доменами Ig и ITIM (TIGIT) и V-домен Ig супрессор активации T-клеток (VISTA).
[0139] Такие антагонисты молекул иммунных контрольных точек могут включать антитела, которые специфически связываются с молекулами иммунных контрольных точек и ингибируют и/или блокируют биологическую активность и функцию молекулы иммунных контрольных точек.
[0140] Другие антагонисты молекул иммунных контрольных точек могут включать антисмысловые нуклеиновые кислоты РНК, которые препятствуют экспрессии молекул иммунных контрольных точек; и небольшие интерферирующие РНК, которые мешают экспрессии молекул молекул иммунных контрольных точек.
[0141] Антагонисты могут дополнительно быть в форме небольших молекул, которые ингибируют или блокируют функцию иммунной контрольной точки. Некоторые неограничивающие их примеры включают NP12 (Aurigene), (D) PPA-1 от Tsinghua Univ, PD-1 с высоким сродством (Stanford); BMS-202 и BMS-8 (Bristol Myers Squibb (BMS), и CA170/ CA327 (Curis/Aurigene); и низкомолекулярные ингибиторы CTLA-4, PD-1, PD-L1, LAG-3 и TIM-3.
[0142] Антагонисты могут дополнительно быть в форме Anticalins®, которые ингибируют или блокируют функцию молекулы иммунных контрольных точек. См., например, Rothe et al. ((2018) BioDrugs 32(3): 233-243).
[0143] Предполагается, что антагонисты могут быть дополнительно в форме Affimers®. Аффимеры представляют собой слитые белки Fc, которые ингибируют или блокируют функцию молекулы иммунных контрольных точек. Другими гибридными белками, которые могут служить антагонистами иммунных контрольных точек, являются гибридные белки иммунных контрольных точек (например, белок AMP-224 против PD-1) и белки против PD-L1, такие как описанные в US2017/0189476.
[0144] Функциональность кандидатных антагонистов молекул иммунных контрольных точек может быть проверена посредством различных способов, известных в данной области и/или раскрытыми в настоящем приложении, такими как способность препятствовать функционированию молекул иммунных контрольных точек в мышиной модели in vitro.
[0145] Агонист ICOS. Настоящее изобретение дополнительно охватывает агонисты ICOS. Агонист ICOS активирует ICOS. ICOS представляет собой положительную костимулирующую молекулу, экспрессирующуюся на активированных Т-клетках, и связывание с ее лигандом способствует их пролиферации (Dong (2001) Nature 409: 97-101).
[0146] В одном варианте осуществления агонист представляет собой ICOS-L, природный лиганд ICOS. Агонист может представлять собой мутированную форму ICOS-L, сохраняющую свойства связывания и активации. Мутированные формы ICOS-L можно проверить на активность в стимулировании ICOS in vitro.
[0147] Антитела к антагонисту или агонисту иммунных контрольных точек. В предпочтительных вариантах осуществления каждый из антагониста и/или агониста молекул иммунных контрольных точек содержит антитело. Как описано в настоящем изобретении, в различных вариантах осуществления антитела могут быть синтетическими, моноклональными или поликлональными и могут быть получены посредством способов, хорошо известных в данной области. Такие антитела специфически связываются с молекулой иммунных контрольных точек посредством антигенсвязывающих сайтов антитела (в отличие от неспецифического связывания). Пептиды иммунных контрольных точек, фрагменты, варианты, слитые белки и т.д. можно использовать в качестве иммуногенов для получения антител, иммунореактивных с ними. Более конкретно, полипептиды, фрагменты, варианты, слитые белки и т.д. содержат антигенные детерминанты или эпитопы, которые вызывают образование антител.
[0148] В более предпочтительных вариантах осуществления антитела по настоящему изобретению представляют собой антитела, которые одобрены, или в процессе одобрения правительством государства, для лечения онкологического пациента-человека. Некоторые неограничивающие примеры данных антител, уже одобренных или находящихся в процессе одобрения, включают следующее: CTLA-4 (ипилимумаб® и тремелимумаб); PD-1 (пембролизумаб, ламбролизумаб, амплиммун-224 (AMP-224)), амплиммун-514 (AMP-514), ниволумаб, MK-3475 (Merck), BI 754091 (Boehringer Ingelheim)) и PD-L1 (атезолизумаб, авелулмаб, дурвалумаб, MPDL3280A (Roche), MED14736 (AZN), MSB0010718C (Merck)); LAG-3 (IMP321, BMS-986016, BI754111 (Boehringer Ingelheim), LAG525 (Novartis), MK-4289 (Merck), TSR-033 (Tesaro).
[0149] В одном иллюстративном аспекте молекулы иммунных контрольных точек CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 и ICOS, и пептиды на основе аминокислотной последовательности CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 и ICOS можно использовать для получения антител, которые специфически связываются с CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 или ICOS. Термин «антитела» включает поликлональные антитела, моноклональные антитела, их фрагменты, такие как F(ab')2 и Fab-фрагменты, одноцепочечные вариабельные фрагменты (scFvs), фрагменты однодоменных антител (VHH или нанотела), фрагменты двухвалентных антител (диатела), а также любые рекомбинантно и синтетически полученные партнеры связывания.
[0150] Антитела, специфичные к опухолеассоциированному антигену (ТАА). В различных вариантах осуществления настоящего изобретения рекомбинантный MVA и описанные в настоящем изобретении способы комбинируют или вводят в комбинации с антителом, специфичным к TAA. В более конкретных вариантах осуществления рекомбинантный MVA и способы, описанные в настоящем изобретении, комбинируют или вводят в комбинации с антителом, специфичным к антигену, который экспрессируется на клеточной мембране опухолевой клетки. В данной области техники известно, что при многих типах рака на мембране опухолевой клетки экспрессируются или сверхэкспрессируются один или более антигенов. См., например, Durig et al. (2002) Leukemia 16: 30-5; Mocellin et al. (2013) Biochim. Biophys. Acta 1836: 187-96; Arteaga (2011) Nat. Rev. Clin. Oncol., doi:10.1038/nrclinonc.2011.177; Finn (2017) Cancer Immunol. Res. 5: 347-54; Ginaldi et al. (1998) J. Clin. Pathol. 51: 364-9. Методы анализа для определения того, экспрессируется или сверхэкспрессируется антиген на опухолевых клетках, хорошо известны в данной области техники (Id.), как и способы получения антител к конкретному антигену.
[0151] В более конкретных вариантах осуществления фармацевтическая комбинация и связанные с ней способы включают антитело, причем антитело является a) специфичным к антигену, который экспрессируется на клеточной мембране опухолевой клетки, и b) содержит Fc-домен. По меньшей мере в одном аспекте характеристики антитела (например, a) и b)) обеспечивают возможность связывания и взаимодействия антитела с эффекторной клеткой, такой как NK-клетка, макрофаг, базофил, нейтрофил, эозинофил, моноциты, тучные клетки и/или дендритные клетки, и обеспечивают возможность связывания антитела с опухолевым антигеном, который экспрессируется на опухолевой клетке. В предпочтительном варианте осуществления антитело содержит Fc-домен. В дополнительном предпочтительном варианте осуществления антитело способно связываться и взаимодействовать с NK-клеткой.
[0152] Некоторые типовые антитела к антигенам, экспрессируемым на опухолевых клетках, предусмотренные настоящим изобретением, включают без ограничения антитело к CD20 (например, ритуксимаб; офатумумаб; тозитумомаб), антитело к CD52 (например, алемтузумаб Кампат®), антитело к EGFR (например, цетуксимаб Эрбитукс®¸ панитумумаб), антитело к CD2 (например, сиплизумаб), антитело к CD37 (например, BI836826), антитело к CD123 (например, JNJ-56022473), антитело к CD30 (например, XmAb2513), антитело к CD38 (например, даратумумаб Дарзалекс®), антитело к PDL1 (например, авелумаб, атезолизумаб, дурвалумаб), антитело к GD2 (например, 3F8, ch14.18, KW-2871, динутуксимаб), антитело к CEA, антитело к MUC1, антитело к FLT3, антитело к CD19, антитело к CD40, антитело к SLAMF7, антитело к CCR4, антитело к B7-H3, антитело к ICAM1, антитело к CSF1R, антитело к CA125 (например, ореговомаб), антитело к FRα (например, MOv18-IgG1, мирветуксимаб соравтансин (IMGN853), MORAb-202), антитело к мезотелин (например, MORAb-009), антитело к TRP2 и антитело к HER2 (например, трастузумаб, Herzuma, ABP 980 и/или пертузумаб).
[0153] В более предпочтительном варианте осуществления антитело, включенное как часть настоящего изобретения, включает антитело, которое при введении пациенту связывается с соответствующим антигеном на опухолевой клетке и индуцирует антителозависимую клеточноопосредованную цитотоксичность (АЗКЦ). В еще более предпочтительном варианте осуществления антитело включает антитело, которое одобрено или находится на стадии предварительного одобрения для лечения рака.
[0154] В еще более предпочтительных вариантах осуществления антитело представляет собой антитело к HER2, антитело к EGFR, и/или антитело к CD20.
[0155] В наиболее предпочтительном варианте осуществления антитело представляет собой антитело к HER2, выбранное из пертузумаба, трастузумаба, Герзумы, ABP 980 и адо-трастузумаба эмтанзина.
[0156] В наиболее предпочтительном варианте осуществления антитело к EGFR и антитело к CD20 представляет собой цетуксимаб и ритуксимаб, соответственно.
[0157] Как описано в настоящем изобретении, в различных вариантах осуществления антитела могут быть синтетическими, моноклональными или поликлональными и могут быть получены посредством способов, хорошо известных в данной области. Такие антитела специфически связываются с TAA посредством антигенсвязывающих сайтов антитела (в отличие от неспецифического связывания). Пептиды, фрагменты, варианты, слитые белки и т.д. TAA можно использовать в качестве иммуногенов для получения антител, иммунореактивных с ними. Более конкретно, полипептиды, фрагменты, варианты, слитые белки и т.д. содержат антигенные детерминанты или эпитопы, которые вызывают образование антител.
[0158] Антитела. В различных вариантах осуществления настоящего изобретения рекомбинантные MVA и способы, описанные в настоящем изобретении, комбинируют и/или вводят в комбинации либо с 1) антителом антагониста или агониста ингибитора иммунных контрольных точек, либо 2) TAA-специфичным антителом.
[0159] Предполагается, что антитела могут быть синтетическими, моноклональными или поликлональными и могут быть получены посредством способов, хорошо известных в данной области. Такие антитела специфически связываются с молекулой иммунных контрольных точек или TAA посредством антигенсвязывающих сайтов антитела (в отличие от неспецифического связывания). Пептиды, фрагменты, варианты, слитые белки и т.д. иммунных контрольных точек и/или TAA можно использовать в качестве иммуногенов для получения антител, иммунореактивных с ними. Более конкретно, полипептиды, фрагменты, варианты, слитые белки и т.д. содержат антигенные детерминанты или эпитопы, которые вызывают образование антител.
[0160] Данные антигенные детерминанты или эпитопы могут быть линейными или конформационными (прерывистыми). Линейные эпитопы состоят из одного участка аминокислот полипептида, в то время как конформационные или прерывистые эпитопы состоят из участков аминокислот из разных участков полипептидной цепи, которые сближаются при сворачивании белка (Janeway, Jr. и Travers, Immuno Biology 3:9 (Garland Publishing Inc., 2nd ed. 1996)). Поскольку свернутые белки имеют сложные поверхности, количество доступных эпитопов весьма велико; однако вследствие конформации белка и стерических препятствий количество антител, которые фактически связываются с эпитопами, меньше количества доступных эпитопов (Janeway, Jr. и Travers, Immuno Biology 2:14 (Garland Publishing Inc., 2nd ed. 1996)). Эпитопы можно идентифицировать посредством любого из способов, известных в данной области.
[0161] Антитела, в том числе фрагменты scFV, которые специфически связываются с TAA или молекулами иммунных контрольных точек, таких как CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 или ICOS, и либо блокируют их функцию («антагонистические антитела») или усиливают/активируют его функцию («агонистические антитела») охватываются настоящим изобретением. Такие антитела можно получить посредством обычных способов.
[0162] В одном варианте осуществления настоящего изобретения охватываются моноклональные антитела к TAA или молекул иммунных контрольных точек или которые либо блокируют («антагонистические антитела»), либо усиливают/активируют («агонистические антитела») функцию молекул ингибиторов иммунных контрольных точек или TAA.
[0163] Антитела способны связываться со своими мишенями как с высокой авидностью, так и специфичностью. Это относительно большие молекулы (~ 150 кДа), которые могут стерически подавлять взаимодействия между двумя белками (например, PD-1 и его целевой лиганд), если сайт связывания антитела находится в непосредственной близости от сайта белок-белкового взаимодействия. Настоящее изобретение также включает антитела, которые связываются с эпитопами в непосредственной близости от сайта связывания лиганда молекулы иммунных контрольных точек.
[0164] В различных вариантах осуществления настоящее изобретение включает антитела, которые препятствуют межмолекулярным взаимодействиям (например, белок-белковые взаимодействия), а также антитела, которые нарушают внутримолекулярные взаимодействия (например, конформационные изменения внутри молекулы). Антитела могут быть проверены на способность блокировать или усиливать/активировать биологическую активность молекулы иммунных контрольных точек. Как поликлональные, так и моноклональные антитела можно получить посредством обычных способов.
[0165] В одном иллюстративном аспекте TAA или молекулы иммунных контрольных точек CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 и ICOS, и пептиды на основе аминокислотной последовательности TAA или CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 и ICOS можно использовать для получения антител, которые специфически связываются с TAA или CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 или ICOS. Термин «антитела» включает поликлональные антитела, моноклональные антитела, их фрагменты, такие как F(ab')2 и Fab-фрагменты, одноцепочечные вариабельные фрагменты (scFvs), фрагменты однодоменных антител (VHH или нанотела), фрагменты двухвалентных антител (диатела), а также любые рекомбинантно и синтетически полученные партнеры связывания. В другом иллюстративном аспекте антитела определены как специфически связывающиеся, если они связываются с молекулой иммунных контрольных точек и, если они связываются с Kd больше или равным около 107 M-1. Сродство партнеров по связыванию или антител можно легко определить с использованием обычных методов, например, описанных Scatchard et al. ((1949) Ann. N.Y. Acad. Sci. 51: 660).
[0166] Поликлональные антитела можно легко получить из различных источников, например из лошадей, коров, коз, овец, собак, кур, кроликов, мышей или крыс, с использованием процедур, хорошо известных в данной области. Как правило, очищенные TAA или CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 и ICOS или пептид на основе аминокислотной последовательности CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 и ICOS, которые соответствующим образом конъюгированы, вводят животному-хозяину обычно посредством парентеральной инъекции. После бустерной иммунизации собирают небольшие образцы сыворотки и испытывают на реактивность по отношению к полипептидам CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 и ICOS. Примеры различных анализов, пригодных для такого определения, включают те, которые описаны в Antibodies: A Laboratory Manual, Harlow и Lane (eds.), Cold Spring Harbor Laboratory Press, 1988; а также процедуры, такие как противоточный иммуноэлектрофорез (CIEP), радиоиммуноанализ, радиоиммунопреципитация, твердофазный иммуноферментный анализ (ELISA), дот-блот-анализы и сэндвич-анализы. См. Патенты США №№ 4,376,110 и 4,486,530.
[0167] Моноклональные антитела можно легко получить с использованием хорошо известных процедур. См., например, процедуры, описанные в Патентах США №№ RE 32,011, 4,902,614, 4,543,439, и 4,411,993; Monoclonal Antibodies, Hybridomas: A New Dimension in Biological Analyses, Plenum Press, Kennett, McKeam, and Bechtol (eds.) (1980).
[0168] Например, животным-хозяевам, таким как мыши, можно вводить выделенную и очищенную молекулу иммунных контрольных точек внутрибрюшинно, по меньшей мере, один раз и предпочтительно, по меньшей мере, дважды с интервалами примерно в 3 недели. Затем сыворотки мышей анализируют посредством обычного способа дот-блоттинга или захвата антитела (ABC) для определения того, какое животное лучше всего подходит для слияния. Примерно через две-три недели мышам внутривенно вводят бустерную дозу молекулы молекул иммунных контрольных точек. Позднее мышей умерщвляют и клетки селезенки сливают с коммерчески доступными клетками миеломы, такими как Ag8.653 (ATCC), в соответствии с установленными протоколами. Вкратце, клетки миеломы несколько раз промывают в среде и сливают с клетками селезенки мыши в соотношении примерно три клетки селезенки на одну клетку миеломы. Сплавляющее средство может представлять собой любое подходящее средство, применяемое в данной области, например, полиэтиленгликоль (PEG). Слияние помещают в планшеты, содержащие среду, которая обеспечивает селективный рост слитых клеток. Затем слитым клеткам обеспечивают возможность роста в течение приблизительно восьми дней. Супернатанты от полученных гибридом собирают и добавляют в планшет, который сначала покрывают антителом козы против мышиного Ig. После промывок в каждую лунку добавляют метку, такую как меченый полипептид молекулы иммунных контрольных точек, с последующей инкубацией. Позже могут быть обнаружены положительные лунки. Положительные клоны можно выращивать в смешанной культуре, а супернатанты затем очищают на колонке с протеином А (Pharmacia).
[0169] Моноклональные антитела по настоящему изобретению могут быть получены с использованием альтернативных методик, таких как описанные в Alting-Mees et al. ((1990) Strategies in Mol. Biol. 3: 1-9, «Monoclonal антитело Expression Libraries: A Rapid Alternative to Hybridomas»), которая включена в настоящий документ посредством ссылки. Подобным образом, партнеры по связыванию могут быть сконструированы с использованием методик рекомбинантной ДНК для включения вариабельных областей гена, кодирующего специфическое связывающее антитело. Такие методики описаны в Larrick et al. ((1989) Biotechnology 7: 394).
[0170] Антигенсвязывающие фрагменты таких антител, которые можно получить посредством обычных методик, также охватываются настоящим изобретением. Примеры таких фрагментов включают без ограничения фрагменты Fab и F(ab’)2. Также представлены фрагменты антитела и производные, полученные посредством методик генной инженерии.
[0171] Моноклональные антитела по настоящему изобретению включают химерные антитела, например, гуманизированные версии мышиных моноклональных антител. Такие гуманизированные антитела могут быть получены посредством известных методик и обладают преимуществом пониженной иммуногенности при введении антител людям. В одном варианте осуществления гуманизированное моноклональное антитело включает вариабельную область мышиного антитела (или только его антигенсвязывающий сайт) и константную область, полученную из человеческого антитела. В качестве альтернативы, фрагмент гуманизированного антитела может содержать антигенсвязывающий сайт мышиного моноклонального антитела и фрагмент вариабельной области (без антигенсвязывающего сайта), полученный из человеческого антитела. Процедуры получения химерных и дополнительно сконструированных моноклональных антител включают процедуры, описанные в Riechmann et al. ((1988) Nature 332: 323), Liu et al. ((1987) Proc. Nat’l. Acad. Sci. 84: 3439), Larrick et al. ((1989) Bio/Technology 7: 934), and Winter and Harris ((1993) TIPS 14: 139). Процедуры трансгенной генерации антител можно найти в GB 2272440, Патентах США №№ 5,569,825 и 5,545,806, оба из которых включены в настоящий документ посредством ссылки.
[0172] Можно использовать антитела, полученные посредством способов генной инженерии, такие как химерные и гуманизированные моноклональные антитела, содержащие как человеческие, так и отличные от человеческих части, которые могут быть получены с использованием стандартных методик рекомбинантной ДНК. Такие химерные и гуманизированные моноклональные антитела могут быть получены посредством генной инженерии с использованием стандартных методик ДНК, известных в данной области, например, с использованием способов, описанных в Robinson et al. Публикации международной заявки на патент WO 87/02671; Akira et al. Европейской заявке на патент 0184187; Taniguchi, M., Европейской заявке на патент 0171496; Morrison et al. Европейской заявке на патент 0173494; Neuberger et al. Публикации международной заявки на патент PCT WO 86/01533; Cabilly et al. Патенте США № 4,816,567; Cabilly et al. Европейской заявке на патент 0125023; Better et al., (1988) Science 240: 1041-1043; Liu et al. (1987) Proc. Nat’l. Acad. Sci. 84: 3439-3443; Liu et al. (1987) J. Immunol. 139: 3521-3526; Sun et al. (1987) Proc. Nat’l. Acad. Sci. 84: 214-218; Nishimura et al. (1987) Cancer Res. 47: 999-1005; Wood et al. (1985) Nature 314: 446-449; и Shaw et al. (1988) J. Natl. Cancer Inst. 80: 1553-1559); Morrison (1985) Science 229: 1202-1207; Oi et al. (1986) BioTechniques 4: 214; Winter Патент США № 5,225,539; Jones et al. (1986) Nature 321: 552 525; Verhoeyan et al. (1988) Science 239: 1534; и Beidler et al. (1988) J. Immunol. 141: 4053-4060.
[0173] В отношении синтетических и полусинтетических антител такие термины охватывают без ограничения фрагменты антител, антитела с переключенным изотипом, гуманизированные антитела (например, мышиные-человеческие, человеческие-мышиные), гибриды, антитела, имеющие множественную специфичность, и молекулы, подобные полностью синтетическим антителам.
[0174] Для терапевтического применения часто предпочтительны «человеческие» моноклональные антитела, имеющие человеческие константные и вариабельные области для сведения к минимуму иммунный ответ пациента против антитела. Такие антитела можно получить посредством иммунизации трансгенных животных, которые содержат гены иммуноглобулинов человека. См. Jakobovits et al. Ann NY Acad Sci 764:525-535 (1995).
[0175] Человеческие моноклональные антитела к TAA или молекула иммунных контрольных точек также могут быть получены посредством конструирования библиотеки комбинаторных иммуноглобулинов, такой как библиотека фагового дисплея Fab или библиотека фагового дисплея scFv, с использованием кДНК легкой цепи и тяжелой цепи иммуноглобулина, полученной из мРНК, полученных из лимфоцитов субъекта. См., например, McCafferty et al. Публикация заявки на патент PCT WO 92/01047; Marks et al. (1991) J. Mol. Biol. 222: 581-597; и Griffths et al. (1993) EMBO J. 12: 725-734. Кроме того, комбинаторная библиотека вариабельных областей антитела может быть создана посредством мутации известного человеческого антитела. Например, вариабельная область человеческого антитела, о которой известно, что она связывает молекулу иммунных контрольных точек, может быть мутирована, например, посредством применения случайно измененных мутагенизированных олигонуклеотидов для создания библиотеки мутированных вариабельных областей, которые затем могут быть проверены на связывание с молекулой иммунных контрольных точек. Способы индукции случайного мутагенеза в областях CDR тяжелой и/или легкой цепей иммуноглобина, способы скрещивания рандомизированных тяжелых и легких цепей для образования пар и способы скрининга можно найти, например, в Barbas et al. Публикации заявки на патент PCT WO 96/07754; Barbas et al. (1992) Proc. Nat'l Acad. Sci. USA 89: 4457-4461.
[0176] Библиотека иммуноглобулинов может быть экспрессирована с помощью популяции дисплейных пакетов, предпочтительно полученных из нитчатого фага, с образованием библиотеки дисплеев антител. Примеры способов и реагентов, особенно подходящих для применения в создании библиотеки отображения антител, можно найти, например, в Ladner et al. Патент США № 5,223,409; Kang et al. Публикация заявки на патент PCT WO 92/18619; Dower et al. Публикация заявки на патент PCT WO 91/17271; Winter et al. Публикация заявки на патент PCT WO 92/20791; Markland et al. Публикация заявки на патент PCT WO 92/15679; Breitling et al. Публикация заявки на патент PCT WO 93/01288; McCafferty et al. Публикация заявки на патент PCT WO 92/01047; Garrard et al. Публикация заявки на патент PCT WO 92/09690; Ladner et al. Публикация заявки на патент PCT WO 90/02809; Fuchs et al. (1991) Bio/Technology 9: 1370 1372; Hay et al. (1992) Hum Antibod Hybridomas 3: 81-85; Huse et al. (1989) Science 246: 1275-1281; Griffths et al. (1993) supra; Hawkins et al. (1992) J. Mol. Biol. 226: 889-896; Clackson et al. (1991) Nature 352: 624-628; Gram et al. (1992) Proc. Nat’l. Acad. Sci. 89: 3576-3580; Garrad et al. (1991) Bio/Technology 9: 1373-1377; Hoogenboom et al. (1991) Nucl. Acid Res. 19: 4133-4137; и Barbas et al. (1991) Proc. Nat’l. Acad. Sci. 88: 7978-7982. После отображения на поверхности дисплейного пакета (например, нитчатого фага) библиотеку антител подвергают скринингу для идентификации и выделения пакетов, которые экспрессируют антитело, которое связывает TAA или молекулу иммунных контрольных точек.
[0177] Рекомбинантный MVA. В более предпочтительных вариантах осуществления настоящего изобретения один или более описанных в настоящем изобретении белков или нуклеотидов включены в рекомбинантный MVA. Как описано и проиллюстрировано в настоящем описании, внутривенное введение рекомбинантных MVA по настоящему изобретению индуцирует в различных аспектах усиленный иммунный ответ у онкологических пациентов. Таким образом, в одном или более предпочтительных вариантах осуществления настоящее изобретение включает рекомбинантный MVA, содержащий первую нуклеиновую кислоту, кодирующую один или более TAA, описанных в настоящем изобретении, и вторую нуклеиновую кислоту, кодирующую CD40L.
[0178] Примерами штаммов вируса MVA, которые можно использовать при практической осуществления настоящего изобретения и которые были депонированы в соответствии с требованиями Будапештского договора, являются штаммы MVA 572, депонированный в Европейской коллекции клеточных культур животных (ECACC), Vaccine Research и Production Laboratory, Public Health Laboratory Service, Centre for Applied Microbiology and Research, Porton Down, Salisbury, Wiltshire SP4 0JG, United Kingdom, под номером депонирования ECACC 94012707 27 января 1994 г., и MVA 575, депонированный в ECACC 00120707 7 декабря 2000 г., MVA-BN, депонированный 30 августа 2000 г. в Европейской коллекции клеточных культур (ECACC) под номером V00083008, и их производные, а также дополнительные типовые штаммы.
[0179] «Производные» MVA-BN относятся к вирусам, демонстрирующим практически такие же характеристики репликации, что и описанный в настоящем изобретении MVA-BN, но демонстрирующие различия в одной или более частях своих геномов. MVA-BN, а также его производные, являются некомпетентными по репликации, что означает неспособность к репродуктивной репликации in vivo и in vitro. Более конкретно, in vitro, MVA-BN или его производные были описаны как способные к репродуктивной репликации в куриных эмбриональных фибробластах (CEF), но не способные к репродуктивной репликации в линии клеток человеческих кератиноцитов HaCat (Boukamp et al. (1988), J. Cell Biol. 106: 761-771), клеточная линия костной остеосаркомы человека 143B (ECACC № депонирования 91112502), клеточная линия почек эмбриона человека 293 (ECACC № депонирования 85120602) и клеточная линия аденокарциномы шейки матки человека HeLa (ATCC № депонирования CCL-2). Кроме того, MVA-BN или его производные имеют показатель амплификации вируса, по меньшей мере в два раза меньший, более предпочтительно в три раза меньший, чем MVA-575 в клетках Hela и линиях клеток HaCaT. Исследования и анализ этих свойств MVA-BN и его производных описан в WO 02/42480 (патентная заявка США № 2003/0206926) и WO 03/048184 (патентная заявка США № 2006/0159699).
[0180] Термин «не способный к репродуктивной репликации» или «отсутствие способности к репродуктивной репликации» в человеческих линиях клеток in vitro, как описано в предыдущих параграфах, описан, например, в WO 02/42480, в которой также описано, как получать MVA, имеющий необходимые свойства, как указано выше. Данный термин относится к вирусу, который имеет показатель амплификации вируса in vitro через 4 суток после инфицирования менее 1 по определению в анализе, описанном в WO 02/42480 или в патенте США № 6761893.
[0181] Термин «неспособность к репродуктивной репликации» относится к вирусу, который имеет показатель амплификации вируса в человеческих линиях клеток in vitro, как описано в предыдущих параграфах, через 4 суток после инфицирования менее 1. Анализы, описанные в WO 02/42480 или Патенте США № 6,761,893, применимы для определения соотношения амплификации вируса.
[0182] Амплификацию или репликацию вируса в человеческих линиях клеток in vitro, как описано в предыдущих параграфах, обычно выражают как соотношение вируса, полученного из инфицированной клетки (выход), к количеству, изначально использованному для инфицирования клетки на первом месте (ввод), и называют «показателем амплификации». Показатель амплификации «1» определяет статус амплификации, при котором количество вируса, полученного из инфицированных клеток, является таким же, как и количество, изначально использованное для инфицирования клеток, что означает, что инфицированные клетки восприимчивы к вирусной инфекции и репродукции. В противоположность этому, показатель менее 1, т.е. снижение выходного по сравнению с вводным уровнем, указывает на отсутствие репродуктивной репликации и, следовательно, ослабление вируса.
[0183] Под «адъювантацией» в настоящем изобретении подразумевается, что конкретный кодируемый белок или компонент рекомбинантного MVA увеличивает иммунный ответ, продуцируемый другим кодируемым(-ыми) белком(-ами) или компонентом(-ами) рекомбинантного MVA.
[0184] Экспрессионные кассеты/регуляторные последовательности. В различных аспектах одну или более описанных в настоящем изобретении нуклеиновых кислот реализуют в одной или более экспрессионных кассетах, в которых одна или более нуклеиновых кислот функционально связаны с последовательностями регуляции экспрессии. «Функционально связанный» означает, что описанные компоненты находятся во взаимосвязи, позволяющей им функционировать предполагаемым образом, например, промотор для транскрипции подлежащей экспрессии нуклеиновой кислоты. Последовательность регуляции экспрессии, функционально связанная с кодирующей последовательностью, соединена так, чтобы обеспечить экспрессию кодирующей последовательности в условиях, совместимых с последовательностью регуляции экспрессии. Последовательности регуляции экспрессии включают, но не ограничиваются этим, соответствующие промоторы, энхансеры, терминаторы транскрипции, стартовый кодон в начале кодирующей белок открытой рамки считывания, сигналы сплайсинга для интронов и находящиеся в рамке считывания стоп-кодоны. Подходящие промоторы включают, но не ограничиваются этим, ранний промотор SV40, промотор RSV, ретровирусный ДКП, аденовирусный главный поздний промотор, немедленно-ранний промотор I CMV человека и различные поксвирусные промоторы, включая, но не ограничиваясь, следующие промоторы вируса осповакцины или полученные из MVA и полученные из FPV: промотор 30K, промотор I3, промотор PrS, промотор PrS5E, промотор Pr7.5K, промотор PrHyb, длинный промотор Pr13.5, промотор 40K, промотор MVA-40K, промотор FPV 40K, промотор 30k, промотор PrSynIIm, промотор PrLE1 и промотор PR1238. Дополнительные промоторы описаны в WO 2010/060632, WO 2010/102822, WO 2013/189611, WO 2014/063832 и WO 2017/021776, которые в полном объеме включены в данный документ посредством ссылки.
[0185] Дополнительные последовательности регуляции экспрессии включают, но не ограничиваются этим, лидерные последовательности, кодоны терминации, сигналы полиаденилирования и любые другие последовательности, необходимые для правильной транскрипции и последующей трансляции последовательности нуклеиновой кислоты, кодирующей необходимый рекомбинантный белок (например, HER2, Brachyury и/или CD40L) в необходимой хозяйской системе. Поксвирусный вектор также может содержать дополнительные элементы, необходимые для переноса и последующей репликации экспрессионного вектора, содержащего последовательность нуклеиновой кислоты, в необходимой хозяйской системе. Специалисту в данной области техники дополнительно понятно, что такие векторы нетрудно сконструировать, используя традиционные способы (Ausubel et al., (1987) в “Current Protocols in Molecular Biology,” John Wiley and Sons, New York, N.Y.), или же они являются коммерчески доступными.
[0186] Способы и схемы дозирования для введения комбинации. В одном или более аспектах комбинации по настоящему изобретению можно вводит как часть гомологичной и/или гетерологичной схемы прайм-буст. Как частично проиллюстрировано данными, показанными на фиг. 7, схема гомологичной прайм-буст иммунизации увеличивает специфичные CD8- и CD4-Т-клеточные ответы субъекта. Таким образом, в одном или более вариантах осуществления предложены комбинация и/или способ для уменьшения размера опухоли и/или повышения выживаемости онкологического пациента, включающие введение онкологическому пациенту комбинации по настоящему изобретению, причем комбинацию вводят как часть гомологичной или гетерологичной схемы прайм-буст.
Создание рекомбинантных вирусов MVA, содержащих трансгены
[0187] Рекомбинантные вирусы MVA по изобретению можно получать обычными способами, известными в данной области техники. Способы получения рекомбинантных поксвирусов или вставки экзогенных кодирующих последовательностей в поксвирусный геном хорошо известны специалисту в данной области техники. Например, способы стандартных методик молекулярной биологии, такие как клонирование ДНК, выделение ДНК и РНК, вестерн-блот-анализ, способы амплификации ОТ-ПЦР и ПЦР, описаны в Molecular Cloning, A Laboratory Manual (2nd ed., Sambrook et al., Cold Spring Harbor Laboratory Press (1989)), и методики работы с вирусами и манипуляции с ними описаны в Virology Methods Manual (Mahy et al. (eds.), Academic Press (1996)). Подобным образом, методики и ноу-хау для обработки, манипуляции и генной инженерии MVA описаны в Molecular Virology: A Practical Approach (Davison & Elliott (eds.), The Practical Approach Series, IRL Press at Oxford University Press, Oxford, UK (1993) (см., например, “Chapter 9: Expression of genes by Vaccinia virus vectors”)) и Current Protocols in Molecular Biology (John Wiley & Son, Inc. (1998) (см., например, Chapter 16, Section IV: “Expression of proteins in mammalian cells using vaccinia viral vector”)).
[0188] Для создания различных рекомбинантных вирусов MVA, описанных в настоящем изобретении, можно использовать разные способы. Последовательность ДНК, подлежащую вставке в вирус, можно поместить в плазмидную конструкцию на основе E. coli, в которую была вставлена ДНК, гомологичная участку ДНК поксвируса. В ином случае последовательность ДНК, подлежащую вставке, можно лигировать к промотору. Связку промотор-ген можно размещать в плазмидной конструкции так, чтобы связка промотор-ген фланкировалась с обоих концов ДНК, гомологичной последовательности ДНК, фланкирующей область поксвирусной ДНК, содержащей несущественный локус. Полученную в результате плазмидную конструкцию можно амплифицировать путем размножения в бактериях E. coli и выделять. Выделенную плазмиду, содержащую генную последовательность ДНК, подлежащую вставке, можно переносить в клеточную культуру, например, куриных эмбриональных фибробластов (CEF), и в то же время инфицировать культуру вирусом MVA. Рекомбинация между гомологичной вирусной ДНК MVA в плазмиде и вирусном геноме, соответственно, может привести к созданию поксвируса, модифицированного присутствием чужеродных последовательностей ДНК.
[0189] В соответствии с предпочтительным вариантом осуществления клетки из подходящей клеточной культуры, например, клетки CEF, можно инфицировать вирусом MVA. После этого инфицированные клетки можно трансфицировать первым плазмидным вектором, содержащим чужеродный или гетерологичный ген или гены, такие как одна или более нуклеиновых кислот, предложенных в настоящем изобретении; предпочтительно под транскрипционным управлением поксвирусного элемента регуляции экспрессии. Как объяснялось выше, плазмидный вектор также содержит последовательности, способные управлять вставкой экзогенной последовательности в выбранный участок вирусного генома MVA. Необязательно, плазмидный вектор также содержит кассету, содержащую маркерный и/или селективный ген, функционально связанный с поксвирусным промотором. Подходящими маркерными или селективными генами являются, например, гены, кодирующие зеленый флуоресцентный белок, β-галактозидазу, неомицин-фосфорибозилтрансферазу или другие маркеры. Использование кассет селективных маркеров упрощает идентификацию и выделение созданного рекомбинантного поксвируса. При этом рекомбинантный поксвирус также можно идентифицировать с помощью ПЦР-технологии. После этого дополнительные клетки можно инфицировать рекомбинантным поксвирусом, полученным как описано выше, и трансфицировать вторым вектором, содержащим второй чужеродный или гетерологичный ген или гены. В случае, если этот ген необходимо внести в другой сайт вставки поксвирусного генома, второй вектор также отличается в гомологичных с поксвирусом последовательностях, управляющих интеграцией второго чужеродного гена или генов в геном поксвируса. После того, как произошла гомологичная рекомбинация, рекомбинантный вирус, содержащий два или более чужеродных или гетерологичных генов, можно выделять. Для внесения дополнительных чужеродных генов в рекомбинантный вирус этапы инфицирования и трансфекции можно повторять, используя рекомбинантный вирус, выделенный на предыдущих этапах, для инфицирования и используя дополнительный вектор, содержащий дополнительный чужеродный ген или гены для трансфекции.
[0190] В альтернативном варианте стадии инфицирования и трансфекции, описанные выше, являются взаимозаменяемыми, т.е. подходящую клетку можно сначала трансфицировать плазмидным вектором, содержащим чужеродный ген, а затем инфицировать поксвирусом. В качестве дополнительного альтернативного варианта также возможно вносить каждый чужеродный ген в разные вирусы, совместно инфицировать клетку всеми полученными рекомбинантными вирусами и проводить скрининг в отношении рекомбинанта, содержащего все чужеродные гены. Третьим альтернативным вариантом является лигирование генома ДНК и чужеродных последовательностей in vitro и восстановление рекомбинированного генома ДНК вируса осповакцины с помощью хелперного вируса. Четвертым альтернативным вариантом является гомологичная рекомбинация в E.coli или другом виде бактерий между геномом вируса MVA, клонированным в виде бактериальной искусственной хромосомы (БИХ) и линейной чужеродной последовательности, фланкируемой последовательностями ДНК, гомологичными последовательностям, фланкирующим необходимый сайт интеграции в геном вируса MVA.
[0191] Одну или более нуклеиновых кислот по настоящему изобретению можно вставлять в подходящий участок вируса MVA или вирусного вектора MVA. Подходящими участками вируса MVA являются несущественные участки генома MVA. Несущественными участками геном MVA могут быть межгенные области или известные делеционные сайты 1-6 генома MVA. В альтернативном, или дополнительном варианте несущественными участками рекомбинантного MVA может быть кодирующая область генома MVA, которая не является важной для вирусного роста. При этом сайты вставки не ограничены этими предпочтительными сайтами вставки в геноме MVA, так как в объем настоящего изобретения входит то, что нуклеиновые кислоты по настоящему изобретению (например, HER2, Brachyury, HERV-K-env, HERV-K-gag, PRAME, FOLR1 и CD40L и/или 4-1BBL) и прилагаемые к ним промоторы, описанные в настоящем изобретении, можно вставлять в любое место вирусного генома при условии возможности получения рекомбинантов, которые можно амплифицировать и размножать по меньшей мере в одной клеточной культуральной системе, такой как куриные эмбриональные фибробласты (клетки CEF).
[0192] Предпочтительно нуклеиновые кислоты по настоящему изобретению можно вставлять в одну или более межгенных областей (МГО) вируса MVA. Термин «межгенная область» относиться преимущественно к участкам вирусного генома, расположенным между двумя соседними открытыми рамками считывания (ОРС) генома вируса MVA, предпочтительно между двумя существенными ОРС генома вируса MVA. В случае MVA в определенных вариантах осуществления ОРС выбрана из ОРС 07/08, ОРС 44/45, ОРС 64/65, ОРС 88/89, ОРС 136/137 и ОРС 148/149.
[0193] В случае вируса MVA нуклеотидные последовательности можно, в дополнительном или альтернативном варианте, вставлять в один или более известных делеционных сайтов, т.е. делеционные сайты I, II, III, IV, V или VI генома MVA. Термин «известный делеционный сайт» относится к тем участками генома MVA, которые были удалены посредством непрерывного пассирования на клетках CEF, характеризуемых на пассаже из 516, по отношению к геному родительского вируса, из которого получен MVA, в частности, родительского вируса осповакцины Анкара, культивируемого на хориоаллантоисе (CVA), например, как описано в Meisinger-Henschel et al. ((2007) J. Gen. Virol. 88: 3249-3259).
Вакцины
[0194] В определенных вариантах осуществления рекомбинантный MVA по настоящему изобретению можно получить в виде части вакцины. Для приготовления вакцин вирус MVA можно конвертировать в физиологически приемлемую форму.
[0195] Типовой способ приготовления приведен ниже. Очищенный вирус хранят при -80°C с титром 5×108 TCID50/мл в готовой смеси 10 мМ Трис, 140 мМ NaCl, pH 7,4. Для приготовления порций вакцины, например, 1×108-1×109 частиц вируса можно лиофилизировать в фосфатно-солевом буфере (ФСБ) в присутствии 2% пептона и 1% человеческого альбумина в ампуле, предпочтительно стеклянной ампуле. В альтернативном варианте порции вакцины можно готовить поэтапной лиофилизацией вируса в лекарственной форме. В определенных вариантах осуществления лекарственная форма содержит дополнительные добавки, такие как маннит, декстран, сахар, глицин, лактоза, поливинилпирролидон, или другие добавки, такие как, включая, но не ограничиваясь этим, антиоксиданты или инертный газ, стабилизаторы или рекомбинантные белки (например, человеческий сывороточный альбумин), подходящие для in vivo введения. Затем ампулу запечатывают, и ее можно хранить при подходящей температуре, например, от 4°C до комнатной температуры, в течение нескольких месяцев. При этом, пока не существует потребности, ампулу хранят предпочтительно при температурах ниже -20°C, наиболее предпочтительно при около -80°C.
[0196] В различных вариантах осуществления, включающих вакцинацию или терапию, лиофилизат растворяют в 0,1-0,5 мл водного раствора, преимущественно физиологического раствора или Трис-буфера, например, 10 мМ Трис, 140 мМ NaCl, pH 7,7. Предполагается, что рекомбинантный MVA, вакцина или фармацевтическая композиция по настоящему изобретению могут быть получены в растворе в диапазоне концентраций 104-1010 TCID50/мл, 105-5×109 TCID50/мл, 106-5×109 TCID50/мл или 107-5×109 TCID50/мл. Предпочтительная доза для людей составляет 106-1010 TCID50, включая дозу 106 TCID50, 107 TCID50, 108 TCID50, 5×108 TCID50, 109 TCID50, 5×109 TCID50 или 1010 TCID50. Оптимизация дозы и количества введений входит в компетенцию и умения специалиста в данной области техники.
[0197] В одном или более предпочтительных вариантах осуществления, приведенных в настоящем изобретении, рекомбинантный MVA внутривенно вводят онкологическому пациенту. В других вариантах осуществления рекомбинантный MVA вводят онкологическому пациенту посредством внутриопухолевой инъекции. В других вариантах осуществления рекомбинантный MVA вводят онкологическому пациенту как внутривенно, так и внутриопухолево одновременно или в различные моменты времени.
[0198] В дополнительных вариантах осуществления антагонист или агонист ингибитора иммунных контрольных точек, или предпочтительно антитело можно вводить либо системно, или местно, т.е. посредством внутрибрюшинного, парентерального, подкожного, внутривенного, внутримышечного, интраназального, внутрикожного или любого другого пути введения, известного квалифицированному практикующему врачу.
[0199] Наборы, композиции и способы применения. В различных вариантах осуществления это изобретение включает наборы, фармацевтические комбинации, фармацевтические композиции и/или иммуногенные комбинации, содержащие a) рекомбинантный MVA, который содержит нуклеиновые кислоты, описанные в настоящем изобретении, и/или b) одно или более антител, описанных в настоящем изобретении.
[0200] Подразумевается, что набор и/или композиция могут содержать один или более контейнеров или флаконов рекомбинантного поксвируса по настоящему изобретению, один или более контейнеров или флаконов антитела по настоящему изобретению вместе с инструкциями по введению рекомбинантного MVA и антитела. Подразумевается, что в более конкретном варианте осуществления набор может содержать инструкции по введению рекомбинантного MVA и антитела в виде первого примирующего введения, а затем одного или более бустерных введений рекомбинантного MVA и антитела.
[0201] Предложенные в настоящем изобретении наборы и/или композиции могут в общем случае содержать один или более фармацевтически приемлемых и/или одобренных носителей, добавок, антибиотиков, консервантов, разбавителей и/или стабилизаторов. Такими вспомогательными веществами могут быть вода, физиологический раствор, глицерин, этанол, смачивающие или эмульгирующие агенты, pH-буферные вещества и т.п. Подходящие носители, как правило, представляют собой большие, медленно метаболизируемые молекулы, такие как белки, полисахариды, полимолочные кислоты, полигликолевые кислоты, полимерные аминокислоты, аминокислотные сополимеры, липидные агрегаты и т.п.
ОПРЕДЕЛЕННЫЕ ИЛЛЮСТРАТИВНЫЕ ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ
[0202] Вариант осуществления 1 представляет собой способ уменьшения размера опухоли и/или повышения выживаемости у субъекта с раковой опухолью, включающий внутриопухолевое введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA), и вторую нуклеиновую кислоту, кодирующую 4-1BBL, причем внутриопухолевое введение рекомбинантного MVA усиливает воспалительный ответ в раковой опухоли, усиливает уменьшение опухоли и/или повышает общую выживаемость субъекта по сравнению с отличной от внутриопухолевой инъекцией рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую TAA и антиген 4-1BBL.
[0203] Вариант осуществления 2 представляет собой способ уменьшения размера опухоли и/или повышение выживаемости у субъекта с раковой опухолью, включающий внутривенное введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA) и вторую нуклеиновую кислоту, кодирующую 4-1BBL, причем внутривенное введение рекомбинантного MVA усиливает ответ естественных клеток-киллеров (NK) и усиливает ответы CD8 T-клеток, специфичных к TAA по сравнению с отличной от внутривенной инъекцией рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую TAA и антиген 4-1BBL.
[0204] Вариант осуществления 3 представляет собой способ уменьшения размера опухоли и/или повышения выживаемости субъекта с раковой опухолью, включающий введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего нуклеиновую кислоту, кодирующей опухолеассоциированный антиген (TAA), и вторую нуклеиновую кислоту, кодирующую 4-1BBL, причем введение рекомбинантный MVA повышает уменьшение опухоли и/или повышает общую выживаемость субъекта по сравнению с введением рекомбинантного MVA и антигена 4-1BBL отдельно.
[0205] Вариант осуществления 4 представляет собой способ индукции усиленного воспалительного ответа в раковой опухоли субъекта, включающий внутриопухолевое введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую первый гетерологичный опухолеассоциированный антиген (TAA), и вторую нуклеиновую кислоту, кодирующую антиген 4-1BBL, причем внутриопухолевое введение рекомбинантного MVA генерирует усиленный воспалительный ответ в опухоли по сравнению с воспалительным ответом, сгенерированным посредством отличной от внутриопухолевой инъекции рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую гетерологичный опухолеассоциированный антиген и антиген 4-1BBL. Такой усиленный воспалительный ответ обсуждается в другом месте в настоящем изобретении и может включать, например, индукцию NK-клеток и Т-клеток.
[0206] Вариант осуществления 5 представляет собой способ уменьшения размера опухоли и/или повышения выживаемости субъекта с раковой опухолью, включающий введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую эндогенный ретровирусный антиген (ERV), и вторую нуклеиновую кислоту, кодирующую 4-1BBL, причем введение рекомбинантного MVA усиливает уменьшение опухоли и/или повышает общую выживаемость субъекта по сравнению с введением рекомбинантного MVA и антигена 4-1BBL отдельно.
[0207] Вариант осуществления 6 представляет собой способ в соответствии с любым из вариантов осуществления 1-5, в котором субъект является человеком.
[0208] Вариант осуществления 7 представляет собой способ в соответствии с любым из вариантов осуществления 1-4, в котором TAA представляет собой эндогенный ретровирусный белок (ERV).
[0209] Вариант осуществления 8 представляет собой способ согласно варианту осуществления 7, причем ERV представляет собой белок ERV, экспрессируемый в опухолевой клетке.
[0210] Вариант осуществления 9 представляет собой способ согласно любому из вариантов осуществления 7-8, в котором ERV происходит из семейства человеческих эндогенных ретровирусных белков K (HERV-K).
[0211] Вариант осуществления 10 представляет собой способ согласно варианту осуществления 9, в котором белок HERV-K выбран из оболочечного белка HERV-K, белка gag HERV-K и белка MEL HERV-K.
[0212] Вариант осуществления 11 представляет собой способ согласно варианту осуществления 9, в котором белок HERV-K выбран из оболочечного белка HERV-K, белка gag HERV-K и белка MEL HERV-K и его иммуногенного фрагмента.
[0213] Вариант осуществления 12 представляет собой способ согласно любому из вариантов осуществления 1-6, в котором TAA выбран из группы, включающей карциноэмбриональный антиген (CEA), ассоциированный с клеточной поверхностью муцин-1 (MUC-1), простатическую кислую фосфатазу (PAP), простатспецифический антиген (PSA), рецептор человеческого эпидермального фактора роста 2 типа (HER-2), сурвивин, связанный с тирозином белок 1 (TRP1), связанный с тирозином белок 1 (TRP2), Brachyury, FOLR1, PRAME, p15 и их комбинации.
[0214] Вариант осуществления 13 представляет собой способ согласно любому из вариантов осуществления 1-6 и 12, в котором TAA выбран из группы, включающей карциноэмбриональный антиген (CEA) и ассоциированный с клеточной поверхностью муцин-1 (MUC-1).
[0215] Вариант осуществления 14 представляет собой способ согласно любому из вариантов осуществления 1-6 и 12, в котором TAA выбран из группы, включающей PAP или PSA.
[0216] Вариант осуществления 15 представляет собой способ в соответствии с любым из вариантов осуществления 1-6, 12 и 14, в котором TAA представляет собой PSA.
[0217] Вариант осуществления 16 представляет собой способ согласно любому из вариантов осуществления 1-6, в котором TAA выбран из группы, включающей следующее: 5-α-редуктаза, α-фетопротеин (AFP), AM-1, APC, April, антиген меланомы B (BAGE), β-катенин, Bcl12, bcr-abl, Brachyury, CA-125, каспаза-8 (CASP-8, также известная как FLICE), катепсины, CD19, CD20, CD21/рецептор комплемента 2 (CR2), CD22/BL-CAM, CD23/FcεRII, CD33, CD35/рецептор комплемента 1 (CR1), CD44/PGP-1, CD45/общий антиген лейкоцитов («LCA»), CD46/белок мембранного кофактора (MCP), CD52/CAMPATH-1, CD55/фактор ускорения распада (DAF), CD59/протектин, CDC27, CDK4, карциноэмбриональный антиген (CEA), c-myc, циклооксигеназа-2 (cox-2), ген, отсутствующий при колоректальном раке («DCC»), DcR3, E6/E7, CGFR, EMBP, Dna78, фарнезилтрансфераза, фактор роста фибробластов-8a (FGF8a), фактор роста фибробластов-8b (FGF8b), FLK-1/KDR, рецептор фолиевой кислоты, G250, семейство генов антигенов меланомы G (GAGE-семейство), гастрин 17, гастрин-высвобождающий гормон, ганглиозид 2 (GD2)/ганглиозид 3 (GD3)/ганглиозид-моносиаловая кислота-2 («GM2»), гонадотропин-высвобождающий гормон (GnRH), UDP-GlcNAc: R1Man (α1-6) R2 [GlcNAc to Man (α1 -6)] β1,6-N-ацетилглюкозаминилтрансфераза V (GnT V), GP1, gp100/Pme117, gp-100-in4, gp15, gp75/тирозин-родственный белок-1 (gp75/TRP-1), хорионический гонадотропин (ХГЧ), гепараназа, HER2, вирус опухоли молочной железы человека (HMTV), белок теплового шока 70 килодальтон («HSP70»), обратная транскриптаза теломеразы человека (hTERT), рецептор-1 инсулиноподобного фактора роста (IGFR-1), рецептор интерлейкина-13 (IL-13R), индуцибельная синтаза оксида азота (iNOS), Ki67, KIAA0205, K-ras, H- ras, N-ras, KSA, LKLR-FUT, ген 1, кодирующий антиген меланомы (MAGE-1), ген 2, кодирующий антиген меланомы (MAGE-2), ген 3, кодирующий антиген меланомы (MAGE-3), ген 4, кодирующий антиген меланомы (MAGE-4), маммаглобин, MAP17, мелан-A/антиген меланомы, распознаваемый Т-клетками-1 (MART-1), мезотелин, MIC A/B, MT-MMP, муцин, тестикоспецифичный антиген NY-ESO-1, остеонектин, p15, P170/MDR1, p53, p97/меланотрансферрин, PAI-1, фактор роста тромбоцитов (PDGF), μPA, PRAME, пробазин, прогенипоэтин, простатспецифический антиген (PSA), простатспецифический мембранный антиген (PSMA), RAGE-1, Rb, RCAS1, SART-1, семейство SSX, STAT3, STn, TAG-72, трансформирующие фактор роста-альфа (TGF-α), трансформирующий фактор роста-бета (TGF-β), тимозин-бета-15, фактор некроза опухоли-альфа (TNF-α), TP1, TRP-2, тирозиназа, фактор роста эндотелия сосудов (VEGF), ZAG, p16INK4 и глутатион-S-трансфераза (GST). Группа включает карциноэмбриональный антиген (CEA), ассоциированный с клеточной поверхностью муцин-1 (MUC-1), простатическую кислую фосфатазу (PAP), простатспецифический антиген (PSA), рецептор человеческого эпидермального фактора роста 2 типа (HER-2), сурвивин, связанный с тирозином белок 1 (TRP1), связанный с тирозином белок 1 (TRP2), Brachyury и их комбинации.
[0218] Вариант осуществления 17 представляет собой способ согласно любому из вариантов осуществления 1-16, в котором рекомбинантный MVA дополнительно содержит третью нуклеиновую кислоту, кодирующую антиген CD40L.
[0219] Вариант осуществления 18 представляет собой способ согласно любому из вариантов осуществления 1-17, дополнительно включающий введение субъекту по меньшей мере одного антагониста или агониста молекул иммунных контрольных точек.
[0220] Вариант осуществления 19 представляет собой способ согласно варианту осуществления 18, в котором антагонист или агонист молекул иммунных контрольных точек выбран из CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 и ICOS.
[0221] Вариант осуществления 20 представляет собой способ согласно любому из вариантов осуществления 18-19, в котором антагонист молекул иммунных контрольных точек представляет собой PD-1 и/или PD-L1.
[0222] Вариант осуществления 21 представляет собой способ согласно варианту осуществления 20, в котором антагонист молекул иммунных контрольных точек дополнительно содержит LAG-3.
[0223] Вариант осуществления 22 представляет собой способ согласно любому из вариантов осуществления 18-21, в котором антагонист молекул иммунных контрольных точек содержит антитело.
[0224] Вариант осуществления 23 представляет собой способ согласно любому из вариантов осуществления 1-17, дополнительно включающий введение субъекту антитела, специфичного ко второму TAA.
[0225] Вариант осуществления 24 представляет собой способ согласно варианту осуществления 23, причем антитело, специфичное ко второму TAA, специфично к антигену, который экспрессируется на клеточной мембране опухоли.
[0226] Вариант осуществления 25 представляет собой способ в соответствии с вариантом осуществления 23, причем антитело, специфичное ко второму TAA, является а) специфичным к антигену, который экспрессируется на клеточной мембране опухоли, и b) содержит домен Fc.
[0227] Вариант осуществления 26 представляет собой фармацевтическую композицию для применения в способе согласно любому из вариантов осуществления 1-25.
[0228] Вариант осуществления 27 представляет собой вакцину для применения в способе согласно любому из вариантов осуществления 1-25.
[0229] Вариант осуществления 28 представляет собой рекомбинантный модифицированный вирус осповакцины Анкара (MVA) для лечения субъекта с раком, при этом рекомбинантный MVA содержит (a) первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA) и (b) вторую нуклеиновую кислоту, кодирующую 4-1BBL.
[0230] Вариант осуществления 29 представляет собой рекомбинантный MVA согласно варианту осуществления 28, в котором TAA представляет собой эндогенный ретровирусный (ERV) белок.
[0231] Вариант осуществления 30 представляет собой рекомбинантный MVA согласно варианту осуществления 29, в котором белок ERV происходит из семейства эндогенных ретровирусных белков K (HERV-K).
[0232] Вариант осуществления 31 представляет собой рекомбинантный MVA согласно варианту осуществления 30, в котором ретровирусный белок K выбран из оболочечного белка HERV-K, белка gag HERV-K и белка HERV-K mel.
[0233] Вариант осуществления 32 представляет собой рекомбинантный MVA согласно любому из вариантов осуществления 28-31, дополнительно содержащий третью нуклеиновую кислоту, кодирующую CD40L.
[0234] Вариант осуществления 33 представляет собой фармацевтическую комбинацию, содержащую а) рекомбинантный MVA в соответствии с любым из вариантов осуществления 28-32 и b) по меньшей мере один из по меньшей мере одного антагониста или агониста молекул иммунных контрольных точек.
[0235] Вариант осуществления 34 представляет собой фармацевтическую комбинацию согласно варианту осуществления 33, в которой антагонист или агонист молекул иммунных контрольных точек выбран из CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 и ICOS.
[0236] Вариант осуществления 35 представляет собой фармацевтическую комбинацию согласно варианту осуществления 34, в которой антагонист молекул иммунных контрольных точек представляет собой PD-1 и/или PD-L1.
[0237] Вариант осуществления 36 представляет собой фармацевтическую комбинацию согласно варианту осуществления 35, в которой антагонист молекул иммунных контрольных точек дополнительно содержит LAG-3.
[0238] Вариант осуществления 37 представляет собой фармацевтическую комбинацию согласно любому из вариантов осуществления 33-36, в которой антагонист молекул иммунных контрольных точек содержит антитело.
[0239] Вариант осуществления 38 представляет собой фармацевтическую комбинацию, содержащую а) рекомбинантный MVA в соответствии с любым из вариантов осуществления 28-32 b) антитело, специфичное ко второму TAA.
[0240] Вариант осуществления 39 представляет собой фармацевтическую комбинацию согласно варианту осуществления 38, в которой антитело, специфичное ко второму TAA, специфично к антигену, который экспрессируется на клеточной мембране опухоли.
[0241] Вариант осуществления 40 представляет собой фармацевтическую комбинацию согласно варианту осуществления 39, в которой антитело, специфичное к второму TAA, является а) специфичным к антигену, который экспрессируется на клеточной мембране опухоли, и b) содержит домен Fc.
[0242] Вариант осуществления 41 представляет собой рекомбинантный MVA согласно любому из вариантов осуществления 28-32, вакцину согласно варианту осуществления 27, фармацевтическую композицию согласно варианту осуществления 26, фармацевтическую комбинацию в соответствии с любым из вариантов осуществления 33-40 для применения с целью уменьшения размера опухоли и/или повышения выживаемости у субъекта с раковой опухолью.
[0243] Вариант осуществления 42 представляет собой рекомбинантный MVA согласно любому из вариантов осуществления 28-32, вакцину согласно варианту осуществления 27, фармацевтическую композицию согласно варианту осуществления 26, фармацевтическую комбинацию согласно любому из вариантов осуществления 33-40 для применения в способе уменьшения размера опухоли и/или повышения выживаемости у субъекта с раковой опухолью, при этом способ включает внутриопухолевое введение субъекту рекомбинантного MVA в соответствии с вариантами осуществления 28-32, вакцины согласно варианту осуществления 27, фармацевтической композиции согласно варианту осуществления 26 или фармацевтической комбинации в соответствии с любым из вариантов осуществления 33-40, причем внутриопухолевое введение усиливает воспалительный ответ в раковой опухоли, усиливает уменьшение опухоли и/или повышает общую выживаемость субъекта по сравнению с отличной от внутриопухолевой инъекцией рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую TAA и антиген 4-1BBL.
[0244] Вариант осуществления 43 представляет собой рекомбинантный MVA согласно любому из вариантов осуществления 28-32, вакцину согласно варианту осуществления 27, фармацевтическую композицию согласно варианту осуществления 26, фармацевтическую комбинацию согласно любому из вариантов осуществления 33-40 для применения в способе уменьшения размера опухоли и/или повышения выживаемости у субъекта с раковой опухолью, при этом способ включает внутривенное введение субъекту рекомбинантного MVA в соответствии с вариантами осуществления 28-32, вакцины согласно варианту осуществления 27, фармацевтической композиции согласно варианту осуществления 26 или фармацевтической комбинации в соответствии с любым из вариантов осуществления 33-40, причем внутривенное введение усиливает уменьшение опухоли и/или повышает общую выживаемость субъекта по сравнению с отличного от внутривенного введения рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую TAA и антиген 4-1BBL.
[0245] Вариант осуществления 44 представляет собой рекомбинантный MVA согласно любому из вариантов осуществления 28-32, вакцину согласно варианту осуществления 27, фармацевтическую композицию согласно варианту осуществления 26, фармацевтическую комбинацию согласно любому из вариантов осуществления 33-40 для применения в способе индукции усиленный воспалительный ответ в раковая опухоль субъект с раком, при этом способ включает внутриопухолевое введение субъекту рекомбинантного MVA согласно вариантам осуществления 28-32, вакцины согласно варианту осуществления 27, фармацевтической композиции согласно варианту осуществления 26 или фармацевтической комбинации согласно любому из вариантов осуществления 33-40, причем внутриопухолевое введение усиливает воспалительный ответ в раковой опухоли субъекта по сравнению с отличной от внутриопухолевой инъекцией рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоты, кодирующие TAA и антиген 4-1BBL.
[0246] Вариант осуществления 45 представляет собой рекомбинантный MVA согласно любому из вариантов осуществления 28-32, вакцину согласно варианту осуществления 27, фармацевтическую композицию согласно варианту осуществления 26, фармацевтическую комбинацию согласно любому из вариантов осуществления 33-40 для применения в способе лечения рака у субъекта.
[0247] Вариант осуществления 46 представляет собой рекомбинантный MVA согласно любому из вариантов осуществления 28-32, вакцину согласно варианту осуществления 27, фармацевтическую композицию согласно варианту осуществления 26, фармацевтическую комбинацию согласно любому из вариантов осуществления 33-40, для применения в способе для лечения рака, при этом рак выбран из группы, включающей следующее: рак молочной железы, рак легкого, рак головы и шеи, рак щитовидной железы, меланома, рак желудка, рак мочевого пузыря, рак почки, рак печени, меланома, рак поджелудочной железы, рак предстательной железы, рак яичника, рак уротелия, рак шейки матки или колоректальный рак.
[0248] Вариант осуществления 47 представляет собой рекомбинантный MVA согласно варианту осуществления 44, в котором усиленный воспалительный ответ локализован в опухоли.
[0249] Вариант осуществления 48 представляет собой способ уменьшения размера опухоли и/или повышения выживаемости у субъекта с раковой опухолью, включающий внутриопухолевое введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA), и вторую нуклеиновую кислоту, кодирующую CD40L, причем внутриопухолевое введение рекомбинантного MVA усиливает воспалительный ответ в раковой опухоли, усиливает уменьшение опухоли и/или повышает общую выживаемость субъекта по сравнению с отличной от внутриопухолевой инъекцией рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую TAA и CD40L.
[0250] Вариант осуществления 49 представляет собой способ уменьшения размера опухоли и/или повышение выживаемости у субъекта с раковой опухолью, включающий внутривенное введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA) и вторую нуклеиновую кислоту, кодирующую CD40L, причем внутривенное введение рекомбинантного MVA усиливает ответ естественных клеток-киллеров (NK) и усиливает ответы CD8 T-клеток, специфичных к TAA по сравнению с отличной от внутривенной инъекцией рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую TAA и антиген CD40L.
[0251] Вариант осуществления 50 представляет собой способ уменьшения размера опухоли и/или повышения выживаемости субъекта с раковой опухолью, включающий введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего нуклеиновую кислоту, кодирующей опухолеассоциированный антиген (TAA), и вторую нуклеиновую кислоту, кодирующую CD40L, причем введение рекомбинантный MVA повышает уменьшение опухоли и/или повышает общую выживаемость субъекта по сравнению с введением рекомбинантного MVA и антигена CD40L отдельно.
[0252] Вариант осуществления 51 представляет собой рекомбинантный MVA согласно любому из вариантов осуществления 28-32, вакцину согласно варианту осуществления 27, фармацевтическую композицию согласно варианту осуществления 26, фармацевтическую комбинацию согласно любому из вариантов осуществления 33-40 для применения в способе уменьшения размера опухоли и/или повышения выживаемости у субъекта с раковой опухолью, при этом способ включает внутривенное и/или внутриопухолевое введение субъекту рекомбинантного MVA согласно вариантам осуществления 28-32, вакцины согласно варианту осуществления 27, фармацевтической композиции согласно варианту осуществления 26 или фармацевтической комбинации согласно любому из вариантов осуществления 33-40, причем указанное внутривенное и/или внутриопухолевое введение усиливает уменьшение опухоли и/или повышает общую выживаемость субъекта по сравнению с отличным от внутривенного или отличным от внутриопухолевого введением любого MVA, выбранного из группы, включающей следующее: 1) рекомбинантный вирус MVA, содержащий первую нуклеиновую кислоту, кодирующую TAA, и вторую нуклеиновую кислоту, кодирующую антиген 4-1BBL; 2) рекомбинантный вирус MVA, содержащий первую нуклеиновую кислоту, кодирующую TAA, и вторую нуклеиновую кислоту, кодирующую антиген CD40L; или 3) рекомбинантный вирус MVA, содержащий первую нуклеиновую кислоту, кодирующую TAA, вторую нуклеиновую кислоту, кодирующую антиген 4-1BBL, и третью нуклеиновую кислоту, кодирующую антиген CD40L.
[0253] Вариант осуществления 52 представляет собой рекомбинантный MVA согласно любому из вариантов осуществления 28-32, вакцину согласно варианту осуществления 27, фармацевтическую композицию согласно варианту осуществления 26, фармацевтическую комбинацию согласно любому из вариантов осуществления 33-40 для применения в способе уменьшения размера опухоли и/или повышения выживаемости у субъекта с раковой опухолью, при этом способ включает внутривенное и внутриопухолевое введение субъекту рекомбинантного MVA согласно вариантам осуществления 28-32, вакцины согласно варианту осуществления 27, фармацевтической композиции согласно варианту осуществления 26 или фармацевтической комбинации согласно любому из вариантов осуществления 33-40, причем указанное внутривенное и внутриопухолевое введение усиливает уменьшение опухоли и/или повышает общую выживаемость субъекта по сравнению с отличным от внутривенного или отличным от внутриопухолевого введения любого MVA, выбранного из группы, включающей следующее: 1) рекомбинантный вирус MVA, содержащий первую нуклеиновую кислоту, кодирующую TAA, и вторую нуклеиновую кислоту, кодирующая антиген 4-1BBL; 2) рекомбинантный вирус MVA, содержащий первую нуклеиновую кислоту, кодирующую TAA, и вторую нуклеиновую кислоту, кодирующую антиген CD40L; или 3) рекомбинантный вирус MVA, содержащий первую нуклеиновую кислоту, кодирующую TAA, вторую нуклеиновую кислоту, кодирующую антиген 4-1BBL, и третью нуклеиновую кислоту, кодирующую антиген CD40L. Указанное внутривенное и внутриопухолевое введение можно осуществлять одновременно или в разное время, что очевидно специалисту в данной области.
ПРИМЕРЫ
[0254] Следующие примеры иллюстрируют данное изобретение, но не должны восприниматься как ограничивающие каким-либо образом объем формулы изобретения.
Пример 1: Конструкция рекомбинантного MVA-TAA-4-1BBL и MVA-TAA-CD40L
[0255] Получение рекомбинантных вирусов MVA, которые воплощают элементы настоящего описания, осуществляли посредством вставки указанных трансгенов с их промоторами в вектор MVA-BN. Трансгены вставляли, используя рекомбинационные плазмиды, содержащие трансгены и селекционную кассету, а также последовательности, гомологичные целевым локусам в MVA-BN. Гомологичную рекомбинацию между вирусным геномом и рекомбинационной плазмидой обеспечивали путем трансфекции рекомбинационной плазмиды в инфицированные MVA-BN клетки CEF. Затем на втором этапе селекционную кассету удаляли с помощью плазмиды, экспрессирующей CRE-рекомбиназу, которая специфически нацелена на сайты loxP, фланкирующие селекционную кассету, вырезая, таким образом, промежуточную последовательность.
[0256] Для конструирования MVA-OVA и MVA-OVA-4-1BBL рекомбинационная плазмида включала трансгены OVA или OVA и 4-1BBL, каждому из которых предшествует промоторная последовательность, а также последовательности, которые идентичны целевому сайту вставки в MVA- BN для обеспечения гомологичной рекомбинации в вирусном геноме.
[0257] Для конструирования MVA-OVA-CD40L рекомбинационная плазмида включала трансгены OVA и CD40L, каждому из которых предшествовала промоторная последовательность, а также последовательности, которые идентичны целевому сайту инсерции в MVA-BN для обеспечения гомологичной рекомбинации в вирусном геноме.
[0258] Для конструирования MVA-gp70-4-1BBL рекомбинационная плазмида включает два трансгена gp70 и 4-1BBL, каждому из которых предшествует промоторная последовательность, а также последовательности, которые идентичны целевому сайту вставки в MVA-BN для обеспечения гомологичности рекомбинации в вирусном геноме. Аналогично, для конструирования MVA-gp70-CD40L необходима рекомбинационная плазмида включает два трансгена gp70 и CD40L, каждому из которых предшествует промоторная последовательность, и соответствующие изменения вносятся в рекомбинационные плазмиды при конструировании MVA-gp70-4-1-BBL- CD40L.
[0259] Для конструирования MVA-HERV-K, MVA-HERV-K-4-1BBL и MVA-HERV-K-4-1BBL-CD40L, рекомбинационная плазмида включала трансгены HERV-K, HERV-K и 4-1BBL и HERV-K, 4-1BBL и CD40L, соответственно. Каждому трансгену или набору трансгенов предшествовала промоторная последовательность, а также последовательности, которые идентичны целевому сайту вставки в MVA-BN для обеспечения гомологичной рекомбинации в вирусном геноме.
[0260] Для получения всех вышеописанных mBN MVA каждую из культур клеток CEF, инокулировали MVA-BN и трансфицировали соответствующей рекомбинационной плазмидой. В свою очередь, образцы из этих клеточных культур инокулировали в культуры CEF в среду, содержащую лекарственные препараты, индуцирующие селективное давление, а флуоресцентные вирусные клоны выделяли путем очищения на основе бляшкообразования. Исчезновение содержащей флуоресцентный белок селекционной кассеты из этих вирусных клонов было опосредовано на втором этапе CRE-опосредованной рекомбинацией, в которой участвовали два сайта loxP, фланкирующие селекционную кассету в каждой конструкции. После второй стадии рекомбинации были сохранены только последовательности трансгена (например, OVA, 4-1BBL, gp70, HERV-K и/или CD40L) с их промоторами, вставленными в целевые локусы MVA-BN. Готовили запас очищенного методом бляшкообразования вируса без селекционной кассеты.
[0261] Экспрессия идентифицированных трансгенов демонстрируется в клетках, инокулированных описанной конструкцией.
[0262] Получение описанных в настоящем изобретении конструкций осуществляли с использованием клонированной версии MVA-BN в бактериальной искусственной хромосоме (ВАС). Плазмиды рекомбинации содержали описанные последовательности трансгена, каждая ниже промотора. Эти плазмиды содержали последовательности, которые также присутствуют в MVA и, следовательно, позволяют проводить специфическое нацеливание на сайт интеграции. Вкратце, инфекционные вирусы восстанавливали из БИХ путем трансфекции ДНК БИХ в клетки BHK-21 и суперинфекции их вирусом фибромы Шоупа в качестве хелперного вируса. После трех дополнительных пассажей на культурах клеток CEF получали не содержащие вирусов-помощников версии конструкций. Иллюстративный способ получения MVA также можно найти в Baur et al. ((2010) Virol. 84: 8743-52, «Immediate-early expression of a recombinant antigen by modified vaccinia virus Ankara breaks the immunodominance of strong vector-specific B8R antigen in acute and memory CD8 T-cell responses»).
Пример 2: 4-1BBL-опосредованная костимуляция Т-клеток CD8 опухолевыми клетками, инфицированными MVA-OVA-4-1BBL, влияет на продукцию цитокинов без потребности в ДК
[0263] Дендритные клетки (ДК) были получены после культивирования клеток костного мозга мышей C57BL/6 в присутствии рекомбинантного Flt3L в течение 14 дней. Клетки B16.F10 (модель меланомы) инфицировали посредством MVA-OVA, MVA-OVA-CD40L или MVA-OVA-4-1BBL при MOI 10 и культивировали в течение ночи при 37°C с 5% CO2. На следующий день инфицированные опухолевые клетки собирали и совместно культивировали, если указано, в присутствии ДК в соотношении 1:1 в течение 4 часов при 37°C с 5% CO2. Интактные OVA (257-264)-специфичные CD8+ Т-клетки очищали посредством магнитного способа от мышей OT-I и добавляли в совместную культуру в соотношении 1:5. Клетки культивировали при 37°C и 5% CO2 в течение 48 часов. Затем культуральный супернатант собирали для анализа концентрации цитокинов посредством Luminex. Результаты показаны на фиг. 1 в виде концентрации супернатанта: IL-6 (фиг. 1A); GM-CSF (фиг. 1B); ИЛ-2 (фиг. 1С); и IFN-γ (фиг. 1D). Данные представлены в виде среднего значения ± СОС.
[0264] В соответствии с тем, что сообщалось ранее, MVA-OVA-CD40L оказал большое влияние на активацию ДК и их способность презентации антигена. Таким образом, FLDC, инфицированный MVA-OVA-CD40L, продуцировал большие количества IL-6 (фиг. 1A). Важно отметить, что OVA-специфичные Т-клеточные ответы могут быть индуцированы исключительно в присутствии ДК, но не непосредственно самими клетками B16.F10, инфицированными MVA-CD40L (фиг. 1B и 1C). Данные результаты показывают четкую потребность ДК в раскрытии преимуществ MVA-OVA-CD40L. Напротив, MVA-OVA-4-1BBL не индуцировал продукцию IL-6 в ДК, но инфицированные MVA-OVA-4-1BBL клетки B16.F10 вызывали секрецию цитокинов активации Т-клеток IFN-γ, IL-2 и GM-CSF независимо от постоянного тока (фиг. 1A-1D).
Пример 3: инфицированные MVA-OVA-4-1BBL опухолевые клетки напрямую (т.е. без необходимости в DC) управляют дифференцировкой антигенспецифичных Т-клеток CD8 в активированных эффекторных Т-клетках
[0265] Дендритные клетки (ДК) были получены после культивирования клеток костного мозга мышей C57BL/6 в присутствии рекомбинантного Flt3L в течение 14 дней. Клетки B16.F10 (модель меланомы) инфицировали посредством MVA-OVA, MVA-OVA-CD40L или MVA-OVA-4-1BBL при MOI 10 и культивировали в течение ночи при 37°C с 5% CO2. На следующий день инфицированные опухолевые клетки собирали и совместно культивировали, если указано, в присутствии ДК в соотношении 1:1 в течение 4 часов при 37°C с 5% CO2. В то же время, интактные OVA (257-264)-специфичные CD8+ Т-клетки очищали посредством магнитного способа от мышей OT-I и добавляли в совместную культуру в соотношении 1:5. Клетки культивировали при 37°C и 5% CO2 в течение 48 часов. Затем клетки окрашивали и анализировали посредством проточной цитометрии. Результаты показаны на фиг. 2 в виде GMFI T-bet на OT-I CD8+Т-клетках (фиг. 2A) и процентное содержание CD44+гранзим B+IFN-γ+TNFα+OT-I CD8+Т-клеток (фиг. 2B). Данные представлены в виде среднего значения ± СОС.
[0266] Результаты показывают, что в отсутствие кросс-представляющих ДК индукция цитотоксических эффекторных Т-клеток гранзим B+и IFNγ+зависела от 4-1BBL (фиг. 2B). В совокупности с результатами, представленными на фиг. 1, данные результаты подтверждают, что, в отличие от кодируемого MVA CD40L, который действует посредством активации ДК, 4-1BBL, кодируемый MVA, действует непосредственно на Т-клетки независимым от ДК образом.
Пример 4: Инфекция MVA, кодирующая либо CD40L, либо 4-1BBL, вызывает гибель опухолевых клеток в линиях опухолевых клеток и макрофагах
[0267] Линии опухолевых клеток B16.OVA (фиг. 3A и 3B), MC38 (фиг. 3C) и B16.F10 (фиг. 3D) были инфицированы при указанной MOI в течение 20 часов. Затем клетки анализировали на их жизнеспособность посредством проточной цитометрии. Уровень сывороточного HMGB1 в образцах с фиг. 3A количественно определяли посредством ELISA (фиг. 3B). Макрофаги, происходящие из костного мозга (BMDM), инфицировали при указанной MOI в течение 20 часов. Затем клетки анализировали на их жизнеспособность посредством проточной цитометрии. Результаты показаны на фиг. 3A-3E. Данные представлены виде среднего значения ± СОС.
[0268] Как показано на фиг. 3A и 3B, инфицирование MVA-OVA или MVA-OVA-CD40L приводило к умеренной индукции гибели клеток по сравнению с опухолевыми клетками, обработанными ФСБ. Интересно, что заражение MVA-OVA-4-1BBL значительно повышало гибель опухолевых клеток через 18 часов после заражения.
[0269] Для дополнительного подтверждения данных результатов на неантигенных клеточных линиях, авторы настоящего изобретения выполнили аналогичные анализы с использованием опухолевых клеток MC38 (фиг. 3C) и B16.F10 (фиг. 3D), инфицированных MVA, MVA-CD40L и MVA-4-1BBL (ни один из которых не кодирует TAA). Соответственно, инфицирование данными MVA индуцировало гибель клеток в данных линиях опухолевых клеток и эффективно уничтожало макрофаги, происходящие из костного мозга (BMDM) (фиг. 3E). В целом, указанные данные продемонстрировали, что инфекция MVA приводит к гибели опухолевых клеток и макрофагов, которая увеличивается, если CD40L или 4-1BBL экспрессируются рекомбинантным MVA.
[0270] Инфекция опухолевых клеток онколитическим вирусом приводит к индукции так называемой иммуногенной гибели клеток (ICD) (Workenhe et al. (2014) Mol. Ther. 22: 251-56). ICD включает высвобождение внутриклеточных белков, таких как кальретикулин, АТФ или HMGB1, которые действуют как алармины для иммунной системы, приводя к усиленной презентации антигена и тем самым вызывая противоопухолевый иммунитет. Авторы настоящего изобретения проверили, приведет ли инфекция MVA к индукции ICD посредством секретируемого HMGB1. Неожиданно авторы настоящего изобретения обнаружили, что MVA-OVA-4-1BBL и MVA-OVA-CD40L индуцировали значительное увеличение HMGB1 по сравнению с MVA-OVA (фиг. 3B).
Пример 5: MVA, кодирующий 4-1BBL, индуцирует активацию NK-клеток in vivo
[0271] Мышей C57BL/6 (n=5/группа) иммунизировали внутривенно либо физиологическим раствором, либо 5×107 TCID50 MVA-OVA («rMVA» на фиг. 4), 5×107 TCID50 MVA-OVA-4-1BBL («rMVA-4-1BBL» в фиг. 4), или 5×107 TCID50 MVA-OVA в комбинации с 200 мкг антитела к 4-1BBL (клон TKS-1). Через 24 часа мышей умерщвляли и селезенки обрабатывали для анализа проточной цитометрии. Результаты показаны на фиг. 4A и фиг. 4B. Показано среднее геометрическое интенсивности флуоресценции (GMFI) CD69 (фиг. 4A) и CD70 (фиг. 4B). Данные показаны виде среднего значения ±СОС, представляющие два независимых эксперимента.
[0272] Результаты показали, что качество ответа NK-клеток повышалось при добавлении 4-1BBL к MVA-OVA по сравнению с внутривенным введением MVA-OVA без 4-1BBL и обоих маркеров активации NK-клеток, CD69 и CD70, были значительно активированы по сравнению с MVA-OVA (фиг. 4A и B). Совместная инъекция блокирующих 4-1BBL антитела показала, что активация NK-клеток, индуцированная MVA-OVA, была полностью 4-1BBL-независимой, но могла быть усилена, если MVA-OVA-4-1BBL доставлял избыточный сигнал 4-1BBL.
Пример 6: Внутривенная иммунизация MVA, кодирующим 4-1BBL, способствует секреции сывороточного IFN-γ in vivo
[0273] Мышей C57BL/6 (n=5/группа) иммунизировали внутривенно либо физиологическим раствором, либо 5×107 TCID50 «rMVA» (= MVA-OVA), 5×107 TCID50 «rMVA-4-1BBL» (= MVA-OVA-4-1BBL), или 5×107 TCID50 MVA-OVA в комбинации с 200 мкг антитела к 4-1BBL (клон TKS-1). Результаты показаны на фиг. 5A и 5B. Данные представлены в виде среднего значения ±СОС. Фиг. 5A: через 6 часов у мышей отбирали кровь, сыворотку отделяли от цельной крови и концентрацию IFN-γ в сыворотке определяли посредством Luminex. Фиг. 5B: через 3, 21 , и 45 часов мышам внутривенно инъецировали брефельдин A для окончания секреции белка. Мышей умерщвляли через 6, 24 и 48 часов после иммунизации и спленоциты анализировали посредством проточной цитометрии.
[0274] Опосредованная 4-1BB активация NK-клеток совпадала с повышенными уровнями в сыворотке NK эффекторного цитокина IFNγ (фиг. 5A). Известно, что NK-клетки при активации продуцируют большое количество IFN-γ. Для определения того, могли ли повышенные уровни IFN-γ в сыворотке происходить из NK-клеток, долю NK-клеток, продуцирующих IFN-γ, определяли в разные моменты времени после внутривенной инъекции указанных рекомбинантных векторов MVA. Через 6 часов после инъекции, когда измеряли высокие уровни IFN-γ в сыворотке, процент IFN-γ+ NK-клеток был самым высоким и после этого медленно снижался (фиг. 5B). Самая высокая частота IFN-γ-положительных NK-клеток наблюдалась при использовании MVA-OVA-4-1BBL. В целом, указанные данные демонстрируют, что внутривенная иммунизация rMVA-4-1BBL приводит к сильной активации NK-клеток и увеличению продукции эффекторного цитокина NK-клеток IFN-γ.
Пример 7: Внутривенная иммунизация rMVA-4-1BBL способствует секреции сывороточного IFN-γ у мышей с опухолью B16.OVA
[0275] Мышей C57BL/6 с опухолью B16.OVA (n=5/группа) были сгруппированы и получили внутривенно. (внутривенно) ФСБ или 5×107 TCID50 MVA-OVA («rMVA» на фиг.) или MVA-OVA-4-1BBL («rMVA-4-1BBL» на фиг.) на 7 день после инокуляции опухоли. Через 6 часов у мышей брали кровь, сыворотку выделяли из цельной крови, и концентрацию IFN-γ в сыворотке определяли посредством Luminex. Результаты показаны на фиг. 6. Данные представлены в виде среднего значения ±СОС.
[0276] Данные, показанные на фиг. 6, демонстрируют, что эффекты, аналогичные эффектам на NK-клетки, которые описаны в других экспериментах, также могут быть получены на модели опухоли меланомы. Через 6 часов после иммунизации уровни IFN-γ в сыворотке были сильно увеличены у мышей с опухолью, иммунизированных MVA-OVA-4-1BBL, что указывает на сильную активацию NK-клеток (фиг. 6).
Пример 8: Внутривенная прайм-буст иммунизация rMVA-4-1BBL усиливает экспансию антиген- и вектор-специфичных CD8+ Т-клеток
[0277] На фиг. 7A-7D показаны антиген- и вектор-специфичные после внутривенной прайм-буст иммунизации rMVA-4-1BBL. Мыши C57BL/6 (n=4/группа) получали внутривенную первичную иммунизацию физиологическим раствором или 5×107 TCID50 rMVA (= MVA-OVA), 5×107 TCID50 rMVA-4-1BBL (= MVA-OVA-4-1BBL) или 5×107 TCID50. rMVA в комбинации с 200 мкг антитела к 4-1BBL (клон TKS-1) в день 0 и бустерную иммунизацию в день 41. У мышей отбирали кровь в дни 6, 21, 35, 48 и 64 дни после первичной иммунизации и выполняли проточный цитометрический анализ периферической крови. Мышей умерщвляли на 70 день после первичной иммунизации. Селезенки собирали и проводили анализ посредством проточной цитометрии.
[0278] Результаты показаны на фиг. 7A-7D. На фиг. 7A показано процентное содержание антиген-(OVA)-специфичных CD8+Т-клеток среди лейкоцитов периферической крови (PBL); и на фиг. 7В показано процентное содержание векторных (B8R)-специфичных CD8+Т-клеток среди PBL. На фиг. 7C показано процентное соотношение (OVA)-специфичных CD8+Т-клеток антигена среди живых клеток. На фиг. 7D показано процентное содержание векторных (B8R)-специфичных CD8+ Т-клеток среди живых клеток. Данные представлены в виде среднего значения ± СОС.
[0279] Результаты показывают, что B8- и OVA-специфичные CD8 Т-клетки достигли максимума на 7 день после первой иммунизации и наблюдалась их дальнейшая экспансия после второй иммунизации в день 41 (фиг. 7A и B). В момент дня 41 наблюдалось явное преимущество rMVA-4-1BBL с точки зрения антигенспецифичного Т-клеточного ответа по сравнению с rMVA, как для B8, так и для OVA. Интересно, что совместная инъекция блокирующего 4-1BBL антитела показала, что rMVA-индуцированные Т-клеточные ответы были полностью 4-1BBL-независимыми, но могли быть усилены, если избыточный сигнал 4-1BBL доставлялся rMVA-4-1BBL (фиг. 7A и B). В соответствии с данными результатами первичная/бустерная иммунизация rMVA-4-1BBL также привела к улучшенному OVA- и B8-специфичному Т-клеточному ответу в селезенке через 70 дней после первой иммунизации (фиг. 7C и D).
Пример 9: Усиление противоопухолевого эффекта внутривенной инъекции вируса MVA, кодирующего TAA и 4-1BBL
[0280] Мышей C57BL/6 с опухолью B16.OVA (n=5/группа) группировали и они получали в/в (внутривенно) ФСБ или 5×107 TCID50 MVA-OVA или 5×107 TCID50 MVA-OVA-4-1BBL в день 7 (черная пунктирная линия) после инокуляции опухоли. Рост опухоли измеряли через равные интервалы. Как показано на фиг. 8, внутривенное введение вируса MVA, кодирующего 4-1BBL, приводило к снижению объема опухоли по сравнению с MVA или контролем (ФСБ) как следствие длительной задержки роста опухолей.
Пример 10: Усиленный противоопухолевый эффект внутриопухолевой инъекции вируса MVA, кодирующего 4-1BBL или CD40L
[0281] Мышей C57BL/6 с опухолью B16.OVA (n=4-5/группа) группировали и они получали внутриопухолево (в/о) ФСБ или 5×107 TCID50 MVA-OVA («rMVA» на фиг.), MVA-OVA-CD40L ( «RMVA-CD40L» на рисунке) или MVA-OVA-4-1BBL («rMVA-4-1BBL» на фиг.) в день 7 (черная пунктирная линия), 12 и 15 (серые пунктирные линии) после инокуляции опухоли. Рост опухоли измеряли через равные интервалы. Как показано на фиг. 9A-9D, усиленный противоопухолевый эффект был реализован посредством внутриопухолевой инъекции вируса MVA, кодирующего TAA и 4-1BBL или CD40L. Более конкретно, как показано на фиг. 9D, значительно большее снижение роста опухоли наблюдалось при использовании вируса MVA, кодирующего 4-1BBL. Несмотря на то, что настоящее изобретение не связано каким-либо конкретным механизмом или способом действия, одна из гипотез различий, наблюдаемых между 4-1BBL и CD40L, заключается в том, что 4-1BBL направлен на активацию NK-клеток и Т-клеток, тогда как CD40L направлен на активацию ДК. Опухоли меланомы B16 больше инфильтрированы Т-клетками (Mosely et al. (2016) рак Immunol. Res. 5(1): 29-41); следовательно, кодирование MVA 4-1BBL более эффективно, чем кодирование CD40L MVA в данной настройке.
[0282] Независимо от точного механизма или пути, посредством которого 4-1BBL и CD40L оказывают свое влияние на рост или диаметр опухоли, данные на фиг. 9 показали, что внутриопухолевое введение MVA, кодирующего 4-1BBL, приводило к длительному контролю роста опухоли, а в некоторых случаях даже в полное отторжение опухоли.
Пример 11: Усиленный противоопухолевый эффект внутриопухолевой инъекции вируса MVA, кодируемого TAA и CD40L, против установленного рака толстой кишки
[0283] Мышей C57BL/6 с опухолью MC38 (n=5/группа) группировали и они получали внутриопухолево (в/о) ФСБ или 5×107 TCID50 MVA-TAA («rMVA» на фиг.) или MVA-TAA-CD40L («rMVA-CD40L» в фиг.) в день 14 (черная пунктирная линия), 19 и 22 (черные пунктирные линии) после инокуляции опухоли. Рост опухоли измеряли через равные интервалы. Результаты показаны на фиг. 10A, 10B и 10C для неантигенных установленных карцином толстой кишки MC38. TAA, экспрессируемые MVA в данных экспериментах, включали антигены AH1A5, p15E и TRP2.
[0284] Данные результаты показывают, что внутриопухолевое введение MVA, кодирующего CD40L, в дополнение к одному или более TAA может значительно замедлить рост опухоли в модели карциномы толстой кишки MC38.
Пример 12: Иммунная блокада контрольных точек и антитела, специфичные к опухолевому антигену, взаимодействуют с внутриопухолевым введением MVA-OVA-4-1BBL
[0285] Клетки меланомы B16.OVA (5×105) вводили подкожно мышам C57BL/6. Когда опухоли достигали примерно 5 мм в диаметре, мышей группировали (n=5/группу) и они получали по показаниям (галочки) 200 мкг IgG2a, антитело к TRP-1 или антитело к PD-1 внутрибрюшинно (в/б). Мышей иммунизировали посредством внутриопухолевого (в/о) введения либо ФСБ, либо 5×107 TCID50 MVA-OVA-4-1BBL в дни 13 (черная пунктирная линия), 18 и 21 (серые пунктирные линии) после инокуляции опухоли. Рост опухоли измеряли через равные интервалы. Результаты показаны на фиг. 11. Если антитело, специфичное к опухолевому ассоциированному антигену (TAA) Trp1 (антитело к Trp1), сочетали с внутриопухолевым введением MVA-OVA-4-1BBL, наблюдалось повышенное снижение опухоли по сравнению с антителом к PD-1 отдельно (фиг. 11, средний ряд). Если антитело к PD-1, молекулу иммунных контрольных точек, объединяли с внутриопухолевым введением MVA-OVA-4-1BBL, наблюдалось повышенное снижение объема опухоли по сравнению с антителом к PD-1 отдельно (фиг. 11, нижний ряд).
[0286] Данные эксперименты демонстрируют, что антитела к PD-1 и к TRP-1 усиливали контроль роста опухоли в качестве отдельных средств, в то время как комбинация любого антитела с MVA-OVA-4-1BBL улучшала терапевтический эффект, оказываемый MVA-OVA-4-1BBL. В данном случае комбинированная терапия внутриопухолевым MVA 4-1BBL либо блокадой контрольной точки, либо антителами, нацеленными на TAA, имела большую терапевтическую активность, чем любая из монотерапий. Указанные данные также указывают на то, что опухолеспецифичные антитела, которые потенциально индуцируют АЗКЦ, можно комбинировать с внутриопухолевыми инъекциями MVA, экспрессирующего 4-1BBL, для синергетического эффекта.
Пример 13: Превосходный противоопухолевый эффект внутриопухолевой инъекции MVA-OVA-4-1BBL по сравнению с лечением посредством агонистического антитела CD137
[0287] Мышей C57BL/6 с опухолью B16.OVA (n=5/группа) группировали и осуществляли внутриопухолевую инъекцию либо ФСБ, 5×107 TCID50 MVA-OVA-4-1BBL, либо 10 мкг антитела к 4-1BB (3H3, BioXcell) в день 7, 12 и 15 (черные пунктирные линии) после инокуляции опухоли. Рост опухоли измеряли через равные интервалы.
[0288] На фиг. 12A показан превосходный противоопухолевый эффект MVA-OVA-4-1BBL по сравнению с агонистическим антителом к 4-1BBL (3H3). На фиг. 12B показано, что внутриопухолевая иммунизация MVA-OVA-4-1BBL вызывала исключительно OVA-специфичный Т-клеточный ответ в крови, тогда как агонистическое антитело к 4-1BBL не индуцировало никаких OVA-специфичных Т-клеток в крови.
[0289] Таким образом, указанные данные показывают, что внутриопухолевое лечение MVA-OVA-4-1BBL более эффективно, чем агонистические антитела к CD137, как с точки зрения опухолеспецифичного ответа Т-клеток, так и с точки зрения контроля роста опухоли.
Пример 14: Усиление противоопухолевого эффекта внутривенной инъекции MVA, кодирующего эндогенный ретровирусный (ERV) антиген Gp70, кодируемый CD40L, в модели опухоли CT26
[0290] Мышей Balb/c с опухолью CT26 (n=5/группа) группировали и они получали внутривенно (в/в) ФСБ или 5×107 TCID50 MVA-BN, MVA-Gp70 или MVA-Gp70-CD40L в день 12 (черная пунктирная линия) после введение опухолей мышам. Рост опухоли измеряли через равные интервалы. Как показано на фиг. 13A и 13B, внутривенное введение вируса MVA, кодирующего эндогенный ретровирусный антиген Gp70, приводило к уменьшению опухоли по сравнению с MVA или контролем (ФСБ). Противоопухолевый эффект дополнительно усиливался, когда CD40L дополнительно кодировался MVA-Gp70-CD40L.
[0291] На фиг. 13C показана индукция Gp70-специфичных CD8 Т-клеток в крови при внутривенной инъекции MVA-Gp70 или MVA-Gp70-CD40L.
[0292] Таким образом, в данных экспериментах был сконструирован MVA, кодирующий модель ERV, которая представляет собой мышиный белок gp70 (оболочечный белок вируса мышиного лейкоза) («MVA-gp70»). Также был получен MVA, дополнительно содержащий костимулирующую молекулу CD40L («MVA-gp70-CD40L»). Противоопухолевый потенциал данных новых конструкций испытывали с использованием модели карциномы толстой кишки CT26.wt. Было показано, что CT26.wТ-клетки экспрессируют высокие уровни gp70 (см., например, Scrimieri (2013) Oncoimmunol 2: e26889). Были получены мыши с опухолью CT26.wt, и, когда размер опухоли составлял по меньшей мере 5 мм × 5 мм, их иммунизировали внутривенно, как указано выше. Иммунизация с использованием только MVA вызывала небольшую задержку роста опухоли. Напротив, иммунизация с использованием MVA-gp70 вызвала полное отторжение 3/5 опухолей (фиг. 13A и B). Еще более поразительные результаты были получены при иммунизации MVA-Gp70-CD40L, которая вызвала отторжение 4/5 опухолей (фиг. 13 A и B).
[0293] Для определения того, коррелируют ли данные противоопухолевые ответы с индукцией gp70-специфичных Т-клеток после иммунизации, повторную стимуляцию крови выполняли с использованием H-2Kd-ограниченного эпитопа gp70 AH1. Данные результаты (фиг. 13C) показывают сильную индукцию gp70-специфичных ответов Т-лимфоцитов CD8 у мышей, обработанных MVA-Gp70 и MVA-Gp70-CD40L (фиг. 13C).
Пример 15: Усиление противоопухолевого эффекта внутривенной инъекции MVA, кодирующего эндогенный ретровирусный антиген Gp70, кодируемый CD40L, в модели опухоли B16.F10
[0294] Мышей C57BL/6 с опухолью B16.F10 (n=5/группа) группировали и они получали внутривенно (iv) ФСБ или 5×107 TCID50 MVA-BN, MVA-Gp70, или MVA-Gp70-CD40L в день 7 (черные точки линия) после инокуляции опухоли, когда размер опухоли составляет приблизительно 5 × 5 мм. Рост опухоли измеряли через равные интервалы. Как показано на фиг. 14А, внутривенное введение вируса MVA, кодирующего эндогенный ретровирусный антиген Gp70 и CD40L, приводило к уменьшению опухоли по сравнению с MVA или контролем (ФСБ).
[0295] На фиг. 14В показана индукция Gp70-специфичных CD8 Т-клеток в крови при внутривенной инъекции MVA-Gp70 или MVA-Gp70-CD40L.
[0296] Таким образом, в данных экспериментах эффективность лечения MVA-Gp70 и MVA-Gp70-CD40L была продемонстрирована на дополнительной независимой модели опухоли. B16.F10 представляет собой клеточную линию меланомы, полученную из C57BL/6, и экспрессирует высокие уровни Gp70 (Scrimieri (2013) Oncoimmunol 2: e26889). Лечение только MVA («MVA-BN») приводило к некоторой задержке роста опухоли B16.F10, сравнимой с эффектом неадъювантного MVA-Gp70 (фиг. 14A). Тем не менее, MVA-Gp70-CD40L приводил к более сильному противоопухолевому эффекту, чем контроль скелета MVA отдельно (фиг. 14A). Дополнительные эксперименты продемонстрировали, что обе группы, получавшие MVA, кодирующий Gp70-антиген, проявляли CD8-Т-клеточные ответы, специфичные для H-2Kb-ограниченного gp70-эпитопа p15e, но не наблюдалось резкого увеличения периферических Т-клеточных ответов, если CD40L также кодировался MVA (фиг. 14B).
Пример 16: Усиление противоопухолевого эффекта внутривенной инъекции вируса MVA, кодирующего gp70 и 4-1BBL [Пример возможного применения]
[0297] Мышей C57BL/6 с опухолью B16.OVA (n=5/группа) группировали и они получали внутривенное ФСБ или 5×107 TCID50 MVA-OVA или MVA-gp70-4-1BBL в день 7 (черная пунктирная линия) после инокуляции опухоли. Рост опухоли измеряют через регулярные промежутки времени. Поскольку мышиные гомологи человеческих эндогенных ретровирусных (ERV) белков не экспрессируются в высокой степени в нормальных тканях мыши и не экспрессируются преимущественно в тканях опухолей мышей, эффективность человеческих ERV не может быть эффективно изучена на мышиной модели. Gp70 представляет собой мышиный белок ERV, который хорошо изучен (см., например,Bronte et al. (2003) J Immunol. 171 (12): 6396-6405; Bashratyan et al. (2017) Eur. J. Immunol. 47: 575-584; и Nilsson et al. (1999) Virus Genes 18: 115-120). Соответственно, исследование вакцины против gp70-специфичного рака на мышах, скорее всего, будет иметь сильную прогностическую ценность в отношении эффективности вакцины против ERV-специфичного рака у людей.
Пример 17: Усиленный противоопухолевый эффект внутриопухолевой инъекции вируса MVA, кодирующего gp70 и либо 4-1BBL, либо CD40L [Пример возможного использования]
[0298] Мышей C57BL/6 с опухолью B16.OVA (n=4-5/группа) группировали и они получали внутриопухолево (в/о) ФСБ или 5×107 TCID50 MVA-OVA, MVA-OVA-CD40L или MVA-OVA-4-1BBL в день 7 (черная пунктирная линия), 12 и 15 (серые пунктирные линии) после инокуляции опухоли. Рост опухоли измеряли через равные интервалы.
Пример 18: Введение rMVA-HERV-K-4-1BBL влияет на продукцию цитокинов посредством прямой презентации антигена инфицированных опухолевых клеток [Пример возможного использования]
[0299] Дендритные клетки (ДК) были получены после культивирования клеток костного мозга мышей C57BL/6 в присутствии рекомбинантного Flt3L в течение 14 дней. Клетки B16.F10 инъецировали с MVA-HERV-K, MVA-HERV-K-CD40L, MVA-HERV-K-4-1BBL, или MVA-HERV-K-4-1BBL-CD40L при MOI 10 и оставляли в течение ночи. На следующий день инфицированные опухолевые клетки собирали и совместно культивировали, если указано, в присутствии DC в соотношении 1:1 в течение 4 часов при 37°C с 5% CO2. CD8+Т-клетки, специфичные для HERV-K, очищали посредством магнитной очистки от мышей, иммунизированных HERV-K, и добавляли в совместную культуру в соотношении 1:5. Клетки культивировали при 37°C и 5% CO2 в течение 48 часов. Затем культуральный супернатант собирали для анализа концентрации цитокинов посредством Luminex. Измерение уровней цитокинов включает (A) IL-6, (B) GM-CSF, (C) IL-2, и (D) IFNγ. Данные представлены виде среднего значения ±СОС.
Пример 19: Введение rMVA-HERV-K-4-1BBL направляет антигенспецифичные CD8+ Т-клетки к активированным эффекторным Т-клеткам посредством прямой презентации антигена инфицированных опухолевых клеток [Пример возможного использования]
[0300] Дендритные клетки (ДК) были получены после культивирования клеток костного мозга мышей C57BL/6 в присутствии рекомбинантного Flt3L в течение 14 дней. Клетки B16.F10 инъецировали с MVA-HERV-K, MVA-HERV-K-CD40L, MVA-HERV-K-4-1BBL, или MVA-HERV-K-4-1BBL-CD40L при MOI 10 и оставляли в течение ночи. На следующий день инфицированные опухолевые клетки собирали и совместно культивировали, если указано, в присутствии DC в соотношении 1:1 в течение 4 часов при 37°C с 5% CO2. В то же время, CD8+Т-клетки, специфичные для HERV-K, очищали посредством магнитной очистки от мышей, иммунизированных HERV-K, и добавляли в совместную культуру в соотношении 1:5. Клетки культивировали при 37°C и 5% CO2 в течение 48 часов. Затем клетки окрашивали и анализировали посредством проточной цитометрии. Цитокиновый анализ проводят для (A) GMFI T-bet на OT-I CD8+Т-клетках и (B) процентного содержания CD44+гранзим B+IFNγ+TNFα+OT-I CD8+Т-клеток. Данные представлены в виде среднего значения ±СОС.
Пример 20: Инфекция rMVA-HERV-K, кодируемая либо CD40L, либо 4-1BBL, вызывает гибель опухолевых клеток в линиях опухолевых клеток и макрофагах [Пример возможного использования]
[0301] Опухолевые клеточные линии B16.OVA (A и B), MC38 (C) и B16.F10 (D) инфицированы при указанной MOI в течение 20 часов. Затем клетки анализировали на их жизнеспособность посредством проточной цитометрии. Сывороточный HMGB1 в образцах из (A) количественно определяют посредством ELISA. Макрофаги, происходящие из костного мозга (BMDM), инфицировали при указанной MOI в течение 20 часов. Затем клетки анализировали на их жизнеспособность посредством проточной цитометрии. Данные представлены виде среднего значения ±СОС.
Пример 21: Внутриопухолевое введение рекомбинантного MVA, кодирующего 4-1BBL, приводит к снижению Treg-клеток и уменьшению истощения T-клеток в опухоли [Пример возможного использования]
[0302] Мышей C57BL/6 с опухолью B16.OVA (n=5/группа) группировали и они получали внутриопухолево (в/о) ФСБ или 5×107 TCID50 MVA-OVA или MVA-OVA-4-1BBL в день 7 (черная пунктирная линия) после инокуляции опухоли. Через пять дней мышей умерщвляли, собирали селезенки и опухоли и окрашивали для оценки инфильтрации Treg и истощения Т-клеток антителами, конъюгированными с флуорохромом. (A) Процент CD4+FoxP3+Т-клеток среди CD45+лейкоцитов, инфильтрирующих опухоль; Средняя геометрическая интенсивность флуоресценции PD-1 (B) и Lag-3 (C) на инфильтрирующих опухоль Т-клеток CD8. Данные представлены виде среднего значения ± СОС.
Пример 22. Блокада иммунной контрольной точки и антитела, специфичные к опухолевому антигену, взаимодействуют с внутриопухолевым введением rMVA gp-70-4-1BBL [Пример возможного использования]
[0303] Мышей C57BL/6 с опухолью B16.OVA (n=5/группа) группировали и они получали по показаниям (галочки) 200 мкг IgG2a, антитело к TRP-1 или антитело к PD-1. Мышей иммунизировали внутриопухолево либо ФСБ, либо 5×107 TCID50 MVA-gp70-4-1BBL в день 13 (черная пунктирная линия), 18 и 21 день (серые пунктирные линии) после инокуляции опухоли. Рост опухоли измеряют через регулярные промежутки времени.
Пример 23: Ответы основной цепи цитокинов/хемокинов MVA-BN на IT-иммунизацию могут быть увеличены посредством адъювантации 4-1BBL.
[0304] Для оценки способности рекомбинантного MVA вызывать воспаление в микроокружении опухоли (TME), цитокины и хемокины анализировали в ткани опухолей B16.OVA. Во-первых, 5×105 клеток B16.OVA подкожно (п/к) имплантировали мышам C57BL/6. В день 10 мышей иммунизировали внутриопухолево (в/о) ФСБ или 2×108 TCID50 MVA-BN, MVA-OVA, или MVA-OVA-4-1BBL (n=5-6 мышей/группа).
[0305] Через шесть часов после инъекции измеряли экспрессию цитокинов и хемокинов (фиг. 15). Экспрессия цитокинов/хемокинов в ткани, обработанной ФСБ, представляет собой базальный воспалительный профиль, вызванный введением иглы в опухоль и сдвиговым давлением физиологического раствора. Цитокины, включая IL-6, IFN-α, IL-15 и TNF-α, а также хемокины, такие как CXCL1, CCL2 и MIP2, были активированы (фиг. 15). Также был обнаружен IL-25 (также известный как IL-17E), который индуцируется активацией NF-κβ и стимулирует выработку IL-8 у людей (Lee et al. (2001) J. Biol. Chem. 276: 1660-64). Интересно, что опухоли, в которые вводили MVA-OVA-4-1BBL, демонстрировали значительное увеличение провоспалительных цитокинов, таких как IL-6, IFN-α или IL-15/IL15Rα, по сравнению с опухолями, в которые инъецировали MVA-BN или опухолевые поражения, в которые инъецировали MVA-OVA.
Пример 24: Цитокиновые/хемокиновые провоспалительные реакции на внутриопухолевую (в/о) иммунизацию усиливаются при использовании MVA-OVA-4-1BBL
[0306] Мышей и опухоли обрабатывали в соответствии с описанием в примере 23. Поразительно, но несколько провоспалительных цитокинов, включая IFN-γ и GM-CSF, продуцировались только после внутриопухолевой иммунизации MVA-OVA-4-1BBL (фиг. 16). Продукция других провоспалительных цитокинов, включая IL-18, CCL5, CCL3 и IL-22, усиливалась посредством внутриопухолевой (в/о) иммунизации с использованием либо MVA-OVA, либо MVA-OVA-4-1BBL, но не только MVA-BN или ФСБ.
[0307] В целом указанные данные демонстрируют, что внутриопухолевая (в/о) иммунизация MVA может вызывать воспалительный сдвиг цитокинов/хемокинов в микроокружении опухоли (TME), тем самым усиливая воспалительный ответ. Повышенные эффекты наблюдались при внутриопухолевой иммунизации MVA-OVA-4-1BBL по сравнению с MVA или MVA-OVA. Таким образом, можно сказать, что добавление 4-1BBL «усилило» рекомбинантный MVA.
Пример 25: Количественный и качественный Т-клеточный анализ TME и дренирующего ЛУ после внутриопухолевой инъекции MVA-OVA-4-1BBL
[0308] Для лучшего понимания клеточных процессов, вызванных воспалением после внутриопухолевой (в/о) инъекции MVA-OVA и MVA-OVA-4-1BBL, осуществляли углубленный анализ инфильтратов врожденного и адаптивного иммунитета в различные моменты времени после внутриопухолевой (в/о) инъекции. Мышам с опухолью B16.OVA внутриопухолево (в/о) вводили либо ФСБ, либо 2×108 TCID50 MVA-OVA или MVA-OVA-4-1BBL. Мышей умерщвляли через 1, 3 и 7 дней после первичной иммунизации. Опухоли и дренирующие опухоль лимфатические узлы (TdLN) удаляли и обрабатывали коллагеназой и ДНКазой, и отдельные клетки анализировали посредством проточной цитометрии. Популяции иммунных клеток анализировали для определения их размера, пролиферативного поведения и функционального состояния.
[0309] Результаты показали, что инъекция в опухоли B16.OVA либо MVA-OVA, либо MVA-OVA-4-1BBL вызвала инфильтрацию лейкоцитов CD45+в опухоли через 7 дней после внутриопухолевой (в/о) иммунизации (фиг. 17, верхний ряд, левая гистограмма). Интересно, что экспансия лейкоцитов CD45+в TdLN наблюдалось уже через 3 дня после в/о (внутриопухолевой) иммунизации (фиг. 17, верхний ряд, правая гистограмма), особенно после инъекции MVA, экспрессирующего 4-1BBL. Данное различие было дополнительно увеличено в TdLN через семь дней после внутриопухолевой (в/о) иммунизации, что позволяет предположить, что иммуно-опосредованные MVA противоопухолевые эффекты начинаются в TdLN уже в день 3 после иммунизации.
[0310] Одним из аспектов противоопухолевой терапии на основе вакцинации является экспансия и восстановление опухолеспецифичных CD8+и CD4+Т-клеток и их обогащение в опухоли. Содержание как CD4+Т-клеток, так и CD8+Т-клеток повышалось в опухоли через неделю после иммунизации (фиг. 17, второй и третий ряд соответственно, гистограммы слева). Содержание CD4+Т-клеток повышалось в опухолях к дню 7, а также в TdLN начиная с дня 3 и достигали пика в день 7 после в/о иммунизации MVA-OVA-4-1BBL. CD8+ Т-клетки в значительной степени способствовали увеличению количества CD45+клеток в опухоли к дню 7. Инъекция MVA-OVA-4-1BBL способствовала дополнительной экспансии популяции Т-лимфоцитов CD8+по сравнению с инъекцией MVA-OVA в обеих опухолях (день 7) и dLN (дни 3 и 7).
[0311] Количественная оценка OVA-специфичных CD8+Т-клеток выявила увеличение в микроокружении опухоли через 7 дней после внутриопухолевой (в/о) иммунизации, особенно в группе, получавшей MVA-OVA-4-1BBL (фиг. 17, внизу слева). Поразительно, что рост OVA-специфичных CD8+Т-клеток в TdLN достиг пика в день 3 после иммунизации, будучи выше в группе, обработанной MVA-OVA-4-1BBL (фиг. 17, внизу справа). В целом указанные данные указывают на то, что внутриопухолевая иммунизация MVA-OVA, особенно MVA-OVA-4-1BBL, усиливает выработку адаптивных иммунных ответов, начиная с 3 дней после обработки в лимфатическом узле, дренирующем опухоль, что приводит к значительному увеличению антигенспецифичных CD8+Т-клеток в микросреде опухоли к дню 7.
Пример 26: Индукция антигенспецифичных CD8+ Т-клеток посредством внутриопухолевой инъекции MVA-OVA-4-1BBL
[0312] OVA-специфичные CD8+Т-клетки в дренирующем опухоль лимфатическом узле (TdLN), индуцированные внутриопухолевой инъекцией MVA-OVA-4-1BBL, проявляли высокую пролиферативную способность. Процент OVA-специфичные CD8+Т-клеток, экспрессирующих Ki67 (индикатор пролиферации клеток), был выше в TdLN после обработки MVA-OVA по сравнению с ФСБ и был дополнительно увеличен у мышей, иммунизированных MVA-OVA-4-1BBL (фиг. 18А). Более того, OVA-специфичные Т-клетки CD8 в опухоли подавляли уровень маркера истощения PD-1 к дню 7 после иммунизации MVA-OVA, а также MVA-OVA-4-1BBL, что указывает на восстановление функциональности (фиг. 18B).
[0313] Клетки Treg (также «регуляторные Т-клетки») являются мощными ингибиторами противоопухолевых иммунных ответов (см., например, Tanaka et al. (2017) Cell Res. 27: 109-118). Внутриопухолевая инъекция MVA-OVA увеличивала OVA-специфичное отношение Teff/Treg в опухоли (т.е. отношение клеток Teff или «эффекторных Т-клеток» к клеткам Treg), и дальнейшее увеличение наблюдалось в день 7 после обработки MVA-OVA-4-1BBL (фиг. 18C). Таким образом, внутриопухолевая обработка с использованием MVA-OVA и, в частности, с использованием MVA-OVA-4-1BBL снижает частоту внутриопухолевого Treg в пользу эффекторных Т-клеток CD8 +, что благоприятно для противоопухолевых иммунных ответов.
Пример 27: Количественный и качественный анализ NK-клеток TME и дренирующего ЛУ после внутриопухолевой инъекции MVA-OVA-4-1BBL
[0314] Количественное определение NK-клеток после в/о иммунизации MVA-OVA показала уменьшение количества NK-клеток в опухоли в день 1 после внутриопухолевой иммунизации (фиг.19, верхний ряд, левая гистограмма). Данные изменения были более выраженными при использовании MVA-OVA-4-1BBL. Одновременно количество NK-клеток в лимфатическом узле, дренирующем опухоль (TdLN), увеличивалось в дни 3 и 7 после иммунизации как MVA-OVA, так и MVA-OVA-4-1BBL (фиг. 19, верхний ряд, правая гистограмма), несмотря на то, что MVA- OVA-4-1BBL индуцировал наибольшее увеличение NK-клеток в TdLN.
[0315] CD69 является маркером ранней активации NK-клеток. Оба вирусных вектора, MVA-OVA и MVA-OVA-4-1BBL, привели к немедленной активации маркера активации CD69 в опухоли, а также в дренирующем лимфатическом узле (TdLN; фиг. 19, второй ряд). Кроме того, в/о иммунизация привела к индукции гранзима B в NK-клетках в различные моменты времени как в опухолях, так и в TdLN, что свидетельствует об усилении цитотоксической функции NK-клеток (фиг. 19, третий ряд).
[0316] Наконец, была проанализирована пролиферативная способность NK-клеток посредством экспрессии Ki67. В день 3 экспрессия Ki67 на NK-клетках была значительно увеличена в опухоли и TdLN мышей, которых внутриопухолево обрабатывали с использованием либо MVA-OVA, либо MVA-OVA-4-1BBL (фиг. 19, последний ряд).
[0317] Данные результаты демонстрируют, что MVA-OVA с адъювантом 4-1BBL (т.е. MVA-OVA-4-1BBL) дополнительно увеличивал экспрессию поверхностных маркеров CD69, гранзима B и Ki67 на NK-клетках после внутриопухолевой инъекции по сравнению с MVA-OVA. Данные эксперименты также показывают значительную роль дренирующих лимфатических узлов (TdLN) в усилении противоопухолевых Т-клеточных и NK-клеточных ответов после внутриопухолевой иммунотерапии.
[0318] Несмотря на то, что настоящее изобретение не связано с каким-либо конкретным механизмом действия, экспансия Т-клеток в TdLN в день 3 и отсроченная инфильтрация Т-клеток в опухоль в день 7 (см. фиг. 17) говорят в пользу сценария, в которых опухолеспецифичные Т-клетки получали первичную вакцинацию и размножаются в TdLN, а затем мигрируют в опухоль для уничтожения опухолевых клеток. Внутриопухолевое введение вирусных векторов также может приводить к активации NK-клеток непосредственно в TdLN, тем самым вызывая дальнейшую активацию ДК.
Пример 28: Роль CD8 Т-клеток во внутриопухолевой терапии рака MVA
[0319] Анализ Т-клеточных ответов в опухоли и TdLN (например, на фиг. 17) показал экспансию опухолеспецифичных Т-клеток в обоих сайтах после внутриопухолевой (в/о) обработки. Были проведены эксперименты для изучения вклада Т-клеток в опосредованные MVA-OVA-4-1BBL противоопухолевые эффекты. В данных экспериментах мышам C57BL/6 вводили клетки меланомы B16.OVA (5×105 клеток) и наблюдали за ростом опухоли после одного из нескольких обработок. Обработки включали внутриопухолевую (в/о) инъекцию ФСБ или MVA-OVA-4-1BBL в присутствии или в отсутствие 100 мкг антител, истощающих CD8-Т-клетки («αCD8», клон 2.43) или антител изотипического контроля. Инъекцию MVA-OVA-4-1BBL выполняли (в/о), когда опухоли достигали 5 мм в диаметре, и повторяли дважды в течение недели. За день до первой инъекции MVA-OVA-4-BBL мышам вводили внутрибрюшинно антитела к CD8 или IgG2b, и данную обработку повторяли четыре раза в течение следующих двух недель. Данные, представленные на фиг. 20, показывают, что Т-клетки CD8 необходимы для эффективной терапии опухолей MVA. Вместе указанные данные показывают, что MVA-индуцированная активация и экспансия опухолеспецифичных Т-лимфоцитов CD8 в опухоли и TdLN являются важными событиями для контроля роста опухоли.
Пример 29: Зависимость от Batf3+ДК противоопухолевых эффектов, опосредованных MVA-OVA и MVA-OVA-4-1BBL
[0320] С целью выяснения лежащих в основе клеточных и молекулярных образований, которые вносят вклад в противоопухолевые иммунные ответы, индуцированные MVA-OVA-4-1BBL, авторы настоящего изобретения исследовали роль различных игроков иммунных клеток. Дендритные клетки (ДК), обладающие способностью эффективно отбирать образцы и представлять антигены и костимулирующие сигналы клеткам адаптивной иммунной системы, считаются критическим фактором противоопухолевого иммунитета. Различные подтипы ДК участвуют в активации мощных иммунных ответов против опухолей, включая CD8α+DC (также известные как «cDC1»). Данная подгруппа ДК обладает уникальной способностью перекрестно представлять антигены во время иммунных ответов, и CD8α+ДК являются основными продуцентами IL-12 в ответ на инфекцию (Hochrein et al. (2001) J. Immunol. 166: 5448-55;  et al. (2014) Eur. J. Immunol. 45: 119-29) и рак (Broz et al. (2014) Cancer Cell 26: 638-52). CD8α+ДК также являются мощными индукторами противоопухолевых CD8+Т-клеток за счет перекрестной представления опухолеассоциированных антигенов (
et al. (2014) Eur. J. Immunol. 45: 119-29) и рак (Broz et al. (2014) Cancer Cell 26: 638-52). CD8α+ДК также являются мощными индукторами противоопухолевых CD8+Т-клеток за счет перекрестной представления опухолеассоциированных антигенов ( et al., (2015) рак Discovery 6: 71-79; Salmon et al. (2016) Immunity 44: 924-38). Развитие CD8α+ДК решающим образом зависит от фактора транскрипции Batf3 (Hildner et al. (2008) Science 322: 1097-1100).
et al., (2015) рак Discovery 6: 71-79; Salmon et al. (2016) Immunity 44: 924-38). Развитие CD8α+ДК решающим образом зависит от фактора транскрипции Batf3 (Hildner et al. (2008) Science 322: 1097-1100).
[0321] Для оценки важности данной подгруппы ДК для внутриопухолевой терапии рака с использованием MVA, использовали мышей с опухолью B16.OVA дикого типа и с дефицитом Batf3 (Batf3 -/-). На фиг. 21A показано, что опухоли B16.OVA росли значительно быстрее в отсутствие перекрестно презентирующих ДК (Batf3 -/-), что указывает на важную роль данной субпопуляции антигенпрезентирующих клеток (APC) в индукции опухолевых иммунных ответов. Как и в предыдущих экспериментах, у мышей дикого типа внутриопухолевая инъекция MVA-OVA приводила к задержке роста опухоли и в одном случае к полному исчезновению опухоли. Данный эффект был улучшен, если мышам вводили MVA-OVA-4-1BBL; у 3 из 5 мышей, получавших MVA-OVA-4-1BBL, опухоль отторгалась (фиг. 21A). Интересно, что в отсутствие кросс-презентирующих ДК (Batf3 -/-) внутриопухолевая иммунотерапия MVA не была нарушена по сравнению с группами WT (фиг. 21A). Тем не менее, Batf3-DC, по-видимому, участвует в индуцированных 4-1BBL противоопухолевых ответах (фиг. 21A, внизу).
[0322] Анализ посредством проточной цитометрии популяций CD8+ T-лимфоцитов в периферической крови через 11 дней после первой иммунизации (фиг. 21B) показал, что OVA-специфичные частоты CD8+ T-клеток были лишь незначительно снижены у носителей Batf3 -/-, иммунизированных MVA-OVA-4-1BBL по сравнению с аналогами дикого типа. Несмотря на то, что настоящее изобретение не связано или не зависит от какого-либо конкретного механизма действия, указанные данные позволяют предположить, что Batf3-зависимые ДК играют излишнюю роль для внутриопухолевой терапии рака с использованием MVA.
Пример 30: Роль NK-клеток при внутриопухолевом введении MVA-OVA-4-1BBL
[0323] Известно, что NK-клетки экспрессируют 4-1BB, и было показано, что лигирование 4-1BB на NK-клетки приводит к повышенной пролиферации и цитотоксичности данных клеток (Muntasell et al. (2017) Curr. Opin. Immunol. 45: 73-81). В более ранних экспериментах (см. фиг. 19) было обнаружено, что внутриопухолевая инъекция MVA-OVA-4-1BBL сильно усиливает активацию маркера CD69, а также маркера цитотоксичности гранзима B на NK-клетках одновременно с усиленной пролиферацией.
[0324] Для изучения роли NK-клеток в 4-1BBL-индуцированном противоопухолевом иммунном ответе, использовали мышей IL15Rα -/- мышей. Альфа-субъединица рецептора IL-15 (IL-15Rα) опосредует высокоаффинное связывание IL-15, плейотропного цитокина, который, как было показано, имеет решающее значение для развития NK-клеток (Lodolce et al. (1998) Immunity 9: 669-76). Получали мышей с опухолью B16.OVA дикого типа и с дефицитом IL15Rα (IL15Rα -/-) и внутриопухолевое иммунизирование либо MVA-OVA, либо MVA-OVA-4-1BBL. Мыши, получавшие MVA-OVA, продемонстрировали аналогичную терапевтическую эффективность независимо от присутствия или отсутствия IL-15Rα (фиг. 22A). Интересно, что преимущества, которые наблюдались у мышей дикого типа при использовании MVA-OVA-4-1BBL (среди которых 3 из 5 мышей отторгали опухоль), были полностью потеряны у мышей с опухолью с дефицитом IL15Rα, получавших MVA-OVA-4-1BBL (в котором у 1 из 5 мышей отторгалась опухоль; см. фиг. 22A). Данные результаты также отразились на выживаемости мышей после инокуляции опухоли (фиг. 22B).
[0325] Известно, что отсутствие IL15Rα не только влияет на развитие NK-клеток, но также снижает гомеостаз Т-клеток и миграцию ЛУ, и выборочно снижает Т-клетки памяти CD8 у мышей (Lodolce et al. (1998) Immunity 9: 669-76). Поэтому также была исследована реакция Т-клеток на данные препараты. В соответствии с предыдущими данными, авторы настоящего изобретения наблюдали индукцию OVA-специфичных CD8 Т-клеток при внутриопухолевой (в/о) иммунизации MVA-OVA у животных дикого типа, которая была дополнительно увеличена с помощью MVA-OVA-4-1BBL (фиг. 22C). Тем не менее OVA-специфичные Т-клеточные ответы у мышей IL15Rα -/- были аналогичны ответам, обнаруженным у мышей дикого типа.
[0326] Несмотря на то, что настоящее изобретение не связано с каким-либо конкретным механизмом или режимом работы, данные результаты показывают, что у мышей с опухолью IL15Rα -/- могут быть вызваны опухолеспецифичные Т-клеточные ответы и, таким образом, подтверждают идею о том, что активация и функция NK-клеток, усиленных 4-1BBL, способствует терапевтической эффективности внутриопухолевого лечения MVA-OVA-4-1BBL.
Пример 31: NK-клеточно-зависимый цитокиновый/хемокиновый профиль в ответ на внутриопухолевую иммунизацию MVA-OVA-4-1BBL
[0327] Для выявления цитокинов, которые избирательно индуцировались взаимодействием 4-1BBL - 4-1BB на NK-клетках, цитокины и хемокины были проанализированы в опухолевой ткани от мышей дикого типа с опухолью B16.OVA или IL15Rα -/-, получавших внутриопухолевое лечение ФСБ или 5×107 TCID50 MVA- OVA или MVA-OVA-4-1BBL.
[0328] Предыдущие эксперименты показали, что большое количество цитокинов и хемокинов увеличивалось через шесть часов после внутриопухолевой инъекции рекомбинантного MVA (фиг. 15 и 16). В данных экспериментах инъекция в опухоли MVA-OVA-4-1BBL показала значительное увеличение по сравнению с инъекцией MVA-OVA для выработки провоспалительных цитокинов или хемокинов, таких как IFN-, CCL3 и CCL5, которые, как известно, продуцируются NK-клетки при стимуляции 4-1BBL (фиг. 23). Данное индуцированное 4-1BBL увеличение было полностью отменено у мышей IL15Rα -/-, демонстрируя, что внутриопухолевая инъекция rMVA-OVA-4-1BBL индуцирует отчетливый профиль цитокинов и хемокинов в микроокружении опухоли через 6 часов после инъекции, что исходит от NK-клеток.
Пример 32: Противоопухолевая эффективность внутриопухолевой иммунизации MVA-gp70-CD40L по сравнению с MVA-gp70-4-1BBL
[0329] Gp70 представляет собой опухолевый аутоантиген, экспрессируемый в ряде моделей сингенных опухолей (B16.F10, CT26, MC38, 4T1, EL4 и т.д.), каждый из которых представляет различные микроокружения опухоли (TME) с точки зрения состава стромы и иммунных клеток. В данном случае была проверена эффективность MVA, кодирующего опухолевый антиген gp70, в дополнение к CD40L или 4-1BBL при внутриопухолевой иммунизации мышей с опухолью B16.F10.
[0330] Клетки меланомы B16.F10 вводили подкожно мышам C57BL/6. Когда опухоли достигли размера ~ 50 мм3, мышей иммунизировали внутриопухолево ФСБ, MVA-gp70, MVA-gp70-4-1BBL, MVA-gp70-CD40L, MVA-4-1BBL или MVA-CD40L; результаты показаны на фиг. 24.
[0331] Иммунизация MVA-gp70 индуцировала временный и умеренный контроль роста опухоли. Данный противоопухолевый эффект может быть усилен, если вирус экспрессирует CD40L. Тем не менее, внутриопухолевая иммунизация MVA-gp70-4-1BBL обеспечивала самые сильные терапевтические эффекты, что привело к полному исчезновению опухоли у 2 из 5 обработанных животных (фиг. 24A).
[0332] Поразительно, что мыши, которые были излечены от опухолей после обработки MVA-gp70-4-1BBL, продемонстрировали потерю пигментации в месте, где находилась опухоль (фиг. 24B). Данная депигментация свидетельствует об аутоиммунном состоянии витилиго и является результатом разрушения меланоцитов самореактивными Т-клетками. Данное разрушение меланоцитов предполагает, что активация иммунной системы рекомбинантным MVA не ограничивается TAA, кодируемой MVA (в данном случае, gp70). Скорее, данная расширенная активация иммунной системы против других антигенов, явление, известное как распространение эпитопа, приводит к более широкому иммунному ответу, который может обеспечить лучший терапевтический результат.
[0333] Для оценки антиген-специфичных Т-клеточных ответов, индуцированных иммунизацией, кровь брали через 11 дней после первой иммунизации и анализировали на наличие антигенспецифичных Т-клеток. Иммунизация с использованием как MVA-gp70, так и MVA-gp70-CD40L, а также MVA-CD40L и MVA-4-1BBL вызвала измеримый p15E-специфичный Т-клеточный ответ, который находился в диапазоне 1-2% (фиг. 24C). Важно отметить, что данный ответ был резко увеличен (> 5 раз) у мышей, получавших MVA-gp70-4-1BBL. Данный антигенспецифичный Т-клеточный ответ на рестимуляцию пептида p15E коррелировал с терапевтической эффективностью в различных группах обработки.
Пример 33: Противоопухолевая эффективность внутриопухолевой иммунизации MVA-gp70-4-1BBL-CD40L.
[0334] Был образован рекомбинантный MVA, экспрессирующий опухолевый антиген gp70 вместе с 4-1BBL и CD40L, и его испытывали внутриопухолево на модели меланомы B16. Клетки меланомы B16.F10 вводили подкожно мышам C57BL/6. Когда опухоли достигли ~ 50 мм3, мышей иммунизировали внутриопухолево с использованием ФСБ, MVA-gp70, MVA-gp70-4-1BBL, MVA-gp70-CD40L, MVA-gp70-4-1BBL-CD40L или соответствующими конструкциями MVA, не экспрессирующими gp70.
[0335] Иммунизация MVA-gp70 индуцировала временный и значительный контроль роста опухоли (фиг. 25A). Данный противоопухолевый эффект может быть усилен, если вирус экспрессирует CD40L или 4-1BBL. Тем не менее, внутриопухолевая иммунизация MVA-gp70-4-1BBL-CD40L привела к сильнейшему терапевтическому эффекту - полному исчезновению опухоли у 4 из 5 обработанных животных (фиг. 25A). Поразительно, что три из четырех излеченных мышей, которых обрабатывали MVA-gp70-4-1BBL-CD40L, продемонстрировали потерю пигментации там, где раньше была опухоль, что свидетельствует об аутоиммунном состоянии витилиго, как обсуждалось выше в примере 32.
[0336] Кроме того, gp70-специфичные Т-клеточные ответы измеряли в крови через 11 дней после первой иммунизации. Иммунизация MVA-gp70 и MVA-gp70-CD40L, а также MVA-CD40L и MVA-4-1BBL вызвала измеримый опухолеспецифичный Т-клеточный ответ, который колебался между 1-2%; данный ответ был резко увеличен (> 5 раз) у мышей, получавших MVA-gp70-4-1BBL (фиг. 25B).
[0337] В целом, в модели меланомы B16.F10 противоопухолевая эффективность может быть увеличена, когда MVA-gp70 адъювантом либо CD40L, либо 4-1BBL, но еще более сильные эффекты наблюдались, если 4-1BBL и CD40L экспрессировались вместе в MVA- gp70-4-1BBL-CD40L.
Пример 34: Внутриопухолевая иммунотерапия MVA-gp70-4-1BBL-CD40L в опухолях CT26.WT
[0338] Затем конструкции испытывали с использованием модели карциномы толстой кишки CT26, которая, как было описано, богата Т-клетками и миелоидными клетками и считается иммуногенной (см., например, Mosely et al. (2016) Cancer Immunol. Res. 5: 29-41). Мышам Balb/c вводили подкожно (п/к) клетки карциномы толстой кишки CT26.wt. Когда опухоль достигала ~ 60 мм3, мышей иммунизировали внутриопухолево с использованием ФСБ, MVA-gp70, MVA-gp70-4-1BBL, MVA-gp70-CD40L, MVA-gp70-4-1BBL-CD40L или MVA-4-1BBL-CD40L.
[0339] Иммунизация MVA-gp70 индуцировала временный и значительный контроль роста опухоли. Данный противоопухолевый эффект не усиливался, если MVA экспрессировал CD40L, но поразительно то, что иммунизация с использованием MVA-gp70-4-1BBL приводила к сильнейшим терапевтическим эффектам, приводящим к полному исчезновению опухоли у всех обработанных животных (фиг. 26A). Тем не менее, обработка с использованием MVA-gp70-4-1BBL-CD40L не привела к лучшей терапевтической эффективности. Следует отметить, что вирусы, которые содержали только костимуляторную молекулу, но не gp70, также приводили к значительной задержке роста опухоли, однако не могли конкурировать с MVA-gp70-4-1BBL. Данные результаты отразились на общей выживаемости обработанных мышей (фиг. 26B).
[0340] Gp70-специфичные Т-клеточные ответы против H2-Ld CD8+Т-клеточного эпитопа AH-1 были легко обнаружены в крови животных, обработанных MVA-gp70 и MVA-gp70-CD40L (фиг. 26C). Данный ответ был резко увеличен (> 10 раз) у мышей, получавших MVA-gp70-4-1BBL, что коррелировало с терапевтической эффективностью, показанной на фиг. 26A и 26B. Обработка с использованием MVA-gp70-4-1BBL-CD40L также усиливала AH-1-специфичные Т-клеточные ответы в крови (фиг. 26C).
Пример 35: Комплексный анализ микросреды опухоли и дренирующего ЛУ опухоли после в/о инъекции MVA-gp70-4-1BBL-CD40L мышам с опухолью B16.F10
[0341] Представленные выше данные показали, что внутриопухолевая обработка мышей с опухолью B16.F10 с помощью MVA-gp70-4-1BBL-CD40L приводило к отторжению опухоли у 80% обработанных мышей (см. фиг. 26). Для изучения микроокружения опухоли (TME) и TdLN в данной модели опухоли мыши с опухолью B16.F10 получали либо ФСБ, либо 5×107 TCID50 MVA-gp70, MVA-gp70-4-1BBL, MVA-gp70-CD40L или MVA-gp70. -4-1BBL-CD40L внутриопухолево (в/о). Мышей умерщвляли через 3 дня после первичной иммунизации. День 3 выбирали на основе предыдущих экспериментов в системе OVA, которые показали изменения как врожденных, так и адаптивных компонентов иммунной системы в этот момент времени (см. фиг. 17). Опухоли и TdLN удаляли и обрабатывали коллагеназой/ДНКазой для анализа отдельных клеток посредством проточной цитометрии. Оценивали численность популяций иммунных клеток, а также их пролиферативное поведение и функциональное состояние.
[0342] Внутриопухолевая инъекция MVA с адъювантом 4-1BBL- и CD40L не обеспечивала преимущества в момент времени дня 3 в количестве CD8 Т-клеток или p15E-специфичных Т-клеток в опухоли, как было определено посредством окрашивания пентамером. Тем не менее в TdLN MVA-gp70 и MVA-gp70-CD40L вызывали экспансию Т-клеток CD8, в то время как добавление 4-1BBL обеспечивало еще больший эффект (фиг. 27, вверху справа). Увеличение, вызванное добавлением 4-1BBL, было еще более выраженным для p15E-специфичных Т-клеток CD8 в TdLN, для которых в/о иммунизация либо MVA-gp70-4-1BBL, либо MVA-gp70-4-1BBL-CD40L увеличивала опухолеспецифичные Т-клетки CD8 (фиг. 27, посередине справа). Количество p15E-специфичных CD8 Т-клеток также коррелировало с пролиферативным состоянием данных клеток; например, добавление 4-1BBL вместе с gp70 и необязательно CD40L к MVA индуцировало наибольшее количество Т-клеток Ki67+gp70-p15E CD8 в TdLN (фиг. 27, внизу справа).
[0343] Указанные данные демонстрируют, что внутриопухолевая (в/о) иммунизация MVA-gp70 усиливает выработку адаптивных иммунных ответов в день 3 после обработки в опухоли и в дренирующем опухоль лимфатическом узле, в то время как адъювантация 4-1BBL или 4-1BBL плюс CD40L специфически увеличивала p15E-специфичные ответы Т-лимфоцитов CD8 в TdLN.
Пример 36: Индукция NK-клеток в опухоли и TdLN после внутриопухолевой инъекции MVA
[0344] Внутриопухолевое (в/о) введение MVA-OVA вызывало активацию и экспансию NK-клеток в день 1 и день 3, соответственно (фиг. 19). Затем была исследована инфильтрация, активация и экспансия NK-клеток в день 3 после инъекции различных конструкций MVA. Количественное определение NK-клеток после в/о иммунизации рекомбинантным MVA показала увеличение количества NK-клеток, инфильтрирующих опухоль (фиг. 28, вверху слева) и TdLN (фиг. 28, вверху справа). Инфильтрация увеличивалась, если MVA кодировал 4-1BBL (например, MVA-gp70-4-1BBL и MVA-gp70-4-1BBL-CD40L). Внутриопухолевая (в/о) инъекция MVA-gp70 индуцировала пролиферацию NK-клеток (Ki67 +) в опухоли (см. фиг. 28, в центре слева) и TdLN (рис. 28, в центре справа), и адъювантацию с 4-1BBL или 4- 1BBL и CD40L усиливали данный эффект в TdLN.
[0345] Гранзим B является маркером цитотоксичности NK-клеток (см., например, Ida et al. (2005) Mod. Rheumatol. 15: 315-22). Гранзим B+NK-клетки индуцировались в опухоли и TdLN после внутриопухолевой инъекции рекомбинантного MVA (фиг. 28, внизу слева). Опять же, добавление 4-1BBL или 4-1BBL-CD40L к рекомбинантному MVA слегка увеличивало количество цитотоксических NK-клеток в TdLN (фиг. 28, внизу справа).
[0346] В целом, указанные данные подчеркивают значительную роль MVA-кодируемого 4-1BBL-CD40L в экспансии и функции NK-клеток и TAA-специфичных Т-клеток после внутриопухолевой (в/о) иммунотерапии. Таким образом, внутриопухолевая обработка рекомбинантным MVA, кодирующим gp70 и 4-1BBL или gp70, 4-1BBL и CD40L, может усиливать Т-клеточные ответы на эндогенный ретровирусный аутоантиген, такой как gp70.
Пример 37: Внутривенная иммунотерапия MVA-gp70-4-1BBL-CD40L у мышей с опухолью CT26.WT
[0347] Обсуждаемые выше эксперименты показали, что новая конструкция MVA, кодирующая опухолевый антиген gp70 вместе с костимулирующими молекулами 4-1BBL и CD40L, была очень сильнодействующей при внутриопухолевом применении (фиг. 25 и 26). Кроме того, в Lauterbach et al. ((2013) Front. Immunol. 4: 251) было обнаружено, что CD40L, кодируемый MVA, усиливает врожденные и адаптивные иммунные ответы при внутривенном введении. В данном случае, авторы настоящего изобретения задавались вопросом, может ли внутривенная (в/в) иммунизация MVA-gp70-4-1BBL-CD40L также обеспечить контроль роста опухоли.
[0348] Клетки карциномы толстой кишки CT26.WT вводили подкожно мышам Balb/c. Когда опухоль достигала ~ 60 мм3, мышей иммунизировали внутривенно ФСБ или MVA-Gp70, MVA-Gp70-4-1BBL, MVA-Gp70-CD40L, MVA-gp70-4-1BBL-CD40L, и MVA-4-1BBL-CD40L (в котором отсутствует gp70). В/в иммунизация MVA-gp70 привела к исчезновению опухоли у 2/5 животных (фиг. 29A). Мыши, которых обрабатывали вирусом, экспрессирующим gp70, либо содержащим 4-1BBL, либо CD40L, показали значительно улучшенный противоопухолевый ответ, что привело к излечению 3/5 и 4/5 мышей, соответственно. Важно отметить, что в/в обработка MVA-gp70-4-1BBL-CD40L привела к длительному контролю роста опухоли у всех обработанных мышей, причем 3/5 мышей отторгали опухоль (фиг. 29A). Следует отметить, что рекомбинантный MVA, который содержал только костимуляторную молекулу, но не gp70, также приводил к значительной задержке роста опухоли, но не приводил к такому же отторжению опухоли, как это наблюдалось с MVA-gp70-4-1BBL, MVA-gp70-CD40L или MVA-gp70-4-1BBL-CD40L (фиг. 29A). Данные результаты отразились на общей выживаемости обработанных мышей (фиг. 29B).
[0349] Анализ опухолево-направленных ответов CD8 Т-клеток в крови путем рестимуляции PBL пептидом выявил значительную индукцию AH1-специфичных CD8 Т-клеток во всех группах обработки MVA, благодаря чему она могла быть дополнительно увеличена в присутствии CD40L (т.е. MVA-gp70-CD40L и MVA-gp70-4-1BBL-CD40L) (фиг. 29C).
Пример 38: рекомбинантный MVA, содержащий антигены HERV-K
[0350] Создан вектор на основе MVA («MVA-mBN489», также называемый «MVA-HERV-Prame-FOLR1-4-1-BBL-CD40L»), содержащий TAA, которые являются белками суперсемейства K эндогенных ретровирусов человека (HERV-K), а именно ERV-K-env и ERV-K-gag. MVA также предназначен для кодирования человеческих FOLR1 и PRAME и для экспрессии h4-1BBL или для экспрессии hCD40L; или экспрессии как h4-1BBL, так и hCD40L.
Пример 39: Внутриопухолевая иммунизация MVA, кодирующим антиген brachyury
[0351] Высокоаттенуированный, нереплицирующийся вирус осповакцины MVA-BN-Brachyury был разработан для включения четырех человеческих трансгенов для индукции специфичного и устойчивого иммунного ответа на различные виды рака. Вектор коэкспрессирует белок TAA человека и три костимулирующие молекулы человека: B7.1 (также известный как CD80), молекулу межклеточной адгезии-1 (ICAM-1, также известную как CD54) и антиген-3, связанный с функцией лейкоцитов (LFA-3, также известный как CD58). Три костимулирующих молекулы (или TRIad of COstimulatory Molecules, TRICOM™) включены для максимального усиления иммунного ответа на человеческом TAA brachyury.
[0352] Brachyury является фактором транскрипции в семействе T-box и является драйвером EMT, процесса, связанного с прогрессированием рака. Он сверхэкспрессируется в раковых клетках по сравнению с нормальной тканью и был связан с устойчивостью раковых клеток к нескольким способам лечения и метастатическим потенциалом. Известно, что виды рака, экспресcирующие brachyury, включают аденокарциному легкого, молочной железы, яичника, хордому, простаты, колоректальную и панкреатическую аденокарциному.
[0353] In vitro и клинические исследования проводили для демонстрации безопасности и потенциальной терапевтической эффективности MVA, кодирующего brachyury; см., например, Hamilton et al. (2013) Oncotarget 4: 1777-90 (“Immunological targeting of tumor cells undergoing an epithelial-mesenchymal transition via a recombinant brachyury-yeast vaccine”); Heery et al. (2015a) J. Immunother. Cancer 3: 132 (“Phase I, dose escalation, clinical trial of MVA-brachyury-TRICOM vaccine demonstrating safety and brachyury-specific T cell responses”); Heery et al. (2015b) Cancer Immunol. Res. 3: 1248-56 (“Phase I trial of a yeast-based therapeutic cancer vaccine (GI-6301) targeting the transcription factor brachyury”)).
[0354] Исследование токсичности повторных доз в соответствии с принципами GLP проводят для оценки любой потенциальной токсичности MVA-BN-Brachyury (MVA-mBN240B) у NHP (яванских макак) в поддержку использования внутривенного пути введения в фазе 1 клинической разработки. Исследование токсичности включает часть биораспределения, оценивающую пространственное и временное распределение MVA-BN-Brachyury в NHP.
[0355] MVA-BN-Brachyury применяют в исследовании III фазы, в котором онкологические пациенты лечат посредством внутриопухолевой инъекции MVA, необязательно в сочетании с другим лечением, таким как, например, облучение и/или ингибиторы контрольных точек.
[0356] Следует понимать, что определенные детали описанных в настоящем изобретении способов и композиций можно варьировать или модифицировать, не отступая от сущности описанного изобретения. Мы заявляем, что все такие модификации и вариации соответствуют сущности и объему приведенной ниже формулы изобретения.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0357] Нуклеотидные и аминокислотные последовательности, перечисленные в приложенном перечне последовательностей, приведены с помощью стандартных буквенных обозначений для нуклеотидных оснований и однобуквенного или трехбуквенного кода для аминокислот по определению 37 C.F.R. 1.822. Приведена только одна цепь каждой последовательности нуклеиновой кислоты, но подразумевается, что комплементарная цепь включена в приведенную цепь любой ссылкой.
Последовательности в перечне последовательностей:
SEQ ID NO:1: аминокислотная последовательность hCD40L из NCBI RefSeq NP_000065.1. (261 аминокислот)
SEQ ID NO:2: hCD40L из NCBI RefSeq NP_000065.1 (792 нуклеотидов)
SEQ ID NO:3: h4-1BBL из NCBI RefSeq NP_003802.1 (254 аминокислот)
SEQ ID NO:4: h4-1BBL из NCBI RefSeq NP_003802.1
SEQ ID NO:1
hCD40L из NCBI RefSeq NP_000065.1. (261 аминокислот)
MIETYNQTSPRSAATGLPISMKIFMYLLTVFLITQMIGSALFAVYLHRRLDKIEDERNLHEDFVFMKTIQRCNTGERSLSLLNCEEIKSQFEGFVKDIMLNKEETKKENSFEMQKGDQNPQIAAHVISEASSKTTSVLQWAEKGYYTMSNNLVTLENGKQLTVKRQGLYYIYAQVTFCSNREASSQAPFIASLCLKSPGRFERILLRAANTHSSAKPCGQQSIHLGGVFELQPGASVFVNVTDPSQVSHGTGFTSFGLLKL
SEQ ID NO:2
hCD40L из NCBI RefSeq NP_000065.1. (792 нуклеотидов)
нт-последовательность:
atgatcgagacatacaaccagacaagccctagaagcgccgccacaggactgcctatcagcatgaagatcttcatgtacctgctgaccgtgttcctgatcacccagatgatcggcagcgccctgtttgccgtgtacctgcacagacggctggacaagatcgaggacgagagaaacctgcacgaggacttcgtgttcatgaagaccatccagcggtgcaacaccggcgagagaagtctgagcctgctgaactgcgaggaaatcaagagccagttcgagggcttcgtgaaggacatcatgctgaacaaagaggaaacgaagaaagagaactccttcgagatgcagaagggcgaccagaatcctcagatcgccgctcacgtgatcagcgaggccagcagcaagacaacaagcgtgctgcagtgggccgagaagggctactacaccatgagcaacaacctggtcaccctggagaacggcaagcagctgacagtgaagcggcagggcctgtactacatctacgcccaagtgaccttctgcagcaacagagaggccagctctcaggctcctttcatcgccagcctgtgcctgaagtctcctggcagattcgagcggattctgctgagagccgccaacacacacagcagcgccaaaccttgtggccagcagtctattcacctcggcggagtgtttgagctgcagcctggcgcaagcgtgttcgtgaatgtgacagaccctagccaggtgtcccacggcaccggctttacatctttcggactgctgaagctgtgatgatag
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Bavarian Nordic A/S
<120> Терапия для лечения рака посредством внутриопухолевого и/или внутривенного введения рекомбинантного MVA, кодирующего 4-1BBL
(CD137) и/или CD40L
<130> BNIT0014PCT
<150> EP 18207238.9
<151> 2018-11-20
<150> US 62/807,720
<151> 2019-02-19
<160> 4
<170> PatentIn версия 3.5
<210> 1
<211> 261
<212> Белок
<213> Homo sapiens
<400> 1
Met Ile Glu Thr Tyr Asn Gln Thr Ser Pro Arg Ser Ala Ala Thr Gly
1 5 10 15
Leu Pro Ile Ser Met Lys Ile Phe Met Tyr Leu Leu Thr Val Phe Leu
20 25 30
Ile Thr Gln Met Ile Gly Ser Ala Leu Phe Ala Val Tyr Leu His Arg
35 40 45
Arg Leu Asp Lys Ile Glu Asp Glu Arg Asn Leu His Glu Asp Phe Val
50 55 60
Phe Met Lys Thr Ile Gln Arg Cys Asn Thr Gly Glu Arg Ser Leu Ser
65 70 75 80
Leu Leu Asn Cys Glu Glu Ile Lys Ser Gln Phe Glu Gly Phe Val Lys
85 90 95
Asp Ile Met Leu Asn Lys Glu Glu Thr Lys Lys Glu Asn Ser Phe Glu
100 105 110
Met Gln Lys Gly Asp Gln Asn Pro Gln Ile Ala Ala His Val Ile Ser
115 120 125
Glu Ala Ser Ser Lys Thr Thr Ser Val Leu Gln Trp Ala Glu Lys Gly
130 135 140
Tyr Tyr Thr Met Ser Asn Asn Leu Val Thr Leu Glu Asn Gly Lys Gln
145 150 155 160
Leu Thr Val Lys Arg Gln Gly Leu Tyr Tyr Ile Tyr Ala Gln Val Thr
165 170 175
Phe Cys Ser Asn Arg Glu Ala Ser Ser Gln Ala Pro Phe Ile Ala Ser
180 185 190
Leu Cys Leu Lys Ser Pro Gly Arg Phe Glu Arg Ile Leu Leu Arg Ala
195 200 205
Ala Asn Thr His Ser Ser Ala Lys Pro Cys Gly Gln Gln Ser Ile His
210 215 220
Leu Gly Gly Val Phe Glu Leu Gln Pro Gly Ala Ser Val Phe Val Asn
225 230 235 240
Val Thr Asp Pro Ser Gln Val Ser His Gly Thr Gly Phe Thr Ser Phe
245 250 255
Gly Leu Leu Lys Leu
260
<210> 2
<211> 792
<212> ДНК
<213> Homo sapiens
<400> 2
atgatcgaga catacaacca gacaagccct agaagcgccg ccacaggact gcctatcagc 60
atgaagatct tcatgtacct gctgaccgtg ttcctgatca cccagatgat cggcagcgcc 120
ctgtttgccg tgtacctgca cagacggctg gacaagatcg aggacgagag aaacctgcac 180
gaggacttcg tgttcatgaa gaccatccag cggtgcaaca ccggcgagag aagtctgagc 240
ctgctgaact gcgaggaaat caagagccag ttcgagggct tcgtgaagga catcatgctg 300
aacaaagagg aaacgaagaa agagaactcc ttcgagatgc agaagggcga ccagaatcct 360
cagatcgccg ctcacgtgat cagcgaggcc agcagcaaga caacaagcgt gctgcagtgg 420
gccgagaagg gctactacac catgagcaac aacctggtca ccctggagaa cggcaagcag 480
ctgacagtga agcggcaggg cctgtactac atctacgccc aagtgacctt ctgcagcaac 540
agagaggcca gctctcaggc tcctttcatc gccagcctgt gcctgaagtc tcctggcaga 600
ttcgagcgga ttctgctgag agccgccaac acacacagca gcgccaaacc ttgtggccag 660
cagtctattc acctcggcgg agtgtttgag ctgcagcctg gcgcaagcgt gttcgtgaat 720
gtgacagacc ctagccaggt gtcccacggc accggcttta catctttcgg actgctgaag 780
ctgtgatgat ag 792
<210> 3
<211> 254
<212> Белок
<213> Homo sapiens
<400> 3
Met Glu Tyr Ala Ser Asp Ala Ser Leu Asp Pro Glu Ala Pro Trp Pro
1 5 10 15
Pro Ala Pro Arg Ala Arg Ala Cys Arg Val Leu Pro Trp Ala Leu Val
20 25 30
Ala Gly Leu Leu Leu Leu Leu Leu Leu Ala Ala Ala Cys Ala Val Phe
35 40 45
Leu Ala Cys Pro Trp Ala Val Ser Gly Ala Arg Ala Ser Pro Gly Ser
50 55 60
Ala Ala Ser Pro Arg Leu Arg Glu Gly Pro Glu Leu Ser Pro Asp Asp
65 70 75 80
Pro Ala Gly Leu Leu Asp Leu Arg Gln Gly Met Phe Ala Gln Leu Val
85 90 95
Ala Gln Asn Val Leu Leu Ile Asp Gly Pro Leu Ser Trp Tyr Ser Asp
100 105 110
Pro Gly Leu Ala Gly Val Ser Leu Thr Gly Gly Leu Ser Tyr Lys Glu
115 120 125
Asp Thr Lys Glu Leu Val Val Ala Lys Ala Gly Val Tyr Tyr Val Phe
130 135 140
Phe Gln Leu Glu Leu Arg Arg Val Val Ala Gly Glu Gly Ser Gly Ser
145 150 155 160
Val Ser Leu Ala Leu His Leu Gln Pro Leu Arg Ser Ala Ala Gly Ala
165 170 175
Ala Ala Leu Ala Leu Thr Val Asp Leu Pro Pro Ala Ser Ser Glu Ala
180 185 190
Arg Asn Ser Ala Phe Gly Phe Gln Gly Arg Leu Leu His Leu Ser Ala
195 200 205
Gly Gln Arg Leu Gly Val His Leu His Thr Glu Ala Arg Ala Arg His
210 215 220
Ala Trp Gln Leu Thr Gln Gly Ala Thr Val Leu Gly Leu Phe Arg Val
225 230 235 240
Thr Pro Glu Ile Pro Ala Gly Leu Pro Ser Pro Arg Ser Glu
245 250
<210> 4
<211> 768
<212> ДНК
<213> Homo sapiens
<400> 4
atggaatacg ccagcgacgc ctctctggac cctgaagctc cttggcctcc agctcctaga 60
gccagggctt gtagagtgct gccttgggct cttgtggctg gacttctgct tctgttgctc 120
ctggctgctg cctgcgcagt gtttcttgct tgtccatggg ctgtgtcagg agccagagca 180
tctcctggat ctgccgcttc tcccagactg agagagggac ctgaactgag ccctgatgat 240
cctgctggac tgctcgacct gagacagggc atgtttgccc agctggtggc ccagaatgtg 300
ctgctgattg atggccctct gagctggtac agcgatcctg gacttgctgg cgttagcctg 360
actggaggcc tgagctacaa ggaggacacc aaagaactgg tggtggccaa ggctggcgtg 420
tactacgtgt tctttcagct ggaactgcgg agagtggtgg caggcgaagg atctggatcc 480
gtgtctctgg cactgcatct gcagcctctg agatctgctg ctggtgcagc tgccctggct 540
ctgacagttg atctgcctcc tgcctccagc gaagccagaa acagcgcctt tggcttccaa 600
ggcagactgc tgcacctgtc tgctggccag agactgggag tgcacctcca cacagaagca 660
agagcaagac acgcctggca gcttacacaa ggcgctacag tgctgggcct gttcagagtg 720
acacctgaga ttccagctgg cttgccatct cctcgcagcg agtaatga 768
<---
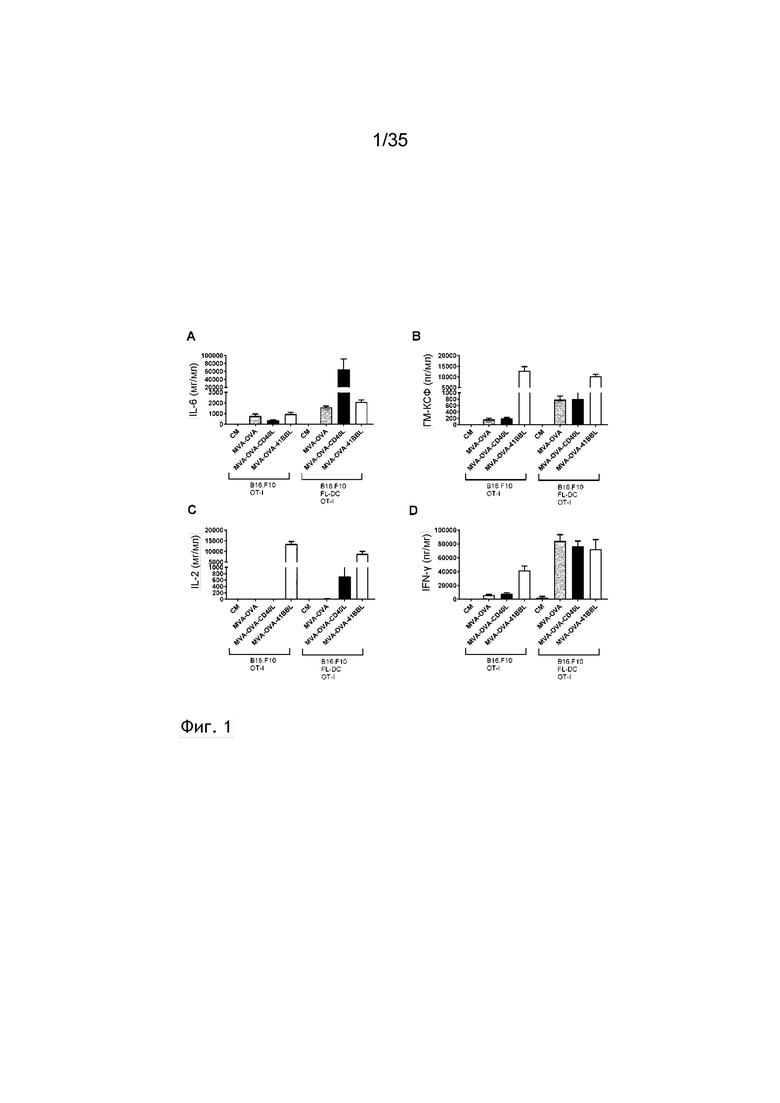
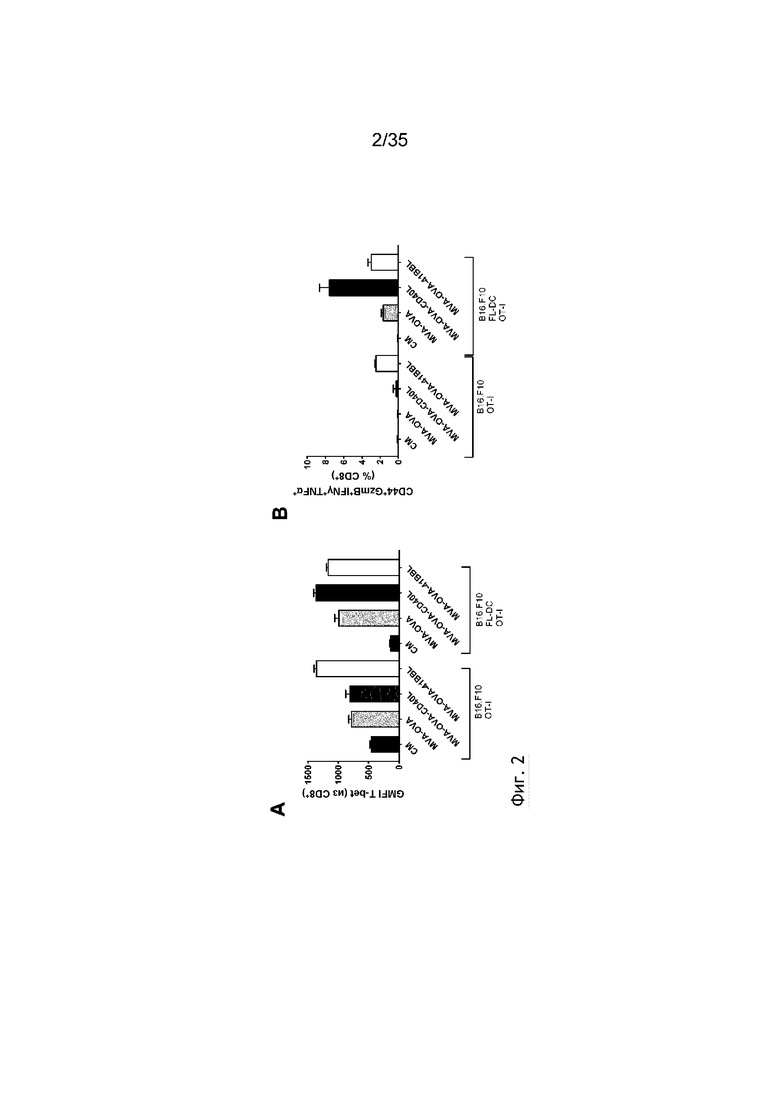
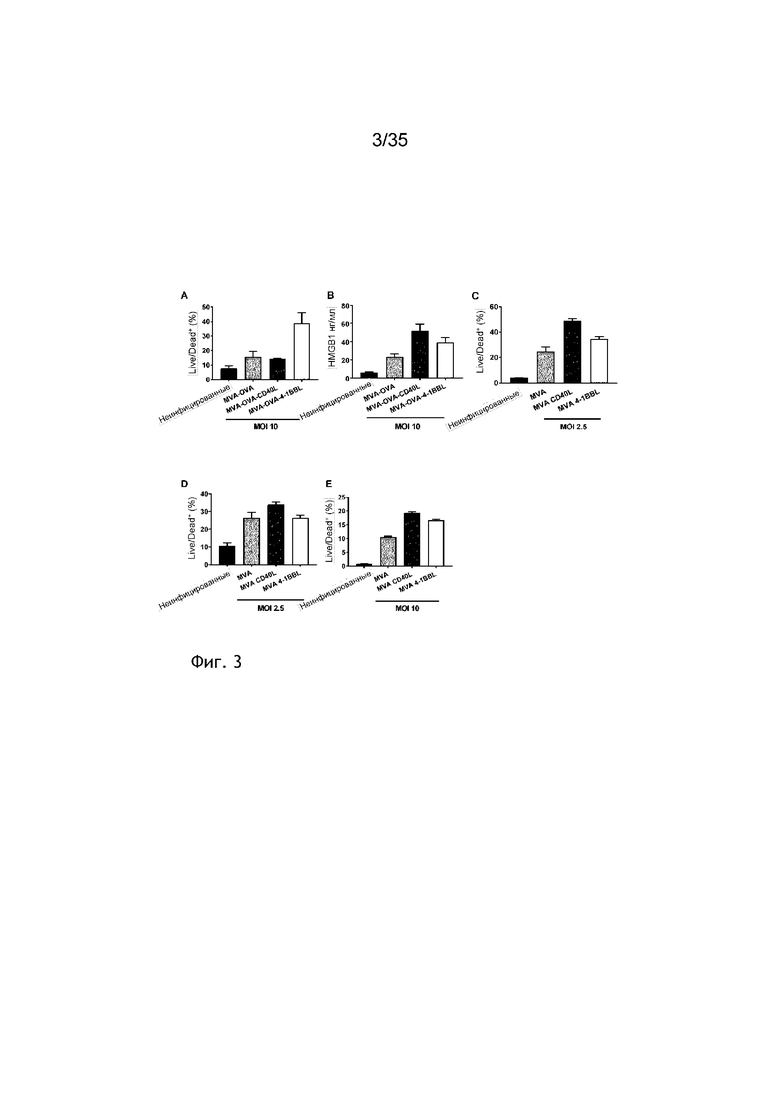
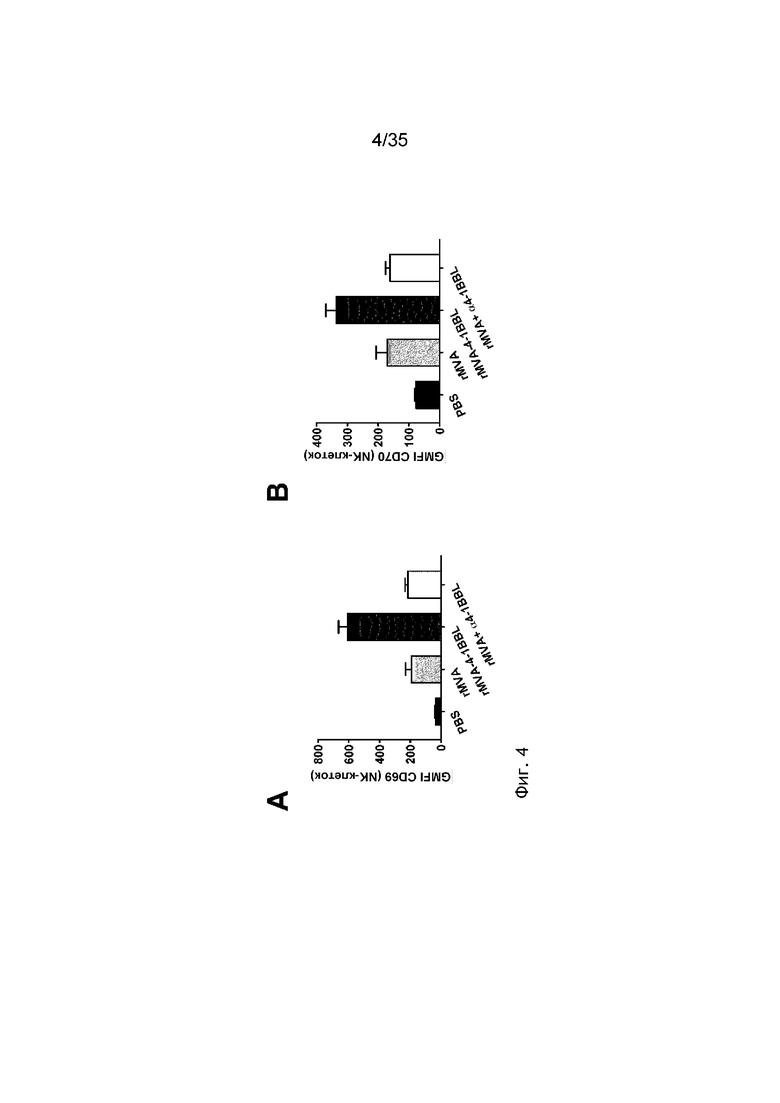
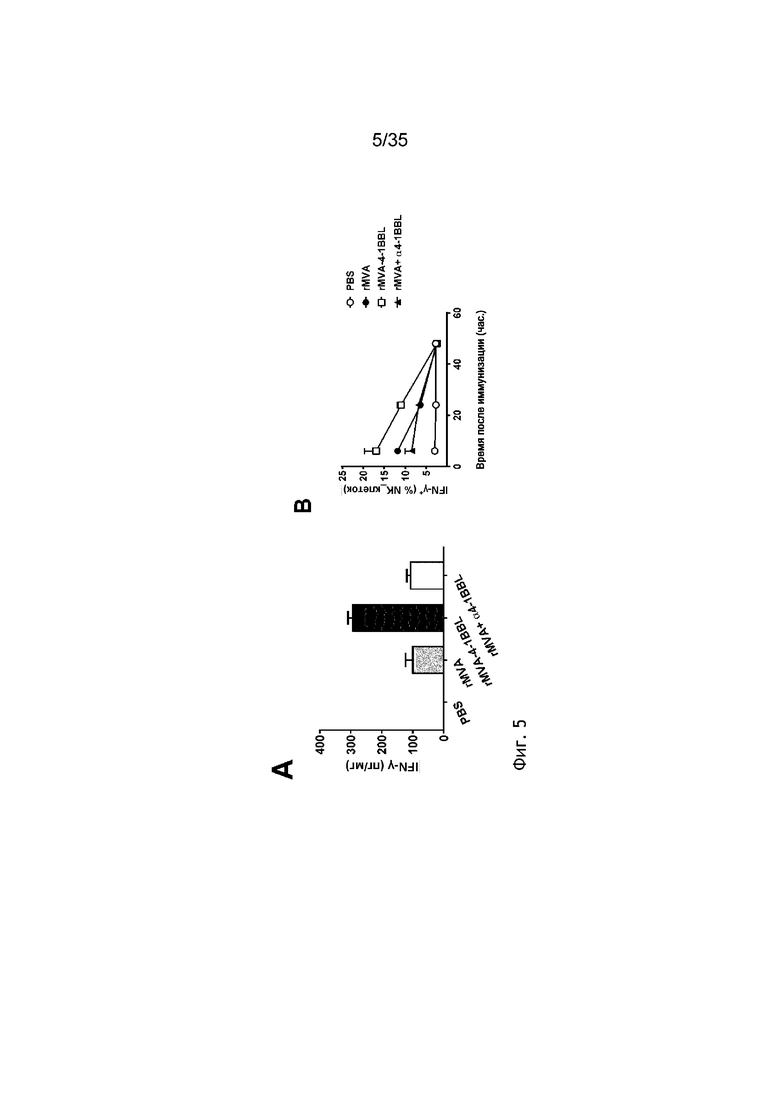
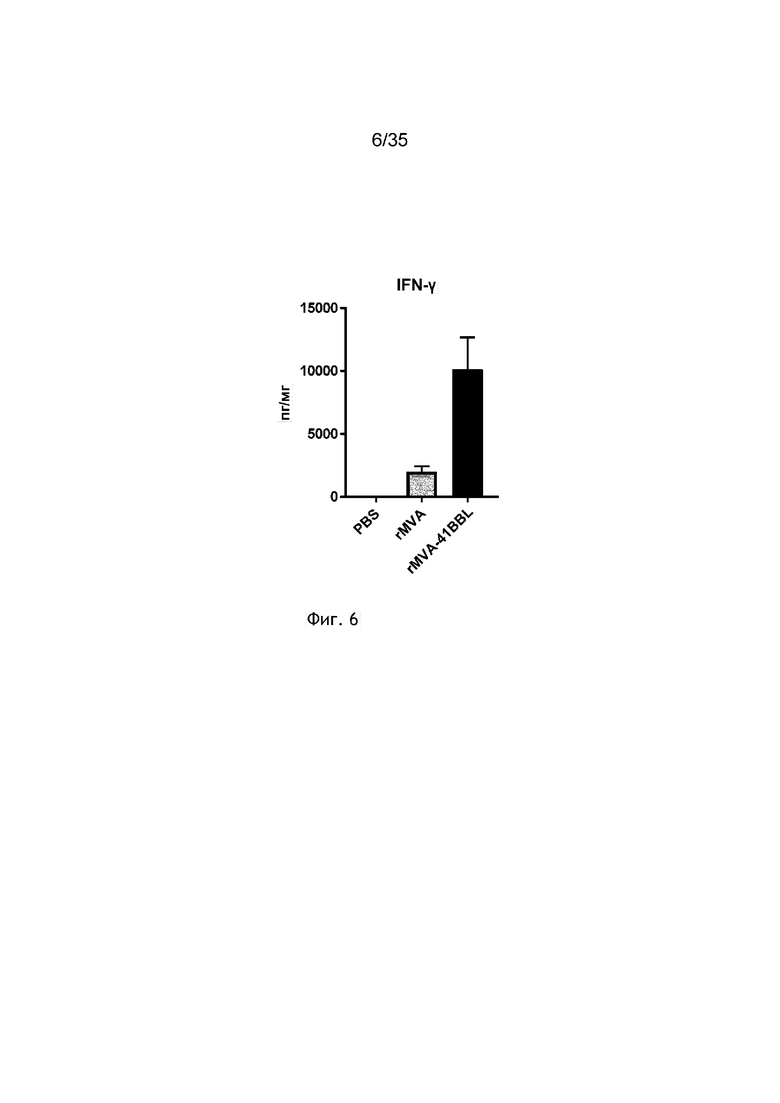


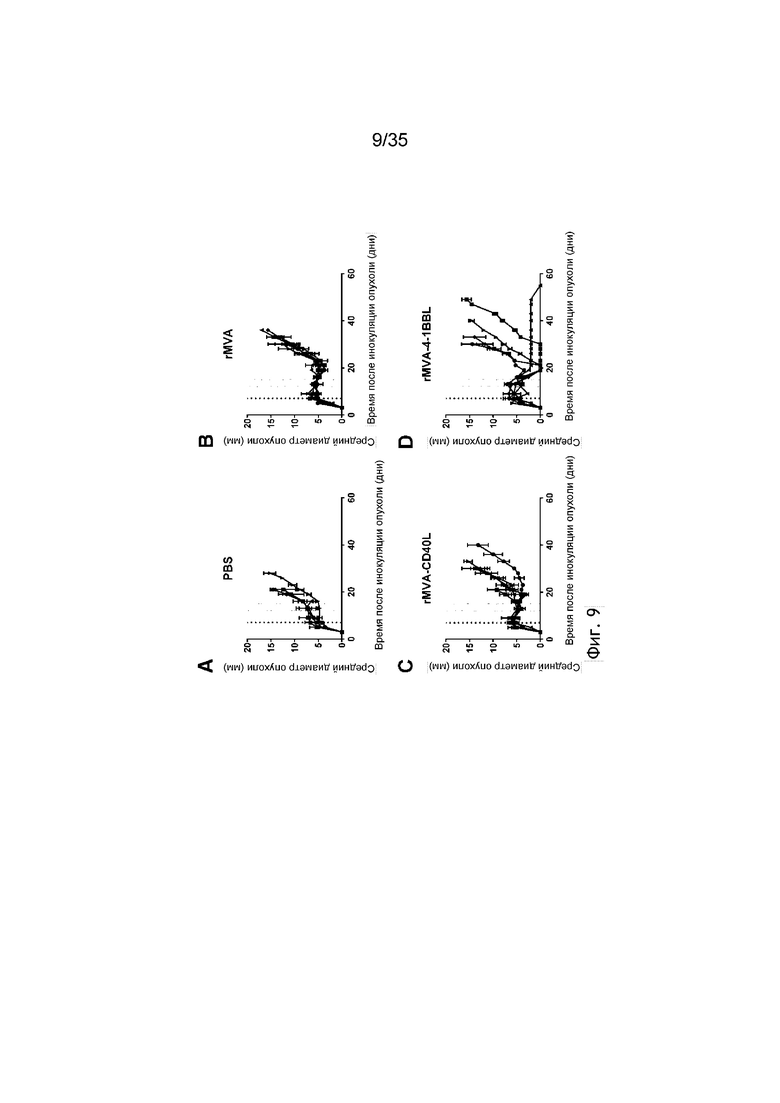
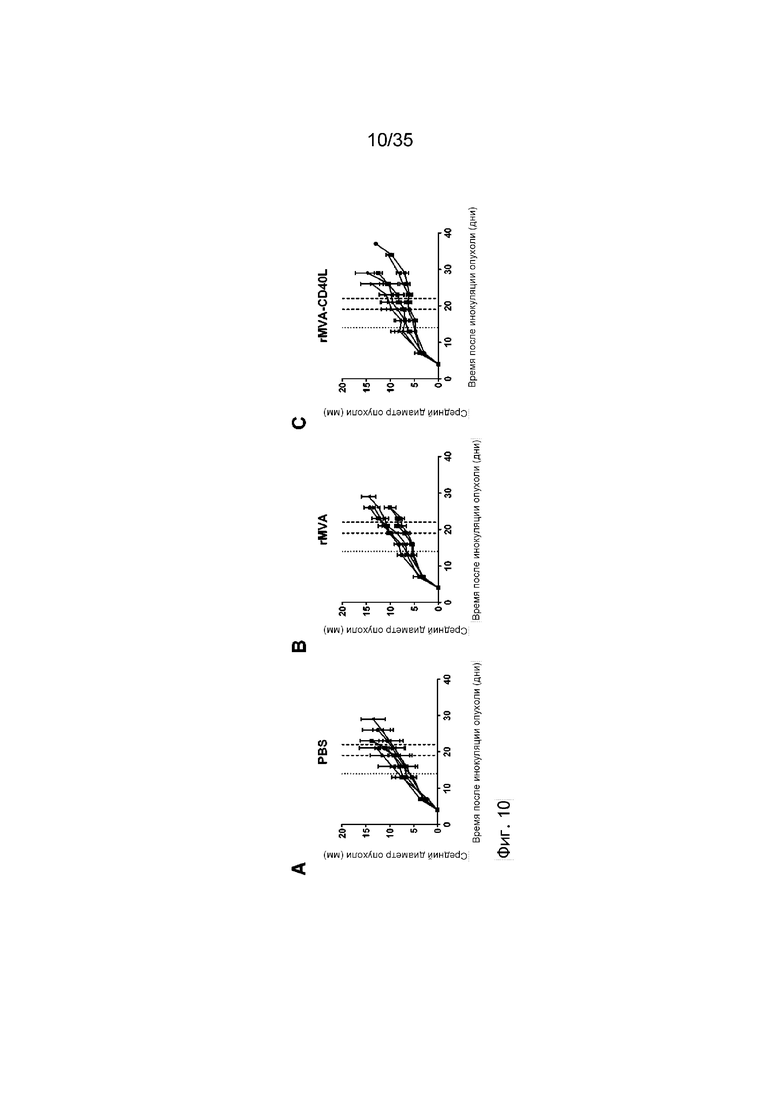
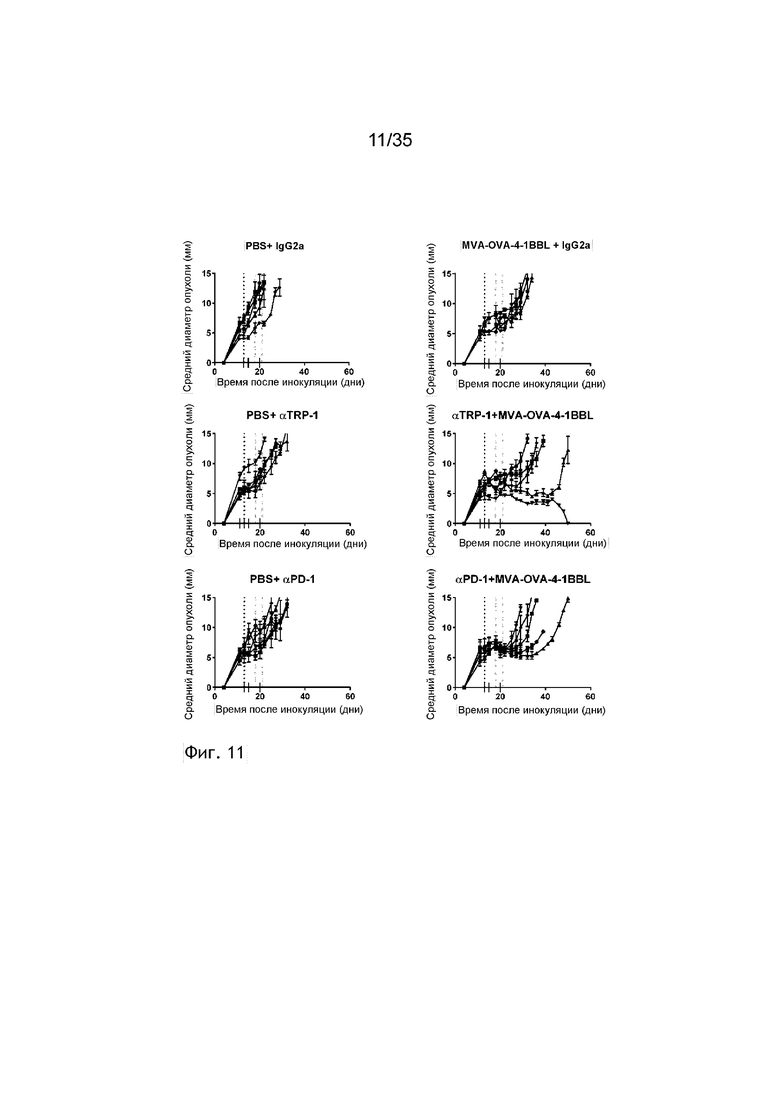
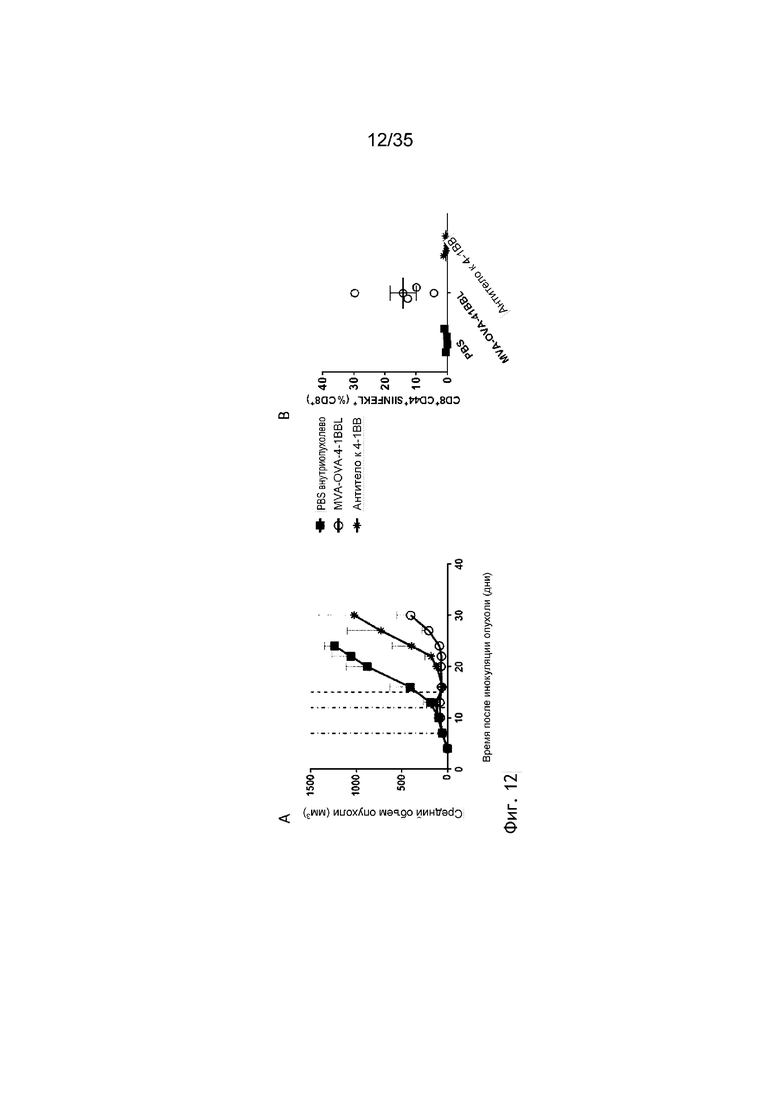
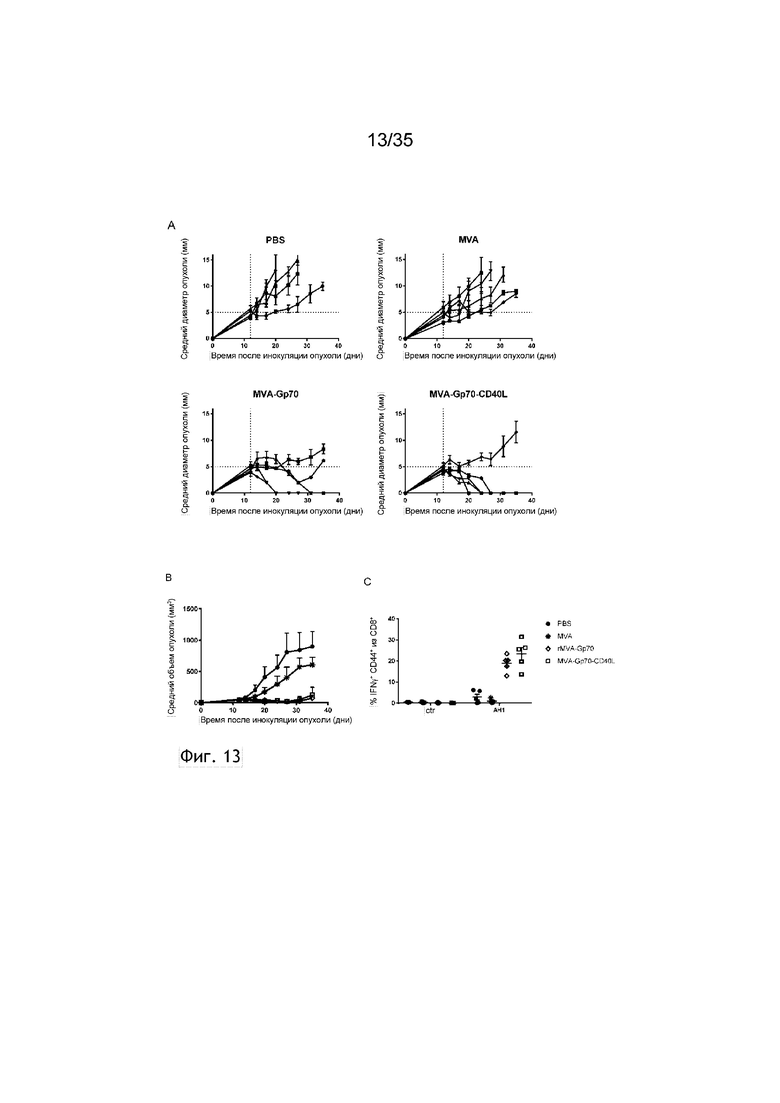
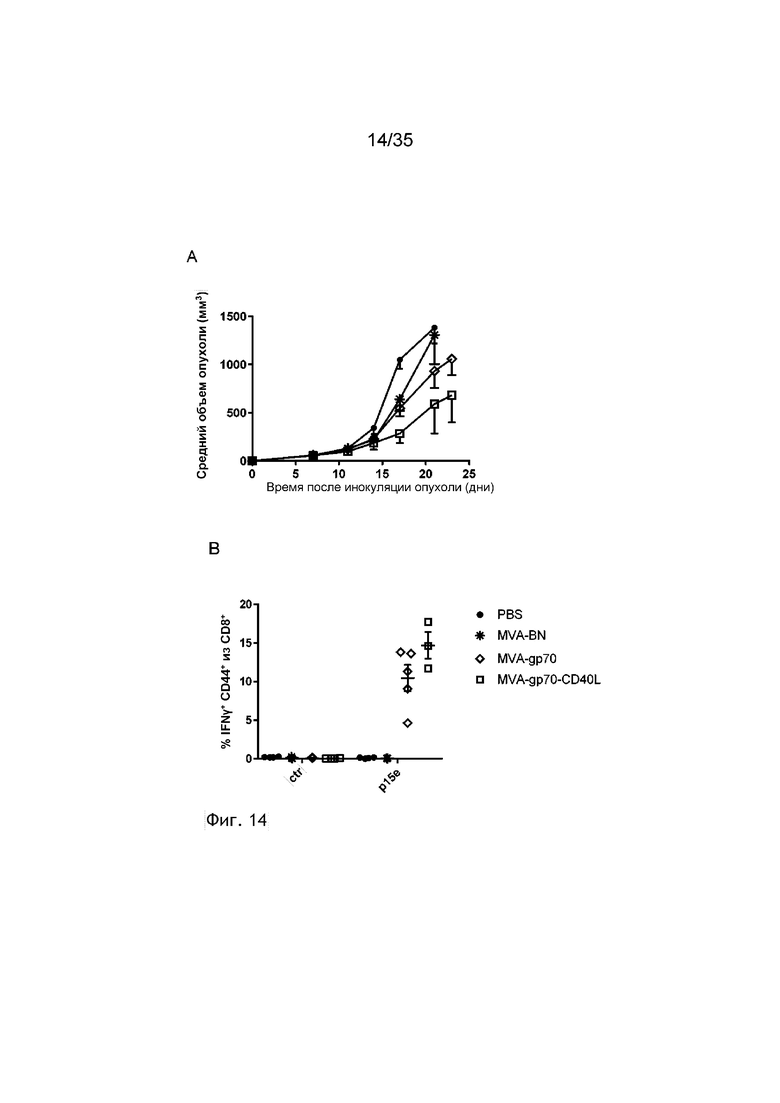
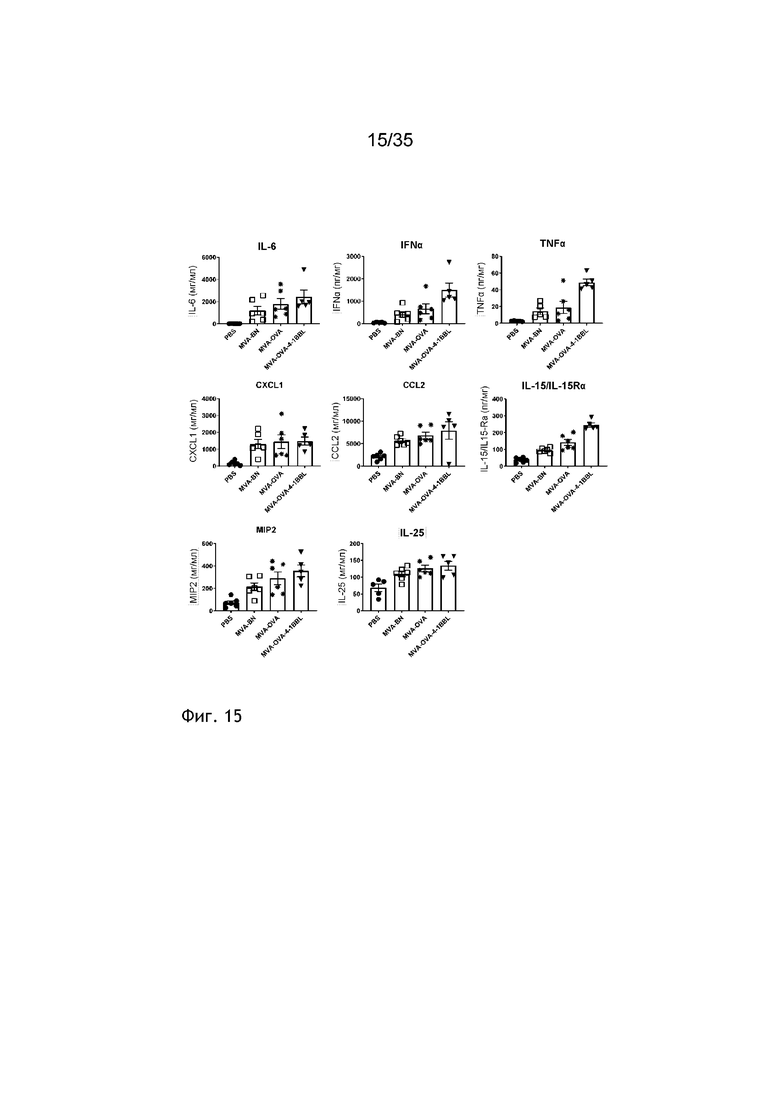
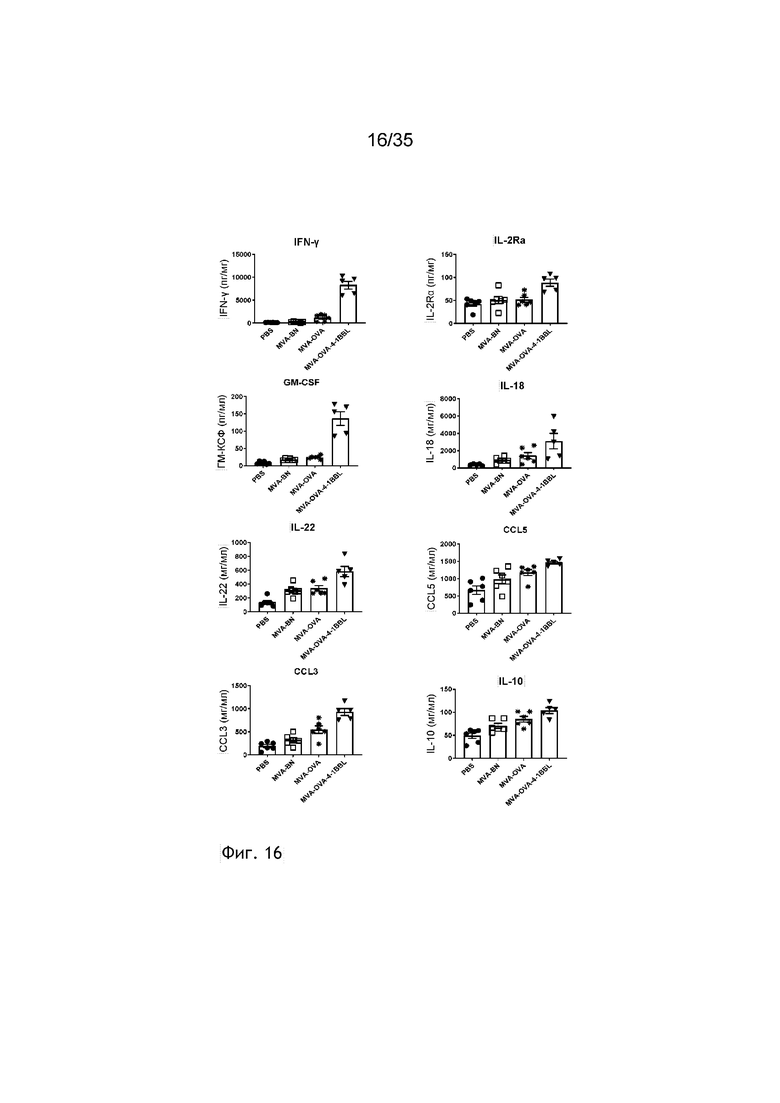
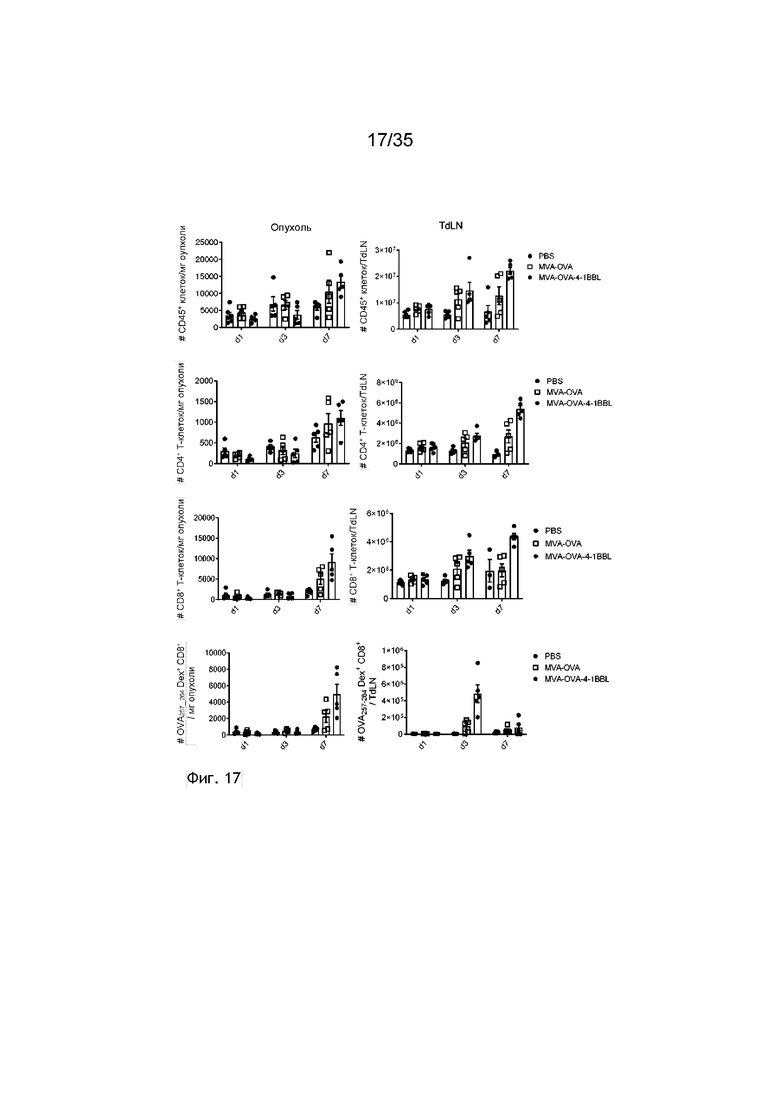
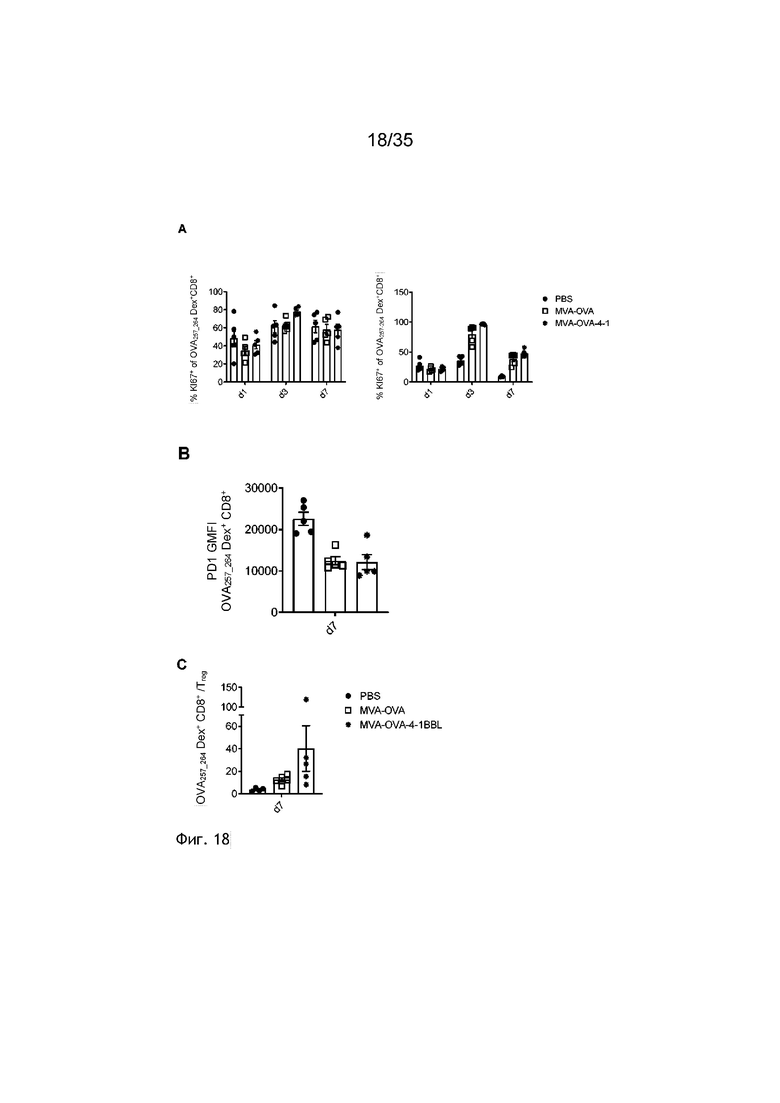

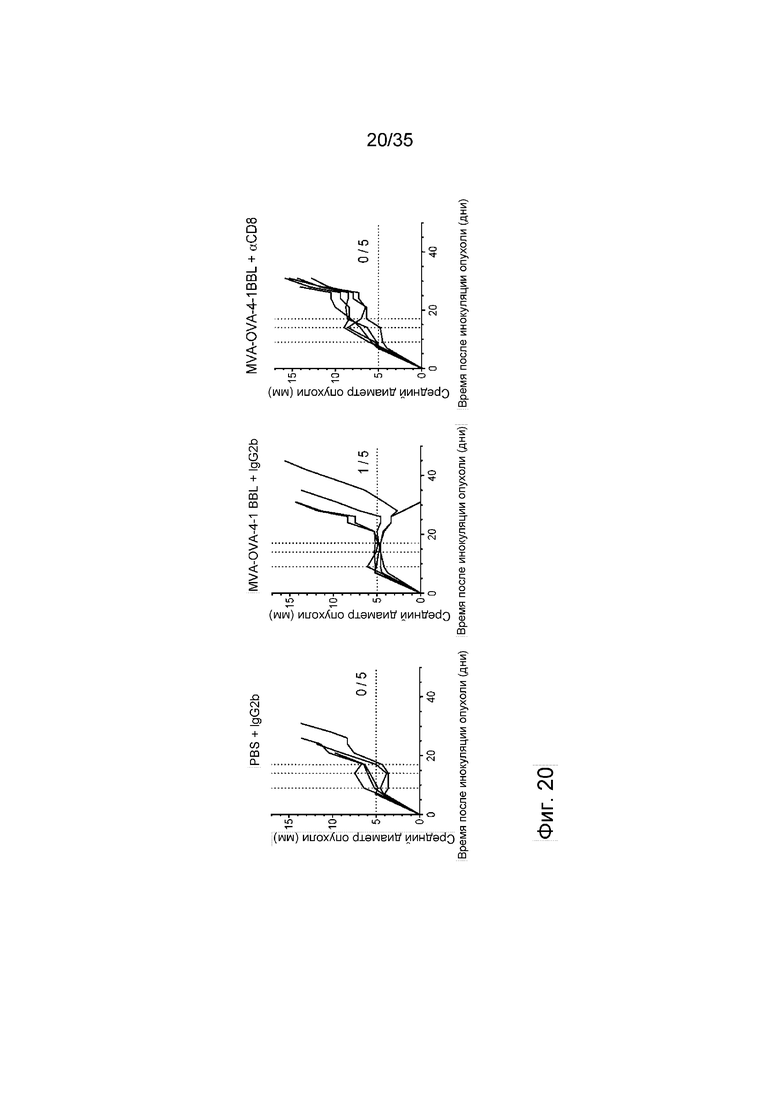
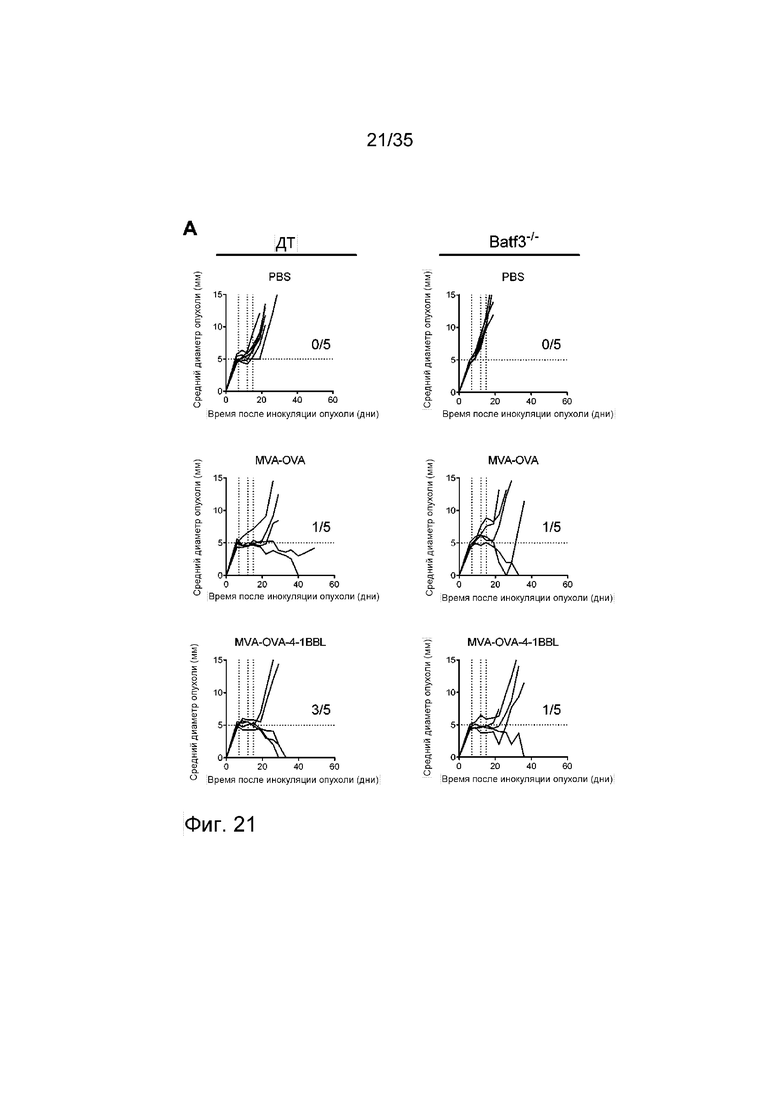
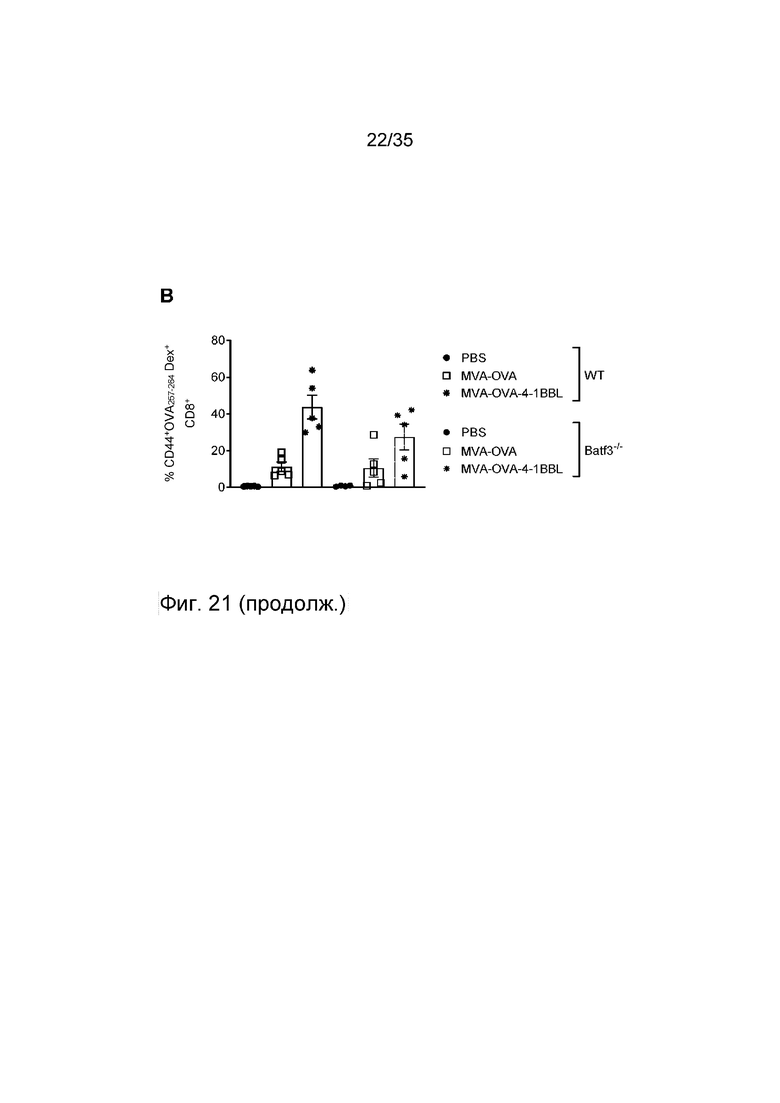
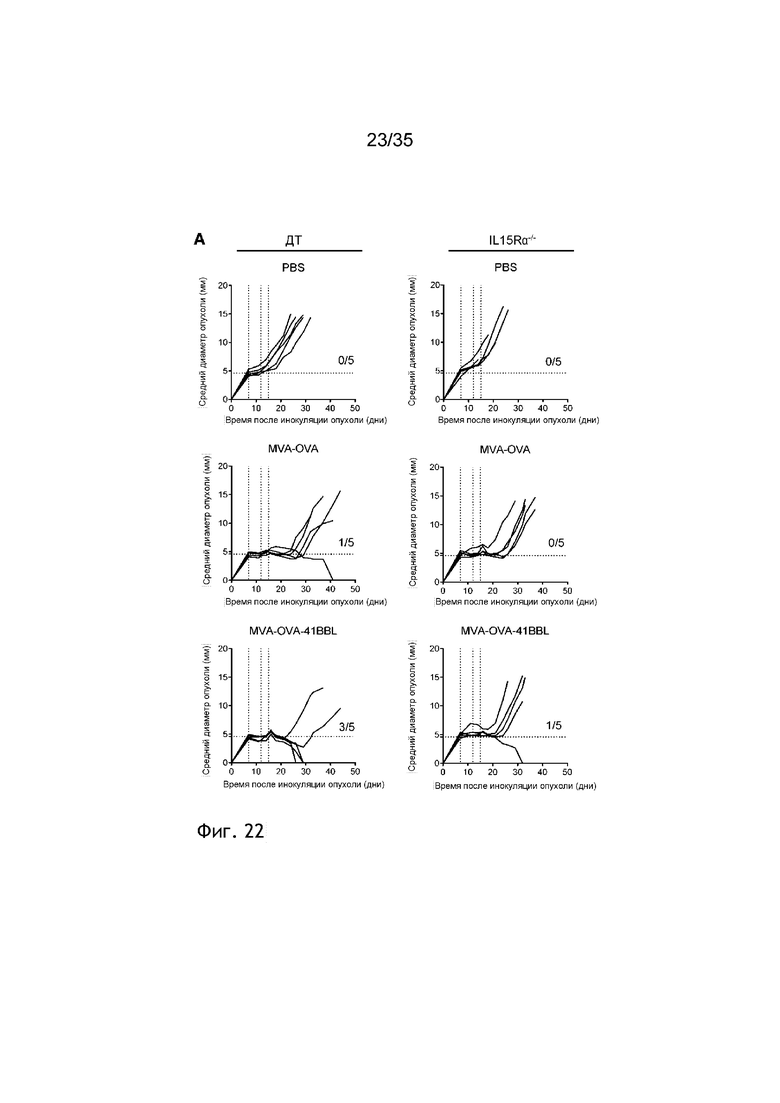
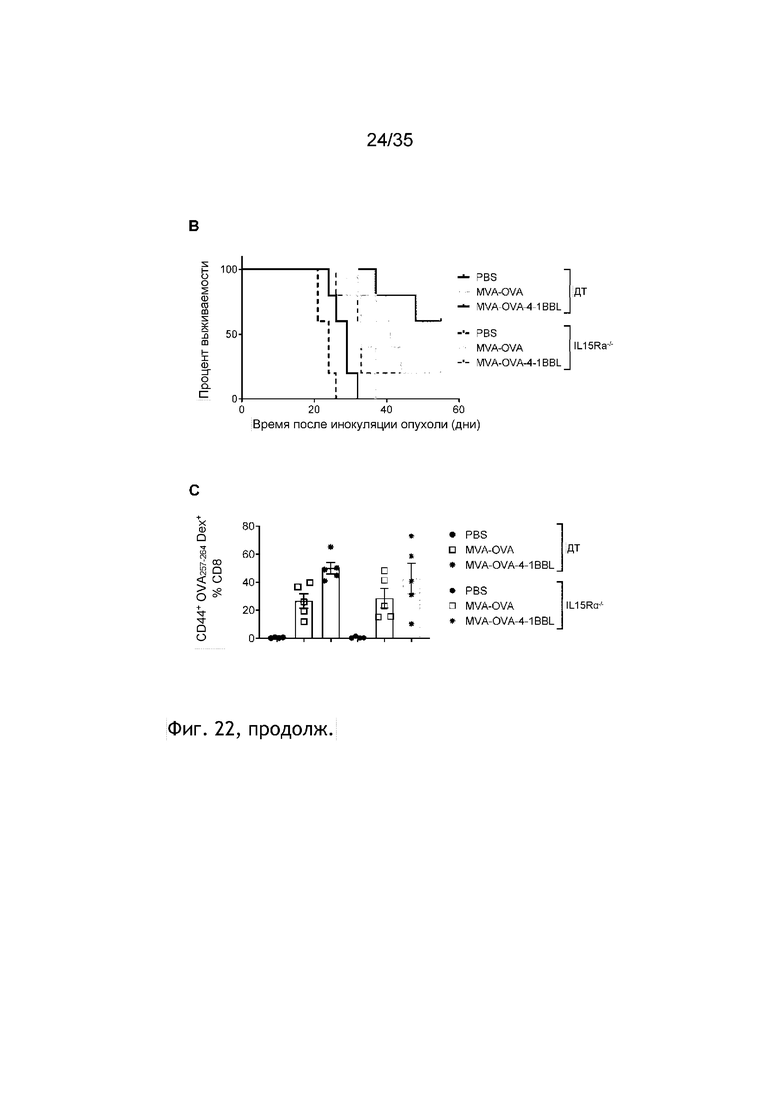
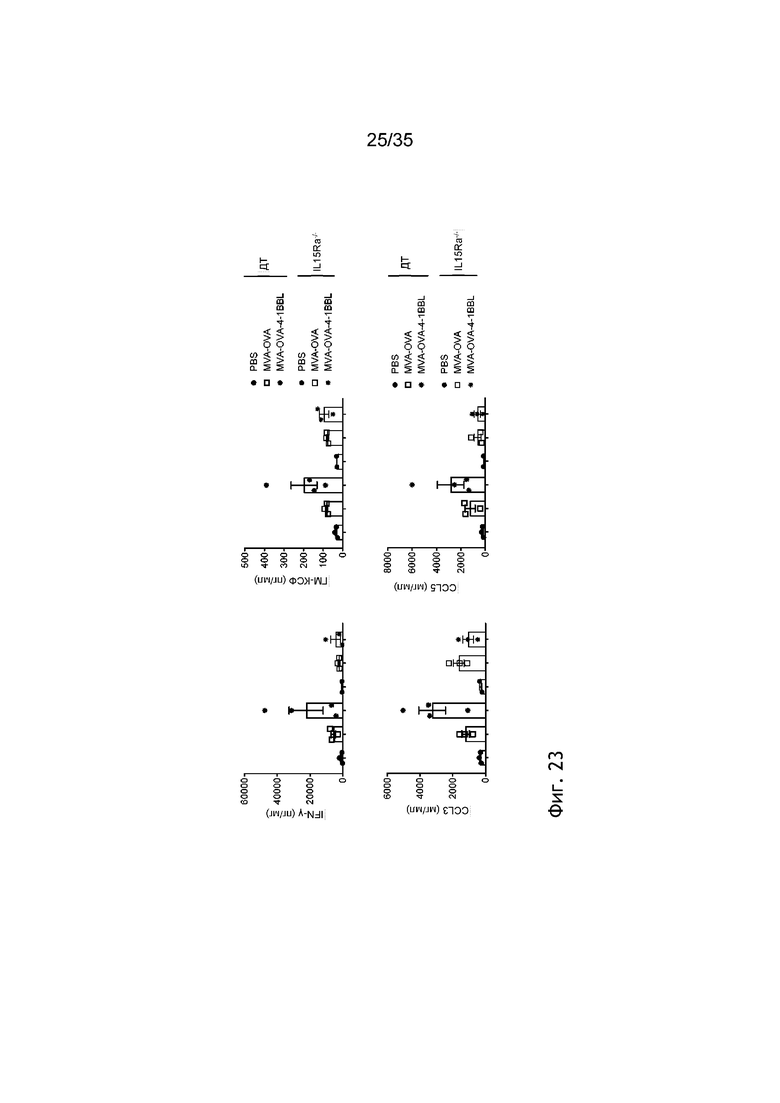


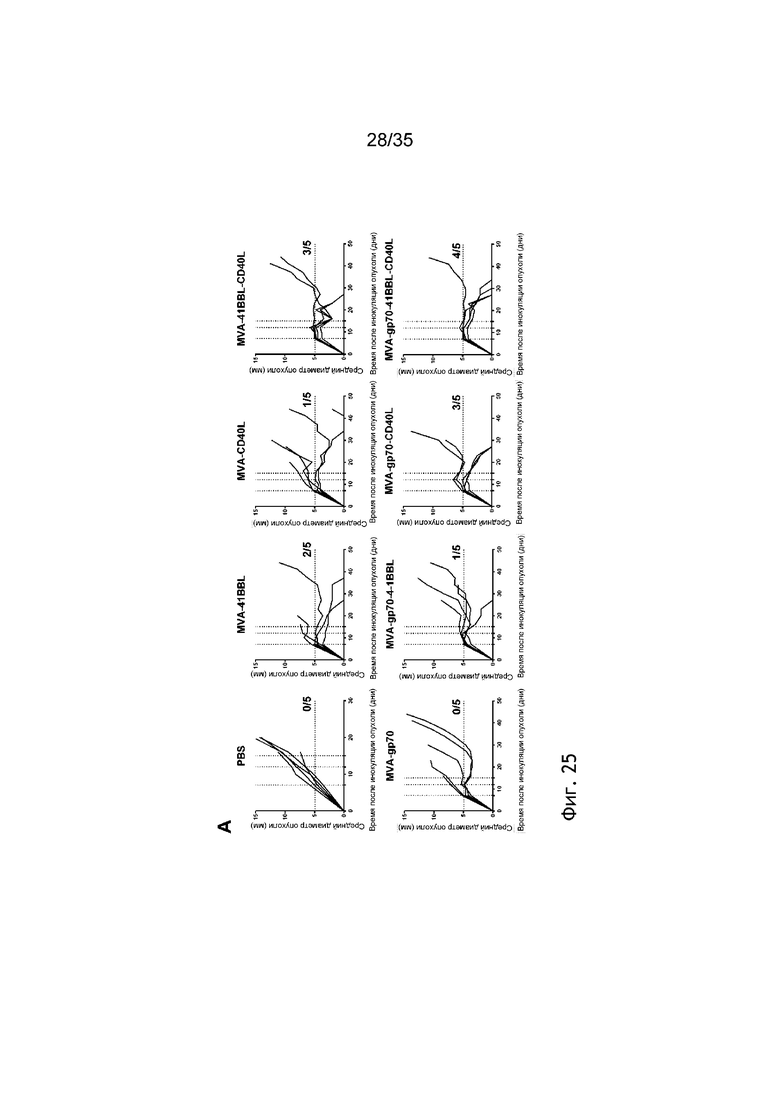

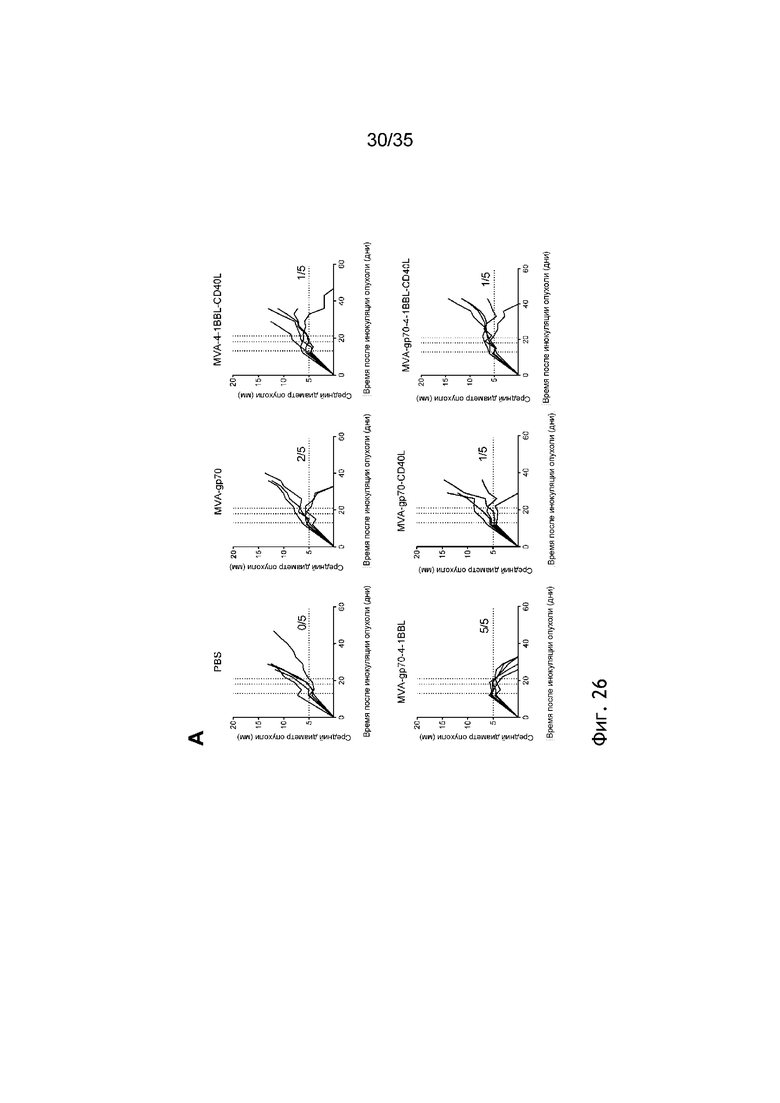
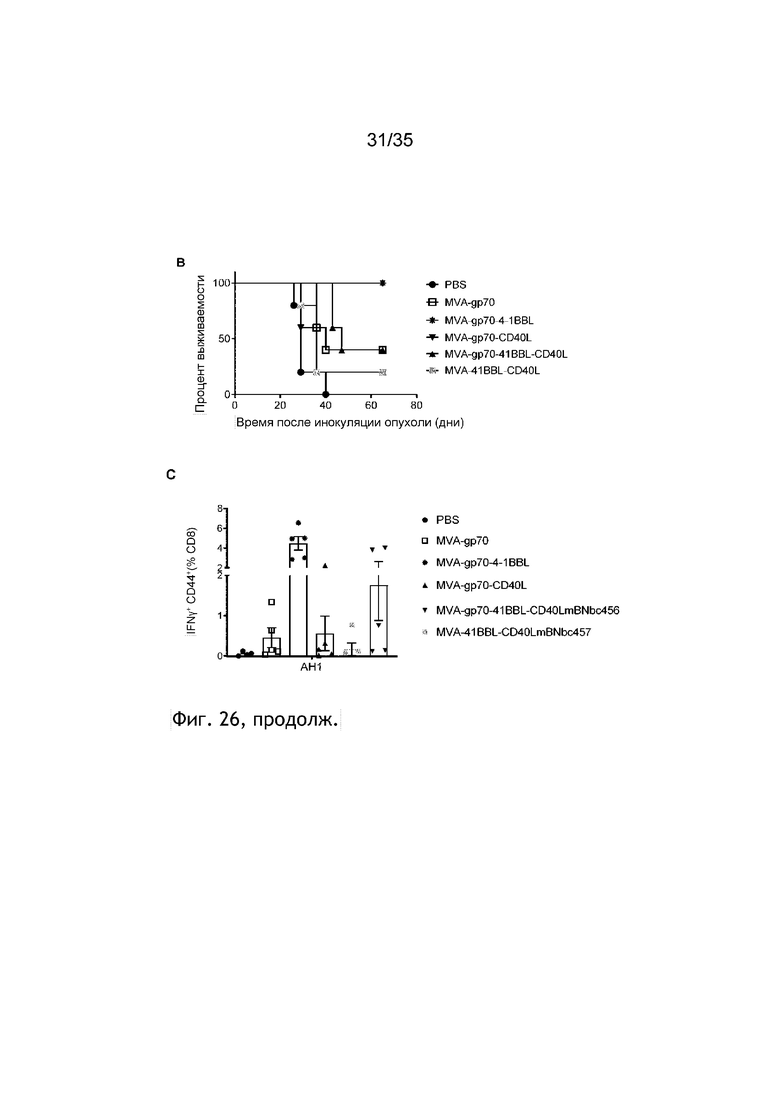
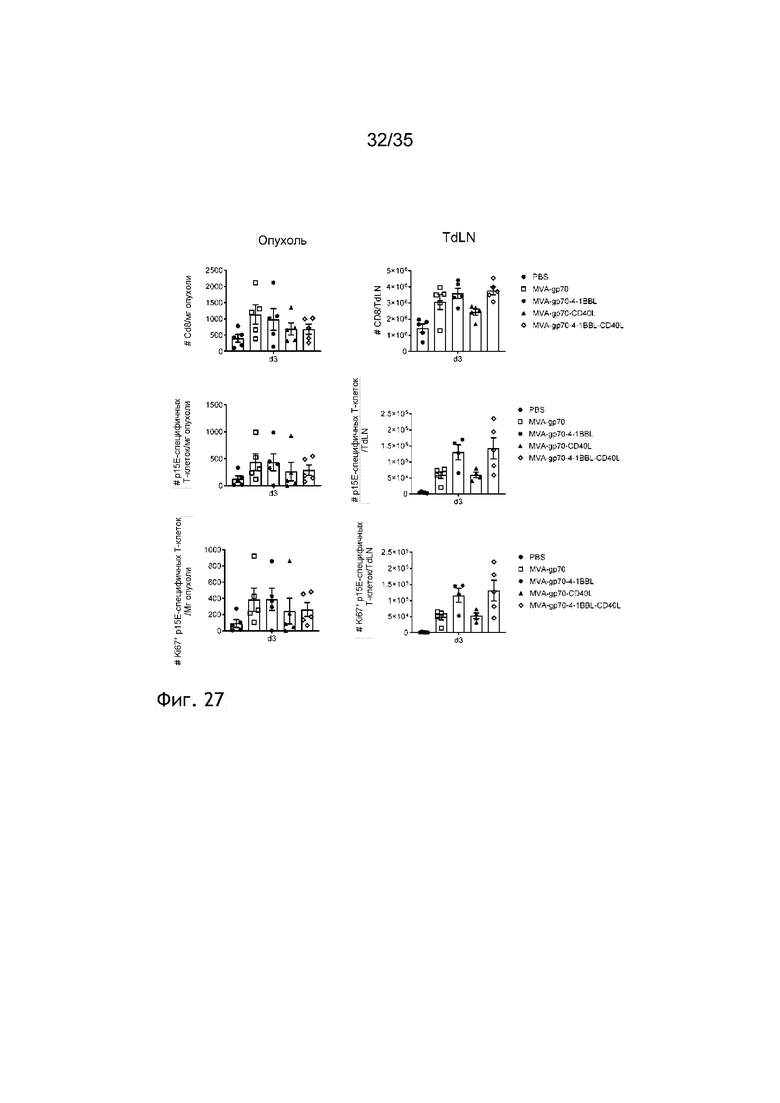
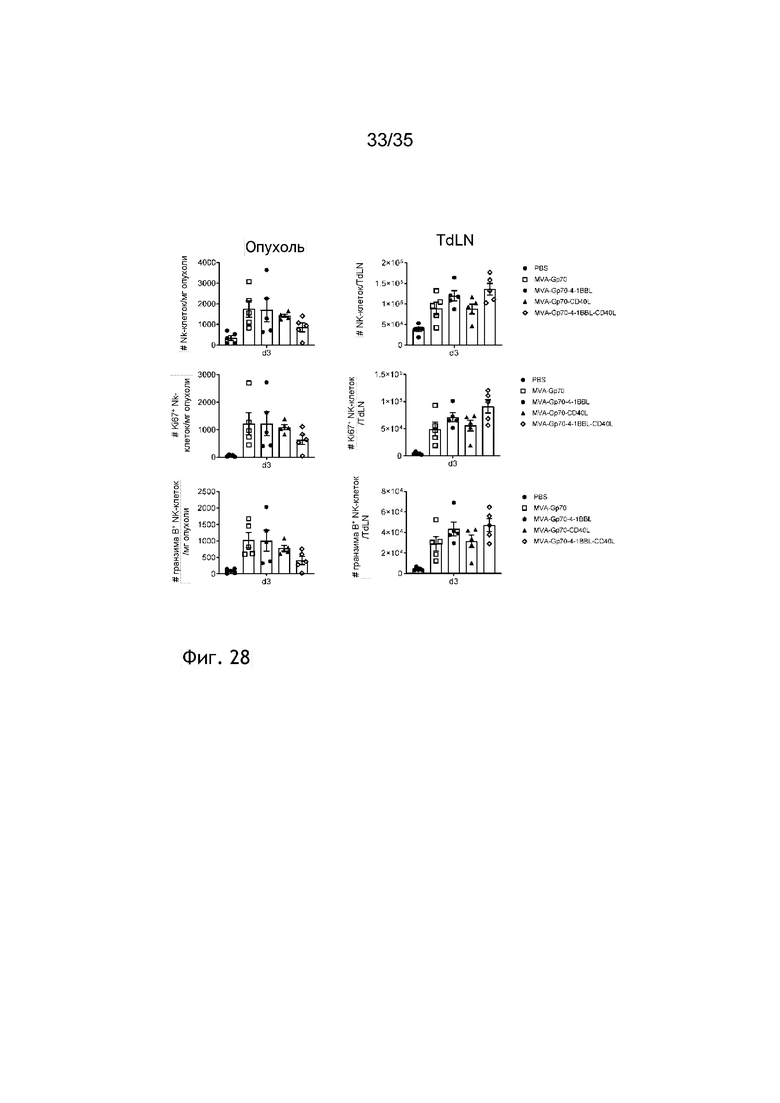
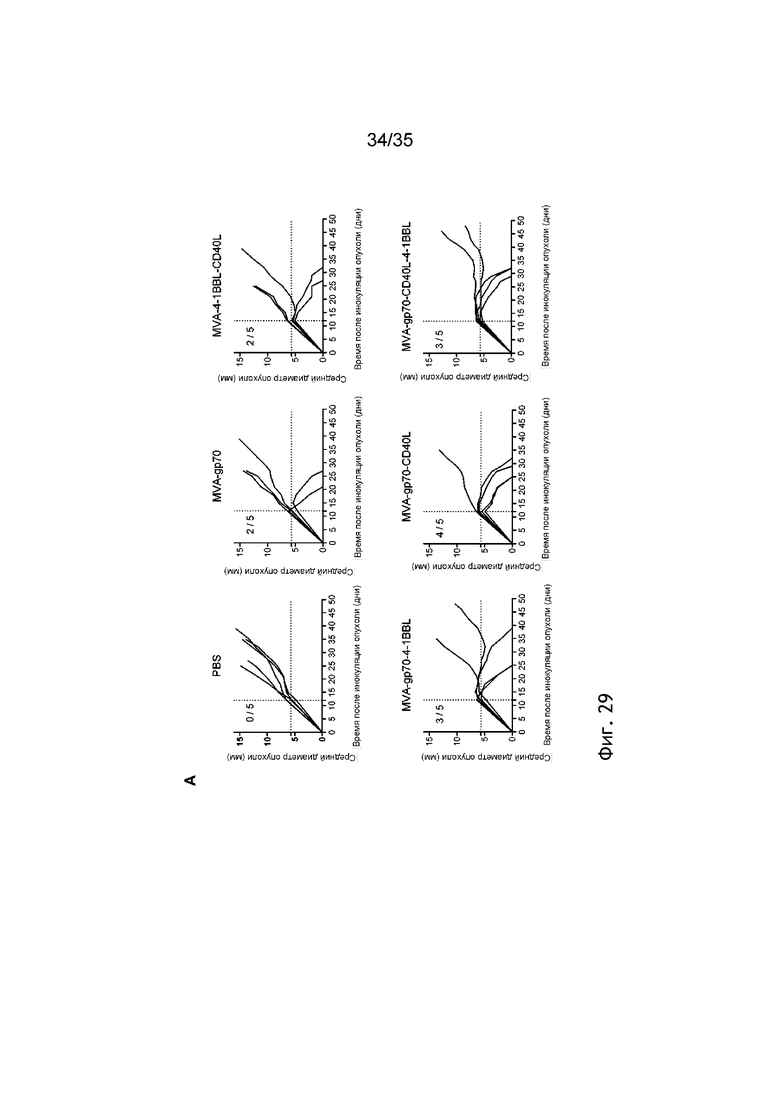
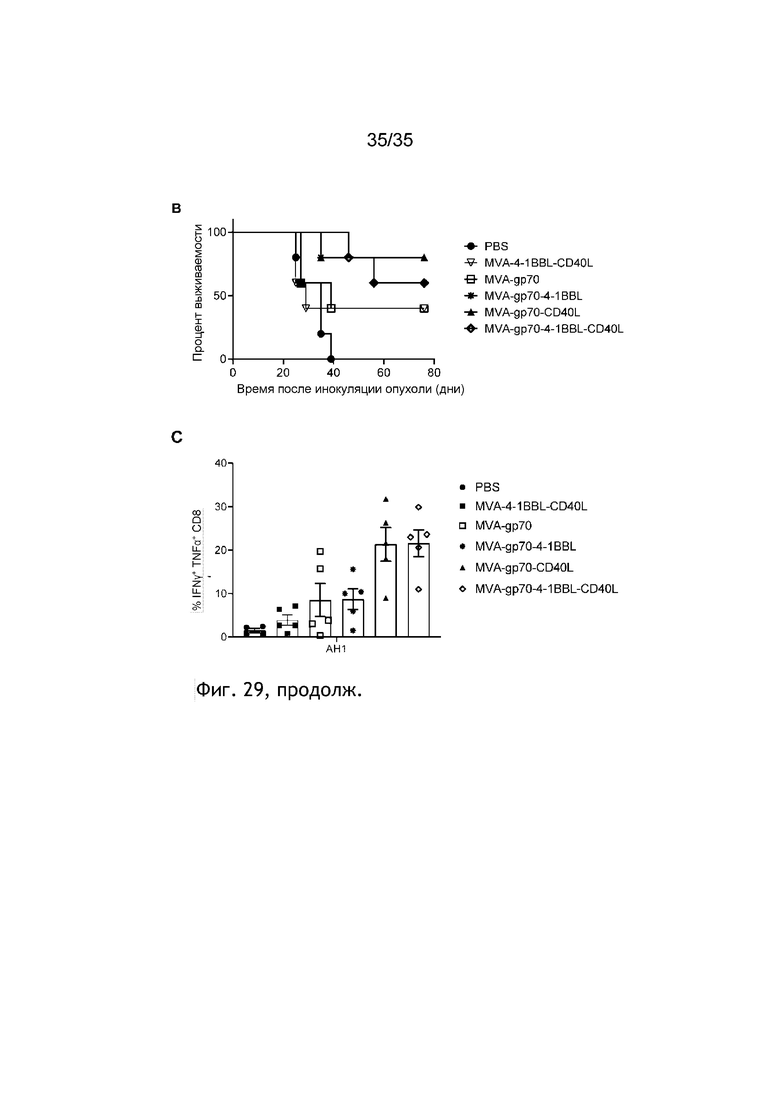
Группа изобретений относится к терапии рака. Предложен способ индукции усиленного воспалительного ответа в раковой опухоли субъекта, включающий внутриопухолевое введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую первый гетерологичный опухолеассоциированный антиген (TAA), вторую нуклеиновую кислоту, кодирующую антиген 4-1BBL, и третью нуклеиновую кислоту, кодирующую антиген CD40L. Также предложена фармацевтическая композиция для индукции усиленного воспалительного ответа в раковой опухоли субъекта и/или уменьшения размера опухоли, содержащая фармацевтически приемлемый носитель и указанный рекомбинантный MVA. Введение рекомбинантного MVA генерирует усиленный воспалительный ответ в опухоли по сравнению с воспалительным ответом, сгенерированным посредством отличной от внутриопухолевой инъекции рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую гетерологичный TAA и антиген 4-1BBL, или по сравнению с воспалительным ответом, сгенерированным введением рекомбинантного MVA, антигена 4-1BBL и антигена CD40L самих по себе. 3 н. и 10 з.п. ф-лы, 29 ил., 39 пр.
1. Способ индукции усиленного воспалительного ответа в раковой опухоли субъекта, включающий внутриопухолевое введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую первый гетерологичный опухолеассоциированный антиген (TAA), вторую нуклеиновую кислоту, кодирующую антиген 4-1BBL, и третью нуклеиновую кислоту, кодирующую антиген CD40L, причем внутриопухолевое введение рекомбинантного MVA генерирует усиленный воспалительный ответ в опухоли по сравнению с воспалительным ответом, сгенерированным посредством отличной от внутриопухолевой инъекции рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую гетерологичный опухолеассоциированный антиген и антиген 4-1BBL.
2. Способ по п.1, в котором субъект является человеком.
3. Способ по п.1, в котором TAA представляет собой эндогенный ретровирусный белок (ERV), экспрессируемый в опухолевой клетке.
4. Способ по п.3, в котором белок ERV происходит из семейства человеческих эндогенных ретровирусов K (HERV-K) и выбран из оболочечного белка HERV-K и белка gag HERV-K.
5. Способ по п.1, в котором TAA выбран из группы, включающей карциноэмбриональный антиген (CEA), ассоциированный с клеточной поверхностью муцин-1 (MUC-1), простатическую кислую фосфатазу (PAP), простатспецифический антиген (PSA), рецептор человеческого эпидермального фактора роста 2-го типа (HER-2), сурвивин, связанный с тирозином белок 1 (TRP1), связанный с тирозином белок 2 (TRP2), Brachyury, PRAME, FOLR1, HERV-K-env, HERV-K-gag, p15, MEL и их комбинации.
6. Способ по п.1, дополнительно включающий введение субъекту по меньшей мере одного антагониста или агониста молекул иммунных контрольных точек CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 или ICOS.
7. Способ по п.1, в котором введение рекомбинантного MVA усиливает ответ естественных клеток-киллеров (NK) и усиливает ответы Т-клеток CD8, специфичных к TAA, по сравнению с невнутриопухолевой инъекцией рекомбинантного вируса MVA, содержащего первую и вторую нуклеиновую кислоту, кодирующую антиген ТАА и 4-1BBL.
8. Фармацевтическая композиция для индукции усиленного воспалительного ответа в раковой опухоли субъекта и/или уменьшения размера опухоли, содержащая фармацевтически приемлемый носитель и рекомбинантный модифицированный вирус осповакцины Анкара (MVA), содержащий a) первую нуклеиновую кислоту, кодирующую опухолеассоциированный антиген (TAA), представляющий собой эндогенный ретровирусный белок (ERV); b) вторую нуклеиновую кислоту, кодирующую 4-1BBL; и с) третью нуклеиновую кислоту, кодирующую антиген CD40L.
9. Фармацевтическая композиция по п.8, где ERV происходит из семейства человеческих ретровирусов K (HERV-K) и выбран из HERV-K-env и HERV-K-gag.
10. Фармацевтическая композиция по п.8, дополнительно содержащая по меньшей мере один антагонист или агонист молекул иммунных контрольных точек, выбранный из антагониста или агониста CTLA-4, PD-1, PD-L1, LAG-3, TIM-3 и ICOS.
11. Способ индукции усиленного воспалительного ответа в раковой опухоли субъекта, включающий внутриопухолевое введение субъекту рекомбинантного модифицированного вируса осповакцины Анкара (MVA), содержащего первую нуклеиновую кислоту, кодирующую первый гетерологичный опухолеассоциированный антиген (TAA), вторую нуклеиновую кислоту, кодирующую антиген 4-1BBL, и третью нуклеиновую кислоту, кодирующую антиген CD40L, причем введение рекомбинантного MVA генерирует усиленный воспалительный ответ в опухоли по сравнению с воспалительным ответом, сгенерированным введением рекомбинантного MVA, антигена 4-1BBL и антигена CD40L самих по себе.
12. Способ по п.11, где TAA представляет собой эндогенный ретровирусный белок (ERV).
13. Способ по п.12, где белок ERV происходит из семейства человеческих ретровирусов K (HERV-K) и выбран из HERV-K-env и HERV-K-gag.
| WO 2014037124 A1, 13.03.2014 | |||
| MATVEEVA, O.V | |||
| Oncolytic Paramyxoviruses: Mechanism of Action, Preclinical and Clinical Studies | |||
| MOLECULAR BIOLOGY | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Устройство для устранения мешающего действия зажигательной электрической системы двигателей внутреннего сгорания на радиоприем | 1922 |
|
SU52A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ приготовления искусственной массы из продуктов конденсации фенолов с альдегидами | 1920 |
|
SU360A1 |
| KRAUS, B | |||
| et al | |||
| Vaccination directed against the human endogenous retrovirus-K envelope protein inhibits tumor growth in a murine model system | |||
| PLOS ONE | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
Авторы
Даты
2024-11-22—Публикация
2019-11-20—Подача