Изобретение относится к области органической химии, к новым биологически активным веществам класса замещенных пиридазин-3(2H)-онов, а именно к N'-(имино(2-((6-(2-метоксифенил)-2-(4-нитробензоил)-3-оксо-2,3-дигидропиридазин-4-ил)амино)-4,5,6,7-тетрагидробензо[b]тиофен-3-ил)метил)-4-нитробензогидразиду формулы:
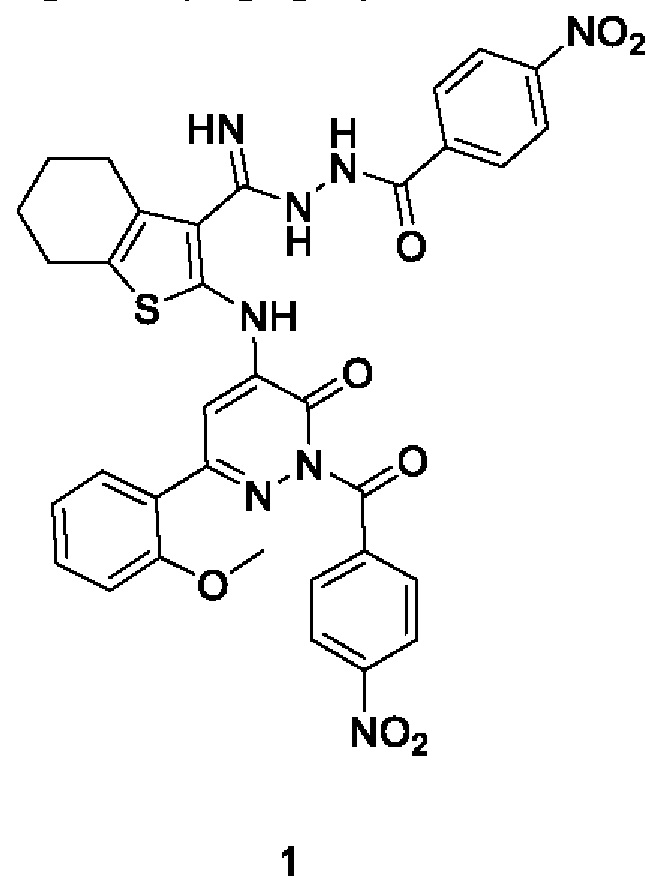
который обладает противовоспалительной активностью, что позволяет предположить его использование в медицине в качестве лекарственного средства с противовоспалительными свойствами и низкой токсичностью.
Аналогом по структуре заявляемому соединению является этиловый эфир 2-[(3-оксо-6-фенил-2-этил-2,3-дигидропиридазин-4-ил)амино]-4,5,6,7-тетрагидробензо[b]тиофен-3-карбоновой кислоты [S.A. Shipilovskikh, А.Е. Rubtsov, Russian Journal of Organic Chemistry, 2014, Vol.50, No. 12, pp.1853-1855, doi: 10.1134/S1070428014120288] формулы:
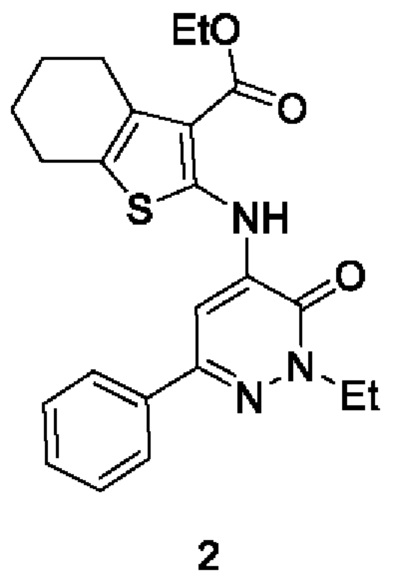
Эталоном сравнения был выбран ортофен формулы:
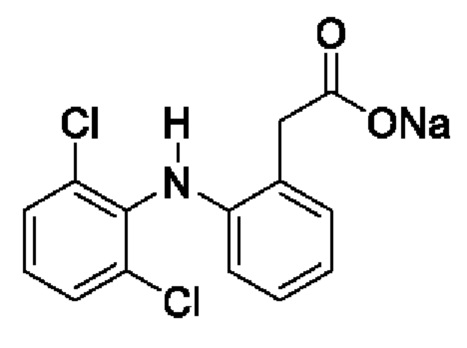
который широко применяется в лечебной практике и является аминопроизводным алифатической кислоты и аналогом по действию [Машковский М.Д. Лекарственные средства. - 15-е изд., перераб., испр. и доп. - М.: ООО «Новая волна», 2005. - с. 170].
Задачей изобретения является поиск веществ в ряду замещенных пиридазин-3(2H)-онов с выраженным противовоспалительным действием и низкой токсичностью.
Поставленная задача достигается получением N'-(имино(2-((6-(2-метоксифенил)-2-(4-нитробензоил)-3-оксо-2,3-дигидропиридазин-4-ил)амино)-4,5,6,7-тетрагидробензо[b]тиофен-3-ил)метил)-4-нитробензогидразида, который обладает противовоспалительной активностью.
Заявляемое соединение 1 синтезируют последовательно в 3 стадии. Первоначально взаимодействием 2-амино-4,5,6,7-тетрагидробензо[b]тиофен-3-карбонитрила 3 с 4-(2-метоксифенил)-2,4-диоксобутановой кислотой 4 в толуоле в присутствии каталитических количеств трифторуксусной кислоты была получена 2-((3-циано-4,5,6,7-тетрагидробензо[b]тиофен-2-ил)амино)-4-(2-метоксифенил)-4-оксобут-2-еновая кислота 5, внутримолекулярной циклизацией которой в присутствии пропионового ангидрида был получен 2-((2-оксо-5-(2-метоксифенил)фуран-3(2H)-илиден)амино)-4,5,6,7-тетрагидробензо[b]тиофен-3-карбонитрил 6. На последней стадии взаимодействием 2-((2-оксо-5-(2-метоксифенил)фуран-3(2H)-илиден)амино)-4,5,6,7-тетрагидробензо[b]тиофен-3-карбонитрила 6 с 4-нитробензогидразидом 7 был получен целевой N'-(имино(2-((6-(2-метоксифенил)-2-(4-нитробензоил)-3-оксо-2,3-дигидропиридазин-4-ил)амино)-4,5,6,7-тетрагидробензо[b]тиофен-3-ил)метил)-4-нитробензогидразид 1. На последней стадии реакция протекает в диоксане при перемешивании и температуре 90°С в течение 1 часа, с последующим удалением растворителя и выделением целевого продукта известными методами по схеме:
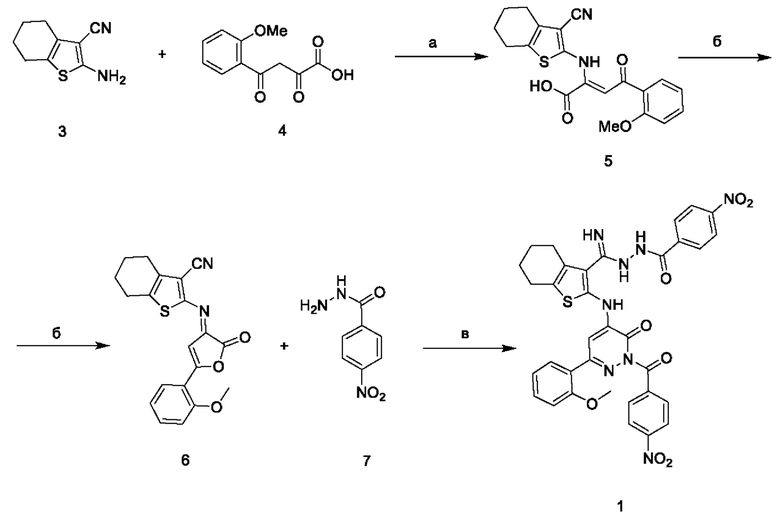
Пример 1. Последовательный многостадийный синтез соединения 1. На первой стадии (условия а) к смеси 356 мг (0,002 моль) 2-амино-4,5,6,7-тетрагидробензо[b]тиофен-3-карбонитрила 3 и 444 мг (0,002 моль) 4-(2-метоксифенил)-2,4-диоксобутановой кислоты 4 прибавляли 10 мл безводного толуола с последующим добавлением 5 мольных % трифторуксусной кислоты. Полученную смесь перемешивали 1 час при температуре 60°С. Затем раствор охлаждали до 0°С, выпавший осадок 2-((3-циано-4,5,6,7-тетрагидробензо[b]тиофен-2-ил)амино)-4-(2-метоксифенил)-4-оксобут-2-еновой кислоты 5 отфильтровывали и сушили 24 часа на воздухе с последующим использованием полученного соединения 5 без дополнительной очистки.
На второй стадии (условия б) полученный осадок 2-((3-циано-4,5,6,7-тетрагидробензо[b]тиофен-2-ил)амино)-4-(2-2-метоксифенил)-4-оксобут-2-еновой кислоты 5 растворяли в 2 мл пропионового ангидрида и перемешивали 2 часа при температуре 120°С. Затем раствор охлаждали до -27°С, выпавший осадок 2-((2-оксо-5-(2-метоксифенил)фуран-3(2H)-илиден)амино)-4,5,6,7-тетрагидробензо[b]тиофен-3-карбонитрила 6 отфильтровывали и сушили 24 часа в вакуумном шкафу при 50°С. Высушенный осадок соединения 6 на следующей стадии использовали без дополнительной очистки.
На последней стадии (условия в) к полученному осадку соединения 6 добавили 7 мл безводного диоксана и 905 мг (0,005 моль) 4-нитробензогидразида, полученную смесь перемешивали в течение 1 часа при температуре 90°С. Раствор охлаждали до 0°С, выпавший осадок отфильтровывали и перекристаллизовывали из этанола.
Выход: 991 мг (70%), оранжевые кристаллы, т.пл. 192-195°С (этанол). Спектр ЯМР 1H (ДМСО-d6), δ, м. д.: 1.71 м (4Н, 2СН2), 2.35 м (2Н, СН2), 2.41 м (2Н, СН2), 3.78 с (3Н, СН3), 6.87 с (1Н, СН), 7.04 м (2Н, Наром), 7.33 м (1Н, Наром), 7.46 м (1H, Наром), 7.76 уш. с. (1H, NH), 8.05 м (2Н, Наром), 8.12 м (2Н, Наром), 8.25 уш. с. (1H, NH), 8.30 м (2Н, Наром), 8.36 м (2Н, Наром), 10.09 уш. с. (1Н, NH), 10.39 уш. с. (1H, NH). Спектр ЯМР 13С (ДМСО-d6), δ, м. д.: 22.3,23.4, 24.0, 24.5,56.3,91.9,112.0, 116.6, 117.4, 120.3, 123.5,124.0, 124.3, 127.6, 128.9, 129.4, 129.8, 131.6, 138.5, 139.5, 141.1, 149.4, 150.0, 156.1, 160.6, 163.2, 164.4, 164.67. Найдено, %: С 57.65; Н 3.96; N 15.82; S 4.51. C34H28N8O8S. Вычислено, %: С 57.62; Н 3.98; N 15.81; S 4.52.
Полученное соединение 1 представляет собой оранжевое кристаллическое вещество, растворимое в ДМСО, ацетоне, не растворимое в воде и гексане.
Пример 2. Острую токсичность (ЛД50, мг/мл) соединения 1 определяли по методу Г.Н. Першина [Першин Г.Н. Методы экспериментальной химиотерапии // М., С.100, 109-117 (1971)]. Соединение 1 вводили внутрибрюшинно белым мышам массой 16-18 г в виде взвеси в 2% крахмальной слизи и наблюдали за поведением и гибелью животных в течение 10 суток. Для исследуемого соединения 1 ЛД50 составляет >1500 мг/кг.
Согласно классификации токсичности препаратов соединение 1 относится к V классу практически нетоксичных препаратов [Измеров Н.Ф., Саноцкий И.В., Сидоров К.К. Параметры токсикометрии промышленных ядов при однократном воздействии: Справочник. М., 1977. - с. 196].
Пример 3. Противовоспалительная активность соединения 1 изучена в опытах на 30 белых беспородных крысах обоего пола массой 220-260 г. Соединение 1 вводили внутрибрюшинно в дозе 50 мг/кг в виде взвеси в 2% крахмальном растворе за час до моделирования острого каррагенинового воспаления. Каррагениновый отек вызывали субплантарной инъекцией 0.1 мл 1% раствора флогогена в заднюю лапу крысы. О противовоспалительной активности судили по изменению выраженности воспаления в динамике, которое регистрировали онкометрически через 2 и 4 часа после моделирования воспаления [Методические рекомендации по экспериментальному изучению нестероидных противовоспалительных веществ, фармакологический комитет МЗ СССР, протокол №22 от 11 ноября 1982. Москва. 1982]. Контрольным животным вводили эквиобъемное количество 2% крахмального раствора. Препаратом сравнения служил ортофен в дозе 10 мг/кг. Результаты испытаний представлены в таблице:
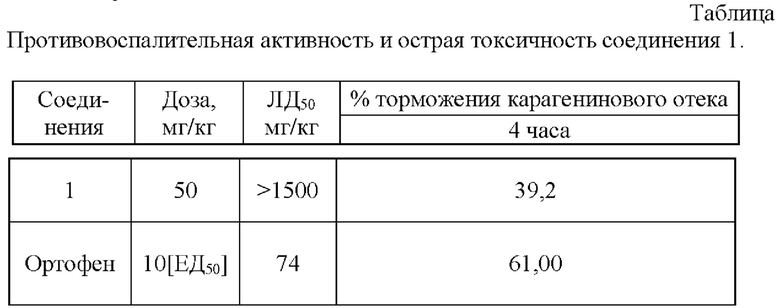
Как видно из таблицы, заявляемое соединение 1 проявляет выраженную противовоспалительную активность и более чем в 20 раз менее токсично, чем препарат сравнения - ортофен. Следовательно, заявляемое соединение 1 может найти применение в медицинской практике в качестве противовоспалительного лекарственного средства.
Изобретение относится к новому биологически активному N'-(имино(2-((6-(2-метоксифенил)-2-(4-нитробензоил)-3-оксо-2,3-дигидропиридазин-4-ил)амино)-4,5,6,7-тетрагидробензо[b]тиофен-3-ил)метил)-4-нитробензогидразиду формулы:
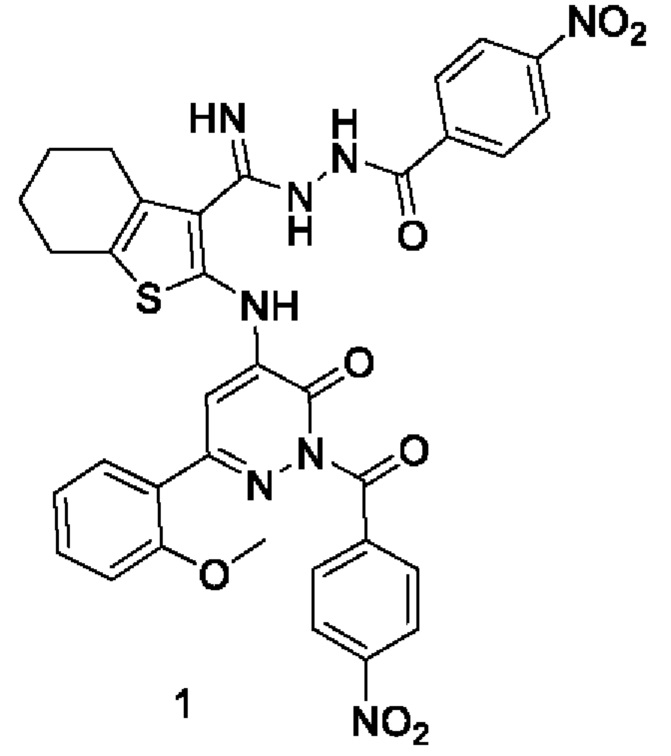
Технический результат: получено соединение с высоким выходом, обладающее выраженной противовоспалительной активностью, а также низкой токсичностью. 1 табл., 3 пр.
N'-(имино(2-((6-(2-метоксифенил)-2-(4-нитробензоил)-3-оксо-2,3-дигидропиридазин-4-ил)амино)-4,5,6,7-тетрагидробензо[b]тиофен-3-ил)метил)-4-нитробензогидразид формулы:
обладающий противовоспалительной активностью.
| S.A | |||
| Shipilovskikh, А.Е | |||
| Rubtsov, Chemistry of Iminofurans | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| ПРИМЕНЕНИЕ АНАЛЬГЕТИЧЕСКОГО СРЕДСТВА НА ОСНОВЕ АМИДА 2-((6-(4-МЕТОКСИФЕНИЛ)-2-МЕТИЛ-3-ОКСО-2,3-ДИГИДРОПИРИДАЗИН-4(1H)-ИЛИДЕН)АМИНО)-4,5,6,7-ТЕТРАГИДРОБЕНЗО[b]ТИОФЕН-3-КАРБОНОВОЙ КИСЛОТЫ | 2023 |
|
RU2809054C1 |
| 2-((6-(2-МЕТОКСИФЕНИЛ)-3-ОКСО-2-ЭТИЛ-2,3-ДИГИДРОПИРИДАЗИН-4-ИЛ)АМИНО)-4,5,6,7-ТЕТРАГИДРОБЕНЗО[b]ТИОФЕН-3-КАРБОНИТРИЛ, ОБЛАДАЮЩИЙ АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2023 |
|
RU2808995C1 |
Авторы
Даты
2024-12-03—Публикация
2024-04-04—Подача