Изобретение относится к области органической химии, а именно к применению индивидуальных соединений класса 3-арилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраонов в качестве средств, обладающих антиоксидантной активностью, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии.
Заявленные соединения 3-арилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраоны 3а-d и способ синтеза их производных известны из уровня техники. Заявляемые соединения являются продуктом взаимодействия 3-ароилпирроло[1,2-a]хиноксалин-1,2,4(5H)-трионов la-d с 3-диазоиндолин-2-оном 2 (Схема 1) (Псевдотрехкомпонентный синтез спиро[фуран-2,3'-оксиндолов]: генерирование диазооксиндола in situ / П.А. Топанов, М.В. Дмитриев, С.Ю. Баландина [и др.] // Журнал общей химии. 2023. - Т. 93, № 11. - С. 1680-1689. DOI 10.31857/S0044460X23110057), образуются по следующей схеме:
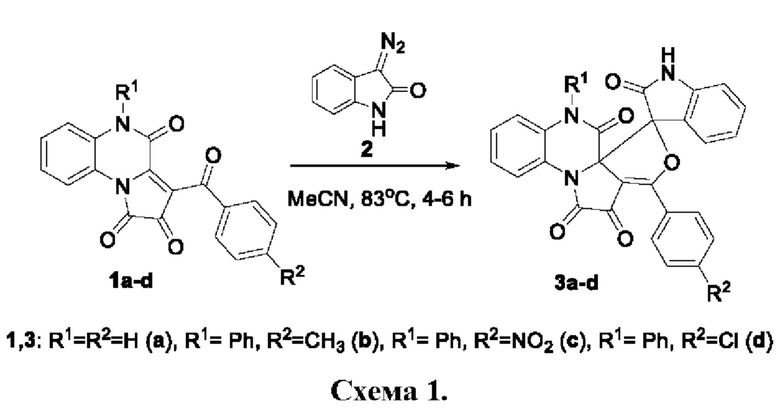
Известна антиоксидантная активность 2а-алкоксикарбонил-5-фенил-1H-спиро[циклопропа[2,3]пирроло[1,2-a]хиноксалин-3,3'-индолин]-1,2,2', 4(2aH,5Н)-тетраонов 4а,b (Схема 2) (Патент № 2798467 С1 Российская Федерация, МПК C07D 498/20. 2а-Алкоксикарбонил-5-фенил-1Н-спиро[циклопропа[2,3]пирроло[1,2-а]хиноксалин-3,3'-индолин]-1,2,2,4(2аН,5Н)-тетраоны: № 2023107333: заявл. 28.03.2023: опубл. 23.06.2023 / И.В. Машевская, П.А. Топанов, М.В. Дмитриев; заявитель Федеральное государственное автономное образовательное учреждение высшего образования "Пермский государственный национальный исследовательский университетʺ), антиоксидантная активность для 3-арилспиро[фуро[3',4':2,3]пирроло[1,2- a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраонов 3а-d ранее не известна.
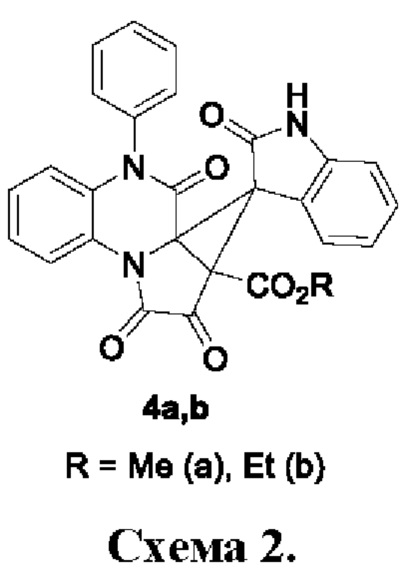
Задачей заявляемого изобретения является изыскание новых соединений, обладающих антиоксидантной активностью, и расширение арсенала средств воздействия на живой организм.
Технический результат - получение новых соединений, которые могут быть использованы в качестве исходного продукта для синтеза новых гетероциклических систем и в фармакологии как обладающие антиоксидантной активностью.
Поставленная задача решается тем, что соединения 3-фенилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон 3а, 3-(n-толил)-7-фенилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон 3b, 3-(4-нитрофенил)-7-фенилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон 3с, 3-(4-хлорфенил)-7-фенилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон 3d обладают выраженной антиоксидантной активностью в отношении свободного радикала 2,2-дифенил-1-пикрилгидразила (DPPH), сопоставимой с активностью коммерчески используемых агидола-1 и аскорбиновой кислоты.
Синтезируют заявляемые соединения путем взаимодействия 3-ароилпирроло[1,2-a]хиноксалин-1,2,4(5H)-трионов la-d с 3-диазоиндолин-2-оном 2 в среде растворителя с последующим выделением целевого продукта, по следующей схеме (Схема 3): 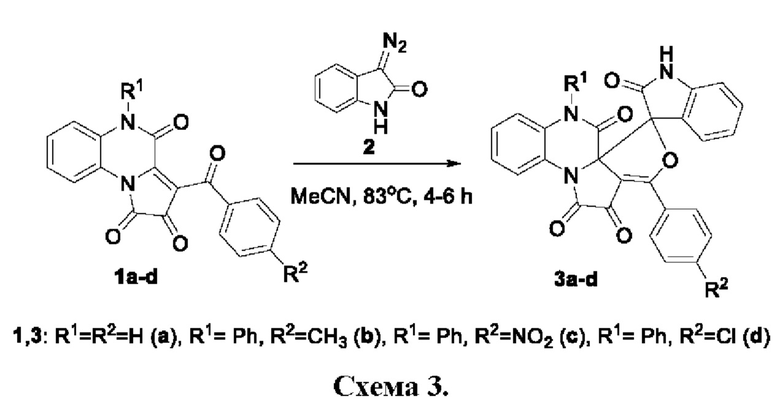
Процесс ведут при температуре 83°С, в качестве растворителя используют безводный ацетонитрил.
Изобретение иллюстрируется следующими примерами.
Пример 1. 3-Фенилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон (3а)
К смеси 0.5 ммоль соединения 1а и 0.5 ммоль 3-диазоиндолин-2-она 2 в виале добавляли 3 мл абсолютного ацетонитрила, нагревали при температуре 83°С в течение 6 ч, образовавшийся осадок отфильтровывали, промывали ацетонитрилом. Выход 70%, т.пл. 270-272°С (AN, разл.).
Соединение (3а) C26H15N3O5.
Найдено, %: С 69.55; Н 3.38; N 9.37.
Вычислено, %: С 69.49; Н 3.36; N 9.35.
Соединение 3а бледно-желтое кристаллическое вещество с высокой температурой плавления, плавящееся с разложением, растворимое при нагревании в ацетонитриле, 1,4-диоксане, растворимое в ДМСО, ДМФА, ацетоне, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
Спектр ЯМР 1Н соединения 3а снят в растворе ДМСО-d6 при частоте 400 МГц: δ=6.60 д (1H, J 7.8 Гц), 6.77 дд (1H, J 7.9 Гц, 1.3 Гц), 6.84 тд (1H, J 1.1 Гц, 1.2 Гц), 6.93 д (2Н, J 4.2 Гц), 7.01 дд (1H, J 8.1 Гц, 1.0 Гц), 7.17 тд (1H, J 8.0 Гц, 1.5 Гц), 7.26 дт (1H, J 1.9 Гц, 4.4 Гц), 7.72 т (2Н, J 1.1 Гц), 7.81-7.87 м (1H), 8.22-8.25 м (2Н), 10.65 с (1H, NHоксиндол), 11.05 c (lH,NH хиноксалин) м.д.
Спектр ЯМР 13С соединения 3а снят в растворе ДМСО-d6 при частоте 100 МГц: δ=71.15 (С3а), 91.91 (С3 оксидол), 105.66, 110.51, 115.64, 121.41, 121.60, 122.12, 122.26, 122.40, 123.68, 125.98, 127.38, 129.25 (2С), 129.94 (2С), 130.40, 132.19, 135.31, 141.44, 160.83 (С=O), 160.96 (С=O), 166.83 (С=O), 169.29 (С=O), 173.65 (С=O)м.д.
Пример 2. 3-(n-Толил)-7-фенилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон(3b)
К смеси 0.5 ммоль соединения 1b и 0.5 ммоль 3-диазоиндолин-2-она 2 в виале добавляли 3 мл абсолютного ацетонитрила, нагревали при температуре 83°С в течение 4 ч, образовавшийся осадок отфильтровывали, промывали ацетонитрилом. Выход 45%, т.пл. 220-221°С (AN, разл.).
Соединение (3b) C33H21N3O5.
Найдено, %: С С 73.50; Н 3.91; N 7.81
Вычислено, %: С, 73.46; Н, 3.92; N, 7.79.
Соединение 3b - бледно-желтое кристаллическое вещество с высокой температурой плавления, плавящееся с разложением, растворимое при нагревании в ацетонитриле, 1,4-диоксане, растворимое в ДМСО, ДМФА, ацетоне, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
Спектр ЯМР 1Н соединения (3b) снят в растворе ДМСО-d6 при частоте 400 МГц: δ=2.48 с (3Н, СН3), 6.35 дд (1H, J 8.3 Гц, 0.9 Гц), 6.63 д (1H, J 7.8 Гц), 6.84 дд (1Н, J 7.9 Гц, 1.5 Гц), 6.89 тд (1H, J 7.7 Гц, 1.1 Гц), 6.92-7.00 м (2Н), 7.09 ддд (1Н, J 8.5 Гц, 7.5 Гц, 1.6 Гц), 7.29 тд (1H, J 7.7 Гц, 1.7 Гц), 7.37 уш с (2Н), 7.53 ддт (6Н, J 20.6 Гц, 14.8 Гц, 7.4 Гц), 8.15 д (2Н, J 8.3 Гц), 10.80 с (1H, NHоксиндол) м.д.
Спектр ЯМР 13С соединения 3b снят в растворе ДМСО-d6 при частоте 100 МГц: δ=21.53 (СН3), 70.97 (С3а), 91.58 (С3оксиндол), 105.15, 110.62, 116.69, 121.82, 122.18, 122.53, 122.59, 122.86, 123.33, 123.62, 127.11, 128.54, 128.72 (2С), 129.54 (2С), 129.92 (2С), 130.05 (2С), 132.27, 133.21, 137.08, 141.45, 146.73, 160.42(С=О), 160.66 (С=O), 167.19 (С=O), 169.50 (С=O), 173.66 (С=O) м.д.
Пример 3. 3-(4-Нитрофенил)-7-фенилспиро[фуро[3',4':2,3]пирроло[1,2-а]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон (3с)
К смеси 0.5 ммоль соединения 1 с и 0.5 ммоль 3-диазоиндолин-2-она 2 в виале добавляли 3 мл абсолютного ацетонитрила, нагревали при температуре 83°С в течение 4 ч, образовавшийся осадок отфильтровывали, промывали ацетонитрилом. Выход 70%, т.пл. 230-231°С (AN, разл.).
Соединение (3с) C32H18N4O7.
Найдено, %: С С 67.42; Н 3.21; N 9.83
Вычислено, %: С, 67.37; Н, 3.18; N, 9.82.
Соединение 3с - желтое кристаллическое вещество с высокой температурой плавления, плавящееся с разложением, растворимое при нагревании в ацетонитриле, 1,4-диоксане, растворимое в ДМСО, ДМФА, ацетоне, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
Спектр ЯМР 1H соединения (3с) снят в растворе ДМСО-d6 при частоте 400 МГц: δ=6.35 дд (1H, J 8.3 Гц, 1.2 Гц), 6.62 д (1H, J 7.8 Гц), 6.84 дд (1H, J 1.9 Гц, 1.6 Гц), 6.90 тд (1H, J 1.1 Гц, 1.2 Гц), 6.97 тд (1H, J 1.6 Гц, 1.0 Гц), 7.07-7.14 м (2Н), 7.29 тд (1H, J 7.8 Гц, 1.3 Гц), 7.38 уш с (2Н), 7.50 тт (1H, J 7.3 Гц, 1.3 Гц), 7.58 т (2Н, J 1.6 Гц), 8.44-8.48 м (2Н), 8.49-8.53 м (2Н), 10.85 с (1H, NHоксиндол) м.д.
Спектр ЯМР 13С соединения 3с снят в растворе ДМСО-d6 при частоте 100 МГц: δ=71.22 (С3а), 92.29 (С3оксиндол), 108.46, 110.58, 116.75, 121.97, 122.07, 122.40, 122.63, 122.94, 124.16, 124.28 (2С), 127.29, 128.60 (2С), 128.68, 129.56 (2С), 130.84 (2С), 131.05, 132.43, 133.25, 136.96, 141.41, 150.62, 159.88 (С=O), 159.90 (С=O), 163.38 (С=O), 169.28 (С=O), 174.33 (С=O) м.д.
Пример 4. 3-(4-Хлорфенил)-7-фенилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон (3d)
К смеси 0.5 ммоль соединения 1d и 0.5 ммоль 3-диазоиндолин-2-она 2 в виале добавляли 3 мл абсолютного ацетонитрила, нагревали при температуре 83°С в течение 5 ч, образовавшийся осадок отфильтровывали, промывали ацетонитрилом. Выход 77%, т.пл. 219-220°С (AN, разл.).
Соединение (3d) C32H18CIN3O5.
Найдено, %: С 68.63; Н 3.28; N 7.53
Вычислено, %: С, 68.64; Н, 3.24; N, 7.50.
Соединение 3d желтое кристаллическое вещество с высокой температурой плавления, плавящееся с разложением, растворимое при нагревании в ацетонитриле, 1,4-диоксане, растворимое в ДМСО, ДМФА, ацетоне, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
Спектр ЯМР 1Н соединения (3d) снят в растворе ДМСО-d6 при частоте 400 МГц: δ=6.32-6.36 м (1H), 6.61 д (1H, J 7.8 Гц), 6.82 дд (1H, J 1.9 Гц, 1.2 Гц), 6.86-6.91 м (1H), 6.99 дт (2Н, J 14.8 Гц, 7.2 Гц), 7.07-7.12 м (1H), 7.25-7.31 м (1H), 7.37 уш с (2Н), 7.49 т (2Н, J 7.3 Гц), 7.55-7.61 м (2Н), 7.80 д (2Н, J 8.6 Гц), 8.24 д (2Н, J 8.6 Гц), 10.82 с (1H, NHоксиндол) м.д.
Спектр ЯМР 13С соединения 3d снят в растворе ДМСО-d6 при частоте 100 МГц: δ=71.08 (С3а), 91.92 (С3 оксиндол), 106.27, 110.59, 116.72, 121.89, 122.10, 122.48, 122.62, 122.89, 123.89, 124.75, 127.19, 128.57, 128.73 (2С), 129.55 (2С), 129.60 (2С), 131.42 (2С), 132.34, 133.22, 137.03, 140.19, 141.42, 160.17 (С=O), 160.32 (С=O), 165.36 (С=O), 169.39 (С=O), 173.99 (С=O) м.д.
Пример 5. Исследование соединений 3а-d на наличие антиоксидантной активности
Антиоксидантная активность изучалась спектрофотометрическим методом по способности растворов исследуемых веществ улавливать ярко окрашенные радикалы 2,2-дифенил-1-пикрилгидразила (DPPH) [Moore J.C., Liangli L.Yu. P. 118-172. DOI: 10.1002/9780470228333.CH9; Wheat Antioxidants (ed. Liangli Yu). Wiley. 2008. DOI: 10.1002/9780470228333].
Фотометрический DPPH реагент содержал 0.2 мМ раствор DPPH в метаноле. Растворы (концентрация 15 мкмоль/мл) исследуемых соединений и эталонов (агидол-1, аскорбиновая кислота) в ДМСО в количестве 100 мкл добавлялись к DPPH реагенту (100 мкл) в лунки 96-луночного планшета. Реакционная смесь выдерживалась при 20°С в течение 20 мин. в темноте. Оптическую плотность реакционных смесей измеряли при 517 нм. Калибровка проводилась по свежеприготовленному раствору DPPH в смеси ДМСО-метанол, 1 к 1. Убыль радикала рассчитывали по формуле:
Убыль радикала (%)=[(А0 - A1)/A0]•100, где А0 поглощение раствора DPPH без исследуемого образца, A1 поглощение раствора DPPH в присутствии исследуемого образца.
Результаты исследований приведены в Таблице.
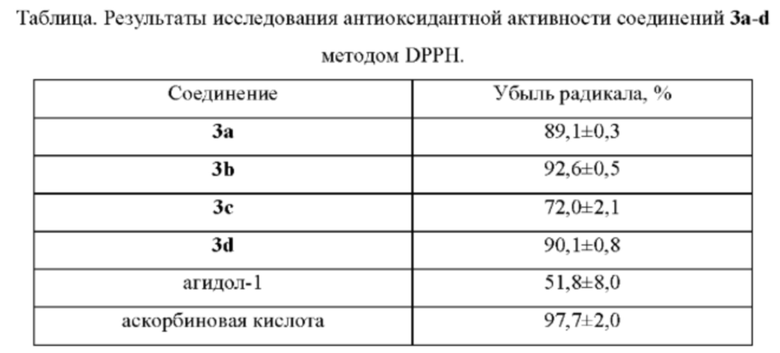
В результате исследования выявлено, что соединения 3а-d проявляют выраженный антиоксидантный эффект, сопоставимый с уровнями промышленно используемых антиоксидантов - агидола-1 и аскорбиновой кислоты.
Предлагаемые вещества 3-фенилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон 3а, 3-(n-толил)-7-фенилспиро[фуро[3',4':2,3]пирроло[1,2 a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон 3b, 3-(4-нитрофенил)-7-фенилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон 3с, 3-(4-хлорфенил)-7-фенилспиро[фуро[3',4':2,3]пирроло[1,2-α]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраон 3d обладают выраженной антиоксидантной активностью и могут найти применение в фармакологии в качестве потенциальных лекарственных средств.
Изобретение относится к области химии и фармацевтики и раскрывает применение 3-арилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраонов 3a-d в качестве средств, обладающих антиоксидантной активностью. 1 табл., 5 пр. 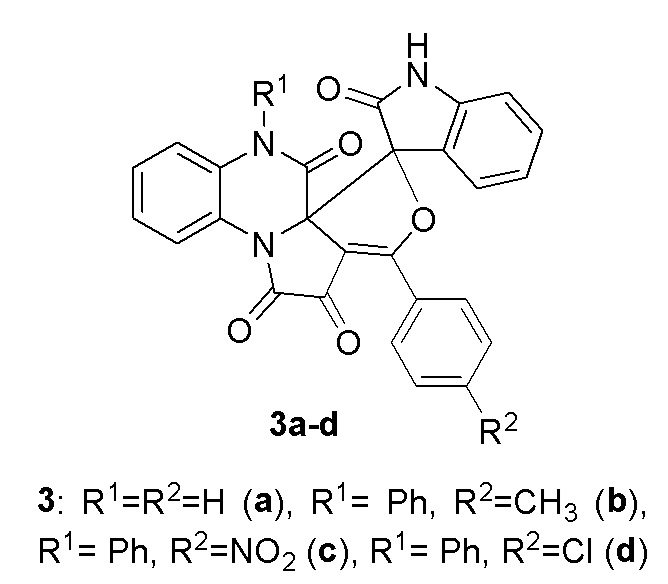
Применение 3-арилспиро[фуро[3',4':2,3]пирроло[1,2-a]хиноксалин-5,3'-индолин]-1,2,2',6(7H)-тетраонов 3a-d
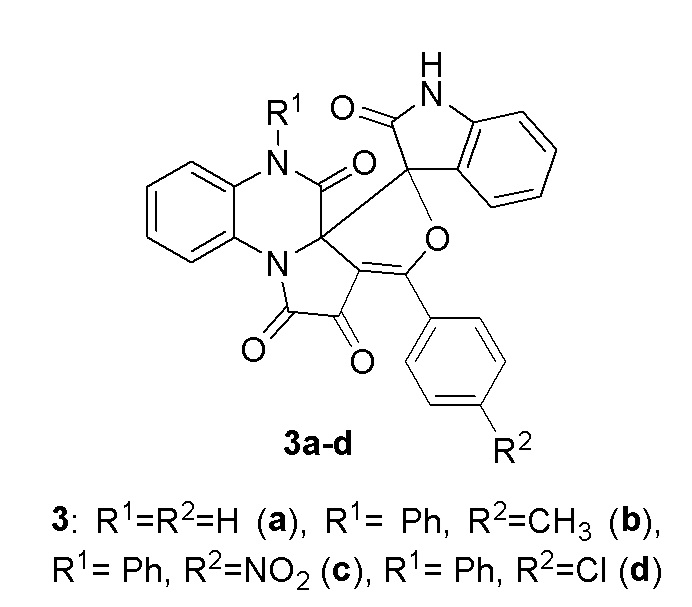
в качестве средств, обладающих антиоксидантной активностью.
| Средство, обладающее антиоксидантной и нейропротекторной активностью | 2021 |
|
RU2777391C1 |
| Применение диметил (3aR*,4R*,9aS*)-4-(4-метоксифенил)-2,3,8-триоксо-1-фенилтетрагидро-6H-пиразоло[1,2-a]пирроло[2,3-c]пиразол-3a,9a(1H,4H)-дикарбоксилата в качестве средства, обладающего антиоксидантной активностью | 2023 |
|
RU2810210C1 |
| ПРИМЕНЕНИЕ 5-(4-МЕТОКСИФЕНИЛ)-4-СПИРО-2,4-ДИГИДРО-3H-ПИРАЗОЛ-3-ОНОВ В КАЧЕСТВЕ СРЕДСТВ, ОБЛАДАЮЩИХ АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ | 2023 |
|
RU2809147C1 |
| 2a-Алкоксикарбонил-5-фенил-1H-спиро[циклопропа[2,3]пирроло[1,2-a]хиноксалин-3,3'-индолин]-1,2,2',4(2aH,5H)-тетраоны | 2023 |
|
RU2798467C1 |
Авторы
Даты
2024-12-03—Публикация
2024-03-27—Подача