Настоящее изобретение относится к области медицины, в частности геронтологии и гериартрии и клинической лабораторной диагностики, и может быть использовано для оценки степени накопления сенесцентных клеток у пожилых пациентов с возраст-ассоциированными заболеваниями и/или преждевременным старением при химиотерапевтическом воздействии с целью принятия клинических решений о назначении специфической терапии и оценки её эффективности.
Из уровня техники известен способ оценки уровня накопления сенесцентных клеток у человека по комплексной оценке таких показателей как уровень экспрессии белка р16, активность β-галактозидазы, скорость репарации ткани по скорости миграции клеток и продукции компонентов внеклеточного матрикса в биоптатах ахиллова сухожилия человека (Kohler J., Popov C., Klotz B., Alberton P., Prall W.C., Haasters F., Müller-Deubert S., Ebert R., Klein-Hitpass L., Jakob F., Schieker M., Docheva D. Uncovering the cellular and molecular changes in tendon stem/progenitor cells attributed to tendon aging and degeneration. Aging Cell. 2013 Dec; 12(6): 988-99. doi: 10.1111/acel.12124.). Однако известный способ требует взятия биопсии материала и использования клеточно-молекулярных методов исследования, не всегда доступных в стандартной клинико-диагностической лаборатории. Указанный метод также не предлагает единой ранжированной шкалы, которая позволяла бы оценивать полученные в дальнейшем результаты в других исследованиях и сравнивать их между собой.
Из уровня техники известен также набор из молекулярных и клеточных маркеров (белки-блокаторы клеточного цикла, белки секреторного фенотипа, ассоциированного со старением (SASP), уровень активности β-галактозидазы, анализ пролиферации клеток в режиме реального времени) для первичных меланоцитов и злокачественных клеток меланомы для обнаружения сенесцентных клеток in vitro (Zimmermann, T.; Pommer, M.; Kluge, V.; Chiheb, C.; Muehlich, S.; Bosserhoff, A.-K. Detection of Cellular Senescence in Human Primary Melanocytes and Malignant Melanoma Cells In Vitro. Cells 2022, 11, 1489. https://doi.org/10.3390/cells11091489). Однако известный набор не позволяет проводить оценку накопления сенесцентных клеток in vivo, требует наличия молекулярно-клеточной лаборатории и не может быть использован в рутинной клинической практике.
Из уровня техники известен способ оценки старения организма по уровню транскрипта микроРНК-22 в исследуемых биологических образцах, в том числе для оценки эффективности ингибиторов старения (WO 2011078037).
Из уровня техники также известен способ обнаружения стареющих клеток или диагностики клеточного старения у субъекта, при котором уровень одной или нескольких выбранных микроРНК (миР let-7a-5p, миР-199a-5p , миР-345-5p, миР-423-3p и миР-125a-5p) количественно определяют в образце от указанного субъекта. Этот способ может использоваться для обнаружения стареющих клеток in vitro, диагностики клеточного старения и/или мониторинга успеха сенолитического лечения (WO 2019002265).
Из уровня техники также известен способ визуализации стареющих клеток с помощью мечения in vivo сенесцентных клеток специфическими агентами (например, пептиды, полипептиды, белки, малые молекулы, антитела и фрагменты антител, нацеленные на стареющие клетки), а также использование их для лечения или профилактики рака, возрастных заболеваний, связанных с курением заболеваний или других заболеваний и расстройств, связанных или вызванных старением клеток у млекопитающих, в том числе человека, которые включают введение одного или нескольких агентов. Агенты, которые специфически связываются со стареющими клетками, могут быть помечены радиоактивной меткой или терапевтической меткой, например цитотоксическим агентом (WO 2009085216).
Из уровня техники также известен способ оценки накопления сенесцентных клеток по специфическому профилю экспрессии белков плазматической мембраны в стареющих клетках методом проточной цитометрии (WO 2015181526).
Из уровня техники также известен способ визуализации бета-галактозидазы и других новых производных гексозы и, в частности, галактозы, как биомаркера сенесцентных клеток с помощью радиоактивной метки и ПЭТ, что можно использовать в качестве индикаторов старения in vitro и in vivo (WO 2018153966).
Из уровня техники также известен способ обнаружения клеток, сверх-экспрессирующих лиганд запрограммированной смерти 2 (PD-L2), в частности, поврежденных и/или стареющих клеток, и их идентификации, а также элиминации (WO 2019002581).
Из уровня техники также известен способ оценки биомаркеров накопления сенесцентных клеток, в том числе в организме человека, по уровню одного или более индикаторов стареющих клеток в биологическом образце, выбранных из группы, состоящей из эйкозаноида, предшественника эйкозаноида, лейкотриена А4 (LTA4), лейкотриена B4 (LTB4), PGD2 и 5-HETE; при этом повышенный уровень указанного одного или более индикаторов является индикатором повышенных уровней стареющих клеток у указанного млекопитающего (WO 2019070407).
Из уровня техники также известен способ определения степени старения субъекта или его клетки, ткани или органа, или оценки физического возраста субъекта, или диагностики прогероидных заболеваний, или оценки степени старения изолированной животной клетки или популяции клеток с помощью определения уровня активации эндогенного ретровируса (ERV) в образце от субъекта или в клетке и сравнение результата обнаружения с эталонным значением уровня активации ERV (WO 2022135486).
Однако, все указанные выше подходы предполагают использование инвазивных методик для получения образцов тканей и клеток с целью оценки биомаркеров клеточного старения или введение экзогенных агентов для мечения таких клеток in vivo, что сопряжено с набором различных рисков для пациента.
Наиболее близким к заявляемому является способ оценки накопления сенесцентных клеток по выявленной связи между жесткостью сосудистой стенки (оцененной по уровню скорости пульсовой волны, СПВ) и известными маркерами накопления сенесцентных клеток в крови, клетках и тканях у пожилых пациентов, а именно содержанием инсулиноподобного фактора роста 1 (IGF-1), молекул адгезии сосудистого эндотелия 1 (VCAM-1), экспрессией р16INK, параметрами прироста мезенхимных стромальных клеток и фибробластов за 96 часов, содержанием интерлейкина-6 (IL-6) в секретоме выделенных клеток как элемента SASP (Сорокина А.Г., Ефименко А.Ю., Григорьева О.А., Новоселецкая Е.С., Басалова Н.А., Александрушкина Н.А., Виговский М.А., Кириллова К.И., Стражеско И.Д., Орлов А.В., Балацкий А.В., Самоходская Л.М., Данилова Н.В., Дьячкова У.Д., Акопян А.А., Какоткин В.В., Асратян Д.А., Акопян Ж.А., Орлова Я.А. Взаимосвязь жесткости магистральных сосудов и биомаркеров накопления сенесцентных клеток у пожилых пациентов. Кардиология. 2022; 62(6): 15-22. https://doi.org/10.18087/cardio.2022.6.n2033). Таким образом, среди общих признаков данного способа с заявляемым можно выделить схожие методы определения биомаркеров сенесцентных клеток на разных уровнях (цитометрический анализ, определение экспрессии белков-блокаторов клеточного цикла методами иммуногистохимического анализа и ПЦР, белков секреторного фенотипа, ассоциированного со старением (SASP), уровня активности β-галактозидазы, анализ пролиферации выделенных в культуру клеток, статистический анализ), а также общую концепцию наличия связей между системными, тканевыми и клеточными биомаркерами накопления сенесцентных клеток. Однако, есть ряд существенных отличий. Во-первых, указанная работа сфокусирована на поиске взаимосвязей между показателем жесткости магистральных артерий, измеренной с помощью СПВ, с рядом плазменных, тканевых и клеточных маркеров накопления сенесцентных клеток. Найденные значимые корреляции позволяют рассматривать СПВ в качестве претендента на включение в панель параметров для оценки и мониторирования биологического возраста организма при различных клинических задачах, однако этот показатель отражает только сосудистое старение. Во-вторых, в данной работе выявлена слабая, хотя и значимая связь СПВ с ключевым биомаркером накопления сенесцентных клеток в тканях – р16INK. Важным отличием является тот факт, что в данной работе исследуемый уровень СПВ оказался связан с различными параметрами, отражающими накопление сенесцентных клеток в организме человека, однако определение многих из этих параметров требует взятие биоптатов тканей в ходе инвазивных хирургических процедур.
Технической проблемой, на решение которой направлено заявляемое изобретение является создание нового способа оценки содержания сенесцентных клеток в организме человека, отражающего накопление этих клеток на тканевом уровне, с помощью набора показателей, определение которых не требует взятия биопсии тканей и может быть проведено методами, доступными в стандартной клинико-диагностической лаборатории.
Задачей изобретения является создание способа оценки степени накопления сенесцентных клеток в организме человека, отличающегося от аналогов возможностью расчёта степени накопления сенесцентных клеток по косвенным показателям, полученным в ходе клинико-лабораторных исследований, без взятия биоптатов ткани.
Техническим результатом, на достижение которого направлено заявленное изобретение, является отнесение пациента к высокой или низкой степени накопления сенесцентных клеток, необходимое для принятия клинического решения по дальнейшей тактике ведения пациента или оценке эффективности геропротекторной, в том числе сенолитической терапии. Результаты, получаемые с помощью заявляемого способа, характеризуются высокой сопоставимостью с результатами, полученными при прямой оценке содержания сенесцентных клеток в биоптате тканей.
Техническая проблема решается путем последовательной оценки параметров, отражающих степень накопления сенесцентных клеток у пациентов и отобранных по результатам математического анализа экспериментальных данных по определению различных биомаркеров сенесцентных клеток на системном, клеточном уровнях у выборки пожилых пациентов. Осуществление способа включает в себя следующие этапы:
- проведение забора периферической венозной крови в стандартную вакуумную пробирку для гематологических исследований;
- определение в образце крови процента CD34+ клеток методом проточной цитометрии;
- определение в образце крови уровня молекулы адгезии сосудистых клеток (VCAM) с помощью соответствующего коммерческого набора для иммуноферментного анализа;
- внесение значений паспортного возраста, процента CD34+ клеток и уровня VCAM в формулу расчета уровня экспрессии p16 в тканях:
Уровень экспрессии p16 в тканях (КСК)=(Возраст пациента-65)*(-0,14)+(CD34+% -0,04)*(-2,27)+(2*VCAM-22,95)*(-0,02)+(VCAM∧4-277415,52)*(2,15*10∧(-7))+6,27,
где «возраст» – возраст пациента в годах, CD34+% – процент CD34+ клеток в периферической крови, VCAM в плазме крови – уровень VCAM в плазме крови в нг/мл, а числовые коэффициенты – константы;
- оценка расчетного значения уровня экспрессии p16 в тканях, в том случае, если его значение больше или равны 4 – пациента относят к группе с высокой степенью накопления сенесцентных клеток, а в том случае, если его значение ниже 4, то пациента относят к группе с низкой степенью накопления сенесцентных клеток.
В отличие от прототипа, в заявленном изобретении предложенная формула накопления сенесцентных клеток в организме определяет расчетное значение уровня р16 – одного из ключевых белков - блокаторов клеточного цикла, отражающего содержание сенесцентных клеток на тканевом и клеточном уровне. Этот белок активируется под воздействием постоянного стресса и приводит к длительной остановке клеточного цикла. С возрастом изменяется экспрессия генов, в том числе генов-регуляторов клеточного цикла. Ингибиторы клеточного цикла, включая p16, гиперэкспрессируются, а те гены, которые кодируют белки, стимулирующие клеточный цикл, репрессируются. Сегодня р16 является одним из самых достоверных биомаркеров клеточного старения. Показано, что более молодой биологический возраст связан с более низким уровнем экспрессии р16, также уровень экспрессии p16 достоверно коррелирует с рядом факторов риска ССЗ и показателем жесткости сосудистой стенки – СПВ.
В отличие от прототипа, в заявленном изобретении в расчетную формулу включен перспективный биомаркер старения, который определяется по уровню CD34+клеток, представляющих собой популяцию стволовых клеток гемопоэтического ряда, и может быть оценен в периферической крови человека. Истощение гемопоэтических стволовых клеток, а также снижение числа и функции эндотелиальных прогениторных клеток является независимым биомаркером раннего субклинического атеросклероза у здоровых людей и может дать дополнительную информацию о возраст-ассоциированных изменениях даже без учета влияния классических факторов риска и воспалительных биомаркеров.
Технической особенностью изобретения является оценка содержания в плазме содержания VCAM, который рассматривается сегодня в панели биомаркеров, отражающих «старческую хрупкость» организма, и изучается в рамках теории сенесцентности. Привлечение и адгезия моноцитов к эндотелию играют решающую роль в инициации атеросклероза. VCAM косвенно отражает степень повреждения сосудистой стенки, и в исследованиях показана взаимосвязь уровня VCAM с показателями жесткости сосудистой стенки. У пациентов пожилого возраста уровень VCAM повышается вне зависимости от наличия или отсутствия факторов сердечно-сосудистого риска.
Таким образом, технический результат достигается за счет того, что способ оценки накопления сенесцентных клеток в организме пожилых пациентов проводится по предложенной с помощью расчёта по косвенным показателям, полученным в ходе клинико-лабораторных исследований, без взятия биоптатов ткани.
Краткое описание чертежей
Изобретение поясняется следующими чертежами.
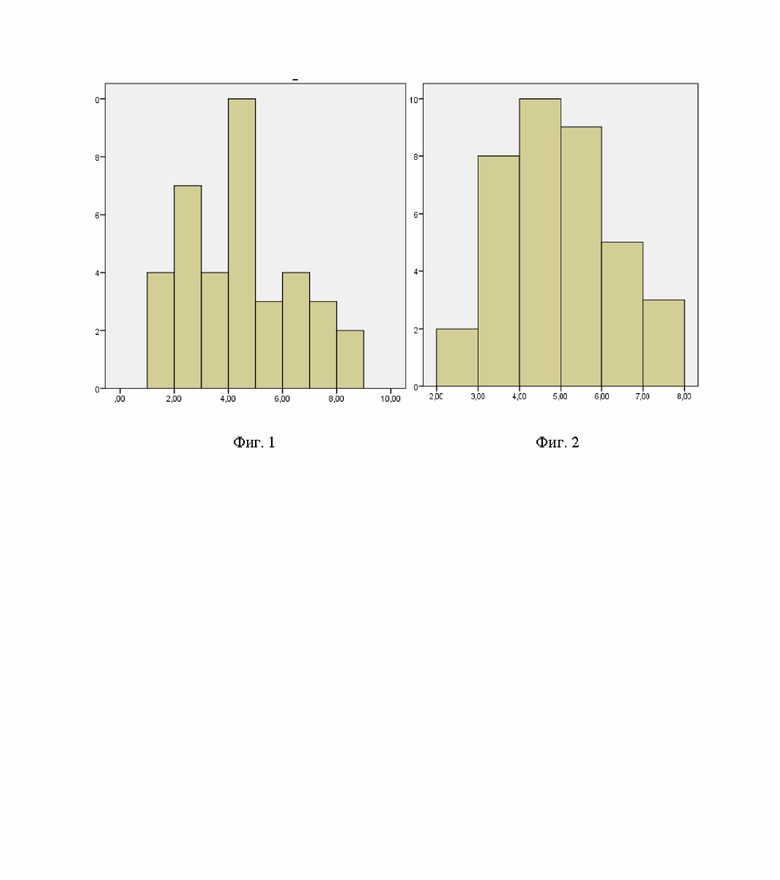
На фиг. 1 представлена гистограмма, отражающая распределение значений расчетного показателя уровня экспрессии p16 в тканях (КСК) среди пациентов в исследованной выборке.
На фиг. 2 представлена гистограмма, отражающая распределение значений показателя экспрессии p16 в тканях, измеренного методом иммуногистохимического анализа, среди пациентов в исследованной выборке.
Осуществление изобретения
Ниже представлено более подробное описание заявляемого изобретения. Настоящее изобретение может подвергаться различным изменениям и модификациям, понятным специалисту на основе прочтения данного описания. Такие изменения не ограничивают объем притязаний.
Пример 1. Получение биоматериалов от пожилых пациентов старше 65 лет и анализ биомаркеров накопления сенесцентных клеток на системном, тканевой и клеточном уровнях
С целью оценки степени накопления сенесцентных клеток было проведено проспективное исследование, в которое вошло 38 пациентов (6 мужчин и 32 женщины в возрасте от 65 до 81 года (медиана 70 лет), соответствующих критериям включения/невключения и давших добровольное информированное согласие на участие в исследовании. Всем пациентам проводили оценку традиционных факторов риска сердечно-сосудистых заболеваний, жесткости артериальной стенки (СПВ оценивали с помощью прибора «BPLab» (ООО «Петр Телегин», Россия) в комплексе с программой Vasotens Office версии 06.04.03) по стандартной методике. У всех пациентов были получены образцы периферической крови, образцы тканей (кожи и подкожной жировой клетчатки). Подробно все этапы пробоподготовки и методы оценки различных биомаркеров сенесцентных клеток на системном, тканевом и клеточной уровнях описаны в публикациях Сорокина А.Г., Ефименко А.Ю., Григорьева О.А., Новоселецкая Е.С., Басалова Н.А., Александрушкина Н.А., Виговский М.А., Кириллова К.И., Стражеско И.Д., Орлов А.В., Балацкий А.В., Самоходская Л.М., Данилова Н.В., Дьячкова У.Д., Акопян А.А., Какоткин В.В., Асратян Д.А., Акопян Ж.А., Орлова Я.А. Взаимосвязь жесткости магистральных сосудов и биомаркеров накопления сенесцентных клеток у пожилых пациентов. Кардиология. 2022; 62(6): 15-22. https://doi.org/10.18087/cardio.2022.6.n2033 и Cорокина А.Г., Орлова Я.А., Григорьева О.А., Новоселецкая Е.С., Басалова Н.А., Александрушкина Н.А., Виговский М.А., Кириллова К.И., Балацкий А.В., Самоходская Л.М., Данилова Н.В., Дьячкова У.Д., Федотов Д.А., Акопян А.А., Какоткин В.В., Асратян Д.А., Акопян Ж.А., Ефименко А.Ю. Создание коллекции биологических образцов разного типа, полученных от пожилых пациентов, для изучения взаимосвязей клинических, системных, тканевых и клеточных биомаркеров накопления сенесцентных клеток при старении. Кардиоваскулярная терапия и профилактика. 2021; 20(8): 3051. https://doi.org/10.15829/1728-8800-2021-3051.
Коротко, в образцах периферической крови оценивали спектр биохимических показателей и уровень плазменных биомаркеров накопления сенесцентных клеток с помощью иммуноферментного анализа, а также содержание CD34+ клеток с помощью проточной цитометрии. Из биоптатов выделяли в культуру стромальные клетки (фибробласты – ФБ и мезенхимные стромальные клетки – МСК), с помощью которых оценивали клеточные биомаркеры сенесцентных клеток, в том числе проводили оценку пролиферативной активности и содержание различных компонентов SASP. В образцах кожи и подкожной жировой ткани, полученных из локализаций, минимально подверженных действию солнечного света и других повреждающих факторов, запускающих клеточное старение, определяли содержание клеток, которые экспрессировали ингибитор клеточного цикла р16/INK4a (р16). Для этого образцы кожи и подкожной жировой ткани фиксировали в 10% забуференном нейтральном формалине в течение 24-48 часов после забора материала. Гистологическая проводка осуществлялась по стандартной методике с использованием 8 смен изопропилового спирта (общая продолжительность – 5,5 часов, температура 37°С) и 3 смен парафина (общая продолжительность – 5 часов, температура 62°С). Затем препараты заливали в парафиновые блоки, которые длительно хранили при комнатной температуре. Далее с парафиновых блоков изготавливали срезы толщиной 3-4 мкм, которые монтировали на предметные стекла (Menzel GmbH&Co KG, Германия). Окрашивание производили по стандартной методике с использованием гематоксилина Майера и эозина (PanReac AppliChem, Испания). Для постановки иммуногистохимических реакций использовались моноклональные мышиные антитела к р16 (клон Е6Н4) в составе набора CINtec Histology Kit (Roche, Германия). Депарафинирование и регидратацию препаратов выполняли вручную, согласно инструкции производителя. Демаскировку антигена осуществляли при помощи Epitope Retrieval Solution, входящего в состав набора CINtec Histology Kit (Roche, Германия) при температуре 95–98°С в течение 10 минут в модуле предобработки (PT-Module). Постановку иммуногистохимических реакций проводили в автоматизированном режиме с помощью иммуностейнера Autostainer 480S (Thermo Fisher Scientific, США). Время инкубации составляло 30 минут. При постановке иммуногистохимических реакций использовали соответствующие положительные и отрицательные контроли. Препараты изучали под световым микроскопом Leica DM LB2. Для подсчета количества положительных клеток использовалась оригинальная методика. Готовые иммуногистохимические препараты сканировали при помощи сканера Leica SCN400. Затем при помощи встроенных морфометрических инструментов измеряли общую площадь срезов жировой ткани и кожи, из которой вычитали площадь артифициальных разрывов на срезах. В подсчет количества клеток включали все положительно окрашенные клетки вне зависимости от их локализации в коже (эпидермис, дерма, придатки кожи) и жировой ткани (фиброзные прослойки в жировой ткани). Положительной считалась ядерно-цитоплазматическая и цитоплазматическая экспрессия биомаркера любой интенсивности. Далее производили вычисление количества р16-положительных клеток на 1 кв. мм ткани.
Согласно полученным результатам, было выявлено от 0,7 до 11 положительно окрашенных клеток на 1 мм2 ткани, среднее содержание 2,9±1,9 клеток. Содержание р16 коррелировало с паспортным возрастом пациентов и показателем жесткости сосудистой стенки, отражающим старение сосудов – СПВ (Табл. 1).
Табл. 1. Связь р16 с возрастом и параметром жесткости сосудистой стенки. Данные многофакторного регрессионного анализа
С помощью корреляционного анализа были выделены наиболее значимые показатели, отражающие накопление сенесцентных клеток на системном, тканевом и клеточном уровнях (с учетом нормального распределения использовался коэффициент корреляции Пирсона r>0.3, при р<0.05), демонстрировавшие положительные и отрицательные корреляции с уровнем экспрессии р16. В качестве маркеров накопления сенесцентных клеток для дальнейшего более глубокого анализа были отобраны следующие: содержание VCAM среди параметров крови, уровень CD34+ клеток, показатели пролиферации МСК и ФБ, а также продукция клетками IL-6 и MCP-1 как компонентов SASP.
С целью построения модели для определения уровня экспрессии р16 в тканях, по уровню других маркёров клеточного старения была использована множественная регрессионная модель и компьютерное моделирование. После нормирования признаков компьютерное моделирование позволило определить модель оценки уровня р16 в тканях с учетом паспортного возраста и по показателям, измеряемым только в периферической крови:
Уровень экспрессии p16 в тканях (КСК)=(Возраст пациента-65)*(-0,14)+(CD34+% -0,04)*(-2,27)+(2*VCAM-22,95)*(-0,02)+(VCAM∧4-277415,52)*(2,15*10∧(-7))+6,27.
Для подтверждения клинической пригодности разработанного способа оценки степени накопления сенесцентных клеток у пациентов было проведено сравнение ряда биомаркеров сенесцентных клеток, определяемых в биоптатах, и оцененного с помощью заявляемого способа.
Так, уровень экспрессии р16 в биоптатах не отличался статистически значимо от прогнозируемого уровня экспрессии р16, определяемого описанным способом. Анализ гистограмм распределения расчетного и измеренного уровня экспрессии р16 (Фиг. 1 и 2) позволил установить пограничное значение – 4 экспрессирующие р16 клетки на кв.мм. Таким образом, если рассчитанное по предложенной формуле значение больше или равны 4 – пациента относят к группе с высокой степенью накопления сенесцентных клеток, а в том случае, если его значение ниже 4, то пациента относят к группе с низкой степенью накопления сенесцентных клеток. Предложенная шкала позволяла стратифицировать пациентов по группам с разной степенью накопления сенесцентных клеток, что коррелировало с показателем сосудистого старения, определяемого по уровню СПВ (Табл. 2).
Табл. 2. Стратификация пациентов по группам с разной степенью накопления сенесцентных клеток, рассчитанной согласно заявленному способу (А) или по прямому определению экспрессии р16 в тканях (Б), коррелирует со средним уровнем сосудистого старения в этих группах, определяемого по уровню СПВ
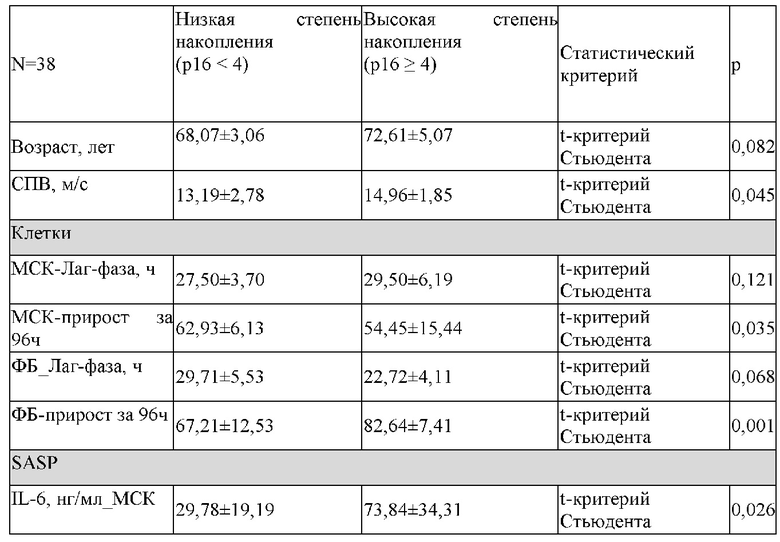
Для оценки прогностической значимости степени накопления сенесцентных клеток определяли корреляции других известных маркеров сенесцентных клеток с уровнем экспрессии р16, определяемым описанным способом (Табл. 3).
Табл. 3. Изучаемые параметры в группах с низкой и высокой степенью накопления сенесцентных клеток
Пример 2. Пример использования заявленного способа у конкретного пациента
Пациентка Л., 80 лет, не входила в исходную выборку, госпитализирована для планового оперативного вмешательства в объеме эндопротезирования коленного сустава. После подписания добровольного информированного согласия осуществлен забор периферической крови, в условиях клинического отделения проведено неинвазивное исследование жесткости артерий (СПВ=17,1м/с). В процессе хирургического вмешательства в асептических условиях операционной получен образец биоматериала (подкожная жировая ткань в количестве 1-5 мл и участок кожи 3-5 кв. мм) для гистологического анализа и выделения клеток.
Из периферической крови выделяли мононуклеарные клетки в градиенте плотности на фиколле (ПанЭко, Россия). С помощью окрашивания мононуклеаров крови флуоресцентно мечеными антителами к биомаркерным белкам субпопуляции прогениторных клеток CD34 и к изотипическому контролю (IgG) для CD34 (флуорофор APC) с дальнейшим анализом методом проточной цитометрии определяли процент CD34+ клеток (CD34+=0,026%).
В образце плазмы определяли показатели содержания в периферическом кровотоке ряда секретируемых стареющими клетками факторов, в том числе VCAM с помощью соответствующего коммерческого набора для иммуноферментного анализа (eBioscience). Содержание VCAM в плазме крови у данной пациентки составило 84,19 нг/мл.
Данные значения были подставлены в формулу расчета коэффициента по заявляемому способу оценки степени накопления сенесцентных клеток у пожилых пациентов:
КСК=(80-65)*(-0,14)+(0,026-0,04)*(-2,27)+(2*84,19-22,95)-(-0,02)+(84,19∧4-277415,52)*(2,15*10∧(-7))+6,27.
Значение коэффициента составило КСК=11,93. Данное значение оказалось выше порогового значения по заявляемому способу, поэтому пациентка была отнесена к группе с высокой степенью накопления сенесцентных клеток.
Затем была проведена проверка полученных данных с помощью вычисления количества р16-положительных клеток на 1 кв.мм ткани в биоптате, полученном от данной пациентки, измеренном методом иммуногистохимического анализа. Полученные результаты показали, что уровень экспрессии р16 в тканях данной пациентки составлял 8,94 кл. на ед. площади ткани, данное значение попадает в 4-ый квартиль распределения частоты встречаемости уровня экспрессии р16 (Фиг. 2), что соответствует высоким значениям данного показателя и подтверждает отнесение пациентки к группе с высокой степенью накопления сенесцентных клеток.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ УНИЧТОЖЕНИЯ СТАРЕЮЩИХ КЛЕТОК И ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ И РАССТРОЙСТВ, АССОЦИИРОВАННЫХ СО СТАРЕНИЕМ | 2015 |
|
RU2716256C2 |
| Лечение глазных болезней типа дегенерации желтого пятна, глаукомы и диабетической ретинопатии с помощью лекарственных средств, устраняющих стареющие клетки | 2018 |
|
RU2815482C2 |
| ТРАНЗИЕНТНОЕ КЛЕТОЧНОЕ ПЕРЕПРОГРАММИРОВАНИЕ ДЛЯ ОБРАЩЕНИЯ СТАРЕНИЯ КЛЕТКИ | 2019 |
|
RU2801316C2 |
| СПОСОБ ДИАГНОСТИКИ ИЛИ ОПРЕДЕЛЕНИЯ РИСКА РАЗВИТИЯ КОГНИТИВНОГО НАРУШЕНИЯ | 2023 |
|
RU2821890C1 |
| СПОСОБ ОЦЕНКИ ВОЗРАСТНЫХ ИЗМЕНЕНИЙ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ ЧЕЛОВЕКА | 2012 |
|
RU2485886C1 |
| ДИАГНОСТИЧЕСКИЕ АНТИТЕЛА К КОНЕЧНЫМ ПРОДУКТАМ ГЛУБОКОГО ГЛИКИРОВАНИЯ | 2018 |
|
RU2788905C2 |
| СПОСОБ КУЛЬТИВИРОВАНИЯ ФИБРОБЛАСТОВ ДЛЯ ЗАМЕСТИТЕЛЬНОЙ ТЕРАПИИ | 2006 |
|
RU2320720C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ, ПРЕДОТВРАЩЕНИЯ И ОБРАЩЕНИЯ СВЯЗАННОГО С ВОЗРАСТОМ ВОСПАЛЕНИЯ И РАССТРОЙСТВ | 2020 |
|
RU2812903C2 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ПРИЖИЗНЕННОЙ ДИАГНОСТИКИ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2023 |
|
RU2821893C1 |
| Способ прогнозирования эффективности консервативного лечения плоскоклеточного рака ротоглотки | 2023 |
|
RU2817324C1 |
Изобретение относится к медицине, а именно к геронтологии, гериартрии, клинической лабораторной диагностике, и может быть использовано для оценки степени накопления сенесцентных клеток у пациентов старше 65 лет. Проводят: а) забор периферической венозной крови, б) выделение из периферической крови фракций мононуклеарных клеток и плазмы, в) определение в образце фракции мононуклеарных клеток крови количества клеток, положительных по маркеру CD34, в процентах (CD34+%), г) определение в образце плазмы крови содержания VCAM в нг/мл, д) расчет коэффициента, отражающего степень накопления сенесцентных клеток в организме, по формуле: КСК=(Возраст пациента-65)*(-0,14)+(CD34+%-0,04)*(-2,27)+(2*VCAM-22,95)*(-0,02) +(VCAM∧4-277415,52)*(2,15*10∧(-7))+6,27, е) определение степени накопления сенесцентных клеток у пациентов старше 65 лет. При получении значения КСК меньше 4 пациента относят в группу с низкой степенью накопления сенесцентных клеток в тканях. При значении КСК выше или равно 4 пациента относят в группу с высокой степенью накопления сенесцентных клеток. Выделение из периферической крови фракций мононуклеарных клеток и плазмы может быть произведено в градиенте плотности на фиколле. Для оценки содержания CD34+ клеток может быть использован метод проточной цитометрии. Для оценки уровня VCAM может быть использован иммуноферментный анализ. Способ обеспечивает возможность отнесения пациента к высокой или низкой степени накопления сенесцентных клеток, необходимого для принятия клинического решения по дальнейшей тактике ведения пациента или оценке эффективности геропротекторной, в том числе сенолитической терапии, за счет расчёта степени накопления сенесцентных клеток по косвенным показателям, полученным в ходе клинико-лабораторных исследований без взятия биоптатов ткани и использования формулы, разработанной на основе мультипараметрического анализа взаимосвязей различных биомаркеров сенесцентных клеток на системном, тканевом и клеточном уровнях. 3 з.п. ф-лы, 2 ил., 3 табл., 2 пр.
1. Способ оценки степени накопления сенесцентных клеток у пациентов старше 65 лет, включающий: а) забор периферической венозной крови, б) выделение из периферической крови фракций мононуклеарных клеток и плазмы, в) определение в образце фракции мононуклеарных клеток крови количества клеток, положительных по маркеру CD34, в процентах (CD34+%), г) определение в образце плазмы крови содержания VCAM в нг/мл, д) расчет коэффициента, отражающего степень накопления сенесцентных клеток в организме, по формуле:
КСК=(Возраст пациента-65)*(-0,14)+(CD34+%-0,04)*(-2,27)+(2*VCAM-22,95)*(-0,02) (VCAM∧4-277415,52)*(2,15*10∧(-7))+6,27,
е) определение степени накопления сенесцентных клеток у пациентов старше 65 лет: при получении значения КСК меньше 4 пациента относят в группу с низкой степенью накопления сенесцентных клеток в тканях, при значении КСК выше или равно 4 пациента относят в группу с высокой степенью накопления сенесцентных клеток.
2. Способ по п.1, характеризующийся тем, что выделение из периферической крови фракций мононуклеарных клеток и плазмы производят в градиенте плотности на фиколле.
3. Способ по п.1, характеризующийся тем, что для оценки содержания CD34+ клеток используют метод проточной цитометрии.
4. Способ по п.1, характеризующийся тем, что для оценки уровня VCAM используют иммуноферментный анализ.
| СОРОКИНА А.Г | |||
| и др | |||
| Взаимосвязь жесткости магистральных сосудов и биомаркеров накопления сенесцентных клеток у пожилых пациентов | |||
| Кардиология | |||
| Способ получения продуктов конденсации фенолов с формальдегидом | 1924 |
|
SU2022A1 |
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
| WO 2015157247 A1, 15.10.2015 | |||
| РАТУШНЫЙ А.Ю | |||
| Иммунофенотип мезенхимальных стромальных клеток при репликативном старении | |||
| Учен | |||
| зап | |||
| Казан | |||
| ун-та | |||
| Сер | |||
| Естеств | |||
| науки | |||
| Электромагнитный прерыватель | 1924 |
|
SU2023A1 |
| Устройство для отыскания металлических предметов | 1920 |
|
SU165A1 |
Авторы
Даты
2024-12-04—Публикация
2023-10-24—Подача