Настоящее изобретение относится к новым соединениям и радиоактивно меченным комплексам, включающим сайт, связывающий опухолевый антиген, прежде всего фрагмент, связывающий простатоспецифический мембранный антиген, и альбумин-связывающий фрагмент, присоединенные через пригодные линкеры и спейсеры, которые предназначены для применения в качестве диагностических и/или терапевтических радиоактивных фармацевтических препаратов. Более подробно, соединения и комплексы по настоящему изобретению сами по себе можно использовать в качестве (тераностических) индикаторов, визуализирующих агентов и терапевтических агентов для обнаружения экспрессирующих опухолевый антиген клеток-мишеней и тканей-мишеней, а также лечения и диагностики рака, такого как экспрессирующие простатоспецифический мембранный антиген (PSMA) клетки-мишени и ткани-мишени, детектируемые при связанном с PSMA раке, например, раке предстательной железы.
Рак предстательной железы продолжает оставаться наиболее распространенным типом рака у мужчин и третьей по значимости причиной летального исхода от рака в западном мире (Ferlay J., Steliarova-Foucher Е., Lortet-Tieulent J., Rosso S., Coebergh J.W., Comber H., Forman D., Bray F. Cancer incidence and mortality patterns in Europe: estimates for 40 countries in 2012. Eur J Cancer, 49, (6), 1374-1403 (2013); Miller K.D., Siegel R.L., Lin С.C., Mariotto A.В., Kramer J.L., Rowland J.H., Stein K.D., Alteri R., Jemal A. Cancer treatment and survivorship statistics, CA Cancer J Clin, 66, (4), 271-289 (2016). По меньшей мере 1-2 миллиона мужчин в западном полушарии страдают от рака предстательной железы, и, по оценкам, это заболевание поражает каждого шестого мужчины в возрасте от 55 до 85 лет. Ежегодно по данным Американского онкологического общества, в США диагностируются примерно 161000 новых случаев рака предстательной железы. 5-летняя выживаемость пациентов с метастатическим раком предстательной железы IV стадии составляет всего около 29%. Лечение метастатического кастрат-резистентного рака предстательной железы (mCRPC) остается сложным, и вариантов лечения пациентов, достигших этой стадии заболевания, не существует. Следовательно, существует безотлагательная необходимость в разработке новых концепций для эффективного лечения указанного заболевания.
Как только метастатический рак предстательной железы становится гормонорезистентным, остается лишь несколько вариантов лечения, часто с неудовлетворительным клиническим успехом. Согласно действующим медицинским рекомендациям, обычно назначается антимитотическая химиотерапия доцетакселом. Однако лечение часто сопровождается серьезными побочными эффектами и лишь незначительным улучшением выживаемости. Поэтому ранняя диагностика и тщательный мониторинг потенциальных рецидивов имеют решающее значение. Диагноз рака предстательной железы основывается на исследовании гистопатологических или цитологических образцов железы. Существующие методы визуализации для мониторинга прогрессирующего или рецидивирующего рака предстательной железы включают компьютерную томографию (СТ), магнитно-резонансную визуализацию (MRT) и ультразвуковое исследование, часто являются недостаточными для эффективного мониторинга и лечения заболевания. Следовательно, существует высокая клиническая потребность в более эффективных инструментах как для ранней диагностики, так и для лечения рака предстательной железы.
Хорошо известно, что опухолевые клетки могут экспрессировать уникальные белки с модифицированной структурой за счет мутации, или в этих клетках может происходить сверхэкспрессия нормальных (то есть немутированных) белков, которые в норме продуцируются в чрезвычайно малых количествах в доброкачественных клетках. Опухолевые антигены можно в общих чертах разделить на две категории в зависимости от характера их экспрессии: опухолевые антигены (TSA), которые присутствуют только на опухолевых клетках, а не на доброкачественных клетках, и ассоциированные с опухолью антигены (ТАА), которые присутствуют в некоторых опухолевых клетках, а также в доброкачественных клетках. TSA обычно формируются в результате мутации протоонкогенов и опухолевых супрессоров, что приводит к аномальному продуцированию белка, тогда как экспрессия ТАА обычно вызывается мутацией других генов, не связанных с образованием опухоли.
Экспрессия таких белков на поверхности опухолевых клеток дает возможность диагностировать и характеризовать заболевание при обнаружении таких опухолевых маркеров. Белковые связывающие агенты или низкомолекулярные лекарственные средства, включающие визуализируемые метки и специфически распознающие такие опухолевые маркеры, обычно используют для диагностики и визуализации рака в неинвазивных условиях.
Новая многообещающая серия низкомолекулярных визуализирующих агентов направлена на простатоспецифический мембранный антиген (PSMA). PSMA, также известный как фолатгидролаза I (FOLH1), представляет собой трансмембранный гликопротеин типа II из 750 аминокислот. Ген PSMA расположен на коротком плече хромосомы 11 и проявляет функции как фолатгидролазы, так и нейропептидазы. Он проявляет нейропептидазную функцию, эквивалентную глутамат-карбоксипептидазе II (GCPII), которая называется «PSMA мозга», и может модулировать глутаматергическую передачу, расщепляя N-ацетиласпартилглутамат (NAAG) с образованием N-ацетиласпартата (NAA) и глутамата (Nan F. и др. J Med Chem, 43, 772-774 (2000)).
Сверхэкспрессия простатоспецифического мембранного антигена (PSMA) наблюдается во множестве случаев рака предстательной железы (Silver D.А., Pellicer, I., Fair W.R., Heston W.D., Cordon-Cardo С. Prostate-specific membrane antigen expression in normal and malignant human tissues. Clin Cancer Res, 3, (1), 81-85 (1997); Cunha A.C., Weigle В., Kiessling A., Bachmann M., Rieber E.P. Tissue-specificity of prostate specific antigens: comparative analysis of transcript levels in prostate and non-prostatic tissues. Cancer Lett, 236, (2), 229-238 (2006)). Следовательно, PSMA представляет собой перспективную мишень для ядерной визуализации и радионуклидной терапии mCRPC (Bouchelouche K., Choyke P.L. Prostate-specific membrane antigen positron emission tomography in prostate cancer: a step toward personalized medicine. Curr Opin Oncol, 28, (3), 216-221 (2016); Haberkorn U., Eder M., Kopka K., Babich J.W., Eisenhut M. New strategies in prostate cancer: prostate-specific membrane antigen (PSMA) ligands for diagnosis and therapy. Clin Cancer Res, 22, (1), 9-15 (2016); Eiber M., Fendler W.P., Rowe S.P., Calais J., Hofman M.S., Maurer Т., Schwarzenboeck S.M., Kratowchil C., Herrmann K., Giesel F.L. Prostate-specific membrane antigen ligands for imaging and therapy. J Nucl Med, 58, (Suppl 2), 67S-76S (2017)). PSMA (i) в основном ограничен предстательной железой (хотя он также обнаруживается в меньших количествах в новообразованной сосудистой системе многих других солидных опухолей, включая рак мочевого пузыря, поджелудочной железы, легких и почек, но не в нормальной системе новообразованных сосудов), (ii) экспрессируется в большом количестве в виде белка на всех стадиях рака предстательной железы (в количестве до 106 молекул PSMA на опухолевую клетку) (iii) присутствует на поверхности клетки, но не попадает в кровоток, и (iv) связан с ферментативной или сигнальной активностью. Более того, экспрессия PSMA в дальнейшем регулируется с повышением активнгости при плохо дифференцированном, нечувствительном к андрогену или метастатическом раке, и экспрессия обычно коррелирует с прогрессированием заболевания.
Уникальная экспрессия PSMA делает его важным маркером рака предстательной железы (а также некоторых других видов рака). Кроме того, PSMA представляет собой большую внеклеточную мишень для агентов визуализации. Интернализация PSMA происходит после связывания с лигандом, и, таким образом, он является не только отличной мишенью для направленной радионуклидной терапии (с использованием излучающих частицы радионуклидов), но и для других терапевтических стратегий, включая опухолеспецифичную доставку иммунотоксинов, ретаргетинг иммунных клеток и активацию пролекарств, вакцины PSMA, плазмидную ДНК и аденовирусную иммунизацию. Кроме того, в связи с низкими уровнями экспрессии PSMA в здоровых тканях существует возможность использовать его при высокодозной терапии с минимальными побочными эффектами.
В прошлом было разработано несколько PSMA-направленных агентов, несущих терапевтические или диагностические фрагменты. Одобренный FDA радиоиммуноконъюгат моноклонального антитела против PSMA (mAb) 7Е11, известный как PROSTASCINT®, использовали для диагностики метастазов и рецидивов рака предстательной железы. Эффективность этого радиофармацевтического агента ограничена в связи с тем фактом, что это антитело связывается с внутриклеточным доменом PSMA, следовательно, может быть направлено только на мертвые клетки. Более того применение моноклональных антител и фрагментов антител в качестве визуализирующих агентов в большинстве случаев ограничено из-за их медленного почечного клиренса, гетерогенного распределения, низкой проницаемости в опухоль и иммуногенной активности.
Для преодоления этих проблем были разработаны различные низкомолекулярные PSMA-направленные агенты, способные связываться с внеклеточным доменом PSMA для визуализации с использованием позитронно-эмиссионной томографии (РЕТ)/СТ и однофотонной эмиссионной компьютерной томографии (SPECT), включая радиоактивно меченный N-[N-[(S)-1,3-дикарбоксипропил]карбамоил]-S-[11С]метил-1-цистеин (DCFBC) и некоторые пептидомиметики-ингибиторы PSMA на основе мочевины (см. Bouchelouche и др., Discov Med. 9 (44): 55-61 (2010 янв), включая MIP-1095 (Hillier и др., Cancer Res., 69 (17): 6932-6940 (2009 сент. 1)), лиганд PSMA, который в настоящее время находится на стадии клинических исследований, и DOTA-конъюгированный ингибитор PSMA-PSMA617, разработанный, как описано в статье Benesova и др. (JNM, 56: 914-920 (2015) и в патенте ЕР 2862857 А1), который распределяется в организме и быстро выводится из крови (J Nucl Med. 56 (11): 1697-1705 (2015). Однако, хотя быстрый и системный доступ преимущественно способствует направленной доставке и проникновению в опухоль, доступные в настоящее время PSMA-направленные агенты несут риск опосредования неспецифических взаимодействий «вне мишени» в нормальных тканях, экспрессирующих мишень, и накопления радиоактивных фармацевтических препаратов в экскреторных органах (например, почки). Таким образом, неопухолевые ткани могут подвергаться дозам облучения, что в конечном итоге приводит к необратимому повреждению тканей. Было продемонстрировано, что различные радиоактивно меченные низкомолекулярные PSMA-направленные агенты (включая PSMA-617) накапливаются в слезных и слюнных железах пациентов и могут вызывать повреждение железистой ткани, особенно при использовании в сочетании с излучающими альфа-частицы радионуклидами (Zechmann и др., Eur J. Nucl Med Mol Imaging, 41 (7): 1280-1292 (2014) и Kratochwil и др., J. Nucl Med., pii: jnumed.117.191395, (2017 13 апр.) doi: 10.2967/jnumed. 117.191395 [Epub]). Одно из возможных решений этой проблемы включает использование PSMA-связывающих агентов с высоким сродством к PSMA (Kratochwil и др., J Nucl Med., 293-298 (2015) и Chatalic и др., Theragnostics, 6: 849-861 (2016)).
Недавно, концепция модификации радиоактивных фармацевтических препаратов альбумин-связывающим фрагментом была использована для PSMA-направленных радиоактивных лигандов с различными группами (Choy С.J., Ling X., Geruntho, J.J., Beyer S.K., Latoche J.D., Langton-Webster В., Anderson C.J., Berkman С.E. 177Lu-Labeled phosphoramidate-based PSMA inhibitors: the effect of an albumin binder on biodistribution and therapeutic efficacy in prostate tumor-bearing mice. Theranostics, 7, (7), 1928-1939 (2017); Kelly J.M., Amor-Coarasa A., Nikolopoulou A., Wustemann Т., Barelli P., Kim D., Williams C. Jr., Zheng X., Bi. С., Hu В., Warren J.D., Hage D.S., DiMagno S.G., Babich J.W. Double targeting ligands with modulated pharmacokinetics for endoradiotherapy of prostate cancer. J Nucl Med (2017); Benesova M., Umbricht C.A., Schibli R., Muller C. Albumin-binding PSMA ligands: optimization of the tissue distribution profile. Mol Pharm, 15, (3), 934-946 (2018); Umbricht C.A., Benesova M., Schibli R., Muller C. Preclinical development of novel PSMA-targeting radioligands: modulation of albumin-binding properties to improve prostate cancer therapy. Mol Pharm, 15, (6), 2297-2306 (2018). Действительно, для таких радиолигандов наблюдался повышенный уровень циркуляции в крови и таким образом, повышенное накопление в опухолевой ткани и улучшенное удерживание по сравнению с PSMA-связывающими лигандами без альбумин-связывающего фрагмента, такого как соединение 177Lu-PSMA-617 (Benesova М., Umbricht С.A., Schibli R., Muller, С. Albumin-binding PSMA ligands: optimization of the tissue distribution profile. Mol Pharm, 15, (3), 934-946 (2018); Umbricht, C.A., Benesova, M., Schibli R., Muller C. Preclinical development of novel PSMA-targeting radioligands: modulation of albumin-binding properties to improve prostate cancer therapy. Mol Pharm 2018, Mol Pharm, 15, (6), 2297-2306 (2018)). Наблюдался высокий уровень удерживания радиоактивности в кровотоке и, следовательно, накопления в других органах и тканях, включая почки, по сравнению со случаем PSMA-связывающих радиоактивных лигандов в отсутствии альбумин-связывающего фрагмента, такого как 177Lu-PSMA-617 (Benesova М., Umbricht С.A., Schibli R., Muller С. Albumin-binding PSMA ligands: optimization of the tissue distribution profile. Mol Pharm, 15, (3), 934-946 (2018).
Например, в статье Choy и др., Theranostics, 7 (7): 1928-1939 (2017), описано исследование 177Lu-меченного ингибитора PSMA на основе фосфорамидата, включающего альбумин-связывающий фрагмент. Хелатирующий агент DOTA, образующий комплекс с радионуклидом 177Lu, присоединен через эфирную связь к необратимому ингибитору PSMA СТТ1298 (ЕР 2970345 А1). Однако мотив связывания PSMA на основе фосфорамидата проявляет только низкую стабильность, особенно при повышенных температурах (повышенные температуры в широком диапазоне кислотных значений рН, приводят к гидролизу фосфорамидатной связи P-N), которые необходимы в условиях координационного взаимодействия для введения радиоактивной метки с использованием хелатирующих агентов, таких как DOTA. Следовательно, исключено использование прямой реакции для введения радиоактивной метки, и перед введением метки необходимо использовать многоступенчатый подход. Таким образом, следует получить 177Lu-DOTA-азид в качестве предшественника, затем предшественник следует присоединить к мотиву производного PSMA, полученного с использованием дибензоциклооктина. Наконец, необходимо провести тщательную очистку связанного соединения с помощью ВЭЖХ, затем упарить (в атмосфере N2) элюент для ВЭЖХ и растворить полученный продукт в физиологической среде. Эту процедуру, вероятно, нельзя использовать в условиях клинического применения, когда получают препараты с высокой активностью. Данные доклинического биораспределения свидетельствуют о низкой эффективности радиоактивно меченного агента, особенно в отношении соотношения опухоль/почки, которое не превышало 1.
Другой подход описан в статье Kelly и др. (Kelly JM, Amor-Coarasa А., Nikolopoulou A., Wustemann Т., Barelli P., Kim D., Williams С, Jr., Zheng X., Bi С., Hu В., Warren JD, Hage DS, DiMagno SG, Babich JW. Double targeting ligands with modulated pharmacokinetics for endoradiotherapy of prostate cancer J Nucl Med 2017), авторы которой оценивали агенты, проявляющие сродство как к PSMA, так и к альбумину (HSA) сыворотки крови человека. Лиганды, разработанные Kelly и др., содержат фрагмент пара(иодфенил)масляной кислоты для связывания с HSA и фрагмент для связывания PSMA на основе мочевины. В соединениях, разработанных Kelly et al., радиоактивный терапевтический йод (1311) присоединен ковалентной связью к фрагменту, связывающему HSA, который, в свою очередь, напрямую присоединен к фрагменту, связывающему PSMA, через углеводородную цепь. Однако исследуемые соединения в значительной степени ограничены с точки зрения применяемого радионуклида, который ограничен йодом. Кроме того, для исследуемых соединений не было продемонстрировано улучшение интернализации/захвата клетками-мишенями.
Структурный фрагмент, (пара-иодфенил)масляная кислота, как ранее было установлено, связывается с высоким сродством с сывороточным альбумином (Dumelin СЕ, Trussel S., Buller F., Trachsel E., Bootz F., Zhang Y., Mannocci L., Beck SC, Drumea-Mirancea M., Seeliger MW, Baltes C, Muggier Т., Kranz F., Rudin M., Melkko S., Scheuermann J., Neri D. A portable albumin binder from a DNA-encoded chemical library. Angew Chem Int Ed Engl, 47, (17), 3196-31201 (2008). Это соединение использовали для модификации очищенных экспресс-методом фрагментов антител, чтобы увеличить время их циркуляции в кровотоке и, следовательно, улучшить фармакокинетику (Trussel S., Dumelin С., Frey K., Villa A., Buller F., Neri D. New strategy for the extension of the serum half-life of antibody fragments. Bioconjug Chem, 20, (12), 2286-2292 (2009). В случае радиоактивных конъюгатов фолиевой кислоты, модификация с тем же связующим альбумина приводит к значительному увеличению поглощения опухолью и значительному снижению удерживания радиоактивности в почках (Miiller С., Struthers Н., Winiger С., Zhernosekov K., Schibli R. DOTA conjugate with an albumin-binding entity enables the first folic acid-targeted 177Lu-radionuclide tumor therapy in mice. J Nucl Med, 54, (1), 124-131 (2013); Siwowska K., Haller S., Bortoli F., Benesova, M. Groehn V., Bernhardt P., Schibli R., Miiller C. Preclinical comparison of albumin-binding radiofolates: impact of linker entities on the in vitro and in vivo properties. Mol Pharm, 14, (2), 523-532 (2017).
Альбумин-связывающие свойства этих PSMA-радиолигандов проявлялись в большей степени по сравнению с ранее наблюдаемыми свойствами для фолат-радиоконъюгатов, включающих тот же самый альбумин-связывающий фрагмент на основе пара-иодфенила. Поэтому предполагалось, что более слабое связывание лигандов PSMA с сывороточным альбумином будет оказывать благоприятный эффект. Структура радиолиганда была сконструирована при замене альбумин-связывающего фрагмента, (пара-иодфенил)масляной кислоты с высокими связывающими свойствами, на (пара-толил)масляную кислоту, которая, как ранее было установлено, проявляет пониженную альбумин-связывающую аффинность. (Dumelin С.Е., Trussel S., Buller F., Trachsel E., Bootz F., Zhang Y., Mannocci L., Beck S.C., Drumea-Mirancea M., Seeliger M.W., Baltes C., Muggier Т., Kranz F., Rudin M., Melkko S., Scheuermann J., Neri D. A portable albumin binder from a DNA-encoded chemical library. Angew Chem Int Ed Engl, 47, (17), 3196-3201 (2008). Соответственно, соединение 177Lu-PSMA-ALB-56, PSMA-связывающий радиолиганд, включающий пара-толил-фрагмент в качестве альбумин-связывающего фрагмента вместо альбумин-связывающего фрагмента на основе пара-иодфенила, характеризовалось более благоприятными соотношениями опухоль-фон, чем соединение 177Lu-PSMA-ALB-53, которое включало пара-йодфенильный фрагмент (Umbricht С.A., Benesova М., Schibli R., Miiller С.Preclinical development of novel PSMA-targeting radioligands: modulation of albumin-binding properties to improve prostate cancer therapy. Mol Pharm, Mol Pharm, 15, (6), 2297-2306 (2018)). Однако в случае соединения 177Lu-PSMA-ALB-56 в крови наблюдались все еще относительно высокие уровни активности, что может указывать на то, что аффинность связывания с альбумином является все еще слишком высокой.
Эти данные свидетельствуют о необходимости уравновешивания связывания PSMA-связывающего радиолиганда с альбумином для достижения оптимального профиля распределения в тканях с высоким уровнем поглощения опухолью, но при этом уровни активности в крови должны быть не слишком высокими, так как могут представлять риск нежелательных побочных эффектов в здоровой ткани.
Несмотря на успехи, достигнутые на протяжении многих лет, диагностика и лечение рака предстательной железы по-прежнему остаются сложной задачей. Необходимы новые диагностические агенты или визуализирующие агенты с высокой селективностью, направленные на раковые опухолевые клетки и проявляющие благоприятные фармакокинетические свойства для быстрой и неинвазивной визуализации опухоли и терапии, а также для раннего выявления и лечения рака.
Таким образом, цель настоящего изобретения заключается в том, чтобы преодолеть недостатки предшествующего уровня техники и удовлетворить потребности в данной области техники.
Эта задача решается за счет предмета, раскрытого в данном контексте, более конкретно, как изложено в прилагаемой формуле изобретения.
В настоящем изобретении предлагается новый класс PSMA-связывающих радиолигандов, которые включают ибупрофен в качестве альбумин связывающего компонента, PSMA-связывающий фрагмент и хелатирующий фрагмент, образуя таким образом трифункциональное соединение.
Хотя настоящее изобретение подробно описано ниже, следует понимать, что это изобретение не ограничивается конкретными методологиями, протоколами и реагентами, описанными в данном контексте, поскольку их можно изменить. Следует также понимать, что используемая в данном контексте терминология не предназначена для ограничения объема настоящего изобретения, которое ограничивается только прилагаемой формулой изобретения. Если не указано иное, все технические и научные термины, используемые в данном документе, имеют те же значения, которые обычно представляются очевидными для специалистов в данной области техники.
В дальнейшем будут описаны элементы настоящего изобретения. Эти элементы перечислены с конкретными вариантами осуществления, однако следует понимать, что они могут быть объединены любым способом и в любом количестве для создания дополнительных вариантов осуществления. Различные описанные примеры и предпочтительные варианты осуществления не должны ограничивать настоящее изобретение только явно описанными вариантами осуществления. Следует понимать, что настоящее описание поддерживает и охватывает варианты осуществления, которые объединяют явно описанные варианты осуществления с любым количеством раскрытых и/или предпочтительных элементов. Кроме того, любые перестановки и комбинации всех описанных элементов в этой заявке следует рассматривать как раскрытые в описании настоящей заявки, если в контексте не указано иное.
В настоящем изобретении, если не указано иное, различные признаки альтернативных и других вариантов осуществления могут быть объединены друг с другом.
Для ясности и простоты приведены следующие определения. Любая техническая характеристика, упомянутая для этих определений, может относиться к каждому варианту осуществления изобретения. Дополнительные определения и пояснения могут быть специально предоставлены в контексте этих вариантов осуществления.
Определения
В данном описании и в приведенных ниже пунктах формулы изобретения, если в контексте не указано иное, термин «включает» и варианты, такие как «включают» и «включающий», следует понимать как включающий упомянутый элемент, число или стадию, но не исключающий любой другой не упомянутый элемент, число или стадию. Термин «состоит из» представляет собой вариант термина «состоит», из которого исключен любой другой не упомянутый элемент, число или стадия. В контексте настоящего изобретения термин «включает» включает термин «состоит из». Таким образом, термин «включающий» включает термин «содержащий» и «состоящий», например, композиция, «включающая» X, может состоять только из X или может включать какой-либо дополнительный элемент, например, X+Y.
Термин в единственном числе и аналогичные ссылки, использованные в контексте настоящего изобретения (прежде всего в формуле изобретения) означает также множественное число, если в данном контексте не указано иное или явно не противоречит контексту. Перечисление интервалов значений предназначено только для того, чтобы упомянуть все отдельные величины, находящиеся внутри интервала. Если не указано иное, каждая отдельная величина включена в описание, как если бы она была упомянута в отдельности. Никакие формулировки в описании не следует понимать как указывающие на любой не заявленный элемент, существенный для применения настоящего изобретения.
Термин «в основном» не исключает термин «полностью», например, композиция, которая «в основном не содержит» Y, может полностью не содержать Y. При необходимости, термин «в основном» можно исключить из определения по настоящему изобретению.
Термин «приблизительно» по отношению к численному значению х означает х±10%.
Термин «гидроксикарбил» означает остатки углеводородных групп, т.е. радикалы углеводородной цепи, предпочтительно независимо выбранные из группы алкил, алкенил, алкинил, арил и аралкил.
Термин «алкил» включает линейный (прямоцепной), разветвленный и циклический радикалы, содержащие 1-30 атомов углерода, предпочтительно 1-20, 1-15, 1-10, 1-8, 1-6, 1-4, 1-3 или 1-2 атомов углерода. Например, термин «C1-12алкил» означает углеводородный радикал, углеродная цепь которого является прямой или разветвленной или циклической и содержит от 1 до 12 атомов углерода. Конкретные примеры алкильных остатков включают метил, этил, пропил, изопропил, бутил, пентил, гексил, октил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил, гексадецил, гептадецил, октадецил, нонадецил, айкозил, геникозил, докозил, трикозил, тетракозил, пентакозил, гексакозил, гептакозил, октакозил, нонакозил или триакозил, включая их различные разветвленные и/или циклические изомеры, например, изобутил, трет-бутил или изопентил. Циклические алкильные изомеры также включены в термин «циклоалкил», использованный в данном контексте, который означает насыщенные алициклические углеводороды, содержащие 3 атома углерода в цикле. «Замещенные» линейные, разветвленные и циклические алкильные группы также включены в данный термин. Термин дополнительно включает «гетероалкил», означающий алкильные группы, где один или более атомов углерода заменены на гетероатом, такой как, не ограничиваясь только ими, N, О и S. Соответственно, термин дополнительно включает «гетероциклил» или «гетероциклоалкил», означающий неароматические циклические соединения, содержащие три или более членов в цикле, в составе которых один или более циклических атомов углерода заменен на гетероатом, такой как, но не ограничиваясь только ими, N, О и S. Гетероциклические группы включают ненасыщенные, частично насыщенные или насыщенные циклические системы, такие как, например, группы имидазолил, имидазолинил и имидазолидинил. Гетероциклические группы включают, но не ограничиваясь только ими, азиридинил, азетидинил, пирролидил, имидазолидинил, пиразолидинил, тиазолидинил, тетрагидротиофенил, тетрагидрофуранил, диоксолил, фуранил, тиофенил, пирролил, пирролинил, имидазолил, имидазолинил, пиразолил, пиразолинил, триазолил, тетразолил, оксазолил, изоксазолил, тиазолил, тиазолинил, изотиазолил, тиадиазолил, оксадиазолил, пиперидил, пиперазинил, морфолинил, тиоморфолинил, тетрагидропиранил, тетрагидротиопиранил, оксатиан, диоксил, дитианил, пиранил, пиридил, пиримидинил, пиридазинил, пиразинил, триазинил, дигидропиридил, дигидродитиинил, дигидродитионил, гомопиперазинил, хинуклидил, индолил, индолинил, изоиндолил, азаиндолил (пирролопиридил), индазолил, индолизинил, бензотриазолил, бензимидазолил, бензофуранил, бензотиофенил, бензтиазолил, бензоксадиазолил, бензоксазинил, бензодитиинил, бензоксатиинил, бензотиазинил, бензоксазолил, бензотиазолил, бензотиадиазолил, бензо[1,3]диоксолил, пиразолопиридил, имидазопиридил (азабензимидазолил), триазолопиридил, изоксазолопиридил, пуринил, ксантинил, аденинил, гуанинил, хинолинил, изохинолинил, хинолизинил, хиноксалинил, хиназолинил, циннолинил, фталазинил, нафтиридинил, птеридинил, тианафталенил, дигидробензотиазинил, дигидробензофуранил, дигидроиндолил, дигидробензодиоксинил, тетрагидроиндолил, тетрагидроиндазолил, тетрагидробензимидазолил, тетрагидробензотриазолил, тетрагидропирролопиридил, тетрагидропиразолопиридил, тетрагидроимидазолопиридил, тетрагидротриазолопиридил и тетрагидрохинолинил. Гетероциклические группы могут являться замещенными или незамещенными. Типичные замещенные гетероциклические группы могут являться монозамещенными или замещенными более одной группами, такими как, но не ограничиваясь только ими, пиридильные группы или морфолинильные группы, которые являются 2-, 3-, 4-, 5- или 6-замещенными, или дизамещенными различными заместителями, такими как указанные выше заместители.
Термин «циклический» включает термин «полициклический», относящийся к структурам, содержащим более одной циклической структуры. Прежде всего, термин «циклический» означает также спироциклические структуры, где два или более циклов имеют один общий атом, и 5 конденсированных полициклических структур, где два или более циклов имеют по меньшей мере 2 общих атома.
Термин «алкенил», использованный в данном контексте, означает линейный, разветвленный и циклический радикалы, содержащие 2-30 атомов углерода, предпочтительно 2-20, 2-15, 2-10, 2-8, 2-6, 2-4 или 2-3 атомов углерода, включающие по меньшей мере одну двойную связь углерод-углерод. Конкретные примеры «алкенильных» групп включают различные алкенильные ненасыщенные аналоги описанных алкильных групп, названных согласно соглашениям, известным специалистам в данной области техники, в зависимости от числа и расположения двойной связи или связей углерод-углерод, например, бутандиилиден, 1-пропанил-3-илиден. «Алкенильные» группы предпочтительно содержат по меньшей мере 1, более предпочтительно по меньшей мере 2, 3, 4, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 двойных связей, где двойная связь предпочтительно расположена в положении 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28 или 29 углеводородной цепи. Алкенильные группы могут быть замещенными или незамещенными.
Термин «алкинил», использованный в данном контексте, включает прямоцепные, разветвленные и циклические радикалы, содержащие 2-30 атомов углерода, предпочтительно 2-20, 2-15, 2-10, 2-8, 2-6, 2-4 или 2-3 атомов углерода, содержащие по меньшей мере одну тройную связь углерод-углерод. Конкретные примеры «алкинильных» групп включают различные алкенильные ненасыщенные аналоги описанных алкильных и алкенильных групп, названных согласно соглашениям, известным специалистам в данной области техники, в зависимости от числа и расположения тройной связи или связей углерод-углерод. «Алкинильные» группы предпочтительно содержат по меньшей мере 1, более предпочтительно по меньшей мере 2, 3, 4, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 тройных связей, где тройная связь предпочтительно расположена в положении 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28 или 29 углеводородной цепи. Алкинильные группы могут быть замещенными или незамещенными.
Термин «арил» означает моноциклическую или полициклическую или конденсированную полициклическую ароматическую кольцевую систему. Термин включает моноциклическую или полициклическую или конденсированную полициклическую ароматическую «гетероарильную» кольцевую систему, где по меньшей мере один атом углерода в цикле заменен на гетероатом. Обычно термины «арил» и «гетероарил» означают группы, содержащие от 3 до 30 атомов углерода, такие как от 3 до 10, предпочтительно от 2 до 6 атомов углерода.
Термины «арилалкил» или «аралкил» используют в данном контексте взаимнозаменяемо и они означают группы, включающие по меньшей мере одну алкильную группу и по меньшей мере одну арильную группу, как описано в данном контексте. В аралкильной группе, как описано в данном контексте, аралкильная группа соединена с другим остатком соединений или конъюгатов по настоящему изобретению через алкильную группу, как показано на примере бензильной группы.
Термин «галоген» или «гало», использованный в данном контексте, включает фтор (F), хлор (Cl), бром (Br), иод (I).
Термин «гетероатом» включает N, О, S и Р, предпочтительно N и О.
Термин «замещенный» означает гидрокарбильную группу, как определено в данном контексте (например, алкильную или алкенильную группу), где одна или более связей с атомом водорода, содержащегося в ней, заменены на связь с другими атомами, которые не являются углеродом и водородом. Замещенные группы включают также группы, в которых одна или более связей с атомом(ами) углерода или водорода заменены на одну или более связей, включая двойные или тройные связи, с гетероатомом. Таким образом, «замещенная» группа является замещенной одним или более заместителей, если не указано иное. В некоторых вариантах замещенная группа замещена 1, 2, 3, 4, 5 или 6 заместителями. Примеры групп заместителей включают галогены (т.е. F, Cl, Br и I), гидроксильные группы, алкоксигруппы, алкеноксигруппы, алкиноксигруппы, арилоксигруппы, аралкилоксигруппы, гетероциклилоксигруппы и гетероциклилалкоксигруппы, карбонильные группы (оксо), карбоксиьные группы, сложноэфирные группы, уретановые группы, оксимные группы, гидроксиламинные группы, алкоксиаминные группы, аралкоксиаминные группы, тиоловые группы, сульфидные группы, сульфоксидные группы, сульфоновые группы, сульфонильные группы, сульфонамидные группы, аминогруппы, N-оксидные группы, гидразиновые группы, гидразидные группы, гидразонные группы, азидные группы, амидные группы, мочевинные группы, амидиновые группы, гуанидиновые группы, енаминовые группы, имидные группы, изоцианатные группы, изотиоцианатные группы, цианатные группы, тиоцианатные группы, иминогруппы, нитрогруппы, нитрильные группы (т.е. CN), галогеналкильные группы, аминоалкильные гуппы, гидроксиалкильные группы и циклоалкильные группы.
Соединения
В первом объекте настоящего изобретения предлагается соединение общей формулы (1)(i) или (1)(ii):
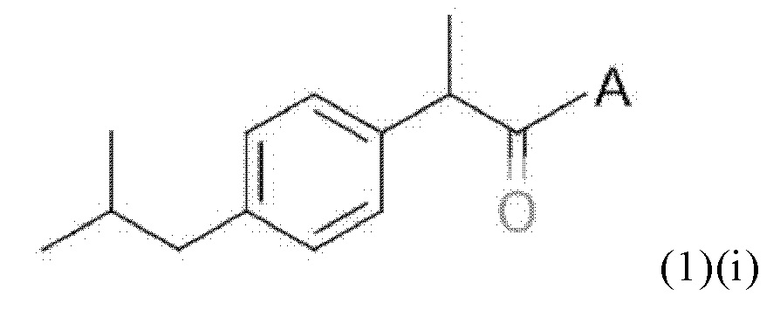
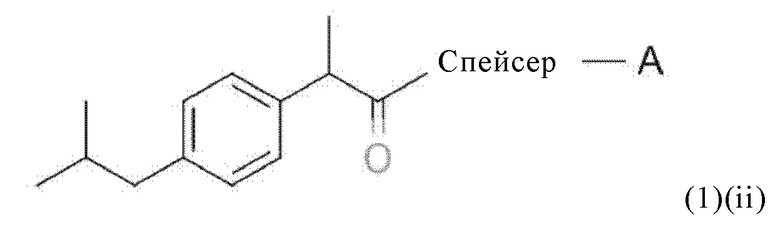
где А означает диагностический или терапевтический агент, включающий участок связывания с опухолевым антигеном, и спейсер, включающий по меньшей мере одну связь C-N.
Соответственно, в настоящем изобретении предлагаются лиганды опухолевого антигена, связывающиеся с белками плазмы (предпочтительно, связывающиеся с белками плазмы лиганды PSMA) с благоприятными фармакокинетическими профилями. Термин «фармакокинетика», использованный в данном контексте, предпочтительно означает стабильность, биодоступность, абсорбцию, биораспределение, период биологического полураспада и/или клиренс терапевтического или диагностического агента в организме субъекта.
В предшествующем уровне техники связывающиеся с альбумином фрагменты использовали для увеличения полупериода циркуляции конъюгатов, для влияния на компартментализацию конъюгатов в крови и для улучшения доставки в экспрессирующие опухолевый антиген клетки-мишени или ткани-мишени, что приводит к возрастанию соотношений опухоль/не мишень для экспрессирующих опухолевый антиген нормальных (не опухолевых) органов. Соответственно, не привязываясь к какой-либо теории, предполагается, что связывающие альбумин фрагменты, используемые в конъюгатах, придают конъюгату улучшенные фармакокинетические свойства. Однако, связывающие альбумин фрагменты из предшествующего уровня техники, используемые в конъюгатах, могут приводить к отчетливому фоновому сигналу (и, таким образом, к нежелательным соотношениям опухоль/фон).
Следовательно, цель данного исследования заключалась в замене ранее использованных связующихся с альбумином агентов на другие связующиеся с альбумином агенты, чтобы найти оптимум между альбумин связывающими свойствами и клиренсом конъюгата (и, например, его радиоактивностью) из фоновых органов и тканей. Авторы настоящего изобретения неожиданно установили, что ибупрофен в качестве связывающего альбумин фрагмента в составе связывающих опухолевый антиген радиолигандов обеспечивает требуемый баланс между свойствами связывания с белками плазмы и клиренсом радиоактивности из фоновых тканей и органов. Это оказалось чрезвычайно неожиданным, так как ранее предполагалось, что ибупрофен теряет свою альбумин-связывающую аффинность при попытках модификации карбоксильной группы молекулы для присоединения ибупрофена к другим остаткам с биофармацевтическими свойствами (см. заявку WO 2008/053360 А2, патент США №2010/172844 и статью Dumelin С.Е., Trussel S., Buller F., Trachsel E., Bootz F., Zhang Y., Mannocci L., Beck S.C., Drumea-Mirancea M., Seeliger M.W., Baltes C., Muggier Т., Kranz F., Rudin M., Melkko S., Scheuermann J., Neri D., A portable albumin binder from a DNA-encoded chemical library, Angew Chem Int Ed Engl, т. 47, №17, cc. 3196-3201 (2008)). Несмотря на это техническое предубеждение, авторами настоящего изобретения было неожиданно установлено, что сбалансированное связывание с альбумином можно обеспечить при соединении ибупрофена через его карбоксильную группу с диагностическим или терапевтическим агентом, включающим участок связывания с опухолевым антигеном.
Альбумин, прежде всего сывороточный альбумин человека (HSA), представляет собой наиболее распространенный белок в плазме (человека) и составляет примерно половину сывороточных белков. Термин «сывороточный альбумин человека» или «НСА», использованный в данном контексте, предпочтительно означает сывороточный белок альбумин, кодируемый геном человека ALB. Более предпочтительно, этот термин относится к белку, охарактеризованному в базе UniProt Асе. № Р02768 (начальная версия 240, последнее изменение 10 мая 2017, или его функциональные варианты, изоформы, фрагменты или (посттрансляционные или иным образом модифицированные) или производные.
Диагностический или терапевтический агент А, использованный в данном контексте, может представлять собой любой агент, используемый в диагностике, профилактике или лечении заболевания (прежде всего рака), пока он включает участок связывания с опухолевым антигеном.
Опухолевые антигены представляют собой белки, которые экспрессируются опухолевыми клетками и могут характеризоваться модифицированной структурой за счет мутации, или которые могут сверхэкспрессироваться по сравнению с нормальными (т.е. не мутироваными) белками, которые обычно продуцируются в экстремально малых количествах в доброкачественных клетках. Опухолевые антигены можно в широком смысле классифицировать на две категории на основании характера их экспрессии: опухолеспецифичные антигены (TSA), которые присутствуют только в опухолевых клетках, и отсутствуют в незлокачественных клетках, и опухолеассоциированные антигены (ТАА), которые присутствуют в некоторых опухолевых клетках и также в незлокачественных клетках. TSA обычно появляются в результате мутации протоонкогенов и опухолевых супрессоров, что приводит к аномальному продуцированию белка, в то время как экспрессию ТАА обычно вызывает мутация других генов, несвязанных с образованием опухоли. Предпочтительно, опухолевый антиген представляет собой простатоспецифичный мембранный антиген (PSMA). Соответственно, предпочтительно, чтобы диагностический или терапевтический агент А включал участок связывания с PSMA.
Кроме сайта связывания для опухолевого антигена диагностический или терапевтический агент А может включать другие компоненты, такие как (другой) активный компонент (для диагностики, профилактики или лечения заболевания, такого как рак) и/или один или более линкеров. Один или более линкеров или спейсеров можно использовать для объединения в одной молекуле различных компонентов, таких как связующиеся с опухолевым антигеном фрагменты, один или более других активных компонентов и, необязательно, ибупрофен в качестве связующегося с альбумином. Например, связующийся с опухолевым антигеном фрагмент, такой как связующийся с PSMA фрагмент (например, как описано в данном контексте), можно присоединять к линкеру, как описано в данном контексте. Например, ибупрофен можно присоединять к спейсеру, как описано в данном контексте.
Предпочтительно, диагностический или терапевтический агент А включает радиометку. Термин «радиоактивный маркер» (или радиоактивная метка), использованный в данном контексте, означает радиоактивную метку, такую как радиоактивное вещество или радиоактивный атом (например, радионуклид). Например, радиоактивная метка может представлять собой неметаллический радионуклид или радиоактивный металл. В то время, как неметаллические радионуклиты, такие как 18F, 11С, 13N, 15O или 124I, можно ковалентно присоединить к органической молекуле, радиоактивные металлы, такие как 99mTc, 67/68Ga, 111In или 177Lu, обычно необходимо координировать через так называемый хелатирующий фрагмент. Соответственно, прежде всего, если диагностический или терапевтический агент А содержит радиоактивный металл в качестве радиометки, то предпочтительно, чтобы диагностический или терапевтический агент А содержал хелатирующий фрагмент. Хелатирующий фрагмент можно соединять с другими компонентами диагностического или терапевтического агента А (с таким как сайт связывания с опухолевым антигеном и\или с ибупрофеном) через линкер. Например, диагностический или терапевтический агент А может включать радиоактивный металл, координированный через хелатирующий фрагмент. Предпочтительно, хелатирующий фрагмент соединен с другими компонентами диагностического или терапевтического агента А (таким как сайт связывания с опухолевым антигеном и/или с ибупрофеном) через линкер.
Термины «лиганд опухолевого антигена» (например, «лиганд PSMA»), «соединение» и «конъюгат» используют взаимозаменяемо и они означают целую молекулу (включая по меньшей мере сайт связывания с опухолевым антигеоми ибупрофен и, необязательно, другие компоненты).
Прежде всего, лиганды опухолевого антигена (такие как лиганды PSMA) по настоящему изобретению (также как «конъюгаты» или «соединения», названные в данном контексте) могут включать:
- первую концевую группу (хелатирующий фрагмент, например, для координации с радиоактивным металлом или координированный с радиоактивным металлом),
- вторую концевую группу (ибупрофен в качестве связывающегося с альбумином фрагмента), и
- третью концевую группу (связывающийся с опухолевым антигеном, такой как фрагмент, связывающийся с PSMA),
ковалентно связанные или соединенные с каждой другой группой через соответствующие линкеры или спейсеры.
Соответственно, в настоящем изобретении предлагается соединение общей формулы (1)(а):
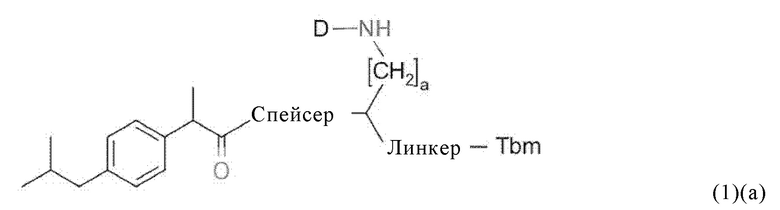
где D означает хелатирующий фрагмент,
Tbm означает остаток, связывающийся с опухолевым антигеном (также называемый связывающимся с опухолевым антигеном фрагментом),
Линкер означает линкер, предпочтительно включающий циклическую группу или ароматическую группу,
Спейсер означает спейсер, включающий связь C-N, и
а означает число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, предпочтительно 0 или 1,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
В общей формуле (1)(а) три концевых группы (ибупрофен, хелатирующий фрагмент (D) и остаток, связывающийся с опухолевым антигеном (Tbm)) соединены через линкер и спейсер, как показано в общей формуле (1)(а) в "точке разветвления" (группа СН):
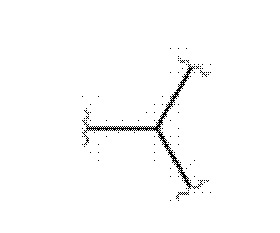
Положение «точки разветвления» (группа СН) в формуле (1)(а) указано ниже стрелкой:
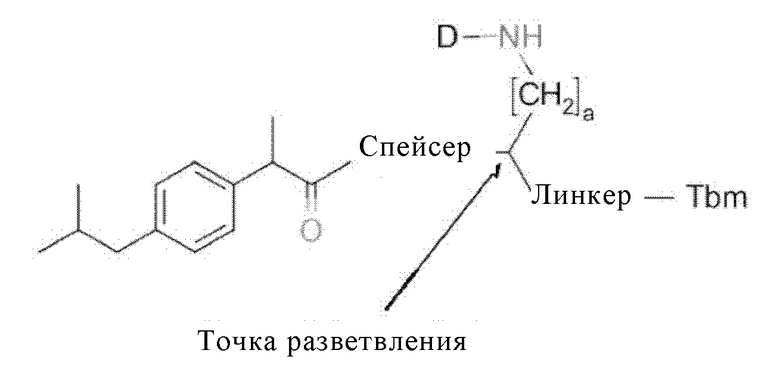
Хелатирующий фрагмент D, остаток, связывающийся с опухолевым антигеном Tbm, линкер и спейсер характеризуются предпочтительными определениями, как описано в данном контексте.
Остатком, связывающимся с опухолевым антигеном (Tbm), предпочтительно является остаток, связывающийся с PSMA (Pbm).
Индекс а предпочтительно выбирают из 0, 1, 2, 3, 4 или 5, более предпочтительно 0, 1 или 2, и наиболее предпочтительно а равен 0.
Следует особо отметить, что структура, отмеченная пунктирной линией в формуле (1)(а), приведенной ниже, включает по меньшей мере одну пептидную связь.
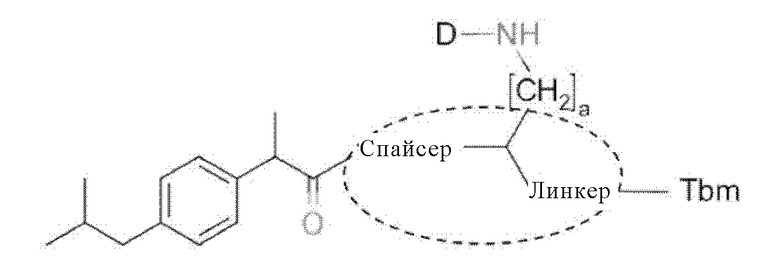
Конъюгаты по настоящему изобретению представляют собой лиганды, проявляющие аффинность как к опухолевому антигену (такому как PSMA), так и к HSA. Термин «лиганд», использованный в данном контексте, означает соединение, способное взаимодействовать (направляться к, связываться с) с мишенью (в данном контексте: HSA или опухолевый антиген, например, PSMA). Конъюгаты по настоящему изобретению можно также определить в отношении их функции как «агенты, направленные на опухолевый антиген» (такие как «агенты, направленные на PSMA»). Предпочтительно, «лиганды» способны селективно связываться с их мишенью. Термин «селективное связывание» означает, что соединение связывается с его мишенью с большей аффинностью по сравнению со связыванием с другим соединением, которое не является для него мишенью.
«Аффинность связывания» представляет собой интенсивность связывающего взаимодействия между лигандом (например, малой органической молекулой, белком или нуклеиновой кислотой) с его мишенью/компонентом связывания. Аффинность связывания обычно измеряют и регистрируют в виде равновесной константы диссоциации (KD), которая представляет собой отношение "скорости диссоциации" (k0ff) к «скорости ассоциации» (kon), которое используют для оценки и ранжирования интенсивности бимолекулярных взаимодействий. «Скорость ассоциации» (Kon) характеризует, насколько быстро лиганд связывается со своей мишенью, а «скорость диссоциации» (Koff) характеризует, насколько быстро происходит диссоциация лиганда и его мишени. KD(Koff/Kon) и аффинность связывания обратно пропорциональны. Таким образом, термин «селективное связывание» предпочтительно означает, что лиганд связывается с его мишенью с KD, меньшей по сравнению с KD его связывания с другим соединением, которое не является его мишенью. Существует много способов измерения аффинности связывания и констант диссоциации, такие как ИФА, анализ задержки электрофоретического сдвига в геле, анализ с соосаждением, равновесный диализ, аналитическое ультрацентрифугирование, поверхностный плазмонный резонанс и спектроскопические методы анализа.
В контексте настоящего изобретения KD связывания фрагмента, связывающегося с опухолевым антигеном, такого как фрагмент, связывающийся с PSMA, с веществом, не являющимся его мишенью, могут превышать по меньшей мере в 1,5 раза, предпочтительно по меньшей мере в 2-, 3-, 5-, 10-, 15-, 20-, 25-, 30-, 35-, 40-, 45-, 50-, 60-, 70-, 80-, 90-, 100- 200-, 300-, 400-, 500-, 750-, или 1000 раз KD связывания указанного конъюгата или остатка с опухолевым антигеном, например, PSMA человека. Аналогичным образом, KD связывания остатка, связывающегося с HAS, с соединением, не являющимся его мишенью, может превышать по меньшей мере в 1,5 раза, предпочтительно по меньшей мере в 2-, 3-, 5-, 10-, 15-, 20-, 25-, 30-, 35-, 40-, 45-, 50-, 60-, 70-, 80-, 90-, 100-200-, 300-, 400-, 500-, 750- или в 1000 раз KD связывания указанного конъюгата или фрагмента с HSA.
В контексте настоящего изобретения конъюгаты могут связываться с опухолевым антигеном (например, PSMA) с большей аффинностью связывания по сравнению с альбумином (HSA). Например, конъюгаты могут связываться с PSMA с высокой аффинностью связывания с величинами KD в наномолярном (нМ) интервале и с умеренной аффинностью с HSA в микромолярном (мкМ) интервале.
Более конкретно предпочтительным является достижение баланса между аффинностями связывания с PSMA и HSA для повышения захвата опухолью, и при этом обеспечить снижение потенциально повреждающих эффектов вне мишени. Прежде всего, конъюгаты по настоящему изобретению могут проявлять более высокую аффинность связывания с PSMA по сравнению со связыванием с HSA.
Связывающийся с PSMA фрагмент
Конъюгаты по настоящему изобретению включают сайт связывания с антигеном, Tbm), который предпочтительно представляет собой фрагмент связывания с PSMA (называемый также «связывающимся с PSMA фрагментом»).
Фрагмент связывания с PSMA предпочтительно характеризуется селективным связыванием с PSMA человека. Определение термина «селективное связывание» приведено выше.
Фрагмент связывания с PSMA может обратимо или необратимо связываться с аффинностью связывания обычно менее приблизительно 100 мкМ (микромолярная концентрация).
Простатоспецифичный мембранный антиген человека (PSMA) (так называемая глутаматкарбоксипептидаза II (GCPII), фолат гидролаза 1, фолил поли-гамма-глутаматкарбоксипептидаза (FGCP), и N-ацетилированная связанная в альфа-положении кислотная дипептидаза I (NAALADase I)) представляют собой трансмембранную цинк-металлопептидазу типа II, которая наиболее интенсивно экспрессируется в нервной системе, предстательной железе, почках и в тонком кишечнике. Ее рассматривают в качестве опухолевого маркера при раке предстательной железы. Термин «простатоспецифичный мембранный антиген человека» или «PSMA», использованный в данном контексте, предпочтительно означает белок, кодируемый геном FOLH1 человека. Более предпочтительно, этот термин означает белок, охарактеризованный в базе UniProt Асе. No. Q04609 (начальная версия 186, последнее изменение 10 мая 2017 г, или его функциональные варианты, изоформы, фрагменты или (посттрансляционные или иным способом модифицированные) производные.
Связывающийся с PSMA фрагмент может обычно представлять собой фрагмент связывания, способной к селективному (и необязательно необратимо) связыванию с мембранным простатоспецифичным антигеном человека (см. статью Chang Rev Urol., т. 6, вып. 10, сс. S13-S18 (2004)).
Фрагмент, связывающийся с PSMA, предпочтительно выбирают по его способности придавать селективную аффинность к PSMA. Предпочтительные связывающиеся с PSMA фрагменты описаны в заявках WO 2013/022797 А1, WO 2015/055318 А1 и в патенте ЕР 2862857 А1, которые в полном объеме включены в данное описание в качестве ссылок.
Соответственно в конъюгате по настоящему изобретению фрагмент, связывающися с PSMA, можно охарактеризовать общей формулой (3), (3)', (3)" или (3)"':
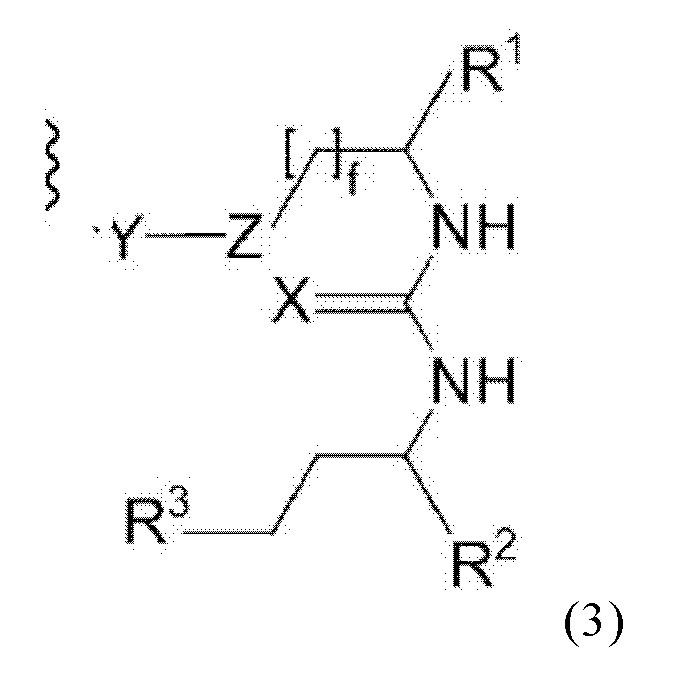
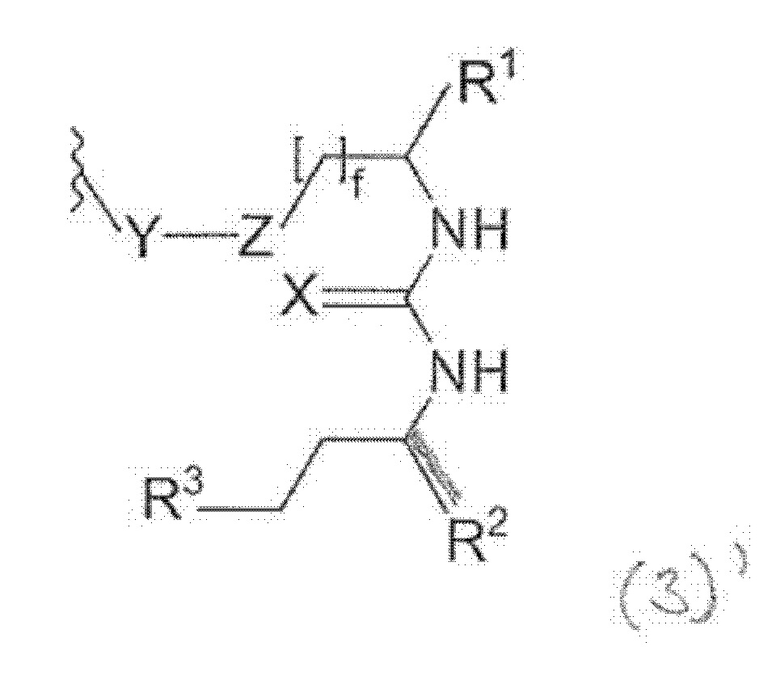
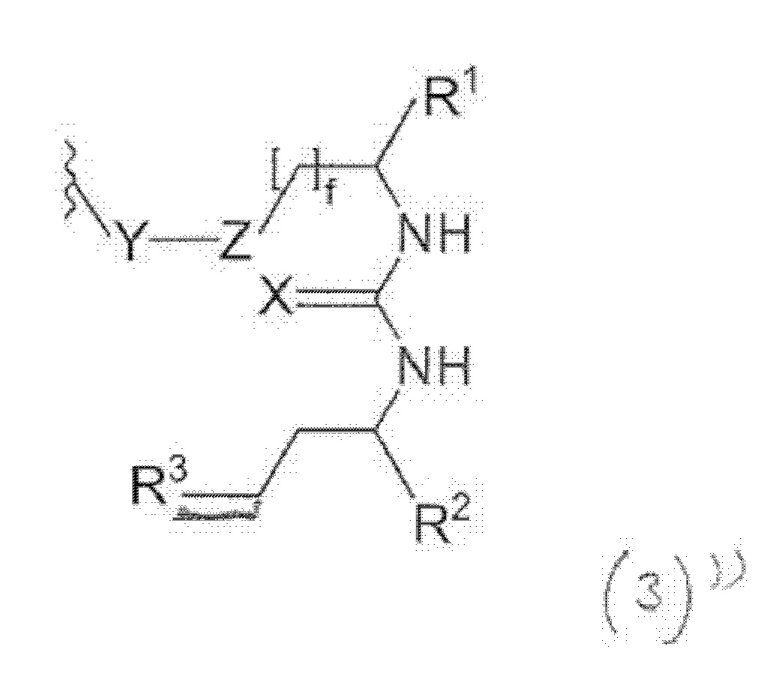
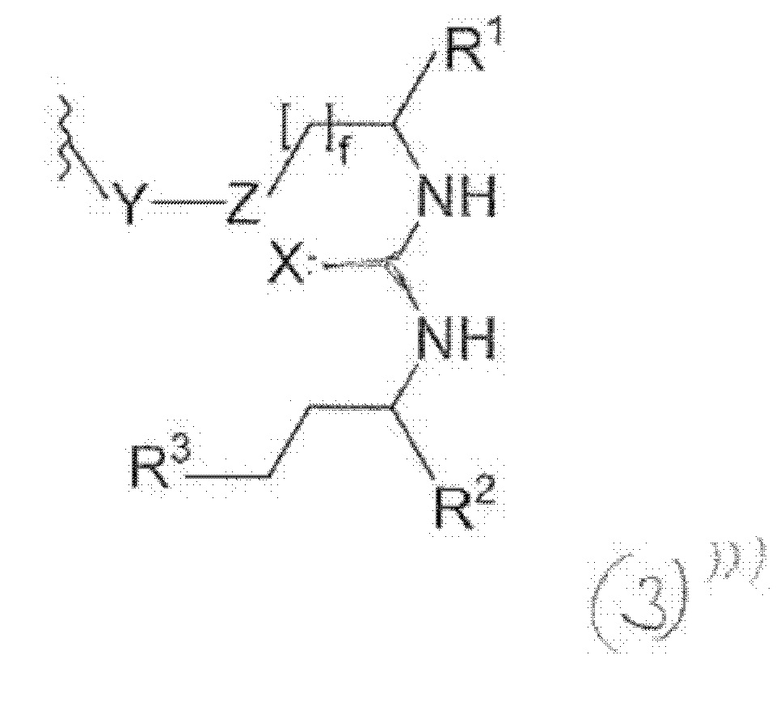
где
X и Y каждый независимо выбирают из О, N или NH или NH2, S или Р,
Z выбирают из замещенной или незамещенной группы СН2,
R1, R2 и R3 каждый независимо выбирают из -СОН, -CO2H, -SO2H, -SO3H, -SO4H, -PO2H, -РО3Н, -PO4H2, -С(O)-(С1-С10)алкил, -С(O)-O(С1-С10)алкил, -С(О)-NHR4, или -C(O)-NR4R5, где R4 и R5 каждый независимо выбирают из Н, связь, (С1-С10)алкилен, F, Cl, Br, I, С(О) или -СН(О), C(S) или -CH(S), -C(S)-NH-бензил-, -С(O)-NH-бензил, -С(O)-(С1-С10)алкилен, -(CH2)p-NH, -(CH2)p-(C1-С10)алкилен, -(CH2)p-NH-C(O)-(CH2)q, -(CHrCH2)t-NH-C(O)-(CH2)p, -(СН2)р-СО-СОН, -(СН2)р-СО-CO2H, -(CH2)p-C(O)NH-C[(CH2)q-COH]3, -С[(СН2)р-СОН]3, -(CH2)p-C(O)NH-C[(CH2)q-CO2H]3, -С[(СН2)р-CO2H]3 или -(СН2)p-(С5-С14)гетероарил, и
f, р, q, r и t каждый независимо означает число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10.
Для приведенных выше общих формул (3)(i)', (3)(ii)" или (3)(iii)"': R2-((3)') или R3 ((3)") присоединены через двойные связи. В формуле (3)"' X присоединен через одинарную связь.
В отношении X и Y следует понимать, что О, N, S или Р при необходимости могут включать атомы водорода. Например, Y может означать О или NH.
Предпочтительно, f означает число, выбранное из 1, 2, 3, 4 или 5, более предпочтительно f равно 2 или 3.
Как отмечено выше, Z выбирают из замещенной или незамещенной группы СН2. Другими словами, Z выбирают из группы СН2 или замещенной группы СН2, в которой один или оба атома водорода могут быть замещены. Например, Z означает СН2 или С=O.
Предпочтительно, Y означает NH и Z означает СН2. Соответственно, фрагмент, связывающийся с PSMA, может быть охарактеризован общей формулой (3)(ii):
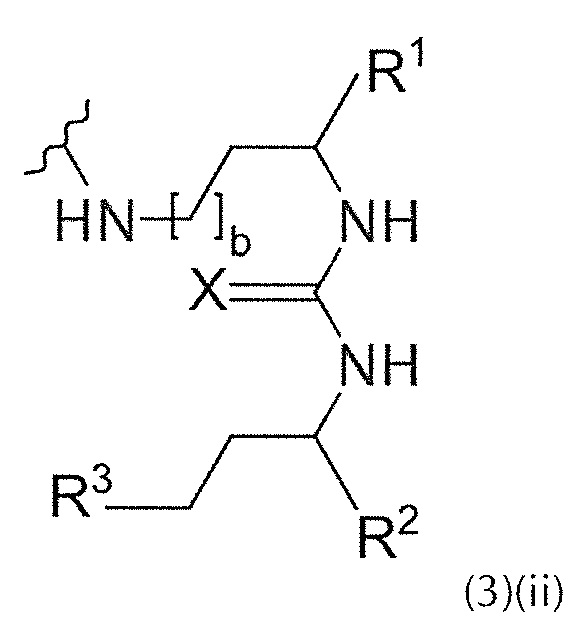
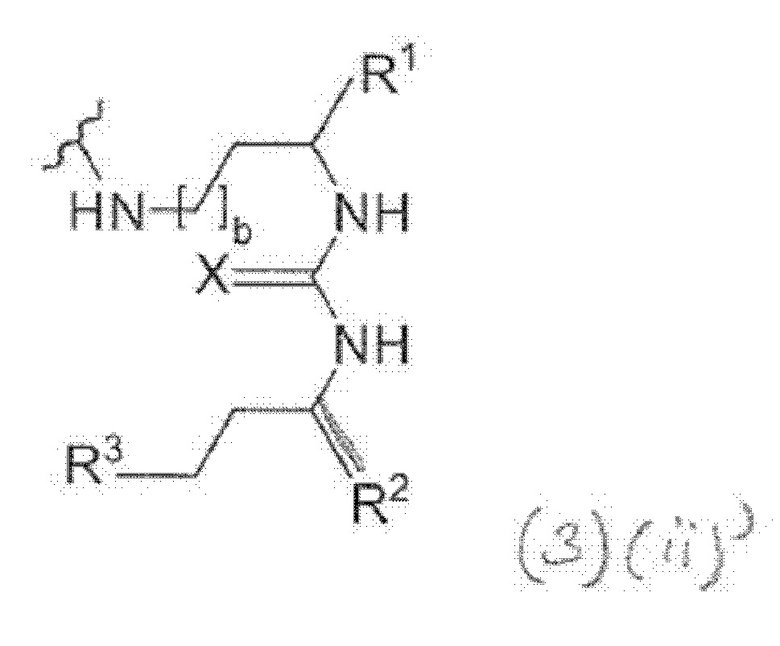
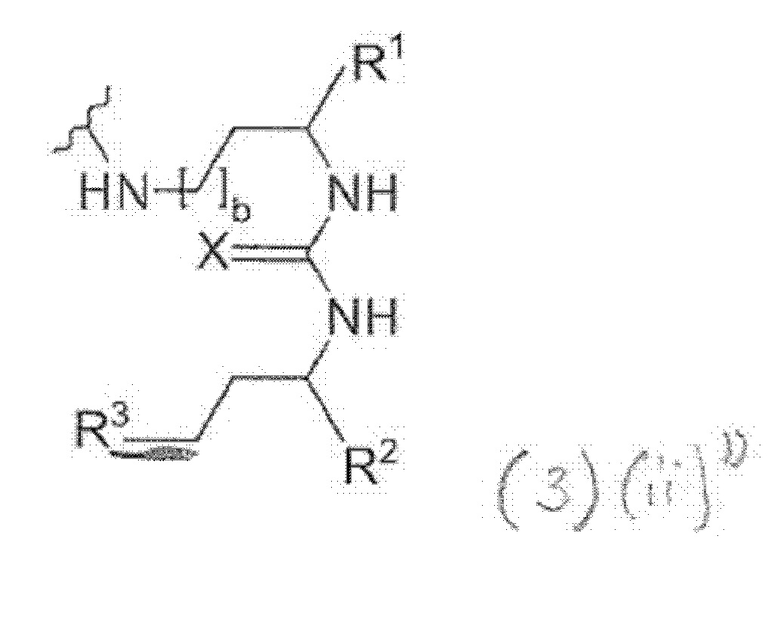
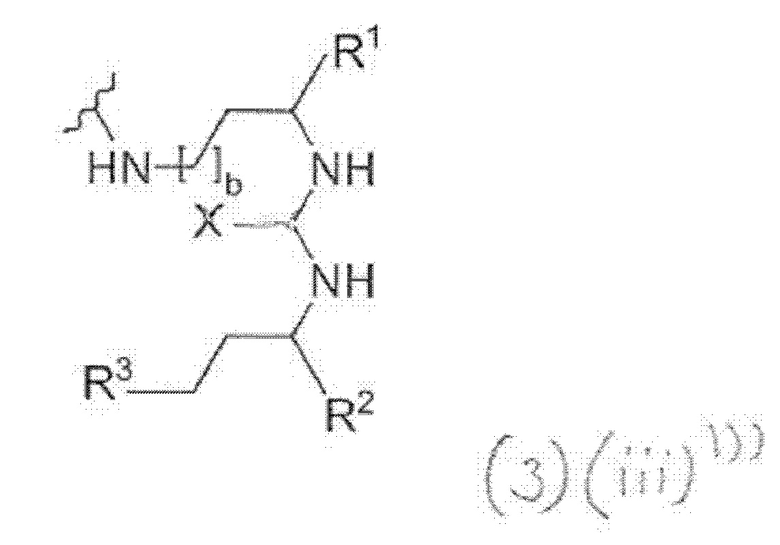
где
X выбирают из О, N или NH или NH2, S или Р,
R1, R2 и R3 каждый независимо выбирают из -СОН, -СО2Н, -SO2H, -SO3H, -SO4H, -PO2H, -РО3Н, -PO4H2, -С(O)-(С1-С10)алкил, -С(O)-O(С1-С10)алкил, -С(О)-NHR4, или -C(O)-NR4R5, где R4 и R5 каждый независимо выбирают из Н, связь, (С1-С10)алкилен, F, Cl, Br, I, С(О) или -СН(О), C(S) или -CH(S), -C(S)-NH-бензил-, -С(O)-NH-бензил, -С(O)-(С1-С10)алкилен, -(CH2)p-NH, -(CH2)p-(C1-С10)алкилен, -(CH2)p-NH-C(O)-(CH2)q, -(CHrCH2)t-NH-C(O)-(CH2)p, -(СН2)р-СО-СОН, -(СН2)р-СО-CO2H, -(CH2)p-C(O)NH-C[(CH2)q-COH]3, -С[(СН2)р-СОН]3, -(CH2)p-C(O)NH-C[(CH2)q-CO2H]3, -С[(СН2)р-CO2H]3 или -(СН2)p-(С5-С14)гетероарил, и
b, р, q, r и t каждый независимо означает число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10.
Для приведенных выше общих формул (3)(i)', (3)(ii)" или (3)(iii)"': R2-((3)') или R3 ((3)") присоединены через двойные связи. В формуле (3)"' X связан через одинарную связь.
В общих формулах (3) и (3)(ii) X предпочтительно означает О.
Более того, предпочтительно в общих формулах (3) и (3)(ii), чтобы R1, R2 и R3 каждый независимо был выбран из -СОН, -CO2H, -SO2H, -SO3H, -SO4H, -РО2Н, -РО3Н, -РО4Н2. Более предпочтительно в общих формулах (3) и (3)(ii) каждый из R1, R2 и R3 означает -СООН.
В общей формуле (3)(ii) b предпочтительно означает число, выбранное из 1, 2, 3, 4 или 5, более предпочтительно b равен 2, 3 или 4, и наиболее предпочтительно b равен 3.
Предпочтительно также в общей формуле (3)(ii), чтобы R1, R2 и R3 каждый означал СООН, X означал О, и b равен 3.
Соответственно, связывающийся с PSMA фрагмент наиболее предпочтительно характеризуется формулой (3)(а):
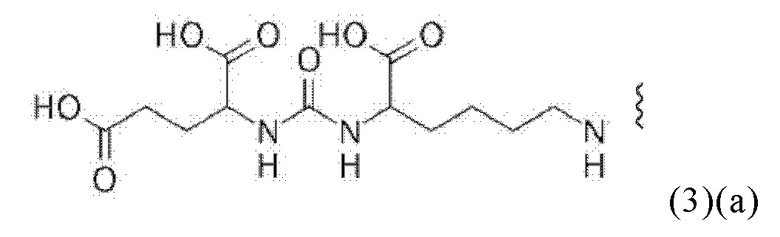
В виде другого особого примера остаток связывания с PSMA может также характеризоваться формулой (3)(b):
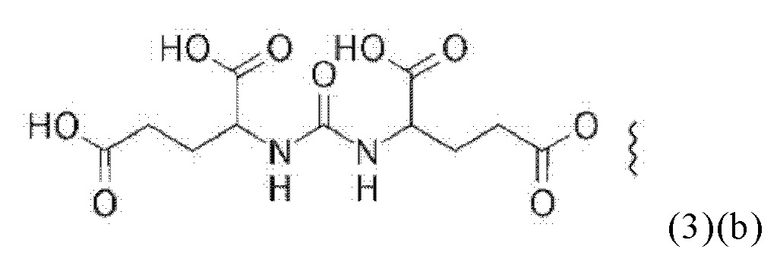
В связи с вышеизложенным в настоящем изобретении также предлагается соединение общей формулы (1)(d):
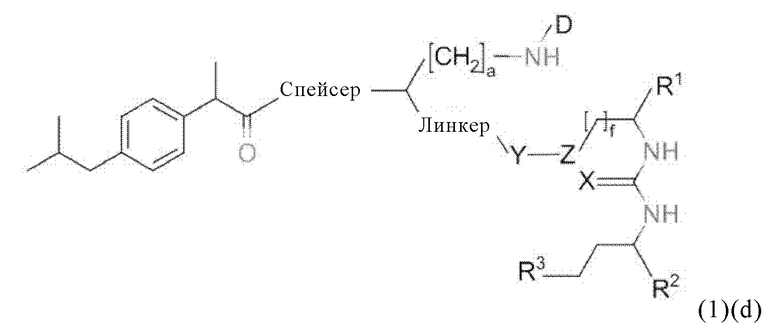
где D, спейсер, линкер и индекс а имеют значения, приведенные для общей формулы (1)(а) (и, предпочтительно, его вариантов), и X, Y, Z, R1, R2, R3 и f имеют значения, как описано для общей формулы (3) (и, предпочтительно, его вариантов),
или его фармацевтически приемлемые соли, сложные эфиры, сольваты или радиоактивно меченные комплексы.
Прежде всего в настоящем изобретении также предлагается соединение общей формулы (1)(е):
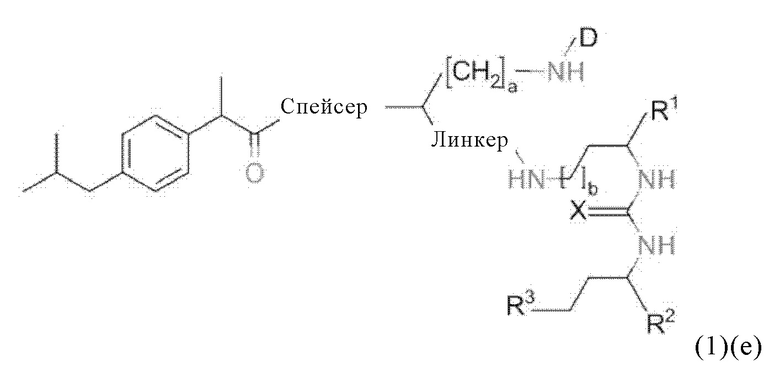
где D, спейсер, линкер и индекс а имеют значения, приведенные для общей формулы (1)(а) (и предпочтительно ее вариантов) и X, R1, R2, R3 и индекс b имеют значения, приведенные для общей формулы (3)(ii) (и предпочтительно ее вариантов),
или его фармацевтически приемлемые соли, сложные эфиры, сольваты или радиоактивно меченные комплексы.
Например, в настоящем изобретении предлагается также соединение общей формулы (1)(f):
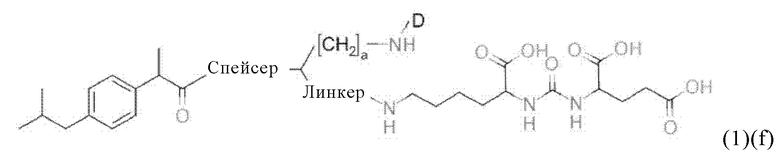
где D, спейсер, линкер и индекс а имеют значения, приведенные для общей формулы (1)(а) (и предпочтительно ее вариантов),
или его фармацевтически приемлемые соли, сложные эфиры, сольваты или радиоактивно меченные комплексы.
Линкер
В конъюгатах по настоящему изобретению связывающийся с опухолевым антигеном фрагмент (например, связывающийся с PSMA фрагмент) может быть присоединен/связан с «точкой разветвления» через пригодный линкер. В описании, приведенном ниже, термин «линкер» используют для описания группы, соединяющей или связывающей и, таким образом, заполняющий расстояние между связывающимся с опухолевым антигеном (например, связывающимся с PSMA фрагментом) и «точкой разветвления» -СН- и/или «разделяя» связывающийся с опухолевым антигеном фрагмент (например, связывающийся с PSMA фрагмент) от остального конъюгата.
Линкер может предпочтительно исключить стерическое препятствие между связывающимся с опухолевым антигеном фрагментом (например, связывающимся с PSMA фрагментом) и другими группами или фрагментами в конъюгате по настоящему изобретению и обеспечивать достаточную подвижность и гибкость. Кроме того, линкер можно предпочтительно конструировать для придания, поддержки и/или обеспечения достаточного связывания с HSA, высокой аффинности связывания с опухолевым антигеном (например, с PSMA) и быстрого и необязательно селективного проникновения, положительных к опухолевому антигену клеток (например, PSMA-) за счет интернализации соединения по настоящему изобретению.
Прежде всего связывающиеся с PSMA фрагменты, такие как связывающиеся с PSMA фрагменты общей формулы (3) или (3)(ii), могут предпочтительно быть присоединены к конъюгату по настоящему изобретению через пригодный линкер, как описано, например, в патенте ЕР 2862857 А1. Указанный линкер может предпочтительно придавать конъюгату по настоящему изобретению оптимизированные липофильные свойства для повышения связывания с PSMA и захвата клетками и интернализации в клетках. Линкер может предпочтительно включать по меньшей мере одну циклическую группу и/или по меньшей мере одну ароматическую группу (прежде всего в группах Q и W в общей формуле (4), приведенной ниже).
Соответственно, в конъюгатах по настоящему изобретению предпочтительный линкер может характеризоваться общей формулой (4):
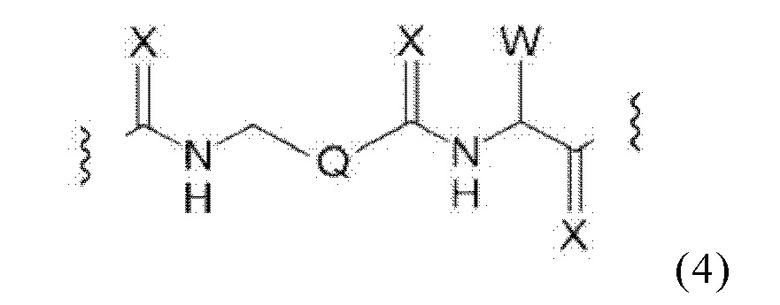
где
X каждый независимо выбирают из О, N, S или Р,
Q выбирают из замещенного или незамещенного алкила, алкиларила и циклоалкила, предпочтительно из замещенного или незамещенного С5-С14арила, С5-С14алкиларила или С5-С14циклоалкила, и
W выбирают из -(СН2)с-арила или -(СН2)с-гетероарила, где с означает число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10.
Не привязываясь к какой-либо теории, считается, что гидрофильные или полярные функциональные группы в составе линкера или в виде боковых групп (прежде всего Q, W) могут преимущественно усиливать свойства связывания с PSMA конъюгата по настоящему изобретению.
Если Q означает замещенный арил, алкиларил или циклоалкил, то типичные заместители приведены в разделе «Определения» выше и включают, не ограничиваясь только ими, галогены (т.е., F, Cl, Br и I), гидроксильные группы, группы алкокси, алкенокси, алкинокси, арилокси, аралкилокси, гетероциклилокси и гетероциклилалкокси, карбонилы (оксо), карбоксильные группы, сложные эфиры, уретаны, оксимы, гидроксиламины, алкоксиамины, аралкоксиамины, тиолы, сульфиды, сульфоксиды, сульфоны, сульфонилы, сульфонамиды, амины, N-оксиды, гидразины, гидразиды, гидразоны, азиды, амиды, мочевины, амидины, гуанидины, енамины, имиды, изоцианаты, изотиоцианаты, цианаты, тиоцианаты, имины, нитрогруппы, нитрилы, (т.е., CN), галогеналкил, аминоалкил, гидроксиалкил, циклоалкил.
Предпочтительно, Q можно выбирать из замещенного или незамещенного С5-С7циклоалкила, более предпочтительно, Q означает циклогексил.
Предпочтительно, W можно выбирать из -(СН2)с-нафтила, -(СН2)c-фенила, -(СН2)с-бифенила, -(СН2)с-индолила, -(СН2)с-бензотиазолила, где с означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. Более предпочтительно, W можно выбирать из -(СН2)-нафтила, -(СН2)-фенила, -(СН2)-бифенила, -(СН2)-индолила или -(СН2)-бензотиазолила. Наиболее предпочтительно, W означает -(СН2)-нафтил.
Предпочтительно, каждый X может означать О.
Соответственно, прежде всего предпочтительный линкер, соединяющий фрагмент, связывающийся с опухолевым антигеном, прежде всего PSMA-связывающий фрагмент, с конъюгатом по настоящему изобретению может характеризоваться следующей структурной формулой (4)(а):
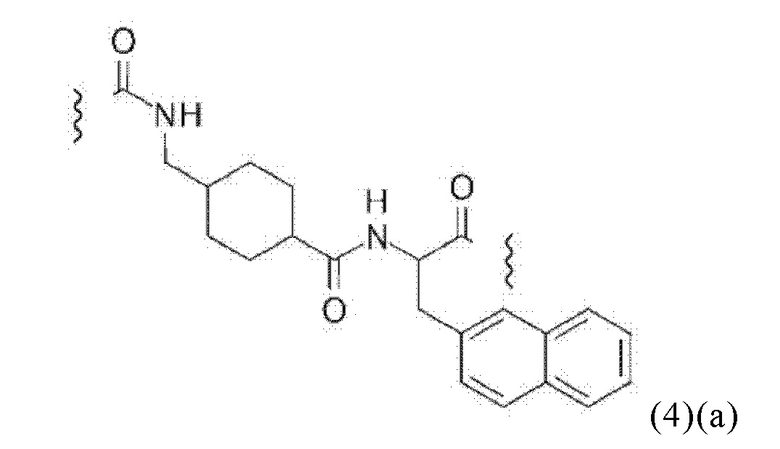
В связи с вышеизложенным, в настоящем изобретении предлагается также соединение общей формулы (1)(g):
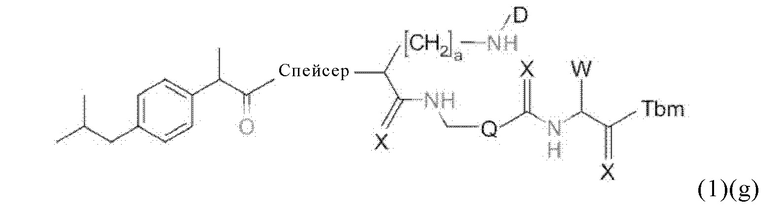
где D, Tbm, спейсер и индекс а имеют значения, приведенные в данном контексте для общей формулы (1)(а) (и, предпочтительно, ее вариантов), и X, Q и W имеют значения, приведенные в данном контексте для общей формулы (4) (и, предпочтительно, ее вариантов),
или его фармацевтически приемлемые соли, сложные эфиры, сольваты или радиоактивно меченные комплексы.
Например, в настоящем изобретении также предлагается соединение общей формулы (1)(h):
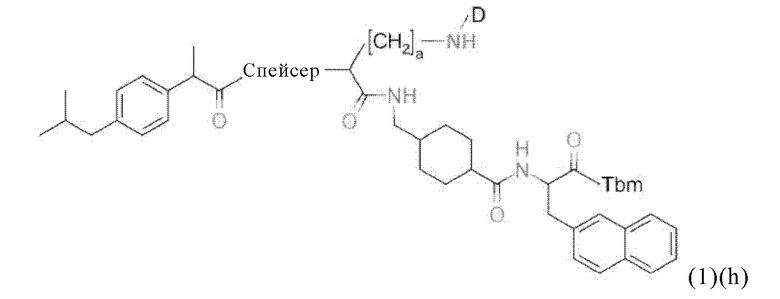
где D, Tbm, спейсер и индекс а имеют значения, приведенные в данном контексте для общей формулы (1)(а) (и, предпочтительно, ее вариантов),
или его фармацевтически приемлемые соли, сложные эфиры, сольваты или радиоактивно меченные комплексы.
В связи с описанными выше вариантами фрагментов для специфичного связывания с опухолевым антигеном, а именно PSMA-связывающегося фрагмента, и в связи с описанными выше вариантами линкеров, в настоящем изобретении предлагается также соединение общей формулы (1)(k):
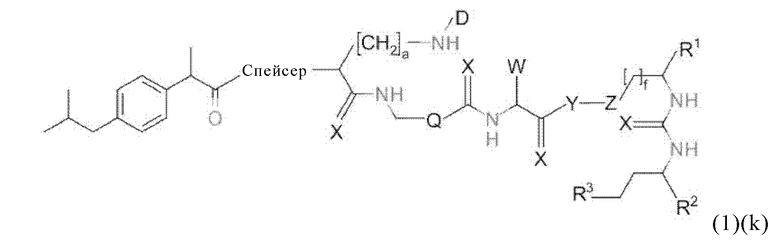
где D, спейсер и индекс а имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно, ее вариантов), Y, Z, R1, R2, R3 и индекс f имеют значения, приведенные при описании общей формулы (3) (и, предпочтительно, ее вариантов), и X, Q и W имеют определения, приведенные при описании общей формулы (4) (и, предпочтительно, ее вариантов),
или его фармацевтически приемлемые соли, сложные эфиры, сольваты или радиоактивно меченные комплексы.
Прежде всего в настоящем изобретении предлагается также соединение общей формулы (1) (l):
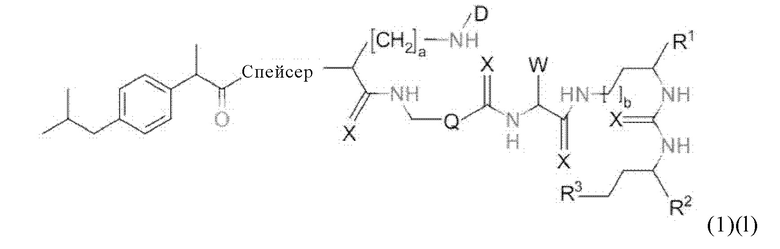
где D, спейсер и индекс а имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно, ее вариантов), R1, R2, R3 и индекс b имеют значения, приведенные при описании общей формулы (3)(ii) (и, предпочтительно, ее вариантов), и X, Q и W имеют значения, приведенные при описании общей формулы (4) (и, предпочтительно, ее вариантов),
или его фармацевтически приемлемые соли, сложные эфиры, сольваты или радиоактивно меченные комплексы.
Прежде всего в настоящем изобретении предлагается также соединение общей формулы (1)(m):
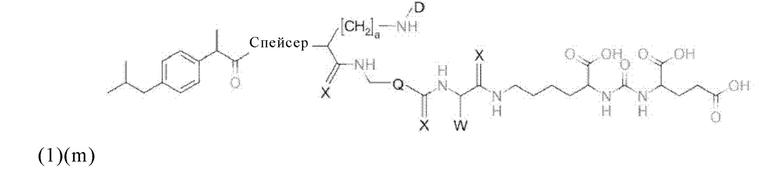
где D, спейсер и индекс а имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно, ее вариантов), R1, R2, R3 и индекс b имеют значения, приведенные при описании общей формулы (3)(ii) (и, предпочтительно, ее вариантов), и X, Q и W имеют значения, приведенные при описании общей формулы (4) (и, предпочтительно, ее вариантов),
или его фармацевтически приемлемые соли, сложные эфиры, сольваты или радиоактивно меченные комплексы.
Например, в настоящем изобретении предлагается также соединение общей формулы (1)(b):
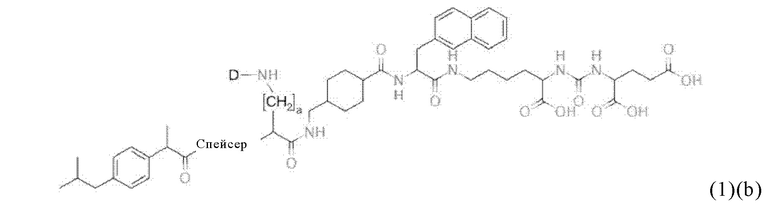
где D, спейсер и индекс а имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно, ее вариантов),
или его фармацевтически приемлемые соли, сложные эфиры, сольваты или радиоактивно меченные комплексы.
Даже еще более конкретно, в настоящем изобретении предлагается также соединение общей формулы (1)(с):
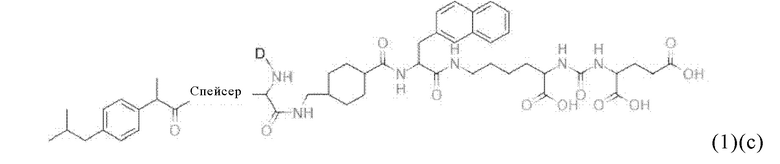
где D и спейсер имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно, ее вариантов),
или его фармацевтически приемлемые соли, сложные эфиры, сольваты или радиоактивно меченные комплексы.
Спейсер
В конъюгатах по настоящему изобретению ибупрофен (в качестве связывающего альбумин фрагмента) конъюгирован (т.е. ковалентно соединен или присоединен) к «точке разветвления» -СН- через «спейсер». В приведенном ниже описании термин «спейсер» используют для специального описания группы, соединяющей и заполняющей расстояние между фрагментом, связывающим альбумин, и «точкой разветвления» -СН-, и/или «отделяющей» эти группы от остальных групп/фрагментов в конъюгате.
Спейсер может предпочтительно исключать стерическое препятствие между ибупрофеном (в качестве связывающего альбумин фрагмента) и другими группами или фрагментами конъюгата по настоящему изобретению и придавать достаточную подвижность и гибкость. Кроме того, спейсер можно предпочтительно конструировать для придания, поддержки и/или обеспечения достаточного связывания с HSA, высокой аффинности связывания с опухолевым антигеном (например, с PSMA) и быстрым и необязательно селективным проникновением клеток, положительных к опухолевому антигену (например, PSMA-) в ходе интернализации соединения по настоящему изобретению.
Авторами настоящего изобретения установлено, что спейсер должен предпочтительно содержать по меньшей мере одну связь C-N. Пригодные спейсеры должны быть предпочтительно стабильными in vivo. Структура спейсера обычно зависит от конъюгата в целом и ее можно выбирать для улучшения функциональности остального конъюгата (такой как связывание с PSMA), связывание с HSA, интернализация и т.п.). Соответственно, например, спейсеры могут характеризоваться жесткой или гибкой структурой и оказывать влияние на липофильность или гидрофильность конъюгата в целом и т.п.
Спейсер может включать линейный или разветвленный, необязательно замещенный С1-С20гидрокарбил, например, включающий до 5 гетероатомов, более предпочтительно С1-С12гидрокарбил, еще более предпочтительно С2-С6гидрокарбил, еще более предпочтительно С2-С4гидрокарбил. Углеводород может предпочтительно включать по меньшей мере один, необязательно до 4 или 5 гетероатомов, предпочтительно выбранных из N. Он содержит одну или две, боле предпочтительно одну связь C-N.
Предпочтительно, спейсер может представлять собой -[CHR6]u-NR7-, где R6 и R7 можно каждый независимо выбирать из Н и разветвленного, неразветвленного и циклического С1-С12гидрокарбила и где и может представлять собой целое число, выбранное из 1,2, 3, 4, 5, 6, 7, 8, 9 или 10. Более предпочтительно, R6 и R7 могут означать Н, и u может означать целое число, выбранное из 2, 3 или 4, более предпочтительно 2 или 4. Более предпочтительно, R6 и R7 могут означать Н и u равно 2 или 4. Спейсер предпочтительно может представлять собой -[CH2]2-NH- или -[CH2]4-NH-.
Соответственно, спейсер в конъюгатах по нпстоящему изобретению может включать или состоять из формулы (2)(а) или (2)(а)' или (2)(а)'':
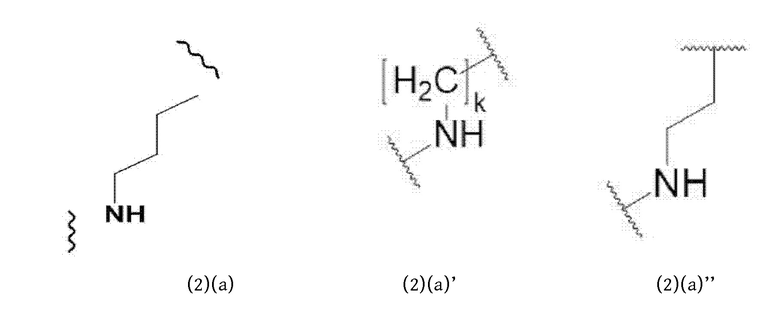
Соединение формулы (2)(а) в данном контексте называют также «лизиновым спейсером» или «спейсер Lys», поскольку он представляет собой спейсер с лизиновой боковой цепью. В формуле (2)(а)' к равен целому числу от 0 до 8, предпочтительно от 2 до 4.
Примеры конъюгатов по настоящему изобретению (например, Ibu-PSMA, Ibu-Dα-PSMA, Ibu-Dβ-PSMA, Ibu-N-PSMA и Ibu-DAB-PSMA, охарактеризованные в прилагаемых примерах) включают ибупрофен, соединенный с «точкой разветвления» через спейсер, включающий или состоящий из формулы (2)(а).
Соответственно, спейсер может включать по меньшей мере один аминокислотный остаток или по меньшей мере одну боковую цепь аминокислотного остатка. Термин «аминокислотный остаток», использованный в данном контексте, означает конкретный мономер аминокислоты в качестве фрагмента спейсера.
Термин «аминокислота» означает любую органическую молекулу, включающую как кислотную (обычно карбоксильную (-СООН)), так и аминофункциональную группу (-NH2). Из одной или обеих указанных групп могут быть необязательно получены производные. Амино- и кислотная группы могут находиться в любом положении по отношению друг к другу, но аминогруппы обычно включают 2-аминокарбоновые кислоты, 3-аминокарбоновые кислоты, 4-аминокарбоновые кислоты и т.д. Аминогруппа может быть присоединена к 1ому, 2ому, 3ему, 4ому, 5ому, 6ому, 7ому, 8ому, 9ому, 10ому (и т.п.) вплоть до 20ому атому углерода в составе аминокислот(ы). Другими словами, аминокислота(ы) могут представлять собой альфа-, бета-, гамма-, дельта-, эпсилон- (и т.п.) вплоть до омега-аминокислоты. Предпочтительно кислотной группой является карбоксильная (-СООН) группа. Однако, другие кислотные группы, выбранные из -ОРО3Н, -РО3Н, -OSO3H или -SO3H, также являются допустимыми.
Аминокислота может являться протеиногенной или непротеиногенной аминокислотой.
Протеиногенными аминокислотами являются 22 аминокислоты, которые в природе включены в полипептиды. Кроме селеноцистеина и пирролизина, все протеиногенные аминокислоты (т.е. остальные 20 протеиногенных аминокислот) кодируются универсальным генетическим кодом. 22 протениногенные аминокислоты включают аргинин, гистидин, лизин, аспарагиновую кислоту, глутаминовую кислоту, серии, треонин, аспарагин, глутамин, цистеин, глицин, пролин, аланин, валин, изолейцин, лейцин, метионин, фенилаланин, тирозин, триптофан,селеноцистеин и пирролизин.
Однако, любое органическое соединение, содержащее аминогруппу (-NH2) и карбоксильную (-СООН) функциональную группу, является аминокислотой. С этой точки зрения любая аминокислота, которая отличается от 22 протеиногенных аминокислот, представляет собой «непротеиногенную» аминокислоту. Например, непротеиногенные аимнокислоты могут отсутствовать в белках (например, карнитин, GABA, левотироксин, 2-аминоизомасляная кислота и нейромедиатор гамма-аминомасляная кислота) или напрямую не продуцируются и их нельзя выделить по стандартному клеточному механизму (например, гидроксипролин и селенометионин). Непротеиногенные аминокислоты могут, например, присутствовать в виде промежуточных продуктов в метаболических путях стандартных аминокислот - например, орнитин и цитрулин присутствуют в цикле мочевины. Примеры включают карнитин, GABA, левотироксин, 2-аминоизомасляную кислоту, гамма-аминомасляную кислоту, гидроксипролин, селенометионин, орнитин, цитруллин, диаминомасляную кислоту, δ-аминолевулиновую кислоту, аминоизомасляную кислоту, диаминопимелиновую кислоту, цистатионин, лантионин и дьенколовую кислоту. В контексте настоящего изобретения, например, диаминомасляная кислота (DAB) является прежде всего предпочтительной непротеиногенной аминокислотой.
Аминокислотный остаток(ки) можно получить из природной аминокислот(ы) или их производных. Прежде всего аминокислотный остаток(ки) можно получить из альфа (α-)аминокислот(ы). Амиокислотва(ы) может представлять собой D- или L-аминокислоту(ы).
Например, аминокислота(ы) может представлять собой D- или L-энантиомер аминокислоты, выбранный из группы, состоящей из аргинина, аспарагина, аспартата, цистеина, глутамата, глутамина, глицина, гистидина, лейцина, лизина, метионина, фенилаланина, пролина, серина, треонина, триптофана, тирозина и/или валина.
Предпочтительно аминокислоту выбирают из лизина, аспартата, аспарагина, диаминомасляной кислоты, фенилаланина, тирозина, треонина, серина, пролина, лейцина, изолейцина, валина, аргинина, гистидина, глутамата, глутамина и аланина. Например, аминокислота(ы) может представлять собой D-или L-энантиомер аминокислоты, выбранной из лизина, аспартата, аспарагина, диаминомасляной кислоты, фенилаланина, тирозина, треонина, серина, пролина, лейцина, изолейцина, валина, аргинина, гистидина, глутамата, глутамина и аланина. Например, аминокислота(ы) является (D-/L-) аспартатом, глутаматом или лизином, таким как D-аспартат, D-глутамат или L-лизин. Например, аминокислота(ы) является (D-/L-) аспартатом, аспарагином, лизином или диаминомасляной кислотой. Например, другой аминокислотный остаток может представлять собой аспартат, аспарагин или диаминомасляную кислоту.
Спейсер может включать 1, 2, 3, 4 или 5 аминокислотных остатков, таких как один или более остатков D-аспартата, один или более остатков D-глутамата и/или один или более остатков L-лизина. В конъюгатах, включающих D-энантиомер, использование D-энантиомера может обеспечивать положительный эффект дополнительного снижения скорости метаболизирования и, следовательно, клиренса из кровотока. Предпочтительно спейсер может включать от 1 до 3 (предпочтительно, 1 или 2) таких аминокислотных остатков, таких как остатки D-аспартата или D-глутамата или остаток (L-)лизина в комбинации с другими аминокислотными остатками (например, аспартат, аспарагин или диаминомасляная кислота). Другими словами, спейсер может включать пептид, который предпочтительно состоит из от 1 до 5 аминокислот, более предпочтительно от 1 до 3 аминокислот, еще более предпочтительно из 1 или 2 аминокислот.
Соответственно, конъюгаты по настоящему изобретению могут включать спейсер формулы (2)(b):
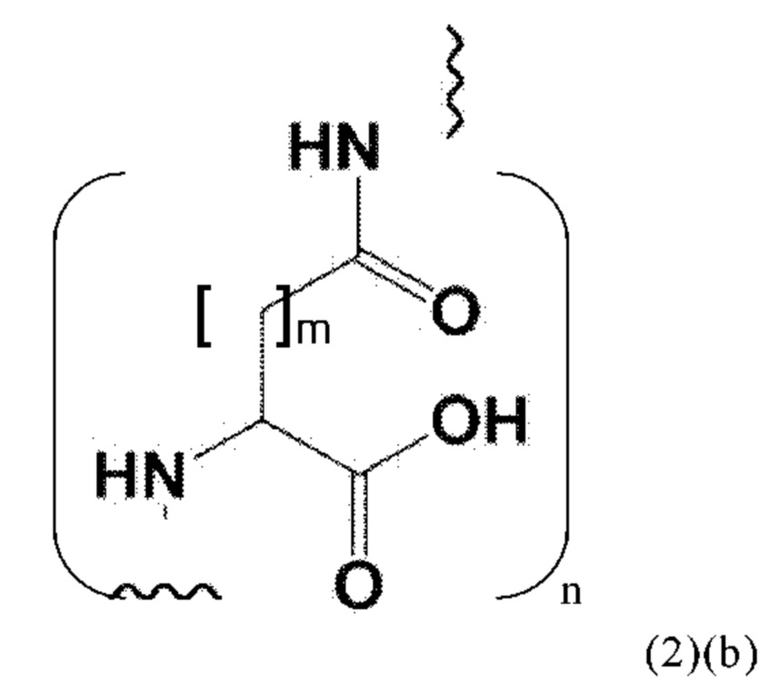
где
m означает целое число, выбранное из 1 или 2, и
n означает целое число, выбранное из 1, 2, 3, 4 или 5, предпочтительно 2 или 3.
В другом варианте спейсер может включать аминокислотный остаток, присоединенный к «точке разветвления» через линейную или разветвленную необязательно замещенную С1-С20гидрокарбильную группу, содержащую по меньшей мере один гетероатом N.
Соответственно, конъюгаты по настоящему изобретению могут включать спейсер формулы (2)(с) или формулы (2)(с)':
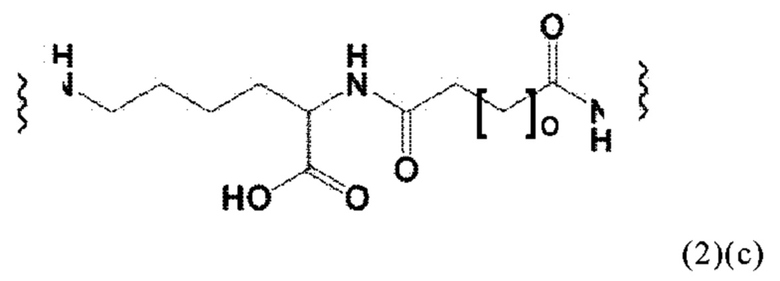
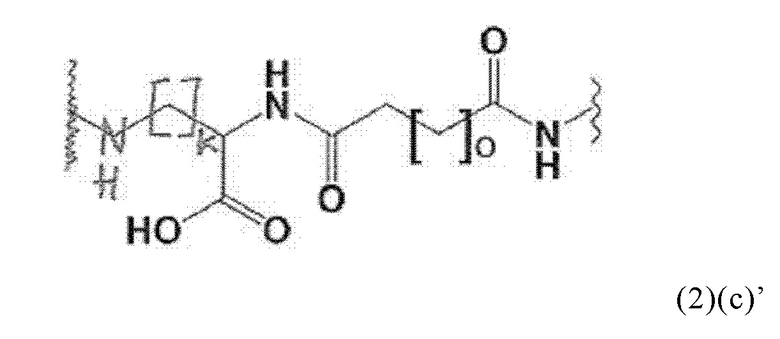
где о означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. Предпочтительно, о равен 5.
В формуле (2)(с)' k означает целое число, выбранное из от 0 до 8, предпочтительно 2, 3 или 4.
Как описано выше, спейсер может включать или состоять из остатка (L-) лизина (например, как показано в формуле (2)(а)). В данном контексте спейсер может дополнительно включать другой аминокислотный остаток. Прежде всего, спейсер может включать или состоять из формулы (2)(d) или (2)(d)' или (2)(d)'':
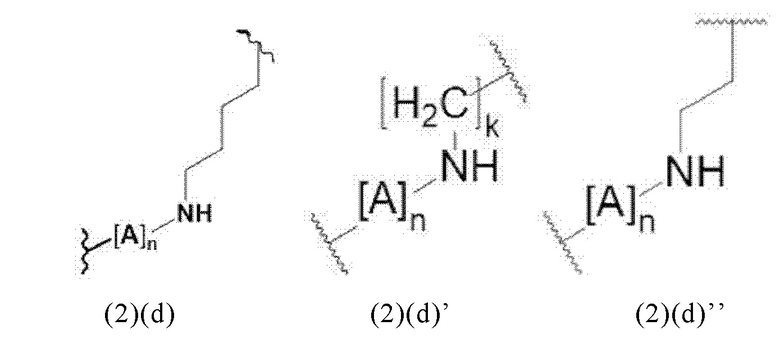
где А означает аминокислотный остаток и n означает целое число, выбранное из 0, 1, 2, 3, 4 или 5, предпочтительно 0 или 1, и где k означает целое число, выбранное от 0 до 8, предпочтительно от 2 до 4.
В формуле (2)(d) А может означать аминокислотный остаток, как описано выше, прежде всего с учетом различных предпочтительных аминокислот. Например, другим аминокислотным остатком может являться аспартат, аспарагин или диаминомасляная кислота.
Например, спейсер может включать или состоять из формулы (2)(d)(i) или формулы (2)(d)(i)':
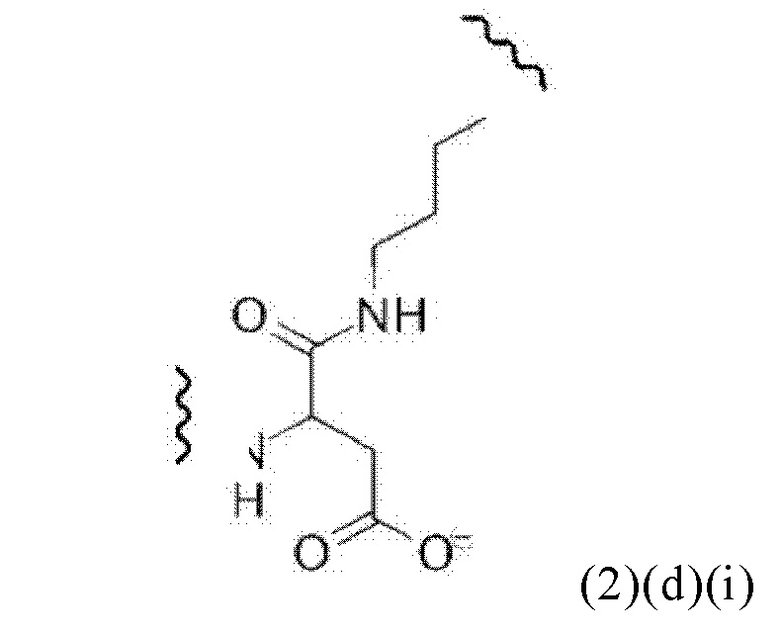
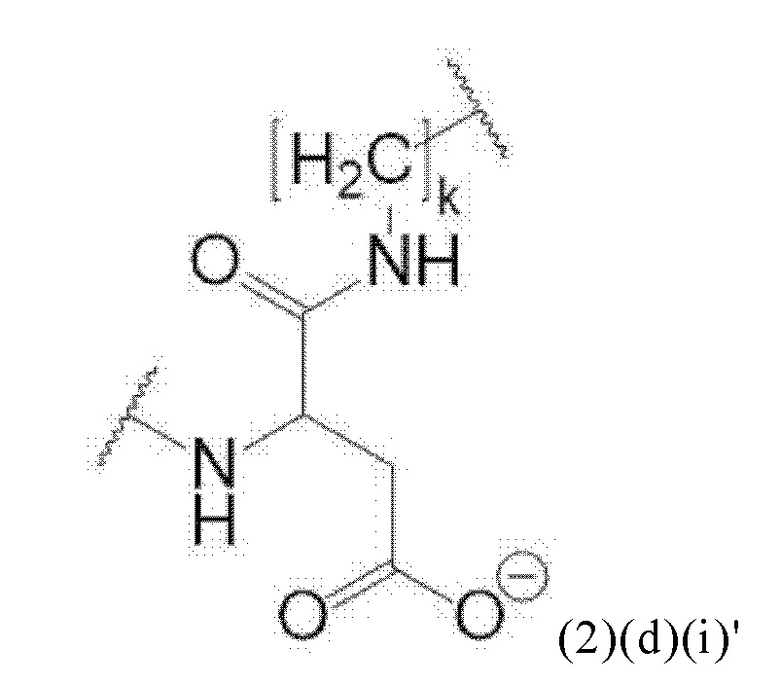
и где k означает целое число, выбранное от 0 до 8, предпочтительно от 2 до 4.
Например, спейсер может включать или состоять из формулы (2)(d)(ii) или формулы (2)(d)(ii)':
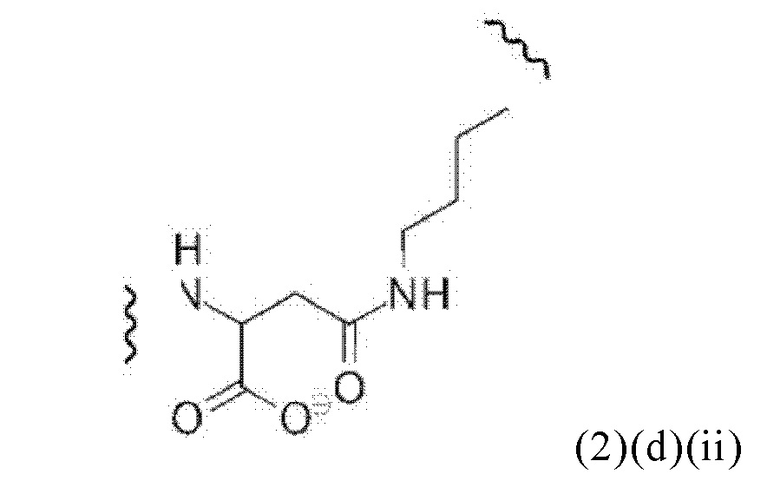
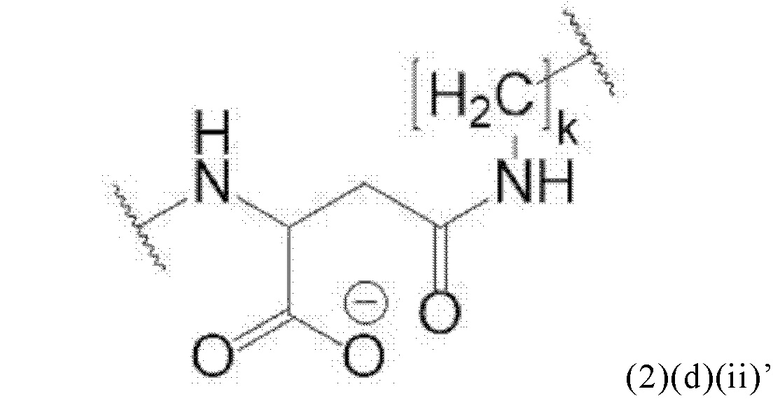
и где k означает целое число, выбранное от 0 до 8, предпочтительно от 2 до 4.
Например, спейсер может включать или состоять из формулы (2)(d)(iii) или формулы (2)(d)(iii)':
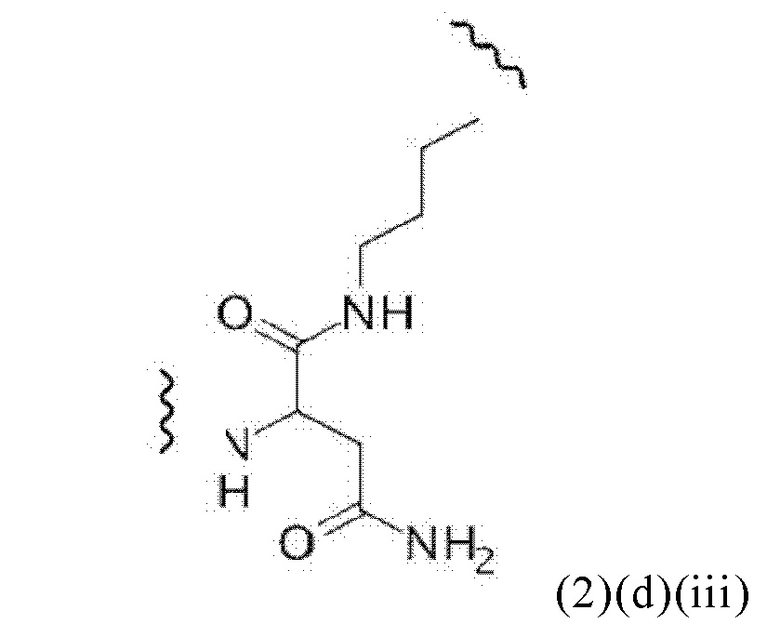
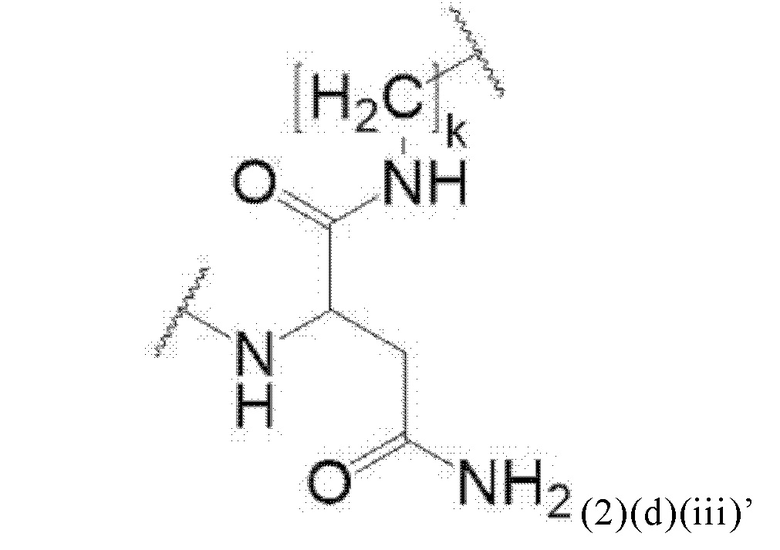
и где k означает целое число, выбранное от 0 до 8, предпочтительно от 2 до 4.
Например, спейсер может включать или состоять из формулы (2)(d)(iv) или формулы (2)(d)(iv)':
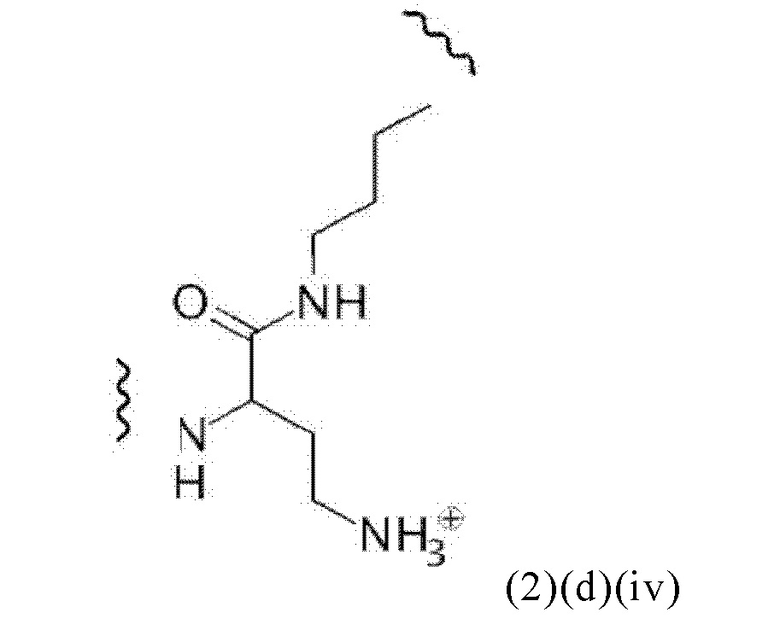
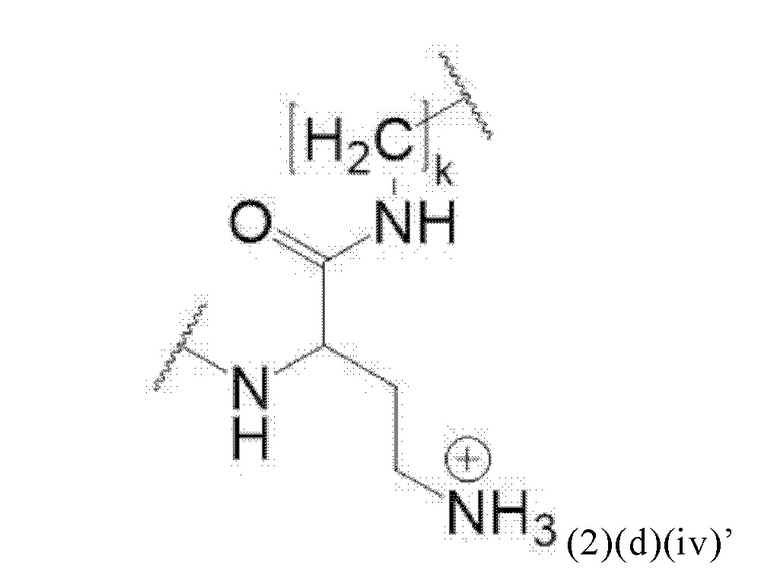
и где k означает целое число, выбранное от 0 до 8, предпочтительно от 2 до 4.
Ввиду приведенного выше в настоящем изобретении предлагается также соединение общей формулы (1)(n):
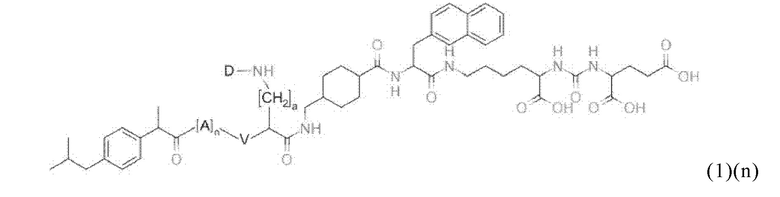
где
D означает хелатирующий фрагмент (например, как описано в данном контексте),
А означает аминокислотный остаток (например, как описано в данном контексте) или его боковую цепь,
V выбирают из одинарной связи, N или NH, или необязательно замещенного С1-С12гидрокарбила, включающего до 3 гетероатомов, где указанный гетероатом предпочтительно выбирают из N,
а означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 (например, как описано в данном контексте), и
n означает целое число, которое выбирают из 0, 1, 2, 3, 4 или 5, предпочтительно из 0 или 1,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Соответственно, в настоящем изобретении предлагается также соединение общей формулы (1)(о):
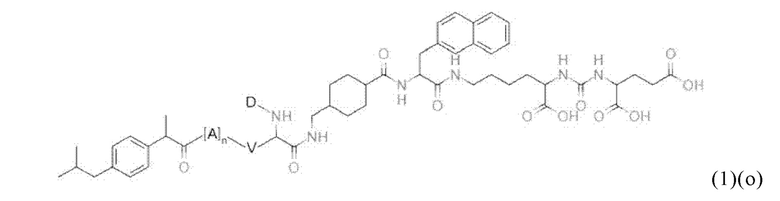
где
D означает хелатирующий фрагмент (например, как описано в данном контексте),
А означает аминокислотный остаток (например, как описано в данном контексте) или его боковую цепь,
V выбирают из одинарной связи, N или NH, или необязательно замещенного С1-С12гидрокарбила, включающего до 3 гетероатомов, где указанный гетероатом предпочтительно выбирают из N,
а означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 (например, как описано в данном контексте), и
n означает целое число, которое выбирают из 0, 1, 2, 3, 4 или 5, предпочтительно из 0 или 1,
k означает целое число, которое выбирают из 0, 1, 2, 3, 4 или 5, 6, 7 или 8, предпочтительно из 2, 3 или 4,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
V в формуле (1)(n) или 1(о) может содержать 1 или 2 связи C-N, предпочтительно 1 связь C-N.
V может означать группу NH в обеих формулах (1)(n) или (1)(о).
Прежде всего, в настоящем изобретение предлагается соединение формулы (6)(а) или формулы (6)(а)':
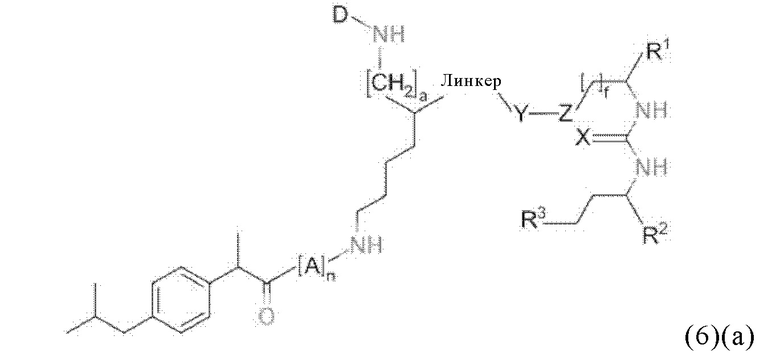
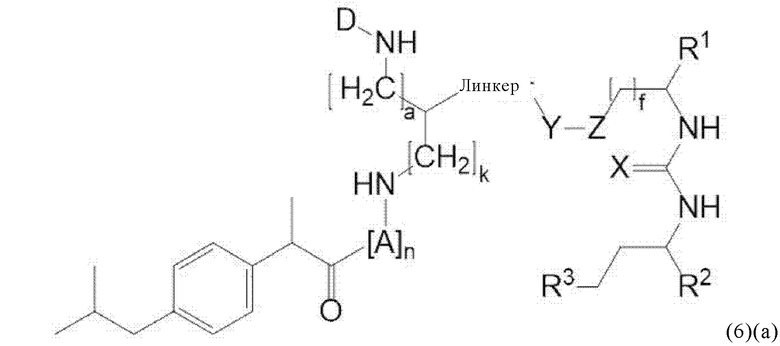
где
D, линкер и индекс а имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно ее вариантов),
X, Y, Z, R1, R2, R3 и f имеют значения, приведенные при описании общей формулы (3) (и, предпочтительно ее вариантов),
А означает аминокислотный остаток (например, как описано в данном контексте),
n означает целое число, выбранное из 0, 1, 2, 3, 4 или 5, предпочтительно из 0 или 1, и
k означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7 или 8, предпочтительно из 2, 3 или 4,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Прежде всего, в настоящем изобретение предлагается соединение формулы (6)(b) или формулы (6)(b)':
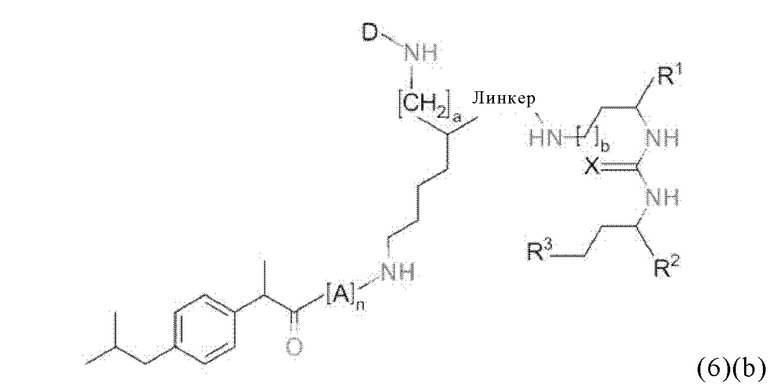
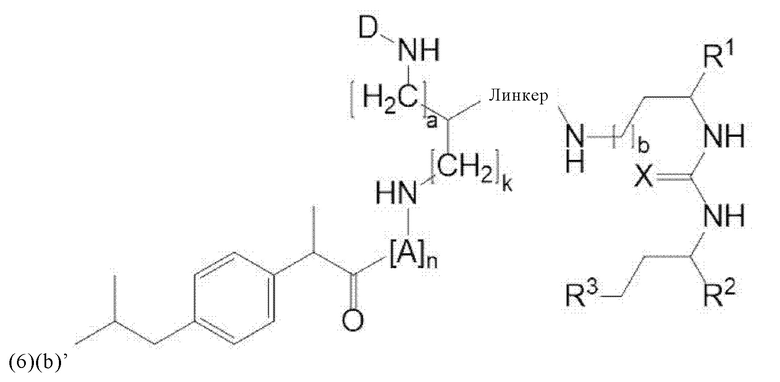
где
D, линкер и индекс а имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно ее вариантов),
X, R1, R2, R3 и b имеют значения, приведенные при описании общей формулы (3) (и, предпочтительно ее вариантов),
А означает аминокислотный остаток (например, как описано в данном контексте),
n означает целое число, выбранное из 0, 1, 2, 3, 4 или 5, предпочтительно из 0 или 1, и
k означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7 или 8, предпочтительно из 2, 3 или 4,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Прежде всего, в настоящем изобретение предлагается соединение формулы (6)(c) или формулы (6)(c)':
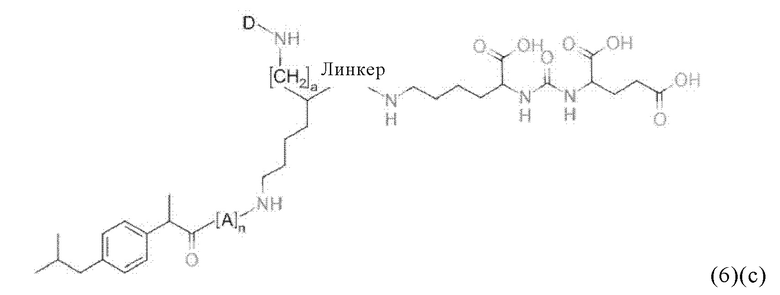
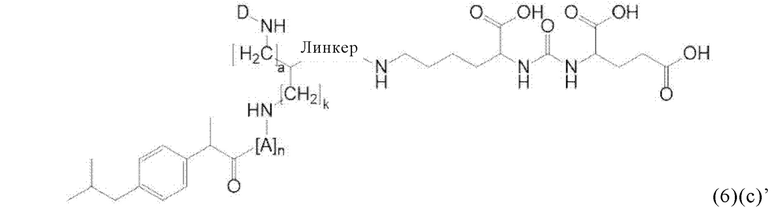
где
D, линкер и индекс а имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно ее вариантов),
А означает аминокислотный остаток (например, как описано в данном контексте),
n означает целое число, выбранное из 0, 1, 2, 3, 4 или 5, предпочтительно из 0 или 1, и
k означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7 или 8, предпочтительно из 2, 3 или 4,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Прежде всего, в настоящем изобретение предлагается соединение формулы (6)(d) или формулы (6)(d)':
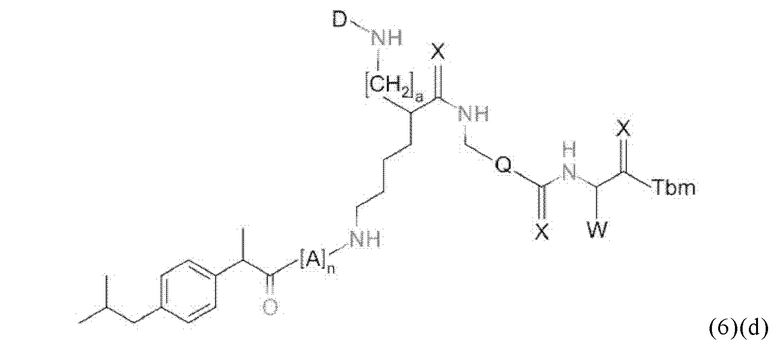
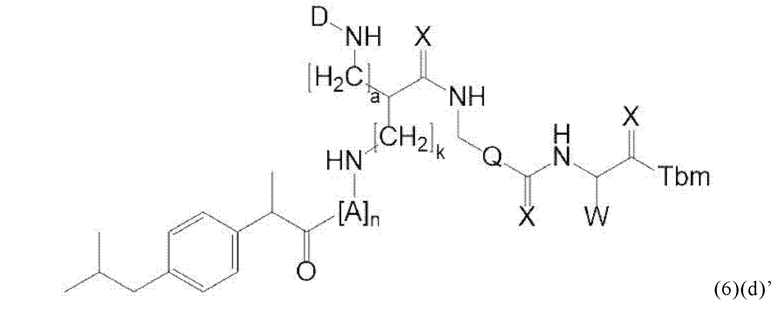
где D, Tbm и а имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно ее вариантов),
X, Q и W имеют значения, приведенные при описании общей формулы (4) (и, предпочтительно ее вариантов),
А означает аминокислотный остаток (например, как описано в данном контексте),
n означает целое число, выбранное из 0, 1, 2, 3, 4 или 5, предпочтительно из 0 или 1, и
k означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7 или 8, предпочтительно из 2, 3 или 4,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Прежде всего, в настоящем изобретение предлагается соединение формулы (6)(e) или формулы (6)(e)':
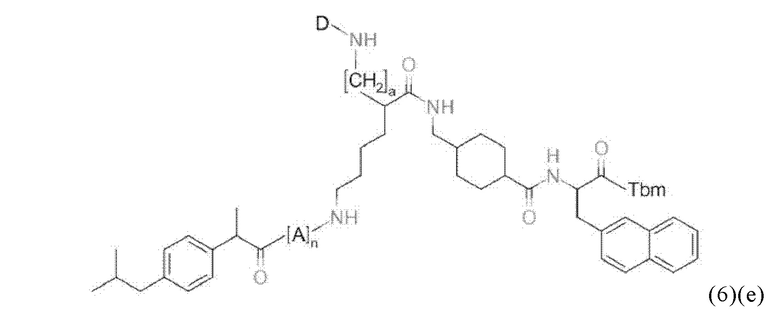
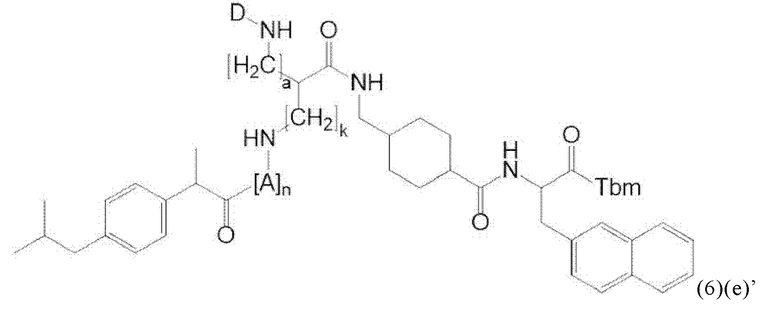
где D, Tbm и а имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно ее вариантов),
А означает аминокислотный остаток (например, как описано в данном контексте),
n означает целое число, выбранное из 0, 1, 2, 3, 4 или 5, предпочтительно из 0 или 1, и
k означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7 или 8, предпочтительно из 2, 3 или 4,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Прежде всего, в настоящем изобретение предлагается соединение формулы (6)(f) или формулы (6)(f)':
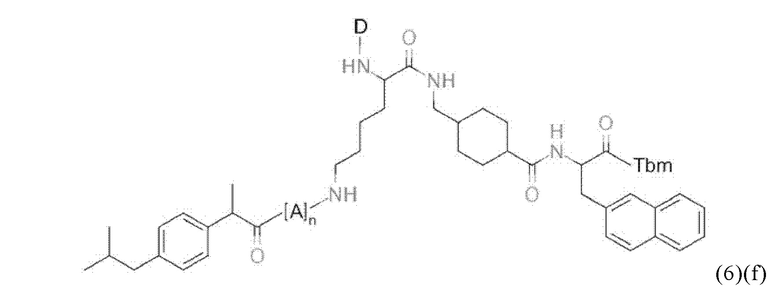
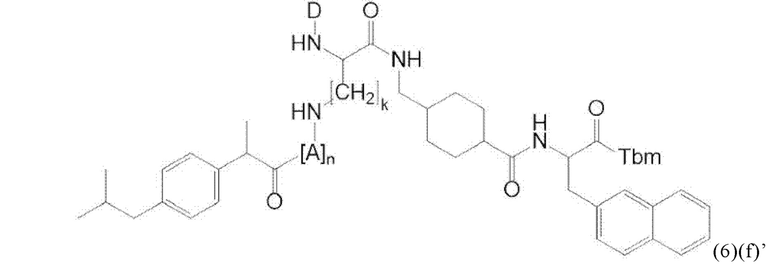
где D и Tbm имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно ее вариантов),
А означает аминокислотный остаток (например, как описано в данном контексте),
n означает целое число, выбранное из 0, 1, 2, 3, 4 или 5, предпочтительно из 0 или 1, и
k означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7 или 8, предпочтительно из 2, 3 или 4,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Прежде всего, в настоящем изобретение предлагается соединение формулы (6)(g) или формулы (6)(g)':
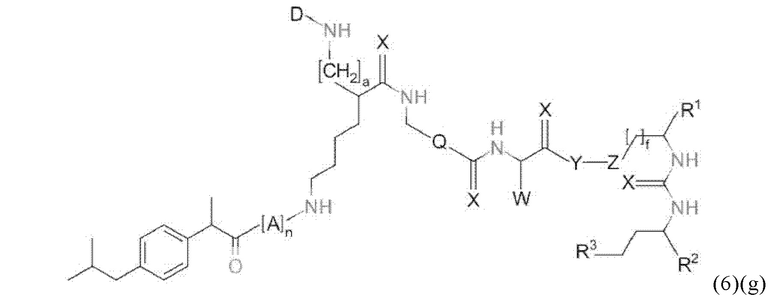
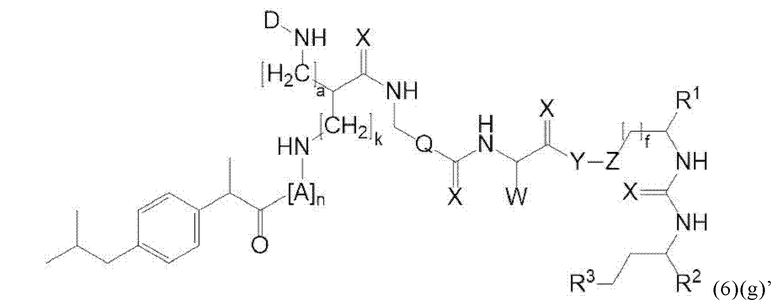
где D и а имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно ее вариантов),
Y, Z, R1, R2, R3 и f имеют значения, приведенные при описании общей формулы (3) (и, предпочтительно ее вариантов),
X, Q и W имеют значения, приведенные при описании общей формулы (4) (и, предпочтительно ее вариантов),
А означает аминокислотный остаток (например, как описано в данном контексте),
n означает целое число, выбранное из 0, 1, 2, 3, 4 или 5, предпочтительно из 0 или 1, и
k означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7 или 8, предпочтительно из 2, 3 или 4,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Прежде всего, в настоящем изобретение предлагается соединение формулы (6)(h) или формулы (6)(h)':
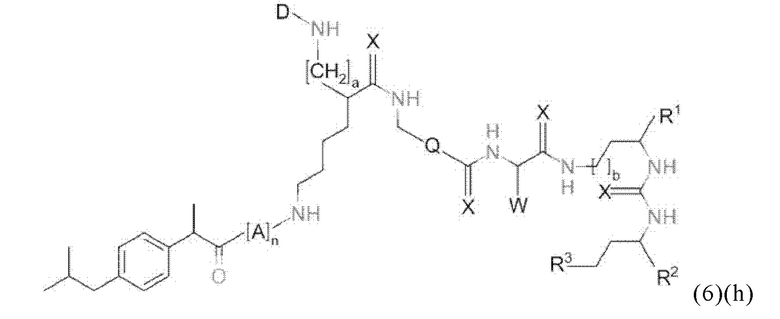
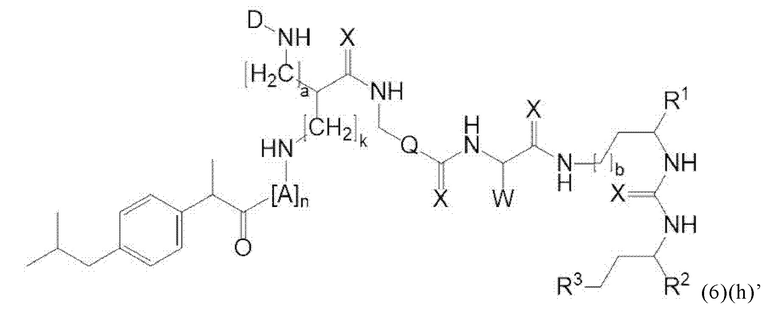
где D и а имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно ее вариантов),
R1, R2, R3 и b имеют значения, приведенные при описании общей формулы (3) (и, предпочтительно ее вариантов),
X, Q и W имеют значения, приведенные при описании общей формулы (4) (и, предпочтительно ее вариантов),
А означает аминокислотный остаток (например, как описано в данном контексте),
n означает целое число, выбранное из 0, 1, 2, 3, 4 или 5, предпочтительно из 0 или 1, и
k означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7 или 8, предпочтительно из 2,3 или 4,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Прежде всего, в настоящем изобретении предлагается также соединение формулы (6)(i) или формулы (6)(i)':
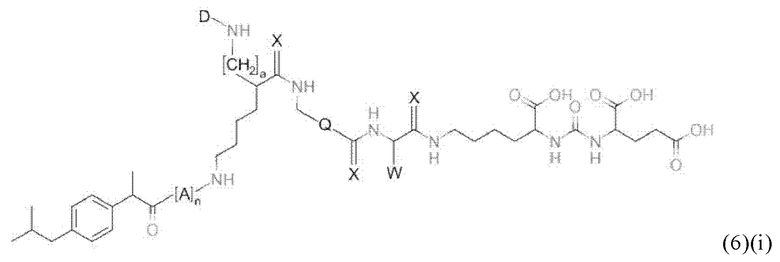
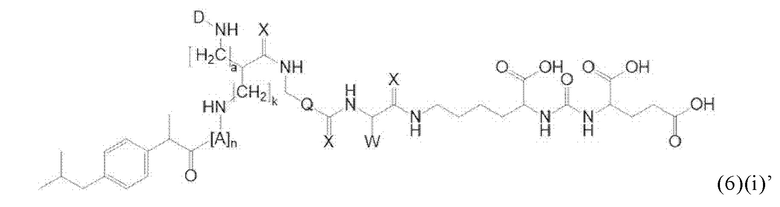
где D и а имеют значения, приведенные при описании общей формулы (1)(а) (и, предпочтительно ее вариантов),
X, Q и W имеют значения, приведенные при описании общей формулы (4) (и, предпочтительно ее вариантов),
А означает аминокислотный остаток (например, как описано в данном контексте),
n означает целое число, выбранное из 0, 1, 2, 3, 4 или 5, предпочтительно из 0 или 1, и
k означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7 или 8, предпочтительно из 2, 3 или 4,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Прежде всего, в настоящем изобретение предлагается соединение формулы (6)(j) или формулы (6)(j)':
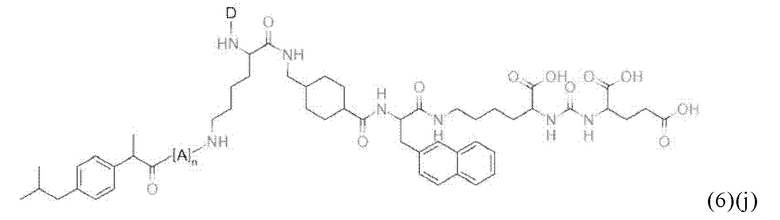
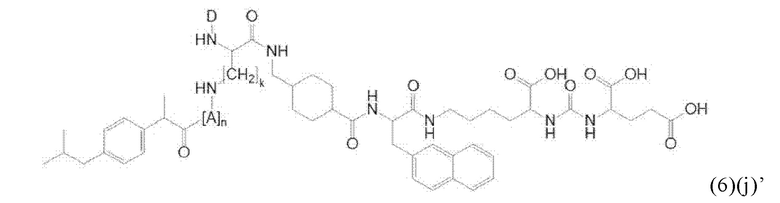
где
D означает хелатирующий фрагмент, как описано в данном контексте,
X, Q и W имеют значения, приведенные при описании общей формулы (4) (и, предпочтительно ее вариантов),
А означает аминокислотный остаток (например, как описано в данном контексте),
n означает целое число, выбранное из 0, 1, 2, 3, 4 или 5, предпочтительно из 0 или 1, и
k означает целое число, выбранное из 0, 1, 2, 3, 4, 5, 6, 7 или 8, предпочтительно из 2, 3 или 4,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Наиболее предпочтительными аминокислотными остатками для формул (6)(а) - (6)(j) являются аспартат, аспарагин и диаминомасляная кислота, или в другом варианте -[А]n отсутствует.
Например, в настоящем изобретении предлагается также соединение формулы (7)(а) или формулы (7)(а)':
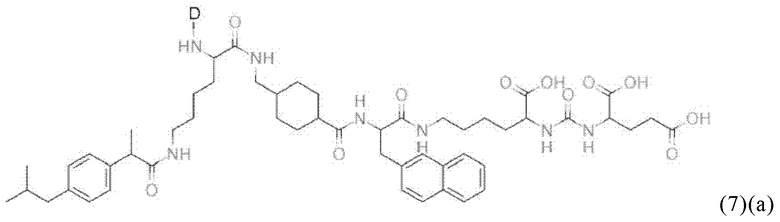
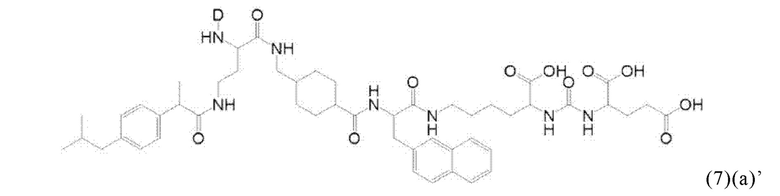
где
D означает хелатирующий фрагмент, как описано в данном контексте,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Например, в настоящем изобретении предлагается также соединение формулы (7)(b) или формулы (7)(b)':
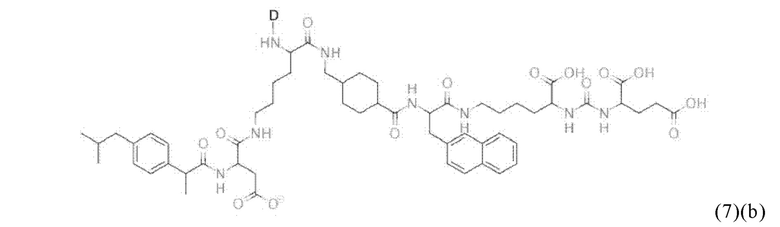
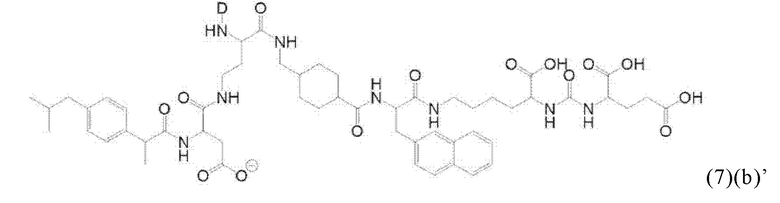
где
D означает хелатирующий фрагмент, как описано в данном контексте,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Например, в настоящем изобретении предлагается также соединение формулы (7)(с) или формулы (7)(с)':
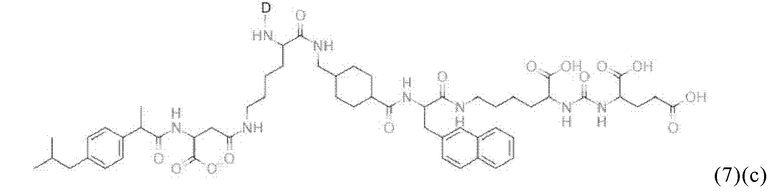
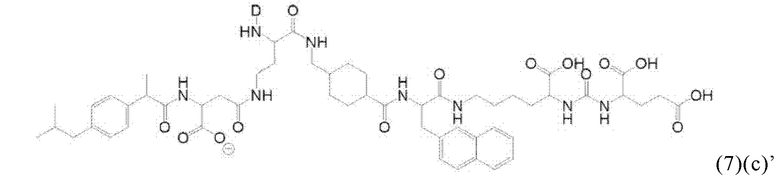
где
D означает хелатирующий фрагмент, как описано в данном контексте,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Например, в настоящем изобретении предлагается также соединение формулы (7)(d) или формулы (7)(d)':
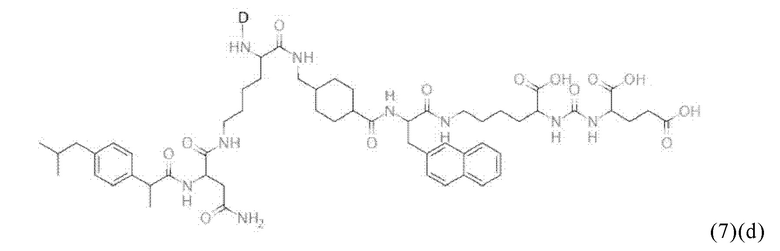
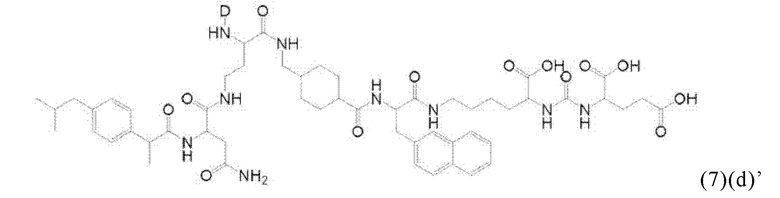
где
D означает хелатирующий фрагмент, как описано в данном контексте, или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Например, в настоящем изобретении предлагается также соединение формулы (7)(е) или формулы (7)(е)'
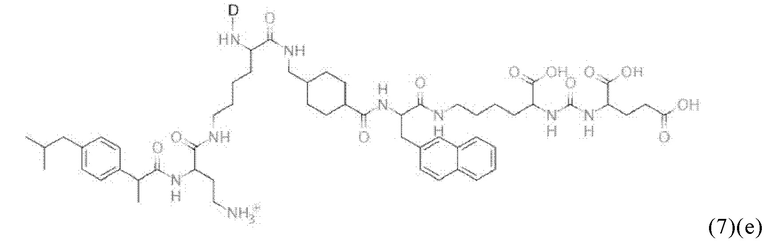
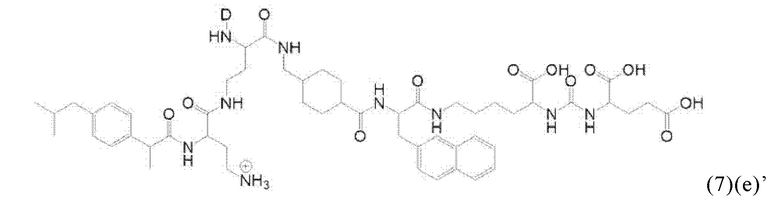
где
D означает хелатирующий фрагмент, как описано в данном контексте,
или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Для всех приведенных выше формул (7)(а), (7)(а)', (7)(b), (7)(b)', (7)(с), (7)(с)', (7)(d), (7)(d)', (7)(е) и (7)(е)' лизиновая боковая цепь в качестве спейсера или части спейсера состоит из 2 или 4 метиленовых групп, связывающих точку разветвления через NH группу лизиновой боковой цепи с группой ибупрофена. В другом варианте 0, 1,3, 5, 6, 7 или 8 метиленовых групп можно использовать в любом из соединений указанных формул.
Хелатирующее соединение
Конъюгаты по настоящему изобретению могут также содержать хелатирующий фрагмент. Например, хелатирующий фрагмент можно использовать для координации радиоактивного металла, например, для получения радиоактивно меченного конъюгата (называемого также радиолигандом).
Термины «хелатирующий фрагмент» или «хелатирующий остаток» используют взаимозаменяемо и означают полидентантные (соединенные несколькими связями) лиганды, способные образовывать две или более отдельные координационные связи («координирующие») с центральным ионом (металла). Более подробно, такие молекулы или молекулы с одной общей электронной парой, можно также назвать «основаниями Льюиса». Центральный ион (металла) обычно образует координационные связи с двумя или более электронными парами хелатирующего агента. Термины «бидентантный хелатирующий агент», «тридентантный хелатирующий агент» и «тетрадентантный хелатирующий агент» известны в данной области техники и означают хелатирующие агенты, содержащие, соответственно, две, три и четыре электронные пары, легкодоступные для самопроизвольной передачи иону металла, координированному хелатирующим агентом. Обычно электронные пары хелатирующего агента образуют координационные связи с одним центральным ионом (металла), однако в некоторых примерах хелатирующий агент может образовывать координационные связи с более чем одним ином металла, при этом возможны различные механизмы образования связей.
Термины «координирующий» и «координация» означают взаимодействие, при котором одна многоэлектронная пара передает координационные связи (координирует), т.е. образует две или более общих неразделенных электронных пар с одним центральным ионом (металла).
Хелатирующий агент предпочтительно выбирают на основе его способности координировать требуемый центральный ион (металла), такой как радионуклид, как описано в данном контексте.
Соответственно, хелатирующее соединение D можно характеризовать одной из следующих формул (5a)-(5jj):
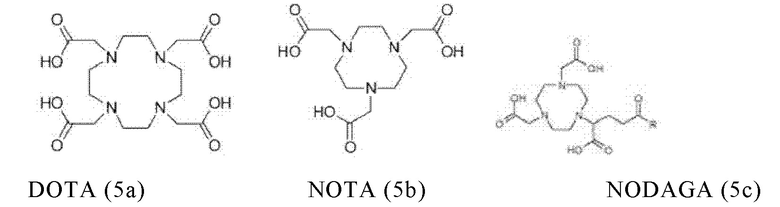
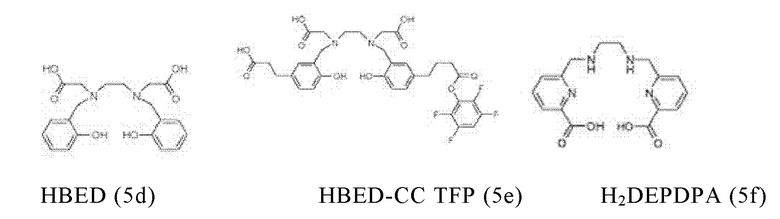
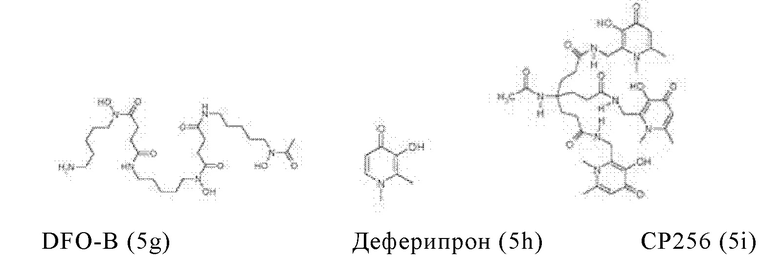
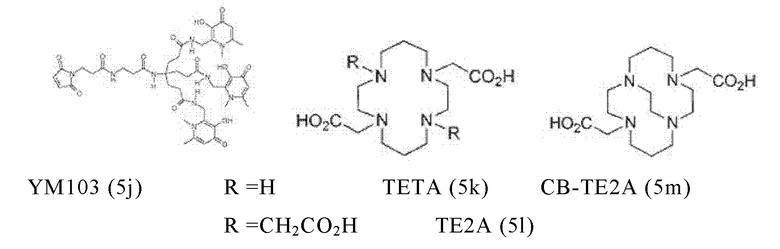
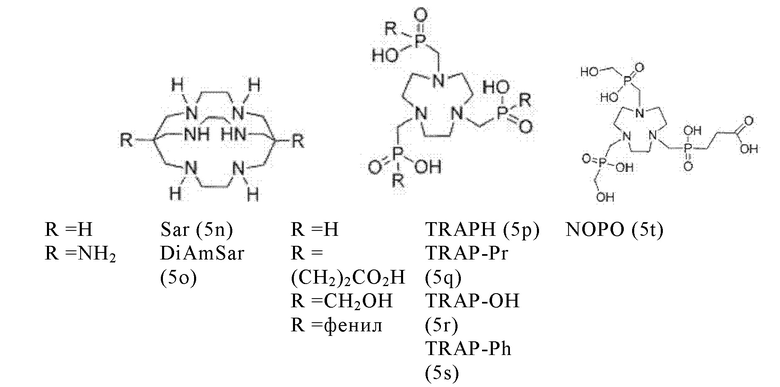
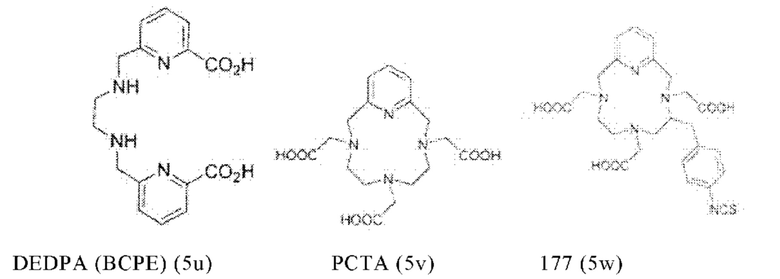
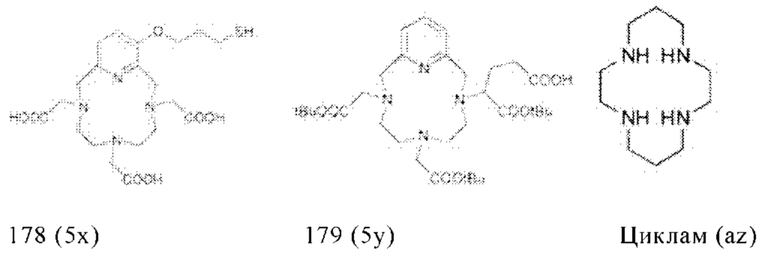
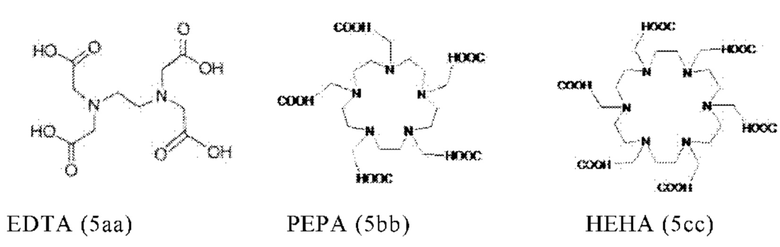
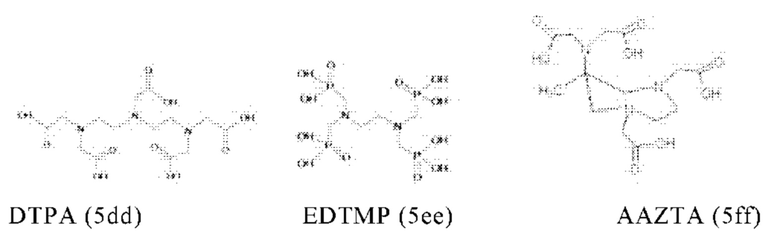
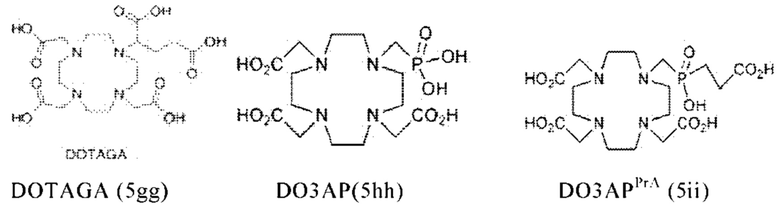
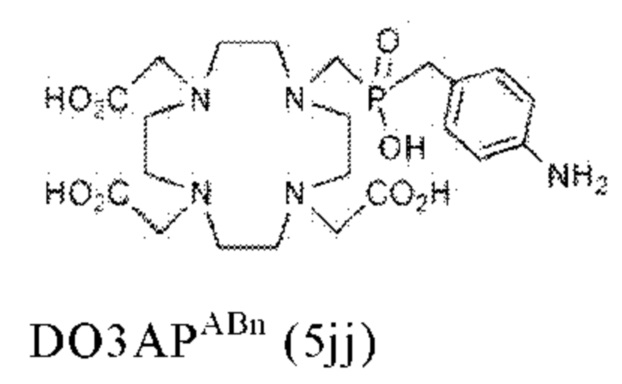
Хелатирующее соединение (D) можно выбирать из любых хелатирующих соединений (5а)-(5jj), как описано выше.
Предпочтительно хелатирующее соединение (D) выбирают из 1,4,7,10-тетраазациклододекан-1,4,7,10-тетрауксусной кислоты (DOTA), N,N''-бис[2-гидрокси-5-(карбоксиэтил)бензил]этилендиамин-N,N''-диуксусной кислоты (HBED-CC), 1,4,7-триазациклононан-1,4,7-триуксусной кислоты (NOTA), 2-(4,7-бис(карбоксиметил)-1,4,7-триазонан-1-ил)глутаровой кислоты (NODAGA), [2-(4,7,10-трис(карбоксиметил)-1,4,7,10-тетраазациклододекан-1-ил)глутаровой кислоты (DOTAGA), 1,4,7-триазациклононанфосфиновой кислоты (TRAP), 1,4,7-триазациклононан-1-[метил(2-карбоксиэтил)фосфиновая кислота]-4,7-бис[метил(2-гидроксиметил)фосфиновой кислоты] (NOPO), 3,6,9,15-тетразабицикло[9,3,1]пентадека-1(15),11,13-триен-3,6,9-триуксусной кислоты (РСТА), N'-{5-[ацетил(гидрокси)амино]пентил}-N-[5-({4-[(5-аминопентил)(гидрокси)амино]-4-оксобутаноил}амино)пентил]-N-гидроксисукцмнамида (DFO) и диэтилентриаминпентауксусной кислоты (DTPA) или их производных.
Более предпочтительно хелатирующее соединение может представлять собой DOTA (1,4,7,10-тетраазациклододекан-1,4,7,10-тетрауксусную кислоту формулы (5а)), NODAGA (2-(4,7-бис(карбоксиметил)-1,4,7-триазонан-1-ил)пентадикарбоновую кислоту формулы (5 с)) или их производные. В некоторых вариантах хелатирующее соединение представляет собой NODAGA.
Например, хелатирующим соединением является DOTA. Преимущество заключается в том, что DOTA эффективно образует комплексы с диагностическими (например, 68Ga) и терапевтическими (например, 90Y или 177Lu) радионуклидами и, таким образом, позволяет использовать один и тот же конъюгат одновременно для визуализации и для лечебных целей, т.е. в качестве терагностического (лечебно-диагностического) агента. Предпочтительными также могут являться производные DOTA, способные к комплексообразованию с радионуклидами скандия (43Sc, 44Sc, 47Sc), включающие DO3AP (соединение формулы (5hh)), DO3APPrA (соединение формулы (5ii)) или DO3APABn (соединение формулы (5jj)), которые описаны в статье Kerdjoudj и др., Dalton Trans., т. 45, сс. 1398-1409 (2016).
Другие предпочтительные хелатирующие соединения в контексте настоящего изобретения включают N,N''-бис[2-гидрокси-5-(карбоксиэтил)бензил]этилендиамин-N,N''-диуксусную кислоту (HBED-CC), 1,4,7-триазациклононан-1,4,7-триуксусную кислоту (NOTA), 2-(4,7,10-трис(карбоксиметил)-1,4,7,10-тетраазациклододекан-1-ил)-глутаровую кислоту (DOTAGA), 1,4,7-триазациклононанфосфиновую кислоту (TRAP), 1,4,7-триазацидононан-1-[метил(2-карбоксиэтил)фосфиновая кислота]-4,7-бис-[метил(2-гидроксиметил)фосфиновую кислоту] (NOPO), 3,6,9,15-тетраазабицикло[9,3,1]пентадека-1(15),11,13-триен-3,6,9-триуксусную кислоту (РСТА), N'-{5-[ацетил(гидрокси)амино]пентил}-]-N-[5-({4-[(5-аминопентил)(гидрокси)амино]-4-оксобутаноил}амино)пентил]-N-гидроксисукцинамид (DFO) и диэтилентриаминпентауксусную кислоту (DTPA).
Хелатирующая группа, например, группа DOTA, может образовывать комплекс с центральным ионом (металла), прежде всего с радионуклидом, как описано в данном контексте. В другом варианте хелатирующая группа, например, DOTA, может не образовывать комплекс с центральным ионом (металла), прежде всего с радионуклидом, как описано в данном контексте, и, таким образом, может присутствовать в некомплексной форме. В случаях, если хелатирующее соединение (например, DOTA) не образует комплекс с указанным ионом металла, то карбоксильные группы хелатирующего соединения могут присутствовать в форме свободной кислоты или в форме соли.
Ниже описаны конкретные типичные конъюгаты по настоящему изобретению, которые являются особо предпочтительными.
Предпочтительный типичный конъюгат по настоящему изобретению представлен формулой (8)(а) или (8)(а)':
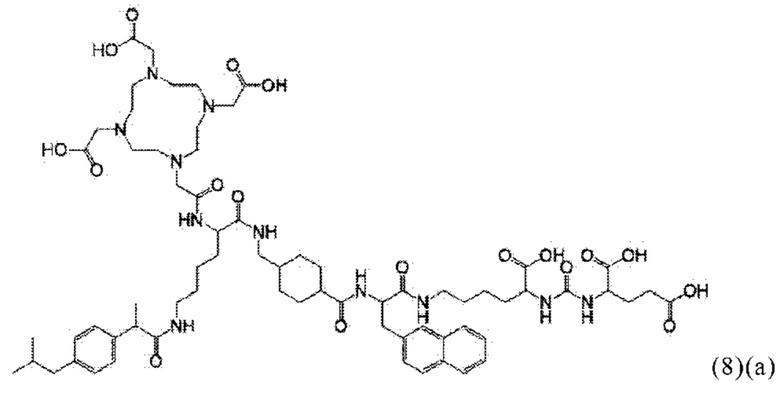
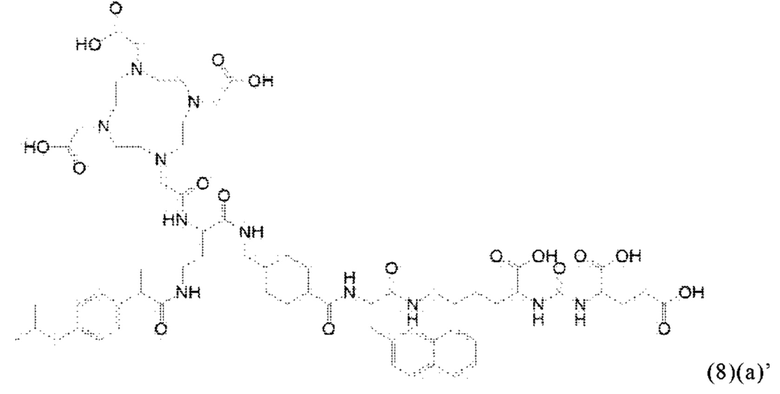
(Соединение формулы (8)(а) также названо «Ibu-PSMA») или его фармацевтически приемлемая соль, сложный эфир, сольват или радоактивно меченный комплекс.
Другой предпочтительный типичный конъюгат по настоящему изобретению представлен формулой (8)(b) или (8)(b)':
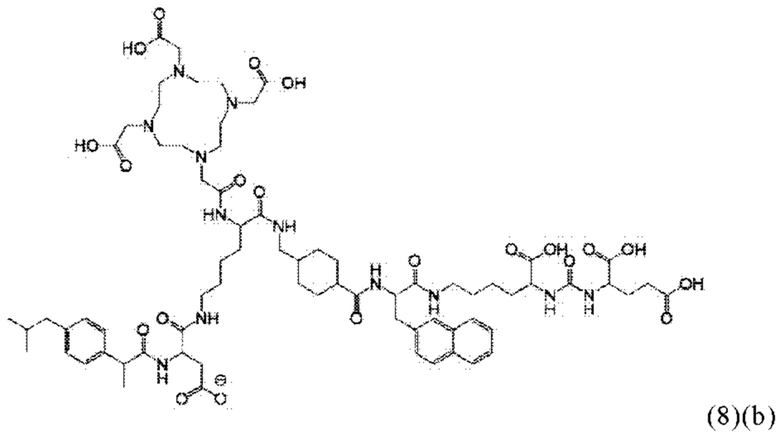
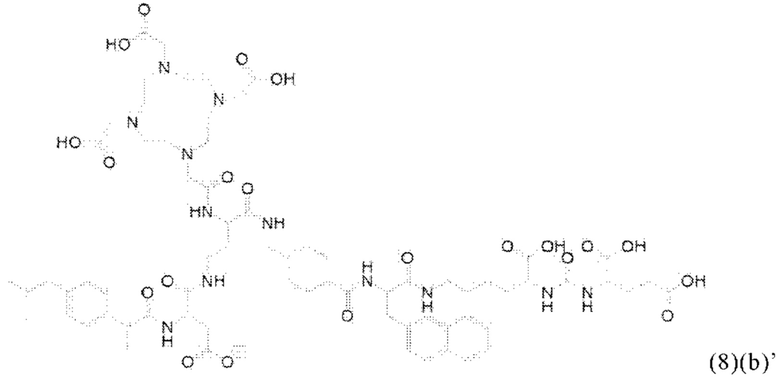
(Соединение формулы (8)(b) также названо «Ibu-Dα-PSMA») или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Другой предпочтительный типичный конъюгат по настоящему изобретению представлен формулой (8)(с) или (8)(с)':
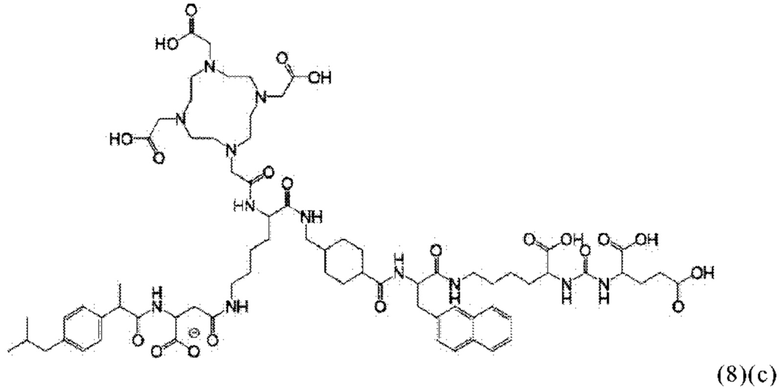
(Соединение формулы (8)(с) также названо «Ibu-Dβ-PSMA») или его фармацевтически приемлемая соль, сложный эфир, сольват или радиоактивно меченный комплекс.
Другой предпочтительный типичный конъюгат по настоящему изобретению представлен формулой (8)(d) или (8)(d)':
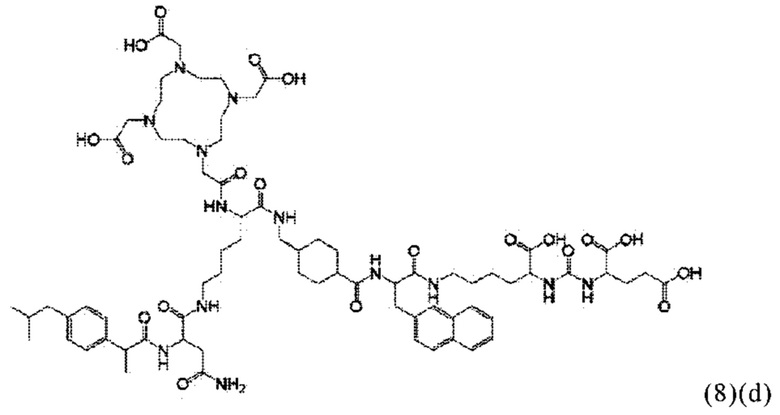
(Соединение формулы (8)(d) также названо «Ibu-N-PSMA») или его фармацевтически приемлемая соль, сложный эфир, сольват или радиактивно меченный комплекс.
Другой предпочтительный типичный конъюгат по настоящему изобретению представлен формулой (8)(e) или (8)(e)':
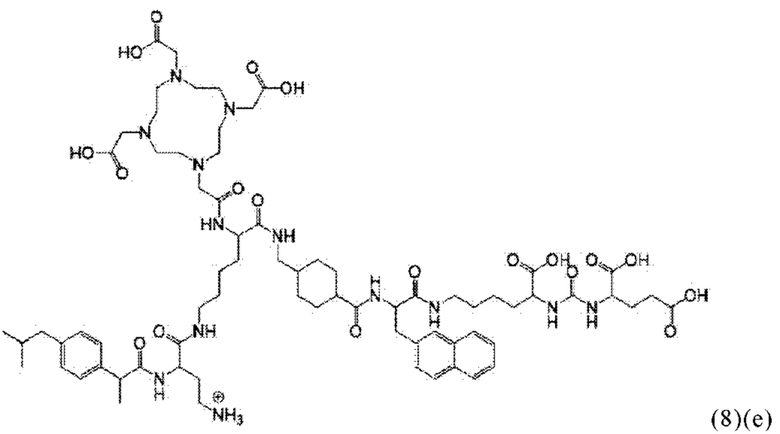
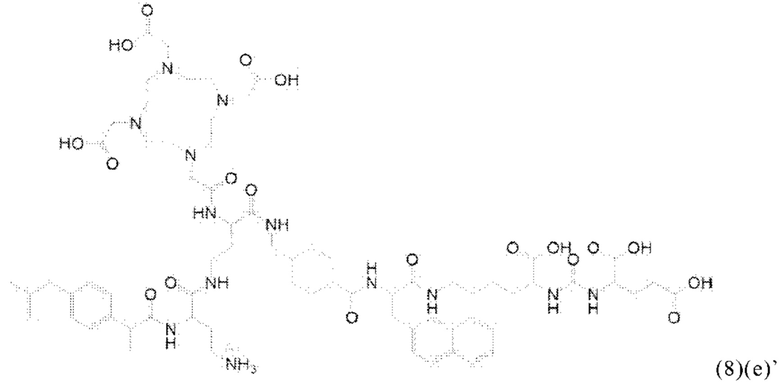
(Соединение формулы (8)(е) также названо «Ibu-DAB-PSMA») или его фармацевтически приемлемая соль, сложный эфир, сольват или радиактивно меченный комплекс.
Соединения всех формул (8)(а), (8)(а)', (8)(b), (8)(b)', (8)(с), (8)(с)', (8)(d), (8)(d)', (8)(е) и (8)(е)' также включают 0, 1, 3, 5, 6, 7 или 8 остатков -[СН]2, соединяющих группу NH в составе боковой цепи лизинового спейсера с точкой разветвления, вместо 2 и 4 метиленовых групп, как показано на приведенной выше формуле.
Фармацевтически приемлемые соли
Настоящее изобретение дополнительно включает фармацевтически приемлемые соли конъюгатов (соединений), описанных в данном контексте.
Получение фармацевтических композиций представляется очевидным специалистам в данной области техники. Фармацевтически приемлемые соли конъюгатов по настоящему изобретению можно получать по стандартным методикам, таким как взаимодействие любого свободного основания и/или кислоты конъюгата по настоящему изобретению по меньшей мере со стехиометрическим количеством требуемой солеобразующей кислоты или основания, соответственно.
Фармацевтически приемлемые соли по настоящему изобретению включают соли с неорганическими катионами, такими как натрий, калий, кальций, магний, цинк и аммоний, и соли с органическим основаниями. Пригодные органические основания включают N-метил-D-глюкамин, аргинин, бензатин, диоламин, оламин, прокам и трометамин. Фармацевтически приемлемые соли по настоящему изобретению включают также соли, полученные из органических или неорганических кислот. Пригодные анионы включают ацетат, адипат, безилат. бромид, камсилат, хлорид, цитрат, эдизилат, эстолат, фумарат, глюцептат, глюконат, глюкуронат, гиппурат, гиклат, гидробромид, гидрохлорид, иодид, изетионат, лактат, лактобионат, малеат, мезилат, метилбромид, метилсульфат, напсилат, нитрат, олеат, памоат, фосфат, полигалактуронат, стеарат, сукцинат, сульфат, сульфосалицилат, таннат, тартрат, терефталат, тозилат и триэтиодид.
Комплексные/некомплексные формы
В настоящем изобретении предлагаются также конъюгаты (соединения), описанные в данном контексте, где хелатирующее соединение (D) может образовывать комплекс с ионом металла (таким ка радионуклид) или может не образовывать комплекс.
Термин «радионуклид» (или «радиоизотоп») относится к изотопам природного или искусственного происхождения с нестабильным отношением нейтронов к протонам, при распаде которых наблюдается корпускулярное излучение (т.е. излучение протонов (альфа-излучение) или электронов (бета-излучение) или электромагнитное излучение (гамма-излучение)). Другими словами, радионуклиды подвергаются радиоактивному распаду. Хелатирующее соединение (D) может образовывать комплекс с любым известным радионуклидом. Указанный радионуклид предпочтительно может быть использован для визуализации или терапии онкологических заболеваний. Такие радионуклиды включают, но не ограничиваясь только ими, 94Tc, 99mTc, 90In, 111In, 67Ga, 68Ga, 86Υ, 90Y, 177Lu, 151Tb, 186Re, 188Re, 64Cu, 67Cu, 55Co, 57Co, 43Sc, 44Sc, 47Sc, 225Ac, 213Bi, 212Bi, 212Pb, 227Th, 153Sm, 166Ho, 152Gd, 153Gd, 157Gd, или 166Dy. Выбор пригодных радионуклидов может зависеть, среди прочего, от химической структуры и хелатирующей способности хелатирующего соединения (D), и предполагаемого применения полученного (в виде комплекса) конъюгата (например, применение для диагностики или терапии). С другой стороны, хелатирующее соединение (D) можно выбирать с учетом предполагаемого радионуклида/радиоактивного металла. Например, для сопутствующей (одновременной) системной радионуклидной терапии можно использовать бэта-излучающие изотопы, такие как 90Y, 131I, 161Tb и 177Lu. При использовании DOTA в качестве хелатирующего агента наиболее эффективным является применение в качестве радионуклидов 68Ga, 43,44,47Sc, 177Lu, 161Tb, 225Ac, 213Bi, 212Bi, 212Pb.
В некоторых предпочтительных вариантах настоящего изобретения радионуклид может представлять собой 177Lu. В некоторых предпочтительных вариантах осуществления настоящего изобретения радионуклид может представлять собой 44Sc. В некоторых предпочтительных вариантах осуществления настоящего изобретения радионуклид может представлять собой 64Cu. В некоторых предпочтительных вариантах осуществления настоящего изобретения радионуклид может представлять собой 68Ga. Наиболее предпочтительно радионуклидом является 177Lu.
Выбор пригодных комбинаций конъюгатов (соединений) и радионуклидов находится в пределах квалификации и знаний специалиста в данной области техники. Например, в некоторых предпочтительных вариантах осуществления хелатирующим соединением может являться DOTA, а радионуклидом может являться 177Lu. В других предпочтительных вариантах осуществления хелатирующим соединением может являться DOTA, а радионуклидом может являться 68Ga. В других предпочтительных вариантах осуществления хелатирующим соединением может являться DOTA, а радионуклидом может являться 44Sc. В еще более предпочтительных вариантах осуществления хелатирующим соединением может являться DOTA, а радионуклидом может являться 64Cu. В других предпочтительных вариантах осуществления хелатирующим соединением может являться NODAGA, а радионуклидом может являться 64Cu.
Сложные эфиры и пролекарства
В настоящем изобретении предлагаются также конъюгаты (соединения) по изобретению в их этерифицированной форме, прежде всего когда этерифицированы свободные карбоксильные группы. Такие этерифицированные соединения могут представлять собой пролекарственные формы конъюгатов по изобретению. Пригодные сложные эфиры пролекарств включают различные алкиловые эфиры, включая насыщенные и ненасыщенные C8-C18 жирные кислоты.
Энантиомеры
Конъюгаты (соединения), описанные в данном контексте, существуют в конкретных геометрических или стереоизомерных формах. Кроме того, соединения могут также являться оптически активными. Конъюгаты по изобретению могут также включать цис- и транс-изомеры, R- и S-энантиомеры, диастереомеры, (D)-изомеры и (L)-энантиомеры, их рацемические смеси и другие их смеси. В заместителе, таком как алкильная группа, могут присутствовать дополнительные ассиметрические атомы углерода. Если, например, требуется конкретный энантиомер группы или конъюгата, его можно получить методом ассиметрического синтеза или при получении производного с хиральным вспомогательным фрагментом, когда полученную смесь диастереомеров разделяют и вспомогательную группу отщепляют, при этом получают очищенные требуемые энантиомеры. В другом варианте, если группа или конъюгат содержит основную функциональную группу, такую как аминогруппа, или кислотную функциональную группу, такую как карбоксильная группа, то образуются диастереомерные соли, содержащие соответствующие оптически активные кислоту или основание, с последующим разделением полученных таким образом диастереомеров с использованием методов фракционной кристаллизации или хроматографических методов, известных специалистам в данной области техники, и с последующим выделением чистых энантиомеров.
Термин «стереоизомер» означает один стереоизомер соединения, который в основном не содержит других стереоизомеров этого соединения. Таким образом стереоизомерно чистое соединение, содержащее один хиральный центр, в основном не будет содержать противоположный энантиомер соединения. Стереоизомерно чистое соединение, содержащее два хиральных центра, в основном не будет содержать других диастереоизомеров соединения. Типичное стереоизомерно чистое соединение включает приблизительно более 80 мас. % одного стереоизомера соединения и менее приблизительно 20 мас. % других стереоизомеров соединения, например, приблизительно более 90 мас. % одного стереоизомера соединения и менее приблизительно 10 мас. % других стереоизомеров соединения, или приблизительно более 95 мас. % одного стереоизомера соединения и менее приблизительно 5 мас. % других стереоизомеров соединения, или приблизительно более 97 мас. % одного стереоизомера соединения и менее приблизительно 3 мас. % других стереоизомеров соединения.
Соответственно, все формулы, раскрытые в данном контексте, включают их энантиомеры и/или стереоизомеры.
Радиоактивно меченные комплексы
Согласно другому объекту, в настоящем изобретении предлагается применение конъюгата (соединения) по изобретению для получения радиоактивно меченных комплексов или их применение в качестве лекарственного препарата или предшественника лекарственного препарата. Такие радиоактивно меченные комплексы предпочтительно включают конъюгат (соединение) по настоящему изобретению согласно настоящему изобретению, и радионуклид. Хелатирующее соединение (D) предпочтительно образует координационную связь с радионуклидом, при этом образуется радиоактивно меченный комплекс. Пригодные радионуклиды можно выбирать из применяемых в тераностике изотопов металлов, и они включают, но не ограничиваясь только ими, 94Tc, 99mTc, 90In, 111In, 67Ga, 68Ga, 86Υ, 90Y, 177Lu, 151Tb, 186Re, 188Re, 64Cu, 67Cu, 55Co, 57Co, 43Sc, 44Sc, 47Sc, 225Ac, 213Bi, 212Bi, 212Pb, 227Th, 153Sm, 166Ho, 152Gd, 153Gd, 157Gd или 166Dy.
Согласно дополнительному объекту, в настоящем изобретении также предлагается комплекс, содержащий радионуклид (предпочтительно, как описано в данном документе) и конъюгат по изобретению.
Фармацевтические композиции
Согласно другому объекту, в настоящем изобретении предлагается также фармацевтическая композиция, включающая конъюгат (соединение) по изобретению (включающая фармацевтически приемлемые соли, сложные эфиры, сольваты или радиоактивно меченные комплексы, как описано в данном контексте), и фармацевтически приемлемый носитель и/или эксципиент.
Термин «фармацевтически приемлемый» относится к соединению или агенту, которые являются совместимыми с конъюгатом по изобретению и не ухудшают его диагностическую или терапевтическую активность и/или существенно не снижают ее. Фармацевтически приемлемые носители предпочтительно характеризуются достаточно высокой чистотой и достаточно низкой токсичностью, чтобы соответствовать условиям, установленным для введения субъекту, нуждающемуся в таком лечении.
Составы, носители и эксципиенты
Фармацевтически приемлемые эксципиенты могут выполнять различные функции и могут включать, но не ограничиваясь только ими, разбавители, наполнители, объемообразующие агенты, носители, дезинтегрирующие агенты, связующие агенты, смазывающие агенты, скользящие агенты, покрытия, растворители и сорастворители, буферные вещества, консерванты, скользящие вещества, адъюванты, антиоксиданты, увлажняющие агенты, антивспениватели, загустители, подсластители, ароматизаторы и смачивающие агенты.
Пригодные фармацевтически приемлемые эксципиенты обычно выбирают на основе состава (фармацевтической) композиции.
Для (фармацевтических) композиций в жидкой форме пригодные фармацевтически приемлемые наполнители, в основном, включают растворители, разбавители или носители, такие как (апирогенная) вода, (изотонические) солевые растворы, такие как фосфатный или цитратный буферный раствор, жирные масла, растительные масла, такие как, например, арахисовое масло, хлопковое масло, кунжутное масло, оливковое масло, кукурузное масло, этанол, полиолы (например, глицерин, пропиленгликоль, полиэтиленгликоль и т.п.), лецитин, ПАВ, консерванты, такие как бензиловый спирт, парабены, хлорбутанол, фенол, аскорбиновая кислота, тимеросал и т.п., изотонические агенты, такие как сахара, многоатомные спирты, такие как маннит, сорбит или хлорид натрия, моностеарат алюминия или желатин, антиоксиданты, такие как аскорбиновая кислота или бисульфит натрия, хелатирующие агенты, такие как этилендиаминтетрауксусная кислота (EDTA), буферные вещества, такие как ацетаты, цитраты или фосфаты, и агенты для регулировки тоничности, такие как хлорид натрия или декстроза, а величину рН можно доводить кислотами или основаниями, такими как соляная кислота или гидроксид натрия. Буферные растворы могут представлять собой гипертонические, изотонические или гипотонические растворы с учетом конкретной эталонной среды, т.е. буферный раствор может характеризоваться более высоком, идентичным или более низким содержанием соли по сравнению с конкретной эталонной средой, при этом предпочтительно следует использовать такие концентрации вышеупомянутых солей, которые не приводят к повреждению клеток из-за осмоса или других концентрационных эффектов. Эталонные среды представляют собой, например, жидкости, которые используют в методах in vivo, такие ка кровь, лимфа, цитозоль или другие жидкости организма, или, например, жидкости, которые можно использовать в качестве эталонных сред в методах in vitro, такие как стандартные буферные растворы или жидкости. Такие стандартные буферные растворы или жидкости известны специалистам в данной области техники.
Жидкие (фармацевтические) композиции, вводимые инъекцией и, прежде всего, внутривенным способом, предпочтительно следует вводить в стерильной и стабильной в условиях получения и хранения форме. Такие композиции обычно перерабатывают в парентерально приемлемые водные апирогенные растворы с пригодным значением рН, и они являются изотоническими и поддерживают стабильность активного ингредиента(ов).
В случае жидких фармацевтических композиций, пригодные фармацевтически приемлемые эксципиенты и носители включают воду, обычно апирогенную воду, изотонический солевой раствор или буферные (водные) растворы, например, фосфатные, цитратные и т.д., буферные растворы. Прежде всего, для (фармацевтических) композиций по изобретению, вводимых инъекцией, можно использовать воду или предпочтительно буферный раствор, более предпочтительно водный буферный раствор, который может содержать натриевую соль, например, по меньшей мере 50 мМ раствор натриевой соли, кальциевой соли, например, по меньшей мере 0,01 мМ раствор кальциевой соли и необязательно калиевой соли, например, не менее 3 мМ калиевой соли.
Соли натрия, кальция и, необязательно, калия могут находиться в форме их галогенидов, например, хлориды, йодиды или бромиды, в форме их гидроксидов, карбонатов, гидрокарбонатов или сульфатов и т.д. Примеры солей натрия, но не ограничиваясь только ими, включают, например, NaCl, NaI, NaBr, Na2CO3, NaHCO3, Na2SO4, примеры необязательных солей калия включают, например, KCl, KI, KBr, K2CO3, KHCO3, K2SO4 и примеры солей кальция включают, например, CaCl2, CaI2, CaBr2, СаСО3, CaSO4, Са(ОН)2. Кроме того, в буферном растворе могут содержаться органические анионы вышеупомянутых катионов.
Буферные растворы, пригодные для введения инъекцией, как определено выше, могут содержать соли, выбранные из хлорида натрия (NaCl), хлорида кальция (CaCl2) и, необязательно, хлорида калия (KCl), где кроме хлоридов могут присутствовать другие анионы. CaCl2 также можно заменить другой солью, такой как KCl. Обычно соли в буферном растворе для инъекций присутствуют в концентрации по меньшей мере 50 мМ хлорида натрия (NaCl), по меньшей мере 3 мМ хлорида калия (KCl) и по меньшей мере 0,01 мМ хлорида кальция (CaCl2). Буферные растворы могут представлять собой гипертонические, изотонические или гипотонические растворы в зависимости от конкретной эталонной среды, т.е. буферный раствор может характеризоваться более высоком, идентичным или более низким содержанием соли по сравнению с конкретной эталонной средой, при этом предпочтительно можно использовать такие концентрации вышеупомянутых солей, которые не приводят к повреждению клеток из-за осмоса или других концентрационных эффектов.
В случае (фармацевтических) композиций в (полутвердой) форме, пригодные фармацевтически приемлемые эксципиенты и носители включают связующие агенты, такие как микрокристаллическая целлюлоза, трагакантовая камедь или желатин, крахмал или лактоза, сахара, такие как, например, лактоза, глюкоза и сахароза, крахмалы, такие как, например, кукурузный крахмал или картофельный крахмал, целлюлоза и ее производные, такие как, например, натриевая соль карбоксиметилцеллюлозы, этилцеллюлоза, ацетат целлюлозы; дезинтегрирующие агенты, такие как альгиновая кислота; смазывающие вещества, такие как стеарат магния; скользящие вещества, такие как стеариновая кислота, стеарат магния; сульфат кальция, коллоидный диоксид кремния и т.п.; подсластители, такие как сахароза или сахарин; и/или ароматизаторы, такие как мята перечная, метилсалицилат или апельсиновый ароматизатор.
В основном, (фармацевтические) композиции для местного введения можно перерабатывать в кремы, мази, гели, пасты или порошкообразные препараты. (Фармацевтические) композиции для перорального введения можно перерабатывать в таблетки, капсулы, жидкости, порошкообразные препараты или в формы для замедленного высвобождения. Однако, согласно предпочтительным вариантам осуществления настоящего изобретения, (фармацевтическая) композиция предназначена для парентерального введения, прежде всего для внутривенной или внутриопухолевой инъекции, и ее соответственно перерабатывают в жидкую или лиофилизированную форму для парентерального введения, как описано в данном контексте. Парентеральные составы обычно хранят во флаконах, мешках (пакетах) для внутривенного вливания, ампулах, картриджах, или в предварительно заполненных шприцах, и их можно вводить в виде инъекционных форм, ингаляционных форм или аэрозолей, при этом предпочтительными являются инъекционные формы.
(Фармацевтическая) композиция может быть представлена в лиофилизированной форме. Лиофилизированные (фармацевтические) композиции перед введением предпочтительно растворяют в пригодном буферном растворе, преимущественно на основе водного носителя.
(Фармацевтическая) композиция предпочтительно включает безопасное и эффективное количество конъюгата (конъюгатов) или радиоактивно меченных комплекса(сов).
Использованный в данном контексте термин «безопасное и эффективное количество» означает количество агента (агентов), достаточное для обеспечения диагноза и/или значительной индукции положительного воздействия на заболевание, предназначенное для лечения или профилактики. В то же время, однако, «безопасное и эффективное количество» должно быть достаточно малым, чтобы исключить серьезные побочные эффекты, то есть обеспечить разумную взаимосвязь между преимуществом и риском. «Безопасное и эффективное количество», кроме того, будет изменяться в зависимости от конкретного состояния, которое требуется диагностировать или лечить, а также от возраста и физического состояния пациента, нуждающегося в таком лечении, тяжести состояния, продолжительности лечения, характера сопутствующей терапии, конкретного используемого фармацевтически приемлемого эксципиента или носителя и подобных факторов.
Конъюгаты (соединения) по изобретению также предназначены для применения при приготовлении лекарственного препарата, предпочтительно для применения при лечении рака или для лечения рака, прежде всего, для лечения и/или профилактики рака предстательной железы, рака поджелудочной железы, рака почек или рака мочевого пузыря.
Набор
Согласно другому объекту, в настоящем изобретении предлагается также набор, включающий конъюгат (конъюгаты) по изобретению (включая фармацевтически приемлемые соли, сложные эфиры, сольваты или их радиоактивно меченные комплексы) и/или фармацевтическую композицию (композиции) по изобретению.
Необязательно, набор может включать по меньшей мере один дополнительный агент, как определено в данном контексте в отношении фармацевтической композиции, включающей радионуклиды, антибактериальные агенты, солюбилизирующие агенты и т.п.
Набор может представлять собой набор из двух или более частей, включающий любые перечисленные выше компоненты в пригодных контейнерах. Например, каждый контейнер может быть представлен в форме флаконов, бутылок, легко сжимаемых бутылок, банок, герметичных туб, конвертов или пакетов, тюбиков или блистерных упаковок или любой другой пригодной формы, при условии, что в контейнере предпочтительно исключено преждевременное смешивание компонентов. Каждый из различных компонентов может быть предоставлен отдельно, или некоторые из различных компонентов могут быть предоставлены вместе (то есть в одном контейнере).
Контейнер также может представлять собой отделение или камеру во флаконе, тубе, банке или конверте, или рукаве, или блистерной упаковке, или бутылке, при условии, что исключен физический контакт содержимого одного отделения с содержимым другого отделения до их преднамеренного смешивания фармацевтом или врачом.
Набор или комплект из компонентов, кроме того, может содержать технические инструкции с информацией о введении и/или дозировке любого из его компонентов.
Терапевтические и диагностические методы и применение
Согласно другому объекту, в настоящем изобретении предлагается конъюгат (соединение) (включающий фармацевтически приемлемые соли, сложные эфиры, сольваты и их радиоактивно меченные комплексы), фармацевтическая композиция или набор по настоящему изобретению для применения в медицине. Более того, в изобретении предлагается также конъюгат или соединение (включающие фармацевтически приемлемые соли, сложные эфиры, сольваты и их радиоактивно меченные комплексы), фармацевтическая композиция или набор по настоящему изобретению для применения в диагностике. Предпочтительно конъюгаты (соединения), фармацевтические композиции или наборы по изобретению предназначены для применения в медицине. Соответственно, изобретение также включает конъюгаты (соединения), фармацевтическую композицию или набор по изобретению для применения в качестве лекарственного средства.
Конъюгаты (соединения) предпочтительно обладают способностью селективно и направленно воздействовать на простатоспецифический мембранный антиген (PSMA). Таким образом в конкретном объекте предлагаются конъюгаты (соединения), фармацевтические композиции или наборы по изобретению для применения в способе выявления присутствия клеток и/или тканей, экспрессирующих PSMA.
PSMA прежде всего экспрессируется в злокачественных раковых клетках. Использованный в данном контексте термин «рак» означает новообразование, прежде всего злокачественное новообразование. Обычно новообразование характеризуется неконтролируемой и обычно быстрой пролиферацией клеток, которые имеют тенденцию проникать в окружающие ткани и метастазировать в отдаленные участки тела. Термин «новообразование» охватывает доброкачественные и злокачественные новообразования. Злокачественные новообразования (рак) обычно характеризуются анаплазией, инвазивностью и/или метастазированием, в то время как доброкачественные новообразования обычно не проявляют ни одно из этих свойств. Термин «рак» включает рост опухоли (например, солидные опухоли), а также другие раки, например, рак крови и лимфатической системы.
Более подробно, PSMA может экспрессироваться, необязательно в повышенных количествах, в клетках рака предстательной железы, клетках рака поджелудочной железы, клетках рака почки или клетках рака мочевого пузыря.
Согласно другому конкретному объекту в изобретении предлагается конъюгат (соединение) по настоящему изобретению (включающий фармацевтически приемлемые соли, сложные эфиры, сольваты и их радиоактивно меченные комплексы), фармацевтическая композиция или набор по настоящему изобретению для применения в способе диагностики, лечения и/или профилактики рака, прежде всего рака предстательной железы, рака поджелудочной железы, рака почки или рака мочевого пузыря.
Термин «диагноз» или «диагностика» относится к процессу идентификации заболевания по его признакам и симптомам, и/или, как в данном случае, к анализу биологических маркеров (таких как гены или белки), свидетельствующих о заболевании.
Термин «лечение» или «терапия» заболевания включает предотвращение или защиту от заболевания (то есть предотвращение развития клинических симптомов), ингибирование заболевания (то есть приостановка или подавление развития клинических симптомов, и/или ослабление симптомов заболевания (то есть, вызывая регрессию клинических симптомов). Следует понимать, что не всегда возможно провести различие между «предотвращением» и «подавлением» заболевания или расстройства, поскольку конечное индуктивное событие или события могут быть неизвестными или латентными. Соответственно, термин «профилактика» следует понимать как обозначающий тип «лечения», который включает в себя как «предотвращение», так и «подавление». Таким образом, термин «лечение» включает в себя «профилактику».
Термин «субъект», «пациент» или «индивидуум», использованный в данном контексте, в основном включает людей и нечеловекоподобных животных и предпочтительно млекопитающих (например, обезьян, включая мартышек, тамаринов, паукообразных обезьян, трехполосых дурукули, верветок, беличьих обезьян и павианов, макак, шимпанзе, орангутанов, горилл, крупный рогатый скот, лошадей, овец, свиней, семейство кошачьих, собак, мышей, крыс, кроликов, морских свинок и т.д.), включая химерных и трансгенных животных и модели болезней. В контексте настоящего изобретения термин «субъект» предпочтительно относится к не человекоподобному примату или человеку, наиболее предпочтительно человеку.
Применение и способы, описанные в данном контексте и относящиеся к диагностике, лечению или профилактике рака, прежде всего рака предстательной железы, рака поджелудочной железы, рака почки или рака мочевого пузыря, могут предпочтительно включать следующие этапы: (а) введение пациенту конъюгата (включающего фармацевтически приемлемые соли, сложные эфиры, сольваты и их радиоактивно меченные комплексы), фармацевтической композиции или набора по настоящему изобретению, (б) получение рентгеновского изображения указанного пациента.
Конъюгаты (соединения), фармацевтические композиции или наборы по изобретению обычно вводят парентеральным методом. Введение можно предпочтительно осуществлять системным методом, например, с использованием внутривенной (в./в.), подкожной, внутримышечной или внутрикожной инъекции. В другом варианте, введение можно осуществлять местным методом, например, с использованием внутриопухолевой инъекции.
Конъюгаты (соединения), фармацевтические композиции или наборы по изобретению можно вводить субъекту, нуждающемуся в таком лечении, несколько раз в день, ежедневно, через день, еженедельно или ежемесячно. Предпочтительно лечение, диагностику или профилактику можно осуществлять с помощью эффективной дозы конъюгатов, фармацевтических композиций или наборов по изобретению.
Эффективные дозы конъюгатов по изобретению можно определять в ходе обычных экспериментов, например с использованием моделей животных. Такие модели включают, но не ограничиваясь только ими, модели кроликов, овец, мышей, крыс, собак и не человекоподобных приматов. Терапевтическую эффективность и токсичность конъюгатов или радиоактивно меченых комплексов по изобретению можно определять по стандартным фармацевтическим методикам на культурах клеток или экспериментальных животных, например, для определения LD50 (доза, летальная для 50% популяции) и ED50 (доза, терапевтически эффективная для 50% популяции). Соотношение токсической дозы и терапевтически эффективной дозы является терапевтическим индексом и его выражают как отношение LD50/ED50. Данные, полученные методами анализа клеточных культур и экспериментов на животных, можно использовать для определения диапазона доз для применения при лечении человека. Доза указанных конъюгатов предпочтительно находится в диапазоне циркулирующих концентраций, который включает ED50 с небольшой токсичностью или в отсутствии токсичности.
Например, терапевтически или диагностически эффективные дозы конъюгатов по изобретению могут находиться в интервале от приблизительно 0,001 мг до 10 мг, предпочтительно приблизительно от 0,01 мг до 5 мг, более предпочтительно от приблизительно от 0,1 мг до 2 мг в стандартной лекарственной форме или приблизительно от 0,01 нмолей до 1 ммоля в стандартной лекарственной форме, прежде всего от 1 нмоля до 1 ммоля в стандартной лекарственной форме, предпочтительно от 1 мкмоля до 1 ммоля в стандартной лекарственной форме. Предполагается также, что терапевтически или диагностически эффективные дозы конъюгатов (соединений) по изобретению могут изменяться (на кг массы тела) в интервале от приблизительно 0,01 мг/кг до 10 г/кг, предпочтительно приблизительно от 0,5 мг/кг до 5 г/кг, более предпочтительно приблизительно от 0,1 мг/кг до 2,5 г/кг. Преимущество заключается в том, что конъюгаты по изобретению в связи с их благоприятными фармакокинетическими свойствами можно вводить в более низких дозах по сравнению с другими лигандами PSMA.
Как указано выше, конъюгаты по изобретению прежде всего пригодны для применения в тераностике, включая доставку в PSMA-экспрессирующие клетки. Используемый в данном контексте термин «терапевтические» включает «только терапевтические», «только диагностические» и «терапевтические и диагностические» методы. В другом объекте настоящего изобретения предлагается способ in vitro детектирования присутствия клеток и/или тканей, экспрессирующих простатоспецифический мембранный антиген (PSMA), причем способ включает а) контактирование указанных PSMA-экспрессирующих клеток и/или тканей с конъгатами по изобретению (включающими их фармацевтически приемлемые соли, сложные эфиры, сольваты и радиоактивно меченные комплексы), с фармацевтическими композициями или наборами, и (б) использование детектирующих средств, необязательно аппаратов для рентгеновской визуализации, с целью выявления указанных клеток и/или тканей.
При осуществлении применения и способов in vivo и in vitro по настоящему изобретению рентгеновскую визуализацию можно проводить с использованием любых средств и методов, известных в данной области техники. Предпочтительно рентгеновская визуализация может включать позитронно-эмиссионную томографию (PET) или однофотонную эмиссионную компьютерную томографию (SPECT). Клетки-мишени или ткани-мишени, выявляемые методом рентгеновской визуализации конъюгата по изобретению, могут включать (необязательно раковые) клетки или ткани предстательной железы, (необязательно раковые) клетки или ткани селезенки, или (необязательно раковые) клетки или ткани почки.
При осуществлении применения и способов in vivo и in vitro по настоящему изобретению присутствие PSMA-экспрессирующих клеток или тканей может указывать на опухоль (клетку) предстательной железы, метастазирующую опухоль (клетку) предстательной железы, опухоль (клетку) почек, опухоль (клетку) поджелудочной железы, опухоль (клетку) мочевого пузыря и их комбинации. Следовательно, конъгаты по изобретению (включающими их фармацевтически приемлемые соли, сложные эфиры, сольваты и радиоактивно меченные комплексы), фармацевтические композиции и наборы прежде всего можно использовать для диагностики (и необязательно для лечения) рака предстательной железы, рака почки, рака поджелудочной железы или рака мочевого пузыря.
Краткое описание фигур
В следующем разделе кратко описаны прилагаемые фигуры. Фигуры предназначены для более подробной иллюстрации настоящего изобретения. Однако они никоим образом не предназначены для ограничения предмета изобретения.
На фиг. 1 представлена схема 1 синтеза связывающего мотива, глютамат-мочевина-лизин, для Ibu-DAB-PSMA.
На фиг. 2 представлена схема 2 синтеза фрагмента линкера, предшественника Ibu-Dab-PSMA.
На фиг. 3 представлена схема 3 синтеза DOTA-конъюгированного предшественника Ibu-Dab-PSMA.
На фиг. 4 представлена схема 4 конденсации дополнительного фрагмента линкера и альбумин-связывающего фрагмента для соединения Ibu-DAB-PSMA.
На фиг. 5 представлены типичные хроматограммы ЖХВР модифицированных ибупрофеном лигандов 177Lu-PSMA, как описано в примере 4. (А) хроматограмма 177Lu-Ibu-PSMA, (В) хроматограмма 177Lu-Ibu-Dβ-PSMA, (С) хроматограмма 177Lu-Ibu-Dα-PSMA, (D) хроматограмма 177Lu-Ibu-N-PSMA, (E) хроматограмма 177Lu-Ibu-DAB-PSMA. На хроматограммах указаны времена удерживания tR.
На фиг. 6 представлены коэффициенты распределения в н-октаноле/PBS соединений 177Lu-Ibu-PSMA, 177Lu-Ibu-Dβ-PSMA, 177Lu-Ibu-Dα-PSMA, 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA, как описано в примере 5, по сравнению с эталонным соединением 177Lu-PSMA-617. Эксперименты проводили три раза (n=3) в пяти параллельных повторах.
На фиг. 7 представлены данные анализа методом ультрафильтрации соединений 177Lu-Ibu-PSMA, 177Lu-Ibu-Dβ-PSMA, 177Lu-Ibu-Dα-PSMA, 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA, как описано в примере 6, по сравнению с соединением 177Lu-PSMA-617. (n=3).
На фиг. 8 представлены данные по захвату и интернализации соединений 177Lu-Ibu-PSMA, 177Lu-Ibu-Dβ-PSMA, 177Lu-Ibu-Dα-PSMA, 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA, как описано в примере 7, по сравнением с соединением 177Lu-PSMA-617. (А) Данные получены с использованием PSMA-положительных клеток РС-3 PIP (n=3). (В) Данные получены с использованием PSMA-положительных клеток РС-3 flu (n=1).
На фиг. 9 представлены данные по биораспределению пяти модифицированных ибупрофеном радиолигандов и соединения 177Lu-PSMA-617, полученные в экспериментах с использованием мышей с привитой опухолью РС-3 PIP/flu, как описано в примере 8. (А) Данные по биораспределению, полученные через 4 ч после инъекции радиолигандов, (В) Данные по биораспределению, полученные через 24 ч после инъекции радиолигандов.
На фиг. 10 представлены соотношения радиоактивности опухоль/фон через 4 и 24 ч после инъекции лигандов 177Lu-PSMA, как описано в примере 8. (А) Соотношение опухоль/кровь, (В) соотношение опухоль/печень и (С) соотношение опухоль/почки для всех лигандов 177Lu-Ibu-PSMA через 4 ч и 24 ч после инъекции.
На фиг. 11 представлена активность в целом организме, измеренная с помощью дозкалибратора через 0 ч, 4 ч, 24 ч, 48 ч и 72 ч после инъекции соответствующих радиолигандов, как описано в примере 9. Активность, измеренная сразу после инъекции, была принята за 100%. Данные для сравнительных радиолигандов 177Lu-PSMA-ALB-53/56 и 177Lu PSMA 617 включены в этот график для сравнения. Точки на графике представляют собой среднее значение для двух мышей, которым вводили один и тот же радиолиганд (n=2).
На фиг. 12 представлены изображения SPECT/CT, полученные через 4 ч после инъекции лигандов 177Lu-PSMA, представленные в виде максимальной интенсивности в программе проекций максимальной интенсивности (MIP). (А) 177Lu-Ibu-PSMA, (В) 177Lu-Ibu-Dβ-PSMA, (С) 177Lu-Ibu-Dβ-PSMA, (D) 177Lu-Ibu-N-PSMA, (E) 177Lu-Ibu-DAB-PSMA. PSMA+ = PSMA-положительный опухолевый ксенотрансплантат РС-3 PIP, PSMA- = PSMA-отрицательный опухолевый ксенотрансплантат РС-3 flu, Кi = почки, BI = мочевой пузырь.
На фиг. 13 представлена схема, на которой показана конденсация фрагмента ибупрофена с предшественником 1 (включающим PSMA-связывающий фрагмент и хелатирующий агент DOTA) для синтеза Ibu-sPSMA.
На фиг. 14 представлена типичная хроматограмма ЖХВР соединения 177Lu-Ibu-sPSMA. На графике указано время удерживания tr.
На фиг. 15 представлена радиолитическая стабильность интактного соединения 177Lu-Ibu-PSMA в процентах в течение 24 ч. (А) Соединение 177Lu-Ibu-sPSMA инкубировали в отсутствии L-аскорбиновой кислоты, (В) соединение 177Lu-Ibu-sPSMA инкубировали в присутствии L-аскорбиновой кислоты (среднее ± СО, n=3). Соединение 177Lu-Ibu-sPSMA проявляло значительно более высокую стабильность по сравнению с соединением 177Lu-PSMA-617 и всеми другими модифицированными ибупрофеном радиолигандами PSMA. Стабильность соединения 177Lu-Ibu-sPSMA сопоставима со стабильностью 177Lu-PSMA-ALB-56.
На фиг. 16 представлены данные анализа ультрафильтрацией соединения 177Lu-Ibu-sPSMA по сравнению с соединением 177Lu-PSMA-617. (n=3).
На фиг. 17 представлены данные по захвату и интернализации соединения 177Lu-Ibu-sPSMA по сравнению с соединением 177Lu-PSMA-617. (А) Данные получены с использованием PSMA-положительных клеток РС-3 PIP (n=3). (В) Данные получены с использованием PSMA-отрицательных клеток РС-3 flu (n=3).
На фиг. 18 представлен график данных по биораспределению соединений 177Lu-Ibu-PSMA, 177Lu-Ibu-DAB-PSMA, 177Lu-Ibu-sPSMA и 177Lu-Ibu-PSMA-617, полученных с использованием мышей с привитой опухолью РС-3 PIP/flu. (А) Данные по биораспределению через 1 ч после инъекции радиолигандов, (В) данные по биораспределению через 4 ч после инъекции радиолигандов, (С) данные по биораспределению через 24 ч после инъекции радиолигандов и (D) данные по биораспределению через 96 ч после инъекции радиолигандов.
На фиг. 19 представлен график соотношений опухоль/фон через 1 ч, 4 ч, 24 ч и 96 ч после инъекции 177Lu-Ibu-sPSMA по сравнению с соединениями 177Lu-Ibu-PSMA и 177Lu-Ibu-DAB-PSMA. (А) Соотношения опухоль/кровь, (В) соотношения опухоль/почки и (С) соотношения опухоль/печень.
На фиг. 20 представлена активность в целом организме, измеренная с помощью дозкалибратора через различные периоды времени после инъекции. Активность, измеренная сразу после инъекции, принята за 100%. Опубликованные данные для соединения 177Lu PSMA 617 включены в графики для сравнения. Точки на графике представляют собой среднее значение для двух мышей, которым вводили один и тот же радиолиганд (n=2-3). (А) На графике указаны данные для всех радиолигандов, (В) на графике указаны данные для 177Lu-Ibu-PSMA, 177Lu-Ibu-DAB-PSMA, 177Lu-PSMA-617 и 177Lu-PSMA-ALB-56 для лучшей визуализации единичных кривых выведения.
На фиг. 21 представлены изображения SPECT/CT, полученные после инъекции соединения 177Lu-Ibu-sPSMA, на которых указана максимальная интенсивность в программе проекций максимальной интенсивности (MIP). (А) Изображения SPECT/CT, полученные через 4 ч после инъекции, (В) изображения SPECT/CT, полученные через 24 ч после инъекции. PSMA+ = PSMA-положительный опухолевый ксенотрансплантат РС-3 PIP; PSMA- = PSMA-отрицательный опухолевый ксенотрансплантат РС-3 flu; Ki = почки, Bl = мочевой пузырь.
На фиг. 22 представлены данные по относительному росту опухоли у контрольных мышей и у мышей, которым вводили (а) низкую дозу активности (2 МБк, 1 наномоль на мышь) или (в) более высокую дозу активности (5 МБк, 1 наномоль на мышь). В каждой группе мышам вводили только носитель (солевой раствор) и ( ), 177Lu-Ibu-DAB-PSMA (
), 177Lu-Ibu-DAB-PSMA ( ), 177Lu-PSMA-617 (
), 177Lu-PSMA-617 ( ) и 177Lu-PSMA-ALB-56 (
) и 177Lu-PSMA-ALB-56 ( ), соответственно, через 6 дней после прививки опухолевых клеток (среднее ± СО, n=6-12). Указаны средние относительные объемы опухоли в каждой группе, пока показатели первой мыши не достигнут конечных значений.
), соответственно, через 6 дней после прививки опухолевых клеток (среднее ± СО, n=6-12). Указаны средние относительные объемы опухоли в каждой группе, пока показатели первой мыши не достигнут конечных значений.
На фиг. 23 представлен график анализа методом Каплана-Мейера с кривыми выживаемости для мышей в каждой группе (n=12). Контрольные мыши и мыши, которым вводили (а) низкую дозу активности (2 МБк, 1 наномоль на мышь) или (в) более высокую дозу активности (5 МБк, 1 наномоль на мышь). Нелеченые контрольные мыши ( ), 177Lu-Ibu-DAB-PSMA (
), 177Lu-Ibu-DAB-PSMA ( ); 177Lu-PSMA-617 (
); 177Lu-PSMA-617 ( ) и 177Lu-PSMA-ALB-56 (
) и 177Lu-PSMA-ALB-56 ( ).
).
На фиг. 24 представлена относительная масса тела (RBW) контрольных мышей и мышей, которым вводили (а) низкую дозу активности (2 МБк, 1 наномоль на мышь) или (в) более высокую дозу активности (5 МБк, 1 наномоль на мышь). Средняя RBW мышей, которым вводили только носитель (солевой раствор) ( ), 177Lu-Ibu-DAB-PSMA (
), 177Lu-Ibu-DAB-PSMA ( ), 177Lu-PSMA-617 (
), 177Lu-PSMA-617 ( ) и 177Lu-PSMA-ALB-56 (
) и 177Lu-PSMA-ALB-56 ( ), соответственно. Указаны средние RBW в каждой группе, пока показатели первой мыши не достигнут конечных значений.
), соответственно. Указаны средние RBW в каждой группе, пока показатели первой мыши не достигнут конечных значений.
Примеры
В следующем разделе представлены конкретные примеры, иллюстрирующие различные варианты осуществления и объекты настоящего изобретения. Однако настоящее изобретение не ограничивается объемом конкретных вариантов осуществления, описанных в данном контексте. Представленные ниже препараты и примеры даны, чтобы специалист в данной области техники мог более ясно понять и применить настоящее изобретение на практике. Однако объем настоящего изобретения не ограничен приведенными в качестве примеров вариантами осуществления, которые предназначены для иллюстрации только отдельных объектов изобретения, и способы, которые являются функционально эквивалентными, включены в объем изобретения. Действительно, для специалистов в данной области техники представляются очевидными различные модификации изобретения в дополнение к описанным в данном контексте из предшествующего описания, прилагаемых фигур и примеров, приведенных ниже. Все такие модификации включены в объем прилагаемой формулы изобретения.
Пример 1
Структурное конструирование типичных лигандов PSMA Для индентификации лигандов PSMA, которые обеспечивают баланс между (i) связыванием радиолиганда с альбумином, чтобы обеспечить оптимальный профиль распределения в ткани с высоким уровнем захвата опухолью, и (ii) уровнями активности в крови, которые не очень высоки, что может привести к риску нежелательных побочных эффектов для здоровых тканей, были сконструированы следующие пять модифицированных ибупрофеном лигандов PSMA (Ibu-PSMA, Ibu-Dα-PSMA, Ibu-Dβ-PSMA, Ibu-N-PSMA и Ibu-DAB-PSMA):
1.1. Ibu-PSMA:
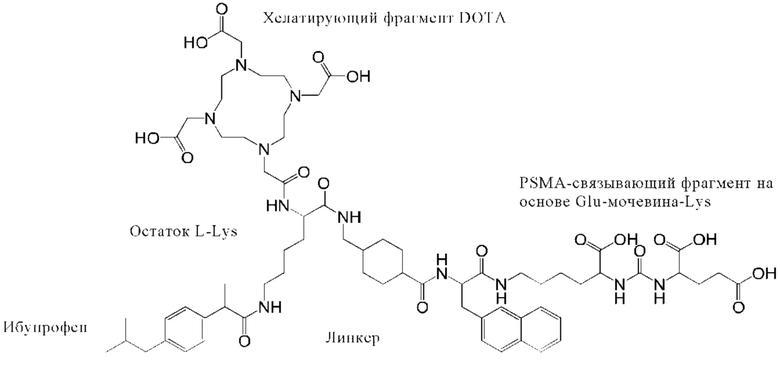
1.2. Ibu-Dα-PSMA:
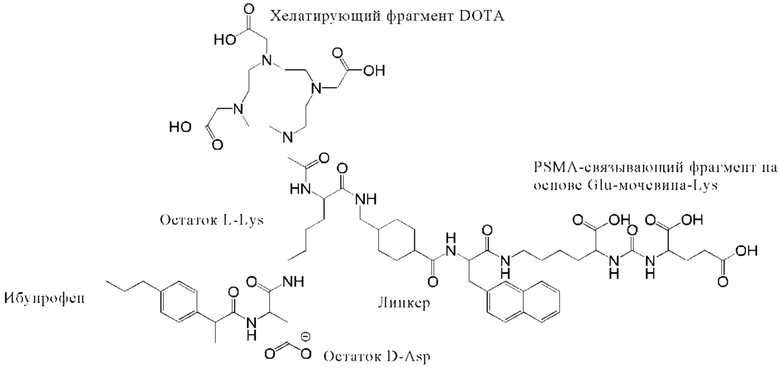
1.3. Ibu-Dβ-PSMA:
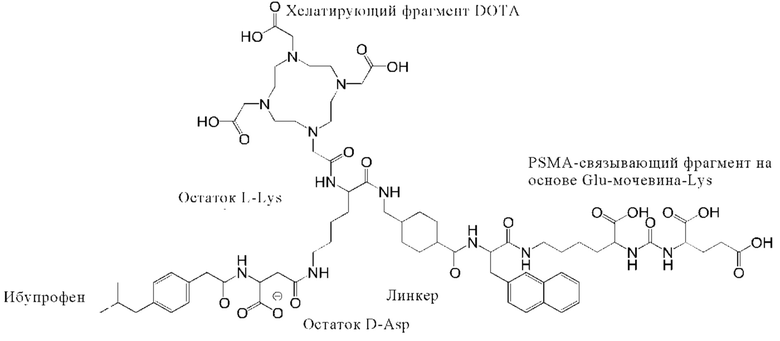
1.4. Ibu-N-PSMA:
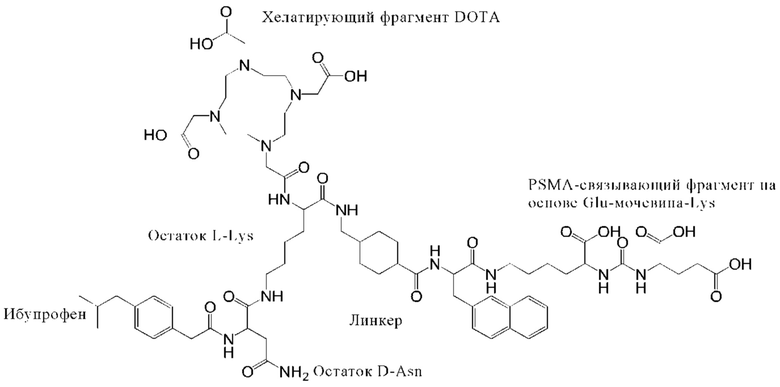
1.5. Ibu-DAB-PSMA:
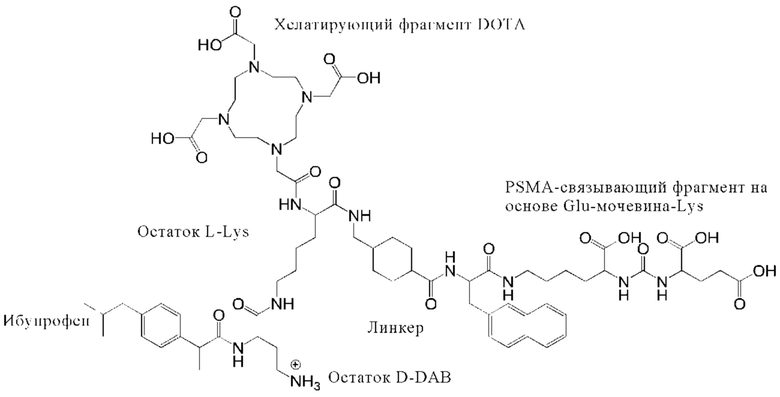
Соединение Ibu-PSMA представляет собой простейший конструкт модифицированного ибупрофеном лиганда PSMA. Этот конструкт был разработан при введении связывающегося с альбумином ибупрофена без какого-либо дополнительного спейсера за счет присоединения ибупрофена непосредственно к остатку лизина. При получении соединений Ibu-Dα-PSMA и Ibu-Dβ-PSMA для введения дополнительного отрицательного заряда в конструкт использовали дополнительный спейсер на основе D-аспарагиновой кислоты (D-Asp, D) (в дополнение к остатку L-Lys). Остаток D-Asp присоединяли либо через α-карбоксильную группу для получения Ibu-Dα-PSMA, либо через β-карбоксильную группу для получения Ibu-Dβ-PSMA. Для получения соединения Ibu-N-PSMA использовали другой дополнительный фрагмент спейсера на основе D-аспарагина (D-Asn, N) (в дополнение к остатку l-Lys). И наконец, для введения в конструкт дополнительного положительного заряда, конструкт Ibu-DAB-PSMA был получен при использовании D-диаминомасляной кислоты (DAB) в качестве дополнительного фрагмента спейсера (в дополнение к остатку L-Lys).
1.6. Ibu-sPSMA
Соединение Ibu-sPSMA конструировали аналогично соединению Ibu-PSMA. В отличие от Ibu-PSMA, в котором остаток ибупрофена присоединен через боковую цепь лизина, в качестве соединительного фрагмента была использована более короткая L-2,4-диаминомасляная кислота (L-DAB).
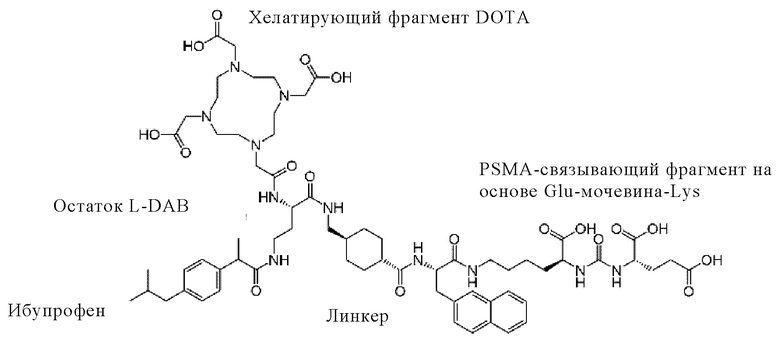
Пример 2
Химический синтез типичных лигандов PSMA 2.1. Стратегия синтеза и анализ лигандов PSMA Все пять предложенных лигандов PSMA с альбумин-связывающим фрагментом синтезировали с использованием твердофазной платформы, как было ранее опубликовано для других лигандов PSMA ((Umbricht С.Α., Benesova Μ., Schibli R., Preclinical development of novel PSMA-targeting radioligands: modulation of albumin-binding properties to improve prostate cancer therapy. Mol Ρharm, Mol Pharm, 75, (6), 2297-2306 (2018)). Этот метод был предложен для использования при разработке описанных модифицированных ибупрофеном лигандов PSMA. Эти лиганды были получены в ходе многостадийного синтеза (17 стадий для Ibu-PSMA и 19 стадий Ibu-Dα-PSMA, Ibu-Dβ-PSMA, Ibu-N-PSMA и Ibu-DAB-PSMA), общие выходы выделенных соединений составляли ≥ 2,8% после очистки методом ЖХВР. Лиганды были охарактеризованы методами аналитической офЖХВР и MALDI-MC, соответственно. Степень очистки соединений составляла ≥ 99,2%. Данные анализа представлены в таблице 1.
Preclinical development of novel PSMA-targeting radioligands: modulation of albumin-binding properties to improve prostate cancer therapy. Mol Ρharm, Mol Pharm, 75, (6), 2297-2306 (2018)). Этот метод был предложен для использования при разработке описанных модифицированных ибупрофеном лигандов PSMA. Эти лиганды были получены в ходе многостадийного синтеза (17 стадий для Ibu-PSMA и 19 стадий Ibu-Dα-PSMA, Ibu-Dβ-PSMA, Ibu-N-PSMA и Ibu-DAB-PSMA), общие выходы выделенных соединений составляли ≥ 2,8% после очистки методом ЖХВР. Лиганды были охарактеризованы методами аналитической офЖХВР и MALDI-MC, соответственно. Степень очистки соединений составляла ≥ 99,2%. Данные анализа представлены в таблице 1.
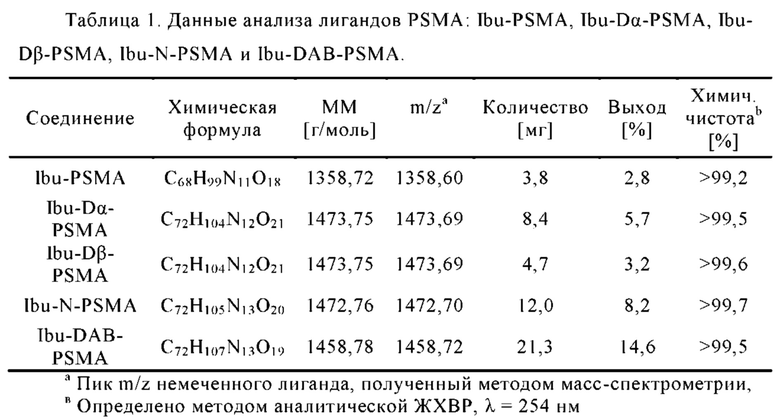
2.2. Синтез предшественника 1
PSMA-направленный фрагмент на основе мочевины, связывающий PSMA, L-Glu-NH-CO-NH-L-Lys, получали на смоле с иммобилизованным 2-хлортритилхлоридом (2-СТ) аналогично тому, как описано в статье Eder и др. (Eder Μ.,  Bauder-Wust U., Hull W. E.,
Bauder-Wust U., Hull W. E.,  C, Mier, W., Haberkorn U., Eisenhut, M. 68Ga-complex lipophilicity and the targeting property of a urea-based PSMA inhibitor for PET imaging. Bioconjug Chem, 23, (4), 688-697 (2012). Фрагмент линкера, содержащий остатки 2-нафтил-L-А1а и trans-циклогексил, синтезировали, как описано ранее в статье Benesova и др. (Benesova Μ.,
C, Mier, W., Haberkorn U., Eisenhut, M. 68Ga-complex lipophilicity and the targeting property of a urea-based PSMA inhibitor for PET imaging. Bioconjug Chem, 23, (4), 688-697 (2012). Фрагмент линкера, содержащий остатки 2-нафтил-L-А1а и trans-циклогексил, синтезировали, как описано ранее в статье Benesova и др. (Benesova Μ., 
 Afshar-Oromieh Α., Kratochwil С, Mier W., Haberkorn U., Корка K., Eder, M. Preclinical evaluation of a tailor-made DOTA-conjugated PSMA inhibitor with optimized linker moiety for imaging and endoradiotherapy of prostate cancer. J Nucl Med, 56, (6), 914-920 (2015). Конъюгат хелатирующего агента DOTA, присоединенного через фрагмент Nα-амино-L-Lys к описанному выше конструкту, получали, как описано в статье Umbricht и др. (Umbricht С.Α., Benesova Μ., Schibli R.,
Afshar-Oromieh Α., Kratochwil С, Mier W., Haberkorn U., Корка K., Eder, M. Preclinical evaluation of a tailor-made DOTA-conjugated PSMA inhibitor with optimized linker moiety for imaging and endoradiotherapy of prostate cancer. J Nucl Med, 56, (6), 914-920 (2015). Конъюгат хелатирующего агента DOTA, присоединенного через фрагмент Nα-амино-L-Lys к описанному выше конструкту, получали, как описано в статье Umbricht и др. (Umbricht С.Α., Benesova Μ., Schibli R.,  . Preclinical development of novel PSMA-targeting radioligands: modulation of albumin-binding properties to improve prostate cancer therapy. Mol Ρharm, 15, (6), 2297-2306 (2018).
. Preclinical development of novel PSMA-targeting radioligands: modulation of albumin-binding properties to improve prostate cancer therapy. Mol Ρharm, 15, (6), 2297-2306 (2018).
Для синтеза PSMA лигандов («предшественник 1») в качестве основы использовали следующий иммобилизованный на смоле предшественник:
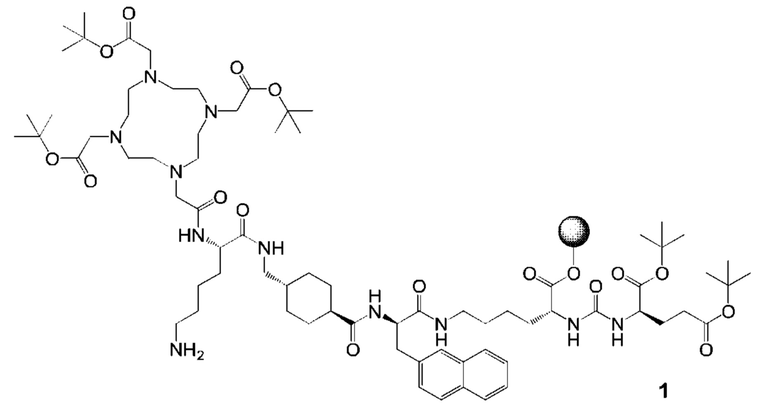
Структура предшественника 1 основана на PSMA-связывающем фрагменте и хелатирующем фрагменте DOTA. Этот предшественник использовали для синтеза пяти типичных лигандов Ibu-PSMA, Ibu-Dα-PSMA, Ibu-Dβ-PSMA, Ibu-N-PSMA и Ibu-DAB-PSMA. Свободную аминогруппу боковой цепи лизина использовали для присоединения ибупрофена, который присоединен напрямую или через фрагмент аминокислоты.
2.3. Синтез Ibu-PSMA
Синтез Ibu-PSMA осуществляли присоединением альбумин-связывающего ибупрофена к иммобилизованному на смоле предшественнику 1. Смолу набухали в безводном дихлорметане (DCM, Acros Organics) в течение 45 мин и затем кондиционировали в N,N-диметилформамиде (DMF, Acros Organics). В расчете на иммобилизованный на смоле предшественник 1 (0,10 ммоля), 4,0-6,0 экв. 2-(4-(2-метилпропил)фенил)пропионовой кислоты (ibuprofen, Sigma Aldrich, 0,400-0,600 ммоля) активировали с использованием 3,96 экв. Ν,Ν,Ν',N'-тетраметил-O-(1H-бензотриазол-1-ил)уроний гексафторфосфата (HBTU, Sigma Aldrich, 0,396-0,594 ммоля) в присутствии 4,0-6,0 экв. DIPEA (Ν,Ν-диизопропилэтиламин, Sigma Aldrich, 0,400-0,600 ммоля) в безводном DMF. Через 2 мин после добавления DIPEA, активированный раствор добавляли к предшественнику 1 и встряхивали в течение 2 ч. Смолу промывали DMF, DCM и диэтиловым эфиром, соответственно, и высушивали при пониженном давлении. Продукт отщепляли от смолы и затем удаляли защитные группы в течение 3-6 ч с использованием смеси, состоящей из трихлоруксусной кислоты (TFA, Sigma Aldrich), триизопропилсилана (TIPS, Sigma Aldrich) и воды Milli-Q в соотношении 95:2,5:2,5 (об./об.). TFA упаривали, неочищенное соединение растворяли в ацетонитриле (ACN, VWR Chemicals) и воде Milli-Q в соотношении 1:2 (об./об.) и очищали хроматографией офЖХВР, при этом получали Ibu-PSMA.
2.4. Синтез Ibu-Dα-PSMA
Дополнительный фрагмент спейсера, D-аспарагиновой кислоты (D-Asp), присоединяли к остатку Νε-L-лизина в составе предшественника 1 перед присоединением к ибупрофену. Иммобилизованный на смоле предшественник 1 предварительно набухали в DCM и кондиционировали в DMF, как описано выше. В расчете на массу предшественника 1 (0,100 ммоля), активировали 4,0 экв. Fmoc- и t-Bu-защищенную d-Asp (Fmoc- D-Asp(O-t-Bu)-OH, Sigma Aldrich, 0,400 ммоля) с использованием 3,96 экв. HBTU (0,396 ммоль) в присутствии 4,0 экв. DIPEA (0,400 ммоля) в безводном DMF. Через 2 мин после добавления DIPEA активированный раствор добавляли к предшественнику 1 и встряхивали в течение 2 ч, смолу промывали DMF. Nα-Fmoc-защитную группу отщепляли при перемешивании со смесью DMF и пиперидина (Fluka) в соотношении 1:1 (об./об.) два раза в течение 5 мин. Смолу снова промывали DMF. Ибупрофен (4,0-6,0 экв., 0,400-0,600 ммоля) активировали с использованием 3,96 экв. HBTU (0,396-0,594 ммоля) в присутствии 4,0-6,0 экв. DIPEA (0,400-0,600 ммоля) в безводном DMF. Через 2 мин после добавления DIPEA активированный раствор добавляли к смоле и встряхивали в течение 2 ч. Затем смолу промывали DMF, DCM и диэтиловым эфиром, соответственно, и высушивали при пониженном давлении. Продукт отщепляли от смолы и одновременно удаляли защитную группу в присутствии смеси, содержащей TFA, TIPS и воду в соотношении 95:2,5:2,5 (об./об.) в течение 3-6 ч. TFA упаривали, неочищенное соединение растворяли в ацетонитриле (ACN, VWR Chemicals) и воде Milli-Q в соотношении 1:2 (об./об.) и очищали с использованием офЖХВР, при этом получали Ibu-Dα-PSMA.
2.5. Синтез Ibu-Dβ-PSMA
Дополнительный фрагмент спейсера, содержащий остаток D-аспарагиновой кислоты (D-Asp), присоединяли к остатку Νε-L-лизина в составе предшественника 1 перед присоединением к ибупрофену. Иммобилизованный на смоле предшественник 1 предварительно набухали в DCM и кондиционировали в DMF, как описано выше. В расчете на массу предшественника 1 (0,100 ммоля), активировали 4,0 экв. Fmoc- и t-Bu-защищенную d-Asp (Fmoc-d-Asp(O-t-Bu)-OH, Sigma Aldrich, 0,400 ммоля) с использованием 3,96 экв. HBTU (0,396 ммоля) в присутствии 4,0 экв. DIPEA (0,400 ммоля) в безводном DMF. Через 2 мин после добавления DIPEA активированный раствор добавляли к предшественнику 1 и встряхивали в течение 2 ч. Na-Fmoc-защитную группу отщепляли при перемешивании со смесью DMF и пиперидина (Fluka) в соотношении 1:1 (об./об.) два раза в течение 5 мин. Смолу снова промывали DMF. Ибупрофен (4,0-6,0 экв., 0,400-0,600 ммоля) активировали с использованием 3,96 экв. HBTU (0,396-0,594 ммоля) в присутствии 4,0-6,0 экв. DIPEA (0,400-0,600 ммоля) в безводном DMF. Через 2 мин после добавления DIPEA активированный раствор добавляли к смоле и встряхивали в течение 2 ч. Смолу промывали DMF, DCM и диэтиловым эфиром, соответственно, и высушивали при пониженном давлении. Продукт отщепляли от смолы и одновременно удаляли защитную группу в присутствии смеси, содержащей TFA, TIPS и воду в соотношении 95:2,5:2,5 (об./об.) в течение 3-6 ч. TFA упаривали, неочищенное соединение растворяли в ацетонитриле (ACN, VWR Chemicals) и воде Milli-Q в соотношении 1:2 (об./об.) и очищали хроматографией офЖХВР, при этом получали Dβ-PSMA.
2.6. Синтез Ibu-N-PSMA
Дополнительный фрагмент спейсера, содержащий остаток D-аспарагина (D-Asn) присоединяли к остатку Νε-L-лизина в составе предшественника 1 перед присоединением к ибупрофену. Иммобилизованный на смоле предшественник 1 предварительно набухали в DCM и кондиционировали в DMF, как описано выше. В расчете на массу предшественника 1 (0,100 ммоля), активировали 4,0 экв. Fmoc- и Trt (trityl)-защищенный D-аспарагин (Fmoc-D-Asn(Trt)-OH, Sigma Aldrich, 0,400 ммоля) с использованием 3,96 экв. HBTU (0,396 ммоля) в присутствии 4,0 экв. DIPEA (0,400 ммоля) в безводном DMF. Через 2 мин после добавления DIPEA активированный раствор добавляли к предшественнику 1 и встряхивали в течение 3 ч. Смолу промывали DMF и Na-Fmoc-защитную группу отщепляли при обработке в присутствии смеси DMF и пиперидина (Fluka) в соотношении 1:1 (об./об.) два раза в течение 5 мин. Смолу снова промывали DMF. Ибупрофен (4,0-6,0 экв., 0,400-0,600 ммоля) активировали с использованием 3,96 экв. HBTU (0,396-0,594 ммоля) в присутствии 4,0-6,0 экв. DIPEA (0,400-0,600 ммоля) в безводном DMF. Через 2 мин после добавления DIPEA, активированный раствор добавляли к смоле и встряхивали в течение 2 ч. Затем смолу промывали DMF, DCM и диэтиловым эфиром, соответственно, и высушивали при пониженном давлении. Продукт отщепляли от смолы в присутствии смеси, содержащей TFA, TIPS и воду в соотношении 95:2,5:2,5 (об./об.), в течение 3-6 ч. t-Bu-защитные группы и дополнительную Trt-защитную группу отщепляли одновременно. TFA упаривали, неочищенное соединение растворяли в ацетонитриле (ACN, VWR Chemicals) и воде Milli-Q в соотношении 1:2 (об./об.) и очищали хроматографией офЖХВР, при этом получали Ibu-N-PSMA.
2.7. Синтез Ibu-DAB-PSMA
Дополнительный фрагмент спейсера, содержащий остаток D-диаминомасляной кислоты, присоединяли к остатку Νε-L-лизина в составе предшественника 1 перед присоединением к ибупрофену. Иммобилизованный на смоле предшественник 1 предварительно набухали в DCM и кондиционировали в DMF, как описано выше. В расчете на массу предшественника 1 (0,100 ммоля), активировали 4,0 экв. Fmoc- и Вое (tert-Butyloxycarbonyl)-защищенной D-диаминомасляной кислоты (DAB; Fmoc-D-Dab(Boc)-OH, Iris Biotech, 0,400 ммоля) с использованием 3,96 экв. HBTU (0,396 ммоля) в присутствии 4,0 экв. DIPEA (0,400 ммоля) в безводном DMF. Через 2 мин после добавления DIPEA, активированный раствор добавляли к предшественнику 1 и встряхивали в течение 3,5 ч. Смолу промывали DMF и Nα-Fmoc-защитную группу отщепляли при перемешивании в присутствии смеси DMF и пиперидина (Fluka) в соотношении 1:1 (об./об.) два раза в течение 5 мин. Смолу снова промывали DMF. Ибупрофен (4,0-6,0 экв., 0,400-0,600 ммоля) активировали с использованием 3,96 экв. HBTU (0,396-0,594 ммоля) в присутствии 4,0-6,0 экв. DIPEA (0,400-0,600 ммоля) в безводном DMF. Через 2 мин после добавления DIPEA активированный раствор добавляли к смоле и встряхивали в течение 2 ч. Затем смолу промывали DMF, DCM и диэтиловым эфиром, соответственно, и высушивали при пониженном давлении. Продукт отщепляли от смолы в присутствии смеси, содержащей TFA, TIPS и воду в соотношении 95:2,5:2,5 (об./об.), в течение 3-6 ч. t-Bu-защитные группы и дополнительную Вос-защитную группу отщепляли одновременно. TFA упаривали, неочищенное соединение растворяли в ацетонитриле (ACN, VWR Chemicals) и воде Milli-Q в соотношении 1:2 (об./об.) и очищали хроматографией офЖХВР, при этом получали Ibu-DAB-PSMA.
2.8. Синтез Ibu-sPSMA
Аналогично ибупрофен-содержащим лигандам PSMA, соединение Ibu-sPSMA получали с использованием твердофазной платформы, как описано ранее (см. также раздел 2 выше) для синтеза других лигандов PSMA (Umbricht С.Α., Mol Pharm, 15 (6):2297-2306 (2018)). Этот лиганд получали с использованием многостадийной схемы синтеза (17 стадий) с общим выходом ≥ 14% после очистки ЖХВР.
2.8.1. Синтез предшественника 1
PSMA-направленный фрагмент на основе мочевины сайт, связывающий PSMA, L-Glu-NH-CO-NH-L-Lys, получали на смоле с иммобилизованным 2-хлортритилхлоридом (2-СТ) аналогично тому, как описано в статье Eder и др. (Eder и др. Bioconjug Chem, 23, (4), 688-697 (2012), см. раздел 2 выше. Фрагмент линкера, содержащий остатки 2-нафтил-L-Ala и trans-циклогексил, синтезировали, как описано ранее в статье Benesova et al. (Benesova и др., J Nucl Med, 56, (6), 914-920 (2015). Однако в этом случае использовали другой предшественник в отличие от соединений, использованных для синтеза других лигандов Ibu-PSMA. Для синтеза использовали более короткий фрагмент линкера, L-диаминомасляной кислоты (короче на два атома углерода по сравнению с L-лизином), который был использован в качестве линкера для синтеза Ibu-PSMA. Присоединение хелатирующего агента DOTA к описанному выше конструкту описано ранее в статье Umbricht и др. (Mol Pharm, 15(6):2297-2306 (2018)).
Следующий иммобилизованный на смоле предшественник (предшественник 1)
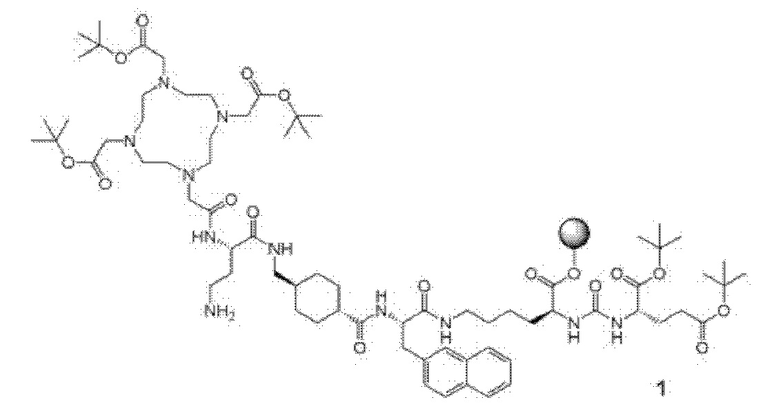
синтезировали на основе схемы синтеза Ibu-sPSMA. Структура предшественника 1 основана на PSMA-связывающем фрагменте и хелатирующем фрагменте DOTA. Этот предшественник включал более короткий связующий фрагмент в отличие от других лигандов Ibu-PSMA, например, Ibu-PSMA.
2.8.2. Синтез Ibu-sPSMA
Синтез Ibu-sPSMA проводили при присоединении связывающего альбумин ибупрофена к иммобилизованному на смоле предшественнику 1 (фиг. 13). Для присоединения ибупрофена использовали свободную γ-аминогруппу боковой цепи диаминомасляной кислоты. Смолу набухали в безводном дихлометане (DCM, Acros Organics) в течение 45 мин и затем кондиционировали в Ν,Ν-диметилформамиде (DMF, Acros Organics). В расчете на иммобилизованный на смоле предшественник 1 (0,10 ммоля), 6,0 экв. 2-(4-(2-метилпропил)фенил)пропионовой кислоты (ibuprofen, Sigma Aldrich, 0,60 ммоля) активировали с использованием 5,94 экв. Ν,Ν,Ν',Ν'-тетраметил-O-(1Н-бензотриазол-1-ил)уроний гексафторфосфата (HBTU, Sigma Aldrich, 0,59 ммоля) в присутствии 8,0 экв. DIPEA (N,N-диизопропилэтиламин, Sigma Aldrich, 0,80 ммоля) в безводном DMF. Через 2 мин после добавления DIPEA, активированный раствор добавляли к предшественнику 1 и встряхивали в течение 2 ч, при этом получали иммобилизованное на смоле соединение 2 (фиг. 13). Смолу промывали DMF, DCM и диэтиловым эфиром, соответственно, и высушивали при пониженном давлении. Продукт отщепляли от смолы и затем удаляли защитные группы в течение 2 ч с использованием смеси, состоящей из трихлоруксусной кислоты (TFA, Sigma Aldrich), триизопропилсилана (TIPS, Sigma Aldrich) и воды Milli-Q в соотношении 95:2,5:2,5 (об./об.), при этом получали неочищенный продукт (фиг. 13). TFA упаривали, неочищенное соединение растворяли в ацетонитриле (ACN, VWR Chemicals) и воде Milli-Q в соотношении 1:2 (об./об.) и очищали хроматографией офЖХВР, при этом получали очищенный Ibu-sPSMA.
Лиганд характеризовали аналитической ЖХВР и масс-спектрометрией MALDI-MS, соответственно. Степень химической очистки соединения составляла ≥ 99%. Данные анализа представлены в табл. 2.

2.9. Синтез соединения Ibu-DAB-PSMA в качестве примера На схемах синтеза 1-4, которые представлены на фиг. 1-4, соответственно, подробно описан синтез соединения Ibu-DAB-PSMA в качестве примера. Синтез других типичных соединений проводили по аналогичной схеме.
Пример 4
Включение метки и стабильность
Исходный раствор описанного в предшествующем уровне техники PSMA-лиганда, PSMA-617 (АВХ GmbH, Radeberg, Германия), получали при разбавлении лиганда в воде MilliQ до конечной концентрации 1 мМ. Соединения Ibu-PSMA, Ibu-Dα-PSMA, Ibu-Dβ-PSMA, Ibu-N-PSMA и Ibu-DAB-PSMA разбавляли в смеси вода Milli-Q/ацетат натрия (0,5 М, рН 8) до конечной концентрации 1 мМ. Во все PSMA-лиганды вводили метку 177Lu (177Lu без носителя добавляли в 0,05 Μ HCl, Isotope Technologies Garching ITG GmbH, Германия) в смеси 1:5 (об./об.) ацетата натрия (0,5 М, рН 8) и HCl (0,05 М, рН ~1) при рН ~4,5. Удельная активность PSMA-лигандов, меченых изотопом 177Lu, составляла 5-50 МБк/нмоль, в зависимости от проводимого эксперимента. Реакционную смесь инкубировали в течение 10 мин при 95°С с последующим контролем качества с использованием оф-ЖХВР на обращенно-фазовой колонке С-18 (Xterra™ MS, С18, 5 мкм, 150×4,6 мм, Waters). Мобильная фаза состояла из воды MilliQ, содержащей 0,1% трифторуксусной кислоты (А) и ацетонитрила (В), градиент от 95% А и 5% В до 20% А и 80% В в течение 15 мин, скорость потока 1,0 мл/мин. Радиолиганды перед нанесением на колонку ЖХВР разбавляли в воде Milli-Q, содержащей Na-DTPA (50 мкМ). На фиг.5 показаны типичные хроматограммы ЖХВР.
Пример 5
Коэффициент распределения н-октанол/PBS
Коэффициент распределения в системе н-октанол/PBS для пяти типичных PSMA связывающих фрагментов, 177Lu-Ibu-PSMA, 177Lu-Ibu-Da-PSMA, 177Lu-Ibu-Dβ-PSMA, 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA, определяли аналогично тому, как описано ранее (Benesova Μ., Umbricht С.Α., Schibli R.,  Albumin-binding PSMA ligands: optimization of the tissue distribution profile. Mol Pharm, 15, (3), 934-946 (2018).
Albumin-binding PSMA ligands: optimization of the tissue distribution profile. Mol Pharm, 15, (3), 934-946 (2018).
Результаты представлены на фиг.6. Все радиолиганды характеризовались гидрофильными свойствами, при этом значения logD составляли < 2,2. Соединения 177Lu-Ibu-PSMA, 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA характеризовались аналогичными значениями, в то время как коэффициенты соединении 177Lu-Ibu-Dβ-PSMA и 177Lu-Ibu-Dα-PSMA незначительно снижались, что указывает на повышенные гидрофильные свойства. Модификация лигандов PSMA ибупрофеном приводила к увеличению гидрофобных свойств радиолигандов по сравнению известным в предшествующем уровне техники PSMA лигандом, 177Lu-PSMA-617, который не содержит альбумин-связывающий фрагмент.
Пример 6
Альбумин связывающие свойства in vitro
Связывающие белки сыворотки крови свойства пяти типичных PSMA связывающих агентов 177Lu-Ibu-PSMA, 177Lu-Ibu-Dα-PSMA, 177Lu-Ibu-Dβ-PSMA, 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA, а также известного в предшествующем уровне техники PSMA агента, 177Lu-PSMA-617 (который не содержит альбумин-связывающий фрагмент) определяли методом анализа ультрафильтрацией аналогично тому, как описано ранее ((Benesova Μ., Umbricht С.Α., Schibli R., Albumin-binding PSMA ligands: optimization of the tissue distribution profile. Mol Pharm, 15, (3), 934-946 (2018). Краткое описание анализа: PSMA-лиганды, меченые изотопом 177Lu, удельная активность которых составляла 50 МБк/нмоль, инкубировали в образцах плазмы человека или в PBS при комнатной температуре. Фракции, не содержащие и содержащие связанные белки плазмы разделяли с использованием ячейки для ультрафильтрации с центрифугированием (ячейки 4104 centrifugal filter units, Millipore, номинальный молекулярно-массовый предел 30000 Да, метилцеллюлозные мембраны для ультрафильтрации). Инкубированный раствор помещали в ячейку для ультрафильтрации и центрифугировали при 2500 об/мин при 20°С в течение 40 мин. Отбирали образцы из фильтрата и определяли радиоактивность на счетчике γ-излучения. Количество связанного с плазмой радиолиганда рассчитывали как долю радиоактивности, измеренную в фильтрате, по отношению к радиоактивности соответствующего исходного, помещенного в ячейку раствора (принята за 100%). Эксперименты проводили не менее 3 раз для каждого радиолиганда.
Albumin-binding PSMA ligands: optimization of the tissue distribution profile. Mol Pharm, 15, (3), 934-946 (2018). Краткое описание анализа: PSMA-лиганды, меченые изотопом 177Lu, удельная активность которых составляла 50 МБк/нмоль, инкубировали в образцах плазмы человека или в PBS при комнатной температуре. Фракции, не содержащие и содержащие связанные белки плазмы разделяли с использованием ячейки для ультрафильтрации с центрифугированием (ячейки 4104 centrifugal filter units, Millipore, номинальный молекулярно-массовый предел 30000 Да, метилцеллюлозные мембраны для ультрафильтрации). Инкубированный раствор помещали в ячейку для ультрафильтрации и центрифугировали при 2500 об/мин при 20°С в течение 40 мин. Отбирали образцы из фильтрата и определяли радиоактивность на счетчике γ-излучения. Количество связанного с плазмой радиолиганда рассчитывали как долю радиоактивности, измеренную в фильтрате, по отношению к радиоактивности соответствующего исходного, помещенного в ячейку раствора (принята за 100%). Эксперименты проводили не менее 3 раз для каждого радиолиганда.
Результаты представлены на фиг. 7. Эксперименты по ультрафильтрации соединений 177Lu-Ibu-PSMA, 177Lu-Ibu-Dα-PSMA, 177Lu-Ibu-Dβ-PSMA, 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA указывают на высокий уровень связывания сывороточных белков, о чем свидетельствует тот факт, что <11% радиолигандов проникают через фильтрационную мембрану после инкубации в плазме человека. Радиолиганды не удерживаются фильтрационной мембраной при инкубации в PBS (в котором белки не содержатся). Соединения 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA характеризуются незначительно сниженным связыванием с белками плазмы по сравнению с другими модифицированными ибупрофеном радиолигандами. Все пять типичных PSMA-связывающих 177Lu-PSMA-лигандоы характеризовались повышенным связыванием с белками плазмы по сравнению с соединением 177Lu-PSMA-617, альбумин-связывающая фракция которого составляет лишь приблизительно 59%.
Пример 7
Исследование интернализации клетками in vitro
Захват и интернализацию клетками соединений Lu-Ibu-PSMA, 177Lu-Ibu-Dα-PSMA, 177Lu-Ibu-Dβ-PSMA, 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA исследовали с использованием PSMA-положительных РС-3 PIP и PSMA-отрицательных РС-3 flu опухолевых клеток, любезно предоставленных профессором др. Martin Pomper (John Hopkins Institutions, Baltimore, U.S., Eiber Μ., Fendler W. P., Rowe S. P., Calais J., Hofman M. S., Maurer Т., Schwarzenboeck S. M., Kratowchil C, Herrmann K., Giesel F. L. Prostate-specific membrane antigen ligands for imaging and therapy. J Nucl Med, 58, (Suppl 2), 67S-76S (2017)). Каждый радиолиганд исследовали в ходе экспериментов, проведенных 3 раза в трех повторах с использованием опухолевых клеток РС-3 PIP и один раз в трех повторах с использованием опухолевых клеток РС-3 flu.
Результаты представлены на фиг. 8. Захват всех радиолигандов опухолевыми клетками РС-3 PIP сопоставим с соединением 177Lu-PSMA-617 после инкубации в течение 2 ч или 4 ч, соответственно (фиг. 8А).
Интернализованная фракция соединений 177Lu-Ibu-PSMA и 177Lu-DβP-PSMA была незначительно выше по сравнению с соединениями 177Lu-Ibu-Dα-PSMA, 177Lu-Ibu-N-PSMA, 177Lu-Ibu-DAB-PSMA и 177Lu-PSMA-617, значения для которых находятся в одном и том же диапазоне (фиг. 8А). Захват всех радиолигандов в опухолевых клетках РС-3 flu составлял <2% через 4 ч, что указывает на высокий уровень захвата PSMA-специфическими клетками (фиг. 8Б).
Пример 8
Исследование биораспределения in vivo
Эксперименты in vivo были одобрены местным ветеринарным отделом и проводились в соответствии со швейцарским законодательством о защите животных. В экспериментах использовали мышей возрастом 5-6 недель (Charles River Laboratories, Sulzfeld, Германия). Самкам бестимусных голых мышей Balb/c подкожно прививали PSMA-положительные клетки РС-3 PIP (6×106 клеток в 100 мкл сбалансированного солевого раствора Хэнкса (HBSS), содержащего Ca2+/Mg2+) в правое плечо и PSMA-отрицательные клетки РС-3 flu (5×106 клеток в 100 мкл HBSS Ca2+/Mg2+) в левое плечо. Через 2 недели размер опухоли достигал приблизительно 80-300 мм*2, который являлся пригодным для проведения экспериментов по биораспределению.
Через 12-15 дней после прививки опухолевыми клетками РС-3 PIP/flu проводили эксперименты по биораспределению. Радиолиганды 177Lu-Ibu-PSMA, 177Lu-Ibu-Dβ-PSMA, 177Lu-Ibu-Dα-PSMA, 177Lu-Ibu-N-PSMA, 177Lu-Ibu-DAB-PSMA и 177Lu-PSMA-617 разбавляли в растворе 0,9% NaCl, содержащем 0,05% бычьего сывороточного альбумина (BSA), для предотвращения прилипания к материалу флаконов и шприцев. Радиолиганды вводили инъекцией в боковую хвостовую вену в объеме 100-200 мкл. Мышей умерщвляли через различные периоды времени после инъекции (п./и.) радиолигандов. Выбранные ткани и органы собирали, взвешивали и радиоактивность измеряли на γ-счетчике. Результаты корректировали на распад и рассчитывали в виде процента инъекционной активности на грамм массы ткани (% ИА/г) (табл. 3 и 4).
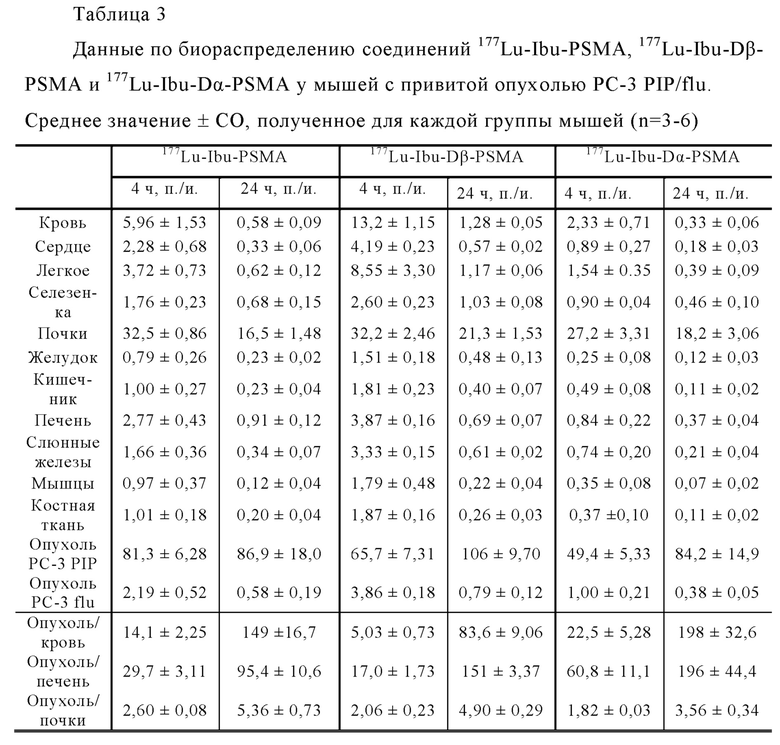

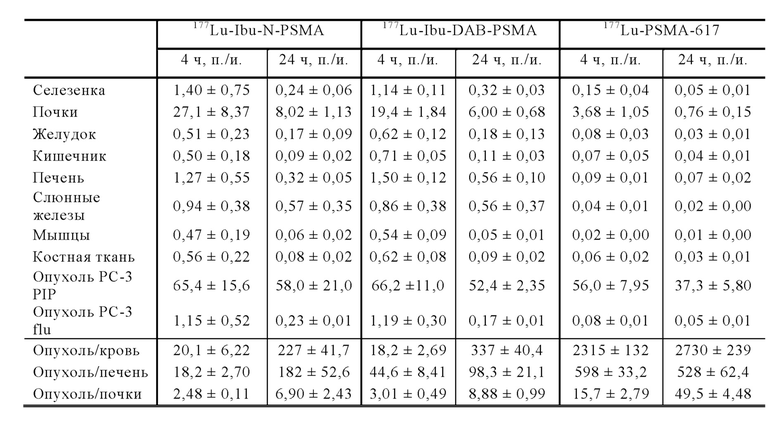
Данные по биораспределению и соотношения опухоль/фон также представлены на фиг. 9 и фиг. 10, соответственно.
Наблюдался наиболее быстрый захват опухолями РС-3 PIP соединения 177Lu-Ibu-PSMA, которое конструировали без включения дополнительного фрагмента-спейсера на основе аминокислоты. Накопление в опухоли достигало 81,3±6,28% ИА/г уже через 4 ч п./и., и даже незначительно повышалось через 24 ч п./и. (86,8±18,0% ИА/г). Для соединений 177Lu-Ibu-Dβ-PSMA, 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA наблюдалось аналогичное накопление в опухолях РС-3 PIP через 4 ч п./и., соответственно (65-66% ИА/г), но различное удерживание в опухолевой ткани. Через 24 ч п./и. был выявлен значительно повышенный захват опухолью соединения 177Lu-Ibu-Dβ-PSMA (106±9,70% ИА/г), в то время как уровни радиоактивности снижались в случае соединений 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA (52-58% ИА/г). В случае соединения 177Lu-Ibu-Dα-PSMA высокий уровень накопления в опухоли наблюдался только через 24 ч (84,2±14,9% ИА/г). Наблюдался более высокий захват опухолью всех радиолигандов, содержащих ибупрофен, по сравнению с уровнями после инъекции известного в уровне техники радиолиганда 177Lu-PSMA-617 (37,3±5,80% ИА/г) через 24 ч п./и. Захват опухолью РС-3 flu (PSMA-отрицательной) составлял уровень, явно ниже уровней в крови после инъекции всех радиолигандов, что подтверждает PSMA-опосредованный захват.
Наиболее высокие уровни активности в крови (13,2±1,15% ИА/г) детектировали для соединения 177Lu-Ibu-Dβ-PSMA через 4 ч п./и., в то время как все другие соединения проявляли более низкое накопление радиоактивности (2,33-5,96% ИА/г) в пуле крови в этот период времени. У мышей, которым вводили инъекцию соединении 177Lu-Ibu-PSMA, 177Lu-Ibu-Dα-PSMA, 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA, наблюдалось быстрое выведение радиоактивности, <0,6% ИА/г через 24 ч, в то время как выведение соединения 177Lu-Ibu-Dβ-PSMA в тот же период времени замедлялось, и составляло лишь ~1,3% ИА/г.
Самый низкий захват почками наблюдался для соединения 177Lu-Ibu-DAB-PSMA как через 4 ч, так и через 24 ч п./и. (19,4±1,84% и 6,00±0,68% ИА/г, соответственно), в то время как захват почками других радиолигандов составлял 27-33% ИА/г через 4 ч п./и. Для соединения 177Lu-Ibu-N-PSMA было выявлено самое быстрое выведение почками, что в результате приводило к уровню 8,02±1,13% ИА/г через 24 ч п./и., который достигал аналогичный соединению 177Lu-Ibu-DAB-PSMA уровень. Уровни радиоактивности во всех других тканях снижались до уровней, ниже уровней в крови и в течение времени продолжали снижаться.
Наблюдались соотношения опухоль/кровь накопленной радиоактивности, аналогичные уровням после инъекции соединений 177Lu-Ibu-PSMA, 177Lu-Ibu-Dα-PSMA, 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA (14-23), но снижались после инъекции соединения 177Lu-Ibu-Dβ-PSMA (5,03±0,73) через 4 ч п./и. Через 24 ч п./и. соотношение опухоль/кровь для соединения 177Lu-Ibu-DAB-PSMA (~337) составляло наиболее высокий уровень, по сравнению с уровнями после введения соединений 177Lu-Ibu-N-PSMA (~227), 177Lu-Ibu-Dα-PSMA (~198), 177Lu-Ibu-PSMA (-149) и 177Lu-Ibu-Dβ-PSMA (~84). Через 4 ч п./и. наблюдались соотношения опухоль/почки, аналогичные уровням после инъекции всех радиолигандов, но эти соотношения отличались примерно в 2 раза через 24 ч п./и. и достигали самых высоких значений после инъекции соединений 177Lu-Ibu-DAB-PSMA и 177Lu-Ibu-N-PSMA. Наиболее высокие соотношения опухоль/печень наблюдались через 24 п.и. для соединений 177Lu-Ibu-Dα-PSMA (196) и 177Lu-Ibu-N-PSMA (182).
Пример 9
Измерение активности in vivo во всем организме
Эксперименты in vivo были одобрены местным ветеринарным отделом и проводились в соответствии со швейцарским законодательством о защите животных. В экспериментах использовали мышей возрастом 5-6 недель (Charles River Laboratories, Sulzfeld, Германия). Самкам бестимусных голых мышей Balb/c подкожно прививали PSMA-положительные клетки РС-3 PIP (6×106 клеток в 100 мкл сбалансированного солевого раствора Хэнкса (HBSS), содержащего Ca2+/Mg2+) в правое плечо и PSMA-отрицательные клетки РС-3 flu (5×106 клеток в 100 мкл HBSS Ca2+/Mg2+) в левое плечо. Через 2 недели размер опухоли достигал приблизительно 80-300 мм2, который являлся пригодным для проведения исследований визуализацией.
Отдельные радиолиганды (удельная активность 30 МБк/нмоль) разбавляли в растворе 0,9% NaCl, содержащем 0,05% бычьего сывороточного альбумина (BSA) и вводили в/в мышам с привитой опухолью РС-3 ΡΙΡ/flu (30 МБк, 1 нмоль, 100 мкл) с целью дальнейшей визуализации SPECT/CT. Исследование мышей проводили с помощью дозкалибратора через 4 ч, 24 ч, 48 ч и 72 ч п.и., соответственно.
Результаты представлены на фиг. 11. При измерении активности во всем организме был выявлен различный характер процесса выведения для отдельных радиолигандов, который наиболее ярко проявлялся через 4 ч. п./и. Самое высокое удерживание в организме наблюдалось через 4 ч п./и. для соединения 177Lu-Ibu-Dβ-PSMA (49%) и более низкое удерживание для соединений 177Lu-Ibu-PSMA (33%), 177Lu-Ibu-Dα-PSMA (29%) и 177Lu-Ibu-DAB-PSMA (17%), при этом самый низкий уровень удерживания радиоактивности в организме наблюдался для соединения 177Lu-Ibu-N-PSMA (12%). Все радиолиганды характеризовались более высоким удерживанием радиоактивности по сравнению с соединением 177Lu-PSMA-617 (6,5%) с ограниченными альбумин-связывающими свойствами. Однако удерживающая активность снижалась по сравнению с радиолигандами для сравнения, 177Lu-PSMA-ALB-53 (93%) и 177Lu-PSMA-ALB-56 (66%), которые вместо ибупрофена содержат альбумин-связывающие фрагменты на основе пара-иодфенил- и пара-толилгрупп, соответственно (Umbricht С.Α., Benesova Μ., Schibli R.,  Preclinical development of novel PSMA-targeting radioligands: modulation of albumin-binding properties to improve prostate cancer therapy. Mol Pharm, Mol Pharm, 75, (6), 2297-2306 (2018)). Во всех случаях модифицированных ибупрофеном радиолигандов, удерживание радиоактивности в организме снижалось в течение времени и достигало уровней удерживающих фракций, аналогичных соединению 177Lu-PSMA-617, через 72 ч п./и. В этот период времени, удерживание для соединения 177Lu-PSMA-ALB-53 и 177Lu-PSMA-ALB-56 составляло лишь 42% и 10% удерживаемой в организме радиоактивности, соответственно.
Preclinical development of novel PSMA-targeting radioligands: modulation of albumin-binding properties to improve prostate cancer therapy. Mol Pharm, Mol Pharm, 75, (6), 2297-2306 (2018)). Во всех случаях модифицированных ибупрофеном радиолигандов, удерживание радиоактивности в организме снижалось в течение времени и достигало уровней удерживающих фракций, аналогичных соединению 177Lu-PSMA-617, через 72 ч п./и. В этот период времени, удерживание для соединения 177Lu-PSMA-ALB-53 и 177Lu-PSMA-ALB-56 составляло лишь 42% и 10% удерживаемой в организме радиоактивности, соответственно.
Пример 10
Визуализация SPECT/CT in vivo
Изображения SPECT/CT получали с использованием сканера SPECT/CT, предназначенного для исследований мелких животных (NanoSPECT/CTTM, Mediso Medical Imaging Systems, Будапешт, Венгрия). Сканирование SPECT/CT проводили в течение 45 мин с последующей компьютерной томографией (СТ) в течение 7,5 мин. Во время сканирования in vivo мышей анестезировали смесью изофлурана и кислорода. Реконструкцию полученных данных осуществляли с использованием программного обеспечения HiSPECT (версия 1.4.3049, Scivis GmbH, Геттинген, Германия). Все изображения обрабатывали с использованием программного обеспечения для пост-обработки VivoQuant (версия 2.10, inviCRO Imaging Services and Software, Бостон, США). Фильтр пост-обработки Гаусса (FWHM = 1,0 мм) использовали для обработки изображений, которые были представлены в масштабе, отрегулированным для обеспечения визуализации наиболее важных органов и тканей, после 5% отсечения нижней шкалы.
Изображения SPECT представлены на фиг. 12, на которой представлена SPECT визуализция ксенотрансплантата опухоли РС-3 PIP (правая сторона), где наблюдается высокая степень накопления радиолигандов, тогда как в опухоли РС-3 flu (левая сторона) накопления радиоактивности не наблюдалось. Через 4 ч также наблюдалась некоторая активность в почках, а также в мочевом пузыре как следствие почечного клиренса.
Пример 11
Оценка in vitro соединения 177Lu-Ibu-sPSMA
В этом примере оценивали влияние более короткого линкера ((СН2)2), в отличии от боковой цепи лизина ((СН2)4), для присоединения ибупрофена в качестве спейсера с целью исследовать возможное влияние длины спейсера на профиль биораспределения радиолиганда. С этой целью было сконструировано и синтезировано соединение Ibu-sPSMA ("s" означает короткий спейсер (short spacer)) (пример 8.2). В соединение Ibu-sPSMA вводили метку 177Lu и проводили доклинические исследования. Исследовали стабильность 177Lu-Ibu-sPSMA, а также его альбумин-связывающие свойства и способность связываться с PSMA-положительными клетками РС-3 PIP. Эксперименты по биораспределению и по визуализации SPECT/CT проводили с использованием мышей с привитой опухолью РС-3 PIP/flu. Новые данные сравнивали с данными, полученными для соединения 177Lu-PSMA-617, и с модифицированными ибупрофеном радиолигандами PSMA или соединением 177Lu-PSMA-ALB-56.
Соединение 177Lu-Ibu-sPSMA исследования in vitro и сравнивали с ранее полученными результатами для 177Lu-PSMA-617 и по возможности с соединением 177Lu-PSMA-ALB-56 (Umbricht et al, Mol Ρharm, 75, (6):2297-2306 (2018)). Исследовали эффективность включения метки, коэффициенты распределения н-октанол/PBS (значения logD) и связывание с альбумином. Эксперименты по захвату и интернализации проводили с использованием линии опухолевых клеток РС-3 PIP, PSMA-трансфектированных, PSMA-положительных опухолевых клеток и линии ложно-трансфектированных PSMA-отрицательных опухолевых клеток РС-3 flu. 11.1 Включение радиоактивной метки Соединение Ibu-sPSMA разбавляли смесью вода Milli-Q/ДМСО в соотношении 3:1(об./об.) до конечной концентрации 1 мМ. В соединение Ibu-sPSMA вводили метку 177Lu (177Lu без добавления носителя, в 0,05 Μ HCl; Isotope Technologies Garching ITG GmbH, Германия) в смеси ацетата натрия (0,5 Μ, рН 8) и HCl (0,05 М, рН ~1) при рН ~4,5. В соединение Ibu-sPSMA вводили метку 177Lu с молярной удельной активностью 5-50 МБк/нмоль, в зависимости от условий проводимого эксперимента. Реакционную смесь инкубировали в течение 10 мин при 95°С с последующим контролем качества с использованием офЖХВР на колонке С-18 (Xterra™ MS, С18, 5 мкм, 150×4,6 мм, Waters). Мобильная фаза состояла из воды MilliQ, содержащей 0,1% трифторуксусной кислоты (А) и ацетонитрил (В), градиент от 95% А и 5% В до 20% А и 80% В, в течение 15 мин при скорости потока 1,0 мл/мин. Радиолиганды перед нанесением на колонку ЖХВР разбавляли водой MilliQ, содержащей Na-DTPA (50 мкМ) (фиг. 14).
11.2 Радиолитическая стабильность
Радиолитическую стабильность оценивали в течение времени для соединения Ibu-sPSMA в ходе трех независимых экспериментов. С этой целью в соединение Ibu-sPSMA включали метку 177Lu в объеме 120 мкл при удельной активности 50 МБк/нмоль при добавлении или без добавления L-аскорбиновой кислоты (3 мг). После контроля качества методом ЖХВР (t = 0, радиохимическая чистота ≥ 98%), растворы с включенной меткой разбавляли солевым раствором до 250 МБк/500 мкл и инкубировали при комнатной температуре. Целостность радиолиганда оценивали с помощью ЖХВР после инкубации через 1 ч, 4 ч и 24 ч, как сообщалось ранее (Siwowska et al., Mol. Pharmaceutical, 14, (2), 523-532 (2017)). Хроматограммы ЖХВР анализировали при интеграции пиков, соответствующих радиоактивно меченному продукту, высвобожденному 177Lu, а также продуктам деградации неизвестной структуры (фиг. 15). Количественную оценку проводили по площади пика интактного продукта в процентах от суммы интегрированных площадей пиков на всей хроматограмме.
11.3. Коэффициент распределения в смеси н-октанол/PBS
Коэффициент распределения соединения 177Lu-Ibu-sPSMA в смеси н-октанол/PBS определяли методом, описанным в статье Benesova Μ. И др. Mol Pharm, 15, (3), 934-946 (2018). Коэффициент распределения для соединения 177Lu-Ibu-sPSMA составлял -2,43±0,01. Модификация лиганда PSMA ибупрофеном приводит к увеличению гидрофобных свойств радиолигандов по сравнению с соединением 177Lu-PSMA-617 (-4,38±0,01). Гидрофобность соединения 177Lu-Ibu-sPSMA находилась в том же самом диапазоне, что и другие модифицированные ибупрофеном лиганды и соединение 177Lu-PSMA-ALB-56 (-2,9±0,2).
11.3. Альбумин-связывающие свойства
Связывание с белками плазмы соединения 177Lu-Ibu-sPSMA оценивали методом ультрафильтрации, как описано в статье Benesova, Μ. et al. (Mol Pharm, 15, (3), 934-946 (2018)). Краткое описание методики: в Ibu-sPSMA-лиганд включали метку 177Lu при молярной удельной активности 50 МБк/нмоль и инкубировали в образцах плазмы или в PBS при 37°С.Не связанные и связанные с плазмой фракции разделяли с использованием ячейки для ультрафильтрации с центрифугированием (ячейки 4104 centrifugal filter units, Millipore, номинальный молекулярно-массовый предел отсечения 30000 Да, метилцеллюлозные мембраны для ультрафильтрации). Инкубированный раствор помещали в ячейку для ультрафильтрации и центрифугировали при 2000 об/мин при 20°С в течение 40 мин. Отбирали образцы из фильтрата и определяли радиоактивность на счетчике γ-излучения. Количество связанного с плазмой радиолиганда рассчитывали, как долю радиоактивности, измеренную в фильтрате, по отношению к соответствующему исходному, помещенному в ячейку раствору (принята за 100%). Эксперименты повторяли 3 раза для каждого радиолиганда.
Результаты экспериментов по ультрафильтрации соединения 177Lu-Ibu-sPSMA свидетельствуют о высоком уровне связывания с сывороточными белками, то есть ~97% радиолиганда удерживается над мембраной для ультрафильтрации после инкубации с плазмой человека. Радиолиганд не удерживался над мембраной для ультрафильтрации после инкубации в PBS (который не содержит белки). Соединение 177Lu-Ibu-sPSMA характеризуется повышенным связыванием с белками плазмы по сравнению с соединением 177Lu-PSMA-617, для которого альбумин-связывающая фракция составляла лишь примерно 59% (фиг. 16).
11.4. Исследование интернализации клетками
Захват и интернализацию клетками соединения 177Lu-Ibu-sPSMA исследовали с использованием PSMA-положительных опухолевых клеток РС-3 PIP и PSMA-отрицательных опухолевых клеток РС-3 flu, любезно предоставленных др. Martin Pomper (Johns Hopkins University School of Medicine, Baltimore, MD, U.S.A.) (Eiber и др., J Nucl Med, 58, (Suppl 2), 67S-76S (2017)). Соединение 177Lu-Ibu-sPSMA исследовали в ходе трех экспериментов в 6 повторах с использованием опухолевых клеток РС-3 PIP, и трех экспериментов в 6 повторах с использованием опухолевых клеток РС-3 flu.
Захват и интернализация соединения 177Lu-Ibu-sPSMA опухолевыми клетками РС-3 PIP лишь незначительно снижались по сравнению с соединением
Lu-PSMA-617 (фиг. 17). Фракция интернализации соединения Lu-Ibu-sPSMA составляла 18% и 22% после инкубации в течение 2 ч или 4 ч, соответственно (фиг. 17А). Захват соединения 177Lu-Ibu-sPSMA опухолевыми клетками РС-3 flu составлял <0.1% через 4 ч, что указывает на высокий уровень PSMA-специфического захвата клетками РС-3 PIP (фиг. 17Б).
11.5 Определение коэффициентов KD
Определяли коэффициенты KD, которые указывают на PSMA-связывающую аффинность нового радиолиганда. Значение KD для соединения 177Lu-Ibu-sPSMA находилось в том же диапазоне, что и другие модифицированные ибупрофеном радиолиганды PSMA и практически не отличалось от значений KD для соединений 177Lu-PSMA-ALB-56 и 177Lu-PSMA-617, которые определяли в аналогичных условиях эксперимента (табл. 5).

Пример 12 Оценка in vivo
Соединение 177Lu-Ibu-sPSMA характеризовали in vivo и данные сравнивали с данными, полученными для соединении 177Lu-PSMA-617 и 177Lu-PSMA-ALB-56.
12.1. Модель опухоли у мышей
В экспериментах использовали мышей возрастом 5-6 недель (Charles River Laboratories, Sulzfeld, Германия). Самкам бестимусных голых мышей Balb/c подкожно прививали PSMA-положительные клетки РС-3 PIP (6×106 клеток в 100 мкл сбалансированного солевого раствора Хэнкса (HBSS) в правое плечо и PSMA-отрицательные клетки РС-3 flu (5×106 клеток в 100 мкл HBSS) в левое плечо. Через две недели размер опухоли достигал приблизительно 80-300 мм3, пригодный для проведения исследований по биораспределению и визуализации.
12.2 Исследование биораспределения
Исследование биораспределения проводили через 12-15 дней после прививки опухолевых клеток РС-3 PIP/flu. Соединение 177Lu-Ibu-sPSMA растворяли в 0,9% NaCl, содержащем 0,054% бычьего сывороточного альбумна (BSA), для предотвращения адгезии к материалу флаконов и шприцев. Радиолиганд вводили инъекцией в боковую хвостовую вену в объеме 100-200 мкл. Мышей умерщвляли через различные периоды времени после инъекции (п./и.) радиолиганда. Выбранные ткани и органы собирали, взвешивали и радиоактивность измеряли на γ-счетчике. Результаты корректировали на распад и рассчитывали в виде процента инъекционной активности на грамм массы ткани (% ИА/г) (табл. 6 и фиг. 18).
Соединение 177Lu-Ibu-sPSMA характеризовалось высоким накоплением в опухолях РС-3 PIP уже через 1 ч п./и. (63±8% ИА/г), которое в дальнейшем повышалось в период вплоть до 24 ч п./и. (132±15% ИА/г), то есть до самого высокого захвата опухолью, наблюдаемого для всех радиолигандов, включающих ибупрофен. Наблюдалось медленное выведение активности из опухолевой ткани, что привело к сохранению активности в опухоли на уровне 57±9% ИА/г через 4 дня после инъекции по сравнению с 20-34% ИА/г для других радиолигандов в тот же момент времени. Захват PSMA-отрицательными клетками flu РС-3 был явно ниже уровней в крови, что подтверждает специфический, PSMA-опосредованный захват в опухолях РС-3 PIP.
Соединение 177Lu-Ibu-sPSMA характеризовалось самыми высокими уровнями активности в крови через 1 ч п./и. (29±4% ИА/г по сравнению с уровнями 13-18% ИА/г для других ибупрофен-содержащих радиолигандов), которые со временем непрерывно снижались до аналогичных уровней активности в крови, как для соединении 177Lu-Ibu-PSMA и 177Lu-Ibu-Da-PSMA через 4 дня после инъекции. По сравнению с уровнями активности в крови быстро выведенных соединений 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA, соединение 177Lu-Ibu-sPSMA характеризовалось примерно в три раза более высокими значениями через 24 ч и 96 ч после инъекции.
Наблюдался очень высокий захват почками (114±15% ИА/г) через 1 ч п./и. по сравнению с захватом на уровне лишь 30-33% ИА/г для соединений 177Lu-Ibu-PSMA, 177Lu-Ibu-N-PSMA и 177Lu-Ibu-DAB-PSMA и уровнем 73±2% ИА/г для соединения 177Lu-Ibu-Dα-PSMA). Однако наблюдалось такое быстрое выведение почками, что уровни активности, аналогичные другим радиолигандам, достигались уже через 4 ч п./и. Аналогичным образом в печени наблюдался высокий уровень накопления активности в ранние периоды времени (17±4% ИА/г через 1 ч п.и. и 7,2±0,5% ИА/г через 4 ч п.и.), но быстрое выведение приводило к аналогичному удерживанию активности в печени через 24 ч п.и. и 96 ч п.и. по сравнению с другими радиолигандами, содержащими ибупрофен.
В таблице 6 представлены данные по биораспределению соединения 177Lu-Ibu-sPSMA у мышей с привитой опухолью РС-3 ΡΙΡ/flu. Данные представлены в виде среднего значения ± СО в процентах инъекционной активности на грамм ткани (% ИА/г), рассчитанного для каждой группы мышей (n=4). Сравнение характеристик соединения 177Lu-Ibu-sPSMA с другими модифицированными ибупрофеном радиолигандами свидетельствует об исключительно высоких уровнях накопления и удерживания активности в PSMA-положительных опухолях РС-3 PIP, что приводит к высоким уровням соотношений опухоль-почки и опухоль-печень, прежде всего в поздние периоды времени.
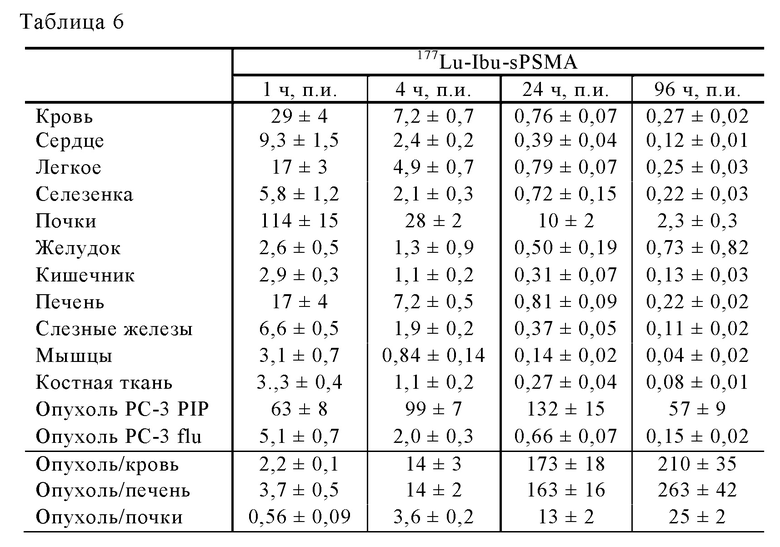
В связи с высокими уровнями активности в крови, прежде всего в ранние периоды времени после инъекции, соотношения накопленной радиоактивности опухоль/кровь для соединения 177Lu-Ibu-sPSMA в значительной степени составляли более низкие значения по сравнению с соединением 177Lu-Ibu-DAB-PSMA, но достигали аналогичных значений, выявленных для соединений 177Lu-Ibu-PSMA, 177Lu-Ibu-Dα-PSMA и 177Lu-Ibu-N-PSMA в более поздние периоды времени (фиг. 19А). Соотношение опухоль/почки для соединения 177Lu-Ibu-sPSMA достигало равных низких значений по сравнению с соединением 177Lu-Ibu-Da-PSMA (0,56±0,09 и 0,59±0,08, соответственно) через 1 ч п./и., но значительно повышалось в течение времени, что приводило к самым высоким соотношениям по сравнению со всеми остальными радиолиогандами во все другие периоды времени (рис. 19Б). Аналогичным образом соотношения опухоль/печень составляли более низкие значения через 1 ч и 4 ч п./и., но превышали значения для других радиолигандов через 24 ч и 96 ч после инъекции (фиг. 19В).
12.3. Измерения активности во всем организме
Все альбумин-связывающие лиганды (молярная активность: 25 МБк/нмоль) разбавляли в 0,9% NaCl, содержащем 0,05% BSA, и вводили внутривенно мышам без привитой опухоли (25 МБк, 1 нмоль, 100 мкл). Активность в организме мышей измеряли в дозкалибраторе через различные периоды времени вплоть до 56 ч п./и. Активность радиолигандов сравнивали с полученными ранее данными для соединения 177Lu-PSMA-617.
Измерения на всем организме выявили различные типы выведения отдельных радиолигандов, которые наиболее значимо проявлялись в ранние периоды времени, вплоть до 8 ч после инъекции (фиг. 20). Среди всех радиолигандов наиболее высокий уровень удерживания наблюдался для соединения 177Lu-Ibu-Dβ-PSMA, с единственным исключением в поздние периоды времени (48 ч и 56 ч п./и.), когда наблюдался более высокий уровень удерживания для соединения 177Lu-PSMA-ALB-56, содержащего пара-иодфенильный фрагмент в качестве более сильного альбумин-связывающего фрагмента. Для других содержащих ибупрофен радиолигандов наблюдался более низкий уровень удерживания в организме по сравнению с соединением Lu-PSMA-ALB-56. Среди всех альбумин-связывающих радиолигандов соединение 177Lu-Ibu-DAB-PSMA характеризовалось самым быстрым типом выведения, при этом удерживаемая активность составляла лишь 18% уже через 4 ч после инъекции по сравнению с другими альбумин-связывающими лигандами (35-73%). Все радиолиганды характеризовались более высоким удерживанием радиоактивности по сравнению с соединением 177Lu-PSMA-617, которое обладало ограниченными альбумин-связывающими свойствами. Во всех случаях удерживание радиоактивности в организме снижалось в течение времени и достигало аналогичных фракций удерживания через 32 ч п./и.
12.4. Визуализация SPECT/CT in vivo
Изображения SPECT/CT получали с использованием сканера SPECT/CT, предназначенного для исследований мелких животных (NanoSPECT/CT™, Mediso Medical Imaging Systems, Будапешт, Венгрия). Сканирование SPECT/CT проводили в течение 45 мин с последующей компьютерной томографией (СТ) в течение 7,5 мин. Во время сканирования in vivo мышей анестезировали смесью изофлурана и кислорода. Реконструкцию полученных данных осуществляли с использованием программного обеспечения HiSPECT (версия 1.4.3049, Scivis GmbH, Геттинген, Германия). Все изображения обрабатывали с использованием программного обеспечения для пост-обработки VivoQuant (версия 2.10, inviCRO Imaging Services and Software, Бостон, США). Фильтр пост-обработки Гаусса (FWHM = 1,0 мм) использовали для обработки изображений, которые были представлены в масштабе, отрегулированным для обеспечения визуализации наиболее важных органов и тканей, после 5% отсечения нижней шкалы.
Изображения SPECT/CT представлены на фиг. 21, на котором показана SPECT визуализация ксенотрансплантата опухоли РС-3 PIP (правая сторона), где наблюдалась высокая степень накопления соединения 177Lu-Ibu-sPSMA, тогда как в опухоли РС-3 flu (левая сторона, фиг. 21) накопления радиоактивности не наблюдалось. Через 4 ч также наблюдалась некоторая активность в почках, а также в мочевом пузыре как следствие почечного выведения. Через 24 ч активность визуализировалась только в опухоли РС-3 PIP (фиг. 21).
Пример 13
Терапевтическое исследование in vivo Терапевтическую эффективность соединения 177Lu-Ibu-DAB-PSMA оценивали in vivo на модели мышей с привитой опухолью (мыши с PSMA-положительной опухолью РС-3 PIP) и данные сравнивали с данными, полученными для соединений 177Lu-PSMA-617 и 177Lu-PSMA-ALB-56 (Eiber и др., J. Nucl. Med., 58 (Suppl. 2) 67S-76S (2017)).
13.1. Модель мышей с опухолью
В экспериментах использовали мышей возрастом 5-6 недель (Charles River Laboratories, Sulzfeld, Германия). Самкам бестимусных голых мышей Balb/c подкожно прививали PSMA-положительные РС-3 PIP-клетки (4×106 клеток в 100 мкл сбалансированного солевого раствора Хэнкса (HBSS) в правое плечо. Через 6 дней размер опухоли достигал приблизительно 30-160 мм3, пригодный для проведения терапевтических исследований in vivo. Мышей умерщвляли, когда выявляли предварительно определенный конечный параметр или когда завершали исследования в день 84. Использовали следующие критерии конечных параметров: (i) потеря массы тела >15%, (ii) объем опухоли >800 мм3, (iii) комбинация потери массы тела >10% и объема опухоли >700 мм3, или (iv) признаки беспокойства и боли или их комбинация.
13.2. Методы
Через 6 дней после подкожной прививки опухолевых клеток РС-3 PIP 4×106 трем группам мышей со статистически сопоставимыми массой тела и объемом опухоли вводили соединение внутривенной инъекцией. В одной группе вводили только носитель (солевой раствор, содержащий 0,05% бычьего сывороточного альбумина (BSA), группа А, n=6), а в двух других группах вводили соединение 177Lu-Ibu-DAB-PSMA (группа В: 2 МБк, 1 нмоль (n=6) и группа С: 5 МБк, 1 нмоль (n=6)) в день 0 в ходе терапевтических исследований (табл. 7). Обследование мышей и оценку параметров терапевтических исследований проводили, как описано в статье Eiber и др., J. Nucl. Med., 58 (Suppl. 2) 67S-76S (2017). Краткое описание исследований: мышей обследовали при измерении массы тела и размера опухоли через каждые два дня в течение 12 недель. Относительную массу тела (RBW) определяли по формуле [BWx/BW0], где BWX означает массу тела в граммах в данный день х, a BW0 означает массу тела в граммах в день 0. Размеры опухоли определяли при измерении самой длинной оси опухоли (L) и ее перпендикулярной оси (W) цифровым штангенциркулем. Объем опухоли (V) рассчитывали по уравнению [V = 0,5 × (LW2)]. Относительный объем опухоли (RTV) определяли по формуле [TVx/TV0], где TVX - объем опухоли в мм3 в данный день х, a TV0 - объем опухоли в мм3 в день 0.
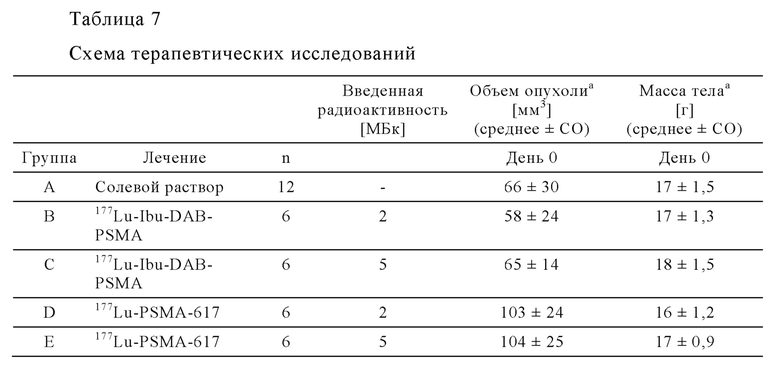

Эффективность радионуклидной терапии выражали как замедление роста опухоли (TGDx), которое рассчитывали, как время, которое требуется для увеличения объема опухоли в χ раз по сравнению с исходным объемом в день 0. Коэффициент замедления роста опухоли [TGDIx=TGDx(T)/TGDx(C)] рассчитывали как отношение TGDx леченых мышей (Т) и TGDx к среднему индексу TGDx контрольных мышей (С) для 5-кратного (х=5, TGD5) увеличения исходного объема опухоли. Среднюю выживаемость рассчитывали с помощью программного обеспечения GraphPad Prism (версия 7). Выживаемость мышей оценивали с использованием кривых Каплана-Мейера для определения средней выживаемости мышей в каждой группе с использованием программного обеспечения Graph Pad Prism (версия 7).
13.3 Результаты терапевтического исследования
Результаты терапевтического исследования объединяли с результатами, полученными в ходе терапевтических исследований, включающих группу мышей, которым вводили инъекцией только носитель (солевой раствор, содержащий 0,05% BSA, группа Α, n=6), соединение 177Lu-PSMA-617 (2 МБк и 5 МБк, группы D и Ε, n=6) и соединение 177Lu-PSMA-ALB-56 (2 ММБк и 5 МБк, группы F и G, n=6) (Eiber и др., J. Nucl. Med., 58 (Suppl. 2) 67S-76S (2017). Рост опухоли в группе леченых мышей значительно замедлялся по сравнению сростом опухоли в контрольной группе не леченных мышей (объединенные данные, n=12) (фиг. 22).
Значения коэффициента замедления роста опухоли 5 (TGDI5) в группах мышей, которым вводили 2 МБк 177Lu-Ibu-DAB-PSMA (1.6) и 177Lu-PSMA-ALB-56 (1.8), соответственно, явно повышались по сравнению с контрольной группой мышей (1,0 установлен как контроль). Лишь значение TGDI5 для мышей, которым вводили 2 МБк соединения 177Lu-PSMA-617 (1,1), было сопоставимо со значением для контрольных мышей (табл. 8).
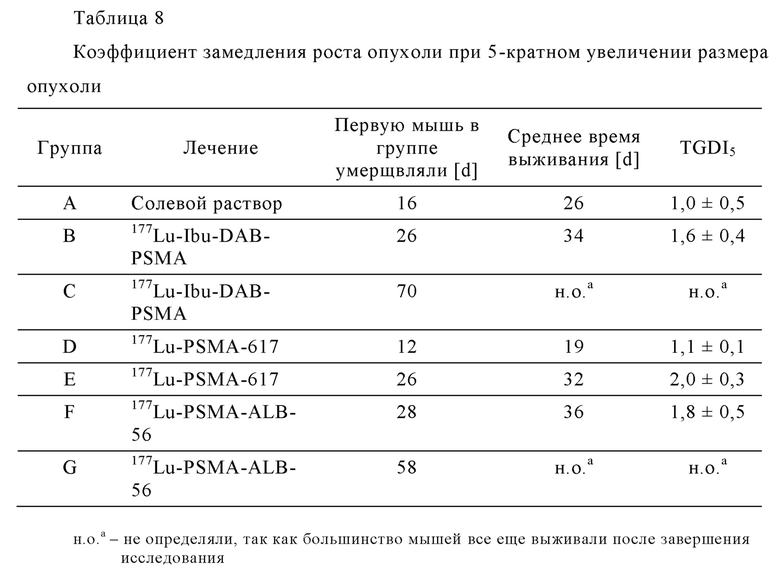
Значения TGDI5 в группах мышей, которым вводили 5 МБк соединения 177Lu-PSMA-617 (2,0), находились в том же диапазоне, что в группах мышей, которым вводили альбумин-связывающие лиганды по 2 МБк на мышь. Значения TGDI5 для мышей, которым вводили 5 МБк соединения 177Lu-Ibu-DAB-PSMA или соединения Lu-PSMA-ALB-56, соответственно, не определяли, так как у четырех мышей в каждой группе опухоль полностью исчезала. Повторного роста опухолей у животных с полной ремиссией не наблюдалось до конца исследования в день 84. В каждой группе повторный рост опухоли у животных с общей ремиссией наблюдался у двух мышей через приблизительно 5 недель после лечения, так что у них наблюдалось достижение конечного параметра в день 70 и день 82 (177Lu-Ibu-DAB-PSMA) и в день 58 и день 68 (177Lu-PSMA-ALB-56), соответственно. Таким образом, среднее время выживания оставалось неопределенным для этих групп мышей, которым вводили 5 МБк соединения 177Lu-Ibu-DAB-PSMA или 5 МБк 177Lu-PSMA-ALB-56, соответственно (фиг. 23). При завершении исследований в день 84 в каждой из этих групп все еще выживали четыре мыши. Среднее время выживания мышей, которым вводили 2 МБк 177Lu-Ibu-DAB-PSMA и 177Lu-PSMA-ALB-56, соответственно, составляло 34 и 36 дней, следовательно, явно увеличивалось по сравнению со средним временем выживания у контрольных мышей (26 дней). С другой стороны, среднее время выживания в группе мышей, которым вводили 2 МБк соединения 177Lu-PSMA-617 (19 дней), сокращалось по сравнению со значениями для всех других групп, включая нелеченных контрольных мышей (фиг. 23).
В день 16, когда у первой контрольной мыши достигался конечный параметр, у мышей во всех группах регистрировали сопоставимую среднюю относительную массу тела (0,93-1,10) (фиг. 24). В момент умерщвления средняя относительная масса тела у мышей, которым вводили 5 МБк соединения 177Lu-Ibu-DAB-PSMA (1,06±0,10) и соединения 177Lu-PSMA-ALB-56 (1,20±0,14), увеличивалась по сравнению со средней относительной массой тела контрольных мышей (0,88±0,05) и мышей, которым вводили соединение 177Lu-PSMA-617 (0,86±0,05). Такие результаты можно объяснить быстрым ростом опухоли у контрольных мышей и мышей, которым вводили соединение 177Lu-PSMA-617 и, следовательно, тем фактом, что у них конечный параметр достигался раньше, чем у мышей, которым вводили соединение 177Lu-Ibu-DAB-PSMA или соединение 177Lu-PSMA-ALB-56 (фиг. 24).
В результате, наблюдалась более высокая эффективность действия соединения 177Lu-Ibu-DAB-PSMA по сравнению с соединением Lu-PSMA-617 для обоих количеств введенной активности (2 МБк/мышь и 5 МБк/мышь, соответственно). В то время как действие соединения 177Lu-Ibu-DAB-PSMA незначительно снижалось по сравнению с соединением 177Lu-PSMA-ALB-56 при более низкой введенной активности (2 МБк/мышь), его эффективность даже немного повышалась при введении более высокого уровня активности (5 МБк/мышь). Улучшенные соотношения опухоль/кровь для соединения 177Lu-Ibu-DAB-PSMA по сравнению с результатами, полученными для соединения 177Lu-PSMA-ALB-56, и результаты этого терапевтического исследования подтвердили преимущество соединения 177Lu-Ibu-DAB-PSMA по сравнению с существующим соединением 177Lu-PSMA-617.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ПСА-СВЯЗЫВАЮЩИЕ АГЕНТЫ И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2787105C2 |
| КОМПЛЕКС, СОДЕРЖАЩИЙ НАЦЕЛИВАЮЩЕЕСЯ НА PSMA СОЕДИНЕНИЕ, СВЯЗАННОЕ С РАДИОНУКЛИДОМ СВИНЦА ИЛИ ТОРИЯ | 2018 |
|
RU2795398C2 |
| Лиганды PSMA для визуализации и эндорадиотерапии | 2018 |
|
RU2807076C2 |
| ПАРААМИНОГИППУРОВАЯ КИСЛОТА (ПАГ) КАК ВЕЩЕСТВО ДЛЯ ЗАЩИТЫ ПОЧЕК | 2020 |
|
RU2804349C2 |
| ПРИМЕНЕНИЕ БИСПЕЦИФИЧЕСКИХ АНТИГЕНСВЯЗЫВАЮЩИХ МОЛЕКУЛ, КОТОРЫЕ СВЯЗЫВАЮТ PSMA И CD3, В КОМБИНАЦИИ С КОСТИМУЛЯЦИЕЙ 4-1BB | 2020 |
|
RU2822092C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСА ПСМА-ТАРГЕТНОГО СОЕДИНЕНИЯ НА ОСНОВЕ МОЧЕВИНЫ Lu-PS-161 И КОМПЛЕКС | 2023 |
|
RU2808636C1 |
| ПСМА-ТАРГЕТНОЕ СОЕДИНЕНИЕ И ЕГО КОМПЛЕКС С РАДИОНУКЛИДАМИ ДЛЯ ТЕРАНОСТИКИ ОПУХОЛЕЙ, ЭКСПРЕССИРУЮЩИХ ПСМА | 2022 |
|
RU2803734C1 |
| АНТАГОНИСТЫ GRPR ДЛЯ ОБНАРУЖЕНИЯ, ДИАГНОСТИКИ И ЛЕЧЕНИЯ GRPR-ПОЗИТИВНОГО ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ | 2013 |
|
RU2693465C2 |
| КОМПЛЕКС ПРОИЗВОДНОГО МОЧЕВИНЫ С РАДИОНУКЛИДНОЙ МЕТКОЙ Tс ДЛЯ ДИАГНОСТИКИ ОПУХОЛЕЙ, ЭКСПРЕССИРУЮЩИХ ПРОСТАТСПЕЦИФИЧЕСКИЙ МЕМБРАННЫЙ АНТИГЕН, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2023 |
|
RU2825402C1 |
| КОНЪЮГАТЫ АНТАГОНИСТА ПЕПТИДА АНАЛОГА БОМБЕЗИНА | 2009 |
|
RU2523531C2 |
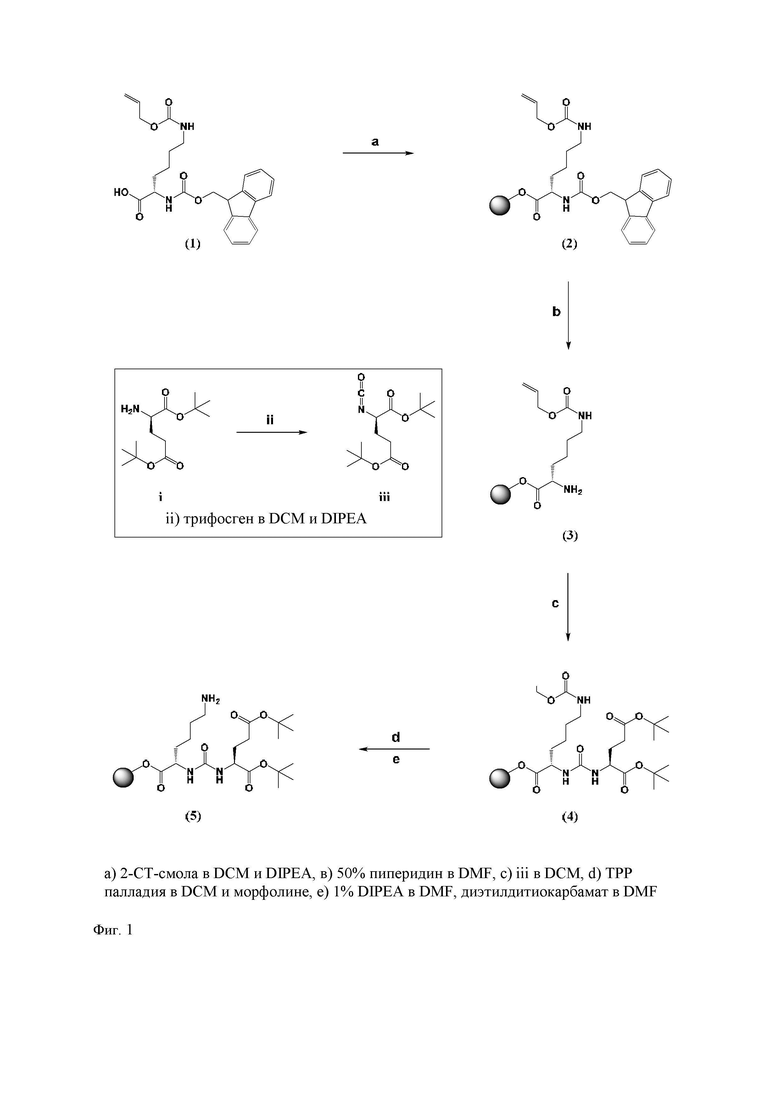
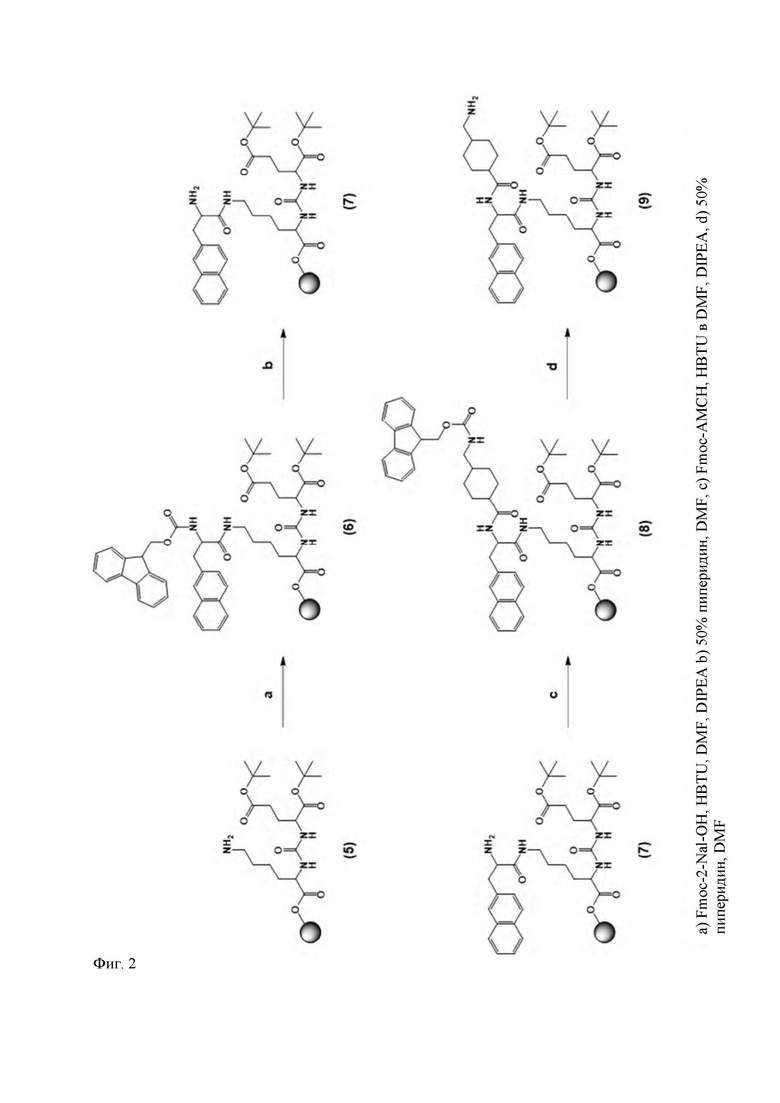
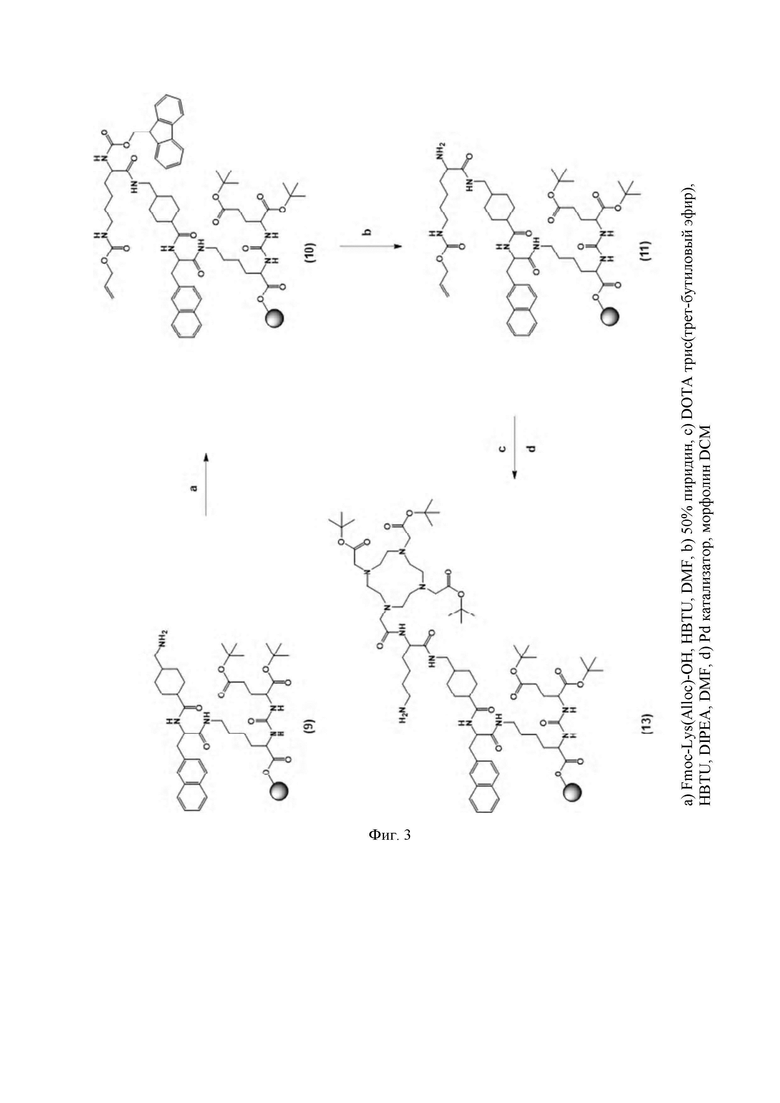
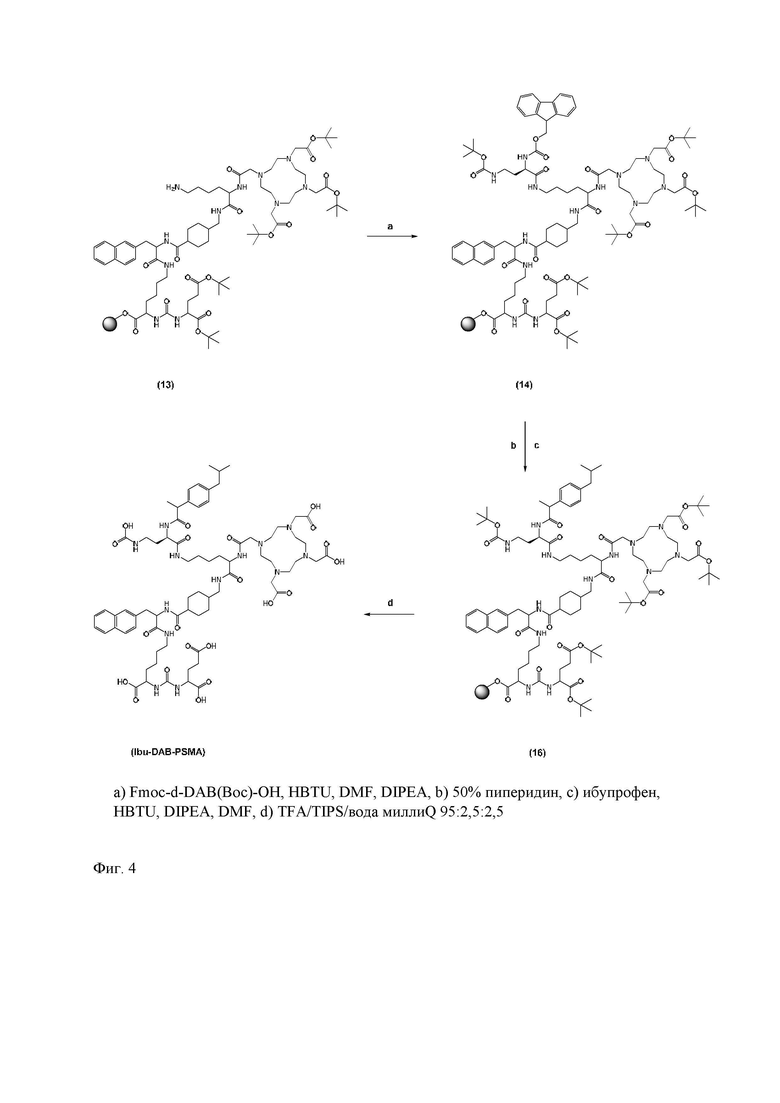
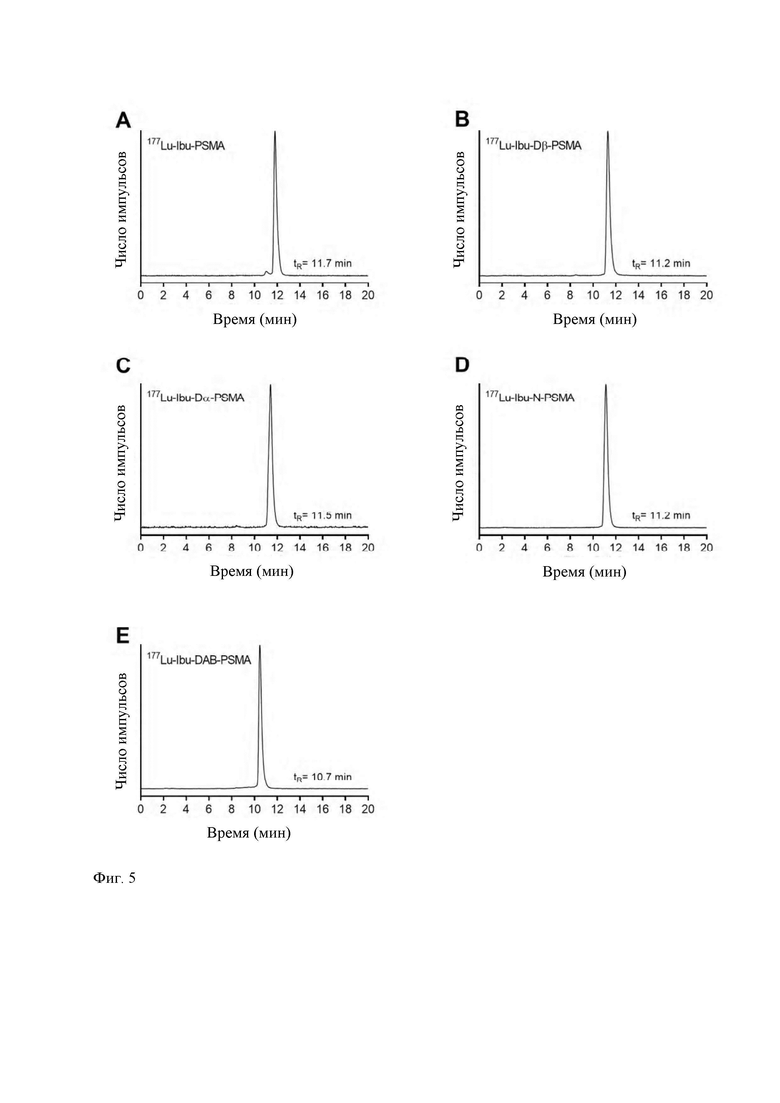
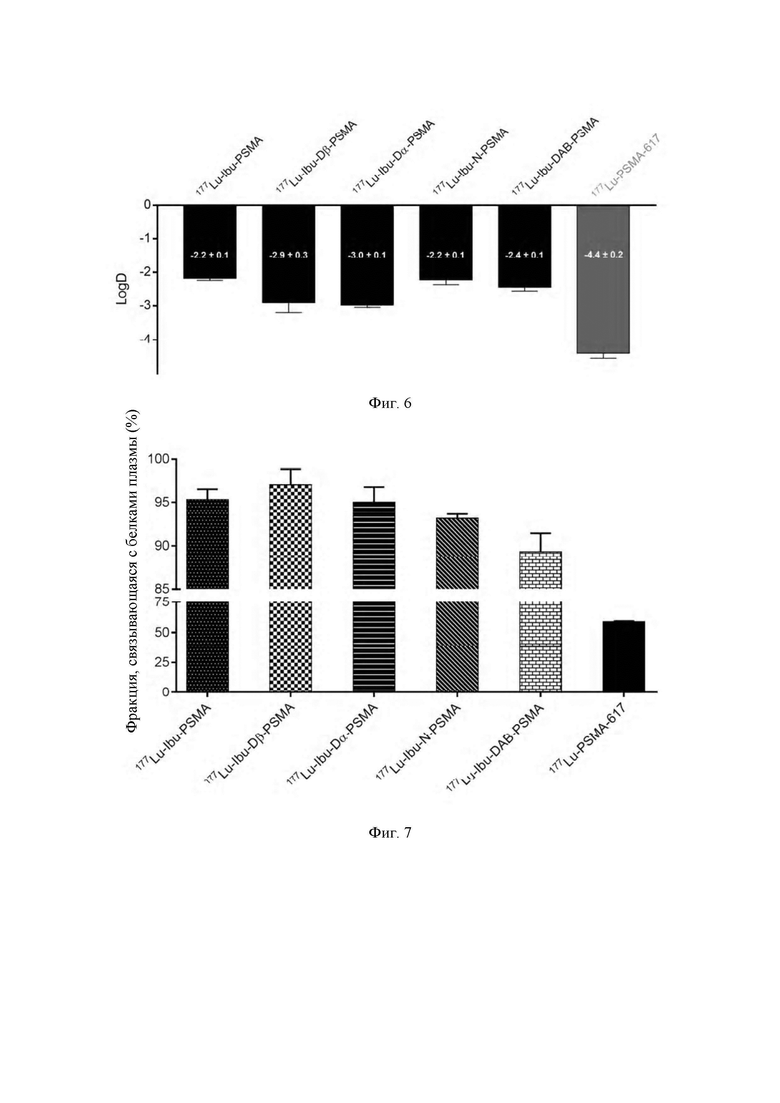
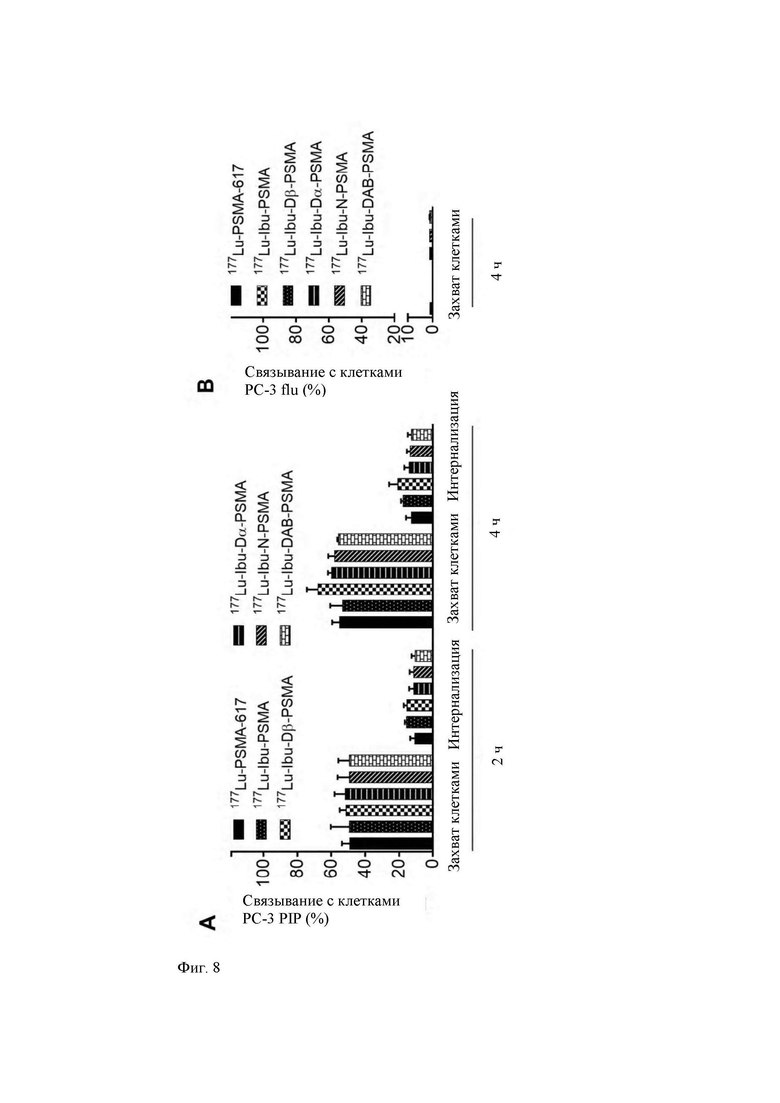
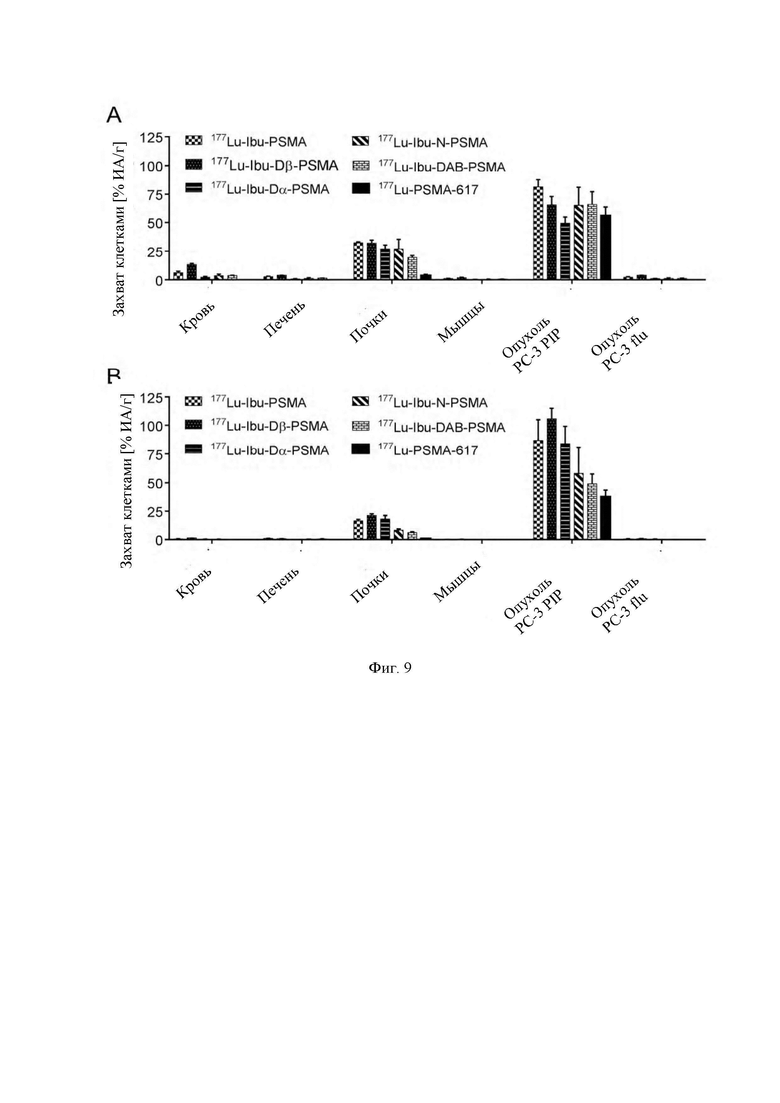

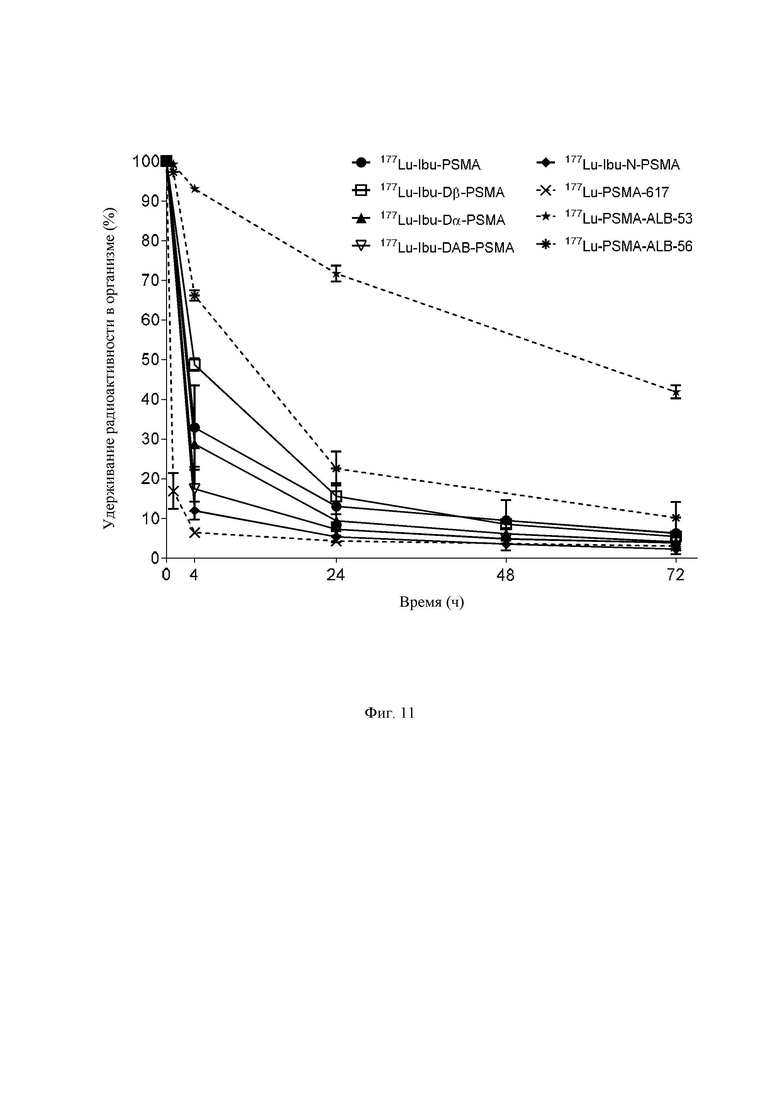
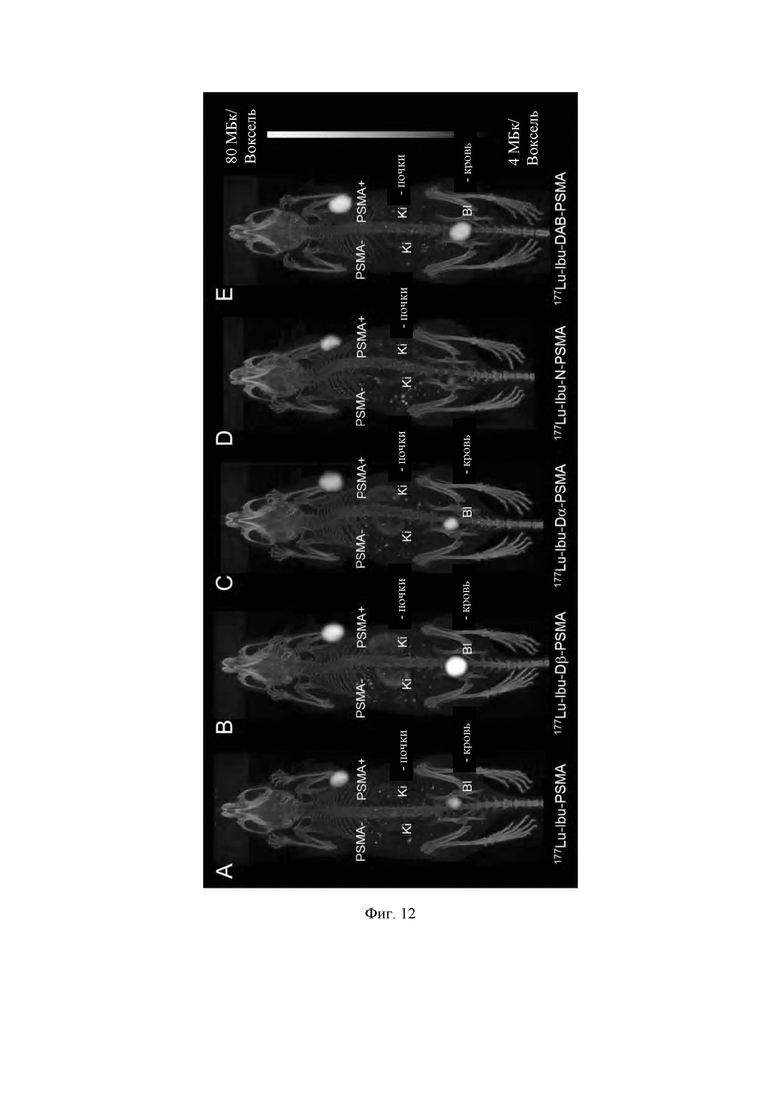
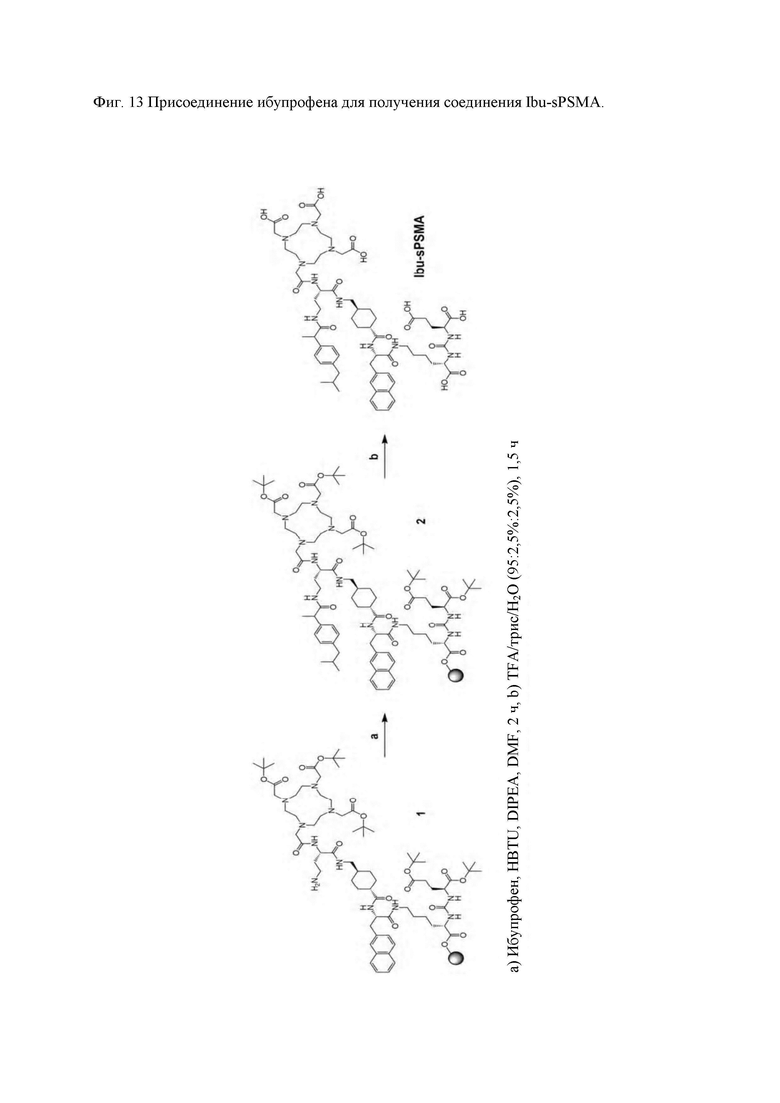
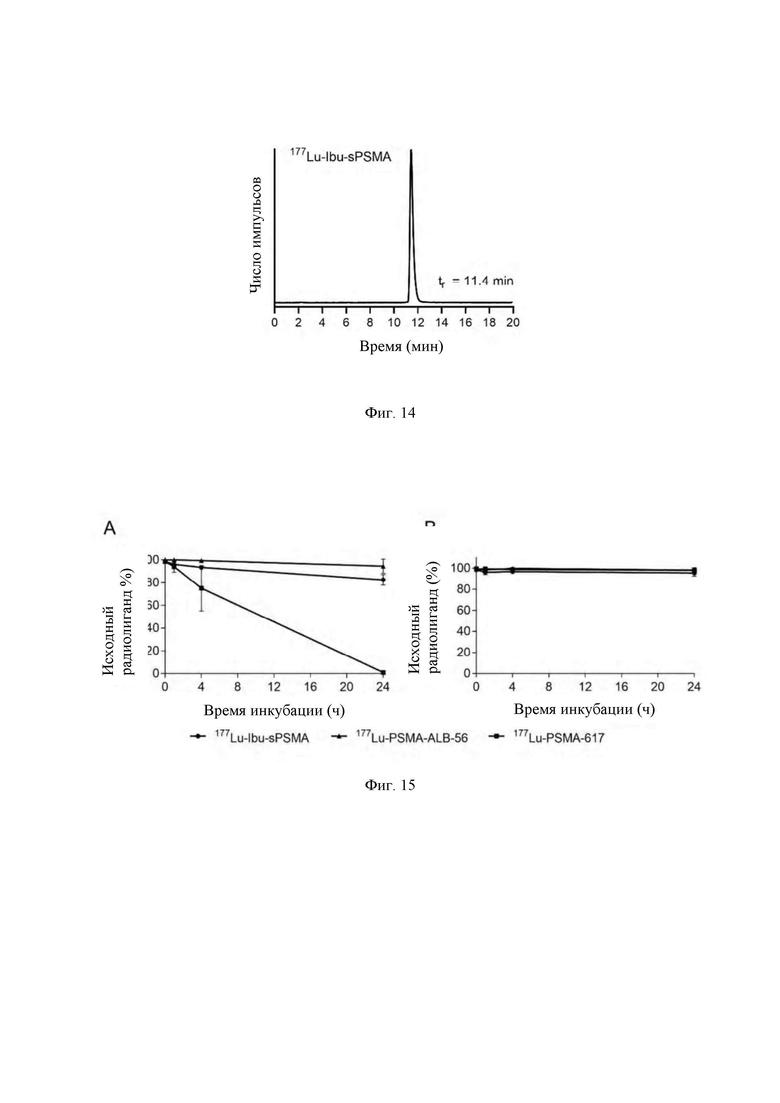
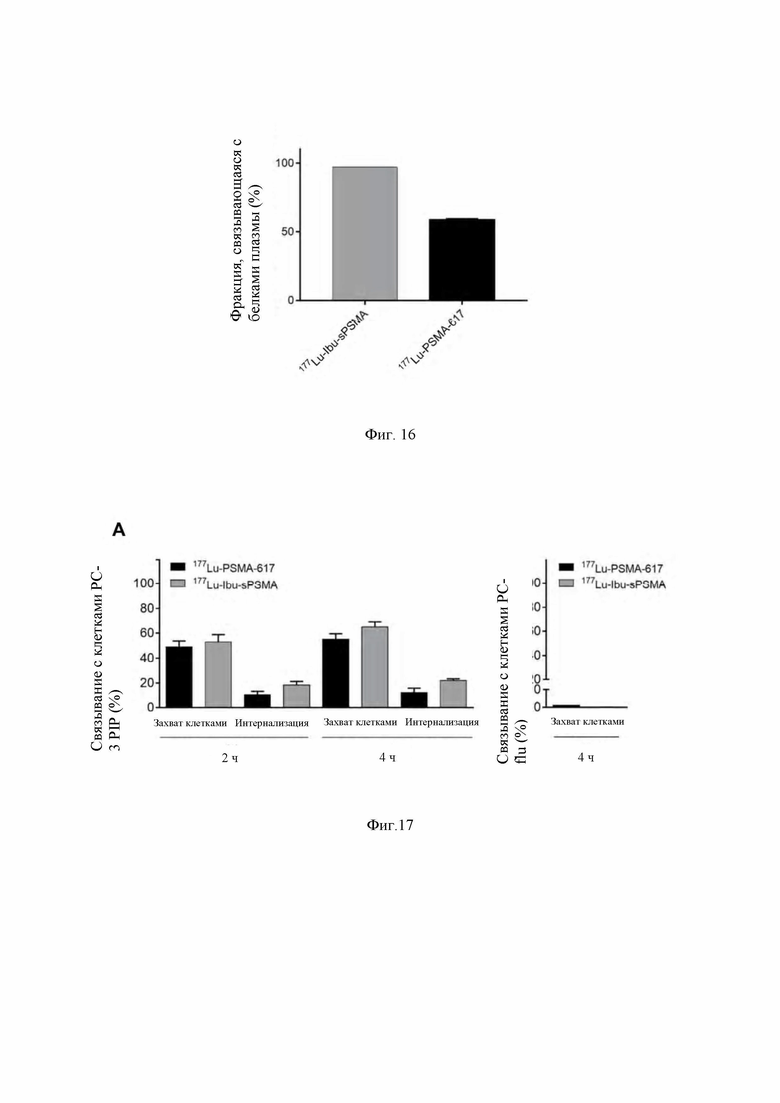
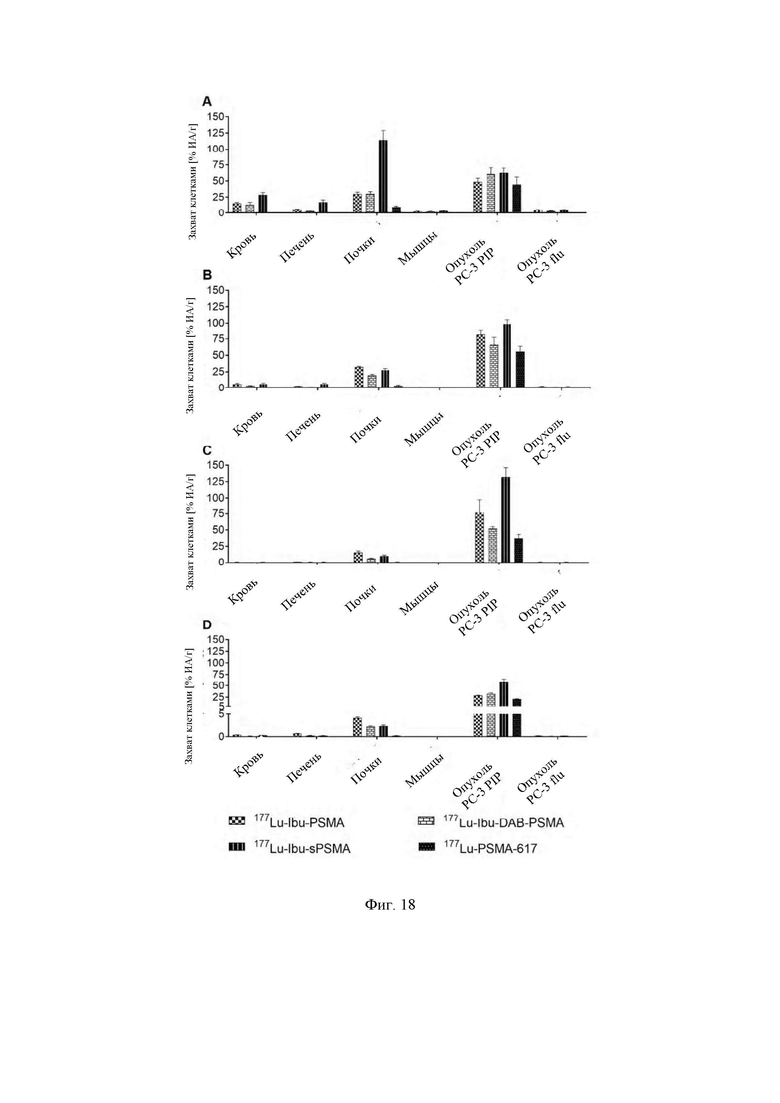
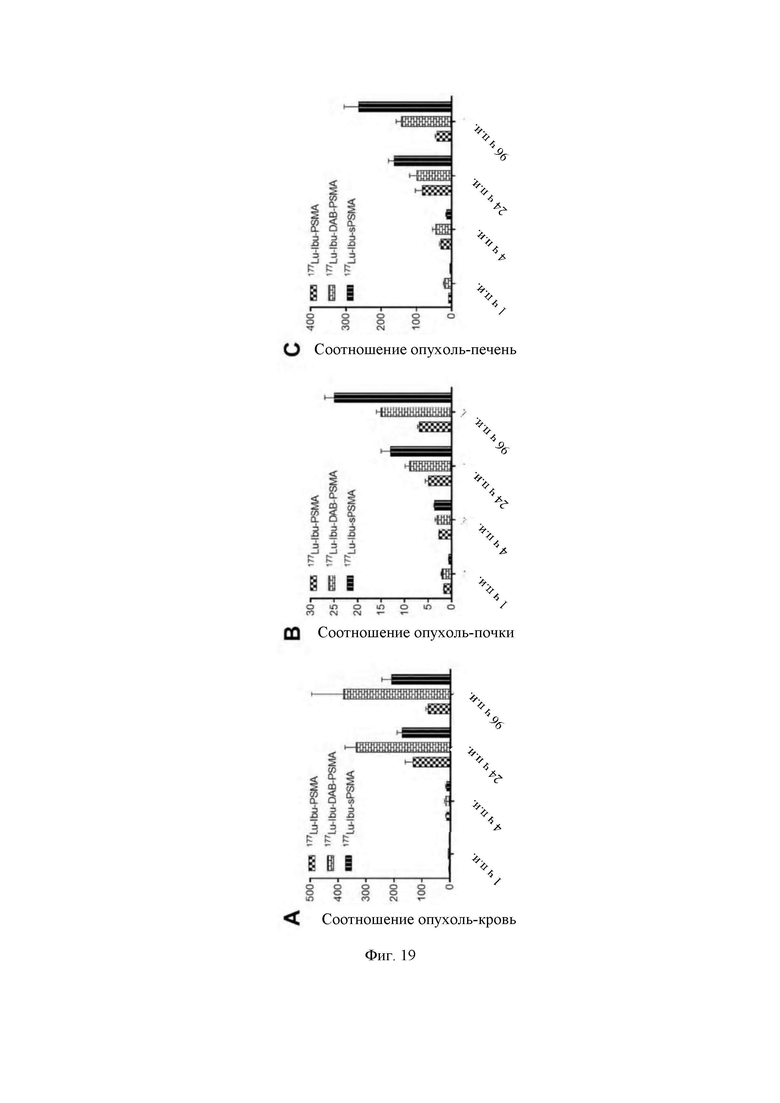
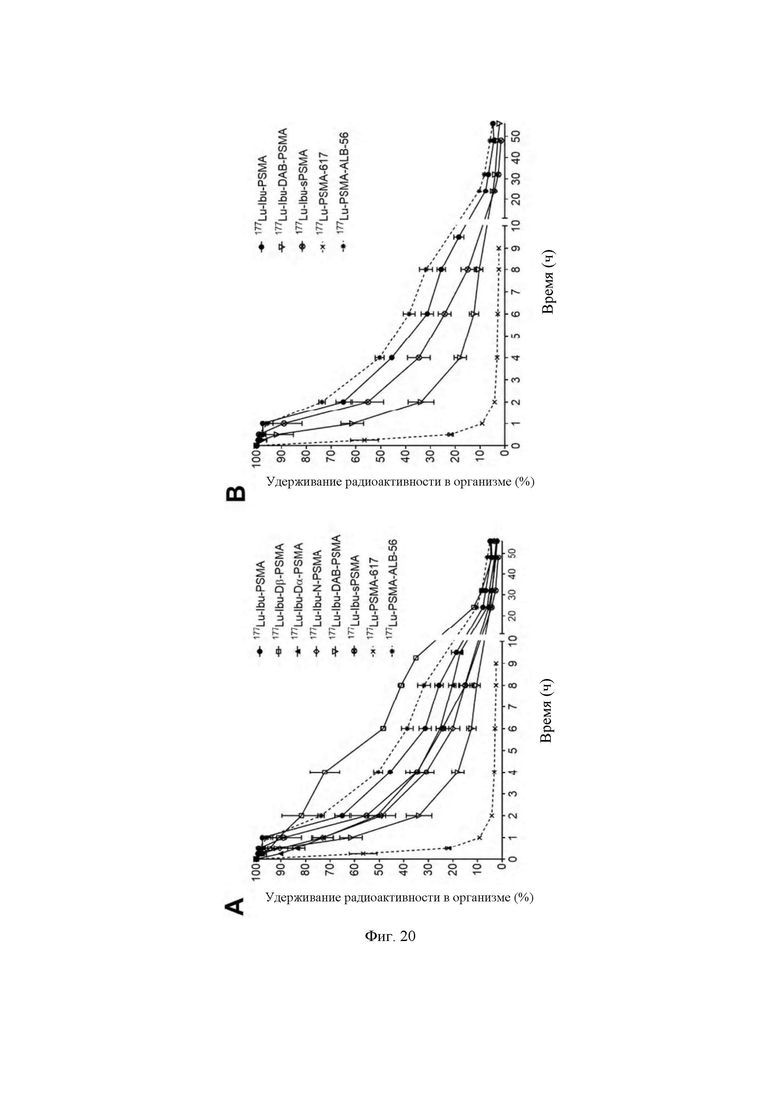
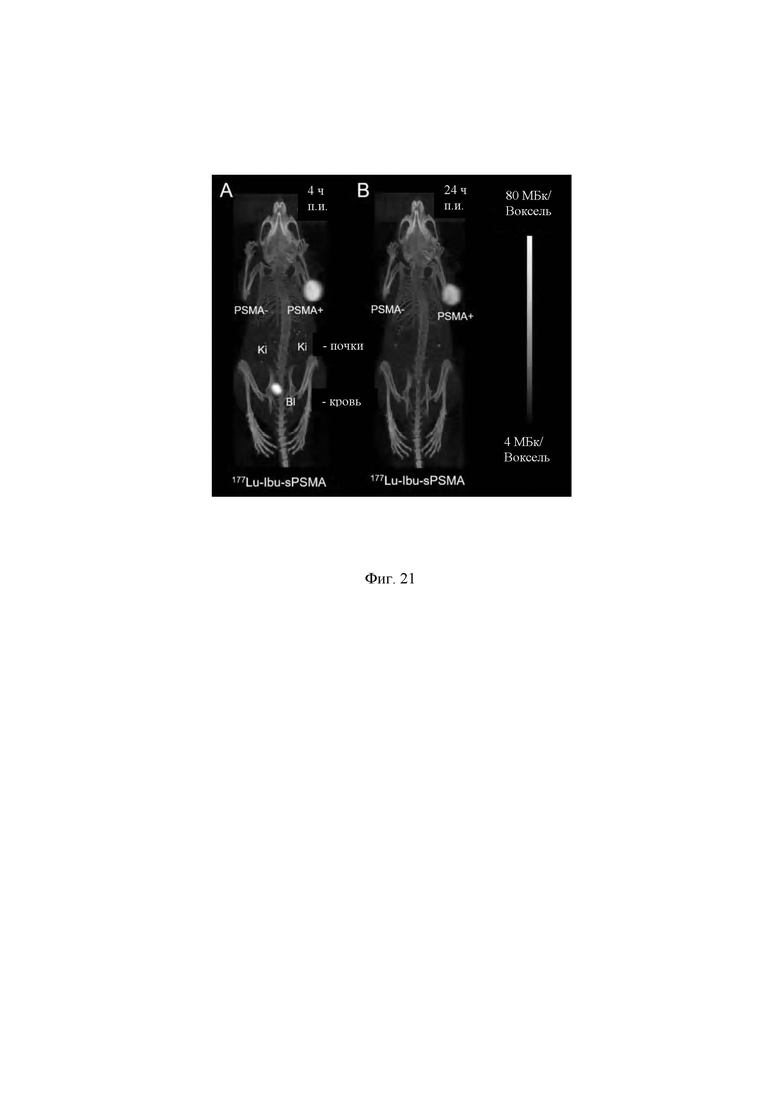
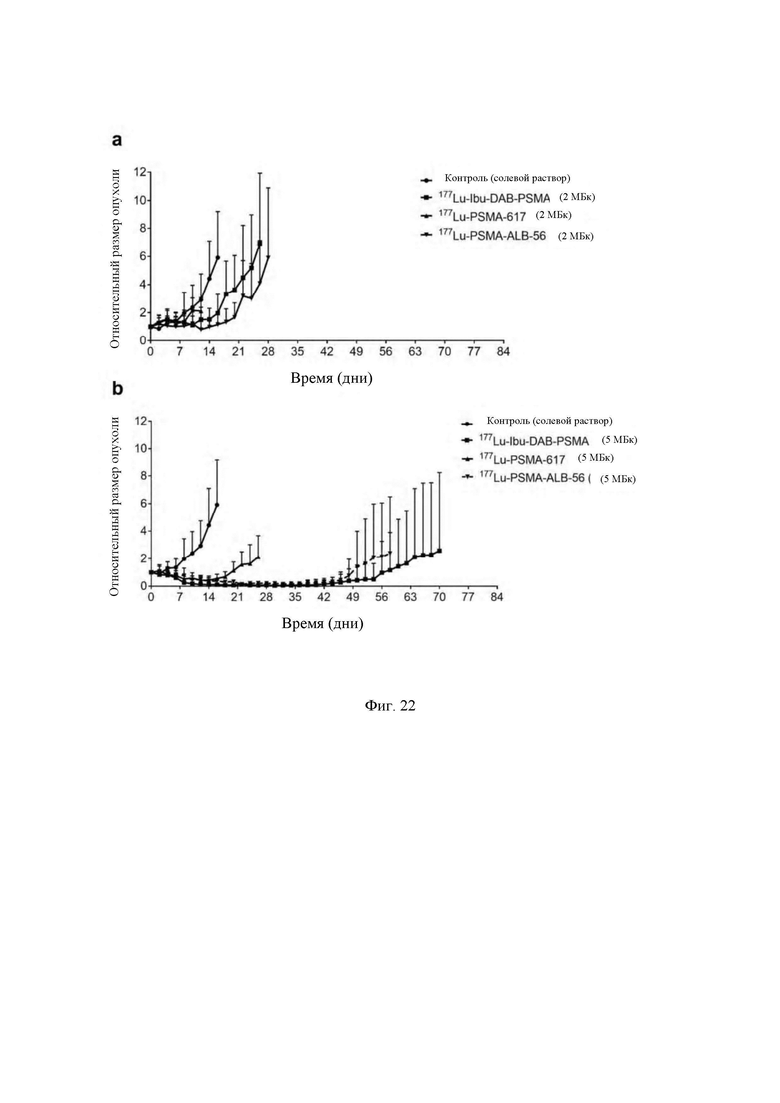
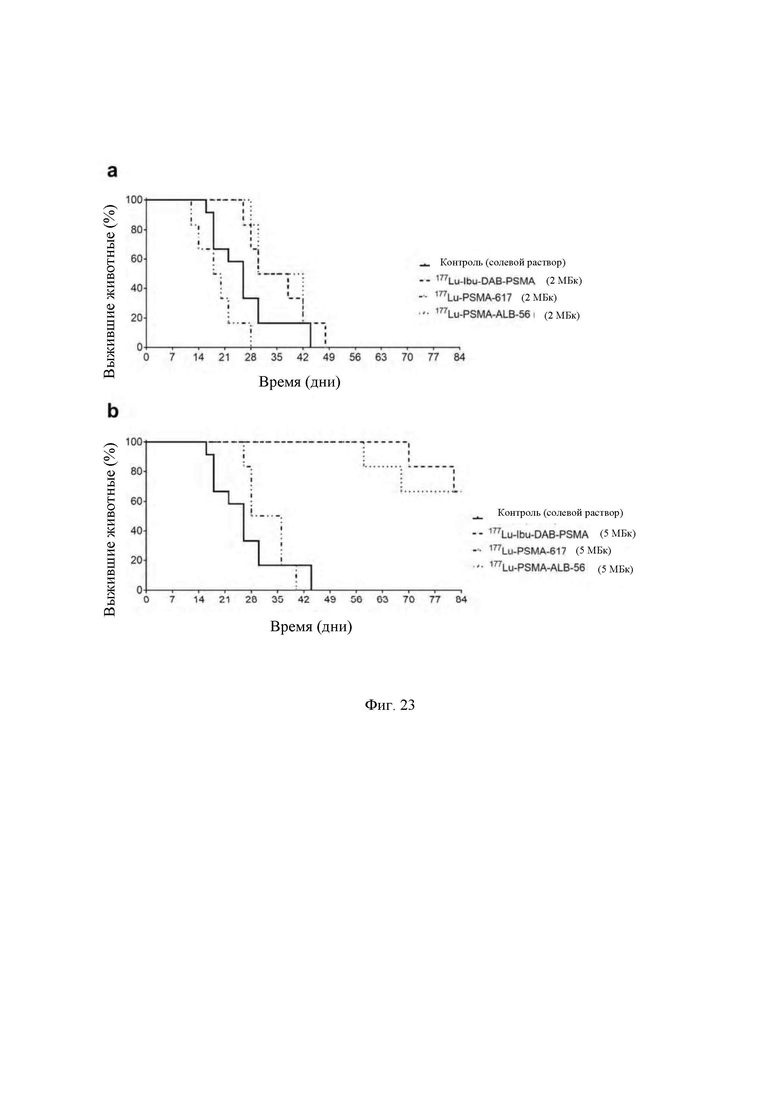
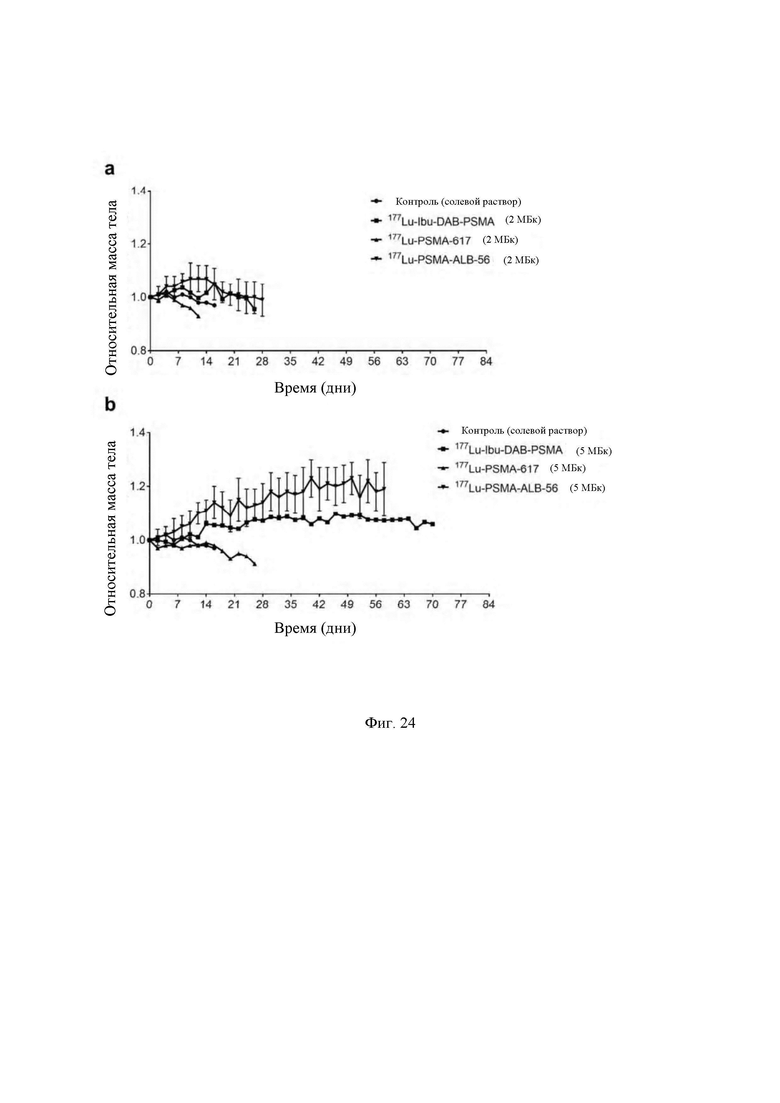
Изобретение относится к соединению общей формулы (1а), относящемуся к PSMA-направленным агентам, где D означает хелатирующий фрагмент, который выбирают из DOTA, HBED-CC, NOTA, NODAGA, DOTAGA, TRAP, NOPO, PCTA, DFO, DTPA, DO3AP, DO3APPrA, DO3APABn или их производных, Tbm означает простатоспецифический мембранный антиген (PSMA)-связывающий остаток, характеризующийся общей формулой (3), где X означает O, Y означает NH, Z означает CH2, R1, R2 и R3 каждый независимо выбирают из -CO2H, и f означает число, выбранное из 1, 2, 3, 4, или 5, линкер означает структурную формулу (4а), спейсер означает структурную формулу (2)(d)’, где А означает аминокислотный остаток или –[A]n отсутствует, и n означает целое число, выбранное из 0 или 1, где аминокислотный остаток выбирают из аспартата, аспарагина, диаминомасляной кислоты, и k означает целое число, выбранное из 1, 2, 3, 4, 5 или 6, и а означает число, выбранное из 0, или его фармацевтически приемлемая соль. Также изобретение относится к применению соединения формулы (1а) для получения радиоактивно меченного комплекса; радиоактивно меченному комплексу, включающему радионуклид и соединение формулы (1а); фармацевтической композиции на основе соединения формулы (1а) или радиоактивно меченного комплекса; набору, включающему соединение формулы (1а), или радиоактивно меченный комплекс, или фармацевтическую композицию; и способу in vitro детектирования присутствия клеток и/или тканей, экспрессирующих простатоспецифический мембранный антиген (PSMA). Технический результат – разработка новых PSMA-направленных агентов, несущих терапевтические или диагностические фрагменты, которые связываются с альбумином. 6 н. и 33 з.п. ф-лы, 24 ил., 8 табл., 12 пр. 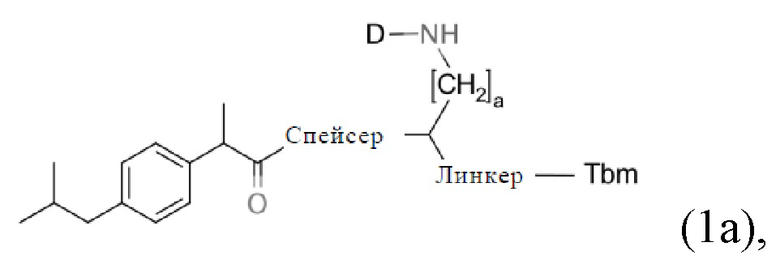
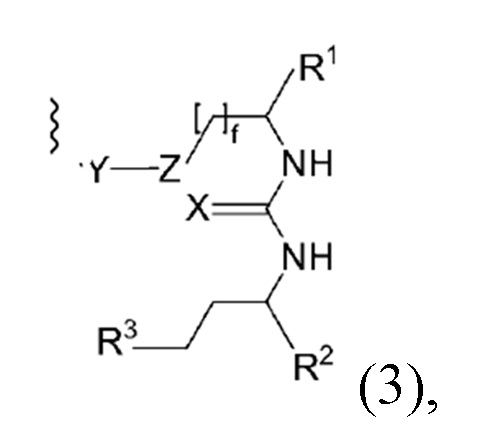
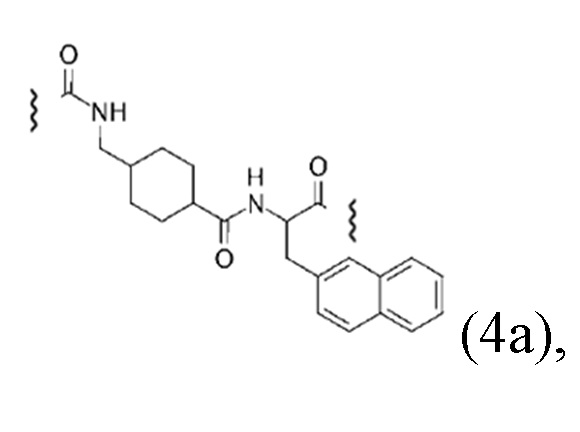
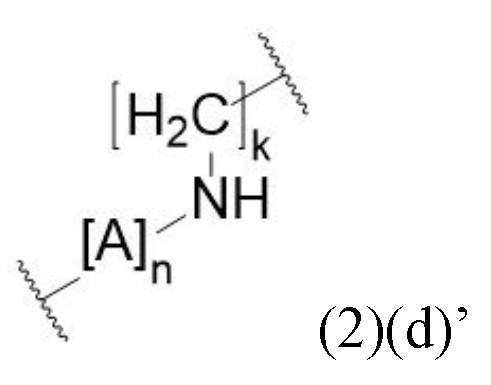
1. Соединение общей формулы (1а):
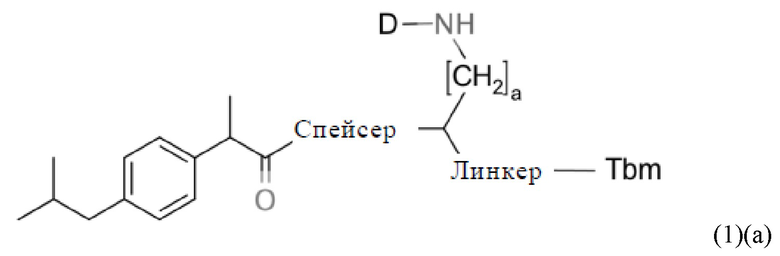
где D означает хелатирующий фрагмент, выбирают из 1,4,7,10-тетраазациклододекан-1,4,7,10-тетрауксусной кислоты (DOTA), N,N"-бис[2-гидрокси-5-(карбоксиэтил)бензил]этилендиамин-N,N"-диуксусной кислоты (HBED-CC), 1,4,7-триазациклононан-1,4,7-триуксусной кислоты (NOTA), 2-(4,7-бис(карбоксиметил)-1,4,7-триазонан-1-ил)глутаровой кислоты (NODAGA), [2-(4,7,10-трис(карбоксиметил)-1,4,7,10-тетраазациклододекан-1-ил)глутаровой кислоты (DOTAGA), 1,4,7-триазациклононанфосфиновой кислоты (TRAP), 1,4,7-триазациклононан-1-[метил(2-карбоксиэтил)фосфиновой кислоты]-4,7-бис[метил(2-гидроксиметил)фосфиновой кислоты] (NOPO), 3,6,9,15-тетразабицикло[9,3,1]пентадека-1(15),11,13-триен-3,6,9-триуксусной кислоты (PCTA), N’-{5-[ацетил(гидрокси)амино]пентил}-N-[5-({4-[(5-аминопентил)(гидрокси)амино]-4-оксобутаноил}амино)пентил]-N-гидроксисукцинамида (DFO), диэтилентриаминпентауксусной кислоты (DTPA), DO3AP, DO3APPrA, DO3APABn или их производных,
Tbm означает простатоспецифический мембранный антиген (PSMA)-связывающий остаток, характеризующийся общей формулой (3):
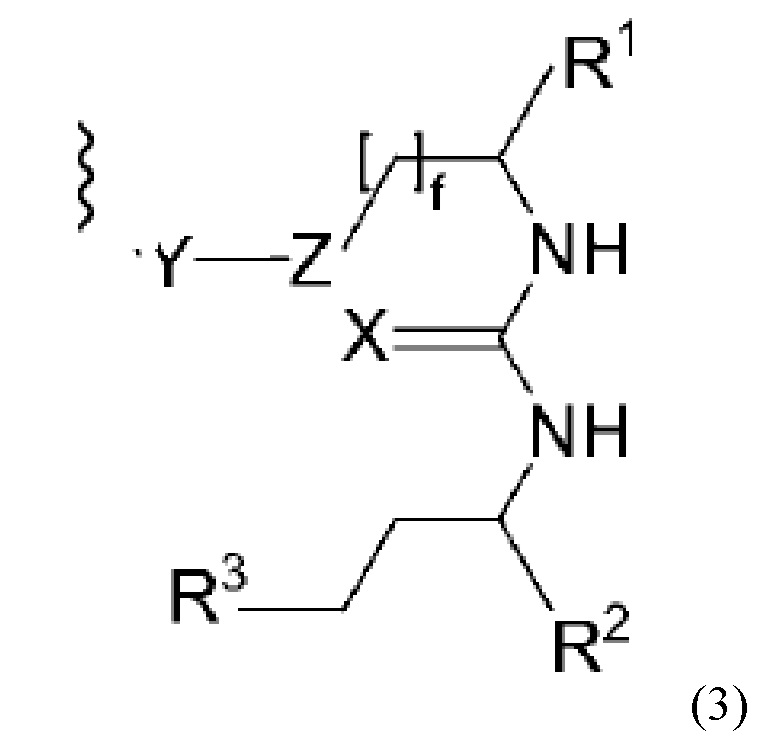
где
X означает O,
Y означает NH,
Z означает CH2,
R1, R2 и R3 каждый независимо выбирают из -CO2H, и
f означает число, выбранное из 1, 2, 3, 4, или 5,
линкер означает структурную формулу (4а):
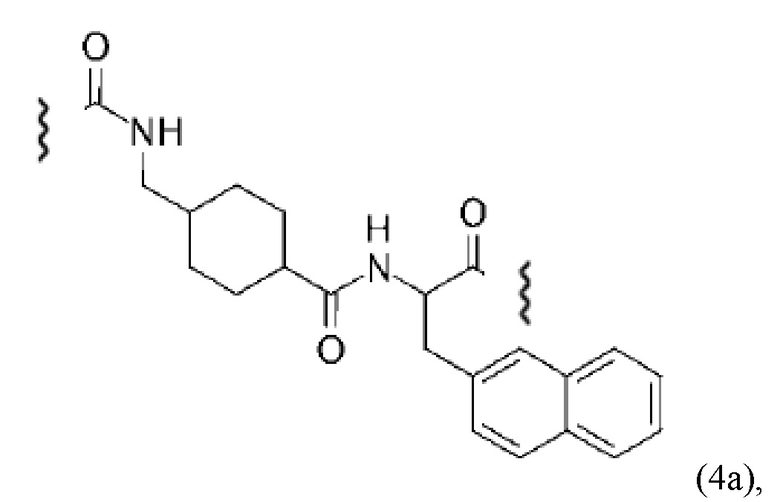
спейсер означает структурную формулу (2)(d)’:
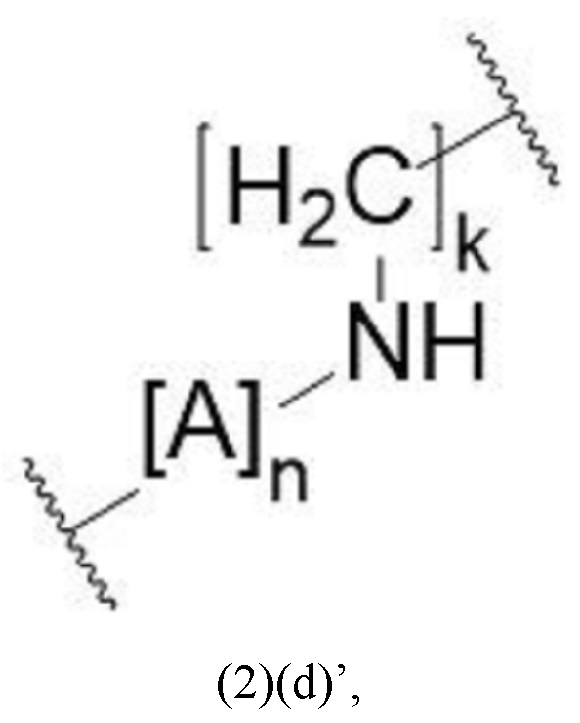
где А означает аминокислотный остаток или –[A]n отсутствует, и n означает целое число, выбранное из 0 или 1, где аминокислотный остаток выбирают из аспартата, аспарагина, диаминомасляной кислоты, и k означает целое число, выбранное из 1, 2, 3, 4, 5 или 6, и
а означает 0,
или его фармацевтически приемлемая соль.
2. Соединение по п. 1, где f означает целое число, выбранное из 1, 2, 3, 4 или 5, предпочтительно f равен 2 или 3.
3. Соединение по любому одному из пп. 1, 2, где PSMA-связывающий остаток характеризуется общей формулой (3)(ii):
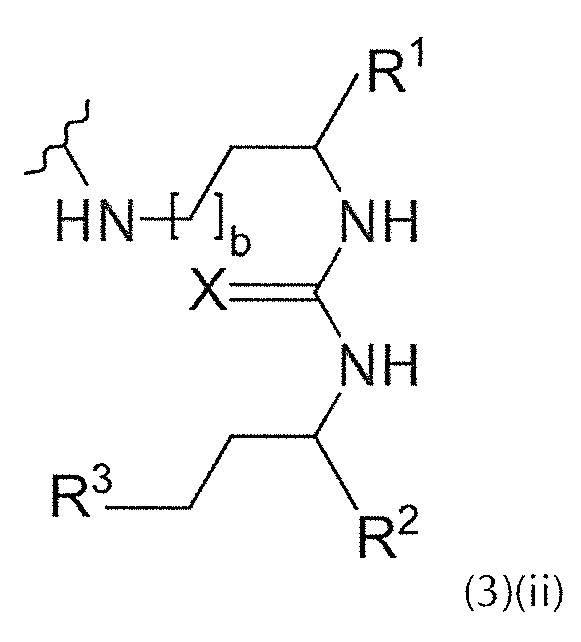 ,
,
где
X означает O,
R1, R2 и R3 каждый представляет собой -CO2H, и
b означает число, выбранное из 1, 2, 3, 4, или 5.
4. Соединение по любому одному из пп. 1-3, где b означает целое число, выбранное из 1, 2, 3, 4 или 5, предпочтительно b означает 2, 3 или 4, более предпочтительно b означает 3.
5. Соединение по любому одному из пп. 1-4, где R1, R2 и R3 каждый представляет собой –COOH, X означает O и b означает 3.
6. Соединение по любому одному из пп. 1-5, где PSMA-связывающий остаток характеризуется формулой (3)(а):
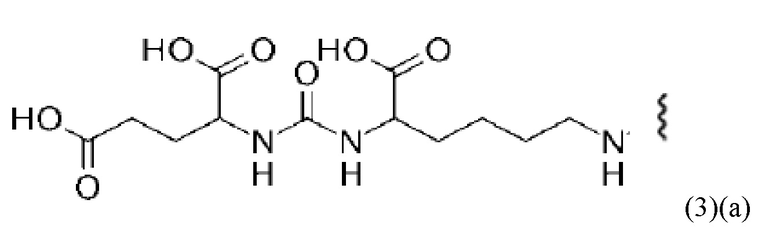
7. Соединение по любому одному из пп. 1-6, где указанное соединение характеризуется общей формулой (1)(b) или (1)(с):
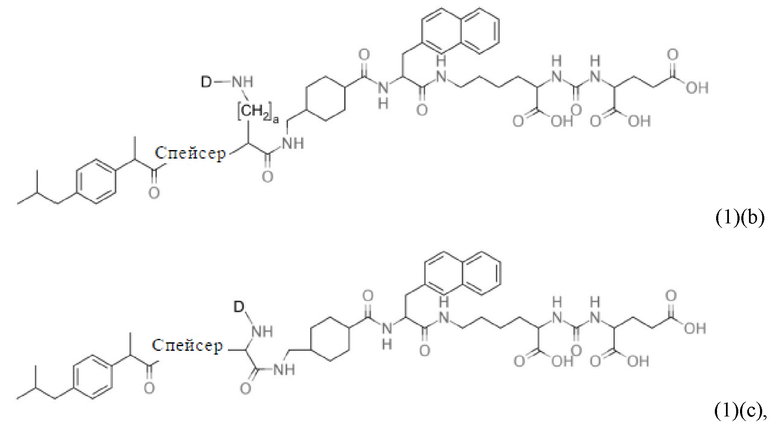
где D и спейсер определены выше, и
а означает 0,
или его фармацевтически приемлемая соль.
8. Соединение по любому одному из пп. 1-7, где спейсер включает или состоит из формулы (2)(a) или формулы (2)(a)’ или формулы (2)(a)’’:
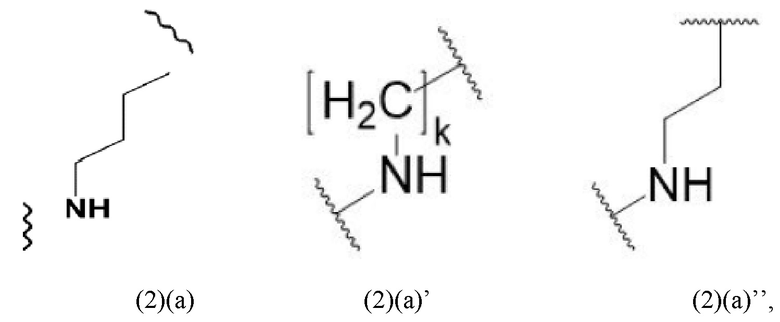
где k означает целое число, выбранное из 1, 2, 3, 4, 5, и 6, предпочтительно
2, 3 или 4.
9. Соединение по любому одному из пп. 1-8, где спейсер включает или состоит из формулы (2)(d):
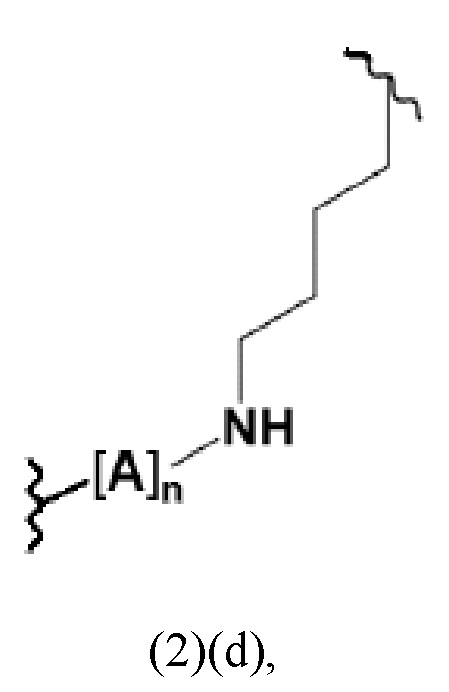
где А означает аминокислотный остаток или –[A]n отсутствует, и n означает целое число, выбранное из 0 или 1, и k определен выше.
10. Соединение по п. 1, где спейсер включает или состоит из формулы (2)(d)(i) или (2)(d)(i)':
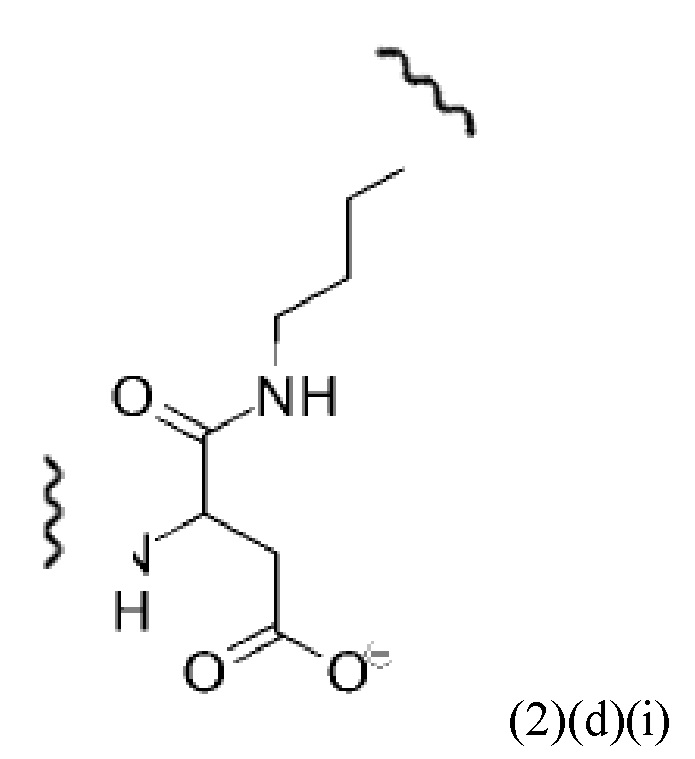
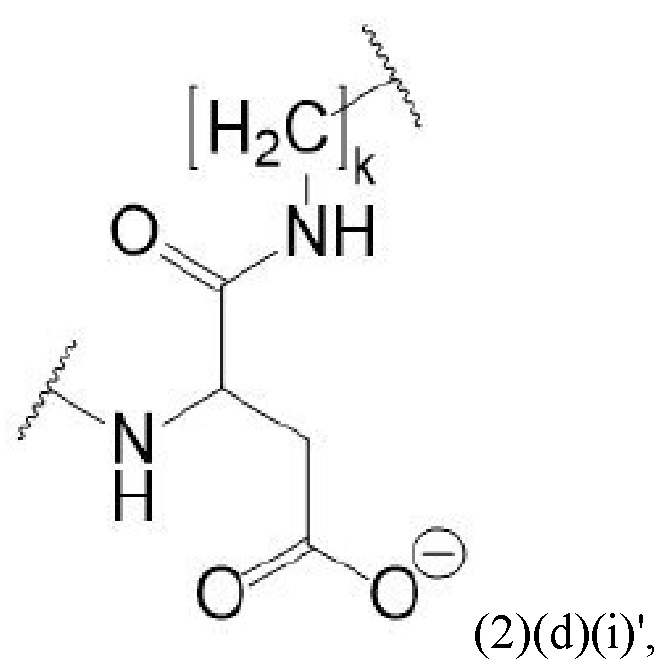
где k определен выше.
11. Соединение по п. 1, где спейсер включает или состоит из формулы (2)(d)(ii) или (2)(d)(ii)’:
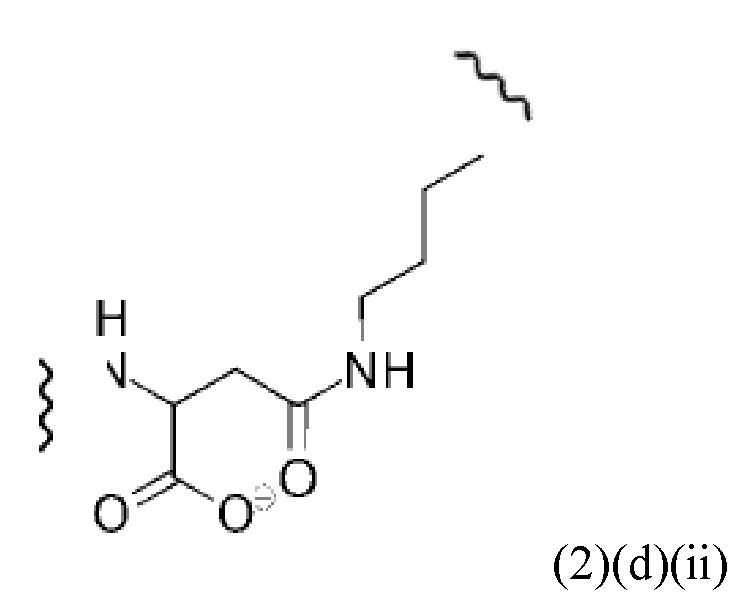
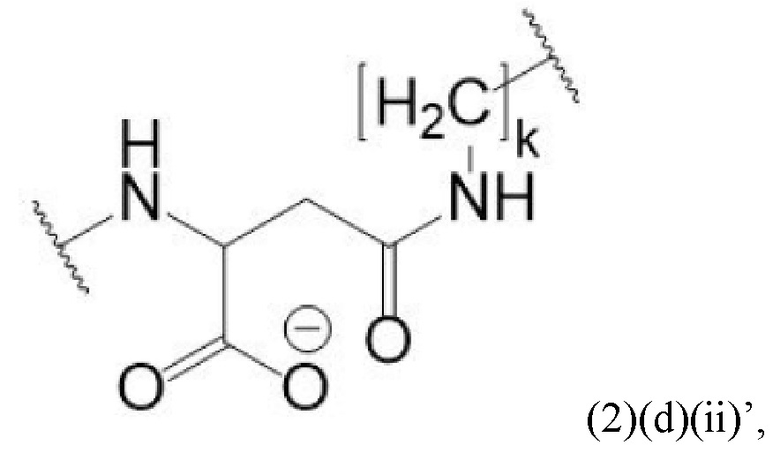
где k определен выше.
12. Соединение по п. 1, где спейсер включает или состоит из формулы (2)(d)(iii) или (2)(d)(iii)’:
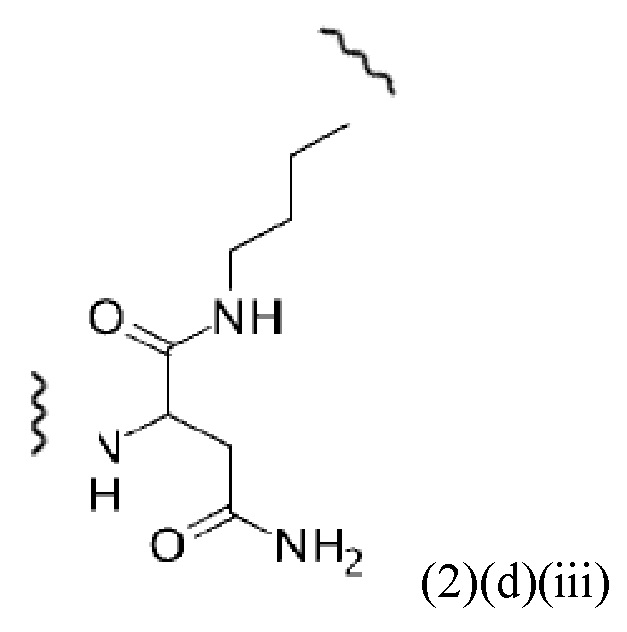
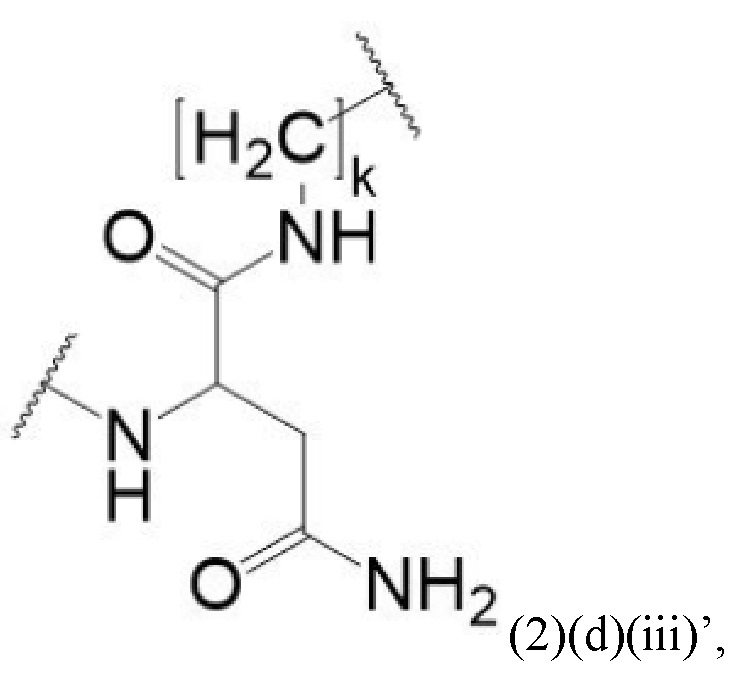
где k определен выше.
13. Соединение по п. 1, где спейсер включает или состоит из формулы (2)(d)(iv) или (2)(d)(iv)’:
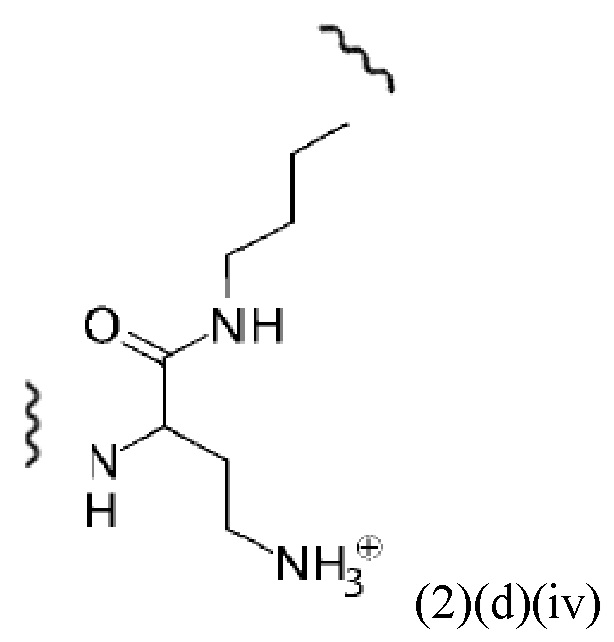
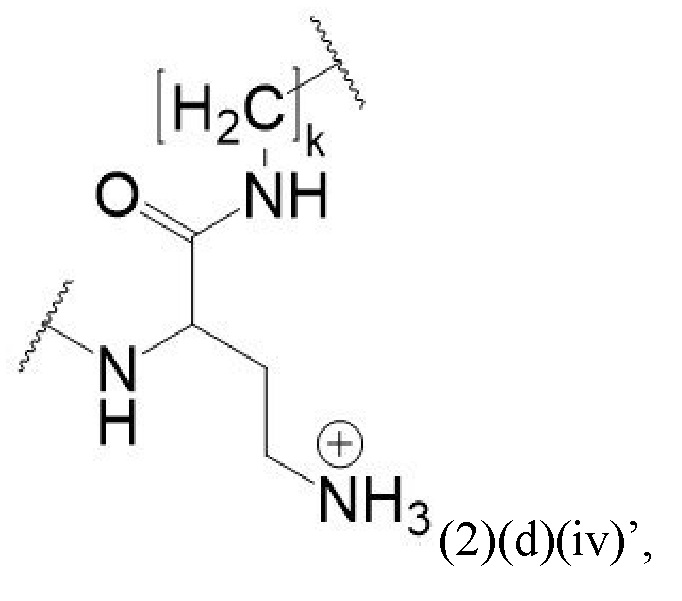
где k определен выше.
14. Соединение по любому одному из пп. 1-13, где указанное соединение характеризуется формулой (7)(а) или (7)(а)’:
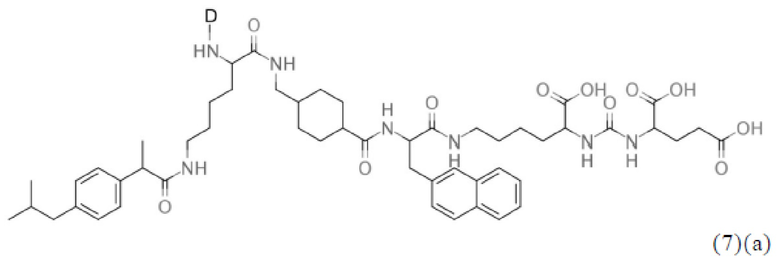
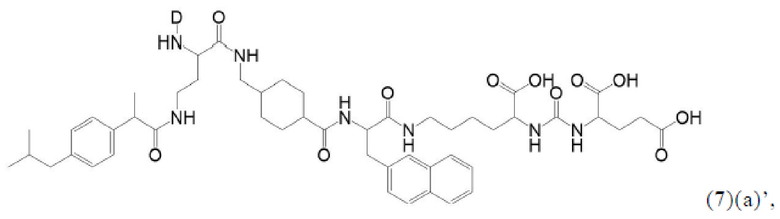
где
D определен выше,
или его фармацевтически приемлемая соль.
15. Соединение по любому одному из пп. 1-13, где указанное соединение характеризуется формулой (7)(b) или (7)(b)’:
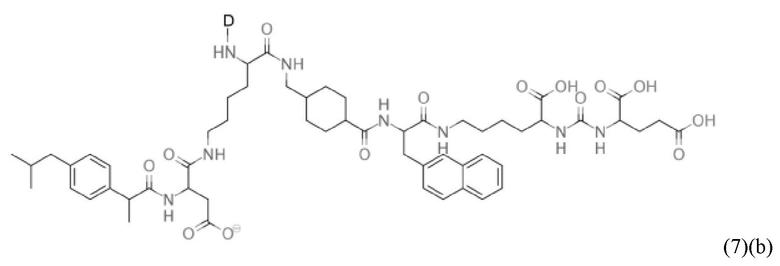
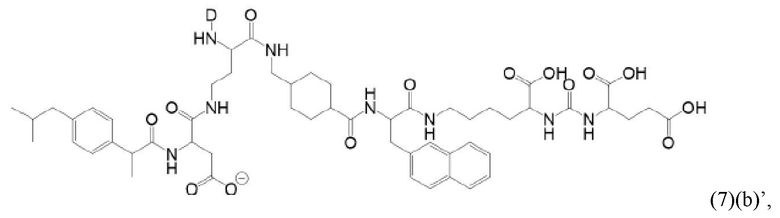
где D определен выше,
или его фармацевтически приемлемая соль.
16. Соединение по любому одному из пп. 1-13, где указанное соединение характеризуется формулой (7)(с) или (7)(с)’:
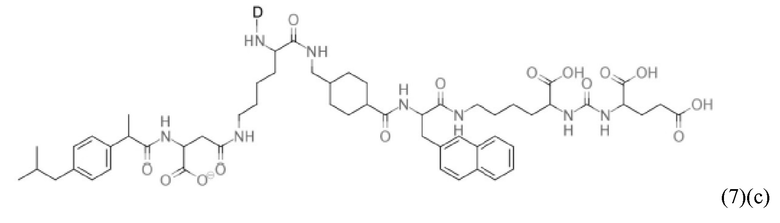
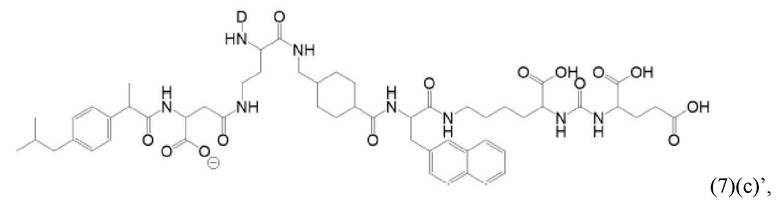
где D определен выше,
или его фармацевтически приемлемая соль.
17. Соединение по любому одному из пп. 1-13, где указанное соединение характеризуется формулой (7)(d) или (7)(d)’:
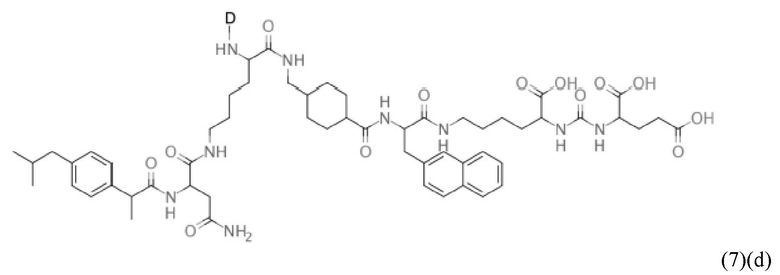
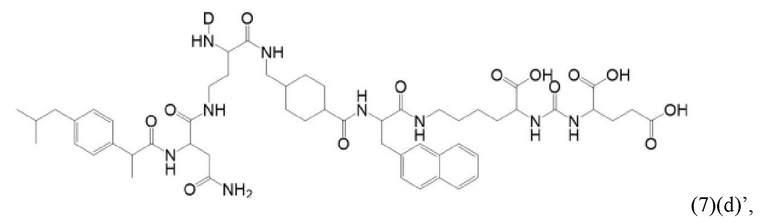
где D определен выше,
или его фармацевтически приемлемая соль.
18. Соединение по любому одному из пп. 1-13, где указанное соединение характеризуется формулой (7)(e) или (7)(e)’
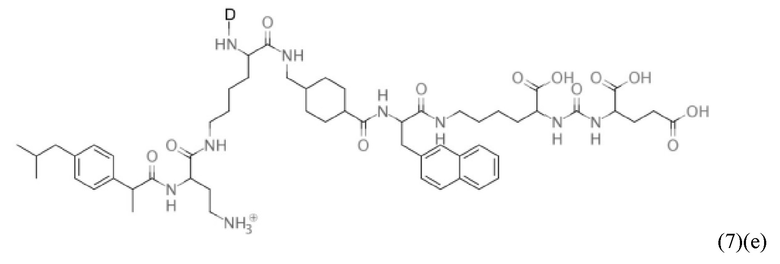
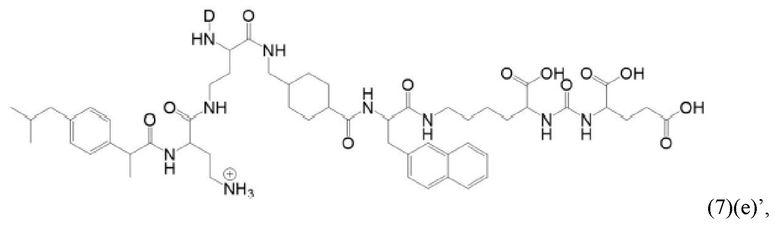
где D определен выше,
или его фармацевтически приемлемая соль.
19. Соединение по п. 1, где хелатирующий фрагмент представляет собой DOTA.
20. Соединение по любому одному из пп. 1-19, где указанное соединение характеризуется структурной формулой (8)(a) или (8)(a)’:
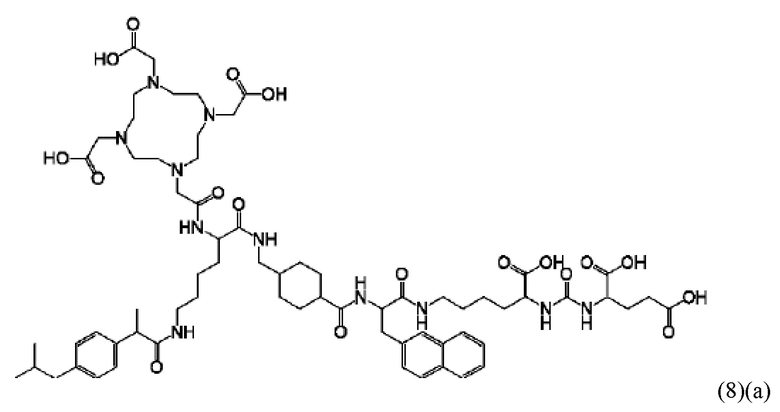
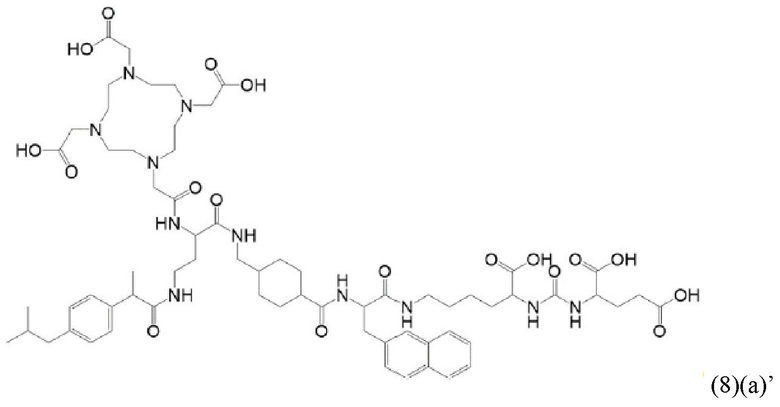
или его фармацевтически приемлемая соль.
21. Соединение по любому одному из пп. 1-19, где указанное соединение характеризуется структурной формулой (8)(b) или (8)(b)’:
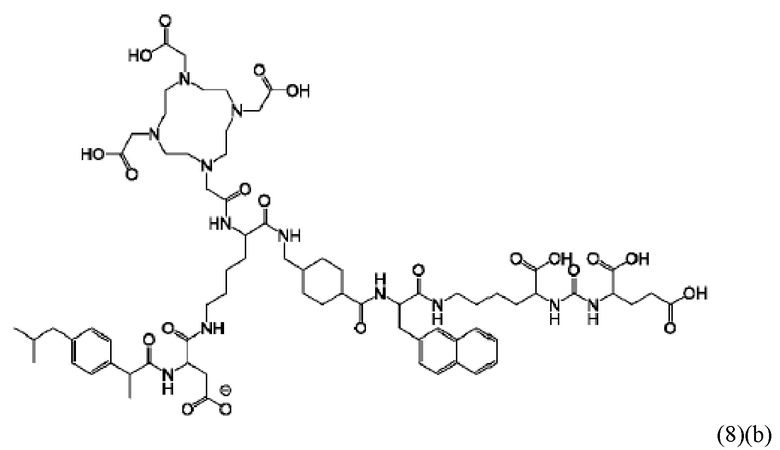
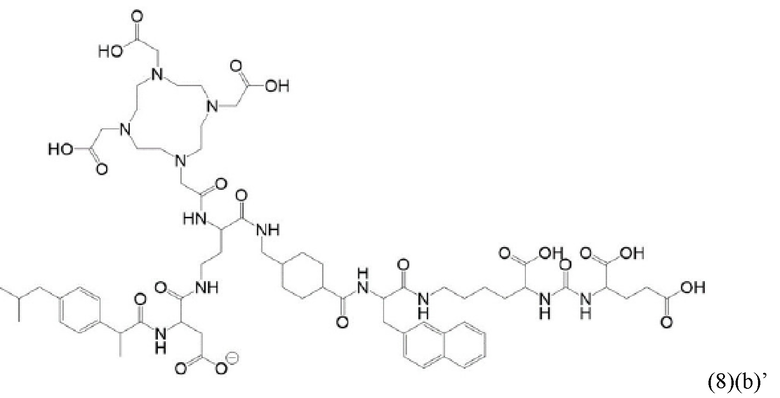
или его фармацевтически приемлемая соль.
22. Соединение по любому одному из пп. 1-19, где указанное соединение характеризуется формулой (8)(с) или (8)(с)’:
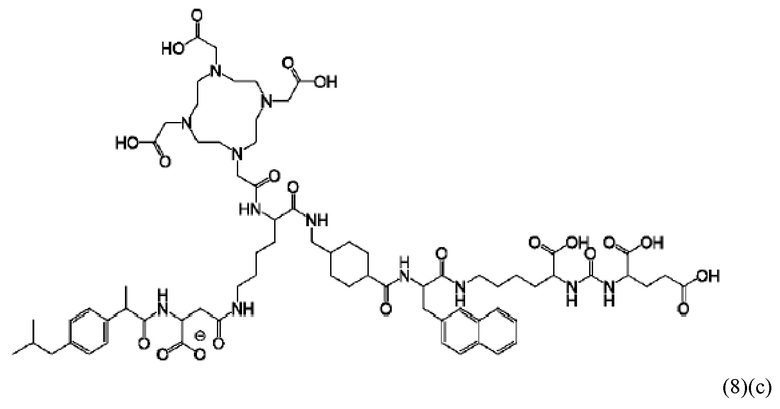
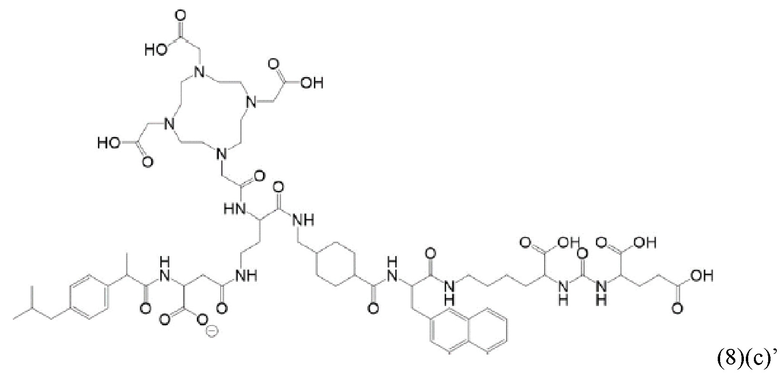
или его фармацевтически приемлемая соль.
23. Соединение по любому одному из пп. 1-19, где указанное соединение характеризуется структурной формулой (8)(d) или (8)(d)’:
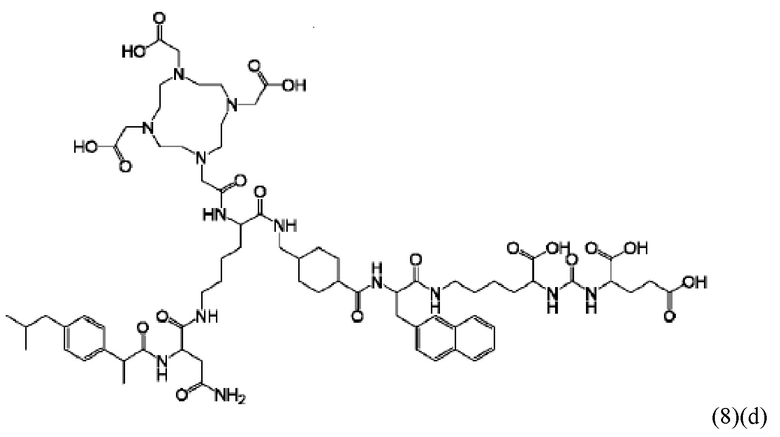
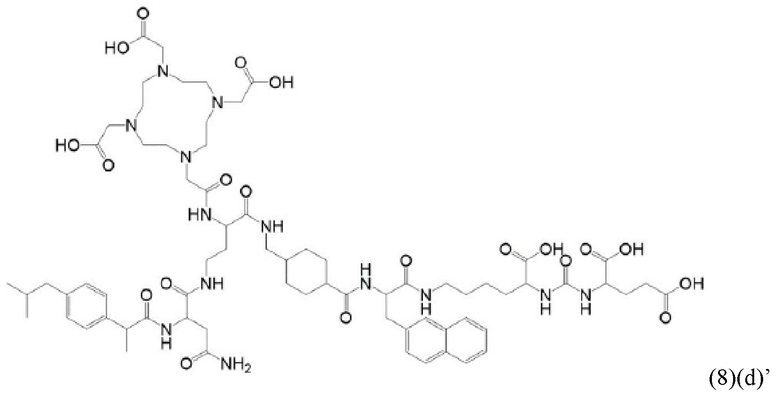
или его фармацевтически приемлемая соль.
24. Соединение по одному любому из пп. 1-19, где указанное соединение характеризуется структурной формулой (8)(е) или (8)(е)’:
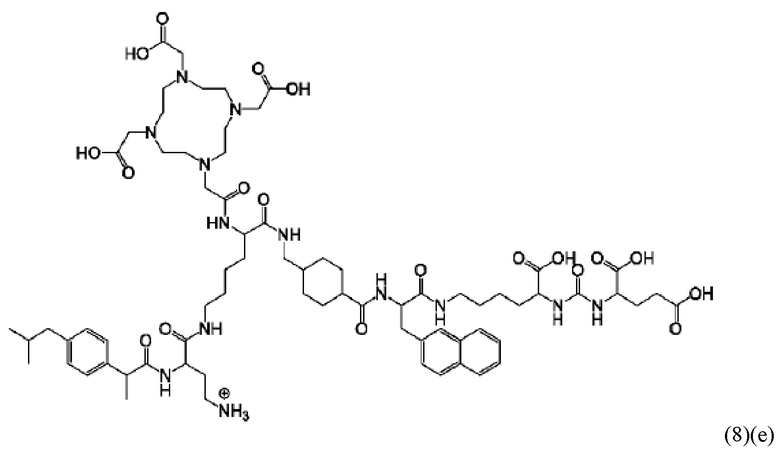
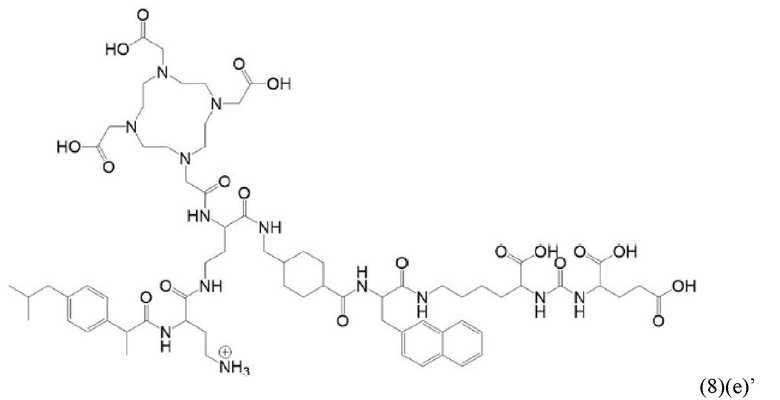
или его фармацевтически приемлемая соль.
25. Применение соединения по любому одному из пп. 1-24 для получения радиоактивно меченного комплекса.
26. Соединение по любому одному из пп. 1-24 для применения в качестве медицинского препарата или предшественника медицинского препарата для диагностики, лечения и/или профилактики рака, связанного с экспрессией PSMA антигена.
27. Радиоактивно меченный комплекс для диагностики, лечения и/или профилактики рака, связанного с экспрессией PSMA антигена, включающий радионуклид и соединение по любому из пп. 1-24.
28. Радиоактивно меченный комплекс по п. 27, где радиоактивную метку выбирают из группы, состоящей из 94Tc, 99mTc, 90In, 111In, 67Ga, 68Ga, 86Y, 90Y, 177Lu, 151Tb, 186Re, 188Re, 64Cu, 67Cu, 55Co, 57Co, 43Sc, 44Sc, 47Sc, 225Ac, 213Bi, 212Bi, 212Pb, 227Th, 153Sm, 166Ho, 152Gd, 153Gd, 157Gd или 166Dy.
29. Радиоактивно меченный комплекс по п. 27 или 28, где радиоактивная метка представляет собой 177Lu.
30. Фармацевтическая композиция для диагностики, лечения и/или профилактики рака, связанного с экспрессией PSMA антигена, включающая эффективное количество соединения по любому из пп. 1-24, или радиоактивно меченный комплекс по любому из пп. 27-29, и необязательно фармацевтически приемлемый носитель, разбавитель и/или эксципиент.
31. Набор для диагностики, лечения и/или профилактики рака, связанного с экспрессией PSMA антигена, включающий соединение по любому одному из пп. 1-24, или его фармацевтически приемлемую соль или радиактивно меченный комплекс, радиоактивно меченный комплекс по любому одному из пп. 27-29 или фармацевтическую композицию по п. 30.
32. Соединение по любому одному из пп. 1-24, радиоактивно меченный комплекс по любому одному из пп. 27-29, фармацевтическая композиция по п. 30 или набор по п. 31 для применения в медицине и/или диагностике рака, связанного с экспрессией PSMA антигена.
33. Соединение по любому одному из пп. 1-24, радиоактивно меченный комплекс по любому одному из пп. 27-29, фармацевтическая композиция по п. 30 или набор по п. 31 для применения в способе детектирования присутствия (изолированных) клеток и/или тканей, экспрессирующих простатоспецифический мембранный антиген (PSMA).
34. Соединение по любому одному из пп. 1-24, радиоактивно меченный комплекс по любому из пп. 27-29, фармацевтическая композиция по п. 30 или набор по п. 31 для применения в способе диагностики, лечения и/или профилактики рака, предпочтительно рака предстательной железы, рака поджелудочной железы, рака почек или рака мочевого пузыря.
35. Соединение, радиоактивно меченный комплекс, фармацевтическая композиция или набор для применения по любому одному из пп. 32-34, где указанные способ или применение включают
(а) введение указанного соединения, радиоактивно меченного комплекса или фармацевтической композиции пациенту, и
(б) получение рентгеновского изображения для указанного пациента.
36. Способ in vitro детектирования присутствия клеток и/или тканей, экспрессирующих простатоспецифический мембранный антиген (PSMA), включающий
(а) контактирование указанных PSMA-экспрессирующих клеток и/или тканей с соединением по любому из пп. 1-24, радиоактивно меченным комплексом по любому из пп. 27-29, фармацевтической композицией по п. 30 или набором по п. 31,
(б) использование детектирующих средств, необязательно рентгеновского изображения, с целью выявления указанных клеток и/или тканей.
37. Соединение, радиоактивно меченный комплекс, фармацевтическая композиция или набор для применения по любому одному из пп. 32-35, или способ по п. 36, где рентгеновское изображение включает позитронно-эмиссионную томографию (PET) или однофотонную эмиссионную компьютерную томографию (SPECT).
38. Соединение, радиоактивно меченный комплекс, фармацевтическая композиция или набор для применения по любому одному из пп. 32-35 или 37, или способ по п. 36 или 37, где указанные одна или более клеток или тканей включают (необязательно канцерогенные) клетки или ткани предстательной железы, (необязательно канцерогенные) клетки или ткани селезенки, или (необязательно канцерогенные) клетки или ткани почек.
39. Соединение, радиоактивно меченный комплекс, фармацевтическая композиция или набор для применения по любому одному из пп. 32-35 или 37-38, или способ по любому из пп. 36-38, где присутствие PSMA-экспрессирующих клеток или тканей указывает на опухоль (клетку) предстательной железы, метастазирующую опухоль (клетку) предстательной железы, опухоль (клетку) почек, опухоль (клетку) поджелудочной железы, опухоль (клетку) мочевого пузыря и их комбинации.
| UMBRICHT C | |||
| A | |||
| et al | |||
| Preclinical Development of Novel PSMA-Targeting Radioligands: Modulation of Albumin-Binding Properties To Improve Prostate Cancer Therapy, MOLECULAR PHARMACEUTICS, 2018, 15(6), pp | |||
| Водяной двигатель | 1922 |
|
SU2297A1 |
| WO 2018098390 A1, 31.05.2018 | |||
| CA 3028978 A1, 28.12.2017 | |||
| АГЕНТЫ, СВЯЗЫВАЮЩИЕСЯ С PSMA, И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2494096C2 |
Авторы
Даты
2024-12-11—Публикация
2019-11-28—Подача