Родственные заявки
Настоящая заявка испрашивает приоритет согласно предварительной заявке на патент США № 62/858968, поданной 7 июня 2019 года, содержание которой включено в данный документ посредством ссылки во всей своей полноте.
Перечень последовательностей
Настоящая заявка содержит перечень последовательностей, который был подан в электронном виде в формате ASCII и настоящим включен посредством ссылки во всей своей полноте. Указанная копия в формате ASCII, созданная 3 июня 2020 года, имеет название 1160430.002000.TXT и размер 634880 байт.
Область техники, к которой относится изобретение
Настоящее изобретение относится, среди прочего, к сконструированным pH-зависимым антителам к кластеру дифференцировки 3 (CD3), в том числе к мультиспецифическим антителам и их функциональным фрагментам, а также к способам и реагентам для их идентификации, выделения, получения и применения.
Предпосылки к созданию изобретения
Клеточные пролиферативные нарушения, такие как рак, характеризуются неконтролируемым ростом субпопуляций клеток. Они являются лидирующей причиной смерти в развитых странах мира и второй по значимости причиной смерти в развивающихся странах, при этом ожидается, что общее число новых случаев рака в год к 2030 году вырастет до 23,6 миллиона. По оценкам Национального института рака в США будет диагностировано почти 2 миллиона новых случаев рака и более 600000 американцев погибнут от рака в 2018 году. Таким образом, онкологическая помощь представляет собой значительную и постоянно возрастающую нагрузку на общество.
Идея использования цитотоксической способности Т-клеток для уничтожения опухолевых клеток путем применения биспецифических антител, целенаправленно воздействующих на CD3, возникла в середине 1980-х годов. (Staerz et al. Nature 1985 314: 628-32). Многие биспецифические антитела, разработанные на сегодняшний день, содержат первый сайт связывания, специфичный в отношении CD3, для рекрутинга и активации Т-клеток, и второй сайт связывания для целевого антигена, ассоциированного с заболеванием, такого как антиген, вырабатываемый опухолевой клеткой. Биспецифические антитела к CD3 активируют поверхностный рецептор CD3 на Т-клетках путем связывания со своим вторым белком-мишенью, экспрессируемым на опухолях, так что доступные Т-клетки могут связываться с экспрессирующими мишень клетками посредством связывания биспецифическим антителом к CD3, независимо от специфичности пептида/МНС их Т-клеточного рецептора. (См., например, Bassan, 2012, Blood 120:5094-95). Связывание Т-клеток и опухолевых клеток с помощью биспецифических антител к CD3 может вызвать резкую регрессию злокачественных новообразований на поздних стадиях и, в некоторых случаях, привести к полной ремиссии. В настоящее время более 25 различных биспецифических антител к CD3 находятся в стадии клинической разработки для лечения гематологических злокачественных новообразований или видов солидного рака путем целенаправленного воздействия на CD19, CD20, CD33 и CD123 или EpCAM, HER2, PSMA и CEA соответственно. (См., например, Liu et al. Front Immunol 2017 8:38).
Хотя биспецифические антитела продемонстрировали значительные преимущества по сравнению с моноспецифическими антителами в отношении лечения и выявления рака, широкому коммерческому применению биспецифических антител препятствует отсутствие эффективных/недорогих способов получения, отсутствие стабильности биспецифических полипептидов и отсутствие длительного периода полужизни в организме человеке. За последние несколько десятилетий было разработано огромное количество способов получения биспецифических моноклональных антител. Однако многие кандидатные биспецифические антитела с исключительной селективностью и высокой эффективностью в отношении представляющей интерес мишени часто имеют проблемы при последующей разработке и в отношении показателей клинической эффективности, включая полиспецифическое связывание (или «полиспецифичность»); нецелевое связывание; неспецифическое связывание; низкие уровни или профили экспрессии в эукариотических клетках-хозяевах, таких как клетки-хозяева млекопитающих и дрожжевые клетки; неудовлетворительные химические и физические свойства, такие как неудовлетворительная стабильность при хранении (например, неудовлетворительная/низкая стабильность в течение срока годности), неудовлетворительная (низкая) растворимость, неудовлетворительная (высокая) вязкость, предрасположенность к агрегации и т.п.; и неудовлетворительные клинические и биофизические профили, такие как неудовлетворительные фармакокинетические профили, неудовлетворительные фармакодинамические профили, быстрая или неудовлетворительная скорость выведения in vivo, короткий период полужизни в кровотоке, некоторые из которых приводят к прекращению их разработки.
Существуют определенные методики и анализы для оценки многих из вышеупомянутых характеристик разрабатываемости для обнаруженных антител в контексте последующих мероприятий по разработке («антитела после обнаружения»), такие как CIC, SIC, BVP-ELISA, TMA и другие анализы; однако такие анализы обычно не подходят для высокопроизводительных форматов на платформах раннего обнаружения антител. Кроме того, для оценки этих свойств, как правило, требуются количества белка от миллиграммов до граммов, таким образом зачастую налагается фактическое ограничение на целый ряд лидерных продуктов, которые, с прагматической точки зрения, можно рассматривать при разработке, и, следовательно, снижается вероятность успеха программы. Вследствие этого, значительные ресурсы зачастую тратятся на попытки усовершенствования лидерных продуктов-кандидатов с неудовлетворительным поведением с помощью небольшого числа запасных вариантов, доступных на более поздних стадиях разработки.
В данной области известны различные антитела к CD3, в том числе форматы моноклональных и биспецифических антител. См., например, патенты США №№ 7262276; 7635472; 7862813; 9587021; и 10174124. Однако многие из этих антител к CD3 характеризуются проблемами разрабатываемости, такими как описанные выше, и/или вызывают выработку цитокинов, что часто приводит к синдрому токсического высвобождения цитокинов (CRS). Поскольку связывающий домен антитела к CD3 из биспецифического антитела активирует все T-клетки, то осуществляется рекрутинг подгруппы CD4+ T-клеток с высоким продуцированием цитокинов. Следовательно, существует потребность в обеспечении антител к CD3, которые проявляют требуемые профили разрабатываемости и/или риска возникновения CRS, и являются безопасными и эффективными, например, при специфическом связывании с CD3, экспрессируемым на T-клетках, активации T-клеток и (пере)направлении активированных T-клеток на цитолиз целевых клеток и осуществлении этого с уменьшенным риском возникновения CRS.
Один из подходов к разработке доменов, связывающих CD3, которые демонстрируют требуемые профили риска возникновения CRS, заключается в конструировании доменов, связывающих CD3, с pH-зависимым связыванием антигена. Включение гистидинов и/или других ионизируемых остатков в связывающие области антител и других белков ранее использовалось для конструирования pH-зависимого связывания антигена (см., например, Igawa et al., Nature Biotechnology 28:1203-1207 (2010)). Протонирование боковых цепей гистидина в связывающих областях может изменять электростатические взаимодействия и/или вызывать конформационные изменения, которые приводят к рН-зависимым различиям в аффинности связывания (Gera et al., PLOS ONE 7(11) e48928. doi:10.1371/ 2012). С учетом того, что диапазон pH человеческой крови составляет приблизительно 7,6-7,8, тогда как опухолевые клетки имеют внеклеточный pH, составляющий приблизительно 6,3-6,5, по меньшей мере частично из-за накопления метаболических кислот, которые неэффективно выводятся из-за неудовлетворительной васкуляризации опухоли, сконструированные заявителем pH-зависимые домены, связывающие CD3, с преимущественным связыванием CD3 при низких (более низких) значениях pH способствуют связыванию и активности в пределах микроокружения опухоли и вокруг него. Без ограничения теорией, считается, что домены, связывающие CD3, сконструированные так, чтобы предпочтительно связываться с CD3 при более низком pH, например pH ~ 6, могут приводить к селективной и устойчивой цитотоксической активности на опухолевом участке или вокруг него, с обеспечением тем самым потенциального снижения или устранения нецелевых эффектов, а также улучшения периода полувыведения и дозирования.
Краткое описание изобретения
Настоящее изобретение относится к сконструированным pH-зависимым антителам к CD3 и их антигенсвязывающим фрагментам, при этом антитела и антигенсвязывающие фрагменты необязательно связываются с CD3 и/или CD3-экспрессирующими клетками с большей аффинностью связывания при pH 6,0, чем при физиологическом pH (pH 7,4), а также способам применения вышеперечисленного.
В определенных вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3, выбранный из группы, состоящей из ADI-48576, ADI-48577, ADI-48587, ADI-48592, ADI-48595, ADI-48635, ADI-48643, ADI-48645, ADI-48650, ADI-48652 и ADI-48666.
В определенных вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3, выбранный из группы, состоящей из ADI-48592, ADI-48595, ADI-48650, ADI-48652, ADI-48662 и ADI-48666.
В определенных вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3, выбранный из группы, состоящей из ADI-48588, ADI-48587, ADI-48577, ADI-48590, ADI-48581, ADI-48575, ADI-48593, ADI-48591, ADI-48647, ADI-48636, ADI-48586, ADI-48646, ADI-48638, ADI-48597, ADI-48601, ADI-48576, ADI-48643, ADI-48624, ADI-48632, ADI-48635 и ADI-48645.
Анализ 258 уникальных клонов, идентифицированных с использованием описанной в данном документе методологии, выявил консенсусные мотивы в области CDRH3. В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH3, где домен, связывающий CDRH3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность AX1DX2YX3HX4FYDV, где X1 представляет собой R или H, где X2 представляет собой A или H, где X3 представляет собой G, H или P, где X4 представляет собой Y, H, D, V, E, S, N, L, M, I, G, A, Q или T, и где необязательно по меньшей мере один из X1, X2, X3 и X4 заменен на H (SEQ ID NO: 1).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH3, где домен, связывающий CDRH3, содержит консенсусный мотив, представленный последовательностью ARDX1YGX2X3X4YDX5, где X1 представляет собой A или H, где X2 представляет собой R или H, где X3 представляет собой H или Y, где X4 представляет собой F или H, где X5 представляет собой H или V, и где необязательно по меньшей мере один из X1, X2, X3, X4 и X5 заменен на H (SEQ ID NO: 2).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH3, где домен, связывающий CDRH3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDAHX1X2YX3X4DX5, где X1 представляет собой G, E или R, где X2 представляет собой R или H, где X3 представляет собой F или H, где X4 представляет собой Y или H, где X5 представляет собой V или H, и где необязательно по меньшей мере один из X2, X3, X4 и X5 заменен на H (SEQ ID NO: 3).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH3, где домен, связывающий CDRH3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDAX1HRX2FYDV, где X1 представляет собой H, Y, S, G, A, T, V или R, где X2 представляет собой Y или H и где необязательно по меньшей мере один из X1 и X2 заменен на H (SEQ ID NO: 4).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH3, где домен, связывающий CDRH3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDX1YHRYFYDX2, где X1 представляет собой H или A, где X2 представляет собой H, V или M и где необязательно по меньшей мере один из X1 и X2 заменен на H (SEQ ID NO: 5).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3, CDRH3, где домен, связывающий CDRH3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность AX1DAYX2X3X4HX5DV, где X1 представляет собой R или H, где X2 представляет собой G или H, где X3 представляет собой H или R, где X4 представляет собой N, F или Y, где X5 представляет собой Y или H и где необязательно по меньшей мере один из X1, X2, X3, и X5 заменен на H (SEQ ID NO: 6).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH3, где домен, связывающий CDRH3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDX1X2GRYFYDV, где X1 представляет собой M, Q или H, где X2 представляет собой R или H и где необязательно по меньшей мере один из X1 и X2 заменен на H (SEQ ID NO: 7).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH3, где домен, связывающий CDRH3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDX1X2X3RYFYDX4, где X1 представляет собой H или A, где X2 представляет собой T, Y или H, где X3 представляет собой G или H, где X4 представляет собой V или H и где необязательно по меньшей мере из X1, X2, X3 и X4 заменен на H (SEQ ID NO: 8).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3, CDRH3, где домен, связывающий CDRH3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность AX1DX2X3X4X5X6X7X8DX9, где X1 представляет собой R или H, где X2 представляет собой A, H, M или Q, где X3 представляет собой Y, H, S, G, A, T, V или R; где X4 представляет собой G, H, P, E или R; где X5 представляет собой H или R, где X6 представляет собой Y, N, F, H, D, E, S, L, M, I, G, A, Q или T; где X7 представляет собой F или H; где X8 представляет собой Y или H; где X9 представляет собой V, H или M; и где необязательно по меньшей мере один из X1, X2, X3, X4, X5, X6, X7, X8 и X9 представляет собой H (SEQ ID NO: 58).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3, CDRH3, где домен, связывающий CDRH3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDAX1X2X3X4FYDX5, где X1 представляет собой T, H или Y, где X2 представляет собой G или H, где X3 представляет собой H или R, где X4 представляет собой V или Y, где X5 представляет собой V или H и где необязательно по меньшей мере один из X1, X2, X3, и X5 заменен на H (SEQ ID NO: 593).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3, CDRH3, где домен, связывающий CDRH3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность AX1DX2X3X4X5X6X7YDX8, где X1 представляет собой R или H, где X2 представляет собой H или A, где X3 представляет собой H или Y, где X4 представляет собой H, G или P, где X5 представляет собой R или H, где X6 представляет собой Y, I или V, где X7 представляет собой F или H, где X8 представляет собой V или H и где необязательно по меньшей мере один из X1, X2, X3, X4, X5, X7 и X8 заменен на H (SEQ ID NO: 596).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность X1INPX2TGX3TX4YSQKFQG, где X1 представляет собой W или Y, где X2 представляет собой A, S, D, G, N, L, V, H или Q, где X3 представляет собой A, T или S и где X4 представляет собой K, V, T, D, Y, F или A (SEQ ID NO: 10).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность X1IX2AGTGX3TX4YSQKFQG, где X1 представляет собой W, Y или F, где X2 представляет собой T, N или D, где X3 представляет собой A, T или L и где X4 представляет собой A, K, V, H, T или N (SEQ ID NO: 11).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность X1IDAGTGX2TX3YSQKFQG, где X1 представляет собой S или W, где X2 представляет собой L, N, D или F и где X3 представляет собой D, Y или K (SEQ ID NO: 12).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность X1IX2AGTGATX3YSQKFQG, где X1 представляет собой G, D или S, где X2 представляет собой I или D и где X3 представляет собой K или D (SEQ ID NO: 13).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность WINPX1TGNTX2YSQKFQG, где X1 представляет собой D, T, L, S или A и где X2 представляет собой D, V, L или N (SEQ ID NO: 14).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность X1INAGTGX2TX3YSQKFQG, где X1 представляет собой Y или W, где X2 представляет собой N, D или А и где X3 представляет собой I или V (SEQ ID NO: 15).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность X1INPX2TGX3TKYSQKFQG, где X1 представляет собой W или Y, где X2 представляет собой D, I или Y и где X3 представляет собой D, Y или Е (SEQ ID NO: 16).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность SIX1AGTGX2TKYSQKFQG, где X1 представляет собой N или V и где X2 представляет собой А или I (SEQ ID NO: 17).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность SINAGTGX1TX2YSQKFQG, где X1 представляет собой F или N и где X2 представляет собой Y или D (SEQ ID NO: 18).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность X1IX2X3GTGX4TDYSQKFQG, где X1 представляет собой D или W, где X2 представляет собой N или H, где X3 представляет собой A или S и где X4 представляет собой A или N (SEQ ID NO: 19).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность WIDPX1TGATX2YSQKFQG, где X1 представляет собой N, H или Y и где X2 представляет собой V или K (SEQ ID NO: 20).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность WIX1PX2TGNTKYSQKFQG, где X1 представляет собой D или N и где X2 представляет собой L, I или V (SEQ ID NO: 21).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность SINAGDANTKYSQKFQG (SEQ ID NO: 22).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность X1IDPX2TGATX3YSQKFQG, где X1 представляет собой D или W, где X2 представляет собой D или V и где X3 представляет собой E или D (SEQ ID NO: 23).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность WINAGDAATVYSQKFQG (SEQ ID NO: 24).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3, CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность X1IX2X3X4X5X6X7TX8YSQKFQG, где X1 представляет собой W, S, Y, F, G или D, где X2 представляет собой N, T, D, V или H, где X3 представляет собой A, P или S, где X4 представляет собой G, A, S, N, D, L, V, H, Q, T, I или Y, где X5 представляет собой D или T, где X6 представляет собой A или G, где X7 представляет собой A, N, T, S, L, D, F, Y или E, где X8 представляет собой V, K, T, D, Y, F, A, H, N, L, I или E и где необязательно по меньшей мере один из X1, X2, X3, X4, X5, X6, X7 и X8 представляет собой H (SEQ ID NO: 59).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH2, где домен, связывающий CDRH2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность WIDAGTGX1TX2YSQKFQG, где X1 представляет собой L, F, N или A и где X2 представляет собой T или K (SEQ ID NO: 595).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH1, где домен, связывающий CDRH1, содержит FNIKDYHMH (SEQ ID NO: 25), SNIKDYYMH (SEQ ID NO: 26) или SNIKDYHMH (SEQ ID NO: 27).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH1, где домен, связывающий CDRH1, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность YTFX1X2X3X4MH, где X1 представляет собой A, K, D, Q, E, N, T, L, Y, S, P, G, H или V, где X2 представляет собой T, S или A, где X3 представляет собой Y или I и где X4 представляет собой A, D, N, S, Y, T, I, V, L, E, P, R или G (SEQ ID NO: 28).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH1, где домен, связывающий CDRH1, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность YTFX1X2X3X4MH, где X1 представляет собой T, D, A, N или V, где X2 представляет собой D, E, G или Q, где X3 представляет собой Y или D и где X4 представляет собой D, A, E, N, S, Y или V (SEQ ID NO: 29).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH1, где домен, связывающий CDRH1, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность YTFTSX1X2MH, где X1 представляет собой A, D или T и где X2 представляет собой D, F, A, M, V или Y (SEQ ID NO: 30).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH1, где домен, связывающий CDRH1, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность YTFX1X2YX3MH, где X1 представляет собой N или T, X2 представляет собой Q или N, а X3 представляет собой S, T или A (SEQ ID NO: 31).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH1, где домен, связывающий CDRH1, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность YTFX1X2YVMH, где X1 представляет собой I или N и где X2 представляет собой K или R (SEQ ID NO: 32).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH1, где домен, связывающий CDRH1, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность FNIKDYYMH (SEQ ID NO: 47).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRH1, где домен, связывающий CDRH1, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность YTFX1X2YX3MH, где X1 представляет собой E, S или T, где X2 представляет собой S или D и где X3 представляет собой A или D (SEQ ID NO: 31).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRL3, где домен, связывающий CDRL3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность X1X2SX3X4X5RX6, где X1 представляет собой H, K или G, где X2 или Q или H, где X3 представляет собой Y или H, где X4 представляет собой S, H, D, T, V, M, или L, где X5 представляет собой R или H, где X6 представляет собой T или H и где необязательно по меньшей мере один из X1, X2, X3, X4, X5 и X6 заменен на H (SEQ ID NO: 33).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRL3, где домен, связывающий CDRL3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность KQSYX1X2RT, где X1 представляет собой H, V, K, W, R, L, G, Y или Q, где X2 представляет собой H, L, E, W, G, M, P, T, Q или V и где необязательно по меньшей мере один из X1 и X2 заменен на H (SEQ ID NO: 34).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRL3, где домен, связывающий CDRL3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность X1QSX2HX3RT, где X1 представляет собой K или H, где X2 представляет собой H, Y, M, S, L, E, G или W, где X3 представляет собой R или K и где необязательно по меньшей мере один из X1 и X2 заменен на H (SEQ ID NO: 35).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRL3, где домен, связывающий CDRL3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность KQSX1X2X3RT, где X1 представляет собой Y или H, X2 представляет собой T, S, V или K, X3 представляет собой R или H и где необязательно по меньшей мере один из X1 и X3 заменен на H (SEQ ID NO: 36).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRL3, где домен, связывающий CDRL3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность KQSX1X2X3RT, где X1 представляет собой H или Y, где X2 представляет собой T, S или Q, где X3 представляет собой R или H и где необязательно по меньшей мере один из X1 и X3 заменен на H (SEQ ID NO: 36).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRL3, где домен, связывающий CDRL3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность X1QSX2X3X4RT, где X1 представляет собой K или H, где X2 представляет собой Y или H, где X3 представляет собой S, H, L, V или K, где X4 представляет собой H, R или E и где необязательно по меньшей мере один из X1, X2, X3 и X4 заменен на H (SEQ ID NO: 598).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRL2, где домен, связывающий CDRL2, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность WASTRES (SEQ ID NO: 37).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRL1, где домен, связывающий CDRL1, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность KSSQSLLX1X2X3X4GX5NX6LA, где X1 представляет собой N или H, где X2 представляет собой A, R или T, где X3 представляет собой R или H, где X4 представляет собой T, P или E, где X5 представляет собой H или K, где X6 представляет собой H или Y и где необязательно по меньшей мере один из X1, X3, X5 и X6 заменен на H (SEQ ID NO: 38).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRL1, где домен, связывающий CDRL1, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность KSSQSLLX1AX2THX3NX4LA, где X1 представляет собой N или H, где X2 представляет собой R или H, где X3 представляет собой K или H, где X4 представляет собой Y или H и где необязательно по меньшей мере один из X1, X2, X3 и X4 заменен на H (SEQ ID NO: 39).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRL1, где домен, связывающий CDRL1, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность KSSQSLLNASTAKNYLA (SEQ ID NO: 40) или KSSQSLLNARTRTNYLA (SEQ ID NO: 41).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRL1, где домен, связывающий CDRL1, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность KSSQSLLNX1X2X3GX4NX5LA, где X1 представляет собой S или A, где X2 представляет собой R или H, где X3 представляет собой E или T, где X4 представляет собой H или K, где X5 представляет собой H или Y, и где необязательно по меньшей мере один из X2, X4, X4 и X5 заменен на H (SEQ ID NO: 42).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRL1, где домен, связывающий CDRL1, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность KSSQSLLNX1X2TGX3NYLA, где X1 представляет собой A или S, где X2 представляет собой R или H, где X3 представляет собой H или K и где необязательно по меньшей мере один из X2 и X3 заменен на H (SEQ ID NO: 594).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3 CDRL1, где домен, связывающий CDRL1, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность KSSQSLLX1AX2X3X4X5NX6LA, где X1 представляет собой N или H, где X2 представляет собой R или Н, где X3 представляет собой T или E, где X4 представляет собой G или H, где X5 представляет собой H или K, где X6 представляет собой H или Y и где необязательно по меньшей мере один из X1, X2, X4, X5 и X6 заменен на H (SEQ ID NO: 597).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело или антигенсвязывающий фрагмент, содержащее домен, связывающий CDRH3, который содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDAX1X2X3X4FYDX5, где X1 представляет собой T, H или Y, где X2 представляет собой G или H, где X3 представляет собой H или R, где X4 представляет собой V или Y, где X5 представляет собой V или H и где необязательно по меньшей мере один из X1, X2, X3, и X5 представляет собой H (SEQ ID NO: 593); домен, связывающий CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9); домен, связывающий CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность FNIKDYYMH (SEQ ID NO: 47); домен, связывающий CDRL3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность KQSX1X2X3RT, где X1 представляет собой H или Y, где X2 представляет собой T, S или Q, где X3 представляет собой R или H и где необязательно по меньшей мере один из X1 и X3 представляет собой H (SEQ ID NO: 36); домен, связывающий CDRL2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WASTRES (SEQ ID NO: 37); и/или домен, связывающий CDRL1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность KSSQSLLNX1X2TGX3NYLA, где X1 представляет собой A или S, где X2 представляет собой R или H, где X3 представляет собой H или K и где необязательно по меньшей мере один из X2 и X3 представляет собой H (SEQ ID NO: 594). В некоторых вариантах осуществления указанное антитело или антигенсвязывающий фрагмент обозначают как связывающую молекулу группы 1, содержащую домен, связывающий CD3, выбранный из ADI-48592, ADI-48595, ADI-48650, ADI-48652, ADI-48662 и ADI-48666.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело или антигенсвязывающий фрагмент, содержащие домен, связывающий CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность AX1DX2X3X4X5X6X7YDX8, где X1 представляет собой R или H, где X2 представляет собой H или A, где X3 представляет собой H или Y, где X4 представляет собой H, G или P, где X5 представляет собой R или H, где X6 представляет собой Y, I или V, где X7 представляет собой F или H, где X8 представляет собой V или H и необязательно где по меньшей мере один из X1, X2, X3, X4, X5, X7, и X8 представляет собой H (SEQ ID NO: 596); домен, связывающий CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9) или последовательность WIDAGTGX1TX2YSQKFQG, где X1 представляет собой L, F, N или A, и где X2 представляет собой T или K (SEQ ID NO: 595); домен, связывающий CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность FNIKDYYMH (SEQ ID NO: 47) или последовательность YTFX1X2YX3MH, где X1 представляет собой E, S или T, где X2 представляет собой S или D и где X3 представляет собой A или D (SEQ ID NO: 31); домен, связывающий CDRL3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность X1QSX2X3X4RT, где X1 представляет собой K или H, где X2 представляет собой Y или H, где X3 представляет собой S, H, L, V или K, где X4 представляет собой H, R или E и необязательно где по меньшей мере один из X1, X2, X3 и X4 представляет собой H (SEQ ID NO: 598); домен, связывающий CDRL2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WASTRES (SEQ ID NO: 37); домен, связывающий CDRL1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность KSSQSLLX1X2X3X4GX5NX6LA, где X1 представляет собой N или H, где X2 представляет собой R или Н, где X3 представляет собой T или E, где X4 представляет собой G или H, где X5 представляет собой H или K, где X6 представляет собой H или Y и где необязательно по меньшей мере один из X1, X2, X4, X5 и X6 представляет собой H (SEQ ID NO: 597). В некоторых вариантах осуществления указанное антитело или антигенсвязывающий фрагмент обозначают как связывающую молекулу группы 2, содержащую домен, связывающий CD3, выбранный из ADI-48588, ADI-48587, ADI-48577, ADI-48590, ADI-48581, ADI-48575, ADI-48593, ADI-48591, ADI-48647, ADI-48636, ADI-48586, ADI-48646, ADI-48638, ADI-48597, ADI-48601, ADI-48576, ADI-48643, ADI-48624, ADI-48632, ADI-48635 и ADI-48645.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело к CD3 или антигенсвязывающий фрагмент, описанные в настоящем документе, где указанные антитело или антигенсвязывающий фрагмент могут вызывать активацию Т-клеток или их уничтожение, демонстрируя при этом сниженную предрасположенность к вызову продуцирования цитокинов до уровней, способных индуцировать синдром высвобождения цитокинов.
В некоторых вариантах осуществления в настоящем изобретении представлены описанные в данном документе антитело или антигенсвязывающий фрагмент к CD3, где указанные антитело или антигенсвязывающий фрагмент могут включать мультиспецифическое антитело.
В некоторых вариантах осуществления в настоящем изобретении представлены описанные в данном документе антитело или антигенсвязывающий фрагмент к CD3, где указанные антитело или антигенсвязывающий фрагмент могут включать биспецифическое антитело.
В некоторых вариантах осуществления в настоящем изобретении представлены описанные в данном документе антитело или антигенсвязывающий фрагмент к CD3, где указанные антитело или антигенсвязывающий фрагмент могут включать scFv.
В некоторых вариантах осуществления в настоящем изобретении представлены описанные в данном документе антитело или антигенсвязывающий фрагмент к CD3, где указанные антитело или антигенсвязывающий фрагмент могут включать по меньшей мере второй антигенсвязывающий фрагмент, который специфически связывается с целевым антигеном онкологического заболевания; целевым антигеном иммуноонкологического заболевания; целевым антигеном нейродегенеративного заболевания; целевым антигеном аутоиммунного нарушения; целевым антигеном инфекционного заболевания; целевым антигеном метаболического заболевания; целевым антигеном когнитивного нарушения; целевым антигеном гематоэнцефалического барьера; или целевым антигеном заболевания крови.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело или антигенсвязывающий фрагмент к CD3, описанные в настоящем документе, где указанные антитело или антигенсвязывающий фрагмент могут содержать по меньшей мере второй антигенсвязывающий домен, который специфически связывается с антигеном, выбранным из группы, состоящей из 17-IA, 4-1BB, 4Dc, 6-кето-PGFla, 8-изо-PGF2a, 8-оксо-dG, Al-аденозинового рецептора, A33, ACE, ACE-2, с, активина A, активина AB, активина B, активина C, активина RIA, активина RIA ALK-2, активина RIB ALK-4, активина RIIA, активина RUB, ADAM, ADAM10, ADAM12, ADAM 15, ADAM 17/T ACE, ADAM8, ADAM9, ADAMTS, ADAMTS4, ADAMTS5, адресинов, aFGF, ALCAM, ALK, ALK-1, ALK-7, альфа-1-антитрипсина, антагониста альфа-V/бета-1, ANG, Ang, APAF-1, APE, APJ, APP, APRIL, AR, ARC, ART, артемина, антиидиотипа, аспарагиновой кислоты, предсердного натрийуретического фактора, интегрина av/b3, Axl, b2M, B7-1, B7-2, B7-H, стимулятора B-лимфоцитов (BlyS), BACE, BACE-1, Bad, BAFF, BAFF-R, Bag-1, BAK, Bax, BCA-1, BCAM, Bel, BCMA, BDNF, b-ECGF, bFGF, BID, Bik, BFM, BLC, BL-CAM, BLK, BMP, BMP-2 BMP-2a, BMP-3-остеогенина, BMP-4 BMP-2b, BMP-5, BMP-6 Vgr-1, BMP-7 (OP-1), BMP-8 (BMP-8a, OP-2), BMPR, BMPR-IA (ALK-3), BMPR-IB (ALK-6), BRK-2, RPK-1, BMPR-II (BRK-3), видов BMP, b-NGF, BOK, бомбезина, костного нейротрофического фактора, BPDE, BPDE-DNA, BTC, фактора комплемента 3 (C3), C3a, C4, C5, C5a, CIO, CA125, CAD-8, кальцитонина, cAMP, раково-эмбрионального антигена (CEA), антигена, ассоциированного с карциномой, катепсина A, катепсина B, катепсина C/DPPI, катепсина D, катепсина E, катепсина H, катепсина L, катепсина O, катепсина S, катепсина V, катепсина X/Z/P, CBL, CCI, CCK2, CCL, CCL1, CCL11, CCL12, CCL13, CCL 14, CCL15, CCL16, CCL17, CCL18, CCL19, CCL2, CCL20, CCL21, CCL22, CCL23, CCL24, CCL25, CCL26, CCL27, CCL28, CCL3, CCL4, CCL5, CCL6, CCL7, CCL8, CCL9/10, CCR, CCR1, CCR10, CCR10, CCR2, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CD1, CD2, CD4, CD5, CD6, CD7, CD8, CD10, CDlla, CDllb, CDllc, CD13, CD14, CD15, CD16, CD18, CD19, CD20, CD21, CD22, CD23, CD25, CD27L, CD28, CD29, CD30, CD30L, CD32, CD33 (белки p67), CD34, CD38, CD40, CD40L, CD44, CD45, CD46, CD49a, CD52, CD54, CD55, CD56, CD61, CD64, CD66e, CD74, CD80 (B7-1), CD89, CD95, CD123, CD137, CD138, CD140a, CD146, CD147, CD148, CD152, CD164, CEACAM5, CFTR, cGMP, CINC, токсина Clostridium botulinum, токсина Clostridium perfringens, CKb8-l, CLC, CMV, CMV UL, CNTF, CNTN-1, COX, C-Ret, CRG-2, CT-1, CTACK, CTGF, CTLA-4, CX3CL1, CX3CR1, CXCL, CXCL1, CXCL2, CXCL3, CXCL4, CXCL5, CXCL6, CXCL7, CXCL8, CXCL9, CXCL10, CXCL11, CXCL12, CXCL13, CXCL14, CXCL15, CXCL16, CXCR, CXCR1, CXCR2, CXCR3, CXCR4, CXCR5, CXCR6, цитокератинового опухолеассоциированного антигена, DAN, DCC, DcR3, DC-SIGN, фактора ускорения распада, des(l-3)-IGF-I (IGF-1 головного мозга), Dhh, дигоксина, DNAM-1, ДНКазы, Dpp, DPPIV/CD26, Dtk, ECAD, EDA, EDA-A1, EDA-A2, EDAR, EGF, EGFR (ErbB-1), EMA, EMMPRIN, EN A, рецептора эндотелина, энкефалиназы, eNOS, Eot, эотаксина-1, EpCAM, эфрина B2/ EphB4, EPO, ERCC, E-селектина, ET-1, фактора Ila, фактора VII, фактора VIIIc, фактора IX, белка активации фибробластов (FAP), Fas, FcRl, FEN-1, ферритина, FGF, FGF-19, FGF-2, FGF3, FGF-8, FGFR, FGFR-3, фибрина, FL, FLIP, Flt-3, Flt-4, фолликулостимулирующего гормона, фракталкина, FZD1, FZD2, FZD3, FZD4, FZD5, FZD6, FZD7, FZD8, FZD9, FZD10, G250, Gas 6, GCP-2, GCSF, GD2, GD3, GDF, GDF-1, GDF-3 (Vgr-2), GDF-5 (BMP-14, CDMP- 1), GDF-6 (BMP-13, CDMP-2), GDF-7 (BMP-12, CDMP-3), GDF-8 (миостатин), GDF-9, GDF- 15 (MIC-1), GDNF, GFAP, GFRa-1, GFR-альфа-1, GFR-альфа-2, GFR-альфа-3, GITR, глюкагона, Glut 4, гликопротеина Ilb/IIIa (GP Ilb/IIIa), GM-CSF, gpl30, gp72, GRO, рилизинг-фактора гормона роста, гаптена (NP-cap или NIP-cap), HB-EGF, HCC, гликопротеина gB оболочки HCMV, гликопротеина gH оболочки HCMV, HCMV UL, гемопоэтического фактора роста (HGF), Hep B gpl20, гепараназы, Her2, Her2/neu (ErbB-2), Her3 (ErbB-3), Her4 (ErbB-4), гликопротеина gB вируса простого герпеса (HSV), гликопротеина gD HSV, HGFA, высокомолекулярного ассоциированного с меланомой антигена (HMW-MAA), gpl20 ВИЧ, V3-петли gp 120 ВИЧ IIIB, HLA, HLA-DR, HM1.24, HMFG PEM, HRG, Hrk, сердечного миозина человека, цитомегаловируса (HCMV) человека, гормона роста человека (HGH), HVEM, 1-309, IAP, ICAM, ICAM-1, ICAM-3, ICE, ICOS, IFNg, Ig, рецептора IgA, IgE, IGF, IGF-связывающих белков, IGF-1R, IGFBP, IGF-I, IGF-II, IL, IL-1, IL-1R, IL-2, IL-2R, IL-4, IL-4R, IL-5, IL-5R, IL-6, IL-6R, IL-8, IL- 9, IL-10, IL-12, IL-13, IL-15, IL-18, IL-18R, IL-23, интерферона (INF)-альфа, INF-бета, INF-гамма, ингибина, iNOS, A-цепи инсулина, B-цепи инсулина, инсулиноподобного фактора роста 1, интегрина-альфа-2, интегрина-альфа-3, интегрина-альфа-4, интегрина-альфа-4/бета-1, интегрина-альфа-4/бета-7, интегрина-альфа-5 (альфа-V), интегрина-альфа-5/бета-1, интегрина-альфа-5/бета-3, интегрина-альфа-6, интегрина-бета-1, интегрина-бета-2, интерферона-гамма, IP-10, 1-TAC, JE, калликреина 2, калликреина 5, калликреина 6, калликреина 11, калликреина 12, калликреина 14, калликреина 15, калликреина L1, калликреина L2, калликреина L3, калликреина L4, KC, KDR, фактора роста кератиноцитов (KGF), ламинина 5, LAMP, LAP, LAP (TGF-1), латентного TGF-1, латентного TGF-1 bpl, LBP, LDGF, LECT2, Lefty, антигена Льюиса Y, антигена, родственного антигену Льюиса Y, LFA-1, LFA-3, Lfo, LIF, LIGHT, липопротеинов, LIX, LKN, Lptn, L-селектина, LT-a, LT-b, LTB4, LTBP-1, легочного сурфактанта, лютеинизирующего гормона, рецептора лимфотоксина-бета, Mac-1, MAdCAM, MAG, MAP2, MARC, MCAM, MCAM, MCK-2, MCP, M-CSF, MDC, Mer, металлопротеазы, рецептора MGDF, MGMT, MHC (HLA-DR), MIF, MIG, MIP, MIP-1-альфа, MK, MMAC1, MMP, MMP-1, MMP-10, MMP-11, MMP-12, MMP-13, MMP-14, MMP-15, MMP-2, MMP-24, MMP-3, MMP-7, MMP-8, MMP-9, MPIF, Mpo, MSK, MSP, муцина (Mucl), MUC18, ингибирующего вещества Мюллера, Mug, MuSK, NAIP, NAP, NCAD, N-кадгерина, NCA 90, NCAM, NCAM, неприлизина, нейротрофина-3,-4 или -6, нейротурина, фактора роста нейронов (NGF), NGFR, NGF-бета, nNOS, NO, NOS, Npn, NRG-3, NT, NTN, OB, OGG1, OPG, OPN, OSM, OX40L, OX40R, pl50, p95, PADPr, паратиреоидного гормона, PARC, PARP, PBR, PBSF, PCAD, P-кадгерина, PCNA, PDGF, PDGF, PDK-1, PECAM, PEM, PF4, PGE, PGF, PGI2, PGJ2, PIN, PLA2, плацентарной щелочной фосфатазы (PLAP), PIGF, PLP, PP14, проинсулина, прорелаксина, белка C, PS, PSA, PSCA, простатического специфического мембранного антигена (PSMA), PTEN, PTHrp, Ptk, PTN, R51, RANK, RANKL, RANTES, A-цепи релаксина, B-цепи релаксина, ренина, респираторно-синцитиального вируса F (RSV), RSV Fgp, Ret, ревматоидных факторов, RLIP76, RPA2, RSK, S100, SCF/KL, SDF-1, серина, сывороточного альбумина, sFRP-3, Shh, SIGIRR, SK-1, SLAM, SLPI, SMAC, SMDF, SMOH, SOD, SPARC, Stat, STEAP, STEAP-II, TACE, TACI, TAG-72 (опухолеассоциированный гликопротеин-72), TARC, TCA-3, T-клеточных рецепторов (например, T-клеточного рецептора альфа/бета), TdT, TECK, TEM1, TEM5, TEM7, TEM8, TERT, PLAP-подобной щелочной фосфатазы семенников, TfR, TGF, TGF-альфа, TGF-бета, панспецифического TGF-бета, TGF-бета RI (ALK-5), TGF-бета RII, TGF-бета Rllb, TGF-бета RIII, TGF-бета 1, TGF-бета 2, TGF-бета 3, TGF-бета 4, TGF-бета 5, тромбина, тимусного Ck-1, тиреостимулирующего гормона, Tie, TIMP, TIQ, тканевого фактора, TMEFF2, Tmpo, TMPRSS2, TNF, TNF-альфа, TNF-альфа/бета, TNF-бета 2, TNFc, TNF-RI, TNF-RII, TNFRSF10A (TRAIL Rl Apo-2, DR4), TNFRSFIOB (TRAIL R2 DR5, KILLER, TRICK-2A, TRICK-B), TNFRSF10C (TRAIL R3 DcRl, LIT, TRID), TNFRSF10D (TRAIL R4 DcR2, TRUNDD), TNFRSF11A (RANK ODF R, TRANCE R), TNFRSFllB (OPG OCIF, TR1), TNFRSF12 (TWEAK R FN14), TNFRSF13B (TACI), TNFRSF13C (BAFF R), TNFRSF14 (HVEM ATAR, HveA, LIGHT R, TR2), TNFRSF16 (NGFR p75NTR), TNFRSF17 (BCMA), TNFRSF 18 (GITR AITR), TNFRSF19 (TROY TAJ, TRADE), TNFRSF19L (RELT), TNFRSFIA (TNF RI CD120a, p55-60), TNFRSFIB (TNF RII CD120b, p75-80), TNFRSF26 (TNFRH3), TNFRSF3 (LTbR TNF RIII, TNFC R), TNFRSF4 (OX40 ACT35, TXGP1 R), TNFRSF 5 (CD40 p50), TNFRSF6 (Fas Apo-1, APT1, CD95), TNFRSF6B (DcR3 M68, TR6), TNFRSF7 (CD27), TNFRSF8 (CD30), TNFRSF9 (4-1BB CD137, ILA), TNFRSF21 (DR6), TNFRSF22 (DcTRAIL R2 TNFRH2), TNFRST23 (DcTRAIL Rl TNFRH1), TNFRSF25 (DR3 Apo-3, LARD, TR-3, TRAMP, WSL-1), TNFSF10 (TRAIL, лиганд Apo-2, TL2), TNFSF11 (TRANCE/RANK, лиганд ODF, лиганд OPG), TNFSF12 (TWEAK лиганд Apo-3, лиганд DR3), TNFSF13 (APRIL TALL2), TNFSF13B (BAFF BLYS, TALL1, THANK, TNFSF20), TNFSF14 (LIGHT, лиганд HVEM, LTg), TNFSF15 (TLIA/VEGI), TNFSF18 (лиганд GITR, лиганд AITR, TL6), TNFSFIA (конектин TNF-a, DIF, TNFSF2), TNFSF1B (TNF-b, LTa, TNFSF1), TNFSF3 (LTb, TNFC, p33), TNFSF4 (лиганд OX40, gp34, TXGP1), TNFSF5 (лиганд CD40, CD154, gp39, HIGM1, IMD3, TRAP), TNFSF6 (лиганд Fas, лиганд Apo-1, лиганд APT1), TNFSF7 (лиганд CD27 CD70), TNFSF8 (лиганд CD30 CD153), TNFSF9 (лиганд 4-1BB, лиганд CD137), TP-1, t-PA, Tpo, TRAIL, TRAIL R, TRAIL-R1, TRAIL-R2, TRANCE, рецептора трансферрина, TRF, Trk, TROP-2, TSG, TSLP, опухолеассоциированного антигена CA 125, опухолеассоциированного антигена, экспрессирующего углевода, родственного антигену Льюиса Y, TWEAK, TXB2, Ung, uPAR, uPAR-1, урокиназы, VCAM, VCAM-1, VECAD, VE-кадгерина, VE-кадгерина-2, VEFGR-1 (flt-1), VEGF, VEGFR, VEGFR-3 (flt-4), VEGI, VFM, вирусных антигенов, VLA, VLA-1, VLA-4, интегрина VNR, факторов фон Виллебранда, WIF- 1, WNT1, WNT2, WNT2B/13, WNT3, WNT3A, WNT4, WNT5A, WNT5B, WNT6, WNT7A, WNT7B, WNT8A, WNT8B, WNT9A, WNT9A, WNT9B, WNT10A, WNT10B, WNT11, WNT16, XCL1, XCL2, XCR1, XCR1, XEDAR, XIAP, XPD, CTLA4 (антиген-4 цитотоксических T-лимфоцитов), PD1 (белок-1 запрограммированной гибели клеток), PD-L1 (лиганд-1 белка запрограммированной гибели клеток), LAG-3 (ген-3 активации лимфоцитов), TIM-3 (белок-3, содержащий домены T-клеточного иммуноглобулина и муцина), рецепторов гормонов и факторов роста.
В некоторых вариантах осуществления в настоящем изобретении представлены описанные в данном документе антитело или антигенсвязывающий фрагмент к CD3, где указанные антитело или антигенсвязывающий фрагмент могут содержать по меньшей мере второй антигенсвязывающий домен, который специфически связывается с антигеном, выбранным из группы, состоящей из BCMA, CTLA4 (антиген-4 цитотоксических T-лимфоцитов), PD1 (белок-1 запрограммированной гибели клеток), PD-L1 (лиганд-1 белка запрограммированной гибели клеток), LAG-3 (ген-3 активации лимфоцитов), TIM-3, CD20, CD2, CD19, Her2, EGFR, EpCAM, FcyRIIIa (CD16), FcyRIIa (CD32a), FcyRIIb (CD32b), FcyRI (CD64), Toll-подобных рецепторов (TLR), TLR4, TLR9, цитокинов, IL-2, IL-5, IL-13, IL-6, IL-17, IL-12, IL-23, TNFa, TGFb, цитокиновых рецепторов, IL-2R, хемокинов, хемокиновых рецепторов, факторов роста, VEGF и HGF.
В некоторых вариантах осуществления в настоящем изобретении представлены антитело или антигенсвязывающий фрагмент к CD3, описанные в настоящем документе, где указанные антитело или антигенсвязывающий фрагмент могут содержаться в химерном антигенном рецепторе (CAR), который необязательно может содержать по меньшей мере один трансмембранный домен и по меньшей мере один внутриклеточный домен Т-клеточного рецептора, необязательно субъединицу CD3ζ и по меньшей мере один костимулирующий домен.
В некоторых вариантах осуществления в настоящем изобретении представлены описанные в данном документе антитело или антигенсвязывающий фрагмент к CD3, где указанные антитело или антигенсвязывающий фрагмент могут включать scFv2-Fc2 и/или scFv-IgG.
В некоторых вариантах осуществления в настоящем изобретении представлены описанные в данном документе антитело или антигенсвязывающий фрагмент к CD3, где указанные антитело или антигенсвязывающий фрагмент могут содержать константный домен IgG.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело или антигенсвязывающий фрагмент к CD3, описанные в настоящем документе, где указанные антитело или антигенсвязывающий фрагмент могут содержать по меньшей мере второй антигенсвязывающий домен, который специфически связывается с антигеном, выбранным из группы, состоящей из Fab-Fc-scFv, «открывалки для бутылок», Mab-scFv, Mab-Fv, двойного scFv, центрального Fv, центрального scFv, одноплечевого центрального scFv, Fab-Fab, Fab-Fv, mAb-Fv, mAb-Fab, DART, BiTE, IgG с универсальной легкой цепью, TandAb, Cross-Mab, SEED, BEAT, TrioMab и DuetMab.
В некоторых вариантах осуществления в описании представлена выделенная или рекомбинантная последовательность нуклеиновой кислоты, кодирующая антитело или антигенсвязывающий фрагмент к CD3, описанные в данном документе.
В некоторых вариантах осуществления в описании представлен вектор экспрессии, содержащий выделенную или рекомбинантную последовательность нуклеиновой кислоты, кодирующую антитело или антигенсвязывающий фрагмент к CD3, описанные в данном документе.
В некоторых вариантах осуществления настоящего изобретения представлена клетка-хозяин, трансфицированная, трансформированная или трансдуцированная последовательностью нуклеиновой кислоты, кодирующей антитело или антигенсвязывающий фрагмент к CD3, описанные в данном документе, или вектор экспрессии, содержащий выделенную или рекомбинантную последовательность нуклеиновой кислоты, кодирующую антитело или антигенсвязывающий фрагмент к CD3, описанные в настоящем документе, где клетка-хозяин необязательно может быть клеткой млекопитающего или дрожжевой клеткой.
В некоторых вариантах осуществления в настоящем изобретении представлена фармацевтическая композиция, содержащая антитело или антигенсвязывающий фрагмент, описанные в данном документе, или клетка-хозяин, описанная в данном документе, и фармацевтически приемлемый носитель и/или вспомогательное вещество.
В некоторых вариантах осуществления в настоящем изобретении представлен способ лечения нарушения у млекопитающего, нуждающегося в таком лечении, где нарушение может включать пролиферативное нарушение, онкологическое нарушение, иммуноонкологическое нарушение, неврологическое нарушение, нейродегенеративное нарушение или аутоиммунное заболевание, и где способ может предусматривать введение эффективного количества по меньшей мере одного антитела или антигенсвязывающего фрагмента, описанных в данном документе, или клетки-хозяина, которая экспрессирует по меньшей мере одно из указанных антитела или антигенсвязывающего фрагмента, описанных в данном документе, необязательно иммунной клетки, кроме того необязательно T- или NK-клетки. В некоторых вариантах осуществления способ может дополнительно предусматривать введение млекопитающему дополнительного терапевтического средства, необязательно при этом млекопитающее является человеком.
В других вариантах осуществления настоящего изобретения представлены антитело к CD3 или его антигенсвязывающий фрагмент, содержащие один или несколько из CDRL1, CDRL2 и CDRL3. Такое антитело в некоторых вариантах осуществления дополнительно содержит CDRH1, CDRH2 и CDRH3.
Краткое описание графических материалов
На фиг. 1А и фиг. 1В показаны способы предварительного насыщения 1 и 2. Фиг. 1A. Способ предварительного насыщения CD3 №1. Дрожжевые клетки предварительно насыщали нативным (небиотинилированным) антигеном CD3 при pH 7,4 в течение 10 минут и дрожжевые клетки промывали при pH 7,4, а затем инкубировали в среде с pH 6,0 в течение 10 минут для обеспечения диссоциации антигена. Контрольные клетки промывали и инкубировали при pH 7,4. Наконец, дрожжевые клетки инкубировали с биотинилированным антигеном CD3 (показано зеленым кружком, отмеченным звездочкой) при pH 6 в течение 10 минут. Контрольные клетки инкубировали с биотинилированным антигеном CD3 при pH 7,4. Связывающие молекулы, меченные при pH 6, затем подвергали сортировке и определению характеристик. Фиг. 1B. Способ предварительного насыщения CD3 № 2. Дрожжевые клетки предварительно насыщали нативным антигеном CD3 при pH 6,0 в течение 10 минут, и промывали при pH 6,0, и инкубировали либо при pH 7,4, либо при pH 6,0 в течение 10 минут. Наконец, дрожжевые клетки инкубировали с биотинилированным антигеном CD3 при противоположном pH (клетки, инкубированные при pH 6,0 на предыдущем этапе, инкубировали при pH 7,4, тогда как клетки, инкубированные при pH 7,4 на предыдущем этапе, инкубировали при pH 6,0) в течение 10 минут. Затем связывающие молекулы, меченные биотинилированным антигеном CD3, подвергали сортировке и определению характеристик.
На фиг. 2 показаны иллюстративные графики FACS для выборок раунда 1 и раунда 2 из одной библиотеки. Аналогичные профили связывания наблюдали для всех библиотек. Вкратце, во время раунда 1 клетки положительно сортировали с использованием 100 нМ гетеродимера CD3εδ человека (HuCD3-hd) при pH 6. Во время раунда 2 клетки положительно сортировали с использованием 100 нМ HuCD3-hd при pH 6,0, отрицательно отсортировали с использованием 100 нМ HuCD3-hd при pH 7,4 или предварительно насыщали с использованием способа № 2, описанного выше. Связывание также подтверждали для CD3 яванского макака (CyCD3-hd) при pH 6,0. Стрелки указывают на отсортированные клетки, которые были перенесены на следующий раунд сортировки.
На фиг. 3 показаны иллюстративные графики FACS из раунда 3 и сравниваются входные данные для положительных значений pH 6,0 и отрицательных значений pH 7,4 из раунда 2. Вкратце, виды из раунда 2 инкубировали со 100 нМ HuCD3-hd при pH 6,0 и 7,4. Совмещенный столбец показывает, что вводная популяция клеток (из видов раунда 2) демонстрирует более высокое связывание при pH 6,0 по сравнению с pH 7,4. Для переноса клеток в следующие раунды отбора применяли способ № 2 предварительного насыщения/переключения.
На фиг. 4 показаны иллюстративные графики FACS из раунда 4 и раунда 5. В раунде 4 сравнивали клетки, инкубированные в 100 нМ HuCD3-hd при pH 6 и pH 7,4. В раунде 4 также сравнивали клетки, подвергнутые способу предварительного насыщения/переключения при pH 6 и pH 7,4. В раунде 5 сравнивали клетки, инкубированные либо в 100 нМ HuCD3-hd, либо в 100 нМ CyCD3-hd при pH 6 (красный) и pH 7,4 (серый).
На фиг. 5A и 5B показан ответ связывания HuCD3. На фиг. 5A показан ответ связывания HuCD3 при pH 6 (ось x) по сравнению с ответом связывания HuCD3 при pH 7,4 (ось y) для 236 уникальных клонов из результатов сортировки в ходе раунда 2/3. На фиг. 5B показаны значения KD для HuCD3 при pH 6 (ось x) по сравнению с HuCD3 при pH 7,4 (ось y) для 236 уникальных клонов из результатов сортировки в ходе раунда 2/3. Синие кружки представляют клоны из раунда 2/3, полученные с помощью сортировки с предварительным насыщением/переключением pH 6,0, желтые кружки представляют клоны из раунда 2/3, полученные с помощью отрицательной сортировки с pH 7,4, а красные кружки представляют исходный клон ADI-26906. Результаты показывают, что виды отрицательной сортировки при pH 7,4 в раунде 2/3 имеют тенденцию давать больше селективных при pH связывающих молекул, но с более слабым ответом или аффинностью при pH 6,0, которые обозначены как связывающие молекулы группы 2. Положительный отбор при pH 6,0 и сортировка с предварительным насыщением/переключением давали клоны со смешанной селективностью, но с более высоким ответом/аффинностью. Такие клоны с более высокой аффинностью при pH 6,0 (например, KD <~ 25 нМ) обозначают как связывающие молекулы группы 1.
На фиг. 6 представлены иллюстративные результаты кинетики экспериментов ForteBio для четырех клонов по сравнению с исходным клоном ADI-26906. KD для каждого клона рассчитывали при pH 7,4 и pH 6,0. Отношение KD получали путем деления KD при pH 7,4 на KD при pH 6,0. Примеры демонстрируют, что некоторые клоны, обозначенные как связывающие молекулы группы 1, такие как SAD10318_P02_A05 (ADI-48595) и SAD10318_P02_C04 (ADI-48592), связываются сильнее (с более низкой KD) при pH 6,0 по сравнению с pH 7,4. Некоторые клоны, обозначенные как связывающие молекулы группы 2, такие как SAD10318_P01_A03 (ADI-48587) и SAD10318_P01_E01 (ADI-48577), не характеризовались связыванием при pH 7,4, при этом характеризовались связыванием при pH 6,0. Аминокислотные замены в областях CDRH3, CDRL1 и CDRL3, которые могут способствовать дифференциальному связыванию, выделены в столбце «последовательность» на фиг. 6 (SEQ ID NO: 576-590 соответственно, в порядке появления). Клоны, такие как ADI-48576, ADI-48577, ADI-48587, ADI-48592, ADI-48595, ADI-48635, ADI-48650, ADI-48652, ADI-48666, ADI-48643 и ADI-48645, демонстрируют pH-зависимое связывание (с более сильным связыванием при pH 6,0 по сравнению со связыванием при pH 7,4), низкие показатели PSR и обеспечивают диапазон аффинности к CD3.
Подробное описание изобретения
Если не определено иное, то все технические и научные термины, используемые в данном документе, имеют такое же значение, которое обычно понятно рядовому специалисту в области техники, к которой относится настоящее изобретение. Используемый в данном документе термин «приблизительно» при использовании в отношении конкретного указанного числового значения означает, что данное значение может отличаться от указанного значения не более чем на 1%. Например, используемое в данном документе выражение «приблизительно 100» включает 99 и 101 и все значения между ними (например, 99,1, 99,2, 99,3, 99,4 и т.д.).
Следует понимать, что аспекты и варианты осуществления настоящего изобретения, описанного в данном документе, включают «содержащий», «состоящий» и «фактически состоящий из» аспектов и вариантов осуществления.
В настоящем документе представлены антитела к CD3 и их антигенсвязывающие фрагменты, которые характеризуются pH-зависимым связыванием и благоприятными профилями разрабатываемости.
«Кластер дифференцировки 3» или «CD3» в целом относится к любому нативному CD3 из любого позвоночного, включая млекопитающих, таких как приматы (например, люди) и грызуны (например, мыши и крысы), если не указано иное, включая, например, цепи CD3ε, CD3γ, CD3α и CD3β. Данный термин охватывает «полноразмерный», непроцессированный CD3 (например, непроцессированный или немодифицированный CD3ε или CD3γ), а также любую форму CD3, которая возникает в результате процессинга в клетке. Данный термин также охватывает встречающиеся в природе варианты CD3, в том числе, например, сплайс-варианты или аллельные варианты. CD3 включает, например, белок CD3ε человека (№ эталонной последовательности в NCBI NP-000724), длина которого составляет 207 аминокислот, и белок CD3γ человека (№ эталонной последовательности в NCBI NP-000064), длина которого составляет 182 аминокислоты. Термин также относится к белку CD3-эпсилон человека или яванского макака, SEQ ID NO: 591 и 592 соответственно (таблица 4). «CD3εN27» и «CD3εN13» означают соответственно 27 N-концевых аминокислот и 13 N-концевых аминокислот CD3, и они необязательно содержат химические модификации или с ними осуществлены конъюгации.
«Антитело к CD3» относится к антителу или его антигенсвязывающему фрагменту, способному связываться с CD3, например, CD3ε и/или CD3γ, например, человеческими CD3ε и/или CD3γ с достаточной аффинностью и/или специфичностью, так что антитело можно использовать как диагностическое и/или терапевтическое средство для нацеливания на CD3. В некоторых вариантах осуществления антитело к CD3 связывается с CD3 с константой диссоциации (KD), составляющей приблизительно 100 x 10-9 М или менее, приблизительно 50 x 10-9 М или менее, приблизительно 25 x 10-9 М или менее, приблизительно 20 х 10-9 М или менее или приблизительно 10 х 10-9 М или менее. В некоторых вариантах осуществления антитело к CD3 связывается с CD3 с константой диссоциации (KD), составляющей приблизительно 5 x 10-9 М или менее. В некоторых вариантах осуществления антитело к CD3 связывается с CD3 с константой диссоциации (KD), составляющей приблизительно 2,5 x 10-9 М или менее. В некоторых вариантах осуществления антитело к CD3 связывается с CD3 с константой диссоциации (KD), составляющей приблизительно 1 x 10-10 М или менее. В некоторых вариантах осуществления KD измеряют с помощью поверхностного плазмонного резонанса, например, BIACORE, с применением измерений интерферометрии биослоев, с применением, например, инструмента FORTEBIO Octet HTX (Pall Life Sciences), или определения аффинности в растворе методом ELISA. В некоторых вариантах осуществления KD измеряют с применением scFv-фрагмента антитела к CD3. В некоторых вариантах осуществления измеряют моновалентную KD. В некоторых вариантах осуществления антитело к CD3 связывается с эпитопом CD3, который является консервативным для CD3 от разных видов, например, обеспечивающим перекрестную реактивность для человека и яванского макака.
Термин «сконструированный pH-зависимый» относится к антителу, имеющему модифицированную аминокислотную последовательность, которая обеспечивает предпочтительное или селективное связывание антигена при определенном pH. Например, исходное антитело может быть сконструировано (например, путем модификации аминокислотной последовательности) для pH-зависимого связывания. PH-зависимое связывание относится к предпочтительному связывания антитела с антигеном при данном pH (или данном диапазоне pH) по сравнению с другим pH (или диапазоном pH). В одном варианте осуществления pH-зависимые антитела предпочтительно или селективно связываются с антигеном при pH, составляющим приблизительно 6, по сравнению с pH, составляющим приблизительно 7. Последовательность антитела может быть модифицирована, например, заменой одним или несколькими ионизируемыми аминокислотными остатками, такими как гистидин, лизин, аргинин, аспарагиновая кислота и глутаминовая кислота. Ионизируемые остатки могут быть заменены на CDR и/или FR. В некоторых вариантах осуществления может присутствовать 1-10 замен на вариант VH или VK. В некоторых вариантах осуществления может присутствовать 1-6 замен на вариант VH или VK.
Термин «синдром высвобождения цитокинов» (или «CRS») относится к провоспалительной положительной обратной связи между цитокинами и иммунными клетками, приводящей к избыточному или неконтролируемому высвобождению провоспалительных цитокинов клетками иммунной системы (см., например, Lee et al., Blood, Vol. 124, pages 188-195 (2014) and Tisoncik et al., Microbiol Mol Biol Rev, Vol. 76, pages 16-32 (2012). После стимуляции и активации T-клетки высвобождают серию цитокинов с таким уровнем и степенью, которые производят неблагоприятные биологические/физиологические эффекты различной степени и тяжести, включая острое воспаление, характеризующееся, например, покраснением кожи (краснотой), набуханием или отеком, жаром (повышением температуры), воспалением (болью) и «нарушением функции» (потерей функции). При локализации в коже или другой ткани биологические/физиологические эффекты характеризуются повышенным кровотоком, который обеспечивает возможность лейкоцитам в сосудах и белкам плазмы крови достигать внесосудистых участков повреждения, повышая местную температуру и приводят к возникновению болевых ощущений, отечности тканей и экстраваскулярному давлению, а также снижению тканевой перфузии. Другие биологические/физиологические эффекты включают нарушение органов и систем, например нарушение функции сердца, респираторный дистресс-синдром у взрослых, нейротоксичность, почечная и/или печеночная недостаточность и диссеминированное внутрисосудистое свертывание крови. Повышенные уровни IFNγ, IL-6, TNFα, TGFбета, IL-2, гранулоцитарномакрофагального колониестимулирующего фактора (GM-CSF), IL-10, IL-8, IL-5 и/или фракталкина прогнозируют и/или вызывают CRS или показывают предрасположенность к вызову CRS после стимуляции T-клеток.
В некоторых вариантах осуществления описанные в данном документе антитела к CD3 и/или их антигенсвязывающие фрагменты разрегулированы и/или модифицированы так, чтобы снизить вероятность или тяжесть CRS, индуцированного антителом. Неограничивающие иллюстративные модификации могут включать молчащие Fc-области (например, полное удаление Fc или модификацию Fc-области для снижения или устранения эффекторной функции) и/или маскирование (например, полипептидная маска, расположенная так, что она снижает или ингибирует способность антитела или его антигенсвязывающего фрагмента специфически связывать CD3).
В данном документе термин «антитело» используется в наиболее широком смысле и охватывает различные структуры антитела, в том числе без ограничения моноклональные антитела, поликлональные антитела, мультиспецифические антитела (например, биспецифические антитела) и/или фрагменты антитела (предпочтительны те фрагменты, которые проявляют требуемую активность связывания антигена).
Используемый в данном документе термин «моноклональное антитело» или «mAb» относится к антителу, полученному из группы фактически однородных антител, т. е. индивидуальных антител, составляющих группу антител, которые являются идентичными и/или связывают один и тот же эпитоп, за исключением возможных вариантов антител, (например, содержащих встречающиеся в природе мутации или мутации, возникающие в ходе получения моноклонального антитела), при этом такие варианты обычно присутствуют в незначительных количествах. В отличие от препаратов поликлональных антител, которые, как правило, содержат разные антитела, направленные против разных детерминант (эпитопов), каждое моноклональное антитело в препарате моноклональных антител направлено на одну детерминанту на антигене.
Что касается мультиспецифических антител, такие антитела содержат по меньшей мере два различных антигенсвязывающих домена, которые распознают и специфически связываются с по меньшей мере двумя различными антигенами. Что касается биспецифических антител, такие антитела содержат два различных антигенсвязывающих домена, которые распознают и специфически связываются с по меньшей мере двумя различными антигенами.
«Отличный антиген» может относиться к различным и/или отдельным белкам, полипептидам или молекулам; а также к различным и/или отдельным эпитопам, при этом такие эпитопы могут содержаться в пределах одного белка, полипептида или другой молекулы.
Термин «эпитоп» относится к антигенной детерминанте, которая взаимодействует со специфическим антигенсвязывающим сайтом в вариабельной области молекулы антитела, известной как паратоп. Один антиген может иметь более одного эпитопа. Таким образом, разные антитела могут связываться с разными областями антигена и могут оказывать разные биологические эффекты. Термин «эпитоп» также относится к сайту на антигене, на который реагируют B- и/или T-клетки. Он также относится к участку антигена, который связывается антителом. Эпитопы могут быть определены как структурные или функциональные. Функциональные эпитопы в целом представляют собой подгруппу структурных эпитопов и содержат остатки, которые напрямую вносят вклад в аффинность взаимодействия. Эпитопы также могут быть конформационными, то есть состоять из нелинейно расположенных аминокислот. В определенных вариантах осуществления эпитопы могут включать детерминанты, которые представляют собой химически активные поверхностные группы молекул, таких как аминокислоты, сахарные боковые цепи, фосфорильные группы или сульфонатные группы, и в определенных вариантах осуществления могут обладать специфическими характеристиками трехмерной структуры и/или специфическими характеристиками заряда.
В некоторых случаях антитело содержит четыре полипептидных цепи: две тяжелые (H) цепи и две легкие (L) цепи, соединенные дисульфидными связями. Существует пять основных классов антител: IgA, IgD, IgE, IgG и IgM, и некоторые из них могут быть дополнительно разделены на подклассы (изотипы), например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2. Константные домены тяжелой цепи, которые соответствуют разным классам иммуноглобулинов, соответственно называются α, δ, ε, γ и μ.
В других случаях антитело может вместо этого содержать его мультимеры (например, IgM) или его антигенсвязывающие фрагменты. Каждая тяжелая цепь состоит из вариабельной области тяжелой цепи («VH») и константной области тяжелой цепи («CH»), которая состоит из доменов CH1, CH2 и CH3. Каждая легкая цепь состоит из вариабельной области легкой цепи («VL») и константной области легкой цепи («CL»). Области VH и VL могут быть дополнительно подразделены на области гипервариабельности, называемые областями, определяющими комплементарность (CDR), чередующиеся с более консервативными областями, называемыми каркасными областями (FR). Каждая VH и VL состоит из трех CDR и четырех FR, расположенных от аминоконца к карбоксиконцу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. В определенных вариантах осуществления настоящего изобретения FR антитела (или его антигенсвязывающего фрагмента) могут быть идентичны последовательностям зародышевой линии человека или могут быть модифицированы естественным или искусственным путем. Аминокислотная консенсусная последовательность может быть определена на основе анализа расположенных рядом друг с другом двух или более CDR. Соответственно, CDR в тяжелой цепи обозначаются как «CDRH1», «CDRH2» и «CDRH3» соответственно, а CDR в легкой цепи обозначаются как «CDRL1», «CDRL2» и «CDRL3».
Если конкретно не указано иное, термин «антитело», используемый в данном документе, охватывает молекулы, содержащие две тяжелые цепи иммуноглобулина и две легкие цепи иммуноглобулина (т. е. «полноразмерное антитело», «интактные антитела» или «целое антитело»), а также их антигенсвязывающие фрагменты.
«Антигенсвязывающий фрагмент» относится к части интактного антитела, которая связывает антиген, с которым связывается интактное антитело (в данном случае CD3). Термины «полноразмерное антитело», «интактное антитело» и «цельное антитело» или подобные используются в данном документе взаимозаменяемо для обозначения антитела, имеющего структуру, которая фактически аналогична структуре нативного антитела.
Антигенсвязывающий фрагмент антитела включает любой встречающийся в природе, получаемый ферментативным путем, синтетический или полученный с помощью методик генной инженерии полипептид или гликопротеин, который специфически связывает антиген с образованием комплекса, включая фрагмент антитела. Примеры антигенсвязывающих фрагментов включают без ограничения Fv, Fab, Fab', Fab'-SH, F(ab')2; диатела; линейные антитела; молекулы одноцепочечных антител (например, только домены scFv или VH или VL) и мультиспецифические антитела, образованные из фрагментов антител. В некоторых вариантах осуществления антигенсвязывающие фрагменты антител к CD3, описанных в настоящем документе, представляют собой scFv.
Как и в случае с молекулами полных антител, антигенсвязывающие фрагменты могут быть моноспецифическими или мультиспецифическими (например, биспецифическими). Мультиспецифический антигенсвязывающий фрагмент антитела может содержать по меньшей мере два отличающихся вариабельных домена, где каждый вариабельный домен способен специфически связываться с отдельным антигеном или с отличающимся эпитопом на одном и том же антигене. В контексте описанного в данном документе антигенсвязывающего фрагмента антитела к CD3 можно использовать различные форматы мультиспецифических антител. Неограничивающие примеры мультиспецифических и биспецифических форматов включают, например, Fab-Fc-scFv («открывалка для бутылок») (XENCOR), Mab-scFv (XENCOR), Mab-Fv (XENCOR), Dual scFv (XENCOR), центральный Fv (XENCOR), центральный scFv(XENCOR), одноплечевой центральный scFv (XENCOR), Fab-Fab (XENCOR), Fab-Fv (XENCOR), mAb-Fv (XENCOR), mAb-Fab (XENCOR), DART (MACROGENICS), BiTE (AMGEN/MICROMET), KiTE, IgG с универсальной легкой цепью (Genentech), TandAb (SFFIMED) Cross-Mab (ROCHE), SEED (EMD SERONO), BEAT (GLENMARK), TrioMab (TRION PHARMA/FRESENIUS BIOTECH), DuetMab (MEDIMMUNE) и другие, которые раскрыты, например, в WO 95/09917; WO 2008/119566; WO 2008/119567; WO2011/121110; WO 2010/037835; WO 2007/042261; WO 2007/110205; WO 2011/121110; WO 2012/055961; WO 2012/16067; WO 2016/086189; WO 2016/182751; WO 2015/006749; WO 2014/049003; WO 2013/177101; WO 2015/128509; US 7,951,917; US 2009/0252729; US 2014/0348839; US 7183076; Mazor et al., Mabs, Vol. 7, pages 377-389 (2015); Muda et al., Protein Engineering, Designe, & Selection, Vol. 24, pages 447-454 (2011) и Del Bano et al., Antibodies, Vol. 5, pages 1-23 (2016). В некоторых вариантах осуществления описанные в данном документе scFv-фрагменты к CD3 содержат один или несколько вариабельных доменов мультиспецифического (например, биспецифического) антитела.
В некоторых вариантах осуществления антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в данном документе, содержатся в мультиспецифическом антителе, в частности, в биспецифическом антителе, которое характеризуется специфичностью связывания со вторым антигеном. Такой второй антиген может быть совершенно другой мишенью, чем первая мишень, или другим эпитопом, присутствующим на той же мишени. В некоторых вариантах осуществления специфичность связывания относится к двум различным эпитопам CD3 (например, CD3ε или CD3γ). В других вариантах осуществления одна из специфичностей связывания предусматривает связывание с CD3 (например, CD3ε или CD3γ), а другая предусматривает связывание с другой биологической молекулой (например, антигеном клеточной поверхности, например, опухолевым антигеном).
Неограничивающие примеры второго антигена, в отношении которого биспецифическое антитело, включающее антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в данном документе, включает мишени , выбранные из группы, состоящей из 17-IA, 4-1BB, 4Dc, 6-кето-PGF1a, 8-изо-PGF2a, 8-оксо-dG, аденозинового рецептора A1, A33, ACE, ACE-2, активина, активина A, активина AB, активина B, активина C, активина RIA, активина RIA/ALK-2, активина RIB/ALK-4, активина RIIA, активина RUB, ADAM, ADAM10, ADAM12, ADAM15, ADAM17/TACE, ADAM8, ADAM9, ADAMTS, ADAMTS4, ADAMTS5, адресинов, aFGF, ALCAM, ALK, ALK-1, ALK-7, альфа-1-антитрипсина, антагониста альфа-V/бета-1, ANG, Ang, APAF-1, APE, APJ, APP, APRIL, AR, ARC, ART, артемина, антиидиотипа, аспарагиновой кислоты, предсердного натрийуретического фактора, интегрина av/b3, Ax1, b2M, B7-1, B7-2, B7-H, стимулятора B-лимфоцитов (BlyS), BACE, BACE-1, Bad, BAFF, BAFF-R, Bag-1, BAK, Bax, BCA-1, BCAM, Bel, BCMA, BDNF, b-ECGF, bFGF, BID, Bik, BIM, BLC, BL-CAM, BLK, BMP, BMP-2/BMP-2a, BMP-3/остеогенина, BMP-4/BMP-2b, BMP-5, BMP-6/Vgr-1, BMP-7 (OP-1), BMP-8 (BMP-8a, OP-2), BMPR, BMPR-IA (ALK-3), BMPR-IB (ALK-6), BRK-2, RPK-1, BMPR-II (BRK-3), видов BMP, b-NGF, BOK, бомбезина, костного нейротрофического фактора, BPDE, BPDE-DNA, BTC, фактора комплемента 3 (C3), C3a, C4, C5, C5a, CIO, CA125, CAD-8, кальцитонина, cAMP, раково-эмбрионального антигена (CEA), ассоциированного с карциномой антигена, катепсина A, катепсина B, катепсина C/DPPI, катепсина D, катепсина E, катепсина H, катепсина L, катепсина O, катепсина S, катепсина V, катепсина X/Z/P, CBL, CCI, CCK2, CCL, CCL1, CCL11, CCL12, CCL13, CCL14, CCL15, CCL16, CCL17, CCL18, CCL19, CCL2, CCL20, CCL21, CCL22, CCL23, CCL24, CCL25, CCL26, CCL27, CCL28, CCL3, CCL4, CCL5, CCL6, CCL7, CCL8, CCL9/10, CCR, CCR1, CCR10, CCR10, CCR2, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CD1, CD2, CD4, CD5, CD6, CD7, CD8, CD10, CD11a, CD11b, CD11c, CD13, CD14, CD15, CD16, CD18, CD19, CD20, CD21, CD22, CD23, CD25, CD27L, CD28, CD29, CD30, CD30L, CD32, CD33 (белки p67), CD34, CD38, CD40, CD40L, CD44, CD45, CD46, CD49a, CD52, CD54, CD55, CD56, CD61, CD64, CD66e, CD74, CD80 (B7-1), CD89, CD95, CD123, CD137, CD138, CD140a, CD146, CD147, CD148, CD152, CD164, CEACAM5, CFTR, cGMP, CINC, токсина Clostridium botulinum, токсина Clostridium perfringens, CKb8-1, CLC, CMV, CMV UL, CNTF, CNTN-1, COX, C-Ret, CRG-2, CT-1, CTACK, CTGF, CTLA-4, CX3CL1, CX3CR1, CXCL, CXCL1, CXCL2, CXCL3, CXCL4, CXCL5, CXCL6, CXCL7, CXCL8, CXCL9, CXCL10, CXCL11, CXCL12, CXCL13, CXCL14, CXCL15, CXCL16, CXCR, CXCR1, CXCR2, CXCR3, CXCR4, CXCR5, CXCR6, цитокератинового опухолеассоциированного антигена, DAN, DCC, DcR3, DC-SIGN, фактора ускорения распада, des(1-3)-IGF-1 (IGF-1 головного мозга), Dhh, дигоксина, DNAM-1, ДНКазы, Dpp, DPPIV/CD26, Dtk, ECAD, EDA, EDA-A1, EDA-A2, EDAR, EGF, EGFR (ErbB-1), EMA, EMMPRIN, EN A, рецептора эндотелина, энкефалиназы, eNOS, Eot, эотаксина-1, EpCAM, эфрина B2/EphB4, EPO, ERCC, E-селектина, ET-1, фактора IIa, фактора VII, фактора VIIIc, фактора IX, белка активации фибробластов (FAP), Fas, FcR1, FEN-1, ферритина, FGF, FGF-19, FGF-2, FGF3, FGF-8, FGFR, FGFR-3, фибрина, FL, FLIP, Flt-3, Flt-4, фолликулостимулирующего гормона, фракталкина, FZD1, FZD2, FZD3, FZD4, FZD5, FZD6, FZD7, FZD8, FZD9, FZD10, G250, Gas 6, GCP-2, GCSF, GD2, GD3, GDF, GDF-1, GDF-3 (Vgr-2), GDF-5 (BMP-14, CDMP-1), GDF-6 (BMP-13, CDMP-2), GDF-7 (BMP-12, CDMP-3), GDF-8 (миостатин), GDF-9, GDF-15 (MIC-1), GDNF, GDNF, GFAP, GFRa-1, GFR-альфа1, GFR-альфа2, GFR-альфа3, GITR, глюкагона, Glut 4, гликопротеина IIb/IIIa (GP IIb/IIIa), GM-CSF, gp130, gp72, GRO, рилизинг-фактора гормона роста, гаптена (NP-cap или NIP-cap), HB-EGF, HCC, гликопротеина gB оболочки HCMV, гликопротеина gH оболочки HCMV, HCMV UL, гемопоэтического фактора роста (HGF), gp120 вируса гепатита B, гепараназы, Her2, Her2/neu (ErbB-2), Her3 (ErbB-3), Her4 (ErbB-4), гликопротеина gB вируса простого герпеса (HSV), гликопротеина gD HSV, HGFA, высокомолекулярного ассоциированного с меланомой антигена (HMW-MAA), gp120 ВИЧ, V3-петли gp 120 ВИЧ IIIB, HLA, HLA-DR, HM1.24, HMFG PEM, HRG, Hrk, сердечного миозина человека, цитомегаловируса (HCMV) человека, гормона роста человека (HGH), HVEM, 1-309, IAP, ICAM, ICAM-1, ICAM-3, ICE, ICOS, IFNg, Ig, рецептора IgA, IgE, IGF, IGF-связывающих белков, IGF-1R, IGFBP, IGF-I, IGF-II, IL, IL-1, IL-1R, IL-2, IL-2R, IL-4, IL-4R, IL-5, IL-5R, IL-6, IL-6R, IL-8, IL-9, IL-10, IL-12, IL-13, IL-15, IL-18, IL-18R, IL-23, интерферона (INF)-альфа, INF-бета, INF-гамма, ингибина, iNOS, A-цепи инсулина, B-цепи инсулина, инсулиноподобного фактора роста 1, интегрина-альфа2, интегрина-альфа3, интегрина-альфа4, интегрина альфа4/бета1, интегрина, альфа4/бета7, интегрина-альфа5 (альфаV), интегрина-альфа5/бета1, интегрина альфа5/бета3, интегрина-альфа6, интегрина-бета1, интегрина-бета2, интерферона-гамма, IP-10, 1-TAC, JE, калликреина 2, калликреина 5, калликреина 6, калликреина 11, калликреина 12, калликреина 14, калликреина 15, калликреина L1, калликреина L2, калликреина L3, калликреина L4, KC, KDR, фактора роста кератиноцитов(KGF), ламинина 5, LAMP, LAP, LAP (TGF-1), латентного TGF-1, латентного TGF-1 bpl, LBP, LDGF, LECT2, Lefty, антигена Льюиса Y, антигена, родственного антигену Льюиса Y, LFA-1, LFA-3, Lfo, LIF, LIGHT, липопротеинов, LIX, LKN, Lptn, L-селектина, LT-a, LT-b, LTB4, LTBP-1, легочного сурфактанта, лютеинизирующего гормона, рецептора лимфотоксина-бета, Mac-1, MAdCAM, MAG, MAP2, MARC, MCAM, MCAM, MCK-2, MCP, M-CSF, MDC, Mer, металлопротеаз, рецептора MGDF, MGMT, MHC (HLA-DR), MIF, MIG, MIP, MIP-1-альфа, MK, MMAC1, MMP, MMP-1, MMP-10, MMP-11, MMP-12, MMP-13, MMP-14, MMP-15, MMP-2, MMP-24, MMP-3, MMP-7, MMP-8, MMP-9, MPIF, Mpo, MSK, MSP, муцина (Muc1), MUC18, ингибирующего вещества Мюллера, Mug, MuSK, NAIP, NAP, NCAD, N-кадгерина, NCA 90, NCAM, NCAM, неприлизина, нейротрофина-3,-4 или -6, нейротурина, фактора роста нейронов (NGF), NGFR, NGF-бета, nNOS, NO, NOS, Npn, NRG-3, NT, NTN, OB, OGG1, OPG, OPN, OSM, OX40L, OX40R, p150, p95, PADPr, паратиреоидного гормона, PARC, PARP, PBR, PBSF, PCAD, P-кадгерина, PCNA, PDGF, PDGF, PDK-1, PECAM, PEM, PF4, PGE, PGF, PGI2, PGJ2, PIN, PLA2, плацентарной щелочной фосфатазы (PLAP), P1GF, PLP, PP14, проинсулина, прорелаксина, белка C, PS, PSA, PSCA, простатического специфического мембранного антигена (PSMA), PTEN, PTHrp, Ptk, PTN, R51, RANK, RANKL, RANTES, RANTES, A-цепи релаксина, B-цепи релаксина, ренина, F респираторно-синцитиального вируса (RSV), Fgp RSV, Ret, ревматоидных факторов, RLIP76, RPA2, RSK, S100, SCF/KL, SDF-1, серина, сывороточного альбумина, sFRP-3, Shh, SIGIRR, SK-1, SLAM, SLPI, SMAC, SMDF, SMOH, SOD, SPARC, Stat, STEAP, STEAP-II, TACE, TACI, TAG-72 (опухолеассоциированный гликопротеин-72), TARC, TCA-3, T-клеточных рецепторов (например, T-клеточного рецептора альфа/бета), TdT, TECK, TEM1, TEM5, TEM7, TEM8, ТРЕТ, PLAP-подобной щелочной фосфатазы семенников, TfR, TGF, TGF-альфа, TGF-бета, панспецифического TGF-бета, TGF-бета RI (ALK-5), TGF-бета RII, TGF-бета Rllb, TGF-бета RIII, TGF-бета1, TGF-бета2, TGF-бета3, TGF-бета4, TGF-бета5, тромбина, тимусного Ck-1, тиреостимулирующего гормона, Tie, TIMP, TIQ, тканевого фактора, TMEFF2, Tmpo, TMPRSS2, TNF, TNF-альфа, TNF-альфа/бета, TNF-бета2, TNFc, TNF-RI, TNF-RII, TNFRSF10A (TRAIL R1, Apo-2, DR4), TNFRSF10B (TRAIL R2, DR5, KILLER, TRICK-2A, TRICK-B), TNFRSF10C (TRAIL R3, DcR1, LIT, TRID), TNFRSF10D (TRAIL R4, DcR2, TRUNDD), TNFRSF11A (RANK, ODFR, TRANCE R), TNFRSF11B (OPG, OCIF, TR1), TNFRSF12 (TWEAK R, FN14), TNFRSF13B (TACI), TNFRSF13C (BAFF R), TNFRSF14 (HVEM, ATAR, HveA, LIGHT R, TR2), TNFRSF16 (NGFR, p75NTR), TNFRSF17 (BCMA), TNFRSF18 (GITR, AITR), TNFRSF19 (TROY, TAJ, TRADE), TNFRSF19L (RELT), TNFRSFIA (TNF RI, CD120a, p55-60), TNFRSFIB (TNF RII, CD120b, p75-80), TNFRSF26 (TNFRH3), TNFRSF3 (LTbR, TNF RIII, TNFC R), TNFRSF4 (OX40, ACT35, TXGP1 R), TNFRSF5 (CD40, p50), TNFRSF6 (Fas, Apo-1, APT1, CD95), TNFRSF6B (DcR3, M68, TR6), TNFRSF7 (CD27), TNFRSF8 (CD30), TNFRSF9 (4-lBB, CD137, ILA), TNFRSF21 (DR6), TNFRSF22 (DcTRAIL R2, TNFRH2), TNFRST23 (DcTRAIL R1, TNFRH1), TNFRSF25 (DR3, Apo-3, LARD, TR-3, TRAMP, WSL-1), TNFSF10 (TRAIL, лиганд Apo-2, TL2), TNFSF11 (TRANCE/RANK, лиганд ODF, лиганд OPG), TNFSF12 (TWEAK лиганд-Apo-3, лиганд DR3), TNFSF13 (APRIL, TALL2), TNFSF13B (BAFF, BLYS, TALL1, THANK, TNFSF20), TNFSF14 (LIGHT, лиганд HVEM, LTg), TNFSF15 (TL1A/VEGI), TNFSF18 (лиганд GITR, лиганд AITR, TL6), TNFSFIA (TNF-a конектин, DIF, TNFSF2), TNFSF1B (TNF-b, LTa, TNFSF1), TNFSF3 (LTb, TNFC, p33), TNFSF4 (лиганд OX40, gp34, TXGP1), TNFSF5 (лиганд CD40, CD154, gp39, HIGM1, IMD3, TRAP), TNFSF6 (лиганд Fas, лиганд Apo-1, лиганд APT1), TNFSF7 (лиганд CD27, CD70), TNFSF8 (лиганд CD30, CD153), TNFSF9 (лиганд 4-lBB, лиганд CD137), TP-1, t-PA, Tpo, TRAIL, TRAIL R, TRAIL-R1, TRAIL-R2, TRANCE, рецептора трансферрина, TRF, Trk, TROP-2, TSG, TSLP, опухолеассоциированного антигена CA 125, опухолеассоциированного антигена, характеризующегося экспрессией углеводного антигена, родственного антигену Льюиса Y, TWEAK, TXB2, Ung, uPAR, uPAR-1, урокиназы, VCAM, VCAM-1, VECAD, VE-кадгерина, VE-кадгерина-2, VEFGR-1 (flt-1), VEGF, VEGFR, VEGFR-3 (flt-4), VEGI, VIM, вирусных антигенов, VLA, VLA-1, VLA-4, интегрина VNR, фактора фон Виллебранда, WIF-1, WNT1, WNT2, WNT2B/13, WNT3, WNT3A, WNT4, WNT5A, WNT5B, WNT6, WNT7A, WNT7B, WNT8A, WNT8B, WNT9A, WNT9A, WNT9B, WNT10A, WNT10B, WNT11, WNT16, XCL1, XCL2, XCR1, XCR1, XEDAR, XIAP, XPD, CTLA4 (антиген-4 цитотоксических T-лимфоцитов), PD1 (белок-1 запрограммированной гибели клеток), PD-L1 (лиганд-1 белка запрограммированной гибели клеток), LAG-3 (ген-3 активации лимфоцитов), TIM-3 (белок-3, содержащий домены T-клеточного иммуноглобулина и муцина), рецепторов гормонов и факторов роста.
Мультиспецифические препараты, содержащие антитела к CD3 и антигенсвязывающие фрагменты, раскрытые в настоящем документе, могут быть получены различными способами, в том числе, без ограничения, при помощи рекомбинантной совместной экспрессии двух пар тяжелая цепь - легкая цепь иммуноглобулина, имеющих разные специфичности (см., Milstein and Cuello, Nature 305: 537 (1983)), WO 93/08829, а также Traunecker et al., EMBO J. 10: 3655 (1991)), и конструирования типа «выступ-во-впадину» (см., например, патент США № 5731168); технологии кроссовера иммуноглобулинов (также известного как обмен Fab-доменов или формат CrossMab) (см., например, WO2009/080253; Schaefer et al., Proc. Natl. Acad. Sci. USA, 108:11187-11192 (2011)); конструирования эффектов электростатической координации с получением Fc-гетеродимерных молекул антитела (WO 2009/089004A1); перекрестной сшивки двух или более антител или фрагментов (см., например, патент США № 4676980 и Brennan et al., Science, 229: 81 (1985)); с применением лейциновых застежек (см., например, Kostelny et al., J. Immunol, 148(5):1547-1553 (1992)); технологии «диатела» (см., например, Hollinger et al., Proc. Natl. Acad. Sci. USA, 90:6444-6448 (1993)); одноцепочечных Fv(sFv)-димеров (см., например, Gruber et al., J. Immunol, 152:5368 (1994)); и триспецифических антител, описанных, например, в Tutt et al. J. Immunol 147: 60 (1991).
В настоящем изобретении также предусмотрена модификация описанных в данном документе антител к CD3, при этом такие модификации включают одну или несколько аминокислотных замен, вставок и/или делеций в областях FR и/или CDR вариабельных доменов тяжелой и легкой цепей. После получения такие производные антитела и/или антигенсвязывающие фрагменты можно исследовать в отношении одного или нескольких требуемых свойств, например улучшенной специфичности связывания, повышенной аффинности связывания, улучшенной разрабатываемости и т.д.
В некоторых вариантах осуществления антитела к CD3 и/или их антигенсвязывающие фрагменты содержат последовательность тяжелой цепи (HC), последовательность легкой цепи (LC), последовательность CDRH3, последовательность CDRH2, последовательность CDRH1, последовательность CDRL3, последовательность CDRL2, последовательность CDRL1 и/или каркасную последовательность. В некоторых вариантах осуществления антитела к CD3 и/или их антигенсвязывающие фрагменты характеризуются по меньшей мере приблизительно 100%, по меньшей мере приблизительно 99%, по меньшей мере приблизительно 98%, по меньшей мере приблизительно 97%, по меньшей мере приблизительно 96%, по меньшей мере приблизительно 95%, по меньшей мере приблизительно 94%, по меньшей мере приблизительно 93%, по меньшей мере приблизительно 92%, по меньшей мере приблизительно 91%, по меньшей мере приблизительно 90%, по меньшей мере приблизительно 89%, по меньшей мере приблизительно 88%, по меньшей мере приблизительно 87%, по меньшей мере приблизительно 86%, приблизительно 85%, по меньшей мере приблизительно 84%, по меньшей мере приблизительно 83%, по меньшей мере приблизительно 82 %, по меньшей мере приблизительно 80% идентичностью аминокислотной последовательности с соответствующими последовательностями антител к CD3, раскрытых в таблице 1 (Ab1-Ab258); и/или всеми промежуточными процентами идентичности. В некоторых вариантах осуществления процент идентичности измеряют с помощью любого хорошо известного алгоритма идентичности последовательностей, такого как FASTA, BLAST или GAP.
В некоторых вариантах осуществления положения остатков, которые не являются идентичными, отличаются консервативными аминокислотными заменами. «Консервативная аминокислотная замена» представляет собой замену, при которой аминокислотный остаток заменен на другой аминокислотный остаток с боковой цепью (R-группой) с аналогичными химическими свойствами (например, зарядом или гидрофобностью). В целом консервативная аминокислотная замена фактически не будет изменять функциональные свойства белка. В тех случаях, когда две или более аминокислотных последовательностей отличаются друг от друга консервативными заменами, процент или степень сходства можно скорректировать в сторону увеличения, с учетом консервативной природы замены. Средства для осуществления данной корректировки хорошо известны специалистам в данной области техники. (см., например, Pearson (1994) Methods Mol. Biol. 24: 307- 331). Примеры групп аминокислот, которые имеют боковые цепи со сходными химическими свойствами, включают 1) алифатические боковые цепи: глицин, аланин, валин, лейцин и изолейцин; 2) алифатические гидроксильные боковые цепи: серин и треонин; 3) амидсодержащие боковые цепи: аспарагин и глутамин; 4) ароматические боковые цепи: фенилаланин, тирозин и триптофан; 5) основные боковые цепи: лизин, аргинин и гистидин; 6) кислотные боковые цепи: аспартат и глутамат и 7) серосодержащие боковые цепи: цистеин и метионин. В некоторых вариантах осуществления группы замен консервативных аминокислотных замен представляют собой валин-лейцин-изолейцин, фенилаланин-тирозин, лизин-аргинин, аланин-валин, глутамат-аспартат и аспарагин-глутамин. В качестве альтернативы в некоторых вариантах осуществления консервативная замена включает любое изменение, характеризующееся положительным значением в матрице логарифмического правдоподобия PAM250, раскрытой в Gonnet et al. (1992) Science 256: 1443 45. В некоторых вариантах осуществления «умеренно консервативное» замещение включает любое изменение, характеризующееся неотрицательным значением в матрице логарифмического правдоподобия PAM250.
Также возможна замена одного или более остатков в CDR или удаление одного или более CDR. В научной литературе описаны антитела, в которых могут быть распределены одна или две CDR для изменения связывания. Padlan et al. (1995 FASEB J. 9:133-139) проанализировали контактные области между антителами и их антигенами, исходя из опубликованных кристаллических структур, и сделали вывод о том, что только от приблизительно одной пятой до одной трети остатков в CDR действительно контактируют с их связанным антигеном. Padlan также обнаружил множество антител, у которых один или два CDR не содержали аминокислот, вступающих в контакт с антигеном (см. также Vajdos et al. 2002 J Mol Biol 320:415-428). Остатки CDR, не контактирующие с антигеном, могут быть идентифицированы на основании предыдущих исследований (например, остатки H60 - H65 в CDRH2 зачастую не являются необходимыми), на основе областей CDR по Kabat, лежащих за пределами CDR по Chothia, с помощью молекулярного моделирования и/или эмпирическим путем. Если исключен CDR или его остаток(остатки), то он обычно заменен на аминокислоту, занимающую соответствующее положение в другой последовательности человеческого антитела, или на консенсусную последовательность для таких последовательностей. Положения для замены в пределах CDR и аминокислоты для замены также могут быть выбраны эмпирическим путем.
В определенных вариантах осуществления замены, вставки или делеции могут встречаться в пределах одной или более CDR сконструированных рН-зависимых антител, связывающих CD3, описанных в данном документе, при условии, что такие изменения сохраняют чувствительность к рН и практически не снижают способность антитела к связыванию антигена. Например, в CDR можно выполнять консервативные изменения (например, консервативный замены, представленные в данном документе), которые практически не снижают аффинность связывания. Такие изменения, например, могут находиться в CDR за пределами остатков, контактирующих с антигеном. В определенных вариантах осуществления вариантов последовательностей VH и VL, представленных выше, каждый CDR является или неизмененным, или содержит не более одной, двух или трех аминокислотных замен.
Применимый способ для идентификации остатков или участков антитела, на которые может быть нацелен мутагенез, называется «аланинсканирующий мутагенез», как описано в Cunningham and Wells (1989) Science, 244:1081-1085. В данном способе идентифицируют остаток или группу целевых остатков (например, заряженных остатков, таких как arg, asp, his, lys и glu) и замещают нейтральной или отрицательно заряженной аминокислотой (например, аланин или полиаланин), чтобы определить, воздействует ли это на взаимодействие антитела с антигеном. В положения аминокислот, демонстрирующие функциональную чувствительность к исходным заменам, могут быть введены дополнительные замены. В качестве альтернативы или дополнения для идентификации точек контакта между антителом и антигеном определяют кристаллическую структуру комплекса антиген-антитело. Такие контактные остатки и соседние остатки могут выступать в качестве кандидатов для замены, на которые оказывают целенаправленное воздействие или которые устраняют. Варианты могут быть подвергнуты скринингу для определения того, обладают ли они требуемыми свойствами.
Вставки в аминокислотной последовательности включают амино- и/или карбоксиконцевые слияния, варьирующиеся по длине от одного остатка до полипептидов, содержащих сотню или более остатков, а также вставки одного или более аминокислотных остатков внутри последовательности. Примеры концевых вставок включают антитело с N-концевым метиониловым остатком. Другие варианты вставок в молекулу антитела включают слияние N- или C-конца антитела с ферментом (например, в случае ADEPT) или полипептидом, который увеличивает время полужизни антитела в сыворотке крови.
Как описано по всему тексту данного документа, антитела к CD3 и/или их антигенсвязывающие фрагменты, представленные в настоящем документе, характеризуются благоприятной разрабатываемостью и, таким образом, считаются относительно разрабатываемыми.
Термин «разрабатываемость» относится к степени, в которой один или более полипептидов из совокупности полипептидов обладает требуемыми характеристиками, такими как, например, требуемая экспрессия, например, в клетках млекопитающих; растворимость; вязкость; агрегация; химическая и/или физическая стабильность; требуемый «срок хранения»; температура плавления; фармакокинетические профили; время полужизни в кровотоке; характеристики клиренса. Такие характеристики могут выступать в качестве независимых признаков, в качестве комбинаций подмножеств таких признаков или все вместе для определения вероятности того, что такой один или более полипептидов могут подвергаться успешной разработке в качестве терапевтического кандидата и, в конечном итоге, одобренного лекарственного средства. Соответственно, из уровня техники в целом понятно, что полипептиды с требуемыми характеристиками разрабатываемости обладают, например, относительно высокой растворимостью, относительно низкой вязкостью, относительно низкой предрасположенностью к агрегации, относительно высокой химической стабильностью, относительно высокой физической стабильностью, относительно продолжительным «сроком хранения», относительно высокой температурой плавления, относительно длительным периодом полужизни в кровотоке, относительно длительным временем клиренса и т. п. Полипептиды с нежелательными характеристиками разрабатываемости обладают, например, относительно низкой растворимостью, относительно высокой вязкостью, относительно высокой предрасположенностью к агрегации, относительно неудовлетворительной химической стабильностью, относительно неудовлетворительной физической стабильностью, относительно коротким «сроком хранения», относительно низкой температурой плавления, относительно коротким периодом полужизни в кровотоке, относительно коротким временем клиренса и т.п.
Способы и анализы, которые можно использовать для определения степени, в которой полипептиды, такие как антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в данном документе, обладают требуемыми свойствами разрабатываемости, доступны в данной области техники и включают, например, анализы PSR (WO 2014/179363 и Xu et al., Protein Eng Des Sel, Vol. 26, pages 663-670 (2013)); анализы SMP и SCP и т. п.; хроматографию перекрестного взаимодействия (CIC); хроматографию самовзаимодействия (SIC); динамическое светорассеяние; эксклюзионную хроматографию (SEC), спектроскопию с динамическим светорассеянием (DLS); фотоннокорреляционную спектроскопию; квазиупругое светорассеяние, круговой дихроизм (CD), измерения вязкости; связывание цельных клеток; методы с применением микропанелей тканей; анализы BVP ELISA; анализы AC-SINS (Liu et al; MAbs, Vol. 6, pages 483-492 (2014); дифференциальную сканирующую калориметрию и т. д. (см., например, He et al., J. Pharm. Sci., Vol. 100(4), pp. 1330-1340 (2011); Wagner et al., Pharm. Develop. & Technol (опубликовано онлайн в 2012 году; протокол передачи гипертекста: informahealthcare.com/doi/abs/10.3109/10837450.2011.649851); Hotzel et al., MAbs, Vol. 4(6), pages 753-7601 (2012); Weiqiang et al., J. Pharm. Sci., Vol. 101(5), pp. 1701-1720 (2012); Banks et al., J. Pharm. Sci., Vol. 101(8), pp. 2720-2732 (2012); Lie et al., J. Pharm. Sci., Vol. 94(9), pp. 1928-1948 (2005); и Payne et al., Biopolymers, Vol. 85(5), pp. 527-533 (2006)).
В некоторых вариантах осуществления антитела, которые идентифицированы как характеризующиеся сниженной разрабатываемостью, считаются такими благодаря их взаимодействию с реагентом полиспецифичности («PSR») и, собственно, называются «полиспецифическими» полипептидами. Такие полиспецифические антитела могут называться относительно «не подлежащими разработке» или считаться антителами с относительно «не возможной разработкой».
«Профиль разрабатываемости» относится к индексу, который может быть присвоен антителам при оценке их разрабатываемости. Профиль разрабатываемости является оценкой или мерой, посредством которой можно оценить, сравнить и/или ранжировать разрабатываемость антител к CD3. Такие профили разрабатываемости служат в качестве оценки степени взаимодействия молекул, связывающих CD3, и содержащих их антител. Степень взаимодействия можно оценить с помощью любого из ряда средств, доступных в данной области техники, которые обеспечивают выходное значение, коррелирующее с силой или аффинностью полипептида в отношении фрагмента, с которым он связывается. Примеры средств включают средства проточной цитометрии, например FACS; ELISA; количественные анализы иммунной аффинности или анализы иммунопреципитации; двугибридные анализы с клетками млекопитающих или двугибридные анализы с дрожжевыми клетками и т. п. В контексте FACS, как продемонстрировано в разделе Примеры, степень взаимодействия между полипептидами из совокупности и PSR можно определять путем получения средней интенсивности флуоресценции (MFI) для каждого выявляемого взаимодействия полипептид-PSR и последующего расположения MFI либо в возрастающем, либо в убывающем порядке, ранжируя тем самым полипептиды из совокупности в соответствии с относительной степенью взаимодействия между каждым выявленным полипептидом и PSR. Такое ранжирование обеспечивает ранжирование полипептидов из совокупности таким образом, что легко определить полипептиды, которые характеризуются улучшенной разрабатываемостью, а также полипептиды, которые характеризуются сниженной разрабатываемостью.
Профиль разрабатываемости также может принимать форму нормализованной оценки, например, путем нормализации разрабатываемости антител к CD3, описанных в настоящем документе, до разрабатываемости стандартного (или контрольного) антитела, например, антитела к HEL.
В определенных вариантах осуществления сконструированные рН-зависимые домены, связывающие CD3, и содержащие их антитела по настоящему изобретению могут быть дополнительно модифицированы так, чтобы они содержали дополнительные небелковые фрагменты, которые известны из уровня техники и являются легкодоступными. Фрагменты, подходящие для дериватизации антитела, включают без ограничения водорастворимые полимеры. Неограничивающие примеры водорастворимых полимеров включают без ограничения полиэтиленгликоль (PEG), сополимеры этиленгликоля/пропиленгликоля, карбоксиметилцеллюлозу, декстран, поливиниловый спирт, поливинилпирролидон, поли-1,3-диоксолан, поли-1,3,6-триоксан, сополимер этилена/малеинового ангидрида, полиаминокислоты (или гомополимеры, или статистические сополимеры), а также декстран или поли(н-винилпирролидон)полиэтиленгликоль, гомополимеры полипропиленгликоля, сополимеры полипропиленоксида/этиленоксида, полиоксиэтилированные полиолы (например, глицерин), поливиниловый спирт и их смеси. Полиэтиленгликольпропиональдегид может иметь преимущества в производстве, которые обусловлены его стабильностью в воде. Полимер может иметь любую молекулярную массу и может быть разветвленным или неразветвленным. Число полимеров, присоединенных к антителу может варьировать, и в случае присоединения более одного полимера они могут представлять собой одинаковые или разные молекулы. Обычно число и/или тип полимеров, применяемых для дериватизации, можно определяться, исходя из факторов, включающих без ограничения конкретные свойства или функции антитела, подлежащие усилению, будет ли производное антитела применяться в терапии при определенных условиях и т.д.
В некоторых вариантах осуществления сконструированные pH-зависимые домены, связывающие CD3, и содержащие их антитела демонстрируют улучшенный профиль разрабатываемости. Профиль разрабатываемости антител к CD3 получают, выполняя один или несколько из анализа PSR; анализа SCP; AC-SINS; ELISA; анализа DSF; анализа Tm; анализа HIC; анализа CIC; или их комбинации.
В других вариантах осуществления антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в настоящем документе, демонстрируют показатель полиспецифичности реагента (PSR), составляющий от приблизительно 0,0 до приблизительно 0,45. В некоторых вариантах осуществления PSR составляет от приблизительно 0,0 до приблизительно 0,4. В некоторых вариантах осуществления PSR составляет от приблизительно 0,0 до приблизительно 0,35. В некоторых вариантах осуществления PSR составляет от приблизительно 0,0 до приблизительно 0,3. В некоторых вариантах осуществления PSR составляет от приблизительно 0,0 до приблизительно 0,25. В некоторых вариантах осуществления PSR составляет от приблизительно 0,0 до приблизительно 0,2. В некоторых вариантах осуществления PSR составляет от приблизительно 0,0 до приблизительно 0,15. В некоторых вариантах осуществления PSR составляет от приблизительно 0,0 до приблизительно 0,1. В некоторых вариантах осуществления показатель 0,0-0,1 соответствует «чистому PSR». В некоторых вариантах осуществления показатель от 0,1 до 0,33 соответствует «низкому PSR». В некоторых вариантах осуществления показатель от 0,33 до 0,66 соответствует «среднему PSR». В некоторых вариантах осуществления показатель 0,66-1,00 соответствует «высокому PSR». В некоторых вариантах осуществления высокий показатель PSR указывает на пониженную (или неудовлетворительную) разрабатываемость. Как правило, чем ниже показатель PSR, тем благоприятнее профиль разрабатываемости антитела.
В других вариантах осуществления антитела к CD3 или их антигенсвязывающий фрагмент, описанные в настоящем документе, демонстрируют показатель HIC, составляющий менее чем приблизительно 10,5 минут (показатель HIC от чистого до низкого). В некоторых вариантах осуществления показатель HIC составляет от приблизительно 10,5 до 11,5 минут (средний показатель HIC). В некоторых вариантах осуществления показатель HIC превышает приблизительно 11,5 минут (высокий показатель HIC). Как правило, чем ниже показатель HIC, тем благоприятнее профиль разрабатываемости антитела.
В других вариантах осуществления антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в настоящем документе, демонстрируют показатель SEC, составляющий менее чем приблизительно 95%, что указывает на то, что антитело является мономером, то есть не агрегируется.
В других вариантах осуществления антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в настоящем документе, демонстрируют Tm, составляющую менее чем приблизительно 65°C.
В некоторых вариантах осуществления антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в данном документе, могут быть дополнительно модифицированы для минимизации эффекторной функции, например, молчащих Fc.
«Эффекторная функция» относятся к видам биологической активности, которые связаны с Fc-областью антитела, которая изменятся в зависимости от изотипа антитела. Примеры эффекторных функций включают связывание C1q и комплементзависимую цитотоксичность (CDC); связывание Fc-рецептора; антителозависимую клеточноопосредованную цитотоксичность (ADCC); фагоцитоз; понижающую регуляцию рецепторов клеточной поверхности (например, B-клеточного рецептора); и B-клеточную активацию.
«Fc-область» представляет собой С-концевую область тяжелой цепи иммуноглобулина, которая содержит по меньшей мере часть константной области, в том числе Fc-области с нативной последовательностью и варианты Fc-областей. Fc-область тяжелой цепи IgG человека может распространяться от Cys226 или от Pro230 до карбокси-конца тяжелой цепи. Однако C-концевой лизин (Lys447) Fc-области может присутствовать или может не присутствовать. Если в данном документе не указано иное, то нумерация аминокислотных остатков в Fc-области или константной области соответствует системе нумерации EU, также называемой индексом EU, как описано в Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md., 1991.
В определенных вариантах осуществления в Fc-область антитела к CD3 по настоящему изобретению может быть введена одна или более аминокислотных модификаций с получением тем самым варианта Fc-области (см., например, US 2012/0251531). Вариант Fc-области может содержать последовательность Fc-области человека (например, Fc-область IgG1, IgG2, IgG3 или IgG4 человека), содержащую аминокислотную модификацию (например, замену) в одном или более аминокислотных положений.
В определенных вариантах осуществления в настоящем изобретении предусмотрен вариант антитела к CD3, обладающий некоторыми, но не всеми эффекторными функциями, что делает его необходимым кандидатом для вариантов применения, в которых важен период полужизни антитела in vivo, в то время как некоторые эффекторные функции (такие как комплементзависимая и ADCC) являются необязательными или вредными. Для подтверждения снижения/устранения активности CDC и/или ADCC можно проводить in vitro и/или in vivo анализы цитотоксичности. Например, можно проводить анализы связывания с Fc-рецептором (FcR), чтобы убедиться в том, что антитело не проявляет связывания с FcγR (следовательно, вероятно, у него отсутствует активность ADCC), но сохраняет способность к связыванию с FcRn. Первичные клетки, опосредующие ADCC (например, NK-клетки), экспрессируют только FcγRIII, при этом моноциты экспрессируют FcγRI, FcγRII и FcγRIII. Экспрессия FcR на гемопоэтических клетках обобщена в таблице 3 на странице 464 в Ravetch and Kinet, Annu. Rev. Immunol. 9:457-492 (1991). Неограничивающие примеры in vitro анализов для оценки активности ADCC у представляющей интерес молекулы описаны в патенте США № 5500362 (см., например, Hellstrom, I. et al. Proc. Nat'l Acad. Sci. USA 83:7059-7063 (1986)) и Hellstrom, I et al., Proc. Nat'l Acad. Sci. USA 82:1499-1502 (1985); патент США № 5821337 (см., Bruggemann, M. et al., J. Exp. Med. 166:1351-1361 (1987)). В качестве альтернативы можно использовать способы анализа без применения радиоактивных веществ (см., например, ACTI™ нерадиоактивный анализ цитотоксичности с применением проточной цитометрии (Cell Technology, Inc., Маунтин-Вью, Калифорния, США) и нерадиоактивный анализ цитотоксичности CytoTox 96® (Promega, Медисон, Висконсин, США)). Применимые эффекторные клетки для таких анализов включают мононуклеарные клетки периферической крови (PBMC) и клетки природные киллеры (NK). В качестве альтернативы или дополнения активность ADCC у представляющей интерес молекулы можно оценивать in vivo, например, на животной модели, такой, которая раскрыта в Clynes et al. Proc. Nat'l Acad. Sci. USA 95:652-656 (1998). Также можно проводить анализы связывания с C1q, чтобы подтвердить, что антитело не способно к связыванию с C1q, и, следовательно, у него отсутствует активность CDC. См., например, ELISA для связывания C1q и C3c в WO 2006/029879 и WO 2005/100402. Для оценки активации комплемента можно осуществлять анализ CDC (см., например, Gazzano-Santoro et al. J. Immunol Methods 202:163 (1996); Cragg, M. S. et al. Blood. 101:1045-1052 (2003); и Cragg, M. S. and M. J. Glennie Blood. 103:2738-2743 (2004)). Связывание с FcRn и определение in vivo клиренса/периода полужизни также можно осуществлять с применением способов, известных из уровня техники (см., например, Petkova, S. B. et al. Int'l. Immunol 18(12):1759-1769 (2006)).
В некоторых вариантах осуществления антитела со сниженной эффекторной функцией включают антитела с заменой одного или более остатков 238, 265, 269, 270, 297, 327 и 329 Fc-области (патенты США №№ 6737056 и 8219149). В некоторых вариантах осуществления такие Fc-мутанты включают Fc-мутантов с заменами в двух или более аминокислотных положениях 265, 269, 270, 297 и 327, включая так называемого Fc-мутанта «DANA» с заменой остатков 265 и 297 на аланин (патенты США №№ 7332581 и 8219149).
В других вариантах осуществления антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в данном документе, дополнительно модифицированы для включения маскирующего средства, например, полипептидной маски, присоединенной посредством расщепляемого линкера.
В некоторых вариантах осуществления антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в данном документе, конъюгированы с терапевтическим фрагментом, с получением таким образом иммуноконъюгата. «Иммуноконъюгат» представляет собой антитело, конъюгированное с одной или несколькими гетерологичными молекулами, такими как, например, антибиотик, второе антитело к CD3, вакцина или токсоид, или любой другой терапевтический фрагмент.
В некоторых вариантах осуществления антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в настоящем документе, изменены для увеличения или уменьшения степени гликозилирования антитела. Добавление или удаление сайтов гликозилирования в антитело к CD3 по настоящему изобретению можно легко осуществлять путем изменения аминокислотной последовательности таким образом, чтобы создавать или удалять один или более сайтов гликозилирования.
Получение антител к CD3 и их антигенсвязывающих фрагментов
Антитела к CD3 и/или их антигенсвязывающие фрагменты могут быть получены с применением рекомбинантных методик. Например, представлены выделенные нуклеиновые кислоты, кодирующие антитело к CD3, описанное в данном документе. Такие нуклеиновые кислоты могут кодировать аминокислотную последовательность, предусматривающую VL, и/или аминокислотную последовательность, предусматривающую VH антитела (например, легкую и/или тяжелую цепи антитела). В дополнительном варианте осуществления представлены один или более векторов (например, векторы экспрессии), содержащих такие нуклеиновые кислоты. В дополнительном варианте осуществления представлена клетка-хозяин, содержащая такие нуклеиновые кислоты. В одном таком варианте осуществления клетка-хозяин содержит (например, была трансформирована с помощью) (1) вектор, содержащий последовательность нуклеиновой кислоты, которая кодирует аминокислотную последовательность, предусматривающую VL антитела, и аминокислотную последовательность, предусматривающую VH антитела, или (2) первый вектор, содержащий нуклеиновую кислоту, которая кодирует аминокислотную последовательность, предусматривающую VL антитела, и второй вектор, содержащий нуклеиновую кислоту, которая кодирует аминокислотную последовательность, предусматривающую VH антитела. В одном варианте осуществления клетка-хозяин является эукариотической, например, клеткой яичников китайского хомячка (CHO) или лимфоидной клеткой (например, клеткой Y0, NS0, Sp20). В одном варианте осуществления представлен способ получения антитела к CD3, где способ предусматривает культивирование клетки-хозяина, содержащей нуклеиновую кислоту, кодирующую представленное выше антитело, при условиях, подходящих для экспрессии антитела, и необязательно извлечение антитела из клетки-хозяина (или культуральной среды клетки-хозяина).
Термин «клетка-хозяин» относится к клеткам, в которые была введена последовательность экзогенной нуклеиновой кислоты, включая потомство таких клеток. Клетки-хозяева включают трансформантов и трансформированные клетки, которые включают первичную трансформированную клетку и полученное от нее потомство без учета количества пассажей.
В случае рекомбинантного получения антитела к CD3 нуклеиновые кислоты, кодирующие антитело, например, описанное выше, выделяют и вставляют в один или более векторов для дальнейшего клонирования в клетку-хозяина и/или экспрессии в ней. Такие нуклеиновые кислоты можно легко выделять и секвенировать с применением традиционных процедур (например, с применением олигонуклеотидных зондов, которые способны специфически связываться с генами, кодирующими тяжелую и легкую цепи антитела).
Подходящие клетки-хозяева для клонирования и/или экспрессии векторов, кодирующих антитело, включают прокариотические или эукариотические клетки. Например, антитело может быть получено в бактериях, в частности, если не требуется гликозилирование и эффекторная функция Fc. Касательно экспрессии фрагментов антитела и полипептидов в бактериях см., например, патенты США №№ 5648237, 5789199 и 5840523. (См. также, Charlton, Methods in Molecular Biology, Vol. 248 (B.K.C. Lo, ed., Humana Press, Totowa, N.J., 2003), pp. 245-254, где описана экспрессия фрагментов антитела в E. coli.) После экспрессии антитело может быть выделено из массы бактериальных клеток в растворимой фракции и может быть дополнительно очищено. Помимо прокариот, подходящими хозяевами для клонирования или экспрессии векторов, кодирующих антитело, являются эукариотические микроорганизмы, такие как мицелиальные грибы или дрожжи, включая грибы и штаммы дрожжей, пути гликозилирования которых были подвергнуты «гуманизации», что приводит к продуцированию антител с частично или полностью человеческим паттерном гликозилирования. См., например, Gerngross, Nat. Biotech. 22:1409-1414 (2004) и Li et al., Nat. Biotech. 24:210-215 (2006); WO 2009/036379; WO 2010/105256; и WO 2012/009568.
В качестве хозяев также могут использоваться культуры клеток растений. См., например, патенты США №№ 5959177, 6040498, 6420548, 7125978 и 6417429 (описывающие технологию PLANTIBODIES™ для получения антител в трансгенных растениях). В качестве хозяев также могут применяться клетки позвоночных организмов. Например, можно применять линии клеток млекопитающих, которые адаптированы для роста в суспензии. Другими примерами применимых линий клеток-хозяев, представляющих собой клетки млекопитающих, является линия клеток почки обезьяны CV1, трансформированная с помощью SV40 (COS-7); линия клеток почки эмбриона человека (293 или клетки 293, описанные, например, в Graham et al., J. Gen Virol. 36:59 (1977)); клетки почки детенышей хомячка (BHK); мышиные клетки Сертоли (клетки TM4, описанные, например, в Mather, Biol. Reprod. 23:243-251 (1980)); клетки почки обезьяны (CV1); клетки почки африканской зеленой мартышки (VERO-76); клетки карциномы шейки матки человека (HELA); клетки почки собаки (MDCK); клетки печени крысы линии Buffalo (BRL 3A); клетки легкого человека (W138); клетки печени человека (Hep G2); клетки опухоли молочной железы мыши (MMT 060562); клетки TRI, описанные, например, в Mather et al., Annals N.Y. Acad. Sci. 383:44-68 (1982); клетки MRC 5; и клетки FS4. Другие применимые линии клеток-хозяев, представляющие собой клетки млекопитающих, включают клетки яичника китайского хомячка (CHO), включая клетки DHFR-CHO (Urlaub et al., Proc. Natl. Acad. Sci. USA 77:4216 (1980)); и линии клеток миеломы, такие как Y0, NS0 и Sp2/0. Обзор некоторых линий клеток-хозяев, представляющих собой клетки млекопитающих, подходящих для получения антител, см, например, в Yazaki and Wu, Methods in Molecular Biology, Vol. 248 (B.K.C. Lo, ed., Humana Press, Totowa, N.J.), pp. 255-268 (2003).
Антитела к CD3 и/или их антигенсвязывающие фрагменты можно идентифицировать, подвергать скринингу, отбирать или характеризовать по их физическим/химическим свойствам и/или биологической активности с помощью различных анализов, известных в данной области, например, ELISA, вестерн-блоттинга и т. д., или могут применяться анализы конкурентного связывания для идентификации антитела, которое конкурирует с антителом к CD3 по настоящему изобретению за связывание с CD3. В иллюстративном анализе конкурентного связывания иммобилизованный CD3 инкубируют в растворе, содержащем первое меченое антитело, которое связывается с CD3, и второе немеченое антитело, которое подлежит тестированию в отношении его способности конкурировать с первым антителом за связывание с CD3. Второе антитело может присутствовать в супернатанте гибридомы. В качестве контроля иммобилизованный CD3 инкубируют в растворе, содержащем первое меченое антитело, но не содержащем второе немеченое антитело. После инкубации при условиях, которые допускают связывание первого антитела с CD3, избыток несвязавшегося антитела удаляют и измеряют количество метки, ассоциированной с иммобилизованным CD3. Если количество метки, ассоциированной с иммобилизированным CD3, значительно снижено в тестовом образце по сравнению с контрольным образцом, тогда это указывает на то, что второе антитело конкурирует с первым антителом за связывание с CD3. См., например, Harlow and Lane (1988) Antibodies: A Laboratory Manual. Ch.14 (Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y.).
Антитела к CD3 и/или их антигенсвязывающие фрагменты, характеризующиеся биологической активностью, можно идентифицировать с использованием стандартных подходов. Биологическая активность может включать, например, связывание с CD3 на поверхности T-клетки или in vivo, in vitro, или ex vivo. В случае мультиспецифического антитела к CD3 (например, биспецифическое антитело с одним плечом, которое связывается с CD3, и другим плечом, которое связывается с другой мишенью, например, антигеном клеточной поверхности, например, опухолевым антигеном), биологическая активность может также включать активацию эффекторных клеток (например, активацию CD8+ и/или CD4+ Т-клеток), рост популяции эффекторных клеток (то есть увеличение количества Т-клеток), сокращение популяции целевых клеток (то есть уменьшение популяции клеток, экспрессирующих вторую биологическую молекулу на поверхности их клеток) и/или уничтожение целевых клеток.
Диагностические и терапевтические пути применения антител к CD3 и их антигенсвязывающих фрагментов
Описанные в данном документе антитела к CD3 и/или антигенсвязывающие фрагменты можно использовать для диагностики и/или осуществления выявления. Применяемый в данном документе термин «осуществление выявления» охватывает количественное или качественное выявление.
В определенных вариантах осуществления представлены меченые антитела к CD3. Антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в данном документе, могут включать метку или фрагмент, который определяют непосредственно (например, флуоресцентные, хромофорные, электронно-плотные, хемилюминесцентные и радиоактивные метки, или опосредованно (например, ферменты или лиганды). Иллюстративные метки включают без ограничения радиоизотопы 32P, 14C, 125I, 3H и 131I, флуорофоры, такие как хелаты редкоземельных металлов или флуоресцеин и его производные, родамин и его производные, дансил, умбеллиферон, люциферазы, например, люциферазу светлячка и бактериальную люциферазу (патент США № 4737456), люциферин, 2,3-дигидрофталазиндионы, пероксидазу хрена (HRP), щелочную фосфатазу, β-галактозидазу, глюкоамилазу, лизоцим, сахаридоксидазы, например, глюкооксидазу, галактозоксидазу и глюкоза-6-фосфат-дегидрогеназу; гетероциклические оксидазы, такие как уриказа и ксантиноксидаза, сопряженные с ферментом, который использует пероксид водорода для окисления красителя-предшественника, с таким как HRP, лактопероксидаза или микропероксидаза; биотин/авидин; спиновые метки; метки на основе бактериофагов; стабильные свободные радикалы и т.п.
-Антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в данном документе, а также фармацевтические композиции таких антител можно применять в терапевтических целях. В одном варианте осуществления антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в данном документе, или фармацевтические композиции, содержащие такие антитела, можно применять для лечения или замедления прогрессирования клеточного пролиферативного нарушения или аутоиммунного нарушения. В некоторых вариантах осуществления антитела к CD3 и их антигенсвязывающие фрагменты можно применять при лечении рака. Опухолевые клетки как правило имеют внеклеточный уровень pH приблизительно 6,3-6,5; описанные в данном документе антитела к CD3 и антигенсвязывающие фрагменты способствуют преимущественному связыванию CD3 при низких (более низких) значениях pH, например, около pH 6, и тем самым способствуют связыванию и активности в пределах микроокружения опухоли и вокруг него. В некоторых вариантах осуществления применение антител к CD и их антигенсвязывающих фрагментов может приводить к селективной и устойчивой цитотоксической активности в опухолевом участке или вокруг него, тем самым снижая или устраняя нецелевые эффекты.
«Нарушение» относится к любому состоянию или заболеванию, лечение которых будет приводить к положительному результату, включая без ограничения хронические и острые нарушения или заболевания, в том числе такие патологические состояния, которые провоцируют рассматриваемое нарушение у млекопитающего.
Термины «клеточное пролиферативное нарушение» и «пролиферативное нарушение» относятся к нарушениям, которые ассоциированы с нарушенной до определенной степени пролиферацией клеток. Нарушения пролиферации клеток включают рак, например опухоль.
Используемый в данном документе термин «опухоль» относится к росту и пролиферации всех неопластических клеток, независимо от того, являются они злокачественными или доброкачественными, и ко всем предраковым и раковым клеткам и тканям.
«Рак» относится к физиологическому состоянию млекопитающих, характеризующемуся нерегулируемым ростом клеток. Примеры рака включают без ограничения карциному, лимфому, бластому, саркому и лейкоз или злокачественные новообразования лимфоидной ткани с более конкретными примерами, включающими без ограничения плоскоклеточный рак (например, эпителиальный плоскоклеточный рак), рак легкого, включая мелкоклеточный рак легкого, немелкоклеточный рак легкого, аденокарциному легкого и плоскоклеточную карциному легкого, рак брюшины, гепатоцеллюлярный рак, желудочный рак или рак желудка, включая гастроинтестинальный рак и гастроинтестинальный стромальный рак, рак поджелудочной железы, глиобластому, рак шейки матки, рак яичника, рак печени, рак мочевого пузыря, рак мочевыводящих путей, гепатому, рак молочной железы, рак толстого кишечника, рак прямой кишки, колоректальный рак, карциному эндометрия или матки, карциному слюнной железы, рак почки или почечный рак, рак предстательной железы, рак вульвы, рак щитовидной железы, карциному печени, карциному анального канала, карциному полового члена, меланому, поверхностно распространяющуюся меланому, меланому типа злокачественного лентиго, виды акральной лентигинозной меланомы, виды узловатой меланомы, множественную миелому и B-клеточную лимфому (включая низкой степени злокачественности/фолликулярную неходжкинскую лимфому (NHL); мелкоклеточную лимфоцитарную (SL) NHL; промежуточной степени злокачественности/фолликулярную NHL; диффузную NHL промежуточной степени злокачественности; иммунобластную NHL высокой степени злокачественности; лимфобластную NHL высокой степени злокачественности; мелкоклеточную NHL с нерассеченными ядрами высокой степени злокачественности; генерализованную NHL; лимфому из клеток мантийной зоны; лимфому, ассоциированную со СПИДом; и макроглобулинемию Вальденстрема); хронический лимфоцитарный лейкоз (CLL); острый лимфобластный лейкоз (ALL); волосатоклеточный лейкоз; хронический миелобластный лейкоз и посттрансплантационное лимфопролиферативное нарушение (PTLD), а также аномальную сосудистую пролиферацию, ассоциированную с факоматозами, отек (такой как ассоциированный с опухолями головного мозга), синдром Мейгса, рак головного мозга, а также рак головы и шеи и ассоциированные с ними метастазы. В определенных вариантах осуществления виды рака, которые поддаются лечению антителами по настоящему изобретению, включают рак молочной железы, колоректальный рак, рак прямой кишки, немелкоклеточный рак легкого, глиобластому, неходжкинскую лимфому (NHL), почечно-клеточный рак, рак предстательной железы, рак печени, рак поджелудочной железы, саркому мягких тканей, саркому Капоши, карциноидную карциному, рак головы и шеи, рак яичника, мезотелиому и множественную миелому. В некоторых вариантах осуществления рак выбран из мелкоклеточного рака легкого, глиобластомы, видов нейробластомы, меланомы, карциномы молочной железы, рака желудка, колоректального рака (CRC) и гепатоцеллюлярной карциномы. При этом в некоторых вариантах осуществления рак выбран из немелкоклеточного рака легкого, колоректального рака, глиобластомы и карциномы молочной железы, в том числе метастатических форм этих видов рака. В других вариантах осуществления рак выбран из класса видов зрелого B-клеточного рака за исключением лимфомы Ходжкина, но включая DLBCL B-клеточного типа из герминативного центра (GCB), активную DLBCL B-клеточного типа (ABC), фолликулярную лимфому (FL), лимфому из клеток мантийной зоны (MCL), острый миелоидный лейкоз (AML), хронический лимфоидный лейкоз (CLL), лимфому из клеток маргинальной зоны (MZL), мелкоклеточный лимфоцитарный лейкоз (SLL), лимфоплазмацитарную лимфому (LL), макроглобулинемию Вальденстрема (WM), лимфому центральной нервной системы (CNSL), лимфому Беркитта (BL), B-клеточный пролимфоцитарный лейкоз, лимфому из клеток маргинальной зоны селезенки, волосатоклеточный лейкоз, лимфому/лейкоз селезенки, неклассифицируемую диффузную B-мелкоклеточную лимфому из красной пульпы селезенки, вариант волосатоклеточного лейкоза, макроглобулинемию Вальденстрема, болезни тяжелых цепей, болезнь тяжелых цепей, болезнь тяжелой γ-цепи, болезнь тяжелой μ-цепи, плазмаклеточную миелому, солитарную плазмацитому кости, внекостную плазмацитому, экстранодальную лимфому из клеток маргинальной зоны лимфоидной ткани слизистых оболочек (MALT-лимфому), узловую лимфому из клеток маргинальной зоны, узловую лимфому из клеток маргинальной зоны у детей, фолликулярную лимфому у детей, первичную кожную лимфому из клеток фолликулярного центра, B-крупноклеточную лимфому, богатую Т-клетками/гистиоцитами, первичную DLBCL ЦНС, первичную кожную DLBCL, ножного типа, EBV-положительную DLBCL у лиц пожилого возраста, DLBCL, ассоциированную с хроническим воспалением, лимфоматоидный гранулематоз, первичную средостенную (тимическую) B-крупноклеточную лимфому, интраваскулярную B-крупноклеточную лимфому, ALK-положительную B-крупноклеточную лимфому, плазмобластную лимфому, B-крупноклеточную лимфому, возникающую при HHV8-ассоциированной многоочаговой болезни Кастлемана, первичную выпотную лимфому: B-клеточную лимфому, неклассифицируемую, занимающую промежуточное положение по признакам между диффузной В-крупноклеточной лимфомой и лимфомой Беркитта, и B-клеточную лимфому, неклассифицируемую, занимающую промежуточное положение по признакам между диффузной В-крупноклеточной лимфомой и классической лимфомой Ходжкина.
Используемое в данном документе «лечение», или «лечить», или «осуществлять лечение» относятся к клиническому вмешательству в попытке изменить естественное течение заболевания у подлежащего лечения индивидуума, и его можно проводить либо для профилактики, либо во время клинического исследования. Требуемые эффекты лечения включают без ограничения предупреждение возникновения или рецидива заболевания, облегчение симптомов, снижение любых непосредственных или опосредованных патологических последствий заболевания, предотвращение метастазирования, снижение скорости прогрессирования заболевания, уменьшение тяжести или облегчение болезненного состояния, а также ремиссию или улучшение прогноза.
Используемые в данном документе термины «предупреждать», «осуществление предупреждения» и «предупреждение» относятся к предупреждению или подавлению развития, или возникновения нарушения или заболевания.
Используемые в данном документе термины «уменьшение тяжести» и «облегчение» относятся к уменьшению или снижению тяжести состояния или любого из его симптомов.
В некоторых вариантах осуществления антитела по настоящему изобретении применяют для замедления развития нарушения или заболевания или для замедления прогрессирования нарушения или заболевания. Используемое в данном документе «замедление прогрессирования» нарушения или заболевания означает задерживание, препятствование, уменьшение скорости, замедление, стабилизацию и/или отсрочивание развития заболевания или нарушения (например, клеточного пролиферативного нарушения, например, рака). Данное замедление может варьировать по времени в зависимости от анамнеза заболевания и/или индивидуума, подлежащего лечению.
Эффективное количество такого антитела или композиции можно вводить индивидууму, страдающему раком или артритом, ревматоидным артритом, колитом, воспалительным заболеванием кишечника, аутоиммунным диабетом I типа и т.д. «Эффективное количество» антитела к CD3, раскрытого в данном документе, или композиции (например, фармацевтической композиции), содержащей такое антитело, представляет собой по меньшей мере минимальное количество, необходимое для достижения требуемого терапевтического или профилактического результата, такого как измеримое улучшение или предупреждение конкретного нарушения, например, клеточного пролиферативного нарушения, например, рака, предпочтительно с минимальными токсическими или вредными эффектами, или без них. Эффективное количество может варьировать, среди прочего, в зависимости от болезненного состояния, возраста, пола и веса пациента, а также способности антитела (или его антигенсвязывающего фрагмента) вызывать требуемый ответ у индивидуума и, в некоторых случаях, путем совместного введения одного или нескольких дополнительных терапевтических средств.
В некоторых вариантах осуществления антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в данном документе, можно применять для усиления иммунной функции у индивидуума, страдающего клеточным пролиферативным нарушением или аутоиммунным нарушением. После введения такое антитело или композиция могут усиливать иммунную функцию у индивидуума, страдающего клеточным пролиферативным нарушением или аутоиммунным нарушением, путем активации эффекторных клеток (например, Т-клеток, например, CD8+ и/или CD4+ Т-клеток, в том числе Treg), роста (увеличения) популяции эффекторных клеток, снижения популяции целевых клеток (например, клетки, экспрессирующие вторую биологическую молекулу, распознаваемую антителом к CD3 по настоящему раскрытию, например, биспецифическим антителом), и/или уничтожения целевой клетки (например, целевой опухолевой клетки).
Антитела к CD3 и/или их антигенсвязывающие фрагменты, раскрытые в данном документе, можно применять для лечения нарушений, в том числе без ограничения пролиферативное нарушение, онкологическое нарушение, иммуноонкологическое нарушение, неврологическое нарушение, когнитивное нарушение, нейродегенеративное нарушение, аутоиммунное нарушение. В одном варианте осуществления эффективное количество такого антитела к CD3 можно вводить отдельно или в комбинации с по меньшей мере одним дополнительным средством индивидууму, страдающему таким нарушением. Таким «индивидуумом» может быть млекопитающее и, в частности, человек.
Неограничивающие иллюстративные дополнительные терапевтические средства включают химиотерапевтическое средство, конъюгат антитело-лекарственное средство (ADC) и/или биологический модификатор. Химиотерапевтические средства могут быть выбраны из циклофосфамида, доксорубицина, винкристина и преднизолона (CHOP). ADC может быть выбран из конъюгата антитела к CD79b и лекарственного средства (такого как антитело к-CD79b-MC-vc-PAB-MMAE или конъюгат антитела к CD79b и лекарственного средства, описанных в любом из патента США № 8088378 и/или US 2014/0030280, или полатузумаб-ведотин), конъюгата антитела к CD19 и лекарственного средства, конъюгата антитела к CD22 и лекарственного средства, конъюгата антитела к CD45 и лекарственного средства и конъюгата антитела к CD32 и лекарственного средства. Биологический модификатор может быть выбран из ингибитора BCL-2 (такого как GDC-0199/ABT-199), леналидомида (Revlimid®), ингибитора PI3K-дельта (такого как иделалисиб (Zydelig®)), антагониста связывания PD-1-оси, агониста, например, антитела-агониста, направленного против активирующей костимулирующей молекулы, например, CD40, CD226, CD28, OX40 (например, AgonOX), GITR, CD137 (также известного как TNFRSF9, 4-1 BB или ILA), CD27 (например, CDX-1127), HVEM или CD127, антагониста, например, антитела-антагониста, направленного против ингибирующей костимулирующей молекулы, например, CTLA-4 (также известной как CD152), PD-1, TIM-3, BTLA, VISTA, LAG-3, B7-H3, B7-H4, IDO (например, 1-метил-D-триптофан (также известного как 1-D-MT)), TIGIT, MICA/B, GITR (например, TRX518) или аргиназы, ипилимумаба (также известного как MDX-010, MDX-101 или Yervoy®), тремелимумба (также известного как тицилимумаб или CP-675,206), урелумаба (также известного как BMS-663513), MGA271, антагониста, направленного против TGF-бета, например, метелимумаба (также известного как CAT-192), фрезолимумаба (также известного как GC1008), LY2157299k, и адоптивного переноса T-клетки (например, цитотоксической T-клетки или CTL), экспрессирующей химерный антигенный рецептор (CAR), например, адоптивного переноса T-клетки, содержащей доминантно-негативный рецептор TGF-бета, например, доминантно-негативный рецептор TGF-бета II типа.
Антитела к CD3 и/или их антигенсвязывающие фрагменты, раскрытые в настоящем документе, можно применять для усиления иммунной функции у индивидуума, например человека, страдающего нарушением, у индивидуума, страдающего таким нарушением. В одном варианте осуществления способ усиления иммунной функции предусматривает введение индивидууму эффективного количества антитела к CD3 для активации эффекторных клеток (например, T-клеток, например, CD8+ и/или CD4+ T-клеток), роста (увеличения) популяции эффекторных клеток, снижения популяции целевых клеток и/или уничтожения целевой клетки (например, целевой опухолевой клетки).
В дополнительном аспекте фармацевтические составы, содержащие антитела к CD3 и/или антигенсвязывающие фрагменты, описанные в данном документе, также предоставляются, например, для применения в любом из вышеуказанных терапевтических способов. Термин «фармацевтический состав» относится к препарату, который находится в такой форме, чтобы обеспечивать биологическую активность содержащегося в нем активного ингредиента, такого как антитела к CD3, описанные в данном документе, чтобы быть эффективным, и который предпочтительно не содержит дополнительных компонентов, которые являются недопустимо токсичными для субъекта, которому будут вводить состав.
В одном варианте осуществления фармацевтический состав содержит любое из антител к CD3, раскрытых в данном документе, и фармацевтически приемлемый носитель. «Фармацевтически приемлемый носитель» относится к ингредиенту в фармацевтическом составе, который не является активным ингредиентом и нетоксичен для субъекта. Фармацевтически приемлемый носитель включает без ограничения буфер, вспомогательное вещество, стабилизатор или консервант. В другом варианте осуществления фармацевтический состав содержит любое из антител к CD3, представленных в данном документе, и по меньшей мере одно дополнительное терапевтическое средство.
Антитела по настоящему изобретению можно применять либо отдельно, либо в комбинации с другими средствами в терапии, например, антитело к CD3 и/или его антигенсвязывающий фрагмент можно вводить совместно по меньшей мере с одним дополнительным терапевтическим средством. В определенных вариантах осуществления дополнительное терапевтическое средство представляет собой химиотерапевтическое средство, средство, ингибирующее рост, цитотоксическое средство, средство, применяемое в лучевой терапии, антиангиогенное средство, апоптическое средство, противотубулиновое средство или другое средство, такое как антагонист рецептора эпидермального фактора роста (EGFR) (например, ингибитор тирозинкиназы), ингибитор HER1/EGFR (например, эрлотиниб (Tarceva™)), ингибитор фактора роста тромбоцитов (например, Gleevec™ (иматиниба мезилат)), ингибитор COX-2 (например, целекоксиб), интерферон, цитокин, антитело, отличное от антитела к CD3 по настоящему изобретению, такое как антитело, которое связывается с одной или более из следующих мишеней: ErbB2, ErbB3, ErbB4, PDGFR-бета, BIyS, APRIL, BCMA VEGF или рецептором(ами) VEGF, TRAIL/Apo2, PD-1, PD-L1, PD-L2 или другим биологически активным или органическим химическим средством.
В некоторых вариантах осуществления в настоящем изобретении представлен способ, где дополнительное терапевтическое средство представляет собой глюкокортикоид. В одном варианте осуществления глюкокортикоид представляет собой дексаметазон.
Такие виды комбинированной терапии, отмеченные выше, охватывают комбинированное введение (при котором два или более терапевтических средств включают в один и тот же или отдельные составы) и раздельное введение, в случае которого введение антитела по настоящему изобретению может происходить до, одновременно и/или после введения дополнительного терапевтического средства или средств. В одном варианте осуществления введение антитела к CD3 и введение дополнительного терапевтического средства происходит в пределах приблизительно одного месяца, или в пределах приблизительно одной, двух или трех недель, или в пределах приблизительно одной, двух, трех, четырех, пяти или шести дней друг от друга. Антитела к CD3 по настоящему изобретению (например, биспецифические антитела к CD3 по настоящему изобретению, которые связываются с CD3 и второй биологической молекулой, например, антигеном клеточной поверхности, например, опухолевым антигеном, таким как TDB-антитело по настоящему изобретению или его вариантом) также можно применять в комбинации с лучевой терапией.
Антитело по настоящему изобретению (и/или любое дополнительное терапевтическое средство) может быть введено с помощью любых подходящих способов, включая парентеральное, внутрилегочное и интраназальное и, если это требуется для местного лечения, внутриочаговое введение. Парентеральные инфузии включают внутримышечное, внутривенное, внутриартериальное, внутрибрюшинное или подкожное введение. В некоторых вариантах осуществления антитело вводят с помощью подкожного введения. В некоторых вариантах осуществления антитело к CD3, введенное с помощью подкожной инъекции, проявляет менее токсичный ответ у пациента, чем то же антитело к CD3, вводимое с помощью внутривенной инъекции. Введение дозы может осуществляться с помощью любого подходящего пути введения, например, посредством инъекций, таких как внутривенные или подкожные инъекции, отчасти в зависимости от того, является ли введение краткосрочным или хроническим. В данном документе подразумеваются различные схемы введения доз, включая без ограничения однократное или множественное введения через различные моменты времени, болюсное введение и импульсную инфузию.
Антитела по настоящему изобретению будут составляться, разделяться на дозы и вводиться в соответствии с надлежащей медицинской практикой. Факторы, рассматриваемые в данном контексте, включают конкретное подлежащее лечению нарушение, конкретного подлежащего лечению млекопитающего, клиническое состояние отдельного пациента, причину нарушения, участок для доставки средства, способ введения, схему введения и другие факторы, известные практикующим врачам. Антитело не должно, но необязательно может быть составлено с одним или более средствами, применяемыми в настоящее время для предупреждения или лечения рассматриваемого нарушения. Эффективное количество таких других средств зависит от количества антитела, присутствующего в составе, типа нарушения или лечения, и других факторов, рассмотренных выше. Их обычно применяют в таких же дозировках и путях введения, которые описаны в данном документе, или в дозировках, составляющих от приблизительно 1 до 99% от дозировок, описанных в данном документе, или в любой дозировке и посредством любого пути, которые эмпирически/клинически определены как подходящие.
В случае предупреждения или лечения заболевания подходящая дозировка антитела по настоящему изобретению (применяемого отдельно или в комбинации с одним или более другими дополнительными терапевтическими средствами) будет зависеть от типа подлежащего лечению заболевания, типа антитела, тяжести и течения заболевания, от того, вводится ли антитело в профилактических или терапевтический целях, предшествующей терапии, клинического анамнеза пациента и ответа на антитело, а также решения лечащего врача. Антитело соответствующим образом вводят пациенту за один момент времени или в течении серии обработок.
В качестве общего предложения терапевтически эффективное количество антитела к CD3, вводимое человеку, будет находиться в диапазоне от приблизительно 0,01 до приблизительно 100 мг/кг веса тела пациента, независимо от того, вводится ли оно за одно или более введений. В некоторых вариантах осуществления, например, антитело применяют из расчета от приблизительно 0,01 до приблизительно 45 мг/кг, от приблизительно 0,01 до приблизительно 40 мг/кг, от приблизительно 0,01 до приблизительно 35 мг/кг, от приблизительно 0,01 до приблизительно 30 мг/кг, от приблизительно 0,01 до приблизительно 25 мг/кг, от приблизительно 0,01 до приблизительно 20 мг/кг, от приблизительно 0,01 до приблизительно 15 мг/кг, от приблизительно 0,01 до приблизительно 10 мг/кг, от приблизительно 0,01 до приблизительно 5 мг/кг или от приблизительно 0,01 до приблизительно 1 мг/кг при ежедневном введении. В одном варианте осуществления антитело к CD3, описанное в данном документе, вводят человеку в дозе, составляющей приблизительно 100 мг, приблизительно 200 мг, приблизительно 300 мг, приблизительно 400 мг, приблизительно 500 мг, приблизительно 600 мг, приблизительно 700 мг, приблизительно 800 мг, приблизительно 900 мг, приблизительно 1000 мг, приблизительно 1100 мг, приблизительно 1200 мг, приблизительно 1300 мг или приблизительно 1400 мг в день 1 циклов продолжительностью 21 день. Доза может вводится в виде однократной дозы или в виде множественных доз (например, 2 или 3 доз), таких как инфузии. В случае повторных введений через несколько дней или более, в зависимости от состояния, лечение обычно будет поддерживаться до проявления требуемого подавления симптомов заболевания. Одна иллюстративная дозировка антитела будет находиться в диапазоне от приблизительно 0,05 мг/кг до приблизительно 10 мг/кг. Таким образом, пациенту могут вводиться одна или более доз, составляющих приблизительно 0,5 мг/кг, 2,0 мг/кг, 4,0 мг/кг или 10 мг/кг (или любая их комбинация). Такие дозы могут вводиться с перерывами, например, через неделю или через три недели (например, так, чтобы пациент получил от приблизительно двух до приблизительно двадцати или, например, приблизительно шесть доз антитела к CD3). Может вводиться начальная более высокая ударная доза с последующими одной или более низкими дозами. Прогресс данной терапии легко отслеживать с помощью традиционных методик и анализов.
В некоторых вариантах осуществления способы по настоящему изобретению могут дополнительно предусматривать дополнительную терапию. Дополнительная терапия может представлять собой лучевую терапию, оперативное вмешательство, химиотерапию, генную терапию, ДНК-терапию, вирусную терапию, РНК-терапию, иммунотерапию, трансплантацию костного мозга, нанотерапию, терапию моноклональными антителами или комбинацию вышеуказанных. Дополнительная терапия может быть представлена в форме адъювантной или неоадъювантной терапии. В некоторых вариантах осуществления дополнительная терапия представляет собой введение низкомолекулярного ферментативного ингибитора или противометастатического средства. В некоторых вариантах осуществления дополнительная терапия представляет собой введение средств, ограничивающих побочные эффекты (например, средств, предназначенных для уменьшения частоты возникновения и/или тяжести побочных эффектов лечения, таких как противорвотные средства и т.д.). В некоторых вариантах осуществления дополнительная терапия представляет собой лучевую терапию. В некоторых вариантах осуществления дополнительная терапия представляет собой хирургическое вмешательство. В некоторых вариантах осуществления дополнительная терапия представляет собой комбинацию лучевой терапии и хирургического вмешательства. В некоторых вариантах осуществления дополнительная терапия представляет собой облучение гамма-лучами. В некоторых вариантах осуществления дополнительная терапия может представлять собой отдельное введение одного или более терапевтических средств, описанных выше.
В другом аспекте настоящего изобретения представлено изделие, содержащее материалы, применимые для лечения, предупреждения и/или диагностики описанных выше нарушений. Изделие содержит контейнер и этикетку или листок-вкладыш на контейнере, или они ассоциированы с ним. Подходящие контейнеры включают, например, бутыли, флаконы, шприцы, мешки для IV-растворов и т. д. Контейнеры могут быть образованы из различных материалов, таких как стекло или пластик. Контейнер содержит композицию, которая собственно сама находится в нем или объединена с другой композицией, эффективной для лечения, предупреждения и/или диагностики состояния, и он может иметь стерильное входное отверстие (например, контейнер может представлять собой мешок для внутривенных растворов или флакон, имеющий пробку, которая протыкается с помощью иглы для подкожных инъекций). По меньшей мере одним активным средством в композиции является антитело по настоящему изобретению. Этикетка или листок-вкладыш указывают на то, что композицию применяют для лечения выбранного состояния. Более того, изделие может содержать (a) первый контейнер с композицией, содержащейся в нем, где композиция содержит антитело по настоящему изобретению; и (b) второй контейнер с композицией, содержащейся в нем, где композиция содержит дополнительное цитотоксическое средство или иное терапевтическое средство. В данном варианте осуществления настоящего изобретения изделие может дополнительно содержать листок-вкладыш указывающий на то, что композиции могут применяться для лечения конкретного состояния. В качестве альтернативы или дополнения изделие может дополнительно содержать второй (или третий) контейнер, содержащий фармацевтически приемлемый буфер, такой как бактериостатическая вода для инъекций (BWFI), забуференный фосфатом солевой раствор, раствор Рингера и раствор декстрозы. Оно может дополнительно включать другие материалы, требуемые с коммерческой позиции и пользовательской точки зрения, включающие другие буферы, разбавители, фильтры, иглы и шприцы.
Соответственно, также предполагается производство и/или получение фармацевтической композиции, содержащей антитела к CD3 и/или антигенсвязывающие фрагменты, раскрытые в данном документе. Композицию можно применять отдельно или в комбинации с другими активными средствами для лечения клеточного пролиферативного нарушения (например, рака) или аутоиммунного нарушения (например, артрита, ревматоидного артрита, колита, воспалительного заболевания кишечника, аутоиммунного диабета I типа и т.д.).
В некоторых вариантах осуществления фармацевтические композиции, содержащие антитела к CD3 и/или их антигенсвязывающие фрагменты, описанные в настоящем документе, могут быть получены, например, путем смешивания такого антитела, характеризующегося требуемой степенью чистоты, с одним или более необязательными фармацевтически приемлемыми носителями (Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980)) в форме лиофилизированных составов или водных растворов, необязательно приготовленных для модифицированного (например, пролонгированного) высвобождения. Иллюстративные лиофилизированные составы на основе антитела описаны в патенте США № 6267958. Водные составы на основе антитела включают составы, описанные в патенте США № 6171586 и WO2006/044908, составы, описанные во втором документе, содержат гистидинацетатный буфер.
Фармацевтически приемлемые носители обычно нетоксичны для реципиентов в используемых дозировках и концентрациях и включают без ограничения буферы, такие как фосфат, цитрат и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты (такие как октадецилдиметилбензиламмония хлорид; гексаметония хлорид; бензалкония хлорид; бензетония хлорид; фенол, бутиловый или бензиловый спирты; алкилпарабены, такие как метил- или пропилпарабен; катехол; резорцин; циклогексанол; 3-пентанол; и мета-крезол); низкомолекулярные (менее чем приблизительно 10 остатков) полипептиды; белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатирующие средства, такие как EDTA; сахара, такие как сахароза, маннит, трегалоза или сорбит; солеобразующие противоионы, такие как натрий; металлосодержащие комплексы (например Zn-белковые комплексы); и/или неионогенные поверхностно-активные вещества, такие как полиэтиленгликоль (PEG). В данном документе иллюстративные фармацевтически приемлемые носители дополнительно включают средства для диспергирования лекарственных средств в межклеточном пространстве, такие как растворимые нейтрально-активные гиалуронидазные гликопротеины (sHASEGP), например, человеческие растворимые PH-20 гиалуронидазные гликопротеины, такие как rHuPH20 (HYLENEX®, Baxter International, Inc.). Определенные иллюстративные sHASEGP и способы применения, предусматривающие rHuPH20, описаны в публикации заявки на патент США №№ 2005/0260186 и 2006/0104968.
Такие составы могут содержать более одного активного ингредиента, если это необходимо для конкретного показания, подлежащего лечению, предпочтительно ингредиенты c комплементарными активностями, которые не оказывают отрицательного воздействия друг на друга и присутствуют в количествах, эффективных для предполагаемой цели. Например, кроме того, может быть необходимым обеспечить дополнительное терапевтическое средство (например, химиотерапевтическое средство, цитотоксическое средство, средство, ингибирующее рост, и/или антигормональное средство).
Активные ингредиенты могут быть заключены в микрокапсулы, полученные, например, с помощью методик коацервации или с помощью полимеризации на границе раздела фаз, например, в гидроксиметилцеллюлозные или желатиновые микрокапсулы и микрокапсулы из поли-(метилметацилата) соответственно, в коллоидные системы для доставки лекарственного средства (например, липосомы, альбуминовые микросферы, микроэмульсии, наночастицы и нанокапсулы) или в макроэмульсии. Такие методики раскрыты в Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980).
ПРИМЕРЫ
Пример 1. Создание библиотек сконструированных pH-зависимых антител к CD3
Библиотеки комбинаторных замен гистидина получали из клона исходного антитела к CD3 ADI-26906 (антитело № 1 в таблице 1). ADI-26906 был первоначально описан в PCT/US2018/031705, которая полностью включена в данный документ посредством ссылки (ADI-26906 не был подвергнут конструированию в отношении pH). Для включения остатков гистидина использовали три конструкции библиотеки: 1) H3 + L3 двойной прыжок плюс L1 одиночные или двойные гистидиновые (His) замены (с вариациями NNK, смежными с His, и без них), что привело к теоретическому разнообразию 3,4 x 105; 2) предварительно созданная библиотека разнообразия H1/H2 плюс двойной прыжок H3, что приводит к теоретическому разнообразию 6,8 x 108, и 3) переходящий синглет H3 + L3 NNK/His или His/NNK, в результате чего теоретическое разнообразие составляет 1,2 x 105. Библиотеки создавали и распространяли, как описано ранее (см., например, WO2009036379; WO2010105256; WO2012009568; Xu et al., Protein Eng Des Sel. 2013 Oct;26(10):663-70). Конструкции L1 синтезировали как полные VK с использованием SGI BioXp (SGI-DNA, La Jolla, CA). Замены ограничивались CDR. Однако предполагается, что замены также могут быть предусмотрены в FR. Анализ последовательности вариантов из каждой библиотеки показал в общей сложности 0-6 замен His на вариант VH или VK.
Выполняли пять раундов отбора с применением трех библиотек против биотинилированного антигена CD3. Для первого раунда отбора для библиотеки H1/H2 плюс H3 выполняли метод сортировки магнитных шариков с использованием системы Miltenyi MACS, по сути как описано в (Siegel et al., J Immunol Methods. 2004 Mar;286(1-2):141-53). Вкратце, ~109 дрожжевых клеток инкубировали с 1 мл 100 нМ биотинилированного антигена CD3 при pH 6,0 в течение 15 минут при комнатной температуре в промывочном буфере FACS PBS с 0,1% BSA при pH 6,0. После однократной промывки 50 мл ледяного промывочного буфера осадок клеток ресуспендировали в 40 мл промывочного буфера и к дрожжам добавляли 500 мкл стрептавидина MicroBeads (Miltenyi Biotec, Бергиш-Гладбах, Германия, № по каталогу 130-048-101) и инкубировали в течение 15 минут при 4°C. Затем дрожжи осаждали, ресуспендировали в 5 мл промывочного буфера и загружали в колонку MACS LS (Miltenyi Biotec, Бергиш-Гладбах, Германия, № по каталогу 130-042-401). После загрузки 5 мл колонку трижды промывали 3 мл промывочного буфера FACS. Затем колонку удаляли из магнитного поля, дрожжи элюировали 5 мл среды для выращивания и затем выращивали в течение ночи. Для двух библиотек с меньшим разнообразием первый раунд отбора проводили с использованием проточной цитометрии (FACS). Вкратце, дрожжевые клетки (~109 дрожжевых клеток/библиотека) инкубировали с 0,25 мл 100 нМ биотинилированного антигена CD3 при pH 6,0 в течение 15 минут при комнатной температуре в промывочном буфере FACS PBS с 0,1% BSA при pH 6,0. Дрожжи промывали буфером FACS и помечали для сортировки.
После первого раунда MACS или FACS выполняли четыре раунда сортировки с использованием методов FACS и переключения pH (см. фигура 1).
Очищенный антиген белка CD3 биотинилировали с использованием набора EZ-Link Sulfo-NHS-Biotinylation Kit (Thermo Scientific). Антигены CD3 концентрировали до ~1 мг/мл и буфер заменяли на PBS перед добавлением реагента для биотинилирования с молярным соотношением 1:7,5 (EZ-Link Sulfo-NHS-Biotinylation Kit, Thermo Scientific, № по каталогу 21425). Смесь выдерживали при 4°C в течение ночи перед другой заменой буфера для удаления свободного биотина из раствора. Биотинилирование подтверждали связыванием меченых белков сенсором со стрептавидином на ForteBio. Успешное биотинилирование белкового антигена CD3 подтверждали обнаруживаемым связыванием со стрептавидин-связанным биосенсором, установленным на интерферометре ForteBio OctetTM Red384 (Pall ForteBio, Менло-Парк, Калифорния, США) в соответствии с рекомендациями производителя (данные не показаны). В способе предварительного насыщения CD3 №1 (показан на фигуре 1A) дрожжевые клетки предварительно насыщали нативным (небиотинилированным) антигеном CD3 при pH 7,4 в течение 10 минут. Затем дрожжевые клетки промывали при pH 7,4 и инкубировали в среде с pH 6,0 в течение 10 минут для диссоциации антигена. Контрольные клетки промывали и инкубировали при pH 7,4. Наконец, дрожжевые клетки инкубировали с биотинилированным антигеном CD3 (показан зеленым кружком, отмеченным звездочкой на фигуре 1A) при pH 6 в течение 10 минут. Контрольные клетки инкубировали с биотинилированным антигеном CD3 при pH 7,4. Связывающие молекулы, меченные при pH 6, затем подвергали сортировке и определению характеристик. В способе предварительного насыщения CD3 №2 (показан на фигуре 1В) дрожжевые клетки предварительно насыщали нативным антигеном CD3 при pH 6,0 в течение 10 минут. Затем дрожжевые клетки промывали при pH 6,0 и инкубировали при pH 7,4 или 6,0 в течение 10 минут. Наконец, дрожжевые клетки инкубировали с биотинилированным антигеном CD3 при противоположном pH (клетки, инкубированные при pH 6,0 на предыдущем этапе, инкубировали при pH 7,4, тогда как клетки, инкубированные при pH 7,4 на предыдущем этапе, инкубировали при pH 6,0) в течение 10 минут. Затем связывающие молекулы, меченные биотинилированным антигеном CD3, подвергали сортировке и определению характеристик.
Три библиотеки из исходных выборок MACS/FACS брали через четыре раунда выборок FACS. Приблизительно 1×108 дрожжей на библиотеку осаждали, трижды промывали промывочным буфером и инкубировали со 100 нМ биотинилированного антигена CD3 отдельно в течение не менее 10 минут при комнатной температуре при pH 6,0, pH 7,4 или обрабатывали путем предварительного насыщения и способа № 2 переключения pH, описанного выше. Затем дрожжи дважды промывали и окрашивали антителом козы к человеческому F(ab’)2 каппа-FITC в разведении 1:100 (Southern Biotech, Бирмингем, Алабама, № по каталогу 2062-02) или стрептавидином-Alexa Fluor 633 (Life Technologies, Гранд Айленд, Нью-Йорк, № по каталогу S21375), разведенным 1:500, или Экстравидин-фикоэртирином (Sigma-Aldrich, Сент-Луис, № по каталогу E4011), разведенным 1:50, вторичные реагенты в течение 15 минут при 4°C. После двукратной промывки ледяным буфером для промывки осадки клеток ресуспендировали в 0,4 мл промывочного буфера и переносили в сортировочные пробирки с сетчатым колпачком. Сортировку проводили с применением сортера FACS ARIA (BD Biosciences) и определяли сортировочные гейты для отбора либо связывающих CD3 при pH 6, либо несвязывающих CD3 при pH 7,4, молекул. Отобранные популяции из первого раунда FACS переводили в следующий раунд.
Второй, третий и четвертый раунды FACS для отобранных выше популяций включали положительные виды для молекул, связывающих CD3, при pH 6,0 и отрицательные виды для уменьшения связывающих молекул при pH 7,4 и полиспецифических связывающих реагентов (Xu et al., Protein Eng Des Sel. 2013 Oct;26(10):663-70). Во втором раунде FACS (R3) клетки обрабатывали посредством предварительного насыщения и переключения pH по способу № 2 (обсужденному выше) или отрицательно сортировали в отношении отобранных несвязывающих молекул при pH 7,4. В третьем раунде FACS (R4) выходы из R3 объединяли с выходами из способа №2 предварительного насыщения CD3 из R2 и подвергали предварительному насыщению CD3 по способу №1. В последнем раунде FACS (R5) выходы R4 проверяли в отношении реактивности PSR и связывания CD3 человека и яванского макака (Cyno) при pH 6 и 7,4. Результаты каждого раунда помещали в чашки, и изоляты отбирали для секвенирования и определения характеристик.
На фигуре 2 показаны иллюстративные графики FACS для выборок раунда 1 и раунда 2 из одной библиотеки. Аналогичные профили связывания наблюдали для всех библиотек. Вкратце, во время раунда 1 клетки положительно сортировали с использованием 100 нМ гетеродимера CD3εδ человека (HuCD3-hd) при pH 6. Во время раунда 2 клетки положительно сортировали с использованием 100 нМ HuCD3-hd при pH 6,0, отрицательно отсортировали с использованием 100 нМ HuCD3-hd при pH 7,4 или предварительно насыщали с использованием способа № 2, описанного выше. Связывание также подтверждали для CD3 яванского макака (CyCD3-hd) при pH 6,0. Стрелки указывают на отсортированные клетки, которые были перенесены на следующий раунд сортировки.
На фигуре 3 показаны иллюстративные графики FACS из раунда 3 и сравниваются входные данные для положительных значений pH 6,0 и отрицательных значений pH 7,4 из раунда 2. Вкратце, виды из раунда 2 инкубировали со 100 нМ HuCD3-hd при pH 6,0 и 7,4. Совмещенный столбец показывает, что вводная популяция клеток (из видов раунда 2) демонстрирует более высокое связывание при pH 6,0 по сравнению с pH 7,4. Для переноса клеток в следующие раунды отбора применяли способ № 2 предварительного насыщения/переключения.
На фигуре 4 показаны иллюстративные графики FACS из раунда 4 и раунда 5. В раунде 4 сравнивали клетки, инкубированные в 100 нМ HuCD3-hd при pH 6 и pH 7,4. В раунде 4 также сравнивали клетки, подвергнутые способу предварительного насыщения/переключения при pH 6 и pH 7,4. В раунде 5 сравнивали клетки, инкубированные либо в 100 нМ HuCD3-hd, либо в 100 нМ CyCD3-hd при pH 6 (красный) и pH 7,4 (серый).
Пример 2. Определение аффинности антитела к CD3 в отношении CD3
Аффинность антител к CD3 в отношении CD3 при pH 6,0 и 7,4 определяли путем измерения их кинетических констант (ka, kd, KD) на ForteBio Octet. Измерения аффинности с помощью ForteBio проводили в целом так, как это описано ранее (Estep et al., MAbs. 2013 5(2):270-8). Вкратце, измерения аффинности с помощью ForteBio проводили путем загрузки антител (IgG) в рабочем режиме на сенсоры AHC. Сенсоры уравновешивали в холостом режиме с помощью буфера для анализа в течение 30 минут, а затем отслеживали в рабочем режиме в течение 60 секунд для установки исходных значений. Для измерения активного связывания сенсоры с загруженными IgG подвергали воздействию 100 нМ антигена (CD3 человека или яванского макака) в течение 3 минут, после чего их переносили в буфер для анализа на 3 минуты для измерения скорости диссоциации. Данные кинетики были подобраны с использованием модели связывания 1:1 в программном обеспечении для анализа данных, предоставленном ForteBio. В таблице 2 представлены кинетические константы для отобранных клонов. В таблице 3 представлена константа равновесной диссоциации (KD) CD3 человека при pH 6,0 и 7,4 для отобранных клонов.
Специфичность антител к CD3 к клеткам CD3+ Jurkat человека по сравнению с клетками CHO-S при pH 6,0 и 7,4 определяли с использованием анализа связывания клеток FACS. Вкратце, CD3+ клетки Jurkat человека и клетки CHO-S подвергали оттаиванию и промывали холодным буфером PBSF, pH 7,4 (PBS+0,1% BSA, pH 7,4). Приблизительно 200000 клеток отбирали аликвотами на лунку 96-луночного планшета и осаждали центрифугированием (5 минут при 500 × g). Клетки промывали либо PBSF pH 7,4, либо PBSF pH 6,0 (PBS+0,1% BSA, pH 6,0), а затем ресуспендировали в 100 мкл либо PBSF pH 7,4, либо PBSF pH 6,0 с антителом IgG, продуцируемым в дрожжах (100 нМ). Смесь (клетки + антитело) инкубировали в течение 20 минут на льду, затем дважды промывали либо PBSF pH 7,4, либо PBSF pH 6,0. Клетки ресуспендировали в 50 мкл йодида пропидия (разведение 1:500) и готовили антитела к IgG-RPE человека (разведение 1:100) либо в PBSF pH 7,4, либо в PBSF pH 6,0, затем инкубировали в течение 20 минут на льду в темноте, до того, как клетки дважды промывали либо PBSF pH 7,4, либо PBSF pH 6,0. Связывание анализировали на FACS Canto II. Средние интенсивности флуоресценции (MFI) при pH 6,0 и 7,4 показаны в таблице 3 для отобранных клонов.
На фигуре 5A показан ответ связывания HuCD3 при pH 6 (ось x) по сравнению с ответом связывания HuCD3 при pH 7,4 (ось y) для 236 уникальных клонов из результатов сортировки в ходе раунда 2/3. На фигуре 5B показаны значения KD для HuCD3 при pH 6 (ось x) по сравнению с HuCD3 при pH 7,4 (ось y) для 236 уникальных клонов из результатов сортировки в ходе раунда 2/3. Синие кружки представляют клоны из раунда 2/3, полученные с помощью сортировки с предварительным насыщением/переключением pH 6,0, желтые кружки представляют клоны из раунда 2/3, полученные с помощью отрицательной сортировки с pH 7,4, а красные кружки представляют исходный клон ADI-26906. Результаты показывают, что виды отрицательной сортировки при pH 7,4 в раунде 2/3 имеют тенденцию давать больше селективных при pH связывающих молекул, но с более слабым ответом или аффинностью при pH 6,0, которые обозначены как связывающие молекулы Группы 2. Положительный отбор при pH 6,0 и сортировка с предварительным насыщением/переключением давали клоны со смешанной селективностью, но с более высоким ответом/аффинностью, которые обозначены как связывающие молекулы группы 1.
Связывающие молекулы группы 1 могут включать, например, ADI-48592 (Ab125), ADI-48595 (Ab178), ADI-48650 (Ab77), ADI-48652 (Ab81), ADI-48662 (Ab116) и ADI-48666 (Ab177). Связывающие молекулы группы 2 могут включать, например, ADI-48588 (Ab58), ADI-48587 (Ab36), ADI-48577 (Ab193), ADI-48590 (Ab91), ADI-48581 (Ab237), ADI-48575 (Ab113), ADI-48593 (Ab158), ADI-48591 (Ab102), ADI-48647 (Ab65), ADI-48636 (Ab230), ADI-48586 (Ab25), ADI-48646 (Ab53), ADI-48638 (Ab22), ADI-48597 (Ab180), ADI-48601 (Ab191), ADI-48576 (Ab182), ADI-48643 (Ab46), ADI-48624 (Ab241), ADI-48632 (Ab15), ADI-48635 (Ab17), а также ADI-48645 (Ab49).
На фигуре 6 представлены иллюстративные результаты кинетики экспериментов ForteBio для четырех клонов по сравнению с исходным клоном ADI-26906. KD для каждого клона рассчитывали при pH 7,4 и pH 6,0. Отношение KD получали путем деления KD при pH 7,4 на KD при pH 6,0. Примеры демонстрируют, что некоторые клоны, обозначенные как связывающие молекулы группы 1, такие как SAD10318_P02_A05 (ADI-48595) и SAD10318_P02_C04 (ADI-48592), характеризуются более сильным связыванием (с более низкой KD) при pH 6,0 по сравнению с pH 7,4. Некоторые клоны, обозначенные как связывающие молекулы группы 2, такие как SAD10318_P01_A03 (ADI-48587) и SAD10318_P01_E01 (ADI-48577), не характеризовались связыванием при pH 7,4, но связывались при pH 6,0. Аминокислотные замены в областях CDRH3, CDRL1 и CDRL3, которые могут способствовать дифференциальному связыванию, выделены в столбце «последовательность» на фиг. 6 (SEQ ID NO: 576-590 соответственно, в порядке появления). В таблице 2 представлены дополнительные данные кинетики и PSR для отобранных клонов. Клоны, такие как ADI-48576, ADI-48577, ADI-48587, ADI-48592, ADI-48595, ADI-48635, ADI-48650, ADI-48652, ADI-48666, ADI-48643 и ADI-48645, демонстрируют pH-зависимое связывание (с более сильным связыванием при pH 6,0 по сравнению со связыванием при pH 7,4), низкие показатели PSR и обеспечивают диапазон аффинности к CD3.
Анализ 258 уникальных клонов, идентифицированных с использованием методологии по настоящему изобретению, выявил консенсусные мотивы в областях CDR. В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность AX1DX2YX3HX4FYDV, где X1 представляет собой R или H, где X2 представляет собой A или H, где X3 представляет собой G, H или P и где X4 представляет собой Y, H, D, V, E, S, N, L, M, I, G, A, Q или T (SEQ ID NO: 1). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3 и X4 представляет собой H. Следующие 120 клонов включают представленный мотив последовательности SAD10318_P01_A02; SAD10318_P01_G02; SAD10318_P01_D03; SAD10318_P01_G03; SAD10318_P01_H03; SAD10318_P02_D05; SAD10318_P02_H05; SAD10318_P02_G06; SAD10318_P03_C08; SAD10318_P03_H08; SAD10318_P03_G09; SAD10318_P04_H10; SAD10318_P04_D11; SAD10319_P01_A01; SAD10319_P01_C01; SAD10319_P01_E01; SAD10319_P01_A02; SAD10319_P01_C02; SAD10319_P01_F02; SAD10319_P01_H02; SAD10319_P01_B03; SAD10319_P01_C03; SAD10319_P01_D03; SAD10319_P01_F03; SAD10319_P02_A04; SAD10319_P02_C04; SAD10319_P02_E04; SAD10319_P02_F04; SAD10319_P02_A05; SAD10319_P02_B05; SAD10319_P02_C05; SAD10319_P02_G05; SAD10319_P02_A06; SAD10319_P02_B06; SAD10319_P02_C06; SAD10319_P02_D06; SAD10319_P02_F06; SAD10319_P02_G06; SAD10319_P03_C07; SAD10319_P03_H07; SAD10319_P03_D08; SAD10319_P03_E08; SAD10319_P03_E09; SAD10319_P03_F09; SAD10319_P04_A10; SAD10319_P04_G10; SAD10319_P04_E11; SAD10319_P04_F11; SAD10319_P04_G11; SAD10319_P04_C12; SAD10319_P04_D12; SAD10320_P01_B01; SAD10320_P01_D01; SAD10320_P01_E01; SAD10320_P01_G01; SAD10320_P01_H01; SAD10320_P01_A02; SAD10320_P01_F02; SAD10320_P01_G02; SAD10320_P01_H02; SAD10320_P01_C03; SAD10320_P01_D03; SAD10320_P01_E03; SAD10320_P01_F03; SAD10320_P01_G03; SAD10320_P02_A04; SAD10320_P02_B04; SAD10320_P02_E04; SAD10320_P02_H04; SAD10320_P02_A05; SAD10320_P02_B05; SAD10320_P02_C05; SAD10320_P02_B06; SAD10320_P02_D06; SAD10320_P02_E06; SAD10320_P03_B07; SAD10320_P03_H07; SAD10320_P03_C08; SAD10320_P03_D08; SAD10320_P03_F08; SAD10320_P03_H08; SAD10320_P03_A09; SAD10320_P03_C09; SAD10320_P03_D09; SAD10320_P03_F09; SAD10320_P04_A10; SAD10320_P04_C10; SAD10320_P04_D10; SAD10320_P04_E10; SAD10320_P04_G10; SAD10320_P04_D11; SAD10320_P04_E11; SAD10320_P04_F11; SAD10320_P04_H11; SAD10320_P04_A12; SAD10320_P04_D12; SAD10320_P04_E12; SAD10320_P04_F12; SAD10319_P05_A01; SAD10319_P05_A05; SAD10319_P05_B02; SAD10319_P05_C01; SAD10319_P05_C03; SAD10319_P05_C05; SAD10319_P05_D02; SAD10319_P05_D03; SAD10319_P05_D05; SAD10319_P05_E04; SAD10319_P05_F01; SAD10319_P06_B10; SAD10319_P06_B11; SAD10319_P06_C10; SAD10319_P06_C12; SAD10319_P06_E08; SAD10319_P06_F07; SAD10319_P06_F10; SAD10319_P06_G09; SAD10319_P06_H07; SAD10319_P06_H08 и SAD10319_P06_H10.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDX1YGX2X3X4YDX5 где X1 представляет собой A или H, где X2 представляет собой R или H, где X3 представляет собой H или Y, где X4 представляет собой F или H, и где X5 представляет собой H или V (SEQ ID NO: 2). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3, X4 и X5 представляет собой H. Следующие 57 клонов включают представленный консенсусный мотив LAD5224_P03_A01; SAD10318_P01_B01; SAD10318_P01_F01; SAD10318_P02_B05; SAD10318_P02_F05; SAD10318_P02_G05; SAD10318_P03_B07; SAD10318_P03_G07; SAD10318_P03_A08; SAD10318_P03_A09; SAD10318_P04_E10; SAD10318_P04_E11; SAD10318_P04_H11; SAD10319_P01_D01; SAD10319_P01_F01; SAD10319_P01_G01; SAD10319_P01_D02; SAD10319_P01_E02; SAD10319_P02_B04; SAD10319_P02_E05; SAD10319_P02_E06; SAD10319_P02_H06; SAD10319_P03_G08; SAD10319_P03_B09; SAD10319_P03_G09; SAD10319_P04_B10; SAD10319_P04_C11; SAD10319_P04_D11; SAD10319_P04_F12; SAD10319_P04_H12; SAD10320_P01_E02; SAD10320_P02_C04; SAD10320_P02_C06; SAD10320_P02_G06; SAD10319_P05_A02; SAD10319_P05_B03; SAD10319_P05_B04; SAD10319_P05_D01; SAD10319_P05_G02; SAD10319_P05_G03; SAD10319_P05_H06; SAD10319_P06_A07; SAD10319_P06_A10; SAD10319_P06_A11; SAD10319_P06_E09; SAD10319_P06_E10; SAD10319_P06_G11; SAD10319_P06_H11; LAD9953_P01_H01; LAD9954_P01_B02; LAD9955_P01_G02; LAD9956_P01_C03; LAD9959_P01_E04; LAD9960_P01_D05; LAD9963_P01_E06; LAD9964_P01_C07 и LAD9966_P01_A08.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDAHX1X2YX3X4DX5, где X1 представляет собой G, E или R, где X2 представляет собой R или H, где X3 представляет собой F или H, где X4 представляет собой Y или H, и где X5 представляет собой V или H (SEQ ID NO: 3). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3, X4 и X5 представляет собой H. Следующие 23 клона включают представленный консенсусный мотив SAD10318_P01_G01; SAD10318_P01_F02; SAD10318_P01_C03; SAD10318_P01_E03; SAD10318_P01_F03; SAD10318_P02_B04; SAD10318_P02_D04; SAD10318_P02_D06; SAD10318_P03_F07; SAD10318_P04_F11; SAD10318_P04_H12; SAD10319_P02_D04; SAD10319_P02_H04; SAD10319_P02_D05; SAD10319_P03_G07; SAD10319_P04_C10; SAD10319_P04_B11; SAD10319_P04_B12; SAD10320_P02_A06; SAD10319_P05_A03; SAD10319_P05_B05; SAD10319_P05_G04 и SAD10319_P06_D12.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность ARDAX1HRX2FYDV, где X1 представляет собой H, Y, S, G, A, T, V или R, и где X2 представляет собой Y или H (SEQ ID NO: 4). В некоторых вариантах осуществления по меньшей мере один из X1 и X2 представляет собой H. Следующие 19 клонов включают представленный консенсусный мотив SAD10318_P01_E01; SAD10318_P01_H01; SAD10318_P01_D02; SAD10318_P02_C04; SAD10318_P02_C05; SAD10318_P02_B06; SAD10318_P02_E06; SAD10318_P03_D09; SAD10318_P04_A12; SAD10319_P02_F05; SAD10319_P03_H08; SAD10320_P01_F01; SAD10320_P01_C02; SAD10320_P01_H03; SAD10320_P02_D05; SAD10320_P02_H05; SAD10320_P03_E07; SAD10320_P04_A11; и SAD10319_P05_G01.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность ARDX1YHRYFYDX2, где X1 представляет собой H или A, и где X2 представляет собой H, V или M (SEQ ID NO: 5). В некоторых вариантах осуществления по меньшей мере один из X1 и X2 представляет собой H. Следующие 15 клона включают представленный консенсусный мотив SAD10318_P01_D01; SAD10318_P01_B02; SAD10318_P01_A03; SAD10318_P02_H04; SAD10318_P02_A05; SAD10318_P03_E07; SAD10318_P03_B08; SAD10318_P03_D08; SAD10318_P03_E08; SAD10318_P03_F08; SAD10318_P03_G08; SAD10318_P03_C09; SAD10318_P04_B11; SAD10319_P01_H01; и SAD10319_P04_E12.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность AX1DAYX2X3X4HX5DV, где X1 представляет собой R или H, где X2 представляет собой G или H, где X3 представляет собой H или R, где X4 представляет собой N, F или Y, и где X5 представляет собой Y или H (SEQ ID NO: 6). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3, X4 и X5 представляет собой H. Следующие 14 клонов включают представленный консенсусный мотив SAD10318_P01_C01; SAD10318_P02_G04; SAD10318_P03_E09; SAD10318_P03_F09; SAD10318_P04_C10; SAD10318_P04_D10; SAD10318_P04_F10; SAD10318_P04_G11; SAD10318_P04_G12; SAD10320_P02_F05; SAD10320_P02_F06; SAD10320_P02_H06; SAD10320_P04_F10; и SAD10319_P05_D04.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность ARDX1X2GRYFYDV, где X1 представляет собой M, Q или H, и где X2 представляет собой R или H (SEQ ID NO: 7). В некоторых вариантах осуществления по меньшей мере один из X1 и X2 представляет собой H. Следующие 7 клонов включают представленный мотив последовательности SAD10318_P02_E04; SAD10318_P04_C11; SAD10318_P04_F12; SAD10319_P02_H05; SAD10320_P01_A03; SAD10320_P01_B03; и SAD10320_P02_E05.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDX1X2X3RYFYDX4, где X1 представляет собой H или A, где X2 представляет собой T, Y или H, где X3 представляет собой G или H, и где X4 представляет собой V или H (SEQ ID NO: 8). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3, и X4 представляет собой H. Следующие клоны включают представленный мотив последовательности ADI-26906; ADI-48584; ADI-57317; ADI-57319; ADI-57323; ADI-57328; ADI-48639; ADI-57300; ADI-57333; ADI-57336; ADI-57337; ADI-48587; ADI-57343; ADI-48648; ADI-48650; ADI-48589; ADI-48652; ADI-48654; ADI-48592; ADI-57401; ADI-57406; ADI-57274; ADI-57413; ADI-57414; ADI-57415; ADI-57416; ADI-57417; ADI-57275; ADI-57427; ADI-57428; ADI-57437; ADI-57438; ADI-48594; ADI-57439; ADI-57440; ADI-57441; ADI-57442; ADI-57443; ADI-57444; ADI-57445; ADI-48666; ADI-48595; ADI-48597; ADI-48576; ADI-57277; ADI-57279; ADI-57280; ADI-57281; ADI-48601; ADI-48577; ADI-57284; ADI-48604; ADI-48606; ADI-57285; ADI-48608; ADI-48609; ADI-48610; ADI-48614; ADI-48615; ADI-48617; ADI-57295; ADI-48580; ADI-48622; ADI-57299; ADI-57300; ADI-48623; ADI-57303; ADI-48582; и ADI-57311.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDX1X2X3X4YFYDX5, где X1 представляет собой H или A, где X2 представляет собой T, Y или H, где X3 представляет собой G или H, X4 представляет собой H, R, V или I, и где X5 представляет собой V или H (SEQ ID NO: 43). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3, X4 и X5 представляет собой H. Следующие 11 клона включают представленный консенсусный мотив ADI-48576; ADI-48577; ADI-48587; ADI-48592; ADI-48595; ADI-48635; ADI-48650; ADI-48652; ADI-48666; ADI-48643; и ADI-48645.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CD3, CDRH3, где домен, связывающий CDRH3, содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность AX1DX2X3X4X5X6X7X8DX9, где X1 представляет собой R или H, где X2 представляет собой A, H, M или Q, где X3 представляет собой Y, H, S, G, A, T, V или R; где X4 представляет собой G, H, P, E или R; где X5 представляет собой H или R, где X6 представляет собой Y, N, F, H, D, E, S, L, M, I, G, A, Q или T; где X7 представляет собой F или H; где X8 представляет собой Y или H; и где X9 представляет собой V, H или M (SEQ ID NO: 58). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3, X4, X5, X6, X7, X8 и X9 представляет собой H. Следующие клоны включают представленный мотив последовательности SAD10318_P01_A02; SAD10318_P01_G02; SAD10318_P01_D03; SAD10318_P01_G03; SAD10318_P01_H03; SAD10318_P02_D05; SAD10318_P02_H05; SAD10318_P02_G06; SAD10318_P03_C08; SAD10318_P03_H08; SAD10318_P03_G09; SAD10318_P04_H10; SAD10318_P04_D11; SAD10319_P01_A01; SAD10319_P01_C01; SAD10319_P01_E01; SAD10319_P01_A02; SAD10319_P01_C02; SAD10319_P01_F02; SAD10319_P01_H02; SAD10319_P01_B03; SAD10319_P01_C03; SAD10319_P01_D03; SAD10319_P01_F03; SAD10319_P02_A04; SAD10319_P02_C04; SAD10319_P02_E04; SAD10319_P02_F04; SAD10319_P02_A05; SAD10319_P02_B05; SAD10319_P02_C05; SAD10319_P02_G05; SAD10319_P02_A06; SAD10319_P02_B06; SAD10319_P02_C06; SAD10319_P02_D06; SAD10319_P02_F06; SAD10319_P02_G06; SAD10319_P03_C07; SAD10319_P03_H07; SAD10319_P03_D08; SAD10319_P03_E08; SAD10319_P03_E09; SAD10319_P03_F09; SAD10319_P04_A10; SAD10319_P04_G10; SAD10319_P04_E11; SAD10319_P04_F11; SAD10319_P04_G11; SAD10319_P04_C12; SAD10319_P04_D12; SAD10320_P01_B01; SAD10320_P01_D01; SAD10320_P01_E01; SAD10320_P01_G01; SAD10320_P01_H01; SAD10320_P01_A02; SAD10320_P01_F02; SAD10320_P01_G02; SAD10320_P01_H02; SAD10320_P01_C03; SAD10320_P01_D03; SAD10320_P01_E03; SAD10320_P01_F03; SAD10320_P01_G03; SAD10320_P02_A04; SAD10320_P02_B04; SAD10320_P02_E04; SAD10320_P02_H04; SAD10320_P02_A05; SAD10320_P02_B05; SAD10320_P02_C05; SAD10320_P02_B06; SAD10320_P02_D06; SAD10320_P02_E06; SAD10320_P03_B07; SAD10320_P03_H07; SAD10320_P03_C08; SAD10320_P03_D08; SAD10320_P03_F08; SAD10320_P03_H08; SAD10320_P03_A09; SAD10320_P03_C09; SAD10320_P03_D09; SAD10320_P03_F09; SAD10320_P04_A10; SAD10320_P04_C10; SAD10320_P04_D10; SAD10320_P04_E10; SAD10320_P04_G10; SAD10320_P04_D11; SAD10320_P04_E11; SAD10320_P04_F11; SAD10320_P04_H11; SAD10320_P04_A12; SAD10320_P04_D12; SAD10320_P04_E12; SAD10320_P04_F12; SAD10319_P05_A01; SAD10319_P05_A05; SAD10319_P05_B02; SAD10319_P05_C01; SAD10319_P05_C03; SAD10319_P05_C05; SAD10319_P05_D02; SAD10319_P05_D03; SAD10319_P05_D05; SAD10319_P05_E04; SAD10319_P05_F01; SAD10319_P06_B10; SAD10319_P06_B11; SAD10319_P06_C10; SAD10319_P06_C12; SAD10319_P06_E08; SAD10319_P06_F07; SAD10319_P06_F10; SAD10319_P06_G09; SAD10319_P06_H07; SAD10319_P06_H08; SAD10319_P06_H10; LAD5224_P03_A01; SAD10318_P01_B01; SAD10318_P01_F01; SAD10318_P02_B05; SAD10318_P02_F05; SAD10318_P02_G05; SAD10318_P03_B07; SAD10318_P03_G07; SAD10318_P03_A08; SAD10318_P03_A09; SAD10318_P04_E10; SAD10318_P04_E11; SAD10318_P04_H11; SAD10319_P01_D01; SAD10319_P01_F01; SAD10319_P01_G01; SAD10319_P01_D02; SAD10319_P01_E02; SAD10319_P02_B04; SAD10319_P02_E05; SAD10319_P02_E06; SAD10319_P02_H06; SAD10319_P03_G08; SAD10319_P03_B09; SAD10319_P03_G09; SAD10319_P04_B10; SAD10319_P04_C11; SAD10319_P04_D11; SAD10319_P04_F12; SAD10319_P04_H12; SAD10320_P01_E02; SAD10320_P02_C04; SAD10320_P02_C06; SAD10320_P02_G06; SAD10319_P05_A02; SAD10319_P05_B03; SAD10319_P05_B04; SAD10319_P05_D01; SAD10319_P05_G02; SAD10319_P05_G03; SAD10319_P05_H06; SAD10319_P06_A07; SAD10319_P06_A10; SAD10319_P06_A11; SAD10319_P06_E09; SAD10319_P06_E10; SAD10319_P06_G11; SAD10319_P06_H11; LAD9953_P01_H01; LAD9954_P01_B02; LAD9955_P01_G02; LAD9956_P01_C03; LAD9959_P01_E04; LAD9960_P01_D05; LAD9963_P01_E06; LAD9964_P01_C07; LAD9966_P01_A08; SAD10318_P01_G01; SAD10318_P01_F02; SAD10318_P01_C03; SAD10318_P01_E03; SAD10318_P01_F03; SAD10318_P02_B04; SAD10318_P02_D04; SAD10318_P02_D06; SAD10318_P03_F07; SAD10318_P04_F11; SAD10318_P04_H12; SAD10319_P02_D04; SAD10319_P02_H04; SAD10319_P02_D05; SAD10319_P03_G07; SAD10319_P04_C10; SAD10319_P04_B11; SAD10319_P04_B12; SAD10320_P02_A06; SAD10319_P05_A03; SAD10319_P05_B05; SAD10319_P05_G04; SAD10319_P06_D12; SAD10318_P01_E01; SAD10318_P01_H01; SAD10318_P01_D02; SAD10318_P02_C04; SAD10318_P02_C05; SAD10318_P02_B06; SAD10318_P02_E06; SAD10318_P03_D09; SAD10318_P04_A12; SAD10319_P02_F05; SAD10319_P03_H08; SAD10320_P01_F01; SAD10320_P01_C02; SAD10320_P01_H03; SAD10320_P02_D05; SAD10320_P02_H05; SAD10320_P03_E07; SAD10320_P04_A11; SAD10319_P05_G01; SAD10318_P01_D01; SAD10318_P01_B02; SAD10318_P01_A03; SAD10318_P02_H04; SAD10318_P02_A05; SAD10318_P03_E07; SAD10318_P03_B08; SAD10318_P03_D08; SAD10318_P03_E08; SAD10318_P03_F08; SAD10318_P03_G08; SAD10318_P03_C09; SAD10318_P04_B11; SAD10319_P01_H01; SAD10319_P04_E12; SAD10318_P01_D01; SAD10318_P01_B02; SAD10318_P01_A03; SAD10318_P02_H04; SAD10318_P02_A05; SAD10318_P03_E07; SAD10318_P03_B08; SAD10318_P03_D08; SAD10318_P03_E08; SAD10318_P03_F08; SAD10318_P03_G08; SAD10318_P03_C09; SAD10318_P04_B11; SAD10319_P01_H01; SAD10319_P04_E12; SAD10318_P02_E04; SAD10318_P04_C11; SAD10318_P04_F12; SAD10319_P02_H05; SAD10320_P01_A03; SAD10320_P01_B03; SAD10320_P02_E05; ADI-26906; ADI-48584; ADI-57317; ADI-57319; ADI-57323; ADI-57328; ADI-48639; ADI-57300; ADI-57333; ADI-57336; ADI-57337; ADI-48587; ADI-57343; ADI-48648; ADI-48650; ADI-48589; ADI-48652; ADI-48654; ADI-48592; ADI-57401; ADI-57406; ADI-57274; ADI-57413; ADI-57414; ADI-57415; ADI-57416; ADI-57417; ADI-57275; ADI-57427; ADI-57428; ADI-57437; ADI-57438; ADI-48594; ADI-57439; ADI-57440; ADI-57441; ADI-57442; ADI-57443; ADI-57444; ADI-57445; ADI-48666; ADI-48595; ADI-48597; ADI-48576; ADI-57277; ADI-57279; ADI-57280; ADI-57281; ADI-48601; ADI-48577; ADI-57284; ADI-48604; ADI-48606; ADI-57285; ADI-48608; ADI-48609; ADI-48610; ADI-48614; ADI-48615; ADI-48617; ADI-57295; ADI-48580; ADI-48622; ADI-57299; ADI-57300; ADI-48623; ADI-57303; ADI-48582; и ADI-57311.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDAX1X2X3X4FYDX5, где X1 представляет собой T, H или Y, где X2 представляет собой G или H, где X3 представляет собой H или R, где X4 представляет собой V или Y, и где X5 представляет собой V или H (SEQ ID NO: 593). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3 и X5 представляет собой H. По меньшей мере, следующие 6 клонов включают представленный консенсусный мотив и обозначены как связывающие молекулы группы 1 ADI-48592, ADI-48595, ADI-48650, ADI-48652, ADI-48662 и ADI-48666.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность AX1DX2X3X4X5X6X7YDX8, где X1 представляет собой R или H, где X2 представляет собой H или A, где X3 представляет собой H или Y, где X4 представляет собой H, G или P, где X5 представляет собой R или H, где X6 представляет собой Y, I или V, где X7 представляет собой F или H, и где X8 представляет собой V или H (SEQ ID NO: 596). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3, X4, X5, X7 и X8 представляет собой H. По меньшей мере следующий 21 клон включает представленный консенсусный мотив и обозначен как связывающие молекулы группы 2 ADI-48588, ADI-48587, ADI-48577, ADI-48590, ADI-48581, ADI-48575, ADI-48593, ADI-48591, ADI-48647, ADI-48636, ADI-48586, ADI-48646, ADI-48638, ADI-48597, ADI-48601, ADI-48576, ADI-48643, ADI-48624, ADI-48632, ADI-48635, и ADI-48645.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9). Следующие 148 клонов включают представленный консенсусный мотив LAD5224_P03_A01; SAD10318_P01_B01; SAD10318_P01_C01; SAD10318_P01_D01; SAD10318_P01_E01; SAD10318_P01_F01; SAD10318_P01_G01; SAD10318_P01_H01; SAD10318_P01_A02; SAD10318_P01_B02; SAD10318_P01_D02; SAD10318_P01_F02; SAD10318_P01_G02; SAD10318_P01_A03; SAD10318_P01_C03; SAD10318_P01_D03; SAD10318_P01_E03; SAD10318_P01_F03; SAD10318_P01_G03; SAD10318_P01_H03; SAD10318_P02_B04; SAD10318_P02_C04; SAD10318_P02_D04; SAD10318_P02_E04; SAD10318_P02_G04; SAD10318_P02_H04; SAD10318_P02_A05; SAD10318_P02_B05; SAD10318_P02_C05; SAD10318_P02_D05; SAD10318_P02_F05; SAD10318_P02_G05; SAD10318_P02_H05; SAD10318_P02_B06; SAD10318_P02_D06; SAD10318_P02_E06;SAD10318_P02_G06; SAD10318_P03_B07; SAD10318_P03_E07; SAD10318_P03_F07; SAD10318_P03_G07; SAD10318_P03_A08; SAD10318_P03_B08; SAD10318_P03_C08; SAD10318_P03_D08; SAD10318_P03_E08; SAD10318_P03_F08; SAD10318_P03_G08; SAD10318_P03_H08; SAD10318_P03_A09; SAD10318_P03_C09; SAD10318_P03_D09;SAD10318_P03_E09; SAD10318_P03_F09; SAD10318_P03_G09; SAD10318_P04_C10; SAD10318_P04_D10; SAD10318_P04_E10; SAD10318_P04_F10; SAD10318_P04_H10; SAD10318_P04_A11; SAD10318_P04_B11; SAD10318_P04_C11; SAD10318_P04_D11; SAD10318_P04_E11; SAD10318_P04_F11; SAD10318_P04_G11; SAD10318_P04_H11; SAD10318_P04_A12; SAD10318_P04_F12; SAD10318_P04_G12; SAD10318_P04_H12; SAD10320_P01_B01; SAD10320_P01_D01; SAD10320_P01_E01; SAD10320_P01_F01; SAD10320_P01_G01; SAD10320_P01_H01; SAD10320_P01_A02; SAD10320_P01_C02; SAD10320_P01_E02; SAD10320_P01_F02; SAD10320_P01_G02; SAD10320_P01_H02; SAD10320_P01_A03; SAD10320_P01_B03; SAD10320_P01_C03; SAD10320_P01_D03; SAD10320_P01_E03; SAD10320_P01_F03; SAD10320_P01_G03; SAD10320_P01_H03; SAD10320_P02_A04; SAD10320_P02_B04; SAD10320_P02_C04; SAD10320_P02_E04; SAD10320_P02_H04; SAD10320_P02_A05; SAD10320_P02_B05; SAD10320_P02_C05; SAD10320_P02_D05; SAD10320_P02_E05; SAD10320_P02_F05; SAD10320_P02_H05; SAD10320_P02_A06; SAD10320_P02_B06; SAD10320_P02_C06; SAD10320_P02_D06; SAD10320_P02_E06; SAD10320_P02_F06; SAD10320_P02_G06; SAD10320_P02_H06; SAD10320_P03_B07; SAD10320_P03_E07; SAD10320_P03_H07; SAD10320_P03_C08; SAD10320_P03_D08; SAD10320_P03_F08; SAD10320_P03_H08; SAD10320_P03_A09; SAD10320_P03_C09; SAD10320_P03_D09; SAD10320_P03_F09; SAD10320_P04_A10; SAD10320_P04_C10; SAD10320_P04_D10; SAD10320_P04_E10; SAD10320_P04_F10; SAD10320_P04_G10; SAD10320_P04_A11; SAD10320_P04_D11; SAD10320_P04_E11; SAD10320_P04_F11; SAD10320_P04_G11; SAD10320_P04_H11; SAD10320_P04_A12; SAD10320_P04_D12; SAD10320_P04_E12; SAD10320_P04_F12; LAD9953_P01_H01; LAD9954_P01_B02; LAD9955_P01_G02; LAD9956_P01_C03; LAD9959_P01_E04; LAD9960_P01_D05; LAD9963_P01_E06; LAD9964_P01_C07; и LAD9966_P01_A08. Кроме того, по меньшей мере следующие 16 клонов включают представленный консенсусный мотив и обозначены как связывающие молекулы группы 2 ADI-48575, ADI-48576, ADI-48577, ADI-48581, ADI-48586, ADI-48587, ADI-48588, ADI-48590, ADI-48591, ADI-48593, ADI-48601, ADI-48646, ADI-48647, ADI-48597, ADI-48643 и ADI-48645.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность X1INPX2TGX3TX4YSQKFQG, где X1 представляет собой W или Y, где X2 представляет собой A, S, D, G, N, L, V, H или Q, где X3 представляет собой A, T или S, и где X4 представляет собой K, V, T, D, Y, F или A (SEQ ID NO: 10). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3 и X4 представляет собой H. Следующие 24 клона включают представленный мотив последовательности SAD10319_P01_E02; SAD10319_P01_H02; SAD10319_P01_B03; SAD10319_P02_A04 SAD10319_P02_B04; SAD10319_P02_C04; SAD10319_P02_F04; SAD10319_P02_H04; SAD10319_P02_A05; SAD10319_P02_C05; SAD10319_P02_C06; SAD10319_P02_E06; SAD10319_P02_F06; SAD10319_P02_G06; SAD10319_P03_D08; SAD10319_P03_F09; SAD10319_P04_G10; SAD10319_P04_C11; SAD10319_P05_A01; SAD10319_P05_A05; SAD10319_P05_G03;SAD10319_P06_A10; SAD10319_P06_C12; и SAD10319_P06_E09.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность X1IX2AGTGX3TX4YSQKFQG, где X1 представляет собой W, Y или F, где X2 представляет собой T, N или D, где X3 представляет собой A, T или L, и где X4 или A, K, V, H, T или N (SEQ ID NO: 11). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3 и X4 представляет собой H. Следующие 23 клона включают представленный консенсусный мотив SAD10319_P01_E01; SAD10319_P01_G01; SAD10319_P01_D02; SAD10319_P01_D03; SAD10319_P02_E05; SAD10319_P02_A06; SAD10319_P03_C07; SAD10319_P03_G07; SAD10319_P03_B09; SAD10319_P03_E09; SAD10319_P04_A10; SAD10319_P04_B10; SAD10319_P04_B11; SAD10319_P04_E12; SAD10319_P05_A02; SAD10319_P05_C05; SAD10319_P05_D01; SAD10319_P05_H06; SAD10319_P06_A07; SAD10319_P06_B11; SAD10319_P06_F07; SAD10319_P06_G09; и SAD10319_P06_H08.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность X1IDAGTGX2TX3YSQKFQG, где X1 представляет собой S или W, где X2 представляет собой L, N, D или F, и где X3 представляет собой D, Y или K (SEQ ID NO: 12). В некоторых вариантах осуществления по меньшей мере один из X1, X2 и X3 представляет собой H. Следующие 17 клонов включают представленный консенсусный мотив SAD10319_P01_C01; SAD10319_P01_D01; SAD10319_P01_H01; SAD10319_P01_F02; SAD10319_P02_D04; SAD10319_P02_D05; SAD10319_P02_F05; SAD10319_P02_H06; SAD10319_P03_G08; SAD10319_P04_D11; SAD10319_P05_A03; SAD10319_P05_B05; SAD10319_P05_C01; SAD10319_P05_D03; SAD10319_P05_F01; SAD10319_P05_G01 и SAD10319_P06_H10.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность X1IX2AGTGATX3YSQKFQG, где X1 представляет собой G, D, или S, где X2 представляет собой I или D, и где X3 представляет собой K или D (SEQ ID NO: 13). В некоторых вариантах осуществления по меньшей мере один из X1, X2 и X3 представляет собой H. Следующие 7 клонов включают представленный консенсусный мотив SAD10319_P02_G05; SAD10319_P05_B02; SAD10319_P05_C03; SAD10319_P05_D05; SAD10319_P06_B10; SAD10319_P06_C10; и SAD10319_P06_D12.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность WINPX1TGNTX2YSQKFQG, где X1 представляет собой D, T, L, S или A, и где X2 представляет собой D, V, L или N (SEQ ID NO: 14). В некоторых вариантах осуществления по меньшей мере один из X1 и X2 представляет собой H. Следующие 6 клонов включают представленный консенсусный мотив SAD10319_P01_A01; SAD10319_P01_F01; SAD10319_P01_C02; SAD10319_P04_F12; SAD10319_P05_E04; и SAD10319_P06_A11.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность X1INAGTGX2TX3YSQKFQG, где X1 представляет собой Y или W, где X2 представляет собой N, D или A, и где X3 представляет собой I или V (SEQ ID NO: 15). В некоторых вариантах осуществления по меньшей мере один из X1, X2 и X3 представляет собой H. Следующие 5 клонов включают представленный консенсусный мотив SAD10319_P01_F03; SAD10319_P02_H05; SAD10319_P02_D06; SAD10319_P03_E08 и SAD10319_P03_H08.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность X1INPX2TGX3TKYSQKFQG, где X1 представляет собой W или Y, где X2 представляет собой D, I или Y и где X3 представляет собой D, Y или E (SEQ ID NO: 16). В некоторых вариантах осуществления по меньшей мере один из X1, X2 и X3 представляет собой H. Следующие 5 клонов включают представленный консенсусный мотив SAD10319_P03_H07; SAD10319_P04_E11; SAD10319_P04_F11; SAD10319_P04_B12; и SAD10319_P04_D12.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность SIX1AGTGX2TKYSQKFQG, где X1 представляет собой N или V, и где X2 представляет собой A или I (SEQ ID NO: 17). В некоторых вариантах осуществления по меньшей мере один из X1 и X2 представляет собой H. Следующие 3 клона включают представленный консенсусный мотив SAD10319_P02_E04; SAD10319_P04_C10 и SAD10319_P04_H12.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность SINAGTGX1TX2YSQKFQG, где X1 представляет собой F или N, и где X2 представляет собой Y или D (SEQ ID NO: 18). В некоторых вариантах осуществления по меньшей мере один из X1 и X2 представляет собой H. Следующие 3 клона включают представленный консенсусный мотив SAD10319_P02_B05; SAD10319_P02_B06 и SAD10319_P05_D02.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность X1IX2X3GTGX4TDYSQKFQG, где X1 представляет собой D или W, где X2 представляет собой N или H, где X3 представляет собой A или S и где X4 представляет собой A или N (SEQ ID NO: 19). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3 и X4 представляет собой H. Следующие 3 клона включают представленный консенсусный мотив SAD10319_P05_B03; SAD10319_P05_B04 и SAD10319_P05_D04.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WIDPX1TGATX2YSQKFQG, где X1 представляет собой N, H или Y и где X2 представляет собой V или K (SEQ ID NO: 20). В некоторых вариантах осуществления по меньшей мере один из X1 и X2 представляет собой H. Следующие 3 клона включают представленный консенсусный мотив SAD10319_P01_C03; SAD10319_P03_G09 и SAD10319_P06_F10.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность WIX1PX2TGNTKYSQKFQG, где X1 представляет собой D или N, и где X2 представляет собой L, I или V (SEQ ID NO: 21). В некоторых вариантах осуществления по меньшей мере один из X1 и X2 представляет собой H. Следующие 3 клона включают представленный консенсусный мотив SAD10319_P01_A02; SAD10319_P04_C12 и SAD10319_P05_G02.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность SINAGDANTKYSQKFQG (SEQ ID NO: 22). Следующие 2 клона включают представленный консенсусный мотив SAD10319_P04_G11 и SAD10319_P06_H07.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность X1IDPX2TGATX3YSQKFQG, где X1 представляет собой D или W, где X2 представляет собой D или V, и где X3 представляет собой E или D (SEQ ID NO: 23). В некоторых вариантах осуществления по меньшей мере один из X1, X2 и X3 представляет собой H. Следующие 2 клона включают представленный консенсусный мотив SAD10319_P05_G04 и SAD10319_P06_E08.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность WINAGDAATVYSQKFQG (SEQ ID NO: 24). Следующие 2 клона включают этот консенсусный мотив SAD10319_P06_G11 и SAD10319_P06_H11.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность X1IX2X3X4X5X6X7TX8YSQKFQG, где X1 представляет собой W, S, Y, F, G или D, где X2 представляет собой N, T, D, V или H, где X3 представляет собой A, P или S, где X4 представляет собой G, A, S, N, D, L, V, H, Q, T, I или Y, где X5 представляет собой D или T, где X6 представляет собой A или G, где X7 представляет собой A, N, T, S, L, D, F, Y или E, и где X8 представляет собой V, K, T, D, Y, F, A, H, N, L, I или E (SEQ ID NO: 59). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3, X4, X5, X6, X7 и X8 представляет собой H. Следующие клоны включают представленный консенсусный мотив SAD10319_P01_E02; SAD10319_P01_H02; SAD10319_P01_B03; SAD10319_P02_A04 SAD10319_P02_B04; SAD10319_P02_C04; SAD10319_P02_F04; SAD10319_P02_H04; SAD10319_P02_A05; SAD10319_P02_C05; SAD10319_P02_C06; SAD10319_P02_E06; SAD10319_P02_F06; SAD10319_P02_G06; SAD10319_P03_D08; SAD10319_P03_F09; SAD10319_P04_G10; SAD10319_P04_C11; SAD10319_P05_A01; SAD10319_P05_A05; SAD10319_P05_G03;SAD10319_P06_A10; SAD10319_P06_C12; SAD10319_P06_E09; SAD10319_P01_E01; SAD10319_P01_G01; SAD10319_P01_D02; SAD10319_P01_D03; SAD10319_P02_E05; SAD10319_P02_A06; SAD10319_P03_C07; SAD10319_P03_G07; SAD10319_P03_B09; SAD10319_P03_E09; SAD10319_P04_A10; SAD10319_P04_B10; SAD10319_P04_B11; SAD10319_P04_E12; SAD10319_P05_A02; SAD10319_P05_C05; SAD10319_P05_D01; SAD10319_P05_H06; SAD10319_P06_A07; SAD10319_P06_B11; SAD10319_P06_F07; SAD10319_P06_G09; SAD10319_P06_H08; SAD10319_P01_C01; SAD10319_P01_D01; SAD10319_P01_H01; SAD10319_P01_F02; SAD10319_P02_D04; SAD10319_P02_D05; SAD10319_P02_F05; SAD10319_P02_H06; SAD10319_P03_G08; SAD10319_P04_D11; SAD10319_P05_A03; SAD10319_P05_B05; SAD10319_P05_C01; SAD10319_P05_D03; SAD10319_P05_F01; SAD10319_P05_G01; SAD10319_P06_H10; SAD10319_P02_G05; SAD10319_P05_B02; SAD10319_P05_C03; SAD10319_P05_D05; SAD10319_P06_B10; SAD10319_P06_C10; SAD10319_P06_D12; SAD10319_P01_A01; SAD10319_P01_F01; SAD10319_P01_C02; SAD10319_P04_F12; SAD10319_P05_E04; SAD10319_P06_A11; SAD10319_P01_F03; SAD10319_P02_H05; SAD10319_P02_D06; SAD10319_P03_E08; SAD10319_P03_H08; SAD10319_P03_H07; SAD10319_P04_E11; SAD10319_P04_F11; SAD10319_P04_B12; SAD10319_P04_D12; SAD10319_P02_E04; SAD10319_P04_C10; SAD10319_P04_H12; SAD10319_P02_B05; SAD10319_P02_B06; SAD10319_P05_D02; SAD10319_P05_B03; SAD10319_P05_B04; SAD10319_P05_D04; SAD10319_P01_C03; SAD10319_P03_G09; SAD10319_P06_F10; SAD10319_P01_A02; SAD10319_P04_C12; SAD10319_P05_G02; SAD10319_P04_G11; SAD10319_P06_H07; SAD10319_P05_G04; SAD10319_P06_E08; SAD10319_P06_G11; и SAD10319_P06_H11.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WIDAGTGX1TX2YSQKFQG, где X1 представляет собой L, F, N или A, и где X2 представляет собой T или K (SEQ ID NO: 595). По меньшей мере следующие 4 клона включают представленный консенсусный мотив и обозначены как связывающие молекулы группы 2 ADI-48636, ADI-48638, ADI-48624 и ADI-48635.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность X1NIKDYX2MH, где X1 представляет собой F или S, и где X2 представляет собой Y или H (SEQ ID NO: 44). В некоторых вариантах осуществления по меньшей мере один из X1 и X2 представляет собой H. В некоторых вариантах осуществления последовательность представляет собой FNIKDYHMH (SEQ ID NO: 25), SNIKDYYMH (SEQ ID NO: 26) или SNIKDYHMH (SEQ ID NO: 27). Следующие 148 клонов включают представленный консенсусный мотив LAD5224_P03_A01; SAD10318_P01_B01; SAD10318_P01_C01; SAD10318_P01_D01; SAD10318_P01_E01; SAD10318_P01_F01; SAD10318_P01_G01; SAD10318_P01_H01; SAD10318_P01_A02; SAD10318_P01_B02; SAD10318_P01_D02; SAD10318_P01_F02; SAD10318_P01_G02; SAD10318_P01_A03; SAD10318_P01_C03; SAD10318_P01_D03; SAD10318_P01_E03; SAD10318_P01_F03; SAD10318_P01_G03; SAD10318_P01_H03; SAD10318_P02_B04; SAD10318_P02_C04; SAD10318_P02_D04; SAD10318_P02_E04; SAD10318_P02_G04; SAD10318_P02_H04; SAD10318_P02_A05;SAD10318_P02_B05; SAD10318_P02_C05; SAD10318_P02_D05; SAD10318_P02_F05; SAD10318_P02_G05; SAD10318_P02_H05; SAD10318_P02_B06; SAD10318_P02_D06; SAD10318_P02_E06; SAD10318_P02_G06; SAD10318_P03_B07; SAD10318_P03_E07; SAD10318_P03_F07; SAD10318_P03_G07; SAD10318_P03_A08; SAD10318_P03_B08; SAD10318_P03_C08; SAD10318_P03_D08; SAD10318_P03_E08; SAD10318_P03_F08; SAD10318_P03_G08; SAD10318_P03_H08; SAD10318_P03_A09; SAD10318_P03_C09; SAD10318_P03_D09; SAD10318_P03_E09; SAD10318_P03_F09; SAD10318_P03_G09; SAD10318_P04_C10; SAD10318_P04_D10; SAD10318_P04_E10; SAD10318_P04_F10; SAD10318_P04_H10; SAD10318_P04_A11; SAD10318_P04_B11; SAD10318_P04_C11; SAD10318_P04_D11; SAD10318_P04_E11; SAD10318_P04_F11; SAD10318_P04_G11; SAD10318_P04_H11; SAD10318_P04_A12; SAD10318_P04_F12; SAD10318_P04_G12; SAD10318_P04_H12; SAD10320_P01_B01; SAD10320_P01_D01; SAD10320_P01_E01; SAD10320_P01_F01; SAD10320_P01_G01; SAD10320_P01_H01; SAD10320_P01_A02; SAD10320_P01_C02; SAD10320_P01_E02; SAD10320_P01_F02; SAD10320_P01_G02; SAD10320_P01_H02; SAD10320_P01_A03; SAD10320_P01_B03; SAD10320_P01_C03; SAD10320_P01_D03; SAD10320_P01_E03; SAD10320_P01_F03; SAD10320_P01_G03; SAD10320_P01_H03; SAD10320_P02_A04; SAD10320_P02_B04; SAD10320_P02_C04; SAD10320_P02_E04; SAD10320_P02_H04; SAD10320_P02_A05; SAD10320_P02_B05; SAD10320_P02_C05; SAD10320_P02_D05; SAD10320_P02_E05; SAD10320_P02_F05; SAD10320_P02_H05; SAD10320_P02_A06; SAD10320_P02_B06; SAD10320_P02_C06; SAD10320_P02_D06; SAD10320_P02_E06; SAD10320_P02_F06; SAD10320_P02_G06; SAD10320_P02_H06; SAD10320_P03_B07; SAD10320_P03_E07; SAD10320_P03_H07; SAD10320_P03_C08; SAD10320_P03_D08; SAD10320_P03_F08; SAD10320_P03_H08; SAD10320_P03_A09; SAD10320_P03_C09; SAD10320_P03_D09; SAD10320_P03_F09; SAD10320_P04_A10; SAD10320_P04_C10; SAD10320_P04_D10; SAD10320_P04_E10; SAD10320_P04_F10; SAD10320_P04_G10; SAD10320_P04_A11; SAD10320_P04_D11; SAD10320_P04_E11; SAD10320_P04_F11; SAD10320_P04_G11; SAD10320_P04_H11; SAD10320_P04_A12; SAD10320_P04_D12; SAD10320_P04_E12; SAD10320_P04_F12; LAD9953_P01_H01; LAD9954_P01_B02; LAD9955_P01_G02; LAD9956_P01_C03; LAD9959_P01_E04; LAD9960_P01_D05; LAD9963_P01_E06; LAD9964_P01_C07; и LAD9966_P01_A08.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность YTFX1X2X3X4MH, где X1 представляет собой A, K, D, Q, E, N, T, L, Y, S, P, G, H или V, где X2 представляет собой T, S или A, где X3 представляет собой Y или I и где X4 представляет собой A, D, N, S, Y, T, I, V, L, E, P, R или G (SEQ ID NO: 28). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3 и X4 представляет собой H. Следующий 61 клон включает представленный консенсусный мотив SAD10319_P01_A01; SAD10319_P01_D01; SAD10319_P01_E01; SAD10319_P01_F01; SAD10319_P01_F02; SAD10319_P01_B03; SAD10319_P01_D03; SAD10319_P01_F03; SAD10319_P02_A04; SAD10319_P02_C04; SAD10319_P02_D04; SAD10319_P02_E04; SAD10319_P02_F04; SAD10319_P02_H04; SAD10319_P02_A05; SAD10319_P02_E05; SAD10319_P02_A06; SAD10319_P02_B06; SAD10319_P02_C06; SAD10319_P02_F06; SAD10319_P02_G06; SAD10319_P02_H06; SAD10319_P03_C07; SAD10319_P03_G07; SAD10319_P03_H07; SAD10319_P03_D08; SAD10319_P03_G08; SAD10319_P03_H08; SAD10319_P03_E09; SAD10319_P03_F09; SAD10319_P03_G09; SAD10319_P04_B11; SAD10319_P04_C11; SAD10319_P04_D11; SAD10319_P04_G11; SAD10319_P04_B12; SAD10319_P04_C12; SAD10319_P04_D12; SAD10319_P04_E12; SAD10319_P05_A01; SAD10319_P05_A02; SAD10319_P05_A05; SAD10319_P05_B02; SAD10319_P05_B03; SAD10319_P05_C03; SAD10319_P05_C05; SAD10319_P05_D02; SAD10319_P05_G02; SAD10319_P05_G03; SAD10319_P05_G04; SAD10319_P06_A07; SAD10319_P06_A11; SAD10319_P06_B11; SAD10319_P06_C12; SAD10319_P06_E09; SAD10319_P06_F07; SAD10319_P06_F10; SAD10319_P06_G09; SAD10319_P06_H07; SAD10319_P06_H08 и SAD10319_P06_H10.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность YTFX1X2X3X4MH, где X1 представляет собой T, D, A, N или V, где X2 представляет собой D, E, G или Q, где X3 представляет собой Y или D и где X4 представляет собой D, A, E, N, S, Y или V (SEQ ID NO: 29). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3 и X4 представляет собой H. Следующие 35 клонов включают представленный консенсусный мотив SAD10319_P01_C01; SAD10319_P01_H01; SAD10319_P01_A02; SAD10319_P01_C02; SAD10319_P01_D02; SAD10319_P01_H02; SAD10319_P01_C03; SAD10319_P02_B04; SAD10319_P02_B05; SAD10319_P02_C05; SAD10319_P02_D05; SAD10319_P02_D06; SAD10319_P02_E06; SAD10319_P03_E08; SAD10319_P03_B09; SAD10319_P04_C10; SAD10319_P04_G10; SAD10319_P04_E11; SAD10319_P04_F11; SAD10319_P04_F12; SAD10319_P05_A03; SAD10319_P05_B05; SAD10319_P05_C01; SAD10319_P05_D01; SAD10319_P05_D03; SAD10319_P05_D05; SAD10319_P05_E04; SAD10319_P05_F01; SAD10319_P05_H06; SAD10319_P06_A10; SAD10319_P06_B10; SAD10319_P06_C10; SAD10319_P06_E10; SAD10319_P06_G11; и SAD10319_P06_H11.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность YTFTSX1X2MH, где X1 представляет собой A, D или T, и где X2 представляет собой D, F, A, M, V или Y (SEQ ID NO: 30). В некоторых вариантах осуществления по меньшей мере один из X1 и X2 представляет собой H. Следующие 7 клонов включают представленный консенсусный мотив SAD10319_P01_G01; SAD10319_P01_E02; SAD10319_P04_A10; SAD10319_P04_B10; SAD10319_P04_H12; SAD10319_P05_B04 и SAD10319_P05_D04.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность YTFX1X2YX3MH, где X1 представляет собой N или T, X2 представляет собой Q или N, и X3 представляет собой S, T или A (SEQ ID NO: 31). В некоторых вариантах осуществления по меньшей мере один из X1, X2 и X3 представляет собой H. Следующие 4 клона включают представленный консенсусный мотив SAD10319_P02_F05; SAD10319_P02_G05; SAD10319_P02_H05 и SAD10319_P05_G01.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность YTFX1PX2YVMH, где X1 представляет собой I или N, и где X2 представляет собой K или R (SEQ ID NO: 32). В некоторых вариантах осуществления по меньшей мере один из X1 и X2 представляет собой H. Следующие 2 клона включают представленный консенсусный мотив SAD10319_P06_D12 и SAD10319_P06_E08.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность FNIKDYYMH (SEQ ID NO: 47). По меньшей мере следующие 6 клонов включают представленный консенсусный мотив и обозначены как связывающие молекулы группы 1 ADI-48592, ADI-48595, ADI-48650, ADI-48652, ADI-48662 и ADI-48666. Кроме того, по меньшей мере следующие 16 клонов включают представленный консенсусный мотив и обозначены как связывающие молекулы группы 2 ADI-48575, ADI-48576, ADI-48577, ADI-48581, ADI-48586, ADI-48587, ADI-48588, ADI-48590, ADI-48591, ADI-48593, ADI-48601, ADI-48646, ADI-48647, ADI-48597, ADI-48643 и ADI-48645.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее домен, связывающий CDRH1, при этом консенсусный мотив, при этом консенсусный мотив содержит последовательность YTFX1X2YX3MH, где X1 представляет собой E, S или T, где X2 представляет собой S или D, и где X3 представляет собой A или D (SEQ ID NO: 31). По меньшей мере следующие 5 клона включают представленный консенсусный мотив и обозначены как связывающие молекулы группы 2 ADI-48636, ADI-48638, ADI-48624, ADI-48632 и ADI-48635.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRL3, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность X1X2SX3X4X5RX6, где X1 представляет собой H, K или G, где X2 представляет собой Q или H, где X3 представляет собой Y или H, где X4 представляет собой S, H, D, T, V, M или L, где X5 представляет собой R или H, и где X6 представляет собой T или H (SEQ ID NO: 33). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3, X4 и X5 представляет собой H. Следующие 156 клонов включают представленный консенсусный мотив LAD5224_P03_A01; SAD10318_P01_B01; SAD10318_P01_C01; SAD10318_P01_D01; SAD10318_P01_E01; SAD10318_P01_G01; SAD10318_P01_B02; SAD10318_P01_D02; SAD10318_P01_F02; SAD10318_P01_G02; SAD10318_P01_A03; SAD10318_P01_C03; SAD10318_P01_D03; SAD10318_P01_E03; SAD10318_P01_F03; SAD10318_P02_B04; SAD10318_P02_C04; SAD10318_P02_D04; SAD10318_P02_E04; SAD10318_P02_H04; SAD10318_P02_A05; SAD10318_P02_B05; SAD10318_P02_C05; SAD10318_P02_F05; SAD10318_P02_G05; SAD10318_P02_H05; SAD10318_P02_D06; SAD10318_P02_E06; SAD10318_P02_G06; SAD10318_P03_E07; SAD10318_P03_F07; SAD10318_P03_A08; SAD10318_P03_B08; SAD10318_P03_C08; SAD10318_P03_D08; SAD10318_P03_E08; SAD10318_P03_F08; SAD10318_P03_G08; SAD10318_P03_H08; SAD10318_P03_D09; SAD10318_P03_G09; SAD10318_P04_D10; SAD10318_P04_F10; SAD10318_P04_H10; SAD10318_P04_B11; SAD10318_P04_C11; SAD10318_P04_D11; SAD10318_P04_E11; SAD10318_P04_F11; SAD10318_P04_G11; SAD10318_P04_H11; SAD10318_P04_F12; SAD10318_P04_G12; SAD10318_P04_H12; SAD10319_P01_A01; SAD10319_P01_C01; SAD10319_P01_D01; SAD10319_P01_E01; SAD10319_P01_F01; SAD10319_P01_G01; SAD10319_P01_H01; SAD10319_P01_A02; SAD10319_P01_C02; SAD10319_P01_D02; SAD10319_P01_E02; SAD10319_P01_F02; SAD10319_P01_H02; SAD10319_P01_B03; SAD10319_P01_C03; SAD10319_P01_D03; SAD10319_P01_F03; SAD10319_P02_A04; SAD10319_P02_B04; SAD10319_P02_C04; SAD10319_P02_D04; SAD10319_P02_E04; SAD10319_P02_F04; SAD10319_P02_H04; SAD10319_P02_A05; SAD10319_P02_B05 SAD10319_P02_C05; SAD10319_P02_D05; SAD10319_P02_E05; SAD10319_P02_F05; SAD10319_P02_G05; SAD10319_P02_H05; SAD10319_P02_A06; SAD10319_P02_B06; SAD10319_P02_C06; SAD10319_P02_D06; SAD10319_P02_E06; SAD10319_P02_F06; SAD10319_P02_G06; SAD10319_P02_H06; SAD10319_P03_C07; SAD10319_P03_G07; SAD10319_P03_H07; SAD10319_P03_D08; SAD10319_P03_E08; SAD10319_P03_G08; SAD10319_P03_H08; SAD10319_P03_B09; SAD10319_P03_E09; SAD10319_P03_F09; SAD10319_P03_G09; SAD10319_P04_A10; SAD10319_P04_B10; SAD10319_P04_C10; SAD10319_P04_G10; SAD10319_P04_B11; SAD10319_P04_C11; SAD10319_P04_D11; SAD10319_P04_E11; SAD10319_P04_F11; SAD10319_P04_G11; SAD10319_P04_B12; SAD10319_P04_C12; SAD10319_P04_D12; SAD10319_P04_E12; SAD10319_P04_F12; SAD10319_P04_H12; SAD10320_P01_D01; SAD10320_P01_F01; SAD10320_P01_C02; SAD10320_P01_E02; SAD10320_P01_B03; SAD10320_P01_H03; SAD10320_P02_C04; SAD10320_P02_E04; SAD10320_P02_H04; SAD10320_P02_B05; SAD10320_P02_D05; SAD10320_P02_H05; SAD10320_P02_A06; SAD10320_P02_E06; SAD10320_P02_F06; SAD10320_P02_G06; SAD10320_P03_B07; SAD10320_P03_H07; SAD10320_P03_F08; SAD10320_P04_A10; SAD10320_P04_E10; SAD10320_P04_G10; SAD10320_P04_A11; SAD10320_P04_F11; SAD10320_P04_D12; SAD10320_P04_F12; LAD9953_P01_H01; LAD9954_P01_B02; LAD9955_P01_G02; LAD9956_P01_C03; LAD9959_P01_E04; LAD9960_P01_D05; LAD9963_P01_E06; LAD9964_P01_C07; и LAD9966_P01_A08.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRL3, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KQSYX1X2RT, где X1 представляет собой H, V, K, W, R, L, G, Y, или Q, и где X2 представляет собой H, L, E, W, G, M, P, T, Q или V (SEQ ID NO: 34). В некоторых вариантах осуществления по меньшей мере один из X1 и X2 представляет собой H. Следующие 45 клонов включают представленный консенсусный мотив SAD10318_P01_F01; SAD10318_P01_H01; SAD10318_P01_A02; SAD10318_P01_G03; SAD10318_P01_H03; SAD10318_P02_G04; SAD10318_P02_D05; SAD10318_P02_B06; SAD10318_P03_G07; SAD10318_P03_A09; SAD10318_P03_C09; SAD10318_P03_E09; SAD10318_P04_A12; SAD10320_P01_B01; SAD10320_P01_E01; SAD10320_P01_G01; SAD10320_P01_A02; SAD10320_P01_F02; SAD10320_P01_G02; SAD10320_P01_C03; SAD10320_P01_D03; SAD10320_P01_E03; SAD10320_P01_F03; SAD10320_P01_G03; SAD10320_P02_B04; SAD10320_P02_A05; SAD10320_P02_C05; SAD10320_P02_F05; SAD10320_P02_B06; SAD10320_P02_D06; SAD10320_P02_H06; SAD10320_P03_E07; SAD10320_P03_C08; SAD10320_P03_D08; SAD10320_P03_H08; SAD10320_P03_C09; SAD10320_P04_C10; SAD10320_P04_D10; SAD10320_P04_F10; SAD10320_P04_D11; SAD10320_P04_E11; SAD10320_P04_G11; SAD10320_P04_H11; SAD10320_P04_A12; и SAD10320_P04_E12.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRL3, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность X1QSX2HX3RT, где X1 представляет собой K или H, где X2 представляет собой H, Y, M, S, L, E, G или W, и где X3 представляет собой R или K (SEQ ID NO: 35). В некоторых вариантах осуществления по меньшей мере один из X1, X2 и X3 представляет собой H. Следующие 14 клонов включают представленный консенсусный мотив SAD10318_P03_B07; SAD10318_P03_F09; SAD10318_P04_C10; SAD10318_P04_E10; SAD10318_P04_A11; SAD10320_P01_H01; SAD10320_P01_H02; SAD10320_P01_A03; SAD10320_P02_A04; SAD10320_P02_E05; SAD10320_P02_C06; SAD10320_P03_A09; SAD10320_P03_D09; и SAD10320_P03_F09.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRL3, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KQSX1X2X3RT, где X1 представляет собой Y или H, X2 представляет собой T, S, V или K, а X3 представляет собой R или H (SEQ ID NO: 36). В некоторых вариантах осуществления по меньшей мере один из X1, X2 и X3 представляет собой H. Следующие 11 клонов включают представленный консенсусный мотив ADI-48576; ADI-48577; ADI-48587; ADI-48592; ADI-48595; ADI-48635; ADI-48650; ADI-48652; ADI-48666; ADI-48645 и ADI-48643.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRL3, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KQSX1X2X3RT, где X1 представляет собой H или Y, где X2 представляет собой T, S или Q, и где X3 представляет собой R или H (SEQ ID NO: 36). В некоторых вариантах осуществления по меньшей мере один из X1 и X3 представляет собой H. По меньшей мере следующие 6 клонов включают представленный консенсусный мотив и обозначены как связывающие молекулы группы 1 ADI-48592, ADI-48595, ADI-48650, ADI-48652, ADI-48662 и ADI-48666.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRL3, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность X1QSX2X3X4RT, где X1 представляет собой K или H, где X2 представляет собой Y или H, где X3 представляет собой S, H, L, V или K, и где X4 представляет собой H, R или E (SEQ ID NO: 598). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3 и X4 представляет собой H. По меньшей мере, следующий 21 клон включает представленный консенсусный мотив и обозначен как связывающие молекулы группы 2ADI-48588, ADI-48587, ADI-48577, ADI-48590, ADI-48581, ADI-48575, ADI-48593, ADI-48591, ADI-48647, ADI-48636, ADI-48586, ADI-48646, ADI-48638, ADI-48597, ADI-48601, ADI-48576, ADI-48643, ADI-48624, ADI-48632, ADI-48635 и ADI-48645.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRL2, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность WASTRES (SEQ ID NO: 37). Следующие 215 клонов включают представленный консенсусный мотив LAD5224_P03_A01; SAD10318_P01_B01; SAD10318_P01_C01; SAD10318_P01_D01; SAD10318_P01_E01; SAD10318_P01_F01; SAD10318_P01_G01; SAD10318_P01_H01; SAD10318_P01_A02; SAD10318_P01_B02; SAD10318_P01_D02; SAD10318_P01_F02; SAD10318_P01_G02; SAD10318_P01_A03; SAD10318_P01_C03; SAD10318_P01_D03; SAD10318_P01_E03; SAD10318_P01_F03; SAD10318_P01_G03; SAD10318_P01_H03; SAD10318_P02_B04; SAD10318_P02_C04; SAD10318_P02_D04; SAD10318_P02_E04; SAD10318_P02_G04; SAD10318_P02_H04; SAD10318_P02_A05; SAD10318_P02_B05; SAD10318_P02_C05; SAD10318_P02_D05; SAD10318_P02_F05; SAD10318_P02_G05; SAD10318_P02_H05; SAD10318_P02_B06; SAD10318_P02_D06; SAD10318_P02_E06; SAD10318_P02_G06; SAD10318_P03_B07; SAD10318_P03_E07; SAD10318_P03_F07; SAD10318_P03_G07; SAD10318_P03_A08; SAD10318_P03_B08; SAD10318_P03_C08; SAD10318_P03_D08; SAD10318_P03_E08; SAD10318_P03_F08; SAD10318_P03_G08; SAD10318_P03_H08; SAD10318_P03_A09; SAD10318_P03_C09; SAD10318_P03_D09; SAD10318_P03_E09; SAD10318_P03_F09; SAD10318_P03_G09; SAD10318_P04_C10; SAD10318_P04_D10; SAD10318_P04_E10; SAD10318_P04_F10; SAD10318_P04_H10; SAD10318_P04_A11; SAD10318_P04_B11; SAD10318_P04_C11; SAD10318_P04_D11; SAD10318_P04_E11; SAD10318_P04_F11; SAD10318_P04_G11; SAD10318_P04_H11; SAD10318_P04_A12; SAD10318_P04_F12; SAD10318_P04_G12; SAD10318_P04_H12; SAD10319_P01_A01; SAD10319_P01_C01; SAD10319_P01_D01; SAD10319_P01_E01; SAD10319_P01_F01; SAD10319_P01_G01; SAD10319_P01_H01; SAD10319_P01_A02; SAD10319_P01_C02; SAD10319_P01_D02; SAD10319_P01_E02; SAD10319_P01_F02; SAD10319_P01_H02; SAD10319_P01_B03; SAD10319_P01_C03; SAD10319_P01_D03; SAD10319_P01_F03; SAD10319_P02_A04; SAD10319_P02_B04; SAD10319_P02_C04; SAD10319_P02_D04; SAD10319_P02_E04; SAD10319_P02_F04; SAD10319_P02_H04; SAD10319_P02_A05; SAD10319_P02_B05; SAD10319_P02_C05; SAD10319_P02_D05; SAD10319_P02_E05; SAD10319_P02_F05; SAD10319_P02_G05; SAD10319_P02_H05; SAD10319_P02_A06; SAD10319_P02_B06; SAD10319_P02_C06; SAD10319_P02_D06; SAD10319_P02_E06; SAD10319_P02_F06; SAD10319_P02_G06; SAD10319_P02_H06; SAD10319_P03_C07; SAD10319_P03_G07; SAD10319_P03_H07; SAD10319_P03_D08; SAD10319_P03_E08; SAD10319_P03_G08; SAD10319_P03_H08; SAD10319_P03_B09; SAD10319_P03_E09; SAD10319_P03_F09; SAD10319_P03_G09; SAD10319_P04_A10; SAD10319_P04_B10; SAD10319_P04_C10; SAD10319_P04_G10; SAD10319_P04_B11; SAD10319_P04_C11; SAD10319_P04_D11; SAD10319_P04_E11; SAD10319_P04_F11; SAD10319_P04_G11; SAD10319_P04_B12; SAD10319_P04_C12; SAD10319_P04_D12; SAD10319_P04_E12; SAD10319_P04_F12; SAD10319_P04_H12; SAD10320_P01_B01; SAD10320_P01_D01; SAD10320_P01_E01; SAD10320_P01_F01; SAD10320_P01_G01; SAD10320_P01_H01; SAD10320_P01_A02; SAD10320_P01_C02; SAD10320_P01_E02; SAD10320_P01_F02; SAD10320_P01_G02; SAD10320_P01_H02; SAD10320_P01_A03; SAD10320_P01_B03; SAD10320_P01_C03; SAD10320_P01_D03; SAD10320_P01_E03; SAD10320_P01_F03; SAD10320_P01_G03; SAD10320_P01_H03; SAD10320_P02_A04; SAD10320_P02_B04; SAD10320_P02_C04; SAD10320_P02_E04; SAD10320_P02_H04; SAD10320_P02_A05; SAD10320_P02_B05; SAD10320_P02_C05; SAD10320_P02_D05; SAD10320_P02_E05; SAD10320_P02_F05; SAD10320_P02_H05; SAD10320_P02_A06; SAD10320_P02_B06; SAD10320_P02_C06; SAD10320_P02_D06; SAD10320_P02_E06; SAD10320_P02_F06; SAD10320_P02_G06; SAD10320_P02_H06; SAD10320_P03_B07; SAD10320_P03_E07; SAD10320_P03_H07; SAD10320_P03_C08; SAD10320_P03_D08; SAD10320_P03_F08; SAD10320_P03_H08; SAD10320_P03_A09; SAD10320_P03_C09; SAD10320_P03_D09; SAD10320_P03_F09; SAD10320_P04_A10; SAD10320_P04_C10; SAD10320_P04_D10; SAD10320_P04_E10; SAD10320_P04_F10; SAD10320_P04_G10; SAD10320_P04_A11; SAD10320_P04_D11; SAD10320_P04_E11; SAD10320_P04_F11; SAD10320_P04_G11; SAD10320_P04_H11; SAD10320_P04_A12; SAD10320_P04_D12; SAD10320_P04_E12; SAD10320_P04_F12; LAD9953_P01_H01; LAD9954_P01_B02; LAD9955_P01_G02; LAD9956_P01_C03; LAD9959_P01_E04; LAD9960_P01_D05; LAD9963_P01_E06; LAD9964_P01_C07; и LAD9966_P01_A08. Дополнительно по меньшей мере следующие 6 клонов включают представленный консенсусный мотив и обозначены как связывающие молекулы группы 1 ADI-48592, ADI-48595, ADI-48650, ADI-48652, ADI-48662 и ADI-48666; и по меньшей мере следующий 21 клон включает представленный консенсусный мотив и обозначен как связывающие молекулы группы 2ADI-48588, ADI-48587, ADI-48577, ADI-48590, ADI-48581, ADI-48575, ADI-48593, ADI-48591, ADI-48647, ADI-48636, ADI-48586, ADI-48646, ADI-48638, ADI-48597, ADI-48601, ADI-48576, ADI-48643, ADI-48624, ADI-48632, ADI-48635 и ADI-48645.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRL1, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KSSQSLLX1X2X3X4GX5NX6LA, где X1 представляет собой N или H, где X2 представляет собой A, R или T, где X3 представляет собой R или H, где X4 представляет собой T, P или E, где X5 представляет собой H или K, и где X6 представляет собой H или Y (SEQ ID NO: 38). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3, X4, X5 и X6 представляет собой H. Следующие 203 клонов включают представленный консенсусный мотив LAD5224_P03_A01; SAD10318_P01_B01; SAD10318_P01_D01; SAD10318_P01_E01; SAD10318_P01_F01; SAD10318_P01_G01; SAD10318_P01_H01; SAD10318_P01_B02; SAD10318_P01_D02; SAD10318_P01_F02; SAD10318_P01_G02; SAD10318_P01_A03; SAD10318_P01_C03; SAD10318_P01_D03; SAD10318_P01_E03; SAD10318_P01_F03; SAD10318_P01_G03; SAD10318_P01_H03; SAD10318_P02_B04; SAD10318_P02_C04; SAD10318_P02_D04; SAD10318_P02_E04; SAD10318_P02_G04; SAD10318_P02_H04; SAD10318_P02_A05; SAD10318_P02_B05; SAD10318_P02_C05; SAD10318_P02_D05; SAD10318_P02_F05; SAD10318_P02_H05; SAD10318_P02_B06; SAD10318_P02_D06; SAD10318_P02_G06; SAD10318_P03_B07; SAD10318_P03_E07; SAD10318_P03_F07; SAD10318_P03_G07; SAD10318_P03_A08; SAD10318_P03_B08; SAD10318_P03_C08; SAD10318_P03_D08; SAD10318_P03_E08; SAD10318_P03_F08; SAD10318_P03_G08; SAD10318_P03_H08; SAD10318_P03_A09; SAD10318_P03_C09; SAD10318_P03_D09; SAD10318_P03_E09; SAD10318_P03_F09; SAD10318_P03_G09; SAD10318_P04_C10; SAD10318_P04_D10; SAD10318_P04_E10; SAD10318_P04_H10; SAD10318_P04_A11; SAD10318_P04_B11; SAD10318_P04_C11; SAD10318_P04_D11; SAD10318_P04_E11; SAD10318_P04_F11; SAD10318_P04_G11; SAD10318_P04_H11; SAD10318_P04_A12; SAD10318_P04_F12; SAD10318_P04_G12; SAD10318_P04_H12; SAD10319_P01_A01; SAD10319_P01_C01; SAD10319_P01_D01; SAD10319_P01_E01; SAD10319_P01_F01; SAD10319_P01_G01; SAD10319_P01_H01; SAD10319_P01_A02; SAD10319_P01_C02; SAD10319_P01_D02; SAD10319_P01_E02; SAD10319_P01_F02; SAD10319_P01_H02; SAD10319_P01_B03; SAD10319_P01_C03; SAD10319_P01_D03; SAD10319_P01_F03; SAD10319_P02_A04; SAD10319_P02_B04; SAD10319_P02_C04; SAD10319_P02_D04; SAD10319_P02_E04; SAD10319_P02_F04; SAD10319_P02_H04; SAD10319_P02_A05; SAD10319_P02_B05; SAD10319_P02_C05; SAD10319_P02_D05; SAD10319_P02_E05; SAD10319_P02_F05; SAD10319_P02_G05; SAD10319_P02_H05; SAD10319_P02_A06; SAD10319_P02_B06; SAD10319_P02_C06; SAD10319_P02_D06; SAD10319_P02_E06; SAD10319_P02_F06; SAD10319_P02_G06; SAD10319_P02_H06; SAD10319_P03_C07; SAD10319_P03_G07; SAD10319_P03_H07; SAD10319_P03_D08; SAD10319_P03_E08; SAD10319_P03_G08; SAD10319_P03_H08; SAD10319_P03_B09; SAD10319_P03_E09; SAD10319_P03_F09; SAD10319_P03_G09; SAD10319_P04_A10; SAD10319_P04_B10; SAD10319_P04_C10; SAD10319_P04_G10; SAD10319_P04_B11; SAD10319_P04_C11; SAD10319_P04_D11; SAD10319_P04_E11; SAD10319_P04_F11; SAD10319_P04_G11; SAD10319_P04_B12; SAD10319_P04_C12; SAD10319_P04_D12; SAD10319_P04_E12; SAD10319_P04_F12; SAD10319_P04_H12; SAD10320_P01_B01; SAD10320_P01_D01; SAD10320_P01_E01; SAD10320_P01_F01; SAD10320_P01_G01; SAD10320_P01_H01; SAD10320_P01_A02; SAD10320_P01_C02; SAD10320_P01_E02; SAD10320_P01_F02; SAD10320_P01_G02; SAD10320_P01_H02; SAD10320_P01_A03; SAD10320_P01_B03; SAD10320_P01_C03; SAD10320_P01_D03; SAD10320_P01_E03; SAD10320_P01_F03; SAD10320_P01_G03; SAD10320_P01_H03; SAD10320_P02_A04; SAD10320_P02_B04; SAD10320_P02_C04; SAD10320_P02_E04; SAD10320_P02_H04; SAD10320_P02_A05; SAD10320_P02_B05; SAD10320_P02_C05; SAD10320_P02_D05; SAD10320_P02_E05; SAD10320_P02_F05; SAD10320_P02_H05; SAD10320_P02_A06; SAD10320_P02_B06; SAD10320_P02_C06; SAD10320_P02_D06; SAD10320_P02_E06; SAD10320_P02_F06; SAD10320_P02_H06; SAD10320_P03_B07; SAD10320_P03_E07; SAD10320_P03_H07; SAD10320_P03_C08; SAD10320_P03_D08; SAD10320_P03_F08; SAD10320_P03_A09; SAD10320_P03_C09; SAD10320_P03_D09; SAD10320_P03_F09; SAD10320_P04_A10; SAD10320_P04_C10; SAD10320_P04_D10; SAD10320_P04_E10; SAD10320_P04_F10; SAD10320_P04_G10; SAD10320_P04_A11; SAD10320_P04_D11; SAD10320_P04_E11; SAD10320_P04_F11; SAD10320_P04_G11; SAD10320_P04_H11; SAD10320_P04_A12; SAD10320_P04_D12; SAD10320_P04_E12; SAD10320_P04_F12; LAD9954_P01_B02; LAD9955_P01_G02; LAD9963_P01_E06 и LAD9966_P01_A08.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRL1, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KSSQSLLX1AX2THX3NX4LA, где X1 представляет собой N или H, где X2 представляет собой R или H, где X3 представляет собой K или H, и где X4 представляет собой Y или H (SEQ ID NO: 39). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3 и X4 представляет собой H. Следующие 10 клонов включают представленный консенсусный мотив SAD10318_P01_C01; SAD10318_P01_A02; SAD10318_P02_G05; SAD10318_P02_E06; SAD10318_P04_F10; LAD9953_P01_H01; LAD9956_P01_C03; LAD9959_P01_E04; LAD9960_P01_D05; и LAD9964_P01_C07.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRL1, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KSSQSLLNASTAKNYLA (SEQ ID NO: 40) или KSSQSLLNARTRTNYLA (SEQ ID NO: 41).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRL1, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KSSQSLLNX1X2X3GX4NX5LA, где X1 представляет собой S или A, X2 представляет собой R или H, X3 представляет собой E или T, X4 представляет собой H или K, а X5 представляет собой H или Y (SEQ ID NO: 42). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X3, X4 и X5 представляет собой H. Следующие 11 клонов включают представленный консенсусный мотив ADI-48576; ADI-48577; ADI-48587; ADI-48592; ADI-48595; ADI-48635; ADI-48645; ADI-48650; ADI-48652; ADI-48643 и ADI-48666.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRL1, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KSSQSLLNX1X2TGX3NYLA, где X1 представляет собой A или S, где X2 представляет собой R или H, и где X3 представляет собой H или K (SEQ ID NO: 594). В некоторых вариантах осуществления по меньшей мере один из X2 и X3 представляет собой H. По меньшей мере следующие 6 клонов включают представленный консенсусный мотив и обозначены как связывающие молекулы группы 1 ADI-48592, ADI-48595, ADI-48650, ADI-48652, ADI-48662 и ADI-48666.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRL1, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KSSQSLLX1AX2X3X4X5NX6LA, где X1 представляет собой N или H, где X2 представляет собой R или H, где X3 представляет собой T или E, где X4 представляет собой G или H, где X5 представляет собой H или K, и где X6 представляет собой H или Y (SEQ ID NO: 597). В некоторых вариантах осуществления по меньшей мере один из X1, X2, X4, X5 и X6 представляет собой H. По меньшей мере следующий 21 клон включает представленный консенсусный мотив и обозначен как связывающие молекулы группы 2ADI-48588, ADI-48587, ADI-48577, ADI-48590, ADI-48581, ADI-48575, ADI-48593, ADI-48591, ADI-48647, ADI-48636, ADI-48586, ADI-48646, ADI-48638, ADI-48597, ADI-48601, ADI-48576, ADI-48643, ADI-48624, ADI-48632, ADI-48635 и ADI-48645.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность AX1DX2YX3HX4FYDV, где X1 представляет собой R или H, где X2 представляет собой A или H, где X3 представляет собой G, H или P и где X4 представляет собой Y, H, D, V, E, S, N, L, M, I, G, A, Q или T (SEQ ID NO: 1); домен, связывающий CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9); WINPX1TGATX2YSQKFQG, где X1 представляет собой S, D, A, N, L или Q и где X2 представляет собой V, T, D, Y или K (SEQ ID NO: 45); или X1IDAGTGATX2YSQKFQG, где X1 представляет собой W, S или D, и где X2 представляет собой A, H, K, T или D (SEQ ID NO: 46); домен, связывающий CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность FNIKDYYMH (SEQ ID NO: 47); связывающий домен CDRL3, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KSQYX1X2RT, где X1 представляет собой S, H, V, K, W, L, G, T, R или Q и где X2 представляет собой H, R, L, K, E, W, G, M, T или V (SEQ ID NO: 48); домен, связывающий CDRL2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WASTRES (SEQ ID NO: 37), и домен, связывающий CDRL1, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KSSQSLLNARTGKNYLA (SEQ ID NO: 49).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDX1YGX2X3X4YDX5 где X1 представляет собой A или H, где X2 представляет собой R или H, где X3 представляет собой H или Y, где X4 представляет собой F или H, и где X5 представляет собой H или V (SEQ ID NO: 2); домен, связывающий CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9) или WIX1AGTGATX2YSQKGQG, где X1 представляет собой T, N или D, и где X2 представляет собой V или K (SEQ ID NO: 50); домен, связывающий CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность FNIKDYYMH (SEQ ID NO: 47) или YTFX1X2YX3MH, где X1 представляет собой T или A, X2 представляет собой E, D, A, S, G или Q, а X3 представляет собой D, A, V или E (SEQ ID NO: 51); связывающий домен CDRL3, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KQSX1SRRT, где X1 представляет собой H или Y (SEQ ID NO: 52); домен, связывающий CDRL2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WASTRES (SEQ ID NO: 37); и связывающий домен CDRL1, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KSSQSLLX1AX2TX3X4NX5LA, где X1 представляет собой N или H, X2 представляет собой R или H, X3 представляет собой G или H, X4 представляет собой K или H, а X5 представляет собой H или Y (SEQ ID NO: 53).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело, содержащее связывающий домен CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDAHX1X2YX3X4DX5, где X1 представляет собой G, E или R, где X2 представляет собой R или H, где X3 представляет собой F или H, где X4 представляет собой Y или H, и где X5 представляет собой V или H (SEQ ID NO: 3); домен, связывающий CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9); домен, связывающий CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность FNIKDYYMH (SEQ ID NO: 47); домен, связывающий CDRL3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность KQSYSRRT (SEQ ID NO: 54); домен, связывающий CDRL2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WASTRES (SEQ ID NO: 37); и связывающий домен CDRL1, содержащий консенсусный мотив, при этом консенсусный мотив включает последовательность KSSQSLLNAX1TGX2NX3LA, где X1 представляет собой H или R, где X2 представляет собой H или K, а X3 представляет собой H или Y (SEQ ID NO: 55).
В некоторых вариантах осуществления в настоящем изобретении представлено антитело или антигенсвязывающий фрагмент, содержащее домен, связывающий CDRH3, который содержит консенсусный мотив, при этом консенсусный мотив содержит последовательность ARDAX1X2X3X4FYDX5, где X1 представляет собой T, H или Y, где X2 представляет собой G или H, где X3 представляет собой H или R, где X4 представляет собой V или Y, где X5 представляет собой V или H и где необязательно по меньшей мере один из X1, X2, X3, и X5 представляет собой H (SEQ ID NO: 593); домен, связывающий CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9); домен, связывающий CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность FNIKDYYMH (SEQ ID NO: 47); домен, связывающий CDRL3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность KQSX1X2X3RT, где X1 представляет собой H или Y, где X2 представляет собой T, S или Q, где X3 представляет собой R или H и где необязательно по меньшей мере один из X1 и X3 представляет собой H (SEQ ID NO: 36); домен, связывающий CDRL2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WASTRES (SEQ ID NO: 37); и/или домен, связывающий CDRL1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность KSSQSLLNX1X2TGX3NYLA, где X1 представляет собой A или S, где X2 представляет собой R или H, где X3 представляет собой H или K и где необязательно по меньшей мере один из X2 и X3 представляет собой H (SEQ ID NO: 594). В некоторых вариантах осуществления указанное антитело или антигенсвязывающий фрагмент обозначают как связывающую молекулу группы 1, содержащую домен, связывающий CD3, выбранный из ADI-48592, ADI-48595, ADI-48650, ADI-48652, ADI-48662 и ADI-48666.
В некоторых вариантах осуществления в настоящем изобретении представлено антитело или антигенсвязывающий фрагмент, содержащие домен, связывающий CDRH3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность AX1DX2X3X4X5X6X7YDX8, где X1 представляет собой R или H, где X2 представляет собой H или A, где X3 представляет собой H или Y, где X4 представляет собой H, G или P, где X5 представляет собой R или H, где X6 представляет собой Y, I или V, где X7 представляет собой F или H, где X8 представляет собой V или H и необязательно где по меньшей мере один из X1, X2, X3, X4, X5, X7, и X8 представляет собой H (SEQ ID NO: 596); домен, связывающий CDRH2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9) или последовательность WIDAGTGX1TX2YSQKFQG, где X1 представляет собой L, F, N или A, и где X2 представляет собой T или K (SEQ ID NO: 595); домен, связывающий CDRH1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность FNIKDYYMH (SEQ ID NO: 47) или последовательность YTFX1X2YX3MH, где X1 представляет собой E, S или T, где X2 представляет собой S или D и где X3 представляет собой A или D (SEQ ID NO: 31); домен, связывающий CDRL3, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность X1QSX2X3X4RT, где X1 представляет собой K или H, где X2 представляет собой Y или H, где X3 представляет собой S, H, L, V или K, где X4 представляет собой H, R или E и необязательно где по меньшей мере один из X1, X2, X3 и X4 представляет собой H (SEQ ID NO: 598); домен, связывающий CDRL2, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность WASTRES (SEQ ID NO: 37); домен, связывающий CDRL1, содержащий консенсусный мотив, при этом консенсусный мотив содержит последовательность KSSQSLLX1X2X3X4GX5NX6LA, где X1 представляет собой N или H, где X2 представляет собой R или Н, где X3 представляет собой T или E, где X4 представляет собой G или H, где X5 представляет собой H или K, где X6 представляет собой H или Y и где необязательно по меньшей мере один из X1, X2, X4, X5 и X6 представляет собой H (SEQ ID NO: 597). В некоторых вариантах осуществления указанное антитело или антигенсвязывающий фрагмент обозначают как связывающую молекулу группы 2, содержащую домен, связывающий CD3, выбранный из ADI-48588, ADI-48587, ADI-48577, ADI-48590, ADI-48581, ADI-48575, ADI-48593, ADI-48591, ADI-48647, ADI-48636, ADI-48586, ADI-48646, ADI-48638, ADI-48597, ADI-48601, ADI-48576, ADI-48643, ADI-48624, ADI-48632, ADI-48635, и ADI-48645.
Материалы и способы
В дополнение к описанию, представленному выше, в примерах использовали следующие материалы и способы.
Продуцирование гетеродимерных антигенов Hu и Cy CD3εδ Fc. Рекомбинантные гетеродимерные Fc-слитые антигены CD3 получали в клетках HEK 293 путем котрансфекции плазмид, кодирующих Hu CD3ε Fc (эктодомен, ECD, остатки 22-126) и CD3δ Fc-HIS (ECD, остатки 22-100) или Cy CD3ε Fc (ECD, остатки 22-117) и CD3δ Fc-HIS (ECD, остатки 22-100), с использованием гетерологичной последовательности сигнального пептида. Хроматографические разделения проводили на компьютеризованной системе для препаративной хроматографии ÄKTA Avant 150 (GE Healthcare Life Sciences), оснащенной встроенным кондуктометрическим датчиком, позволяющим отслеживать поточную концентрацию соли в ходе прогона. Осветленные культуральные супернатанты очищали с помощью Ni Sepharose 6 Fast Flow (GE Healthcare Life Sciences), которая удаляет гомодимер CD3εε Fc-HIS. Гетеродимер CD3εδ Fc-HIS отделяли от гомодимера CD3δδ Fc-HIS с помощью Mono Q 10/100 GL с применением линейного градиента KCl в буфере Tris при pH 8,5.
Пептиды. N-концевые пептиды CD3ε, биотинилированные на C-конце, получали от New England Peptide. Все пептиды поставлялись при чистоте ≥95%. Пептиды конструировали на основе первичной последовательности Hu CD3ε и кристаллической структуры Hu CD3εδ, связанного с OKT3 (Kjer-Nielsen L. et al. PNAS 2004). Пептид CD3εN27 имеет последовательность H2N-QDGNEEMGSITQTPYQVSISGTTVILT[K/SCBiot(dPEG4)]-амид (SEQ ID NO: 56), а пептид CD3εN13 имеет последовательность H2N-QDGNEEMGGITQT[K/SCBiot(dPEG4)]-амид (SEQ ID NO: 57).
Биотинилирование антигенов. Антигены CD3 биотинилировали с применением набора для биотинилирования EZ-Link Sulfo-NHS от Pierce. Антитело козы к F(ab’)2-каппа человека, конъюгированное с FITC (LC-FITC), экстравидин-PE (EA-PE) и стрептавидин-633 (SA-633) получали соответственно от Southern Biotech, Sigma и Molecular Probes. Стрептавидиновые микрогранулы и колонки для LC-разделения MACS приобретали у Miltenyi Biotec.
Размножение клеточных линий и анализы мечения клеток. Человеческие CD3+ клетки Jurkat (ATCC TIB-152) и CD3- клетки Jurkat (ATCC TIB-153) получали от ATCC. Клетки HSC-F яванского макака получали из лаборатории ресурсов реактивов от приматов, отличных от человека, в NIH. Все линии клеток культивировали в средах RPMI 1640 GlutaMax, дополненных 10% фетальной бычьей сыворотки (FBS).
Мечение клеток проводили путем разделения на аликвоты, содержащие 100000-200000 клеток на лунку, в 96-луночном аналитическом планшете. Клетки центрифугировали при 500 x g в течение 5 мин. при 4°C, затем ресуспендировали в 100 мкл 100 нМ IgG и инкубировали при комнатной температуре в течение 20 мин. Затем клетки трижды промывали в буфере (забуференный фосфатом солевой раствор (PBS)/0,1% бычьего сывороточного альбумина (BSA) и ресуспендировали во вторичном реагенте, как правило, в антителе козы к R человека, конъюгированному с PE (Southern Biotech). Планшет анализировали на FACSCanto (BD Biosciences) с применением устройства для ввода образцов HTS. Данные проточной цитометрии анализировали в отношении медианной интенсивности флуоресценции в канале R-PE.
Способы FACS-отбора с давлением аффинности. Вкратце, клетки дрожжей (по меньшей мере ~2 x 107 клеток/параметр мечения) инкубировали с достаточным объемом биотинилированного антигена, чтобы обеспечить стехиометрический избыток относительно среднего числа презентирования IgG. Параметры мечения альбумина представляют собой 100-1 нМ в равновесных условиях; как правило, мечение проводили в течение от 20 мин. до нескольких часов при комнатной температуре в буфере для промывки FACS (забуференный фосфатом солевой раствор (PBS)/0,1% бычьего сывороточного альбумина (BSA)). Затем после трехкратной промывки с помощью буфера для промывки, дрожжи окрашивали с помощью вторичных реагентов, конъюгата антитела к легкой цепи человека с FITC (LC-FITC), разбавленного 1:100, и либо стрептавидина-633 (SA-633), разбавленного 1:500, либо экстравидина-фикоэритрина (EA-PE), разбавленного 1:50, в течение 15 мин. при 4°C. После двукратной промывки с помощью ледяного буфера для промывки клеточные осадки ресуспендировали в буфере для промывки в типичном объеме, составляющем по меньшей мере 1 мл на 1 x 107 дрожжей и переносили в пробирки для сортировки, закрытые защелкивающейся крышкой с ситом. Сортировку проводили с применением сортера FACS ARIA (BD Biosciences) и определяли сортировочные гейты для отбора связывающих молекул. После последнего раунда сортировки дрожжи высевали и отдельные колонии отбирали для определения характеристик.
Продуцирование антитела в дрожжах и его очистка. Клоны дрожжей выращивали до насыщения, а затем индуцировали в течение 48 ч. при 30°C со встряхиванием. После индукции клетки дрожжей осаждали и супернатанты собирали для очистки. IgG очищали с использованием колонки с белком A и элюировали с помощью уксусной кислоты, pH 2,0. Fab-фрагменты получали с помощью расщепления под действием папаина и очищали путем пропускания через KappaSelect или CaptureSelect IgG-CH1 (GE Healthcare LifeSciences).
Продуцирование антитела в HEK и его очистка. Экспрессию IgG в клетках млекопитающих выполняли путем субклонирования антител в новый вектор экспрессии с последующими временной трансфекцией и экспрессией в HEK293ADI1, моноклональной линией клеток, полученной из HEK293 (DSMZ), выбранной из-за роста без образования скоплений, скорости роста и трансфицируемости. Вкратце, векторы экспрессии, содержащие представляющее интерес антитело, трансфицировали путем образования комплекса с реагентом для трансфекции с последующим воздействием на клетки HEK в течение одного часа, после чего следовало разбавление питательной средой до конечной плотности, составляющей 4 миллиона клеток на мл. Затем клетки культивировали в течение 7 дней с подпиткой свежей средой через каждые 48 часов. Через 7 дней супернатант собирали после центрифугирования и проводили очистку с применением белка A. При необходимости добавочно использовали очистку на колонке CHT для достижения >95% мономеров.
Анализы связывания клеток. CD3+ клетки Jurkat человека и клетки CHO-S (Invitrogen/ ThermoFisher) подвергали оттаиванию и промывали холодным буфером PBSF, pH 7,4 (PBS+0,1% BSA, pH 7,4). Приблизительно 200000 клеток отбирали аликвотами на лунку 96-луночного планшета (FACS Assay Plate VWR BD 353263) и осаждали центрифугированием (5 минут при 500 × g). Клетки промывали либо PBSF pH 7,4, либо PBSF pH 6,0 (PBS+0,1% BSA, pH 6,0), а затем ресуспендировали в 100 мкл либо PBSF pH 7,4, либо PBSF pH 6,0 с антителом IgG (100 нМ), продуцируемым в дрожжах, как описано выше. Смесь (клетки + антитело) инкубировали в течение 20 минут на льду, затем дважды промывали либо PBSF pH 7,4, либо PBSF pH 6,0. Клетки ресуспендировали в 50 мкл йодида пропидия (Roche; разведение 1:500) и готовили антитела к IgG-RPE человека (Southern Biotech; разведение 1:100) либо в PBSF pH 7,4, либо в PBSF pH 6,0, затем инкубировали в течение 20 минут на льду в темноте, до того, как клетки дважды промывали либо PBSF pH 7,4, либо PBSF pH 6,0. Связывание анализировали на FACS Canto II.
Измерения KD с помощью ForteBio (интерферометрия биослоя; BLI). Измерения аффинности с помощью ForteBio проводили в целом так, как это описано ранее (Estep, P., et al., High throughput solution-based measurement of antibody-antigen affinity and epitope binning. MAbs, 2013. 5(2): p. 270-8). Вкратце, измерения аффинности с помощью ForteBio проводили путем загрузки IgG в рабочем режиме на сенсоры AHC. Сенсоры уравновешивали в холостом режиме с помощью буфера для анализа в течение 30 мин., а затем отслеживали в рабочем режиме в течение 60 секунд для установки исходных значений. Сенсоры с загруженными IgG подвергали воздействию 100 нМ антигена (например, CD3) в течение 5 мин., после чего их переносили в буфер для анализа на 5 мин. для измерения скорости диссоциации. Кинетику анализировали с применением модели связывания 1:1.
Получение PSR. Реагент полиспецифической реактивности (PSR) получали так, как это описано, например, в WO 2014/179363 и Xu et.al., Protein Eng Des Sel, 26(10):663-670 (2013). Вкратце, 2,5 литра клеток CHO-S применяли в качестве начального материала. Клетки осаждали при 2400 x g в течение 5 мин. в 500-мл центрифужных бутылях, заполненных до 400 мл. Клеточные осадки объединяли, а затем ресуспендировали в 25 мл буфера B и осаждали при 2400 x g в течение 3 мин. Буфер декантировали и промывку повторяли еще раз. Клеточные осадки ресуспендировали в 3x объеме осадка буфера B, содержащего 1x ингибиторы протеаз (Roche, Complete, без EDTA), с применением гомогенизатора Polytron, при этом клетки выдерживали на льду. Затем гомогенат центрифугировали при 2400 x g в течение 5 мин. и супернатант выдерживали и дополнительно однократно осаждали (2400 x g/5 мин.) с тем, чтобы обеспечить удаление неразрушенных клеток, клеточного дебриса и ядер; полученный супернатант представляет собой препарат общего белка. Затем супернатант переносили в две 45-мл центрифужные пробирки Nalgene Oak Ridge и осаждали при 40000 x g в течение 40 мин. при 4°C. Затем супернатанты, содержащие отделенные цитозольные белки (SCP), переносили в чистые пробирки Oak Ridge и дополнительно однократно центрифугировали при 40000 x g. Параллельно осадки, содержащие мембранную фракцию (EMF), выдерживали и центрифугировали при 40000 в течение 20 мин. для удаления остаточного супернатанта. Затем осадки с EMF ополаскивали с помощью буфера B. Затем 8 мл буфера B добавляли к осадкам, содержащим мембраны, для разрыхления осадков и их переносили в гомогенизатор Даунса. После гомогенизации осадков их переносили в 50-мл коническую пробирку, и они представляли собой конечный препарат EMF.
Один миллиард клеток млекопитающих (например, CHO, HEK293, Sf9) при концентрации ~106 - 107 клеток/мл переносили из среды культивирования тканей в 4x 250 мл конические пробирки и осаждали при 550 x g в течение 3 мин. Все последующие стадии проводили при 4°C или на льду с ледяными буферами. Клетки промывали с помощью 100 мл PBSF (1x PBS + 1 мг/мл BSA) и объединяли в одной конической пробирке. После удаления супернатанта затем клеточный осадок ресуспендировали в 30 мл буфера B (50 мМ HEPES, 0,15 M NaCl, 2 мМ CaCl2, 5 мМ KCl, 5 мМ MgCl2, 10% глицерина, pH 7,2) и осаждали при 550 x g в течение 3 мин. Супернатант из буфера B декантировали и клетки ресуспендировали в 3x объеме осадка буфера B с 2,5x ингибитором протеаз (Roche, Complete, без EDTA). С этого момента и далее в буфер B включены ингибиторы протеаз. Клетки гомогенизировали четыре раза на протяжении 30-секундных импульсов (гомогенизатор Polytron, PT1200E) и мембранную фракцию осаждали при 40000 x g в течение 1 часа при 4°C. Осадок ополаскивали с помощью 1 мл буфера B; супернатант выдерживали, и он представляет собой. Осадок переносили в гомогенизатор Даунса с 3 мл буфера B и ресуспендировали путем медленного подъема и опускания пестика в ходе 30-35 движений. Обогащенную мембранную фракцию (EMF) переносили в новую пробирку для сбора, промывая пестик для сбора всего возможного белка. Концентрацию белка в очищенной EMF определяли с применением набора для анализа белка Dc (BioRad). Чтобы солюбилизировать EMF, ее переносили в буфер для солюбилизации (50 мМ HEPES, 0,15 M NaCl, 2 мМ CaCl2, 5 мМ KCl, 5 мМ MgCl2, 1% н-додецил-b-D-мальтопиранозида (DDM), 1x ингибитор протеаз, pH 7,2) с получением конечной концентрации 1 мг/мл. Смесь перемешивали в течение ночи при 4°C путем вращения с последующим центрифугированием в пробирке объемом 50 мл Oak Ridge (Fisher Scientific, 050529-ID) при 40000 x g в течение 1 часа. Собирали супернатант, который представляет собой растворимые мембранные белки (SMP), и количественно оценивали выход белка так, как это описано выше.
Для биотинилирования готовили исходный раствор NHS-LC-биотина в соответствии с протоколом производителя (Pierce, Thermo Fisher). Вкратце, 20 мкл реагента биотина добавляли на каждый 1 мг образца EMF и инкубировали при 4°C в течение 3 часов при аккуратном перемешивании. Объем доводили до 25 мл с помощью буфера B и переносили в центрифужную пробирку Oak Ridge. Биотинилированную EMF (b-EMF) осаждали при 40000 x g в течение 1 часа и дважды промывали с помощью 3 мл буфера C (буфер B без глицерина), не нарушая целостность осадка. Остаточный раствор удаляли. Осадок ресуспендировали с помощью гомогенизатора Даунса в 3 мл буфера C так, как это описано ранее. Теперь ресуспендированный осадок представлял собой биотинилированную EMF (b-EMF). Проводили солюбилизацию, как это описано выше, для получения b-SMP.
Анализы связывания PSR. Анализы проводили в целом так, как это описано, например, в Xu et al. Protein Eng Des Sel, 26(10):663-670 (2013). Чтобы охарактеризовать профиль PSR моноклональных антител, презентированных на дрожжах, два миллиона дрожжей, презентирующих IgG, переносили в 96-луночный аналитический планшет и осаждали при 3000 x g в течение 3 мин. для удаления супернатанта. Осадок ресуспендировали в 50 мкл свежеприготовленного разбавления 1:10 исходных растворов b-PSR и инкубировали на льду в течение 20 минут. Клетки дважды промывали с помощью 200 мкл холодного PBSF и осадок ресуспендировали в 50 мкл смеси для вторичного мечения (экстравидин-R-PE, антитело к LC человека, конъюгированное с FITC и йодидом пропидия). Смесь инкубировали на льду в течение 20 минут с последующими двумя промывками с помощью 200 мкл ледяного PBSF. Клетки ресуспендировали в 100 мкл ледяного PBSF и планшет прогоняли на FACSCanto (BD Biosciences) с применением устройства для ввода образцов HTS. Данные проточной цитометрии анализировали в отношении средней интенсивности флуоресценции в канале R-PE и нормализовали относительно надлежащих контролей для оценки неспецифического связывания. Ранее были описаны многочисленные способы презентации или отображения антител или фрагментов антител на поверхности дрожжей, все из которых соответствуют данному протоколу (Blaise et al., Gene, 342(2):211-8 (2004), Boder and Wittrup, Nat Biotechnol., 15(6):553-7 (1997), Kuroda and Ueda, Biotechnol Lett., 33(1):1-9 (2011), Orcutt and Wittrup, Springer Protocols: Antibody Engineering, 1:207-233 (2010), Rakestraw et al., Protein Eng Des Sel., 24(6):525-30 (2011), Sazinsky et al., Proc Natl Acad Sci U S A., 105(51):20167-72 (2008), Tasumi et al., Proc Natl Acad Sci U S A., 106(31):12891-6 (2009)).
Кинетический анализ с помощью ForteBio. Устройства FortBio Octet HTX применяли в 12-канальном режиме (8 сенсоров на канал, 96 сенсоров на эксперимент) с одним из сенсоров AHC, SA или AHQ. Устройство управлялось посредством программного обеспечения, поставляемого производителем (версия 8.2 и 9.0). Названия образцов и концентрации вводились на страницу данных о планшете, а белки, ассоциированные с сенсором, идентифицировались в колонке «информация» на странице данных сенсора. Данные экспериментов по кинетике собирали на 90 или 180 с исходного уровня, 180 с фазы ассоциации и 180 с фазы диссоциации. Все файлы сохраняли на сетевой диск общего пользования согласно правилу формирования названий, которые идентифицируют формат эксперимента.
HIC. Образцы IgG1 подвергали замене буфера на 1 M сульфат аммония и 0,1 M фосфат натрия при pH 6,5 с применением 0,5-мл спин-колонки Zeba 40 кДа (Thermo Pierce, № по кат. 87766). Градиент солей устанавливали на колонке Dionex ProPac HIC-10 от 1,8 M сульфата аммония, 0,1 M фосфата натрия при pH 6,5 до таких же параметров без аммония сульфата. Градиент пропускали на 17 мин. при расходе 0,75 мл/мин. В конце прогона добавляли стадию промывки ацетонитрилом для удаления всего оставшегося белка, а колонку снова уравновешивали посредством 7 объемов колонки перед следующим циклом введения. Значения времени удерживания пиков отслеживали при поглощении A280 и концентрации сульфата аммония при элюировании рассчитывали на основе градиента и расхода.
LCMS. Образцы mAb восстанавливали с помощью DTT с последующей передачей анализа LCMS вниз на масс-спектрометр Bruker maXis4G, соединенный с Agilent 1100 HPLC (Agilent). Для удаления соли из образцов применяли колонку для обращенно-фазовой хроматографии POROS R2 10 мкм (2,1 x 30 мм). Быстрый поток LC при 2 мл/мин. обеспечивает разделение между образцом и солью, и элюирование образцов и регенерация колонки завершались в пределах цикла 2,1 мин. T-образное соединение применяли для доставки только 0,15 мл/мин. потока образца в масс-спектрометр для анализа образца. Масс-спектрометр Bruker Maxis 4G прогоняли в режиме положительных ионов с детекцией в диапазоне 750-2500 масса/заряд. Остальные параметры источника устанавливали следующим образом: капилляр был установлен на 5500В, распылитель на 4,0 бар, сушильный газ из расчета 4,0 л/мин. и температуру сушки устанавливали на 200°C.
MS-спектры анализировали с применением программы для анализа данных Bruker версии 4.1, а деконволюцию осуществляли с применением максимально энтропийной деконволюции с массой в диапазоне 20-30 кДа.
Неофициальный перечень последовательностей представлен в таблице 1. В неофициальном перечне последовательностей представлена аминокислотная последовательность вариабельной области тяжелой цепи («НС») с подчеркнутыми CDR каждой из вариабельных областей тяжелой цепи и вариабельной области легкой цепи («LC») с подчеркнутыми CDR каждой из вариабельных областей легкой цепи.
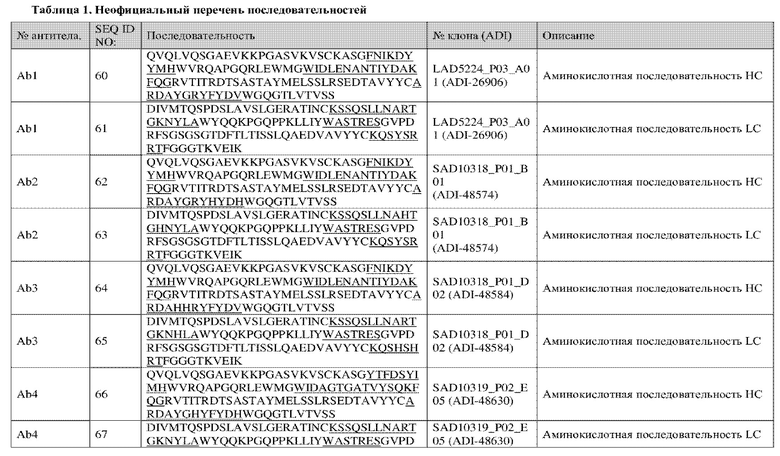
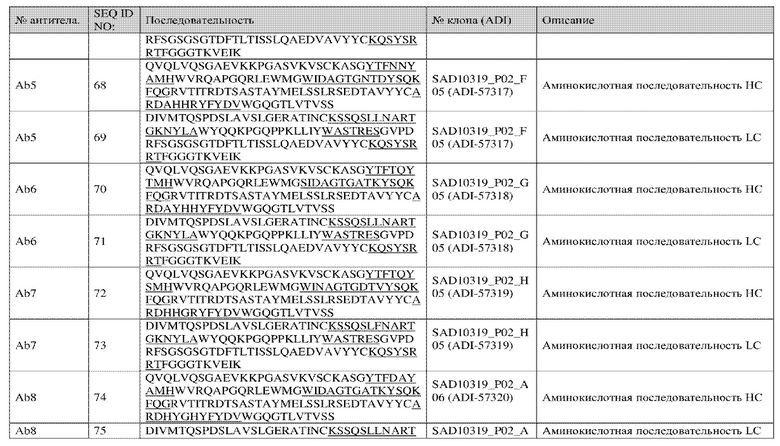
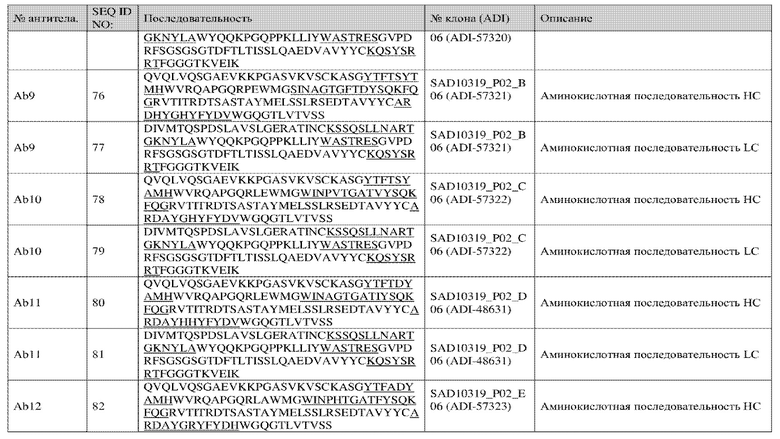
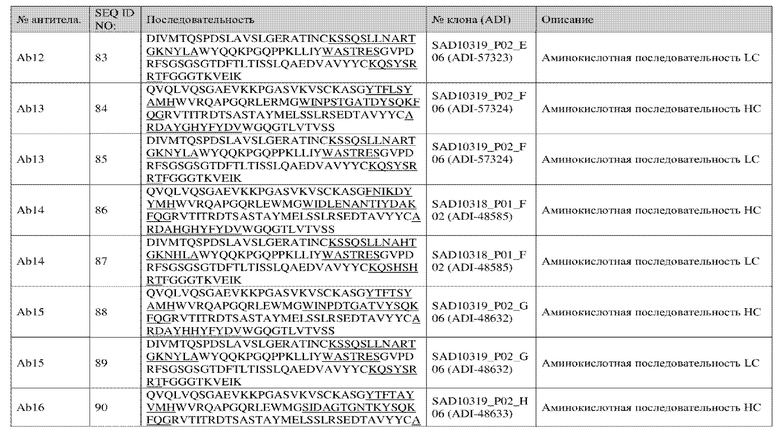
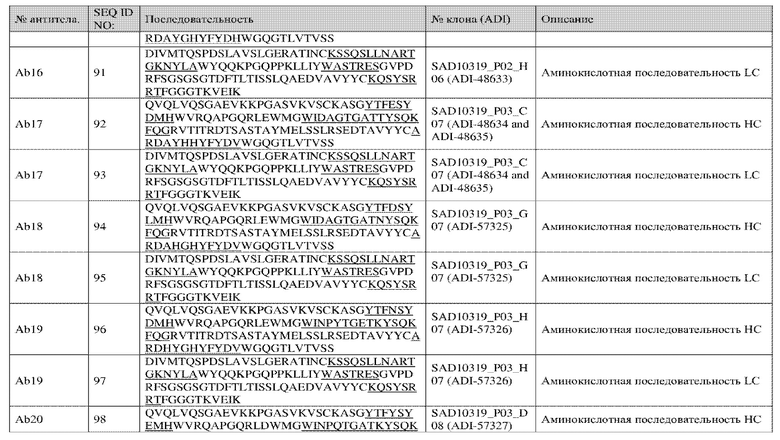
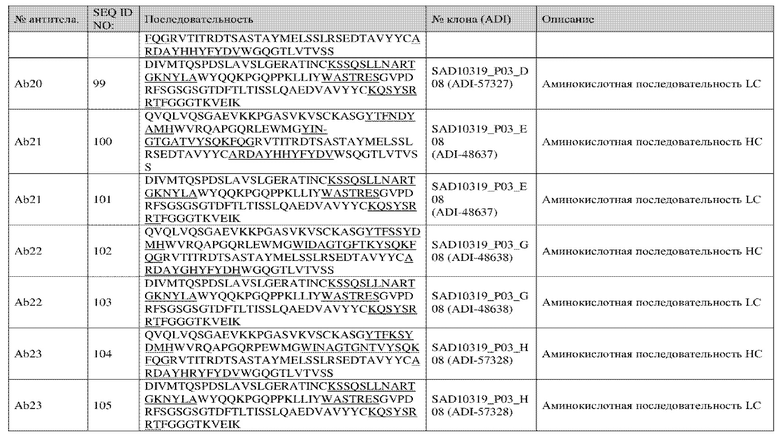
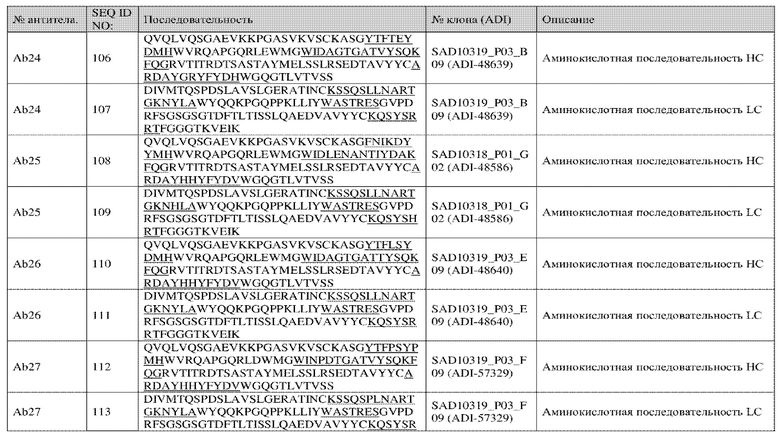
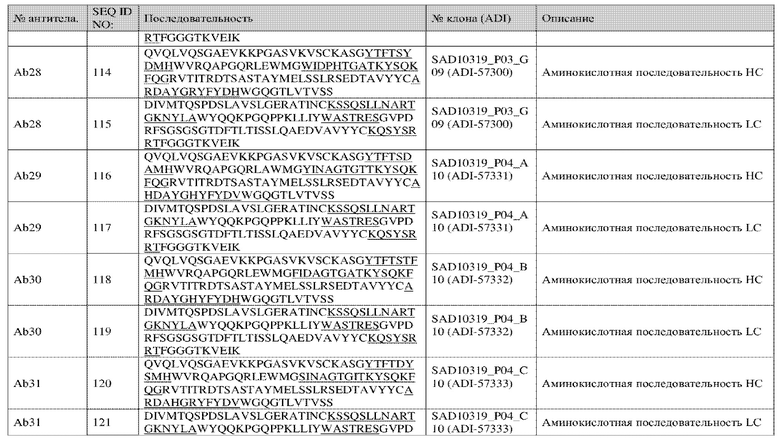
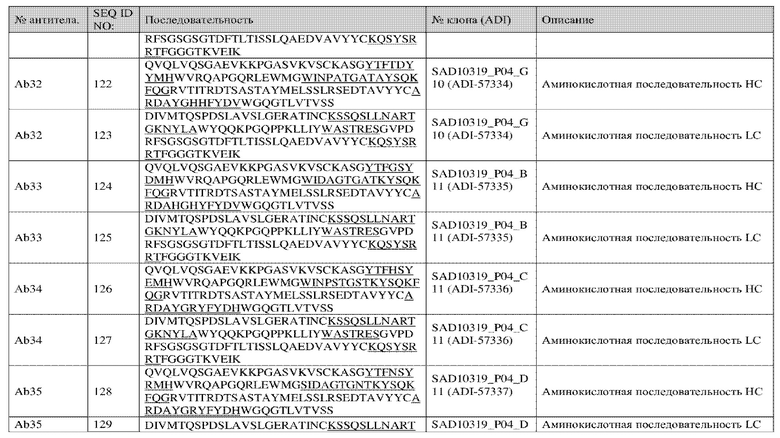
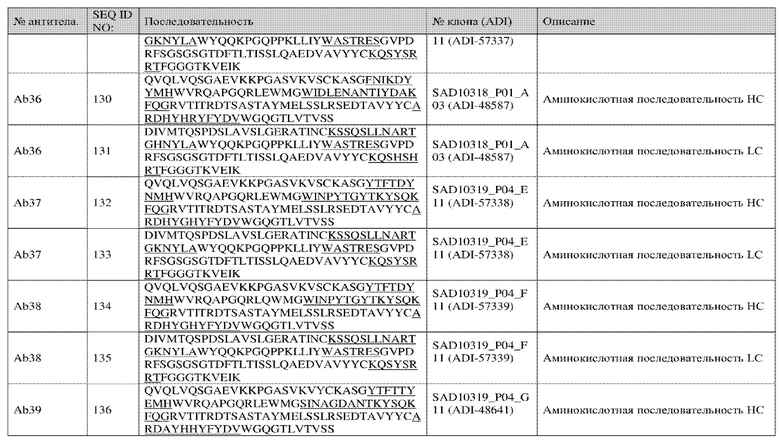
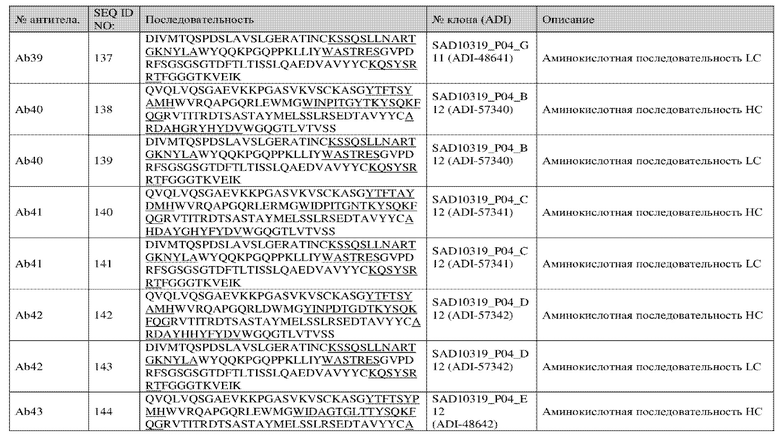
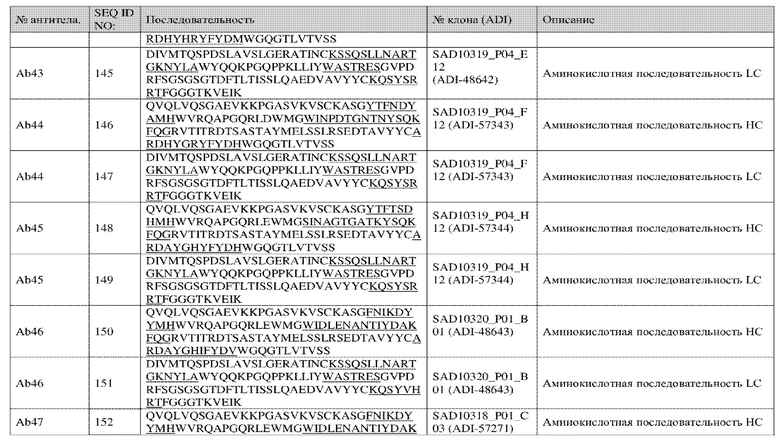
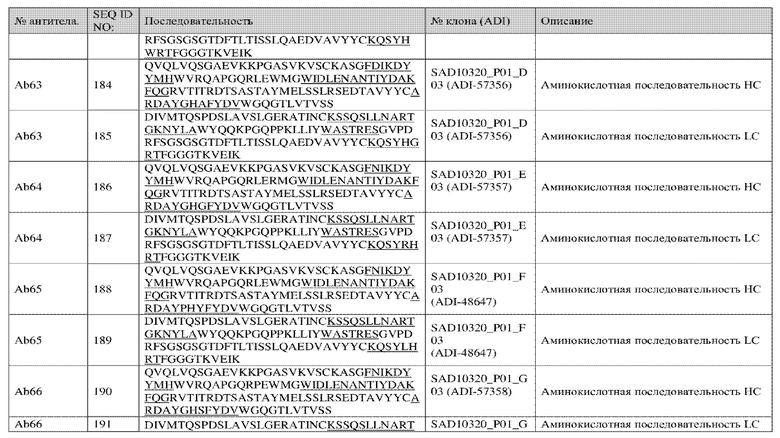
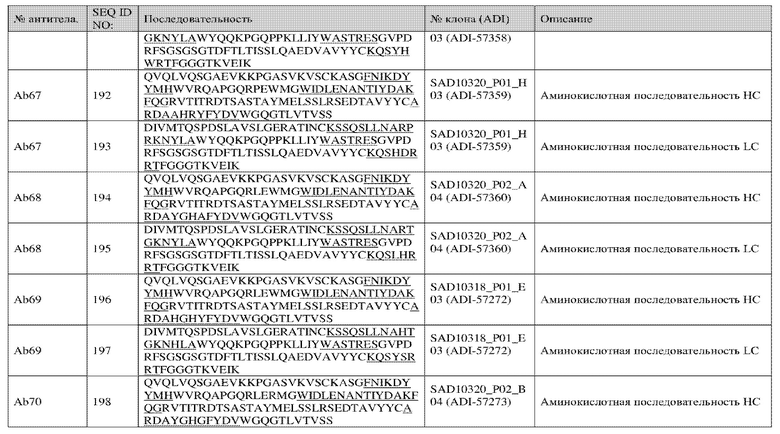
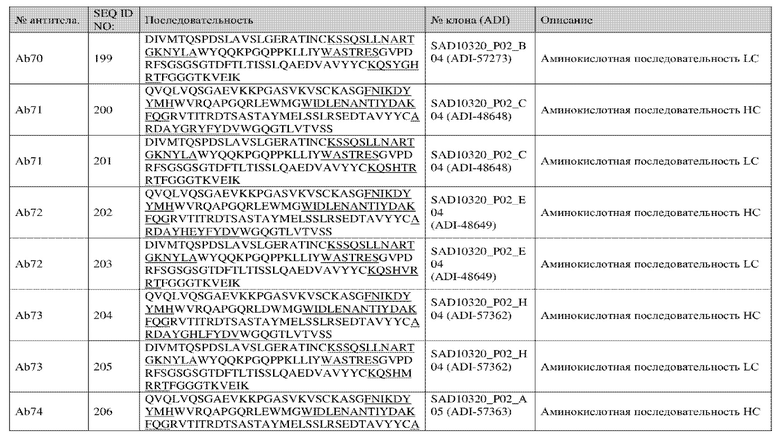
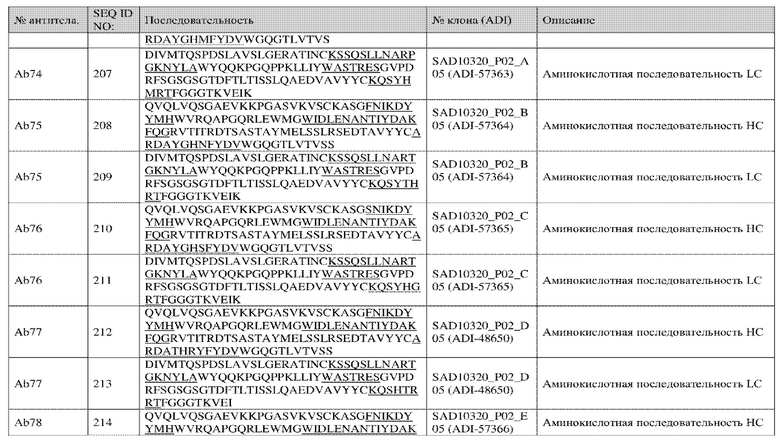
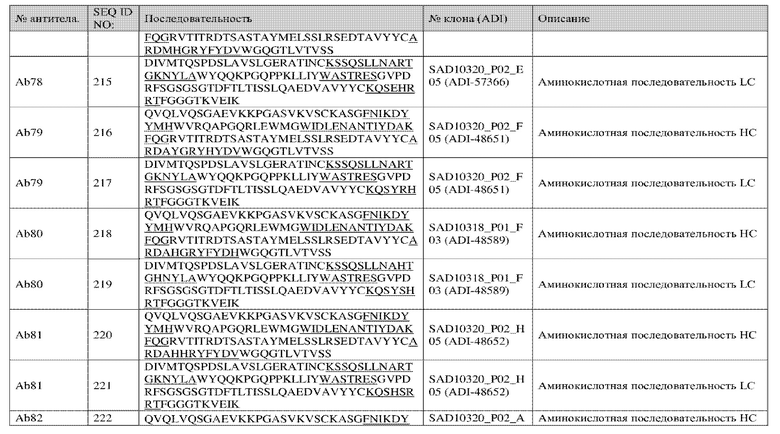
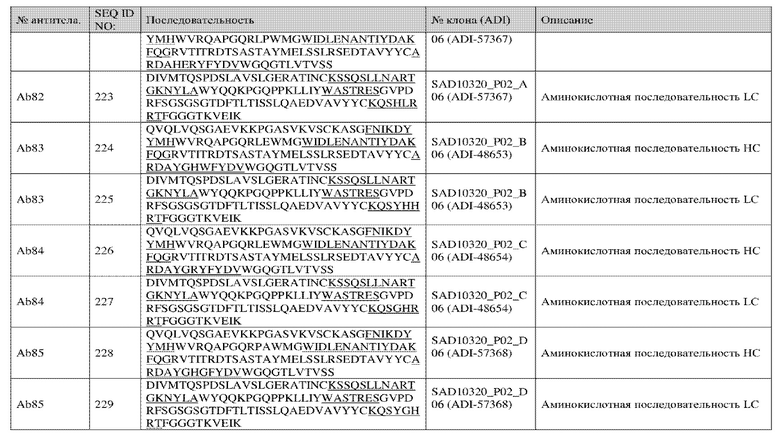
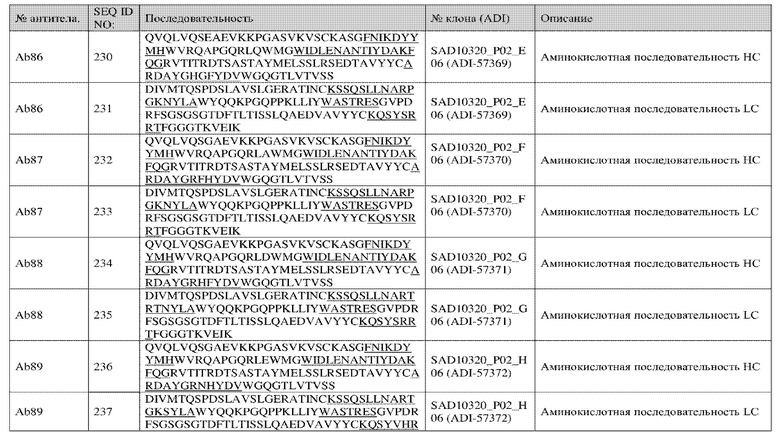
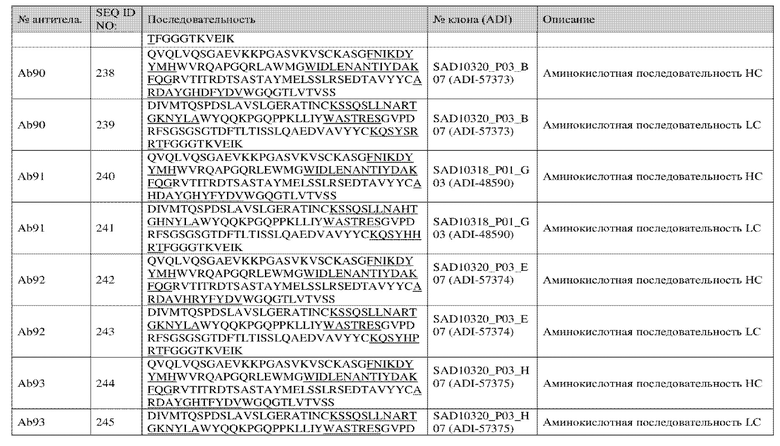
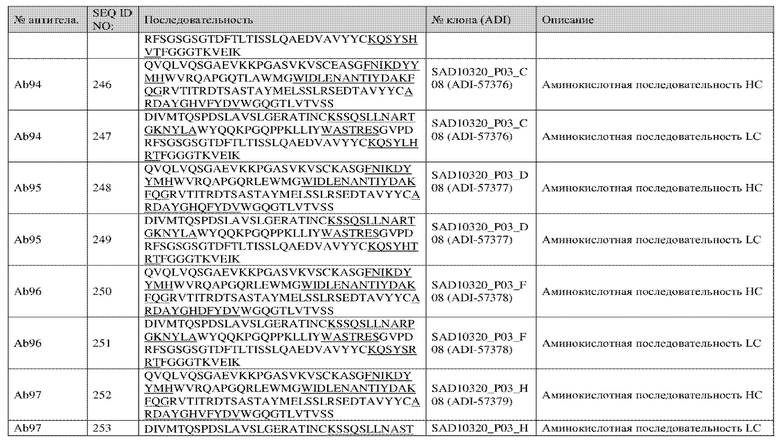
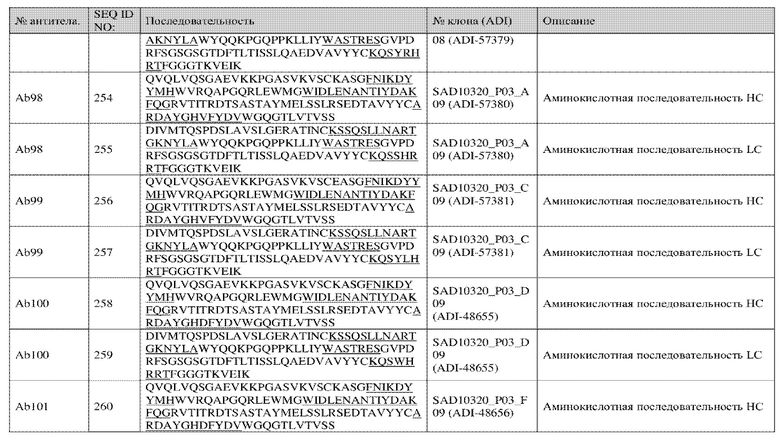
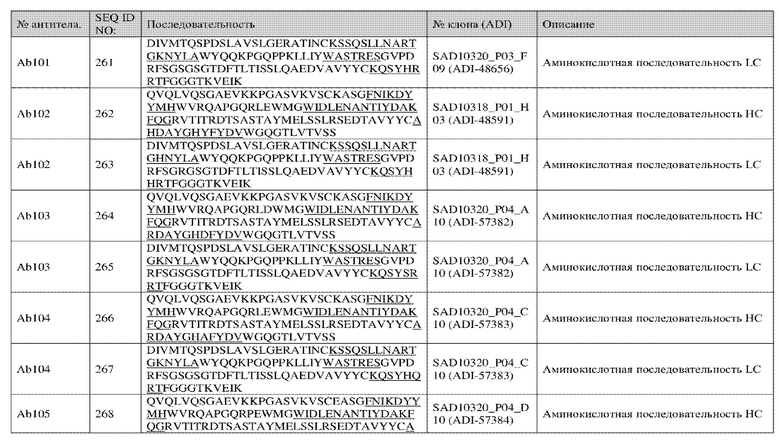
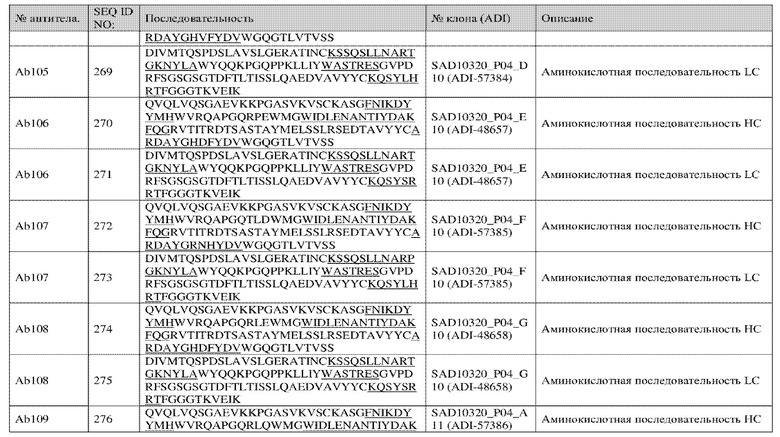
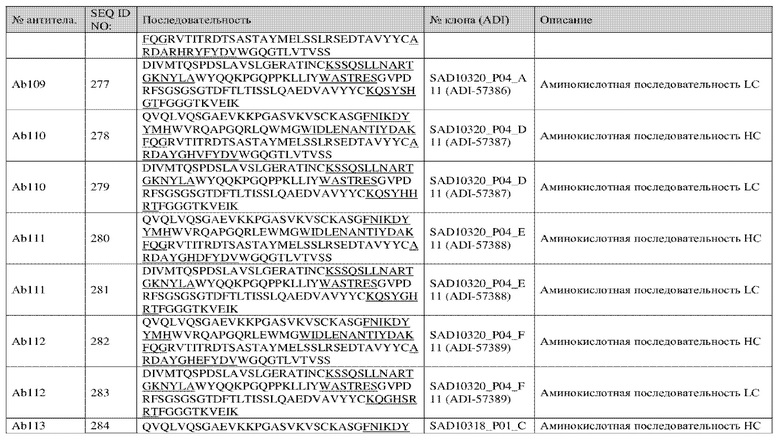
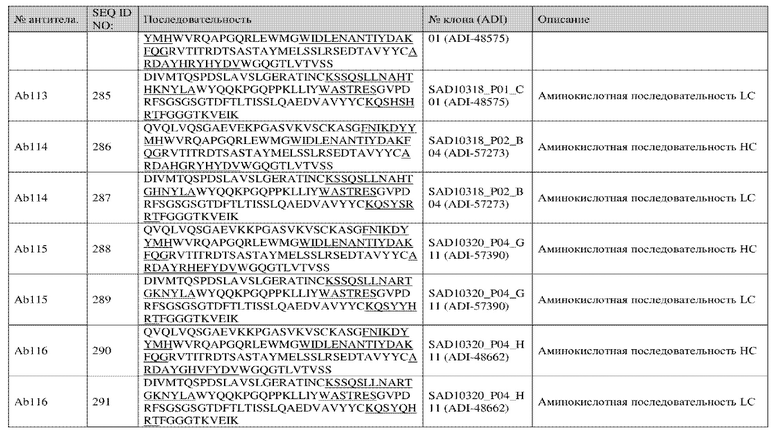
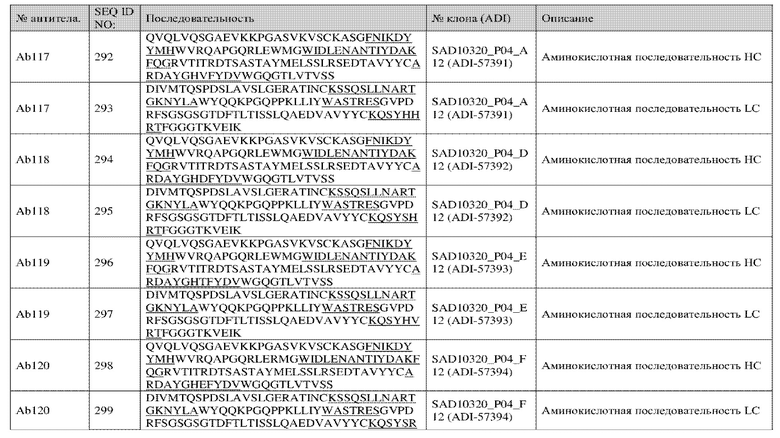
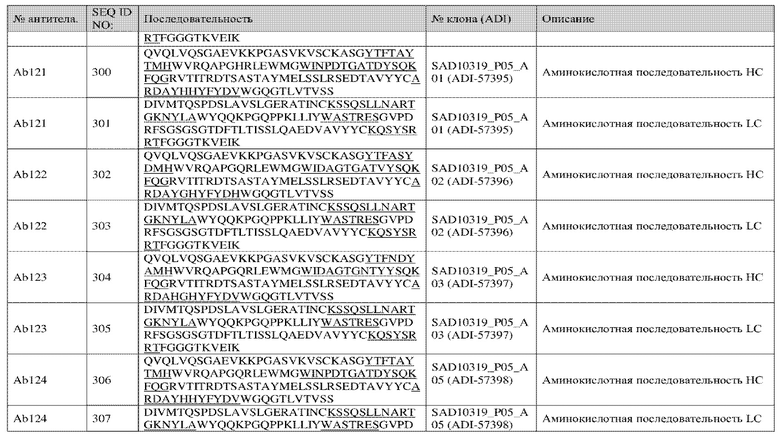
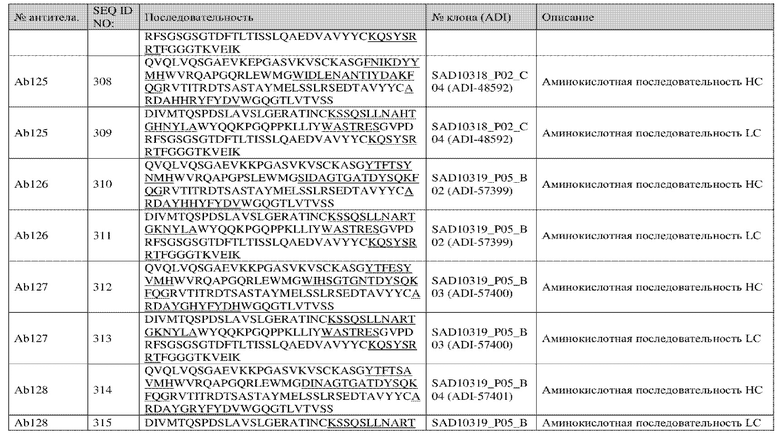
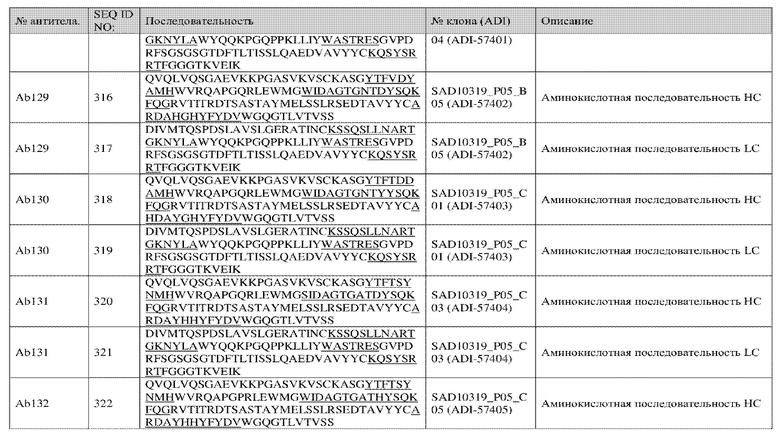
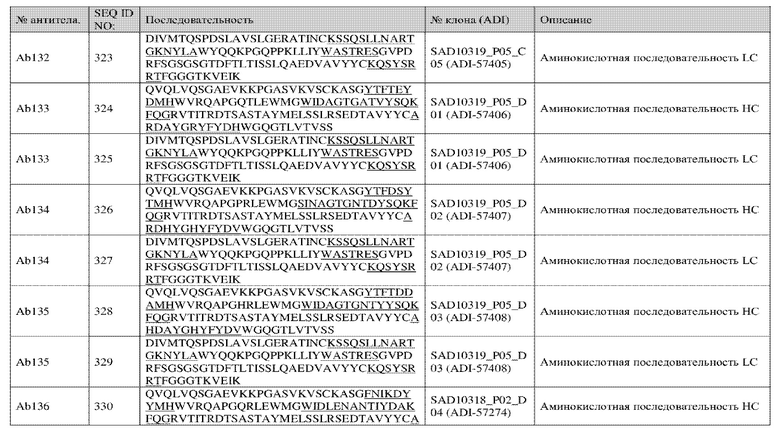
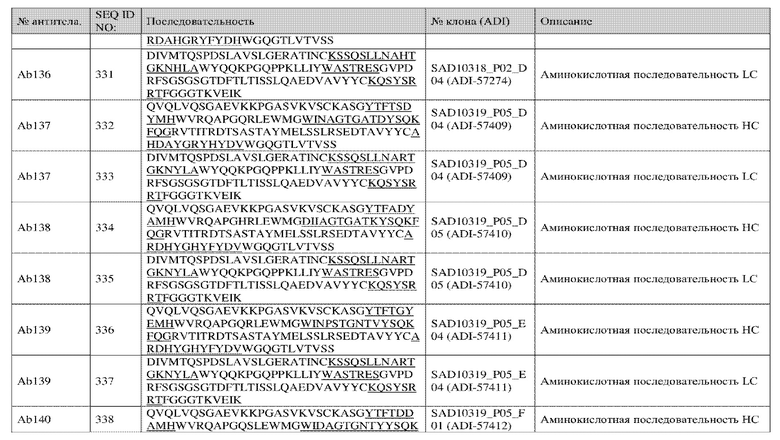
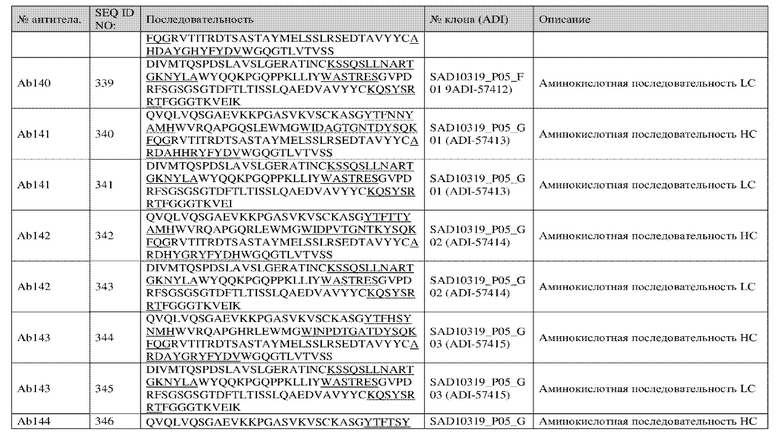
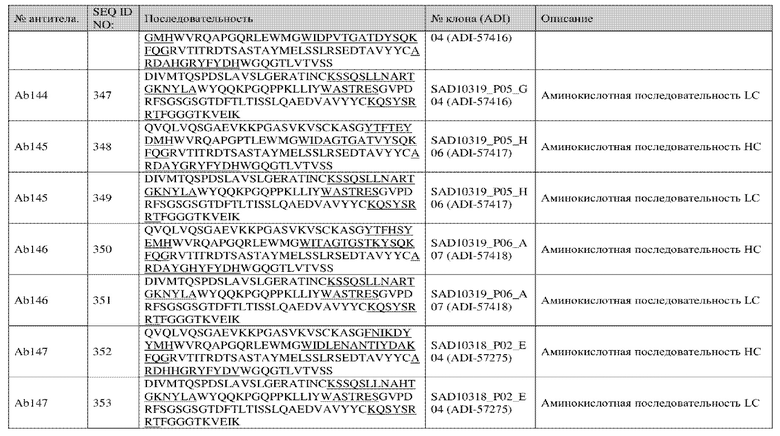
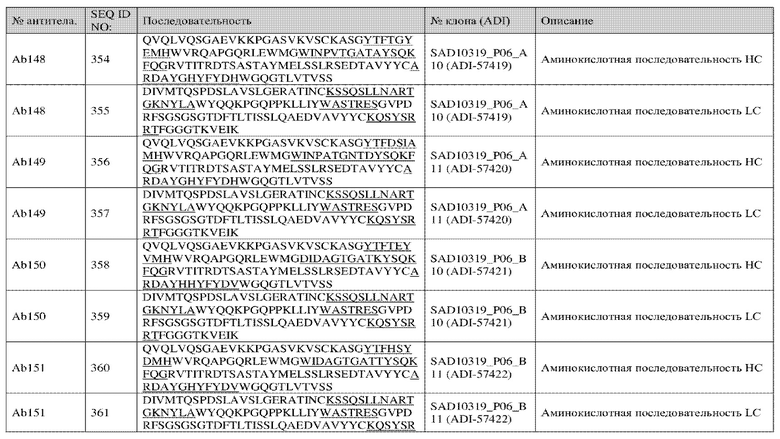
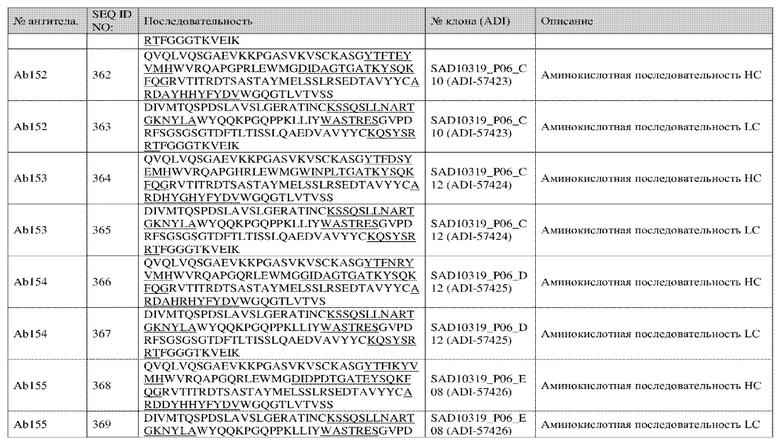
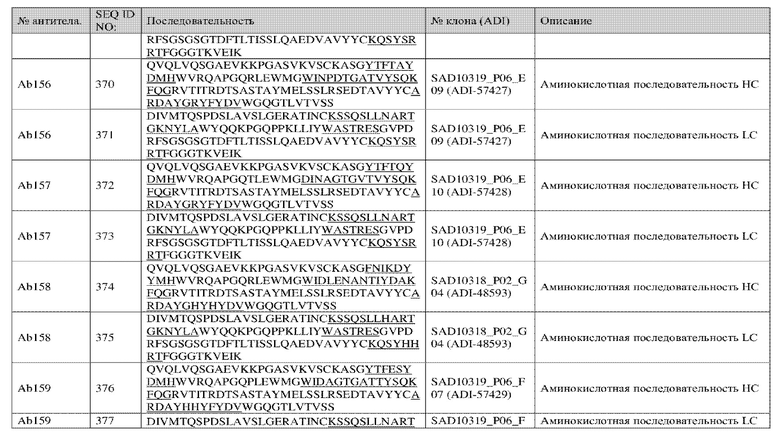
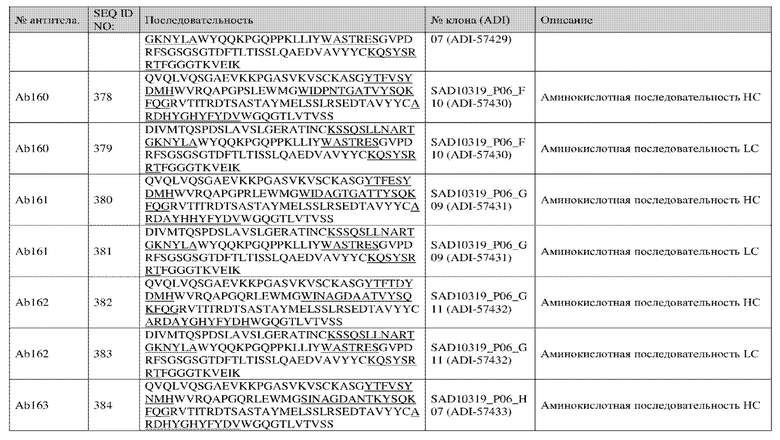
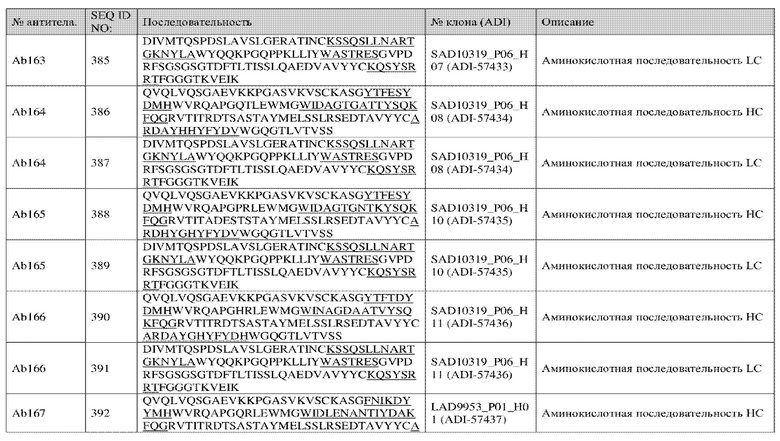
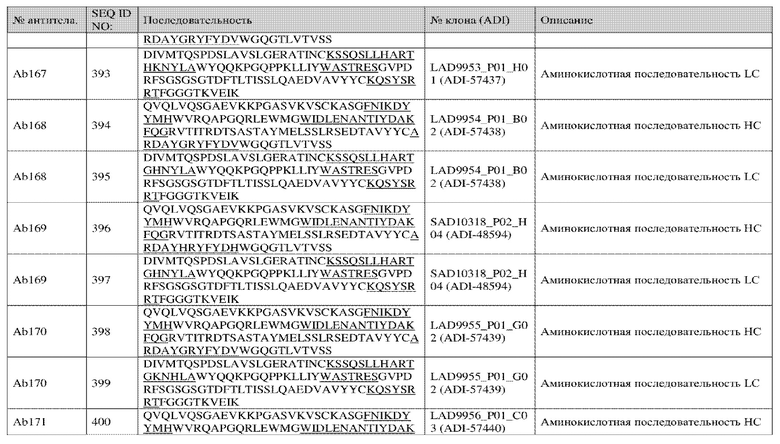
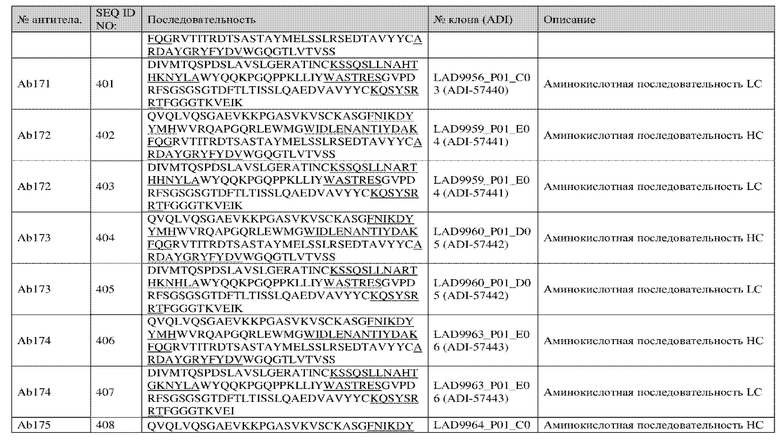
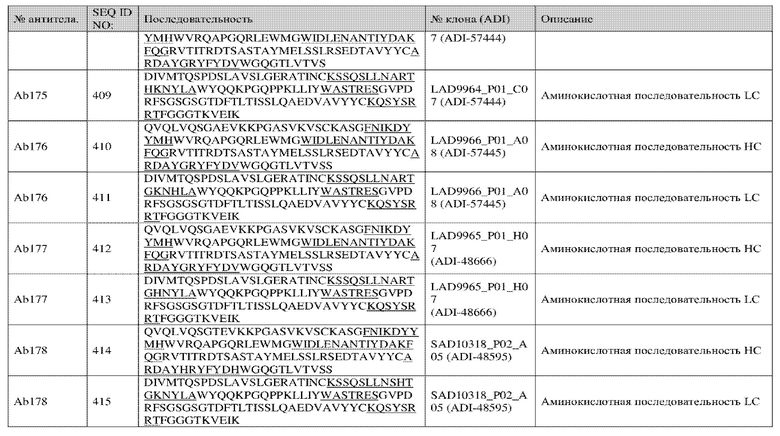
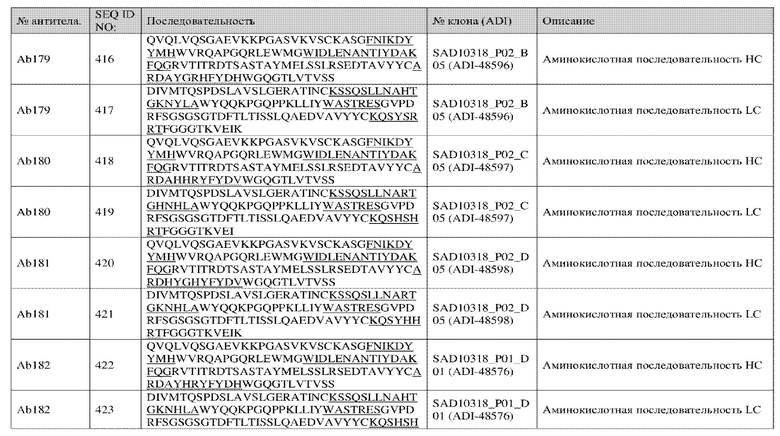
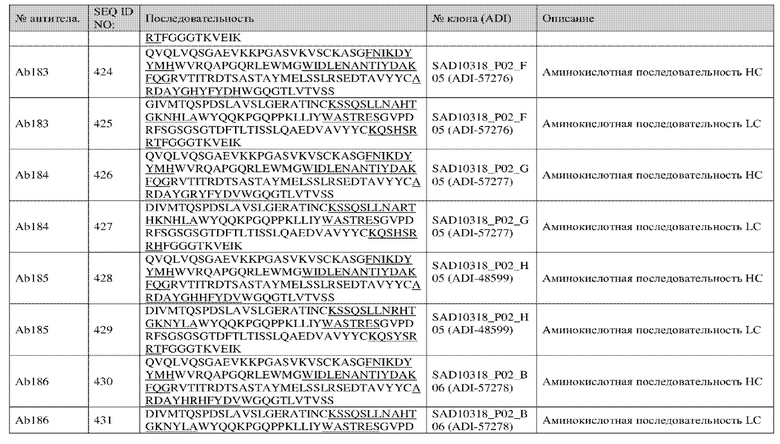
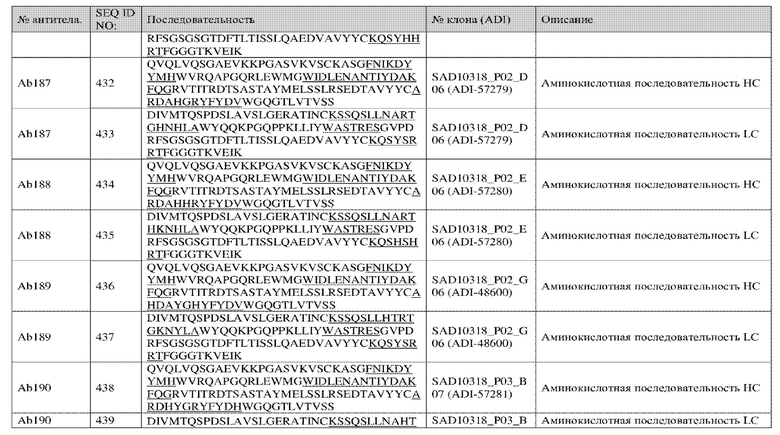
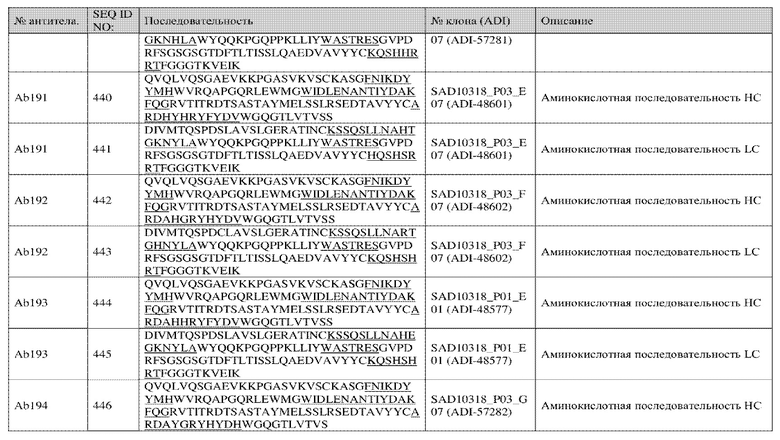
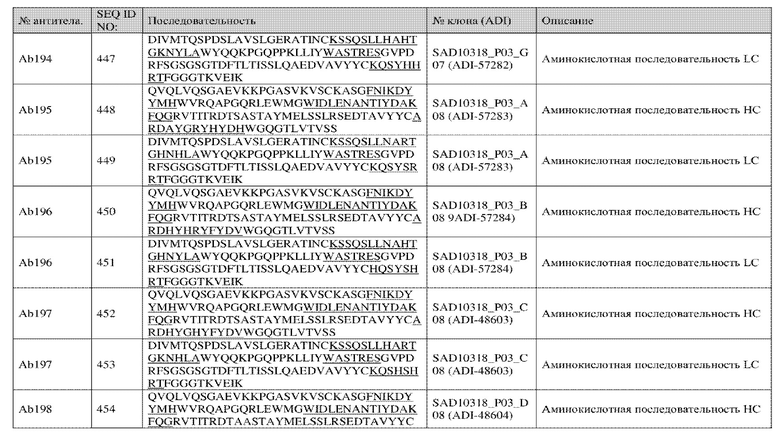
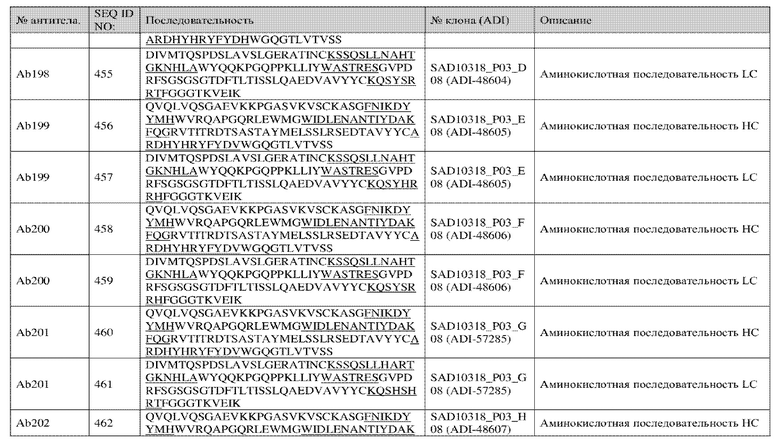
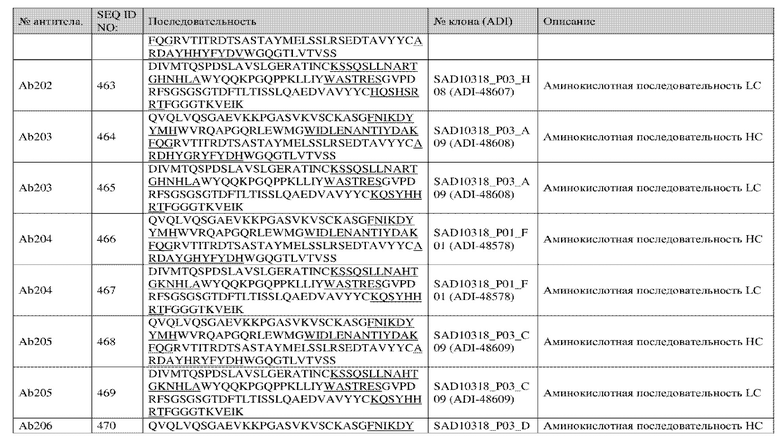
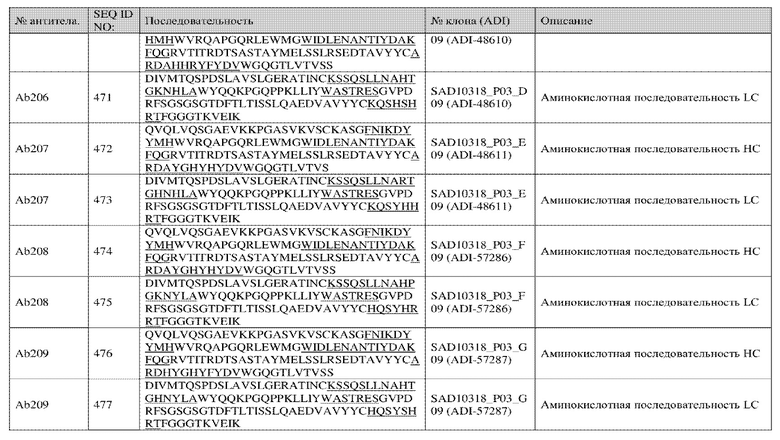
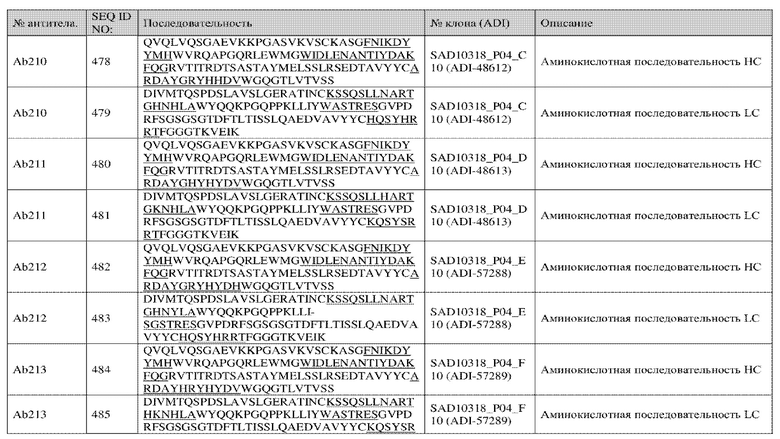
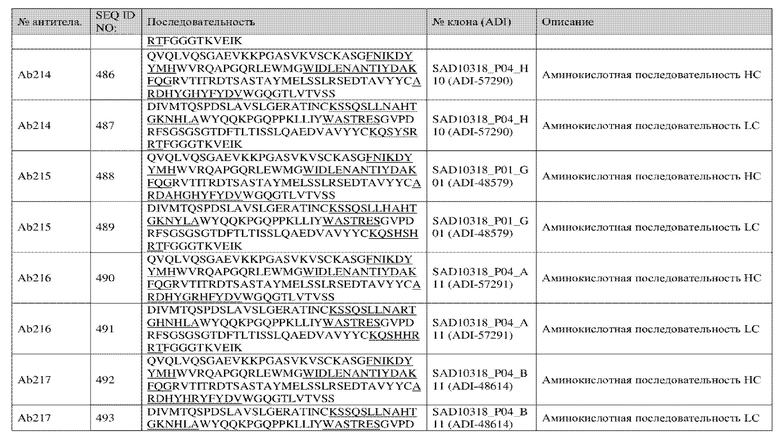
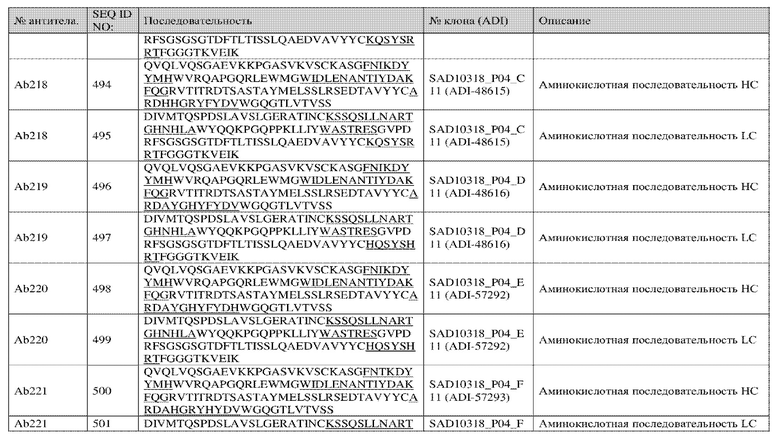
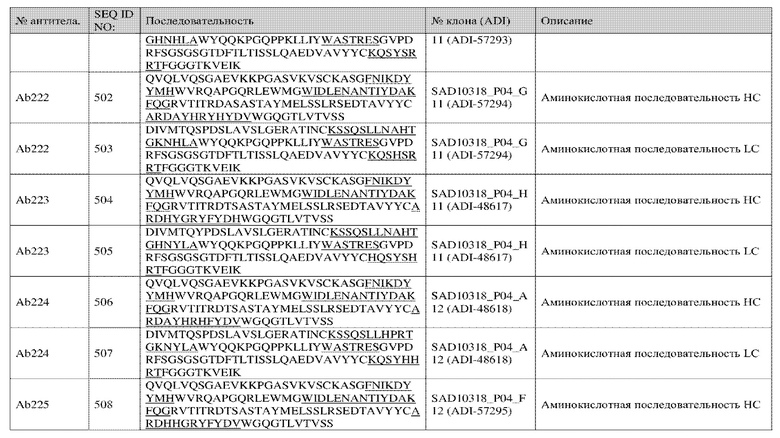
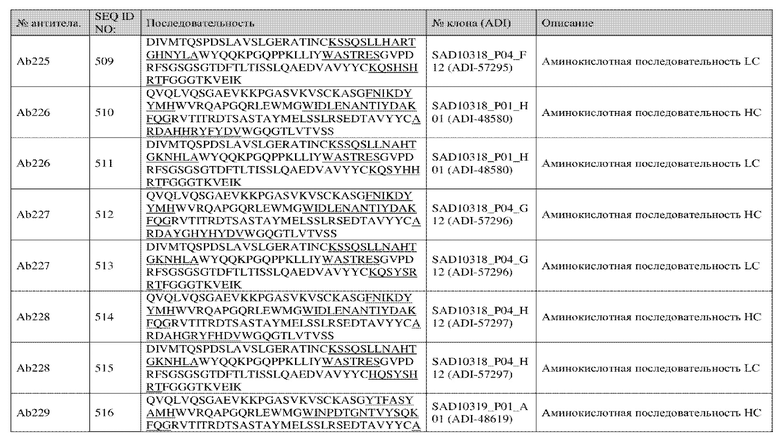
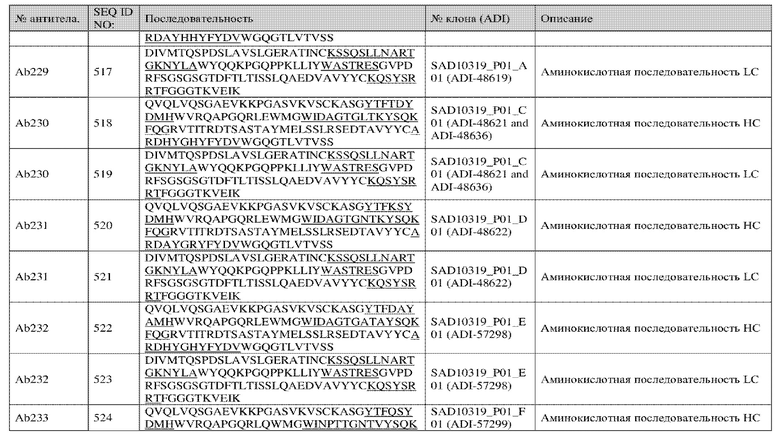
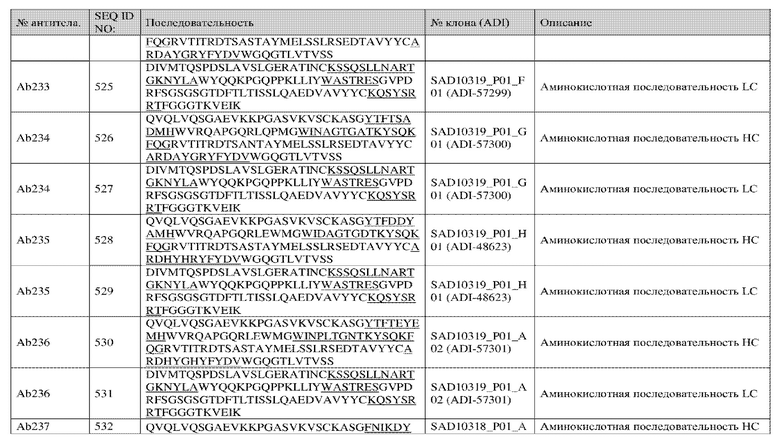
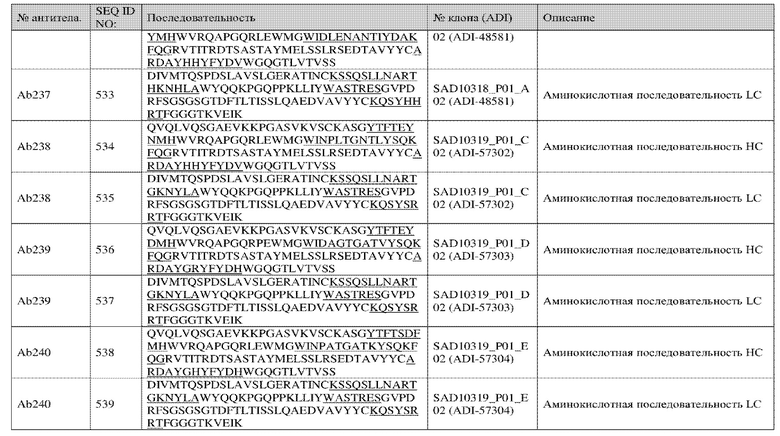
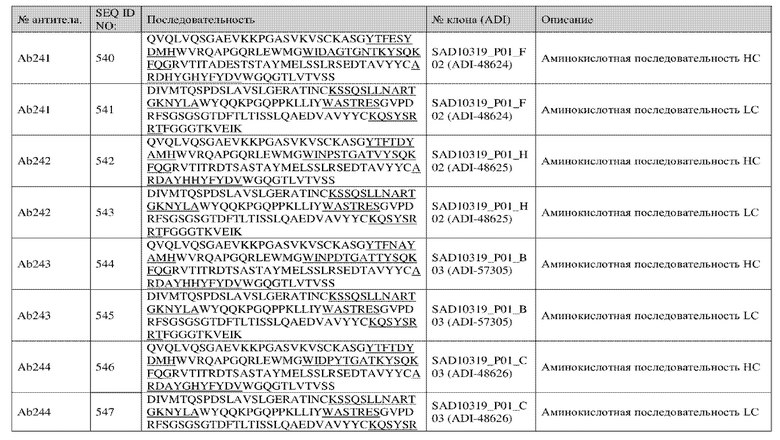
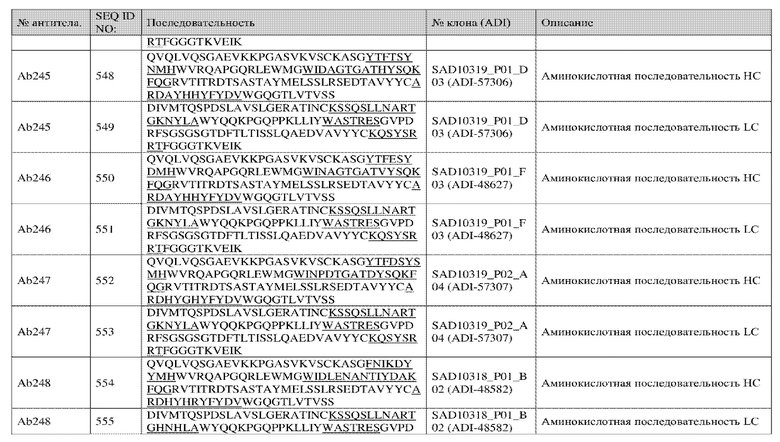
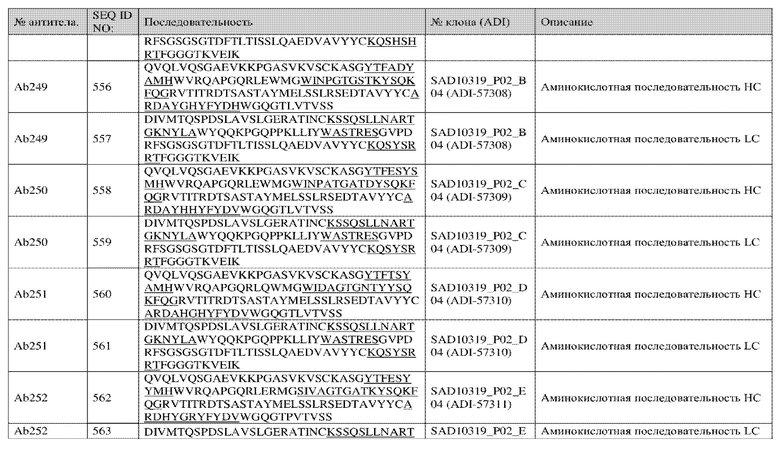
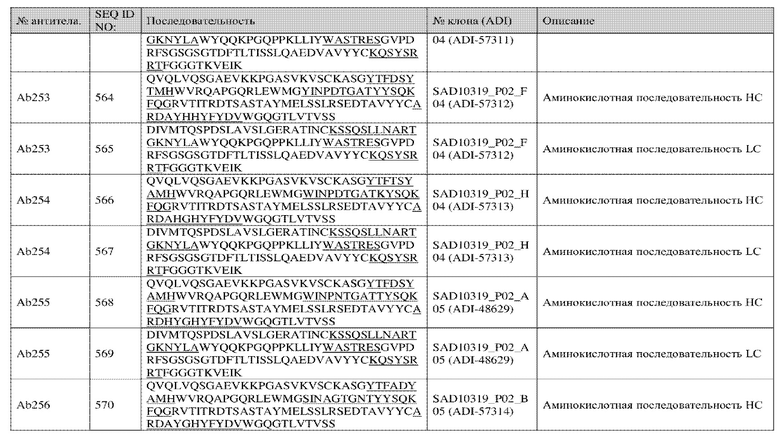

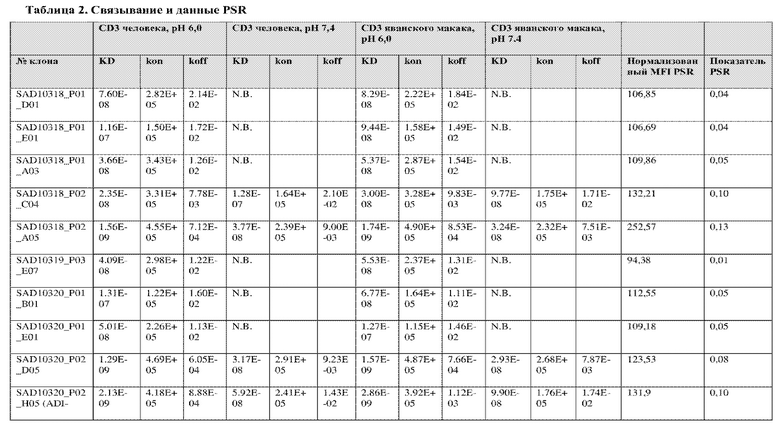
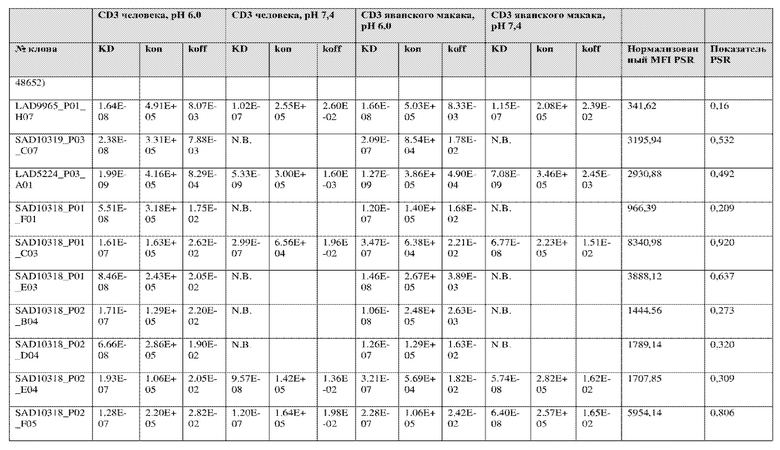
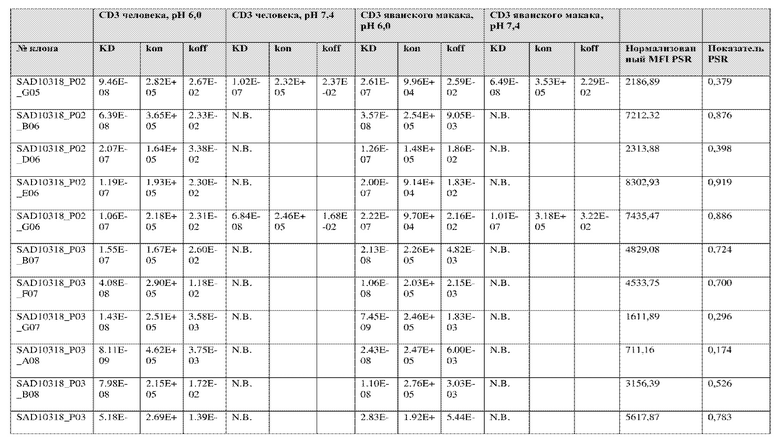
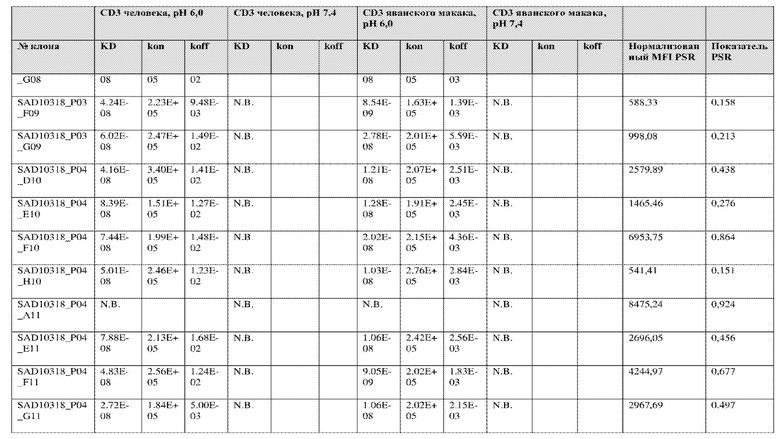
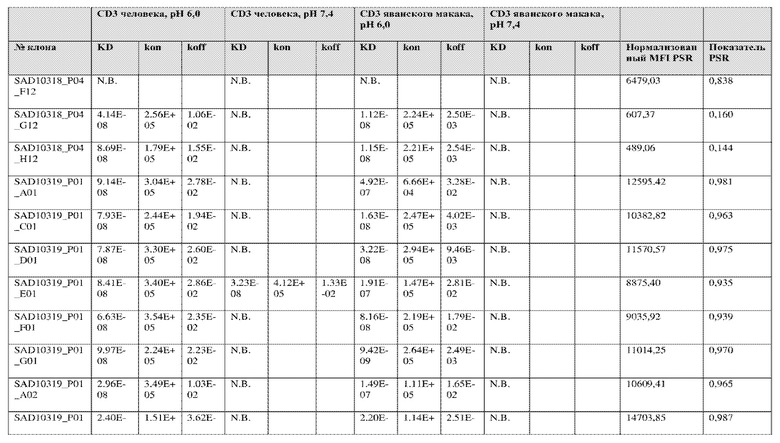
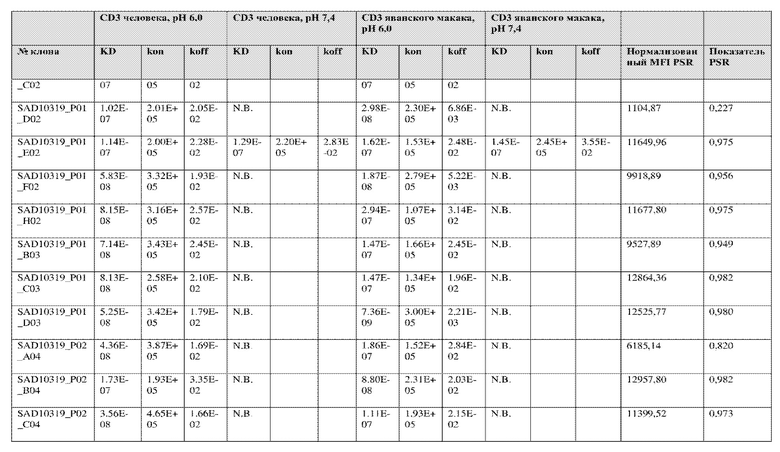
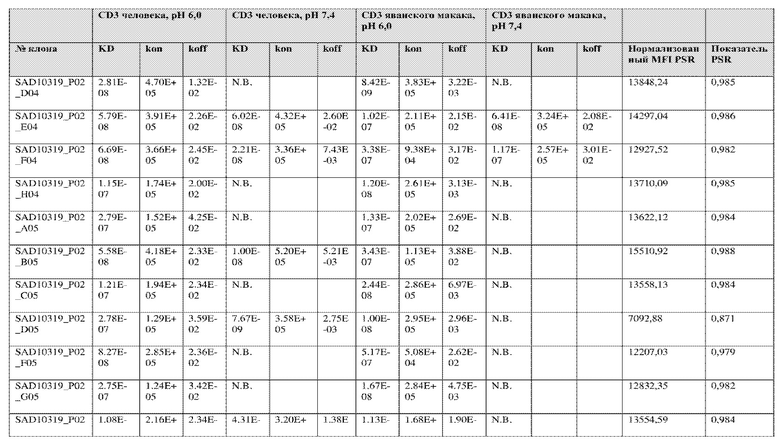
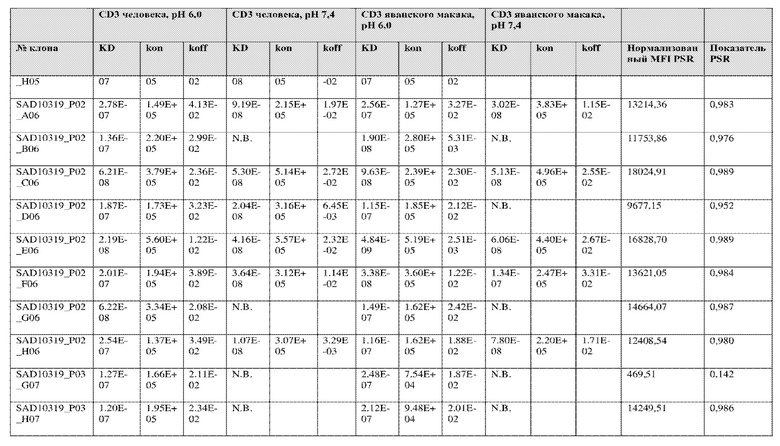
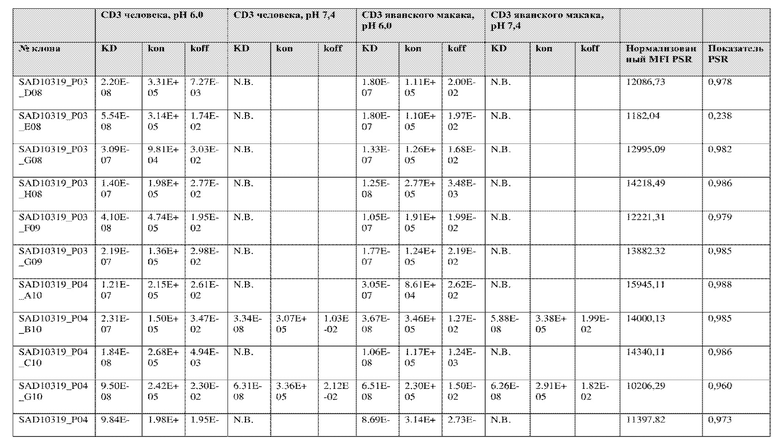
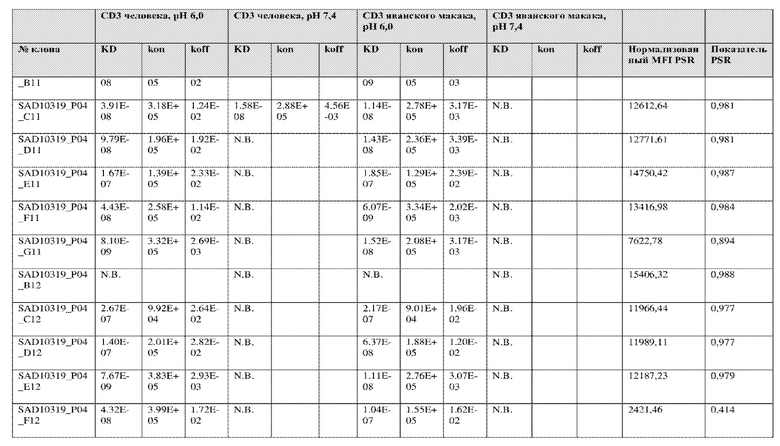
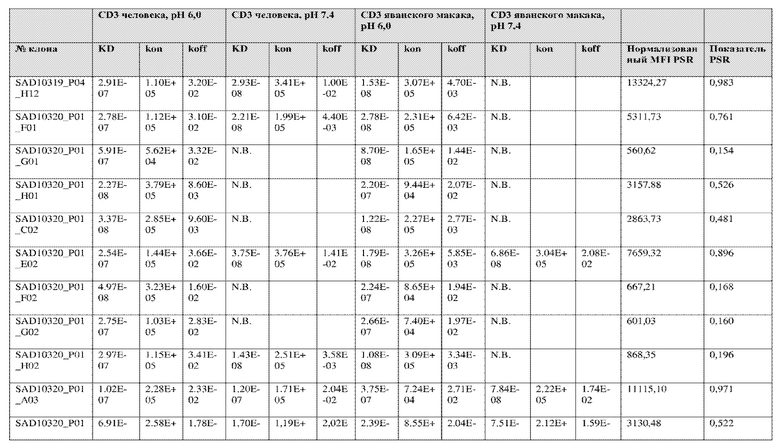
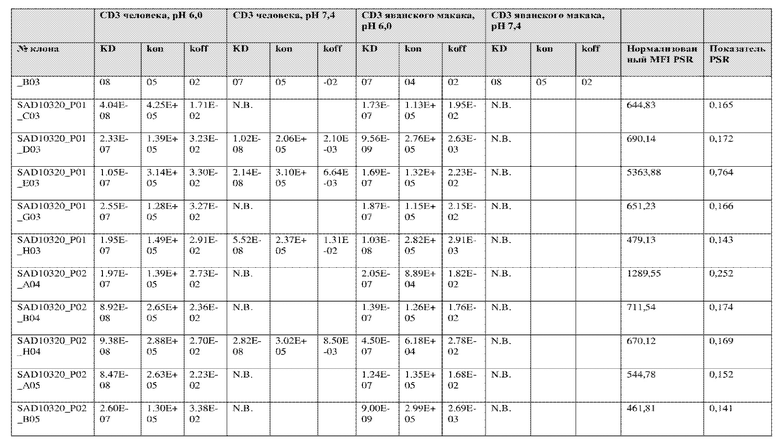
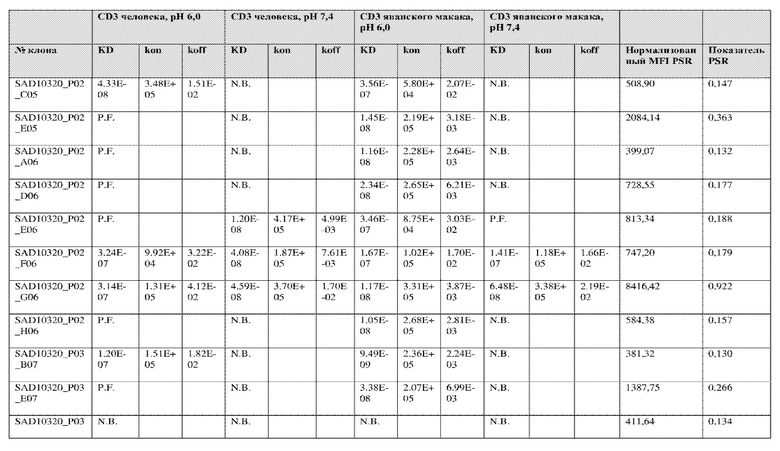
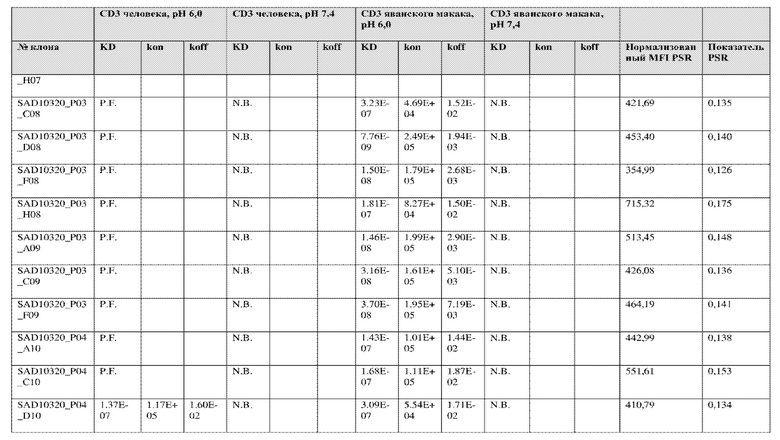
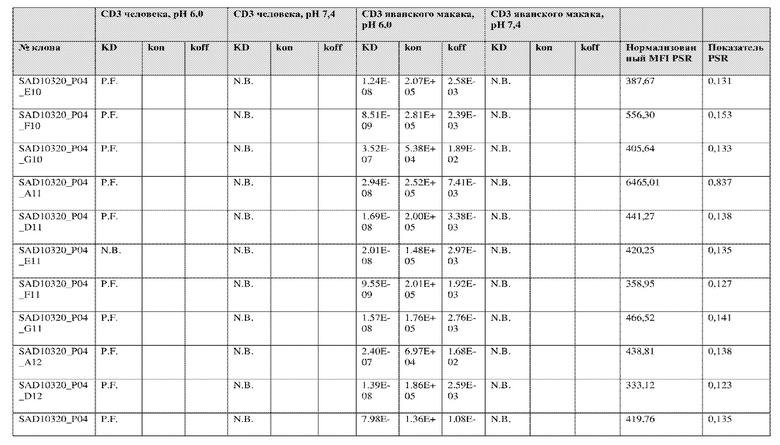
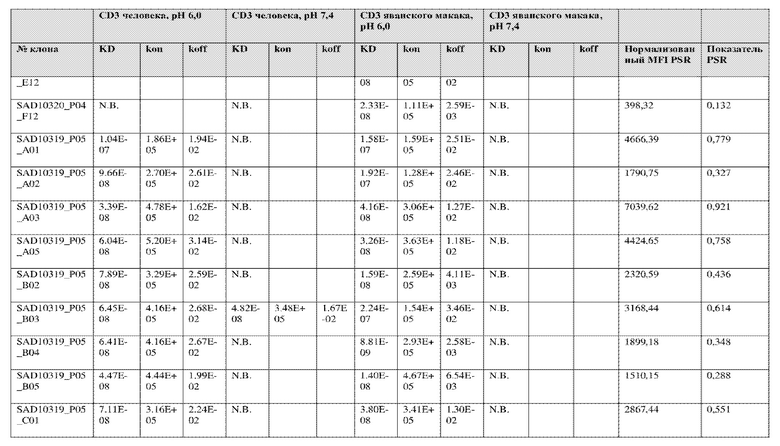
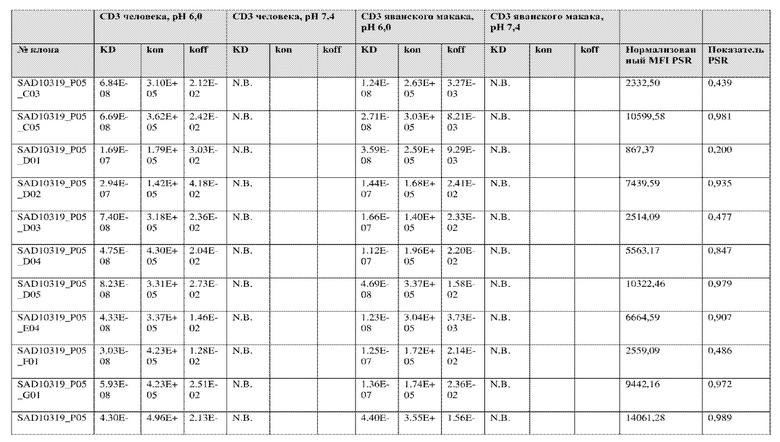
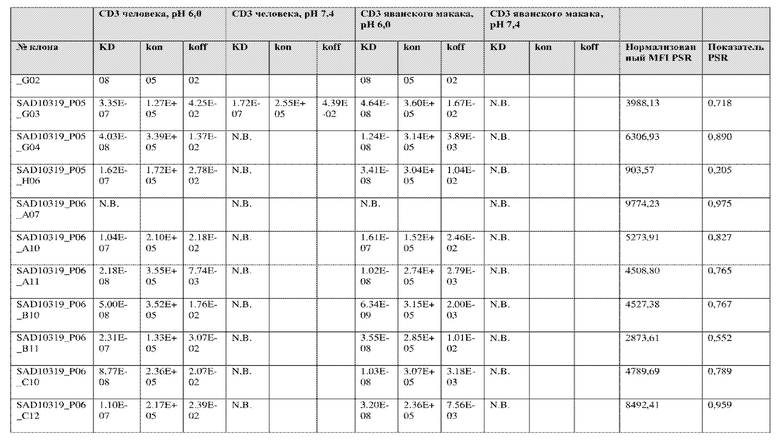
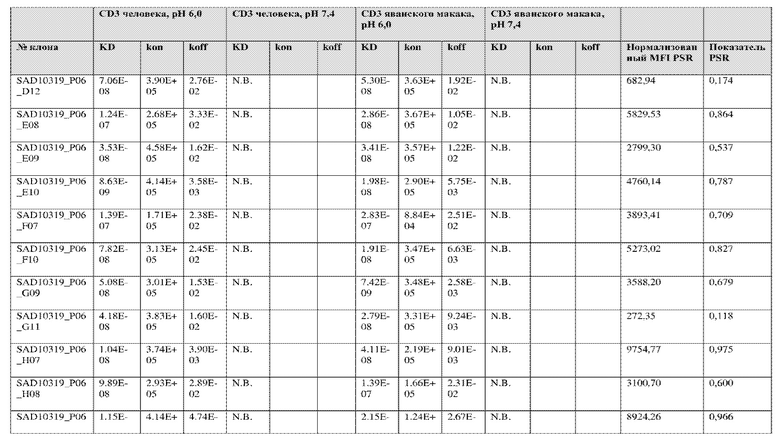
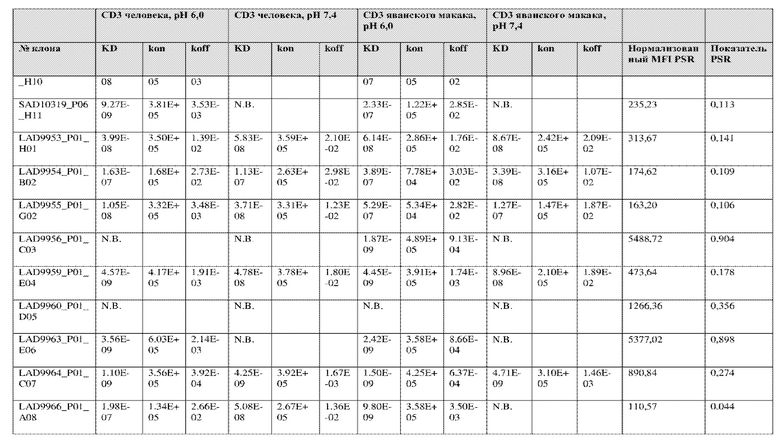
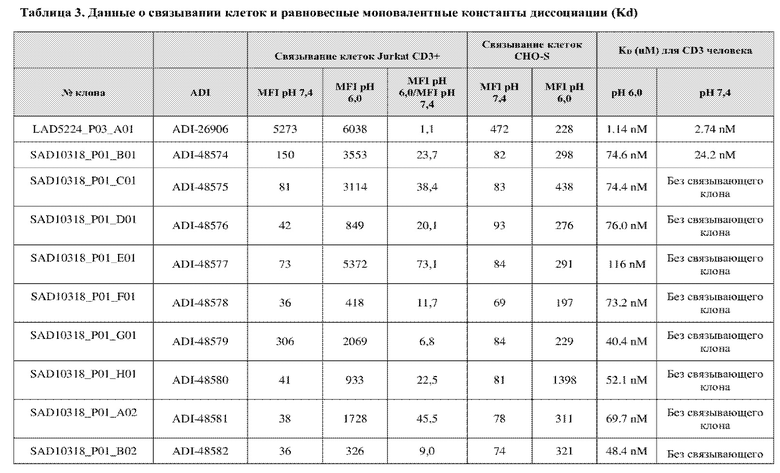
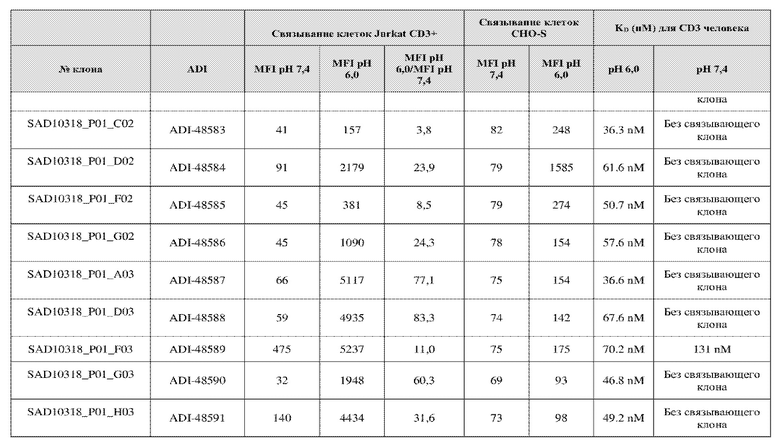
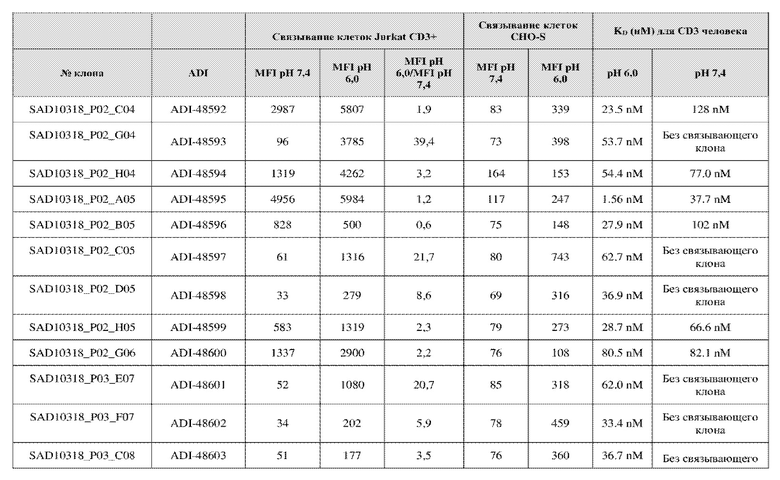
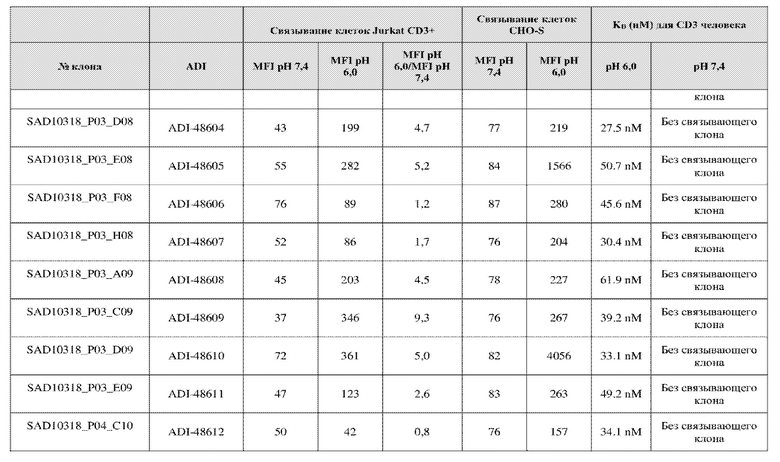
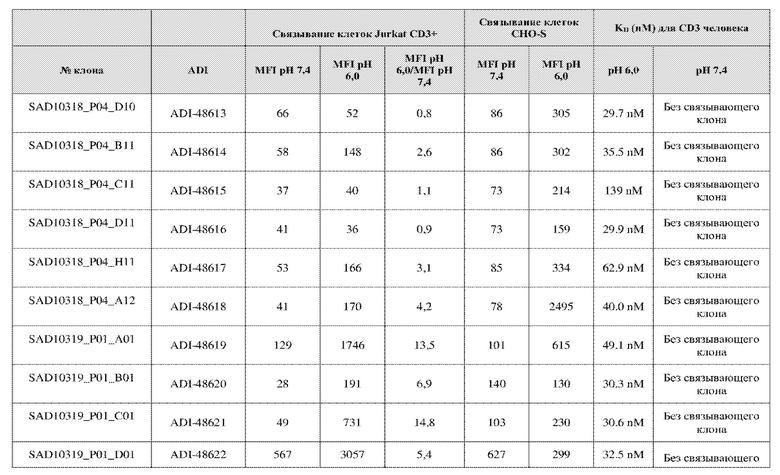
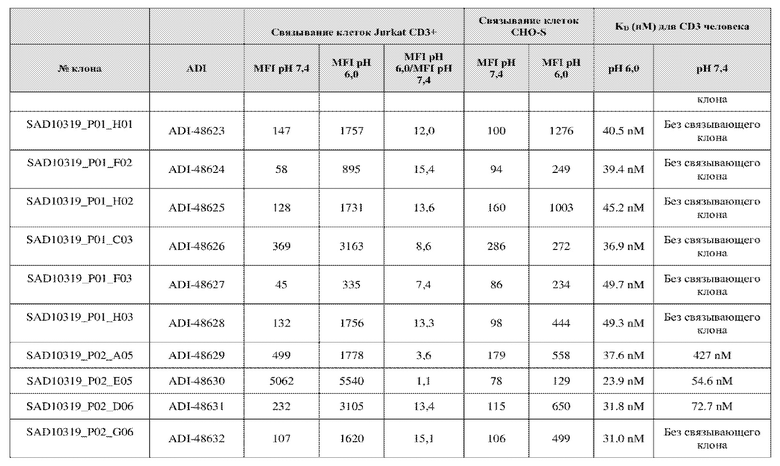
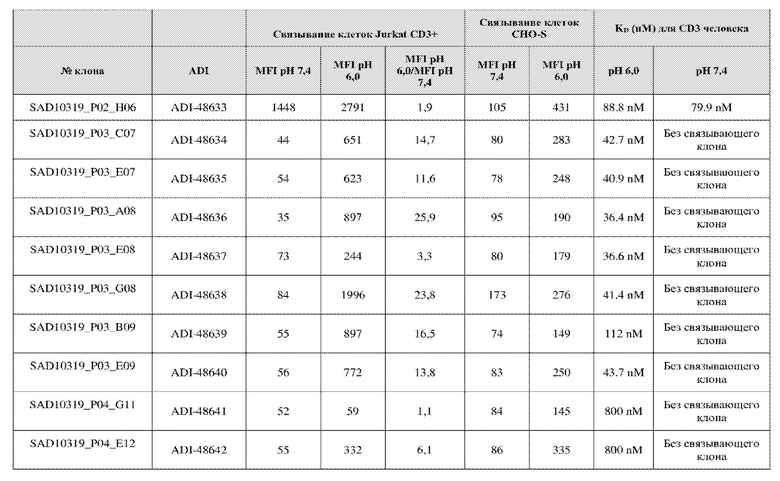
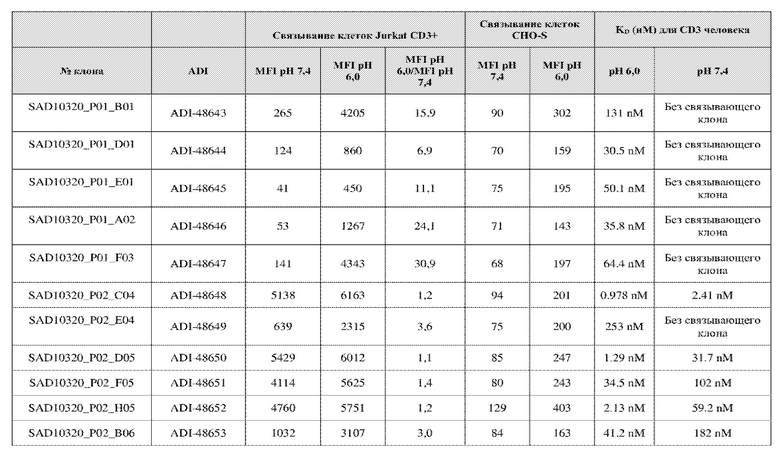
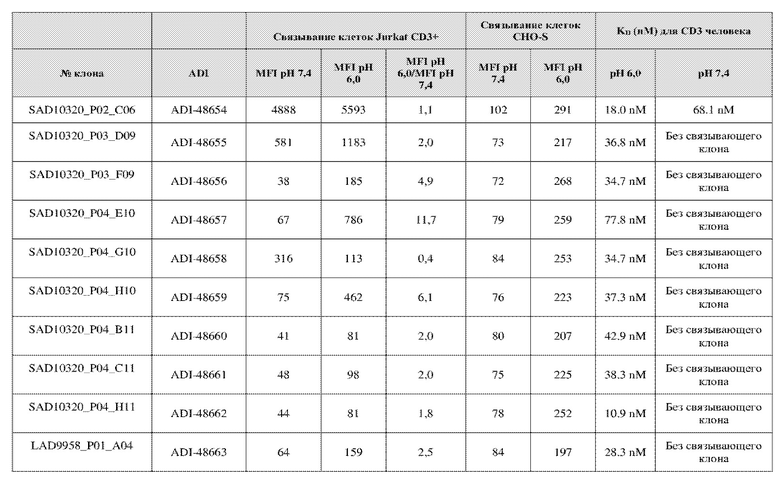
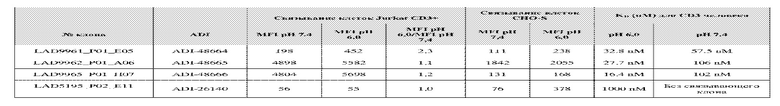
Таблица 4. Последовательности CD3ε человека и яванского макака
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> АДИМАБ, ЛЛК
<120> СКОНСТРУИРОВАННЫЕ PH-ЗАВИСИМЫЕ АНТИТЕЛА К CD3, А ТАКЖЕ СПОСОБЫ
ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ
<130> 1160430.002000
<150> 62/858,968
<151> 2019-06-07
<160> 598
<170> PatentIn версии 3.5
<210> 1
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (2)..(2)
<223> R или H
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> A или H
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> G, H или P
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> Y, H, D, V, E, S, N, L, M, I, G, A, Q или T
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 1
Ala Xaa Asp Xaa Tyr Xaa His Xaa Phe Tyr Asp Val
1 5 10
<210> 2
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> A или H
<220>
<221> Модифицированный остаток
<222> (7)..(7)
<223> R или H
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> H или Y
<220>
<221> Модифицированный остаток
<222> (9)..(9)
<223> F или H
<220>
<221> Модифицированный остаток
<222> (12)..(12)
<223> H или V
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 2
Ala Arg Asp Xaa Tyr Gly Xaa Xaa Xaa Tyr Asp Xaa
1 5 10
<210> 3
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> G, E или R
<220>
<221> Модифицированный остаток
<222> (7)..(7)
<223> R или H
<220>
<221> Модифицированный остаток
<222> (9)..(9)
<223> F или H
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> Y или H
<220>
<221> Модифицированный остаток
<222> (12)..(12)
<223> V или H
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 3
Ala Arg Asp Ala His Xaa Xaa Tyr Xaa Xaa Asp Xaa
1 5 10
<210> 4
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> H, Y, S, G, A, T, V или R
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> Y или H
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 4
Ala Arg Asp Ala Xaa His Arg Xaa Phe Tyr Asp Val
1 5 10
<210> 5
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> H или A
<220>
<221> Модифицированный остаток
<222> (12)..(12)
<223> H, V или M
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 5
Ala Arg Asp Xaa Tyr His Arg Tyr Phe Tyr Asp Xaa
1 5 10
<210> 6
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (2)..(2)
<223> R или H
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> G или H
<220>
<221> Модифицированный остаток
<222> (7)..(7)
<223> H или R
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> N, F или Y
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> Y или H
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 6
Ala Xaa Asp Ala Tyr Xaa Xaa Xaa His Xaa Asp Val
1 5 10
<210> 7
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> M, Q или H
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> R или H
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 7
Ala Arg Asp Xaa Xaa Gly Arg Tyr Phe Tyr Asp Val
1 5 10
<210> 8
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> H или A
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> T, Y или H
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> G или H
<220>
<221> Модифицированный остаток
<222> (12)..(12)
<223> V или H
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 8
Ala Arg Asp Xaa Xaa Xaa Arg Tyr Phe Tyr Asp Xaa
1 5 10
<210> 9
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 9
Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe Gln
1 5 10 15
Gly
<210> 10
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (1)..(1)
<223> W или Y
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> A, S, D, G, N, L, V, H или Q
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> A, T или S
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> K, V, T, D, Y, F или A
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 10
Xaa Ile Asn Pro Xaa Thr Gly Xaa Thr Xaa Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 11
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (1)..(1)
<223> W, Y или F
<220>
<221> Модифицированный остаток
<222> (3)..(3)
<223> T, N или D
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> A, T или L
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> A, K, V, H, T или N
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 11
Xaa Ile Xaa Ala Gly Thr Gly Xaa Thr Xaa Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 12
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (1)..(1)
<223> S или W
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> L, N, D или F
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> D, Y или K
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 12
Xaa Ile Asp Ala Gly Thr Gly Xaa Thr Xaa Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 13
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (1)..(1)
<223> G, D или S
<220>
<221> Модифицированный остаток
<222> (3)..(3)
<223> I или D
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> K или D
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 13
Xaa Ile Xaa Ala Gly Thr Gly Ala Thr Xaa Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 14
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> D, T, L, S или A
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> D, V, L или N
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 14
Trp Ile Asn Pro Xaa Thr Gly Asn Thr Xaa Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 15
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (1)..(1)
<223> Y или W
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> N, D или A
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> I или V
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 15
Xaa Ile Asn Ala Gly Thr Gly Xaa Thr Xaa Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 16
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (1)..(1)
<223> W или Y
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> D, I или Y
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> D, Y или E
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 16
Xaa Ile Asn Pro Xaa Thr Gly Xaa Thr Lys Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 17
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (3)..(3)
<223> N или V
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> A или I
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 17
Ser Ile Xaa Ala Gly Thr Gly Xaa Thr Lys Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 18
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> F или N
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> Y или D
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 18
Ser Ile Asn Ala Gly Thr Gly Xaa Thr Xaa Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 19
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (1)..(1)
<223> D или W
<220>
<221> Модифицированный остаток
<222> (3)..(3)
<223> N или H
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> A или S
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> A или N
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 19
Xaa Ile Xaa Xaa Gly Thr Gly Xaa Thr Asp Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 20
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> N, H или Y
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> V или K
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 20
Trp Ile Asp Pro Xaa Thr Gly Ala Thr Xaa Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 21
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (3)..(3)
<223> D или N
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> L, I или V
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 21
Trp Ile Xaa Pro Xaa Thr Gly Asn Thr Lys Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 22
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 22
Ser Ile Asn Ala Gly Asp Ala Asn Thr Lys Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 23
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (1)..(1)
<223> D или W
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> D или V
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> E или D
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 23
Xaa Ile Asp Pro Xaa Thr Gly Ala Thr Xaa Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 24
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 24
Trp Ile Asn Ala Gly Asp Ala Ala Thr Val Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 25
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 25
Phe Asn Ile Lys Asp Tyr His Met His
1 5
<210> 26
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 26
Ser Asn Ile Lys Asp Tyr Tyr Met His
1 5
<210> 27
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 27
Ser Asn Ile Lys Asp Tyr His Met His
1 5
<210> 28
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> A, K, D, Q, E, N, T, L, Y, S, P, G, H или V
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> T, S или A
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> Y или I
<220>
<221> Модифицированный остаток
<222> (7)..(7)
<223> A, D, N, S, Y, T, I, V, L, E, P, R или G
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 28
Tyr Thr Phe Xaa Xaa Xaa Xaa Met His
1 5
<210> 29
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> T, D, A, N или V
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> D, E, G или Q
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> Y или D
<220>
<221> Модифицированный остаток
<222> (7)..(7)
<223> D, A, E, N, S, Y или V
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 29
Tyr Thr Phe Xaa Xaa Xaa Xaa Met His
1 5
<210> 30
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> A, D или T
<220>
<221> Модифицированный остаток
<222> (7)..(7)
<223> D, F, A, M, V или Y
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 30
Tyr Thr Phe Thr Ser Xaa Xaa Met His
1 5
<210> 31
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> Xaa может представлять собой Glu, Ser, Thr или Asn (E, S, T или N)
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> Xaa может представлять собой Ser, Asp, Gln или Asn (S, D, Q или N)
<220>
<221> Модифицированный остаток
<222> (7)..(7)
<223> Xaa может представлять собой Ala, Asp, Ser или Thr (A, D, S или T)
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 31
Tyr Thr Phe Xaa Xaa Tyr Xaa Met His
1 5
<210> 32
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> I или N
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> K или R
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 32
Tyr Thr Phe Xaa Xaa Tyr Val Met His
1 5
<210> 33
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (1)..(1)
<223> H, K или G
<220>
<221> Модифицированный остаток
<222> (2)..(2)
<223> Q или H
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> Y или H
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> S, H, D, T, V, M или L
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> R или H
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> T или H
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 33
Xaa Xaa Ser Xaa Xaa Xaa Arg Xaa
1 5
<210> 34
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> H, V, K, W, R, L, G, Y или Q
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> H, L, E, W, G, M, P, T, Q или V
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 34
Lys Gln Ser Tyr Xaa Xaa Arg Thr
1 5
<210> 35
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (1)..(1)
<223> K или H
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> H, Y, M, S, L, E, G или W
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> R или K
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 35
Xaa Gln Ser Xaa His Xaa Arg Thr
1 5
<210> 36
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> Y или H
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> Xaa может представлять собой Thr, Ser, Val, Lys или Gln (T, S, V, K или
Q)
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> R или H
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 36
Lys Gln Ser Xaa Xaa Xaa Arg Thr
1 5
<210> 37
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 37
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 38
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> N или H
<220>
<221> Модифицированный остаток
<222> (9)..(9)
<223> A, R или T
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> R или H
<220>
<221> Модифицированный остаток
<222> (11)..(11)
<223> T, P или E
<220>
<221> Модифицированный остаток
<222> (13)..(13)
<223> H или K
<220>
<221> Модифицированный остаток
<222> (15)..(15)
<223> H или Y
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 38
Lys Ser Ser Gln Ser Leu Leu Xaa Xaa Xaa Xaa Gly Xaa Asn Xaa Leu
1 5 10 15
Ala
<210> 39
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> N или H
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> R или H
<220>
<221> Модифицированный остаток
<222> (13)..(13)
<223> K или H
<220>
<221> Модифицированный остаток
<222> (15)..(15)
<223> Y или H
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 39
Lys Ser Ser Gln Ser Leu Leu Xaa Ala Xaa Thr His Xaa Asn Xaa Leu
1 5 10 15
Ala
<210> 40
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 40
Lys Ser Ser Gln Ser Leu Leu Asn Ala Ser Thr Ala Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 41
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 41
Lys Ser Ser Gln Ser Leu Leu Asn Ala Arg Thr Arg Thr Asn Tyr Leu
1 5 10 15
Ala
<210> 42
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (9)..(9)
<223> S или A
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> R или H
<220>
<221> Модифицированный остаток
<222> (11)..(11)
<223> E или T
<220>
<221> Модифицированный остаток
<222> (13)..(13)
<223> H или K
<220>
<221> Модифицированный остаток
<222> (15)..(15)
<223> H или Y
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 42
Lys Ser Ser Gln Ser Leu Leu Asn Xaa Xaa Xaa Gly Xaa Asn Xaa Leu
1 5 10 15
Ala
<210> 43
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> H или A
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> T, Y или H
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> G или H
<220>
<221> Модифицированный остаток
<222> (7)..(7)
<223> H, R, V или I
<220>
<221> Модифицированный остаток
<222> (12)..(12)
<223> V или H
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 43
Ala Arg Asp Xaa Xaa Xaa Xaa Tyr Phe Tyr Asp Xaa
1 5 10
<210> 44
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (1)..(1)
<223> F или S
<220>
<221> Модифицированный остаток
<222> (7)..(7)
<223> Y или H
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 44
Xaa Asn Ile Lys Asp Tyr Xaa Met His
1 5
<210> 45
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> S, D, A, N, L или Q
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> V, T, D, Y или K
<400> 45
Trp Ile Asn Pro Xaa Thr Gly Ala Thr Xaa Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 46
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (1)..(1)
<223> W, S или D
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> A, H, K, T или D
<400> 46
Xaa Ile Asp Ala Gly Thr Gly Ala Thr Xaa Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 47
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 47
Phe Asn Ile Lys Asp Tyr Tyr Met His
1 5
<210> 48
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> S, H, V, K, W, L, G, T, R или Q
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> H, R, L, K, E, W, G, M, T или V
<400> 48
Lys Ser Gln Tyr Xaa Xaa Arg Thr
1 5
<210> 49
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 49
Lys Ser Ser Gln Ser Leu Leu Asn Ala Arg Thr Gly Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 50
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (3)..(3)
<223> T, N или D
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> V или K
<400> 50
Trp Ile Xaa Ala Gly Thr Gly Ala Thr Xaa Tyr Ser Gln Lys Gly Gln
1 5 10 15
Gly
<210> 51
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> T или A
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> E, D, A, S, G или Q
<220>
<221> Модифицированный остаток
<222> (7)..(7)
<223> D, A, V или E
<400> 51
Tyr Thr Phe Xaa Xaa Tyr Xaa Met His
1 5
<210> 52
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> H или Y
<400> 52
Lys Gln Ser Xaa Ser Arg Arg Thr
1 5
<210> 53
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> N или H
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> R или H
<220>
<221> Модифицированный остаток
<222> (12)..(12)
<223> G или H
<220>
<221> Модифицированный остаток
<222> (13)..(13)
<223> K или H
<220>
<221> Модифицированный остаток
<222> (15)..(15)
<223> H или Y
<400> 53
Lys Ser Ser Gln Ser Leu Leu Xaa Ala Xaa Thr Xaa Xaa Asn Xaa Leu
1 5 10 15
Ala
<210> 54
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 54
Lys Gln Ser Tyr Ser Arg Arg Thr
1 5
<210> 55
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> H или R
<220>
<221> Модифицированный остаток
<222> (13)..(13)
<223> H или K
<220>
<221> Модифицированный остаток
<222> (15)..(15)
<223> H или Y
<400> 55
Lys Ser Ser Gln Ser Leu Leu Asn Ala Xaa Thr Gly Xaa Asn Xaa Leu
1 5 10 15
Ala
<210> 56
<211> 28
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (28)..(28)
<223> Lys/SCBiot(dPEG4)
<220>
<223> C-концевой амид
<400> 56
Gln Asp Gly Asn Glu Glu Met Gly Ser Ile Thr Gln Thr Pro Tyr Gln
1 5 10 15
Val Ser Ile Ser Gly Thr Thr Val Ile Leu Thr Lys
20 25
<210> 57
<211> 14
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (14)..(14)
<223> Lys/SCBiot(dPEG4)
<220>
<223> C- концевой амид
<400> 57
Gln Asp Gly Asn Glu Glu Met Gly Gly Ile Thr Gln Thr Lys
1 5 10
<210> 58
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (2)..(2)
<223> R или H
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> A, H, M или Q
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> Y, H, S, G, A, T, V или R
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> G, H, P, E, R
<220>
<221> Модифицированный остаток
<222> (7)..(7)
<223> H или R
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> Y, N, F, H, D, E, S, L, M, I, G, A, Q или T
<220>
<221> Модифицированный остаток
<222> (9)..(9)
<223> F или H
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> Y или H
<220>
<221> Модифицированный остаток
<222> (12)..(12)
<223> V, H или M
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 58
Ala Xaa Asp Xaa Xaa Xaa Xaa Xaa Xaa Xaa Asp Xaa
1 5 10
<210> 59
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<220>
<221> Модифицированный остаток
<222> (1)..(1)
<223> W, S, Y, F, G или D
<220>
<221> Модифицированный остаток
<222> (3)..(3)
<223> N, T, D, V или H
<220>
<221> Модифицированный остаток
<222> (4)..(4)
<223> A, P или S
<220>
<221> Модифицированный остаток
<222> (5)..(5)
<223> G, A, S, N, D, L, V, H, Q, T, I или Y
<220>
<221> Модифицированный остаток
<222> (6)..(6)
<223> D или T
<220>
<221> Модифицированный остаток
<222> (7)..(7)
<223> A или G
<220>
<221> Модифицированный остаток
<222> (8)..(8)
<223> A, N, T, S, L, D, F, Y или E
<220>
<221> Модифицированный остаток
<222> (10)..(10)
<223> V, K, T, D, Y, F, A, H, N, L, I или E
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<400> 59
Xaa Ile Xaa Xaa Xaa Xaa Xaa Xaa Thr Xaa Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 60
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 60
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 61
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 61
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 62
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 62
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr His Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 63
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 63
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 64
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 64
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 65
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 65
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 66
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 66
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asp Ser Tyr
20 25 30
Ile Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 67
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 67
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 68
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 68
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asn Asn Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Asn Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 69
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 69
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 70
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 70
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gln Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ser Ile Asp Ala Gly Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 71
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 71
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 72
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 72
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gln Tyr
20 25 30
Ser Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Ala Gly Thr Gly Asp Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His His Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 73
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 73
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Phe Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 74
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 74
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asp Ala Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 75
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 75
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 76
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 76
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Pro Glu Trp Met
35 40 45
Gly Ser Ile Asn Ala Gly Thr Gly Phe Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 77
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 77
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 78
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 78
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Val Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 79
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 79
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 80
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 80
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Ala Gly Thr Gly Ala Thr Ile Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 81
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 81
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 82
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 82
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ala Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Ala Trp Met
35 40 45
Gly Trp Ile Asn Pro His Thr Gly Ala Thr Phe Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 83
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 83
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 84
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 84
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Leu Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Arg Met
35 40 45
Gly Trp Ile Asn Pro Ser Thr Gly Ala Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 85
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 85
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 86
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 86
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 87
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 87
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 88
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 88
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asp Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 89
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 89
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 90
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 90
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ala Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ser Ile Asp Ala Gly Thr Gly Asn Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 91
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 91
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 92
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 92
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Glu Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Thr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 93
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 93
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 94
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 94
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asp Ser Tyr
20 25 30
Leu Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Asn Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 95
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 95
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 96
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 96
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asn Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Tyr Thr Gly Glu Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 97
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 97
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 98
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 98
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Tyr Ser Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Asp Trp Met
35 40 45
Gly Trp Ile Asn Pro Gln Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 99
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 99
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 100
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 100
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asn Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Tyr Ile Asn Gly Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe Gln
50 55 60
Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr Met
65 70 75 80
Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Ser Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ser
115
<210> 101
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 101
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 102
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 102
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Phe Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 103
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 103
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 104
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 104
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Lys Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Pro Glu Trp Met
35 40 45
Gly Trp Ile Asn Ala Gly Thr Gly Asn Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 105
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 105
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 106
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 106
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 107
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 107
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 108
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 108
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 109
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 109
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 110
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 110
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Leu Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Thr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 111
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 111
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 112
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 112
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Pro Ser Tyr
20 25 30
Pro Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Asp Trp Met
35 40 45
Gly Trp Ile Asn Pro Asp Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 113
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 113
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Pro Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 114
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 114
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro His Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 115
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 115
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 116
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 116
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Asp
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Ala Trp Met
35 40 45
Gly Tyr Ile Asn Ala Gly Thr Gly Thr Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 117
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 117
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 118
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 118
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Thr
20 25 30
Phe Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Phe Ile Asp Ala Gly Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 119
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 119
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 120
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 120
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Ser Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ser Ile Asn Ala Gly Thr Gly Ile Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 121
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 121
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 122
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 122
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Ala Thr Gly Ala Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His His Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 123
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 123
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 124
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 124
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Gly Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 125
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 125
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 126
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 126
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe His Ser Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Ser Thr Gly Ser Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 127
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 127
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 128
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 128
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asn Ser Tyr
20 25 30
Arg Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ser Ile Asp Ala Gly Thr Gly Asn Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 129
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 129
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 130
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 130
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 131
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 131
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 132
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 132
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Tyr Thr Gly Tyr Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 133
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 133
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 134
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 134
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Gln Trp Met
35 40 45
Gly Trp Ile Asn Pro Tyr Thr Gly Tyr Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 135
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 135
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 136
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 136
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Tyr Cys Lys Ala Ser Gly Tyr Thr Phe Thr Thr Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ser Ile Asn Ala Gly Asp Ala Asn Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 137
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 137
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 138
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 138
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Ile Thr Gly Tyr Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly Arg Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 139
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 139
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 140
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 140
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ala Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Arg Met
35 40 45
Gly Trp Ile Asp Pro Ile Thr Gly Asn Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 141
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 141
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 142
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 142
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Asp Trp Met
35 40 45
Gly Tyr Ile Asn Pro Asp Thr Gly Asp Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 143
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 143
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 144
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 144
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Pro Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Leu Thr Thr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr His Arg Tyr Phe Tyr Asp Met Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 145
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 145
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 146
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 146
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asn Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Asp Trp Met
35 40 45
Gly Trp Ile Asn Pro Asp Thr Gly Asn Thr Asn Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 147
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 147
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 148
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 148
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Asp
20 25 30
His Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ser Ile Asn Ala Gly Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 149
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 149
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 150
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 150
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Ile Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 151
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 151
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Val His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 152
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 152
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly Arg Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 153
<211> 111
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 153
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Arg
20 25 30
His Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
100 105 110
<210> 154
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 154
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Gly Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 155
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 155
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 156
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 156
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Val Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 157
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 157
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Lys His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 158
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 158
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Pro Ala Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Ser His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 159
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 159
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gly His
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 160
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 160
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Ser Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 161
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 161
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Leu Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 162
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 162
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Asp Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Asn Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 163
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 163
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Lys Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 164
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 164
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Pro His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 165
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 165
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Glu Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 166
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 166
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Asp Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Gly His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 167
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 167
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Pro Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gly His
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 168
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 168
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Ala Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg His Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 169
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 169
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 170
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 170
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Arg Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Thr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 171
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 171
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Trp His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 172
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 172
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Gln Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Ser Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 173
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 173
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Glu Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 174
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 174
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 175
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 175
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 176
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 176
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Ser Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 177
<211> 111
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 177
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Met His Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
100 105 110
<210> 178
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 178
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Arg Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 179
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 179
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Ser His Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 180
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 180
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gln His Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 181
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 181
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 182
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 182
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Ser Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 183
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 183
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Trp Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 184
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 184
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asp Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Ala Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 185
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 185
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Gly Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 186
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 186
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Arg Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Gly Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 187
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 187
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Arg His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 188
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 188
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Pro His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 189
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 189
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Leu His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 190
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 190
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Pro Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Ser Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 191
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 191
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Trp Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 192
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 192
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Pro Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Ala His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 193
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 193
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Pro Arg Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Asp Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 194
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 194
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Ala Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 195
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 195
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Leu His Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 196
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 196
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 197
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 197
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 198
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 198
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Arg Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Gly Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 199
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 199
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Gly His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 200
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 200
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 201
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 201
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Thr Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 202
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 202
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His Glu Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 203
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 203
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Val Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 204
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 204
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Asp Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Leu Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 205
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 205
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Met Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 206
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 206
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Met Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser
115
<210> 207
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 207
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Pro Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Met Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 208
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 208
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Asn Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 209
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 209
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Thr His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 210
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 210
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Ser Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Ser Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 211
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 211
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Gly Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 212
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 212
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Thr His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 213
<211> 111
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 213
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Thr Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
100 105 110
<210> 214
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 214
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Met His Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 215
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 215
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Glu His Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 216
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 216
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 217
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 217
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Arg His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 218
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 218
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 219
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 219
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 220
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 220
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 221
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 221
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 222
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 222
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Pro Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Glu Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 223
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 223
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Leu Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 224
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 224
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Trp Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 225
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 225
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 226
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 226
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 227
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 227
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Gly His Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 228
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 228
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Pro Ala Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Gly Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 229
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 229
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Gly His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 230
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 230
Gln Val Gln Leu Val Gln Ser Glu Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Gln Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Gly Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 231
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 231
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Pro Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 232
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 232
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Ala Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Phe His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 233
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 233
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Pro Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 234
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 234
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Asp Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg His Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 235
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 235
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Arg Thr Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 236
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 236
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Asn His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 237
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 237
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Ser Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Val His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 238
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 238
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Ala Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Asp Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 239
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 239
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 240
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 240
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 241
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 241
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 242
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 242
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Val His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 243
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 243
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Pro Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 244
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 244
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Thr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 245
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 245
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser His Val Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 246
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 246
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Glu Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Thr Leu Ala Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Val Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 247
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 247
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Leu His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 248
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 248
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Gln Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 249
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 249
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Thr Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 250
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 250
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Asp Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 251
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 251
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Pro Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 252
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 252
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Val Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 253
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 253
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Ser Thr Ala Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Arg His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 254
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 254
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Val Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 255
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 255
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Ser His Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 256
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 256
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Glu Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Val Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 257
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 257
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Leu His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 258
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 258
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Asp Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 259
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 259
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Trp His Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 260
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 260
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Asp Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 261
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 261
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 262
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 262
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 263
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 263
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Arg Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 264
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 264
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Asp Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Asp Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 265
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 265
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 266
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 266
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Ala Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 267
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 267
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Gln Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 268
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 268
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Glu Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Pro Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Val Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 269
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 269
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Leu His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 270
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 270
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Pro Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Asp Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 271
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 271
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 272
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 272
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Thr Leu Asp Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Asn His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 273
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 273
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Pro Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Leu His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 274
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 274
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Asp Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 275
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 275
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 276
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 276
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Gln Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Arg His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 277
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 277
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser His Gly Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 278
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 278
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Gln Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Val Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 279
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 279
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 280
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 280
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Asp Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 281
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 281
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Gly His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 282
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 282
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Glu Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 283
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 283
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Gly His Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 284
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 284
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His Arg Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 285
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 285
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr His Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 286
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 286
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Glu Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly Arg Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 287
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 287
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 288
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 288
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Arg His Glu Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 289
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 289
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Tyr His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 290
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 290
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Val Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 291
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 291
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Gln His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 292
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 292
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Val Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 293
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 293
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 294
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 294
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Asp Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 295
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 295
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 296
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 296
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Thr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 297
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 297
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Val Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 298
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 298
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Arg Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Glu Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 299
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 299
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 300
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 300
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly His Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asp Thr Gly Ala Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 301
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 301
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 302
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 302
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ala Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 303
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 303
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 304
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 304
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asn Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Asn Thr Tyr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 305
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 305
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 306
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 306
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ala Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asp Thr Gly Ala Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 307
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 307
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 308
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 308
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Glu Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 309
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 309
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 310
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 310
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Pro Ser Leu Glu Trp Met
35 40 45
Gly Ser Ile Asp Ala Gly Thr Gly Ala Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 311
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 311
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 312
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 312
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Glu Ser Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile His Ser Gly Thr Gly Asn Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 313
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 313
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 314
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 314
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ala
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Asp Ile Asn Ala Gly Thr Gly Ala Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 315
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 315
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 316
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 316
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Val Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Asn Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 317
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 317
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 318
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 318
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Asp
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Asn Thr Tyr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 319
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 319
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 320
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 320
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ser Ile Asp Ala Gly Thr Gly Ala Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 321
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 321
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 322
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 322
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Pro Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr His Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 323
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 323
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 324
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 324
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Thr Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 325
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 325
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 326
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 326
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asp Ser Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Pro Arg Leu Glu Trp Met
35 40 45
Gly Ser Ile Asn Ala Gly Thr Gly Asn Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 327
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 327
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 328
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 328
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Asp
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly His Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Asn Thr Tyr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 329
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 329
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 330
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 330
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 331
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 331
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 332
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 332
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Asp
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Ala Gly Thr Gly Ala Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Asp Ala Tyr Gly Arg Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 333
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 333
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 334
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 334
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ala Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly His Arg Leu Glu Trp Met
35 40 45
Gly Asp Ile Ile Ala Gly Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 335
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 335
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 336
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 336
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Ser Thr Gly Asn Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 337
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 337
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 338
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 338
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Asp
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Ser Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Asn Thr Tyr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 339
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 339
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 340
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 340
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asn Asn Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Ser Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Asn Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 341
<211> 111
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 341
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
100 105 110
<210> 342
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 342
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Thr Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Val Thr Gly Asn Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 343
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 343
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 344
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 344
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe His Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly His Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asp Thr Gly Ala Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 345
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 345
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 346
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 346
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Val Thr Gly Ala Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 347
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 347
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 348
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 348
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Pro Thr Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 349
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 349
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 350
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 350
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe His Ser Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Thr Ala Gly Thr Gly Ser Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 351
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 351
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 352
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 352
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His His Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 353
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 353
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 354
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 354
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Val Thr Gly Ala Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 355
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 355
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 356
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 356
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asp Ser Ile
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Ala Thr Gly Asn Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 357
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 357
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 358
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 358
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Asp Ile Asp Ala Gly Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 359
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 359
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 360
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 360
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe His Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Thr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 361
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 361
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 362
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 362
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Pro Arg Leu Glu Trp Met
35 40 45
Gly Asp Ile Asp Ala Gly Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 363
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 363
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 364
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 364
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asp Ser Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly His Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Leu Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 365
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 365
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 366
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 366
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asn Arg Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Gly Ile Asp Ala Gly Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Arg His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser
115
<210> 367
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 367
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 368
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 368
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ile Lys Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Asp Ile Asp Pro Asp Thr Gly Ala Thr Glu Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Asp Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 369
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 369
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 370
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 370
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ala Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asp Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 371
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 371
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 372
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 372
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gln Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Thr Leu Glu Trp Met
35 40 45
Gly Asp Ile Asn Ala Gly Thr Gly Val Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 373
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 373
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 374
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 374
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 375
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 375
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu His Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 376
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 376
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Glu Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Pro Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Thr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 377
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 377
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 378
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 378
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Val Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Pro Ser Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Asn Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 379
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 379
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 380
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 380
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Glu Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Pro Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Thr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 381
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 381
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 382
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 382
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Ala Gly Asp Ala Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 383
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 383
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 384
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 384
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Val Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ser Ile Asn Ala Gly Asp Ala Asn Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 385
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 385
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 386
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 386
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Glu Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Thr Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Thr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 387
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 387
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 388
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 388
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Glu Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Pro Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Asn Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 389
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 389
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 390
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 390
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly His Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Ala Gly Asp Ala Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 391
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 391
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 392
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 392
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 393
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 393
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu His Ala
20 25 30
Arg Thr His Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 394
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 394
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 395
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 395
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu His Ala
20 25 30
Arg Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 396
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 396
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 397
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 397
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu His Ala
20 25 30
Arg Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 398
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 398
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 399
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 399
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu His Ala
20 25 30
Arg Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 400
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 400
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 401
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 401
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr His Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 402
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 402
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 403
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 403
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr His His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 404
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 404
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 405
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 405
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr His Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 406
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 406
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 407
<211> 111
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 407
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
100 105 110
<210> 408
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 408
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser
115
<210> 409
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 409
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr His Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 410
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 410
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 411
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 411
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 412
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 412
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 413
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 413
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 414
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 414
Gln Val Gln Leu Val Gln Ser Gly Thr Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 415
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 415
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
His Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 416
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 416
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg His Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 417
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 417
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 418
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 418
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 419
<211> 111
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 419
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile
100 105 110
<210> 420
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 420
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 421
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 421
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 422
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 422
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 423
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 423
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 424
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 424
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 425
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 425
Gly Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 426
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 426
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 427
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 427
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr His Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser Arg Arg His Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 428
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 428
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His His Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 429
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 429
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Arg
20 25 30
His Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 430
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 430
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His Arg His Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 431
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 431
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 432
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 432
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 433
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 433
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 434
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 434
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 435
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 435
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr His Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 436
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 436
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala His Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 437
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 437
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu His Thr
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 438
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 438
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 439
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 439
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His His Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 440
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 440
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 441
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 441
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys His Gln
85 90 95
Ser His Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 442
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 442
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly Arg Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 443
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 443
Asp Ile Val Met Thr Gln Ser Pro Asp Cys Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 444
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 444
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 445
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 445
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Glu Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 446
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 446
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr His Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser
115
<210> 447
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 447
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu His Ala
20 25 30
His Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 448
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 448
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr His Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 449
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 449
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 450
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 450
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 451
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 451
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys His Gln
85 90 95
Ser Tyr Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 452
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 452
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 453
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 453
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu His Ala
20 25 30
Arg Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 454
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 454
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ala Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr His Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 455
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 455
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 456
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 456
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 457
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 457
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His Arg Arg His Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 458
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 458
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 459
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 459
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg His Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 460
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 460
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 461
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 461
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu His Ala
20 25 30
Arg Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 462
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 462
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 463
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 463
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys His Gln
85 90 95
Ser His Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 464
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 464
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 465
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 465
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 466
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 466
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 467
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 467
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 468
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 468
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 469
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 469
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 470
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 470
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
His Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 471
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 471
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 472
<211> 118
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 472
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser
115
<210> 473
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 473
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 474
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 474
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 475
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 475
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Pro Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys His Gln
85 90 95
Ser Tyr His Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 476
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 476
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 477
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 477
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys His Gln
85 90 95
Ser Tyr Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 478
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 478
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr His His Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 479
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 479
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys His Gln
85 90 95
Ser Tyr His Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 480
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 480
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 481
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 481
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu His Ala
20 25 30
Arg Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 482
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 482
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr His Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 483
<211> 111
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 483
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Ser Gly Ser Thr Arg Glu Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
65 70 75 80
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys His Gln Ser
85 90 95
Tyr His Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 484
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 484
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His Arg Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 485
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 485
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr His Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 486
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 486
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 487
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 487
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 488
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 488
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 489
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 489
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu His Ala
20 25 30
His Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 490
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 490
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly Arg His Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 491
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 491
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His His Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 492
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 492
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 493
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 493
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 494
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 494
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His His Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 495
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 495
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 496
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 496
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 497
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 497
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys His Gln
85 90 95
Ser Tyr Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 498
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 498
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 499
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 499
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys His Gln
85 90 95
Ser Tyr Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 500
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 500
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Thr Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly Arg Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 501
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 501
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 502
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 502
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Ala Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His Arg Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 503
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 503
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 504
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 504
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 505
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 505
Asp Ile Val Met Thr Gln Tyr Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys His Gln
85 90 95
Ser Tyr Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 506
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 506
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His Arg His Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 507
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 507
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu His Pro
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 508
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 508
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His His Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 509
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 509
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu His Ala
20 25 30
Arg Thr Gly His Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 510
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 510
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 511
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 511
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 512
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 512
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr His Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 513
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 513
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 514
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 514
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly Arg Tyr Phe His Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 515
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 515
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
His Thr Gly Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys His Gln
85 90 95
Ser Tyr Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 516
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 516
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ala Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asp Thr Gly Asn Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 517
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 517
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 518
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 518
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Leu Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 519
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 519
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 520
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 520
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Lys Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Asn Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 521
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 521
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 522
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 522
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asp Ala Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Ala Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 523
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 523
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 524
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 524
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Gln Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Gln Trp Met
35 40 45
Gly Trp Ile Asn Pro Thr Thr Gly Asn Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 525
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 525
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 526
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 526
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Ala
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Gln Pro Met
35 40 45
Gly Trp Ile Asn Ala Gly Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 527
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 527
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 528
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 528
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asp Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Asp Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 529
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 529
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 530
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 530
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Glu Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Leu Thr Gly Asn Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 531
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 531
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 532
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 532
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 533
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 533
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr His Lys Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr His His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 534
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 534
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Leu Thr Gly Asn Thr Leu Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 535
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 535
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 536
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 536
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Glu Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Pro Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 537
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 537
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 538
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 538
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Asp
20 25 30
Phe Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Ala Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 539
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 539
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 540
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 540
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Glu Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Asn Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 541
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 541
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 542
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 542
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Ser Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 543
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 543
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 544
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 544
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asn Ala Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asp Thr Gly Ala Thr Thr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 545
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 545
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 546
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 546
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Pro Tyr Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 547
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 547
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 548
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 548
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Ala Thr His Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 549
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 549
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 550
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 550
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Glu Ser Tyr
20 25 30
Asp Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Ala Gly Thr Gly Ala Thr Val Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 551
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 551
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 552
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 552
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asp Ser Tyr
20 25 30
Ser Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asp Thr Gly Ala Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 553
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 553
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 554
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 554
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Phe Asn Ile Lys Asp Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asp Leu Glu Asn Ala Asn Thr Ile Tyr Asp Ala Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr His Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 555
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 555
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly His Asn His Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser His Ser His Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 556
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 556
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ala Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Gly Thr Gly Ser Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp His Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 557
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 557
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 558
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 558
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Glu Ser Tyr
20 25 30
Ser Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Ala Thr Gly Ala Thr Asp Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 559
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 559
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 560
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 560
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Gln Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Asn Thr Tyr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 561
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 561
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 562
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 562
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Glu Ser Tyr
20 25 30
Tyr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Arg Met
35 40 45
Gly Ser Ile Val Ala Gly Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly Arg Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Pro Val Thr Val Ser Ser
115
<210> 563
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 563
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 564
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 564
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asp Ser Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Tyr Ile Asn Pro Asp Thr Gly Ala Thr Tyr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 565
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 565
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 566
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 566
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asp Thr Gly Ala Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 567
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 567
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 568
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 568
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asp Ser Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Asn Thr Gly Ala Thr Thr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 569
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 569
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 570
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 570
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ala Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Ser Ile Asn Ala Gly Thr Gly Asn Thr Tyr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 571
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 571
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 572
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 572
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Asn Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro Leu Thr Gly Thr Thr Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala Tyr His His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 573
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 573
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 574
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 574
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Asn Asp Tyr
20 25 30
Ala Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Ala Trp Met
35 40 45
Gly Trp Ile Asp Ala Gly Thr Gly Asn Thr Tyr Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ala His Gly His Tyr Phe Tyr Asp Val Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 575
<211> 112
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид
<400> 575
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ala
20 25 30
Arg Thr Gly Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Ser Arg Arg Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 576
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 576
Ala Arg Asp Ala Tyr Gly Arg Tyr Phe Tyr Asp Val
1 5 10
<210> 577
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 577
Lys Ser Ser Gln Ser Leu Leu Asn Ala Arg Thr Gly Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 578
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 578
Lys Gln Ser Tyr Ser Arg Arg Thr
1 5
<210> 579
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 579
Ala Arg Asp Ala Tyr His Arg Tyr Phe Tyr Asp His
1 5 10
<210> 580
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 580
Lys Ser Ser Gln Ser Leu Leu Asn Ser His Thr Gly Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 581
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 581
Lys Gln Ser Tyr Ser Arg Arg Thr
1 5
<210> 582
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 582
Ala Arg Asp Ala His His Arg Tyr Phe Tyr Asp Val
1 5 10
<210> 583
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 583
Lys Ser Ser Gln Ser Leu Leu Asn Ala His Thr Gly His Asn Tyr Leu
1 5 10 15
Ala
<210> 584
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 584
Lys Gln Ser Tyr Ser Arg Arg Thr
1 5
<210> 585
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 585
Ala Arg Asp His Tyr His Arg Tyr Phe Tyr Asp Val
1 5 10
<210> 586
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 586
Lys Ser Ser Gln Ser Leu Leu Asn Ala Arg Thr Gly His Asn Tyr Leu
1 5 10 15
Ala
<210> 587
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 587
Lys Gln Ser His Ser His Arg Thr
1 5
<210> 588
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 588
Ala Arg Asp Ala His His Arg Tyr Phe Tyr Asp Val
1 5 10
<210> 589
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 589
Lys Ser Ser Gln Ser Leu Leu Asn Ala His Glu Gly Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 590
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
пептид
<400> 590
Lys Gln Ser His Ser His Arg Thr
1 5
<210> 591
<211> 335
<212> Белок
<213> Homo sapiens
<400> 591
Gln Asp Gly Asn Glu Glu Met Gly Gly Ile Thr Gln Thr Pro Tyr Lys
1 5 10 15
Val Ser Ile Ser Gly Thr Thr Val Ile Leu Thr Cys Pro Gln Tyr Pro
20 25 30
Gly Ser Glu Ile Leu Trp Gln His Asn Asp Lys Asn Ile Gly Gly Asp
35 40 45
Glu Asp Asp Lys Asn Ile Gly Ser Asp Glu Asp His Leu Ser Leu Lys
50 55 60
Glu Phe Ser Glu Leu Glu Gln Ser Gly Tyr Tyr Val Cys Tyr Pro Arg
65 70 75 80
Gly Ser Lys Pro Glu Asp Ala Asn Phe Tyr Leu Tyr Leu Arg Ala Arg
85 90 95
Val Cys Glu Asn Cys Met Glu Met Asp Gly Gly Ser Asp Lys Thr His
100 105 110
Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val
115 120 125
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
130 135 140
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
145 150 155 160
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
165 170 175
Thr Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser
180 185 190
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
195 200 205
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
210 215 220
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
225 230 235 240
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
245 250 255
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
260 265 270
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
275 280 285
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
290 295 300
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
305 310 315 320
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330 335
<210> 592
<211> 326
<212> Белок
<213> Macaca fascicularis
<400> 592
Gln Asp Gly Asn Glu Glu Met Gly Ser Ile Thr Gln Thr Pro Tyr Gln
1 5 10 15
Val Ser Ile Ser Gly Thr Thr Val Ile Leu Thr Cys Ser Gln His Leu
20 25 30
Gly Ser Glu Ala Gln Trp Gln His Asn Gly Lys Asn Lys Glu Asp Ser
35 40 45
Gly Asp Arg Leu Phe Leu Pro Glu Phe Ser Glu Met Glu Gln Ser Gly
50 55 60
Tyr Tyr Val Cys Tyr Pro Arg Gly Ser Asn Pro Glu Asp Ala Ser His
65 70 75 80
His Leu Tyr Leu Lys Ala Arg Val Cys Glu Asn Cys Met Glu Met Asp
85 90 95
Gly Gly Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
100 105 110
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
115 120 125
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
130 135 140
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
145 150 155 160
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Ala
165 170 175
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
180 185 190
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
195 200 205
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
210 215 220
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
225 230 235 240
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
245 250 255
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
260 265 270
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
275 280 285
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
290 295 300
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
305 310 315 320
Ser Leu Ser Pro Gly Lys
325
<210> 593
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<220>
<221> другой признак
<222> (5)..(5)
<223> Xaa может представлять собой Thr, His или Tyr (T, H или Y)
<220>
<221> другой признак
<222> (6)..(6)
<223> Xaa может представлять собой Gly или His (G или H)
<220>
<221> другой признак
<222> (7)..(7)
<223> Xaa может представлять собой His или Arg (H или R)
<220>
<221> другой признак
<222> (8)..(8)
<223> Xaa может представлять собой Val или Tyr (V или Y)
<220>
<221> другой признак
<222> (12)..(12)
<223> Xaa может представлять собой Val или His (V или H)
<400> 593
Ala Arg Asp Ala Xaa Xaa Xaa Xaa Phe Tyr Asp Xaa
1 5 10
<210> 594
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<220>
<221> другой признак
<222> (9)..(9)
<223> Xaa может представлять собой Ala или Ser (A или S)
<220>
<221> другой признак
<222> (10)..(10)
<223> Xaa может представлять собой Arg или His (R или H)
<220>
<221> другой признак
<222> (13)..(13)
<223> Xaa может представлять собой His или Lys (H или K)
<400> 594
Lys Ser Ser Gln Ser Leu Leu Asn Xaa Xaa Thr Gly Xaa Asn Tyr Leu
1 5 10 15
Ala
<210> 595
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<220>
<221> другой признак
<222> (8)..(8)
<223> Xaa может представлять собой Leu, Phe, Asn или Ala (L, F, N или A)
<220>
<221> другой признак
<222> (10)..(10)
<223> Xaa может представлять собой Thr или Lys (T или K)
<400> 595
Trp Ile Asp Ala Gly Thr Gly Xaa Thr Xaa Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 596
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<220>
<221> другой признак
<222> (2)..(2)
<223> Xaa может представлять собой Arg или His (R или H)
<220>
<221> другой признак
<222> (4)..(4)
<223> Xaa может представлять собой His или Ala (H или A)
<220>
<221> другой признак
<222> (5)..(5)
<223> Xaa может представлять собой His или Tyr (H или Y)
<220>
<221> другой признак
<222> (6)..(6)
<223> Xaa может представлять собой His, Gly или Pro (H, G или P)
<220>
<221> другой признак
<222> (7)..(7)
<223> Xaa может представлять собой Arg или His (R или H)
<220>
<221> другой признак
<222> (8)..(8)
<223> Xaa может представлять собой Tyr, Ile или Val (Y, I или V)
<220>
<221> другой признак
<222> (9)..(9)
<223> Xaa может представлять собой Phe или His (F или H)
<220>
<221> другой признак
<222> (12)..(12)
<223> Xaa может представлять собой Val или His (V или H)
<400> 596
Ala Xaa Asp Xaa Xaa Xaa Xaa Xaa Xaa Tyr Asp Xaa
1 5 10
<210> 597
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<220>
<221> другой признак
<222> (8)..(8)
<223> Xaa может представлять собой Asn или His (N или H)
<220>
<221> другой признак
<222> (10)..(10)
<223> Xaa может представлять собой Arg или His (R или H)
<220>
<221> другой признак
<222> (11)..(11)
<223> Xaa может представлять собой Thr или Glu (T или E)
<220>
<221> другой признак
<222> (12)..(12)
<223> Xaa может представлять собой Gly или His (G или H)
<220>
<221> другой признак
<222> (13)..(13)
<223> Xaa может представлять собой His или Lys (H или K)
<220>
<221> другой признак
<222> (15)..(15)
<223> Xaa может представлять собой His или Tyr (H или Y)
<400> 597
Lys Ser Ser Gln Ser Leu Leu Xaa Ala Xaa Xaa Xaa Xaa Asn Xaa Leu
1 5 10 15
Ala
<210> 598
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> См. поданное описание для подробного описания
замен и предпочтительных вариантов осуществления
<220>
<221> другой признак
<222> (1)..(1)
<223> Xaa может представлять собой His или Lys (H или K)
<220>
<221> другой признак
<222> (4)..(4)
<223> Xaa может представлять собой His или Tyr (H или Y)
<220>
<221> другой признак
<222> (5)..(5)
<223> Xaa может представлять собой Ser, His, Leu, Val или Lys (S, H, L, V или
K)
<220>
<221> другой признак
<222> (6)..(6)
<223> Xaa может представлять собой His, Arg или Glu (H, R или E)
<400> 598
Xaa Gln Ser Xaa Xaa Xaa Arg Thr
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛО К TIGIT И ЕГО ИСПОЛЬЗОВАНИЕ | 2019 |
|
RU2786434C2 |
| СВЯЗЫВАЮЩИЕ ДОМЕНЫ АНТИТЕЛА К CD3 И СОДЕРЖАЩИЕ ИХ АНТИТЕЛА, А ТАКЖЕ СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2018 |
|
RU2807040C2 |
| БЕЛОК, СВЯЗЫВАЮЩИЙСЯ С NKG2D, CD16 И С ОПУХОЛЕСПЕЦИФИЧЕСКИМ АНТИГЕНОМ | 2018 |
|
RU2788531C2 |
| ПОЛИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ БЕЛКИ, НАЦЕЛЕННЫЕ НА NKG2D, CD16 И TROP2 | 2018 |
|
RU2820629C2 |
| ПОЛИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ БЕЛКИ, НАЦЕЛЕННЫЕ НА CAIX, ANO1, МЕЗОТЕЛИН, TROP2, СEA ИЛИ КЛАУДИН-18.2 | 2018 |
|
RU2792671C2 |
| Белки, связывающие NKG2D, CD16 и опухолеассоциированный антиген | 2018 |
|
RU2816716C2 |
| БЕЛОК, СВЯЗЫВАЮЩИЙСЯ С NKG2D, CD16 И С ОПУХОЛЕСПЕЦИФИЧЕСКИМ АНТИГЕНОМ | 2018 |
|
RU2826991C2 |
| БЕЛКИ, СВЯЗЫВАЮЩИЕ ВСМА, NKG2D И CD16 | 2018 |
|
RU2805254C2 |
| БЕЛКИ, СВЯЗЫВАЮЩИЕ CD33, NKG2D И CD16 | 2018 |
|
RU2820603C2 |
| ГЕТЕРОДИМЕРНЫЕ Fc-СЛИТЫЕ БЕЛКИ IL15/IL15Rα | 2017 |
|
RU2779938C2 |
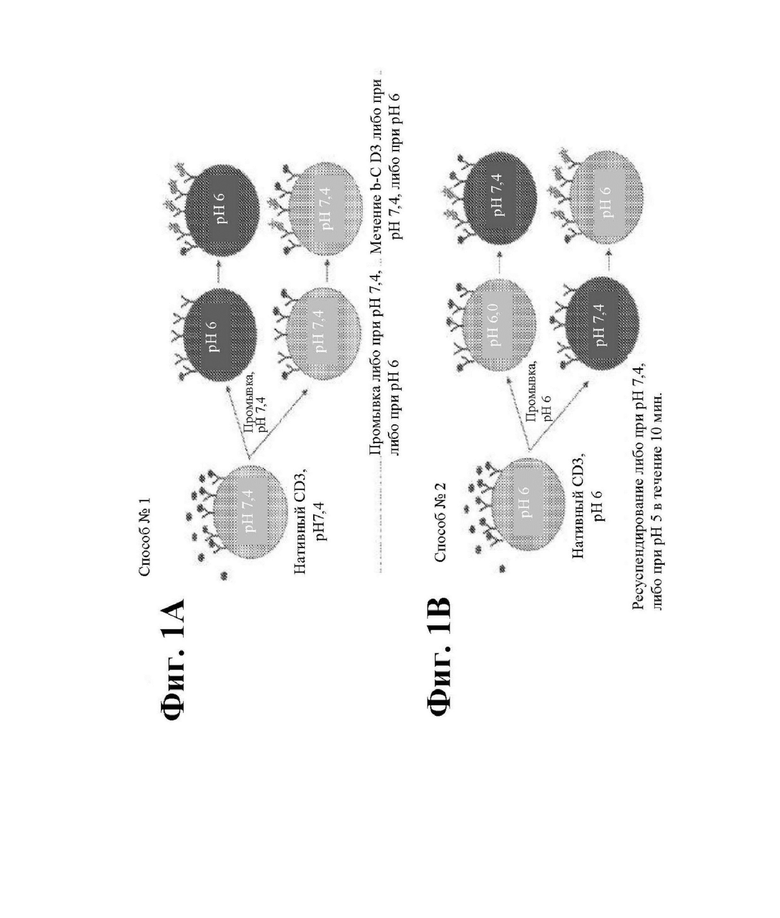
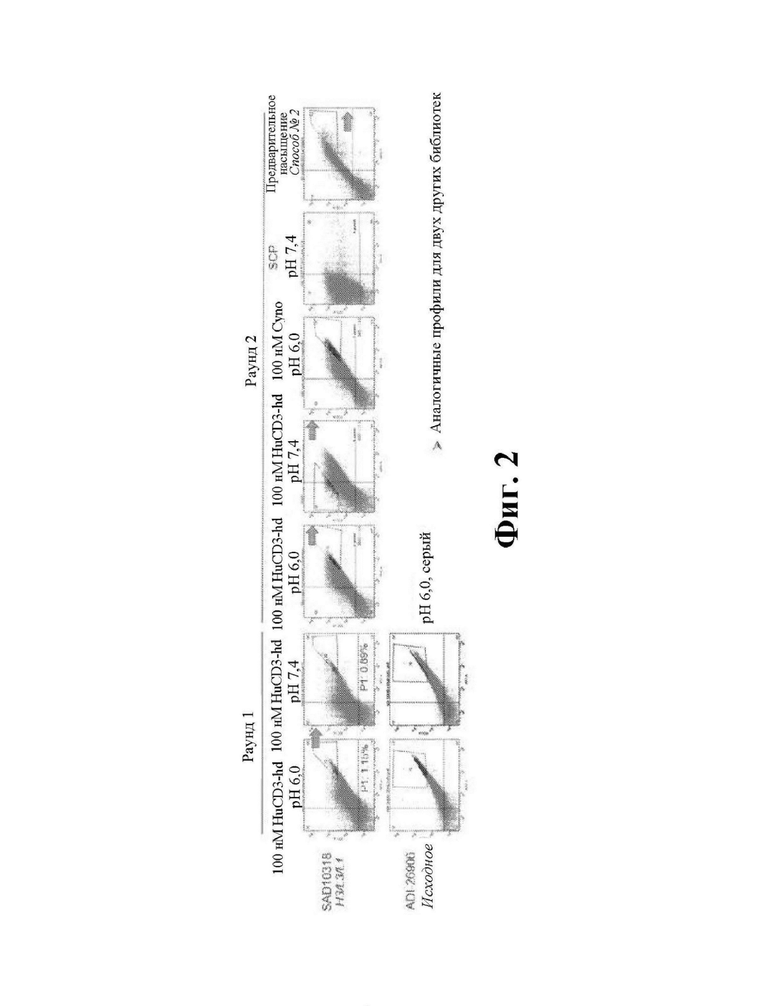
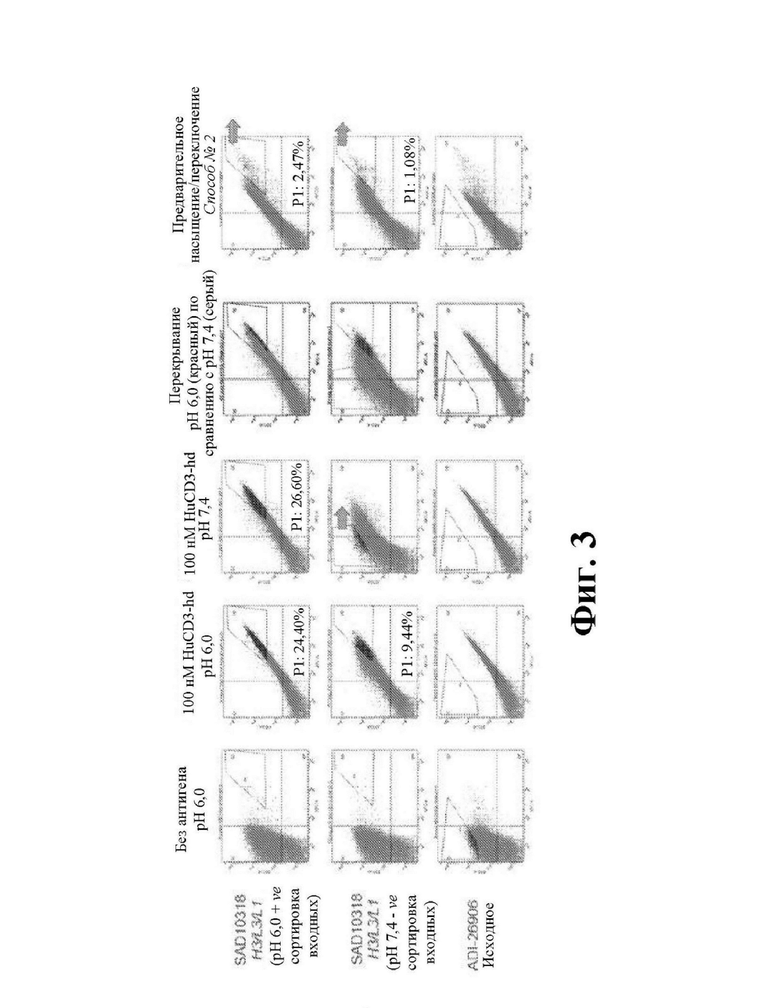
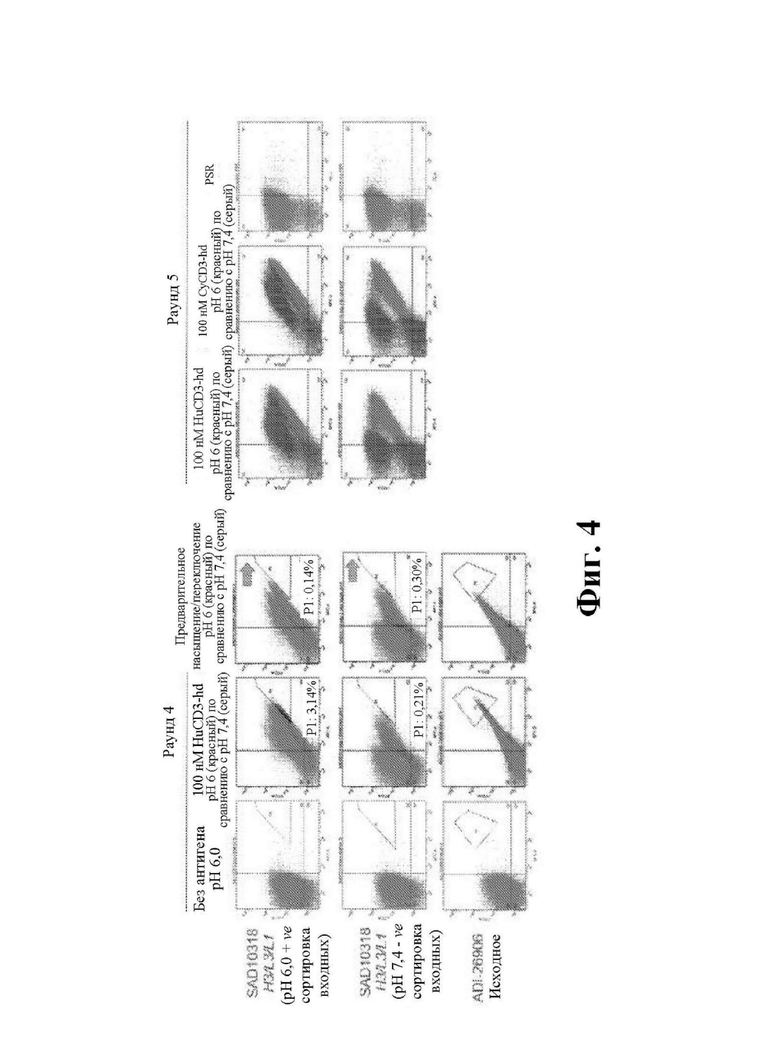
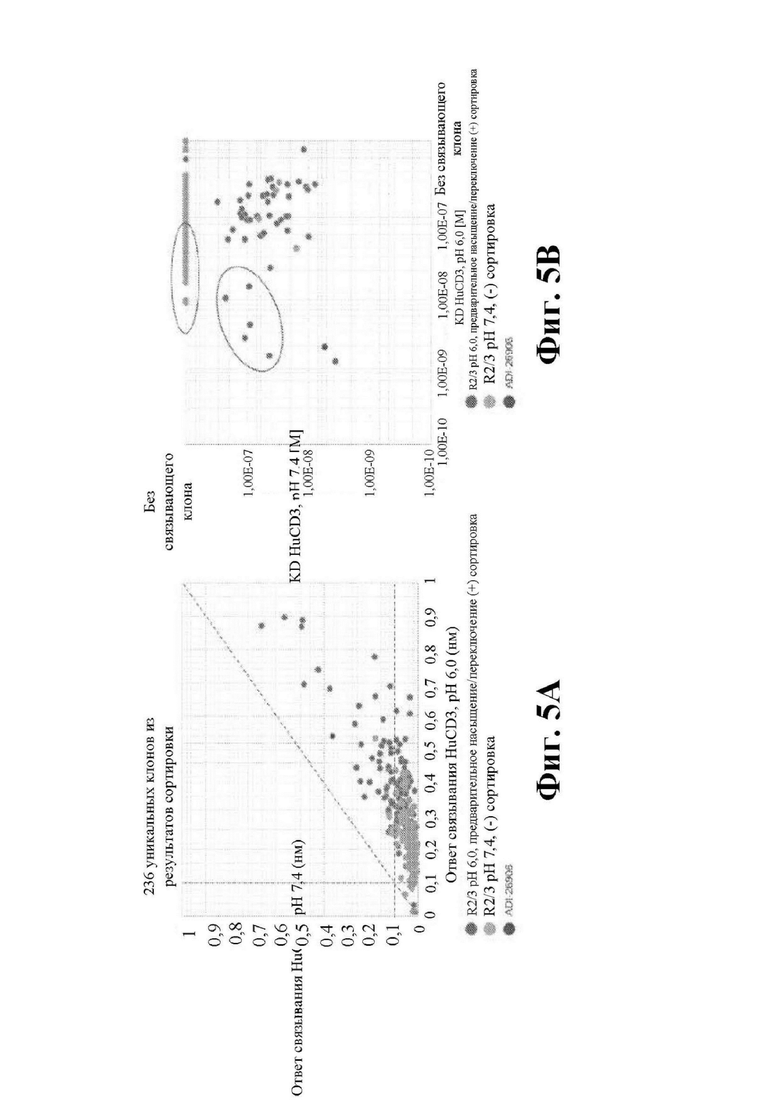

Изобретение относится к области биохимии, в частности к анти-CD3 антителу или антигенсвязывающему фрагменту антитела. Также раскрыты нуклеиновая кислота, кодирующая указанное антитело, экспрессирующий вектор, клетка-хозяин для экспрессии указанного антитела, фармацевтическая композиция, содержащая указанное антитело. Раскрыт способ лечения нарушения у млекопитающего с помощью указанного антитела. Изобретение позволяет эффективно лечить нарушения у млекопитающего с помощью указанного антитела. 13 н. и 46 з.п. ф-лы, 6 ил., 4 табл., 2 пр.
1. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела, содержащие:
(A) вариабельную область тяжелой цепи (VH) содержащую CDRH1, CDRH2 и CDRH3; и
(B) вариабельную область легкой цепи (VL), содержащую CDRL1, CDRL2 и CDRL3,
где
(i) указанный CDRH1 содержит аминокислотную последовательность:
(i-1) FNIKDYYMH (SEQ ID NO: 47); или
(i-2) YTFX1X2X3X4MH (SEQ ID NO: 29), где X1 представляет собой D, X2 представляет собой D, X3 представляет собой Y и X4 представляет собой A;
(ii) указанный CDRH2 содержит аминокислотную последовательность:
(ii-1) WIDLENANTIYDAKFQG (SEQ ID NO: 9); или
(ii-2) X1IDAGTGX2TX3YSQKFQG (SEQ ID NO: 12), где X1 представляет собой W, X2 представляет собой D, X3 представляет собой K;
(iii) указанный CDRH3 содержит аминокислотную последовательность
ARDX1YHRYFYDX2 (SEQ ID NO: 5), где X1 представляет собой H и X2 представляет собой V;
(iv) указанный CDRL1 содержит аминокислотную последовательность:
(iv-1) KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой R и X3 представляет собой H;
(iv-2) KSSQSLLX1X2X3X4GX5NX6LA (SEQ ID NO: 38), где X1 представляет собой H, X2 представляет собой A, X3 представляет собой R, X4 представляет собой T, X5 представляет собой K и X6 представляет собой H;
(iv-3) KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой R, X3 представляет собой T, X4 представляет собой H и X5 представляет собой H;
(iv-4) KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой H и X3 представляет собой H;
(iv-5) KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой H и X3 представляет собой K;
(iv-6) KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой H, X3 представляет собой T, X4 представляет собой K и X5 представляет собой H; или
(iv-7) KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой R и X3 представляет собой K;
(v) указанный CDRL2 cодержит аминокислотную последовательность
WASTRES (SEQ ID NO: 37); и
(vi) указанный CDRL3 содержит аминокислотную последовательность:
(vi-1) KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой H, X2 представляет собой S и X3 представляет собой H;
(vi-2) X1QSX2X3X4RT (SEQ ID NO: 598), где X1 представляет собой H, X2 представляет собой Y, X3 представляет собой S и X4 представляет собой H;
(vi-3) X1QSX2X3X4RT (SEQ ID NO: 598), где X1 представляет собой H, X2 представляет собой H, X3 представляет собой S и X4 представляет собой R;
(vi-4) KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой Y, X2 представляет собой S и X3 представляет собой R;
(vi-5) X1X2SX3X4X5RX6 (SEQ ID NO: 33), где X1 представляет собой K, X2 представляет собой Q, X3 представляет собой Y, X4 представляет собой S, X5 представляет собой R и X6 представляет собой H; или
(vi-6) X1X2SX3X4X5RX6 (SEQ ID NO: 33), где X1 представляет собой K, X2 представляет собой Q, X3 представляет собой Y, X4 представляет собой H, X5 представляет собой R и X6 представляет собой H.
2. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по п. 1, где в (vi) указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой H, X2 представляет собой S, X3 представляет собой H.
3. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по п. 1 или 2, где
в (i) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47) и
в (ii) указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9).
4. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по п. 1, где:
(I) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3, содержащиеся, соответственно, в SEQ ID NO: 130, и указанный CDRL1, указанный CDRL2 и указанный CDRL3 содержат последовательности CDRL1, CDRL2 и CDRL3, содержащиеся, соответственно, в SEQ ID NO: 131;
(II) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3, содержащиеся, соответственно, в SEQ ID NO: 460, и указанный CDRL1, указанный CDRL2 и указанный CDRL3 содержат последовательности CDRL1, CDRL2 и CDRL3, содержащиеся, соответственно, в SEQ ID NO: 461;
(III) аминокислотная последовательность указанного CDRH1, указанного CDRH2, и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3, содержащиеся, соответственно, в SEQ ID NO: 554, и указанный CDRL1, указанный CDRL2 и указанный CDRL3 содержат последовательности CDRL1, CDRL2 и CDRL3, содержащиеся, соответственно, в SEQ ID NO: 555;
(IV) аминокислотная последовательность указанного CDRH1, указанного CDRH2, и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3, содержащиеся, соответственно, в SEQ ID NO: 450, и указанный CDRL1, указанный CDRL2 и указанный CDRL3 содержат последовательности CDRL1, CDRL2 и CDRL3, содержащиеся, соответственно, в SEQ ID NO: 451;
(V) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3, содержащиеся, соответственно, в SEQ ID NO: 440, и указанный CDRL1, указанный CDRL2 и указанный CDRL3 содержат последовательности CDRL1, CDRL2 и CDRL3, содержащиеся, соответственно, в SEQ ID NO: 441;
(VI) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3, содержащиеся, соответственно, в SEQ ID NO: 492, и указанный CDRL1, указанный CDRL2 и указанный CDRL3 содержат последовательности CDRL1, CDRL2 и CDRL3, содержащиеся, соответственно, в SEQ ID NO: 493;
(VII) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3, содержащиеся, соответственно, в SEQ ID NO: 458, и указанный CDRL1, указанный CDRL2 и указанный CDRL3 содержат последовательности CDRL1, CDRL2 и CDRL3, содержащиеся, соответственно, в SEQ ID NO: 459;
(VIII) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3, содержащиеся, соответственно, в SEQ ID NO: 456, и указанный CDRL1, указанный CDRL2 и указанный CDRL3 содержат последовательности CDRL1, CDRL2 и CDRL3, содержащиеся, соответственно, в SEQ ID NO: 457; или
(IX) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3, содержащиеся, соответственно, в SEQ ID NO: 528, и указанный CDRL1, указанный CDRL2 и указанный CDRL3 содержат последовательности CDRL1, CDRL2 и CDRL3, содержащиеся, соответственно, в SEQ ID NO: 529.
5. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по п. 1, где:
(I) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой R и X3 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой H, X2 представляет собой S и X3 представляет собой H;
(II) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLX1X2X3X4GX5NX6LA (SEQ ID NO: 38), где X1 представляет собой H, X2 представляет собой A, X3 представляет собой R, X4 представляет собой T, X5 представляет собой K и X6 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой H, X2 представляет собой S и X3 представляет собой H;
(III) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой R, X3 представляет собой T, X4 представляет собой H и X5 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой H, X2 представляет собой S и X3 представляет собой H;
(IV) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой H и X3 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность X1QSX2X3X4RT (SEQ ID NO: 598), где X1 представляет собой H, X2 представляет собой Y, X3 представляет собой S и X4 представляет собой H;
(V) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой H и X3 представляет собой K; и
указанный CDRL3 содержит аминокислотную последовательность X1QSX2X3X4RT (SEQ ID NO: 598), где X1 представляет собой H, X2 представляет собой H, X3 представляет собой S и X4 представляет собой R;
(VI) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой H, X3 представляет собой T, X4 представляет собой K и X5 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой Y, X2 представляет собой S и X3 представляет собой R;
(VII) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой H, X3 представляет собой T, X4 представляет собой K и X5 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность X1X2SX3X4X5RX6 (SEQ ID NO: 33), где X1 представляет собой K, X2 представляет собой Q, X3 представляет собой Y, X4 представляет собой S, X5 представляет собой R и X6 представляет собой H;
(VIII) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой H, X3 представляет собой T, X4 представляет собой K и X5 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность X1X2SX3X4X5RX6 (SEQ ID NO: 33), где X1 представляет собой K, X2 представляет собой Q, X3 представляет собой Y, X4 представляет собой H, X5 представляет собой R и X6 представляет собой H; или
(IX) указанный CDRH1 содержит аминокислотную последовательность YTFX1X2X3X4MH (SEQ ID NO: 29), где X1 представляет собой D, X2 представляет собой D, X3 представляет собой Y и X4 представляет собой A;
указанный CDRH2 содержит аминокислотную последовательность X1IDAGTGX2TX3YSQKFQG (SEQ ID NO: 12), где X1 представляет собой W, X2 представляет собой D, X3 представляет собой K;
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой R и X3 представляет собой K; и
указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой Y, X2 представляет собой S и X3 представляет собой R.
6. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по п. 4 или 5, где
(1) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3, содержащиеся, соответственно, в SEQ ID NO: 130, и указанный CDRL1, указанный CDRL2 и указанный CDRL3 содержат последовательности CDRL1, CDRL2 и CDRL3, содержащиеся, соответственно, в SEQ ID NO: 131; или
(2) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой R и X3 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой H, X2 представляет собой S и X3 представляет собой H.
7. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по п. 4 или 5, где:
в (I) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 130 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 131;
в (II) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 460 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 461;
в (III) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 554 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 555;
в (IV) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 450 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 451;
в (V) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 440 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 441;
в (VI) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 492 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 493;
в (VII) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 458 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 459;
в (VIII) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 456 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 457; или
в (IX) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 528 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 529.
8. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по п 4 или 5, где указанный VH и указанный VL содержат аминокислотные последовательности:
в (I) SEQ ID NOS: 130 и 131 соответственно;
в (II) SEQ ID NOS: 460 и 461 соответственно;
в (III) SEQ ID NOS: 554 и 555 соответственно;
в (IV) SEQ ID NOS: 450 и 451 соответственно;
в (V) SEQ ID NOS: 440 и 441 соответственно;
в (VI) SEQ ID NOS: 492 и 493 соответственно;
в (VII) SEQ ID NOS: 458 и 459 соответственно;
в (VIII) SEQ ID NOS: 456 и 457 соответственно; или
в (IX) SEQ ID NOS: 528 и 529 соответственно.
9. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по любому из пп. 1-8, где указанный VH и указанный VL содержат аминокислотные последовательности SEQ ID NOS: 130 и 131 соответственно.
10. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по любому из предыдущих пунктов, которые содержат scFv, Fv, Fab, Fab', а Fab'-SH, а F(ab')2, диатело, scFv2-Fc2 или scFv-IgG.
11. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по любому из пп. 1-9, содержащие:
(A) тяжелую цепь, содержащую VH и константную область тяжелой цепи (CH); и
(B) легкую цепь, содержащую VL и константную область легкой цепи (CL).
12. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по п. 11, которое включает молекулу иммуноглобулина, состоящую из двух указанных тяжелых цепей и двух указанных легких цепей, соединенных между собой дисульфидными связями, или мультимер указанной молекулы иммуноглобулина.
13. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по п. 11 или 12, которое представляет собой или содержит антитело IgG, IgA, IgD, IgE или IgM.
14. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по п. 11 или 12, которое представляет собой или содержит антитело IgG1, IgG2, IgG3, IgG4, IgA1 или IgA2.
15. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по любому из пп. 1-14, которое содержится в химерном антигенном рецепторе (CAR).
16. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по п. 15, где указанный CAR содержит по меньшей мере один трансмембранный домен, по меньшей мере один внутриклеточный домен из Т-клеточного рецептора и по меньшей мере один костимулирующий домен.
17. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по п. 16, где по меньшей мере один трансмембранный домен представляет собой субъединицу CD3ζ.
18. Анти-CD3 антитело или антигенсвязывающий фрагмент антитела по любому из пп. 1-17, который содержит константный домен IgG.
19. Выделенная или рекомбинантная нуклеиновая кислота, кодирующая анти-CD3 антитело или антигенсвязывающий фрагмент антитела по любому из предшествующих пунктов.
20. Экспрессирующий вектор, содержащий выделенную или рекомбинантную молекулу нуклеиновой кислоты по п. 19.
21. Клетка-хозяин для экспрессии анти-CD3 антитела или антигенсвязывающего фрагмента антитела по любому из пп. 1-18, которая трансфицирована, трансформирована или трансдуцирована нуклеиновой кислотой по п. 18.
22. Клетка-хозяин для экспрессии анти-CD3 антитела или антигенсвязывающего фрагмента антитела по любому из пп. 1-18, которая трансфицирована, трансформирована или трансдуцирована экспрессирующим вектором по п. 20.
23. Клетка-хозяин по п. 21 или 22, которая представляет собой эукариотическую клетку.
24. Клетка-хозяин по п. 21 или 22, которая представляет собой клетку млекопитающих или клетку дрожжей.
25. Клетка-хозяин по п. 21 или 22, которая представляет собой клетку яичника китайского хомячка (CHO), клетку эмбриональной почки человека (HEK) или лимфоидную клетку.
26. Клетка-хозяин по п. 21 или 22, которая представляет собой прокариотическую клетку.
27. Клетка-хозяин по п. 21 или 22, которая представляет собой бактериальную клетку.
28. Фармацевтическая композиция для усиления иммунной функции, содержащая анти-CD3 антитело или антигенсвязывающий фрагмент антитела по любому из пп. 1-18 или клетку-хозяин по любому из пп. 21-27 и фармацевтически приемлемый носитель и/или эксципиент.
29. Мультиспецифическое антитело или фрагмент антитела, который содержит:
(I) первый антигенсвязывающий домен, который специфически связывается с CD3;
(II) второй антигенсвязывающий домен, который специфически связывается со вторым антигеном, отличным от CD3;
где первый антигенсвязывающий домен содержит:
(A) вариабельную область тяжелой цепи (VH), содержащую CDRH1, CDRH2 и CDRH3; и
(B) вариабельную область легкой цепи (VL), содержащую CDRL1, CDRL2 и CDRL3,
где:
(i) указанный CDRH1 содержит аминокислотную последовательность:
(i-1) FNIKDYYMH (SEQ ID NO: 47); или
(i-2) YTFX1X2X3X4MH (SEQ ID NO: 29), где X1 представляет собой D, X2 представляет собой D, X3 представляет собой Y и X4 представляет собой A;
(ii) указанный CDRH2 содержит аминокислотную последовательность:
(ii-1) WIDLENANTIYDAKFQG (SEQ ID NO: 9); или
(ii-2) X1IDAGTGX2TX3YSQKFQG (SEQ ID NO: 12), где X1 представляет собой W, X2 представляет собой D, X3 представляет собой K;
(iii) указанный CDRH3 содержит аминокислотную последовательность ARDX1YHRYFYDX2 (SEQ ID NO: 5), где X1 представляет собой H и X2 представляет собой V;
(iv) указанный CDRL1 содержит аминокислотную последовательность:
(iv-1) KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой R и X3 представляет собой H;
(iv-2) KSSQSLLX1X2X3X4GX5NX6LA (SEQ ID NO: 38), где X1 представляет собой H, X2 представляет собой A, X3 представляет собой R, X4 представляет собой T, X5 представляет собой K и X6 представляет собой H;
(iv-3) KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой R, X3 представляет собой T, X4 представляет собой H и X5 представляет собой H;
(iv-4) KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой H и X3 представляет собой H;
(iv-5) KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой H и X3 представляет собой K;
(iv-6) KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой H, X3 представляет собой T, X4 представляет собой K и X5 представляет собой H; или
(iv-7) KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой R и X3 представляет собой K;
(v) указанный CDRL2 содержит аминокислотную последовательность WASTRES (SEQ ID NO: 37); и
(vi) указанный CDRL3 содержит аминокислотную последовательность:
(vi-1) KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой H, X2 представляет собой S и X3 представляет собой H;
(vi-2) X1QSX2X3X4RT (SEQ ID NO: 598), где X1 представляет собой H, X2 представляет собой Y, X3 представляет собой S и X4 представляет собой H;
(vi-3) X1QSX2X3X4RT (SEQ ID NO: 598), где X1 представляет собой H, X2 представляет собой H, X3 представляет собой S и X4 представляет собой R;
(vi-4) KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой Y, X2 представляет собой S и X3 представляет собой R;
(vi-5) X1X2SX3X4X5RX6 (SEQ ID NO: 33), где X1 представляет собой K, X2 представляет собой Q, X3 представляет собой Y, X4 представляет собой S, X5 представляет собой R и X6 представляет собой H; или
(vi-6) X1X2SX3X4X5RX6 (SEQ ID NO: 33), где X1 представляет собой K, X2 представляет собой Q, X3 представляет собой Y, X4 представляет собой H, X5 представляет собой R и X6 представляет собой H.
30. Мультиспецифическое антитело или фрагмент антитела по п. 29, где в (vi) указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой H, X2 представляет собой S и X3 представляет собой H.
31. Мультиспецифическое антитело или фрагмент антитела по п. 29 или 30, где
в (i) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47) и
в (ii) указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9).
32. Мультиспецифическое антитело или фрагмент антитела по п. 29, где:
(I) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3 соответственно, содержащиеся в SEQ ID NO: 130, и аминокислотная последовательность указанного CDRL1, указанного CDRL2 и указанного CDRL3 содержит последовательности CDRL1, CDRL2 и CDRL3 соответственно, содержащиеся в SEQ ID NO: 131;
(II) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3 соответственно, содержащиеся в SEQ ID NO: 460, и аминокислотная последовательность указанного CDRL1, указанного CDRL2 и указанного CDRL3 содержит последовательности CDRL1, CDRL2 и CDRL3 соответственно, содержащиеся в SEQ ID NO: 461;
(III) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3 соответственно, содержащиеся в SEQ ID NO: 554, и аминокислотная последовательность указанного CDRL1, указанного CDRL2 и указанного CDRL3 содержит последовательности CDRL1, CDRL2 и CDRL3 соответственно, содержащиеся в SEQ ID NO: 555;
(IV) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3 соответственно, содержащиеся в SEQ ID NO: 450, и аминокислотная последовательность указанного CDRL1, указанного CDRL2 и указанного CDRL3 содержит последовательности CDRL1, CDRL2, и CDRL3 соответственно, содержащиеся в SEQ ID NO: 451;
(V) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3 соответственно, содержащиеся в SEQ ID NO: 440, и аминокислотная последовательность указанного CDRL1, указанного CDRL2 и указанного CDRL3 содержит последовательности CDRL1, CDRL2 и CDRL3 соответственно, содержащиеся в SEQ ID NO: 441;
(VI) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3 соответственно, содержащиеся в SEQ ID NO: 492, и аминокислотная последовательность указанного CDRL1, указанного CDRL2 и указанного CDRL3 содержит последовательности CDRL1, CDRL2 и CDRL3 соответственно, содержащиеся в SEQ ID NO: 493;
(VII) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3 соответственно, содержащиеся в SEQ ID NO: 458, и аминокислотная последовательность указанного CDRL1, указанного CDRL2 и указанного CDRL3 содержит последовательности CDRL1, CDRL2 и CDRL3 соответственно, содержащиеся в SEQ ID NO: 459;
(VIII) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3 соответственно, содержащиеся в SEQ ID NO: 456, и аминокислотная последовательность указанного CDRL1, указанного CDRL2 и указанного CDRL3 содержит последовательности CDRL1, CDRL2 и CDRL3 соответственно, содержащиеся в SEQ ID NO: 457; или
(IX) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3 соответственно, содержащиеся в SEQ ID NO: 528, и аминокислотная последовательность указанного CDRL1, указанного CDRL2 и указанного CDRL3 содержит последовательности CDRL1, CDRL2 и CDRL3 соответственно, содержащиеся в SEQ ID NO: 529.
33. Мультиспецифическое антитело или фрагмент антитела по п. 29, где:
(I) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой R и X3 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой H, X2 представляет собой S и X3 представляет собой H;
(II) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLX1X2X3X4GX5NX6LA (SEQ ID NO: 38), где X1 представляет собой H, X2 представляет собой A, X3 представляет собой R, X4 представляет собой T, X5 представляет собой K и X6 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой H, X2 представляет собой S и X3 представляет собой H;
(III) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой R, X3 представляет собой T, X4 представляет собой H и X5 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой H, X2 представляет собой S и X3 представляет собой H;
(IV) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой H и X3 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность X1QSX2X3X4RT (SEQ ID NO: 598), где X1 представляет собой H, X2 представляет собой Y, X3 представляет собой S и X4 представляет собой H;
(V) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой H и X3 представляет собой K; и
указанный CDRL3 содержит аминокислотную последовательность X1QSX2X3X4RT (SEQ ID NO: 598), где X1 представляет собой H, X2 представляет собой H, X3 представляет собой S и X4 представляет собой R;
(VI) указанный CDRH1, содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой H, X3 представляет собой T, X4 представляет собой K и X5 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой Y, X2 представляет собой S и X3 представляет собой R;
(VII) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой H, X3 представляет собой T, X4 представляет собой K и X5 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность X1X2SX3X4X5RX6 (SEQ ID NO: 33), где X1 представляет собой K, X2 представляет собой Q, X3 представляет собой Y, X4 представляет собой S, X5 представляет собой R и X6 представляет собой H;
(VIII) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой H, X3 представляет собой T, X4 представляет собой K и X5 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность X1X2SX3X4X5RX6 (SEQ ID NO: 33), где X1 представляет собой K, X2 представляет собой Q, X3 представляет собой Y, X4 представляет собой H, X5 представляет собой R и X6 представляет собой H; или
(IX) указанный CDRH1 содержит аминокислотную последовательность YTFX1X2X3X4MH, где X1 представляет собой D, X2 представляет собой D, X3 представляет собой Y и X4 представляет собой A (SEQ ID NO: 29);
указанный CDRH2 содержит аминокислотную последовательность X1IDAGTGX2TX3YSQKFQG (SEQ ID NO: 12), где X1 представляет собой W, X2 представляет собой D, X3 представляет собой K;
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой R и X3 представляет собой K; и
указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой Y, X2 представляет собой S и X3 представляет собой R.
34. Мультиспецифическое антитело или фрагмент антитела по п. 32 или 33, где:
(1) аминокислотная последовательность указанного CDRH1, указанного CDRH2 и указанного CDRH3 содержит последовательности CDRH1, CDRH2 и CDRH3 содержащиеся, соответственно, в SEQ ID NO: 130, и указанный CDRL1, указанный CDRL2 и указанный CDRL3 содержит последовательности CDRL1, CDRL2 и CDRL3 содержащиеся, соответственно, в SEQ ID NO: 131; или
(2) указанный CDRH1 содержит аминокислотную последовательность FNIKDYYMH (SEQ ID NO: 47);
указанный CDRH2 содержит аминокислотную последовательность WIDLENANTIYDAKFQG (SEQ ID NO: 9);
указанный CDRL1 содержит аминокислотную последовательность KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой R и X3 представляет собой H; и
указанный CDRL3 содержит аминокислотную последовательность KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой H, X2 представляет собой S и X3 представляет собой H.
35. Мультиспецифическое антитело или фрагмент антитела по п. 32 или 33, где:
в (I) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 130 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 131;
в (II) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 460 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 461;
в (III) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 554 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 555;
в (IV) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 450 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 451;
в (V) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 440 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 441;
в (VI) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 492 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 493;
в (VII) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 458 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 459;
в (VIII) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 456 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности SEQ ID NO: 457; или
в (IX) аминокислотная последовательность VH имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 528 и аминокислотная последовательность VL имеет по меньшей мере 90% или по меньшей мере 95% идентичности с SEQ ID NO: 529.
36. Мультиспецифическое антитело или фрагмент антитела по п. 32 или 33, где указанные VH и VL содержат аминокислотные последовательности согласно:
в (I) SEQ ID NOS: 130 и 131 соответственно;
в (II) SEQ ID NOS: 460 и 461 соответственно;
в (III) SEQ ID NOS: 554 и 555 соответственно;
в (IV) SEQ ID NOS: 450 и 451 соответственно;
в (V) SEQ ID NOS: 440 и 441 соответственно;
в (VI) SEQ ID NOS: 492 и 493 соответственно;
в (VII) SEQ ID NOS: 458 и 459 соответственно;
в (VIII) SEQ ID NOS: 456 и 457 соответственно; или
в (IX) SEQ ID NOS: 528 и 529 соответственно.
37. Мультиспецифическое антитело или фрагмент антитела по любому из пп. 29-36, где указанные VH и VL содержат аминокислотные последовательности согласно SEQ ID NOS: 130 и 131 соответственно.
38. Мультиспецифическое антитело или фрагмент антитела по любому из пп. 29-37, которое является биспецифическим.
39. Мультиспецифическое антитело или фрагмент антитела по любому из пп. 29-38, которое содержит:
(i) scFv, Fv, Fab, Fab', Fab'-SH, F(ab')2, диатело, scFv2-Fc2 или scFv-IgG;
(ii) (A) тяжелую цепь, содержащую VH и константную область тяжелой цепи (CH), и (B) легкую цепь, содержащую VL и константную область легкой цепи (CL);
(iii) молекулу иммуноглобулина, состоящую из двух тяжелых цепей и двух легких цепей, соединенных между собой дисульфидными мостиками, или мультимер указанной молекулы иммуноглобулина;
(iv) антитело IgG, IgA, IgD, IgE или IgM; или
(v) антитело IgG1, IgG2, IgG3, IgG4, IgA1 или IgA2.
40. Мультиспецифическое антитело или фрагмент антитела по любому из пп. 29-39, где указанный второй антиген представляет собой: целевой антиген онкологического заболевания; целевой антиген иммуноонкологического заболевания; целевой антиген нейродегенеративного заболевания; целевой антиген аутоиммунного нарушения; целевой антиген инфекционного заболевания; целевой антиген метаболического заболевания; целевой антиген когнитивного нарушения; целевой антиген гематоэнцефалического барьера или целевой антиген заболевания крови.
41. Мультиспецифическое антитело или фрагмент антитела по любому из пп. 29-40, где указанный второй антиген выбран из группы, состоящей из 17-IA, 4-1BB, 4Dc, 6-кето-PGFla, 8-изо-PGF2a, 8-оксо-dG, Al-аденозинового рецептора, A33, ACE, ACE-2, активина, активина A, активина AB, активина B, активина C, активина RIA, активина RIA ALK-2, активина RIB ALK-4, активина RIIA, активина RUB, ADAM, ADAM10, ADAM12, ADAM15, ADAM17/T ACE, ADAM8, ADAM9, ADAMTS, ADAMTS4, ADAMTS5, адресинов, aFGF, ALCAM, ALK, ALK-1, ALK-7, альфа-1-антитрипсина, антагониста альфа-V/бета-1, ANG, Ang, APAF-1, APE, APJ, APP, APRIL, AR, ARC, ART, артемина, антиидиотипа, аспарагиновой кислоты, предсердного натрийуретического фактора, интегрина av/b3, Axl, b2M, B7-1, B7-2, B7-H, стимулятора B-лимфоцитов (BlyS), BACE, BACE-1, Bad, BAFF, BAFF-R, Bag-1, BAK, Bax, BCA-1, BCAM, Bel, BCMA, BDNF, b-ECGF, bFGF, BID, Bik, BFM, BLC, BL-CAM, BLK, BMP, BMP-2 BMP-2a, BMP-3-остеогенина, BMP-4 BMP-2b, BMP-5, BMP-6 Vgr-1, BMP-7 (OP-1), BMP-8 (BMP-8a, OP-2), BMPR, BMPR-IA (ALK-3), BMPR-IB (ALK-6), BRK-2, RPK-1, BMPR-II (BRK-3), видов BMP, b-NGF, BOK, бомбезина, костного нейротрофического фактора, BPDE, BPDE-DNA, BTC, фактора комплемента 3 (C3), C3a, C4, C5, C5a, CIO, CA125, CAD-8, кальцитонина, cAMP, раково-эмбрионального антигена (CEA), карциномоассоциированного антигена, катепсина A, катепсина B, катепсина C/DPPI, катепсина D, катепсина E, катепсина H, катепсина L, катепсина O, катепсина S, катепсина V, катепсина X/Z/P, CBL, CCI, CCK2, CCL, CCL1, CCL11, CCL12, CCL13, CCL 14, CCL15, CCL16, CCL1 7, CCL18, CCL19, CCL2, CCL20, CCL21, CCL22, CCL23, CCL24, CCL25, CCL26, CCL27, CCL28, CCL3, CCL4, CCL5, CCL6, CCL7, CCL8, CCL9/10, CCR, CCR1, CCR10, CCR10, CCR2, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CD1, CD2, CD4, CD5, CD6, CD7, CD8, CD10, CDlla, CDllb, CDllc, CD13, CD14, CD15, CD16, CD18, CD19, CD20, CD21, CD22, CD23, CD25, CD27L, CD28, CD29, CD30, CD30L, CD32, CD33 (белки p67), CD34, CD38, CD40, CD40L, CD44, CD45, CD46, CD49a, CD52, CD54, CD55, CD56, CD61, CD64, CD66e, CD74, CD80 (B7-1), CD89, CD95, CD123, CD137, CD138, CD140a, CD146, CD147, CD148, CD152, CD164, CEACAM5, CFTR, cGMP, CINC, токсина Clostridium botulinum, токсина Clostridium perfringens, CKb8-l, CLC, CMV, CMV UL, CNTF, CNTN-1, COX, C-Ret, CRG-2, CT-1, CTACK, CTGF, CTLA-4, CX3CL1, CX3CR1, CXCL, CXCL1, CXCL2, CXCL3, CXCL4, CXCL5, CXCL6, CXCL7, CXCL8, CXCL9, CXCL10, CXCL11, CXCL12, CXCL13, CXCL14, CXCL15, CXCL16, CXCR, CXCR1, CXCR2, CXCR3, CXCR4, CXCR5, CXCR6, цитокератинового опухолеассоциированного антигена, DAN, DCC, DcR3, DC-SIGN, фактора ускорения распада, des(l-3)-IGF-I (IGF-1 головного мозга), Dhh, дигоксина, DNAM-1, ДНКазы, Dpp, DPPIV/CD26, Dtk, ECAD, EDA, EDA-A1, EDA-A2, EDAR, EGF, EGFR (ErbB-1), EMA, EMMPRIN, EN A, рецептора эндотелина, энкефалиназы, eNOS, Eot, эотаксина-1, EpCAM, эфрина B2/ EphB4, EPO, ERCC, E-селектина, ET-1, фактора Ila, фактора VII, фактора VIIIc, фактора IX, белка активации фибробластов (FAP), Fas, FcRl, FEN-1, ферритина, FGF, FGF-19, FGF-2, FGF3, FGF-8, FGFR, FGFR-3, фибрина, FL, FLIP, Flt-3, Flt-4, фолликулостимулирующего гормона, фракталкина, FZD1, FZD2, FZD3, FZD4, FZD5, FZD6, FZD7, FZD8, FZD9, FZD10, G250, Gas 6, GCP-2, GCSF, GD2, GD3, GDF, GDF-1, GDF-3 (Vgr-2), GDF-5 (BMP-14, CDMP- 1), GDF-6 (BMP-13, CDMP-2), GDF-7 (BMP-12, CDMP-3), GDF-8 (миостатин), GDF-9, GDF- 15 (MIC-1), GDNF, GFAP, GFRa-1, GFR-альфа-1, GFR-альфа-2, GFR-альфа-3, GITR, глюкагона, Glut 4, гликопротеина Ilb/IIIa (GP Ilb/IIIa), GM-CSF, gpl30, gp72, GRO, рилизинг-фактора гормона роста, гаптена (NP-cap или NIP-cap), HB-EGF, HCC, гликопротеина gB оболочки HCMV, гликопротеина gH оболочки HCMV, HCMV UL, гемопоэтического фактора роста (HGF), Hep B gpl20, гепараназы, Her2, Her2/neu (ErbB-2), Her3 (ErbB-3), Her4 (ErbB-4), гликопротеина gB вируса простого герпеса (HSV), гликопротеина gD HSV, HGFA, высокомолекулярного меланомоассоциированного антигена (HMW-MAA), gpl20 ВИЧ, V3-петли gp 120 ВИЧ IIIB, HLA, HLA-DR, HM1.24, HMFG PEM, HRG, Hrk, сердечного миозина человека, цитомегаловируса (HCMV) человека, гормона роста человека (HGH), HVEM, 1-309, IAP, ICAM, ICAM-1, ICAM-3, ICE, ICOS, IFNg, Ig, рецептора IgA, IgE, IGF, IGF-связывающих белков, IGF-1R, IGFBP, IGF-I, IGF-II, IL, IL-1, IL-1R, IL-2, IL-2R, IL-4, IL-4R, IL-5, IL-5R, IL-6, IL-6R, IL-8, IL- 9, IL-10, IL-12, IL-13, IL-15, IL-18, IL-18R, IL-23, интерферона (INF)-альфа, INF-бета, INF-гамма, ингибина, iNOS, A-цепи инсулина, B-цепи инсулина, инсулиноподобного фактора роста 1, интегрина-альфа-2, интегрина-альфа-3, интегрина-альфа-4, интегрина-альфа-4/бета-1, интегрина-альфа-4/бета-7, интегрина-альфа-5 (альфа-V), интегрина-альфа-5/бета-1, интегрина-альфа-5/бета-3, интегрина-альфа-6, интегрина-бета-1, интегрина-бета-2, интерферона-гамма, IP-10, 1-TAC, JE, калликреина 2, калликреина 5, калликреина 6, калликреина 11, калликреина 12, калликреина 14, калликреина 15, калликреина L1, калликреина L2, калликреина L3, калликреина L4, KC, KDR, фактора роста кератиноцитов (KGF), ламинина 5, LAMP, LAP, LAP (TGF-1), латентного TGF-1, латентного TGF-1 bpl, LBP, LDGF, LECT2, Lefty, антигена Льюиса Y, антигена, родственного антигену Льюиса Y, LFA-1, LFA-3, Lfo, LIF, LIGHT, липопротеинов, LIX, LKN, Lptn, L-селектина, LT-a, LT-b, LTB4, LTBP-1, легочного сурфактанта, лютеинизирующего гормона, рецептора лимфотоксина-бета, Mac-1, MAdCAM, MAG, MAP2, MARC, MCAM, MCAM, MCK-2, MCP, M-CSF, MDC, Mer, металлопротеазы, рецептора MGDF, MGMT, MHC (HLA-DR), MIF, MIG, MIP, MIP-1-альфа, MK, MMAC1, MMP, MMP-1, MMP-10, MMP-11, MMP-12, MMP-13, MMP-14, MMP-15, MMP-2, MMP-24, MMP-3, MMP-7, MMP-8, MMP-9, MPIF, Mpo, MSK, MSP, муцина (Mucl), MUC18, ингибирующего вещества Мюллера, Mug, MuSK, NAIP, NAP, NCAD, N-кадгерина, NCA 90, NCAM, NCAM, неприлизина, нейротрофина-3, -4 или -6, нейротурина, фактора роста нейронов (NGF), NGFR, NGF-бета, nNOS, NO, NOS, Npn, NRG-3, NT, NTN, OB, OGG1, OPG, OPN, OSM, OX40L, OX40R, pl50, p95, PADPr, паратиреоидного гормона, PARC, PARP, PBR, PBSF, PCAD, P-кадгерина, PCNA, PDGF, PDGF, PDK-1, PECAM, PEM, PF4, PGE, PGF, PGI2, PGJ2, PIN, PLA2, плацентарной щелочной фосфатазы (PLAP), PIGF, PLP, PP14, проинсулина, прорелаксина, белка C, PS, PSA, PSCA, простатического специфического мембранного антигена (PSMA), PTEN, PTHrp, Ptk, PTN, R51, RANK, RANKL, RANTES, A-цепи релаксина, B-цепи релаксина, ренина, F респираторно-синцитиального вируса (RSV), RSV Fgp, Ret, ревматоидных факторов, RLIP76, RPA2, RSK, S100, SCF/KL, SDF-1, серина, сывороточного альбумина, sFRP-3, Shh, SIGIRR, SK-1, SLAM, SLPI, SMAC, SMDF, SMOH, SOD, SPARC, Stat, STEAP, STEAP-II, TACE, TACI, TAG-72 (опухолеассоциированный гликопротеин-72), TARC, TCA-3, T-клеточных рецепторов (например, T-клеточного рецептора альфа/бета), TdT, TECK, TEM1, TEM5, TEM7, TEM8, TERT, PLAP-подобной щелочной фосфатазы семенников, TfR, TGF, TGF-альфа, TGF-бета, панспецифического TGF-бета, TGF-бета RI (ALK-5), TGF-бета RII, TGF-бета Rllb, TGF-бета RIII, TGF-бета 1, TGF-бета 2, TGF-бета 3, TGF-бета 4, TGF-бета 5, тромбина, тимусного Ck-1, тиреостимулирующего гормона, Tie, TIMP, TIQ, тканевого фактора, TMEFF2, Tmpo, TMPRSS2, TNF, TNF-альфа, TNF-альфа/бета, TNF-бета 2, TNFc, TNF-RI, TNF-RII, TNFRSF10A (TRAIL Rl Apo-2, DR4), TNFRSFIOB (TRAIL R2 DR5, KILLER, TRICK-2A, TRICK-B), TNFRSF10C (TRAIL R3 DcRl, LIT, TRID), TNFRSF10D (TRAIL R4 DcR2, TRUNDD), TNFRSF11A (RANK ODF R, TRANCE R), TNFRSFllB (OPG OCIF, TR1), TNFRSF12 (TWEAK R FN14), TNFRSF13B (TACI), TNFRSF13C (BAFF R), TNFRSF14 (HVEM ATAR, HveA, LIGHT R, TR2), TNFRSF16 (NGFR p75NTR), TNFRSF17 (BCMA), TNFRSF 18 (GITR AITR), TNFRSF19 (TROY TAJ, TRADE), TNFRSF19L (RELT), TNFRSFIA (TNF RI CD120a, p55-60), TNFRSFIB (TNF RII CD120b, p75-80), TNFRSF26 (TNFRH3), TNFRSF3 (LTbR TNF RIII, TNFC R), TNFRSF4 (OX40 ACT35, TXGP1 R), TNFRSF 5 (CD40 p50), TNFRSF6 (Fas Apo-1, APT1, CD95), TNFRSF6B (DcR3 M68, TR6), TNFRSF7 (CD27), TNFRSF8 (CD30), TNFRSF9 (4-1BB CD137, ILA), TNFRSF21 (DR6), TNFRSF22 (DcTRAIL R2 TNFRH2), TNFRST23 (DcTRAIL Rl TNFRH1), TNFRSF25 (DR3 Apo-3, LARD, TR-3, TRAMP, WSL-1), TNFSF10 (TRAIL, лиганд Apo-2, TL2), TNFSF11 (TRANCE/RANK, лиганд ODF, лиганд OPG), TNFSF12 (TWEAK лиганд-Apo-3, лиганд DR3), TNFSF13 (APRIL TALL2), TNFSF13B (BAFF BLYS, TALL1, THANK, TNFSF20), TNFSF14 (LIGHT, лиганд HVEM, LTg), TNFSF15 (TLIA/VEGI), TNFSF18 (лиганд GITR, лиганд AITR, TL6), TNFSFIA (конектин TNF-a, DIF, TNFSF2), TNFSF1B (TNF-b, LTa, TNFSF1), TNFSF3 (LTb, TNFC, p33), TNFSF4 (лиганд OX40, gp34, TXGP1), TNFSF5 (лиганд CD40, CD154, gp39, HIGM1, IMD3, TRAP), TNFSF6 (лиганд Fas, лиганд Apo-1, лиганд APT1), TNFSF7 (лиганд CD27 CD70), TNFSF8 (лиганд CD30 CD153), TNFSF9 (лиганд 4-1BB, лиганд CD137), TP-1, t-PA, Tpo, TRAIL, TRAIL R, TRAIL-R1, TRAIL-R2, TRANCE, рецептора трансферрина, TRF, Trk, TROP-2, TSG, TSLP, опухолеассоциированного антигена CA 125, опухолеассоциированного антигена, характеризующегося экспрессией углеводного антигена, родственного антигену Льюиса Y, TWEAK, TXB2, Ung, uPAR, uPAR-1, урокиназы, VCAM, VCAM-1, VECAD, VE-кадгерина, VE-кадгерина-2, VEFGR-1 (flt-1), VEGF, VEGFR, VEGFR-3 (flt-4), VEGI, VFM, вирусных антигенов, VLA, VLA-1, VLA-4, интегрина VNR, факторов фон Виллебранда, WIF- 1, WNT1, WNT2, WNT2B/13, WNT3, WNT3A, WNT4, WNT5A, WNT5B, WNT6, WNT7A, WNT7B, WNT8A, WNT8B, WNT9A, WNT9A, WNT9B, WNT10A, WNT10B, WNT11, WNT16, XCL1, XCL2, XCR1, XCR1, XEDAR, XIAP, XPD, CTLA4 (антиген-4 цитотоксических T-лимфоцитов), PD1 (белок-1 запрограммированной гибели клеток), PD-L1 (лиганд-1 белка запрограммированной гибели клеток), LAG-3 (ген-3 активации лимфоцитов), TIM-3 (белок-3, содержащий домены T-клеточного иммуноглобулина и муцина), рецепторов гормонов и факторов роста.
42. Мультиспецифическое антитело или фрагмент антитела по любому из пп. 29-41, где указанный второй антиген выбран из группы, состоящей из BCMA, CTLA4 (антиген-4 цитотоксических T-лимфоцитов), PD1 (белок-1 запрограммированной гибели клеток), PD-L1 (лиганд-1 белка запрограммированной гибели клеток), LAG-3 (ген-3 активации лимфоцитов), TIM-3, CD20, CD2, CD19, Her2, EGFR, EpCAM, FcyRIIIa (CD16), FcyRIIa (CD32a), FcyRIIb (CD32b), FcyRI (CD64), Toll-подобных рецепторов (TLR), TLR4, TLR9, цитокинов, IL-2, IL-5, IL-13, IL-6, IL-17, IL-12, IL-23, TNFa, TGFb, цитокиновых рецепторов, IL-2R, хемокинов, хемокиновых рецепторов, факторов роста, VEGF и HGF.
43. Мультиспецифическое антитело или фрагмент антитела по любому из пп. 29-42, которые содержат константный домен IgG.
44. Мультиспецифическое антитело или фрагмент антитела по любому из пп. 29-43, где указанное антитело предусматривает мультиспецифический формат, выбранный из группы, состоящей из Fab-Fc-scFv, «открывалки для бутылок», Mab-scFv, Mab-Fv, двойного scFv, центрального Fv, центрального scFv, одноплечевого центрального scFv, Fab-Fab, Fab-Fv, mAb-Fv, mAb-Fab, DART, BiTE, IgG с универсальной легкой цепью, TandAb, Cross-Mab, SEED, BEAT, TrioMab и DuetMab.
45. Выделенная или рекомбинантная нуклеиновая кислота, кодирующая мультиспецифическое антитело или фрагмент антитела по любому из пп. 29-44, содержащая:
(1) первую последовательность нуклеиновой кислоты, кодирующую первый антигенсвязывающий домен, который специфически связывается с CD3; и
(2) вторую последовательность нуклеиновой кислоты, кодирующую второй антигенсвязывающий домен, который специфически связывается со вторым антигеном, отличным от CD3,
где первый антигенсвязывающий домен содержит:
(A) указанный VH содержащий указанный CDRH1, указанный CDRH2 и указанный CDRH3; и
(B) указанный VL содержит указанный CDRL1, указанный CDRL2 и указанный CDRL3,
где:
(i) указанный CDRH1 содержит аминокислотную последовательность:
(i-1) FNIKDYYMH (SEQ ID NO: 47); или
(i-2) YTFX1X2X3X4MH (SEQ ID NO: 29), где X1 представляет собой D, X2 представляет собой D, X3 представляет собой Y и X4 представляет собой A;
(ii) указанный CDRH2 содержит аминокислотную последовательность:
(ii-1) WIDLENANTIYDAKFQG (SEQ ID NO: 9); или
(ii-2) X1IDAGTGX2TX3YSQKFQG (SEQ ID NO: 12), где X1 представляет собой W, X2 представляет собой D, X3 представляет собой K;
(iii) указанный CDRH3 содержит аминокислотную последовательность ARDX1YHRYFYDX2 (SEQ ID NO: 5), где X1 представляет собой H и X2 представляет собой V;
(iv) указанный CDRL1 содержит аминокислотную последовательность:
(iv-1) KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой R и X3 представляет собой H;
(iv-2) KSSQSLLX1X2X3X4GX5NX6LA (SEQ ID NO: 38), где X1 представляет собой H, X2 представляет собой A, X3 представляет собой R, X4 представляет собой T, X5 представляет собой K и X6 представляет собой H;
(iv-3) KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой R, X3 представляет собой T, X4 представляет собой H и X5 представляет собой H;
(iv-4) KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой H и X3 представляет собой H;
(iv-5) KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой H и X3 представляет собой K;
(iv-6) KSSQSLLNX1X2X3GX4NX5LA (SEQ ID NO: 42), где X1 представляет собой A, X2 представляет собой H, X3 представляет собой T, X4 представляет собой K и X5 представляет собой H; или
(iv-7) KSSQSLLNX1X2TGX3NYLA (SEQ ID NO: 594), где X1 представляет собой A, X2 представляет собой R, X3 представляет собой K;
(v) указанный CDRL2 содержит аминокислотную последовательность WASTRES (SEQ ID NO: 37); и
(vi) указанный CDRL3 содержит аминокислотную последовательность:
(vi-1) KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой H, X2 представляет собой S и X3 представляет собой H;
(vi-2) X1QSX2X3X4RT (SEQ ID NO: 598), где X1 представляет собой H, X2 представляет собой Y, X3 представляет собой S и X4 представляет собой H;
(vi-3) X1QSX2X3X4RT (SEQ ID NO: 598), где X1 представляет собой H, X2 представляет собой H, X3 представляет собой S и X4 представляет собой R;
(vi-4) KQSX1X2X3RT (SEQ ID NO: 36), где X1 представляет собой Y, X2 представляет собой S и X3 представляет собой R;
(vi-5) X1X2SX3X4X5RX6 (SEQ ID NO: 33), где X1 представляет собой K, X2 представляет собой Q, X3 представляет собой Y, X4 представляет собой S, X5 представляет собой R и X6 представляет собой H; или
(vi-6) X1X2SX3X4X5RX6 (SEQ ID NO: 33), где X1 представляет собой K, X2 представляет собой Q, X3 представляет собой Y, X4 представляет собой H, X5 представляет собой R и X6 представляет собой H.
46. Вектор экспрессии, содержащий выделенную или рекомбинантную нуклеиновую кислоту по п. 45.
47. Клетка-хозяин для экспрессии мультиспецифического антитела или фрагмента антитела по любому из пп. 29-44, которая трансфицирована, трансформирована или трансдуцирована нуклеиновой кислотой по п. 45.
48. Клетка-хозяин для экспрессии мультиспецифического антитела или фрагмента антитела по любому из пп. 29-44, которая трансфицирована, трансформирована или трансдуцирована вектором экспрессии по п. 46.
49. Клетка-хозяин по п. 47 или 48, которая представляет собой эукариотическую клетку.
50. Клетка-хозяин по п. 47 или 48, которая представляет собой клетку млекопитающих или клетку дрожжей.
51. Клетка-хозяин по п. 47 или 48, которая представляет собой клетку яичника китайского хомячка (CHO), клетку эмбриональной почки человека (HEK) или лимфоидную клетку.
52. Клетка-хозяин по п. 47 или 48, которая представляет собой прокариотическую клетку.
53. Клетка-хозяин по п. 47 или 48, которая представляет собой бактериальную клетку.
54. Фармацевтическая композиция для усиления иммунной функции, содержащая мультиспецифическое антитело или фрагмент антитела по любому из пп. 29-44 или клетку-хозяина по любому из пп. 45-53 и фармацевтически приемлемый носитель и/или вспомогательное вещество.
55. Способ лечения нарушения у млекопитающего, нуждающегося в таком лечении, где нарушение включает пролиферативное нарушение, онкологическое нарушение, иммуноонкологическое нарушение, неврологическое нарушение, нейродегенеративное нарушение или аутоиммунное нарушение, где способ включает введение эффективного количества по меньшей мере одного анти-CD3 антитела или антигенсвязывающего фрагмента по любому из пп. 1-18, или мультиспецифического антитела или фрагмента антитела по любому из пп. 29-44, или клетки-хозяина по любому из пп. 21-27 или 47-53.
56. Способ по п. 55, где клетка хозяин представляет собой иммунную клетку.
57. Способ по п. 56, где иммунная клетка представляет собой Т- или NK-клетку.
58. Способ по любому из пп. 55-57, где способ дополнительно включает введение млекопитающему дополнительного терапевтического средства.
59. Способ по любому из пп. 55-58, где млекопитающее является человеком.
| WO 2018208864 A1, 15.11.2018 | |||
| RU 2020138026 А, 21.05.2019 | |||
| WO 2016116626 А1, 28.07.2016. |
Авторы
Даты
2024-12-18—Публикация
2020-06-08—Подача