Область техники
Изобретение относится к биотехнологии и биохимии, а именно моноклональному тяжелоцепочечному антителу верблюдовых, специфически связывающемуся с белком Spike вируса SARS-CoV-2.
Уровень техники
Вирус SARS-Cov-2 является возбудителем острой респираторной инфекции COVID-19, заболевания, в отдельных случаях характеризующегося тяжелым течением и развитием обширного поражения легочного эпителия. Для специфической противовирусной терапии COVID-19 могут применяться препараты на основе антител, нейтрализующих вирус SARS-Cov-2. Нейтрализующие антитела способны специфически и с высокой степенью сродства связываться с участком RBD шиповидного (S) белка вируса SARS-Cov-2 и препятствовать взаимодействию шиповидного белка и рецептора ACE2, расположенного на поверхности эпителиальных клеток, за счет чего происходит блокирование возможности проникновения вируса в клетку. Антитела, связывающиеся с другими областями шиповидного белка SARS-Cov-2, не обладают нейтрализующей активностью, но могут быть использованы для иммунодиагностики SARS-Cov-2 при помощи иммуноферментного анализа. Антитела к шиповидному белку SARS-Cov-2 могут иметь различную структуру: это могут быть антитела вида IgA, IgD, IgE, IgG или IgM, полученные из различных видов животных или человека, за связывание с шиповидным белком в составе таких белковых молекул ответственны участки VH и VL тяжелых и легких цепей; либо фрагменты указанных антител, такие как Fab, представляющие собой спаренные участки VH-CH1 и VL-CH1, либо ScFv, представляющие собой единую полипептидную цепь, содержащую участки VH и VL, соединенные гибким полипептидным линкером, либо тяжелоцепочечные антитела или их фрагменты. Последние представляют собой антитела особой структуры, лишенные легких цепей, которые встречаются в организме животных семейства верблюдовые. За связывание с белком-мишенью в составе таких антител отвечает единственный домен VHH, который эволюционно приспособлен к функционированию без вариабельного домена легкой цепи. Домен VHH обладает более протяженными участками связывания антигена CDR1 и CDR3, а также каркасными областями, имеющими ряд гидрофильных замен, что обеспечивает таким антителам хорошие физико-химические свойства и способность связываться с антигенами со сродством и специфичностью, сравнимыми или превосходящими таковые у антител традиционной структуры. Домен VHH тяжелоцепочечного антитела, называемый также нанотелом, обладает наименьшим размером среди всех фрагментов антител, способных специфически распознавать мишени (`15 кДа по сравнению с ~35 кДа для фрагментов ScFv), высокой стабильностью и хорошей тканевой проникающей способностью.
Известны различные антитела традиционной структуры, способные специфически связываться с доменом RBD вируса SARS-Cov-2 и обладающие нейтрализующей активностью. Известно моноклональное антитело к RBD фрагменту в составе S белка вируса SARS-CoV-2 [Патентная заявка РФ № 2020138183, МПК C12N 1/00 (2006.01), опубл. 2020.11.20]. Описан также изолированный фрагмент ДНК, кодирующий участки легкой и тяжелой цепи указанного антитела, и антигенсвязывающий фрагмент указанного моноклонального антитела. Специфичность моноклонального антитела к RBD фрагменту в составе S белка вируса SARS-CoV-2 подтверждена методами иммуноферментного анализа, иммуноблоттинга, иммуноцитохимического и иммуногистохимического окрашивания. Установлена нуклеотидная последовательность вариабельных доменов моноклонального антитела. Изобретение позволяет получить новые моноклональные антитела, селективно связывающие RBD фрагмент в составе S белка вируса SARS-CoV-2. Указанное моноклональное антитело обладает традиционной структурой, и для него не описана возможность использования в виде фрагмента ScFv, кроме того, для производства такого антитела необходимо использовать исключительно эукариотические экспрессионные системы.
Известны наноантитела и их фрагменты, обладающие способностью связываться с доменом RBD шиповидного белка SARS-CoV-2, либо другими областями шиповидного белка, в том числе, обладающие нейтрализующей активностью в отношении SARS-CoV-2. В качестве примера рассмотрена заявка (CN, 112010967B, МПК C07K 16/10, A61P 11/00, A61P 31/14, G01N 33/56983, A61K 2039/505, C07K 2317/565, C07K 2317/567, C07K 2317/569, C07K 2317/76, G01N 2333/165, опубл. 2020.12.01), раскрывающая новое наноантитело, обладающее нейтрализующей активностью в отношении коронавируса SARS-CoV-2, метод его приготовления и применения. Наноантитело обладает малым молекулярным весом, высоким сродством к SARS-CoV-2 и низкой стоимостью производства. В изобретении раскрыты последовательности CDR1, CDR2 и CDR3, обеспечивающие распознавание эпитопов в составе домена RBD шиповидного белка SARS-CoV-2. Указанное наноантитело отличается от наноантитела, описанного в настоящей заявке последовательностями CDR1, CDR2 и CDR3 и распознаваемыми эпитопами в составе шиповидного белка SARS-CoV-2. Подобное относится и к другим известным наноантителам к шиповидному белку SARS-CoV-2.
Известна генетическая конструкция для экспрессии рекомбинантного белка RBD вируса SARS-CoV-2, штамм клеток яичника китайского хомячка CHO-S-RBD, продуцирующего рекомбинантный белок - рецептор-связывающий домен (RBD) вируса SARS-CoV-2, который может быть использован для диагностических целей [Патент РФ №2723008, C07K 14/165, опубл. 08.06.2020]. Описан так же способ получения штамма клеток яичника китайского хомячка CHO-S-RBD продуцента рекомбинантного белка RBD вируса SARS-CoV-2, содержащий определенную генетическую конструкцию, введение указанной генетической конструкции в клетки путем липофекции; селекцию клеток на антибиотике Hygromycin B. Раскрыта информация о штамме клеток яичника китайского хомячка CHO-S-RBD, продуценте рекомбинантного белка RBD вируса SARS-CoV-2. Описаны способы получения рекомбинантного белка RBD вируса SARS-CoV-2 включающие: культивирование штамма клеток яичника китайского хомячка CHO-S-RBD; хроматографическую очистку рекомбинантного белка RBD вируса SARS-CoV-2 из культуральной среды штамма клеток яичника китайского хомячка CHO-S-RBD; подтверждение получения рекомбинантного белка RBD вируса SARS-CoV-2. Создан рекомбинантный белок RBD вируса SARS-CoV-2 для выявления антител к SARS-CoV-2. Создана тест-система для иммуноферментного анализа сыворотки или плазмы крови человека. Разработан способ для анализа сыворотки или плазмы крови реконвалесцентов COVID-19 для отбора образцов наиболее перспективных для терапии пациентов, инфицированных SARS-CoV-2. Разработан способ анализа сыворотки или плазмы крови человека для определения титра антител к вирусу SARS-CoV-2. Изобретение предоставляет быструю и эффективную тест-систему для определения наиболее перспективных образцов сыворотки или плазмы крови реконвалесцентов COVID-19 для терапии пациентов, инфицированных SARS-CoV-2. Изобретение позволяет сократить время и упростить процедуру анализа сыворотки или плазмы крови реконвалесцентов COVID-19 для отбора образцов наиболее перспективных для терапии пациентов, инфицированных SARS-CoV-2. Перечисленные технические решения не используют антитела или их фрагменты, нацеленные на шиповидный белок SARS-CoV-2.
Краткое описание изобретения
Задачи, решаемые с помощью настоящего изобретения
Целью настоящего изобретения является получение однодоменного антитела или его фрагмента к шиповидному белку вируса SARS-CoV-2, которые могут обладать нейтрализующей активностью в отношении вируса SARS-CoV-2 за счет связывания с шиповидным белком и предотвращения его взаимодействия с клеточным рецептором ACE2, а также фармацевтической композиции, содержащей их в качестве активного ингредиента.
Средства для решения задач
В результате проведенных исследовательских работ авторами были получены однодоменные антитела, способные селективно связываться с шиповидным белком вируса SARS-CoV-2. Для полученных наноантител были определены последовательности участков CDR и определена способность блокировать взаимодействие между вирусным шиповидным белком и клеточным рецептором ACE2.
Согласно одному варианту осуществления, изобретение относится к следующему.
Тяжелоцепочечное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с S-белком вируса SARS-CoV-2, содержащее области определения комплементарности (CDR),
где антитело выбрано из группы, состоящей из:
(1) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:1,
CDR2 с последовательностью SEQ ID NO:12, и
CDR3 с последовательностью SEQ ID NO:23;
(2) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:2,
CDR2 с последовательностью SEQ ID NO:13, и
CDR3 с последовательностью SEQ ID NO:24;
(3) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:3,
CDR2 с последовательностью SEQ ID NO:14, и
CDR3 с последовательностью SEQ ID NO:25;
(4) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:4,
CDR2 с последовательностью SEQ ID NO:15, и
CDR3 с последовательностью SEQ ID NO:26;
(5) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:5,
CDR2 с последовательностью SEQ ID NO:16, и
CDR3 с последовательностью SEQ ID NO:27;
(6) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:6,
CDR2 с последовательностью SEQ ID NO:17, и
CDR3 с последовательностью SEQ ID NO:28;
(7) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:7,
CDR2 с последовательностью SEQ ID NO:18, и
CDR3 с последовательностью SEQ ID NO:29;
(8) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:8,
CDR2 с последовательностью SEQ ID NO:19, и
CDR3 с последовательностью SEQ ID NO:30;
(9) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:9,
CDR2 с последовательностью SEQ ID NO:20, и
CDR3 с последовательностью SEQ ID NO:31;
(10) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:10,
CDR2 с последовательностью SEQ ID NO:21, и
CDR3 с последовательностью SEQ ID NO:32;
(11) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:11,
CDR2 с последовательностью SEQ ID NO:22, и
CDR3 с последовательностью SEQ ID NO:33;
2. Антитело или антигенсвязывающий фрагмент по п.1, которое ингибирует связывание S-белка вируса SARS-CoV-2 и клеточного рецептора ACE2.
3. Антитело или антигенсвязывающий фрагмент по п.1, которое представляет собой IgA, IgD, IgE, IgG или IgM; моноклональное антитело или поликлональное антитело
Осуществление изобретения
Описанные в документе антитела могут относиться к молекулам иммуноглобулинов, которые способны специфически связываться с определенной мишенью, в частности, остатками сахаров в составе полипептидов, полипептидами или белками при помощи как минимум одного сайта распознавания антигена, который расположен в вариабельном участке иммуноглобулиновой молекулы. Антитела могут являться моноклональными или олигоклональными.
Антитела могут относиться к тяжелоцепочечным иммуноглобулинам верблюдовых, состоящим из гомодимеров особых тяжелых цепей иммуноглобулинов, в которых отсутствуют константные домены CH1, а вариабельные домены содержат более протяженные участки CDR1 и CDR3.
Антитела могут принадлежать к различным классам иммуноглобулинов, в частности, IgA, IgM, IgG или любому их подклассу. Разделение иммуноглобулинов на различные классы производят основываясь на особенностях аминокислотной последовательности константных участков тяжелых цепей антитела.
Антитела к шиповидному белку вируса SARS-CoV-2 могут представлять собой тяжелоцепочечные антитела IgG, в частности, IgG1 или IgG2, или иной подкласс IgG. Кроме того, антитела к шиповидному белку либо их антигенсвязывающие фрагменты могут быть представлены в виде мономеров, либо мультимеров, в том числе, гетеромультимеров.
Антигенсвязывающие фрагменты тяжелоцепочечных антител, описанных в данном документе, также называемые наноантителами, является функциональным и структурным компонентом антитела и обеспечивает способность связывания с антигеном как в составе полноразмерного антитела, так и в виде отдельного белка. Антигенсвязывающий фрагмент может быть получен как в результате протеолитического расщепления полноразмерного антитела, так и путем экспрессии его последовательности в гетерологической экспрессионной системе, в клетках прокариот (например, e. coli), или эукариот (например, в клеточных линиях HEK-293 либо CHO).
Термин "специфически связывается" является термином, хорошо известным специалистам в данной области, и способы определения специфического связывания антител с антигеном или конкретным эпитопом в его составе хорошо известны. Например, следует учитывать, что антитело или его антигенсвязывающий фрагмент, которые специфически связываются с одним эпитопом в составе шиповидного белка SARS-CoV-2, могут связываться с указанным эпитопом в составе шиповидного белка SARS-CoV-2 с более высокой аффинностью и активностью связывания, быстрее и/или с большей продолжительностью, чем с другим эпитопом или отличными от эпитопа сайтами. Однако антитело или его антигенсвязывающий фрагмент, которые специфически связываются с первой мишенью, не исключаются из специфического связывания со второй мишенью.
Моноклональное антитело означает препарат молекул антител, в котором отдельные молекулы антител являются идентичными, за исключением присутствия небольшого количества мутантных вариантов. Моноклональные антитела нацелены на один эпитоп и являются высокоспецифическими. Кроме того, в отличии от поликлональных антител, которые нацеливается на разные антигены или разные эпитопы, каждое моноклональное антитело нацеливается на один эпитоп антигена. Определение "моноклональное" указывает на свойство антитела, и оно не должно истолковываться как ограниченное необходимостью получения антител конкретным способом.
Антитело к шиповидному белку SARS-CoV-2 в соответствии с настоящим изобретением или его антигенсвязывающий фрагмент могут быть дополнительно модифицированы в соответствии с общими техническими принципами, хорошо известными специалистам в данной области, с помощью различных способов модификации отдельно или в комбинации.
Пример 1. Получение наноантител к шиповидному белку SARS-CoV-2
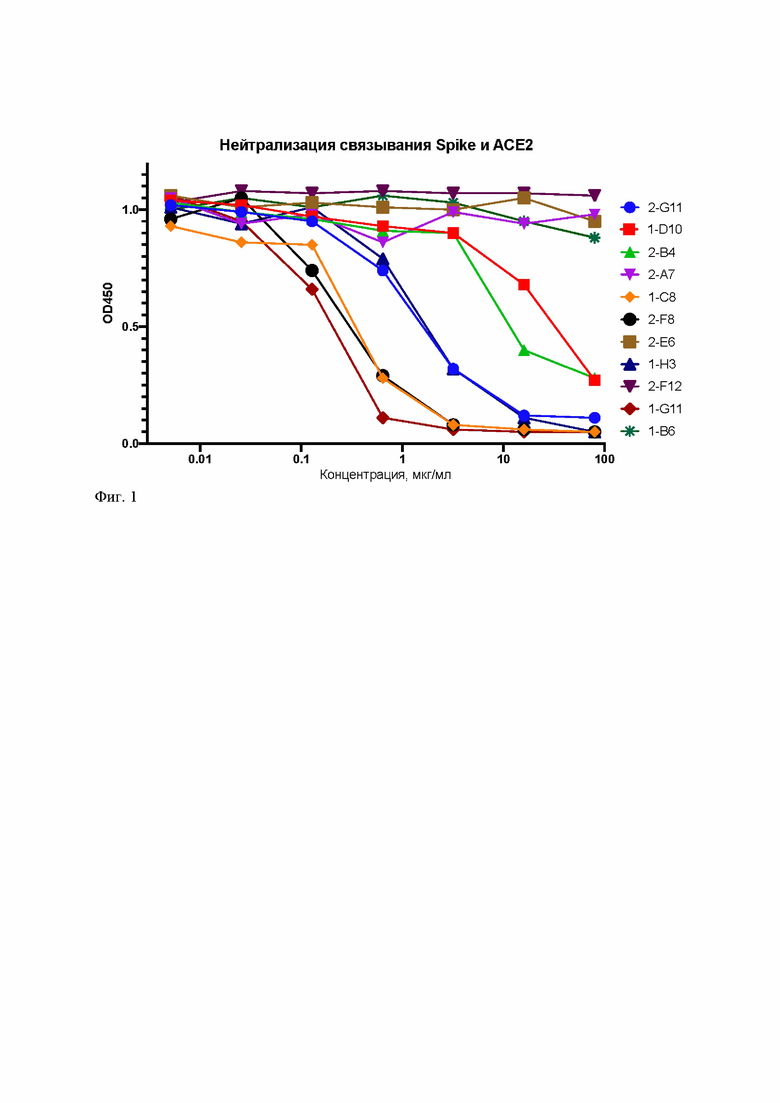
Животное семейства верблюдовые (альпака) было подвергнуто троекратной иммунизации рекомбинантным тримерным шиповидным белком SARS-CoV-2, который был предварительно наработан в эукариотической экспрессионной системе. Для первичной иммунизации использовали 350 мкг шиповидного белка, растворенного в 500 мкл фосфатно-солевого буфера, смешанные с 500 мкл полного адьюванта Фрейнда. Иммунизацию производили серией подкожных и внутримышечных инъекций в область кожной складки правой передней ноги. Для повторных иммунизаций использовали по 250 мкг шиповидного белка, растворенного в 500 мкл фосфатно-солевого буфера, смешанные с 500 мкл неполного адьюванта Фрейнда, способом, аналогичным указанному выше. Иммунизации производили с интервалом в 3 недели. Через 5 дней после третьей иммунизации, у животного забирали 100 мл периферической крови венозной пункцией, из цельной крови проводили выделение фракции мононуклеарных клеток. К выделенной фракции добавляли 50 мкг биотинилированного шиповидного белка и проводили иммуномагнитную сепарацию связавшихся с шиповидным белком клеток, экспрессирующих специфичные к нему В-клеточные рецепторы, после чего из выделенной клеточной фракции экстрагировали тотальную клеточную РНК. Из препаратов РНК получали кДНК в реакции обратной транскрипции с праймером CGCCATCAAGGTACCAGTTGA, полученный образец кДНК использовали для амплификации специфических последовательностей, кодирующих участки VHH тяжелоцепочечных антител с праймерами GAACAGACCACCATGTCTAGASARKTGCRRSTSGTRGAGWCYGKGGGRGG, GATCGGATCCGGTTGTGGTTTTGGTGTCTTGGG и GATCGGATCCGGGGGGTCTTCGCTGTGGTGCG. Наработку кодирующих последовательностей проводили в реакции ПЦР с последующим электрофоретическим разделением продуктов реакции и выделением специфического продукта длиной 300-500 п.н. при помощи твердофазной экстракции. Затем препарат подвергали рестрикции при помощи эндонуклеаз XbaI и BamHI и лигировали в фагмиду pHEN2-XB. Лигазную смесь электропорировали в электрокомпетентные клетки штамма TG-1, которые затем высеивали на 25-см чашки с LB-агаром и карбенициллином в концентрации 100 мг/мл. Выросшие колонии объединяли и использовали бактериальную культуру для получения фаговых библиотек путем инфекции экспоненциально растущей в жидкой среде бактериальной культуры бактериофагом M13KO7. Полученные препараты фаговых библиотек преципитировали в присутствии PEG/NaCl и концентрировали, после чего проводили определение инфекционного титра предельными разведениями. Для проведения первого раунда селекции в обеих фаговых библиотеках в качестве мишени использовали полноразмерный тримерный шиповидный белок SARS-Cov-2, сорбированный на поверхности поликарбонатных пробирок. После проведения первого раунда селекции, фаговые библиотеки использовали для заражения культуры бактериальных клеток TG-1, которые затем повторно высеивали на 25-см чашки с LB-агаром и карбенициллином, а затем экспансировали в жидкой среде после заражения хелперным фагом M13KO7 и концентрировали для проведения второго раунда селекции. Второй раунд селекции был проведен на каждой из библиотек в двух постановках: в первом случае, в качестве мишени также использовался полноразмерный шиповидный белок, а во втором – рецептор-связывающий домен RBD. Целью второго раунда было обогащение наборов последовательностей вариантами, селективно связывающимися с функционально-активной областью шиповидного белка и, как следствие, имеющими большие шансы на обладание нейтрализующей активностью. После проведения вторых раундов селекции, зараженные культуры клеток TG-1 высеивали 25-см чашки с LB-агаром и карбенициллином, после чего анализировали индивидуальные колонии на наличие вставок целевой длины (300-500 п.н.), затем отобранные целевые моноклональные препараты бактерий использовали для получения моноклональных бактериофагов, экспонирующих в составе оболочечного белка pIII антигенсвязывающие фрагменты однодоменных антител. Полученные препараты использовали для оценки специфичности связывания с шиповидным белком SARS-Cov-2 при помощи иммуноферментного анализа с детекцией моноклональными антителами к pIII, мечеными пероксидазой хрена. Клоны, характеризовавшиеся высокой специфичностью связывания с мишенью, были использованы для заражения бактериальной клеточной линии HB-2151 и получения культур клеток-продуцентов растворимых антигенраспознающих фрагментов однодоменных антител, меченых полигистидиновой меткой. Наработанные и очищенные препараты нанотел исследовали методом конкурентного иммуноферментного анализа (Фиг. 1) для поиска вариантов, обладающих способностью прерывать взаимодействие между шиповидным белком SARS-Cov-2 и рецептором ACE2, их степень сродства к рецептору-мишени была определена методом биослойной интерферометрии (Фиг. 2), после чего биологическая активность оценена в эксперименте с нейтрализацией репортерных лентивирусных векторов, псевдотипированных шиповидным белком на клеточной линии HEK-293, гиперэкспрессирующей ACE2, и в опытах по нейтрализации натурального SARS-Cov-2 на клеточной линии Vero (Фиг. 3).
Изобретение иллюстрировано следующими материалами.
Фиг. 1 – результаты конкурентного ИФА с растворимыми нанотелами к шиповидному белку SARS-Cov-2 и внеклеточной частью рецептора ACE2
Фиг. 2 – таблица значений константы диссоциации, измеренной методом биослойной интерферометрии для некоторых вариантов блокирующих нанотел к шиповидному белку, а также указание последовательностей, кодирующих их области CDR.
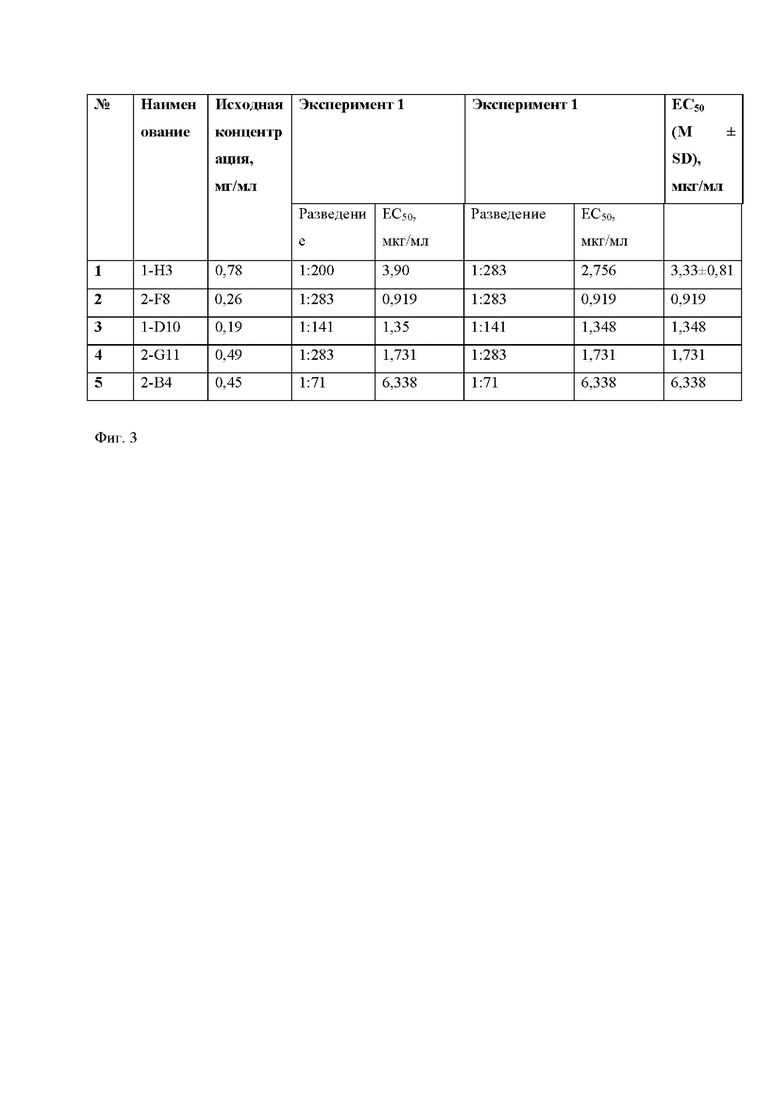
Фиг. 3 – таблица значений минимальных титров нанотел к шиповидному белку, в присутствие которых наблюдалось подавление инфекции SARS-Cov-2 монослоя чувствительных клеток Vero.
Перечень последовательностей
SEQ ID NO 1: GSIFSIRIMG
SEQ ID NO 2: GVTFTNYGMG
SEQ ID NO 3: GRTFESYAMG
SEQ ID NO 4: GSIFSNNAMA
SEQ ID NO 5: RSIGNINAMG
SEQ ID NO 6: ENIVGTRAMA
SEQ ID NO 7: GLTFSSSAMG
SEQ ID NO 8: GRAFTMPAMG
SEQ ID NO 9: GRTLRTYDMG
SEQ ID NO 10: ERTFSEYAVG
SEQ ID NO 11: GRAFSNYVMG
SEQ ID NO 12: TTTISGIGTYYADSVKG
SEQ ID NO 13: AIRRSGGITYNEDSVKG
SEQ ID NO 14: AISWSGGSTYYADSVKG
SEQ ID NO 15: SITGGGNTKYADSVKG
SEQ ID NO 16: AISWSGGSTHYADSVTG
SEQ ID NO 17: TIFTTSTTYYTPSVKG
SEQ ID NO 18: NINWSGGHTYYRDSVKG
SEQ ID NO 19: GINWSGSRTAYADSVKN
SEQ ID NO 20: AIRWSSGYQYYTDSVRG
SEQ ID NO 21: GINWSGSNTHYGESVKG
SEQ ID NO 22: AISRGGATTSYADSVKG
SEQ ID NO 23: YVRDKDGRAY
SEQ ID NO 24: AVGPVTATLTRNPADFGS
SEQ ID NO 25: AASTFRSDGAALYLDEYDY
SEQ ID NO 26: NTDPPLGTWAVEYDY
SEQ ID NO 27: AADTYGLGYDLLNLLASIDY
SEQ ID NO 28: NTAAVNERTS
SEQ ID NO 29: AVASNDYGLPSEKFLYDY
SEQ ID NO 30: AADRQIQDKVDVTAAEYDY
SEQ ID NO 31: AAKLALSSIDSPESEYPY
SEQ ID NO 32: AADHNLATDLTLFALGLLDYDY
SEQ ID NO 33: AAESARRVAVRTRADDYDS
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство и способ терапии и экстренной профилактики заболеваний, вызываемых вирусом SARS-CoV-2 на основе рекомбинантного антитела и гуманизированного моноклонального антитела | 2021 |
|
RU2769223C1 |
| ПОЛИПЕПТИДНЫЙ МОДУЛЬ ДЛЯ СВЯЗЫВАНИЯ КОНСЕРВАТИВНОГО ЭПИТОПА РЕЦЕПТОР-СВЯЗЫВАЮЩЕГО ДОМЕНА БЕЛКА SPIKE КОРОНАВИРУСА SARS-COV-2 | 2022 |
|
RU2809183C1 |
| БИСПЕЦИФИЧЕСКОЕ МОНОКЛОНАЛЬНОЕ АНТИТЕЛО ПРОТИВ SARS-COV-2 | 2022 |
|
RU2791749C1 |
| Однодоменное антитело ламы Н5 и его производное H5-Fc, специфически связывающие RBD-домен S-белка вируса SARS-CoV-2, обладающие вируснейтрализующей активностью | 2022 |
|
RU2793967C1 |
| Тяжелоцепочечные моноклональные антитела, специфически связывающиеся с S белком вируса SARS-CoV-2, и способ их применения для терапии заболеваний, вызываемых различными вариантами вируса SARS-CoV-2 | 2024 |
|
RU2836313C1 |
| Моноклональное антитело к RBD фрагменту в составе S белка вируса SARS-CoV-2 | 2020 |
|
RU2744274C1 |
| Моноклональное антитело iC1 и его антигенсвязывающий фрагмент, селективно связывающие рецептор-связывающий домен Spike-белка вируса SARS-CoV-2, обладающие вируснейтрализующей активностью | 2023 |
|
RU2817696C1 |
| Моноклональное антитело iC2 и его антигенсвязывающий фрагмент, селективно связывающие рецептор-связывающий домен Spike-белка вируса SARS-CoV-2, обладающие вируснейтрализующей активностью | 2023 |
|
RU2817697C1 |
| Экспрессионный вектор на основе аденоассоциированного вируса, несущий гены рекомбинантных антител, и его применение для профилактики заболеваний, вызываемых вирусом гриппа А и вирусом SARS-CoV-2 | 2023 |
|
RU2817792C1 |
| ПОЛИВАЛЕНТНАЯ ВЕКТОРНАЯ ВАКЦИНА HVT | 2020 |
|
RU2832110C1 |

Изобретение относится к области биотехнологии, в частности к тяжелоцепочечному антителу или его антигенсвязывающему фрагменту, которое специфически связывается с S-белком вируса SARS-CoV-2. Изобретение эффективно для ингибирования связывания S-белка вируса SARS-CoV-2 и клеточного рецептора ACE2. 2 з.п. ф-лы, 3 ил., 1 пр.
1. Тяжелоцепочечное антитело или его антигенсвязывающий фрагмент, которое специфически связывается с S-белком вируса SARS-CoV-2, содержащее области определения комплементарности (CDR),
где антитело выбрано из группы, состоящей из:
(1) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:1,
CDR2 с последовательностью SEQ ID NO:12, и
CDR3 с последовательностью SEQ ID NO:23;
(2) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:2,
CDR2 с последовательностью SEQ ID NO:13, и
CDR3 с последовательностью SEQ ID NO:24;
(3) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:3,
CDR2 с последовательностью SEQ ID NO:14, и
CDR3 с последовательностью SEQ ID NO:25;
(4) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:4,
CDR2 с последовательностью SEQ ID NO:15, и
CDR3 с последовательностью SEQ ID NO:26;
(5) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:5,
CDR2 с последовательностью SEQ ID NO:16, и
CDR3 с последовательностью SEQ ID NO:27;
(6) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:6,
CDR2 с последовательностью SEQ ID NO:17, и
CDR3 с последовательностью SEQ ID NO:28;
(7) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:7,
CDR2 с последовательностью SEQ ID NO:18, и
CDR3 с последовательностью SEQ ID NO:29;
(8) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:8,
CDR2 с последовательностью SEQ ID NO:19, и
CDR3 с последовательностью SEQ ID NO:30;
(9) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:9,
CDR2 с последовательностью SEQ ID NO:20, и
CDR3 с последовательностью SEQ ID NO:31;
(10) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:10,
CDR2 с последовательностью SEQ ID NO:21, и
CDR3 с последовательностью SEQ ID NO:32;
(11) антитела, содержащего
CDR1 с последовательностью SEQ ID NO:11,
CDR2 с последовательностью SEQ ID NO:22, и
CDR3 с последовательностью SEQ ID NO:33.
2. Антитело или антигенсвязывающий фрагмент по п.1, которое ингибирует связывание S-белка вируса SARS-CoV-2 и клеточного рецептора ACE2.
3. Антитело или антигенсвязывающий фрагмент по п.1, которое представляет собой IgA, IgD, IgE, IgG или IgM; моноклональное антитело или поликлональное антитело.
| CN 112010967 B, 23.03.2021 | |||
| Моноклональное антитело к RBD фрагменту в составе S белка вируса SARS-CoV-2 | 2020 |
|
RU2744274C1 |
| CHRISTOPHER O | |||
| BARNES et al., SARS-CoV-2 neutralizing antibody structures inform therapeutic strategies, Nature, 2020, Vol.588, N.7839, pp | |||
| ПРИСПОСОБЛЕНИЕ ДЛЯ ИЗМЕЛЬЧЕНИЯ ПЛАСТА, ОТВАЛИВАЕМОГО ПЛУГОМ | 1914 |
|
SU682A1 |
| BIN JU et al., Human neutralizing antibodies elicited by SARS-CoV-2 infection, Nature, 2020, Vol.584 | |||
| LIANG MF et al., SARS patients-derived | |||
Авторы
Даты
2023-04-11—Публикация
2021-06-11—Подача