Согласно настоящей заявке испрашивается приоритет в соответствии с европейской патентной заявкой ЕР 19382674.0, поданной 2 августа 2019 года.
Область техники
Настоящее изобретение в общем относится к области меланоцит-связанных нарушений. В частности, настоящее изобретение относится к пептидам, обладающим способностью регулировать меланогенез, либо промотируя, либо снижая продукцию меланина, а также ингибировать пролиферацию злокачественных меланоцитов, к фармацевтическим и косметическим композициям, содержащим их в качестве активных ингредиентов, а также к их применению в терапевтических и косметических применениях.
Уровень техники
В ходе процесса, называемого меланогенезом, меланоциты продуцируют меланин, который представляет собой пигмент, обнаруживаемый в коже, глазах, волосах, полости носа и внутреннем ухе. Этот меланогенез приводит к длительной пигментации, которая отличается от пигментации, возникающей в результате окисления уже существующего меланина.
Существуют как основной, так и активированный уровни меланогенеза, в основном люди со светлой кожей имеют низкий основной уровень меланогенеза. Воздействие УФ-В излучения вызывает усиление меланогенеза. Цель меланогенеза состоит в защите гиподермы, слоя под кожей, от повреждения УФ-В излучением. Цвет меланина является черным, что позволяет ему поглощать большую часть УФ-В света и блокировать его прохождение через эпидермис.
Известно, что в течение жизни у человека развиваются явные изменения окраски его кожи и, таким образом, например, появляются отметины на коже лица, груди и рук у пожилых людей, которые являются явными признаками старения. Кроме того, постоянное чрезмерное воздействие УФ-излучения вызывает не только ускоренное старение кожи, известное как фотостарение, которое характеризуется появлением признаков старения кожи в гораздо более раннем возрасте, в том числе появлением отметин на тех участках кожи, которые подверглись чрезмерному воздействию УФ-излучения, но также может привести к образованию гиперпигментированных раковых поражений или меланомы.
Часто происходят случаи, когда на участке кожи человека плотность меланина в меланоцитах больше, чем в окружающих участках, и, как следствие, цвет пораженного участка темнее, чем цвет остальных участков этого человека. Эти участки известны как участки гиперпигментации. Причинами гиперпигментации являются гормональные изменения, меланодермия, лентиго, пегая кожа, болезнь Аддисона, повышенная чувствительность к ультрафиолетовому излучению из-за агентов, которые благоприятствуют действию радиации (фототоксические вещества), или гиперпигментация как следствие воспалительного поражения. Отметины, связанные с акне, экземой, шрамами или удалением волос, относятся к этому последнему типу гиперпигментации и являются отметинами, которые могут сохраняться даже несколько лет.
Кожа человека может также иметь участки с более низкими плотностями меланина, чем в окружающих участках. Витилиго, себорейная экзема, отрубевидный лишай и поствоспалительный эффект являются общими причинами потери пигмента. Таким образом, уменьшение неравномерности пигментации, вызванной либо старением и/или фотостарением, либо гормональными нарушениями, либо поствоспалительными процессами, и, в частности, восстановление пигментации на участках, пораженных витилиго, посредством местных применений представляет интерес для косметического и фармацевтического сектора.
Пигментные нарушения являются глобальной проблемой. Несмотря на распространенность, пигментные нарушения по-прежнему трудно поддаются лечению.
Основные подходы к лечению нарушений гиперпигментации в основном основаны на предотвращении продукции меланина гиперактивными меланоцитами или стимулировании удаления меланина из эпидермиса посредством увеличения скорости обновления эпидермальных клеток. Ряд агентов, которые ингибируют тирозиназу, фермент, ограничивающий скорость, участвующий в синтезе меланина, в настоящее время используют для лечения нарушений гиперпигментации с умеренным успехом. Эти агенты включают гидрохинон, койевую кислоту (также называемую «КА»), арбутин, мехинол и азелаиновую кислоту. Контактный дерматит является распространенным побочным эффектом, возникающим у 15% пациентов, получающих эти агенты, что ограничивает их использование. Эффективность этих агентов значительно варьируется от пациента к пациенту. Ретиноиды для местного применения снижают эпидермальный меланин посредством ингибирования тирозиназы, а также увеличивают эпидермальную скорость обновления, способствуя тем самым рассредоточению и удалению меланина. Тем не менее, раздражающий дерматит может быть частым побочным эффектом, и следует соблюдать осторожность при назначении более высоких концентраций ретиноидов для местного применения на более темных типах кожи, поскольку возникающее в результате раздражение может привести к эритеме, шелушению и дальнейшей поствоспалительной гиперпигментации. Лазерная терапия иногда может быть эффективной при гиперпигментации. Однако она создает серьезную проблему для пациентов с более темной кожей, у которых повышен основной эпидермальный меланин, который также является мишенью при этих длинах волн.
Нарушения депигментации также связаны с воспалительным и аутоиммунным патогенезом, поэтому кортикостероиды для местного применения и иммуномодуляторы могут быть полезны в схеме лечения. Поскольку поствоспалительная гипопигментация обычно клинически проявляется после устранения воспалительного процесса, те же агенты для местного применения могут не быть полезными на этой поздней стадии. Фототерапию, включающую без ограничения псоралены плюс УФ-А (перорально или местно), псоралены и естественный солнечный свет, УФ-В, УФ-В узкого диапазона и эксимерные лазеры с длиной волны 308 нм, использовали для лечения как гипопигментации, так и депигментации. Нарушения депигментации (например, витилиго) могут быть особенно трудно поддающимися лечению из-за полного отсутствия меланоцитов в межфолликулярном эпидермисе. Следовательно, терапия направлена на рекрутинг или трансплантацию меланоцитов в эти места.
Таким образом, несмотря на предпринятые усилия, все еще существует потребность в разработке дополнительных молекул (пептидов), которые могут эффективно регулировать активность меланоцитов и, следовательно, могут быть эффективными для лечения пигментных нарушений.
Сущность изобретения
Авторы настоящего изобретения обнаружили, что пептиды согласно последовательностям SEQ ID NO: 1 и 2 эффективно регулируют активность меланоцитов.
С одной стороны, авторы настоящего изобретения неожиданно обнаружили, что пептиды согласно настоящему изобретению участвуют в пути меланогенеза. Таким образом, некоторые из пептидов стимулировали продукцию меланина, что может быть признаком активации меланоцита, тогда как другие, такие как F22 и F29, существенно снижали количество меланина. Еще более примечательным является тот факт, что пептиды согласно настоящему изобретению более эффективно регулируют продукцию меланина по сравнению с другими соединениями, известными в данной области техники. В этом отношении было обнаружено, что когда КА, который обычно используют при гиперпигментации, применяли при концентрации 1 мкМ, снижение было значительно более низким, чем снижение, достигаемое с помощью пептидов согласно настоящему изобретению при той же концентрации. Таким образом, эти данные не только подтверждают влияние пептидов согласно настоящему изобретению на продукцию меланина, но также показывают, что они даже более эффективны, чем другие соединения, доступные в данной области техники, которые в настоящее время используют с той же целью.
С другой стороны, авторы настоящего изобретения обнаружили, что эти пептиды регулируют активность меланоцитов не только в отношении образования меланина, но также в отношении клеточной пролиферации. Как также показано в Таблице 2, пептиды согласно настоящему изобретению были активны при ингибировании пролиферации раковых клеток, в частности клеточных линий меланомы, включая клеточные линии метастатической меланомы.
Таким образом, согласно первому аспекту настоящее изобретение относится к пептиду или его фармацевтически или косметически приемлемой соли, причем пептид имеет аминокислотную последовательность, на по меньшей мере 85% идентичную последовательности согласно SEQ ID NO: 1 или 2:

где
«m», «n», «р» и «q» представляют собой целые числа и выбраны из 0 и 1,
«mx», «nx», «рх» и «qx» представляют собой целые числа и выбраны из 0 и 1,
причем С-терминальный конец соответствует С(O)R4,
причем N-терминальный конец соответствует -NHR5,
R4 представляет собой радикал, выбранный из группы, состоящей из -ОН и -NR17R18,
R5 представляет собой радикал, выбранный из группы, состоящей из Н, (C1-С20)алкила и (С1-С10)алкила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (C1-С10)алкила, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12, и
R17 и R18 представляют собой радикалы, независимо выбранные из группы, состоящей из -Н и (С1-С10)алкила и (С1-С10)алкила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (С1-С10)алкила, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12, причем пептид необязательно включает линкерный бирадикал «L» формулы (I)
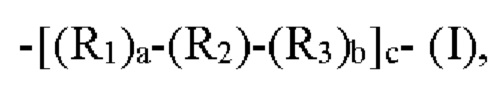
который представляет собой соединение альфа-атома углерода аминокислоты, расположенной в положении с альфа-атомом углерода аминокислоты, расположенной в положении «i+4» или «i+7» в пептидной последовательности,
где
«а» и «b» являются одинаковыми или различными и представляют собой 0 или 1, «с» составляет от 1 до 10,
R1 и R3 представляют собой бирадикалы, независимо выбранные из группы, состоящей из (С1-С10)алкила, (С1-С10)алкила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (С1-С10)алкила, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12, (С2-С10)алкенила, (С2-С10)алкенила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (С1-С10)алкила, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12, (С2-С10)алкинила и (С2-С10)алкинила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (С1-С10)алкила, -CR6, -NR7R8, -SRg, -SOR10, -SO2R11 и -CO2R12,
R2 представляет собой бирадикал, выбранный из группы, состоящей из -О-, С(=O), C(=O)NR13, С(=O)O, S(=O), S(=O)2, NR14, (С1-С10)алкила, (С2-С10)алкенила, (С2-С10)алкинила, -NR15-NR16-, -N=N-, -S-S- и известной кольцевой системы, содержащей от 3 до 14 членов, причем система содержит от 1 до 3 колец, где:
каждое из колец является насыщенным, частично ненасыщенным или ароматическим,
кольца являются изолированными, частично или полностью конденсированными,
каждый из членов, образующих известную кольцевую систему, выбран из группы, состоящей из -СН-, -СН2-, -NH-, -N-, -SH-, -S- и -О-, и
кольцевая система необязательно замещена одним или более радикалами, независимо выбранными из группы, состоящей из галогена, -ОН, -NO2, (С1-С10)алкила, (С1-С10)галоалкила и (С1-С10)алкил-O-, и
R6, R7, R8, R9, R10, R11, R12, R13, R14, R15 и R16 представляют собой радикалы, независимо выбранные из группы, состоящей из -Н и (С1-С10)алкила, и
причем аминокислоты, которые соединены линкером, имеют формулу (II)
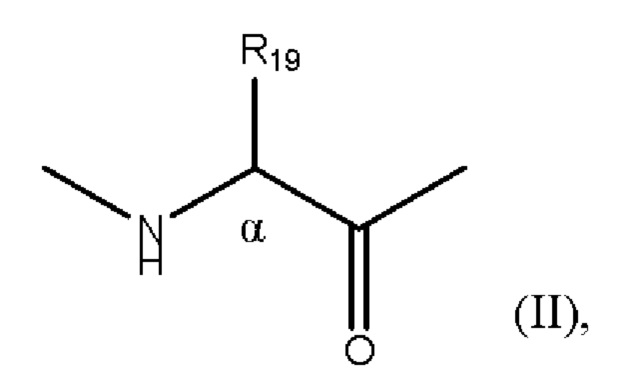
где
R19 представляет собой монорадикал, выбранный из группы, состоящей из (C1-С10)алкила, (С2-С10)алкенила, (С2-С10)алкинила и известной кольцевой системы, содержащей от 3 до 14 членов, причем система содержит от 1 до 3 колец, где:
каждое из колец является насыщенным, частично ненасыщенным или ароматическим,
кольца являются изолированными, частично или полностью конденсированными,
каждый из членов, образующих известную кольцевую систему, выбран из группы, состоящей из -СН-, -СН2-, -NH-, -N-, -SH-, -S- и -О-.
Согласно второму аспекту настоящее изобретение относится к косметической или фармацевтической композиции, содержащей косметически или терапевтически эффективное количество пептида, как определено согласно первому аспекту настоящего изобретения, вместе с приемлемыми косметическими или фармацевтическими вспомогательными веществами и/или носителями.
Согласно третьему аспекту настоящее изобретение относится к пептиду или его фармацевтически приемлемой соли, как определено согласно первому аспекту настоящего изобретения, или фармацевтической композиции согласно второму аспекту настоящего изобретения, для применения в качестве лекарственного средства. Этот аспект может быть альтернативно сформулирован как применение пептида или его фармацевтически приемлемой соли, как определено согласно первому аспекту настоящего изобретения, или фармацевтической композиции согласно второму аспекту настоящего изобретения для получения лекарственного средства для лечения заболевания. Этот аспект может быть альтернативно сформулирован как способ лечения заболевания, причем способ предусматривает введение эффективного терапевтического количества пептида или его фармацевтически приемлемой соли, как определено согласно первому аспекту, или фармацевтической композиции согласно второму аспекту настоящего изобретения субъекту, нуждающемуся в этом.
Согласно четвертому аспекту настоящее изобретение относится к пептиду или его фармацевтической соли, как определено согласно первому аспекту настоящего изобретения, или фармацевтической композиции, как определено согласно второму аспекту настоящего изобретения, для применения для лечения рака. Этот аспект альтернативно может быть сформулирован как применение пептида или его фармацевтической соли, как определено согласно первому аспекту настоящего изобретения, или фармацевтической композиции, как определено согласно второму аспекту настоящего изобретения, для получения лекарственного средства для лечения рака. Этот аспект альтернативно может быть сформулирован как способ лечения рака, причем способ предусматривает введение эффективного терапевтического количества пептида или его фармацевтической соли, как определено согласно первому аспекту настоящего изобретения, или фармацевтической композиции, как определено согласно второму аспекту настоящего изобретения, субъекту, нуждающемуся в этом.
Согласно пятому аспекту настоящее изобретение также относится к нетерапевтическому применению пептида или его косметической соли, как определено согласно первому аспекту настоящего изобретения, или косметической композиции, как определено согласно второму аспекту настоящего изобретения, для регуляции меланогенеза, в частности для снижения или увеличения продукции меланина.
Согласно последнему аспекту настоящее изобретение относится к косметическому способу лечения гипер- или гипопигментации у субъекта, нуждающегося в этом, причем способ предусматривает нанесение пептида или его косметической соли, как определено согласно пятому аспекту, или косметической композиции, как определено согласно второму аспекту настоящего изобретения, на пораженный участок, страдающий гипер-или гипопигментацией.
Согласно другим аспектам настоящее изобретение относится к (а) комбинации, содержащей пептид или его фармацевтическую соль, как определено согласно первому или второму аспекту настоящего изобретения, и терапевтический агент, в частности противораковый агент, (b) комбинации, содержащей пептид или его фармацевтическую соль, как определено согласно первому или второму аспекту настоящего изобретения, и терапевтический агент, в частности противораковый агент, для применения в качестве лекарственного средства, более конкретно для применения для лечения рака, (с) пептиду или его фармацевтической соли, как определено согласно первому или второму аспекту настоящего изобретения, для применения в комбинированной терапии для профилактики или лечения рака, где терапия предусматривает его введение субъекту одновременно, последовательно или раздельно с противораковым агентом, и (d) противораковому агенту для применения в комбинированной терапии с пептидом или его фармацевтической солью, как определено согласно первому или второму аспекту настоящего изобретения, где применение предусматривает профилактику или лечение рака.
Краткое описание чертежей
На фиг. 1 показан процент меланина в обработанных клетках меланомы относительно необработанных клеток меланомы. В качестве положительного контроля применяли койевую кислоту (КА) при различных концентрациях (0,1, 1 и 10 мкМ).
Подробное описание изобретения
Все термины, используемые в настоящем документе, если не указано иное, следует понимать в их обычном значении, известном в данной области техники. Другие более конкретные определения определенных терминов, используемых в настоящей заявке, изложены ниже и предназначены для применения единообразно во всем описании и формуле изобретения, если иное явно изложенное определение не обеспечивает более широкое определение.
Для целей настоящего изобретения любые приведенные диапазоны включают как нижнюю, так и верхнюю конечные точки диапазона.
Настоящее изобретение относится к пептидам, содержащим последовательности, которые на по меньшей мере 85% идентичны SEQ ID NO: 1 или 2, как указано выше.
В контексте настоящего изобретения термин «идентичность» относится к проценту остатков, которые идентичны в двух последовательностях, когда последовательности оптимально выровнены. Если при оптимальном выравнивании положение в первой последовательности занято тем же аминокислотным остатком, что и соответствующее положение во второй последовательности, последовательности проявляют идентичность в отношении этого положения. Уровень идентичности между двумя последовательностями (или «процент идентичности последовательностей») измеряют как отношение числа идентичных положений, общих для последовательностей, к размеру последовательностей (т.е. процент идентичности последовательностей = (количество идентичных положений / общее число положений) ×100).
Ряд математических алгоритмов для быстрого получения оптимального выравнивания и вычисления идентичности между двумя или более последовательностями известен и включен в ряд доступных программных обеспечений. Примеры таких программных обеспечений включают, среди прочего, программы для анализа аминокислотной последовательности MATCH-BOX, MULTAIN, GCG, FASTA и ROBUST. Предпочтительные программные обеспечения для анализа включают программы ALIGN, CLUSTAL W и BLAST (например, BLAST 2.1, BL2SEQ и их более поздние версии).
Для анализа аминокислотной последовательности для определения идентичности используют весовую матрицу, как например, матрицы BLOSUM (например, матрицы BLOSUM45, BLOSUM50, BLOSUM62 и BLOSUM80), матрицы сравнения аминокислот по Gonnet или матрицы РАМ (например, матрицы РАМ30, РАМ70, РАМ120, РАМ 160, РАМ250 и РАМ350).
Программы BLAST обеспечивают анализ по меньшей мере двух аминокислотных последовательностей либо путем выравнивания выбранной последовательности относительно множества последовательностей в базе данных (например, GenSeq), либо посредством BL2SEQ между двумя выбранными последовательностями. Программы BLAST предпочтительно модифицируются фильтрующими программами низкой сложности, такими как программы DUST или SEG, которые предпочтительно интегрированы в операции программы BLAST. Если используют присутствие гэпа (или оценки гэпа), оценку гэпа предпочтительно устанавливают между приблизительно -5 и -15. Подобные параметры гэпа можно использовать с другими программами по мере необходимости. Программы BLAST и лежащие в их основе принципы подробно описаны в, например, Altschul et al., «Basic local alignment search tool», 1990, J. Mol. Biol, v. 215, pages 403-410.
Для анализа множественных последовательностей можно использовать программу CLUSTAL W. Желательно выполнять программу CLUSTAL W с использованием «динамических» (а не «быстрых») установок. Аминокислотные последовательности оценивают с использованием вариабельного набора матриц BLOSUM в зависимости от уровня идентичности между последовательностями. Программа CLUSTAL W и лежащие в ее основе принципы работы подробно описаны в, например, Higgins et al., «CLUSTAL V: improved software for multiple sequence alignment)), 1992, CABIOS, 8(2), pages 189-191.
В контексте настоящего изобретения термин «фармацевтически или косметически приемлемая соль» относится к тем солям, которые с медицинской точки зрения являются подходящими для использования в контакте с тканями человека и низших животных без чрезмерной токсичности, раздражения, аллергической реакции и тому подобного и соответствуют разумному соотношению польза/риск. Фармацевтически и косметически приемлемые соли хорошо известны в данной области техники. Примерами фармацевтически и косметически приемлемых нетоксичных солей присоединения кислот являются соли аминогруппы, образованные с неорганическими кислотами, такими как соляная кислота, бромистоводородная кислота, фосфорная кислота, серная кислота и перхлорная кислота, или с органическими кислотами, такими как уксусная кислота, трифторуксусная кислота, щавелевая кислота, малеиновая кислота, винная кислота, лимонная кислота, янтарная кислота или малоновая кислота, или с использованием других способов, используемых в данной области техники, таких как ионный обмен. Другие фармацевтически и косметически приемлемые соли включают адипат, альгинат, аскорбат, аспартат, бензолсульфонат, бензоат, бисульфат, борат, бутират, камфорат, камфорсульфонат, цитрат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, формиат, фумарат, глюкогептонат, глицерофосфат, глюконат, гемисульфат, гептаноат, гексаноат, гидройодид, 2-гидроксиэтансульфонат, лактобионат, лактат, лаурат, л аурил сульфат, малат, малеат, малонат, метансульфонат, 2-нафталинсульфонат, никотинат, нитрат, олеат, оксалат, пальмитат, памоат, пектинат, персульфат, 3-фенилпропионат, фосфат, пикрат, пивалат, пропионат, стеарат, сукцинат, сульфат, тартрат, тиоцианат, п-толуолсульфонат, ундеканоат, валерат и тому подобное. Соли, полученные из соответствующих оснований, включают щелочной металл, щелочноземельный металл и аммоний. Иллюстративные соли щелочных или щелочноземельных металлов включают натрий, литий, калий, кальций, магний и тому подобное. Дополнительные фармацевтически и косметически приемлемые соли включают при необходимости нетоксичные катионы аммония, четвертичного аммония и амина, образованные с использованием противоионов, таких как галогенид, гидроксид, карбоксилат, сульфат, фосфат, нитрат, низший алкилсульфонат и арилсульфонат.
Термин (С1-С10)алкил относится к насыщенной неразветвленной или разветвленной алкильной цепи, имеющей от 1 до 10 атомов углерода. Иллюстративными неограничивающими примерами являются метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, н-пентил, нео-пентил и н-гексил.
Термин (С1-С20)алкил относится к насыщенной неразветвленной или разветвленной алкильной цепи, имеющей от 1 до 20 атомов углерода.
Термин (С2-С10)алкенил относится к насыщенной неразветвленной или разветвленной алкильной цепи, имеющей от 2 до 10 атомов углерода, а также содержащей одну или более двойных связей. Иллюстративными неограничивающими примерами являются этенил, пропенил, бутенил, 1-метил-2-бутен-1-ил и тому подобное.
Термин (С2-С10)алкинил относится к насыщенной неразветвленной или разветвленной алкильной цепи, имеющей от 2 до 20 атомов углерода, а также содержащей одну или более тройных связей. Примеры включают среди прочего этинил, 1-пропинил, 2-бутинил, 1,3-бутадинил, 4-пентинили 1-гексинил.
Термин «галоген» относится к группе в периодической таблице, состоящей из пяти химически родственных элементов: фтора (F), хлора (Cl), брома (Br), йода (I) и астата (At).
Термин (С1-С10)галоалкил относится к группе, полученной в результате замещения одного или более атомов водорода (С1-С10)алкильной группы одним или более, предпочтительно от 1 до 6, атомами галогена, которые могут быть одинаковы или различными. Примеры включают, среди прочего, трифторметил, фторметил, 1-хлорэтил, 2-хлорэтил, 1-фторэтил, 2-фторэтил, 2-бромэтил, 2-йодоэтил, 2,2,2-трифторэтил, пентафторэтил, 3-фторпропил, 3-хлорпропил, 2,2,3,3-тетрафторпропил, 2,2,3,3,3-пентафторпропил, гептафторпропил, 4-фторбутил и нонафторбутил.
В контексте настоящего изобретения термин «известная» кольцевая система относится к кольцевой системе, которая химически осуществима и известна в данной области техники, и, таким образом, подразумевает исключение тех кольцевых систем, которые химически невозможны.
Согласно настоящему изобретению, когда кольцевая система образована «изолированными» кольцами, это означает, что кольцевая система образована двумя, тремя или четырьмя кольцами, и указанные кольца связаны посредством связи атома одного кольца с атомом другого кольца. Термин «изолированный» также охватывает вариант осуществления, согласно которому кольцевая система имеет только одно кольцо. Иллюстративными неограничивающими примерами известных кольцевых систем, состоящих из одного кольца, являются производные от: циклопропила, циклобутила, циклопентила, циклгексила, циклогептила, циклопропенила, циклобутенила, циклопентенила, фенила и циклогептенила.
Согласно настоящему изобретению, когда кольцевая система имеет «полностью конденсированные» кольца, это означает, что кольцевая система образована двумя, тремя или четырьмя кольцами, в которых два или более атомов являются общими для двух соседних колец. Иллюстративными неограничивающими примерами являются 1,2,3,4-тетрагидронафтил, 1-нафтил, 2-нафтил, антрил или фенантрил.
Согласно настоящему изобретению, когда кольцевая система является «частично конденсированной», это означает, что кольцевая система образована тремя или четырьмя кольцами, при этом по меньшей мере два из указанных колец полностью конденсированы (т.е. два или более атомов являются общими для двух соседних колец), а оставшееся (оставшиеся) кольцо (кольца) связано (связаны) посредством связи атома одного кольца с атомом одного из конденсированных колец.
Если не указано иное, аминокислоты, образующие пептиды согласно настоящему изобретению, могут иметь L- или D-конфигурацию.
Аминокислоты, используемые при конструировании пептидов согласно настоящему изобретению, могут быть получены путем органического синтеза или получены другими путями, такими как, например, расщепление или выделение из природного источника.
Согласно одному варианту осуществления первого аспекта настоящего изобретения пептид отличен от пептида согласно последовательности SEQ ID NO: 24, 25 или 26.
Согласно одному варианту осуществления первого аспекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид представляет собой пептид, в котором тип являются одинаковыми. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид представляет собой пептид, в котором р и q являются одинаковыми. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, тип представляют собой 1, и р и q представляют собой 0. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, тип представляют собой 0, и р и q представляют собой 1.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид представляет собой линейный пептид.
В контексте настоящего изобретения термин «линейный пептид» означает, что он не включает бирадикал «L».
Согласно одному варианту осуществления первого аспекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид представляет собой линейный пептид, состоящий из SEQ ID NO: 1, где:
- когда «m» и «n» являются одинаковыми, тогда «р» отличен от «q», и
- когда m представляет собой 0, и n=p=1, тогда q представляет собой 1.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид представляет собой линейный пептид, состоящий из SEQ ID NO: 1, и выбран из пептидов, в которых:
- по меньшей мере три из m, n, р и q являются одинаковыми, или в качестве альтернативы
- когда «m» представляет собой 0, и «n» представляет собой 1, тогда «р» представляет собой 0, и «q» представляет собой 0 или 1, или, в качестве альтернативы,
- когда «m» представляет собой 0, и «n» представляет собой 1, тогда «р» представляет собой 0, и «q» представляет собой 1.
Согласно одному варианту осуществления первого аспекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид представляет собой пептид, в котором mx и nx являются одинаковыми. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид представляет собой пептид, в котором рх и qx являются одинаковыми. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, mx и nx представляют собой 1, и рх и qx представляют собой 0. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, mx и nx представляют собой 0, и рх и qx представляют собой 1.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, содержащий линкер «L», где а=1. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, содержащий линкер «L», где b=1. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, содержащий линкер «L», где с=1. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, содержащий линкер «L», где a=b=c=1.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, содержащий линкер «L», где R1 и R3 представляют собой бирадикалы, независимо выбранные из группы, состоящей из (С1-С10)алкила, (С2-С10)алкенила и (С2-С10)алкинила. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, содержащий линкер «L», где R1 и R3 являются одинаковыми или разными и представляют собой (С1-С10)алкил.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, содержащий линкер «L», где R2 представляет собой бирадикал, выбранный из группы, состоящей из -О-, С(=O), C(=O)NR13, С(=O)O, S(=O), S(=O)2, NR14, (С1-С10)алкила, (С2-С10)алкенила, (С2-С10)алкинила, -NR15-NR16-, -N=N-, -S-S- и известной кольцевой системы, состоящей из одного кольца, имеющего от 3 до 6 членов, причем кольцо:
является насыщенным, частично насыщенным или ароматическим,
каждый из членов, образующих известную кольцевую систему, выбран из группы, состоящей из -СН-, -СН2-, -NH-, -N-, -SH-, -S- и -О-, и
причем кольцевая система необязательно замещена одним или более радикалами, независимо выбранными из группы, состоящей из галогена, -ОН, -NO2, (С1-С10)алкила, (С1-С10)галоалкила и (С1-С10)алкил-O-.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, содержащий линкер «L», где R2 представляет собой бирадикал, выбранный из группы, состоящей из (С1-С10)алкила, (С2-С10)алкенила и (С2-С10)алкинила. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, содержащий линкер «L», где R2 представляет собой (С2-С10)алкенил.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, содержащий линкер «L», где R1 и R3 являются одинаковыми или различными и представляют собой (С1-С10)алкил, и R2 представляет собой (С2-С10)алкенил.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, содержащий линкер «L», где R1 и R3 являются одинаковыми или различными и представляют собой (С1-С10)алкил, R2 представляет собой (С2-С10)алкенил, и a=b=c=1.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, в котором R19 выбран из группы, состоящей из (С1-С10)алкила, (С2-С10)алкенила и (С2-С10)алкинила. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, в котором R19 представляет собой (С1-С10)алкильный монорадикал. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, содержащий линкер «L», где R1, R3 и R19 являются одинаковыми или различными и представляют собой (С1-С10)алкил, и R2 представляет собой (С2-С10)алкенил.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, в котором R4 представляет собой -ОН (т.е. С-терминальный конец представляет собой -С(О)ОН). Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, в котором R4 представляет собой -NR17R18, причем R17 и R18 имеют одинаковое значение. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, N-терминальный конец соответствует -NH2. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, С-терминальный и N-терминальный концы пептида согласно настоящему изобретению соответственно представляют собой -С(O)ОН и -NH2. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, С-терминальный и N-терминальный концы пептида согласно настоящему изобретению соответственно представляют собой -C(O)NH2 и -NH2.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, С-терминальный и N-терминальный концы пептида согласно настоящему изобретению соответственно представляют собой C-(О)ОН и -NHR5, где R5 выбран из (С1-С20)алкила и (С1-С10)алкила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (С1-С10)алкила, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, С-терминальный и N-терминальный концы пептида согласно настоящему изобретению соответственно представляют собой -C(O)R4 и -NH2, где R4 означает -NHR18, и R18 представляет собой радикал, выбранный из группы, состоящей из (С1-С10)алкила и (С1-С10)алкила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (С1-С10)алкила, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, С-терминальный и N-терминальный концы пептида согласно настоящему изобретению соответственно представляют собой -C(O)R4 и -NH2, где R4 означает -NR17R18, и R17 и R18 представляют собой радикалы, независимо выбранные из группы, состоящей из (С1-С10)алкила и (С1-С10)алкила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (С1-С10)алкила, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, линкерный бирадикал формулы (I) расположен между альфа-атомом углерода аминокислоты, расположенной в положении «i» в пептидной последовательности SEQ ID NO: 1, и альфа-атомом кислорода аминокислоты, расположенной в положении «i+7» в пептидной последовательности SEQ ID NO: 1.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль выбраны из группы, состоящей из аминокислотных последовательностей SEQ ID NO: 3-8:
SEQ ID NO: 3
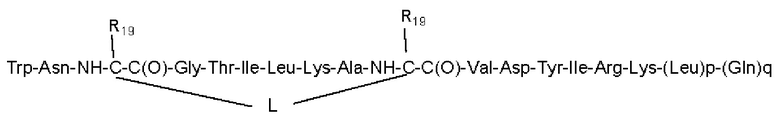
SEO ID NO:4
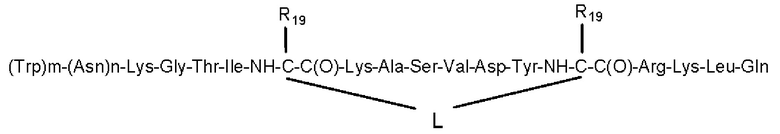
SEQ ID NO: 5
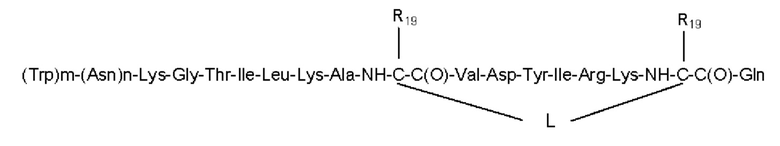
SEQ ID NO: 6
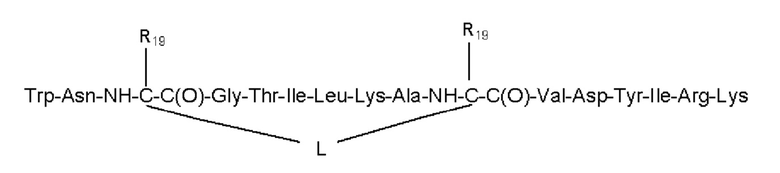
SEQ ID NO: 7
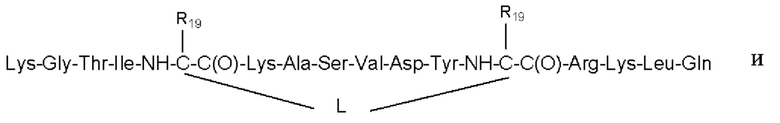
SEO ID NO: 8
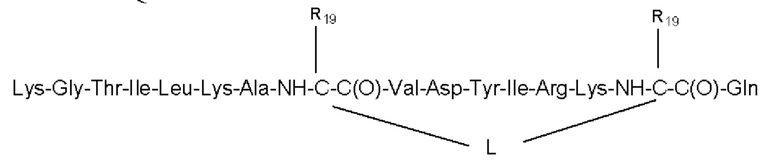
где «m», «n», «p», «q», «L» и «R19» имеют значения, как определено согласно любому из предшествующих вариантов осуществления.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, линкерный бирадикал формулы (I) расположен между альфа-атомом углерода аминокислоты, расположенной в положении «i» в пептидной последовательности SEQ ID NO: 2, и альфа-атомом кислорода аминокислоты, расположенной в положении «i+7» в пептидной последовательности SEQ ID NO: 2.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль выбраны из группы, состоящей из аминокислотных последовательностей SEQ ID NO: 9-16:
SEQ ID NO: 9
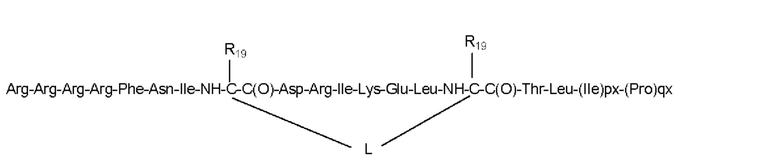
SEQ ID NO: 10
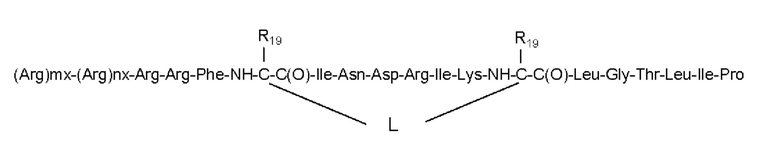
SEQ ID NO: 11
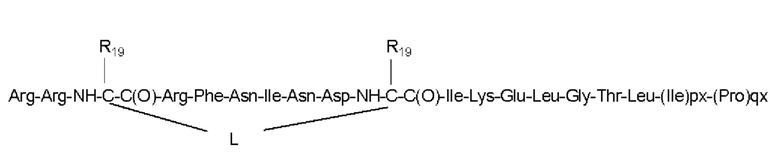
SEQ ID NO: 12
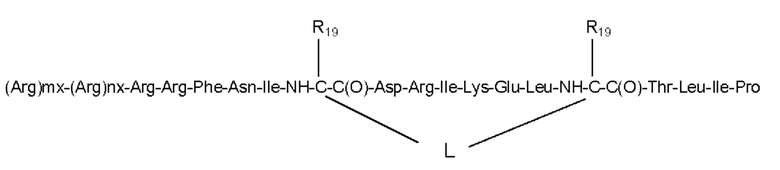
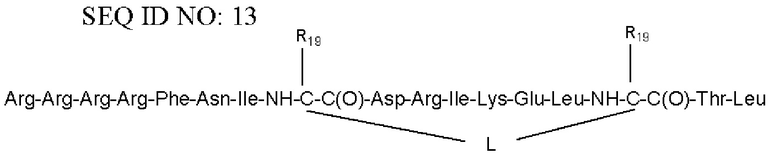
SEQ ID NO: 14
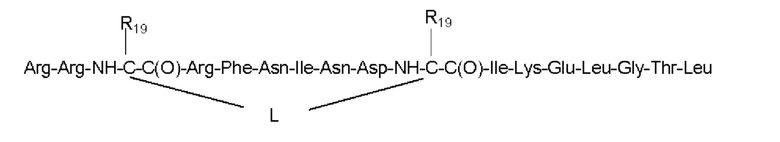
SEQ ID NO: 15
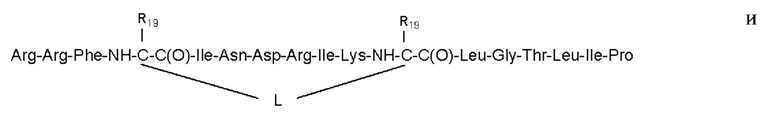
SEO ID NO: 16
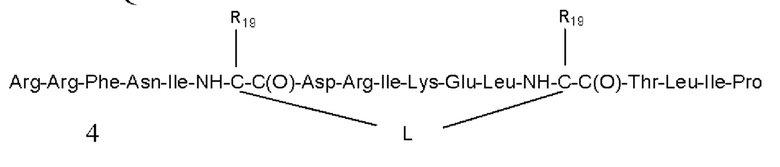
где «mx», «nx», «px», «qx», «L» и «R19» имеют значения, как определено согласно любому из предшествующих вариантов осуществления.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляют собой пептид, который на по меньшей мере 85% идентичен последовательности согласно SEQ ID NO: 3-8, где R1, R3 и R19 являются одинаковыми или различными и представляют собой (С1-С10)алкил, и R2 представляет собой (С2-С10)алкенил. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляют собой пептид, который на по меньшей мере 85% идентичен последовательности согласно SEQ ID NO: 3-8, где R1, R3 и R19 являются одинаковыми или различными и представляют собой (С1-С10)алкил, R2 представляет собой (С2-С10)алкенил, С-терминальный конец выбран из -С(O)ОН и -CONH2, и N-терминальный конец представляет собой -NH2.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляют собой пептид, который на по меньшей мере 85% идентичен последовательности согласно SEQ ID NO: 9-16, где R1, R3 и R19 являются одинаковыми или различными и представляют собой (С1-С10)алкил, и R2 представляет собой (С2-С10)аженил. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляют собой пептид, который на по меньшей мере 85% идентичен последовательности согласно SEQ ID NO: 9-16, где R1, R3 и R19 являются одинаковыми или различными и представляют собой (С1-С10)алкил, R2 представляет собой (С2-С10)алкенил, С-терминальный конец выбран из -С(O)ОН и -CONH2, и N-терминальный конец представляет собой -NH2.
Согласно другому варианту осуществления первого объекта настоящего изобретения пептид представляет собой пептид, на по меньшей мере 85% идентичный аминокислотной последовательности, или его фармацевтическую или косметическую соль, выбранные из группы, состоящей из последовательности SEQ ID NO: 17-23:
SEQ ID NO: 17 (далее также упоминается в настоящем документе как «F22»)
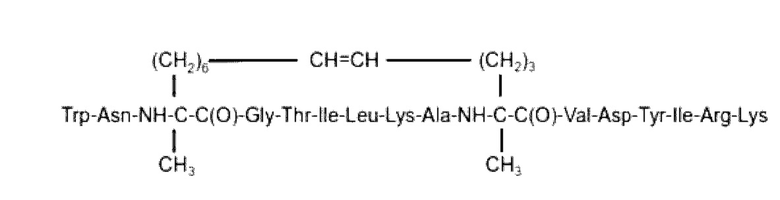
SEQ ID NO: 18 (далее также упоминается в настоящем документе как «F29»)
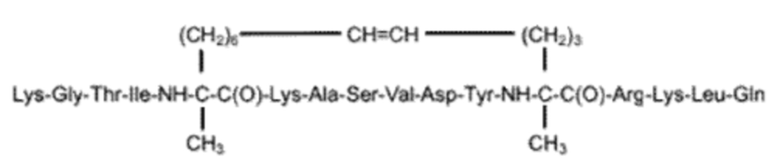
SEQ ID NO: 19 (далее также упоминается в настоящем документе как «F31»)
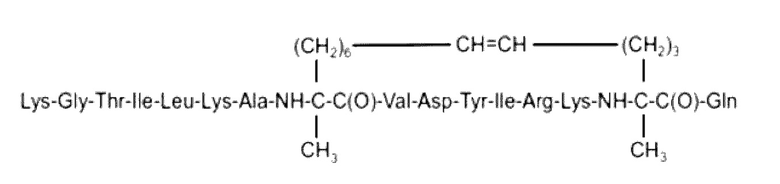
SEQ ID NO: 20 (далее также упоминается в настоящем документе как «F05»)
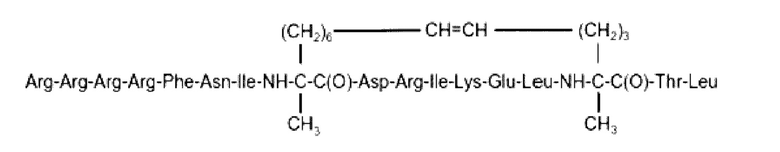
SEQ ID NO: 21 (далее также упоминается в настоящем документе как «F13»)
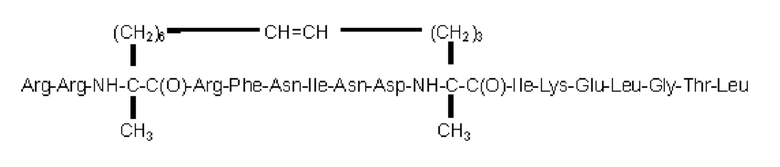
SEQ ID NO: 22 (далее также упоминается в настоящем документе как «F16»)
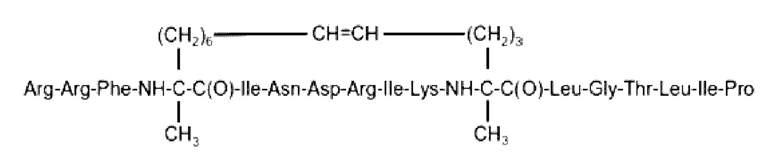
SEQ ID NO: 23 (далее также упоминается в настоящем документе как «F18»)
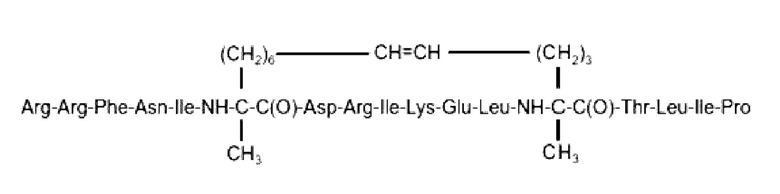
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, который имеет идентичность 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% с любой из последовательностей SEQ ID NO: 1-23, и «m», «n», «р», «q», «mx», «nx», «рх», «qx», L и R19 имеют значения, как определено в любом из вариантов осуществления выше. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или его соль представляет собой пептид, который имеет идентичность 100% с любой из последовательностей SEQ ID NO: 1-23, и «m», «n», «р», «q», «mx», «nK», «рх», «qx», L и R19 имеют значения, как определено в любом из вариантов осуществления выше. Согласно одному варианту осуществления, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, два аминокислотных остатка, соединенные линкером, не учитывают при проведении выравнивания для определения идентичных положений для подтверждения степени идентичности.
Согласно одному варианту осуществления первого аспекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид согласно первому аспекту конъюгирован с фрагментом, таким как метка, лекарственное средство или проникающий в клетку пептид. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид конъюгирован с меткой. Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, метка конъюгирована с N- или С-терминальным концом пептида.
В контексте настоящего изобретения термин «метка» представляет собой молекулу или соединение, которые могут быть обнаружены различными способами, включая флуоресценцию, электропроводность, радиоактивность, размер и тому подобное. Метка может быть по своей природе способна испускать сигнал, например, флуоресцентная метка, которая излучает свет с определенной длиной волны после возбуждения светом с другой более низкой характерной длиной волны. В качестве альтернативы метка может быть не способна испускать сигнал сама по себе, но она может быть способна связываться с другим соединением, которое испускает сигнал. Примером этой последней ситуации является метка, такая как биотин, который сам по себе не испускает сигнал, но который может быть обнаружен при связывании с мечеными молекулами авидина или стрептавидина. Другими примерами этого последнего типа метки являются лиганды, которые специфически связываются с определенными рецепторами. Детектируемо меченым рецепторам позволяют связываться со специфическими маркерами рецептора, меченого лигандами, чтобы визуализировать такие маркеры.
Метки, которые можно использовать в соответствии с настоящим изобретением, включают без ограничения молекулу электронно-спинового резонанса, флуоресцентную молекулу, хемилюминесцентную молекулу, радиоизотоп, субстрат фермента, фермент, молекулу биотина, молекулу авидина, молекулу переноса электрического заряда, полупроводниковый нанокристалл, полупроводниковую наночастицу, коллоидный нанокристалл золота, лиганд, микрошарик, магнитный шарик, парамагнитную молекулу, квантовую точку, хромогенный субстрат, аффинную молекулу, белок, пептид, нуклеиновую кислоту, углевод, гаптен, антиген, антитело, фрагмент антитела и липид.
Радиоизотопы могут быть обнаружены с помощью пленочных приемников или устройств с зарядовой связью (CCD), лиганды могут быть обнаружены путем связывания рецептора, имеющего флуоресцентную, хемилюминесцентную или ферментную метку, а микрошарики могут быть обнаружены с помощью электронной или атомно-силовой микроскопии.
Конъюгацию метки с пептидом можно проводить в соответствии с обычными протоколами, хорошо известными специалистам в данной области техники.
Согласно другому варианту осуществления пептид согласно первому аспекту настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, конъюгирован с лекарственным средством. Согласно одному варианту осуществления лекарственное средство конъюгировано с N-терминальным концом пептида.
Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид конъюгирован с проникающим в клетку пептидом.
В контексте настоящего изобретения термин «проникающий в клетку пептид» («СРР») относится к коротким пептидам, которые облегчают поглощение клетками различных молекулярных грузов (от наноразмерных частиц до небольших химических молекул и крупных фрагментов ДНК). «Груз» связан с пептидами через C(t)- или N(t)-конец либо посредством химического связывания ковалентными связями, либо посредством нековалентных взаимодействий. Функция СРР заключается в доставке груза в клетки, процесс, который обычно происходит посредством эндоцитоза. Существующее в настоящее время использование ограничено отсутствием клеточной специфичности в доставке грузов, опосредованной СРР, и недостаточным пониманием способов их поглощения. СРР в общем имеют аминокислотный состав, который либо содержит высокое относительное содержание положительно заряженных аминокислот, таких как лизин или аргинин, либо имеет последовательности, которые содержат чередующуюся модель полярных/заряженных аминокислот и неполярных, гидрофобных аминокислот. Эти два типа структур называются поликатионными или амфипатическими, соответственно. Третий класс СРР представляет собой гидрофобные пептиды, которые содержат только аполярные остатки с низким суммарным зарядом или имеют гидрофобные аминокислотные группы, которые важны для поглощения клетками. Конъюгацию СРР с пептидом согласно настоящему изобретению можно проводить в соответствии с хорошо известными обычными протоколами, такими как твердофазный синтез или селективное кэппирование в растворе, (см. Copolovici D. М. et al., «Cell-Penetrating Peptides: Design, Synthesis, and Applications», 2014, ACS Nano, 2014, 8 (3), pp 1972 1994). Согласно другому варианту осуществления первого объекта настоящего изобретения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, проникающим в клетку пептидом является поликатионный СРР, полиАrg или, в качестве альтернативы, пенетратин.
Способ получения пептидов согласно первому аспекту настоящего изобретения предуcматривает:
(1.а) связывание посредством конденсации соответствующих аминокислот пептида с соединением формулы (III) и соединением формулы (IV), которые соответствуют аминокислотам, упоминаемым как «i» и «i+4» или «i+7». Соединения (III) и (IV) представляют собой соединения, которые далее подвергают последующей стадии циклизации с образованием бирадикала «L»:
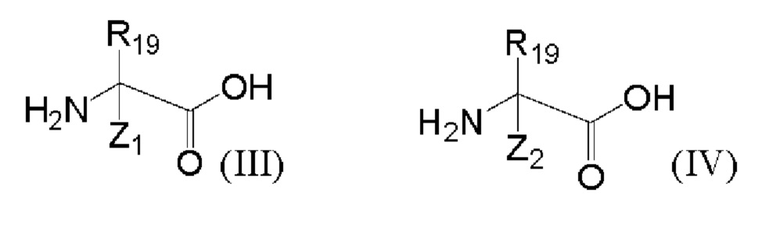
где R19 имеет значения, как определено выше, Z1 и Z2 являются одинаковыми или различными и представляют собой (С2-С10)алкенил, и
(1.b) стадию циклизации, предусматривающую метатезис с закрытием кольца Z1 и Z2 (см. Kim Young-Woo et al., «Synthesis of all-hydrocarbon stapled a-helical peptides by ring-closing olefin metathesis», Nature Protocols, 2011, 6(6), p.761-771, Scott J. M. et al., «Application of Ring-Closing Metathesis to the Synthesis of Rigidified Amino Acids and Peptides», J. Am. Chem. Soc, 1996, v. 118 (40), pp 9606-9614), проводимую в растворе с катализатором Граббса (поколения I или II), или, в качестве альтернативы,
(2а) связывание посредством конденсации необходимых аминокислот, включая соединение формулы (V) и соединение формулы (VI), которые соответствуют аминокислотам, упоминаемым как «i» и «i+4» или «i+7». Соединения (V) и (VI) представляют собой соединения, которые далее подвергают последующей стадии циклизации с образованием бирадикала «L»:
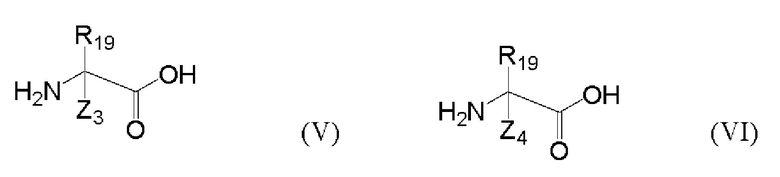
где R19 имеет значения, как определено выше, Z3 и Z4 являются одинаковыми или различными, выбранными из группы, состоящей из галогена, -SH, -NHR2O, -ОН, (С2-С10)алкил-SH, (С1-С10)алкил-ОН, (С1-С10)алкил-NHR21, С(=O)ОН, (C1-C10)C(=O)OH, C(=O)NHR22, (C1-C10)алкилС(=O)NHR23, OR24, С(=O)-галогена, C(=O)-OR25, S(=O)-галогена, S(=O)-OR26, S(=O)2R27, где R20, R21 R22, R23, R24, R25 R26 и R27 представляют собой монорадикалы, выбранные из группы, состоящей из водорода, (С1-С10)алкила, (С2-С10)алкенила и (С2-С10)алкинила, известной кольцевой системы, содержащей от 3 до 14 атомов углерода, причем система содержит от 1 до 3 колец, где:
каждое из колец является насыщенным, частично ненасыщенным или ароматическим,
кольца являются изолированными, частично или полностью конденсированными,
каждый из членов, образующих известную кольцевую систему, выбран из группы, состоящей из -СН-, -СН2-, -NH-, -N-, -SH-, -S- и -О-, и
кольцевая система необязательно замещена одним или более радикалами, независимо выбранными из группы, состоящей из галогена, -ОН, -NH2, -SH, С(=O)-галоген (С1-С10)галоалкила и (С1-С10)алкил-O-, и
(2b) стадию циклизации, предусматривающую реакцию связывания между радикалами Z3 и Z4, или, в качестве альтернативы,
(3а) связывание посредством конденсации соответствующих аминокислот пептида с соединением формулы (VII) и соединением формулы (VIII), которые соответствуют аминокислотам, упоминаемым как «i» и «i+4» или «i+7». Соединения (VII) и (VIII) представляют собой соединения, которые далее подвергают последующей стадии циклизации с образованием бирадикала «L»:
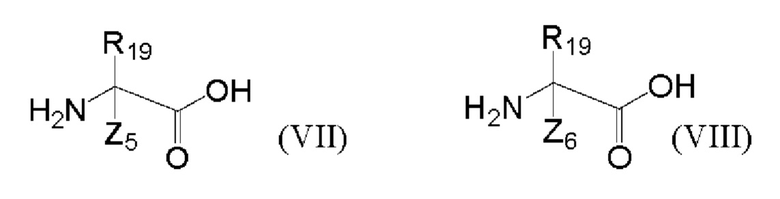
где R19 имеет значения, как определено выше, один из Z5 и Z6 представляет собой (С2-С10)алкинил, а другой представляет собой (С2-С10)алкилN3, и
(3.b) стадию циклизации, предусматривающую конденсацию радикалов Z5 и Z6 согласно хорошо известным протоколам, таким как Cu(I)-опосредованная реакция 1,3-диполярного циклоприсоединения Хьюсгена (также известная как «клик» реакция) с получением 1,4-замещенного 1,2,3-триазольного мостика (см. Kolb Н.С.et al., «The growing impact of click chemistry on drug discovery», 2003, Drug Discov Today, 8(24): 1128-1137).
Способ получения пептида в соответствии со вторым аспектом настоящего изобретения предусматривает связывание путем конденсации карбоксильной группы или С-конца одной аминокислоты с аминогруппой или N-концом другой, причем эту реакцию связывания повторяют необходимое количество раз до получения желаемого пептида.
Соединения формул (III), (IV), (V), (VI), (VII) и (VIII) являются коммерчески доступными и связывают путем конденсации с уже сформированной частью пептидной последовательности. Эти соединения могут нести шарики для соответствующего твердофазного синтеза пептида, а также защитные группы карбокси, амино или боковой цепи. Иллюстративными неограничивающими примерами соединений являются 2-(2'-пропенил)аланин, 2-(3'-бутенил)глицин, 2-(4'-пентенил)аланин, 2-(6'-гептенил)аланин, 2-(7'-октенил)аланин, аллилглицин, 5-азидонорвалин и альфа-пропаргилаланин, среди прочих.
Стадию «связывания» можно проводить в твердой фазе, следуя протоколу «удаление защитной группы-промывка-связывание-промывка», путем конденсации карбоксильной группы одной аминокислоты с аминогруппой другого аминокислотного остатка, используя аминокислоты, как определено выше, а также альфа-альфа-дизамещенные аминокислоты формул (II)-(VII).
Общий принцип твердофазного синтеза пептидов состоит в повторении циклов удаление защитной группы-промывка-связывание-промывка. Свободный N-концевой амин пептида, присоединенного к твердой фазе, связан с одной N-защищенной аминокислотной единицей. Затем у этой единицы удаляют защитную группу, высвобождая новый N-концевой амин, к которому может быть присоединена дополнительная аминокислота. Аминокислоты имеют реакционноспособные фрагменты на N- и С-концах, что облегчает связывание аминокислот в ходе синтеза. Многие аминокислоты также имеют реакционноспособные функциональные группы боковой цепи, которые могут взаимодействовать со свободными концами или другими группами боковой цепи в ходе синтеза и удлинения пептида и отрицательно влиять на выход и чистоту. Для облегчения надлежащего синтеза аминокислот с минимальной реакционной способностью боковых цепей были разработаны химические группы, которые связываются со специфическими функциональными группами аминокислот и блокируют или защищают функциональные группы от неспецифических реакций. Эти защитные группы, хотя и обширны по своей природе, могут быть разделены на три группы, а именно: N-концевые защитные группы, С-концевые защитные группы (в основном используемые в жидкофазном синтезе) и защитные группы боковой цепи.
Для связывания пептидов, как правило, активируют карбоксильную группу. Это важно для ускорения реакции. Существует два основных типа активирующих групп: карбодиимиды и триазололы. Однако использование пентафторфениловых сложных эфиров (FDPP, PFPOH) и ВОР-С1 полезно для циклизации пептидов.
Очищенные отдельные аминокислоты реагируют с этими защитными группами перед синтезом, а затем их селективно удаляют на определенных стадиях синтеза пептидов.
Иллюстративные смолы, которые можно применять согласно настоящему изобретению включают без ограничения: (1) алкениловые смолы (например, смола REM, связанная с полимером винилсульфоновая смола, винил-полистирольная смола), (2) амин-функционализированные смолы (например, амидиновая смола, N-(4-бензилоксибензил)гидроксиламин, связанный с полимером, (аминометил)полистирол, связанный с полимером(R)-(+)-а-метилбензиламин, 2-хлортритильная смола Кнорра, 2-N-Emoc-амино-дибензоциклогепта-1,4-диен, связанная с полимером смола, 4-[4-(1-Fmoc-аминоэтил)-2-метокси-5-нитрофенокси]бутирамидометил-полистирольная смола, 4-бензилоксибензиламин, связанный с полимером, 4-карбоксибензолсульфонамид, связанный с полимером, бис(трет-бутоксикарбонил)тиопсевдомочевина, связанная с полимером, диметиламинометил-полистирол, Emoc-3-амино-3-(2-нитрофенил)пропионовая кислота, связанная с полимером, N-метил-аминометилированный полистирол, смола PAL, амидная смола Зибера, трет-бутил N-(2-меркаптоэтил)карбамат, связанный с полимером, трифенилхлорметан-4-карбоксамид, связанный с полимером), (3) бензгидриламиновые (ВНА) смолы (например, 2- хлорбензгидрил хлорид, связанный с полимером, НМРВ-бензгидриламин, связанный с полимером, 4-метилбензгидрол, связанный с полимером, бензгидрилхлорид, связанный с полимером, бензгидриламин, связанный с полимером), (4) Br-функционализированные смолы (например, 4-(бензилокси)бензилбромид, связанный с полимером, 4-бромполистирол, броминированная смола РРОА, броминированная смола Ванга, бромацеталь, связанный с полимером, бромполистирол, HypoGel® 200 Br, полистирол А-Br для пептидного синтеза, бромид селена, связанный с полимером, TentaGel HL-Br, TentaGel MB-Br, TentaGel S-Br), (5) хлорметиловые смолы (например, 5-[4-(хлорметил)фенил]пентил]стирол, связанный с полимером, 4-(бензилокси)бензилхлорид, связанный с полимером, 4-метоксибензгидрилхлорид, связанный с полимером), (6) СНО-функционализированные смолы (например, (4-формил-3-метоксиффеноксиметил)полистирол, (4-формил-3-метоксифеноксиметил)полистирол, 3-бензилоксибензальдегид, связанный с полимером, 4-бензилокси-2,6-диметоксибензальдегид, связанный с полимером, формилполистирол, HypoGel® 200 СНО, индольная смола, полистирол А-CH(OEt)2, TentaGel HL-CH(OEt)2), (7) Cl-функционализированные смолы (например, бензоилхлорид, связанный с полимером, (хлорметил)полистирол, смола Меррифилда), (8) CO2H функционализированные смолы (например, карбоксиэтилполистирол, HypoGel® 200 СООН, полистирол AM-СООН, TentaGel HL-СООН, TentaGel MB-СООН, TentaGel S-COOH), (9) Hypo-Gel смолы (например, HypoGel® 200 FMP, HypoGel® 200 PHB, HypoGel® 200 Trt-OH, HypoGel® 200 HMB), (10) I-функционализированные смолы (например, 4-иодфенол, связанный с полимером, иодполистирол), Janda-Jels™ (JandaJel смола Ринка, JandaJel-NH2, JandaJel-CI, JandaJel-4-меркаптофенол, JandaJel-OH, JandaJel-1-(3-диметиламинопропил)-3-этилкарбодиимид, JandaJel-1,3,4,6,7,8-гексагидро-2Н-пиримидо- [1,2-а] пиримидин, JandaJel-морфолин, JandaJel-полипиридин, JandaJel-трифенилфосфин, JandaJel-смола Ванга), (11) МВНА смолы (3[4'-(гидроксиметил)фенокси]пропионовая кислота-4-метилбензгидриламиновая смола, 4-(гидроксиметил)феноксиуксусная кислота, связанная с полимером МВНА смола, HMBA-4-метилбензгидриламин, связанный с полимером, 4-метилбензгидриламин гидрохлорид, связанный с полимером (амин)), (12) NH2 функционализированные смолы ((аминометил)полистирол, (аминометил)полистирол, HypoGel® 200 NH2, полистирол AM-NH2, 2-аминоэтилированные полистироловые микросферы, 2-бромэтилированные полистироловые микросферы, 2-гидроксиэтилированные полистироловые микросферы, TentaGel HL-NH2, Tentagel М Br, Tentagel М NH2, Tentagel М ОН, TentaGel MB-NH2, TentaGel S-NH2, TentaGel S-NH2), (13) ОН-функционализированные смолы (например, 4-гидроксиметилбензойная кислота, связанная с полимером, гидроксиметиловые смолы, ОН- функционализированные смолы Ванга), (14) оксимовые смолы (например, 4-хлорбензолфеноноксим, связанный с полимером, бензофеноноксим, связанный с полимером, 4-метоксибензофеноноксим, связанный с полимером), (15) смолы PEG (например, этиленгликоль, связанный с полимером), (16) Boc-/Blz смолы пептидного синтеза (например, Boc-Lys(Boc)-Lys[Boc-Lys(Boc)]-Cys(Acm)-b-Ala-O-PAM смола, Boc-Lys(Fmoc)-Lys[Boc-Lys(Fmoc)]-b-Ala-O-Pam смола, Boc-Lys(Boc)-Lys[Boc-Lys(Boc)]-Lys{Boc-Lys(Boc)-Lys[Boc-Lys(Boc)]}-b-Ala-O-PAM смола, Boc-Lys(Fmoc)-Lys[Boc-Lys(Fmoc)]-Lys[Boc-Lys(Fmoc)-Lys{Boc-Lys(Fmoc)]}-b-Ala-O-PAM смола, Boc-Lys(Boc)-Lys[Boc-Lys(Boc)]-Lys{Boc-Lys(Boc)-LysfBoc-Lys(Boc)]}-Cys(Acm)-b-Ala-O-PAM смола, предварительно загруженные смолы РАМ), (17) Fmoc-/t-Bu смолы пептидного синтеза (например, Fmoc-Lys(Fmoc)-Lys[Fmoc-Lus(Fmoc)]-b-Ala-O-смола Ванга, Fmoc-Lys(Fmoc)-Lys[Fmoc-Lys(Fmoc)]-Lys{Fmoc-Lus(Fmoc)-Lus[Fmoc-Lus(Fmoc)]}-b-Ala-O-смола Ванга, предварительно загруженные тритиловые смолы TentaGel® S, предварительно загруженные смолы TentaGel®, предварительно загруженные тритиловые смолы, предварительно загруженные смолы Ванга, тритиловые смолы, предварительно загруженные аминоспиртами), (19) тиол-функционализированные смолы (например, HypoGel® 200 S-Trt, полистирол AM-S-тритил, TentaGel HL-S-тритил, TentaGel MB-S-тритил, TentaGel S-S-тритил), и (20) смолы Ванга (например, Fmoc-Ala-смола Ванга, Emoc-Arg(Pbf)-смола Ванга, Fmoc-Arg(Pmc)-смола Ванга, Fmoc-Asn(Trt)-смола Ванга, Emoc-Asp(OtBu)-смола Ванга, Fmoc-Cys(Acm)-смола Ванга, Emoc-Cys(StBu)-смола Ванга, Fmoc-Cys(Trt) Смола Ванга, Fmoc-Gln(Trt)-смола Ванга, Emoc-Gly(OtBu)-смола Ванга, Fmoc-Gly-смола Ванга, Emoc-His(Trt)-смола Ванга, Fmoc-Ile-смола Ванга, Fmoc-Leu-смола Ванга, Emoc-Lys(Вос)-смола Ванга, Fmoc-Met-смола Ванга, Fmoc-D-Met-смола Ванга, Fmoc-Phe-смола Ванга, Fmoc-Pro-смола Ванга, Emoc-Ser(tBu)-смола Ванга, Emoc-Ser(Trt)-смола Ванга, Emoc-Thr(tBu)-смола Ванга, Fmoc-Trp(Boc) Смола Ванга, Fmoc-Trp-смола Ванга, Emoc-Tyr(tBu)-смола Ванга, Fmoc-Val-смола Ванга).
смола Ринка, JandaJel-NH2, JandaJel-CI, JandaJel-4-меркаптофенол, JandaJel-OH, JandaJel-1-(3-диметиламинопропил)-3-этилкарбодиимид, JandaJel-1,3,4,6,7,8-гексагидро-2Н-пиримидо- [1,2-а] пиримидин, JandaJel-морфолин, JandaJel-полипиридин, JandaJel-трифенилфосфин, JandaJel-смола Ванга), (11) МВНА смолы (3[4'-(гидроксиметил)фенокси]пропионовая кислота-4-метилбензгидриламиновая смола, 4-(гидроксиметил)феноксиуксусная кислота, связанная с полимером МВНА смола, HMBA-4-метилбензгидриламин, связанный с полимером, 4-метилбензгидриламин гидрохлорид, связанный с полимером (амин)), (12) NH2 функционализированные смолы ((аминометил)полистирол, (аминометил)полистирол, HypoGel® 200 NH2, полистирол AM-NH2, 2-аминоэтилированные полистироловые микросферы, 2-бромэтилированные полистироловые микросферы, 2-гидроксиэтилированные полистироловые микросферы, TentaGel HL-NH2, Tentagel М Br, Tentagel М NH2, Tentagel М ОН, TentaGel MB-NH2, TentaGel S-NH2, TentaGel S-NH2), (13) ОН-функционализированные смолы (например, 4-гидроксиметилбензойная кислота, связанная с полимером, гидроксиметиловые смолы, ОН- функционализированные смолы Ванга), (14) оксимовые смолы (например, 4-хлорбензолфеноноксим, связанный с полимером, бензофеноноксим, связанный с полимером, 4-метоксибензофеноноксим, связанный с полимером), (15) смолы PEG (например, этиленгликоль, связанный с полимером), (16) Boc-/Blz смолы пептидного синтеза (например, Boc-Lys(Boc)-Lys[Boc-Lys(Boc)]-Cys(Acm)-b-Ala-O-PAM смола, Boc-Lys(Fmoc)-Lys[Boc-Lys(Fmoc)]-b-Ala-O-Pam смола, Boc-Lys(Boc)-Lys[Boc-Lys(Boc)]-Lys{Boc-Lys(Boc)-Lys[Boc-Lys(Boc)]}-b-Ala-O-PAM смола, Boc-Lys(Fmoc)-Lys[Boc-Lys(Fmoc)]-Lys[Boc-Lys(Fmoc)-Lys{Boc-Lys(Fmoc)]}-b-Ala-O-PAM смола, Boc-Lys(Boc)-Lys[Boc-Lys(Boc)]-Lys{Boc-Lys(Boc)-LysfBoc-Lys(Boc)]}-Cys(Acm)-b-Ala-O-PAM смола, предварительно загруженные смолы РАМ), (17) Fmoc-/t-Bu смолы пептидного синтеза (например, Fmoc-Lys(Fmoc)-Lys[Fmoc-Lus(Fmoc)]-b-Ala-O-смола Ванга, Fmoc-Lys(Fmoc)-Lys[Fmoc-Lys(Fmoc)]-Lys{Fmoc-Lus(Fmoc)-Lus[Fmoc-Lus(Fmoc)]}-b-Ala-O-смола Ванга, предварительно загруженные тритиловые смолы TentaGel® S, предварительно загруженные смолы TentaGel®, предварительно загруженные тритиловые смолы, предварительно загруженные смолы Ванга, тритиловые смолы, предварительно загруженные аминоспиртами), (19) тиол-функционализированные смолы (например, HypoGel® 200 S-Trt, полистирол AM-S-тритил, TentaGel HL-S-тритил, TentaGel MB-S-тритил, TentaGel S-S-тритил), и (20) смолы Ванга (например, Fmoc-Ala-смола Ванга, Emoc-Arg(Pbf)-смола Ванга, Fmoc-Arg(Pmc)-смола Ванга, Fmoc-Asn(Trt)-смола Ванга, Emoc-Asp(OtBu)-смола Ванга, Fmoc-Cys(Acm)-смола Ванга, Emoc-Cys(StBu)-смола Ванга, Fmoc-Cys(Trt) Смола Ванга, Fmoc-Gln(Trt)-смола Ванга, Emoc-Gly(OtBu)-смола Ванга, Fmoc-Gly-смола Ванга, Emoc-His(Trt)-смола Ванга, Fmoc-Ile-смола Ванга, Fmoc-Leu-смола Ванга, Emoc-Lys(Вос)-смола Ванга, Fmoc-Met-смола Ванга, Fmoc-D-Met-смола Ванга, Fmoc-Phe-смола Ванга, Fmoc-Pro-смола Ванга, Emoc-Ser(tBu)-смола Ванга, Emoc-Ser(Trt)-смола Ванга, Emoc-Thr(tBu)-смола Ванга, Fmoc-Trp(Boc) Смола Ванга, Fmoc-Trp-смола Ванга, Emoc-Tyr(tBu)-смола Ванга, Fmoc-Val-смола Ванга).
«Защитная группа» (PG) относится к группе атомов, которые при присоединении к реакционноспособной группе в молекуле маскируют, снижают или предотвращают эту реакционную способность.
Подходящие амино-защитные группы включают метилкарбамат, этилкарбамат, 9-флуоренилметилкарбамат (Fmoc), 9-(2-сульфо)флуоренилметилкарбамат, 9-(2,7-дибром)флуоренилметилкарбамат, 2,7-ди-трет-бутил-[9-(10,10-диоксо-10,10,10,10-тетрагидротиоксантил)]метилкарбамат (DBD-Tmoc), 4-метоксифенацилкарбамат (Phenoc), 2,2,2-трихлорэтилкарбамат (Troc), 2-триметилсилилэтилкарбамат (Теос), 2-фенилэтилкарбамат (hZ), 1-(1-адамантил)-1-метилэтилкарбамат (Adpoc), 1,1-диметил-2-галогеноэтилкарбамат, 1,1-диметил-2,2-дибромэтилкарбамат (DB-трет-ВОС), 1,1-диметил-2,2,2-трихлорэтилкарбамат (ТСВОС), 1-метил-1-(4-бифенилил)этилкарбамат (Врос), 1-(3,5-ди-трет-бутилфенил)-1-метилэтил карбамат (трет-Bumeoc), 2-(2'- и 4'-пиридил)этилкарбамат (Руос), 2-(N,N-дициклогексилкарбоксамидо)этилкарбамат, трет-бутилкарбамат (ВОС), 1-адамантил карбамат (Adoc), винилкарбамат (Voc), аллилкарбамат (Alloc), 1-изопропилаллилкарбамат (Ipaoc), циннамилкарбамат (Сое), 4-нитроциннамилкарбамат (Noc), 8-хинолилкарбамат, N-гидроксипиперидинил-карбамат, алкилдитиокарбамат, бензилкарбамат (Cbz), пара-метоксибензил-карбамат (Moz), пара-нитробензилкарбамат, пара-бромбензилкарбамат, пара-хлорбензилкарбамат, 2,4-дихлорбензилкарбамат, 4-метилсульфинилбензил-карбамат (Msz), 9-антрилметилкарбамат, дифенилметилкарбамат, 2-метилтиоэтилкарбамат, 2-метилсульфонилэтилкарбамат, 2-(пара-толуолсульфонил)этилкарбамат, [2-(1,3-дитианил)]метилкарбамат (Dmoc), 4-метилтиофенилкарбамат (Mtpc), 2,4-диметилтиофенилкарбамат (Bmpc), 2-фосфониоэтилкарбамат (Реос), 2-трифенилфосфониоизопропилкарбамат (Ррос), 1,1-диметил-2-цианоэтилкарбамат, мета-хлор-пара-ацилоксибензил-карбамат, пара-(дигидроксиборил)бензилкарбамат, 5-бензизоксазолилметил-карбамат, 2-(трифторметил)-6-хромонилметилкарбамат (Тсгос), мета-нитрофенилкарбамат, 3,5-диметоксибензилкарбамат, орто-нитробензил-карбамат, 3,4-диметокси-6-нитробензилкарбамат, фенил(орто-нитрофенил)метилкарбамат, фенотиазинил-(10)-карбонильное производное, N'-napa-толуолсульфониламинокарбонильное производное, N'-фениламинотиокарбонильное производное, трет-амилкарбамат, S-бензил-тиокарбамат, пара-цианобензилкарбамат, циклобутилкарбамат, циклогексил-карбамат, циклопентилкарбамат, циклопропилметилкарбамат, пара-децилоксибензилкарбамат, 2,2-диметоксикарбонилвинилкарбамат, орто-(N,N-диметилкарбоксамидо)бензилкарбамат, 1,1-диметил-3-(N,N-диметилкарбоксамидо)пропилкарбамат, 1,1-диметилпропинилкарбамат, ди(2-пиридил)метилкарбамат, 2-фуранилметилкарбамат, 2-йодэтилкарбамат, изоборинилкарбамат, изобутилкарбамат, изоникотинилкарбамат, пара-(пара-метоксифенилазо)бензилкарбамат, 1-метилциклобутилкарбамат, 1-метилциклогексилкарбамат, 1-метил-1-циклопропилметилкарбамат, 1-метил-1-(3,5-диметоксифенил)этилкарбамат, 1-метил-1-(пара-фенилазофенил)этилкарбамат, 1-метил-1-фенилэтилкарбамат, 1-метил-1-(4-пиридил)этилкарбамат, фенилкарбамат, пара-(фенилазо)бензилкарбамат, 2,4,6-три-трет-бутилфенилкарбамат, 4-(триметиламмоний)бензилкарбамат, 2,4,6-триметилбензилкарбамат, формамид, ацетамид, хлорацетамид, трихлорацетамид, трифторацетамид, фенилацетамид, 3-фенилпропанамид, пиколинамид, 3-пиридилкарбоксамид, N-бензоилфенилаланильное производное, бензамид, пара-фенилбензамид, орто-нитрофенилацетамид, орто-нитрофеноксиацетамид, ацетоацетамид, (N'-дитиобензилоксикарбониламино)ацетамид, 3-(пара-гидроксифенил)пропанамид, 3-(орто-нитрофенил)пропанамид, 2-метил-2-(орто-нитрофенокси)пропанамид, 2-метил-2-(орто-фенилазофенокси)пропанамид, 4-хлорбутанамид, 3-метил-3-нитробутанамид, орто-нитроциннамид, N-ацетилметиониновое производное, орто-нитробензамид, орто-(бензоилоксиметил)бензамид, 4,5-дифенил-3-оксазолин-2-он, N-фталимид, N-дитиасукцинимид (Dts), N-2,3-дифенилмалеимид, М-2,5-диметилпиррол, N-1,1,4,4-тетраметилдисилилазациклопентановый аддукт (STABASE), 5-замещенный 1,3-диметил-1,3,5-триазациклогексан-2-он, 5-замещенный 1,3-дибензил-1,3,5-триазациклогексан-2-он, 1-замещенный 3,5-динитро-4-пиридон, N-метиламин, N-аллиламин, N-[2-(триметилсилил)этокси]метиламин (SEM), N-3-ацетоксипропиламин, N-(1-изопропил-4-нитро-2-оксо-3-пиролин-3-ил)амин, четвертичные аммониевые соли, N-бензиламин, N-ди(4-метоксифенил)метиламин, N-5-дибензосубериламин, N-трифенилметиламин (Tr), N-[(4-метоксифенил)дифенилметил]амин (MMTr), N-9-фенилфлуорениламин (PhF), N-2,7-дихлор-9-флуоренилметиленамин, N-ферроценилметиламино (Fcm), N-2-пиколиламино-N'-оксид, N-1,1-диметилтиометиленамин, N-бензилиденамин, N-пара-метоксибензилиденамин, N-дифенилметиленамин, N-[(2-пиридил)мезитил]метиленамин, N-(N',N'-диметиламинометилен)амин, N,N'-изопропилидендиамин, N-пара-нитробензилиденамин, N-салицилиденамин, N-5-хлорсалицилиденамин, N-(5-хлор-2-гидроксифенил)фенилметиле намин, N-циклогексилиденамин, N-(5,5-диметил-3-оксо-1-циклогексенил)амин, N-борановое производное, производное N-дифенилбориновой кислоты, N-[фенил(пентакарбонилхром-или вольфрам)карбонил]амин, N-хелат меди, N-хелат цинка, N-нитроамин, N-нитрозоамин, N-аминоксид, дифенилфосфинамид (Dpp), диметилтиофосфинамид (Mpt), дифенилтиофосфинамид (Ppt), диалкилфосфорамидаты, дибензилфосфорамидат, дифенилфосфорамидат, бензолсульфенамид, орто-нитробензолсульфенамид (Nps), 2,4-динитробензолсульфенамид, пентахлорбензолсульфенамид, 2-нитро-4-метоксибензолсульфенамид, трифенилметилсульфенамид, 3-нитропиридинсульфенамид (Npys), пара-толуолсульфонамид (Ts), бензолсульфонамид, 2,3,6,-триметил-4-метоксибензолсульфонамид (Mtr), 2,4,6-триметоксибензолсульфонамид (Mtb), 2,6-диметил-4-метоксибензолсульфонамид (Pme), 2,3,5,6-тетраметил-4-метоксибензолсульфонамид (Mte), 4-метоксибензолсульфонамид (Mbs), 2,4,6-триметилбензолсульфонамид (Mts), 2,6-диметокси-4-метилбензолсульфонамид (iMds), 2,2,5,7,8-пентаметилхроман-6-сульфонамид (Pmc), метансульфонамид (Ms), β-триметилсилилэтансульфонамид (SES), 9-антраценсульфонамид, 4-(4',8'-диметоксинафтилметил)бензолсульфонамид (DNMBS), бензилсульфонамид, трифторметилсульфонамид и фенацилсульфонамид.
Примеры подходящим образом защищенных карбоновых кислот дополнительно включают без ограничения силил-, алкил-, алкенил-, арил- и арилалкил-защищенные карбоновые кислоты. Примеры подходящих силильных групп включают триметилсилил, триэтилсилил, трет-бутилдиметилсилил, трет-бутилдифенилсилил, триизопропилсилил и тому подобное. Примеры подходящих алкильных групп включают метил, бензил, п-метоксибензил, 3,4-диметоксибензил, тритил, трет-бутил, тетрагидропиран-2-ил. Примеры подходящих алкенильных групп включают аллил. Примеры подходящих арильных групп включают необязательно замещенный фенил, бифенил или нафтил. Примеры подходящих арилалкильных групп включают необязательно замещенный бензил (например, п-метоксибензил (МРМ), 3,4-диметоксибензил, О-нитробензил, и-нитро бензил, п-галобензил, 2,6-дихлорбензил, п-цианобензил) и 2 - и 4-пиколил.
Согласно второму аспекту настоящее изобретение относится к фармацевтической или косметической композиции.
В контексте настоящего изобретения выражение «терапевтически эффективное количество» относится к количеству соединения, которое при введении проходит в кровоток и является достаточным для предотвращения развития или облегчения до некоторой степени одного или более симптомов заболевания, на которое оно направлено. Конкретная доза пептида, вводимого в соответствии с настоящим изобретением, конечно, будет определяться конкретными обстоятельствами, связанными с данным случаем, включая вводимое соединение, путь введения, конкретное состояние, подлежащее лечению, и подобные условия. Согласно одному варианту осуществления согласно второму аспекту настоящего изобретения фармацевтическая композиция представляет собой композицию для парентерального введения. Согласно другому варианту осуществления фармацевтическая композиция предназначена для перорального введения.
В контексте настоящего изобретения выражение «косметически эффективное количество» относится к количеству соединения, которое при его применении (например, местно) удерживается в кожной ткани (например, на подкожном уровне), не достигая в значительной степени или не достигая кровотока, оказывая, таким образом, местное действие на структуру кожи. Конкретная доза пептида, вводимая в соответствии с настоящим изобретением, конечно, будет определяться конкретными обстоятельствами данного случая. Согласно одному варианту осуществления настоящего изобретенияетению «косметически эффективное количество» пептида согласно настоящему изобретению выше, равно или ниже количества, необходимого для достижения терапевтического эффекта при его введении парентеральным путем, в частности внутривенным путем.
Термин «фармацевтически приемлемый» относится к вспомогательным вещества или носителям, подходящим для использования в фармацевтической технологии получения композиций медицинского назначения.
Термин «косметически приемлемый», который используется в настоящем документе взаимозаменяемо, относится к вспомогательным вещества или носителям, подходящим для использования при контакте с кожей человека без чрезмерной токсичности, несовместимости, нестабильности, аллергической реакции, среди прочего.
Выражение «вспомогательные вещества и/или носители» относится к приемлемым веществам, композициям или носителям. Каждый компонент должен быть фармацевтически или косметически приемлемым в контексте совместимости с другими ингредиентами композиции. Он также должен быть подходящим для использования в контакте с тканями или органами человека и животных, не относящихся к человеку, без чрезмерной токсичности, раздражения, аллергической реакции, иммуногенности или других проблем или осложнений, согласно разумному соотношению польза/риск. Примерами подходящих приемлемых вспомогательных веществ являются растворители, дисперсионные среды, разбавители или другие жидкие носители, вспомогательные добавки для дисперсии или суспензии, поверхностно-активные вещества, изотонические агенты, загустители или эмульгаторы, консерванты, твердые связующие вещества, смазывающие вещества и тому подобное. За исключением случаев, когда какая-либо обычная вспомогательная среда несовместима с веществом или его производными, например, из-за того, что вызывает какой-либо нежелательный биологический эффект или иным образом взаимодействует вредоносным образом с любым другим компонентом (компонентами) фармацевтической или косметической композиции, ее использование предполагается в объеме настоящего изобретения.
Составы фармацевтических и косметических композиций, описанные в настоящем документе, могут быть получены любым способом, известным или впоследствии разработанным в области фармакологии и косметики. Как правило, такие способы получения предусматривают стадию объединения активного ингредиента (пептида) с наполнителем и/или одним или более другими вспомогательными ингредиентами, а затем, при необходимости и/или если желательно, формование и/или упаковку продукта в желаемую форму однократной дозы или множества доз.
Фармацевтическая композиция согласно настоящему изобретению может быть получена, упакована и/или продана без упаковки в виде единичной стандартной дозы и/или в виде множества единичных стандартных доз. В контексте настоящего изобретения термин «стандартная доза» означает дискретное количество фармацевтической композиции, содержащее заданное количество активного ингредиента.
Относительные количества активного ингредиента (т.е. пептида, как определено в любом из предшествующих аспектов и вариантов осуществления), приемлемых вспомогательных веществ и/или любых дополнительных ингредиентов в композиции согласно настоящему изобретению будут варьироваться в зависимости от идентичности, размера и/или состояние субъекта, подлежащего лечению, и, кроме того, в зависимости от пути введения композиции.
Приемлемые вспомогательные вещества, используемые при получении этих композиций, включают без ограничения инертные разбавители, диспергирующие и/или гранулирующие агенты, поверхностно-активные вещества и/или эмульгаторы, средства для улучшения распадаемости, связывающие вещества, консерванты, буферные агенты, смазывающие агенты и/или масла. Такие вспомогательные вещества необязательно могут быть включены в составы согласно настоящему изобретению. Вспомогательные вещества, такие как масло какао и воск для суппозиториев, красители, вещества для покрытия, подсластители, ароматизаторы и отдушки, могут присутствовать в композиции согласно решению состава.
Иллюстративные разбавителей включают без ограничения карбонат кальция, карбонат натрия, фосфат кальция, дикальцийфосфат, сульфат кальция, гидрофосфат кальция, фосфата натрия, лактозу, сахарозу, целлюлозу, микрокристаллическую целлюлозу, каолин, маннит, сорбит, инозитол, хлорид натрия, сухой крахмал, кукурузный крахмал, порошкообразный сахар и их комбинации.
Иллюстративные гранулирующие и/или диспергирующие агенты включают без ограничения картофельный крахмал, кукурузный крахмал, крахмал маниока, натрий крахмал гликолят, глины, альгиновую кислоту, гуаровую камедь, цитрусовую пульпу, агар, бентонит, целлюлозу и древесные продукты, природную губку, катионнообменные смолы, карбонат кальция, силикаты, карбонат натрия, поперечно-сшитый поли(винилпирролидон)(кросповидон), натрий карбоксиметил крахмал (натрий крахмал гликолят), карбоксиметилцеллюлозу, поперечно-сшитую натрий карбоксиметил целлюлозу (кросскармелозу), метилцеллюлозу, прежелатинизированный крахмал (крахмал 1500), микрокристаллический крахмал, нерастворимый в воде крахмал, кальций карбоксиметил целлюлозу, силикат алюминия магния (Veegum), лаурилсульфат натрия, соединения четвертичного аммония, а также их комбинации.
Иллюстративные поверхностно-активные вещества и/или эмульгаторы включают без ограничения природные эмульгаторы (например, гуммиарабик, агар, альгиновую кислоту, альгинат натрия, трагакант, хондрус, холестерин, ксантан, пектин, желатин, яичный желток, казеин, ланолин, холестерин, воск и лецитин), коллоидные глины (например, бентонит [силикат алюминия] и Veegum [силикат магния алюминия]), производные аминокислот с длинными цепями, спирты высокой молекулярной массы (например, стеариловый спирт, цетиловый спирт, олеиловый спирт, триацетинмоностеарат, этиленгликоль дистеарат, глицерил моностеарат и пропиленгликоль моностеарат, поливиниловый спирт), карбомеры (например, карбоксиполиметилен, полиакриловую кислоту, полимеры акриловой кислоты и карбоксивиниловые полимеры), каррагинан, производные целлюлозы (например, натрий карбоксиметилцеллюлозу, порошкообразную целлюлозу, гидроксиметилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропил метилцеллюлозу, метилцеллюлозу), сложные эфиры сорбитана и жирных кислот (например, полиоксиэтиленсорбитана монолаурат [Tween 20], полиоксиэтиленсорбитан [Tween 60], полиоксиэтиленсорбитана моноолеат [Tween 80], сорбитана монопальмитат [Span 40], сорбитана моностеарат [Span 60], сорбитана тристеарат [Span 65], глицерил моноолеат, сорбитана моноолеат [Span 80]), сложные эфиры полиоксиэтилена (например, полиоксиэтилена моностеарат [Myrj 45], полиоксиэтилен гидрированное касторовое масло, полиэтоксилированное касторовое масло, полиоксиметилен стеарат и Solutol), сложные эфиры сахарозы и жирных кислот, сложные эфиры полиэтиленгликоля и жирных кислот (например, Cremophor), простые эфиры полиоксиэтилена (например, лауриловый простой эфир полиоксиэтилена [BriJ 30]), поли(винилпирролидон), монолаурат диэтиленгликоля, олеат триэтаноламина, олеат натрия, олеат калия, этилолеат, олеиновую кислоту, этиллаурат, лаурилсульфат натрия, Pluronic F68, Poloxamer 188, бромид цетримония, хлорид цетилпиридиния, хлорид бензалкония, докузат натрия и т.д. и/или их комбинации.
Иллюстративные связывающие агенты включают без ограничения крахмал (например, кукурузный крахмал или крахмальный клей), желатин, сахара (например, сахарозу, глюкозу, декстрозу, декстрин, мелассу, лактозу, лактит, маннит), природные и синтетические смолы (например, гуммиарабик, альгинат натрия, экстракт ирландского мха, камедь панвар, камедь гхатти, растительный клей из шелухи, карбоксиметилцеллюлозу, метилцеллюлозу, этилцеллюлозу, гидроксиэтилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, микрокристаллическую целлюлозу, ацетат целлюлозы, поливинилпирролидон, силикат алюминия магния (Veegum) и арабиногалактана лиственницу), альгинаты, полиэтиленоксид, полиэтиленгликоль, неорганические соли кальция, кремниевую кислоту, полиметакрилаты, воски, воду, спирт и их комбинации.
Иллюстративные консерванты могут включать антиоксиданты, хелатообразующие агенты, противомикробные консерванты, противогрибковые консерванты, спиртовые консерванты, кислотные консерванты и другие консерванты. Примеры антиоксидантов включают, не ограничиваясь этим, альфа токоферол, аскорбиновую кислоту, аскорбилпальмитат, бутилированный гидроксианизол, бутилированный гидрокситолуол, монотиоглицерин, метабисульфит калия, пропионовую кислоту, пропилгаллат, аскорбат натрия, бисульфит натрия, метабисульфит натрия и сульфит натрия. Примеры хелатообразующих агентов включают этилендиаминтетрауксусную кислоту (EDTA), моногидрат лимонной кислоты, динатрий эдетат, дикалий эдетат, этилендиаминтетрауксусную кислоту, фумаровую кислоту, яблочную кислоту, фосфорную кислоту, эдетат натрия, винную кислоту и тринатрий эдетат. Примеры противомикробных консервантов включают, не ограничиваясь этим, хлорид бензалкония, хлорид бензетония, бензиловый спирт, бронопол, цетримид, хлорид цетилпиридиния, хлоргексидин, хлорбутанол, хлоркрезол, хлорксиленол, крезол, этиловый спирт, глицерин, гексетидин, имидмочевину, фенол, феноксиэтанол, фенилэтиловый спирт, нитрат фенилртути, пропиленгликоль и тимеросал. Примеры противогрибковых консервантов включают, не ограничиваясь этим, бутилпарабен, метилпарабен, этилпарабен, пропилпарабен, бензойную кислоту, гидроксибензойную кислоту, бензоат калия, сорбат калия, бензоат натрия, пропионат натрия и сорбиновую кислоту. Примеры спиртовых консервантов включают, не ограничиваясь этим, этанол, полиэтиленгликоль, фенол, фенольные соединения, бисфенол, хлорбутанол, гидроксибензоат и фенилэтиловый спирт. Примеры кислотных консервантов включают, не ограничиваясь этим, витамин А, витамин С, витамин Е, бета-каротин, лимонную кислоту, уксусную кислоту, дегидроуксусную кислоту, аскорбиновую кислоту, сорбиновую кислоту и фитиновую кислоту. Другие консерванты включают, не ограничиваясь этим, токоферол, токоферола ацетат, детероксима мезилат, цетримид, бутилированный гидроксианизол (ВНА), бутилированный гидрокситолуол (ВНТ), этилендиамин, лаурилсульфат натрия (SLS), лаурилэфирсульфат натрия (SLES), бисульфит натрия, метабисульфит натрия, сульфит калия, метабисульфит калия, Glydant Plus, Phenonip, метилпарабен, Germall 115, Germaben II, Neolone, Kathon и Euxyl. Согласно определенным вариантам осуществления консервант представляет собой антиоксидант.Согласно другим вариантам осуществления консервант представляет собой хелатообразующий агент.
Иллюстративные буферные агенты включают без ограничения цитратные буферные растворы, ацетатные буферные растворы, фосфатные буферные растворы, хлорид аммония, карбонат кальция, хлорид кальция, цитрат кальция, глюбионат кальция, глюцептат кальция, глюконат кальция, D-глюконовая кислота, глицерофосфат кальция, лактат кальция, пропановая кислота, левулинат кальция, пентановая кислота, двухосновный фосфат кальция, фосфорная кислота, трехосновный фосфат кальция, фосфат гидроксида кальция, ацетат калия, хлорид калия, глюконат калия, смеси калия, двухосновный фосфат калия, одноосновный фосфат калия, смеси фосфатов калия, ацетат натрия, бикарбонат натрия, хлорид натрия, цитрат натрия, лактат натрия, двухосновный фосфат натрия, одноосновный фосфат натрия, смеси фосфатов натрия, трометамин, гидроксид магния, гидроксид алюминия, альгиновая кислота, апирогенная вода, изотонический солевой раствор, раствор Рингера, этиловый спирт и их комбинации.
Иллюстративные смазывающие вещества включают без ограничения стеарат магния, стеарат кальция, стеариновую кислоту, диоксид кремния, тальк, солод, глицерил беганат, гидрогенизированные растительные масла, полиэтиленгликоль, бензоат натрия, ацетат натрия, хлорид натрия, лейцин, лаурилсульфат магния, лаурилсульфат натрия и их комбинации.
Иллюстративные масла включают без ограничения миндальное масло, масло семечек абрикоса, масло авокадо, масло бабассу, масло бергамота, масло семян черной смородины, масло бораго, масло можжевельника, масло ромашки, масло канолы, масло тмина, масло карнаубы, касторовое масло, коричное масло, масло какао, кокосовое масло, масло печени трески, масло кофе, кукурузное масло, масло семян хлопчатника, жир эму, эвкалиптовое масло, масло энотеры, рыбий жир, масло семян льна, гераниол, масло бутылочной тыквы, масло виноградных семян, масло фундука, масло иссопа, изопропилмиристат, масло жожоба, масло лакового дерева, лавандиновое масло, масло лаванды, масло лимона, масло лицеа кубеба, масло ореха макадамия, масло мальвы, масло семян манго, масло семян пенника лугового, жир норки, масло мускатного ореха, оливковое масло, апельсиновое масло, жир атлантического большеголова, пальмовое масло, масло ядер кокосового ореха, масло косточек персика, арахисовое масло, масло макового семени, масло тыквенных семян, масло семян рапса, масло рисовых отрубей, масло розмарина, саффлоровое масло, масло сандалового дерева, масло саскваны, масла душистых трав, масло облепихи крушинной, масло кунжута, масло дерева ши, силикон, соевое масло, подсолнечное масло, масло чайного дерева, масло артишока, масло цубаки (камелии), ветиверовое масло, масло грецкого ореха и масло зародышей пшеницы. Исллюстративные масла включают без ограничения бутилстеарат, триглицерид каприловой кислоты, триглицерид каприновой кислоты, циклометикон, диэтилсебацинат, диметикон 360, изопропилмиристат, минеральное масло, октилдодеканол, олеиловый спирт, силиконовое масло и их комбинации.
Жидкие лекарственные формы для парентерального введения включают без ограничения фармацевтически приемлемые липосомальные эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. В дополнение к активным ингредиентам жидкие лекарственные формы могут содержать инертные разбавители, обычно используемые в данной области техники, такие как, например, вода или другие растворители, солюбилизирующие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (в частности, хлопковое масло, арахисовое масло, кукурузное масло, масло жмыха зародышей, оливковое масло, касторовое масло и кунжутное масло), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и сложные эфиры жирных кислот и сорбитана и их смеси. Согласно определенным вариантам осуществления для парентерального введения конъюгаты согласно настоящему изобретению смешивают с солюбилизирующими агентами, такими как полиэтоксилированное касторовое масло (например, CREMOPHOR™), спирты, масла, модифицированные масла, гликоли, полисорбаты, циклодекстрины, полимеры и их комбинации.
Препараты для инъекций, например, стерильные водные или масляные суспензии для инъекций, могут быть составлены в соответствии с известным уровнем техники с использованием подходящих диспергирующих или смачивающих агентов и суспендирующих агентов. Стерильный препарат для инъекции может представлять собой стерильный инъекционный раствор, суспензию или эмульсию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. В число приемлемых носителей и растворителей, которые могут быть использованы, входят вода, раствор Рингера, U.S.Р. и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды обычно применяют стерильные нелетучие масла. Для этой цели можно использовать любое легкое нелетучее масло, включая синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, применяют для получения препаратов для инъекции. В качестве альтернативы, препарат может быть в форме липосом.
Составы для инъекций могут быть стерилизованными, например, путем фильтрации через фильтр, удерживающий бактерии, или путем включения стерилизующих агентов в виде стерильных твердых композиций, которые могут быть растворены или диспергированы в стерильной воде или другой стерильной среде для инъекций перед применением.
Чтобы продлить действие лекарственного средства, часто желательно замедлить всасывание лекарственно средства при подкожной или внутримышечной инъекции. Это может быть достигнуто посредством использования жидкой суспензии кристаллического или аморфного материала с плохой растворимостью в воде. Тогда скорость всасывания лекарственного средства будет зависеть от его скорости растворения, которая, в свою очередь, может зависеть от размера и формы кристаллов. В качестве альтернативы, замедленное всасывание парентерально вводимой лекарственной формы достигают путем растворения или суспендирования лекарственного средства в масляном носителе.
Пептиды согласно настоящему изобретению могут быть в микрокапсулированной форме с одним или более вспомогательными веществами, как указано выше. Согласно одному варианту осуществления пептиды согласно настоящему изобретению составлены в липосомах.
Должно быть ясно, что пептиды и фармацевтические композиции согласно настоящему изобретению можно использовать в комбинированных терапиях. Конкретная комбинация терапий (терапевтических средств или процедур) для применения в комбинированном режиме будет учитывать совместимость желаемых терапевтических средств и/или процедур и желаемый терапевтический эффект, который должен быть достигнут. Должно быть ясно, что применяемые терапии могут достигать желаемого эффекта для одной и той же цели (например, конъюгат согласно настоящему изобретению, полезный для обнаружения опухолей, можно вводить одновременно с другим агентом, полезным для обнаружения опухолей), или они могут достигать разных эффектов (например, контроль любых побочных эффектов).
Фармацевтическую композицию согласно настоящему изобретению можно вводить либо отдельно, либо в комбинации с одним или более другими терапевтическими средствами. Под «в сочетании с» не подразумевается, что агенты должны вводиться одновременно и/или быть составлены для совместной доставки, хотя эти способы доставки входят в объем настоящего изобретения. Композиции можно вводить одновременно с одним или более другими желаемыми терапевтическими средствами или медицинскими процедурами, до или после них. Как правило, каждый агент будет вводиться при дозе и/или по графику, определенному для этого агента. Кроме того, настоящее изобретение охватывает доставку пептидов или фармацевтических композиций в комбинации с агентами, которые могут улучшать их биодоступность, снижать и/или модифицировать их метаболизм, ингибировать их выведение и/или модифицировать их распределение в организме.
Конкретная комбинация терапий для применения в комбинированной схеме будет учитывать совместимость желаемых терапевтических средств и/или процедур, и/или желаемый терапевтический эффект, который должен быть достигнут. Следует понимать, что применяемые терапии могут достигать желаемого эффекта при одном и том же нарушении (например, пептид согласно настоящему изобретению можно вводить одновременно с другим биологически активным агентом, используемым для лечения того же нарушения), и/или они могут приводить к разным эффектам (например, контроль любых побочных эффектов). Далее понятно, что биологически активные агенты, используемые в этой комбинации, можно вводить вместе в одной композиции или вводить раздельно в разных композициях.
Выражение «в комбинации с» также включает возможность конъюгации (посредством химико-физических взаимодействий) пептида согласно настоящему изобретению с любым из дополнительных агентов, упомянутых выше и ниже, которые могут быть либо терапевтическими агентами, либо агентами для улучшения профиля пептида (например, биодоступности), среди прочего.
Согласно одному варианту осуществления пептиды согласно настоящему изобретению вводят в комбинации с одним или более противораковыми агентами. Противораковым агентом может быть, например, без ограничения метотрексат, винкристин, адриамицин, цисплатин, не содержащие сахар хлорэтилнитрозомочевины, 5-фторурацил, митомицин С, блеомицин, доксорубицин, дакарбазин, таксол, фрагилин, мегламин GLA, валрубицин, кармустаин и полиферпосан, MMI270, BAY 12-9566, ингибитор фарнесилтрансферазы RAS, ингибитор фарнесилтрансферазы, ММР, MTA/LY231514, ЬУ264618/лометексол, Гламолек, CI-994, TNP-470, Гикамтин/Топотекан, РКС412, Валсподар/Р8С833, Новантрон/Митроксантрон, Метарет/Сурамин, Батимастат, Е7070, ВСН-4556, CS-682, 9-АС, AG3340, AG3433, Инцел/УХ-710, VX-853, ZD0101, ISI641, ODN 698, ТА 2516/Мармистат, ВВ2516/Мармистат, CDP 845, D2163, PD183805, DX895 if, Лемонал DP 2202, FK 317, Пицибанил/OK-432, AD 32/Валрубицин, Метастрон/производное стронция, Темодал/Темозоломид, Эвацет/липосомальный доксорубицин, Ютаксан/Паклитаксел, Таксол/Паклитаксел, Кселод/Капецитабин, Фуртулон/Доксифлуридин, Циклопакс/паклитаксел для перорального введения, Оральный Таксоид, SPU-077/Цисплатин, HMR 1275/Флавопиридол, СР-358 (774)/EGFR, СР-609 (754)/RAS онкогенный ингибитор, BMS-182751/платина для перорального введения, UFT (Tegafur/Uracil), Эргамизол/Левамизол, Енилурацил/776С85/5Fu энхансер, Кампто/Левамизол, Камптозар/Иринотекан, Томудекс/Ралтитрексед, Лейстатин/Кладрибин, Паксекс/Паклитаксел, Доксил/липосомальный доксорубицин, Келикс/липосомальный доксорубицин, Флудара/Флударабин, Фармарубицин/Эпирубицин, ДепоЦит, ZD 1839, LU 79553/Бис-Нафталимид, LU 103793/Доластин, Келикс/липосомальный доксорубицин, Гемзар/Гемцитабин, ZD 0473/Анормед, YM 116, «зерна» йода, ингибиторы CDK4 и CDK2, ингибиторы PARP, 04809/Дексифосфамид, Ифес/Меснекс/Ифосфамид, Вумон/Тенипозид, Параплатин/Карбоплатин, Плантинол/цисплатин, Вепезид/Этопозид, ZD 9331, Таксотер/Доцетаксел, пролекарство гуанина арабинозид, Аналог Таксана, нитрозомочевины, алкилирующие агенты, такие как мелфелан и циклофосфамид, Аминоглутетимид, Аспарагиназу, Бусульфан, Карбоплатин, Хлоромбуцил, Цитарабин HCl, Дактиномицин, Даунорубицин НС1, Эстрамустин фосфат натрия, Этопозид (VP 16-213), Флоксуридин, Фторурацил (5-FU), Флутамид, Гидроксимочевину (гидроксикарбамид), Ифосфамид, Интерферон Альфа-2а, Альфа-2b, Лейпролида ацетат (аналог фактора высвобождения LHRH), Ломустин (CCNU), Мехлорэтамин HCl (азотный аналог горчичного газа), Меркаптопурин, Месну, Митотан, Митоксантрон HCl, Октреотид, Пликамицин, Прокарбазин HCl, Стрептозоцин, Тамоксифена цитрат, Тиогуанин, Тиотепу, Винбластина сульфат, Амсакрин (m-AMSA), Азацитидин, Эритропоэтин, Гексаметилмеламин (НММ), Интерлейкин 2, Митогуазон (метил-GAG; метилглиоксаль-бис-гуанилгидразон; MGBG), Пентостатин (2'-дезоксикоформицин), Семустин (метил-CCNU), Тенипозид (VM-26) или Виндезина сульфат, ингибиторы сигнальной трансдукции (такие как ингибиторы МЕК, BRAF, АКТ, her2, mTOR и PI3K).
Как проиллюстрировано ниже, пептиды согласно первому аспекту настоящего изобретения полезны для терапевтического лечения меланомы, особенно метастатической меланомы, путем снижения пролиферации злокачественных меланоцитов. Согласно одному варианту осуществления, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, когда пептид или фармацевтическую композицию применяют с терапевтической целью, их вводят перорально или парентерально.
Настоящее изобретение также относится к нетерапевтическому применению пептида или его косметической соли для регулирования меланогенеза, в частности, для уменьшения или увеличения продукции меланина. Все варианты осуществления, представленные выше в отношении пептида и косметической композиции, также являются вариантами осуществления этого аспекта. Согласно одному варианту осуществления, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид предназначен для применения для лечения гиперпигментации (посредством уменьшения количества меланина) или гипопигментации (посредством увеличения количества меланина). Согласно другому варианту осуществления нетерапевтического применения, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, оно регулирует меланогенез в коже или волосах, в частности в коже. Согласно другому варианту осуществления, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, субъект не страдает раком кожи. Согласно одному варианту осуществления, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, когда пептид или косметическую композицию применяют для нетерапевтической/косметической цели, их применяют местно.
Настоящее изобретение также относится к косметическому способу лечения гипер-или гипопигментации, предусматривающему применение пептида или его косметической соли, как определено согласно первому аспекту, или косметической композиции, как определено согласно второму аспекту настоящего изобретения. Этот косметический способ не охватывает терапевтический способ. Все варианты осуществления, приведенные выше в отношении пептида и косметической композиции, также являются вариантами осуществления данного аспекта. Согласно одному варианту осуществления косметического способа, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или косметическую композицию наносят на кожу и/или волосы. Согласно одному варианту осуществления косметического способа, необязательно в комбинации с любым из вариантов осуществления, приведенных выше или ниже, пептид или косметическую композицию наносят на кожу.
Настоящее изобретение также относится к пигментирующей композиции, такой как местная косметическая или фармацевтическая пигментирующая композиция, содержащая пептид или его соль, как определено в любом из вариантов осуществления, приведенных выше.
Настоящее изобретение также относится к депигментирующей композиции, такой как местная косметическая или фармацевтическая депигментирующая композиция, содержащая пептид или его соль, как определено в любом из вариантов осуществления, приведенных выше.
Во всем описании и формуле изобретения слово «содержать» и варианты этого слова не предназначены для исключения других технических признаков, добавок, компонентов или стадий. Кроме того, слово «содержать» охватывает случай «состоящий из». Дополнительные цели, преимущества и признаки настоящего изобретения станут очевидными для специалистов в данной области техники при изучении описания или могут быть изучены при практическом осуществлении настоящего изобретения. Следующие примеры представлены в целях иллюстрации и не предназначены для ограничения настоящего изобретения. Кроме того, настоящее изобретение охватывает все возможные комбинации конкретных и предпочтительных вариантов осуществления, описанных в настоящем документе.
Примеры
1. Материалы и способы
Общая методика синтеза
Соединения IDP-F
Материалы приобретали следующим образом: Fmoc-защищенные а-аминокислоты (-), амидная смола Ринка МВНА (Tianjin Nankai HECHENG S&T Co., Ltd), HBTU ((2-(1Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония гексафторфосфат), GL Biochem), N-метилморфолин (Sinopharm Chemical Reagent Co., Ltd.), янтарный ангидрид (Aladdin), ацетонитрил (Xingke Chemical), нингидрин (Sinopharm Chemical Reagent Co., Ltd.), пиперидин (Vertellus), диметилформамид, DMF (Zhejiang jiangshan chemical со., Ltd), трифторуксусная кислота, TFA (трифторуксусная кислота, Solvay), TIS (тиоанизол, Solvay)
Кратко, линейные полипептиды синтезировали вручную с использованием SPPS (твердофазный синтез пептидов) на основе Fmoc на амидной смоле Ринка МВНА в качестве носителя.
Использовали следующий протокол:
1. Защитную группу Fmoc удаляли с помощью 20% пиперидина в DMF.
2. Смолу промывали с помощью DMF пять раз.
3. Последующую Fmoc-защищенную аминокислоту связывали в течение 45 мин с использованием Fmoc-AA (3 экв.), HBTU (3 экв.) и N-метилморфолина (6 экв.).
4. Смолу промывали с помощью DMF пять раз. Связывание проверяли посредством нингидриновой реакции.
5. Повторяли начиная со стадии 1.
6. N-терминальный конец кэппировали посредством реакции с янтарным ангидридом (10 экв.) и N-метилморфолином (10 экв.).
Пептид отщепляли от смолы и удаляли защитную группу путем воздействия раствора F (95% TFA, 2,5% воды, 2,5% TIS), и лиофилизировали.
Лиофилизированные пептиды очищали посредством ВЭЖХ с обращенной фазой с использованием колонки С18 (детали см. в характеристике соединений). Пептиды идентифицировали с помощью LC-MS-ESI. Все масс-спектральные данные для всех соединений приведены ниже в таблице 1.
Материалы приобретали следующим образом: Fmoc-защищенные а-аминокислоты (включают олефиновые аминокислоты Fmoc-[(S)-2-(4 пентенил)аланин]ОН, Fmoc-[(R)-2-(4-пентенил)аланин]ОН, Emoc-[(8)-2-(7-октенил)аланин]ОН, Fmoc-[(R)-2-(4пентенил)аланин] ОН, 2-(6-хлор-1-Н-бензотриазол-1-ил)-1,1,3,3-тетраметиламиния гексафторфосфат (TBTU), смолы, диметилформамид (DMF), N,N-диизопропилэтиламин (DIEA), трифторуксусная кислота (TFA), 1,2-дихлорэтан (DCE), катализатор Граббса Ru(IV) и пиперидин приобретали у различных поставщиков.
Кратко, линейные полипептиды синтезировали на автоматическом синтезаторе с использованием твердофазной химии пептидов Fmoc. Только связывание с олефиновыми аминокислотами выполняли вручную после удаления смол из реакционного сосуда, как описано в предшествующей части.
Реакцию метатезиса с замыканием кольца проводили в растворе с катализатором Граббса первого поколения после отщепления линейного пептида от смолы, как описано Scott J. М. и коллегами (Scott J.M. et al., «Application of Ring-Closing Metathesis to the Synthesis of Rigidified Amino Acids and Peptides», 1996, J. Am. Chem. Soc, 1996, 118 (40), pp 9606 9614).
Пептид с удаленной защитной группой осаждали метил-трет-бутиловым простым эфиром при 4°С и лиофилизировали.
Лиофилизированные пептиды очищали посредством ВЭЖХ с обращенной фазой с использованием колонки С18 (подробности см. в характеристике соединений). Пептиды идентифицировали с помощью LC-MS-ESI. Все масс-спектральные данные для всех соединений приведены ниже в таблице 1.
Условия ВЭЖХ:
IDP-F05. Соединение очищали посредством ВЭЖХ-RP (С-18 колонка, подвижная фаза А: H2O с 0,1% TFA, подвижная фаза В: ацетонитрил с 0,1% TFA) с применением линейного градиента 30%-40% В в течение 20 минут (R. Т.=10,2). Степень чистоты 95,06% посредством ВЭЖХ,
IDP-F13. Соединение очищали посредством ВЭЖХ-RP (С-18 колонка, подвижная фаза А: H2O с 0,1% TFA, подвижная фаза В: ацетонитрил с 0,1% TFA) с применением линейного градиента 32%-42% В в течение 20 минут (R. Т.=14,26). Степень чистоты 97,5% посредством ВЭЖХ,
IDP-F16. Соединение очищали посредством ВЭЖХ-RP (С-18 колонка, подвижная фаза А: H2O с 0,1% TFA, подвижная фаза В: ацетонитрил с 0,1% TFA) с применением линейного градиента 35%-45% В в течение 20 минут (R. Т.=7,30). Степень чистоты 95,7% посредством ВЭЖХ,
IDP-F18. Соединение очищали посредством ВЭЖХ-RP (С-18 колонка, подвижная фаза А: H2O с 0,1% TFA, подвижная фаза В: ацетонитрил с 0,1% TFA) с применением линейного градиента 51%-61% В в течение 20 минут (R. Т.=10,97-11,97). Степень чистоты 95,6% посредством ВЭЖХ,
IDP-F22. Соединение очищали посредством ВЭЖХ-RP (С-18 колонка, подвижная фаза А: H2O с 0,1% TFA, подвижная фаза В: ацетонитрил с 0,1% TFA) с применением линейного градиента 53%-63% В в течение 20 минут (R. Т.=10,1-11,36). Степень чистоты 97,06% посредством ВЭЖХ,
IDP-F29. Соединение очищали посредством ВЭЖХ-RP (С-18 колонка, подвижная фаза А: H2O с 0,1% TFA, подвижная фаза В: ацетонитрил с 0,1% TFA) с применением линейного градиента 30%-40% В в течение 20 минут (R. Т.=8,91). Степень чистоты ≤50% посредством ВЭЖХ,
IDP-F31. Соединение очищали посредством ВЭЖХ-RP (С-18 колонка, подвижная фаза А: H2O с 0,1% TFA, подвижная фаза В: ацетонитрил с 0,1% TFA) с применением линейного градиента 38%-48% В в течение 20 минут (R. Т.=10,65). Степень чистоты 95,49% посредством ВЭЖХ,
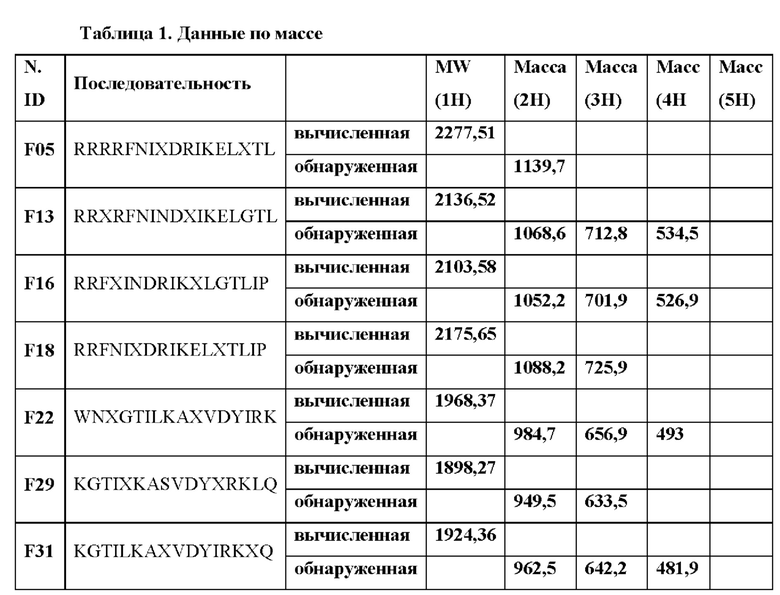
Бирадикал X представляет собой соединений формулы:
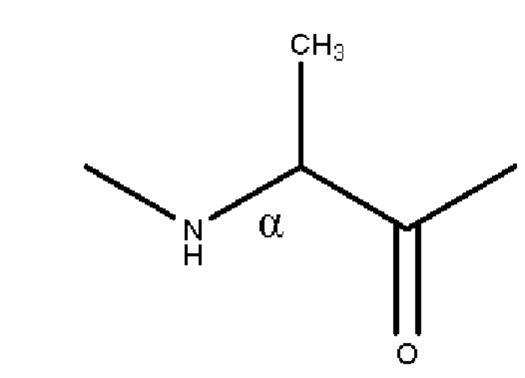
и бирадикал L, соответствующий -(CH2)3-СН=СН-(CH2)3- или -(CH2)6-СН=СН-(CH2)3-, связывает оба радикала X в каждой последовательности.
Клеточные линии:
SK-MEL-28, кожа, злокачественная меланома человека, АТСС-НТВ-72™.
IGR-37, кожа, меланома человека, происходящая из места метастазирования: паховый лимфатический узел.
IGR-39, кожа, меланома человека, происходящая из места метастазирования: паховый лимфатический узел.
B16-F10, кожа, мышиная меланома, ATCC-CRL-6475™.
501-MEI, кожа, злокачественная меланома человека.
Клеточная культура
Клеточные линии SK-MEL-28, IGR-37, IGR-39, B16-F10, 501-MEL и А-375 культивировали в инкубаторе при 37°С в среде Игла, модифицированной Дульбекко (Invitrogen Life Technologies, Foster City, CA), содержащей 10% инактивированной фетальной телячьей сыворотки (FBS, Dutscher, France), пенициллин (50 ЕД/мл) и сульфат стрептомицина (50 мг/мл) (Gibco BRL, Germany). В ходе стадии амплификации и анализа прилипшие клетки промывали DPBS (физиологический раствор, забуференный фосфатом Дульбекко, Sigma D1283) три раза, а затем обрабатывали в течение 5 минут трипсином ([0,5 г/мл]/ЕЭТА [0,2 г/мл]) (Gibco-BRL, 15400054) в растворе DPBS при 37°С, и сразу после отделения переносили в культуральную среду. Клетки подсчитывали в камере Нейбауэра после мечения с Tripan-Blue. Каждый анализ проводили только тогда, когда жизнеспособность превышала 90%.
Анализ жизнеспособности
Клеточные линии SK-MEL-28, IGR-37, B16-F10, 501-MEL и А-375 высевали с плотностью 1000 клеток/лунку на 96-луночные планшеты. Через 24 часа добавляли тестируемые соединения для вычисления эффективности при концентрации 10 мкМ с серийными разведениями. Контролями были необработанные клетки. Каждый эксперимент проводили с тремя повторениями.
Клетки инкубировали в течение 72 ч в инкубаторе в атмосфере СО2 при 37°С. Жизнеспособность клеток измеряли с помощью колориметрического МТТ (3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия бромид). МТТ инкубировали еще 4 ч, после чего среду удаляли. DMSO добавляли для растворения формазанового продукта и измеряли оптическую плотность при 570 нм с помощью устройства для считывания микропланшетов (MULTISKAN, Labsystems). Проценты жизнеспособности клеток вычисляли путем деления значения оптической плотности клеток, обработанных данным соединением, на значение оптической плотности необработанных клеток.
Статистический анализ
Анализ данных проводили путем вычисления процента нормализованной жизнеспособности клеток по сравнению со значениями отрицательного контроля, который считали равным 100%. Кривую доза/ответ строили с помощью сигмоидального уравнения доза-ответ (переменный наклон), а значения ЕС50 вычисляли следующим образом:
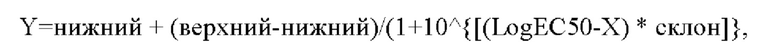
где X представляет собой концентрацию соединения (масштаб log), a Y представляет собой ответ.
Вычисления и построения графиков проводили с применением GraphPad Prism (Prism 6 для Windows).
2. Результаты
2.1 Результаты по эффективности
В таблицах 2а, 2b и 2с приведена антипролиферативная активность для нескольких клеточных линий меланомы при 10 мкМ.
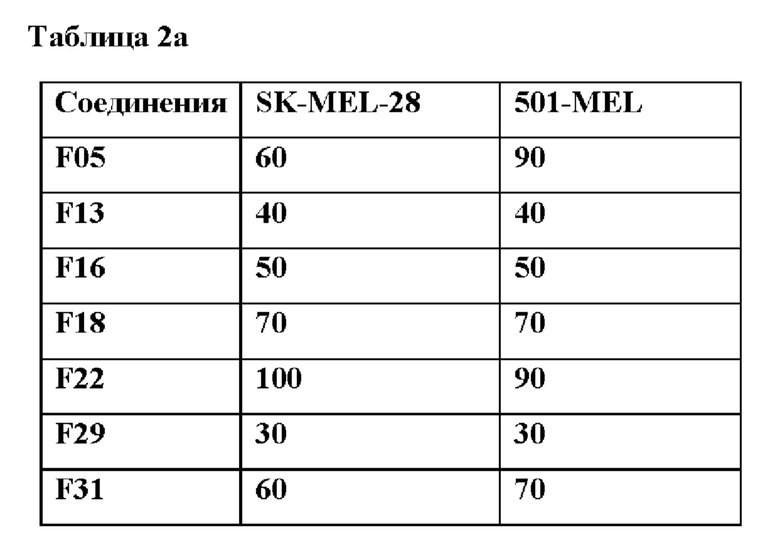


Все пептиды согласно настоящему изобретению проявляют значительную противораковую активность в отношении протестированных клеточных линий меланомы, даже агрессивных фенотипов.
2.2 Измерение содержания меланина в клетках меланомы B16-F10
Клетки меланомы B16-F10 высевали в культуральную колбу объемом 25 см2 и инкубировали в течение 24 часов. Затем добавляли 0,1 мкМ α-MSH и клетки обрабатывали вышеупомянутыми пептидами в дозах ниже соответствующих IC50 в течение 48 часов инкубации. После двукратной промывки фосфатно-солевым буфером клетки растворяли в 1 мл 1Н NaOH. Для измерения содержания меланина аликвоты по 100 мкл раствора затем помещали на 96-луночные планшеты и измеряли оптическую плотность при 450 нм с помощью считывателя микропланшетов. Активность против меланина выражали в процентном содержании меланина по отношению к необработанным клеткам меланомы. В качестве положительного контроля использовали койевую кислоту (КА) при различных концентрациях (0,1, 1 и 10 мкМ).
Результаты суммированы на фиг. 1. Как видно, пептиды согласно настоящему изобретению участвуют в пути меланогенеза. Таким образом, одни пептиды стимулируют продукцию меланина, что может быть признаком активации меланоцитов, тогда как другие, такие как F22 и F29, резко снижают количество меланина. Еще более примечательным является тот факт, что пептиды согласно настоящему изобретению более эффективно регулируют меланоциты по сравнению с другими соединениями. В связи с этим было обнаружено, что при использовании КА при концентрации 1 мкМ снижение было существенно ниже, чем снижение, достигаемое при использовании пептида согласно настоящему изобретению F22 при той же концентрации.
Таким образом, эти данные не только подтверждают влияние пептидов согласно настоящему изобретению на активность меланоцитов, но также показывают, что они даже более эффективны, чем другие соединения, доступные в имеющемся на сегодняшний день уровне техники, которые в настоящее время используются с той же целью.
2.3 Определения депигментирующей активности на эмбрионах рыбок данио.
Формирование пигмента пигментным эпителием сетчатки (RPE) в ходе развития рыбок данио начинается приблизительно через 24 часа после оплодотворения, а затем прогрессирует в направлении дорсолатеральной кожи, где меланоциты распределяются. Количественное биохимическое определение меланина проводили на необработанных эмбрионах по сравнению с эмбрионами, обработанными соединением F22. F22 растворяли в IX PBS до сток-раствора. Для того, чтобы приступить к инкубации эмбрионов рыбок данио с лекарственным средством, F22 серийно разбавляли в среде ЕЗ, с получением 2,5 мкМ в конечном объеме 1 мл.
Количественный анализ меланина
Собирали по 50 эмбрионов на исследование с тремя повторениями и растворяли в лизирующем буфере при 95°С в течение 30 минут.200 мкл раствора помещали на 96-луночный планшет и количественно определяли общее содержание меланина с использованием спектрометра при 490 нм. Результаты сравнивали с синтетическим меланином. Получали стандартную кривую путем нанесения на график среднего значения измерения при 490 нм с поправкой на фон для каждого стандарта меланина в зависимости от его концентрации в мкг/мл. Стандартную кривую использовали для определения концентрации белка меланина в каждом неизвестном образце.
Анализ изображений:
Эмбрионы помещали в роботизированную микрофлюидную систему VAST (Union Biometrica), которая позволяет автоматически осуществлять аспирацию, размещение и вращение зародышей под микроскопом (Leica, DM6-B). После того, как эмбрионы были расположены под прямым углом (вид сверху), изображения получали с помощью бортовой камеры VAST. Для каждого зародыша было получено одно верхнее изображение. Для количественной оценки использовали программу FIJI. Изображения RGB преобразовывали в 8-ми битные и определяли ориентацию зародышей. Фиксированный порог применяли для создания бинарных масок изображений. Конкретную область представляющих интерес ROI выбирали в зависимости от ориентации зародыша. ROI генерировали таким образом, что глаза были исключены из количественного определения. Затем измеряли сегментированные области внутри ROI с помощью команды «Анализ пикселей». Уровень пигментации представляли как сумму всех пикселей в этих областях.
Результаты. Количественное определение меланина


На основании обоих используемых количественных оценок можно сделать вывод, что существуют доказательства депигментирующего эффекта соединения F22 при концентрации 2,5 мкМ при анализе количества биохимического меланина и сравнении с анализом исследования изображений.
Перечень процитированных источников
Altschul et al., «Basic local alignment search tool», 1990, J. Mol. Biol, v. 215, pages 403-410,
Copolovici D. M. et al., «Cell-Penetrating Peptides: Design, Synthesis, and Applications)), 2014, ACS Nano, 2014, 8 (3), pp 1972-1994,
Higgins et al., «CLUSTAL V: improved software for multiple sequence alignment)), 1992, CABIOS, 8(2), pages 189-191,
Kim Young-Woo et al., «Synthesis of all-hydrocarbon stapled a-helical peptides by ring-closing olefin metathesis)), Nature Protocols, 2011, 6(6), p.761-771,
Kolb H.C. et al., «The growing impact of click chemistry on drug discovery)), 2003, Drug Discov Today, 8(24): 1128-1137), и
Scott J.M. et al., «Application of Ring-Closing Metathesis to the Synthesis of Rigidified Amino Acids and Peptides)), 1996, J. Am. Chem. Soc, 1996, 118 (40), pp 9606-9614.
В целях полноты различные аспекты настоящего изобретения изложены в следующих пронумерованных пунктах:
Пункты
1. Пептид или его фармацевтически или косметически приемлемая соль, причем пептид имеет аминокислотную последовательность, на по меньшей мере 85% идентичную последовательности согласно SEQ ID NO: 1 или 2:

где
«m», «n», «р» и «q» представляют собой целые числа и выбраны из 0 и 1,
«mx», «nx», «рх» и «qx» представляют собой целые числа и выбраны из 0 и 1,
причем С-терминальный конец соответствует С(O)R4,
причем N-терминальный конец соответствует -NHR5,
R4 представляет собой радикал, выбранный из группы, состоящей из -ОН и -NR17R18,
R5 представляет собой радикал, выбранный из группы, состоящей из -Н, (C1-С20)алкила и (С1-С10)алкила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (С1-С10)алкила, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12, и
R17 и R18 представляют собой радикалы, независимо выбранные из группы, состоящей из -Н, (С1-С10)алкила и (С1-С10)алкила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (С1-С10)алкила, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12, причем пептид необязательно включает линкерный бирадикал «L» формулы (I)
-[(R1)a-(R2)-(R3)b]c- (I),
который представляет собой соединение альфа-атома углерода аминокислоты, расположенной в положении с альфа-атомом углерода аминокислоты, расположенной в положении «i+4» или «i+7» в пептидной последовательности,
где
«а» и «b» являются одинаковыми или различными и представляют собой 0 или 1, «с» составляет от 1 до 10,
R1 и R3 представляют собой бирадикалы, независимо выбранные из группы, состоящей из (С1-С10)алкила, (С1-С10)алкила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (С1-С10)алкила, -ORe, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12, (С2-С10)алкенила, (С2-С10)алкенила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (С1-С10)алкила, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12, (С2-С10)алкинила и (С2-С10)алкинила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (С1-С10)алкила, -CR6, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12,
R2 представляет собой бирадикал, выбранный из группы, состоящей из -О-, С(=O), C(=O)NR13, С(=O)O, S(=O), S(=O)2, NR14, (С1-С10)алкила, (С2-С10)алкенила, (С2-С10)алкинила, -NR15-NR16-, -N=N-, -S-S- и известной кольцевой системы, содержащей от 3 до 14 членов, причем система содержит от 1 до 3 колец, где:
каждое из колец является насыщенным, частично ненасыщенным или ароматическим,
кольца являются изолированными, частично или полностью конденсированными, каждый из членов, образующих известную кольцевую систему, выбран из группы, состоящей из -СН-, -СН2-, -NH-, -N-, -SH-, -S- и -О-, и
кольцевая система необязательно замещена одним или более радикалами, независимо выбранными из группы, состоящей из галогена, -ОН, -NO2, (С1-С10)алкила, (С1-С10)галоалкила и (С1-С10)алкил-O-, и
R6, R7, R8, R9, R10, R11, R12, R13, R14, R15 и R16 представляют собой радикалы, независимо выбранные из группы, состоящей из -Н и (С1-С10)алкила, и
причем аминокислоты, которые соединены линкером, имеют формулу (II)
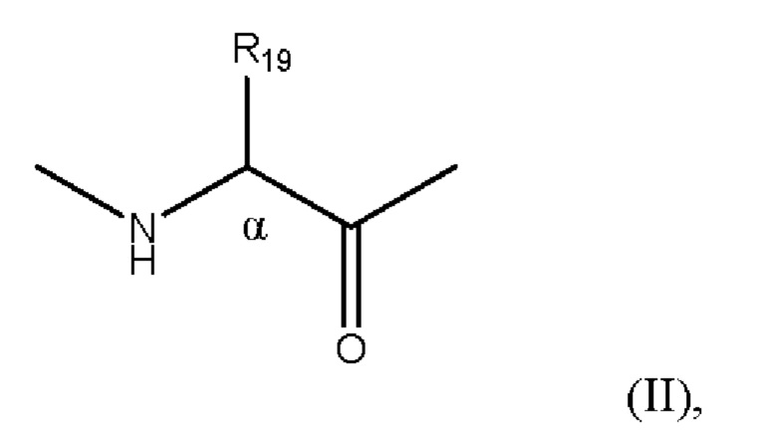
где
R19 представляет собой монорадикал, выбранный из группы, состоящей из (C1-С10)алкила, (С2-С10)алкенила, (С2-С10)алкинила и известной кольцевой системы, содержащей от 3 до 14 членов, причем система содержит от 1 до 3 колец, где:
каждое из колец является насыщенным, частично ненасыщенным или ароматическим,
кольца являются изолированными, частично или полностью конденсированными, каждый из членов, образующих известную кольцевую систему, выбран из группы, состоящей из -СН-, -СН2-, -NH-, -N-, -SH-, -S- и -О-.
2. Пептид согласно пункту 1, который имеет идентичность 100% с последовательностью согласно SEQ ID NO: 1 или 2.
3. Пептид согласно любому из предшествующих пунктов, где линкерный бирадикал формулы (I) расположен между альфа-атомом углерода аминокислоты, расположенной в положении «i» в пептидной последовательности согласно SEQ ID NO: 1, и альфа-атомом углерода аминокислоты, расположенной в положении «i+7» в пептидной последовательности согласно SEQ ID NO: 1, или, в качестве альтернативы, расположен между альфа-атомом углерода аминокислоты, расположенной в положении «i» в пептидной последовательности согласно SEQ ID NO: 2, и альфа-атомом углерода аминокислоты, расположенной в положении «i+7» в пептидной последовательности согласно SEQ ID NO: 2.
4. Пептид согласно любому из предшествующих пунктов, где а=b=с=1.
5. Пептид согласно любому из предшествующих пунктов, где
R1 и R3 представляют собой бирадикалы, независимо выбранные из группы, состоящей из (С1-С10)алкила, (С2-С10)алкенила и (С2-С10)алкинила,
R2 представляет собой бирадикал, выбранный из группы, состоящей из (C1-С10)алкила, (С2-С10)алкенила и (С2-С10)алкинила, и
R19 представляет собой монорадикал, выбранный из группы, состоящей из (C1-С10)алкила, (С2-С10)алкенила и (С2-С10)алкинила.
6. Пептид согласно любому из предшествующих пунктов, где R1, R3 и R19 представляют собой (С1-С10)алкил, и R2 представляет собой (С2-С10)алкенил.
7. Пептид согласно любому из предшествующих пунктов, где С-терминальный конец соответствует -С(O)ОН или -C(O)NH2, и N-терминальный конец соответствует -NH2.
8. Пептид согласно любому из предшествующих пунктов, который на по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% или 100% идентичен пептидной последовательности SEQ ID NO: 3-16, где «L», «R19», «m», «n», «p», «q», «mx», «nx», «рх» и «qx» имеют значения, как определено в любом из предшествующих пунктов.
9. Пептид согласно любому из предшествующих пунктов, который представляет собой пептид с аминокислотной последовательностью, на по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% или 100% идентичной аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 17-23.
10. Фармацевтическая или косметическая композиция, содержащая терапевтически или косметически эффективное количество пептида, как определено в любом из пунктов 1-9, вместе с приемлемыми фармацевтическими или косметическими вспомогательными веществами и/или носителями.
11. Нетерапевтическое применение пептида или его косметической соли, как определено в любом из пунктов 1-9, или косметической композиции, как определено в пункте 10, для регуляции меланогенеза, в частности для уменьшения или увеличения продукции меланина.
12. Нетерапевтическое применение пептида согласно пункту 11 для лечения гиперпигментации или гипопигментации.
13. Пептид или его фармацевтическая соль, как определено в любом из пунктов 1-9, или фармацевтическая композиция, как определено в пункте 10, для применения в качестве лекарственного средства.
14. Пептид или его фармацевтическая соль, как определено в любом из пунктов 1-9, или фармацевтическая композиция, как определено в пункте 10, для применения для лечения и/или профилактики рака, в частности меланомы, как например, метастатической меланомы.
15. Пептид или его фармацевтическая соль, как определено в любом из пунктов 1-9, или фармацевтическая композиция, как определено в пункте 10, для применения для лечения и/или профилактики заболевания, связанного с нарушением регуляции меланогенеза, в частности посредством ингибирования пролиферации злокачественных меланоцитов.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ИДП ДИСКАВЕРИ ФАРМА, С.Л.
<120> МЕЛАНОЦИТ-РЕГУЛИРУЮЩИЕ ПЕПТИДЫ
<130> P5219PC00
<150> EP19382674.0
<151> 2019-08-02
<160> 26
<170> PatentIn version 3.5
<210> 1
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<223> the peptide comprises a linker birradical of formula (I)
-[(R1)a-(R2)-(R3)b]c- connecting an amino acid at position "i"
with an amino acid at position "i+3" or "i+7"
<220>
<221> MISC_FEATURE
<223> R1 and R3 are birradicals independently selected from the group
consisting of: (C1-C10)alkyl; (C1-C10)alkyl substituted;
(C2-C10)alkenyl; (C2-C10)alkenyl substituted; (C2-C10)alkynyl;
and (C2-C10)alkynyl substituted;
<220>
<221> MISC_FEATURE
<223> "(C1-C10)alkyl substituted" means (C1-C10)alkyl substituted by
one or more radicals selected from: halogen, (C1-C10)alkyl, OR6
,NR7R8, SR9, SOR10, SO2R11 and CO2R12
<220>
<221> MISC_FEATURE
<223> "(C2-C10)alkenyl substituted" means (C2-C10)alkenyl substituted
by one or more radicals selected from: halogen, (C1-C10)alkyl,
OR6 ,NR7R8, SR9, SOR10, SO2R11 and CO2R12
<220>
<221> MISC_FEATURE
<223> "(C2-C10)alkynyl substituted" means (C2-C10)alkynyl substituted
by one or more radicals selected from: halogen, (C1-C10)alkyl,
OR6 ,NR7R8, SR9, SOR10, SO2R11 and CO2R12
<220>
<221> MISC_FEATURE
<223> R2 is a birradical selected from: -O-, C(=O), C(=O)NR13, C(=O)O,
S(=O), S(=O)2, NR14, (C1-C10)alkyl, (C2-C10)alkenyl,
(C2-C10)alkynyl, -NR15-NR16-, -N=N-, -S-S-, and a known ring
system comprising from 3 to 14 members optionally substituted
<220>
<221> MISC_FEATURE
<223> "a" and "b" are the same or different and are 0 or 1; and "c" is
comprised from 1 to 10
<220>
<221> MISC_FEATURE
<223> the amino acids which are connected by the linker of formula (I),
being of formula (II) -NH-C(R19)-C(=O)-, wherein R19 is a
monoradical selected from (C1-C10)alkyl, (C2-C10)alkenyl,
(C2-C10)alkynyl and a known ring system comprising from 3 to 14
<220>
<221> MISC_FEATURE
<223> the C-terminal end corresponds to -C(O)R4, wherein R4 is selected
from -OH and-NR17R18
<220>
<221> MISC_FEATURE
<223> the N-terminal end corresponds to -NHR5, wherein R5 is selected
from -H, (C1-C20)alkyl and C1-C10)alkyl substituted by one or
more radicals selected from the group consisting of: halogen,
(C1-C10)alkyl, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11, and -CO2R1
<220>
<221> MISC_FEATURE
<223> known ring system "optionally substituted" means that the system
is optionally substituted by one or more radicals independently
selected from halogen,OH,NO2,(C1-C10)alkyl,(C1-C10)haloalkyl and
(C1-C10)alkyl-O-
<220>
<221> MISC_FEATURE
<223> R6 to R16 are radicals independently selected from H and
(C1-C10)alkyl
<220>
<221> MISC_FEATURE
<223> R17 to R18 are radicals independently selected from H,
(C1-C10)alkyl, and (C1-C10)alkyl substituted by one or more
radicals selected from the group consisting of: halogen,
(C1-C10)alkyl, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11, and -CO2R12
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> X means (Trp)m, wherein m is 0 or 1
<220>
<221> MISC_FEATURE
<222> (2)..(2)
<223> X means (Asn)n, wherein n is 0 or 1
<220>
<221> MISC_FEATURE
<222> (17)..(17)
<223> X means (Leu)p, wherein p is 0 or 1
<220>
<221> MISC_FEATURE
<222> (18)..(18)
<223> X means (Gln)q, wherein q is 0 or 1
<400> 1
Xaa Xaa Lys Gly Thr Ile Leu Lys Ala Ser Val Asp Tyr Ile Arg Lys
1 5 10 15
Xaa Xaa
<210> 2
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<223> the peptide comprises a linker birradical of formula (I)
-[(R1)a-(R2)-(R3)b]c- connecting an amino acid at position "i"
with an amino acid at position "i+3" or "i+7"
<220>
<221> MISC_FEATURE
<223> R1 and R3 are birradicals independently selected from the group
consisting of: (C1-C10)alkyl; (C1-C10)alkyl substituted;
(C2-C10)alkenyl; (C2-C10)alkenyl substituted; (C2-C10)alkynyl;
and (C2-C10)alkynyl substituted;
<220>
<221> MISC_FEATURE
<223> "(C1-C10)alkyl substituted" means (C1-C10)alkyl substituted by
one or more radicals selected from: halogen, (C1-C10)alkyl,
OR6,NR7R8, SR9, SOR10, SO2R11 and CO2R12
<220>
<221> MISC_FEATURE
<223> "(C2-C10)alkenyl substituted" means (C2-C10)alkenyl substituted
by one or more radicals selected from: halogen, (C1-C10)alkyl,
OR6 ,NR7R8, SR9, SOR10, SO2R11 and CO2R12
<220>
<221> MISC_FEATURE
<223> "(C2-C10)alkynyl substituted" means (C2-C10)alkynyl substituted
by one or more radicals selected from: halogen, (C1-C10)alkyl,
OR6 ,NR7R8, SR9, SOR10, SO2R11 and CO2R12
<220>
<221> MISC_FEATURE
<223> R2 is a birradical selected from: -O-, C(=O), C(=O)NR13, C(=O)O,
S(=O), S(=O)2, NR14, (C1-C10)alkyl, (C2-C10)alkenyl,
(C2-C10)alkynyl, -NR15-NR16-, -N=N-, -S-S-, and a known ring
system comprising from 3 to 14 members optionally substituted
<220>
<221> MISC_FEATURE
<223> "a" and "b" are the same or different and are 0 or 1; and "c" is
comprised from 1 to 10
<220>
<221> MISC_FEATURE
<223> the amino acids which are connected by the linker of formula (I),
being of formula (II) -NH-C(R19)-C(=O)-, wherein R19 is a
monoradical selected from (C1-C10)alkyl, (C2-C10)alkenyl,
(C2-C10)alkynyl and a known ring system comprising from 3 to 14
<220>
<221> MISC_FEATURE
<223> the C-terminal end corresponds to -C(O)R4, wherein R4 is selected
from -OH and-NR17R18
<220>
<221> MISC_FEATURE
<223> the N-terminal end corresponds to -NHR5, wherein R5 is selected
from -H, (C1-C20)alkyl, and (C1-C10)alkyl substituted by one or
more radicals selected from the group consisting of: halogen,
(C1-C10)alkyl, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11, and -CO2R12
<220>
<221> MISC_FEATURE
<223> the "known ring system" comprises from 1 to 3 rings, each one of
the rings being (a) saturated, partially saturated or aromatic,
and (b) isolated, partially or totally fused; and each member
being selected from CH,CH2,NH,N,SH,S,and O
<220>
<221> MISC_FEATURE
<223> known ring system "optionally substituted" means that the system
is optionally substituted by one or more radicals independently
selected from halogen,OH,NO2,(C1-C10)alkyl,(C1-C10)haloalkyl and
(C1-C10)alkyl-O-
<220>
<221> MISC_FEATURE
<223> R6 to R16 are radicals independently selected from H and
(C1-C10)alkyl
<220>
<221> MISC_FEATURE
<223> R17 to R18 are radicals independently selected from H,
(C1-C10)alkyl, and (C1-C10)alkyl substituted by one or more
radicals selected from the group consisting of: halogen,
(C1-C10)alkyl, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11, and -CO2R12
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> X means (Arg)mx, wherein mx is 0 or 1
<220>
<221> MISC_FEATURE
<222> (2)..(2)
<223> X means (Arg)nx, wherein nx is 0 or 1
<220>
<221> MISC_FEATURE
<222> (18)..(18)
<223> X means (Ile)px, wherein px is 0 or 1
<220>
<221> MISC_FEATURE
<222> (18)..(18)
<223> X means (Pro)qx, wherein qx is 0 or 1
<220>
<221> misc_feature
<222> (19)..(19)
<223> Xaa can be any naturally occurring amino acid
<400> 2
Xaa Xaa Arg Arg Phe Asn Ile Asn Asp Arg Ile Lys Glu Leu Gly Thr
1 5 10 15
Leu Xaa Xaa
<210> 3
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (3)..(3)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of the amino acid at
position 10 by a linker "L"
<220>
<221> MISC_FEATURE
<222> (10)..(10)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of the amino acid at
position 3 by a linker "L"
<220>
<221> MISC_FEATURE
<222> (17)..(17)
<223> X means (Leu)p, wherein p is 0 or 1
<220>
<221> MISC_FEATURE
<222> (18)..(18)
<223> X means (Gln)q, wherein q is 0 or 1
<400> 3
Trp Asn Xaa Gly Thr Ile Leu Lys Ala Xaa Val Asp Tyr Ile Arg Lys
1 5 10 15
Xaa Xaa
<210> 4
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> X means (Trp)m, wherein m is 0 or 1
<220>
<221> MISC_FEATURE
<222> (2)..(2)
<223> X means (Asn)n, wherein n is 0 or 1
<220>
<221> MISC_FEATURE
<222> (7)..(7)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 14 by the linker "L
<220>
<221> MISC_FEATURE
<222> (14)..(14)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 7 by the linker "L
<400> 4
Xaa Xaa Lys Gly Thr Ile Xaa Lys Ala Ser Val Asp Tyr Xaa Arg Lys
1 5 10 15
Leu Gln
<210> 5
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> X means (Trp)m, wherein m is 0 or 1
<220>
<221> MISC_FEATURE
<222> (2)..(2)
<223> X means (Asn)n, wherein n is 0 or 1
<220>
<221> MISC_FEATURE
<222> (10)..(10)
<223> the amino acid is of formula (II), the alpha carbon atom of this
amino acid being connected to the alpha carbon of the amino acid
at position 17 by linker "L"
<220>
<221> MISC_FEATURE
<222> (17)..(17)
<223> the amino acid is of formula (II), the alpha carbon atom of this
amino acid being connected to the alpha carbon of the amino acid
at position 10 by linker "L"
<400> 5
Xaa Xaa Lys Gly Thr Ile Leu Lys Ala Xaa Val Asp Tyr Ile Arg Lys
1 5 10 15
Xaa Gln
<210> 6
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (3)..(3)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 10 by linker "L"
<220>
<221> MISC_FEATURE
<222> (10)..(10)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 3 by linker "L"
<400> 6
Trp Asn Xaa Gly Thr Ile Leu Lys Ala Xaa Val Asp Tyr Ile Arg Lys
1 5 10 15
<210> 7
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of the amino acid at
position 12 by the linker "L"
<220>
<221> MISC_FEATURE
<222> (12)..(12)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of the amino acid at
position 5 by the linker "L"
<400> 7
Lys Gly Thr Ile Xaa Lys Ala Ser Val Asp Tyr Xaa Arg Lys Leu Gln
1 5 10 15
<210> 8
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (8)..(8)
<223> the amino acid is of formula (II), the alpha carbon atom of this
amino acid being connected to the alpha carbon of amino acid at
position 15 by the linker "L"
<220>
<221> MISC_FEATURE
<222> (15)..(15)
<223> the amino acid is of formula (II), the alpha carbon atom of this
amino acid being connected to the alpha carbon of amino acid at
position 8 by the linker "L"
<400> 8
Lys Gly Thr Ile Leu Lys Ala Xaa Val Asp Tyr Ile Arg Lys Xaa Gln
1 5 10 15
<210> 9
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (8)..(8)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 15 by the linker "L"
<220>
<221> MISC_FEATURE
<222> (15)..(15)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 8 by the linker "L"
<220>
<221> MISC_FEATURE
<222> (18)..(18)
<223> X means (Ile)px, wherein px is 0 or 1
<220>
<221> MISC_FEATURE
<222> (19)..(19)
<223> X means (Pro)qx, wherein qx is 0 or 1
<400> 9
Arg Arg Arg Arg Phe Asn Ile Xaa Asp Arg Ile Lys Glu Leu Xaa Thr
1 5 10 15
Leu Xaa Xaa
<210> 10
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> X means (Arg)mx, wherein mx is 0 or 1
<220>
<221> MISC_FEATURE
<222> (2)..(2)
<223> X means (Arg)nx, wherein nx is 0 or 1
<220>
<221> MISC_FEATURE
<222> (6)..(6)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 13 by the linker "L"
<220>
<221> MISC_FEATURE
<222> (13)..(13)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 6 by the linker "L"
<400> 10
Xaa Xaa Arg Arg Phe Xaa Ile Asn Asp Arg Ile Lys Xaa Leu Gly Thr
1 5 10 15
Leu Ile Pro
<210> 11
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (3)..(3)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 10 by the linker "L"
<220>
<221> MISC_FEATURE
<222> (10)..(10)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 3 by the linker "L"
<220>
<221> MISC_FEATURE
<222> (18)..(18)
<223> X means (Ile)px, wherein px is 0 or 1
<220>
<221> MISC_FEATURE
<222> (19)..(19)
<223> X means (Pro)qx, wherein qx is 0 or 1
<400> 11
Arg Arg Xaa Arg Phe Asn Ile Asn Asp Xaa Ile Lys Glu Leu Gly Thr
1 5 10 15
Leu Xaa Xaa
<210> 12
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> X means (Arg)mx, wherein mx is 0 or 1
<220>
<221> MISC_FEATURE
<222> (2)..(2)
<223> X means (Arg)nx, wherein nx is 0 or 1
<220>
<221> MISC_FEATURE
<222> (8)..(8)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 15 by the linker "L"
<220>
<221> MISC_FEATURE
<222> (15)..(15)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 8 by the linker "L"
<400> 12
Xaa Xaa Arg Arg Phe Asn Ile Xaa Asp Arg Ile Lys Glu Leu Xaa Thr
1 5 10 15
Leu Ile Pro
<210> 13
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (8)..(8)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 15 by the linker "L"
<220>
<221> MISC_FEATURE
<222> (15)..(15)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 8 by the linker "L"
<400> 13
Arg Arg Arg Arg Phe Asn Ile Xaa Asp Arg Ile Lys Glu Leu Xaa Thr
1 5 10 15
Leu
<210> 14
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (3)..(3)
<223> the amino acid is of formula (II), the alpha carbon atom of this
amino acid being connected to the alpha carbon of amino acid at
position 10 by the linker "L"
<220>
<221> MISC_FEATURE
<222> (10)..(10)
<223> the amino acid is of formula (II), the alpha carbon atom of this
amino acid being connected to the alpha carbon of amino acid at
position 3 by the linker "L"
<400> 14
Arg Arg Xaa Arg Phe Asn Ile Asn Asp Xaa Ile Lys Glu Leu Gly Thr
1 5 10 15
Leu
<210> 15
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (4)..(4)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 11 by the linker "L"
<220>
<221> MISC_FEATURE
<222> (11)..(11)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 4 by the linker "L"
<400> 15
Arg Arg Phe Xaa Ile Asn Asp Arg Ile Lys Xaa Leu Gly Thr Leu Ile
1 5 10 15
Pro
<210> 16
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (6)..(6)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 13 by the linker "L"
<220>
<221> MISC_FEATURE
<222> (13)..(13)
<223> the amino acid is of formula (II), the alpha carbon of this amino
acid being connected to the alpha carbon of amino acid at
position 6 by the linker "L"
<400> 16
Arg Arg Phe Asn Ile Xaa Asp Arg Ile Lys Glu Leu Xaa Thr Leu Ile
1 5 10 15
Pro
<210> 17
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (3)..(3)
<223> the amino acid is of formula (II), being R19 a -CH3 radical; the
alpha carbon of this amino acid being connected to the alpha
carbon of amino acid at position 10 by the linker
-(CH2)6-CH=CH-(CH2)3-
<220>
<221> MISC_FEATURE
<222> (10)..(10)
<223> the amino acid is of formula (II), being R19 a -CH3 radical; the
alpha carbon of this amino acid being connected to the alpha
carbon of amino acid at position 3 by the linker
-(CH2)6-CH=CH-(CH2)3-
<400> 17
Trp Asn Xaa Gly Thr Ile Leu Lys Ala Xaa Val Asp Tyr Ile Arg Lys
1 5 10 15
<210> 18
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> the amino acid is of formula (II) being R19 a -CH3 radical; the
alpha carbon of this amino acid being connected to the alpha
carbon of amino acid at position 12 by the linker
-(CH2)6-CH=CH-(CH2)3-
<220>
<221> MISC_FEATURE
<222> (12)..(12)
<223> the amino acid is of formula (II) being R19 a -CH3 radical; the
alpha carbon of this amino acid being connected to the alpha
carbon of amino acid at position 5 by the linker
-(CH2)6-CH=CH-(CH2)3-
<400> 18
Lys Gly Thr Ile Xaa Lys Ala Ser Val Asp Tyr Xaa Arg Lys Leu Gln
1 5 10 15
<210> 19
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (8)..(8)
<223> the amino acid is of formula (II) being R19 a -CH3 radical; the
alpha carbon of this amino acid being connected to the alpha
carbon of amino acid at position 15 by the linker
-(CH2)6-CH=CH-(CH2)3-
<220>
<221> MISC_FEATURE
<222> (15)..(15)
<223> the amino acid is of formula (II) being R19 a -CH3 radical; the
alpha carbon of this amino acid being connected to the alpha
carbon of amino acid at position 8 by the linker
-(CH2)6-CH=CH-(CH2)3-
<400> 19
Lys Gly Thr Ile Leu Lys Ala Xaa Val Asp Tyr Ile Arg Lys Xaa Gln
1 5 10 15
<210> 20
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (8)..(8)
<223> the amino acid is of formula (II), being R19 a -CH3 radical; the
alpha carbon of this amino acid being connected to the alpha
carbon of amino acid at position 15 by the linker
-(CH2)6-CH=CH-(CH2)3-
<220>
<221> MISC_FEATURE
<222> (15)..(15)
<223> the amino acid is of formula (II), being R19 a -CH3 radical; the
alpha carbon of this amino acid being connected to the alpha
carbon of amino acid at position 8 by the linker
-(CH2)6-CH=CH-(CH2)3-
<400> 20
Arg Arg Arg Arg Phe Asn Ile Xaa Asp Arg Ile Lys Glu Leu Xaa Thr
1 5 10 15
Leu
<210> 21
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (3)..(3)
<223> the amino acid is of formula (II), being R19 a -CH3 radical; the
alpha carbon of this amino acid is connected to the alpha carbon
of amino acid at position 10 by the linker -(CH2)6-CH=CH-(CH2)3-
<220>
<221> MISC_FEATURE
<222> (10)..(10)
<223> the amino acid is of formula (II), being R19 a -CH3 radical; the
alpha carbon of this amino acid is connected to the alpha carbon
of amino acid at position 4 by the linker -(CH2)6-CH=CH-(CH2)3-
<400> 21
Arg Arg Xaa Arg Phe Asn Ile Asn Asp Xaa Ile Lys Glu Leu Gly Thr
1 5 10 15
Leu
<210> 22
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (4)..(4)
<223> the amino acid is of formula (II), being R19 a -CH3 radical; the
alpha carbon of this amino acid being connected to the alpha
carbon of amino acid at position 11 by the linker
-(CH2)6-CH=CH-(CH2)3-
<220>
<221> MISC_FEATURE
<222> (11)..(11)
<223> the amino acid is of formula (II), being R19 a -CH3 radical; the
alpha carbon of this amino acid being connected to the alpha
carbon of amino acid at position 4 by the linker
-(CH2)6-CH=CH-(CH2)3-
<400> 22
Arg Arg Phe Xaa Ile Asn Asp Arg Ile Lys Xaa Leu Gly Thr Leu Ile
1 5 10 15
Pro
<210> 23
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (6)..(6)
<223> the amino acid is of formula (II), being R19 a -CH3 radical; the
alpha carbon of this amino acid is connected to the alpha carbon
of amino acid at position 13 by the linker -(CH2)6-CH=CH-(CH2)3-
<220>
<221> MISC_FEATURE
<222> (13)..(13)
<223> the amino acid is of formula (II), being R19 a -CH3 radical; the
alpha carbon of this amino acid is connected to the alpha carbon
of amino acid at position 6 by the linker -(CH2)6-CH=CH-(CH2)3-
<400> 23
Arg Arg Phe Asn Ile Xaa Asp Arg Ile Lys Glu Leu Xaa Thr Leu Ile
1 5 10 15
Pro
<210> 24
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 24
Trp Asn Lys Gly Thr Ile Leu Lys Ala Ser Val Asp Tyr Ile Arg Lys
1 5 10 15
<210> 25
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 25
Asn Lys Gly Thr Ile Leu Lys Ala Ser Val Asp Tyr Ile Arg Lys Leu
1 5 10 15
<210> 26
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> peptide
<400> 26
Lys Gly Thr Ile Leu Lys Ala Ser Val Asp Tyr Ile Arg Lys Leu Gln
1 5 10 15
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИДЫ И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ, НАРУШЕНИЙ ИЛИ СОСТОЯНИЙ, АССОЦИИРОВАННЫХ С МУТАНТНЫМ р53 | 2017 |
|
RU2762089C2 |
| ТВЕРДЫЕ КОМПОЗИЦИИ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ | 2018 |
|
RU2777206C2 |
| УЛУЧШЕННЫЕ ПЕПТИДНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ NASH И ДРУГИХ РАССТРОЙСТВ | 2019 |
|
RU2790209C2 |
| ВАКЦИНА ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ ФИЗИЧЕСКОГО РАССТРОЙСТВА, СВЯЗАННОГО С РЕНИН-АКТИВИРУЕМОЙ АНГИОТЕНЗИНОВОЙ СИСТЕМОЙ И ПРИМЕНЕНИЕ ПЕПТИДА ДЛЯ ЕЕ ПОЛУЧЕНИЯ. | 2010 |
|
RU2534883C2 |
| Конструкции для направленного редактирования генов и способы с их применением | 2020 |
|
RU2832109C2 |
| IL-17A-связывающие полипептиды | 2016 |
|
RU2749712C2 |
| ПРИМЕНЕНИЕ АНТИТЕЛА ПРОТИВ О-АЦЕТИЛИРОВАННОГО ГАНГЛИОЗИДА GD2 ДЛЯ УЛУЧШЕНИЯ ТЕРАПЕВТИЧЕСКОГО ПОТЕНЦИАЛА ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2017 |
|
RU2771173C2 |
| ЭЛЕМЕНТЫ, СВЯЗЫВАЮЩИЕСЯ С ИЛ-1 БЕТА | 2013 |
|
RU2711118C2 |
| АНТИТЕЛО ПРОТИВ ГЛИПИКАНА-3 И ЕГО ПРИМЕНЕНИЕ | 2016 |
|
RU2744245C2 |
| СИСТЕМА ПРЕЗЕНТАЦИИ ПЕПТИДОВ НА КЛЕТОЧНОЙ ПОВЕРХНОСТИ | 2016 |
|
RU2739593C2 |
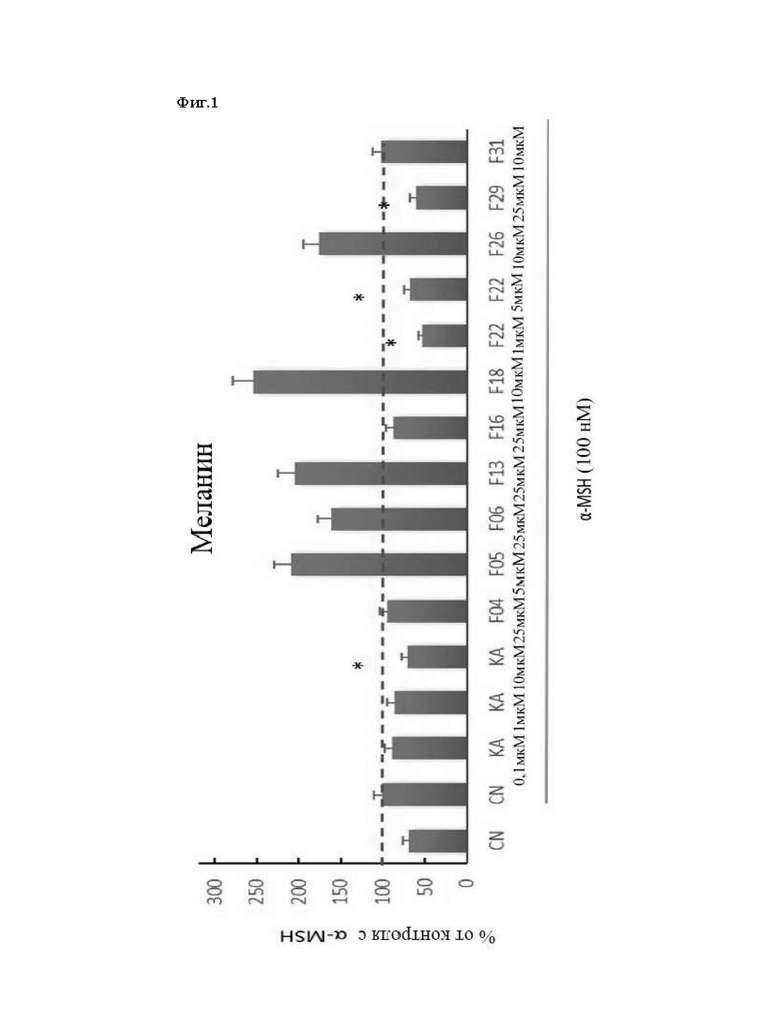
Изобретения относятся к биотехнологии, в частности к области меланоцит-связанных нарушений. Предложены меланоцит-регулирующие пептиды, фармацевтические и косметические композиции, содержащие их в качестве активных ингредиентов, а также их применения для регуляции меланогенеза, лечения или профилактики меланомы и заболевания, связанного с нарушением регуляции меланогенеза. Пептид имеет аминокислотную последовательность (Trp)m-(Asn)n-Lys-Gly-Thr-Ile-Leu-Lys-Ala-Ser-Val-Asp-Tyr-Ile-Arg-Lys-(Leu)p-(Gln)q (SEQ ID NO: 1) или (Arg)mx-(Arg)nx-Arg-Arg-Phe-Asn-Ile-Asn-Asp-Arg-Ile-Lys-Glu-Leu-Gly-Thr-Leu-(Ile)px-(Pro)qx (SEQ ID NO: 2). Пептид дополнительно включает линкерный бирадикал «L» формулы (I) -[(R1)a-(R2)-(R3)b]c- (I), который представляет собой соединение альфа-атома углерода аминокислоты, расположенной в положении «i», с альфа-атомом углерода аминокислоты, расположенной в положении «i+7» в пептидной последовательности. Аминокислоты, которые соединены линкером, имеют формулу 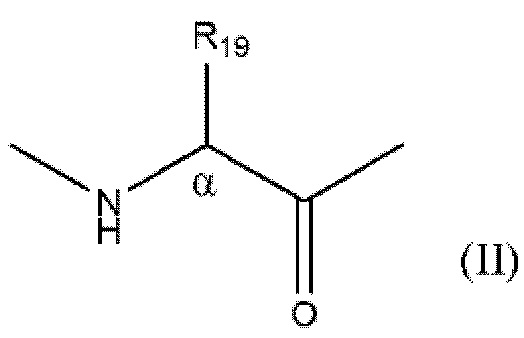 . Предложенные пептиды регулируют меланогенез либо промотируя, либо снижая продукцию меланина, ингибируют пролиферацию злокачественных меланоцитов, позволяют эффективно регулировать активность меланоцитов не только в отношении образования меланина, но также в отношении клеточной пролиферации, и могут быть эффективными для лечения пигментных нарушений. 7 н. и 8 з.п. ф-лы, 1 ил., 4 табл.
. Предложенные пептиды регулируют меланогенез либо промотируя, либо снижая продукцию меланина, ингибируют пролиферацию злокачественных меланоцитов, позволяют эффективно регулировать активность меланоцитов не только в отношении образования меланина, но также в отношении клеточной пролиферации, и могут быть эффективными для лечения пигментных нарушений. 7 н. и 8 з.п. ф-лы, 1 ил., 4 табл.
1. Пептид или его фармацевтически или косметически приемлемая соль, регулирующие активность меланоцитов, причем пептид имеет аминокислотную последовательность SEQ ID NO: 1 или 2:
(Trp)m-(Asn)n-Lys-Gly-Thr-Ile-Leu-Lys-Ala-Ser-Val-Asp-Tyr-Ile-Arg-Lys-(Leu)p-(Gln)q (SEQ ID NO: 1)
(Arg)mx-(Arg)nx-Arg-Arg-Phe-Asn-Ile-Asn-Asp-Arg-Ile-Lys-Glu-Leu-Gly-Thr-Leu-(Ile)px-(Pro)qx (SEQ ID NO: 2),
где
«m», «n», «p» и «q» представляют собой целые числа и выбраны из 0 и 1,
«mx», «nx», «px» и «qx» представляют собой целые числа и выбраны из 0 и 1,
C-терминальный конец соответствует –C(O)R4,
N-терминальный конец соответствует –NHR5,
R4 представляет собой радикал, выбранный из группы, состоящей из –OH и –NR17R18,
R5 представляет собой радикал, выбранный из группы, состоящей из –H, (C1-C20)алкила и (C1-C10)алкила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (C1-C10)алкила, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12, и
R17 и R18 представляют собой радикалы, независимо выбранные из группы, состоящей из -H, (C1-C10)алкила и (C1-C10)алкила, замещенного одним или более радикалами, выбранными из группы, состоящей из галогена, (C1-C10)алкила, -OR6, -NR7R8, -SR9, -SOR10, -SO2R11 и -CO2R12,
причем пептид дополнительно включает линкерный бирадикал «L» формулы (I)
-[(R1)a-(R2)-(R3)b]c- (I),
который представляет собой соединение альфа-атома углерода аминокислоты, расположенной в положении «i», с альфа-атомом углерода аминокислоты, расположенной в положении «i+7» в пептидной последовательности,
где
«a», «b» и «с» представляют собой 1,
R1 и R3 представляют собой бирадикалы, независимо выбранные из группы, состоящей из (C1-C10)алкила, (C2-C10)алкенила, и (C2-C10)алкинила,
R2 представляет собой бирадикал, выбранный из группы, состоящей из (C1-C10)алкила, (C2-C10)алкенила, и (C2-C10)алкинила, и
причем аминокислоты, которые соединены линкером, имеют формулу (II)
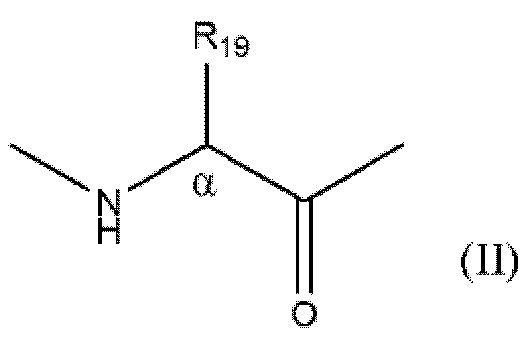 ,
,
где
R19 представляет собой монорадикал, выбранный из группы, состоящей из (C1-C10)алкила, (C2-C10)алкенила, и (C2-C10)алкинила.
2. Пептид по п. 1, где R1, R3 и R19 представляют собой (C1-C10)алкил, и R2 представляет собой (C2-C10)алкенил.
3. Пептид по любому из предшествующих пунктов, где C-терминальный конец соответствует -C(O)OH или -C(O)NH2, и N-терминальный конец соответствует -NH2.
4. Пептид по любому из предшествующих пунктов, который на 100% идентичен пептидной последовательности согласно SEQ ID NO: 3 - 16, где «L», «R19», «m», «n», «p», «q», «mx», «nx», «px» и «qx» имеют значения, как определено в любом из предшествующих пунктов.
5. Пептид по любому из предшествующих пунктов, который на 100% идентичен аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 17 - 23.
6. Конъюгат для регуляции активности меланоцитов, включающий пептид по любому из предшествующих пунктов, где пептид конъюгирован с меткой, лекарственным средством, проникающим в клетку пептидом или PROTAC.
7. Фармацевтическая композиция для регуляции активности меланоцитов, содержащая терапевтически эффективное количество пептида или его фармацевтически приемлемой соли, как определено в любом из пп. 1-5, или конъюгата, как определено в п. 6, вместе с приемлемыми фармацевтическими вспомогательными веществами и/или носителями.
8. Фармацевтическая композиция по п. 7, которая представляет собой местную композицию.
9. Косметическая композиция для регуляции активности меланоцитов, содержащая косметически эффективное количество пептида или его косметически приемлемой соли, как определено в любом из пп. 1-5, или конъюгата, как определено в п. 6, вместе с приемлемыми косметическими вспомогательными веществами и/или носителями.
10. Косметическая композиция по п. 9, которая представляет собой местную композицию.
11. Применение пептида или его фармацевтической соли, как определено в любом из пп. 1-5, конъюгата, как определено в п. 6, фармацевтической композиции, как определено в любом из пп. 7, 8, или косметической композиции, как определено в любом из пп. 9, 10, для регуляции меланогенеза.
12. Применение по п. 11 для лечения гиперпигментации или гипопигментации.
13. Применение пептида или его фармацевтической соли, как определено в любом из пп. 1-5, конъюгата, как определено в п. 6, или фармацевтической композиции, как определено в любом из пп. 7, 8, для лечения или профилактики меланомы.
14. Применение по п. 13, для лечения или профилактики метастатической меланомы.
15. Применение пептида или его фармацевтической соли, как определено в любом из пп. 1-5, конъюгата, как определено в п. 6, или фармацевтической композиции, как определено в любом из пп. 7, 8, для лечения или профилактики заболевания, связанного с нарушением регуляции меланогенеза.
| WO 2019115480 A1, 20.06.2019 | |||
| WO 03106491 A2, 24.12.2003 | |||
| US 7217539 B2, 15.05.2007 | |||
| WO 2019025433 A1, 07.02.2019 | |||
| MURAKAMI H | |||
| ET AL | |||
| Sumoylation modulates transcriptional activity of MITF in a promoter-specific manner: Sumoylation modulates transcriptional activity of MITF | |||
| PIGMENT CELL RESEARCH, 2005, v.18, no.4, p.265-277, DOI: |
Авторы
Даты
2025-02-21—Публикация
2020-07-31—Подача