Изобретение относится к медицине и может быть использовано для лечения дисбиоза кишечника в постоперационном периоде у больных с черепно-мозговой травмой.
Нарушение качественного и количественного состава микробиоты кишечника, приводящих к его дисбиозу, отмечаются в послеоперационном периоде у всех без исключения, больных с черепно-мозговой травмой, находящихся как в остром критическом состоянии [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С.Петрикова. Москва: ГЭОТАР, 2023. - 1166 с. Мазурок В.А., Головкин А.С., Баутин А.Е. и др. Желудочно-кишечный тракт при критических состояниях: первый страдает, последний, кому уделяют внимание. Вестник интенсивной терапии. 2016. № 2. С. 28-37], так и в хроническом критичесчком состоянии [Гречко А.В., Буякова И.В., Белобородова Н.В. Дисфункция микробиоты у пациентов с повреждением головного мозга, находящихся в хроническом критическом состоянии. Российский неврологический журнал. 2022;27(1):94-104. Zandalasini М., Pelizzari L., Ciardi G. et al. Bowel dysfunctions after acquired brain injury: a scoping review. Front. Hum. Neurosci. 2023. 17:1146054].
В послеоперационном периоде у пациентов с черепно-мозговой травмой факторами развития дисбиоза кищечника являются травматическая, ишемическая, гипоксическая и воспалительная альтерация не только центральной нервной системы, но и других органов и систем, обусловливающая полное истощение их компенсаторных механизмов [Национальное руководство. Интенсивная терапия / Под редакцией И.Б. Заболотских, Д.Н. Проценко 2-е издание, переработанное и дополненное. Москва: Гэотар-медицина, 2021. 2208 с]. Кроме того, раннее назначение массивной антибактериальной терапии, способствующее отрицательной реформации качественного и количественного состава кишечной микробиоты, заключающейся в превалировнии условно-патогенных микроорганизмов над другими представителями кишечной микробиоты, негативно значительно изменяет ее метаболизм, который оказывает дестабилизирующее действие на макроорганизм [Beloborodova N.V., Grechko A.V., Olenin A.Yu. Metabolomic discovery of microbiota dysfunction as the cause of pathology. Metabolomics - New Insights into Biology and Medicine, 2019].
Именно поэтому развитие дисбиоза является предиктором продолжительного пребывания данных больных в отделениях интенсивной терапии и стационаре [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва,: ГЭОТАР, 2023. - 1166 с].
Важным является и то, что у больных с черепно-мозговой травмой послеоперационный период осложняется сепсисом [Sekino, N., Selim, М. & Shehadah, А. Sepsis-associated brain injury: underlying mechanisms and potential therapeutic strategies for acute and long-term cognitive impairments. J Neuroinflammation 19, 101 (2022). https://doi.org/10.1186/sl2974-022-02464-4].
Именно при сепсисе дисбиоз кишечника негативно изменяет содержание в крови фенилкарбоновых кислот, которые, многократно возрастая [Белобородова Н.В., Мороз В.В., Бедова А.Ю., Осипов А.А., Саршор Ю.Н., Черневская Е.А. Участие ароматических микробных метаболитов в развитии тяжелой инфекции и сепсиса. Анестезиология и реаниматология. 2016;61(3):202-208], способствовали ухудшению тяжести общего состояния больных и увеличению их летальности [Белобородова Н.В., Острова И.В. Сепсис-ассоциированная энцефалопатия (обзор). Общая реаниматология. 2017; 13(5): 121-139].
Учитывая, что пациенты с черепно-мозговой травмой, которые в раннем постоперационном периоде находятся в остром критическом состоянии [Национальное руководство. Интенсивная терапия / Под редакцией И.Б. Заболотских, Д.Н. Проценко 2-е издание, переработанное и дополненное. Москва: Гэотар-медицина, 2021. 2208 с], в течение небольшого промежутка времени переходят в хроническое критическое состояние с последующим сохранением у них дисбиоза кишечника [Parfenov A.L., Razzhivin V.P., Petrova M.V. Chronic critical illness: current aspects of the problem (review). Sovremennye tehnologii v medicine 2022; 14(3): 70-83. Гречко A.B., Буякова И.В., Белобородова H.B. Дисфункция микробиоты у пациентов с повреждением головного мозга, находящихся в хроническом критическом состоянии. Российский неврологический журнал. 2022; 27 (1):94-104] [Beloborodova N.V., Grechko A.V., Olenin A.Yu. Metabolomic discovery of microbiota dysfunction as the cause of pathology. Metabolomics - New Insights into Biology and Medicine. 2019].
Поэтому у пациентов с черепно-мозговой травмой, находящихся в хроническом критическом состоянии в условиях длительно существующих грубых нарушений качественного и количественного состава микробиоты кишечника, так называемые условно патогенные и патогенные бактерии активизируют в нем инвертируемые метаболические процессы и способствуют поражению его слизистой оболочки, что, в свою очередь, не может споосбствовать улучшению общего состояния пациентов [Белобородова Н.В. Метаболизм микробиоты при критических состояниях (обзор и постулаты). Общая реаниматология. 2019;15(6):62-79].
Именно дисбиоз кишечника становится основой для мальабсорбции и усугубления ишемии в его подслизистом и мышечном слоях, что приводит к повреждению метасимпатической иннервации кишечника и дальнейшему усугублению нарушений гомеостаза, тем самым замыкая порочный патогенетический круг у пациентов с поражением центральной нервной системы [Сирота Г.Г., Кирилина СИ., Сирота B.C., Лебедева М.Н., Иванова Е.Ю., Первухин С.А. и др. Кишечная и нутритивная недостаточность при осложненной травме шейного отдела позвоночника // Политравма. 2018. №. 3. С. 20-26].
Именно нормальный качественный и количественный состав микробиоты кишечника участвует в регулировании нервной и эндокринной систем макрорганизма посредством нейромедиаторов ацетилхолина, норадреналина, дофамина, серотонина, гистамина и гамма-аминомасляной кислоты, а также синтеза глицина, таурина, аспарагиновой кислоты [Балеев М.С., Рябков М.Г., Перльмуттер О.А., Фраерман А.П., Шейко Г.Е., Смирнов И.И., Шалин В.В., Леонтьев А.Е. Дисфункция пищеварительного тракта в остром периоде травмы спинного мозга (обзор литературы) // Политравма. 2021. № 3, С. 82-90].
В свою очередь, негативное изменение состава микробиоты кишечника непосредственно отрицательно влияет на состояние центральной и периферической нервной системы пациента [Сирота Г.Г., Кирилина СИ., Сирота B.C., Лебедева М.Н., Иванова Е.Ю., Первухин С.А. и др. Кишечная и нутритивная недостаточность при осложненной травме шейного отдела позвоночника // Политравма. 2018. №. 3. С.20-26].
Кроме того, возникающий дисбиоз кишечника, особенно сопровождающийся ростом патогенной микрофлоры, подавляющей нормальную микробиоту, уже в ранние сроки болезни прямо коррелирует с интенсивностью воспаления в области повреждения и осложняет восстановление двигательной функции [Iwasaki М, Akiba Y, Kaunitz JD. Recent advances in vasoactive intestinal peptide physiology and pathophysiology: focus on the gastrointestinal system. F1000Research. 2019; (8): 1-13. Kigerl KA, Popovich PG. Gut dysbiosis and recovery of function after spinal cord injury. Oxford Research Encyclopedia of Neuroscience. 2019; 15(1): 60-67].
Дисбиоз кишечника у больных с черепно-мозговой травмой, находящихся в хроническом критическом состоянии, является ответственным за нарушение его моторной, секреторной, всасывательной, эндокринной, иммунной, эвакуаторной и барьерной функций [Eldahan КС, Rabchevsky AG. Autonomic dysreflexia after spinal cord injury: systemic pathophysiology and methods of management. Autonomic Neuroscience. 2018; (209): 59-70. Steensgaard R, Bonne S, Wojke P, Kasch H. SCI-SCREEN: a more targeted nutrition screening model to detect spinal cord-injured patients at risk of malnutrition. Rehabil Nurs. 2019; 44(1): 11-19. White AR, Holmes GM. Investigating neurogenic bowel in experimental spinal cord injury: where to begin? Neural regeneration research. 2019; 14(2): 222-231].
Дисбиоз кишечника у больных с черепно-мозговой травмой, находящихся в хроническом критическом состоянии, увеличивает риск клинически значимых дефицитных состояний: гипопротеинемии, липопротеинемии, авитаминоза, недостатка минеральных веществ, электролитных соединений, аминокислот, моно- и дисахаридов [Bernardi М, Fedullo AL, Bernardi Е. Diet in neurogenic bowel management: A viewpoint on spinal cord injury. World J Gastroenterol. 2020; 26(20): 2479-2497. Montesinos-Magraner L, Castellano-Tejedor C, Frias A, Launois P, Rojas-Cuotto K, Gonzalez-Viejo MA. Spanish validation of the autonomic standards assessment form in spinal cord injuries. Rehabilitacion (Madr). 2019; 53(1): 20-27. Bazzocchi G. Changes in gut microbiota in the acute phase after spinal cord injury correlate with severity of the lesion. Scientific reports. 2021; (11)1: 1-13].
Поэтому у пациентов с черепно-мозговой травмой, находящихся в хроническом критическом состоянии развивается дисбаланс нутритивного статуса, нарушение всасывания жидкости, пассажа химуса, задержка опорожнения ампулы прямой кишки или, напротив, недержание каловых масс [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва: ГЭОТАР, 2023. 1166 с. Bazzocchi G. Changes in gut microbiota in the acute phase after spinal cord injury correlate with severity of the lesion. Scientific reports. 2021; (11)1: 1-13. Qi Z, Middleton JW, Malcolm A. Bowel dysfunction in spinal cord injury. Current gastroenterology reports. 2018; 20(10): 47-58. White AR, Holmes GM. Anatomical and functional changes to the colonic neuromuscular compartment after experimental spinal cord injury. Journal of Neurotrauma. 2018; 35(9): 1079-1090].
В результате дисбиоза кишечника не только усугубляется его ишемия и гипоксия, но и возникает трансклокация микроорганизмов в системный кровоток, катализирующая системное воспаление и развитие сепсиса, которые значимо ухудшают клинические исходы и результаты лечения [Сепсис: классификация, клинико-диагностическая концепция и лечение / практ.рук. / под ред. Б. Р. Гельфанда. - 4-е изд., доп.и перераб. М.: МИА, 2017. - 214 с].
Кроме того, существенно негативно измененный состав кишечной микрофлоры, который необходим для синтеза аминокислот и витаминов, обусловливает возникновение дефицита Н-биотина и витамина D, приводящие к повышению холестерина и нарушению обмена кальция, что, в свою очередь, является дополнительными субстратами для развития вторичных осложнений течения существующей патологии [Fung С, Vanden Berghe P. Functional circuits and signal processing in the enteric nervous system. Cell Mol Life Sci. 2020; 77(22): 4505-4522., Ивашкин В.Т., Ивашкин К.В. Кишечный микробном как фактор регуляции деятельности энтеральной и центральной нервной системы // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2017. Т. 27, № 5. С.11-19].
Более того, образующаяся существенная нехватка витаминов группы В ведет к нарушению трофики нервных клеток и соответственно иннервации [Lussi С, Frotzler А, Jenny A, Schaefer DJ, Kressig RW, Scheel-Sailer A.Nutritional blood parameters and nutritional risk screening in patients with spinal cord injury and deep pressure ulcer-a retrospectivechart analysis. Spinal Cord. 2018; 56(2): 168-175], что становится значимым фактором в замкнутом патогенетическом круге нарушений микробиологического пейзажа кишечника [Евсеев М.А., Фомин B.C., Никитин В.Е. Патогенетические аспекты развития синдрома энтеральной недостаточности в послеоперационном периоде // Анналы хирургии. 2018. Т. 23, № 1. С.5-13].
Принимая во внимание тот факт, что собственные питательные потребности тонкого кишечника на 50% и толстого кишечника на 80% удовлетворяются за счет питания из их же полости, на фоне значимого качественного и количественного отрицательного реформирования микробиоты кишечника способствующему его дисбиозу, становится понятным, что продолжительность непрограмируемого апоптоза клеток слизистой оболочки кишечника будет длительной по срокам [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва,: ГЭОТАР, 2023. 1166 с].
В свою очередь, дисфункция кишечника и возникающая на ее фоне нутритивная недостаточность у больных [Евсеев М.А., Фомин B.C., Никитин В.Е. Патогенетические аспекты развития синдрома энтеральной недостаточности в послеоперационном периоде //Анналы хирургии. 2018. Т. 23, № 1. С.5-13. Балеев М.С., Рябков М.Г., Перльмуттер О.А. и др. Дисфункция пищеварительного тракта в остром периоде травмы спинного мозга (обзор литературы) // Политравма. 2021. № 3. С.82-90], перенесших как острое критическое состояние [Мазурок В.А., Головкин А.С., Баутин А.Е. и др. Желудочно-кишечный тракт при критических состояниях: первый страдает, последний, кому уделяют внимание. Вестник интенсивной терапии. 2016. № 2. С.28-37], так и хроническое критическое состояние [Parfenov A.L., Razzhivin V.P., Petrova M.V. Chronic critical illness: current aspects of the problem (review). Sovremennye tehnologii v medicine 2022; 14(3): 70-83. Гречко A.B., Буякова И.В., Белобородова Н.В. Дисфункция микробиоты у пациентов с повреждением головного мозга, находящихся в хроническом критическом состоянии. Российский неврологический журнал. 2022; 27 (1):94-104] напрямую связана со степенью выраженности его дисбиоза [Beloborodova N.V., Grechko A.V., Olenin A.Yu. Metabolomic discovery of microbiota dysfunction as the cause of pathology. Metabolomics - New Insights into Biology and Medicine. 2019]. Действительно, практически невозможно действенно купировать питательную недосттаочность у больных на фоне существующего дисбиоза кишечника, который, в свою очередь определяет дисфункцию данного органа [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва,: ГЭОТАР, 2023. 1166 с].
Принимая во внимание все выше сказанное, становится аксиомально ясным, что лечение дисбиоза кишечника для купирования его дисфункции [Балеев М.С., Рябков М.Г., Перльмуттер О.А. и др. Дисфункция пищеварительного тракта в остром периоде травмы спинного мозга (обзор литературы) // Политравма. 2021. № 3. С. 82-90], на сегодняшний момент развития медицины, должно быть целенаправленно патогенетическим и осуществляться с помощью метабиотиков [Шендеров Б.А., Ткаченко Е.И., Лазебник Л.Б., Ардатская М.Д., Синица А.В., Захарченко М.М. Метабиотики - новая технология профилактики и лечения заболеваний, связанных с микроэкологическими нарушениями в организме человека. Экспериментальная и клиническая гастроэнтерология. 2018;151(3):83-92].
Именно применение в программе лечения дисбиоза кишечника метабиотиков создает значимые и положительные условия для развития адекватного микробиома у пациентов даже на фоне критически негативного изменения его качественного и количественного состава [Гречко А.В., Буякова И.В., Белобородова Н.В. Дисфункция микробиоты у пациентов с повреждением головного мозга, находящихся в хроническом критическом состоянии. Российский неврологический журнал. 2022;27(1):94-104. Шендеров Б.А., Ткаченко Е.И., Захарченко М.М., Синица А.В. Метабиотики: перспективы, вызовы и возможности. Медицинский алфавит.2019;2(13):43-48].
На сегодняшний день развития медицины использование пробиотиков при лечении дисбиоза кишечника не является патогенетически обоснованным и значимым вследствие того, что они являются живыми микроорганизмами, что требует нормальной работы желудочно-кишечного тракта, которая не возможна при имеющейся патологии, а также существования определенных условий для их колонизации [Шендеров Б.А., Ткаченко Е.И., Лазебник Л.Б., Ардатская М.Д., Синица А.В., Захарченко М.М. Метабиотики - новая технология профилактики и лечения заболеваний, связанных с микроэкологическими нарушениями в организме человека. Экспериментальная и клиническая гастроэнтерология. 2018;151(3):83-92], которые значимо нарушены у больных находящихся в острых [Белобородова Н.В. Метаболизм микробиоты при критических состояниях (обзор и постулаты). Общая реаниматология. 2019;15(6):62 79] или хроничеких [Bazzocchi G. Changes in gut microbiota in the acute phase after spinal cord injury correlate with severity of the lesion. Scientific reports. 2021; (11)1: 1-13] критических состояниях.
Лечение дисбиоза кишечника метабиотиками полярно отличается от терапии пробиотиками [Salminen S. et al. The International Scientific Association of Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of postbiotics // Nat. Rev. Gastroenterol. Hepatol. Springer US, 2021. Vol.0123456789. Vinderola G, Sanders ME, Salminen S. The Concept of Postbiotics. Foods. 2022 Apr 8;11(8): 1077. doi: 10.3390/foods11081077. PMID: 35454664; PMCID: PMC9027423].
Это связано с тем, что метабиотики, в сравнении с пробиотиками, не замещают собственную микрофлору кишечника чужеродными живыми микроорганизмами, а катализитуют рост ее собственной микробиоты [Shenderov В. A. Metabiotics: novel idea or natural development of probiotic conception // Microb. Ecol. Health Dis. 2013. Vol.24. P. 203 299].
Метабиотики - это новое поколение препаратов, имеющих в своем составе полезные метаболические продукты пробиотических бактерий, которые не только способствуют росту полезной аутомикрофлоры и подавлению вредоносной для устранения и профилактики дисбактериоза, но и созданию благоприятного микроклимата для регенерации поврежденного эпителия кишечника [Плотникова Е.Ю., Грачева Т.Ю. Метабиотики - комплексное решение дисбиотических проблем при различных заболеваниях. РМЖ. 2018;5(II):72-76. Żołkiewicz J, Marzec A, Ruszczyński M, Feleszko W. Postbiotics-A Step Beyond Pre- and Probiotics. Nutrients. 2020 Jul 23;12(8):2189. doi: 10.3390/nul2082189. PMID: 32717965; PMCID: PMC7468815].
Также метабиотики отличаются от пробиотиков [Pierre Singer, Annika Reintam Blaser, Mette M. Berger, Philip C. Calder, Michael Casaer, Michael Hiesmayr, Konstantin Mayer, Juan Carlos Montejo-Gonzalez, Claude Pichard, Jean-Charles Preiser, Wojciech Szczeklik, Arthur R.H. van Zanten, Stephan C. Bischoff. ESPEN practical and partially revised guideline: Clinical nutrition in the intensive care unit. Clinical Nutrition. 2023. Vol.9. - P. 1671-1689] тем, что если для высушенных пробиотиков необходима активация в кишечнике, после которой они могут начать выработку метаболитов, то метабиотики содержат уже готовые метаболиты и не требуют дополнительной активации [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва: ГЭОТАР, 2023. 1166 с. Ma L, Tu Н, Chen Т. Postbiotics in Human Health: A Narrative Review. Nutrients. 2023 Jan 6;15(2):291. doi: 10.3390/nu15020291. PMID: 36678162; PMCID: PMC9863882. Cuevas-González PF, Liceaga AM, Aguilar-Toalá JE. Postbiotics and paraprobiotics: From concepts to applications. Food Res Int. 2020 Oct;136:109502. doi: 10.1016/j.foodres.2020.109502. Epub 2020 Jun 30. PMID: 32846581].
Именно метабиотики, составляющими которых являются продукты метаболизма или структурные компоненты пробиотических микроорганизмов, клеточные компоненты, метаболиты и сигнальные молекулы пробиотических культур, способны оптимизировать специфичные для организма физиологические функции, регуляторные и метаболические процессы, осуществляют не только пищеварительную функцию, но и синтез всевозможных субстанций, способствующих нормализации метаболических процессов у больного, с компрометированным кишечником [Плотникова Е.Ю., Грачева Т.Ю. Метабиотики - комплексное решение дисбиотических проблем при различных заболеваниях. РМЖ. 2018;5(П):72-76]. В этой связи создание управляемого микробиоценоза кишечника [Микробиота / под ред. Е. Л. Никоновой и Е. Л. Поповой // Медиа Сфера. - 2019. - С.20 30. Кайбышева, В. О. Пробиотики с позиции доказательной медицины / В. О. Кайбышева, Е. Л. Никонов // Доказательная гастроэнтерология. - 2019. - 8 (3). - С.45 54], за счет нормализации представителей эндогенной микробиоты кишечника [Adak A., Han G. Verständnis der Darmmikrobiota und ihrer Funktionalität. Cell Mol Life Sci. 2019;76:473-493. doi: 10.1007/s00018-018-2943-4. -DOI - PubMed] у больных с помощью метабиотиков, позволит улучшить лечебные эффекты осуществляемого энтерального питания, способствующих уменьшению питательной и полиорганной недостаточности [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва,: ГЭОТАР, 2023. 1166 с. Сепсис: классификация, клинико-диагностическая концепция и лечение / практ.рук. / под ред. Б. Р. Гельфанда. - 4-е изд., доп.и перераб. М.: МИА, 2017. - 214 с].
Кроме того, у больных для усиления и улучшения их терапевтических результатов метабиотики могут применяться как изолированно, так и комплексным методом, который, в свою очередь, при его использовании реализуют оптимальный лечебный эффект [Плотникова Е.Ю., Грачева Т.Ю. Метабиотики - комплексное решение дисбиотических проблем при различных заболеваниях. РМЖ. 2018;5(II):72-76. Ma L, Tu Н, Chen Т. Postbiotics in Human Health: A Narrative Review. Nutrients. 2023 Jan 6;15(2):291. doi: 10.3390/nul5020291. PMID: 36678162; PMCID: PMC9863882. Cuevas-González PF, Liceaga AM, Aguilar-Toalá JE. Postbiotics and paraprobiotics: From concepts to applications. Food Res Int. 2020 Oct;136:109502. doi: 10.1016/j.foodres.2020.109502. Epub 2020 Jun 30. PMID: 32846581].
Это связано с тем, что микробиота желудочно-кишечного тракта представлена общей численностью около 1015 клеток, а совокупный вес микроорганизмов в его просвете составляет около 3 килограммов [Shenderov В.A. et al. METABIOTICS. Cham: Springer International Publishing, 2020. 123 с. Мазурок В.А., Головкин A.C., Баутин А.Е. и др. Желудочно-кишечный тракт при критических состояниях: первый страдает, последний, кому уделяют внимание. Вестник интенсивной терапии, 2016. №2. С.28-37].
Примерно 90% микроорганизмов желудочно-кишечного тракта являются анаэробами толстой кишки, а из них около 60% составляют бифидобактерии, адгезированные на эпителиоцитах толстой кишки [Малкоч А.В., Бельмер СВ. Кишечная микрофлора и значение пребиотиков для ее функционирования. Лечащий врач. 2006; 4: 60-65. Adak A., Han G. Verstandnis der Darmmikrobiota und ihrer Funktionalitat. Cell Mol Life Sci. 2019;76:473-493. doi: 10.1007/s00018-018-2943-4. - DOI - PubMed].
Поэтому восстановленная с помощью метабиотиков микрофлора кишечника способствует нормализации деятельности иммунитета, так как 60% иммунных клеток организма находятся в слизистой оболочке кишечника [Shenderov В. A. et al. METABIOTICS. Cham: Springer International Publishing, 2020. 123 с], которая также одновременно является физическим барьером против движения патогенных микроорганизмов через слизистую оболочку кишечника в лимфатическую систему, особенно при возникновении критического состояния вследствие болезни, которая нарушает баланс между микрофлорой хозяина и кишечника, способствуя колонизации, чрезмерному росту и перемещению патогенов и микробных продуктов через слизистый барьер кишечника [Мазурок В.А., Головкин А.С, Баутин А.Е. и др. Желудочно-кишечный тракт при критических состояниях: первый страдает, последний, кому уделяют внимание. Вестник интенсивной терапии. 2016. № 2. С. 28-37. Aller J.M., Crowley S.M., Low Н.Т. usw. Darmepithel: zentraler Koordinator der Immunitat der Schleimhaut. Die Trends von Immunol. 2019;39:677-696. doi: 10.1016/j.it.2018.04.002. - DOI - PubMed], вызывая системное воспаление и сепсис [Сепсис: классификация, клинико-диагностическая концепция и лечение / практ.рук. / под ред. Б. Р. Гельфанда. - 4-е изд., доп.и перераб. М.: МИА, 2017. - 214 с. Agudelo-Ochoa G.M., Valdes-Duque В.Е., Giraldo-Giraldo NA usw. Darm-Mikrobiota-Profile bei kritisch kranken Patienten, potentielle Biomarker und Variable des Sepsis-Risikos. Darmkeime. 2020; 12:1707610. doi: 10.1080/19490976.2019.1707610].
Важным является и то, что метабиотики, являющиеся продуктами расщепления пробиотических бактериальных клеток на фрагменты, которые включают в себя частицы их клеточной стенки и внутриклеточного содержимого, в виде метафильтратов имеют ряд преимуществ по отношению к классическим пробиотикам, а именно обладают высокой биодоступностью, невступления в конфликт с собственной микрофлорой, имеют четкую химическую структуру, не разрушаются в желудке и быстро продвигаются до кишечника [Shenderov В.A. et al. METABIOTICS. Cham: Springer International Publishing, 2020. 123 c], обусловливают снижение риска микробной транслокации и системного воспаления [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва,: ГЭОТАР, 2023. 1166 с. Сепсис: классификация, клинико-диагностическая концепция и лечение / практ.рук. / под ред. Б.Р. Гельфанда. - 4-е изд., доп.и перераб. М.: МИА, 2017. - 214 с], могут применяться в высоких дозах [Gouri, Ezaz A.; Richards, David М.; Rahimi, Eric F.; Krill, Joseph Т.; Jelinek, Katherine A.; Dupont, Andrew W. (9. Dezember 2014). „Systematischer Überblick über randomisierte kontrollierte Studien zu Probiotika, Prabiotika und Synbiotika bei entztindlichen Darmerkrankungen". Klinische und experimentelle Gastroenterologie. 7: 473-487. doi:10.2147/CEG.S27530. PMC 4266241. PMID 25525379. Singhi S. S., Kumar S. (2016). „Probiotika bei kritisch kranken Kindern". Studie F1000 (Ubersicht). 5: 407. doi:10.12688/fl000research.7630.1. PMC 4813632. PMID 27081478. Бовбель, И.Э. Современные представления о микробиоте кишечника и возможности эффективного применения пробиотиков в практике врача-педиатра / И.Э Бовбель // Медицинские новости. - 2017. - № 2. - С. 25-31].
Целью использования метабиотиков в программе комплексного лечения больных в острых и хронических критических состояниях является их позитивное влияние на кишечную флору посредством увеличения числа полезных анаэробных бактерий и уменьшение популяции патогенных микроорганизмов для купирования дисбиоза желудочно-кишечного тракта [Shenderov В.A. et al. METABIOTICS. Cham: Springer International Publishing, 2020. 123 c. Salminen S. et al. The International Scientific Association of Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of postbiotics // Nat. Rev. Gastroenterol. Hepatol. Springer US, 2021. Vol.0123456789. Vinderola G, Sanders ME, Salminen S. The Concept of Postbiotics. Foods. 2022 Apr 8; 11(8): 1077. doi: 10.3390/foodsl 1081077. PMID: 35454664; PMCID: PMC9027423. Zolkiewicz J, Marzec A, Ruszczynski M, Feleszko W. Postbiotics-A Step Beyond Pre- and Probiotics. Nutrients. 2020 Jul 23;12(8):2189. doi: 10.3390/nul2082189. PMID: 32717965; PMCID: PMC7468815], что позволит нормализовать компрометированное пищеварение и улучшить метаболизм, снижающие имеющиеся дисфункции органов и систем [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва, ГЭОТАР, 2023. 1166 с. Сепсис: классификация, клинико-диагностическая концепция и лечение / практ.рук. / под ред. Б.Р. Гельфанда. - 4-е изд., доп.и перераб. М.: МИА, 2017. - 214 с].
Известен метабиотический препарат Хилак форте [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва,: ГЭОТАР, 2023. - 1166 с.] для осуществления способа лечения различных диарейных расстройств кишечника [Торговое наименование лекарственного препарата: Хилак форте. Международное непатентованное или химическое наименование: Метаболиты бактерий Escherichia coli, Enterococcus faecalis, Lactobacillus acidophilus, Lactobacillus helveticus. Фармако-терапевтическая группа препарата: Противодиарейное средство]. Механизм действия Хилак форте на нормализацию состава и функций микробиоты и восстановления деятельности кишечника косвено опосредован входящим в него компонентами, а именно содержащихся в нем короткоцепочных жирных кислот, способствующих нормализации кишечного микробиоценоза за счет его роста и активности, а также регенерации поврежденных эпителиальных клеток кишечника [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва,: ГЭОТАР, 2023. - 1166 с]. Это свидетельствует о том, что Хилак форте оказывает только непрямое влияние, в отличие от оригинального метабиотического многокомпонентного препарата, содержащего композицию не только лизатов лактобактерий и бифидобактерий, но и переносящего субстрата - мальтодекстрина и питательных субстратов на основе концентрата для безалкогольного напитка Камбиочай, гуммиарабика и молочной пищевой кислоты, осуществляющего влияние непосредственно на качественный и количественный состав компрометированной микрофлоры кишечника [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва,: ГЭОТАР, 2023. 1166 с].
Это особенно неактуально для больных, находящихся в острых [Мазурок В.А., Головкин А.С., Баутин А.Е. и др. Желудочно-кишечный тракт при критических состояниях: первый страдает, последний, кому уделяют внимание. Вестник интенсивной терапии. 2016. № 2. С.28-37] и хронических [Гречко А.В., Буякова И.В., Белобородова Н.В. Дисфункция микробиоты у пациентов с повреждением головного мозга, находящихся в хроническом критическом состоянии. Российский неврологический журнал. 2022;27(1):94-104. Zandalasini М., Pelizzari L., Ciardi G. et al. Bowel dysfunctions after acquired brain injury: a scoping review. Front. Hum. Neurosci. 2023. 17:1146054] критических состояниях, у которых имеется выраженные и длительно существующие значимые негативные изменения качественного и количественного состава микрофлоры кишечника [Гречко А.В., Буякова И.В., Белобородова Н.В. Дисфункция микробиоты у пациентов с повреждением головного мозга, находящихся в хроническом критическом состоянии. Российский неврологический журнал. 2022; 27 (1):94-104], заключающиеся в уменьшении полезных бактерий и увеличении патогенных бактерий [Белобородова Н.В. Метаболизм микробиоты при критических состояниях (обзор и постулаты). Общая реаниматология. 2019;15(6):62-79. Beloborodova N.V., Grechko A.V., Olenin A.Yu. Metabolomic discovery of microbiota dysfunction as the cause of pathology. Metabolomics - New Insights into Biology and Medicine. 2019]. В этой ситуации данные нарушения не могут эффективно нивелироваться Хилак форте вследствие отсутствия у него прямого действия на качественный и количественный состав микрофлоры кишечника [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва,: ГЭОТАР, 2023. - 1166 с].
Недостатком данного препарата, как следует из сведений государственного реестра лекарственных средств [Фармако-терапевтическая группа препарата: Противодиарейное средство], является невозможность его использования для лечения дисбиоза кишечника у больных в острых и хронических критических состояниях из-за отсутствия прямых показаний к лечению дисбиоза кишечника [Показания к применению препарат Хилак форте. Компания Ратиофарм Рус (Германия). Для посещения официального веб-сайта организации используйте следующий адрес http://www.ratiopharm.com].
Известен метабиотический препарат Актофлор-С [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва,: ГЭОТАР, 2023. 1166 с.], содержащий: в миллиграммах на миллилитр: янтарная кислота - не менее 14,0, аспарагиновая кислота - 0,91, глутаминовая кислота - 6,71, аланин - 2,03, глицин - 1,2, валин - 6,68, лейцин - 1,5, лизин - 6,67, метионин - 3,4, муравьиная кислота -10,49, уксусная кислота в пересчете на ацетат натрия - 116, молочная кислота - 24,7. Учитывая данные сведения, по качественномцу и количественному составу Актофлор-С, а также показания к его применению из государственного реестра лекарственных средств [Сведения из государственного реестра лекарственных средств: Продукция: биологически активная добавка к пище «АКТОФЛОР-С». Изготовитель: ООО «Гротекс», Получатель: ООО «Симбиом». Область применения: для реализации населению в качестве биологически активной добавки к пище - источника янтарной кислоты], становится ясным, что препарат может применяться как дополнительный источник органических кислот, янтарной кислоты, аминокислот, для восстановления кишечной микрофлоры и нормализации ее метаболической активности, которые могут быть нарушены, в том числе в результате заболеваний желудочно-кишечного тракта, для устранения симптомов кишечных расстройств и для улучшения обмена веществ, укрепления иммунитета, повышения общей сопротивляемости организма к инфекциям и стрессу [Инструкция препарата Актофлор-С. Изготовитель: ООО «Гротекс», Получатель: ООО «Симбиом»].
Механизм действия Актофлор-С на нормализацию состава и функций микробиоты и восстановления деятельности кишечника косвенно опосредован входящими в него компонентами, а именно содержащимся в нем комплексом аминокислот и органических кислот, являющихся аналогами метаболитов пробиотических бактерий и осуществляющих синергическое действие данных компонентов, входящих в состав комплекса [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва,: ГЭОТАР, 2023. 1166 с]. Это свидетельствует том, что непосредственно на качественный и количественный состав микрофлоры кишечника Актофлор-С оказывает только непрямое влияние. Это особенно неактуально для больных, находящихся в острых [Мазурок В.А., Головкин А.С, Баутин А.Е. и др. Желудочно-кишечный тракт при критических состояниях: первый страдает, последний, кому уделяют внимание. Вестник интенсивной терапии. 2016. №2. С.28-37] и хронических [Гречко А.В., Буякова И.В., Белобородова Н.В. Дисфункция микробиоты у пациентов с повреждением головного мозга, находящихся в хроническом критическом состоянии. Российский неврологический журнал. 2022;27(1):94-104. Zandalasini М., Pelizzari L., Ciardi G. et al. Bowel dysfunctions after acquired brain injury: a scoping review. Front. Hum. Neurosci. 2023. 17:1146054] критических состояниях, у которых имеются выраженные и длительно существующие значимые негативные изменения качественного и количественного состава микрофлоры кишечника [Гречко А.В., Буякова И.В., Белобородова Н.В. Дисфункция микробиоты у пациентов с повреждением головного мозга, находящихся в хроническом критическом состоянии. Российский неврологический журнал. 2022; 27 (1):94-104], заключающиеся в уменьшении полезных и увеличении патогенных бактерий [Белобородова Н.В. Метаболизм микробиоты при критических состояниях (обзор и постулаты). Общая реаниматология. 2019;15(6):62-79. Beloborodova N.V., Grechko A.V., Olenin A.Yu. Metabolomic discovery of microbiota dysfunction as the cause of pathology. Metabolomics - New Insights into Biology and Medicine. 2019]. В этой ситуации, данные нарушения не могут эффективно нивелироваться Актофлор-С, вследствие отсутствия у него прямого действия на качественный и количественный состав компрометированной микрофлоры кишечника [Национальное руководство «Парентаральное и энтеральное питание»» под редакцией С.С. Петрикова. Москва,: ГЭОТАР, 2023. - 1166 с].
Недостатком данного препарата, как следует из сведений государственного реестра лекарственных средств [Продукция: биологически активная добавка к пище «АКТОФЛОР-С»], является невозможность его использования для лечения и профилактики дисбиоза кишечника у больных в острых и хронических критических состояниях из-за отсутствия прямых показаний к лечению дисбиоза кишечника [Инструкция препарата Актофлор-С. Изготовитель: ООО «Гротекс», Получатель: ООО «Симбиом»].
Известна метабиотическая (патент CN115161348A) композиция, содержащая продукт ферментации штамма Lactobacillus salivarius АР-32 и штамм Lactobacillus plantarum LPL28 с массовым соотношением 0,5-2:1-2:1-2:0,5-2 продукта ферментации, Продукт ферментации штамма Lactobacillus acidophilus TYCA06 и Bifidobacterium longum infantum subsp., продукт ферментации штамма infantis BLI-02, продукт ферментации штамма Lactobacillus plantarum LPL28, продукт ферментации штамма Lactobacillus acidophilus TYCA06 и Bifidobacterium longum infantum. Массовое соотношение продукта ферментации подвида штамма BLI-02 составляет 0,5-1:1-1,5:1,5-2:1-2; предпочтительно 0,5-1:1:2:1-2; более предпочтительно 0,5:1:2:1. Данная композиция применяется в качестве: антибактериального средства, ингибирующего по меньшей мере одно из Escherichia coli, Salmonella, Staphylococcus aureus и Helicobacter pylori, средства, повышающего иммунитет, средства для лечения бактериальной диареи, приготовления гипогликемических продуктов, снижающих уровень мочевой кислоты.
Недостатком данной композиции является невозможность ее использования для лечения дисбиоза кишечника у больных в острых и хронических критических состояниях.
Технической задачей изобретения является повышение эффективности лечения дисбиоза кишечника у больных в остром и хроническом критическом состояниях.
Техническим результатом изобретения является повышение эффективности лечения дисбиоза кишечника в постоперационном периоде у больных с черепно-мозговой травмой.
Указанный технический результат достигается тем, что способ лечения дисбиоза кишечника в постоперационном периоде у больных с черепно-мозговой травмой, в котором вводят метабиотический препарат, отличающийся тем, что метабиотический препарат содержит: комплекс лизатов штаммов бактерий: Streptococcus thermophilus В-2011, Bifidobacterium bifidum АС-1579, Bifidobacterium adolescentis AC-1245, Bifidobacterium animalis AC-1248, Bifidobacterium longum AC-1243, Bifidobacterium breve AC-1570, Bifidobacterium infantis AC-1732, Lactobacillus acidophilus B-12024, Lactobacillus acidophilus B-1880, Lactobacillus plantarum B-11007, Lactobacillus plantarum B-11264, Lactobacillus delbrueckii subsp.bulgaricus B-2746, Lactobacillus salivarius B-2214, Lactobacillus salivarius B-2216, Lactobacillus rhamnosus B-8238, Lactobacillus rhamnosus B-6778, Lactobacillus helveticus B-2370, Lactobacillus helveticus B-2371, и питательные субстраты, в следующем соотношении, масс.%:
при этом метабиотический препарат вводят в дозе 0,2 грамма 2 раза в сутки в течение 21 дня.
Возможность достижения технического результата обуслолена тем, что:
Лизат штамма Streptococcus thermophilus В-2011 действует в просвете желудочно-кишечного тракта как антагонист, ингибитор и конкурент патогенных бактерий что, в свою очередь, способствует уменьшению выраженности патологического процесса. [Desaka, Natsumi; Ota, Chinatsu; Nishikawa, Hitomi; Yasuda, Kayo; Ishii, Naoaki; Bito, Tomohiro; Chisinau, Yukio; Naito, Yuji; Higashimura, Yasuki (January 2022). «Streptococcus thermophilus prolongs lifespan by activating the DAF-16-mediated antioxidant pathway in Caenorhabditis elegans.» Journal of Clinical Biochemistry and Nutrition. 70 (1). 7-13. Martinovic A, Cocuzzi R, Arioli S, Mora D.
Лизат штамма Bifidobacterium bifidum AC-1579 обладает иммуномодулирующим и гепатопротективным действием, поддерживает нормальную работу кишечника, увеличивает эффективность терапии синдрома раздраженного кишечника, за счет своих короткоцепочных жирных кислот положительно влияет на жировой обмен, энергетический гомеостаз и метаболизм микробиоты [Sebastian J. Muderspach, Kenneth Jensen, Kristian B.R.M. Krogh, Leila Lo Leggio Chapter 14 - Structure, function, and protein engineering of GH53 β-1,4-galactanases. In Foundations and Frontiers in Enzymology. Glycoside Hydrolases, Academic Press. 2023. P. 295-322. D. Roy Probiotics. Comprehensive Biotechnology (Third Edition). Pergamon. 2019. P. 649-661. Пробиотики и пребиотики / Всемирная гастроэнтерологическая организация (WGO). Практические рекомендации. 2008].
Лизат штамма Bifidobacterium adolescentis АС-1245 способствует позитивному влиянию на деятельность кожи, сосудов и опорно-двигательного аппарата, мозга и желудочно-кишечного тракта, обмена липидов и кальция Лизат Bifidobacterium adolescentis содержит молочную кислоту, что обеспечивает не только противопатогенную защиту кишечника, но и поддерживает нормальную среду в нем [Козин С.В., Кравцов А.А., Кравченко С.В., Иващенко Л.И. Антиоксидантный и анксиолитический эффекты Bifidobacterium adolescentis и Lactobacillus acidophilus в условиях нормобарической гипоксии с гиперкапнией // Вопросы питания. 2021. Т. 90, № 2. С.63-72. Деррьен, Мюриэль; Туррони, Франческа; Вентура, Марко; ван Синдерен, Доуве. Представление об эндогенных видах бифидобактерий в микробиоте кишечника человека в зрелом возрасте. Тенденции в микробиологии. 2022. 30 (10). Р. 940 947. Идальго-Кантабрана, С, Дельгадо, С, Руис, Л., Руас-Мадьедо, П., Санчес, Б., Маргольес, А.. «Бифидобактерий и их воздействие на здоровье». Спектр микробиологии. Американское общество микробиологии. 2017 г. 5. (3)].
Лизат штамма Bifidobacterium animalis АС-1248 обладает антиоксидантными, иммуномодулирующими, противомикробными и антибактериальными свойствами. Ультрализат на основе Bifidobacterium animalis содержит фрагменты мембран бактерий, пептиды, аминокислоты, органические короткоцепочечные кислоты, полисахариды, липиды, некоторые витамины, кофакторы ферментов и другие соединения, стимулирующие рост и жизнедеятельность собственной микрофлоры [Е.М.М. Quigley Bifidobacterium animalis spp.Lactis. The Microbiota in Gastrointestinal Pathophysiology. Academic Press. 2017. P. 127-130. Faqir Muhammad Anjum, Farhan Saeed, Muhammad Afzaal, Ali Ikram, Muhammad Azam The effect of thermal processing on probiotics stability. Advances in Dairy Microbial Products. Woodhead Publishing. 2022. P. 295-302].
Лизат штамма Bifidobacterium longum AC-1243 имеет иммуномодулирующие, противомикробные, противоопухолевые и антиаллергические свойства, а также может применяться для профилактики и лечения заболевания, вызванного Clostridium difficile. Лизат на основе Bifidobacterium longum содержит фрагменты мембран бактерий, молочную кислоту, пептидогликаны, экзополисахариды, тейхоевые кислоты, пептиды, аминокислоты и другие соединения, стимулирующие рост и жизнедеятельность собственной микрофлоры. [Bonfrate L., Di Palo D.M., Celano G., Albert A., Vitellio P., De Angelis M. et al. Effects of Bifidobacterium longum BB536 and Lactobacillus rhamnosus HN001 in IBS patients // Eur. J. Clin. Invest. 2020. Vol.50. Article ID el3201. Clinical response and changes of cytokines and zonulin levels in patients with diarrhoea-predominant irritable bowel syndrome treated with bifidobacterium longum ESI for 8 or 12 weeks: a preliminary report // J. Clin. Med. 2020. Vol.9, N 8. P. 2353].
Лизат штамма Bifidobacterium breve AC-1570 обладает иммуномодулирующими, противоопухолевыми и противовоспалительными свойствами, а также стимулирует рост и жизнедеятельность собственной микрофлоры. За счет имеющейся масляной кислоты [Yang J and Yang H Antibacterial Activity of Bifidobacterium breve Against Clostridioides difficile. Front. Cell. Infect. Microbiol.2019. doi: 10.3389/fcimb.2019.00288. Захарова Ю.В., Леванова Л.А. Современные представления о таксономии, морфологических и функциональных свойствах бифидобактерий. Фундаментальная и клиническая медицина. 2018. Т 3. № 1. С. 90-101. Гури Я., Ричарде Д.М., Рахими Э.Ф., Крилл Дж. Т., Елинек К.А., Дюпон А.В. Систематический обзор рандомизированных контролируемых исследований пробиотиков, пребиотиков и синбиотиков при воспалительных заболеваниях кишечника. Гастроэнтерол Clin Exp (Обзор). 2014. 7: 473-87].
Лизат штамма Bifidobacterium infantis АС-1732 снижает риск инфекционных кишечных заболеваний, способствует нормализации метаболизма глюкозы. Лизат Bifidobacterium infantis содержит фрагменты мембран бактерий, короткоцепочечные жирные кислоты, пептиды, белки, экзополисахариды, тейхоевые кислоты, пептидогликаны, аминокислоты, бактериоцины и другие соединения, которые, снижая рН в просвете кишечника, ингибируют рост патогенных бактерий, поддерживают целостность эпителия кишечника, защищают его от химических воздействий, увеличивают биодоступность минералов и снабжают энергией клетки эпителия кишечника [Liu М, Gao Н, Miao J, Zhang Z, Zheng L, Li F, Zhou S, Zhang Z, Li S, Liu H, Sun J. Helicobacter pylori infection in humans and phytotherapy, probiotics, and emerging therapeutic interventions: a review. Front Microbiol. 2024 Jan 10;14:1330029. doi: 10.3389/fmicb.2023.1330029. Yang J, Yang H. Antibacterial Activity of Bifidobacterium breve Against Clostridioides difficile. Front Cell Infect Microbiol. 2019. 7;9:288. Бухарин О.В., Иванова Е.В., Чайникова И.Н., Перунова Н.Б., Никифоров И.А., Челпаченко О.Е., Бондаренко Т.А., Бекпергенова А.В. Влияние кишечных микросимбионтов на продукцию цитокинов в системе in vitro. Медицинская иммунология. 2023; 25(6). 1371-1388].
Лизат штамма Lactobacillus acidophilus В-12024 и Штамм Lactobacillus acidophilus В-1880 обладает иммуностимулирующими, противоаллергическими, антимикробными и противовоспалительными свойствами, что поддерживает работу кишечника и стимулирует роста собственной микробиоты [Козин СВ., Кравцов А.А., Кравченко СВ., Иващенко Л.И. Антиоксидантный и анксиолитический эффекты Bifidobacterium adolescentis и Lactobacillus acidophilus в условиях нормобарической гипоксии с гиперкапнией // Вопросы питания. 2021. Т. 90, № 2. С.63-72. Claire Buchta Rosean, Tzu-Yu Feng, Francesca N. Azar, Melanie R. Rutkowski, Chapter Five - Impact of the microbiome on cancer progression and response to anti-cancer therapies. Advances in Cancer Research. Academic Press. Volume 143. 2019. P. 255-294].
Лизат штамма Lactobacillus plantarum B-l 1007 и Штамм Lactobacillus plantarum B-l1264 обладает иммуномодулирующей активностью, а также антимикробным и пребиотическим эффектами, что способствует нормализации работы кишечника. Лизат Lactobacillus plantarum содержит фрагменты мембран бактерий, молочную кислоту, пептиды, аминокислоты, полисахариды, витамины группы В, и короткоцепочечные жирные кислоты, которые, стимулируют рост и жизнедеятельность собственной микрофлоры кишечника [Fidanza М., Panigrahi P., Kollmann T.R. Lactiplantibacillus plantarum-Nomad and Ideal Probiotic.2021. Front. Microbiol. 12:712236].
Лизат штамма Lactobacillus delbrueckii subsp.Bulgaricus B-2746 способствует усилению барьерной функции кишечника и увеличению популяции собственных бифидобактерий, лактобацилл и лактококков, что обусловливает эффект иммуномодуляция [El Kafsi Н., Binesse J., Loux V. tt all. Lactobacillus delbrueckii ssp.lactis and ssp.bulgaricus: a chronicle of evolution in action. BMC Genomics. 2014 May 28;15(1):407. doi: 10.1186/1471-2164-15-407].
Лизат штамма Lactobacillus salivarius B-2214 и Штамм Lactobacillus salivarius B-2216 обладает антимикробной и антиоксидантной активностью. Метаболиты и компоненты ее клеточной стенки стимулируют рост и жизнедеятельность собственной микрофлоры кишечника [Chit Laa Poh, Kanwal Khalid, Hui Xuan Lim. Chapter 23 -Probiotics: A solution to the prevention of antimicrobial resistance. In Developments in Microbiology. Antibiotics - Therapeutic Spectrum and Limitations. 2023. P. 595-609. Zeneng Wang, Lucas J. Osborn. 5.11 - The microbiome and cardiovascular disease: Implications in Precision Medicine. Comprehensive Precision Medicine. Elsevier. 2024. P. 145-168].
Лизат штамма Lactobacillus rhamnosus B-8238 и Штамм Lactobacillus rhamnosus B-6778 обладает иммунной, антимикробной активностью в отношении патогенных микроорганизмов. Содержащаяся конъюгированная линолевая кислота в составе лизата является мощным антиоксидантом, антиканцерогеном и антикатаболиком [Bonfrate L., Di Palo D.M., Celano G., Albert A, Vitellio P., De Angelis M. et al. Effects of Bifidobacterium longum BB536 and Lactobacillus rhamnosus HN001 in IBS patients // Eur. J. Clin. Invest. 2020. Vol.50. Article ID e13201. Claire Buchta Rosean, Tzu-Yu Feng, Francesca N. Azar, Melanie R. Rutkowski. Chapter Five - Impact of the microbiome on cancer progression and response to anti-cancer therapies. Advances in Cancer Research. Academic Press. Volume 143. 2019. Pages 255-294].
Лизат штамма Lactobacillus helveticus B-2370 и Штамм Lactobacillus helveticus B-2371 обладает антимикробными и пребиотическими свойствами, что способствует нормализации микрофлоры кишечника и стимулирует его иммунные клетки. Лизат Lactobacillus способен угнетать потенциально вредные бактерии и предотвращать желудочно-кишечные инфекции, а также положительно влиять на состав кишечной микробиоты [Griffiths M.W., Tellez A.M. Lactobacillus helveticus: the proteolytic system. Front. Microbiol. 2013. 4.30. doi: 10.3389/fmicb.2013.00030. Taverniti V and Guglielmetti S Health-promoting properties of Lactobacillus helveticus. Front. Microbio.2012. 3:392. doi: 10.3389/fmicb.2012.00392].
Применение лизата термофильного стрептококка в сочетании с комплексом лизатов лактобактерий и бифидобактерий приводит к синергизму их лечебных эффектов, что позволяет значительно эффективнее купировать дисбиоз кишечника за счет позитивной регуляции качественного и количественного состава микрофлоры, а также быстрее нормализовывать его многочисленные функции, в особенности иммунную. Более того, комбинация метабиотиков помимо восстановления кишечной флоры может обеспечивать ее более высокую антимикробную активность против патогенных микроорганизмов, в частности сальмонелл, кишечной палочки, золотистого стафилококка и снижать дозу применяемых антибиотиков [Британская энциклопедия «Streptococcus». Британская энциклопедия онлайн. 13 апреля 2011 года. Британская энциклопедия «Термофил». Британская энциклопедия онлайн, 2011. 24 апреля 2011 года. «Streptococcus Thermophilus: бактерия, безвредная для здоровья». Международные научные сотрудники. 14 ноября 2006. Веб. 25 апреля 2011. Худ, Керенза; Наттолл, Джеки; Гиллеспи, Дэвид; Шепард, Виктория; Вуд, Фиона; Дункан, Донна; Стэнтон, Хелен; Эспинасс, Од; Вуттон, Мэнди; Ачарья, Аруна; Аллен, Стивен; Байер, Энтони; Картер, Бен; Коэн, Дэвид; Фрэнсис, Ник; Хоу, Робин; Манцурани, Эфи; Томас-Джонс, Эмма; Тогхилл, Алун; Батлер, Кристофер С.(2014). «Оценка технологий здравоохранения» 18 (63): 1-84. doi: 10.3310/hta18630. ISSN 1366-5278. PMC 4781053. PMID 25331573. Hamdaoui, Nora &Azghar, All & Benkirane, Chaymae & Bouaamali, Haytham & Mouncif, Mohamed & OU-yahia, Douaae & Guerrouj, Bouchra & Assahraou, Abdessalam & Maleeb, Adil & Mustapha, Meziane& Alkowni, Raed & Jodeh, Shehdeh. (2023). Probiotic properties and antibiotic susceptibility assessment of Streptococcus thermophilus isolates. 10.21203/rs.3.rs-2917183/vl].
Метабиотический препарат для лечения дисбиоза кишечника у больных с черепно-мозговой травмой получают следующим образом. При этом предварительно проводят культивирование отдельно биомассы каждого из указанных выше штаммов бактерий в питательной водной среде в течение 16-24 часов до достижения высокой (109 КОЕ/мл) плотности микроорганизмов при оценке методом микроскопии. Затем полученную биомассу штаммов бактерий заданного штамма сливают, отфильтровывают сквозь сито в чистые продезинфицированные емкости и хранят до получения результатов контроля качества не более 7 суток, соблюдая температуру хранения+4-+10°С. После подтверждения контроля качества биомассы заданного штамма бактерий составляющей не менее 1×109 КОЕ/мл в емкость с данной биомассой вносят протеолитический фермент, осуществляют перемешивание при заданной оптимальной температуре работы фермента в течение 3 ч, затем проводят пастеризацию при 95°С в течение 60 минут, таким образом получают лизаты всех заявленных в формуле штаммов бактерий. После этого производят смешивание, всех полученных лизатов штаммов бактерий, мальтодекстрина, молочной кислоты и концентрата для безалкогольного напитка Камбиочай в заданном соотношении компонент масс.%. Затем данную смесь пастеризуют при температуре 95°С в течение 60 минут, охлаждают до температуры 40°С и проводят сушку при рН 3,0 4,0 и температуре 80°С на распылительной сушилке.
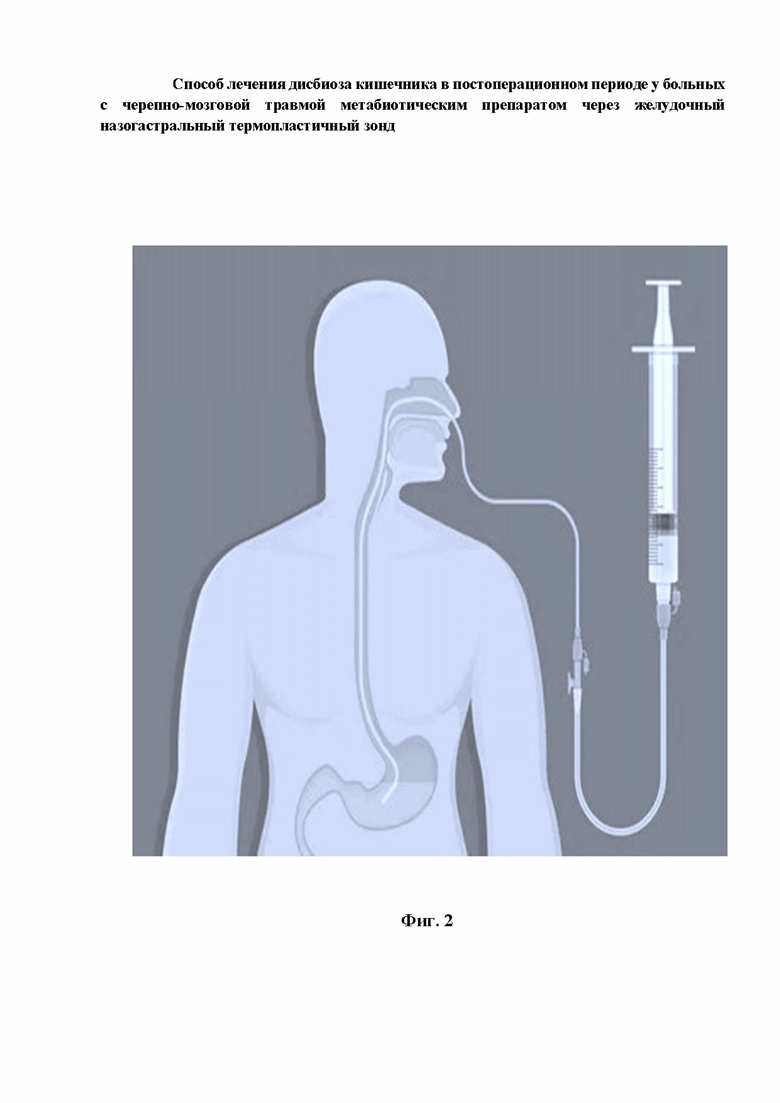
Метабиотический препарат для лечения дисбиоза кишечника у больных с черепно-мозговой травмой вводят перорально или через желудочный назогастральный термопластичный зонд в дозе 0,2 грамма 2 раза в сутки в течение 21 дня.
На фиг.1 представлена схема ввода метабиотического препарата перорально.
На фиг.2 представлена схема ввода метабиотического препарата через желудочный назогастральный термопластичный зонд.
В таблице 1 представлены результаты лечения дисбиоза кишечника в постоперационном периоде у больных с черепно-мозговой травмой за период от 1 до 21 суток со стандартной инфузионной терапией и питанием без применения заявленного метабиотического препарата группы I и результаты лечения кишечника в постоперационном периоде у больных с черепно-мозговой травмой за период от 1 до 21 суток со стандартной инфузионной терапией и питанием, вводили заявленный метабиотический препарат в дозе 0,2 грамма 2 раза в сутки за период от 1 до 21 суток группы II. Данные результаты представлены в виде значений: медианы (верхнего и нижнего квартиля) - Me (Ql; Qh).
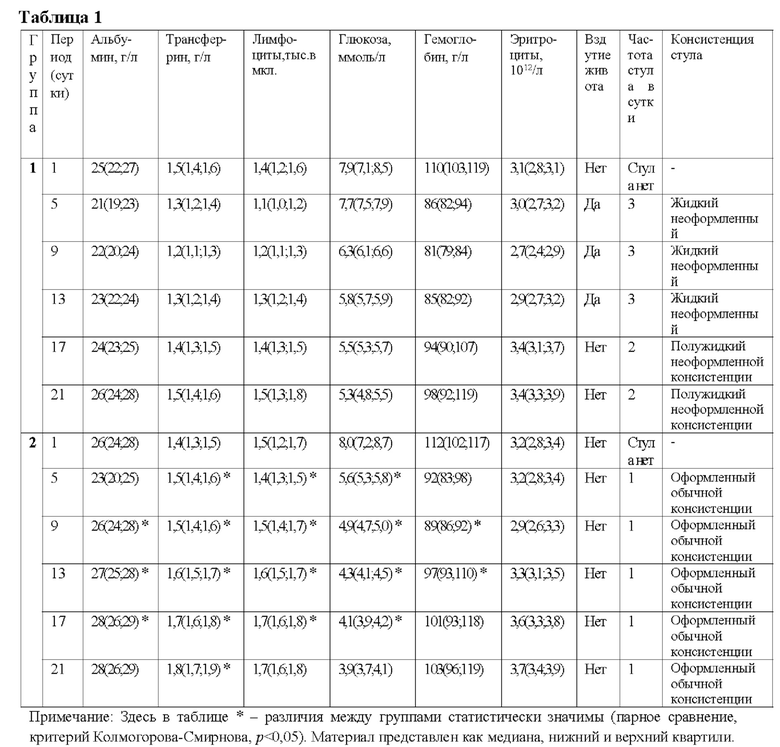
Как следует из данных, представленных в таблице 1, у больных группы II применение в программе лечения заявленного метабиотического препарата в дозе 0,2 грамма 2 раза в сутки за период от 1 до 21 суток способствовало статистически достоверному улучшению функционирования желудочно-кишечного тракта, а также содержанию в плазме крови альбумина, трансферрина, абсолютного количества лимфоцитов, глюкозы и гемоглобина, по сравнению с аналогичными параметрами больных группы I.
При этом применение заявленного препарата в дозе 0,2 грамма не менее 2 раз в сутки основано на сравнении с результатами его применения в дозе 0,2 грамма 1 раз в сутки.
В таблице 2 представлены результаты лечения дисбиоза кишечника в постоперационном периоде у больных с черепно-мозговой травмой за период от 1 до 21 суток со стандартной инфузионной терапией и питанием и введениемм заявленногого метабиотического препарата в дозе 0,2 грамма 1 раза в сутки за период от 1 до 21 суток, группы I и результаты лечения кишечника в постоперационном периоде у больных с черепно-мозговой травмой за период от 1 до 21 суток со стандартной инфузионной терапией и введением заявленного метабиотического препарата в дозе 0,2 грамма 2 раза в сутки за период от 1 до 21 суток группы П. Данные результаты представлены в виде значений: медианы (верхнего и нижнего квартиля) -Me (Ql; Qh).
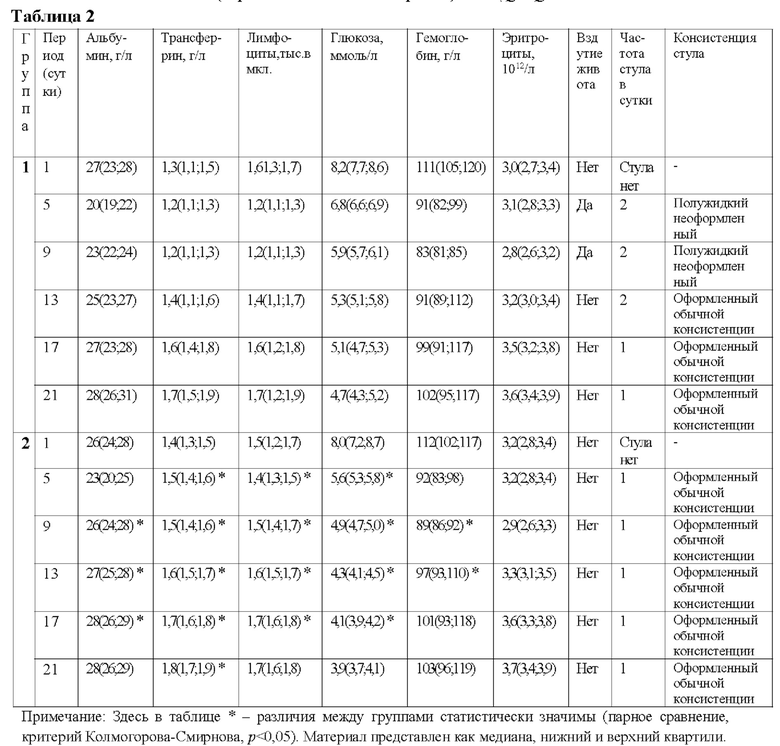
Как следует из данных, представленных в таблице 2, у больных группы II применение в программе лечения заявленного метабиотического препарата в дозе 0,2 грамма 2 раза в сутки за период от 1 до 21 суток способствовало статистически достоверному улучшению на 5 и 9 сутки периода наблюдения функционирования желудочно-кишечного тракта, содержанию в плазме крови альбумина, трансферрина, абсолютного количества лимфоцитов, глюкозы и на 9 сутки - гемоглобина по сравнению с аналогичными параметрами больных группы I, у которых использовался метабиотический препарат в дозе 0,2 грамма 1 раз в сутки за период от 1 до 21 суток способствовало статистически достоверному улучшению на 17 и 21 сутки.
Таким образом, на основании вышеизложенного, очевидно, что использование заявленного метабиотического препарата в дозе 0,2 грамма 2 раза в сутки является оптимальным для действенного лечения дисбиоза кишечника у больных с черепно-мозговой травмой за период от 1 до 21 суток.
Клинический пример 1
Больной А., 32 года, 12.06.2023 года в 12 часов 20 минут доставлен в отделение реанимации и интенсивной терапии городской клинической больницы №1 имени А.Н. Кабанова, в состоянии медикаментозного сна с интубационной трубкой на искусственной вентиляции легких, из неотложной нейрохирургической операционной, где ему проводилось оперативное лечение опорожнение субдуральной гематомы в объеме 160 миллилитров вследствие полученной черепно-мозговой трамы.
В отделении реанимации и интенсивной терапии больному продолжена искусственная вентиляция легких в режиме управляемого дыхания, назначены анальгетики, седативные препараты, ингибиторы протонной помпы, антибактериальная и инфузионно-трансфузионная терапия, а также нутритивная поддержка. Больному в левый носовой ход установлен термопластичный назогастральный зонд для декомпресии желудка и введения метабиотического препарата в дозе 0,2 грамма 2 раза в сутки.
Используемый метабиотический препарат содержит: комплекс лизатов штаммов бактерий по классификации ВКПМ (Всероссийская коллекция промышленных микроорганизмов, НИЦ «Курчатовский институт») с датой депонирования 05.02.2023:
Streptococcus thermophilus В-2011, Bifidobacterium bifidum АС-1579, Bifidobacterium adolescentis AC-1245, Bifidobacterium animalis AC-1248, Bifidobacterium longum AC-1243, Bifidobacterium breve AC-1570, Bifidobacterium infantis AC-1732, Lactobacillus acidophilus B-12024, Lactobacillus acidophilus B-l880, Lactobacillus plantarum B-11007, Lactobacillus plantarum B-l 1264, Lactobacillus delbrueckii subsp.bulgaricus B-2746, Lactobacillus salivarius B-2214, Lactobacillus salivarius B-2216, Lactobacillus rhamnosus B-8238, Lactobacillus rhamnosus B-6778, Lactobacillus helveticus B-2370, Lactobacillus helveticus B-2371, переносящий и питательный субстраты в следующем соотношении компонент, масс.%:
В общем анализе крови больного регистрируется количество эритроцитов - 3,3⋅1012/л, а наличие в них гемоглобина - 111 г/л. В биохимическом анализе содержание в плазме крови глюкозы - 8,7 ммоль/л, альбумина - 24 г/л, трансферрина - 1,4 г/л, а абсолютного количества лимфоцитов - 1,6 тысячи в микролитре.
Осуществляемые у больного с черепно-мозговой травмой, находящегося в критическом состоянии в течение пяти суток, метабиотическая терапия на фоне выше указанного стандартного лечения способствовали не только неимению симптомов дисбиоза кишечника, о чем свидетельствовали отсутствие его вздутия, нормальная частота стула - 1 раз в сутки, а также его оформленность и обычность консистенции, но и улучшению параметров питательного статуса, что подтверждалось увеличением в плазме крови альбумина до 25 г/л, трансферрина до 1,6 г/л и абсолютного количества лимфоцитов до 1,5 тысяч в микролитре.
Отсутствие дисбиоза кишечника у больного подтверждалось не только снижением глюкозы крови до 5,6 ммоль/л, но и отсутствием уменьшения количества эритроцитов 3,4⋅1012/л в циркулирующей крови.
На девятые сутки у больного регистрируется отсутствие симптомов дисбиоза кишечника, что подтверждается неимением его вздутия, нормальной частотой стула 1 раз в сутки, а также его оформленностью и обычностью консистенции. В это же время фиксируется дальнейшее улучшение питательного статуса, которое подтверждается данными альбумина - 27 г/л, трансферрина - 1,6 г/л и абсолютного количества лимфоцитов - 1,7 тысяч в микролитре.
Это способствовало тому, что у больного начали регистрироваться элементы сознания и возникновение самостоятельного дыхания. По этой причине больной был переведен с предыдущего режима искусственной вентиляции легких на более физиологический режим искусственной вентиляции легких, а именно самостоятельного дыхания с постоянной поддержкой давлением в дыхательных путях.
На тринадцатые сутки у больного не фиксируются симптомы дисбиоза кишечника, что подтверждается неимением его вздутия, нормальной частотой стула 1 раз в сутки, а также его оформленностью и обычностью консистенции. В эти же сроки отмечается сохраняющаяся стабильность параметров питательного статуса, которая подтверждается данными альбумина - 27 г/л, трансферрина - 1,6 г/л и абсолютного количества лимфоцитов - 1,7 тысяч в микролитре. Также у больного продолжается положительная динамика по уровню сознания и дыхания, что способствовало переводу пациента на еще более физиологический режим искусственной вентиляции поддержку давлением.
Осуществляемая метабиотическая терапия и энтеральное питание способствовали тому, что на семнадцатые сутки больной, у которого отсутствовали симптомы дисбиоза кишечника, что подтверждалось отсутствием его вздутия, нормальной частотой стула 1раз в сутки, а также его оформленностью и обычностью консистенции, а также фиксировалось динамическое улучшение параметров питательного статуса, о чем свидетельствовали данные в альбумина - 28 г/л, трансферрина до 1,7 г/л и абсолютного количества лимфоцитов до 1,7 тысяч в микролитре, не только пришел в сознание и стал доступен продуктивному вербальному контакту, но и начал адекватно самостоятельно дышать - частота дыханий - 20 в минуту, что, в свою очередь, потребовало прекращение искусственной вентиляции легких.
На двадцать первые сутки лечения в отделении реанимации и интенсивной терапии у больного фиксируется ясное сознание и адекватное самостоятельное дыхание - 18 в минуту. В связи с затруднением глотания, вследствие черепно-мозговой травмы больному, продолжает проводиться введение в назогастральный зонд метабиотического препарата в дозе 0,2 грамма 2 раза в сутки.
В это время у больного, как и на протяжении всего времени пребывания в отделения реанимации и интенсивной терапии, не обнаруживалось симптомов дисбиоза кишечника, что подтверждалось отсутствием его вздутия, нормальной частотой стула 1раз в сутки, а также его оформленностью и обычностью консистенции. Также у больного фиксировалась стабильность параметров питательного статуса, о чем свидетельствовали данные альбумина - 28 г/л, трансферрина до 1,7 г/л и абсолютного количества лимфоцитов до 1,7 тысяч в микролитре.
На 22 сутки у больного, в связи с восстановлением акта глотания, убран назогастральный зонд. Симптомов дисбиоза кишечника нет. На 23 сутки больной переведен в профильное нейрохирургическое отделение для дальнейшего лечения.
Клинический пример 2
Больной Б., 39 лет, 23.08.2023 года в 20 часов 10 минут доставлен в отделение реанимации и интенсивной терапии городской клинической больницы №1 имени А.Н. Кабанова, в состоянии медикаментозного сна с интубационной трубкой на искусственной вентиляции легких, из неотложной нейрохирургической операционной, где ему проводилось оперативное лечение опорожнение субдуральной гематомы в объеме 130 миллилитров вследствие полученной черепно-мозговой трамы.
В отделении реанимации и интенсивной терапии больному продолжена искусственная вентиляция легких в режиме управляемого дыхания, назначены анальгетики, седативные препараты, ингибиторы протонной помпы, антибактериальная и инфузионно-трансфузионная терапия, а также нутритивная поддержка. Больному в левый носовой ход установлен термопластичный назогастральный зонд для декомпресии желудка и введения метабиотического препарата в дозе 0,2 грамма 2 раза в сутки.
Используемый метабиотический препарат содержит: комплекс лизатов штаммов бактерий по класификации ВКПМ (Всероссийская коллекция промышленных микроорганизмов, НИЦ «Курчатовский институт») с датой депонирования 05.02.2023:
Streptococcus thermophilus В-2011, Bifidobacterium bifidum АС-1579, Bifidobacterium adolescentis AC-1245, Bifidobacterium animalis AC-1248, Bifidobacterium longum AC-1243, Bifidobacterium breve AC-1570, Bifidobacterium infantis AC-1732, Lactobacillus acidophilus B-12024, Lactobacillus acidophilus B-1880, Lactobacillus plantarum B-11007, Lactobacillus plantarum B-11264, Lactobacillus delbrueckii subsp.bulgaricus B-2746, Lactobacillus salivarius B-2214, Lactobacillus salivarius B-2216, Lactobacillus rhamnosus B-8238, Lactobacillus rhamnosus B-6778, Lactobacillus helveticus B-2370, Lactobacillus helveticus B-2371, переносящий и питательный субстраты в следующем соотношении компонент, масс.%:
В общем анализе крови больного регистрируется количество эритроцитов - 3,3⋅1012/л, а наличие в них гемоглобина - 112 г/л. В биохимическом анализе содержание в плазме крови глюкозы 8,5 ммоль/л, альбумина - 24 г/л, трансферрина - 1,4 г/л, а абсолютного количества лимфоцитов - 1,2 тысячи в микролитре.
Осуществляемые у больного с черепно-мозговой травмой, находящегося в критическом состоянии, в течение пяти суток, метабиотическая терапия на фоне выше указанного стандартного лечения, способствовали не только неимению симптомов дисбиоза кишечника, о чем свидетельствовали отсутствие его вздутия, нормальная частота стула 1 раз в сутки, а также его оформленность и обычность консистенции, но и улучшению параметров питательного статуса, что подтверждалось увеличением в плазме крови альбумина до 25 г/л, трансферрина до 1,5 г/л и абсолютного количества лимфоцитов до 1,4 тысяч в микролитре.
Отсутствие дисбиоза кишечника у больного подтверждалось не только снижением глюкозы крови до 5,6 ммоль/л, но и отсутствием уменьшения количества эритроцитов 3,3⋅1012/л в циркулирующей крови.
На девятые сутки у больного регистрируется отсутствие симптомов дисбиоза кишечника, что подтверждается неимением его вздутия, нормальной частотой стула 1 раз в сутки, а также его оформленностью и обычностью консистенции. В это же время, фиксируется дальнейшее улучшение питательного статуса, которое подтверждается данными альбумина - 29 г/л, трансферрина - 1,7 г/л и абсолютного количества лимфоцитов - 1,8 тысяч в микролитре.
Это способствовало тому, что у больного начали регистрироваться элементы сознания и возникновение самостоятельного дыхания. По этой причине больной был переведен с предыдущего режима искусственной вентиляции легких на более физиологический режим искусственной вентиляции легких, а именно самостоятельного дыхания с постоянной поддержкой давлением в дыхательных путях.
На тринадцатые сутки у больного не фиксируются симптомы дисбиоза кишечника, что подтверждается неимением его вздутия, нормальной частотой стула 1 раз в сутки, а также его оформленностью и обычностью консистенции. В эти же сроки отмечается стабильность параметров питательного статуса, которая подтверждается данными альбумина - 29 г/л, трансферрина - 1,7 г/л и абсолютного количества лимфоцитов - 1,8 тысяч в микролитре. Также у больного продолжается положительная динамика по уровню сознания и дыхания, что способствовало переводу пациента на еще более физиологический режим искусственной вентиляции поддержку давлением.
Осуществляемая метабиотическая терапия и энтеральное питание способствовали тому, что на семнадцатые сутки больной, у которого отсутствовали симптомы дисбиоза кишечника, что подтверждалось отсутствием его вздутия, нормальной частотой стула - 1 раз в сутки, а также его оформленностью и обычностью консистенции, а также фиксировалось динамическое улучшение параметров питательного статуса, о чем свидетельствовали данные в альбумина - 29 г/л, трансферрина до 1,8 г/л и абсолютного количества лимфоцитов до 1,8 тысяч в микролитре, не только пришел в сознание и стал доступен продуктивному вербальному контакту, но и начал адекватно самостоятельно дышать - частота дыханий - 21 в минуту, что, в свою очередь, потребовало прекращение искусственной вентиляции легких. Кроме того, у больного отмечается частичное восстановление глотательного рефлекса.
На девятнадцатые сутки у больного на фоне полного восстановление глотательного рефлекса, убран назогастральный зонд. Метабиотический препарат в дозе 0,2 грамма 2 раза в сутки больной употребляет перорально.
На двадцать перые сутки лечения в отделении реанимации и интенсивной терапии у больного фиксируется ясное сознание и адекватное самостоятельное дыхание - 18 в минуту, а также спосбность самостоятельно употреблять перорально метабиотический препарат в дозе 0,2 грамма 2 раза в сутки.
В это время у больного, как и на протяжении всего времени пребывания в отделения реанимации и интенсивной терапии, не обнаруживалось симптомов дисбиоза кишечника, что подтверждалось отсутствием его вздутия, нормальной частотой стула - 1 раз в сутки, а также его оформленностью и обычностью консистенции. Также у больного фиксировалась стабильность параметров питательного статуса, о чем свидетельствовали данные альбумина до 29 г/л, трансферрина до 1,8 г/л и абсолютного количества лимфоцитов до 1,8 тысяч в микролитре.
На 22 сутки больной переведен в профильное нейрохирургическое отделение для дальнейшего лечения.
Клинический пример 3
Больной В., 41 год, 11.09.2023 года в 16 часов 05 минут доставлен в отделение реанимации и интенсивной терапии городской клинической больницы №1 имени А.Н. Кабанова, в состоянии медикаментозного сна с интубационной трубкой на искусственной вентиляции легких, из неотложной нейрохирургической операционной, где ему проводилось оперативное лечение опорожнение субдуральной гематомы в объеме ПО миллилитров вследствие полученной черепно-мозговой трамы.
В отделении реанимации и интенсивной терапии больному продолжена искусственная вентиляция легких в режиме управляемого дыхания, назначены анальгетики, седативные препараты, ингибиторы протонной помпы, антибактериальная и инфузионно-трансфузионная терапия, а также нутритивная поддержка. Больному в левый носовой ход установлен термопластичный назогастральный зонд для декомпресии желудка и введения метабиотического препарата в дозе 0,2 грамма 2 раза в сутки.
Используемый метабиотический препарат содержит: комплекс лизатов штаммов бактерий по класификации ВКПМ (Всероссийская коллекция промышленных микроорганизмов, НИЦ «Курчатовский институт») с датой депонирования 05.02.2023:
Streptococcus thermophilus В-2011, Bifidobacterium bifidum АС-1579, Bifidobacterium adolescentis AC-1245, Bifidobacterium animalis AC-1248, Bifidobacterium longum AC-1243, Bifidobacterium breve AC-1570, Bifidobacterium infantis AC-1732, Lactobacillus acidophilus B-12024, Lactobacillus acidophilus B-1880, Lactobacillus plantarum B-11007, Lactobacillus plantarum B-11264, Lactobacillus delbrueckii subsp.bulgaricus B-2746, Lactobacillus salivarius B-2214, Lactobacillus salivarius B-2216, Lactobacillus rhamnosus B-8238, Lactobacillus rhamnosus B-6778, Lactobacillus helveticus B-2370, Lactobacillus helveticus B-2371, переносящий и питательный субстраты в следующем соотношении компонент, масс.%:
В общем анализе крови больного регистрируется количество эритроцитов - 3⋅1012/л, а наличие в них гемоглобина - 107 г/л. В биохимическом анализе содержание в плазме крови глюкозы - 7,7 ммоль/л, альбумина - 24 г/л, трансферрина - 1,3 г/л, а абсолютного количества лимфоцитов - 1,2 тысячи в микролитре.
Осуществляемые у больного с черепно-мозговой травмой, находящегося в критическом состоянии, в течение пяти суток, метабиотическая терапия на фоне выше указанного стандартного лечения, способствовали не только неимению симптомов дисбиоза кишечника, о чем свидетельствовали отсутствие его вздутия, нормальная частота стула - 1раз в сутки, а также его оформленность и обычность консистенции, но и улучшению параметров питательного статуса, что подтверждалось увеличением в плазме крови альбумина до 25 г/л, трансферрина до 1,5 г/л и абсолютного количества лимфоцитов до 1,5 тысяч в микролитре.
Отсутствие дисбиоза кишечника у больного подтверждалось не только снижением глюкозы крови до 5,7 ммоль/л, но и отсутствием уменьшения количества эритроцитов -3,1⋅1012/л в циркулирующей крови.
На девятые сутки у больного регистрируется отсутствие симптомов дисбиоза кишечника, что подтверждается неимением его вздутия, нормальной частотой стула 1 раз в сутки, а также его оформленностью и обычностью консистенции. В это же время, фиксируется дальнейшее улучшение питательного статуса, которое подтверждается данными альбумина - 28 г/л, трансферрина - 1,6 г/л и абсолютного количества лимфоцитов - 1,6 тысяч в микролитре. В эти же сроки у больного регистрируются элементы сознания и возникновение самостоятельного дыхания. Это послужило причиной перевода больного с предыдущего режима искусственной вентиляции легких на более физиологический режим искусственной вентиляции легких, а именно самостоятельного дыхания с постоянной поддержкой давлением в дыхательных путях.
На тринадцатые сутки у больного не фиксируются симптомы дисбиоза кишечника, что подтверждается неимением его вздутия, нормальной частотой стула - 1раз в сутки, а также его оформленностью и обычностью консистенции. В эти же сроки отмечается дальнейшая стабилизация параметров питательного статуса, которое подтверждается данными альбумина - 29 г/л, трансферрина - 1,7 г/л и абсолютного количества лимфоцитов - 1,7 тысяч в микролитре. Также у больного отмечается восстановление акта глотания, ясного сознания с возможностью продуктивного вербального контакта и стабильное самостоятельное дыхание 22 в минуту, что потребовало прекращение искусственной вентиляции легких.
Осуществляемая метабиотическая терапия на фоне стандартного лечения способствовали тому, что на семнадцатые сутки больной, у которого отсутствовали симптомы дисбиоза кишечника, что подтверждалось неимением его вздутия, нормальной частотой стула 1 раз в сутки, а также его оформленностью и обычностью консистенции, а также фиксировалось динамическое улучшение параметров питательного статуса, о чем свидетельствовали данные в альбумина - 29 г/л, трансферрина до 1,8 г/л и абсолютного количества лимфоцитов до 1,8 тысяч в микролитре. В эти же сроки, у больного полностью восстановился глотательный рефлекс. По этой причине у него убран назогастральный зонд, а метабиотический препарат в дозе 0,2 грамма 2 раза в сутки больной употребляет перорально.
На двадцать первые сутки лечения в отделении реанимации и интенсивной терапии у больного фиксируется ясное сознание и адекватное самостоятельное дыхание - 17 в минуту, а также способность самостоятельно употреблять метабиотический препарат в дозе 0,2 грамма 2 раза в сутки.
В это время, у больного, как и на протяжении всего времени пребывания в отделения реанимации и интенсивной терапии не обнаруживалось симптомов дисбиоза кишечника, что подтверждалось отсутствием его вздутия, нормальной частотой стула - 1 раз в сутки, а также его оформленностью и обычностью консистенции. Также, у больного фиксировалась стабильность параметров питательного статуса, о чем свидетельствовали данные альбумина до 29 г/л, трансферрина до 1,9 г/л и абсолютного количества лимфоцитов до 1,8 тысяч в микролитре.
На 22 сутки больной переведен в профильное нейрохирургическое отделение для дальнейшего лечения.
Таким образом, решается техническая задача - повышение эффективности лечения дисбиоза кишечника у больных в постоперационном периоде с черепно-мозговой травмой. В предлагаемом способе лечения дисбиоза кишечника в постоперационном периоде у больных с черепно-мозговой травмой метабиотический препарат должен использоваться в дозе 0,2 грамма 2 раза в сутки в течение 21 дня. При этом предлагаемый нами способ простой в применении, неинвазивен, не требует высоких материальных затрат, лишен недостатков, которые встречаются в других изученных нами способах лечения дисбиоза кишечника. Использование метабиотического препарата для лечения дисбиоза кишечника у больных с черепно-мозговой травмой в постоперационном периоде позволит уменьшать выраженность питательной и полиорганной недостаточности для снижения летальности.
| название | год | авторы | номер документа |
|---|---|---|---|
| Энтеральная диабетическая смесь, содержащая метабиотический комплекс и β-глюканы, для лечения питательной недостаточности у больных в критических состояниях | 2024 |
|
RU2832794C1 |
| Способ лечения питательной недостаточности у больных с сепсисом энтеральной смесью, содержащей метабиотический комплекс и β-глюканы | 2024 |
|
RU2828960C1 |
| Способ лечения питательной недостаточности у больных с острым респираторным дистресс-синдромом легкой, средней и тяжелой степени энтеральной смесью, содержащей метабиотический комплекс и β-глюканы | 2024 |
|
RU2834562C1 |
| Способ лечения гестационного сахарного диабета у беременных женщин во втором и третьем триместрах специализированной диетической лечебно-профилактической диабетической смесью Нутризет Д. | 2024 |
|
RU2839803C1 |
| СРЕДСТВО ДЛЯ ВОССТАНОВЛЕНИЯ КИШЕЧНОГО МИКРОБИОЦЕНОЗА ПРИ ДИСБИОЗАХ | 2015 |
|
RU2593584C1 |
| Способ получения кормовой композиции с функциональными свойствами для птицеводства | 2023 |
|
RU2819889C1 |
| Жидкий симбиотик и способ его получения | 2022 |
|
RU2805957C1 |
| СПОСОБ ПРОИЗВОДСТВА КАПСУЛИРОВАННОЙ ФОРМЫ ПРОБИОТИЧЕСКОЙ ПИЩЕВОЙ ДОБАВКИ | 2021 |
|
RU2795965C1 |
| Способ производства сухого кисломолочного продукта | 2022 |
|
RU2801106C1 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ПРОБИОТИЧЕСКИЕ И ПРЕБИОТИЧЕСКИЕ КОМПОНЕНТЫ И НЕОРГАНИЧЕСКИЕ СОЛИ С ЛАКТОФЕРРИНОМ | 2010 |
|
RU2536939C2 |
Изобретение относится к биотехнологии и медицине. Предложен способ лечения дисбиоза кишечника в постоперационном периоде у больных с черепно-мозговой травмой. Способ предусматривает введение метабиотического препарата, содержащего в заданном соотношении компонентов, масс.%: комплекс лизатов штаммов бактерий Bifidobacterium bifidum, Bifidobacterium adolescentis, Bifidobacterium animalis, Bifidobacterium longum, Bifidobacterium breve, Bifidobacterium longum infantis, Lactobacillus acidophilus, Lactobacillus plantarum, Lactobacillus delbrueckii subsp.bulgaricus, Lactobacillus salivarius, Lactobacillus rhamnosus, Lactobacillus helveticus, Streptococcus thermophilus, мальтодекстрин, концентрат для безалкогольного напитка Камбиочай, гуммиарабик и молочную пищевую кислоту. Метабиотический препарат вводят в дозе 0,2 грамма 2 раза в сутки в течение 21 дня. Изобретение обеспечивает эффективное лечение дисбиоза кишечника в постоперационном периоде у больных с черепно-мозговой травмой. 2 ил., 2 табл., 3 пр.
Способ лечения дисбиоза кишечника в постоперационном периоде у больных с черепно-мозговой травмой, в котором вводят метабиотический препарат, отличающийся тем, что метабиотический препарат содержит: комплекс лизатов штаммов бактерий: Streptococcus thermophilus В-2011, Bifidobacterium bifidum АС-1579, Bifidobacterium adolescentis AC-1245, Bifidobacterium animalis AC-1248, Bifidobacterium longum AC-1243, Bifidobacterium breve AC-1570, Bifidobacterium longum infantis AC-1732, Lactobacillus acidophilus B-12024, Lactobacillus acidophilus B-1880, Lactobacillus plantarum B-11007, Lactobacillus plantarum B-11264, Lactobacillus delbrueckii subsp. bulgaricus B-2746, Lactobacillus salivarius B-2214, Lactobacillus salivarius B-2216, Lactobacillus rhamnosus B-8238, Lactobacillus rhamnosus B-6778, Lactobacillus helveticus B-2370, Lactobacillus helveticus B-2371, и питательные субстраты в следующем соотношении, масс.%:
при этом метабиотический препарат вводят в дозе 0,2 грамма 2 раза в сутки в течение 21 дня.
| Милентьева И.С | |||
| и др | |||
| Исследование и разработка пробиотических БАД на основе метаболитов бактерий Bifidobacterium и Lactobacillus | |||
| Новейшие достижения в области медицины, здравоохранения и здоровьесберегающих технологий | |||
| Сборник материалов I Международного конгресса | |||
| Под общей редакцией А.Ю | |||
| Просекова | |||
| Кемерово, 2022, с.286-289 | |||
| WO 2019207316 A1, |
Авторы
Даты
2025-03-11—Публикация
2024-05-16—Подача