Область техники
Группа изобретений относится к области биотехнологии, иммунологии и вирусологии. Созданы тяжелоцепочечные моноклональные антитела, специфически связывающиеся с S белком вируса SARS-CoV-2 и обладающие вируснейтрализующей активностью, нуклеиновая кислота кодирующая тяжелоцепочечное моноклональное антитело и клетка-продуцент, содержащая данную нуклеиновую кислоту. Предложен также способ применения таких антител для терапии заболеваний, вызываемых вирусом SARS-CoV-2.
Уровень техники
31 декабря 2019 года во Всемирную организацию здравоохранения (ВОЗ) поступила информация о вспышке пневмонии неизвестной этиологии в городе Ухань (Китайская Народная Республика). Возбудителем заболевания оказался одноцепочечный РНК-содержащий вирус SARS-CoV-2, относящийся к семейству Coronaviridae, к линии Beta-CoV B.
Коронавирус SARS-CoV-2 может передаваться воздушно-капельным, воздушно-пылевым, контактным, фекально-оральным способами, а также через контаминированные предметы и поверхности (фомиты), через кровь, от матери ребенку и от животных к человеку (Механизмы передачи вируса SARS-CoV-2 и их значение для выбора мер профилактики, Резюме научных исследований, 9 июля 2020 г. ВОЗ). За несколько месяцев вирус распространился по всему миру, и в январе 2020 года ВОЗ объявила эпидемию, связанную с SARS-CoV-2, чрезвычайной ситуацией в области здравоохранения международного значения, а в марте 2020 года охарактеризовала распространение болезни как пандемию.
Заболевание, которое вызывает SARS-CoV-2 получило собственное название COVID-19. Это потенциально тяжелая острая респираторная инфекция, которая может протекать как в легкой, так и в тяжелой форме, и сопровождаться такими осложнениями, как пневмония, острый респираторный дистресс-синдром, острая дыхательная недостаточность, острая сердечная недостаточность, острая почечная недостаточность, септический шок, кардиомиопатии, и др. На начало 2023 года в России было зафиксировано 22 550 395 случаев заражения, из которых 396 974 привели к летальному исходу (Карелина, С. И. Анализ статистических данных за период эпидемии с 2020 г.- по 2023 г. Новой коронавирусной инфекции на территории РФ и ее субъектов по данным средств массовой информации / С. И. Карелина, Я. О. Кашпур, Е. А. Косарева // Universum: медицина и фармакология. - 2023. - Тт. 4-5. - № 98. - С. 42-46.) . В настоящее время фиксируется около 20000 случаев заражения и около 100 летальных случаев ежедневно. Это заболевание представляет серьезную угрозу для здоровья общества (Hu, B. Characteristics of SARS-CoV-2 and COVID-19 / B. Hu, H. Guo, P. Zhou, Z.-L. Shi // Nature Reviews Microbiology. - 2021. - Vol. 19. - № 3. - P. 141-154., Posner, J. Monoclonal Antibodies: Past, Present and Future / J. Posner, P. Barrington, T. Brier, A. Datta-Mannan. - Text: electronic // Concepts and Principles of Pharmacology : Handbook of Experimental Pharmacology / eds. J. E. Barrett [et al.]. - Cham : Springer International Publishing, 2019. - Vol. 260. - P. 81-141. - URL: https://link.springer.com/10.1007/164_2019_323 (date accessed: 20.05.2024).).
Существующие методы терапии COVID-19 разделяют на две крупные группы, которые строятся вокруг различных целей: применение противовирусных препаратов и использование методов, направленных на поддержание организма больного. Противовирусные средства, предназначенные для борьбы с COVID-19, включают многочисленные классы лекарств, такие как ингибиторы полимеразы, протеазы, нуклеозидные и нуклеотидные обратной транскриптазы, а также другие противовирусные препараты. С другой стороны, методы лечения, ориентированные на организм инфицированного человека, включают в себя использование терапии с нейтрализующими антителами, ингибиторы янус-киназы, стероиды и другие медикаменты, направленные на укрепление иммунной системы и смягчение симптомов заболевания (Kim, S. COVID-19 Drug Development / S. Kim // Journal of Microbiology and Biotechnology. - 2022. - Vol. 32. - № 1. - P. 1-5., Yüce, M. COVID-19 diagnosis - A review of current methods / M. Yüce, E. Filiztekin, K. G. Özkaya // Biosensors and Bioelectronics. - 2021. - Vol. 172. - P. 112752.).
Одним из перспективных подходов к терапии коронавирусной инфекции является применение антител против определенных антигенных детерминант вируса. Это обусловлено двумя основными причинами: высокой специфичностью антител и технологичностью их промышленного производства. (В.С. Смирнов, Арег А. Тотолян. Некоторые возможности иммунотерапии при коронавирусной инфекции. Инфекция и иммунитет 2020, Т. 10, № 3, с. 446-458).
В настоящее время в мире получено несколько десятков моноклональных антител специфично связывающих различные эпитопы S белка вируса SARS-CoV-2:
4A8, COV2-2676, 5-7, S2M28, C1717, C1520 - связывающие NTD домен S1 субъединицы S белка.
76E1, COV44-62, COV44-79, VN01H1, VP12E7, C77G12 - связывающие FP домен S2 субъединицы S белка.
CB6, LY-CoV555, S309, CR3022, LY-CoV1404, 2-36- связывающие RBD домен S1 субъединицы S белка.
S2P6, CC40.8, WS6 - связывающие S2 субъединицу S белка.
Перечисленные антитела обладают специфической активностью в отношении вируса SARS-CoV-2 вариантов Альфа, Дельта и Омикрон.
В целом, препараты на основе классических антител имеют ряд недостатков, к которым относятся:
- трудоемкость генно-инженерных манипуляций;
- трудности, связанные с узнаванием некоторых «скрытых» эпитопов;
- необходимость внутривенного введения, что влечет за собой дополнительную
нагрузку на систему здравоохранения;
- дорогостоящее производство антител.
Решением проблемы может стать использование однодоменных антител (наноантител), которые в природе можно найти у представителей семейства верблюдовые. Благодаря относительно небольшому размеру однодоменные антитела обладают благоприятными биофизическими свойствами и дешевле в производстве, чем стандартные моноклональные антитела. Они могут быть получены с использованием прокариотических или эукариотических систем экспрессии. Их небольшой размер, а также длинные, определяющие комплементарность участки тяжелой цепи позволяют им нацеливаться на вогнутые эпитопы. Кроме того, наноантитела можно распылять и доставлять прямо в легкие пациента с Covid-19 с помощью ингалятора, что представляет собой лучшую альтернативу внутривенно вводимым классическим антителам (Ram Sasisekharan. Preparing for the Future - Nanobodies for Covid-19? April 22, 2021 N Engl J Med 2021; 384:1568-1571 DOI: 10.1056/NEJMcibr2101205)
Частным вариантом однодоменных антител являются тяжелоцепочечные антитела, представляющие собой однодоменные антитела, слитые с Fc-фрагментом Ig. Такие тяжелоцепочечные антитела могут обладать более высокой авидностью и улучшенными фармакокинетическими свойствами по сравнению с однодоменными антителами (Voronina DV, Shcheblyakov DV, Favorskaya IA, Esmagambetov IB, Dzharullaeva AS, Tukhvatulin AI, Zubkova OV, Popova O, Kan VY, Bandelyuk AS, Shmarov MM, Logunov DY, Naroditskiy BS, Gintsburg AL. Cross-Reactive Fc-Fused Single-Domain Antibodies to Hemagglutinin Stem Region Protect Mice from Group 1 Influenza a Virus Infection. Viruses. 2022 Nov 10;14(11):2485. doi: 10.3390/v14112485. PMID: 36366583; PMCID: PMC9698552.)
Известно решение (CN 112500480 A, дата публикации 16.03.2021), в котором разработаны варианты однодоменного антитела против вируса SARS-CoV-2, соответствующий вектор экспрессии, а также линия клеток, способная экспрессировать вышеуказанные варианты однодоменного антитела, и способ получения вариантов данного антитела.
Известно решение (CN 111825762 A, дата публикации 27.10.2020), в котором разработано несколько вариантов наноантитела к домену RBD S белка вируса SARS-COV-2, а также способ применения вариантов наноантитела для приготовления лекарственных средств для ингибирования вирусной инфекции SARS-COV-2 и приготовлении реагентов или наборов для тестирования вируса SARS-COV-2.
В патенте CN 112094342 A, дата публикации 18.12.2020, представлено биэпитопное специфическое антитело, происходящее из альпака, или его антигенсвязывающий фрагмент, который связывается с доменом RBD SARS-CoV-2 с высоким сродством, что может использоваться для профилактики, лечения и / или диагностики инфекции SARS-CoV-2.
Известно решение CN 112062839 A, дата публикации 11.12.2020, в котором описано создание наноантитела к S белку SARS-CoV-2, а также способ его использования для приготовления реагента для лечения и / или диагностики инфекции, вызванной коронарирусом SARS-CoV-2.
Также известно решение CN 112062840 A, дата публикации 11.12.2020, предусматривающее разработку наноантитела к S белку SARS-CoV-2 , а также способ его использования для приготовления реагента для лечения и/или диагностики инфекции, вызванной коронарирусом SARS-CoV-2.
В изобретении RU 27934141 C2, дата публикации 11.04.2023, получены однодоменные наноантитела, специфичные к RBD вируса SARS-CoV-2, изучена аффинность полученных антител и их нейтрализующая активность.
Известно изобретение RU 2763001 C1, дата публикации 24.12.2021, где были получены однодоменные антитела и их модификации (в том числе однодоменные антитела, слитые с Fc-фрагментом IgG, то есть тяжелоцепочечные антитела) которые связываются с доменом RBD вируса SARS-CoV-2. Показано, что такие антитела могут быть использованы терапии и экстренной профилактики инфекции, вызванной вирусом SARS-CoV-2.
Данное решение, как наиболее близкое к заявленному, было выбрано авторами патента за прототип. Однако, недостатком прототипа является отсутствие данных по эффективности антител против вновь появляющихся вариантов вируса SARS-CoV-2 - XBB1, XBB 1.5, XBB 1.9, XBB 1.16, XBB2, Eris, Pirola, JN.1.
Таким образом, существует потребность в создании нового антитела, специфически связывающегося с S белком вируса SARS-CoV-2, для терапии и экстренной профилактики заболеваний, вызываемых вирусом SARS-CoV-2, лишенного указанного недостатка.
Раскрытие сущности заявленной группы изобретений
Задачей заявленной группы изобретений является расширение арсенала антител для терапии заболеваний, вызываемых вирусом SARS-CoV-2.
Технический результат группы изобретений заключается в создании тяжелоцепочечного моноклонального антитела, которое эффективно связывает S белок вируса SARS-CoV-2, нейтрализуют вирус SARS-CoV-2 и может быть использовано для терапии заболеваний, вызываемых вирусом SARS-CoV-2. Кроме того, технический результат заключается в том, что разработанное антитело, обладает широким спектром вирус-нейтрализующей активности против различных вариантов вируса SARS-CoV-2.
В первом варианте группы изобретений, указанный технический результат достигается за счет тяжелоцепочечного моноклонального антитела, специфически связывающегося с S-белком вируса SARS-CoV-2, обладающего вируснейтрализующей активностью и имеющее аминокислотную последовательность SEQ ID NO:1, или тяжелоцепочечного моноклонального антитела, специфически связывающегося с S-белком вируса SARS-CoV-2 и имеющего аминокислотную последовательность SEQ ID NO:2.
В частных случаях осуществления, тяжелоцепочечное моноклональное антитело ппредставляет собой однодоменное антитело, имеющее аминокислотную последовательность SEQ ID NO:3, или SEQ ID NO:4, модифицированное Fc-фрагментом IgG человека.
Указанные тяжелоцепочечные моноклональные антитела, также обладают широким спектром вирус-нейтрализующей активности в отношении различных вариантов вируса SARS-CoV-2 - в частности В.1.1.1, B.1.617.2 (Delta), XBB1, XBB 1.5, XBB 1.9, XBB 1.16, Eris, Pirola, JN.1.
Во втором варианте группы изобретений, технический результат достигается за счет нуклеиновой кислоты, имеющей нуклеотидную последовательность, кодирующую тяжелоцепочечное моноклональное антитело по первому варианту.
Кроме того, по третьему варианту группы изобретений, создана клетка-продуцент, содержащая нуклеиновую кислоту, имеющую нуклеотидную последовательность любого из указанных выше антител, и экспрессирующая данное антитело.
Также по четвертому варианту группы изобретений разработан способ терапии заболевания, вызываемого вирусом SARS-CoV-2 в его различных вариантах, заключающийся во введении в организм млекопитающих любого из указанных выше антител в эффективном количестве.
Краткое описание чертежей
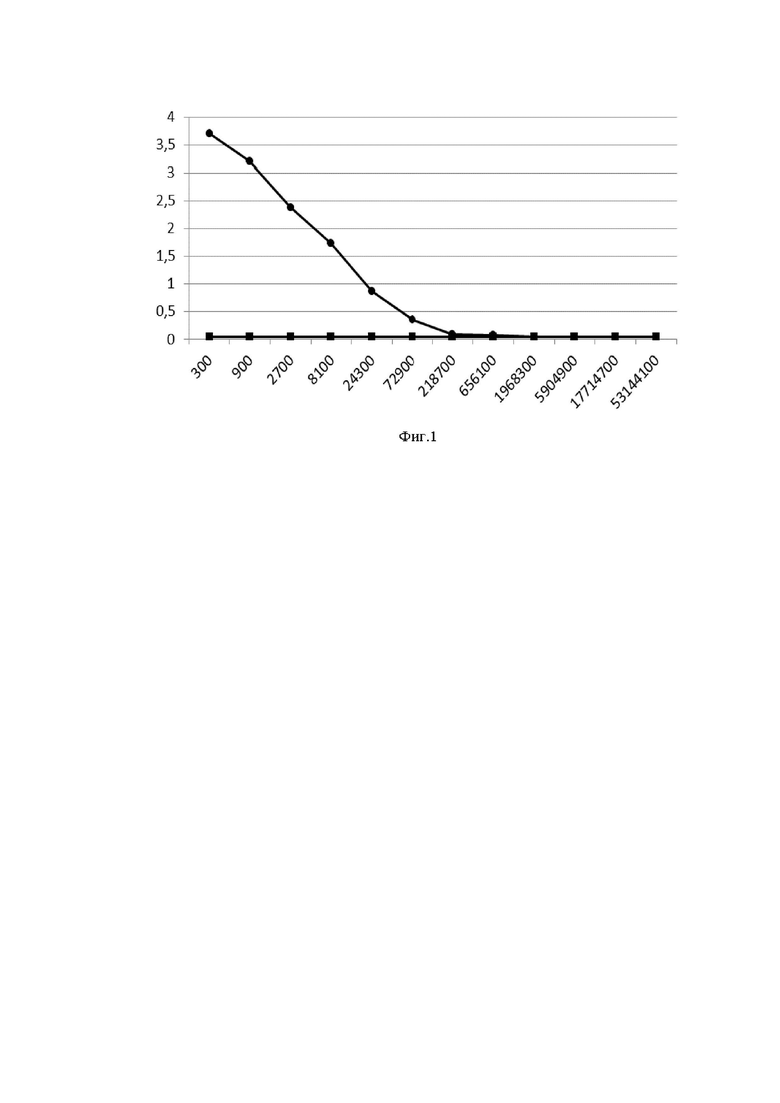
На фиг. 1 представлены данные по определению титра специфических антител к S-белку в сыворотке крови верблюда после полного цикла иммунизации.
Ось ординат - оптическая плотность раствора при длине волны 450 нм;
Ось абсцисс - разведения сыворотки крови верблюда.
 - Уровень специфического сигнала сыворотки верблюда на рекомбинантный S-белок вируса SARS-CoV-2 варианта Омикрон ХВВ.1:
- Уровень специфического сигнала сыворотки верблюда на рекомбинантный S-белок вируса SARS-CoV-2 варианта Омикрон ХВВ.1:
 - Уровень сигнала сыворотки верблюда на BSA (отрицательный контроль).
- Уровень сигнала сыворотки верблюда на BSA (отрицательный контроль).
На фиг. 2 представлена электрофореграмма анализа результатов очистки однодоменных антител аффинной хроматографией, где
М - маркер молекулярного веса;
1-7 - образцы однодоменных антител.
На фиг. 3 представлено схематическое изображение аминокислотной последовательности однодоменных антител, где
1 - N-конец;
2 - последовательность однодоменного антитела;
3 - His-tag (гистидиновая метка);
4 - C-конец.
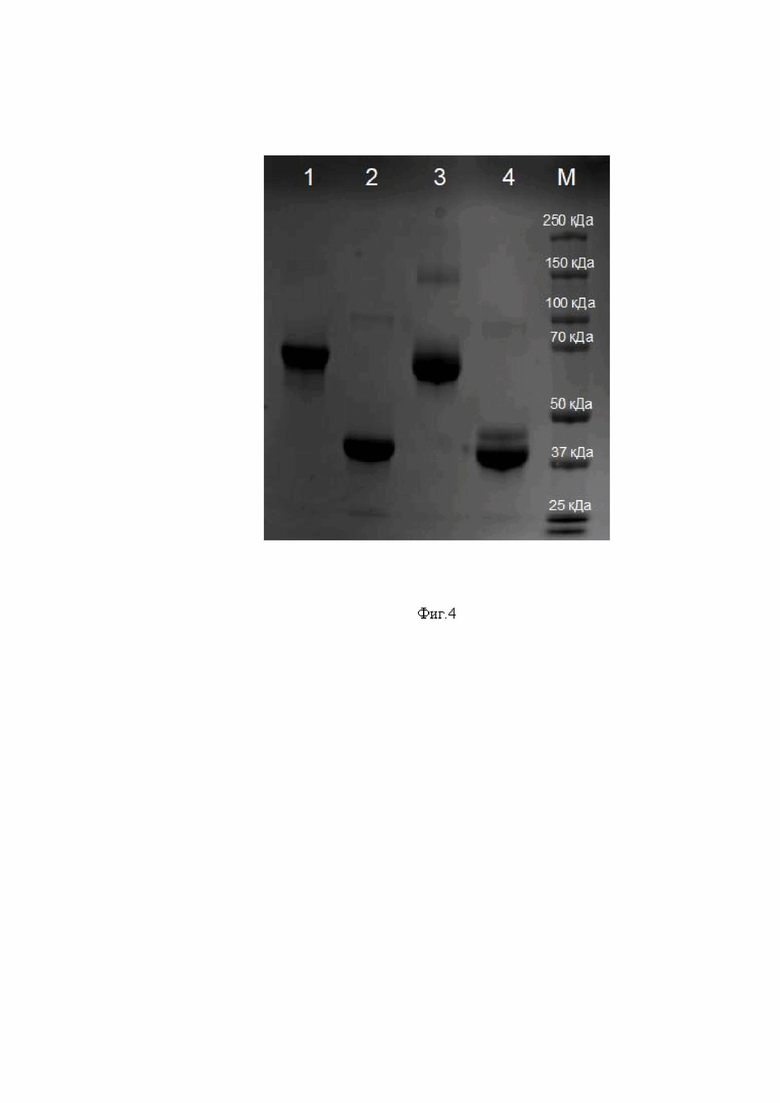
На фиг. 4 представлена электрофореграмма анализа результатов очистки тяжелоцепочечных моноклональных антител B5-Fc и B10-Fc аффинной хроматографией, где
М - маркер молекулярного веса;
1 - образец тяжелоцепочечного моноклонального антитела B5-Fc в не восстанавливающих условиях;
2 - образец тяжелоцепочечного моноклонального антитела B5-Fc в восстанавливающих условиях;
3 - образец тяжелоцепочечного моноклонального антитела B10-Fc в не восстанавливающих условиях;
4 - образец тяжелоцепочечного моноклонального антитела B10-Fc в восстанавливающих условиях;
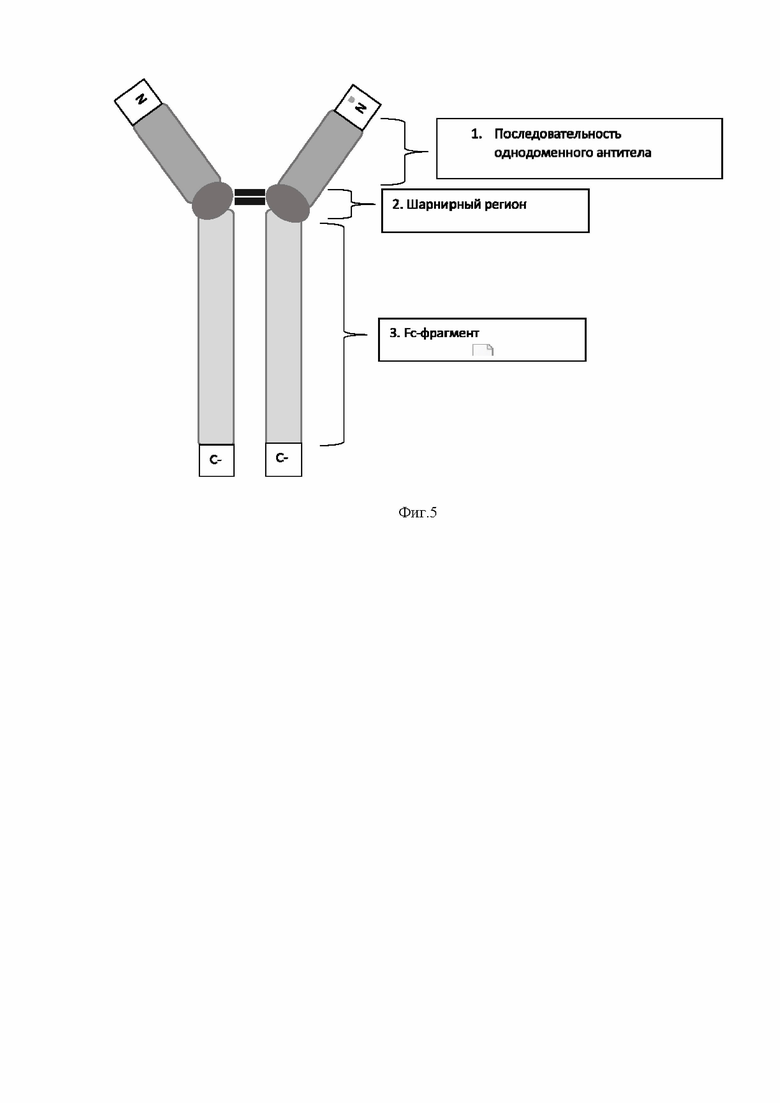
На фиг. 5 представлено схематическое изображение аминокислотной последовательности тяжелоцепочечного моноклонального антитела,
1 - последовательность однодоменного антитела В5 или В10;
2 - шарнирный регион;
3 - Fc-фрагмент IgG1 человека.
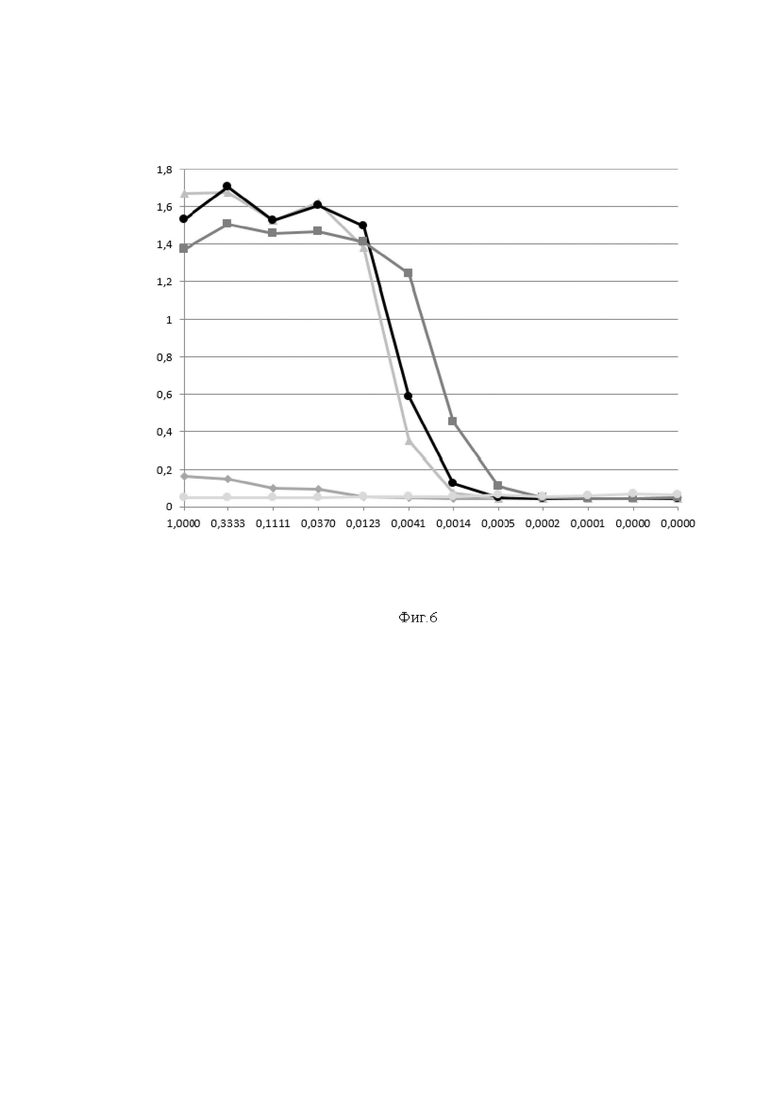
На фиг. 6 представлены результаты анализа специфической активности тяжелоцепочечного моноклонального антитела B5-Fc отношении S-белка различных вариантов вируса SARS-CoV-2.
Ось ординат - оптическая плотность раствора при длине волны 450 нм:
Ось абсцисс - концентрация антитела B5-Fc, нг/мл.
 - Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта В.1.1.1;
- Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта В.1.1.1;
 - Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта Дельта;
- Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта Дельта;
 - Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта Омикрон ВА.1;
- Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта Омикрон ВА.1;
 - Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта Омикрон ХВВ.1;
- Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта Омикрон ХВВ.1;
 - Уровень сигнала антитела на BSA (отрицательный контроль).
- Уровень сигнала антитела на BSA (отрицательный контроль).
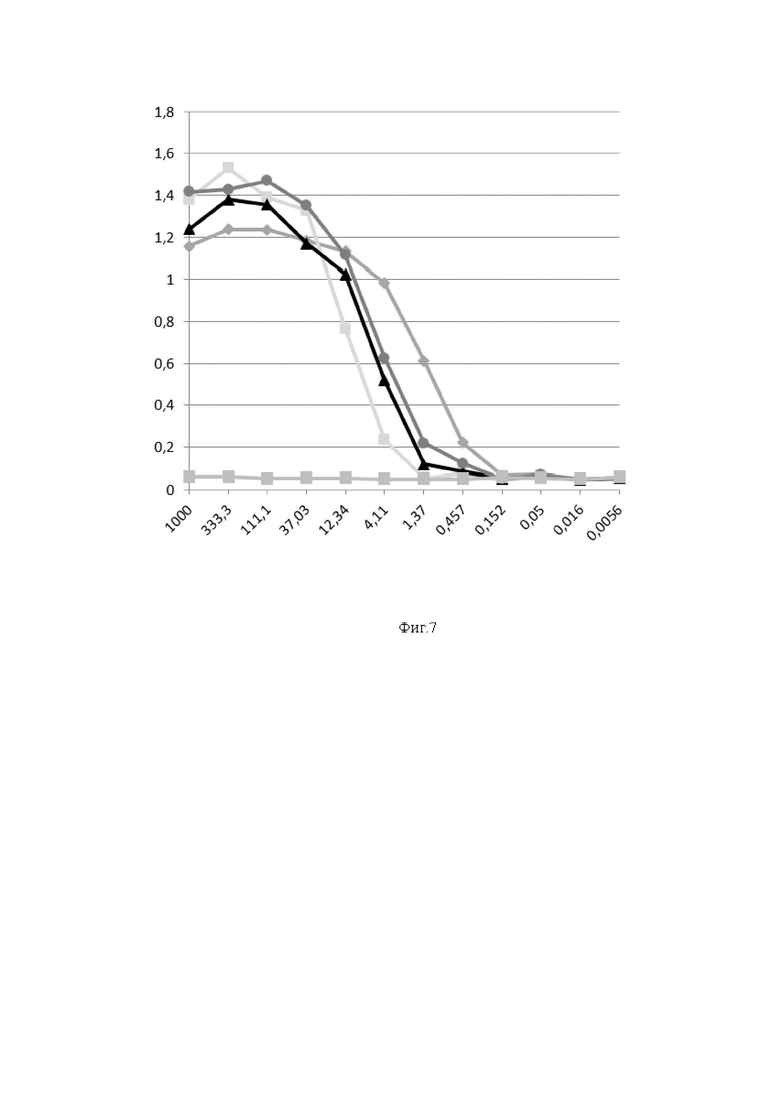
На фиг. 7 представлены результаты анализа специфической активности тяжелоцепочечного моноклонального антитела B10-Fc отношении S-белка различных вариантов вируса SARS-CoV-2.
Ось ординат - оптическая плотность раствора при длине волны 450 нм;
Ось абсцисс - концентрация антитела B10-Fc, нг/мл.
 - Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта В.1.1.1;
- Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта В.1.1.1;
 - Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта Дельта;
- Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта Дельта;
 - Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта Омикрон ВА.1;
- Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта Омикрон ВА.1;
 - Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта Омикрон ХВВ.1;
- Уровень специфического антитела сигнала на рекомбинантный S-белок вируса SARS-CoV-2 варианта Омикрон ХВВ.1;
 - Уровень сигнала антитела на BSA (отрицательный контроль).
- Уровень сигнала антитела на BSA (отрицательный контроль).
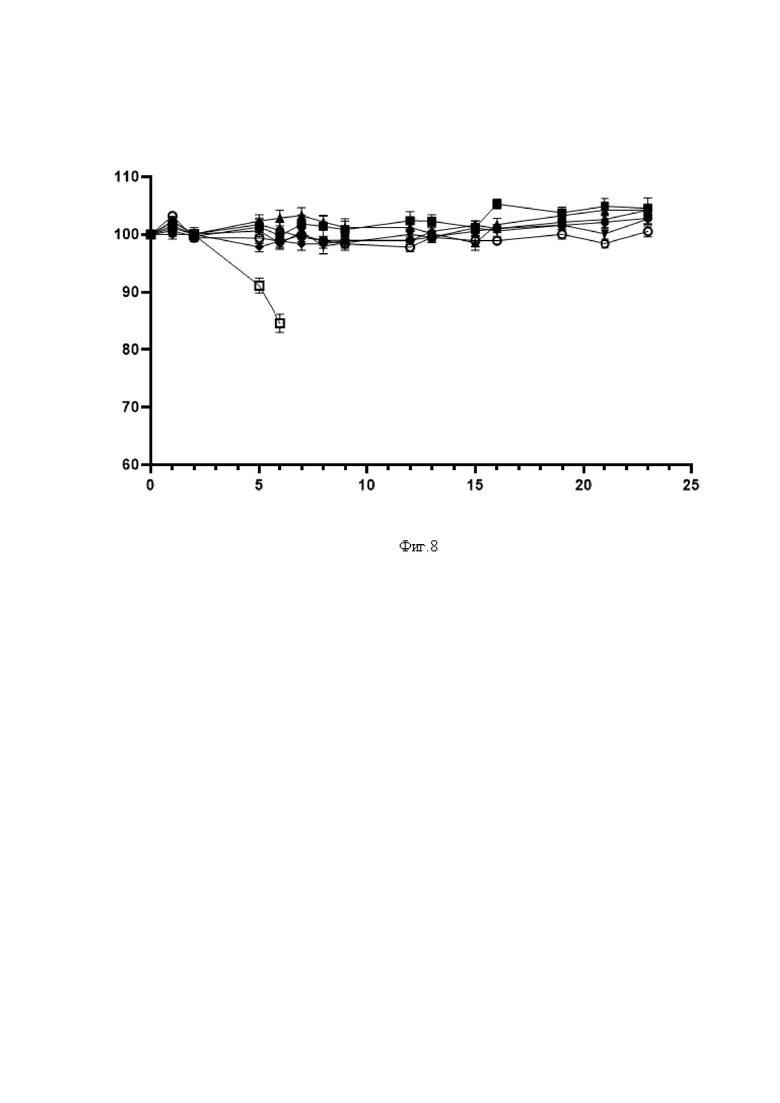
На фиг. 8 представлены результаты анализа изменения веса животных, которым вводили созданные тяжелоцепочечные моноклональные антитела, и животных из группы плацебо в течение 23 суток после заражения SARS-CoV-2. В каждой временной точке для каждой группы животных вес представлен в виде арифметического среднего.
Ось ординат - изменение веса животных от начального, %;
Ось абсцисс - время после заражения животных вирусом SARS-CoV-2, дни.
 животные, которые получили антитело B5-Fc (1 мг/кг), через 1 час после заражения SARS-CoV-2;
животные, которые получили антитело B5-Fc (1 мг/кг), через 1 час после заражения SARS-CoV-2;
 животные, которые получили антитело B5-Fc (1 мг/кг), через 6 часов после заражения SARS-CoV-2;
животные, которые получили антитело B5-Fc (1 мг/кг), через 6 часов после заражения SARS-CoV-2;
 животные, которые получили антитело B5-Fc (1 мг/кг), через 24 часа после заражения SARS-CoV-2;
животные, которые получили антитело B5-Fc (1 мг/кг), через 24 часа после заражения SARS-CoV-2;
 животные, которые получили антитело B10-Fc (1 мг/кг), через 1 час после заражения SARS-CoV-2;
животные, которые получили антитело B10-Fc (1 мг/кг), через 1 час после заражения SARS-CoV-2;
 животные, которые получили антитело B10-Fc (1 мг/кг), через 6 часов после заражения SARS-CoV-2;
животные, которые получили антитело B10-Fc (1 мг/кг), через 6 часов после заражения SARS-CoV-2;
 животные, которые получили антитело B10-Fc (1 мг/кг), через 24 часа после заражения SARS-CoV-2;
животные, которые получили антитело B10-Fc (1 мг/кг), через 24 часа после заражения SARS-CoV-2;
 - группа плацебо.
- группа плацебо.
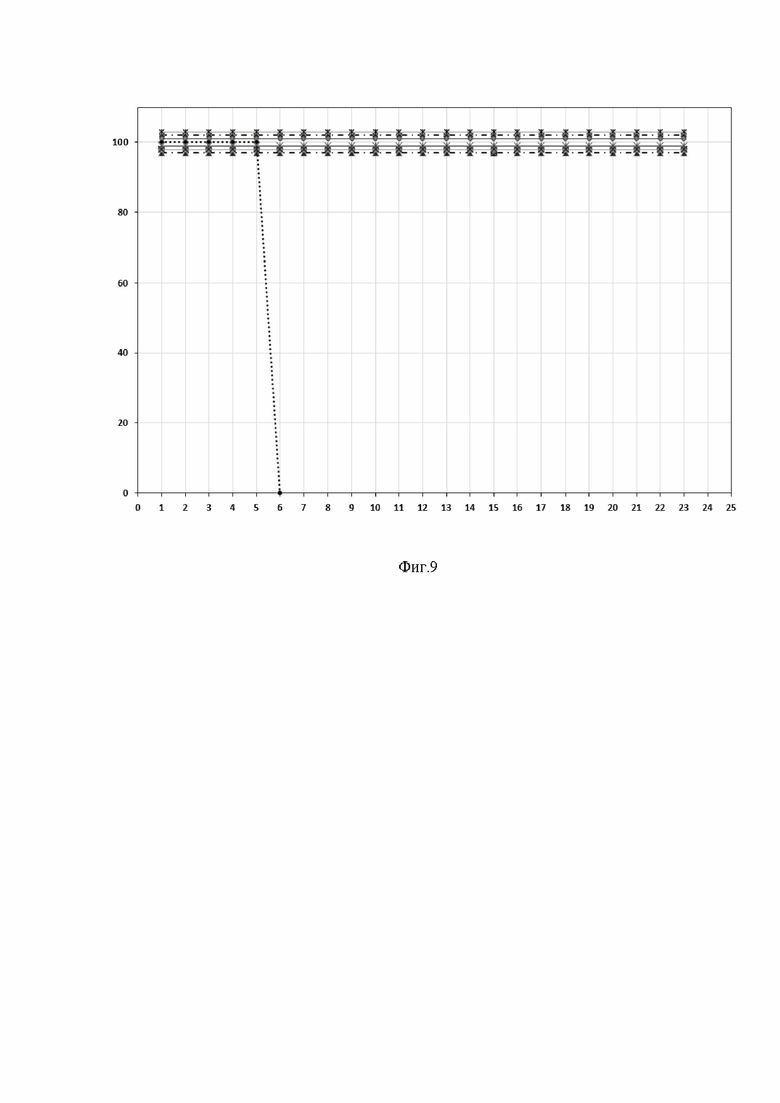
На фиг. 9 представлены результаты выживаемости животных, которым вводили созданные тяжелоцепочечные моноклональные антитела, и животных из группы плацебо в течение 23 суток после заражения SARS-CoV-2.
Ось ординат - выживаемость, %;
Ось абсцисс - время после заражения животных вирусом SARS-CoV-2, дни.
 - животные, которые получили антитело B5-Fc (1 мг/кг), через 1 час после заражения SARS-CoV-2;
- животные, которые получили антитело B5-Fc (1 мг/кг), через 1 час после заражения SARS-CoV-2;
 - животные, которые получили антитело B5-Fc (1 мг/кг), через 6 часов после заражения SARS-CoV-2;
- животные, которые получили антитело B5-Fc (1 мг/кг), через 6 часов после заражения SARS-CoV-2;
 - животные, которые получили антитело B5-Fc (1 мг/кг), через 24 часа после заражения SARS-CoV-2;
- животные, которые получили антитело B5-Fc (1 мг/кг), через 24 часа после заражения SARS-CoV-2;
 - животные, которые получили антитело B10-Fc (1 мг/кг), через 1 час после заражения SARS-CoV-2;
- животные, которые получили антитело B10-Fc (1 мг/кг), через 1 час после заражения SARS-CoV-2;
 - животные, которые получили антитело B10-Fc (1 мг/кг), через 6 часов после заражения SARS-CoV-2;
- животные, которые получили антитело B10-Fc (1 мг/кг), через 6 часов после заражения SARS-CoV-2;
 - животные, которые получили антитело B10-Fc (1 мг/кг), через 24 часа после заражения SARS-CoV-2;
- животные, которые получили антитело B10-Fc (1 мг/кг), через 24 часа после заражения SARS-CoV-2;
 - группа плацебо.
- группа плацебо.
Осуществление группы изобретений
В первой варианте изобретения раскрывается тяжелоцепочечное моноклональное антитело, специфически связывающееся с S белком вируса SARS-CoV-2, обладающее вируснейтрализующей активностью и имеющее аминокислотную последовательность SEQ ID NO:1 или SEQ ID NO:2.
Для получения данного антитела осуществляли цикл иммунизации двугорбого верблюда рекомбинантными аденовирусами человека 26 и 5 серотипов, экспрессирующих гены S белка вируса SARS-CoV-2 варианта омикрон ВА1 и ВА2, инактивированным вирусом SARS-CoV-2 варианта омикрон ВА5, а также рекомбинантным белком S вируса SARS-CoV-2 варианта омикрон ХВВ1, полученным в клеточной линии СНО и очищенным металл-аффинной и эксклюзионной хроматографией. Эффективность иммунизации подтверждали оценкой титра специфических к S белку вируса SARS-CoV-2 антител в сыворотке крови животного, а также изучением титра вирус-нейтрализующей активности сыворотки крови иммунизированного животного в отношении различных вариантов вируса SARS-CoV-2. Далее, у животных выделяли мононуклеарные клетки периферической крови, из которых получали РНК. На основе РНК синтезировали кДНК. На матрице полученной кДНК ставили гнездовую ПЦР, позволяющую амплифицировать последовательности однодоменных антител. Таким образом была получена библиотека ампликонов последовательностей однодоменных антител.
Специалистам в данной области известно, что в целях осуществления настоящего изобретения, возможно использование не только мононуклеарных клеток, а также цельной крови, лимфатических узлов, селезенки, тимуса или других клеток и органов иммунизированного животного, экспрессирующих однодоменные антитела. Также специалистам в данной области известно, что в целях осуществления настоящего изобретения возможно использование синтетических библиотек последовательностей однодоменных антител.
Селекцию антител проводили методом фагового дисплея с использованием паннинга на антигене (S белок вируса SARS-CoV-2). Специалистам в данной области известно, что в целях осуществления настоящего изобретения, возможно использование других подходов селекции, таких как паннинг на вирусных частицах, паннинг в растворе биотинилированного антигена, паннинг с использованием конкурентного связывания и элюции. Также специалистам в данной области известно, что в целях осуществления настоящего изобретения возможно использование других методов селекции, таких как рибосомный дисплей, дрожжевой дисплей. В результате селекции были отобраны однодоменные антитела, нейтрализующие различные варианты вируса SARS-CoV-2, имеющие аминокислотную последовательность SEQ ID NO:3 и SEQ ID NO:4.
Специалистам в данной области известно, что в целях осуществления настоящего изобретения последовательности однодоменных антител, специфических S белку вируса SARS-CoV-2, могут содержать в себе аминокислотные замены, которые не сказываются на вторичной и третичной структуре однодоменных антител и не влияют на их способность связывать и нейтрализовать вирус SARS-CoV-2. Более того, поскольку в связывании с антигеном участвуют только антигенсвязывающие петли (CDR домены) однодоменных антител, то, как известно специалистам в данной области, любой иммуноглобулин или его аналог, содержащий такие же аминокислотные последовательности CDR доменов, попадает под объем настоящего изобретения. Более того, последовательности CDR доменов могут содержать замены/делеции/вставки аминокислот, которые при парном выравнивании аминокислотных последовательностей обеспечивают гомологичность не менее 70% и не оказывают качественного влияния на способность связываться с антигеном. Таким образом, под объем настоящего изобретения попадают все иммуноглобулины или их аналоги, содержащие последовательности CDR доменов, гомология которых составляет не менее 70% с предлагаемыми последовательностями.
Специалистам в данной области известно, что в целях осуществления настоящего изобретения последовательности однодоменных антител, специфических к S белку вируса SARS-CoV-2, могут быть модифицированы путем присоединения различных белков, белковых доменов и тэгов, таких, например, как НА-тэг, Flag-тэг, GST-тэг, GFP белок, RFP белок, биотин и другие.
Нуклеотидную последовательность однодоменных антител определяли методом секвенирования. Специалистам в данной области известно, что в целях осуществления настоящего изобретения нуклеотидные последовательности, кодирующие однодоменные антитела, могут отличаться, основываясь на принципе вырожденности генетического кода. Таким образом, под объем настоящего изобретения попадают все последовательности нуклеотидов, кодирующие аминокислотные последовательности однодоменных антител SEQ ID NO:3, SEQ ID NO:4. Например, нуклеотидные последовательности SEQ ID NO:1, SEQ ID NO:2.
Нуклеотидные последовательности тяжелоцепочечных моноклональных антител (SEQ ID NO:1 и SEQ ID NO:2) были созданы генно-инженерным путем на основе нуклеотидной последовательности однодоменных антител (SEQ ID NO:7 и SEQ ID NO:8) и нуклеотидной последовательности Fc-фрагмента иммуноглобуллина G1 человека. Специалистам в данной области известно, что в целях осуществления настоящего изобретения нуклеотидные последовательности, кодирующие тяжелоцепочечные моноклональные антитела, могут отличаться, основываясь на принципе вырожденности генетического кода. Таким образом, под объем настоящего изобретения попадают все последовательности нуклеотидов, кодирующие аминокислотные последовательности тяжелоцепочечных моноклональных антител (SEQ ID NO:1 и SEQ ID NO:2). Например, нуклеотидные последовательности SEQ ID NO:5 и SEQ ID NO:6.
С помощью методов генной инженерии была получена клетка-продуцент, содержащая нуклеотидную последовательность тяжелоцепочечных моноклональных антител и экспрессирующая тяжелоцепочечных моноклональных антител SEQ ID NO:1, или SEQ ID NO:2. Таким образом, например, были получены: клетка-продуцент на основе клеточной линии СНО, экспрессирующая тяжелоцепочечное моноклональное антитело SEQ ID NO:1; клетка-продуцент на основе клеточной линии СНО, экспрессирующая тяжелоцепочечное моноклональное антитело SEQ ID NO:2. Специалистам в данной области известно, что в целях осуществления настоящего изобретения в качестве продуцента можно использовать другие эукариотические системы экспрессии. При необходимости способ получения дополнительно включает в себя выделение и очистку любым способом, известным в данной области.
Таким образом, авторами патента были получены варианты тяжелоцепочечных моноклональных антител, специфически связывающихся с S белком вируса SARS-CoV-2, обладающее вируснейтрализующей активностью в отношении различных вариантов вируса SARS-CoV-2. Также были получены: нуклеиновая кислота, имеющая нуклеотидную последовательность, кодирующую соответствующее тяжелоцепочечное моноклональное антитело и клетка-продуцент, содержащая данную нуклеиновую кислоту и экспрессирующая соответствующее антитело.
Кроме того, авторами патента разработан способ терапии заболеваний, вызываемых вирусом SARS-CoV-2, заключающийся во введении в организм млекопитающих в эффективном количестве любого из разработанных вариантов антител. Результаты терапии приведены ниже.
Осуществление изобретения подтверждается следующими примерами.
Пример 1.
Получение иммунной библиотеки кДНК однодоменных антител верблюда.
На первом этапе работы была разработана схема иммунизации верблюда различными антигенами для получения иммунной библиотеки однодоменных антител, обладающих широким спектром нейтрализующей активности в отношении различных вариантов вируса SARS-CoV-2. Было проведено 2 цикла иммунизации. Схема иммунизации верблюда в представлена в таблице 1.
Таблица 1. Схема иммунизации верблюда для получения иммунной библиотеки однодоменных антител.
Интервал между введениями антигена составлял 14 дней, а интервал между циклами иммунизации составлял 1 месяц. Эффективность иммунизации верблюда подтверждали при помощи определения титра антител специфичных к S-белку вируса SARS-CoV-2 в сыворотке крови при помощи реакции непрямого ИФА. В качестве антигена на поверхность планшета сорбировали антиген - рекомбинантный белок ECD-S-XBB, использованный ддля иммунизации. Результаты непрямого ИФА представлены на фигуре 1. В результате титр специфических антител к S-белку вируса SARS-CoV-2 варианта Омикрон XBB.1 в крови верблюда после цикла иммунизации составил 1 на 72900, что говорит о выраженном гуморальном иммунном ответе у верблюда после проведенного цикла иммунизации.
Через 7 дней после последней иммунизации у верблюда отбирали 50,0 мл периферической крови и выделяли мононуклеарные клетки на градиенте фиколла 1,077 (Панэко, Россия). Изолированные мононуклеарные клетки использовали для выделения тотальной РНК реагентом Trizol (Invitrogene, США) согласно протоколу фирмы-производителя. Выделенную РНК использовали в качестве матрицы для синтеза кДНК со случайными праймерами и ревертазой SuperScriptIII (Invitrogene, США). На матрице, полученной кДНК, ставили гнездовую ПЦР, позволяющую амплифицировать последовательности однодоменных антител. Для этой процедуры использовали высокоточную полимеразу Q5 (NEB, Великобритания) и специфические праймеры, содержащие на концах сайты рестрикции.
Таким образом, в результате проведенной работы были получены ампликоны, которые являются иммунной библиотекой кДНК однодоменных антител верблюда.
Пример 2. Получение, продукция и очистка однодоменных антител
Ампликоны, полученные в примере 1 гидролизовали рестриктазами и клонировали в фагмидный вектор, гидролизованный по тем же сайтам. Затем трансформировали клетки E.coli (штамм TG1) фагмидными векторами, полученными в результате клонирования.
Суспензию бактериальных клонов-трансформантов клеток E.coli (штамм TG1) использовали для продукции рекомбинантных бактериофагов с использованием бактериофага-помощника M13KO7 (NEB, Великобритания) согласно протоколу фирмы-производителя. Рекомбинантные бактериофаги осаждали путем преципитации полиэтиленгликолем (PEG/NaCl). Таким образом, получена библиотека рекомбинантных бактерифагов с титром 1012 трансдуцирующих единиц/мл суспензии.
Селекцию специфических рекомбинантных бактериофагов осуществляли путем паннинга на антигене исходной библиотеки бактериофагов. Для этого рекомбинантный белок ECD-S-XBB (использованный для иммунизации верблюда в примере 1) иммобилизовали в лунке иммунологического планшета в 50,0 мМ карбонатно-бикарбонатном буфере в течение ночи. Не связавшийся белок удаляли, а лунку блокировали 5% раствором сухого молока в фосфатном буфере в течение 1 часа при комнатной температуре. Затем добавляли суспензию 1011 рекомбинантных бактерифагов и инкубировали 1 час при комнатной температуре. Не связавшиеся бактерифаги отмывали коллоидным 0,1% раствором детергента Твин-20 в фосфатном буфере. Связавшиеся бактериофаги элюировали при помощи раствора трипсина (0,1 мг/мл). Элюированные бактериофаги использовали для трансдукции клеток E.coli TG1, которые затем высевали на агаризованные чашки в разведении, позволяющем изолировать индивидуальные колонии. Полученные колонии использовали для наращивания бактериальной массы и выделения плазмидной ДНК. Плазмиды секвенировали для определения нуклеотидных последовательностей, кодирующих однодоменные антитела. Было определено 15 индивидуальных последовательностей.
Для продукции однодоменных антител к интенсивно делящимся клеткам E.coli TG1, полученных из колоний на предыдущем этапе, добавляли 1,0 мкМ изопропил тиогалактопиранозид (IPTG) (Хеликон, Россия), спустя 4 часа бактериальную массу использовали для выделения рекомбинантных белков на колонке HisTrap FF 5 мл («GE Healthcare Life Sciences», США) с использованием хроматографической системы AKTA start («GE Healthcare Life Sciences», США), согласно протоколу фирмы-производителя. Результаты хроматографической очистки однодоменных антител представлены на фигуре 2. Данный пример демонстрирует простоту и эффективность продукции и очистки однодоменных антител в бактериальной системе экспрессии. Таким образом были получены очищенные препараты однодоменных антител. Одинаковые результаты были получены для всех 15 однодоменных антител. Схематичное изображение аминокислотных последовательностей однодоменных антител представлено на фигуре 3.
Пример 3. Определение вируснейтрализующей активности однодоменных антител.
Целью данной работы являлась оценка способности полученных однодоменных антител нейтрализовать вирус SARS-CoV-2 (Омикрон ХВВ.1 - hCoV-19/Russia/SPE-RII-4422S/2022). Реакцию нейтрализации вируса SARS-CoV-2 ставили в варианте постоянная доза вируса - разведения образца однодоменных антител. Готовили образцы однодоменных антител в культуральной среде ДМЕМ с 2% инактивированной фетальной бычьей сывороткой, далее смешивали со 100 БОЕ вируса SARS-CoV-2, инкубировали 1 час при 37°С и добавляли к клеткам Vero E6. Исходные концентрации препаратов однодоменных антител составляла 0,5-1 мг/мл. Конечные разведения однодоменных антител составили 1/20-1/1280. Клетки инкубировали при 37°С в 5% СО2. Через 96 часов производили учет развития цитопатического действия вируса на культуру клеток визуально по оценке нарушения монослоя клеток. За вируснейтрализующий титр однодоменных антител принимали высшее их разведение, при котором происходит подавление цитопатического действия в 2-х лунках из 3-х.
Данные по вируснейтрализующей активности выбранных антител представлены в таблице 2.
Таблица 2. Вируснейтрализующая активность полученных однодоменных антител.
Как видно из представленных данных 2 образца обладали наиболее выраженной вируснейтрализующей активностью (рабочая концентрация менее 0,02 мкг/мл). Два образца однодоменных антител (В5 и В10), обладающих наиболее выраженной вируснейтрализующей активностью, были выбраны для дальнейших исследований.
Таким образом, в результате проведенной работы было получено два однодоменных антитела (SEQ ID NO:3 и SEQ ID NO:4), обладающих высокой вируснейтрализующей активностью.
Пример 4. Получение, продукция и очистка тяжелоцепочечных моноклональных антител.
Тяжелоцепочечные моноклональные антитела представляют собой однодоменные антитела, модифицированные Fc-фрагментом иммуноглобуллина человека - B5-Fc и B10-Fc, соответственно.
Данная модификация однодоменных антител позволит улучшить их фармакокинетические свойства за счет добавления Fc-фрагмента IgG1 человека и его правильного гликозилирования в эукариотических клетках-продуцентах. Кроме того, модификация Fc-фрагментом позволит антителам активировать систему комплимента и связываться с Fc-рецепторами на поверхности иммунокомпитентных клеток. Кроме того, за счет димеризации паратопов однодоменных антител Fc-фрагментом потенциально можно повысить авидность антитела.
На первом этапе работы разработали дизайн аминокислотной последовательности тяжелоцепочечных моноклональных антител B5-Fc и B10-Fc (SEQ ID NO:1, или SEQ ID NO:2), которые представляют собой однодоменные антитела B5 и B10 (SEQ ID NO:3, или SEQ ID NO:4), модифицированное Fc-фрагментом иммуноглобулина G1 человека. На основе аминокислотной последовательности были получены нуклеотидные последовательности тяжелоцепочечных моноклональных антител, которые были синтезированы в компании ЗАО «Евроген». Полученные нуклеотидные последовательности клонировали в вектор (плазмидная ДНК) для экспрессии в эукариотических клетках. Далее проводили трансфекцию клеток линии СНО полученными экспрессионными векторами с использованием системы - реагент PEI 25 kDa (Polyscience, США) и питательная среда BalanCD Transfectory CHO (FujiFILM Irvine scientific, США). Соотношение PEI:ДНК (экспрессионный вектор) использовали 5:1. Клетки культивировали в колбах Эрленмейера в течение 10 дней. После чего культуральную жидкость осветляли центрифугированием при 5000g. Антитело очищали аффинной хроматографией на системе AKTA PURE (Cytiva, США), используя колонки MAbSelect SuRe 1 мл (Cytiva, Швеция) в соответствии с протоколом производителя. Дополнительную очистку и замену буфера проводили на колонке ХК 26/100 (Cytiva, Швеция), упакованной сорбентом Superdex 200 pg (Cytiva, Швеция). Чистоту полученных препаратов B5-Fc и B10-Fc, определяли методом вертикального электрофореза в полиакриламидном геле в восстанавливающих и не восстанавливающих условиях (фиг. 4). В результате вертикального электрофореза была продемонстрирована высокая чистота полученных препаратов и их подлинность. Молекулярные массы полос тяжелоцепочечных моноклональных антител на геле соответствовали теоретическим (около 40 кДа в восстанавливающих условиях и около 70-80 кДа в не восстанавливающих). Схематичное изображение аминокислотной последовательности тяжелоцепочечных моноклональных антител представлено на фигуре. 5. Специфическая активность полученных препаратов B5-Fc и B10-Fc была подтверждена методом непрямого ИФА. В качестве антигенов на планшет сорбировали очищенный S-белок вируса SARS-CoV-2 различных штаммов - варианта В1.1.1, варианта Дельта, варианта ВА.1 и варианта ХВВ.1. Определяли специфический титр антител к каждому из антигенов в отдельности. Для анализа использовали 12 трехкратных разведений антител от 1 мкг/мл до 5,6 пг/мл. в качестве конъюгата использовали коммерческие антитела, меченные пероксидазой, 933NA (Cytiva, США). Результаты специфической активности тяжелоцепочечного моноклонального антитела B5-Fc в отношении различных антигенов, представлены на фигуре 6. Результаты специфической активности тяжелоцепочечного моноклонального антитела B10-Fc в отношении различных антигенов, представлены на фигуре 7. В результате было показано, что оба полученных тяжелоцепочечных моноклональных антитела обладают выраженной специфической активностью в отношении S-белка различных вариантов вируса SARS-CoV-2 в концентрации несколько нг/мл.
Таким образом, в результате проведенной работы были получены тяжелоцепочечные моноклональные антитела, представляющее собой однодоменные антитела, модифицированное Fc-фрагментом иммуноглобулина G1 человека, имеющее конечную аминокислотную последовательность SEQ ID NO:1, или SEQ ID NO:2.
Пример 5. Определение вируснейтрализующей активности тяжелоцепочечных моноклональных антител в отношении различных вариантов вируса SARS-CoV-2.
Целью данного эксперимента являлась оценка способности разработанных тяжелоцепочечных моноклональных антител нейтрализовать вирус SARS-CoV-2 различных вариантов, в том числе вариантов, вызывающих опасение (VOC), а также сравнить вирус-нейтрализующую активность тяжелоцепочечных моноклональных антител B5-Fc и B10-Fc с соответствующими однодоменными антителами B5 и B10. На первом этапе работы подготовили образцы антител B5-Fc и B10-Fc (SEQ ID NO:1, или SEQ ID NO:2), а также B5 и B10 (SEQ ID NO:3, или SEQ ID NO:4) в культуральной среде ДМЕМ с 2% инактивированной фетальной бычьей сывороткой. Затем полученные образцы антител смешивали со 100 БОЕ вируса SARS-CoV-2 (различных вариантов), инкубировали 1 час при 37°С и добавляли к клеткам Vero E6. Клетки инкубировали при 37°С в 5% СО2. Через 96 часов производили учет развития цитопатического действия вируса на культуру клеток визуально по оценке нарушения монослоя клеток. За вируснейтрализующий титр антител принимали высшее их разведение, при котором происходит подавление цитопатического действия в 2-х лунках из 3-х. В результате были определены следующие рабочие вируснейтрализующие концентрации антител, представленные в таблице 3.
Таблица 3. Вирус-нейтрализующая активность тяжелоцепочечных моноклональных антител B5-Fc и B10-Fc, а также однодоменных антител B5 и B10, против различных вариантов вируса SARS-CoV-2.
Как видно из представленных данных, полученные тяжелоцепочечные моноклональные антитела B5-Fc и B10-Fc, как и исходные однодоменные антитела B5 и B10 обладают вируснейтрализующей активностью в отношении широкого спектра различных штаммов вируса SARS-CoV-2, в том числе вариантов, вызывающих опасение.
Пример 6. Разработка способа терапии заболевания, вызванного вирусом SARS-CoV-2.
Терапевтическую эффективность препаратов тяжелоцепочечных моноклональных антител B5-Fc (SEQ ID NO:1) и B10-Fc (SEQ ID NO:2) оценивали на модели инфекции, вызванной вирусом SARS-CoV-2, у АСЕ2-трансгенных мышей. Данные животные были выбраны, так как они высоко чувствительны к инфекции SARS-CoV-2. Летальность животных после заражения вирусом SARS-CoV-2 составляет 100%.
В работе использовали вирус SARS-CoV-2 (hCoV-19/Russia/Moscow_PMVL-1/2020), изолированный в 2020 году в ФГБУ «НИЦЭМ им. Н.Ф.Гамалеи» Минздрава России, хранящийся в Государственной коллекции вирусов. Инфекционный титр вируса 107 TCID50/мл. Животных заражали вирусом SARS-CoV-2 интраназально в дозе 2*105 TCID50 на животное, далее вводили препарат тяжелоцепочечных моноклональных антител или плацебо, согласно таблице 4.
Таблица 4. Дизайн экспериментального изучения эффективности тяжелоцепочечных моноклональных антител B5-Fc и B10-Fc.
В течение 23 суток после заражения оценивали вес и выживаемость животных.
На фиг. 8 представлены данные динамики веса животных после заражения. На фиг. 9 представлены данные выживаемости животных после заражения. По результатам исследования было показано, что однократное системное (внутривенное) введение препарата тяжелоцепочечных моноклональных антител B5-Fc и B10-Fc в дозе 1 мг/кг животным через час, 6 часов и 24 часа после заражения позволяет защитить животных от инфекции, вызванной вирусом SARS-CoV-2. Специалисту среднего уровня очевидно, что препарат антитела также может вводиться внутримышечно, внутрибрюшинно, интраназально или подкожно.
У всех животных, получивших препарат, не было зафиксировано снижения веса более 5%. Гибель зараженных животных, получивших препарат, отсутствовала. Тогда как в контрольной группе животных после заражения наблюдается снижение массы тела, к 8 суткам все животные из группы контроля погибли.
Таким образом, можно сделать вывод, что разработанные однодоменные антитела и их производные могут быть использованы для терапии заболевания, вызванного вирусом SARS-CoV-2.
Пример 7. Изучение протективной активности тяжелоцепочечных моноклональных антител против различных вариантов вируса SARS-CoV-2.
Целью данной работы являлась изучение возможности терапии инфекции, вызванной различными вариантами вируса SARS-CoV-2, при помощи разработанным тяжелоцепочечных моноклональных антител. В экспериментах использовали модель инфекции сирийских хомячков, так как их рецепторы ACE2 обладают высоким сродством к SARS-CoV-2.
Для изучения протективной активности тяжелоцепочечных моноклональных антител B5-Fc и B10-Fc (SEQ ID NO:1 и SEQ ID NO:2) в отношении различных вариантов вируса SARS-CoV-2, сирийских хомячков заражали интраназально, в дозе 106 TCID50/животное. В исследовании была изучена протективная активность антител против 5 различных вариантов вируса (В.1.1.1, XBB.1.16, EG.5.1.1, XBB.1.9.1, JN.1). Для исследования был выбран внутривенный путь введения препарата в дозе 1 мг/кг через 1 час после заражения, однако препарат также может вводиться внутривенно, внутримышечно, интраназально или подкожно.
В исследовании было использовано 100 сирийских хомячков (по 50 животных для антитела B5-Fc и для антитела B10-Fc, соответственно), массой 35-45 грамм, по 5 животных в опытной (препарат антител) и контрольной (плацебо) группах, для каждого из 5 вариантов вируса SARS-CoV-2. Схема эксперимента представлена в таблице 5. На четвертый день после заражения животных подвергали эвтаназии, выделяли легкие и далее оценивали вирусную нагрузку в легких опытных и контрольных животных при помощи титрования на постоянной культуре клеток почки африканской зеленой мартышки - Vero E6.
Таблица 5. Дизайн и результаты эксперимента по исследованию протективности тяжелоцепочечных моноклональных антител в терапевтическом режиме применения на сирийских хомячках.
В исследовании использовали штаммы вируса SARS-CoV-2, изолированные в ФГБУ «НИЦЭМ им. Н.Ф.Гамалеи» Минздрава России, хранящийся в Государственной коллекции вирусов: B.1.1.1 hCoV-19/Russia/Moscow_PMVL-1/2020; ХВВ.1.9.1 hCoV-19/Russia/MOW-PMVL-OM0223O11/2023; ХВВ.1.16 hCoV-19/Russia/MOW-PMVL-OM0223O420/2023; Омикрон EG.5.1 hCoV-19/Russia/SPE-RII-21139S/2023; Омикрон JN.1- hCoV-19/Russia/MOW-PMVL-LSCV-LD134/2023.
Исходя из полученных данных, представленных в таблице 5, было продемонстрировано значительное снижение вирусной нагрузки в легких сирийских хомячков, получивших тяжелоцепочечные моноклональные антитела B5-Fc и B10-Fc через час после заражения вирусами SARS-CoV-2. Кроме того, достоверное снижение вирусной нагрузки было продемонстрировано при заражение всеми использованными вариантами вируса SARS-CoV-2, что указывает на то, что полученные тяжелоцепочечные моноклональные антитела B5-Fc и B10-Fc, обладают выраженной защитной активностью в режиме терапии против широкого спектра различных вариантов вируса SARS-CoV-2.
Полученные результаты свидетельствуют о том, что введение препарата тяжелоцепочечных моноклональных антител B5-Fc и B10-Fc (SEQ ID NO:1 и SEQ ID NO:2) позволяет защитить млекопитающих от клинических проявлений инфекции, вызванной летальной дозой вируса SARS-CoV-2. Специалисту среднего уровня очевидно, что другие созданные антитела, обладающие вируснейтрализующей активностью, также могут защищать млекопитающих от клинических проявлений инфекции, вызванной вирусом SARS-CoV-2.
Таким образом, в результате проведенных экспериментов был разработан способ терапии инфекций, вызываемых вирусом SARS-CoV-2 различных вариантов и штаммов, заключающийся во введении в организм млекопитающих в эффективном количестве любого созданного тяжелоцепочечного моноклонального антитела.
Промышленная применимость
Все приведенные примеры подтверждают эффективность созданных тяжелоцепочечных моноклональных антител, обладающих вируснейтрализующей активностью, и обладающих терапевтическими и протективными свойствами против вируса SARS-CoV-2 и их промышленную применимость.
--->
<ST26SequenceListing dtdVersion="V1_3" fileName="Тяжелоцепочечные
моноклональные антитела_2.xml" softwareName="WIPO Sequence"
softwareVersion="2.3.0" productionDate="2024-08-16">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>1</ApplicationNumberText>
<FilingDate>2024-08-07</FilingDate>
</ApplicationIdentification>
<ApplicantFileReference>1</ApplicantFileReference>
<ApplicantName languageCode="ru">Федеральное Государственное
Бюджетное Учреждение «Национальный исследовательский центр
эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи»
Министерства здравоохранения Российской Федерации</ApplicantName>
<ApplicantNameLatin>federalnoe gosudarstvennoe biudzhetnoe
uchrezhdenie Natsionalnyi issledovatelskii tsentr epidemiologii i
mikrobiologii imeni pochetnogo akademika N F Gamalei Ministerstva
zdravookhraneniia Rossiiskoi Federatsii</ApplicantNameLatin>
<InventionTitle languageCode="ru">Тяжелоцепочечные моноклональные
антитела, специфически связывающиеся с S белком вируса SARS-CoV-2, и
способ их применения для терапии заболеваний, вызываемых различными
вариантами вируса SARS-CoV-2.</InventionTitle>
<SequenceTotalQuantity>8</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>358</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..358</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q2">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QVTLKESGGGSVQAGGSLRLSCKDSPYQIHNRYMGWFRQVPNKAREGVAAID
SQGRTTYADSVKGRFTISKDNSKNTLYLQMDSLKAEDTAMYYCAADIVFWHEDRPLEPTSYKHWGQGTQV
TVSSEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDG
VEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTL
PPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGN
VFSCSVMHEALHNHYTQKSLSLSPGK</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="2">
<INSDSeq>
<INSDSeq_length>357</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..357</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q4">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QVQLQESGGGSVQAGGSLRLSCTPSGFTVHDSDMGWYRVKPGNECELVTTLF
GDGDTYYADSVKDRFIISQDNAKNTVYLQMNNLKPEDTAKYHCVARGVGVYGMHWFCGEYNFAGQGTQVT
VSSEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGV
EVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLP
PSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNV
FSCSVMHEALHNHYTQKSLSLSPGK</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="3">
<INSDSeq>
<INSDSeq_length>126</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..126</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q6">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Camelus bactrianus</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QVTLKESGGGSVQAGGSLRLSCKDSPYQIHNRYMGWFRQVPNKAREGVAAID
SQGRTTYADSVKGRFTISKDNSKNTLYLQMDSLKAEDTAMYYCAADIVFWHEDRPLEPTSYKHWGQGTQV
TVSS</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="4">
<INSDSeq>
<INSDSeq_length>125</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..125</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q8">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Camelus bactrianus</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QVQLQESGGGSVQAGGSLRLSCTPSGFTVHDSDMGWYRVKPGNECELVTTLF
GDGDTYYADSVKDRFIISQDNAKNTVYLQMNNLKPEDTAKYHCVARGVGVYGMHWFCGEYNFAGQGTQVT
VSS</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="5">
<INSDSeq>
<INSDSeq_length>1074</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..1074</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q10">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>caggtcaccttgaaggagtctggggggggctcggtgcaggctggagggtctc
tgaggctctcctgtaaagactctccttaccagatccataaccgctacatgggatggttccgccaagttcc
aaataaggcgcgcgagggggtcgcggcaattgatagtcaaggtaggacaacgtacgcagactccgtgaaa
ggtcgattcaccatctccaaagacaactccaagaacaccctgtatcttcaaatggacagcctgaaagctg
aagacactgccatgtattactgtgcggcggatattgtcttctggcatgaggaccggcctctcgaaccgac
ttcgtataaacactggggacaggggacccaggtcaccgtctcctcagaacctaagtcctgtgacaagacc
cacacctgtccaccttgtcctgctccagagctgcttggaggtccaagcgtgttcctgtttcctcccaaac
ctaaggacaccctgatgatctccaggacaccagaagtgacctgtgtcgttgtggacgtctctcacgagga
tcctgaggtgaagttcaactggtatgtggatggtgtggaggtccacaatgccaagaccaaacccagagag
gaacagtacaacagcacctacagagtcgtgagtgtgttgaccgtgctgcatcaagactggctgaatggca
aggaatataagtgcaaagtgagcaacaaagcacttcctgctcccatcgagaagaccatctccaaagccaa
aggacaacctagagaacctcaagtctacaccctgccaccctccagagaagagatgaccaaaaaccaagtg
tctctgacctgtcttgtcaaaggcttctatccctctgacattgctgtggagtgggagagcaatggacaac
ctgagaacaactataagaccacaccacctgtcctggacagtgatggctccttctttctgtatagtaagct
gacagtggacaagagcaggtggcagcaaggcaatgtcttctcctgcagtgtgatgcatgaagccttgcac
aaccactacacccagaagagcctgtctttgtctcctggcaag</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="6">
<INSDSeq>
<INSDSeq_length>1071</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..1071</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q14">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>caggtgcagctgcaggagtcggggggaggctcggtgcaggctggagggtctc
tgagactctcctgtacaccctctggattcacggttcatgattctgacatgggctggtaccgggtgaagcc
tgggaatgagtgcgaattggttacaacactttttggcgatggcgacacatactatgcggactccgtgaag
gaccgcttcatcatctcccaagacaacgccaagaacacggtatatctgcagatgaacaacctgaagcctg
aggatacggccaagtatcattgcgtggcgcggggcgtcggggtctacggtatgcactggttctgtgggga
atataacttcgcgggccaggggacccaggtcactgtctcctcagaacctaagtcctgtgacaagacccac
acctgtccaccttgtcctgctccagagctgcttggaggtccaagcgtgttcctgtttcctcccaaaccta
aggacaccctgatgatctccaggacaccagaagtgacctgtgtcgttgtggacgtctctcacgaggatcc
tgaggtgaagttcaactggtatgtggatggtgtggaggtccacaatgccaagaccaaacccagagaggaa
cagtacaacagcacctacagagtcgtgagtgtgttgaccgtgctgcatcaagactggctgaatggcaagg
aatataagtgcaaagtgagcaacaaagcacttcctgctcccatcgagaagaccatctccaaagccaaagg
acaacctagagaacctcaagtctacaccctgccaccctccagagaagagatgaccaaaaaccaagtgtct
ctgacctgtcttgtcaaaggcttctatccctctgacattgctgtggagtgggagagcaatggacaacctg
agaacaactataagaccacaccacctgtcctggacagtgatggctccttctttctgtatagtaagctgac
agtggacaagagcaggtggcagcaaggcaatgtcttctcctgcagtgtgatgcatgaagccttgcacaac
cactacacccagaagagcctgtctttgtctcctggcaag</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="7">
<INSDSeq>
<INSDSeq_length>378</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..378</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q16">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Camelus bactrianus</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>caggtcaccttgaaggagtctggggggggctcggtgcaggctggagggtctc
tgaggctctcctgtaaagactctccttaccagatccataaccgctacatgggatggttccgccaagttcc
aaataaggcgcgcgagggggtcgcggcaattgatagtcaaggtaggacaacgtacgcagactccgtgaaa
ggtcgattcaccatctccaaagacaactccaagaacaccctgtatcttcaaatggacagcctgaaagctg
aagacactgccatgtattactgtgcggcggatattgtcttctggcatgaggaccggcctctcgaaccgac
ttcgtataaacactggggacaggggacccaggtcaccgtctcctca</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="8">
<INSDSeq>
<INSDSeq_length>375</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..375</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q18">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>Camelus bactrianus</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>caggtgcagctgcaggagtcggggggaggctcggtgcaggctggagggtctc
tgagactctcctgtacaccctctggattcacggttcatgattctgacatgggctggtaccgggtgaagcc
tgggaatgagtgcgaattggttacaacactttttggcgatggcgacacatactatgcggactccgtgaag
gaccgcttcatcatctcccaagacaacgccaagaacacggtatatctgcagatgaacaacctgaagcctg
aggatacggccaagtatcattgcgtggcgcggggcgtcggggtctacggtatgcactggttctgtgggga
atataacttcgcgggccaggggacccaggtcactgtctcctca</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Однодоменное антитело и его модификации, специфически связывающиеся с RBD S белка вируса SARS-CoV-2, и способ их применения для терапии и экстренной профилактики заболеваний, вызываемых вирусом SARS-CoV-2 | 2021 |
|
RU2763001C1 |
| Однодоменные наноантитела против шиповидного белка вируса SARS-CoV-2 | 2021 |
|
RU2794141C2 |
| Средство и способ терапии и экстренной профилактики заболеваний, вызываемых вирусом SARS-CoV-2 на основе рекомбинантного антитела и гуманизированного моноклонального антитела | 2021 |
|
RU2769223C1 |
| Гуманизированное моноклональное антитело, специфически связывающиеся с RBD S белка вируса SARS-CoV-2, средство и способ для терапии и экстренной профилактики заболеваний, вызываемых вирусом SARS-CoV-2 | 2021 |
|
RU2765731C1 |
| Однодоменное антитело ламы Н5 и его производное H5-Fc, специфически связывающие RBD-домен S-белка вируса SARS-CoV-2, обладающие вируснейтрализующей активностью | 2022 |
|
RU2793967C1 |
| Экспрессионный вектор на основе аденоассоциированного вируса, несущий гены рекомбинантных антител, и его применение для профилактики заболеваний, вызываемых вирусом гриппа А и вирусом SARS-CoV-2 | 2023 |
|
RU2817792C1 |
| Экспрессионный вектор на основе аденоассоциированного вируса и способ его применения для экстренной профилактики и профилактики заболеваний, вызываемых вирусом SARS-CoV-2 (варианты) | 2022 |
|
RU2777404C1 |
| Плазмидная генетическая конструкция pET21a_SKP, обеспечивающая экспрессию в прокариотической системе E.coli рекомбинантного белка SKP, и рекомбинантный белок SKP, обладающий широконейтрализующими свойствами однодоменного наноантитела против SARS-CoV-2 | 2024 |
|
RU2839376C1 |
| Моноклональное антитело iC2 и его антигенсвязывающий фрагмент, селективно связывающие рецептор-связывающий домен Spike-белка вируса SARS-CoV-2, обладающие вируснейтрализующей активностью | 2023 |
|
RU2817697C1 |
| Моноклональное антитело iC1 и его антигенсвязывающий фрагмент, селективно связывающие рецептор-связывающий домен Spike-белка вируса SARS-CoV-2, обладающие вируснейтрализующей активностью | 2023 |
|
RU2817696C1 |

Группа изобретений относится к области биотехнологии, иммунологии и вирусологии. Предложено тяжелоцепочечное моноклональное антитело, специфически связывающееся с S белком вируса SARS-CoV-2. Тяжелоцепочечное моноклональное антитело обладает вируснейтрализующей активностью и имеет аминокислотную последовательность SEQ ID NO:1 или SEQ ID NO:2. Также предложены нуклеиновая кислота, имеющая нуклеотидную последовательность, кодирующую указанное тяжелоцепочечное моноклональное антитело, клетка-продуцент, содержащая данную нуклеиновую кислоту, и способ терапии заболевания, вызванного вирусом SARS-CoV-2, с использованием указанного тяжелоцепочечного моноклонального антитела. Группа изобретений обеспечивает создание тяжелоцепочечных моноклональных антител, которые эффективно связывают S белок вируса SARS-CoV-2, нейтрализуют вирус SARS-CoV-2 и могут быть использованы для терапии заболеваний, вызываемых вирусом SARS-CoV-2. Кроме того, разработанное антитело обладает широким спектром вируснейтрализующей активности против различных вариантов вируса SARS-CoV-2. 4 н. и 2 з.п. ф-лы, 9 ил., 5 табл., 7 пр.
1. Тяжелоцепочечное моноклональное антитело, для терапии заболевания, вызванного вирусом SARS-CoV-2, специфически связывающееся с S белком вируса SARS-CoV-2, обладающее вируснейтрализующей активностью и имеющее аминокислотную последовательность SEQ ID NO:1 или SEQ ID NO:2.
2. Тяжелоцепочечное моноклональное антитело по п.1, отличающееся тем, что представляет собой однодоменное антитело, имеющее аминокислотную последовательность SEQ ID NO:3 или SEQ ID NO:4, модифицированное Fc-фрагментом IgG человека.
3. Тяжелоцепочечное моноклональное антитело по любому из пп.1 или 2, отличающееся тем, что обладает вируснейтрализующей активностью в отношении широкого спектра вариантов вируса SARS-CoV-2, в частности В.1.1.1, B.1.617.2, XBB1, XBB 1.5, XBB 1.9, XBB 1.16, Eris, Pirola, JN.1.
4. Нуклеиновая кислота, имеющая нуклеотидную последовательность, кодирующую тяжелоцепочечное моноклональное антитело по п.1 или 2.
5. Клетка-продуцент для экспрессии антитела по любому из пп.1 или 2, содержащая соответствующую нуклеиновую кислоту по п.4.
6. Способ терапии заболевания, вызванного вирусом SARS-CoV-2, включающий введение в организм млекопитающих антитела по любому из пп.1 или 2 в эффективном количестве.
| Однодоменное антитело и его модификации, специфически связывающиеся с RBD S белка вируса SARS-CoV-2, и способ их применения для терапии и экстренной профилактики заболеваний, вызываемых вирусом SARS-CoV-2 | 2021 |
|
RU2763001C1 |
| Однодоменные наноантитела против шиповидного белка вируса SARS-CoV-2 | 2021 |
|
RU2794141C2 |
| Однодоменное антитело ламы Н5 и его производное H5-Fc, специфически связывающие RBD-домен S-белка вируса SARS-CoV-2, обладающие вируснейтрализующей активностью | 2022 |
|
RU2793967C1 |
| CN 111848789 A, 30.10.2020 | |||
| WO 2023076881 A1, 04.05.2023 | |||
| CN 112094342 A, 18.12.2020 | |||
| В | |||
| П | |||
| Баклаушев и др | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2025-03-12—Публикация
2024-08-29—Подача