Область техники.
Изобретение относится к плазмидной генетической конструкции pET21a_SKP, обеспечивающей экспрессию в прокариотической системе E. coli рекомбинантного белка SKP, и рекомбинантному белку SKP, обладающему широко-нейтрализующими свойствами однодоменного антитела против SARS-CoV-2 и может быть использовано в генной инженерии, биотехнологии и медицине. Рекомбинантный белок SKP может служить компонентом для создания диагностикумов COVID-19.
Уровень техники.
Несмотря на проведенную вакцинацию населения, до сих пор остается необходимость в дополнительных средствах диагностики и терапии COVID-19. Это обусловлено появлением новых штаммов SARS-CoV-2, против которых вакцины на основе Уханьского штамма Wu-1 имеют значительно меньшую эффективность.
Для защиты людей, которым вакцинация противопоказана по медицинским показателям, а также для терапии заболевания при его тяжелом протекании могут быть использованы моноклональные антитела, нейтрализующие SARS-CoV-2. Моноклональные терапевтические антитела хорошо зарекомендовали себя в мировой практике, в настоящее время одобрено или находятся на одобрении в США и Европе 173 моноклональных антитела [www.antibodysociety.org/antibody-therapeutics-product-data].
Спайковый поверхностный белок SARS-CoV-2 имеет большое количество гликозилированных участков, что ограничивает доступ для антител классической структуры (Watanabe Y. et al, 2020). Распознавание антигенных детерминант такого белка, однако, возможно однодоменными антителами (VHH, variable heavy-heavy, наноантитела), которыми обладают животные семейства Верблюдовых. Однодоменные антитела состоят только из тяжелых цепей иммуноглобулинов (variable heavy-heavy, VHH-антитела, наноантитела) [Maass DR, 2007]. Этот тип антител образовался в результате мутации в шарнирной области тяжелой цепи, что привело к делеции участка связывания тяжелой и легкой цепей на фоне мутации в шарнирной области тяжелой цепи тяжелоцепочечного антитела. Однодоменные антитела обладают рядом преимуществ перед традиционными антителами и уже широко используются для решения ряда научных и медицинских задач [Van Bockstaele 2009; Gorchakov, А.А., 2021]. Они конформационно более стабильны при различных рН и широком температурном диапазоне, имеют высокую растворимость, а также из-за своих небольших размеров способны связываться с теми участками эпитопа, которые недоступны классическим антителам.
Получение однодоменных антител, специфичных в отношении вирусных патогенов, является перспективным направлением конструирования терапевтических препаратов [Detalle L., 2015; Есмагамбетов И.Б., 2021]. В частности, большое число работ посвященных использованию наноантител для противодействия SARS-CoV-2 было опубликовано с начала пандемии COVID-19 [Lu Q, Zhang Z, 2021, Zebardast A., 2022].
Ближайшие аналоги.
В настоящее время одобренных препаратов на основе однодоменных антител и их производных для лечения COVID-19 не имеется.
Известно мышиное моноклональное антитело, специфически связывающее RBD фрагмент в составе S белка вируса SARS-CoV-2, обладающее способностью нейтрализовать живой SARS-CoV-2 in vitro (патент RU 2744274 С1, опубл. 04.03.2021). Недостатком данного антитела является его высокая иммуногенность по отношению к человеку, что делает критически опасным его внутривенное введение.
Известна разработка американских исследователей по получению наноантитела, специфически связывающегося с RBD SARS-CoV-2, описанная в патенте (WO 2021/224606). Авторы с помощью фагового дисплея отобрали перспективные варианты наноантител, специфически узнающих RBD SARS-CoV-2. Затем переклонировали последовательность отобранного наноантитела в экспрессионный вектор pADL-23c. Продукцию наноантител проводили также в BL21(DE3). Принципиальным отличием нашей разработки является другая последовательность, кодирующая наноантитело против SARS-CoV-2. Также разработчики проверяли специфическое взаимодействие полученного наноантитела только со штаммом Alpha SARS-CoV-2.
Известна большая библиотека однодоменных антител к S-белку SARS-CoV-2, в том числе к его RBD участку, в том числе нейтрализующих in vitro живой вирус SARS-CoV-2, а также лентивирус, псевдотипированный S-белком SARS-CoV-2 (заявка WO 2022040603 А2, опубл. 24.02.2022).
Российские исследователи (RU 2793967 С1) получили однодоменное антитело Н5 и его производное H5-Fc, специфически связывающие RBD-домен S-белка вируса SARS-CoV-2, обладающее вируснейтрализующей активностью. Отличием нашей разработки является другая последовательность, кодирующая наноантитело против SARS-CoV-2.
Также известна разработка по получению наноантитела, специфически связывающегося с RBD SARS-CoV-2, описанная в патенте (WO 2022/221120 А1). Отличием от нашей разработки является наработка рекомбинантного белка в эукариотических клетках. Недостатком данного патента является отсутствие электрофореграммы в ПААГ, что не позволяет оценить выход и чистоту белка.
Известно однодоменное антитело, специфически связывающееся с RBDS белка вируса SARS-CoV-2, обладающее вируснейтрализующей активностью и имеющее аминокислотную последовательность SEQ ID NO: 1, или SEQ ID NO: 2, или SEQ ID NO: 3 (патент RU 2763001 С1, опубл. 24.12.2021). В указанном патенте показаны нейтрализующие свойства нескольких однодоменных антител, а также способность одного из этих антител (р2 с5) в виде химерного белка, слитого с Fc-фрагментом IgGl человека (p2c5-fc), нейтрализовать SARS-CoV-2 in vivo в моделях АСЕ2-трансгенных мышей и сирийского хомячка. Принципиальным отличием нашей разработки является другая последовательность, кодирующая наноантитело против SARS-CoV-2.
Однако, в указанном аналоге однодоменные антитела обладают недостаточной широтой вирусной нейтрализации (данные представлены относительно только одного штамма).
Наиболее близким аналогом (прототипом) является плазмидная генетическая конструкция pET21_Ab_CoV-2_1.3, обеспечивающая экспрессию рекомбинантного белка AB_COV-2_1.3 в прокариотической системе Е. col, обладающего свойствами однодоменного наноантитела против SARS-CoV-2, имеющего размер 5925 п.н. и рекомбинантный белок AB_COV-2_1.3, обладающий свойствами однодоменного наноантитела против SARS-CoV-2 (патент RU 2798508, опубл. 23.06.2023 г.). Изобретение позволяет получить хороший выход белка в растворимой форме. Однако полученное наноантитело не проверялось на способность нейтрализовать различные штаммы вируса SARS-CoV-2.
Раскрытие изобретения.
Техническим результатом заявленной группы изобретений является расширение арсенала однодоменных наноантител для диагностики вируса SARS-CoV-2, а также получение широконейтрализующих антител с высоким и стабильным экспрессионным выходом, способных диагностировать различные штаммы указанного вируса.
Заявляемая плазмидная генетическая конструкция pET21a_SKP обеспечивает экспрессию рекомбинантного белка SKP с высоким и стабильным выходом в периплазме бактерий E. coli, и простоту всевозможных генно-инженерных манипуляций, адаптации для конкретных задач.
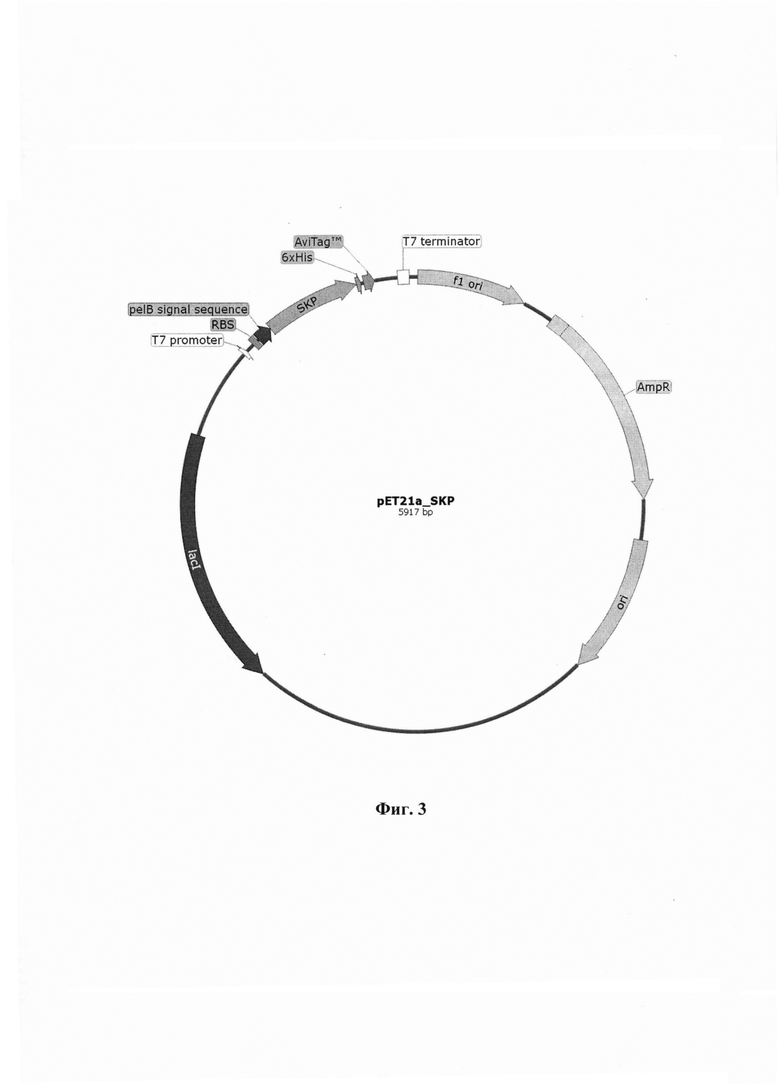
Указанный технический результат достигается созданием плазмидной генетической конструкции pET21a_SKP, содержащая ген, кодирующий наноантитело, для получения рекомбинантного белка SKP в прокариотической системе экспрессии E. coli, имеющая размер 5917 п.н., нуклеотидную последовательность SEQ ID NO: 1 и содержащая в соответствии с физической и генетической картой, представленной на фиг. 3, следующие элементы:
 ген fl ori (координаты с 12 по 467 п.н.) начало репликации бактериофага; стрелка указывает направление синтеза (+) цепи;
ген fl ori (координаты с 12 по 467 п.н.) начало репликации бактериофага; стрелка указывает направление синтеза (+) цепи;
 ген AmpR (координаты с 599 по 1459 п.н.), в качестве генетического маркера, определяющего устойчивость (кодирует бета-лактамазу) к ампициллину клеток бактерии E. coli, трансформированных рекомбинантной плазмидой рЕТ21 a_SKP;
ген AmpR (координаты с 599 по 1459 п.н.), в качестве генетического маркера, определяющего устойчивость (кодирует бета-лактамазу) к ампициллину клеток бактерии E. coli, трансформированных рекомбинантной плазмидой рЕТ21 a_SKP;
 участок начала репликации ori (координаты с 1630 по 2218 п.н.);
участок начала репликации ori (координаты с 1630 по 2218 п.н.);
 ген белка репрессора lacI (координаты с 3648 п.н. по 4730 п.н.) - ДНК-связывающий белок, который ингибирует экспрессию генов E. coli и обеспечивает экспрессию целевого рекомбинантного белка VHH после добавления индуктора изопропил-β-D-1-тиогалактопиранозида (IPTG);
ген белка репрессора lacI (координаты с 3648 п.н. по 4730 п.н.) - ДНК-связывающий белок, который ингибирует экспрессию генов E. coli и обеспечивает экспрессию целевого рекомбинантного белка VHH после добавления индуктора изопропил-β-D-1-тиогалактопиранозида (IPTG);
 промотор фага Т7 (координаты с 5117 по 5135 п.н.), обеспечивающий экспрессию последовательности гена SKP в прокариотических клетках E. coli;
промотор фага Т7 (координаты с 5117 по 5135 п.н.), обеспечивающий экспрессию последовательности гена SKP в прокариотических клетках E. coli;
 RBS (координаты с 5175 по 5197 п.н.) сайт посадки рибосомы;
RBS (координаты с 5175 по 5197 п.н.) сайт посадки рибосомы;
 последовательность, кодирующая лидерный пептид pelB (координаты с 5205 по 5270 п.н.), последовательность в составе белка, которая обеспечивает экспорт белка из клетки;
последовательность, кодирующая лидерный пептид pelB (координаты с 5205 по 5270 п.н.), последовательность в составе белка, которая обеспечивает экспорт белка из клетки;
 ген SKP (координаты с 5271 по 5672 п.н.), кодирующий однодоменное антитело против SARS-CoV-2;
ген SKP (координаты с 5271 по 5672 п.н.), кодирующий однодоменное антитело против SARS-CoV-2;
 6×His (координаты с 5673 по 5690 п.н.), для очистки антитела против SARS-CoV-2;
6×His (координаты с 5673 по 5690 п.н.), для очистки антитела против SARS-CoV-2;
 пептидная метка AviTag (координаты с 5703 по 5747 п.н.), обеспечивающая ферментативное биотинилирование;
пептидная метка AviTag (координаты с 5703 по 5747 п.н.), обеспечивающая ферментативное биотинилирование;
 Т7 terminator (координаты с 5845 по 5892 п.н.) область терминатора транскрипции бактериофага Т7.
Т7 terminator (координаты с 5845 по 5892 п.н.) область терминатора транскрипции бактериофага Т7.
Указанный технический результат достигается также тем, что получен рекомбинантный белок SKP, экспрессируемый в прокариотической системе E. coli плазмидной генетической конструкцией pET21a_SKP по п. 1, обладающий широконейтрализующими свойствами однодоменного наноантитела против SARS-CoV-2, имеющий молекулярную массу 23 кДа и аминокислотную последовательность SEQ ID NO: 2.
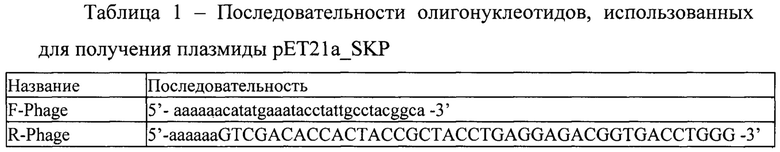
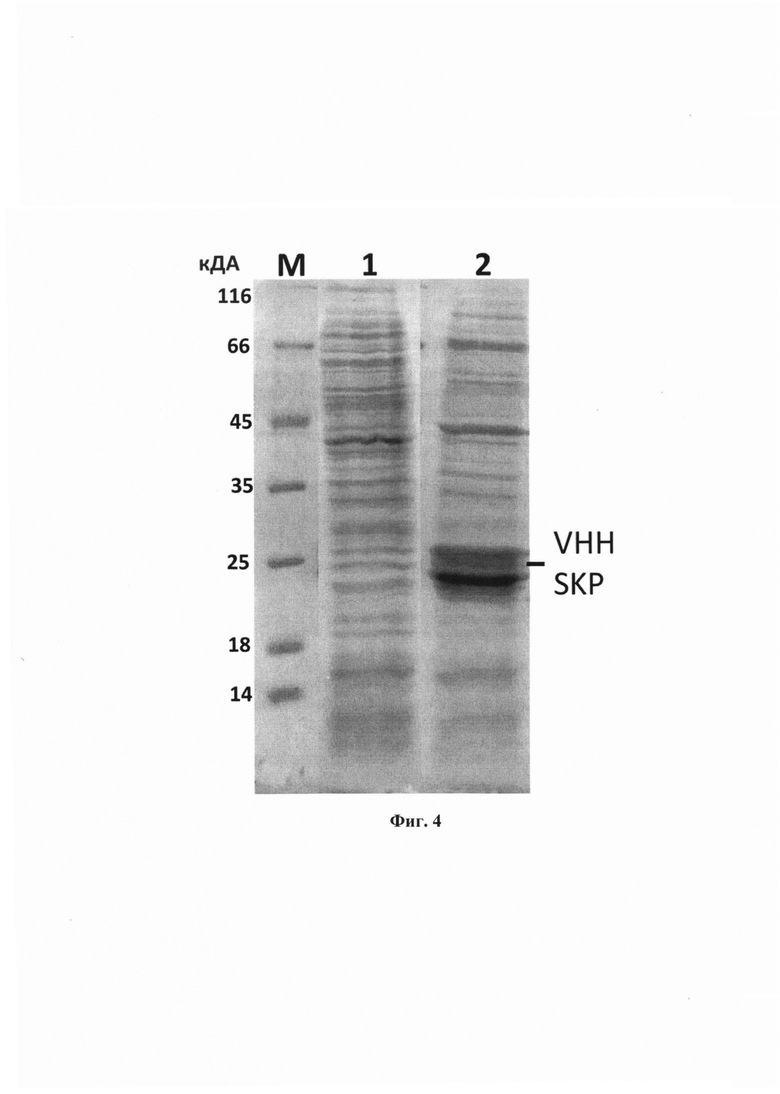
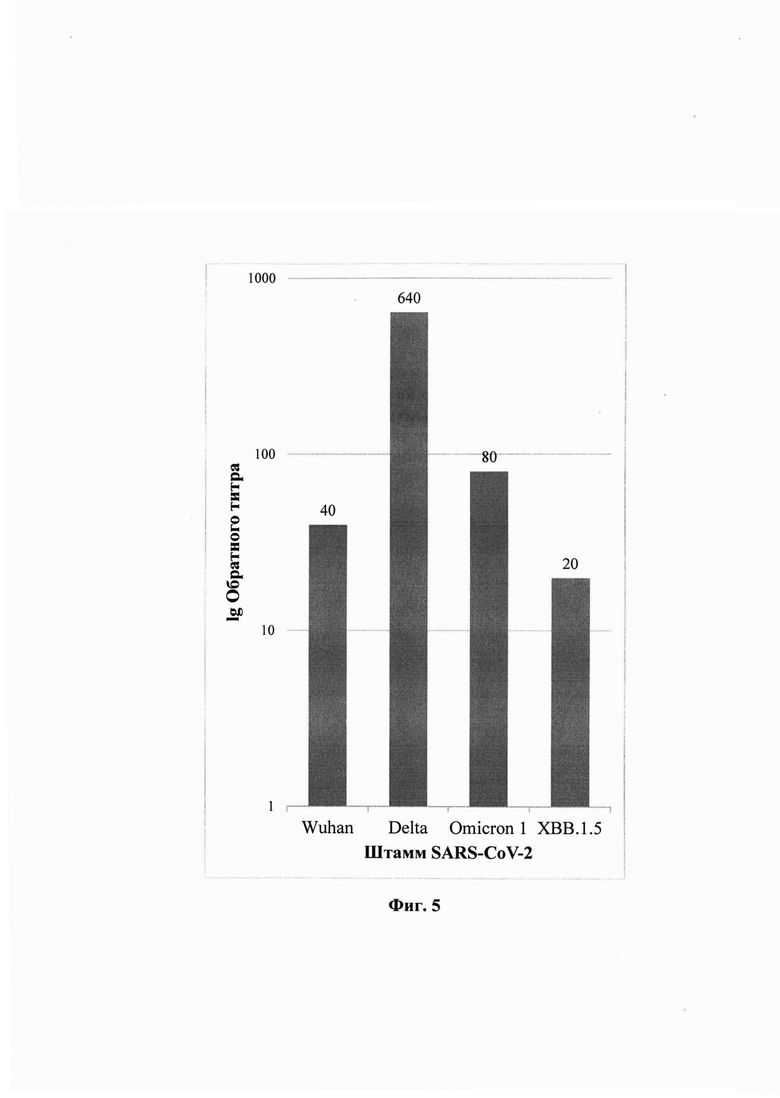
Изобретение поясняется графическими материалами, представленными на фиг. 1 -5 и таблице 1. На фиг. 1 приведена нуклеотидная последовательность плазмидной генетической конструкции рЕТ21а_ SKP. На фиг. 2 представлена аминокислотная последовательность рекомбинантного белка однодоменного антитела SKP против SARS-CoV-2. На фиг. 3 изображена физическая и генетическая карта плазмидной генетической конструкции pET21a_SKP. На фиг. 4 представлена электрофореграмма фракций клеточных белков бактерий Е. coli BL21/pET21a_SKP. Электрофореграмма в 15% ПААГ, окрашивание Кумасси G-250. Примечания: М - маркер молекулярной массы белков (15-250 кДа); 1 - лизат идуцированных клеток, трансформированных исходной плазмидой рЕТ21а (отрицательный контроль); 2 - лизат индуцированных клеток, трансформированных pET21a_SKP. На фиг. 5 представлены результаты уровня нейтрализации полученного рекомбинантного белка SKP с различными штаммами вируса SARS-CoV-2. Примечание: в качестве отрицательного контроля (К-) использовали питательную среду; штаммы вируса SARS-CoV-2 WuhanHiCoV-19/Australia/VIC01/2020 (Wuhan-Hu-1), Delta-hCoV-19/Russia/PSK-2804/2021 (Delta (B.1.617.2)) Omicron 1-hCoV-19/Russia/Moscow171619-031221/2021 (Omicron (B.1.1.529), и XBB hCov-19/Russia/TYU-SRC-8642/2023). В таблице 1 представлены последовательности синтезированных олигонуклеотидов, использованных для получения плазмиды pET21a_SKP.
Для лучшего понимания сущности предлагаемого изобретения ниже приведены примеры его осуществления. Все стандартные генно-инженерные и микробиологические манипуляции, а также амплификацию и секвенирование ДНК проводили по известным методикам [Маниатис Т., Фрич Э, Сэмбрук Дж. Молекулярное клонирование, М: Мир, 1984; Клонирование ДНК. Методы. Под ред. Д. Гловера, Пер. с англ., Москва, Мир, 1988; Saiki R.K. et al. Science. 1988, 239(4839): 487-491; Sanger F. et al. Proc. Nat. Acad. Sci. 1977, 74: 5463-5467].
Пример 1. Конструирование плазмидной генетической конструкции pET21a_SKP, обеспечивающей синтез рекомбинантного белка SKP, обладающий широконейтрализующими свойствами однодоменного антитела против SARS-CoV-2
В состав вектора рЕТ21 а(-) была клонирована последовательность SEQ ID NO: 1 (фиг. 1), кодирующая наноантитело против SARS-CoV-2, имеющее аминокислотную последовательность SEQ ID NO: 2 (фиг. 2). Последовательности праймеров, использованные для сборки плазмиды pET21a_SKP, представлены в таблице 1.
С помощью ПЦР была амплифицирована нуклеотидная последовательность SKP, кодирующая наноантитело против SARS-CoV-2. ПНР проводили с использованием ПЦР-амплификатора «БИС» фирмы ООО БИС-Н (Россия). Реакционная смесь объемом 50 мкл, содержащая 2 мкг ДНК (плазмида pHEN2-SKP), 10 пкМ каждого праймера (F-Phage и R-Phage) (таблица 1), 10 мкл 5х Q5 реакционного буфера, 10 мкл 5×Q5 High GC Enhancer, смесь дезоксинуклеотидтрифосфатов (дАТФ, дЦТФ, дТТФ, дГТФ по 2,5 мМ) и 0.5 ед. Q5 High-Fidelity ДНК-полимеразы, реакцию осуществляли при следующих параметрах: 10 с - 98°С, 10 с - 58°С, 30 с - 72°С (30 циклов). Готовые амплификаты были выделены и очищены из геля с помощью набора «Gel Extraction Kit» фирмы Qiagen (Германия) в соответствии с инструкцией производителя.
Предварительно наработанную и очищенную плазмиду рЕТ21а(-) и готовый амплификат обрабатывали эндонуклеазами рестрикции FauNDI и Sail. Реакцию гидролиза проводили в условиях, рекомендованных производителем. С целью очистки линеаризованного вектора, плазмидную ДНК наносили на 1%-й агарозный гель и выделяли из геля с использованием набора «Gel Extraction Kit» фирмы Qiagen (Германия). Реакцию лигирования проводили с использованием ДНК-лигазы бактериофага Т4 («СибЭнзим», г. Новосибирск). Реакция проводилась при +4°С в течение ночи. Полученной лигазной смесью трансформировали компетентные клетки E. coli штамм Neb Stable.
Первичную проверку на наличие вставки проводили при помощи ПЦР с колонии. Разделение продуктов амплификации проводили в 1%-м агарозном геле с последующим окрашиванием бромистым этидием (0,5 мкг/мл).
Положительные колонии, культивировали в 5 мл среды LB с ампициллином (50 мкг/мл) в течение ночи при 37°С при 170 об/мин. Затем плазмидную ДНК выделяли из бактериальных клеток с помощью коммерческих наборов DNAminikit фирмы «Qiagen» согласно рекомендациям производителя. Первичную структуру экспрессионного вектора подтверждали секвенированием. Секвенирование проводили по методу Сэнгера в ЦКП «Геномика» СО РАН (г.Новосибирск). В результате была получена рекомбинантная плазмида pET21a_SKP, обеспечивающая синтез наноантитела против SARS-CoV-2, генетическая и физическая карта которой представлена на фиг. 3.
Секвенирование плазмидной ДНК положительных клонов в районе встройки позволило отобрать клоны с отсутствием дефектов встраиваемых генов (вставки, делеции, замены), после чего из отобранных клонов была наработана и выделена целевая плазмидная ДНК.
Пример 2. Получение штамма Е. coli - продуцента рекомбинантного белка
При создании прокариотической системы экспрессии гена SKP, кодирующего однодоменное антитело против SARS-Cov-2, использовали штамм BL21(DE3) культуры клеток E. coli (Novagen, США).
2.1. Трансформация «компетентных» клеток Е. coli рекомбинантной плазмидой.
К «компетентным» клеткам BL21(DE3) добавляли 10 мкл лигазной смеси, инкубировали на льду в течение 30 минут. После этого клетки подвергали «температурному шоку» при 42°С в течение 45 сек. Охлаждали клетки на льду в течение 2 минут, затем добавляли 200 мкл среды «S.O.B» (Super Optimal Broth) и инкубировали при 37°С в течение 60 минут. По окончании инкубации трансформированные клетки высевали на чашку Петри с твердой питательной средой LB (Lysogeny broth) (среда LB с 1,5% агара), содержащей антибиотик (ампициллин, 50-100 мкг/мл).
2.2. Культивирование трансформированной культуры клеток E. coli и индукция синтеза рекомбинантного белка SKP
Клетки E. coli штамма BL21(DE3), трансформированные вектором pET21a_SKP, селективно культивировали в 150 мл жидкой питательной среды LB с добавлением ампициллина натриевой соли в рабочей концентрации 20 мкг/мл. Синтез целевого рекомбинантного белка индуцировали с добавлением 0,5 мМ IPTG (изопропил-β-D-тиогалактозид) и култивированием при 30°, 180 об/мин. Отбор клонов E. coli - продуцентов проводили по наличию синтезируемого целевого белка по результатам электрофореграммы лизатов клеток в 10% -ном полиакриламидном геле (фиг. 4) с додецилсульфатом натрия (SDS-ПААГ) (см. пример 3). В качестве контроля использовали, полученный аналогичным способом, лизат идуцированных клеток, трансформированных исходной плазмидой рЕТ21а.
Пример 3. Белковый электрофорез в полиакриламидном геле с додецилсульфатом натрия (SDS-ПААГ)
Электрофорез проводили в разрешающем геле (состав: 30% акриламида; 1,5 М Tris (рН 8,8); 10% SDS; 10% аммония персульфата; TEMED (tetramethylethylenediamine) 1 мкл/мл) и концентрирующем геле (состав: 30% акриламида; 1М Tris (рН 6,8); 10% SDS; 10% аммония персульфата; TEMED 1 мкл/мл) в различных буферных растворах (верхний -5Х трис-глициновый буферный раствор рН 8,3 (состав: 1,25 мМ Tris; 1,25 М глицина; 0,5% SDS), нижний - 1X трис-ацетатный буферный раствор рН 8,0 (состав: 40 мМ Tris - HCl; 40 мМ уксусной кислоты; 2 мМ EDTA (этилендиаминтетрауксусная кислота). Биологический материал смешивали с буферным раствором для нанесения, кипятили 5 минут и наносили в верхний концентрирующий гель. SDS-ПААГ вели при напряжении ~10 В/см в концентрирующем геле, ~180 В в разрешающем геле. Окраску гелей проводили при помощи раствора Кумасси G-250.
Пример 4. Очистка рекомбинантного белка SKP в денатурирующих условиях
Очистку рекомбинантного белка SKP, содержащего полигистидиновый блок, проводили аффинной хроматографией на Ni-хеллатной смоле, согласно протоколу фирмы-производителя (Qiagen). Полученные клеточные лизаты штамма E. coli - продуцента и очищенный рекомбинантной белок анализировали методом белкового электрофореза по методу Лэммли (Laemmli UK. Cleavage of structural proteins during the assembly of the head of bacteriophage T4. / Nature. 1970; 227(5259): 680-685) в SDS-ПААГ. В качестве контроля использовали полученный аналогичным способом лизат клеток E. coli штамма BL21(DE3), содержавший векторную плазмиду рЕТ21а. Электрофоретическая подвижность в 10% SDS-ПААГ (см. пример 3) синтезируемого белка - 23 кДа. Концентрацию рекомбинантного белка измеряли визуально по данным электрофореграммы (фиг. 4) и при помощи набора «Bio-Rad Protein Assay Kit» в соответствии с рекомендациями производителя на спектрофотометре.
Пример 5. Вируснейтрализация
Титр вируснейтрализующих антител определяли при помощи реакции вируснейтрализации. С этой целью были использован штаммы вируса SARS-CoV-2 Wuhan-CoV-19/Australia/VIC01/2020 (Wuhan-Hu-1), Delta - hCoV-19/Russia/PSK-2804/2021 (Delta (B. 1.617.2)), Omicron 1 - hCoV-19/Russia/Moscow171619-031221/2021 (Omicron (B. 1.1.529)) и XBB.1.5 hCov-19/Russia/TYU-SRC-8642/2023, полученные из Государственной коллекции возбудителей вирусных инфекций и риккетсиозов ФБУН ГНЦ ВБ «Вектор» Роспотребнадзора. К препаратам моноклональных антител в разных разведениях добавляли вирус в равной пропорции 1:1 и инкубировали 1 час при 37°С. Затем смесь наносили в дублях на монослой культуры клеток Vero в объеме 100 мкл/лунку. Учет результатов проводили визуально. Любое специфическое поражение культуры клеток в лунке учитывали, как цитопатическое действие (ЦПД). Титром считали последнее разведение, при котором регистрировали защиту монослоя культуры клеток в лунках от ЦПД вируса. В качестве положительного контроля использовали 20-кратное разведение образца сыворотки крови реконвалесцента COVID-19 с ранее установленным титром 1:80. В качестве отрицательного контроля использовали питательную среду. Результаты вируснейтрализующей активности приведены на фиг. 5.
Таким образом, заявляемый технический результат подтверждается примерами 1-5 описания изобретения, в соответствии с которыми получены:
- плазмидная генетическая конструкция рЕТ21а_ SKP, содержащая в своем составе ген, кодирующий однодоменное наноантитело против SARS-Cov-2. Трансформированная рекомбинантной плазмидой культура клеток E. coli BL21/DE3(+) при индукции IPTG осуществляет синтез однодоменного антитела с молекулярной массой 23 кДа. На N-конце рекомбинантный белок SKP содержит полигистидиновый тракт для аффинной очистки;
- высокоочищенный рекомбинантный белок SKP, обладающий свойствами широконейтрализующего наноантитела с высоким и стабильным экспрессионным выходом, способного нейтрализовать как минимум четыре штамма вируса SARS-Cov-2.
--->
<?xml version="1.0" encoding="UTF-8"?>
<!DOCTYPE ST26SequenceListing PUBLIC "-//WIPO//DTD Sequence Listing
1.3//EN" "ST26SequenceListing_V1_3.dtd">
<ST26SequenceListing dtdVersion="V1_3"
fileName="Приложение_Перечень последовательностей_Плазмида pET21a_SKP
и наноантитело против SARS-CoV-2.xml" softwareName="WIPO Sequence"
softwareVersion="2.3.0" productionDate="2024-08-29">
<ApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>123456</ApplicationNumberText>
<FilingDate>2024-08-21</FilingDate>
</ApplicationIdentification>
<ApplicantFileReference>1234</ApplicantFileReference>
<EarliestPriorityApplicationIdentification>
<IPOfficeCode>RU</IPOfficeCode>
<ApplicationNumberText>1234567</ApplicationNumberText>
<FilingDate>2024-08-09</FilingDate>
</EarliestPriorityApplicationIdentification>
<ApplicantName languageCode="ru">Федеральное бюджетное учреждение
науки «Государственный научный центр вирусологии и биотехнологии
«Вектор» Федеральной службы по надзору в сфере защиты прав
потребителей и благополучия человека (ФБУН ГНЦ ВБ «Вектор»
Роспотребнадзора)</ApplicantName>
<ApplicantNameLatin>Federalnoe byudzhetnoe uchrezhdenie nauki
"Gosudarstvennyj nauchnyj tsentr virusologii i biotekhnologii
"Vektor" Federalnoj sluzhby po nadzoru v sfere zashchity
prav potrebitelej i blagopoluchiya cheloveka (FBUN GNTS VB
"Vektor" Rospotrebnadzora) (RU)</ApplicantNameLatin>
<InventionTitle languageCode="ru">Плазмидная генетическая
конструкция pET21a_SKP, обеспечивающая экспрессию в прокариотической
системе Е.coli рекомбинантного белка SKP, и рекомбинантный
белок SKP, обладающий широконейтрализующими свойствами однодоменного
наноантитела против SARS-CoV-2</InventionTitle>
<SequenceTotalQuantity>2</SequenceTotalQuantity>
<SequenceData sequenceIDNumber="1">
<INSDSeq>
<INSDSeq_length>5917</INSDSeq_length>
<INSDSeq_moltype>DNA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..5917</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>other DNA</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q2">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>tggcgaatgggacgcgccctgtagcggcgcattaagcgcggcgggtgtg
gtggttacgcgcagcgtgaccgctacacttgccagcgccctagcgcccgctcctttcgctttcttccctt
cctttctcgccacgttcgccggctttccccgtcaagctctaaatcgggggctccctttagggttccgatt
tagtgctttacggcacctcgaccccaaaaaacttgattagggtgatggttcacgtagtgggccatcgccc
tgatagacggtttttcgccctttgacgttggagtccacgttctttaatagtggactcttgttccaaactg
gaacaacactcaaccctatctcggtctattcttttgatttataagggattttgccgatttcggcctattg
gttaaaaaatgagctgatttaacaaaaatttaacgcgaattttaacaaaatattaacgtttacaatttca
ggtggcacttttcggggaaatgtgcgcggaacccctatttgtttatttttctaaatacattcaaatatgt
atccgctcatgagacaataaccctgataaatgcttcaataatattgaaaaaggaagagtatgagtattca
acatttccgtgtcgcccttattcccttttttgcggcattttgccttcctgtttttgctcacccagaaacg
ctggtgaaagtaaaagatgctgaagatcagttgggtgcacgagtgggttacatcgaactggatctcaaca
gcggtaagatccttgagagttttcgccccgaagaacgttttccaatgatgagcacttttaaagttctgct
atgtggcgcggtattatcccgtattgacgccgggcaagagcaactcggtcgccgcatacactattctcag
aatgacttggttgagtactcaccagtcacagaaaagcatcttacggatggcatgacagtaagagaattat
gcagtgctgccataaccatgagtgataacactgcggccaacttacttctgacaacgatcggaggaccgaa
ggagctaaccgcttttttgcacaacatgggggatcatgtaactcgccttgatcgttgggaaccggagctg
aatgaagccataccaaacgacgagcgtgacaccacgatgcctgcagcaatggcaacaacgttgcgcaaac
tattaactggcgaactacttactctagcttcccggcaacaattaatagactggatggaggcggataaagt
tgcaggaccacttctgcgctcggcccttccggctggctggtttattgctgataaatctggagccggtgag
cgtgggtctcgcggtatcattgcagcactggggccagatggtaagccctcccgtatcgtagttatctaca
cgacggggagtcaggcaactatggatgaacgaaatagacagatcgctgagataggtgcctcactgattaa
gcattggtaactgtcagaccaagtttactcatatatactttagattgatttaaaacttcatttttaattt
aaaaggatctaggtgaagatcctttttgataatctcatgaccaaaatcccttaacgtgagttttcgttcc
actgagcgtcagaccccgtagaaaagatcaaaggatcttcttgagatcctttttttctgcgcgtaatctg
ctgcttgcaaacaaaaaaaccaccgctaccagcggtggtttgtttgccggatcaagagctaccaactctt
tttccgaaggtaactggcttcagcagagcgcagataccaaatactgtccttctagtgtagccgtagttag
gccaccacttcaagaactctgtagcaccgcctacatacctcgctctgctaatcctgttaccagtggctgc
tgccagtggcgataagtcgtgtcttaccgggttggactcaagacgatagttaccggataaggcgcagcgg
tcgggctgaacggggggttcgtgcacacagcccagcttggagcgaacgacctacaccgaactgagatacc
tacagcgtgagctatgagaaagcgccacgcttcccgaagggagaaaggcggacaggtatccggtaagcgg
cagggtcggaacaggagagcgcacgagggagcttccagggggaaacgcctggtatctttatagtcctgtc
gggtttcgccacctctgacttgagcgtcgatttttgtgatgctcgtcaggggggcggagcctatggaaaa
acgccagcaacgcggcctttttacggttcctggccttttgctggccttttgctcacatgttctttcctgc
gttatcccctgattctgtggataaccgtattaccgcctttgagtgagctgataccgctcgccgcagccga
acgaccgagcgcagcgagtcagtgagcgaggaagcggaagagcgcctgatgcggtattttctccttacgc
atctgtgcggtatttcacaccgcatatatggtgcactctcagtacaatctgctctgatgccgcatagtta
agccagtatacactccgctatcgctacgtgactgggtcatggctgcgccccgacacccgccaacacccgc
tgacgcgccctgacgggcttgtctgctcccggcatccgcttacagacaagctgtgaccgtctccgggagc
tgcatgtgtcagaggttttcaccgtcatcaccgaaacgcgcgaggcagctgcggtaaagctcatcagcgt
ggtcgtgaagcgattcacagatgtctgcctgttcatccgcgtccagctcgttgagtttctccagaagcgt
taatgtctggcttctgataaagcgggccatgttaagggcggttttttcctgtttggtcactgatgcctcc
gtgtaagggggatttctgttcatgggggtaatgataccgatgaaacgagagaggatgctcacgatacggg
ttactgatgatgaacatgcccggttactggaacgttgtgagggtaaacaactggcggtatggatgcggcg
ggaccagagaaaaatcactcagggtcaatgccagcgcttcgttaatacagatgtaggtgttccacagggt
agccagcagcatcctgcgatgcagatccggaacataatggtgcagggcgctgacttccgcgtttccagac
tttacgaaacacggaaaccgaagaccattcatgttgttgctcaggtcgcagacgttttgcagcagcagtc
gcttcacgttcgctcgcgtatcggtgattcattctgctaaccagtaaggcaaccccgccagcctagccgg
gtcctcaacgacaggagcacgatcatgcgcacccgtggggccgccatgccggcgataatggcctgcttct
cgccgaaacgtttggtggcgggaccagtgacgaaggcttgagcgagggcgtgcaagattccgaataccgc
aagcgacaggccgatcatcgtcgcgctccagcgaaagcggtcctcgccgaaaatgacccagagcgctgcc
ggcacctgtcctacgagttgcatgataaagaagacagtcataagtgcggcgacgatagtcatgccccgcg
cccaccggaaggagctgactgggttgaaggctctcaagggcatcggtcgagatcccggtgcctaatgagt
gagctaacttacattaattgcgttgcgctcactgcccgctttccagtcgggaaacctgtcgtgccagctg
cattaatgaatcggccaacgcgcggggagaggcggtttgcgtattgggcgccagggtggtttttcttttc
accagtgagacgggcaacagctgattgcccttcaccgcctggccctgagagagttgcagcaagcggtcca
cgctggtttgccccagcaggcgaaaatcctgtttgatggtggttaacggcgggatataacatgagctgtc
ttcggtatcgtcgtatcccactaccgagatatccgcaccaacgcgcagcccggactcggtaatggcgcgc
attgcgcccagcgccatctgatcgttggcaaccagcatcgcagtgggaacgatgccctcattcagcattt
gcatggtttgttgaaaaccggacatggcactccagtcgccttcccgttccgctatcggctgaatttgatt
gcgagtgagatatttatgccagccagccagacgcagacgcgccgagacagaacttaatgggcccgctaac
agcgcgatttgctggtgacccaatgcgaccagatgctccacgcccagtcgcgtaccgtcttcatgggaga
aaataatactgttgatgggtgtctggtcagagacatcaagaaataacgccggaacattagtgcaggcagc
ttccacagcaatggcatcctggtcatccagcggatagttaatgatcagcccactgacgcgttgcgcgaga
agattgtgcaccgccgctttacaggcttcgacgccgcttcgttctaccatcgacaccaccacgctggcac
ccagttgatcggcgcgagatttaatcgccgcgacaatttgcgacggcgcgtgcagggccagactggaggt
ggcaacgccaatcagcaacgactgtttgcccgccagttgttgtgccacgcggttgggaatgtaattcagc
tccgccatcgccgcttccactttttcccgcgttttcgcagaaacgtggctggcctggttcaccacgcggg
aaacggtctgataagagacaccggcatactctgcgacatcgtataacgttactggtttcacattcaccac
cctgaattgactctcttccgggcgctatcatgccataccgcgaaaggttttgcgccattcgatggtgtcc
gggatctcgacgctctcccttatgcgactcctgcattaggaagcagcccagtagtaggttgaggccgttg
agcaccgccgccgcaaggaatggtgcatgcaaggagatggcgcccaacagtcccccggccacggggcctg
ccaccatacccacgccgaaacaagcgctcatgagcccgaagtggcgagcccgatcttccccatcggtgat
gtcggcgatataggcgccagcaaccgcacctgtggcgccggtgatgccggccacgatgcgtccggcgtag
aggatcgagatctcgatcccgcgaaattaatacgactcactataggggaattgtgagcggataacaattc
ccctctagaaataattttgtttaactttaagaaggagatatacatatgaaatacctattgcctacggcag
ccgctggattgttattactcgcggcccagccggccatggcccaggtgcagctgcaggagtttgggggagg
attggtgcaggctgggggctctctgagactctcctgtgcagcctctggacgcaccttcagtaggtatgcc
atgggctggttccgccaggctccagggaaggagcgtgagtttgtagcagctattacctgggatggtggta
gcacatactatgcagactccgtgaagggccgattcaccatctccagagacaacgccaagaacacggtgta
tctgcaaatgaacagcctgaaacctgaggacacggccgtttattactgtgcagcagggggaaaccactac
tatagtggtaattactacttgtgggatgagtatgactactggggccaggggacccaggtcaccgtctcct
caggtagcggtagtggtgtcgaccatcatcaccatcatcatggtagcggatccggtctgaatgatatttt
tgaagcccagaaaatcgaatggcacgaataatagtctcgagcaccaccaccaccaccactgagatccggc
tgctaacaaagcccgaaaggaagctgagttggctgctgccaccgctgagcaataactagcataacccctt
ggggcctctaaacgggtcttgaggggttttttgctgaaaggaggaactatatccggat</INSDSeq_se
quence>
</INSDSeq>
</SequenceData>
<SequenceData sequenceIDNumber="2">
<INSDSeq>
<INSDSeq_length>134</INSDSeq_length>
<INSDSeq_moltype>AA</INSDSeq_moltype>
<INSDSeq_division>PAT</INSDSeq_division>
<INSDSeq_feature-table>
<INSDFeature>
<INSDFeature_key>source</INSDFeature_key>
<INSDFeature_location>1..134</INSDFeature_location>
<INSDFeature_quals>
<INSDQualifier>
<INSDQualifier_name>mol_type</INSDQualifier_name>
<INSDQualifier_value>protein</INSDQualifier_value>
</INSDQualifier>
<INSDQualifier id="q4">
<INSDQualifier_name>organism</INSDQualifier_name>
<INSDQualifier_value>synthetic construct</INSDQualifier_value>
</INSDQualifier>
</INSDFeature_quals>
</INSDFeature>
</INSDSeq_feature-table>
<INSDSeq_sequence>QVQLQEFGGGLVQAGGSLRLSCAASGRTFSRYAMGWFRQAPGKEREFVA
AITWDGGSTYYADSVKGRFTISRDNAKNTVYLQMNSLKPEDTAVYYCAAGGNHYYSCNYYLWDEYDYWGQ
GTQVTVSSGSGSGVD</INSDSeq_sequence>
</INSDSeq>
</SequenceData>
</ST26SequenceListing>
<---




Изобретение относится к биотехнологии. Создана плазмидная генетическая конструкция pET21a_SKP, обеспечивающая экспрессию однодоменного антитела против SARS-CoV-2 в прокариотической системе E. coli, имеющая размер 5917 п.н. и нуклеотидную последовательность SEQ ID NO: 1. Получен рекомбинантный белок SKP, экспрессируемый в прокариотической системе E. coli плазмидной генетической конструкцией pET21a_SKP по п. 1, обладающий широконейтрализующими свойствами однодоменного наноантитела против SARS-CoV-2, имеющий молекулярную массу 23 кДа и аминокислотную последовательность SEQ ID NO: 2. Техническим результатом группы изобретений является расширение арсенала однодоменных наноантител для диагностики вируса SARS-CoV-2, а также получение широконейтрализующих антител с высоким и стабильным экспрессионным выходом. 2 н.п. ф-лы, 5 ил., 1 табл., 5 пр.
1. Плазмидная генетическая конструкция pET21a_SKP, обеспечивающая экспрессию однодоменного антитела против SARS-CoV-2 в прокариотической системе E. coli, имеющая нуклеотидную последовательность SEQ ID NO: 1, размер 5917 п.н., и содержащая в соответствии с физической и генетической картой следующие элементы:
- ген fl ori начала репликации бактериофага, имеющий координаты с 12 по 467 п.н.;
- ген AmpR, кодирующий бета-лактамазу, используемый в качестве генетического маркера, определяющего устойчивость к ампициллину клеток бактерии E. coli, трансформированных рекомбинантной плазмидой pET21a_SKP, и имеющий координаты с 599 по 1459 п.н.;
- участок начала репликации ori, имеющий координаты с 1630 по 2218 п.н.;
- ген белка репрессора lacI, имеющий координаты с 3648 п.н. по 4730 п.н. и являющийся ДНК-связывающим белком, который ингибирует экспрессию генов E. coli и обеспечивает экспрессию целевого рекомбинантного белка VHH после добавления индуктора изопропил-β-D-1-тиогалактопиранозида (IPTG);
- промотор фага Т7, имеющий координаты с 5117 по 5135 п.н. и обеспечивающий экспрессию последовательности гена SKP в прокариотических клетках E. coli;
- RBS - сайт посадки рибосомы, имеющий координаты с 5175 по 5197 п.н.;
- последовательность, кодирующая лидерный пептид pelB и имеющая координаты с 5205 по 5270 п.н. - последовательность в составе белка, которая обеспечивает экспорт последнего из клетки;
- ген SKP, кодирующий однодоменное антитело против SARS-CoV-2 и имеющий координаты с 5271 по 5672 п.н.;
- 6×His для очистки антитела против SARS-CoV-2, имеющий координаты с 5673 по 5690 п.н.;
- пептидная метка AviTag, обеспечивающая ферментативное биотинилирование и имеющая координаты с 5703 по 5747 п.н.;
- Т7 terminator - область терминатора транскрипции бактериофага Т7, имеющий координаты с 5845 по 5892 п.н.
2. Рекомбинантный белок SKP, экспрессируемый в прокариотической системе E. coli плазмидной генетической конструкцией pET21a_SKP по п. 1, обладающий широконейтрализующими свойствами однодоменного наноантитела против SARS-CoV-2, имеющий молекулярную массу 23 кДа и аминокислотную последовательность SEQ ID NO: 2.
| СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИММУНОГЛОБУЛИНА IGA2m1-ИЗОТИПА В КЛЕТКАХ МЛЕКОПИТАЮЩИХ | 2022 |
|
RU2801178C1 |
| Широко нейтрализующее антитело против SARS-CoV-2 | 2022 |
|
RU2810476C1 |
| US 20210347858 A1, 11.11.2021. | |||
Авторы
Даты
2025-04-30—Публикация
2024-09-24—Подача