ПРИТЯЗАНИЕ НА ПРИОРИТЕТ
Настоящая заявка испрашивает приоритет на основании заявки на патент США с серийным № 62/824190, поданный 26 марта 2019 г., содержание которой включено в данный документ посредством ссылки во всей своей полноте.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит перечень последовательностей, который был подан в электронном виде в формате ASCII и настоящим включен посредством ссылки во всей своей полноте. Указанная ASCII-копия, созданная 11 августа 2021 года, имеет название PAT058487_SL.txt и размер 785 байт.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к C16-производным рапамицина, которые являются ингибиторами mTORC1.
УРОВЕНЬ ТЕХНИКИ
В клетках млекопитающих киназа "мишень рапамицина" (mTOR) существует в виде двух различных мультибелковых комплексов, описанных как комплекс mTORC1 и комплекс mTORC2, оба из которых воспринимают сигналы доступности питательных веществ и энергии, и интегрируют входящие сигналы от факторов роста и сигнального пути стресса. mTORC1 интегрирует сигналы от факторов роста и питательных веществ и контролирует клеточный рост и метаболизм (Laplante M. et al. Cell. (2012) 149(2):274-93). mTORC1 представляет собой ключевой регулятор трансляции белка и аутофагии. mTORC1 является чувствительным к аллостерическим ингибиторам mTOR, таким как рапамицин и аналоги рапамицина (так называемые ‘рапалоги'). Механизм действия рапамицина и полученных ранее рапалогов предусматривает образование внутриклеточного комплекса с FK50-связывающими белками, такими как FKBP12, FKBP12.6, FKBP13, FKBP25, FKBP51 или FKBP52 (данные FKBP будут обозначаться в данном документе как "FKBP" или "виды FKBP"), с последующим связыванием комплекса FKBP-рапалог с доменом FRB (FK506-рапамицин-связывающим) mTOR. См. März A.M. et al. Mol Cell Biol. (2013) 33(7):1357-1367. Такое взаимодействие комплекса FKBP-рапалог с mTORC1 приводит к аллостерическому ингибированию mTORC1. Рапамицин и рапалоги, такие как RAD001 (эверолимус, Afinitor®), получили клиническое значение за ингибирование активности mTORC1, который ассоциирован с пролиферативными нарушениями, приводящими как к доброкачественным, так и злокачественным новообразованиям. См. Royce M.E. et al. Breast Cancer (Auckl). (2015) 9:73-79; Pleniceanu O. et al. Kidney Int Rep. (2018) 3(1):155-159, и различные другие показания.
Рапамицин представляет собой известный макролидный антибиотик, продуцируемый Streptomyces hygoscopius, см. например, McAlpine, J.B., et al., J. Antibiotics (1991) 44:688; Schreiber, S.L.; et al., J. Am. Chem. Soc. (1991) 113:7433; патент США № 3929992. Следующее правило нумерации атомов рапамицина и его производных, применяемое в данном документе, показано ниже.
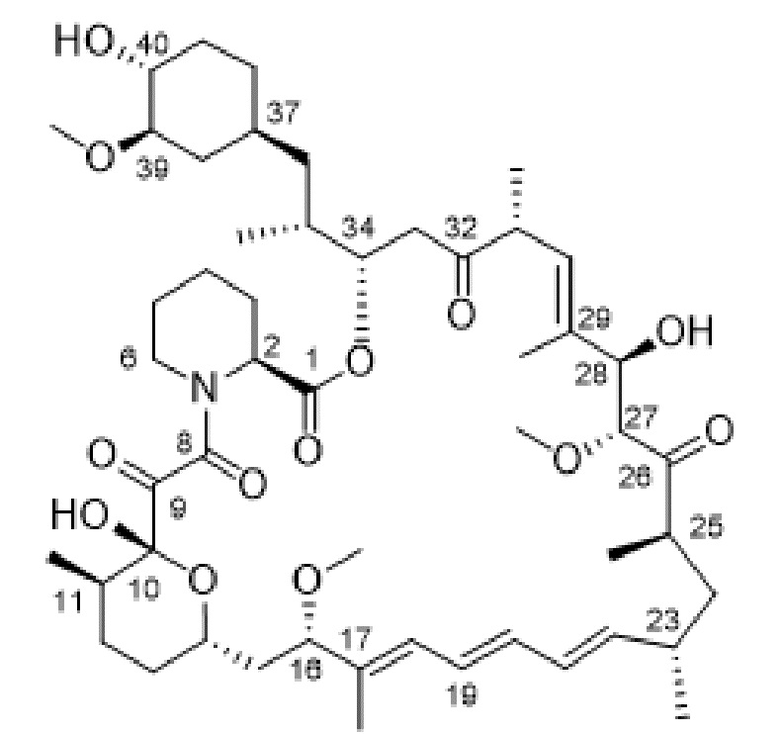
Рапамицин является эффективным иммуносупрессором, и также было показано, что он характеризуется противоопухолевой и противогрибковой активностью. Как было показано, он применим в предупреждении или лечении системной красной волчанки, воспаления легких, инсулинозависимого сахарного диабета, кожных болезней, таких как псориаз, пролиферации гладкомышечных клеток и утолщения интимы после повреждения сосудов, T-клеточного лейкоза/лимфомы у взрослых, злокачественных карцином, воспалительного заболевания сердца, анемии и повышенного разрастания аксонов. Однако его применимость в качестве фармацевтического средства ограничена его крайне низкой и изменчивой биодоступностью. Более того, рапамицин трудно составлять, что делает сложным получение устойчивых натуральных композиций.
На животных моделях рапамицин и рапалоги увеличивают продолжительность жизни и/или задерживают появление возрастных заболеваний. Старение, подобно другим биологическим процессам, контролируется сигнальными путями, такими как путь TOR (в данном случае называемый "TOR", чтобы охватить системы дрожжей C. elegans) и путь mTORC1 у млекопитающих. Модуляция передачи сигнала через TOR и mTORC1 увеличивает продолжительность жизни и задерживает появление возрастных заболеваний у широкого круга организмов, от мух до млекопитающих. Например, ингибирование пути TOR за счет генетической мутации увеличивает продолжительность жизни у дрожжей, C. elegans и дрозофилы, а ингибирование пути mTORC1 увеличивало продолжительность жизни у мышей (Kaeberlein et al., Science (2005) 310:1193-1196; Kapahi et al., Curr Biol (2004) 14:885-890; Selman et al., Science (2009) 326:140-144; Vellai et al., Nature (2003) 426:620; R. A. Miller et al. Aging Cell. (2014) 13(3): 468-477). Кроме того, ингибитор mTORC1 рапамицин увеличивал продолжительность жизни у мышей даже при введении на поздних стадиях жизни (Harrison et al., Nature (2009) 460(7253):392-395). Эти данные указывают на возможность того, что лекарственные средства, которые нацеливаются на путь TOR у млекопитающих (mTOR), будут оказывать терапевтическое воздействие на старение и возрастные заболевания у людей. Отчет о клиническом испытании с применением рапамицина у мужчин преклонного возраста был описан M. Leslie в Science, 2013, 342. J. Mannick et al. описывает в Sci Transl Med. (2014) 6(268): 268ra179, что ингибирование mTORC1 улучшает иммунную функцию у людей преклонного возраста. Однако исследователи с настороженно отнеслись к применению доступных в настоящее время ингибиторов mTORC1 в испытаниях касательно старения людей вследствие их побочных эффектов (включающих иммуносупрессию, виды цитопении, стоматит, желудочно-кишечное расстройство и интерстициальный пневмонит).
Фармакологическое ингибирование пути mTORC1 либо до возникновения неврологических повреждений, либо непосредственно после них, может предотвращать патологические изменения в головном мозге животных и развитие спонтанных периодических эпилептических припадков на модели приобретенной эпилепсии (Zeng et al., The mammalian target of rapamycin signaling pathway mediates epileptogenesis in a model of temporal lobe epilepsy; J. Neurosci., (2009) pp. 6964-6972). Следовательно, считается, что рапамицин и рапалоги также имеют потенциальную ценность при таких показаниях.
Было показано, что рапалоги в малых дозах являются эффективными у человека в ситуации фиброза печени и почек.
Митохондриальная миопатия (MM) является наиболее распространенным проявлением приобретенного митохондриального заболевания и демонстрирует многостороннюю тканеспецифическую реакцию на стресс: (1) транскрипционную реакцию, включающую метаболические цитокины FGF21 и GDF15; (2) ремоделирование одноуглеродного метаболизма и (3) реакцию несвернутых митохондриальных белков. Khan et al. описывают в Cell Metabolism 26, 419-428, 1 августа 2017 г., что данные процессы являются частью одной интегрированной митохондриальной реакции на стресс (ISRmt), которая контролируется с помощью mTORC1 в скелетной мышце. Дефект репликации mtDNA активирует mTORC1, который запускает интегрированную митохондриальную реакцию на стресс путем активации ATF4 с индуцированием de novo синтеза нуклеотидов и серина, 1C-цикла и продуцирования FGF21 и GDF15. Ингибирование mTORC1 рапамицином снижало экспрессию всех компонентов ISRmt (интегрированной митохондриальной реакции на стресс), улучшало все клинические признаки MM и обращало прогрессирование MM даже на поздней стадии, без индуцирования биогенеза митохондрий. Следовательно, считается, что рапамицин и рапалоги также имеют потенциальную ценность при таких показаниях.
Таким образом, остается потребность в обеспечении новых ингибиторов mTORC1, которые являются улучшенными лекарственными средствами-кандидатами, проявляющими баланс между надлежащей активностью, стабильностью и биодоступностью.
КРАТКОЕ ОПИСАНИЕ
Соединения формулы (I) представляют собой ингибиторы mTORC1 и применимы в лечении нарушений, в частности возрастных нарушений, или заболеваний и нарушений, для лечения которых в настоящее время одобрено применение рапамицина или любого из рапалогов. Замена метоксигруппы при C16, описанная в данном документе, обеспечивает соединения, проявляющие баланс между надлежащей активностью, стабильностью и биодоступностью. Соединения формулы (I) являются эффективными в ингибировании mTORC1 за счет селективного связывания с FKBP12 в ситуациях, при которых уровни FKBP12 являются достаточными для ингибирования mTORC1.
В одном аспекте в настоящем изобретении предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль, где:
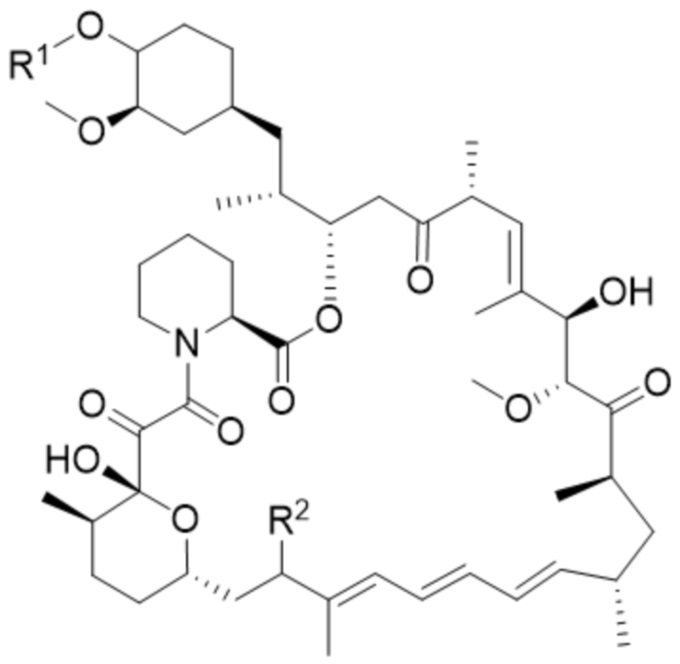 (I),
(I),
R1 выбран из группы, состоящей из водорода, C1-6алкила, гидроксил-C1-6алкила и гетеро-C1-6алкила; и
R2 представляет собой 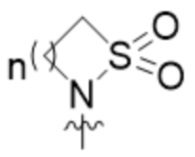 , где n составляет 1, 2 или 3.
, где n составляет 1, 2 или 3.
В одном варианте осуществления в настоящем изобретении предусмотрена фармацевтическая композиция, содержащая терапевтически эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли и один или несколько фармацевтически приемлемых носителей.
В одном варианте осуществления в настоящем изобретении предусмотрена фармацевтическая комбинация, содержащая терапевтически эффективное количество соединения формулы (I) или его фармацевтически приемлемой соли и одно или несколько терапевтически активных средств.
В другом аспекте в настоящем изобретении предусмотрен способ лечения нарушения или заболевания, опосредованного путем mTOR, у субъекта, нуждающегося в этом, при этом способ предусматривает введение субъекту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
В другом аспекте в настоящем изобретении предусмотрен способ лечения заболевания или нарушения у субъекта, где ткань-мишень, орган-мишень или клетки-мишени, ассоциированные с патологическим процессом, приводящим к заболеванию или нарушению, характеризуются уровнями FKBP12, достаточными для ингибирования mTORC1, при этом способ предусматривает введение субъекту, нуждающемуся в этом, терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
В другом аспекте в настоящем изобретении предусмотрен способ лечения заболевания или нарушения у субъекта, который характеризуется уровнями FKBP12, достаточными для ингибирования mTORC1, или субъекта, в отношении которого было установлено, что он характеризуется такими уровнями, при этом способ предусматривает введение субъекту, нуждающемуся в этом, терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
В другом аспекте в настоящем изобретении предусмотрен способ лечения возрастного заболевания или нарушения у субъекта, нуждающегося в этом, при этом способ предусматривает введение субъекту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
В одном варианте осуществления возрастное заболевание или нарушение выбрано из саркопении, атрофии кожи, видов старческой гемангиомы, видов себорейного кератоза, атрофии головного мозга (также называемой деменцией), атеросклероза, артериосклероза, эмфиземы легких, остеопороза, остеоартрита, высокого кровяного давления, видов катаракты, макулярной дегенерации, глаукомы, инсульта, нарушения мозгового кровообращения (видов инсульта), хронического заболевания почек, ассоциированного с диабетом заболевания почек, нарушения функции печени, фиброза печени, аутоиммунного гепатита, гиперплазии эндометрия, метаболической дисфункции, реноваскулярного заболевания, тугоухости, нарушения способности к передвижению (например, старческой астении), снижения когнитивной функции, ригидности сухожилий, дисфункции сердца, такой как гипертрофия сердца, и/или систолическая и/или диастолическая дисфункция, и/или гипертензия, и/или дилятационная кардиомиопатия, дисфункции сердца, которая приводит к снижению фракции выброса, иммунного старения, болезни Паркинсона, болезни Альцгеймера, рака, иммунного старения, приводящего к раку вследствие снижения иммунного надзора, инфекций, обусловленных снижением иммунной функции, хронической обструктивной болезни легких (COPD), ожирения, потери вкуса, потери обоняния, артрита и диабета II типа (в том числе осложнений, возникших в результате диабета, таких как почечная недостаточность, слепота и нейропатия).
В другом аспекте в настоящем изобретении предусмотрен способ лечения заболевания или нарушения у субъекта, нуждающегося в этом, при этом способ предусматривает введение субъекту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, где заболевание или нарушение выбрано из:
- видов васкулопатии трансплантата;
- пролиферации и миграции гладкомышечных клеток, приводящих к утолщению интимы сосудов, закупорке кровеносных сосудов, обструктивному коронарному атеросклерозу, рестенозу;
- аутоиммунных заболеваний и воспалительных состояний;
- астмы;
- заболеваний, ассоциированных со множественной лекарственной резистентностью (MDR);
- грибковых инфекций;
- воспаления;
- инфекции;
- возрастных заболеваний;
- нейродегенеративных заболеваний;
- пролиферативных нарушений, например рака;
- эпилептических припадков и связанных с эпилептическими припадками нарушений и
- митохондриальной миопатии и митохондриального стресса.
В другом аспекте в настоящем изобретении предусмотрен способ лечения рака у субъекта, нуждающегося в этом, при этом способ предусматривает введение субъекту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
В одном варианте осуществления способ дополнительно предусматривает применение ингибитора PD-1/PDL-1.
В одном варианте осуществления рак выбран из рака почки, почечно-клеточной карциномы, колоректального рака, саркомы матки, рака эндометрия матки, рака эндометрия, рака молочной железы, рака яичника, рака шейки матки, рака желудка, фибросаркомы, рака поджелудочной железы, рака печени, меланомы, лейкоза, множественной миеломы, рака носоглотки, рака предстательной железы, рака легкого, глиобластомы, астроцитомы, аденокарциномы, рака мочевого пузыря, мезотелиомы, рака головы, рабдомиосаркомы, саркомы, лимфомы и рака шеи.
В одном варианте осуществления нарушение представляет собой нарушение со стороны печени, которое включает процесс фиброза и/или воспаления, например фиброз печени, который возникает на терминальной стадии заболевания печени; цирроз печени; печеночную недостаточность, обусловленную токсичностью; неалкогольный стеатогепатит или NASH и алкогольный стеатоз.
В одном варианте осуществления нарушение представляет собой нарушение со стороны почек, которое включает процесс фиброза или воспаления в почке, например, фиброз почек или гломерулосклероз, который возникает в результате острого повреждения почек, приводящего к хроническому заболеванию почек. В одном варианте осуществления нарушение со стороны почек представляет собой хроническое заболевание почек, возникающее в ситуации диабетической нефропатии. В одном варианте осуществления хроническое заболевание почек приводит к почечной недостаточности.
В одном варианте осуществления нарушение представляет собой дисфункцию сердца, например инфаркт миокарда или гипертрофию сердца. В одном варианте осуществления дисфункция сердца представляет собой систолическую и/или диастолическую дисфункцию. В одном варианте осуществления дисфункция сердца представляет собой гипертензию. В одном варианте осуществления дисфункция сердца приводит к снижению фракции выброса. В одном варианте осуществления дисфункция сердца может характеризоваться сохраненной фракцией выброса. В одном варианте осуществления дисфункция сердца приводит к дилятационной кардиомиопатии.
В одном варианте осуществления нарушение представляет собой иммунное старение, приводящее к раку вследствие снижения иммунного надзора.
В одном варианте осуществления нарушение представляет собой рак, включающий опухоли, которые подвергают лечению посредством иммунотерапии. В одном варианте осуществления субъекта ранее подвергали лечению посредством одного из рапамицина, RAD001 или другого рапалога. В одном варианте осуществления рак включает опухоли, для которых показано, что путь mTOR является активированным, в том числе ситуации, при которых имеется мутация в гене Tsc1 или при которых микроокружение опухоли надлежащим образом подвергается лечению рапалогом.
Подробности одного или нескольких вариантов осуществления настоящего изобретения изложены в данном документе. Другие признаки, цели и преимущества настоящего изобретения будут очевидны из фигур, подробного описания, примеров и формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На фиг. 1A и 1B изображены линейные графики, показывающие снижение уровня S6K1(Thr389) в клетках 293T дикого типа (фиг. 1A) и с нокаутом по FKBP12 (фиг. 1B) после обработки соединением 1 (сплошная линия) и RAD001 (пунктирная линия). Клетки обрабатывали в трех повторностях. На оси Y представлен процент снижения уровня pS6K1(Thr389) относительно уровня в клетках, обработанных средами без рапалога (среды с добавлением DMSO). На оси X представлены концентрации соединения 1 и RAD001.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
Если не указано иное, термин "соединения по настоящему изобретению" или "соединение по настоящему изобретению" относится к соединениям формулы (I) и иллюстративным соединениям и их солям, а также ко всем стереоизомерам (в том числе диастереоизомерам и энантиомерам), ротамерам, таутомерам и меченным изотопом соединениям (включая замещения дейтерием), а также образованным природным путем фрагментам.
Термин "терапевтически эффективное количество" соединения по настоящему изобретению относится к количеству соединения по настоящему изобретению, которое будет вызывать биологический или медицинский ответ у субъекта, например, снижение или подавление активности фермента или белка, или уменьшение тяжести симптомов, облегчение состояний, замедление или задержку прогрессирования заболевания или предупреждение заболевания и т. д. В одном варианте осуществления термин "терапевтически эффективное количество" относится к количеству соединения по настоящему изобретению, которое при введении субъекту является эффективным для (1) по меньшей мере частичного облегчения или снижения тяжести состояния, или нарушения, или заболевания, (i) опосредованных путем mTOR, или (ii) ассоциированных с активностью mTOR, или (iii) характеризующихся активностью (нормальной или аномальной) mTOR; или (2) снижения или подавления активности mTOR; или (3) снижения или подавления экспрессии mTOR. В одном варианте осуществления термин "терапевтически эффективное количество" относится к количеству соединения по настоящему изобретению, которое при введении в клетку, или ткань, или неклеточный биологический материал, или среду является эффективным для по меньшей мере частичного снижения или подавления активности mTOR или по меньшей мере частичного снижения или подавления экспрессии mTOR.
Применяемый в данном документе термин "субъект" относится к приматам (например, людям, мужчинам или женщинам), собакам, кошкам, кроликам, морским свинкам, свиньям, крысам и мышам. В определенных вариантах осуществления субъектом является примат. В других вариантах осуществления субъектом является человек.
Применяемые в данном документе термины "вводить", "осуществление введения" или "введение" относятся к имплантации, всасыванию, приему внутрь, осуществлению инъекции, ингаляции или иному введению соединения по настоящему изобретению или фармацевтической композиции на его основе.
Применяемый в данном документе термин "подавлять", "подавление" или "осуществление подавления" относятся к снижению или ослаблению данного состояния, симптома или нарушения, или заболевания, или значительному снижению исходного уровня активности в отношении биологической активности или процесса.
Применяемый в данном документе термин "лечить", "осуществление лечения" или "лечение" любого заболевания или нарушения относится к облегчению, задержке наступления, снижению тяжести заболевания или нарушения (т. е. замедлению или остановке развития заболевания или по меньшей мере одного из его клинических симптомов) или снижению или уменьшению по меньшей мере одного физического параметра или биомаркера, ассоциированных с заболеванием или нарушением, в том числе таких, которые могут не ощущаться пациентом. В одном варианте осуществления "лечение", "лечить" или "осуществление лечения" предусматривают, что признаки или симптомы заболевания, нарушения или состояния уже развились или наблюдаются. В других вариантах осуществления лечения может применяться в отсутствие признаков или симптомов заболевания или состояния. Например, лечение может применяться в отношении предрасположенного индивидуума до появления симптомов (например, с учетом симптомов в анамнезе и/или с учетом генетических факторов или других факторов предрасположенности). Лечение также может быть продолжено после устранения симптомов, например, для задержки наступления или предупреждения рецидива.
Применяемый в данном документе термин "предупреждать", "осуществление предупреждения" или "предупреждение" любого заболевания или нарушения относится к профилактическому лечению заболевания или нарушения; или задержке возникновения или прогрессирования заболевания или нарушения.
Применяемое в данном документе "возрастное заболевание или нарушение" относится к любому заболеванию или нарушению, у которых частота возникновения в популяция или тяжесть протекания у индивидуума коррелируют увеличением возраста. Более конкретно возрастное заболевание или нарушение представляет собой заболевание или нарушение, частота возникновения которого у людей старше 65 лет по меньшей мере в 1,5 раза превышает таковую у людей в возрасте 25-35 лет. Примеры возрастных нарушений включают без ограничения саркопению, атрофию кожи, виды старческой гемангиомы, виды себорейного кератоза, атрофию головного мозга (также называемую деменцией), атеросклероз, артериосклероз, эмфизему легких, остеопороз, остеоартрит, высокое кровяное давление, виды катаракты, макулярную дегенерацию, глаукому, инсульт, нарушение мозгового кровообращения (виды инсульта), хроническое заболевание почек, ассоциированное с диабетом заболевание почек, нарушение функции печени, фиброз печени, аутоиммунный гепатит, гиперплазию эндометрия, метаболическую дисфункцию, реноваскулярное заболевание, тугоухость, нарушение способности к передвижению (например, старческую астению), снижение когнитивной функции, ригидность сухожилий, дисфункцию сердца, такую как гипертрофия сердца, систолическая или диастолическая дисфункция, гипертензия, дилятационная кардиомиопатия, дисфункцию сердца, которая приводит к снижению фракции выброса, иммунное старение, болезнь Паркинсона, болезнь Альцгеймера, рак, иммунное старение, приводящее к раку вследствие снижения иммунного надзора, инфекций, обусловленных снижением иммунной функции, хроническую обструктивную болезнь легких (COPD), ожирение, потерю вкуса, потерю обоняния, артрит и диабета II типа (в том числе осложнения, возникшие в результате диабета, такие как почечная недостаточность, слепота и нейропатия).
Применяемый в данном документе субъект является "нуждающимся" в лечении, если в результате такого лечения такой субъект получит пользу с биологической, медицинской точки зрения или улучшится качество его жизни.
Применяемые в данном документе термины в форме единственного числа и подобные термины, используемые в контексте настоящего изобретения (в частности, в контексте формулы изобретения), следует истолковывать как охватывающие как форму единственного числа, так и форму множественного числа, если в данном документе не указано иное, или это явно не противоречит контексту.
Термин "алкил" относится к радикалу насыщенный углеводородной группы с прямой или разветвленной цепью, содержащему от 1 до 6 атомов углерода ("C1-6алкил"). В некоторых вариантах осуществления алкильная группа содержит 1-5 атомов углерода ("C1-5алкил"). В некоторых вариантах осуществления алкильная группа содержит 1-4 атомов углерода ("C1-4алкил"). В некоторых вариантах осуществления, алкильная группа содержит 1-3 атома углерода ("C1-3алкил"). В некоторых вариантах осуществления, алкильная группа содержит 1-2 атома углерода ("C1-2алкил"). В некоторых вариантах осуществления алкильная группа содержит 1 атом углерода ("C1алкил"). В некоторых вариантах осуществления алкильная группа содержит 2-6 атомов углерода ("C2-6алкил"). Примеры C1-6алкильных групп включают метил (C1), этил (C2), пропил (C3) , (например, н-пропил, изопропил), бутил (C4), ( например, н-бутил, трет-бутил, втор-бутил, изобутил), пентил (C5) ( например, н-пентил, 3-пентанил, амил, неопентил, 3-метил-2-бутанил, третичный амил) и гексил (C6) ( например, н-гексил).
"Гетероалкил" относится к алкильной группе, который дополнительный содержит по меньшей мере один гетероатом (например, 1, 2, 3 или 4 гетероатома), выбранный из кислорода, азота или серы, в пределах (т. е. вставленный между смежными атомами углерода) основной цепи и/или помещенный в одно или несколько ее концевых положений. В некоторых вариантах осуществления гетероалкильная группа представляет собой насыщенную группу, содержащую 1-6 атомов углерода и 1 или несколько гетероатомов в пределах основной цепи ("гетеро-C1-6алкил"). В некоторых вариантах осуществления гетероалкильная группа представляет собой насыщенную группу, содержащую 1-5 атомов углерода и 1 или 2 гетероатома в пределах основной цепи ("гетеро-C1-5алкил"). В некоторых вариантах осуществления гетероалкильная группа представляет собой насыщенную группу, содержащую 1-4 атома углерода и 1 или 2 гетероатома в пределах основной цепи ("гетеро-C1-4алкил"). В некоторых вариантах осуществления гетероалкильная группа представляет собой насыщенную группу, содержащую 1-3 атома углерода и 1 гетероатом в пределах основной цепи ("гетеро-C1-3алкил"). В некоторых вариантах осуществления гетероалкильная группа представляет собой насыщенную группу, содержащую 1-2 атома углерода и 1 гетероатом в пределах основной цепи ("гетеро-C1-2алкил"). В некоторых вариантах осуществления гетероалкильная группа представляет собой насыщенную группу, содержащую 1 атом углерода и 1 гетероатом ("гетеро-C1алкил"). В некоторых вариантах осуществления гетероалкильная группа представляет собой насыщенную группу, содержащую 2-6 атомов углерода и 1 или 2 гетероатома в пределах основной цепи ("гетеро-C2-6алкил").
"Гидрокси-C1-6алкил" относится к алкильной группе, замещенной одной или несколькими -OH группами. Примеры гидрокси-C1-6алкильных групп включают HO-CH2-, HO-CH2CH2- и -CH2-CH(OH)CH3.
"Гидрокси" или "гидроксил" относится к -OH.
"Галогено" или "галоген" относятся к фтору (фтор, -F), хлору (хлор, -Cl), брому (бром, -Br) или йоду (йод, -I). В одном варианте осуществления, галоген относится к фтору, хлору или брому.
Применяемое в данном документе определение каждого выражения, например, алкил, m, n и т. д., если
оно встречается более одного раза в какой-либо структуре, предусматривается как независимое от его определения
где-либо еще в той же структуре.
Определения конкретных функциональных групп и химических терминов описаны более подробно ниже. Химические элементы определены в соответствии с Периодической таблицей элементов, CAS-версия, Handbook of Chemistry and Physics, 75-ое изд., форзац, и конкретные функциональные группы обычно указаны, как описано там же. Кроме того, общие принципы органической химии, а также конкретные функциональные фрагменты и реакционноспособные группы описаны в Thomas Sorrell, Organic Chemistry, University Science Books, Sausalito, 1999; Smith and March, March's Advanced Organic Chemistry, 5th Edition, John Wiley & Sons, Inc., New York, 2001; Larock, Comprehensive Organic Transformations, VCH Publishers, Inc., New York, 1989; и Carruthers, Some Modern Methods of Organic Synthesis, 3rd Edition, Cambridge University Press, Cambridge, 1987.
Определенные соединения по настоящему изобретению могут существовать в конкретных геометрических или стереоизомерных формах. Если, например, требуется конкретный энантиомер соединения по настоящему изобретению, его можно получать путем асимметрического синтеза, либо путем дериватизации с помощью хирального вспомогательного вещества, где полученную смесь диастереомеров разделяют и вспомогательную группу отщепляют с получением чистых требуемых энантиомеров. В качестве альтернативы, если молекула содержит основную функциональную группу, такую как амино, или кислотную функциональную группу, такую как карбоксил, то получают диастереомерные соли с соответствующей оптически активной кислотой или основанием, а затем полученные таким образом диастереомеры разделяют с помощью фракционной кристаллизации или хроматографических методов, широко известных в данной области техники, и впоследствии выделяют чистые энантиомеры.
Если не указано иное, то подразумевается, что структуры, изображенные в данном документе, также включают геометрические (или конформационные) формы данной структуры, например, R- и S-конфигурации для каждого центра асимметрии, Z- и E-изомеры для двойной связи и конформационные Z- и E-изомеры. Следовательно, в объем настоящего изобретения входят отдельные стереохимические изомеры, а также смеси из энантиомеров, диастереомеров и геометрических (или конформационных) изомеров раскрытых соединений. Если не указано иное, то в объем настоящего изобретения входят все таутомерные формы соединений по настоящему изобретению. Кроме того, если не указано иное, также подразумевается, что структуры, изображенные в данном документе, включают соединения, которые отличаются только присутствием одного или нескольких изотопно-обогащенных атомов. Например, в объем настоящего изобретения входят соединения со структурами, раскрытыми в данном документе, включающие замену водорода на дейтерий или тритий или замену углерода на углерод, обогащенный 13C или 14C. Такие соединения применимы, например, в качестве аналитических инструментов, в качестве зондов в биологических анализах или в качестве терапевтических средств в соответствии с настоящим изобретением.
"Энантиомерный избыток" или "% энантиомерного избытка" композиции может быть рассчитан с применением приведенного ниже уравнения. В приведенном ниже примере композиция содержит 90% одного энантиомера, например, S-энантиомера, и 10% другого энантиомера, т. е., R-энантиомера.
э.и.=(90-10)/100 * 100=80%.
Таким образом, композиция, содержащая 90% одного энантиомера и 10% другого
энантиомера, как считается, характеризуется энантиомерным избытком, составляющим 80%. Соединения или композиции, описанные в данном документе, могут характеризоваться энантиомерным избытком одной формы соединения, например, S-энантиомера, составляющим по меньшей мере 50%, 75%, 90%, 95% или 99%. Другими словами, такие соединения или композиции характеризуются энантиомерным избытком S-энантиомера относительно R-энантиомера.
Если предпочтителен конкретный энантиомер, то в некоторых вариантах осуществления его можно получать по сути свободным от соответствующего энантиомера, и он может также называться "оптически обогащенным". Применяемый в данном документе "оптически обогащенный" означает, что в состав соединения входит значительно большая доля одного энантиомера. В определенных вариантах осуществления в состав соединения входит по меньшей мере приблизительно 90% по весу предпочтительного энантиомера. В других вариантах осуществления в состав соединения входит по меньшей мере приблизительно 95%, 98% или 99% по весу предпочтительного энантиомера. Предпочтительные энантиомеры можно выделять из рацемических смесей с помощью любого способа, известного специалистам в данной области техники, в том числе хиральной жидкостной хроматографии высокого давления (HPLC), а также образования и кристаллизации хиральных солей, или получать с помощью асимметрического синтеза. См., например, Jacques et al., Enantiomers, Racemates and Resolutions (Wiley Interscience, New York, 1981); Wilen, et al., Tetrahedron 33:2725 (1977); Eliel, E.L. Stereochemistry of Carbon Compounds (McGraw-Hill, NY, 1962); Wilen, S.H. Tables of Resolving Agents and Optical Resolutions с. 268 (E.L. Eliel, Ed., Univ. of Notre Dame Press, Notre Dame, IN 1972).
Все способы, описанные в данном документе, можно осуществлять в любом подходящем порядке, если иное не указано в данном документе, или это иным образом явно не противоречит контексту. Представленное в данном документе применение всех возможных примеров или вводных слов перед примерном (например, "такой как") предназначено исключительно для лучшего освещения настоящего изобретения и не предполагает ограничения объема настоящего изобретения, заявленного далее.
Любые полученные смеси изомеров можно разделять на основе физико-химических отличий их составляющих на чистые или по сути чистые геометрические или оптические изомеры, диастереомеры, рацематы, например, с помощью хроматографии и/или фракционной кристаллизации.
Любые полученные рацематы конечных продуктов или промежуточных соединений можно разделять на оптические антиподы с помощью известных способов, например, путем разделения их диастереомерных солей, полученных с помощь оптически активной кислоты или основания, и высвобождения оптически активного кислотного или основного соединения. В частности, основный фрагмент можно использовать таким образом для разделения соединений по настоящему изобретению на их оптические антиподы, например, путем фракционной кристаллизации соли, образованной с оптически активной кислотой, например, винной кислотой, дибензоилвинной кислотой, диацетилвинной кислотой, ди-O,O'-п-толуоилвинной кислотой, миндальной кислотой, яблочной кислотой или камфор-10-сульфоновой кислотой. Рацемические продукты также можно разделять с помощью хиральной хроматографии, например, жидкостной хроматографии высокого давления (HPLC) с применением хирального адсорбента.
Соединения, раскрытые в данном документе, могут также характеризоваться не встречающимися в природе соотношениями изотопов атомов по одному или нескольким атомам, которые образуют такие соединения. Например, соединения могут быть помечены радиоактивной меткой с помощью радиоактивных изотопов, таких как, например, дейтерий (2H), тритий (3H), углерод-13 (13C) или углерод-14 (14C). Подразумевается, что все изотопные варианты соединений, раскрытых в данном документе, независимо от того, являются ли они радиоактивными или нет, находятся в пределах объема настоящего изобретения. Кроме того, предполагается, что все таутомерные формы соединений, описанных в данном документе, находятся в пределах объема настоящего изобретения.
Термин "таутомеры" относится к соединениям, которые являются взаимозаменяемыми формами конкретной структуры соединения и которые отличаются перемещениями атомов водорода и электронов. Таким образом, две структуры могут находиться в равновесии благодаря движению π-электронов и атома (обычно H). Например, енолы и кетоны являются таутомерами, поскольку они быстро взаимопревращаются при обработке либо кислотой, либо основанием. Другим примером таутомерии являются аци- и нитроформы фенилнитрометана, которые подобным образом образуются при обработке кислотой или основанием. Таутомерные формы могут иметь значение для достижения оптимальной химической реакционной способности и биологической активности соединения, представляющего интерес.
Соединения
В одном аспекте в настоящем изобретении предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль, где:
 (I),
(I),
R1 выбран из группы, состоящей из водорода, C1-6алкила, гидроксил-C1-6алкила и гетеро-C1-6алкила; и
R2 представляет собой  , где n составляет 1, 2 или 3.
, где n составляет 1, 2 или 3.
В одном варианте осуществления R1 выбран из группы, состоящей из гидроксила и 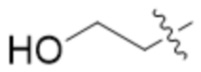 .
.
В одном варианте осуществления R2 представляет собой 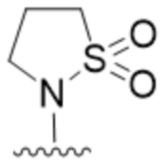 или
или 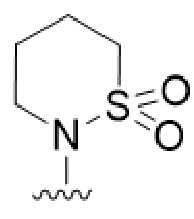 .
.
В одном варианте осуществления R2 представляет собой  .
.
В одном варианте осуществления R2 представляет собой  .
.
В одном варианте осуществления R1 выбран из группы, состоящей из гидроксила и  ; и R2 представляет собой
; и R2 представляет собой  или
или  .
.
В одном варианте осуществления соединение или его фармацевтически приемлемая соль выбраны из:
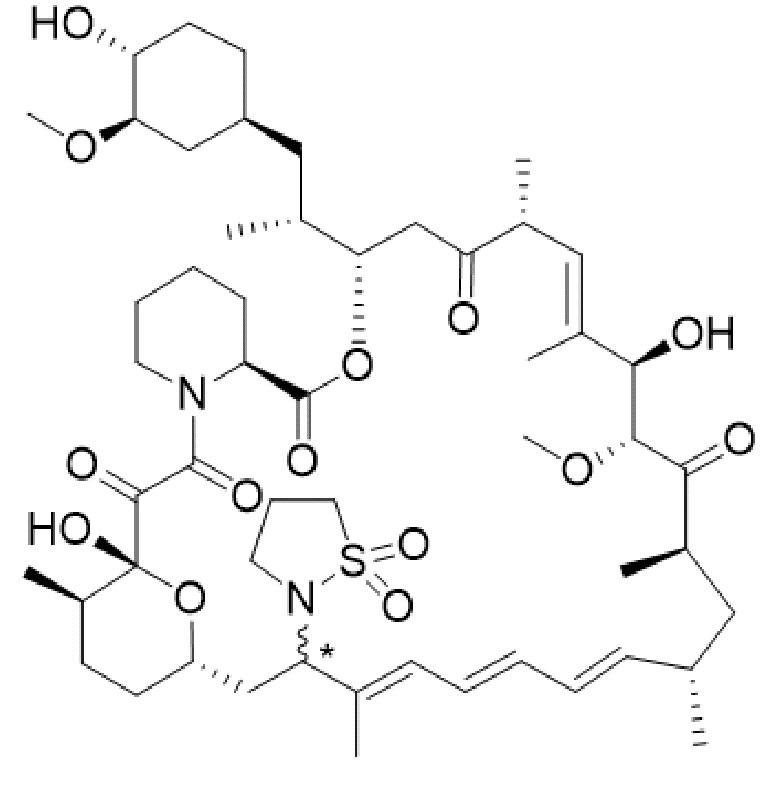
* Абсолютная стереохимическая конфигурация при C16 не определена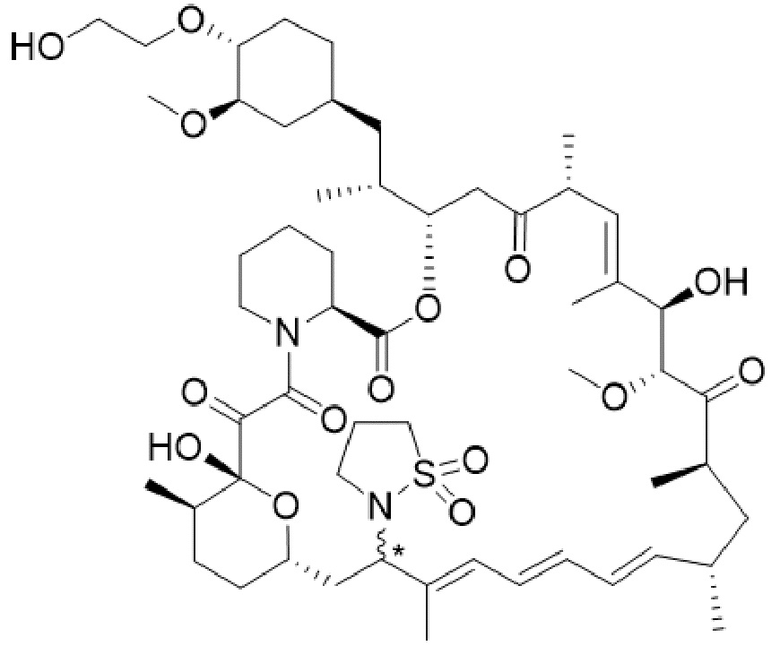
* Абсолютная стереохимическая конфигурация при C16 не определена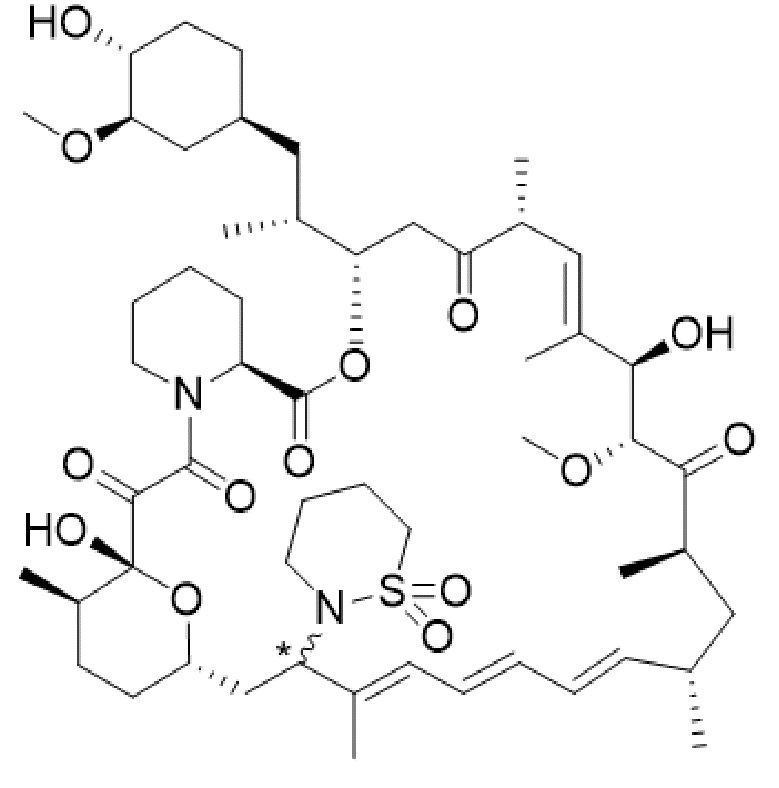
* Абсолютная стереохимическая конфигурация при C16 не определена
Фармацевтически приемлемые соли
Для путей применения, описанных в данном документе, также предусматриваются фармацевтически приемлемые соли этих соединений. Применяемые в данном документе термины "соль" или "соли" относятся к соли присоединения кислоты или присоединения основания на основе соединения по настоящему изобретению. "Соли" включают, в частности, "фармацевтически приемлемые соли". Термин "фармацевтически приемлемые соли" относится к солям, которые сохраняют биологическую эффективность и свойства соединений, раскрытых в данном документе, и которые, как правило, не являются биологически или иным образом нежелательными. Во многих случаях соединения, раскрытые в данном документе, способны к образованию солей с кислотой и/или основанием за счет присутствия амино- и/или карбоксильных групп или подобных им групп.
Фармацевтически приемлемые соли присоединения кислоты могут быть образованы с помощью неорганических кислот и органических кислот.
Неорганические кислоты, из которых могут быть получены соли, включают, например, хлористоводородную кислоту, бромистоводородную кислоту, серную кислоту, азотную кислоту, фосфорную кислоту и т. п.
Органические кислоты, с помощью которых могут быть получены соли, включают, например, уксусную кислоту, пропионовую кислоту, гликолевую кислоту, щавелевую кислоту, малеиновую кислоту, малоновую кислоту, янтарную кислоту, фумаровую кислоту, винную кислоту, лимонную кислоту, бензойную кислоту, миндальную кислоту, метансульфоновую кислоту, этансульфоновую кислоту, толуолсульфоновую кислоту, сульфосалициловую кислоту и т.п.
Фармацевтически приемлемые соли присоединения основания могут быть образованы с помощью неорганических и органических оснований.
Неорганические основания, из которых могут быть получены соли, включают, например, соли аммония и металлов из групп I-XII периодической таблицы элементов. В определенных вариантах осуществления соли получены из натрия, калия, аммония, кальция, магния, железа, серебра, цинка и меди; в частности, подходящие соли включают аммониевые, калиевые, натриевые, кальциевые и магниевые соли.
Органические основания, из которых могут быть получены соли, включают, например, первичные, вторичные и третичные амины, замещенные амины, в том числе встречающиеся в природе замещенные амины, циклические амины, основные ионообменные смолы и т.п. Определенные органические амины включают изопропиламин, бензатин, холинат, диэтаноламин, диэтиламин, лизин, меглюмин, пиперазин и трометамин.
В другом аспекте в настоящем изобретении предусмотрено соединение формулы (I) в форме соли, представляющей собой ацетат, аскорбат, адипат, аспартат, бензоат, безилат, бромид/гидробромид, бикарбонат/карбонат, бисульфат/сульфат, камфорасульфонат, капрат, хлорид/гидрохлорид, хлортеофиллонат, цитрат, этандисульфонат, фумарат, глюцептат, глюконат, глюкуронат, глутамат, глутарат, гликолят, гиппурат, гидройодид/йодид, изетионат, лактат, лактобионат, лаурилсульфат, малат, малеат, малонат, манделат, мезилат, метилсульфат, мукат, нафтоат, напсилат, никотинат, нитрат, октадеканоат, олеат, оксалат, пальмитат, памоат, фосфат/гидрофосфат/дигидрофосфат, полигалактуронат, пропионат, себацат, стеарат, сукцинат, сульфосалицилат, сульфат, тартрат, тозилат, трифенатат, трифторацетат или ксинафоат.
Фармацевтические композиции
В другом аспекте в настоящем изобретении предусмотрена фармацевтическая композиция, содержащая одно или несколько соединений формулы (I) или их фармацевтически приемлемую соль и один или несколько фармацевтически приемлемых носителей. Термин "фармацевтически приемлемый носитель" относится к фармацевтически-приемлемому материалу, композиции или носителю, такому как жидкий или твердый наполнитель, разбавитель, вспомогательное вещество, растворитель или инкапсулирующий материал, задействованный в переносе или транспортировке любой указанной композиции или ее компонента. Каждый носитель должен быть "приемлемым" с точки зрения совместимости с указанной композицией и ее компонентами и не причинять вреда пациенту. Некоторые примеры материалов, которые могут выполнять функцию фармацевтически приемлемых носителей, включают: (1) сахара, такие как лактоза, глюкоза и сахароза; (2) крахмалы, такие как кукурузный крахмал и картофельный крахмал; (3) целлюлозу и ее производные, такие как карбоксиметилцеллюлоза натрия, этилцеллюлоза и ацетат целлюлозы; (4) порошкообразный трагакант; (5) солод; (6) желатин; (7) тальк; (8) вспомогательные вещества, такие как масло какао и воски для суппозиториев; (9) масла, такие как арахисовое масло, хлопковое масло, сафлоровое масло, кунжутное масло, оливковое масло, кукурузное масло и соевое масло; (10) гликоли, такие как пропиленгликоль; (11) полиолы, такие как глицерин, сорбит, маннит и полиэтиленгликоль; (12) сложные эфиры, такие как этилолеат и этиллаурат; (13) агар; (14) буферные средства, такие как гидроксид магния и гидроксид алюминия; (15) альгиновую кислоту; (16) апирогенную воду; (17) изотонический солевой раствор; (18) раствор Рингера; (19) этиловый спирт; (20) фосфатно-буферные растворы и (21) другие нетоксичные совместимые вещества, используемые в фармацевтических составах.
Композиции по настоящему изобретению можно вводить перорально, парентерально, с помощью спрея для ингаляции, местно, ректально, назально, трансбуккально, вагинально или посредством вживленного резервуара. Применяемый в данном документе термин "парентеральный" включает методики подкожной, внутривенной, внутримышечной, внутрисуставной, внутрисиновиальной, внутригрудинной, интратекальной, внутрипеченочной, внутриочаговой и внутричерепной инъекции или инфузии. В некоторых вариантах осуществления композиции по настоящему изобретению вводят перорально, внутрибрюшинно или внутривенно. Стерильные инъекционные формы композиций по настоящему изобретению могут представлять собой водную или масляную суспензию. Такие суспензии могут быть составлены в соответствии с методиками, известными в данной области техники, с применением подходящих диспергирующих или смачивающих средств и суспендирующих средств. Стерильный инъекционный препарат также может представлять собой стерильный инъекционный раствор или суспензию в нетоксичном приемлемом для парентерального введения разбавителе или растворителе, например, раствор в 1,3-бутандиоле. К числу приемлемых сред-носителей и растворителей, которые можно использовать, относятся вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды традиционно используют стерильные нелетучие масла.
С этой целью можно использовать любое нелетучее масло без вкуса, в том числе синтетические моно- или диглицериды. Жирные кислоты, такие как олеиновая кислота и ее глицеридные производные, применимы для получения инъекционных препаратов, так же как и природные фармацевтически приемлемые масла, таких как оливковое масло или касторовое масло, в частности, в их полиоксиэтилированных вариантах. Данные масляные растворы или суспензии также могут содержать разбавитель или диспергирующее вещество на основе длинноцепочечного спирта, такие как карбоксиметилцеллюлоза или подобные диспергирующие средства, которые обычно применяются в составах фармацевтически приемлемых лекарственных форм, содержащих эмульсии и суспензии. Для целей составления также можно применять другие общепринятые поверхностно-активные вещества, такие как Tween®, виды Span и другие эмульгирующие средства или усилители биодоступности, которые обычно применяются в изготовлении фармацевтически приемлемых твердых, жидких и прочих лекарственных форм.
Фармацевтически приемлемые композиции по настоящему изобретению могут вводиться перорально в любой лекарственной форме, приемлемой для перорального введения, в том числе без ограничения в виде капсул, таблеток, водных суспензий или растворов. В случае таблеток для перорального применения общепринятые носители включают лактозу и кукурузный крахмал. Как правило, также добавляют смазывающие средства, такие как стеарат магния. Применимые разбавители для перорального введения в форме капсул включают лактозу и высушенный кукурузный крахмал. Если водные суспензии требуются для перорального применения, активный ингредиент комбинируют с эмульгирующими и суспендирующими средствами. При необходимости также можно добавлять определенные подслащивающие, ароматизирующие и красящие средства.
В качестве альтернативы фармацевтически приемлемые композиции по настоящему изобретению можно вводить в форме суппозиториев для ректального введения. Их можно получать путем смешивания средства с подходящим, не вызывающим раздражения вспомогательным веществом, которое является твердым при комнатной температуре, но становится жидким при ректальной температуре, и следовательно, будет плавиться в полости прямой кишки с высвобождением лекарственного средства. Такие материалы включают масло какао, пчелиный воск и полиэтиленгликоли.
Фармацевтически приемлемые композиции по настоящему изобретению также можно вводить местно, особенно если мишень для лечения включает легкодоступные для местного нанесения зоны или органы, в том числе при заболеваниях глаз, кожи или нижних отделов кишечного тракта. Подходящие составы для местного применения можно легко получать для каждой из таких зон или органов. В случае нижних отделов кишечного тракта местное применение можно осуществлять с помощью состава для ректального суппозитория (см. выше) или с помощью подходящего состава для клизмы. Также можно применять местные трансдермальные пластыри.
В случае некоторых видов местного применения фармацевтически приемлемые композиции можно составлять в форме подходящей мази, содержащей активный компонент, суспендированный или растворенный в одном или нескольких носителях. Носители для местного введения по настоящему изобретению включают без ограничения минеральное масло, жидкий вазелин, белый вазелин, пропиленгликоль, полиоксиэтилен, соединение на основе полиоксипропилена, эмульгирующих воск и воду. В качестве альтернативы фармацевтически приемлемые композиции можно составлять в форме подходящего лосьона или крема, содержащих активные компоненты, суспендированные или растворенные в одном или нескольких фармацевтически приемлемых носителях. Подходящие носители включают без ограничения минеральное масло, сорбитанмоностеарат, полисорбат 60, воск га основе сложных эфиров цетилового спирта, цетеариловый спирт, 2-октилдодеканол, бензиловый спирт и воду.
Фармацевтически приемлемые композиции по настоящему изобретению также можно вводить с помощью назального аэрозоля или ингаляции. Такие композиции получают в соответствии с методиками, общеизвестными в данной области техники для фармацевтических составов, и их можно получать в виде растворов в солевом растворе, с использованием бензилового спирта или других подходящих консервантов, стимуляторов абсорбции для повышения биодоступности, фторуглеводородов и/или других традиционных солюбилизирующих или диспергирующих средств. Количество соединений по настоящему изобретению, которые можно объединять с материалами-носителями для получения композиции в виде единичной лекарственной формы, будет варьироваться в зависимости от подвергаемого лечению реципиента и конкретного способа введения. Предпочтительно композиции должны быть составлены таким образом, чтобы пациенту, принимающему данные композиции, можно было вводить ингибитор в пределах диапазона дозировки 0,01-100 мг/кг массы тела/сутки.
Меченные изотопами соединения
Также предусмотрено, что соединение формулы (I) или его фармацевтически приемлемая соль представляют собой немеченые формы, а также меченные изотопами формы соединений. Меченные изотопами соединения характеризуются структурами, изображенными посредством формул, приведенных в данном документе, за исключением того, что один или несколько атомов заменены атомом, характеризующимся выбранными атомной массой или массовым числом. Примеры изотопов, которые можно включать в соединения по настоящему изобретению, включают изотопы водорода, углерода, азота, кислорода, фосфора, фтора и хлора, такие как 2H, 3H, 11C, 13C, 14C, 15N, 18F 31P, 32P, 35S, 36Cl, 123I, 124I, 125I соответственно. В настоящее изобретение включены различные меченные изотопами соединения, определенные в данном документе, например, соединения, в которых присутствуют радиоактивные изотопы, такие как 3H и 14C, или соединения, в которых присутствуют изотопы, не являющиеся радиоактивными, такие как 2H и 13C. Такие меченные изотопами соединения применимы в исследованиях метаболизма (с применением 14C), в исследованиях кинетики реакций (например, с применением 2H или 3H), в методиках обнаружения или визуализации, таких как позитронно-эмиссионная томография (PET) или однофотонная эмиссионная компьютерная томография (SPECT), в том числе в анализах распределения лекарственного средства или субстрата в тканях, или при радиационной терапии пациентов. В частности, меченное 18F соединение может быть особенно пригодным для исследований с помощью PET или SPECT. Меченные изотопами соединения формулы (I), (Ia) или (Ib), или их фармацевтически приемлемые соли обычно можно получать с помощью традиционных методик, известных специалистам в данной области техники, или с помощью способов, аналогичных описанным в прилагаемых примерах и способах получения, с применением подходящего меченого изотопом реагента вместо немеченого реагента, используемого ранее.
Кроме того, замещение более тяжелыми изотопами, в частности, дейтерием (т. е., 2H или D), может обеспечивать определенные терапевтические преимущества, обусловленные более высокой метаболической стабильностью, например, увеличение периода полувыведения in vivo, или снижение требований в отношении дозировки, или улучшение терапевтического индекса. Понятно, что дейтерий в данном контексте рассматривается как заместитель соединения формулы (I) или его фармацевтически приемлемой соли. Концентрация такого более тяжелого изотопа, в частности дейтерия, может быть определена с помощью коэффициента изотопного обогащения. Применяемый в данном документе термин "коэффициент изотопного обогащения" означает отношение содержания изотопа к распространенности в природе указанного изотопа. В случае если заместитель в соединении по настоящему изобретению обозначается как дейтерий, такое соединение характеризуется коэффициентом изотопного обогащения для каждого указанного атома дейтерия, составляющим по меньшей мере 3500 (введение 52,5% дейтерия по каждому обозначенному атому дейтерия), по меньшей мере 4000 (введение 60% дейтерия), по меньшей мере 4500 (введение 67,5% дейтерия), по меньшей мере 5000 (введение 75% дейтерия), по меньшей мере 5500 (введение 82,5% дейтерия), по меньшей мере 6000 (введение 90% дейтерия), по меньшей мере 6333,3 (введение 95% дейтерия), по меньшей мере 6466,7 (введение 97% дейтерия), по меньшей мере 6600 (введение 99% дейтерия) или по меньшей мере 6633,3 (введение 99,5% дейтерия).
Дозировки
Токсичность и терапевтическую эффективность соединений по настоящему изобретению, в том числе фармацевтически приемлемые соли и дейтерированные варианты, можно определять с помощью стандартных фармацевтических процедур в культурах клеток или на экспериментальных животных. LD50 представляет собой дозу, летальную для 50% популяции. ED50 представляет собой дозу, терапевтически эффективную для 50% популяции. Соотношение доз между токсичным и терапевтическим эффектами (LD50/ED50) представляет собой терапевтический индекс. Соединения, которые демонстрируют высокие терапевтические индексы, являются предпочтительными. Хотя можно применять соединения, которые демонстрируют токсичные побочные эффекты, следует позаботиться о разработке системы доставки, которая направляет такие соединения в месторасположение пораженной ткани, с целью сведения к минимуму потенциального повреждения неинфицированных клеток и снижения, таким образом, побочных эффектов.
Данные, полученные из анализов культуры клеток и исследований на животных, можно применять для составления диапазона дозировок для применения у людей. Дозировка таких соединений может находиться в пределах диапазона циркулирующих концентраций, который включает ED50 при небольшой токсичности или ее отсутствии. Дозировка может варьироваться в пределах данного диапазона в зависимости от используемой лекарственной формы и используемого пути введения. Для любого соединения терапевтически эффективную дозу можно первоначально оценить с помощью анализов на культуре клеток. Дозу можно составлять на животных моделях с достижением диапазона циркулирующих концентраций в плазме крови, который включает IC50 (т. е. концентрацию тестируемого соединения, которая обеспечивает полумаксимальное подавление симптомов), определенную на культуре клеток. Такую информацию можно использовать для более точного определения применимых доз у людей. Уровни в плазме крови можно измерять, например, с помощью высокоэффективной жидкостной хроматографии.
Также следует понимать, что конкретная дозировка и схема лечения для любого конкретного пациента будет зависеть от разнообразных факторов, в том числе активности конкретного используемого соединения, возраста, массы тела, общего состояния здоровья, пола, диеты, времени введения, скорости выведения, комбинации лекарственных средств, и решения лечащего врача, и тяжести конкретного заболевания, подвергаемого лечению. Количество соединения по настоящему изобретению в композиции также будет зависеть от конкретного соединения в композиции.
Все способы, описанные в данном документе, можно осуществлять в любом подходящем порядке, если иное не указано в данном документе, или это иным образом явно не противоречит контексту. Представленное в данном документе применение всех возможных примеров или вводных слов перед примерном (например, "такой как") предназначено исключительно для лучшего освещения настоящего изобретения и не предполагает ограничения объема настоящего изобретения, заявленного далее.
Любой асимметрический атом (например, углерод и т. п.) в соединении(-ях) по настоящему изобретению может находиться в рацемической или энантиомерно обогащенной форме, например, в (R)-, (S)- или (R,S)-конфигурации. В определенных вариантах осуществления каждый асимметрический атом характеризуется по меньшей мере 50% энантиомерным избытком, по меньшей мере 60% энантиомерным избытком, по меньшей мере 70% энантиомерным избытком, по меньшей мере 80% энантиомерным избытком, по меньшей мере 90% энантиомерным избытком, по меньшей мере 95% энантиомерным избытком или по меньшей мере 99% энантиомерным избытком в (R)- или (S)-конфигурации. Заместители при атомах с ненасыщенными двойными связями могут, если это возможно, находиться в цис- (Z)- или транс- (E)-форме.
Соответственно, применяемое в данном документе соединение по настоящему изобретению может находиться в форме одного из возможных стереоизомеров, ротамеров, атропоизомеров, таутомеров или их смесей, например, в виде по сути чистых геометрических (цис- или транс-) стереоизомеров, диастереоизомеров, оптических изомеров (антиподов), рацематов или их смесей.
Любые полученные смеси стереоизомеров можно разделять на основе физико-химических отличий их составляющих на чистые или по сути чистые геометрические или оптические изомеры, диастереомеры, рацематы, например, с помощью хроматографии и/или фракционной кристаллизации.
Любые полученные рацематы соединений по настоящему изобретению или промежуточных соединений могут быть разделены на оптические антиподы посредством известных способов, например, посредством разделения их диастереомерных солей, полученных с помощью оптически активных кислоты или основания, и высвобождения оптически активных кислотного или основного соединения. В частности, основный фрагмент можно использовать таким образом для разделения соединений по настоящему изобретению на их оптические антиподы, например, путем фракционной кристаллизации соли, образованной с оптически активной кислотой, например, винной кислотой, дибензоилвинной кислотой, диацетилвинной кислотой, ди-O,O'-п-толуоилвинной кислотой, миндальной кислотой, яблочной кислотой или камфор-10-сульфоновой кислотой. Рацемические соединения по настоящему изобретению или рацемические промежуточные соединения также могут быть разделены посредством хиральной хроматографии, например жидкостной хроматографии высокого давления (HPLC) с применением хирального адсорбента.
Заболевания и нарушения
Соединений формулы (I) применимы в лечении заболевания или нарушения, выбранного из:
видов васкулопатии трансплантата;
пролиферации и миграции гладкомышечных клеток, приводящих к утолщению интимы сосудов, закупорке кровеносных сосудов, обструктивному коронарному атеросклерозу, рестенозу;
аутоиммунных заболеваний и воспалительных состояний;
астмы;
заболеваний, ассоциированных со множественной лекарственной резистентностью (MDR);
грибковых инфекций;
воспаления;
инфекции;
возрастных заболеваний;
нейродегенеративных заболеваний;
пролиферативных нарушений, например, рака,
эпилептических припадков и связанных с эпилептическими припадками нарушений и
митохондриальной миопатии и митохондриального стресса.
В другом аспекте соединение, раскрытое в данном документе, можно применять для лечения состояний, которые, как было показано, повышают вероятность возникновения возрастных заболеваний, таких как ситуации, при которых происходит повышение уровня цитокинов, вызывающих старение (например, IL6).
В другом аспекте соединение, раскрытое в данном документе, можно применять для лечения нарушений, которые включают процесс фиброза и/или воспаления, например, нарушений со стороны печени и почек. Примеры включают фиброз печени, который возникает на терминальной стадии заболевания печени; цирроз печени; печеночную недостаточность, обусловленную токсичностью; неалкогольный стеатогепатит или NASH и алкогольный стеатоз. Другой пример представляет собой фиброз почек, который возникает в результате острого повреждения почек, приводящего к хроническому заболеванию почек. Диабетическая нефропатия может индуцировать фиброз и воспаление почек. Зачастую заболевание почек вызывает сердечную недостаточность в результате повышения кровяного давления; оно также может быть ассоциировано с фиброзом сердца.
В другом аспекте соединения по настоящему изобретению можно применять для лечения сердечной недостаточности. (Buss, S.J. et al. Beneficial effects of Mammalian target of rapamycin inhibition on left ventricular remodeling after myocardial infarction. J Am Coll Cardiol. (2009) 54(25): 2435-46; Buss, S.J. et al. Augmentation of autophagy by mTOR-inhibition in myocardial infarction: When size matters. Autophagy. (2010) 6(2):304-6.
В другом аспекте соединения по настоящему изобретению можно применять для лечения фиброза печени у пациентов, перенесших трансплантацию печени. (Villamil, F.G. et al. Fibrosis progression in maintenance liver transplant patients with hepatitis C recurrence: a randomized study of RAD001 vs. calcineurin inhibitors. Liver Int. (2014) 34(10):1513-21).
Васкулопатии трансплантата включают атеросклероз.
Аутоиммунные заболевания и воспалительные состояния включают, в частности, воспалительные состояния с этиологией, включающей аутоиммунный компонент, такие как артрит (например, ревматоидный артрит, прогрессирующий хронический артрит и деформирующий артрит) и ревматические заболевания. Конкретные аутоиммунные заболевания, при которых можно использовать соединения формулы (I), включают аутоиммунные гематологические нарушения (в том числе, например, гемолитическую анемию, апластическую анемию, врожденную апластическую анемию и идиопатическую тромбоцитопению), системную красную волчанку, полихондрию, склеродермию, гранулематоз Вегенера, дерматомиозит, хронический активный гепатит, миастению гравис, псориаз, синдром Стивенса-Джонсона, идиопатический синдром мальабсорбции, аутоиммунное воспалительное заболевание кишечника (включая, например, язвенный колит и болезнь Крона), эндокринную офтальмопатию, болезнь Грейвса, саркоидоз, рассеянный склероз, первичный билиарный цирроз, ювенильный диабет (сахарный диабет I типа), увеит (передний и задний), синдром сухого глаза и весенний кератоконъюнктивит, интерстициальный фиброз легких, псориатический артрит, гломерулонефрит (с нефротическим синдромом и без него, например, включая идиопатический нефротический синдром или нефропатию минимальных изменений) и ювенильный дерматомиозит.
Соединения по настоящему изобретению также могут применяться при лечении заболеваний, обусловленных множественной лекарственной резистентностью (MDR), что предусматривает повышение эффективности других химиотерапевтических средств при лечении и контроле состояний с множественной лекарственной резистентностью, таких как рак с множественной лекарственной резистентностью или СПИД с множественной лекарственной резистентностью. MDR является особенно проблематичной у пациентов, страдающих раком, и пациентов со СПИДом, которые не отвечают на традиционную химиотерапию, поскольку Pgp выводит лекарственный препарат из клеток.
Соединения по настоящему изобретению также могут применяться в лечении инфекции, которая включает инфекцию, обусловленную патогенами, имеющими Mip или Mip-подобные факторы.
Возрастные заболевания включают саркопению, атрофию кожи, виды старческой гемангиомы, виды себорейного кератоза, атрофию головного мозга (также называемую деменцией), атеросклероз, артериосклероз, эмфизему легких, остеопороз, остеоартрит, высокое кровяное давление, виды катаракты, макулярную дегенерацию, глаукому, инсульт, нарушение мозгового кровообращения (виды инсульта), хроническое заболевание почек, ассоциированное с диабетом заболевание почек, нарушение функции печени, фиброз печени, аутоиммунный гепатит, гиперплазию эндометрия, метаболическую дисфункцию, реноваскулярное заболевание, тугоухость, нарушение способности к передвижению (например, старческую астению), снижение когнитивной функции, ригидность сухожилий, дисфункцию сердца, такую как гипертрофия сердца, и/или систолическая и/или диастолическая дисфункция, и/или гипертензия, и/или дилятационная кардиомиопатия, дисфункцию сердца, которая приводит к снижению фракции выброса, иммунное старение, болезнь Паркинсона, болезнь Альцгеймера, рак, иммунное старение, приводящее к раку вследствие снижения иммунного надзора, инфекций, обусловленных снижением иммунной функции, хроническую обструктивную болезнь легких (COPD), ожирение, потерю вкуса, потерю обоняния, артрит и диабета II типа (в том числе осложнения, возникшие в результате диабета, такие как почечная недостаточность, слепота и нейропатия).
Нейродегенеративные заболевания включают болезнь Хантингтона, болезнь Паркинсона, спиноцеребеллярную атаксию 3 типа, болезнь Альцгеймера, болезнь двигательных нейронов и периферическую нейропатию.
Пролиферативные нарушения включают рак. Такие состояния включают состояния, перечисленные в патенте США № 9669032, например, рак почки, почечно-клеточную карциному, колоректальный рак, саркому матки, рак эндометрия матки, рак эндометрия, рак молочной железы, рак яичника, рак шейки матки, рак желудка, фибросаркому, рак поджелудочной железы, рак печени, меланому, лейкоз, множественную миелому, рак носоглотки, рак предстательной железы, рак легкого, глиобластому, астроцитому, аденокарциному, рак мочевого пузыря, мезотелиому, рак головы, рабдомиосаркому, саркому, лимфому и рак шеи.
Эпилептические припадки и связанные с эпилептическими припадками нарушения включают синдром Веста, фокальную кортикальную дисплазию (FCD), комплекс туберозного склероза (TSC), детскую абсансную эпилепсию, доброкачественную фокальную эпилепсию детского возраста, ювенильную миоклоническую эпилепсию (JME), эпилепсию височной доли, эпилепсию лобной доли, рефрактерную эпилепсию, синдром Леннокса-Гасто, эпилепсию затылочной доли, синдром Протея, синдром гемимегалэнцефалии (HMEG), синдром мегалэнцефалии (MEG), мегалэнцефалию-капиллярную мальформацию (MCAP) и мегалэнцефалию-полимикрогирию-полидактилию-синдром гидроцефалии (MPPH).
Митохондриальная миопатия и митохондриальный стресс представляют собой митохондриальные нарушения, описанные в Chinnery, P.F. (2015); EMBO Mol. Med. 7, 1503-1512; Koopman, W.J. et al., (2016); EMBO Mol. Med. 8, 311-327 и Young, M.J., and Yound and Copeland, W.C. (2016); Curr. Opin. Genet. Dev. 38, 52-62.
Поддающиеся лечению состояния, которые, как было показано, повышают вероятность возникновения возрастных заболеваний, включают старение, например иммунное старение. Оно диагностируется по (i) увеличению уровня циркулирующих цитокинов, таких как IL-6, но также по (ii) стареющим клеткам, обнаруженным в мышцах, почках, печени, головном мозге, среди нейронов, в печени, поджелудочной железе или сердце; или также по (iii) снижению эффективности репарации ДНК, что может быть продемонстрировано увеличением уровня транскрипции повторяющихся элементов, включая гены, кодируемые транспозонами.
Способы применения
В настоящем изобретении предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль для лечения заболеваний и нарушений, описанных в данном документе, например, возрастных нарушений, или заболеваний и нарушений, для лечения которых в настоящее время одобрено применение рапалогов, таких как RAD001.
В одном аспекте в настоящем изобретении предусмотрен способ лечения нарушения или заболевания, опосредованного путем mTOR, у субъекта, нуждающегося в этом, при этом способ предусматривает введение субъекту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
В другом аспекте в настоящем изобретении предусмотрен способ лечения заболевания или нарушения у субъекта, где ткань-мишень, орган-мишень или клетки-мишени, ассоциированные с патологическим процессом, приводящим к заболеванию или нарушению, характеризуются уровнями FKBP12, достаточными для ингибирования mTORC1, при этом способ предусматривает введение субъекту, нуждающемуся в этом, терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
В другом аспекте в настоящем изобретении предусмотрен способ лечения заболевания или нарушения у субъекта, который характеризуется уровнями FKBP12, достаточными для ингибирования mTORC1, или субъекта, в отношении которого было установлено, что он характеризуется такими уровнями, при этом способ предусматривает введение субъекту, нуждающемуся в этом, терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли.
В одном варианте осуществления заболевание или нарушение выбрано из саркопении, атрофии кожи, видов старческой гемангиомы, видов себорейного кератоза, атрофии головного мозга, атеросклероза, артериосклероза, эмфиземы легких, остеопороза, остеоартрита, высокого кровяного давления, видов катаракты, макулярной дегенерации, глаукомы, инсульта, нарушения мозгового кровообращения (видов инсульта), хронического заболевания почек, ассоциированного с диабетом заболевания почек, нарушения функции печени, фиброза печени, аутоиммунного гепатита, гиперплазии эндометрия, метаболической дисфункции, реноваскулярного заболевания, тугоухости, нарушения способности к передвижению, снижения когнитивной функции, ригидности сухожилий, дисфункции сердца, такой как гипертрофия сердца, систолическая или диастолическая дисфункция, гипертензия, дилятационная кардиомиопатия, дисфункции сердца, которая приводит к снижению фракции выброса, иммунного старения, болезни Паркинсона, болезни Альцгеймера, рака, иммунного старения, приводящего к раку вследствие снижения иммунного надзора, инфекций, обусловленных снижением иммунной функции, хронической обструктивной болезни легких (COPD), ожирения, потери вкуса, потери обоняния, артрита и диабета II типа, в том числе осложнений, возникших в результате диабета, таких как почечная недостаточность, слепота и нейропатия.
В одном варианте осуществления нарушение представляет собой фиброз печени.
В другом аспекте в настоящем изобретении предусмотрен способ лечения заболевания или нарушения у субъекта, нуждающегося в этом, при этом способ предусматривает введение субъекту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, фармацевтической композиции, содержащей соединение формулы (I) или его фармацевтически приемлемую соль, или фармацевтической комбинации, содержащей соединение формулы (I) или его фармацевтически приемлемую соль, где нарушение или заболевание выбрано из:
- видов васкулопатии трансплантата;
- пролиферации и миграции гладкомышечных клеток, приводящих к утолщению интимы сосудов, закупорке кровеносных сосудов, обструктивному коронарному атеросклерозу, рестенозу;
- аутоиммунных заболеваний и воспалительных состояний;
- астмы;
- заболеваний, ассоциированных со множественной лекарственной резистентностью (MDR);
- грибковых инфекций;
- воспаления;
- инфекции;
- возрастных заболеваний;
- нейродегенеративных заболеваний;
- пролиферативных нарушений, в частности рака;
- эпилептических припадков и связанных с эпилептическими припадками нарушений и
- митохондриальной миопатии и митохондриального стресса.
В одном варианте осуществления нарушение представляет собой нарушение, которое включает процесс фиброза и/или воспаления.
В одном варианте осуществления нарушение выбрано из нарушений со стороны печени и почек.
В одном варианте осуществления нарушение со стороны печени выбрано из фиброза печени, который возникает на терминальной стадии заболевания печени; цирроза печени; печеночной недостаточности, обусловленной токсичностью; неалкогольного стеатогепатита или NASH и алкогольного стеатоза.
В одном варианте осуществления нарушение со стороны почек представляет собой фиброз почек.
В одном варианте осуществления фиброз почек возникает в результате острого повреждения почек.
В одном варианте осуществления нарушение со стороны почек представляет собой хроническое нарушение со стороны почек.
В одном варианте осуществления нарушение со стороны почек представляет собой диабетическую нефропатию.
В другом аспекте в настоящем изобретении предусмотрен способ лечения возрастного нарушения или заболевания у субъекта, нуждающегося в этом, при этом способ предусматривает введение субъекту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, фармацевтической композиции, содержащей соединение формулы (I) или его фармацевтически приемлемую соль, или фармацевтической комбинации, содержащей соединение формулы (I) или его фармацевтически приемлемую соль, где нарушение или заболевание выбрано из саркопении, атрофии кожи, видов старческой гемангиомы, видов себорейного кератоза, атрофии головного мозга, атеросклероза, артериосклероза, эмфиземы легких, остеопороза, остеоартрита, высокого кровяного давления, видов катаракты, макулярной дегенерации, глаукомы, инсульта, нарушения мозгового кровообращения (видов инсульта), хронического заболевания почек, ассоциированного с диабетом заболевания почек, нарушения функции печени, фиброза печени, аутоиммунного гепатита, гиперплазии эндометрия, метаболической дисфункции, реноваскулярного заболевания, тугоухости, нарушения способности к передвижению, снижения когнитивной функции, ригидности сухожилий, дисфункции сердца, такой как гипертрофия сердца, и/или систолическая и/или диастолическая дисфункция, и/или гипертензия, дисфункции сердца, которая приводит к снижению фракции выброса, иммунного старения, болезни Паркинсона, болезни Альцгеймера, рака, иммунного старения, приводящего к раку вследствие снижения иммунного надзора, инфекций, обусловленных снижением иммунной функции, хронической обструктивной болезни легких (COPD), ожирения, потери вкуса, потери обоняния, артрита и диабета II типа, в том числе осложнений, возникших в результате диабета, таких как почечная недостаточность, слепота и нейропатия.
В другом аспекте в настоящем изобретении предусмотрен способ лечения рака у субъекта, при этом способ предусматривает введение субъекту терапевтически эффективного количества соединения формулы (I) или его фармацевтически приемлемой соли, фармацевтической композиции, содержащей соединение формулы (I) или его фармацевтически приемлемую соль, или фармацевтической комбинации, содержащей соединение формулы (I) или его фармацевтически приемлемую соль.
В одном варианте осуществления способ дополнительно предусматривает применение ингибитора PD-1/PDL-1.
В одном варианте осуществления рак выбран из рака почки, почечно-клеточной карциномы, колоректального рака, саркомы матки, рака эндометрия матки, рака эндометрия, рака молочной железы, рака яичника, рака шейки матки, рака желудка, фибросаркомы, рака поджелудочной железы, рака печени, меланомы, лейкоза, множественной миеломы, рака носоглотки, рака предстательной железы, рака легкого, глиобластомы, рака мочевого пузыря, мезотелиомы, рака головы, рабдомиосаркомы, саркомы, лимфомы и рака шеи.
В другом аспекте в настоящем изобретении предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль, фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, или фармацевтическая комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, для применения в качестве лекарственного препарата.
В другом аспекте в настоящем изобретении предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль, фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, или фармацевтическая комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, для применения в предупреждении или лечении нарушения или заболевания, опосредованного путем mTOR.
В другом аспекте в настоящем изобретении предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль, фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, или фармацевтическая комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, для применения в предупреждении или лечении нарушения или заболевания, выбранного из:
- видов васкулопатии трансплантата;
- пролиферации и миграции гладкомышечных клеток, приводящих к утолщению интимы сосудов, закупорке кровеносных сосудов, обструктивному коронарному атеросклерозу, рестенозу;
- аутоиммунных заболеваний и воспалительных состояний;
- астмы;
- заболеваний, ассоциированных со множественной лекарственной резистентностью (MDR);
- инфекций, обусловленных грибами;
- воспаления;
- инфекции;
- возрастных заболеваний;
- нейродегенеративных заболеваний;
- пролиферативных нарушений, в частности рака;
- эпилептических припадков и связанных с эпилептическими припадками нарушений и
- митохондриальной миопатии и митохондриального стресса.
В другом аспекте в настоящем изобретении предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль, фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, или фармацевтическая комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, для применения в предупреждении или лечении нарушения или заболевания, которое включает процесс фиброза и/или воспаления.
В одном варианте осуществления нарушение выбрано из нарушений со стороны печени и почек.
В одном варианте осуществления нарушение со стороны печени выбрано из фиброза печени, который возникает на терминальной стадии заболевания печени; цирроза печени; печеночной недостаточности, обусловленной токсичностью; неалкогольного стеатогепатита или NASH и алкогольного стеатоза.
В одном варианте осуществления нарушение со стороны почек представляет собой фиброз почек, который возникает в результате острого повреждения почек.
В одном варианте осуществления нарушение со стороны почек представляет собой хроническое нарушение со стороны почек.
В одном варианте осуществления нарушение со стороны почек представляет собой диабетическую нефропатию.
В другом аспекте в настоящем изобретении предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль, фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, или фармацевтическая комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, для применения в лечении возрастного нарушения или заболевания, выбранного из саркопении, атрофии кожи, видов старческой гемангиомы, видов себорейного кератоза, атрофии головного мозга (также называемой деменцией), атеросклероза, артериосклероза, эмфиземы легких, остеопороза, остеоартрита, высокого кровяного давления, видов катаракты, макулярной дегенерации, глаукомы, инсульта, нарушения мозгового кровообращения (видов инсульта), хронического заболевания почек, ассоциированного с диабетом заболевания почек, нарушения функции печени, фиброза печени, аутоиммунного гепатита, гиперплазии эндометрия, метаболической дисфункции, реноваскулярного заболевания, тугоухости, нарушения способности к передвижению (например, старческой астении), снижения когнитивной функции, ригидности сухожилий, дисфункции сердца, такой как гипертрофия сердца, и/или систолическая и/или диастолическая дисфункция, и/или гипертензия, и/или дилятационная кардиомиопатия, дисфункции сердца, которая приводит к снижению фракции выброса, иммунного старения, болезни Паркинсона, болезни Альцгеймера, рака, иммунного старения, приводящего к раку вследствие снижения иммунного надзора, инфекций, обусловленных снижением иммунной функции, хронической обструктивной болезни легких (COPD), ожирения, потери вкуса, потери обоняния, артрита и диабета II типа (в том числе осложнений, возникших в результате диабета, таких как почечная недостаточность, слепота и нейропатия).
В другом аспекте в настоящем изобретении предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль, фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, или фармацевтическая комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, для применения в лечении рака.
В другом аспекте в настоящем изобретении предусмотрено соединение формулы (I) или его фармацевтически приемлемая соль, фармацевтическая композиция, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, или фармацевтическая комбинация, содержащая соединение формулы (I) или его фармацевтически приемлемую соль, для применения в лечении рака почки, почечно-клеточной карциномы, колоректального рака, саркомы матки, рака эндометрия матки, рака эндометрия, рака молочной железы, рака яичника, рака шейки матки, рака желудка, фибросаркомы, рака поджелудочной железы, рака печени, меланомы, лейкоза, множественной миеломы, рака носоглотки, рака предстательной железы, рака легкого, глиобластомы, рака мочевого пузыря, мезотелиомы, рака головы, рабдомиосаркомы, саркомы, лимфомы или рака шеи.
В другом аспекте в настоящем изобретении предусмотрено применение соединения формулы (I) или его фармацевтически приемлемой соли для изготовления лекарственного препарата.
В другом аспекте в настоящем изобретении предусмотрено применение соединения формулы (I) или его фармацевтически приемлемой соли для изготовления лекарственного препарата для лечения нарушения или заболевания, опосредованного путем mTOR.
В другом аспекте в настоящем изобретении предусмотрено применение соединения формулы (I) или его фармацевтически приемлемой соли для изготовления лекарственного препарата для лечения нарушения или заболевания, выбранного из:
- видов васкулопатии трансплантата;
- пролиферации и миграции гладкомышечных клеток, приводящих к утолщению интимы сосудов, закупорке кровеносных сосудов, обструктивному коронарному атеросклерозу, рестенозу;
- аутоиммунных заболеваний и воспалительных состояний;
- астмы;
- заболеваний, ассоциированных со множественной лекарственной резистентностью (MDR);
- грибковых инфекций;
- воспаления;
- инфекции;
- возрастных заболеваний;
- нейродегенеративных заболеваний;
- пролиферативных нарушений, например рака;
- эпилептических припадков и связанных с эпилептическими припадками нарушений и
- митохондриальной миопатии и митохондриального стресса.
В другом аспекте в настоящем изобретении предусмотрено применение соединения формулы (I) или его фармацевтически приемлемой соли для изготовления лекарственного препарата для лечения нарушения или заболевания, которое включает процесс фиброза или воспаления.
В одном варианте осуществления нарушение выбрано из нарушений со стороны печени и почек.
В одном варианте осуществления нарушение со стороны печени выбрано из фиброза печени, который возникает на терминальной стадии заболевания печени; цирроза печени; печеночной недостаточности, обусловленной токсичностью; неалкогольного стеатогепатита или NASH и алкогольного стеатоза.
В одном варианте осуществления нарушение со стороны почек представляет собой фиброз почек, который возникает в результате острого повреждения почек.
В одном варианте осуществления нарушение со стороны почек представляет собой хроническое нарушение со стороны почек.
В одном варианте осуществления нарушение со стороны почек представляет собой диабетическую нефропатию.
В другом аспекте в настоящем изобретении предусмотрено применение соединения формулы (I) или его фармацевтически приемлемой соли для изготовления лекарственного препарата для изготовления лекарственного препарата для предупреждения или лечения возрастного нарушения или заболевания, выбранного из саркопении, атрофии кожи, видов старческой гемангиомы, видов себорейного кератоза, атрофии головного мозга (также называемой деменцией), атеросклероза, артериосклероза, эмфиземы легких, остеопороза, остеоартрита, высокого кровяного давления, видов катаракты, макулярной дегенерации, глаукомы, инсульта, нарушения мозгового кровообращения (видов инсульта), хронического заболевания почек, ассоциированного с диабетом заболевания почек, нарушения функции печени, фиброза печени, аутоиммунного гепатита, гиперплазии эндометрия, метаболической дисфункции, реноваскулярного заболевания, тугоухости, нарушения способности к передвижению, снижения когнитивной функции, ригидности сухожилий, дисфункции сердца, такой как гипертрофия сердца, и/или систолическая и/или диастолическая дисфункция, и/или гипертензия, и/или дилятационная кардиомиопатия, дисфункции сердца, которая приводит к снижению фракции выброса, иммунного старения, болезни Паркинсона, болезни Альцгеймера, рака, иммунного старения, приводящего к раку вследствие снижения иммунного надзора, инфекций, обусловленных снижением иммунной функции, хронической обструктивной болезни легких (COPD), ожирения, потери вкуса, потери обоняния, артрита и диабета II типа (в том числе осложнений, возникших в результате диабета, таких как почечная недостаточность, слепота и нейропатия).
В другом аспекте в настоящем изобретении предусмотрено применение соединения формулы (I) или его фармацевтически приемлемой соли для изготовления лекарственного препарата для изготовления лекарственного препарата для предупреждения или лечения рака.
В другом аспекте в настоящем изобретении предусмотрено применение соединения формулы (I) или его фармацевтически приемлемой соли для изготовления лекарственного препарата для изготовления лекарственного препарата для лечения рака почки, почечно-клеточной карциномы, колоректального рака, саркомы матки, рака эндометрия матки, рака эндометрия, рака молочной железы, рака яичника, рака шейки матки, рака желудка, фибросаркомы, рака поджелудочной железы, рака печени, меланомы, лейкоза, множественной миеломы, рака носоглотки, рака предстательной железы, рака легкого, глиобластомы, рака мочевого пузыря, мезотелиомы, рака головы, рабдомиосаркомы, саркомы, лимфомы или рака шеи.
Способы получения соединения формулы (I)
В другом аспекте в настоящем изобретении предусмотрен способ получения соединения по настоящему изобретению в соответствии со схемами 1 и 2.
Схема 1
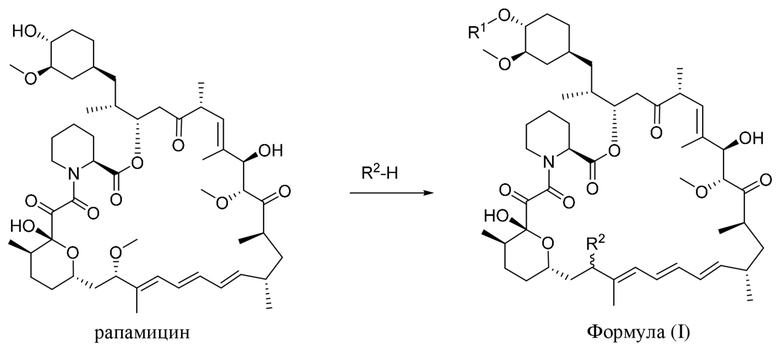
Соединение формулы (I), где R1 представляет собой водород, и R2 является таким, как определено для формулы (I), может быть получено путем осуществление реакции рапамицина с R2-H, где R2 является таким, как определено для формулы (I), в присутствии реагента, подходящего для реакции замещения, например, п-толуолсульфоновой кислоты, в присутствии подходящего растворителя, например, дихлорметана. Например, подходящие условия являются следующими:
1) R2-H, п-толуолсульфоновая кислота-H2O, дихлорметан, комнатная температура;
2) R2-H, трифторуксусная кислота, -40°C, дихлорметан (см. EP1212331 B1);
3) R2-H, 5M LiClO4, Et2O (0.1M), комнатная температура (см. TL, 1995, 43, 7823);
4) R2-H, Cp2HfCl2-AgClO4 (катализатор Сузуки), 4A MS, дихлорметан, комнатная температура (см. TL, 1995, 43, 7823);
5) R2-H, BF3-OEt2 или Zn(OTf)2, THF, 0°C (см. TL, 1994, 37, 6835);
6) R2-H, ZnCl2, дихлорметан, 0°C (см. JOC, 1994, 59, 6512).
Схема 2
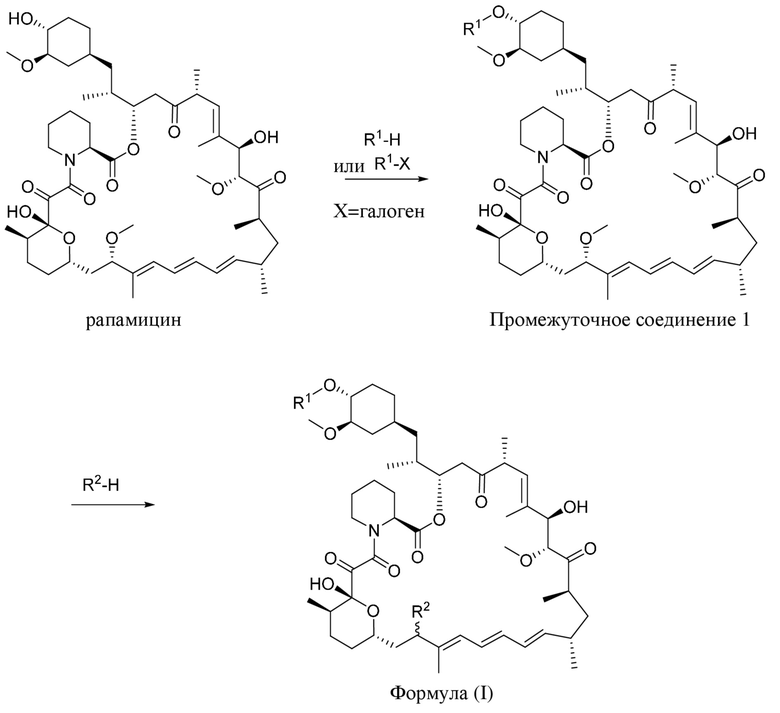
Соединение формулы (I), где R1 выбран из группы, состоящей из C1-6алкила, гидроксил-C1-6алкила и гетеро-C1-6алкила; а R2 является таким, как определено для формулы (I), может быть получено путем осуществление реакции рапамицина с R1-H или R1-X с получением промежуточного соединения 1, с последующим осуществлением реакции с R2-H. В одном варианте осуществления рапамицин вводят в реакцию с R1-H или R1-X в условиях алкилирования для получения промежуточного соединения 1. В одном варианте осуществления промежуточное соединение 1 вводят в реакцию с R2-H в условиях реакции замещения, например, представленных в данном документе, с получением соединения формулы (I).
ПРИМЕРЫ
В настоящем изобретении изложены следующие примеры. Примеры синтеза и биологические примеры, описанные в данной заявке, представлены для иллюстрации соединений, фармацевтических композиций и способов, предусмотренных в данном документе, и их не следует рассматривать как каким бы то ни было образом ограничивающие их объем.
Соединения, предусмотренные в данном документе, можно получать из легкодоступных исходных материалов с использованием модификаций конкретных протоколов синтеза, изложенных ниже, как будет общеизвестно специалистам в данной области техники. Будет понятно, что если указаны типичные или предпочтительные условия процесса (т. е. значения температуры реакции, значения времени, мольные соотношения реагентов, растворители, значения давления и т. д.), если не указано иное, также можно использовать другие условия процесса. Оптимальные реакционные условия могут изменяться в зависимости от конкретных используемых реагентов или растворителей, но такие условия могут быть определены специалистами в данной области техники посредством обычных процедур оптимизации.
Кроме того, для специалистов в данной области техники будет очевидно, что применение традиционных защитных групп может быть необходимым для предотвращения прохождения нежелательных реакций с определенными функциональными группами. Выбор подходящей защитной группы для конкретной функциональной группы, а также подходящие условия для защиты и снятия защиты являются общеизвестными в данной области техники. Например, многочисленные защитные группы, и их введение и удаление, описаны в Greene et al., Protecting Groups in Organic Synthesis, Second Edition, Wiley, New York, 1991, и литературных источниках, цитируемых в приведенном документе.
Рапамицин и его производные, например, соединения формулы (I), существуют в виде зависимого от растворителя и pH равновесия шестичленный и семичленных полукетальных форм, показанных ниже как A, B и C (схема 3). См. The Journal of Antibiotics (Tokyo) (1991) 44(6):688-90 и Tetrahedron Letters (1992) 33(33):4139-4142. Рапамицин и его производные также существуют в виде смеси цис- и транс-амидов, показанных ниже как A и C. [См. Mierke, D. F., Schmieder, P., Karuso, P. and Kessler, H. (1991), Conformational Analysis of the cis‐ and trans‐Isomers of FK506 by NMR and Molecular Dynamics. Helvetica Chimica Acta, 74: 1027-1047.] ЯМР-характеристики, показанные в примерах, соответствуют только главной равновесной форме, наблюдаемой при указанных условиях в дейтерированном растворителе.
Схема 3
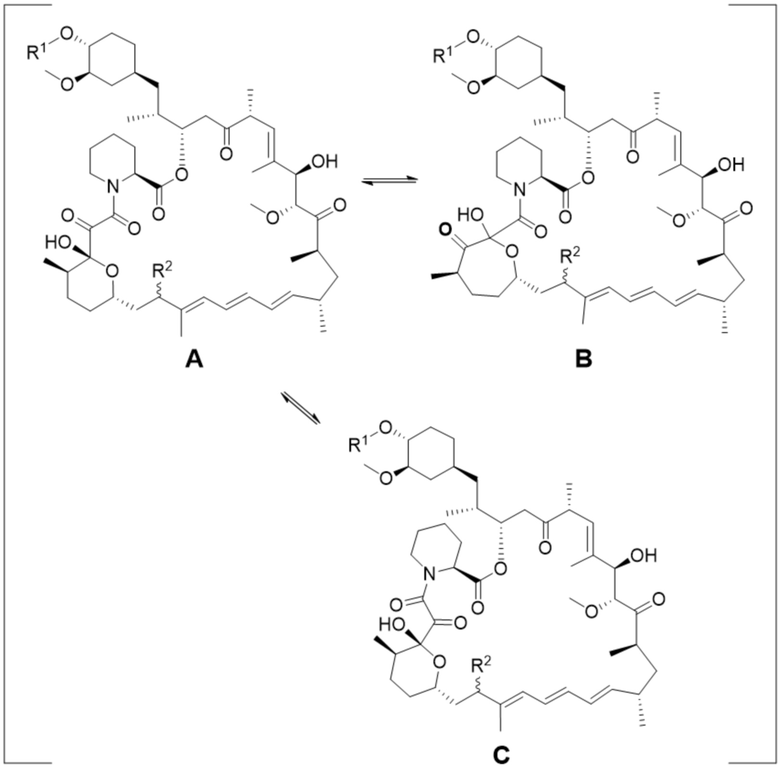
где:
R1 выбран из группы, состоящей из водорода, C1-6алкила, гидроксил-C1-6алкила и гетеро-C1-6алкила; и
R2 представляет собой  , где n составляет 1, 2 или 3.
, где n составляет 1, 2 или 3.
Получение соединений
Соединения по настоящему изобретению можно получать, как описано в следующих примерах.
Список сокращений
Следующие сокращения, используемые в данном документе ниже, имеют соответствующие значения.
A ангстрем
кат. катал итический
ACN ацетонитрил
d дублет
dd дублет дублетов
DCM дихлорметан
DMSO диметилсульфоксид
ESIMS масс-спектрометрия с ионизацией электрораспылением
EtOAc этилацетат
экв. эквивалент
FA муравьиная кислота
ЯМР HSQC ядерный магнитный резонанс в условиях гетероядерной одноквантовой когерентности
HPLC высокоэффективная жидкостная хроматография
HRMS масс-спектрометрия высокого разрешения
h часы
Гц герц
MeCN ацетонитрил
MeOH метанол
М моль/л
m мультиплет
мг миллиграмм
МГц мегагерц
мл миллилитр(миллилитры)
мин минуты
ммоль миллимоль
ЯМР ядерный магнитный резонанс
PEI полиэтиленимин
PPU пропилпиридилмочевина
q квартет
rt комнатная температура
мкл микролитр(микролитры)
мкМ мкмоль/л
s синглет
SFC сверхкритическая флюидная хроматография
TLC тонкослойная хроматография
t триплет
TsOH моногидрат пара-толуолсульфоновой кислоты
Способы, применяемые для очистки соединений из примеров
Очистку промежуточных соединений и конечных продуктов осуществляли с помощью хроматографии с нормальной или обращенной фазой.
Флэш-хроматография
Хроматографию с нормальной фазой проводили с применением предварительно заполненных SiO2 картриджей (например, колонки RediSep® Rf от Teledyne Isco, Inc.) при элюировании с помощью градиентов подходящих систем растворителей (например, гексаны и этилацетат; DCM и MeOH; или если не указано иное).
Пример 1. Синтез соединения 1
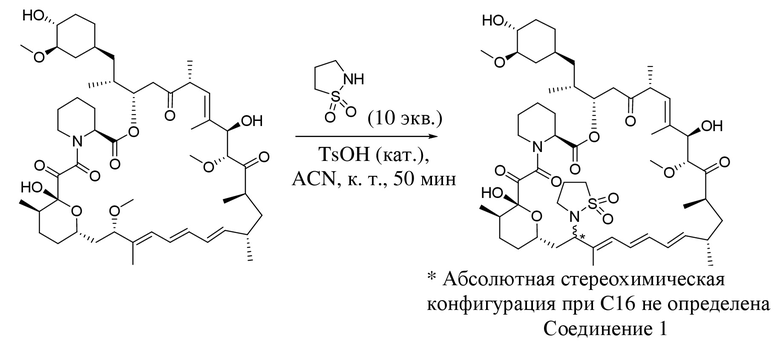
Рапамицин (0,549 г, 0,601 ммоль) объединяли с изотиазолидин-1,1-диоксидом (0,728 г, 6,01 ммоль) в безводном ацетонитриле (3,0 мл) в реакционном сосуде. Добавляли TsOH (0,011 г, 0,060 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 50 минут. Реакционную смесь разбавляли солевым раствором и экстрагировали трижды с помощью EtOAc. Органические экстракты объединяли, сушили над Na2SO4, декантировали и концентрировали с получением неочищенного продукта в виде желтого масла (~1 г). Неочищенный продукт очищали с помощью колоночной флэш-хроматографии на силикагеле (0-50% ацетона в гептане, градиентное элюирование ISCO CombiFlash, колонка FLH-R10017B-ISO40 с 40 г силикагеля SiliCycle с размером частиц 15-40 мкм, TLC 40% ацетона в гептане, визуализация под УФ). Фракции, содержащие продукт, проверяли с помощью LCMS, и фракции с самой высокой чистотой объединяли и концентрировали с получением соединения 1 (0,315 г, 0,298 ммоль, выход 49,7%) в виде белого твердого вещества
Соединение 1: ESIMS [M+NH4]+ 1020,7, [M-H]- 1001,8
HRMS: [M+Na]+ 1025,5367.
1H ЯМР (400 МГц, Хлороформ-d) δ 6,39 (dd, J=14,7, 10,7 Гц, 1H), 6,22 (dd, J=14,7, 10,6 Гц, 1H), 6,07 (dd, J=14,9, 10,6 Гц, 1H), 6,00 (d, J=10,9 Гц, 1H), 5,40 (d, J=10,0 Гц, 1H), 5,33 (dd, J=14,8, 9,8 Гц, 1H), 5,24-5,17 (m, 1H), 5,00 (td, J=5,9, 3,5 Гц, 1H), 4,57 (dd, J=10,8, 2,4 Гц, 2H), 4,27 (d, J=3,8 Гц, 1H), 4,05-3,94 (m, 2H), 3,63-3,48 (m, 2H), 3,39 (s, 3H), 3,33 (s, 4H), 3,30-3,16 (m, 2H), 3,11-2,98 (m, 2H), 2,98-2,85 (m, 2H), 2,68 (dd, J=17,5, 6,5 Гц, 1H), 2,52 (dd, J=17,3, 5,4 Гц, 1H), 2,47-2,38 (m, 2H), 2,38-2,31 (m, 1H), 2,31-2,25 (m, 2H), 2,23-2,15 (m, 1H), 1,99 (m, 2H), 1,92-1,85 (m, 1H), 1,82 (m, 5H), 1,76-1,70 (m, 6H), 1,64 (m, 4H), 1,58-1,43 (m, 3H), 1,40 (m, 1H), 1,34 (m, 1H), 1,25 (m, 2H), 1,18-1,11 (m, 1H), 1,11-1,00 (m, 10H), 1,00-0,84 (m, 7H), 0,57 (q, J=11,9 Гц, 1H).
Пример 2. Синтез соединений 2 и 3
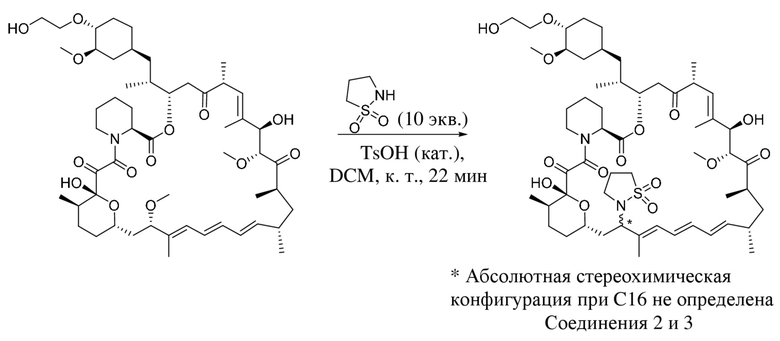
RAD001 (эверолимус, 1,0 г, 1,044 ммоль) объединяли с изотиазолидин-1,1-диоксидом (1,264 г, 10,44 ммоль) в безводном дихлорметане (5,2 мл) в реакционном сосуде. Добавляли одной порцией TsOH (0,020 г, 0,104 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 22 минут.
Реакционную смесь разбавляли насыщенным водным раствором NaHCO3 и затем экстрагировали четыре раза с помощью EtOAc. Органические экстракты объединяли, сушили над Na2SO4, декантировали и концентрировали с получением неочищенного продукта в виде оранжевой смолы (2,181 г).
Порцию (1,436 г) неочищенного продукта очищали с помощью колоночной флэш-хроматографии на силикагеле (15-50% ацетона в гептане, градиентное элюирование ISCO CombiFlash, колонка FLH-R10017B-ISO40 с 40 г силикагеля SiliCycle с размером частиц 15-40 мкм, TLC 40% ацетона в гептане, визуализация под УФ). При элюировании в ходе TLC наблюдали два пятна.
Фракции, содержащие продукт, проверяли с помощью LCMS и фракции из первого пика элюирования с самой высокой чистотой объединяли и концентрировали с получением соединения 2 (0,080 г, 0,073 ммоль, выход 6,95%) в виде белого твердого вещества.
Соединение 2: ESIMS [M+NH4]+ 1064,8, [M-H]- 1046,3.
HRMS: экспериментальная величина для C55H86N2O15SNa: 1069,5248.
1H ЯМР (400 МГц, Хлороформ-d) δ 6,45-6,24 (m, 2H), 6,13 (dd, J=15,1, 9,7 Гц, 1H), 5,96 (d, J=9,8 Гц, 1H), 5,62 (dd, J=15,1, 8,6 Гц, 1H), 5,48-5,37 (m, 1H), 5,30 (d, J=5,9 Гц, 1H), 5,20 (s, 1H), 5,14 (q, J=5,9 Гц, 1H), 4,14 (d, J=6,5 Гц, 1H), 3,88-3,72 (m, 3H), 3,72-3,65 (m, 2H), 3,62-3,56 (m, 2H), 3,50-3,47 (m, 1H), 3,45-3,38 (m, 5H), 3,33 (s, 3H), 3,28-3,04 (m, 6H), 3,04-2,89 (m, 2H), 2,89-2,71 (m, 1H), 2,71 (d, J=5,6 Гц, 1H), 2,34-2,21 (m, 4H), 2,14-2,08 (m, 1H), 2,07-1,98 (m, 2H), 1,97-1,83 (m, 3H), 1,82 (m, 1H), 1,77-1,69 (m, 7H), 1,63-1,48 (m, 4H), 1,44-1,37 (m, 3H), 1,34-1,18 (m, 5H), 1,14-1,09 (dd, J=6,8, 2,9 Гц, 4H), 1,08-0,83 (m, 14H), 0,75-0,64 (m, 1H).
Фракции, содержащие продукт, проверяли с помощью LCMS и фракции из второго пика элюирования с самой высокой чистотой объединяли и концентрировали с получением соединения 3 (0,085 г, 0,077 ммоль, 7,39%) в виде белого твердого вещества.
Соединение 3: ESIMS [M+NH4]+ 1064,7, [M-H]- 1046,1.
HRMS: экспериментальная величина для C55H86N2O15SNa: 1069,5630.
1H ЯМР (400 МГц, Хлороформ-d) δ 6,39 (dd, J=14,7, 10,8 Гц, 1H), 6,22 (dd, J=14,7, 10,6 Гц, 1H), 6,07 (dd, J=14,9, 10,6 Гц, 1H), 6,00 (d, J=10,8 Гц, 1H), 5,41 (dt, J=10,0, 1,5 Гц, 1H), 5,33 (dd, J=14,9, 9,8 Гц, 1H), 5,23-5,17 (m, 1H), 5,00 (m, 1H), 4,59-4,51 (m, 2H), 4,27 (m, 1H), 4,04-3,94 (m, 2H), 3,81-3,72 (m, 1H), 3,69 (m, 2H), 3,63-3,49 (m, 3H), 3,43 (s, 3H), 3,32 (s, 3H), 3,28-2,89 (m, 6H), 2,68 (dd, J=17,4, 6,4 Гц, 1H), 2,55-2,23 (m, 8H), 2,19 (d, J=16,0 Гц, 1H), 2,05-1,97 (m, 2H), 1,92-1,77 (m, 5H), 1,76-1,68 (m, 6H), 1,68-1,58 (m, 4H), 1,57-1,47 (m, 2H), 1,47-1,34 (m, 2H), 1,33-1,20 (m, 3H), 1,16-1,10 (m, 1H), 1,04 (t, J=6,5 Гц, 7H), 0,99-0,84 (m, 11H), 0,64 (q, J=12,0 Гц, 1H).
Пример 3. Синтез соединения 4
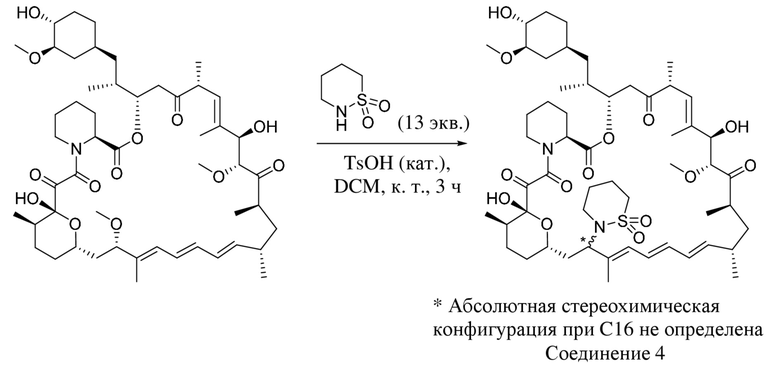
Рапамицин (0,464 г, 0,508 ммоль) объединяли с 1,4-бутансультамом (0,892 г, 6,60 ммоль) в реакционном сосуде. Твердые вещества растворяли в безводном дихлорметане (2,5 мл). Добавляли одной порцией TsOH (9,65 мг, 0,051 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение трех часов.
Реакционную смесь разбавляли насыщенным водным раствором NaHCO3 и четыре раза экстрагировали с помощью EtOAc. Органические экстракты объединяли, сушили над Na2SO4, подвергали вакуумной фильтрации через целит и концентрировали с получением неочищенного продукта в виде оранжево-желтого твердого вещества (~1,2 г).
Неочищенный продукт очищали с помощью колоночной флэш-хроматографии на силикагеле (0-70% ацетона в гептане, градиентное элюирование Isco CombiFlash, колонка с 40 г диоксида кремния RediSep GOLD, TLC в 50% ацетона в гептане, визуализация под УФ) с получением соединения 4 (0,060 г, 0,056 ммоль, выход 11,0%) в виде желтого твердого вещества.
Соединение 4: ESIMS [M+NH4]+ 1037,7, [M-H]- 1015,7.
HRMS: экспериментальная величина для C54H84N2O14SNa: 1039,5544.
1H ЯМР (600 МГц, Хлороформ-d) δ 6,38 (dd, J=14,8, 10,8 Гц, 1H), 6,22 (dd, J=14,8, 10,6 Гц, 1H), 6,07 (dd, J=15,0, 10,6 Гц, 1H), 5,96 (d, J=10,8 Гц, 1H), 5,37 (d, J=10,1 Гц, 1H), 5,33 (dd, J=15,0, 9,9 Гц, 1H), 5,19 (d, J=5,6 Гц, 1H), 5,06 (dt, J=9,7, 4,4 Гц, 1H), 4,84-4,78 (m, 1H), 4,30 (t, J=2,4 Гц, 1H), 4,18 (s, 1H), 4,07 (m, 1H), 4,03 (m, 1H), 3,66 (d, J=13,9 Гц, 1H), 3,39 (s, 3H), 3,37-3,29 (m, 5H), 3,22 (dq, J=10,1, 6,6 Гц, 1H), 3,16-3,12 (m, 1H), 3,09-3,04 (m, 1H), 3,02-2,97 (m, 2H), 2,96-2,89 (m, 1H), 2,69 (dd, J=17,7, 5,5 Гц, 1H), 2,45-2,38 (m, 2H), 2,33-2,16 (m, 5H), 2,04-1,94 (m, 2H), 1,82 (s, 3H), 1,81-1,68 (m, 8H), 1,65-1,59 (m, 7H), 1,56-1,42 (m, 4H), 1,41-1,20 (m, 5H), 1,13-0,96 (m, 9H), 0,93 (dd, J=8,9, 6,6 Гц, 6H), 0,88 (m, 3H), 0,57 (q, J=11,9 Гц, 1H).
Пример 4. Биологические анализы и данные
Активность соединения в соответствии с настоящим изобретением оценивали с помощью следующих способов in vitro.
Определение фармакологических характеристик
Материалы и способы
Клеточный анализ для определения активности рапалогов. Активность рапалогов определяли с применением анализа на основе клеток MEF TSC1-/-. Клетки MEF TSC1-/- представляют собой эмбриональные фибробласты мыши с дефицитом по комплексу-1 туберозного склероза - TSC1, который оказывает отрицательную регуляцию на сигнальный путь mTORC1, и, значит, они демонстрируют конститутивную активацию mTORC1, приводящую к фосфорилированию (активации) последующих молекул. Данный клеточный анализ применяют для измерения ингибирования (дефосфорилирования) S6 и 4EBP1 под действием рапалогов или другими ингибиторов mTOR.
Клетки MEF TSC1-/- высевали в покрытые поли-D-лизином 384-луночные планшеты Greiner с прозрачным дном и инкубировали на протяжении ночи при 37°C, 5% CO2. На следующий день клетки промывали 8 раз раствором "сильного голода" (1 л DPBS+1 г D(+)-глюкозы + 10 мл 7,5% раствора бикарбоната натрия + 20 мл 1 М HEPES) и инкубировали в течение дополнительных 2 часов в том же растворе. Затем клетки обрабатывали соединениями с понижающейся концентрацией (8 значений при разбавлениях в 3,16-раз) и инкубировали в течение 2 часов при 37°C, 5% CO2. Клетки фиксировали с помощью 4% параформальдегида в течение 30 мин и 5 раз промывали с помощью TBS-EDTA с последующим иммунным окрашиванием меченными флуоресцентной меткой антителами к pS6 (Ser240/244) (Cell Signaling №9468) и p4EBP1 (Thr 37/46) (Cell Signaling №5123). Ядра делали видимыми с помощью красителя Hoechst (ThermoFisher Scientific №H3570). Клетки визуализировали (InCell 600) с использованием соответствующих каналов флуоресценции и активность ингибиторов mTOR определяли с помощью IC50 (нМ) pS6.
Получение клеток 293T с нокаутом по FKPB12. Систему CRISPR/Cas9 применяли для доставки рибонуклеопротеиновых комплексов, содержащих последовательность направляющей РНК (gRNA), которая нацеливается на FKBP12 (GCCACTACTCACCGTCTCCT (SEQ ID NO: 1)), в клетки 293T с применением набора Amaxa® 4D-Nucleofector™ X (Lonza, V4XC-2032). Клоны клеток подвергали скринингу путем иммуноблоттинга с применением антитела к FKBP12 (Novus, NB300-508) и отбирали одиночные клоны, демонстрирующие полный нокаут FKBP12 (отсутствие измеримого уровня FKBP12).
Обработка клеток 293T дикого типа (WT) и с нокаутом по FKBP12 с помощью RAD001 и соединения 1. Клетки 293T WT и с нокаутом по FKBP12 высевали при плотности, составляющей 30000 клеток на лунку, в покрытые поли-D-лизином 96-луночные планшеты (Corning, № 354461) в модифицированную Дульбекко среду Игла (ThermoFisher, № 11995-065), дополненную 10% фетальной бычьей сыворотки (ThermoFisher, № 16140-071). Клетки инкубировали при 37°C, 5% CO2 в течение 48 часов, до достижения ими ~80% конфлюэнтности. Клетки обрабатывали с помощью RAD001 и соединения 1 с использованием диапазона доз из 12-значений от 1000 нМ до 0,0033 нМ в течение 2 часов при 37°C в двух повторностях. Среду, дополненную чистым диметилсульфоксидом (DMSO), применяли в качестве контроля для обоих соединений. Количества фосфорилированного S6K1 (Thr389) определяли с помощью набора для сэндвич-ELISA (Cell signaling, № 7063C) в соответствии с протоколом производителя.
SPR-анализ для определения аффинности связывания с FK506-связывающими белками (FKBP).
Слияния FKBP с N-концевой avi-his6 меткой ("his6" раскрытой как SEQ ID NO: 2), содержащие FKBP12, FKBP51 и FKBP52, экспрессировали в E. coli и очищали с применением стандартный хроматографии. Каждый белок впоследствии иммобилизировали на чипе со стрептавидином в приборе для SPR Biacore 8K (GE Healthcare). В режиме одноциклового кинетического анализа титрации соединения пропускали при скорости 45 мкл/мин над каждой поверхностью с применением 2-минутной фазы ассоциации и 30-минутной фазы диссоциации в буфере, содержащем 50 мМ Tris с pH 7,5/150 мМ NaCl/0,01% Tween 20/1 мМ DTT/2% DMSO. Данные аппроксимировали с применением одноциклового кинетического анализа для низкомолекулярных соединений (LMW). Приведены равновесные константы диссоциации (KD).
Различные показатели фармакологии рапалогов могут достигаться в различных типах клеток или тканей в зависимости от: 1) относительной распространенности гомологов FKBP в данных клетках/тканях, и 2) специфичности связывания рапалогов с данными различными гомологами FKBP (Mol. Cell Biol. (2013) 33:1357-1367).
Результаты
Активность соединений по настоящему изобретению (таблица 1) в качестве ингибиторов mTOR in vitro определяли с помощью IC50 (нМ) pS6 в клетках MEF TSC1-/-.
Таблица 1
Значения IC50 рассчитывают как средние из нескольких анализов.
Равновесные константы диссоциации (KD) с FKBP12, FKBP51 и FKBP52 для соединений по настоящему изобретению перечислены в таблице 2.
Таблица 2
(n=7)
(n=1)
(n=1)
(n=7)
(n=7)
(n=6)
(n=1)
(n=1)
(n=5)
(n=5)
(n=4)
(n=2)
(n=2)
Ингибирование mTORC1 под действием соединения 1 зависит специфически от FKBP12, в то время как остальные FKBP в дополнение к FKBP12 могут усиливать эффект RAD001.
Количества фосфорилированного S6K1 (Thr389) измеряли в клетках 293T дикого типа и с нокаутом по FKBP12, обработанных с помощью соединения 1 или RAD001. S6K1 является нижележащей мишенью mTORC1, и фосфорилирование его рапалог-чувствительного сайта Thr389 используется в качестве показателя функциональной активности mTORC1 (Lee, C. H., Inoki, K. and Guan, K. L. (2007). mTOR pathway as a target in tissue hypertrophy. Annu. Rev. Pharmacol. Toxicol. 47, 443-467). В клетках 293T дикого типа как соединение 1, так и RAD001 были эффективными в достижении ~70-80% ингибирования фосфорилирования S6K1(Thr389) (фигура 1A). В отсутствие FKBP12 соединение 1 более не приводило к ингибированию фосфорилирования S6K1(Thr389) при всех протестированных концентрациях, в то же время не более ~50% ингибирования S6K1(Thr389) достигалось с участием RAD001, что демонстрирует, что RAD001 может действовать через другие FKBP, кроме FKBP1, при этом соединению 1 для проявления его активности требуется FKBP12 (фигура 1B).
Не ограничиваясь конкретной теорией, такие результаты свидетельствуют о том, что ингибирующий эффект соединения 1 в отношении mTORC1 опосредован только FKBP12; т. е. соединение 1 является высокоселективным в отношении FKBP12, и следовательно он требуется для ингибирования mTORC1. В случае RAD001, напротив, другие FKBP в дополнение к FKBP12 усиливают его способность ингибировать mTORC1. Исходя из высокой специфичности соединения 1 в отношении FKBP12, фармакологические эффекты соединения 1 могут быть селективными для клеток, в которых FKBP12 является преобладающим гомологом и где FKBP12 экспрессируется на достаточных уровнях, с одновременным недопущением ингибирования mTORC1 в клетках с низкой (недостаточной) экспрессией FKBP12.
Таким образом, после описания нескольких аспектов нескольких вариантов осуществления, специалистам в данной области техники должны быть понятны различные изменения, модификации и улучшения. Подразумевается, что такие изменения, модификации и улучшения являются частью настоящего изобретения и находятся в пределах сущности и объема настоящего изобретения. Соответственно, вышеприведенное описание и графические материалы приведены только в качестве примера.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> NOVARTIS AG
<120> ПРОИЗВОДНЫЕ РАПАМИЦИНА, СОДЕРЖАЩИЕ ИЗОТИАЗОЛИДИН-1,1-ДИОКСИД И 1,4-
БУТАНСУЛЬТОН, И ПУТИ ИХ ПРИМЕНЕНИЯ
<130> PAT058487
<140>
<141>
<150> PCT/IB2020/052825
<151> 2020-03-25
<150> 62/824,190
<151> 2019-03-26
<160> 2
<170> PatentIn версия 3.5
<210> 1
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетический олигонуклеотид
<400> 1
gccactactc accgtctcct 20
<210> 2
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: Синтетическая 6xHis метка
<400> 2
His His His His His His
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ РАПАМИЦИНА | 2018 |
|
RU2807188C2 |
| C26-СВЯЗАННЫЕ АНАЛОГИ РАПАМИЦИНА В КАЧЕСТВЕ ИНГИБИТОРОВ mTOR | 2019 |
|
RU2826559C2 |
| С40-, С28- И С-32-СВЯЗАННЫЕ АНАЛОГИ РАПАМИЦИНА В КАЧЕСТВЕ ИНГИБИТОРОВ MTOR | 2019 |
|
RU2805211C2 |
| АНАЛОГИ РАПАМИЦИНА КАК ИНГИБИТОРЫ mTOR | 2018 |
|
RU2828109C2 |
| ПРИМЕНЕНИЕ АНТАГОНИСТОВ МИОСТАТИНА, СОДЕРЖАЩИЕ ИХ КОМБИНАЦИИ И ИХ ПРИМЕНЕНИЕ | 2016 |
|
RU2781401C2 |
| ДИПЕПТИДИЛКЕТОАМИД META-МЕТОКСИФЕНИЛПРОИЗВОДНЫЕ И ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2787766C2 |
| СПОСОБЫ, СОЕДИНЕНИЯ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ СВЯЗАННЫХ С АНГИОТЕНЗИНОМ ЗАБОЛЕВАНИЙ | 2014 |
|
RU2688163C2 |
| Замещенные цианопирролидины, обладающие активностью ингибиторов USP30 | 2020 |
|
RU2822680C1 |
| ИНГИБИТОРЫ ДЕКАРБОКСИЛАЗЫ ПОЛУАЛЬДЕГИДА α-АМИНО-β-КАРБОКСИМУКОНОВОЙ КИСЛОТЫ | 2019 |
|
RU2841136C2 |
| ТЕТРАГИДРОПИРАНИЛ АМИНО-ПИРРОЛОПИРИМИДИНОН И СПОСОБЫ ЕГО ПРИМЕНЕНИЯ | 2020 |
|
RU2747991C1 |
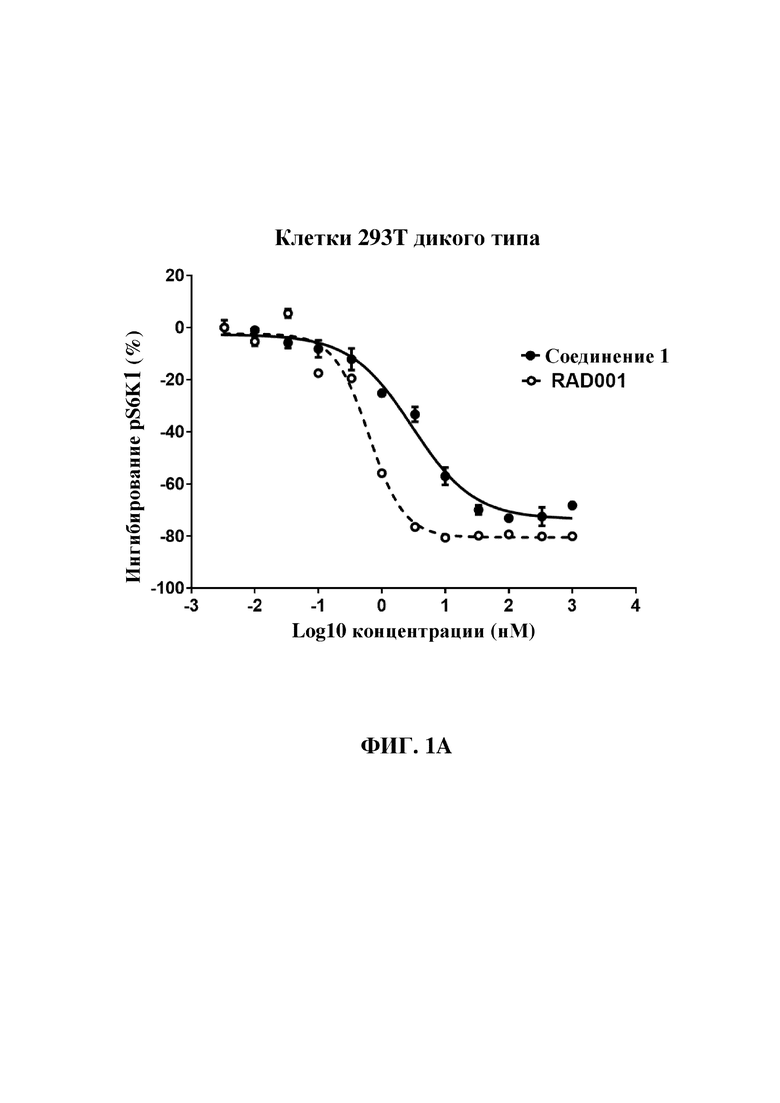
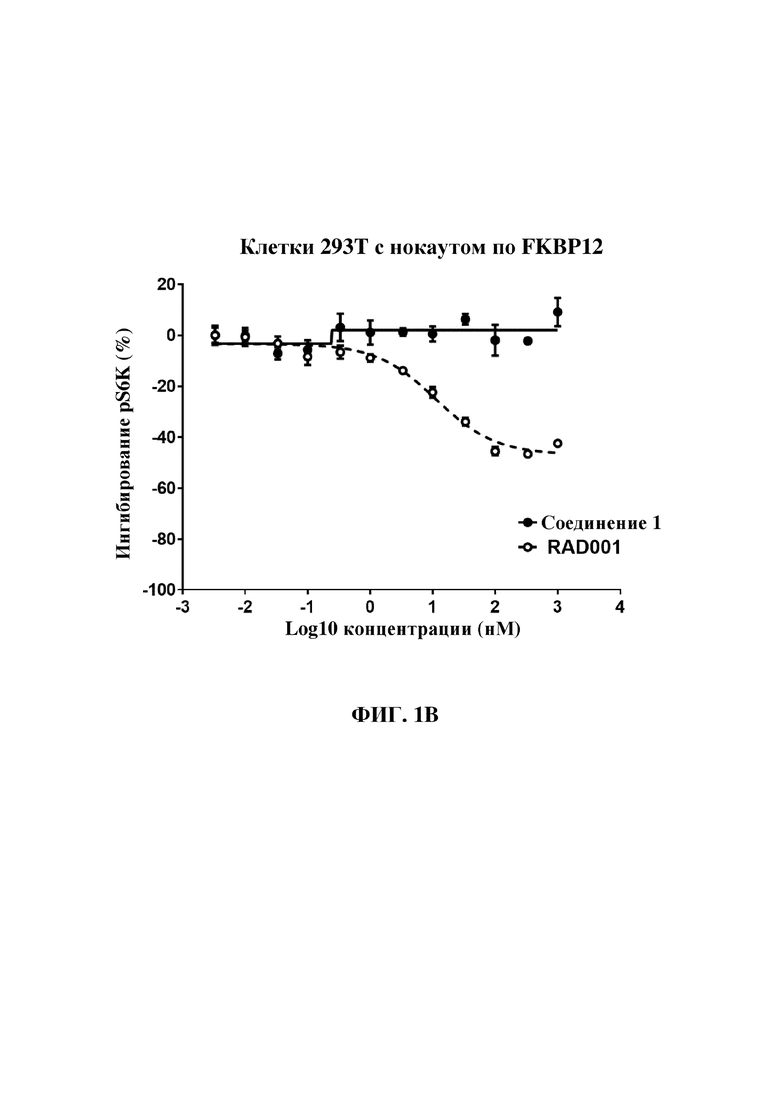
Изобретение относится к соединению формулы (I) или его фармацевтически приемлемой соли, которые являются ингибиторами mTORC1. В формуле (I) R1 выбран из группы, состоящей из водорода и гидроксил-C1-6алкила, и R2 представляет собой 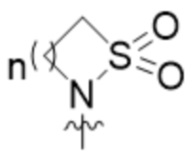 , где n составляет 1, 2 или 3. Изобретение относится также к конкретным соединениям формулы (I). 4 н. и 3 з.п. ф-лы, 1 ил., 2 табл., 4 пр.
, где n составляет 1, 2 или 3. Изобретение относится также к конкретным соединениям формулы (I). 4 н. и 3 з.п. ф-лы, 1 ил., 2 табл., 4 пр.
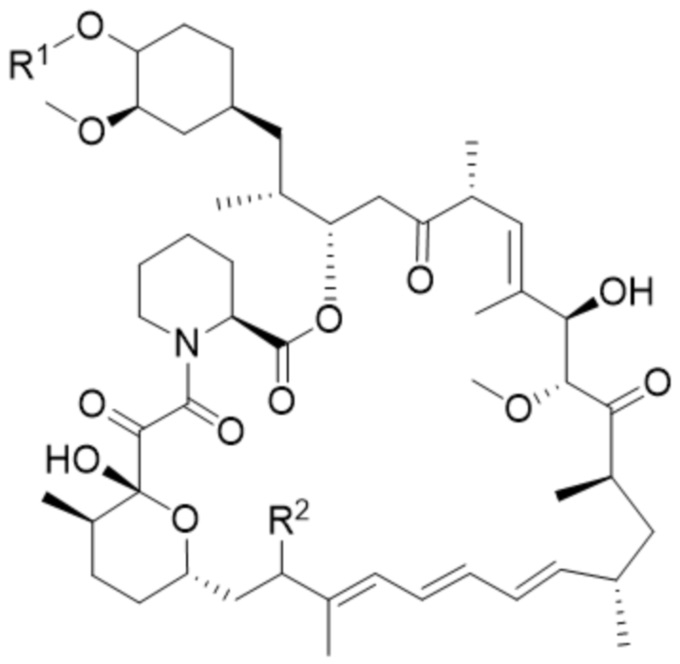 (I)
(I)
1. Соединение формулы (I) или его фармацевтически приемлемая соль
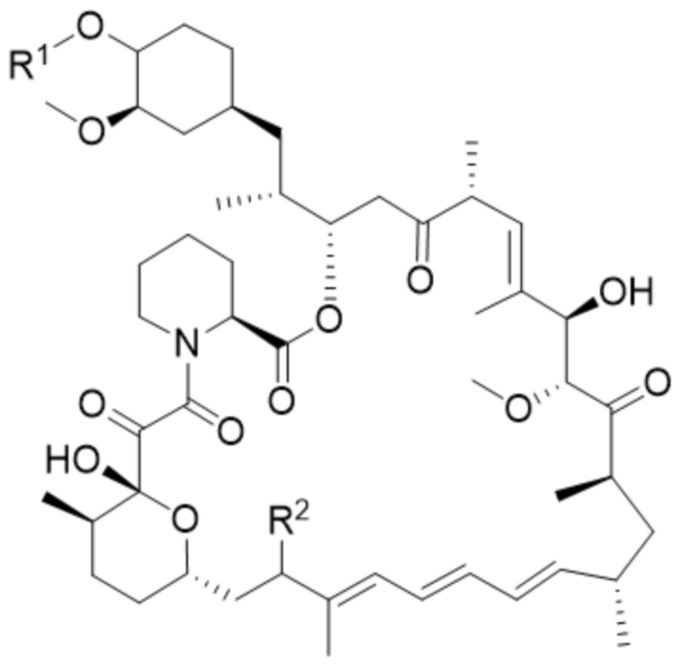 (I),
(I),
где R1 выбран из группы, состоящей из водорода и гидроксил-C1-6алкила; и
R2 представляет собой 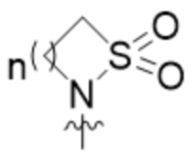 , где n составляет 1, 2 или 3.
, где n составляет 1, 2 или 3.
2. Соединение по п. 1 или его фармацевтически приемлемая соль, где R1 выбран из группы, состоящей из водорода и 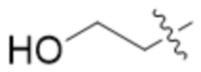 .
.
3. Соединение по п. 1 или 2 или его фармацевтически приемлемая соль, где R2 представляет собой 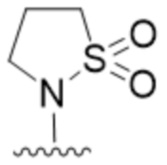 .
.
4. Соединение по п. 1 или 2 или его фармацевтически приемлемая соль, где R2 представляет собой 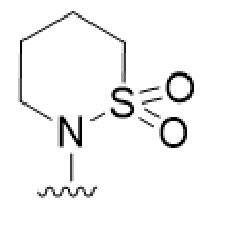 .
.
5. Соединение структурной формулы
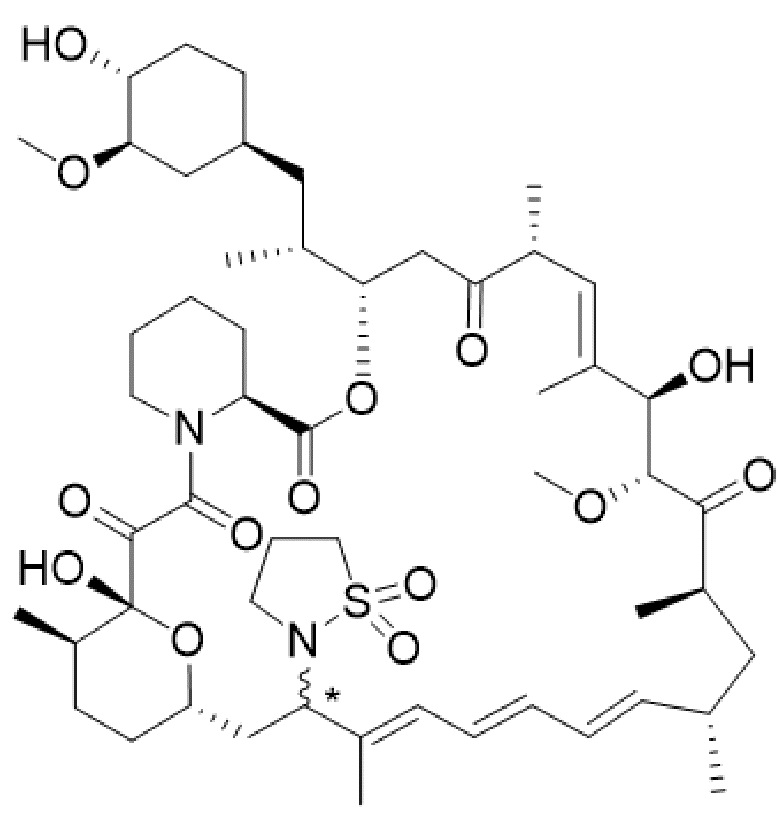
или его фармацевтически приемлемая соль.
6. Соединение структурной формулы
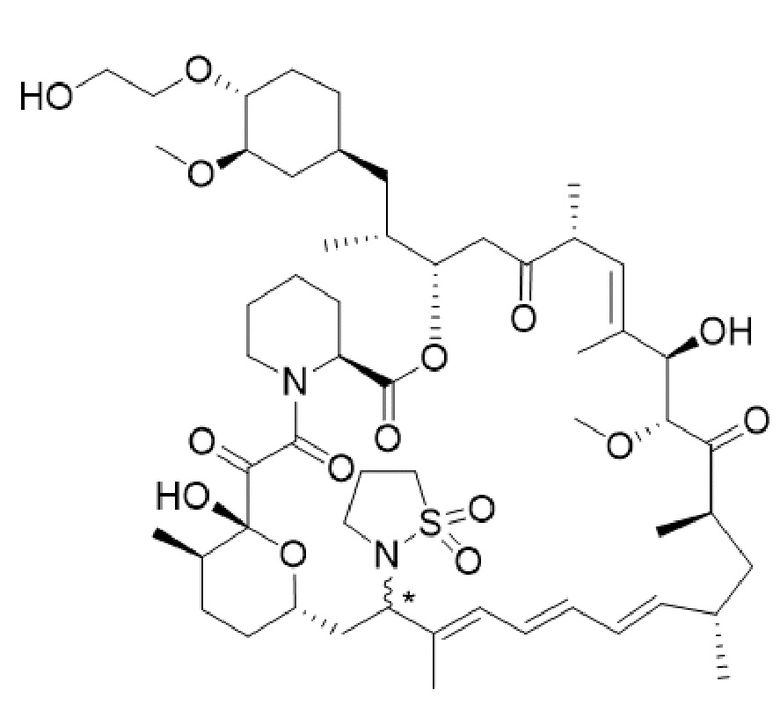
или его фармацевтически приемлемая соль.
7. Соединение структурной формулы
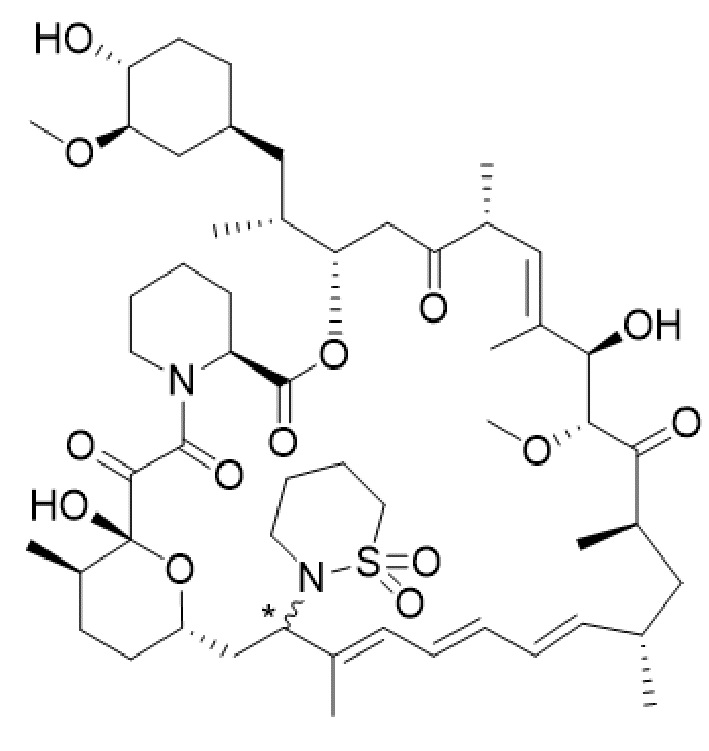
или его фармацевтически приемлемая соль.
| WO 2017044720 А1, 16.03.2017 | |||
| Способ получения перегретого пара и устройство для его осуществления | 1982 |
|
SU1212331A3 |
| WO 2007096174 А1, 30.08.2007 | |||
| J | |||
| I | |||
| LUENGO ET AL., Manipulation of the Rapamycin Effector Domain | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| ORG | |||
| CHEM., 1994, vol | |||
| Устройство для охлаждения водою паров жидкостей, кипящих выше воды, в применении к разделению смесей жидкостей при перегонке с дефлегматором | 1915 |
|
SU59A1 |
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| ДВИГАТЕЛЬ ДИЗЕЛЯ ДЛЯ ТЕПЛОВОЗА | 1926 |
|
SU6512A1 |
| ПРОИЗВОДНЫЕ РАПАМИЦИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ СТИМУЛИРОВАНИЯ ИММУНОДЕПРЕССИИ | 1993 |
|
RU2126409C1 |
Авторы
Даты
2025-03-19—Публикация
2020-03-25—Подача