Изобретение относится к области медицины, конкретно к фармакологии, и касается применения N-карбамоил-метил-4-фенил-2-пирролидона для повышения уровня нейротрофического фактора головного мозга (BDNF) в крови животных в модели хронического непредсказуемого умеренного стресса.
В настоящее время синдром профессионального выгорания (СПВ) признан медицинским расстройством и имеет собственный код Международной классификации болезней (МКБ) - МКБ-10 (Z73.0 - Burn-out, Переутомление) и МКБ-11 (QD85 - Burnout). В МКБ-11 СПВ определяется как синдром, являющийся результатом хронического стресса на рабочем месте, с которым не удается справиться. Он характеризуется тремя проявлениями: 1) чувством изнеможения или истощения энергии (feelings of energy depletion or exhaustion); 2) повышенная психическая дистанцированность от работы или чувство негативизма или цинизма по отношению к работе; и 3) чувство неэффективности и отсутствия выполненного долга [1].
В научно-популярной литературе, в СМИ, в интернете и повседневной речи данное состояние получило устойчивое выражение - эмоциональное выгорание.
В научную литературу термин «выгорание» ввела Кристина Маслач (Maslach С), которая определила это состояние как постепенный процесс утомления, появление цинизма и снижение интереса к профессиональной деятельности [2]. Позже Maslach С.и Jackson S.E. разработали более строгое и функциональное определение выгорания как психологического синдрома, характеризующегося эмоциональным истощением, деперсонализацией и снижением чувства профессиональной эффективности и разработали опросник MBI, как единый инструмент оценки (Maslach Burnout Inventory, МВ1) [3]-[4].
Данная трехфакторная модель Maslach С. является наиболее распространенной, и взята за основу в определения синдрома выгорания в МКБ.
Хотя концепция выгорания, предложенная Maslach С. и Jackson S.E, остается наиболее общепринятой в научной литературе, существуют и другие определения или формулировки. Так, например, концепция эмоционального выгорания, выдвинутая Shirom А. и Melamed S., описывает выгорание как хроническое истощение энергетических ресурсов человека из-за хронического стресса. В этой концепции СПВ включает развитие физической усталости, эмоционального истощения и снижения когнитивных функций, что значительно отличается от определения Maslach С. [5]. Однако все концепции выгорания, несмотря на некоторые различия, подчеркивают истощение (физическое и эмоциональное) как основной компонент СПВ [6].
Выгорание рассматривалось изначально как явление, исключительно связанное с профессиональным контекстом. Но, на сегодняшний день это термин приобрел более широкое понимание и таким образом, выгорание, определяемое как симптомы истощения из-за длительного воздействия любой эмоционально сложной ситуации, не может быть определено как исключительно связанное с работой [6].
В современной литературе обсуждается несколько теорий развития выгорания, которые не противоречат друг другу, а дополняют друг друга. Рассматриваются следующие теории: (1) социальная когнитивная теория; (2) теория социального обмена; (3) организационная теория; (4) структурная теория; (5) «требования-ресурсы»; (6) теория эмоционального заражения [7]. Теория «требования-ресурсы» (Demands-Resources Theory) постулирует, что выгорание происходит, когда образуется дисбаланс между требованиями к работе и ресурсами, в том числе внутренними, которые необходимы для выполнения работы. Требования к работе - те факторы, которые требуют постоянных физических или умственных усилий и связаны с определенными физиологическими затратами из-за активации гипоталамо-гипофизарно-надпочечниковой системы и психологическими затратами (например, субъективная усталость, снижение концентрации внимания и переопределение требований к задаче). Когда восстановление перед лицом таких требований оказывается недостаточным или неадекватным, возникает состояние физического и психического истощения [8].
Как видно из описанных подходов, СПВ рассматривается, в основном, как психологический феномен. Но, будучи по своей природе психологическим феноменом, СПВ приводит к ряду неблагоприятных последствий, затрагивающих и физиологические функции организма. Изначально последствия СПВ носят психологический характер, но сохраняясь с течением времени, они переходят в неблагоприятное воздействие на физическое/биологическое здоровье и поведение человека, что, в свою очередь, имеет нежелательные последствия для общества. Психологические изменения, вызванные синдромом выгорания на работе, происходят как на когнитивном, так и на эмоциональном уровнях. Различные исследования связывают этот синдром с проблемами концентрации и памяти, трудностями в принятии решений, снижением способности справляться с возникшими сложностями, тревожностью, депрессией, неудовлетворенностью жизнью, низкой самооценкой, бессонницей, раздражительностью и повышенным потреблением алкоголя и табака [9]. Индивидуумы с более высоким уровнем выгорания чаще страдают от различных проблем со здоровьем, таких как мышечно-скелетная боль, заболевания органов желудочно-кишечного тракта, сердечно-сосудистые заболевания, головные боли, повышенная восприимчивость к инфекциям, а также бессонница и хроническая усталость [10].
Важно отметить и то, что все симптомы проявляются неодинаково у всех людей, и они не обязательно должны возникать у всех индивидуумов, подверженных СПВ, что характеризует СПВ как синдром, течение которого высоко вариативно. Форма и развитие этих индивидуальных последствий (психологических, медицинских и поведенческих) крайне разнообразны. В этом смысле, хотя их не всегда легко разграничить, были описаны четыре уровня синдрома эмоционального выгорания от легкой формы с некоторой усталостью и снижением работоспособности до экстремальной (изоляция, агрессивность, экзистенциальный кризис, хроническая депрессия и попытки самоубийства) [7].
Большинство исследований СПВ сфокусировано на изучении функциональных изменений гипоталамо-гипофизарной-надпочечниковой (ГГН) оси. Это обоснованно, поскольку ГГН ось вместе с вегетативной нервной системой являются двумя ключевыми компонентами острой стрессовой реакции, ответственными за мобилизацию успешного адаптивного ответа на различные стрессоры. Функция ГГН оси при выгорании в основном оценивалась по изменению уровня кортизола, как при пробуждении, так и за сутки. Несмотря на большое количество исследований по данному направлению, полученные результаты носят разнонаправленный характер. В 2019 году были проанализированы данные 41 исследования на людях по изучению влияния различных форм выгорания на уровень кортизола [6]. В 50% исследований не было выявлено устойчивой связи между СПВ и уровнем кортизола, увеличение уровня у индивидуумов с СПВ было показано в 20% исследованиях, и снижение - в 30%.
По мнению ряда исследователей при правильном измерении кортизол является отличным индикатором острых стрессовых реакций, тогда как его применимость в качестве маркера хронического стресса весьма сомнительна, в том числе из-за наличия существенных циркадных и ультрадианных колебаний уровня этого гормона. Общепризнано, что функциональная активность ГГН оси может быть нарушена у пациентов с СПВ, но для понимания динамики этих изменений необходимы дополнительные исследования [6].
Физиологическая реакция на стресс также включает выброс анаболических гормонов с защитными и регенеративными свойствами. Наиболее часто изучаемым анаболическим гормоном является дегидроэпиандростерон (ДГЭА). Однако результаты о взаимосвязи уровня ДГЭА и СПВ также не однозначные: показано увеличение, уменьшение, уровня ДГЭА при СПВ, или отсутствие различий между контрольной группой и группой с СПВ. Отсутствие однозначных результатов о связи СПВ отмечается и при анализе данных по уровням тестостерона, прогестерона и эстрадиола, гормонов щитовидной железы и/или тиреотропного гормона, пролактина. Исследования были посвящены изучению потенциальных изменений С-реактивного белка, цитокинов, общего числа лейкоцитов в крови, изменениям популяционного состава лимфоцитов. Но в этих исследованиях также не было выявлено убедительной связи между изменениями иммунологических биомаркеров и СПВ [6].
Дополнительную трудность в диагностике СПВ представляет дифференциальная диагностика с депрессией. Предполагается, что метилирование ДНК является возможным звеном, связывающим индивидуальную реакцию на стресс и психопатологию, и может рассматриваться как потенциальный биомаркер расстройств, связанных со стрессом. При СПВ и депрессии отмечены различные паттерны метилирования гена нейротрофического фактора головного мозга (BDNF). Метилирование тирозингидроксилазы (ТН) коррелировало с выгоранием в одном исследовании [11].
В последнее время активно изучается связь BDNF и СПВ. Показано, влияние полиморфизма гена BDNF на предрасположенность к развитию СПВ [12]-[13]. Показано также, что уровень BDNF в сыворотке крови ниже у индивидуумов, имеющих более высокую степень выраженности СПВ [14]-[15]. Изменения метилирования ДНК BDNF могут играть важную роль в снижении уровня белка BDNF при выгорании. Наличие депрессивных симптомов может иметь дополнительное влияние на эти изменения [16].
При СПВ может изменяться и уровень таких белков, такие как сосудистый эндотелиальный фактор роста (VEGF) и эпидермальный фактор роста (EGF). У пациентов с выгоранием наблюдали значительно более низкие уровни EGF, VEGF и BDNF. Учитывая важную роль BDNF и VEGF в пластичности мозга и нейрогенезе, снижение их уровня после длительного воздействия стресса может указывать на повышенный риск повреждения нейронов и когнитивных нарушений в этой группе пациентов [17].
Таким образом, по результатам клинических исследований, проведенных за последние несколько лет (2017-2021), можно заключить, что BDNF является наиболее перспективным из биологических маркеров кандидатом для диагностики СПВ, так как при СПВ наблюдается снижение концентрации этого фактора в крови, более того, степень снижения коррелирует со степенью выраженности СПВ.
Кроме физиологических изменений, у пациентов с СПВ отмечено ухудшение памяти, концентрации внимания по сравнению с показателями здоровых людей [18]. Исследования нейробиологических механизмов показали функциональное нарушение нейрональных сетей, связывающих лимбическую систему с префронтальной корой, и уменьшение объемов структур в базальных ганглиях на фоне СПВ [19].
В целом, следует отметить, что на сегодняшний день надежных биомаркеров СПВ, за исключением BDNF, не найдено, о чем свидетельствуют данные метаанализов и обзорных статей [6], [19], [20]. Более того, диагностика СПВ представляет определенные трудности в связи с общностью симптомов СПВ и такими расстройствами, как депрессия и тревожные расстройства. Также растет объем исследований, подтверждающих наличие некоей связи эмоционального истощения и депрессии. Предполагается, что выгорание и депрессия являются «отдельными явлениями, хотя они могут иметь несколько общих качественных характеристик» [21]. Предполагается также, что депрессия и эмоциональное выгорание - две взаимосвязанные, но разные концепции. В одном из масштабных исследований, целью которого было ответить на вопрос приводит ли СПВ к развитию депрессивно-подобной симптоматики, по результатам оценки состояния более чем 3000 врачей был сделан вывод о том, что СПВ является предиктором депрессивно-подобной симптоматики, а не наоборот [22]. С другой стороны, на склонность к развитию СПВ влияют некоторые индивидуальные особенности. Выявлено, что среди индивидуальных характеристик важнейшей переменной является депрессия.
Депрессия может быть причиной или последствием СПВ [23]. Некоторые исследователи подчеркивают тесную взаимосвязь эмоционального выгорания и депрессии, указывая на широкий спектр схожих симптомов [24]. Также существует мнение, что, что нет достаточных доказательств, чтобы предположить, что выгорание является отдельной сущностью, и предлагается рассматривать два основных симптома выгорания (истощение и деперсонализация) как депрессивные реакции на стрессовую профессиональную среду [25]. Таким образом, на сегодняшний день вопрос о том, в какой степени синдром эмоционального выгорания является отдельным заболеванием с определенными диагностическими критериями, обсуждается в научной литературе и существуют различные точки зрения. Обе патологии расцениваются как расстройства, связанные со стрессом. Уже понятно, что ни один из биологических маркеров не является достаточно информативным для дифференциальной диагностики, и вместо поиска одного конкретного отличительного маркера будущие исследования должны быть сосредоточены на разработке индексов выгорания и депрессии, которые комплексно оценивают различные факторы - генетические, нейробиологические, физиологические и факторы окружающей среды [26].
Для диагностики СПВ используются опросники, наиболее распространенным из которых является MBI (Maslach Burnout Inventory), предложенный К. Маслач [3] и его модификации. Также используются и другие опросники: CESQT (Questionnaire for the Evaluation of Burnout Syndrome), BAT (Burnout Assessment Tool), SMBQ (Shirom-Melamed Burnout Questionnaire) и другие [6].
В 2011 был предложен подход с комплексной оценкой СПВ с использованием так называемого индекса износа (allostatic load), который представляет собой сводный индекс показателей кумулятивной нагрузки на несколько органов и тканей, прежде всего биомаркеров, связанных с нейроэндокринной, сердечно-сосудистой, иммунной и метаболической системами, наряду с опросниками, позволяющими выявить состояние хронического стресса, эмоционального выгорания и депрессии. Используя данный индекс (путем сравнения ряда показателей с клиническими нормами) в исследовании было показано, что повышенный индекс связан с повышенным хроническим стрессом, симптомами эмоционального выгорания, но не с депрессивными симптомами. Авторы предполагают, что данный подход может быть полезен для оценки состояния СПВ, в том числе и с профилактической точки зрения [27].
Учитывая высокую социальную и экономическую значимость данного заболевания, что в особенности проявилось на фоне пандемии COVID-19 [28], актуальной задачей является поиск средств эффективной терапии СПВ.
Проблемы поиска таких препаратов связаны с высокой индивидуальной вариативностью протекания СПВ, сложностями дифференциальной диагностики, в том числе между СПВ и депрессией, отсутствием однозначных биомаркеров состояния, наличием факторов предрасположенности к развитию СПВ, отсутствием стандартов медикаментозного лечения, эффективных экспериментальных моделей СПВ.
Поиск средств фармакологической коррекции СПВ является актуальной задачей, так как на настоящий момент нет стандартных схем медикаментозного лечения СПВ. Современные стратегии преодоления СПВ, в основном, направлены на создание условий, предотвращающих риск развития СПВ. Для этого предложены различные подходы, включая снижение влияния стрессовых факторов (таких как перегруженный рабочий график) на работе, оптимизация организации работы, повышение профессиональных навыков, развитие навыков преодоления трудностей (например, когнитивная реструктуризация, разрешение конфликтов, тайм-менеджмент), периодическое тестирование работников на предмет наличия признаков СПВ, основное место в стратегии преодоления СПВ занимает психотерапия [7].
Медикаментозное лечение профессионального выгорания в основном симптоматическое: оно включает меры по профилактике и лечению симптомов. Поскольку симптомы различаются по степени тяжести у разных людей, существует индивидуальный подход при разработке плана интервенционного лечения, направленного на возникающие симптомы, а также сопутствующие расстройства, такие как тревога, беспокойство, головные боли, нарушения сна, проблемы, связанные с концентрацией внимания, постоянное чувство усталости, раздражительность, депрессия, повышенная чувствительность к боли, восприимчивость к инфекциям, мышечное напряжение, головокружения, желудочно-кишечные расстройства, гипертония, сердечно-сосудистые заболевания и другие расстройства.
Описанные симптомы стресса можно временно облегчить с помощью лекарственных средств, хотя они не устраняют причину стресса. Терапевтический эффект анксиолитиков и седативных средств, состоящий, в том числе, в снижении раздражительности и психомоторного возбуждения, хорошо известен. Анксиолитики назначают когда ожидаемая польза от лечения превышает потенциальную опасность. Основной проблемой является риск развития лекарственной зависимости. Люди, которым трудно справляться со стрессом, тревогой или нарушениями сна, могут злоупотреблять седативными средствами или стать зависимыми от них. Существуют также серьезные парадоксальные реакции, которые могут возникать в связи с использованием седативных средств, которые могут включать депрессию с суицидальными тенденциями или без них, фобии, агрессивное поведение и симптомы, иногда ошибочно диагностируемые как психозы. Анксиолитики иногда вызывают ухудшение памяти. Ухудшение памяти само по себе может привести в будущем к снижению работоспособности и, следовательно, является фактором риска СПВ [30].
Выгорание часто характеризуется нарушением сна. Стресс нарушает циркадный ритм секреции кортизола. Предполагается, что нарушение сна может играть роль в развитии усталости при выгорании [31]. При бессоннице рекомендуется кратковременное лечение снотворными. Снотворные следует назначать в наименьшей эффективной дозе на короткий период времени. При необходимости длительного лечения следует рекомендовать прерывистую терапию. Длительное использование не рекомендуется, поскольку может развиться толерантность.
Оптимальным лечением является сочетание гипнотиков с когнитивно-поведенческой терапией. Когнитивно-поведенческие стратегии более сложны в реализации и требуют больше времени, но их эффекты сохраняются дольше, до двух лет после окончания лечения [30]-[32].
Низкие дозы некоторых антидепрессантов перед сном могут улучшить сон. Например, доксепин в дозе от 25 до 50 мг, пароксетин в дозе от 5 до 20 мг, тразодон в дозе 50 мг, тримипрамин в дозе от 75 до 200 мг. Тем не менее, антидепрессанты следует использовать в низких дозах, главным образом, когда стандартные снотворные средства не переносятся (редко), или в более высоких дозах при наличии депрессии [30].
Симптомы эмоционального выгорания в значительной степени связаны с эндокринной функцией, с функционированием гипоталамо-гипофизарной оси. Показано, что антидепрессанты, снижая уровень кортизола, могут еще больше снижать этот уровень у пациентов с выгоранием. Предполагается, что кортизол как диагностический маркер мог бы быть полезен в диагностике СПВ у врачей. Действительно высокий или очень низкий уровень кортизола является предупреждением о потенциальном выгорании, а также о риске проблем с психическим здоровьем в целом. Изучение возможных взаимосвязей между подтипами эмоционального выгорания и физиологическими переменными, такими как уровень кортизола, может оказаться весьма полезным при выборе наиболее подходящего лечения для каждого конкретного подтипа [27].
При лечении эмоционального выгорания при реабилитации пациентов необходимо учитывать состояние истощения. Витамины и минералы имеют решающее значение для устранения дисфункции надпочечников и системы гипоталамо-гипофизарно-надпочечниковой системы. Соответственно витамины, пищевые добавки также рассматриваются как одного из возможных дополнений симптоматической терапии [30].
Многие растительные вещества могут рассматриваться как «адаптогены», то есть вещества, повышающее способность организма противостоять стрессу и оказывающее уравновешивающее действие на различные системы организма, такие как иммунная, центральная нервная и сердечно-сосудистая системы. Предполагается, что использование адаптогенов также может быть полезным в терапии СПВ. Однако необходимы дальнейшие исследования для определения эффективности добавок у людей, и особенно у пациентов с выгоранием [30].
Таким образом, на сегодняшний день, как наиболее перспективные направления терапии СПВ, рассматриваются различные психотерапевтические методики и медикаментозное лечение с включением седативных средств, анксиолитиков, антидепрессантов, гормональных средств, а также растительных адаптогенов, витаминов.
В частности известен патент KR 102348044 В1, раскрывающий применение для профилактики, лечения и улучшения синдрома эмоционального выгорания композицию, включающую экстракт плодов женьшеня и одно или несколько веществ, выбранных из группы, состоящей из красного женьшеня, дудника, василькового масла, оленьих рогов и магнолии [33].
Известна патентная заявка WO 2020099595 А1, раскрывающая применение экстракта вербены лимонной для лечения соматоформных заболеваний, таких как синдром выгорания [34].
В заявке WO 2003086352 А1 раскрывается применение модуляторов ГАМК-А рецепторов, например бензодиазепинов для улучшения сна, связанного с нарушенным исполнением профессиональных обязанностей [35].
Известна патентная заявка US 2018185375 А1, касающаяся способа лечения расстройств, выбранных из расстройств настроения, тревожных расстройств, биполярных расстройств, нарушений сна, расстройства поведения, СДВГ, эмоционального выгорания, синдрома хронической усталости, ожирения, депрессии, социальной тревоги и т.п., включающего введение субъекту терапевтически эффективного количества первого агента, выбранного из антагониста CRF-1 и ингибитора кортизола; и второго агента, выбранногой из селективного ингибитора обратного захвата серотонина (СИОЗС), бета-блокатора, антипсихотика, азапирона и альфа-адренергического агониста [36].
Известные терапевтические средства недостаточно эффективны, поскольку либо устраняют лишь некоторые симптомы, либо оказывают побочные действия, например вызывают эффекты сонливости, заторможенности, или наоборот бессоницы, возможно возникновение зависимости.
Задачей настоящего изобретения является поиск нового эффективного средства для терапии СПВ как вещества с высокой терапевтической активностью в отношении комплекса симптомов СПВ, сочетающейся с отсутствием выраженных побочных действий.
Данная задача была решена выявлением возможности применения в качестве средства медикаментозной терапии СПВ фонтурацетама.
Фонтурацетам - известный препарат, который относится к фармакотерапевтической группе ноотропных препаратов. Он обладает выраженным антиамнестическим действием, способствует консолидации памяти, улучшению внимания, обладает анксиолитической активностью, регулирует процессы активации и торможения ЦНС, улучшает настроение. Оказывает положительное воздействие на обменные процессы и кровообращение мозга, стимулирует окислительно-восстановительные процессы, повышает энергетический потенциал организма за счет утилизации глюкозы. Повышает содержание норадреналина, дофамина и серотонина в мозге, не влияет на содержание ГАМК и не связывается ни с ГАМКд, ни с ГАМКв рецепторами. Стимулирующее действие проявляется в его способности оказывать умеренно выраженный эффект в отношении двигательных реакций, в повышении физической работоспособности, в выраженном антагонизме каталептическому действию нейролептиков, а также в ослаблении выраженности снотворного действия этанола и гексенала. Обладает иммуностимулирующими свойствами. Умеренный психостимулирующий эффект препарата сочетается с анкиолитической активностью, улучшает настроение, оказывает некоторый анальгезирующий эффект. Адаптогенное действие проявляется в повышении устойчивости организма к стрессу в условиях чрезмерных психических и физических нагрузок [37].
Несмотря на многочисленные изученные фармакологические эффекты фонтурацетама, в научной и патентной литературе не описано его использование в терапии синдрома профессионального выгорания (СПВ). На настоящий момент фонтурацетам не применяется с этими целями.
Нами на модели хронического непредсказуемого умеренного стресса впервые было показано, что применение фонтурацетама снижает выраженность характерных для СПВ симптомов, таких как психическая и физическая утомляемость, снижение работоспособности, апатия, сниженное настроение, снижение когнитивных функций.
Техническим результатом изобретения является возможность применения N-карбамоил-метил-4-фенил-2-пирролидона для повышения уровня нейротрофического фактора головного мозга (BDNF) в крови животных в модели хронического непредсказуемого умеренного стресса.
Проведенные нами исследования касаются фармакологических эффектов фонтурацетама на экспериментальных моделях, позволяющих моделировать СПВ.
В экспериментах было подтверждено наличие у фонтурацетама механизма фармакологического действия, связанного с ингибированием дофаминового транспортера (DAT), и механизма действия, не связанного с DAT. В частности, фонтурацетам не приводил к ожидаемому увеличению двигательной активности у DAT-KO крыс, что косвенно свидетельствует о том, что именно через механизм, опосредованный ингибированием DAT, реализуются стимулирующие эффекты фонтурацетама при терапии СПВ. Установленное стимулирующее влияние фонтурацетама на двигательную активность обосновывает его применение при физической утомляемости, которая наблюдается у пациентов с СПВ.
Также эффективность фонтурацетама была продемонстрирована на модели хронического умеренного непредсказуемого стресса (CUMS). Было проведено два эксперимента, в которых были отобраны и подтверждены в плане воспроизводимости маркеры поведенческих и биохимических изменений, возникающих в результате хронического стресса и позволяющих воспроизводить симптомы СПВ. На основании полученных результатов был сделан вывод о том, что разработанный протокол позволяет воспроизводить следующие симптомы: снижение массы тела, увеличение концентрации гормонов стресса в крови - кортикостерон, кортизол (изменений уровня ДГЭА не установлено), снижение концентрации BDNF в крови, снижение когнитивной функции (по результатам теста «Распознавание нового объекта), увеличение уровня тревожности (по результатам теста «Приподнятый крестообразный лабиринт»), изменение стратегии поведения в тесте принудительного плавания (тест Порсолта).
Было показано, что применение экспериментальной модели хронического непредсказуемого умеренного стресса в контрольной группе животных привело к следующим физиологическим, поведенческим и биохимическим изменениям: значительному замедлению прироста массы тела, развитию когнитивных нарушений (по результатам теста «Распознавание нового объекта»), увеличению уровня тревожности (по результатам теста «ПКЛ»), поведенческой дезадаптации (по результатам теста Порсолта), к повышению гормонов-маркеров стресса -кортикостерона и кортизола, снижению уровня BDNF (нейротрофический фактов, снижение которого ассоциировано с развитием СПВ по данным клинических исследований) в крови. Выявленные изменения отражают клинические симптомы СПВ, что позволяет рассматривать данную экспериментальную модель как применимую для оценки эффективности лекарственных кандидатов, направленных на терапию СПВ.
Полученные результаты на модели CUMS в совокупности с имеющимися клиническими данными о адаптогенном эффекте фонтурацетама позволяют прогнозировать наличие у фонтурацетама положительного терапевтического влияния на общее физическое состояние у пациентов с установленным СПВ и обосновывают применение фонтурацетама при нарушениях адаптационных возможностей организма и физической утомляемости у пациентов с СПВ.
Исследования эффекта фонцетурама на модели распознавания нового объекта у стрессированных крыс по сравнению с контрольной стрессированной группой продемонстрировали улучшение когнитивных функцийи (память, внимание, обучаемость) у стрессированных животных. Полученные на модели CUMS результаты позволяют прогнозировать наличие у фонтурацетама улучшающего когнитивные функции терапевтического действия у пациентов с установленным СПВ и обосновывают применение фонтурацетама для улучшения когнитивных функций у таких пациентов, а также позволяют предполагать, что фонтурацетам будет обладать анксиолитическим действием у пациентов с СПВ, и обосновывают применение фонтурацетама при повышенной тревожности у таких пациентов.
По результатам теста Порсолта стрессированные крысы, получавшие фонтурацетам, демонстрировали активную стратегию поведения, которая характеризовалась высоким уровнем активного поведения и низким уровнем времени неподвижности. Зарегистрированное на модели CUMS изменение поведенческой «стратегии отчаяния», характерной для подвергшихся стрессу крыс, свидетельствует о потенциальном влиянии фонтурацетама на стратегии поведения, а именно о том, что фонтурацетам будет способствовать превалированию стратегий преодоления трудностей - копинг-стратегий. Полученные данные обосновывают применение фонтурацетама при снижении адаптационных возможностей организма и нарушении стратегии преодоления трудностей - копинг-стратегии у пациентов с СПВ.
Исследования на стрессированных крысах показали, что фонтурацетам в исследованном диапазоне доз (10-100 мг/кг) препятствовал повышению концентрации кортикостерона и кортизола в крови стрессированных крыс, приводил к повышению концентрации BDNF в крови. Таким образом, фонтурацетам препятствует повышению уровня «гормонов стресса», что может предотвращать наблюдаемое на фоне стресса нарушение функционирования гипоталамо-гипофизарной оси и связанных с этим патологических изменений. Полученные результаты позволяют рассматривать применение фонтурацетама для снижения выраженности поведенческих, нейроэндокринньгх и соматических нарушений, которые возникают на фоне развития СПВ и обосновывают применение фонтурацетама при психической и физической утомляемости и при снижении адаптационных возможностей организма у пациентов с СПВ.
По совокупности всех полученных результатов наиболее выраженный фармакологический эффект в отношении коррекции нарушений, индуцированных хроническим стрессом у крыс (улучшение когнитивной функции, активная стратегия поведения в тесте Порсолта, анксиолитический эффект, снижение уровня гормонов стресса, увеличение концентрации BDNF, снижение которого ассоциировано с развитием СПВ по данным клинических исследований) оказал фонтурацетам.
Данные результаты позволяют использовать фонтурацетам при терапии СПВ, в том числе, при нарушении стратегий преодоления трудностей - копинг-стратегии).
Описание фигур.
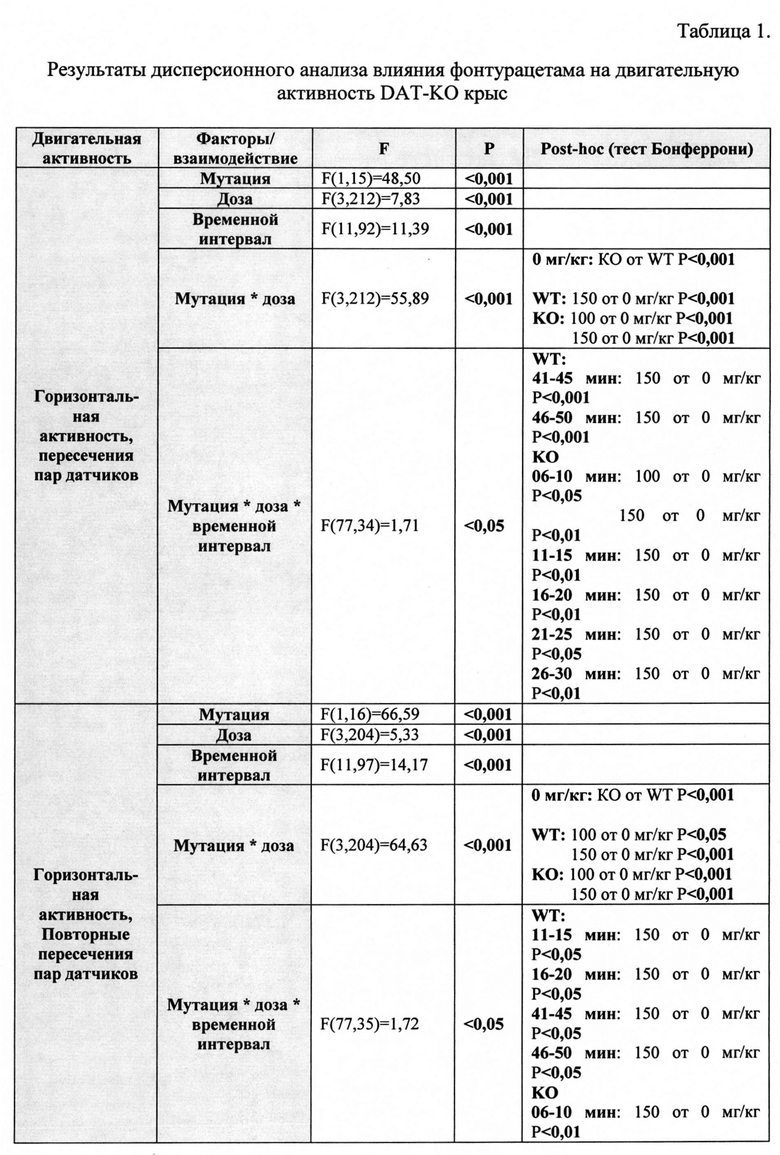
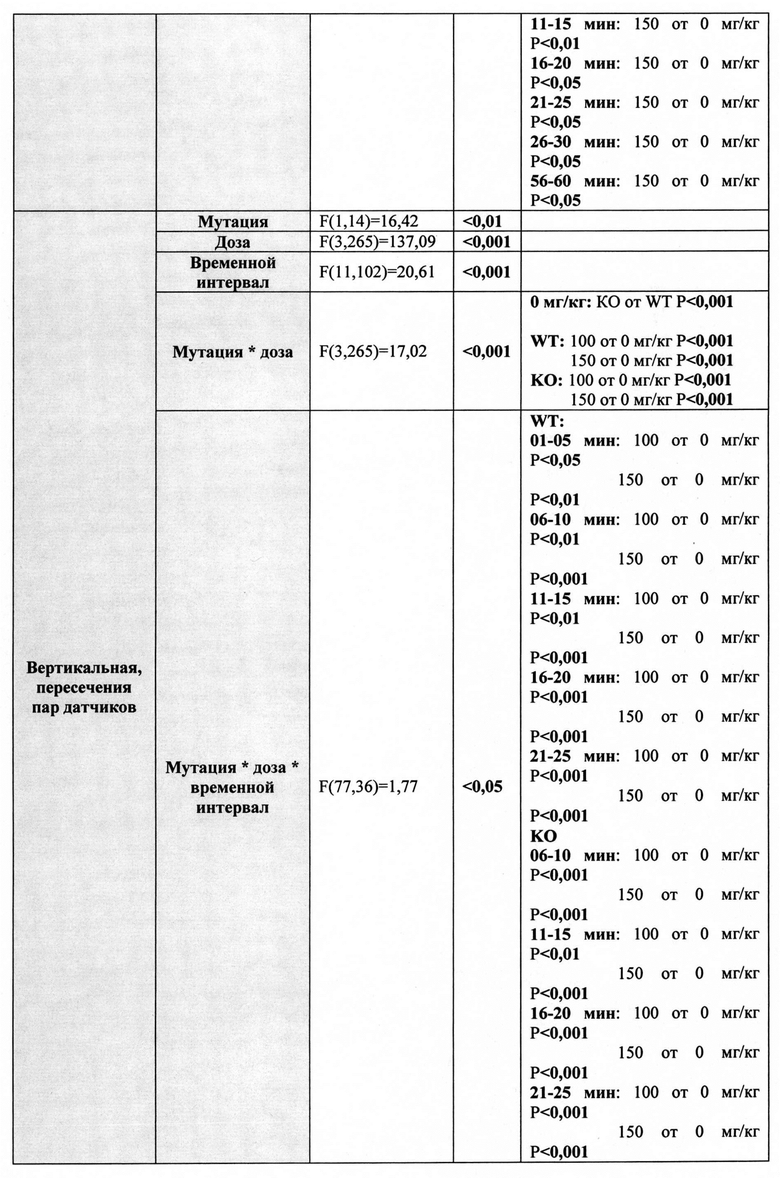
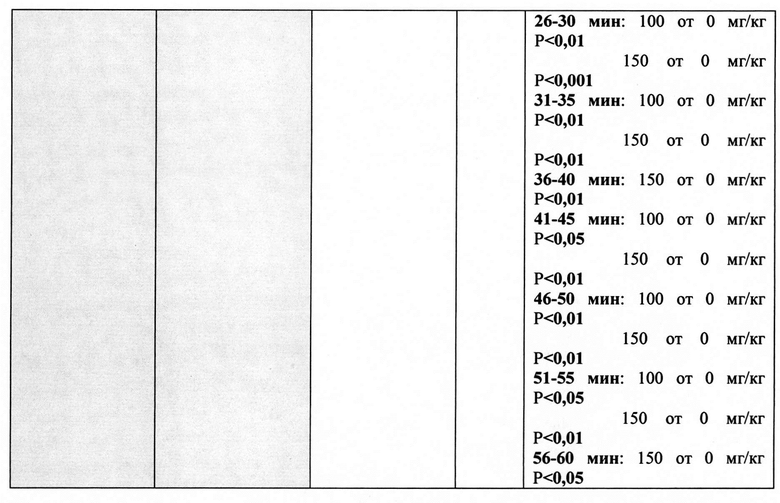
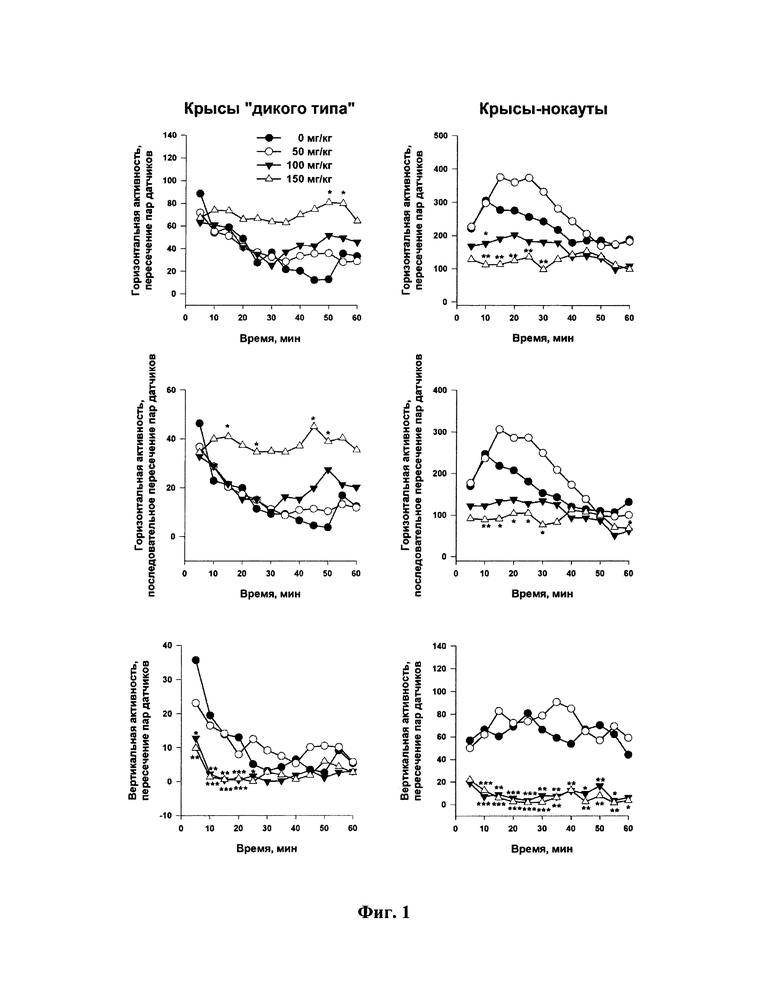
Фиг. 1. Влияние фонтурацетама (50, 100, 150 мг/кг) на горизонтальную и вертикальную двигательную активность DAT-KO крыс и животных «дикого типа». Данные представлены в виде средних ± стандартная ошибка. n=8 для каждой группы. * - Р<0,05, ** - Р<0,01, *** - Р<0,001 (тест Бонферрони) по сравнению с двигательной активностью крыс в контрольной группе в соответствующей временной интервал.
Возможность осуществления изобретения может быть проиллюстрирована нижеприведенными примерами, но не ограничивается ими.
Пример 1.
Влияние фонтурацетама на двигательную активность DAT-KO и WT крыс.
Целью исследования явилось сравнительное изучение эффектов фонтурацетама на двигательную активность крыс, нокаутных по гену без дофаминового транспортера (DAT-KO), как экспериментальной модели СПВ и крыс «дикого типа» (WT).
Экспериментальный протокол оценки двигательной активности крыс был одобрен Комиссией по содержанию и использованию животных в ПСПбГМУ им. И.П. Павлова (№100_81_012017/3_900).
ЛАБОРАТОРНЫЕ ЖИВОТНЫЕ. Эксперименты выполнены на взрослых (возраст от 2 месяцев) самцах генетически-модифицированных крыс, нокаутных по гену DAT, (массой от 200 г) из колонии Отдела психофармакологии Института фармакологии им. А.В. Вальдмана разного генетического статуса: DAT-KO (n=16) и крысах «дикого типа» (WT) (n=16).
ГЕНОТИПИРОВАНИЕ. Молекулярно-генетическое исследование крыс выполнено в отделе молекулярно-генетических и нанобиологических технологий НИЦ ПСПбГМУ им. И.П. Павлова. Биоматериалом для анализа являлись биоптаты наружного уха, полученные с помощью ушного перфоратора (FST, США) у детенышей в возрасте 28 дней (день отъема от матери). Место перфорации уха одновременно являлось индивидуальной меткой особи. Таким образом, отсутствие отдельной инвазивной процедуры по забору биоматериала позволило минимизировать стресс у животных. Выявление нокаута гена дофаминового транспортера Slc6a3 выполняли методом полимеразной цепной реакции (ПЦР) с последующим рестрикционным анализом по протоколу, адаптированному из работы Leo D. с соавт. [38].
Из биоптатов выделяли геномную ДНК стандартным фенол-хлороформным способом. ПЦР проводили в смеси объемом 15 мкл, содержащей 0,15 мкл раствора Taq М полимеразы (арт. 751-50, Алкор Био); 1,5 мкл ПЦР-буфера и 2,25 мкл раствора MgCl2 25 мМ (поставляются в комплекте с полимеразой); 1,5 мкл смеси дезоксинуклеозидтрифосфатов по 25 мМ каждого (арт. R1121, ThermoScientific); 6,1 мкл деионизированной воды; 1,5 мкл раствора ДНК; по 10 пмоль прямого (5'-TCCTGGTCAAGGAGCAGAAC-3') и обратного (5'-CACAGGTAGGGAAACCTCCA-3') праймеров (Синтол). ПЦР проводили в амплификаторе Т100 Thermal Cycler (Bio-Rad) по протоколу: 95°С - 15 мин; 35 циклов (95°С - 30 с, 60°С - 30 с, 72°С - 45 с); 72°С - 5 мин. Получали ПЦР-продукт длиной 170 или 175 пар оснований (п.о.) в случае наличия или отсутствия мутации, соответственно, поскольку нокаут гена Slc6a3 является результатом делеции 5 п. о., приводящей к образованию стоп-кодона. Рестрикционный анализ проводили при 55°С в течение 20 часов в смеси объемом 20 мкл, содержащей 0,3 мкл эндонуклеазы рестрикции BtsIMutI (арт.R0664S, New England BioLabs); 2,0 мкл буфера CutSmart (поставляется в комплекте с BtsIMutI); 12,7 мкл деионизированной воды; 5,0 мкл ПЦР-продукта. Продукты рестрикционного анализа подвергали электрофоретическому разделению в 6% полиакриламидном геле, окрашивали в водном растворе этидия бромида и визуализировали в приборе Gel Doc XR Plus (Bio-Rad). Вариантам гена DAT соответствовали длины фрагментов ДНК: WT -104 и 71 п. о.; DAT-KO-170 п. о.; НТ-170, 104 и 71 п. о.
СОДЕРЖАНИЕ ЖИВОТНЫХ: Крыс содержали в группах сиблингов (3-5 особей) в клетках TIV (Tecniplast, Италия) со свободным доступом к фильтрованной водопроводной воде (Водоочиститель АКВАФОР В150 Фаворит, Санкт-Петербург, Россия) и пище (полнорационный экструдированный корм для лабораторных животных, формула ПК 120-1, ООО «Лабораторкорм», Россия) в помещении #3-10 с контролируемыми условиями: температура воздуха - 21±1°С; влажность - 50±20%; световой цикл -12 ч свет /12 ч темнота.
ДИЗАЙН ИССЛЕДОВАНИЯ:
В течение трех дней перед тестом животных приучали к рукам экспериментатора и внутрибрюшинным инъекциям: крыс брали в руки, мягко фиксировали и делали внутрибрюшинные инъекции 0,9% раствора NaCl в объеме 1 мл/кг. В зависимости от индивидуальной реакции животных манипуляции осуществляли в течение 1-3 мин ежедневно.
В исследовании применен within-subject дизайн. Фонтурацетам (ООО «Гелеспон», Россия) в дозах 50; 100; 150 мг/кг или только растворитель (контрольная группа) вводили по схеме «Латинский квадрат» с интервалом между тестами не менее 96 часов.
Фонтурацетам растворяли в 10% водном растворе диметилсульфоксида в день выполнения тестов и вводили внутрибрюшинно в объеме 1 мл/кг непосредственно перед посадкой крыс в экспериментальную установку Для регистрации двигательной активности крыс использовали модифицированную под модель СПВ установку «Актометр», состоящую из 2-х освещаемых тусклым светом (3(МЮ лк) звукоизоляционных камер с принудительной приточной вентиляцией и подсветкой, в каждой из которых в гнездах стойки может быть размещено до пяти боксов (25 × 35,5 × 34 см) из прозрачного оргстекла. В гнезде стойки для каждого бокса находятся 3 фотодатчика на высоте 5 см для измерения горизонтальной активности и 8 датчиков на высоте 14 см - для измерения вертикальной активности. Камеры подключены к компьютеру, и с помощью программного обеспечения MED-PC (MED Associates, Inc., East Fairfield, VT, США) производится регистрацию перекрываний фотодатчиков нижнего (отдельно -последовательные пересечения) и верхнего рядов. Длительность теста составляла 60 мин (12 пятиминутных интервалов).
Регистрируемые показатели:
Показатели горизонтальной двигательной активности:
• Общее число перекрываний фотодатчиков нижнего ряда;
• Количество последовательных перекрываний датчиков нижнего ряда. Показатели вертикальной двигательной активности:
• Количество перекрываний датчиков верхнего ряда.
Анализ данных. Обработку полученных данных выполняли с помощью пакета статистических программ IBM SPSS Statistics 21 (IBM, Нью-Йорк, США). Для обработки использовали дисперсионный анализ смешанного типа (межгрупповой фактор: «мутация» (2 уровня: нокауты; «дикий тип»), внутригрупповые факторы: «доза» (4 уровня: 0; 50; 100; 150 мг/кг), «интервал времени» (12 уровней: 1-5 мин; 6-10 мин и т.д. до 55-60 мин), случайный фактор: «номер крысы») на предварительно ранжированных данных. Различия считали значимыми при р<0,05. Межгрупповые сравнения выполняли с использованием теста Бонферрони.
РЕЗУЛЬТАТЫ.
Данные проведенного эксперимента представлены на Фиг. 1. Детальные результаты статистического анализа представлены в Таблице 1.
Было показано, что горизонтальная и вертикальная двигательная активность крыс-нокаутов после введения растворителя была многократно выше, чем у контрольных животных. У крыс с интактным DAT (крысы «дикого типа») введение фонтурацетама сопровождалось дозозависимым увеличением горизонтальной и уменьшением вертикальной двигательной активности. В случае DAT-KO крыс действие фонтурацетама в дозах 100 и 150 мг/кг сопровождалось снижением горизонтальной и вертикальной двигательной активности животных. При анализе зависимости действия фонтурацетама от времени (Фиг. 1) заметно, что стимулирующее действие фонтурацетама 150 мг/кг на горизонтальную двигательную активность крыс «дикого типа» проявлялось, начиная со второй 5-минутки и продолжалось до конца экспериментальной сессии. Хотя увеличение двигательной активности крыс «дикого типа» после введения вещества в дозе 100 мг/кг не достигало статистически значимого уровня ни на одной из 5-минуток, было заметно, что сильнее всего стимулирующее действие данной дозы фонтурацетама проявлялось во второй половине экспериментальной сессии. Угнетающее действие фонтурацетама в дозах 100 и 150 мг/кг на горизонтальную и вертикальную двигательную активность DAT-KO крыс было наиболее выражено во время первой половины экспериментальной сессии.
Крысы без DAT демонстрировали многократно повышенный уровень двигательной активности. Действие фонтурацетама сопровождалось повышением горизонтальной двигательной активности у крыс с функционирующим транспортером, которое может объясняться ингибированием DAT. При этом введение фонтурацетама приводило к снижению горизонтальной активности у крыс-нокаутов, выявленный эффект аналогичен продемонстрированному ранее «парадоксальному успокаивающему» действию таких веществ-релизеров дофамина у животных без DAT как амфетамин и метилфенидат.
В результате проведенных исследований подтверждено наличие у фонтурацетама механизма, связанного с ингибированием DAT, и механизма действия, не связанного с DAT.
В эксперименте установлено, что у нокаутных по гену бе)з дофаминового транспортера (DAT-KO) крыс фонтурацетам не приводил к ожидаемому увеличению двигательной активности (в то время как у крыс «дикого типа» у которых этот эксперссирующий транспортер ген присутствует и функционирует) двигательная активность при введение фонтурацетами увеличивалась. Т.о. это косвенно может свидетельствует о том, что именно через механизм, опосредованный ингибированием DAT, реализуются биологические эффекты фонтурацетама при состояниях СПВ.
Пример 2.
Целью исследования явилось изучение терапевтической эффективности фонтурацетама (ООО «Гелеспон», Россия) на модели хронического непредсказуемого умеренного стресса (Chronic unpredictable mild stress, CUMS) у крыс.
Задачи исследования:
1. Моделирование синдрома профессионального выгорания (СПВ) на модели хронического непредсказуемого умеренного стресса у крыс;
2. Оценка терапевтической эффективности препарата МНН: фонтурацетам на модели хронического непредсказуемого умеренного стресса у крыс;
3. Сравнительный анализ эффектов препарата МНН: фонтурацетам и препарата позитивного контроля (МНН: мезокарб).
Экспериментальный протокол был рассмотрен на биоэтической комиссии на соответствие проекта исследования принципам «Трех R» и Директиве 2010/63/EU. Исследование было одобрено для проведения (№БЭК 1.7/22 от 02.03.2022 г., проголосовало 16 человек).
В качестве вещества сравнения был использован мезокарб - психостимулятор, у которого среди показаний к применению присутствуют разные виды астенических состояний, протекающих с вялостью, апатией, снижением работоспособности.
В исследовании фонтурацетам и мезокарб были использованы в виде водного раствора, содержащего полисорбат-80 в концентрации 2 и 10%, соответственно. Контрольная группа животных получала водный раствор полисорбата (2% и 10%).
ЛАБОРАТОРНЫЕ ЖИВОТНЫЕ. Крысы Wistar, самцы, вес на начало эксперимента - 194-291 г. Источник получения - питомник АО «НПО «ДОМ ФАРМАЦИИ». Лабораторных животных до начала исследования содержали 7 дней для адаптации при групповом содержании в клетках. Во время этого периода у животных каждый день контролировали клиническое состояние путем визуального осмотра. В период адаптации в течение 3-4 дней животных хендлировали (приучали к рукам).
СОДЕРЖАНИЕ ЖИВОТНЫХ: Крыс содержали при температуре воздуха 18-26°С и влажности 46-65%. Световой режим 12 ч темноты /12 ч света. Животных содержали в стандартных пластиковых клетках, на подстиле. Животные группы №1 (контроль, без патологии) содержались группой по 3 особи. Животные групп №2-6 (стресс) содержались индивидуально, за исключением дней, когда создавалось переполнение клетки содержания (5 особей в клетке - по 1 крысе из каждой группы). Животные получали корм для содержания лабораторных животных ПК-120 (АО «Гатчинский комбикормовый завод», Россия), приготовленный по ГОСТ 34566-2019 «Комбикорма полнорационные для лабораторных животных. Технические условия». Животным давали воду, очищенную ad libitum.
ДИЗАЙН ИССЛЕДОВАНИЯ: Общее число групп в эксперименте - 6.
Группа №1 - контрольная (без патологии, получала 2%-ный раствор полисорбата 80).
Группа №2 - контрольная (с патологией, получала 10%-ный раствор полисорбата 80).
Группы №3-5 - патология + терапия (фонтурацетам, 10 мг/кг, 30 мг/кг, 100 мг/кг).
Группа №6 - патология + терапия (мезокарб, 5 мг/кг).
Препараты или носитель вводили животным ежедневно в течение 28 дней, внутрижелудочно, поскольку этот способ является аналогом перорального, который планируется использовать в клинической практике. Индукция стресса.
У животных групп №2-6 моделировался хронический непредсказуемый умеренный стресс (Chronic unpredictable mild stress, CUMS). В течение 21 дня животных ежедневно подвергали воздействию умеренных стрессогенных факторов, чередующихся в непредсказуемом для животных порядке.
В данном исследовании были использованы следующие стрессорные факторы:
1. Переполнение клетки содержания (5 крыс в клетке, рассчитанной под индивидуальное содержание, на 24 ч).
2. Депривация сна (стресс по Жуве) в течение 24 ч. В клетку содержания помещали платформу-цилиндр высотой 6 см и диаметром 6,5 см. Затем клетку наполняли холодной водой на 3 см от дна. Крыс помещали на платформу, окруженную водой. Приспосабливаясь спать на платформе, животное в моменты расслабления мышц падает в воду, затем снова возвращается на платформу, в результате в течение суток лишается сна.
3. Мокрый подстил в течение 24 ч;
4. Наклон стандартной клетки содержания на 45 градусов в течение 22 ч;
5. Фиксация животного в рестрейнере на 2 ч;
6. Водная депривация в течение 24 ч;
7. Пищевая депривация в течение 24 ч.
Крысы подвергались 7 стрессорным факторам 3 раза, таким образом, общая продолжительность формирования патологии составила 21 день.
До начала воздействия стрессогенных факторов и на 21-й и 29-й дни эксперимента у животных забирали кровь для биохимического анализа. Для оценки концентрации BDNF кровь забирали только на 29-й день. Массу тела регистрировали еженедельно. Фонтурацетам, мезокарб (контроль) вводили ежедневно с 1-го по 28-й дни эксперимента. По окончании индукции стресса проводили ряд поведенческих тестов. Тест «Распознавание нового объекта» проводили в период 23-25-й дни, тест «Приподнятый крестообразный лабиринт» - 26-й день, тест Порсолта - 27-28-й дни. На 29-й день животных эвтаназировали.
Эвтаназия. В соответствии с Директивой 2010/63/EU Европейского Парламента и Совета Европейского Союза по охране животных, используемых в научных целях от 22 сентября 2010 г., животных эвтаназировали с применением диоксида углерода (СО2) с последующим перерезанием основных кровеносных сосудов. Данный вид эвтаназии животных сопровождался минимумом боли, страдания и дистресса и проведен компетентными сотрудниками.
Анализ данных. Для всех данных была применена описательная статистика: данные проверяли на соответствие закону нормального распределения с помощью критерия Шапиро-Уилка {Shapiro-Wilk's W test). Для оценки данных с признаками нормального распределения использовали однофакторный дисперсионный анализ {One-way ANOVA). Для оценки связанных данных использовали дисперсионный анализ с повторными измерениями {Repeated measures ANOVA, RMANOVA), В случае обнаружения достоверного влияния исследуемого фактора последующие межгрупповые сравнения {post hoc analysis) проводили с использованием критерия Тьюки (Tukey's test analysis). Для подтверждения тенденций, выявленных критерием Тьюки, использовали критерий Даннета (Dunnett'закону нормального распределения, использовали критерий Краскела-Уоллиса (Kruskal-Wallis) с дальнейшим применением апостериорного критерия Данна (метода средних рангов) для множественных сравнений в случае обнаружения достоверного влияния исследуемого фактора. Различия определяли при уровне значимости р<0,05. Статистический анализ выполняли с помощью лицензированного программного обеспечения Prism 9 (GraphPad Software, США). РЕЗУЛЬТАТЫ.
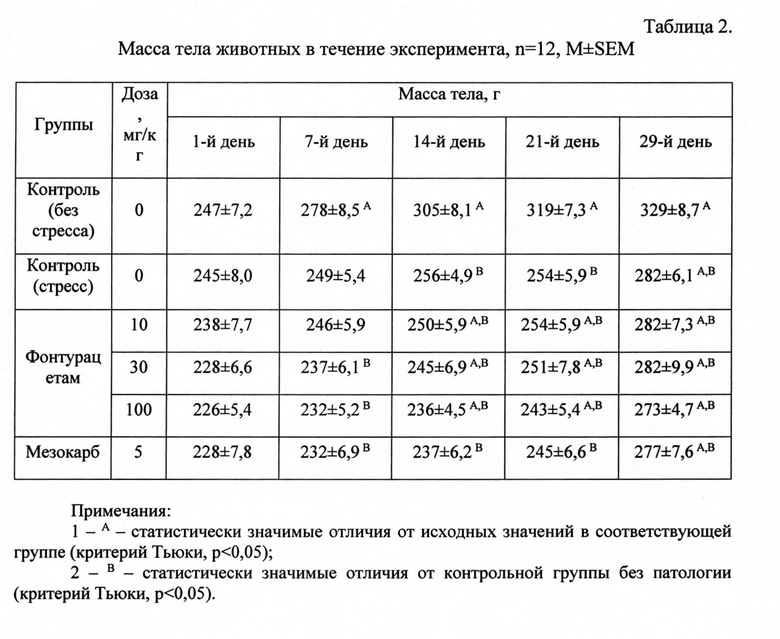
Оценка влияния фонтурацетама и мезокарба на динамику массы тела.
Результаты представлены в Таблице 2. Хронический стресс привел к значительному замедлению прироста массы тела у контрольных крыс. У стрессированных крыс, получавших фонтурацетам и мезокарб, увеличения темпов прироста массы тела по сравнению с контрольными стрессированными животными не наблюдалось. Отсутствие терапевтического эффекта, вероятно, обусловлено тем, что тестируемый объект и объект сравнения обладают анорексигенной активностью при курсовом применении. Тем не менее, стоит отметить, что статистически значимое увеличение массы тела относительно исходных значений в период моделирования стресса было зарегистрировано именно в группах фонтурацетама (весь диапазон доз).
Оценка влияния фонтурацетама и мезокарба на память и обучение.
Тест на распознавание объектов - это широко используемый поведенческий тест для исследования различных аспектов обучения и памяти у грызунов. Тест основан на естественном стремлении грызунов исследовать новое. В данном тесте животное должно изучить окружающую обстановку, запомнить объекты в течение обучающей (ознакомительной) сессии и затем в тестовой сессии помнить знакомый (старый) объект и отличать его от нового объекта.
Экспериментальная камера представляла собой бокс размером 80×80×30 см с непрозрачными бортами, дно которого не покрыто подстилочным материалом.
Тест выполнялся в 3 этапа (сессии):
1) адаптация к экспериментальным условиям (10 мин, 23-й день эксперимента);
2) ознакомление с двумя одинаковыми объектами (10 мин, 24-й день);
3) предъявление старого и нового объектов (10 мин, тестовая сессия, 25-й день).
В тестовой сессии фиксировалось общее время (в секундах), потраченное на изучение каждого объекта (обнюхивание, лизание, касание объекта или подход к нему на расстояние <1 см). Для оценки распознавания объекта был рассчитан индекс предпочтения (формула 1) [43]:
Индекс предпочтения = Тновый / (Тновый + Тстарый) (1),
Тновый - это время, потраченное на изучение нового объекта, секунды
Тстарый - это время, потраченное на изучение старого объекта, секунды
В течение всех сессий теста также была оценена локомоторная активность животных (количество пересеченных квадратов; количество центровых посещений; количество свободных стоек; количество пристеночных стоек).
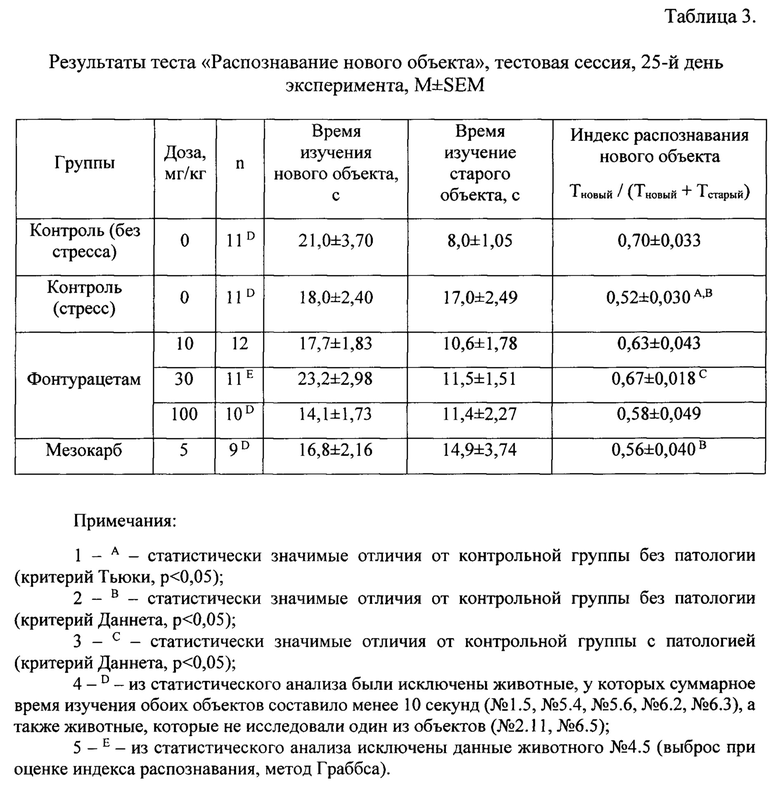
Результаты представлены в Таблице 3. Из анализа были исключены животные, у которых суммарное время изучения обоих объектов составило менее 10 секунд, а также животные, которые не исследовали один из объектов, поскольку в таких случаях невозможно утверждать, что животные потратили достаточное количество времени на изучение объектов, чтобы различать их между собой [43].
Контрольные стрессированные крысы больше времени уделяли изучению старого объекта по сравнению с контрольными нестрессированными крысами (тенденция, фактор «группа» р=0,07).
Фонтурацетам в дозе 30 мг/кг привел к значимому увеличению индекса распознавания нового объекта по сравнению с контрольной стрессированной группой. В группе, получавшей фонтурацетам в дозе 10 мг/кг, наблюдалась аналогичная тенденция, не достигшая статистической значимости. Мезокарб также не способствовал улучшению процессов обучения и памяти стрессированных крыс.
При оценке локомоторной активности крыс в рамках данного теста было отмечено увеличение активности в группах, получавших фонтурацетам, в дозах 30 мг/кг и 100 мг/кг, и в группе мезокарба.
Оценка влияния фонтурацетама и мезокарба на уровень тревожности. Оценку проводили в тесте «Приподнятый крестообразный лабиринт». Исходя из традиционных представлений, тесты на тревожность (ПКЛ, открытое поле, темно-светлая камера) основаны на конфликте между естественным стремлением грызунов исследовать новое и стремлением избегать неизвестное [44].
Животным предлагается выбор между аверсивными (исследование открытого/освещенного пространства) и неаверсивными (исследование закрытого/неосвещенного пространства) стимулами. Предпочтение крыс исследовать открытые пространства свидетельствует о сниженном уровне тревожности.
Установка «Приподнятый крестообразный лабиринт» (ПКЛ) состояла из крестообразно расходящихся от центральной площадки под прямым углом 4-х рукавов: два противоположных, светлых, из прозрачного пластика, и два закрытых, темных. Центральная площадка и пол открытых рукавов прозрачны, тогда как пол и стенки закрытых рукавов окрашены в темный цвет.
Процедура тестирования осуществлялась при обычном освещении с интенсивностью светового потока в 300 лк. Длительность теста - 3 мин.
Оцениваемые параметры:
- общая продолжительность пребывания в «темных» и «светлых» рукавах;
- число заходов в темные и светлые рукава;
- количество стоек в центральной части;
- количество болюсов дефекации;
- количество попыток покинуть установку.
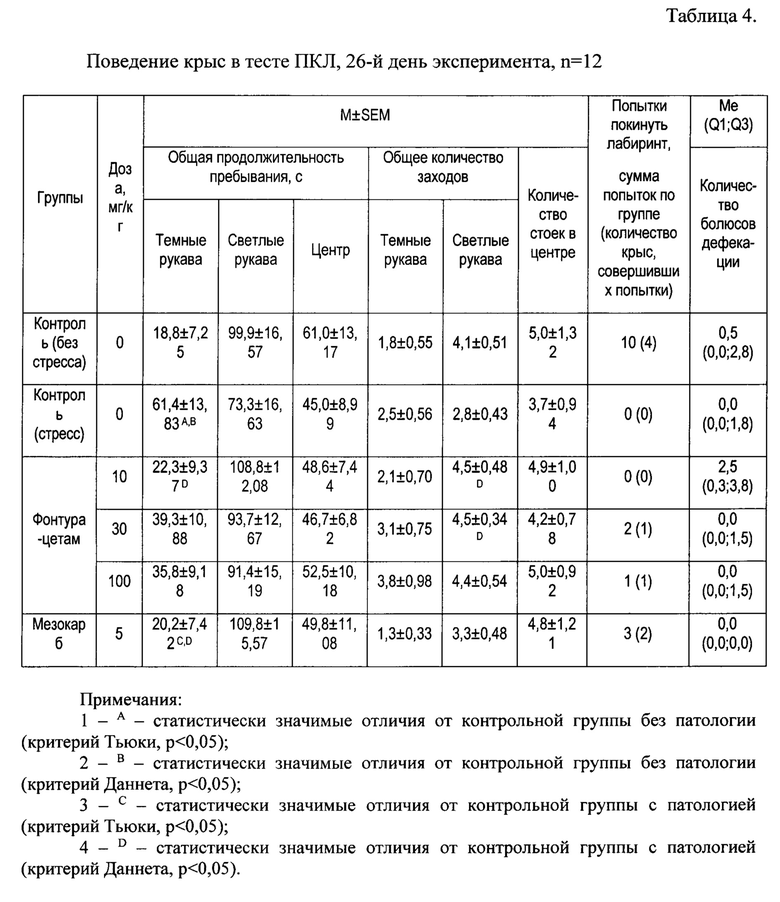
В данном эксперименте поведение контрольных стрессированных крыс характеризировалось повышенным уровнем тревожности. Результаты представлены в Таблице 4. Поведение стрессированных животных, получавших фонтурацетам в дозах 10 и 30 мг/кг, было сопоставимо с поведением контрольных животных без патологии (доза 100 мг/кг - аналогичная тенденция к снижению уровня тревожности). В группах, получавших дозы 30 мг/кг и 100 мг/кг, отмечены случаи попыток покинуть лабиринт (усиление ориентировочно-исследовательского поведения), что также указывает на снижение тревожности у стрессированных крыс, получавших терапию фонтурацетамом. Терапия с использованием мезокарба схожим образом оказала сопоставимые с фонтурацетамом эффекты: стрессированные крысы, получавшие мезокарб, предпочитали светлые рукава, достоверно меньше времени проводили в темных рукавах по сравнению со стрессированными крысами без лечения. Таким образом, терапия фонтурацетамом в исследованном диапазоне доз и мезокарбом в дозе 5 мг/кг способствовала снижению тревожного поведения у крыс, подвергшихся хроническому стрессу, по результатам теста ПКЛ.
Оценка влияния фонтурацетама и мезокарба на депрессивно-подобное поведение в тесте Порсолта.
Тест Порсолта (тест принудительного плавания) используется для оценки депрессивно-подобного поведения и эффективности антидепрессантов. Для тестирования принудительного плавания были использованы 4 цилиндра из оргстекла (d=20 см; h=45 см), которые были заполнены водой (температура воды 24±1°С) до глубины 30 см. Цилиндры были отделены друг от друга непрозрачными перегородками, не позволяющими животным видеть друг друга во время теста. После каждого теста проводили замену воды и мытье цилиндра, поскольку было показано, что вторичное использование воды может влиять на поведение животных из-за наличия ольфакторных «сигналов тревоги» [45].
Процедура представляла собой «классический» двухдневный протокол теста форсированного плавания [46]. В первый день (претест - этап выработки состояния «поведенческого отчаяния» [46] или пассивной копинг-стратегии [47]) крысы помещались в цилиндры с водой на 15 мин. Через 24 ч после первой посадки животным вводили исследуемые объекты. Через 1 ч после введения экспериментальные животные снова помещались в цилиндры с водой на 5 мин (тест - этап оценки стратегии поведения). В претесте (за первые 5 мин) и тесте (за 5 мин) анализировали следующие элементы поведения (продолжительность в секундах):
I. Неподвижность (пассивное поведение):
1) неподвижность (дрейфование - отсутствие движений конечностями или выполнение мелких движений конечностями и хвостом для удержания головы на поверхности воды).
II. Подвижность:
2) плавание (ориентирование, сопровождающееся совершением движений всеми конечностями);
3) гребля (ориентирование, перемещение с помощью ритмичных движений задних конечностей);
4) залезание/карабканье на стенку (поведение избегания - тело крысы в вертикальном положении, интенсивные движения всех конечностей с выбросом передних лап над поверхностью воды с касанием стенки цилиндра);
5) ныряние (поведение избегания - активное погружение под воду, перемещение по направлению ко дну цилиндра).
В тесте также было подсчитано количество находящихся в воде болюсов дефекации (индекс эмоциональности).
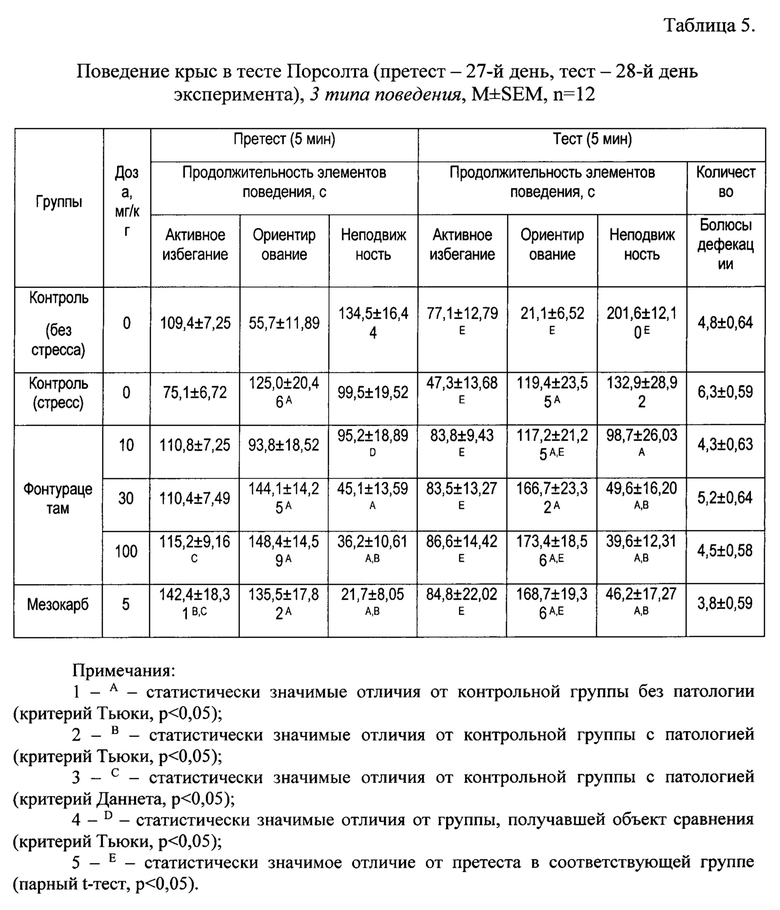
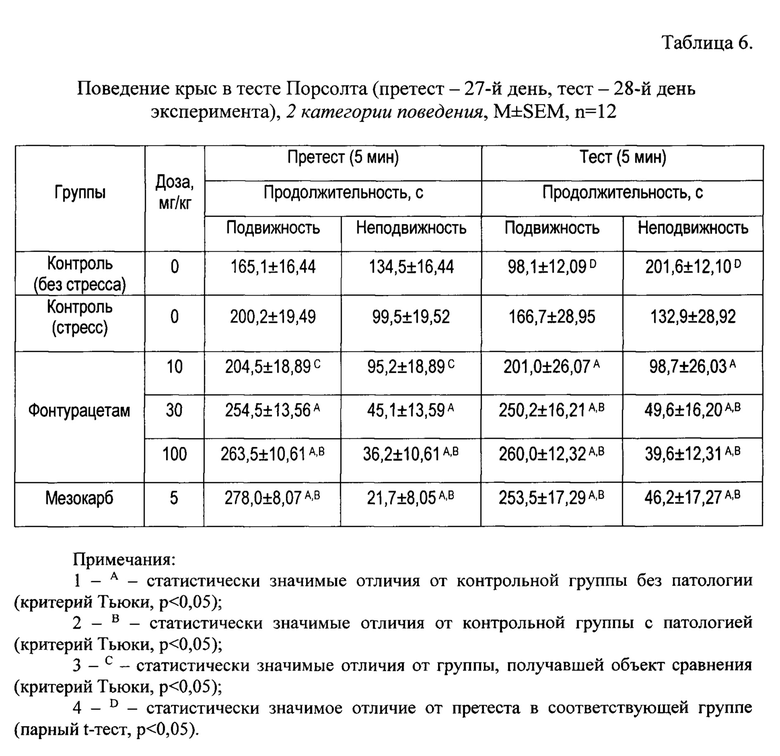
В Таблице 5 представлены данные и результаты их статистической обработки по 3 типам поведения, в Таблице 6 - по 2 категориям поведения.
Претест. Уже на этапе претеста можно отметить различия в стратегии поведения двух контрольных групп. Контрольные крысы без патологии при первом ознакомлении с условиями теста отдавали предпочтение реакциям активного избегания, контрольные стрессированные крысы - поведению ориентирования. Реакции борьбы у стрессированных крыс были снижены относительно контрольных животных без патологии. В группах, получавших препараты, наблюдалось дозозависимое увеличение времени подвижности и снижение времени неподвижности в сравнении с обеими контрольными группами.
Тест. Контрольная стрессированная группа характеризовалась высокой индивидуальной вариабельностью по показателям общей подвижности и неподвижности. Внутри группы животные принимали противоположные стратегии поведения: у половины животных время подвижности выраженно снижалось и нарастало время неподвижности (от претеста к тесту), у второй половины - наоборот (или оставалось таким же, как на претесте). В связи с этим увеличение общего времени подвижности и снижение неподвижности у стрессированных крыс относительно контроля без патологии отмечено только на уровне тенденции (р=0,07).
Стрессированные крысы, получавшие фонтурацетам во всем диапазоне доз и мезокарб, демонстрировали выраженное увеличение времени подвижности и снижение времени неподвижности относительно обеих контрольных групп. Продолжительность активного избегания у стрессированных крыс, получавших терапию исследуемыми объектами, была выше по сравнению с контрольными стрессированными животными (без статистической значимости). По показателю «количество болюсов дефекации» (индекс эмоциональности) влияния фактора «группа» не выявлено.
Ключевым отличием в поведении контрольных стрессированных крыс от контрольных животных, не подвергавшихся хроническому стрессу, является их стратегия преодоления стрессовой ситуации (копинг-стратегия) в условиях теста принудительного плавания. Контрольные животные без патологии демонстрировали единую стратегию поведения: у всех животных из группы уменьшалось время подвижности и увеличивалось время неподвижности на тесте по сравнению с претестом. У данных животных наблюдался переход от активной стратегии на претесте к пассивной стратегии поведения в тесте: реакции борьбы (карабканье и ныряние) и поведение ориентирования (плавание и гребля) ко 2-му дню тестирования угасали и сменялись в сторону неподвижности. В настоящий момент смена активной стратегии на пассивную стратегию поведения в условиях неизбегаемого острого стресса (принудительное плавание в замкнутом пространстве) рассматривается исследователями как поведенческая адаптация и успешная копинг-стратегия, характеризующая процесс обучения, который способствует выживанию.
Контрольные стрессированные животные внутри группы принимали противоположные стратегии поведения: часть животных демонстрировала переход к пассивной стратегии, другая часть - наоборот, увеличивали время подвижности (за счет поведения ориентирования). Учитывая однонаправленную реакцию контрольных нестрессированных крыс на условия теста, можно сказать, что у стрессированных крыс отсутствует подобная адаптивная реакция.
У стрессированных крыс, получавших фонтурацетам и мезокарб, на обоих этапах теста наблюдалась активная копинг-стратегия, время неподвижности в целом не изменялось от претеста к тесту. Данные животные демонстрировали высокий уровень активности в сравнении с обеими контрольными группами. В группах фонтурацетама эффект был дозозависимым: продолжительность активного поведения нарастала, а продолжительность неподвижности уменьшалась с увеличением дозы. В группе мезокарба также регистрировался высокий уровень активного поведения, который был сопоставим с показателями группы, получавшей максимальную дозу мезокарба.
Таким образом, в тесте Порсолта стрессированные крысы, получавшие фонтурацетам, демонстрировали активную стратегию поведения, которая характеризовалась высоким уровнем активного поведения и низким уровнем неподвижности, в отличие от контрольных крыс без патологии, которые демонстрировали пассивную стратегию поведения.
Оценка влияния фонтурацетама и мезокарба на уровень гормонов стресса (кортикостерон, кортизол), уровень BDNF, С-пептида и уровень триглицеридов
Для оценки уровня гормонов стресса, С-пептида, триглицеридов кровь у животных была забрана на 3 точках: 1-й день (исходная точка), 21-й день (по окончании периода моделирования стресса), 29-й день (по окончании эксперимента). Для оценки уровня BDNF кровь отбирали по окончании эксперимента (29-й день). На всех точках кровь была взята прижизненно из хвостовой вены, под общей ингаляционной анестезией с применением изофлурана Аерран (Бакстер Хелскэа, США) и ИзоНик (Chemical Iberica, Испания). Кровь забиралась в утренние часы (с 9:00 до 10:30). Поскольку образцы крови отбирались для анализа уровня гормонов-маркеров стресса (кортикостерон и кортизол), была выбрана процедура взятия крови под анестезией вместо стандартной процедуры прижизненного забора крови с фиксацией в рестрейнере, чтобы избежать возможного влияния острого стресса, вызванного иммобилизацией. Для минимизации влияния острого стресса на уровни кортикостерона и кортизола всех животных до начала эксперимента хендлировали, а также приучали к боксу (затравочной камере), который использовался для ингаляционной наркотизации изофлураном.
В крови определяли следующие показатели:
1. Гормоны-маркеры стресса и маркера СПВ:
• Концентрация кортикостерона;
• Концентрация кортизола;
• BDNF;
2. Маркер нарушения метаболизма глюкозы:
• Концентрация С-пептида. Профессиональное выгорание является предиктором диабета 2 типа [48], поэтому для выявления возможных метаболических нарушений была измерена концентрация С-пептида в крови.
3. Концентрация триглицеридов.
Концентрацию гормонов в плазме крови крыс определяли методом иммуноферментного анализа с использованием коммерчески доступных наборов (набор для определения концентрации кортизола «Кортизол-ИФА-Бест», REF Х-3964, (АО «Вектор-Бест», Россия); набор для определения концентрации С-пептида «Elisa kit for C-Peptide», №CEA447Ra, (Cloud-Clone Corp., USA); набор для определения концентрации кортикостерона «Corticosterone ELISA» REF EIA-4164 (DRG Instruments GmbH, Germany)
Оптическую плотность растворов измеряли на многофункциональном микропланшетном анализаторе «CLARIOstar» (BMG Labtech, Германия) при двух длинах волн 450 нм (основная длина волны) и 650 нм (референсная длина волны).
Концентрацию триглицеридов определяли в свежеполученных образцах сыворотки. Анализ выполняли с помощью набора реагентов Liquick Cor-TG30, ref 2-262, (PZ Cormay S.A., Польша). Анализ выполнен на автоматическом биохимическом анализаторе Accent-200 (PZ Cormay S.A., Польша).
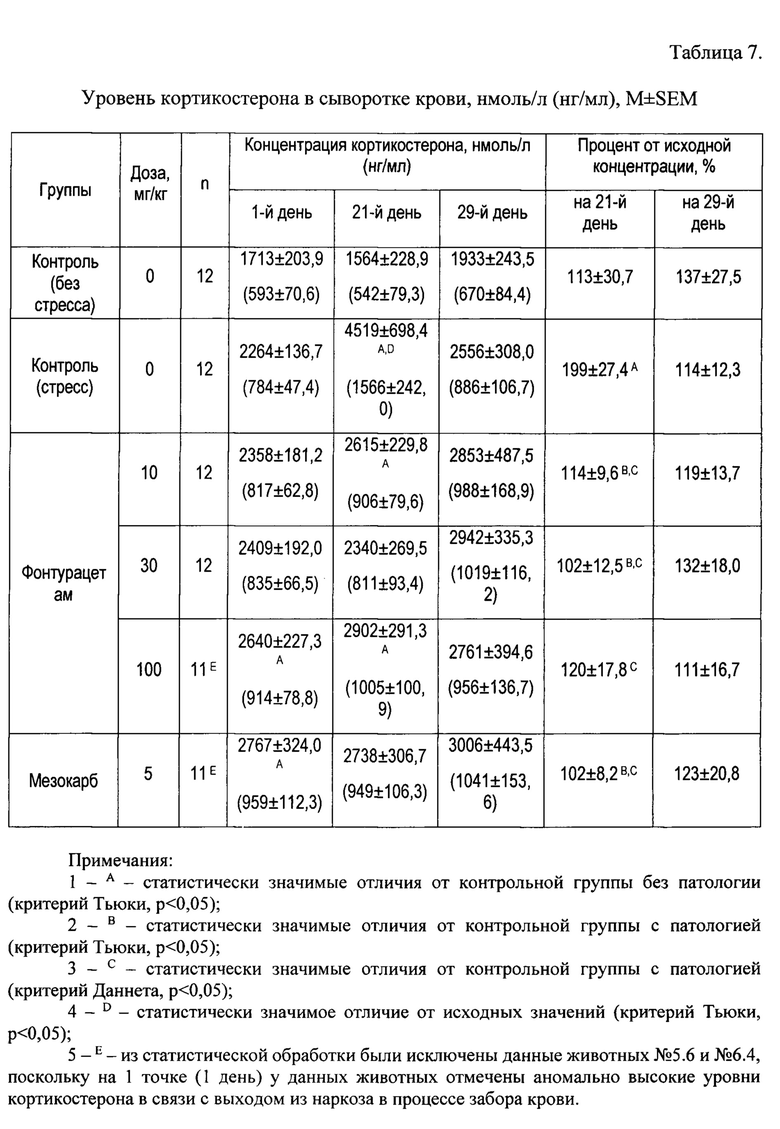
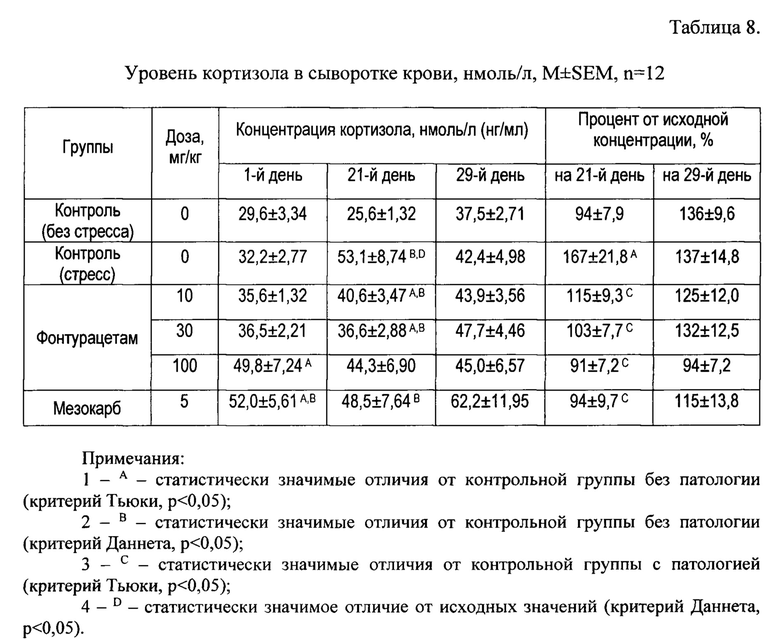
Кортикостерон и кортизол (гормоны-маркеры стресса) и BDNF (нейротрофический фактор, снижение которого в крови по данным клинических исследований ассоциировано с развитием СПВ).
Результаты исследования представлены в Таблицах 7-9. Учитывая наличие достоверных различий в исходном уровне кортизола и кортикостерона между группами, для оценки влияния терапии на уровни гормонов стрессированных крыс был рассчитан и проанализирован процент от исходной концентрации каждого из гормонов на 21-й и 29-й дни эксперимента. Уровни кортикостерона и кортизола контрольных стрессированных животных значимо возрастали к 21-му дню эксперимента относительно контроля без патологии. У стрессированных крыс, получавших терапию, к 21-му дню эксперимента уровни гормонов стресса снижались до показателей контрольной группы без патологии и статистически значимо отличались от показателей контрольных стрессированных крыс.
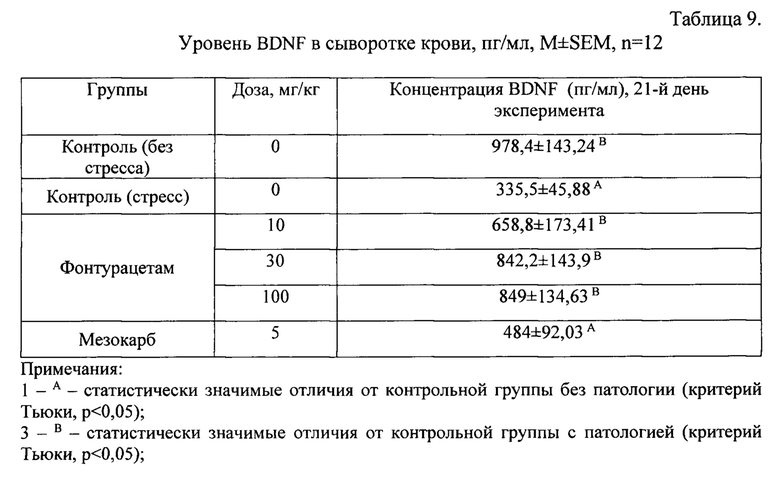
Таким образом, фонтурацетам в исследованном диапазоне доз и мезокарб в дозе 5 мг/кг на фоне моделируемого хронического стресса препятствовали повышению концентрации кортикостерона и кортизола у стрессированных крыс. Концентрация BDNF у стрессированных крыс была значимо ниже, чем у контрольных (без патологии). Терапия с применением фонтурацетама приводила к увеличению концентрации BDNF. Эффект нарастал в диапазоне доз 10-30 мг/кг, увеличение дозы до 100 мг/кг не усиливало эффект. Мезокарб значимо не повлиял на данный показатель.
С-пептид (маркер нарушения метаболизма глюкозы). Хронический стресс не привел к изменениям уровня С-пептида у контрольных крыс относительно показателей контрольных животных без патологии. Терапия исследуемыми объектами не оказала значимого влияния на уровень С-пептида у стрессированных крыс, по сравнению с контрольными группами и относительно исходных показателей (данные не представлены).
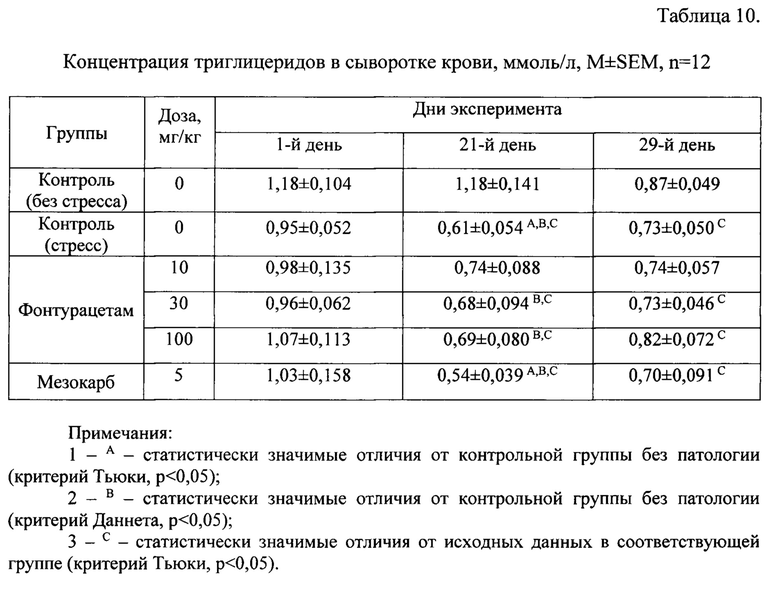
Уровень триглицеридов. В Таблице 10 представлены данные по концентрации триглицеридов в сыворотке крови животных. По окончании периода моделирования стресса (21-й день) у контрольных стрессированных крыс концентрация триглицеридов была ниже по сравнению с контрольной группой без патологии, а также относительно исходных значений. У стрессированных крыс, получавших мезокарб и фонтурацетам наблюдалось аналогичное изменение. Снижение уровня триглицеридов на 21-й день эксперимента было максимально выражено у стрессированных крыс, получавших мезокарб, в группах фонтурацетама наблюдалась некоторая дозозависимость. Известно, что фонтурацетам и мезокарб обладают анорексигенной активностью при курсовом применении [37], [40]. Снижение массы тела у крыс может приводить к снижению уровня триглицеридов. В данном случае снижение уровня триглицеридов у стрессированных животных, получавших фонтурацетам и мезокарб, может быть связано не столько со стрессогенным воздействием, а со снижением потребления корма и замедлением прироста массы тела, вызванных введением объектов. Таким образом, терапия фонтурацетамом в исследованном диапазоне доз и мезокарбом в дозе 5 мг/кг не предотвращала вызванное стрессом снижение уровня триглицеридов, что согласуется с фармакологическим профилем действия этих веществ.
Таким образом, представленные экспериментальные данные доказывают возможность применения фонцетурама для терапии СПВ, что позволяет рассматривать его как перспективный препарат для введения в клиническую практику.
Список литературы
[1] Burn-out an "occupational phenomenon": International Classification of Diseases // WHO.
[2] Maslach C, Leiter M.P. Burnout. Hum. Behav. 1976; 5:16-22.
[3] Maslach C, Jackson S.E. Maslach Burnout Inventory. Manual. Consulting Psychologists Press; Palo Alto, С A, USA: 1981.
[4] Maslach C, Leiter MP. Understanding the burnout experience: recent research and its implications for psychiatry. World Psychiatry. 2016 Jun; 15(2):103-11.
[5] Shirom A. Job-related burnout: a review. In Handbook of Occupational Health
Psychology, pp 245-265. Eds С Quick & LE Tetrick. Washington, DC: American Psychological Association, 2003.
[6] Jonsdottir IH, Sjors Dahlman A. MECHANISMS IN ENDOCRINOLOGY: Endocrine and immunological aspects of burnout: a narrative review. Eur J Endocrinol. 2019 Mar 1; 180(3):R147-R158.
[7] Edu-Valsania S, Laguia A, Moriano JA. Burnout: A Review of Theory and Measurement. Int J Environ Res Public Health. 2022 Feb 4; 19(3): 1780.
[8] Bakker AB, Demerouti E. Job demands-resources theory: Taking stock and looking forward. J Occup Health Psychol. 2017 Jul; 22(3):273-285.
[9] Salvagioni DAJ, Melanda FN, Mesas AE, Gonzalez AD, Gabani FL, Andrade SM. Physical, psychological and occupational consequences of job burnout: A systematic review of prospective studies. PLoS One. 2017 Oct 4; 12(10):e0185781.
[10] Giorgi G, Arcangeli G, Perminiene M, Lorini C, Ariza-Montes A, Fiz-Perez J, Di Fabio A, Mucci N. Work-Related Stress in the Banking Sector: A Review of Incidence, Correlated Factors, and Major Consequences. Front Psychol. 2017 Dec 12; 8:2166.
[11] Bakusic J, Schaufeli W, Claes S, Godderis L. Stress, burnout and depression: A systematic review on DNA methylation mechanisms. J Psychosom Res. 2017 Jan; 92:34-44.
[12] He SC, Wu S, Wang C, Wang DM, Wang J, Xu H, Wang L, Zhang XY. Interaction between job stress, serum BDNF level and the BDNF rs2049046 polymorphism in job burnout. J Affect Disord. 2020 Apr 1; 266:671-677.
[13] Jia H, He M, Zhang X, Li Y, He SC, Zhang XY. The relationship between job stress and job burnout moderated by BDNF rs6265 polymorphism. Psychopharmacology (Berl). 2021 Oct; 238(10):2963-2971.
[14] He SC, Wu S, Wang C, Wang DM, Wang J, Xu H, Wang L, Zhang XY. Interaction between job stress, serum BDNF level and the BDNF rs2049046 polymorphism in job burnout. J Affect Disord. 2020 Apr 1; 266:671-677.
[15] He SC, Zhang YY, Zhan JY, Wang C, Du XD, Yin GZ, Cao B, Ning YP, Soares JC, Zhang XY. Burnout and cognitive impairment: Associated with serum BDNF in a Chinese Han population. Psychoneuroendocrinology. 2017 Mar; 77:236-243.
[16] Bakusic J, Ghosh M, Polli A, Bekaert B, Schaufeli W, Claes S, Godderis L. Epigenetic perspective on the role of brain-derived neurotrophic factor in burnout. Transl Psychiatry. 2020 Oct 19; 10(1):354.
[17] Sjors Dahlman A, Blennow K, Zetterberg H, Glise K, Jonsdottir IH. Growth factors and neurotrophins in patients with stress-related exhaustion disorder. Psychoneuroendocrinology. 2019 Nov; 109:104415.
[18] Jonsdottir IH, Nordlund A, Ellbin S, Ljung T, Glise K, Wahrborg P, Wallin A. Cognitive impairment in patients with stress-related exhaustion. Stress. 2013 Mar; 16(2):181-90.
[19] Grossi G, Perski A, Osika W, Savic I. Stress-related exhaustion disorder - clinical manifestation of burnout? A review of assessment methods, sleep impairments, cognitive disturbances, and neuro-biological and physiological changes in clinical burnout. Scandinavian journal of psychology 56.6 (2015): 626-636..
[20] Danhof-Pont MB, van Veen T, Zitman FG. Biomarkers in burnout: a systematic review. J Psychosom Res. 2011 Jun; 70(6):505-24.
[21] Iacovides A, Fountoulakis KN, Kaprinis S, Kaprinis G. The relationship between job stress, burnout and clinical depression. J Affect Disord. 2003 Aug; 75(3):209-21.
[22] Hakanen J J, Schaufeli WB. Do burnout and work engagement predict depressive symptoms and life satisfaction? A three-wave seven-year prospective study. J Affect Disord. 2012 Dec 10; 141(2-3):415-24.
[23] Golonka K, Mojsa-Kaja J, Blukacz M, Gawlowska M, Marek T. Occupational burnout and its overlapping effect with depression and anxiety. Int J Occup Med Environ Health. 2019 Apr 3; 32(2):229-244.
[24] van Dam A. Subgroup Analysis in Burnout: Relations Between Fatigue, Anxiety, and Depression. Front Psychol. 2016 Feb 4; 7:90.
[25] Bianchi R, Schonfeld IS, Laurent E. Burnout-depression overlap: a review. Clin Psychol Rev. 2015 Mar; 36:28-41. [26] Orosz A, Federspiel A, Haisch S, Seeher C, Dierks T, Cattapan K. A biological perspective on differences and similarities between burnout and depression. Neurosci Biobehav Rev. 2017 Feb; 73:l 12-122.
[27] Juster RP, Sindi S, Marin MF, Perna A, Hashemi A, Pruessner JC, Lupien SJ. A clinical allostatic load index is associated with burnout symptoms and hypocortisolemic profiles in healthy workers. Psychoneuroendocrinology. 2011 Jul; 36(6):797-805.
[28] Raudenska J, Steinerova V, Javurkova A, Urits I, Kaye AD, Viswanath O, Varrassi G. Occupational burnout syndrome and post-traumatic stress among healthcare professionals during the novel coronavirus disease 2019 (COVID-19) pandemic. Best Pract Res Clin An.
[29] West CP, Dyrbye LN, Shanafelt TD. Physician burnout: contributors, consequences and solutions. J Intern Med. 2018 Jun; 283(6):516-529.
[30] Kakiashvili T, Leszek J, Rutkowski K. The medical perspective on burnout. Int J Occup Med Environ Health. 2013 Jun; 26(3):401-12.
[31] Ekstedt M, Soderstrom M, Akerstedt T, Nilsson J, S0ndergaard HP, Aleksander P. Disturbed sleep and fatigue in occupational burnout. Scand J Work Environ Health. 2006 Apr; 32(2):121-31.
[32] Ahola К, Honkonen T, Virtanen M, Kivimaki M, Isometsa E, Aromaa A, Lonnqvist J. Interventions in relation to occupational burnout: the population-based health 2000 study. J Occup Environ Med. 2007 Sep; 49(9):943-52.
[33] Publication of KR102348044 B1 от 2022-01-10. [34] Publication of WO 2020099595 A1 от 22.05.2020.
[35] Publication of WO03086352 Al от 2003-10-23. [36] Publication of US2018185375 A1 от 2018-07-05.
[37] Lueptow LM. Novel Object Recognition Test for the Investigation of Learning and Memory in Mice. J Vis Exp.2017 Aug 30; (126):55718. doi: 10.3791/55718.
[88] Ennaceur A. Tests of unconditioned anxiety - pitfalls and disappointments. Physiol Behav. 2014 Aug; 135:55-71.
[39] Abel EL, Bilitzke PJ. A possible alarm substance in the forced swimming test. Physiol Behav. 1990 Aug; 48(2):233-9.
[40] Porsolt RD, Anton G, Blavet N, Jalfre M. Behavioural despair in rats: a new model sensitive to antidepressant treatments. Eur J Pharmacol. 1978 Feb 15; 47(4):379-91.
[41] West AP. Neurobehavioral studies of forced swimming: the role of learning and memory in the forced swim test. Prog Neuropsychopharmacol Biol Psychiatry. 1990; 14(6):863-77.
[42] Porsolt RD, Anton G, Blavet N, Jalfre M. Behavioural despair in rats: a new model sensitive to antidepressant treatments. Eur J Pharmacol. 1978 Feb 15; 47(4):379-91. Molendijk ML, de Kloet ER. Coping with the forced swim stressor: Current state-of-the-art. Behav Brain Res. 2019 May 17; 364:1-10.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения фенотипа стрессированных крыс с моделированным тревожно-фобическим расстройством | 2024 |
|
RU2830034C1 |
| 9-[2-(4-ИЗОПРОПИЛФЕНОКСИ)ЭТИЛ]АДЕНИН, ОБЛАДАЮЩИЙ АНТИДЕПРЕССАНТНЫМ И ПРОТИВОСТРЕССОРНЫМ ДЕЙСТВИЕМ | 2013 |
|
RU2529817C1 |
| Низкомолекулярный миметик мозгового нейротрофического фактора с анальгетическим, анксиолитическим и антиаддиктивным действием | 2020 |
|
RU2759023C2 |
| НОВЫЕ СОСТАВЫ N-КАРБАМОИЛМЕТИЛ-4-ФЕНИЛ-2-ПИРРОЛИДОНА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ОЖИРЕНИЯ | 2019 |
|
RU2732245C1 |
| ГАЛАКТООЛИГОСАХАРИДНАЯ КОМПОЗИЦИЯ И ЕЕ ПРИМЕНЕНИЕ ДЛЯ ПРЕДОТВРАЩЕНИЯ ИЛИ ЛЕЧЕНИЯ КОГНИТИВНОЙ ДИСФУНКЦИИ И ЭМОЦИОНАЛЬНЫХ РАССТРОЙСТВ ПРИ ПСИХОНЕВРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЯХ ИЛИ СТАРЕНИИ | 2014 |
|
RU2663696C2 |
| Новый состав N-карбамоилметил-4-фенил-2-пирролидона | 2017 |
|
RU2696277C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИДЕПРЕССАНТНЫМ, АНКСИОЛИТИЧЕСКИМ, НЕЙРОПРОТЕКТОРНЫМ И ИММУНОСТИМУЛИРУЮЩИМ ДЕЙСТВИЕМ | 2010 |
|
RU2429834C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНКСИОЛИТИЧЕСКИМ ДЕЙСТВИЕМ, НА ОСНОВЕ ГИДРИРОВАННЫХ ПИРИДО(4,3-b)ИНДОЛОВ (ВАРИАНТЫ), ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2007 |
|
RU2338533C1 |
| Способ моделирования хронического эмоционально-информационного стресса в эксперименте | 2018 |
|
RU2697655C1 |
| Новые составы N-карбамоилметил-4-фенил-2-пирролидона | 2018 |
|
RU2699669C1 |
Изобретение относится к области медицины, конкретно к фармакологии, и касается применения N-карбамоил-метил-4-фенил-2-пирролидона (фонтурацетама) в модели хронического умеренного непредсказуемого стресса. По результатам проведенных исследований предлагается применение N-карбамоил-метил-4-фенил-2-пирролидона для повышения уровня нейротрофического фактора головного мозга (BDNF) в крови животных в модели хронического непредсказуемого умеренного стресса. 1 ил., 10 табл., 2 пр.
Применение N-карбамоил-метил-4-фенил-2-пирролидона для повышения уровня нейротрофического фактора головного мозга (BDNF) в крови животных в модели хронического непредсказуемого умеренного стресса.
| СПОСОБ КОРРЕКЦИИ НАРУШЕНИЙ ИММУННОГО И ПСИХОЭМОЦИОНАЛЬНОГО СТАТУСА ОРГАНИЗМА ПРИ ЭКСПЕРИМЕНТАЛЬНОМ ИНФОРМАЦИОННОМ СТРЕССЕ | 2010 |
|
RU2432949C1 |
| ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ АНТИДЕПРЕССИВНОЙ АКТИВНОСТЬЮ | 2003 |
|
RU2232578C1 |
| WO 2014005720 A1, 09.01.2014 | |||
| ФИРСТОВА Ю.Ю | |||
| и др | |||
| Влияние ноотропных препаратов на уровень BDNF в гиппокампе и коре мозга мышей с различной эффективностью исследовательского поведения | |||
| Экспериментальная и клиническая фармакология, 2009, Т | |||
| Термосно-паровая кухня | 1921 |
|
SU72A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
Авторы
Даты
2025-03-24—Публикация
2023-12-11—Подача