Область техники
Настоящее изобретение относится к области биофармацевтических препаратов и, в частности, относится к ряду вариантов Fc-фрагментов антител IgG2 человека. Эти варианты имеют повышенную аффинность связывания с FcγRIIB. Ожидается, что агонистические антитела, содержащие такие варианты Fc-фрагмента, будут иметь лучшую агонистическую активность.
Предшествующий уровень техники
Разработка биомакромолекулярных лекарственных средств обеспечивает новые методы и возможности лечения различных заболеваний, в частности молекулярной направленной терапии, основанной на антителах и константных областях тяжелой цепи (включающих Fc-фрагменты), включая антитела и слитые белки константных областей тяжелой цепи, которые имеют большой успех в области биофармацевтических средств и продолжают оставаться в центре внимания в этой области.
В соответствии с разными функциями, биомакромолекулы могут быть в основном разделены на три категории: эффекторные молекулы, которые освобождают мишени (молекулы и клетки), блокирующие молекулы, которые блокируют мишень-вовлеченные сигнальные пути и агонистические молекулы, которые активируют сигнальные пути, расположенные ниже мишени. В последние годы в иммунотерапии опухоли были сделаны важные открытия. Этому способствует использования антител, которые увеличивают активность иммунных клеток, которые убивают опухоли путем блокирования молекул, ингибирующих иммунные контрольные точки. Тем не менее существует большое количество больных раком, не отвечающих на существующие средства лечения. Следовательно, с одной стороны, необходимо оптимизировать существующие средства иммунотерапии опухолей; с другой стороны, необходимо разрабатывать новые лекарственные средства для иммунотерапии опухоли. Следует отметить, что существует класс средств для иммунотерапии опухоли, называемый "Агонистические антитела", которые способны усиливать противоопухолевый иммунный ответ, чтобы опосредованно убивать опухолевые клетки путем связывания целевых молекул на поверхности иммунной клетки, которые пропускают сигнал активации и активируют важные сигнальные пути иммуноактивации, контролируемые целевыми молекулами. Однако в то время как агонистические антитела для иммунотерапии опухолей продемонстрировали свой огромный потенциал в животных моделях и были широко приняты и оценены в качестве хорошей концепции иммунотерапии опухоли, исследования и разработка таких антител еще не были успешными и являются серьезной проблемой в области иммунотерапии опухоли. Кроме того, активация агонистическими антителами также представляет собой эффективное средство вмешательства и регуляции ключевых сигнальных путей других биологических процессов и имеет широкую перспективу применения в области профилактики и лечения заболеваний. Например, активация иммуносупрессивного сигнального пути может быть полезной для смягчения воспаления и аутоиммунных симптомов.
Антитело, главным образом, взаимодействует с FcγR посредством его константной области и аффинность связывания разных антител с FcγR также варьирует, что также влияет на функцию антитела in vivo. Модификация Fc антитела является важным средством и тенденцией для оптимизации терапевтических антител, где изменение аффинности взаимодействия Fc-области антитела с ключевым белком, таким как FcγR, является очень эффективным способом оптимизировать активность антитела.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Для решения вышеприведенных проблем в настоящем изобретении предложены аминокислотные мутации и комбинации, способные повысить аффинность Fc-фрагмента к FcγRIIB путем выполнения мутационной модификации в Fc-области на основе IgG; и Fc, содержащие эти аминокислотные мутации могут быть использованы для оптимизации активности антитела, в частности, для улучшения активационной активности агонистического антитела.
В первом аспекте настоящего изобретения предложен мутантный полипептидный Fc-фрагмент, имеющий следующие признаки:
(1) указанный мутантный полипептидный Fc-фрагмент имеет мутацию по сравнению с соответствующим Fc-фрагментом дикого типа до мутации; и
(2) аффинность мутантной Fc-области к FcγRIIB повышена по сравнению с Fc-областью дикого типа; и Fc дикого типа представляет собой Fc дикого типа IgG2.
В другом предпочтительном воплощении мутантный полипептидный Fc-фрагмент имеет мутацию, выбранную из группы, состоящей из: L328, Н268, S267, Р271, G327 или их комбинации, по сравнению с соответствующим Fc-фрагментом дикого типа до мутации;
где нумерация всех аминокислот основана на нумерации EU для IgG.
В другом предпочтительном воплощении аффинность может быть воплощена как степень обогащения скрининга или сигнал в анализе связывания.
В другом предпочтительном воплощении Fc-фрагмент дикого типа представляет собой область от остатка в 233-м положении до остатка в 332-м положении аминокислотной последовательности IgG2 в соответствии с EU нумерацией IgG, и аминокислотная последовательность Fc-фрагмента дикого типа является такой, как показано в SEQ ID NO: 20.
В другом предпочтительном воплощении, мутантный полипептидный Fc-фрагмент имеет повышенную аффинность к FcγRIIB по сравнению с Fc-фрагментом дикого типа.
В другом предпочтительном воплощении аффинность мутантного полипептидного Fc-фрагмента к FcγRIIB увеличена более чем в 1 раз по сравнению с аффинностью Fc-фрагмента дикого типа к FcγRIIB; предпочтительно выше в 2, 3, 4, 5, 10, 20, 50 или 100 раз.
В другом предпочтительном воплощении аффинность мутантного полипептидного Fc-фрагмента к активирующим FcγR меньше, чем аффинность к FcγRIIB.
В другом предпочтительном воплощении аффинность мутантного полипептидного Fc-фрагмента к FcγRIIB повышена и аффинность мутантного полипептидного Fc-фрагмента к активирующим FcγR снижена (соотношение I/A выше, чем это соотношение для Fc-фрагмента дикого типа), по сравнению с Fc-фрагментом дикого типа.
В другом предпочтительном воплощении соотношение (RIIB/RIIAR) аффинности мутантного полипептидного Fc-фрагмента к FcγRIIB и FcγRIIA131R выше, чем это соотношение для IgG2 дикого типа.
В другом предпочтительном воплощении активирующие FcγR содержат: FcγRI, FcγRIIA131H, FcγRIIA131R, FcγRIIIA158F и FcγRIIIA158V.
В другом предпочтительном воплощении мутация L328 включает L328W, L328E, L328Y, L328F, L328M, L328A, L328G, L328N, L328P, L328R, L328V; предпочтительно L328W или L328E.
В другом предпочтительном воплощении, мутация Н268 включает H268D, H268S, Н268Е, H268K, H268N, предпочтительно представляет собой H268D, H268S или Н268Е.
В другом предпочтительном воплощении, мутация S267 включает S267E, S267V, S267D, S267M, S267Q, S267A, S267G, S267R, S267N, S267W; предпочтительно S267E, S267V, S267D, S267M; более предпочтительно представляет собой S267E.
В другом предпочтительном воплощении, мутация Р271 включает Р271С, P271G, P271V, Р271А, P271W, P271Y, P271Q, Р271Т, P271L P271L, P271S; предпочтительно представляет собой Р271С, P271G, P271V, Р271А, P271W, P271Y, P271Q, Р271Т; более предпочтительно представляет собой Р271С, P271G.
В другом предпочтительном воплощении, мутация G327 включает G327A, G327L, G327S; предпочтительно G327A.
В другом предпочтительном воплощении мутантный полипептидный Fc-фрагмент имеет мутацию, выбранную из группы, состоящей из L328W, L328E, H268D, H268S, Н268Е, S267E, A330S, P233G, P271G, Р271С, P271V, Р271А, P271W, P271Y, G327A, или их комбинацию, по сравнению с Fc-фрагментом дикого типа; где нумерация всех аминокислот основана на Eu нумерации IgG.
В другом предпочтительном воплощении мутантный полипептидный Fc-фрагмент имеет мутацию по меньшей мере в одном из L328 и Н268 по сравнению с Fc-фрагментом дикого типа, и конкретные мутации в мутантном полипептидном Fc-фрагменте выбраны из одной из группы, состоящей из: L328W, L328E, H268D, H268S, Н268Е, H268D/S298L/L328W, S267V/S298L/L328W, V234M/S267E/S298L/L328W, A235W/V266L/S298L/L328W, V234Q/A235G/P238L/S239V/H268D/G327A/L328E/A330S/I332T, S239V/V266L/S298L/L328W, V266L/L328W, V266L/S267D/H268D/E269D/P271Q, S267E/H268S/E269D, P233F/V266L/S298L/L328W, V266L/S298L/L328W, V234Q/A235G/P238L/S239V/G327A/L328E/A330S/I332T, V266L/S267E/H268S/E269V, V266L/S267E/H268S/E269V/P271C, V266L/S267E/H268S/E269A/P271C, S267V/S298G/L328W, V266L/S267M/H268E/P271Q, V266L/S267E/H268S/E269G/P271T, V234Q/V266L/S267D/H268D/E269D/P271Q, V234Q/A235G/P238L/S239V/S267E/H268S/E269D, V266L/S267E/H268S/P271V, V234Q/A235G/P238L/S239V/S267E/S298L/G327A/L328E/A330S/I332T, V234Q/V266L/S267E/H268S/E269V, L328E/I332T; где нумерация всех аминокислот основана на Eu нумерации IgG.
В другом предпочтительном воплощении, мутантный полипептидный Fc-фрагмент имеет мутацию в S267 относительно Fc-фрагмента дикого типа, и конкретная мутация в мутантном полипептидном Fc-фрагменте выбрана из одной из группы, состоящей из: S267E/A330S, S267E/S298G, P233G/S267E, V234M/S267E/S298G/I332L, P233G/S267E/S298G, V266L/S267E/E269K/P271G, P238Q/S267E, S267A/P271C, S267A/P271G, S267E/D270H, S267E/P271C, S267E/P271V, S267E/P271W, S267E/P271Y, S267E/S298R, S267M/P271C, S267M/P271G, S267V/S298L, S267E/P329R; где нумерация всех аминокислот основана на Eu нумерации IgG.
В другом предпочтительном воплощении, мутантный полипептидный Fc-фрагмент имеет мутацию в S267 относительно Fc-фрагмента дикого типа и конкретная мутация в мутантном полипептидном Fc-фрагменте выбрана из одной из групп, состоящей из: S267E/A330S, S267E/S298G, P233G/S267E, V234M/S267E/S298G/I332L, P233G/S267E/S298G, V266L/S267E/E269K/P271G, S267E/P271C; где нумерация всех аминокислот основана на Eu нумерации IgG.
В другом предпочтительном воплощении мутантный полипептидный Fc-фрагмент имеет мутацию в Р271 относительно Fc-фрагмента дикого типа, и конкретная мутация в мутантном полипептидном Fc-фрагменте выбрана из одной из группы, состоящей из: V266L/S267E/E269K/P271G, V266A/P271C, V266A/P271G, S267A/P271C, S267A/P271G, S267E/P271C, S267E/P271V, S267E/P271W, S267E/P271Y, S267M/P271C, S267M/P271G, V266G/P271C, P271A/S298R, P271G/G236V, P271G/P329S, P271G/P331C, P271G/P331T, P271G/S298D, P271G/S298E, P271G/S298G, P271G/S298K, P271G/S298L, P271G/S298N, P271G/S298R, P271G/T299A, P271G/T299M, P271G/T299S, P271G/T299W, P271G/I332L; где нумерация всех аминокислот основана на Eu нумерации IgG.
В другом предпочтительном воплощении мутантный полипептидный Fc-фрагмент имеет мутацию в G327 относительно Fc-фрагмента дикого типа, и конкретная мутация в мутантном полипептидном Fc-фрагменте выбрана из одной из группы, состоящей из: G327A/A330R, G327A/A330V, G327A/I332A, G327A/I332C, G327A/I332E.
В другом предпочтительном воплощении конкретная мутация мутантного полипептидного Fc-фрагмента относительно Fc-фрагмента дикого типа выбрана из одной из группы, состоящей из: H268D/S298L/L328W, S267V/S298L/L328W, V234M/S267E/S298L/L328W, A235W/V266L/S298L/L328W, V234Q/A235G/P238L/S239V/H268D/G327A/L328E/A330S/I332T; где нумерация всех аминокислот основана на Eu нумерации IgG.
Во втором аспекте настоящего изобретения предложен мутантную Fc-область иммуноглобулина, содержащий мутантный полипептидный Fc-фрагмент в соответствии с первым аспектом настоящего изобретения.
В другом предпочтительном воплощении иммуноглобулин представляет собой человеческий IgG2.
В другом предпочтительном воплощении мутантная Fc-область иммуноглобулина имеет повышенную аффинность к FcγRIIB по сравнению с Fc-областью IgG2 дикого типа.
В другом предпочтительном воплощении аффинность мутантной Fc-области иммуноглобулина к FcγRIIB повышена более чем 1 раз по сравнению с аффинностью Fc-фрагмента IgG2 дикого типа к FcγRIIB; предпочтительно выше в 2, 3, 4, 5, 10, 20, 50 или 100 раз.
В другом предпочтительном воплощении, аффинность может быть воплощена как степень обогащения скрининга или сигнал в анализе связывания.
В другом предпочтительном воплощении аффинность мутантной Fc-области иммуноглобулина к активирующему FcγR ниже, чем аффинность к FcγRIIB.
В другом предпочтительном воплощении аффинность мутантной Fc-области иммуноглобулина к FcγRIIB повышена, а аффинность мутантной Fc-области иммуноглобулина к активирующему FcγR снижена (соотношение I/A выше, чем это соотношение для Fc-области IgG2 дикого типа), по сравнению с Fc-областью IgG2 дикого типа.
В другом предпочтительном воплощении соотношение (RIIB/RIIAR) аффинности мутантной Fc-области иммуноглобулина к FcγRIIB и FcγRIIA131R выше, чем это соотношение для IgG2 дикого типа.
В третьем аспекте настоящего изобретения предложено антитело, содержащее мутантный полипептидный Fc-фрагмент в соответствии с первым аспектом настоящего изобретения или мутантную Fc-область иммуноглобулина в соответствии со вторым аспектом настоящего изобретения.
В другом предпочтительном воплощении антитело представляет собой антитело на основе остова IgG2 человека.
В другом предпочтительном воплощении антитело представляет собой агонистическое антитело.
В другом предпочтительном воплощении антитело специфически нацелено на суперсемейство рецепторов фактора некроза опухоли.
В другом предпочтительном воплощении антитело способно специфически связываться с мишенью, выбранной из группы, состоящей из CD40, DR5, ОХ40, CD137, CD27, CD30, GITR, HVEM, TACI, DR4, FAS или их комбинации.
В другом предпочтительном воплощении антитело способно специфически связываться с ОХ40.
В другом предпочтительном воплощении антиген, на который нацелено антитело, представляет собой молекулу иммунного рецептора или их комбинацию.
В другом предпочтительном воплощении антиген, на который нацелено антитело, представляет собой молекулу иммуносупрессивного рецептора, которая выбрана из группы, состоящей из: PD-1, CTLA-4, VISTA, TIM-3, BTLA, LAG-3 или их комбинации.
В другом предпочтительном воплощении антитело представляет собой человеческое антитело, гуманизированное антитело или химерное антитело.
В другом предпочтительном воплощении антитело представляет собой моноклональное антитело или поликлональное антитело, предпочтительно моноклональное антитело.
В четвертом аспекте настоящего изобретения предложен слитый белок, содержащий мутантный полипептидный Fc-фрагмент в соответствии с первым аспектом настоящего изобретения, мутантную Fc-область иммуноглобулина в соответствии со вторым аспектом настоящего изобретения или антитело в соответствии с третьим аспектом настоящего изобретения.
В другом предпочтительном воплощении слитый белок дополнительно содержит другие белковые последовательности, имеющие функции агониста рецепторов, или их фрагменты.
В другом предпочтительном воплощении другой белок, имеющий функцию агониста рецепторов, представляет собой цитокин семейства генов TNF.
В другом предпочтительном воплощении, другой белок, имеющий функцию агониста рецепторов, содержит молекулу лиганда иммунного рецептора.
В другом предпочтительном воплощении другой белок, имеющий функцию агониста рецепторов, содержит молекулу лиганда иммунного рецептора, выбранную из любой из группы, состоящей из: CD80, CD86, ICOSL, OX40L, CD137L, CD40L, CD30L, CD27L, CD244, CD150, CD48, CD84, CD319, Ly118 или CD229, или их комбинацию.
В другом предпочтительном воплощении другой белок, имеющий функцию агониста рецепторов, содержит молекулу лиганда иммунного рецептора, и молекула лиганда иммунного рецептора выбрана из группы, состоящей из: PD-L1, PD-L2, В7-Н3, В7-Н4, CD47, VISTA, HVEM, GAL9 или их комбинации.
В другом предпочтительном воплощении слитый белок может дополнительно содержать последовательность метки, полезную для экспрессии и/или очистки; предпочтительно, последовательность метки включает метку 6His, метку НА и/или метку FLAG.
В пятом аспекте настоящего изобретения предложен выделенный полинуклеотид, кодирующий мутантный полипептидный Fc-фрагмент в соответствии с первым аспектом настоящего изобретения, мутантную Fc-область иммуноглобулина в соответствии со вторым аспектом настоящего изобретения, антитело в соответствии с третьим аспектом настоящего изобретения или рекомбинантный белок в соответствии с четвертым аспектом настоящего изобретения.
В шестом аспекте настоящего изобретения предложен вектор, содержащий выделенный полинуклеотид в соответствии с пятым аспектом настоящего изобретения.
В другом предпочтительном воплощении вектор выбран из группы, состоящей из ДНК, РНК, вирусных векторов, плазмид, транспозонов, других систем передачи генов или их комбинаций.
В другом предпочтительном воплощении вектор содержит вирусный вектор, такой как вектор лентивируса, аденовируса, вируса AAV (аденоассоциированный вирус), ретровируса, или их комбинации.
В седьмом аспекте настоящего описания предлагается клетка-хозяин, содержащую вектор в соответствии с шестым аспектом настоящего описания или имеющая полипептид в соответствии с пятым аспектом настоящего описания, интегрированный в геном этой клетки;
или клетка-хозяин, экспрессирует мутантный полипептидный Fc-фрагмент в соответствии с первым аспектом настоящего изобретения, мутантную Fc-область иммуноглобулина в соответствии со вторым аспектом настоящего изобретения, антитело в соответствии с третьим аспектом настоящего изобретения или рекомбинантный белок в соответствии с четвертым аспектом настоящего изобретения.
В другом предпочтительном воплощении клетка-хозяин включает прокариотическую клетку или эукариотическую клетку.
В другом предпочтительном воплощении клетка-хозяин выбрана из группы, состоящей из: E coli, дрожжевых клеток, клеток насекомых, клеток птиц и клеток млекопитающих.
В восьмом аспекте настоящего изобретения предложена фармацевтическая композиция, содержащая:
(а) мутантный полипептидный Fc-фрагмент в соответствии с первым аспектом настоящего изобретения, мутантную Fc-область иммуноглобулина в соответствии со вторым аспектом настоящего изобретения, антитело в соответствии с третьим аспектом настоящего изобретения или рекомбинантный белок в соответствии с четвертым аспектом настоящего изобретения; и
(б) фармацевтически приемлемый носитель.
В другом предпочтительном воплощении фармацевтическая композиция может дополнительно содержать другие лекарственные средства для лечения опухолей, такие как цитотоксические лекарственные средства.
В другом предпочтительном воплощении фармацевтическая композиция может дополнительно содержать другие активные вещества, имеющие функцию агониста рецептора.
В другом предпочтительном воплощении фармацевтическая композиция представляет собой инъекционную лекарственную форму.
В девятом аспекте настоящего изобретения предложен способ получения мутантного полипептидного Fc-фрагмента в соответствии с первым аспектом настоящего изобретения, мутантной Fc-области иммуноглобулина в соответствии со вторым аспектом настоящего изобретения, антитела в соответствии с третьим аспектом настоящего изобретения или рекомбинантного белка в соответствии с четвертым аспектом настоящего изобретения, включающий стадии:
(1) культивирование клетки-хозяина в соответствии с седьмым аспектом изобретения в подходящих условиях с получением культуры, содержащей указанный мутантный полипептидный Fc-фрагмент, указанную мутантную Fc-область иммуноглобулина, указанное антитело или указанный рекомбинантный белок; и
(2) очистка и/или выделение указанного мутантного полипептидного Fc-фрагмента, указанной мутантной Fc-области иммуноглобулина, указанного антитела или указанного рекомбинантного белка из культуры, полученной на стадии (1).
В другом предпочтительном воплощении очистка может быть выполнена посредством очистки на аффинной колонке с белком А с получением целевого антитела. В другом предпочтительном воплощении очистка может быть выполнена посредством очистки на аффинной колонке с белком G с получением целевого антитела.
В другом предпочтительном воплощении чистота целевого антитела после очистки и/или выделения составляет более 95%, более 96%, более 97%, более 98%, более 99%, предпочтительно 100%.
В десятом аспекте настоящего изобретения предложено применение мутантного полипептидного Fc-фрагмента в соответствии с первым аспектом настоящего изобретения, мутантной Fc-области иммуноглобулина в соответствии со вторым аспектом настоящего изобретения, антитела в соответствии с третьим аспектом настоящего изобретения, рекомбинантного белка в соответствии с четвертым аспектом настоящего изобретения, полинуклеотида в соответствии с пятым аспектом настоящего изобретения, вектора в соответствии с шестым аспектом настоящего изобретения и/или клетки-хозяина в соответствии с седьмым аспектом настоящего изобретения, в изготовлении фармацевтической композиции для иммунотерапии опухоли, для уменьшения воспаления и/или уменьшения аутоиммунных симптомов.
В одиннадцатом аспекте настоящего изобретения предложен способ лечения заболевания, включающий стадии: введение субъекту, нуждающемуся в этом, мутантного полипептидного Fc-фрагмента в соответствии с первым аспектом настоящего изобретения, мутантной Fc-области иммуноглобулина в соответствии со вторым аспектом настоящего изобретения, антитела в соответствии с третьим аспектом настоящего изобретения, рекомбинантного белка в соответствии с четвертым аспектов настоящего изобретения, полинуклеотида в соответствии с пятым аспектом настоящего изобретения, вектора в соответствии с шестым аспектом настоящего изобретения, клетки-хозяина в соответствии с седьмым аспектом настоящего изобретения, и/или фармацевтической композиции в соответствии с восьмым аспектом настоящего изобретения.
В другом предпочтительном воплощении субъект включает млекопитающее, предпочтительно человека.
В другом предпочтительном воплощении заболевание выбрано из группы, состоящей из: опухолей, воспалительных заболеваний, аутоиммунных заболеваний или их комбинаций.
В другом предпочтительном воплощении рак включает, без ограничения ими, рак молочной железы, рак предстательной железы, рак легкого, рак яичника, рак шейки матки, рак кожи, меланому, рак толстой кишки, рак желудка, рак печени, рак пищевода, рак почки, рак горла, рак щитовидной железы, рак поджелудочной железы, рак яичка, рак головного мозга, рак кости и рак крови (такой как лейкемия, хронический лимфоцитарный лейкоз) и т.д.
В другом предпочтительном воплощении рак включает, без ограничения ими, базально-клеточную карциному, рак желчных протоков, рак мочевого пузыря, рак кости, рак головного мозга и центральной нервной системы (CNS), рак шейки матки, хориокарциному, колоректальный рак, рак соединительной ткани, рак пищеварительной системы, рак эндометрия, рак пищевода, рак глаза, рак головы и шеи, рак желудка, эпителиальное новообразование, рак почки, рак горла, рак печени, рак легкого (мелкоклеточный, немелкоклеточный), лимфому (включая лимфому Ходжкина и неходжкинскую лимфому); меланому; нейробластому; рак полости рта (например губы, языка, рта и глотки); рак яичника; рак поджелудочной железы; ретинобластому; рабдомиосаркому; рак прямой кишки; рак дыхательных путей; саркому; рак кожи; рак желудка; рак яичка; рак щитовидной железы; рак матки; рак мочевой системы; и другие виды рака и саркомы.
В другом предпочтительном воплощении способ может быть использован для стимуляции иммунного ответа для лечения опухолей путем ингибирования или задержки роста опухоли или уменьшения размера опухоли.
В другом аспекте настоящего изобретения дополнительно предложен способ скрининга аминокислотных мутаций, повышающих аффинность протеин-молекулярного связывания, где способ включает следующие стадии:
1) определение последовательности родительского белка, введение аминокислотных мутаций в последовательность родительского белка посредством ПЦР;
2) конструирование родительского белка и мутантного белка в экспрессионном векторе с получением библиотеки мутаций;
3) трансфекция экспрессионного вектора в клетки млекопитающих и экспрессирование родительского белка и мутантного белка на клеточной поверхности;
4) инкубация меченных взаимодействующих молекул и клеток млекопитающих, и выбор меченых клеток млекопитающих с помощью проточной цитометрии или магнитно-активированной сортировки;
5) извлечение ДНК из меченых клеток млекопитающих, секвенирование ДНК и анализ изменения соотношений для последовательностей до и после сортировки;
где аминокислотная мутация, в которой соотношение после сортировки значительно выше, чем соотношение до сортировки, представляет собой аминокислотную мутацию, способную повысить аффинность связывания белка и взаимодействующей молекулы.
Данный метод скрининга может эффективно отбирать различные аминокислотные мутации, очень удобен и эффективен, и может использоваться для скрининга аминокислотных мутаций, которые усиливают различные белок-белковые взаимодействия или взаимодействия белка с другими молекулами.
Положительное влияние настоящего изобретения включает: модифицированный Fc-фрагмент или Fc-фрагмент по настоящему изобретению, который имеет повышенную аффинность к FcγRIIB, а некоторые из них имеют пониженную аффинность к активирующим FcγR при повышенной аффинности к FcγRIIB. Эти белки могут быть использованы для конструирования, модификации или оптимизации активационной активности антител или слитых белков. В частности, можно создать агонистическую активность антитела или слитого белка на основе остова IgG2 человека. Таким образом, можно предложить белки со значительно повышенной агонистической активностью для лечения опухолей, воспалительных заболеваний, аутоиммунных заболеваний или их комбинации, что имеет значительную перспективу для применения.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
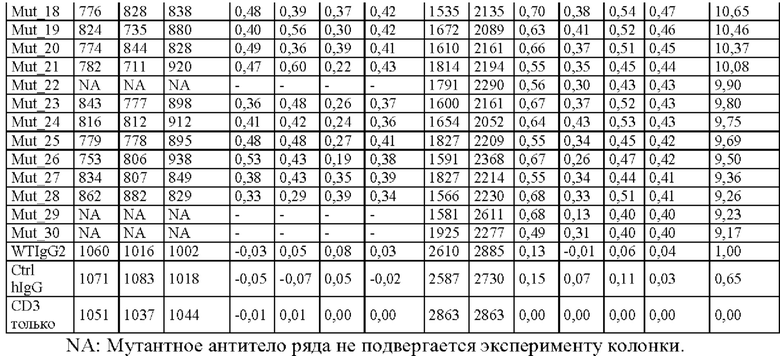
НА ФИГ. 1 показана конструкция плазмиды для экспонирования антител на поверхности клеток млекопитающих.
НА ФИГ. 2 показано схематическое изображение процесса отбора мутаций. В частности, этот процесс включает: создание библиотеки мутаций и перенос ее в клетки с помощью ретровируса; библиотека мутаций Fc экспрессируется на поверхности клеток; отбирают клетки с высокой аффинностью к FcγRIIB; выделяют ДНК и секвенируют с помощью высокопроизводительного секвенирования (NSG); анализируют обогащение различных мутаций после сортировки по сравнению с их количеством до сортировки и отбирают мутации с относительно высоким коэффициентом обогащения по сравнению с диким типом.
НА ФИГ. 3 показана Eu нумерация аминокислот СН2 на IgG2 Fc человека.
НА ФИГ. 4 показано, что сортировка с помощью проточной цитометрии может постепенно обогащать клетки высокой аффинностью связывания с FcγRIIB. Показаны результаты сортировки человеческих клеток IgG2 дикого типа и человеческих клеток IgG2 библиотеки LibraryMix после одного или двух раундов сортировки с FcγRIIB соответственно.
НА ФИГ. 5 показано, что аффинность связывания клеток, отобранных из библиотеки, с FcγRIIB значительно улучшена. Показаны результаты проточной цитометрии IgG2 человеческих клеток дикого типа и клеточных библиотек после двух раундов сортировки с FcγRIIB соответственно.
НА ФИГ. 6 показана схематическое изображение двух типов библиотек комбинированных мутаций. Тип I: комбинированная точечная мутация четырех областей, то есть каждая из областей P233-V240, V266-P271, S298-T299 и G327-I332 имеет 0-1 мутацию, и комбинированная мутация содержит 0-4 точечные мутации. Тип II: комбинированная мутация множественных аминокислот в одной области, то есть области P233-V240, V266-P271, S298-T299 или G327-I332 имеют комбинированную мутацию внутри каждой области (соответственно 0-7, 0-6, 0-2 и 0-6 комбинированных мутаций).
НА ФИГ. 7 показаны результаты проточной цитометрии для библиотеки IgG2_С01 и библиотеки IgG2_С02 после сортировки с помощью проточной цитометрии и IgG2 дикого типа. Соотношение клеток, связывающихся с FcγRIIB в библиотеке IgG2_C01 и библиотеке IgG2_C02 улучшено.
НА ФИГ. 8 показана аффинность связывания клеток библиотеки Cmix и библиотеки С2 с FcγRIIB до ("_befor") и после ("_1-ый" и "_2-ой") сортировки с помощью проточной цитометрии. Результаты показывают, что соотношение связывания клеток с FcγRIIB в отсортированной библиотеке постепенно увеличивается (2-ое>1-ое>befor).
НА ФИГ. 9 показана аффинность связывания разных Fc-мутантов антитела IgG2 с FcγRI (выражена в виде сигнала ELISA: поглощение при 650 нм (А650)).
НА ФИГ. 10 показана аффинность связывания разных Fc-мутантов антитела IgG2 с FcγRIIA131H (выражена в виде сигнала ELISA: поглощение при 650 нм (А650)).
НА ФИГ. 11 показана аффинность связывания разных Fc-мутантов антитела IgG2 с FcγRIIA131R (выражена в виде сигнала ELISA: поглощение при 650 нм (А650)).
НА ФИГ. 12 показана аффинность связывания разных Fc-мутантов антитела IgG2 с FcγRIIB (выражена в виде сигнала ELISA: поглощение при 650 нм (А650)).
НА ФИГ. 13 показана аффинность связывания разных Fc-мутантов антитела IgG2 с FcγRIIIA158F (выражена в виде сигнала ELISA: поглощение при 650 нм (А650)).
НА ФИГ. 14 показана аффинность связывания разных Fc-мутантов антитела IgG2 с FcγRIIIA158V (выражена в виде сигнала ELISA: поглощение при 650 нм (А650)).
НА ФИГ. 15 показана аффинность связывания мутантов IgG2, соответствующих IgG1 V11 (hIgG1V11) с FcγRIIA131H и FcγRIIB с помощью ELISA (выражена в виде сигнала ELISA: поглощение при 650 нм (А650)).
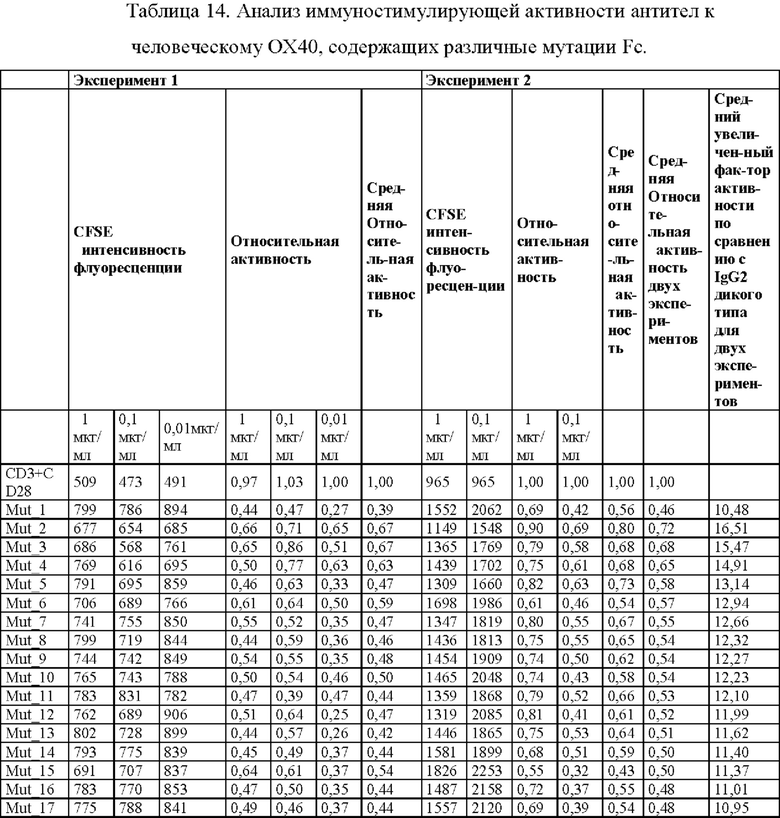
НА ФИГ. 16 показаны результаты анализа активационной активности разных антител против человеческого ОХ40 с мутантным Fc антитела, представленные в виде гистограммы средней флуоресцентной интенсивности CFSE CD4-положительных клеток (чем ниже сигнал CFSF, тем выше активность).
НА ФИГ. 17 показаны результаты анализа активационной активности разных антител против человеческого ОХ40 с мутантным Fc антитела, представленные в виде гистограммы средней флуоресцентной интенсивности CFSE CD4-положительных клеток (чем ниже сигнал CFSF, тем выше активность).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Если не указано иное, научные и технические термины, используемые здесь, следует понимать, как имеющие значение, обычно подразумеваемое специалистом в данной области. Если не требуется иное, при использовании здесь, термины в единственном числе включают значение во множественном числе и наоборот. В целом, при использовании в данном описании изобретения, терминология и методы культивирования/инкубации клеток и тканей, молекулярной биологии, иммунологии, химии белков и нуклеиновых кислот, описанных в данном документе, уже известны и обычно используются в данной области.
Методы и техники, используемые в настоящем изобретении, обычно выполняются, как в обычных практиках, и как описано в общих и специализированных ссылках, указанных и обсуждаемых в этом раскрытии, если не указано иное. Например, ссылка может быть сделана на следующие работы: Molecular Cloning: A Laboratory Manual, Sambrook et al., the 2nd Edition, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., 1989; Current Protocols in Molecular Biology, Ausubel et al. Greene Publishing Associates, 1992; Antibodies: A Laboratory Manual, Harlow and Lane, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., 1990, все из которых включены в данное описание во всей полноте. Ферментативные реакции и очистки выполняют, следуя инструкциям производителей или как известно в данной области техники или как указано в настоящем раскрытии. Используемая здесь терминология, методы исследования и методики из биологии, фармакологии, медицины и фармацевтической химии являются такими, которые уже известны и обычно используются в данной области. Химический синтез, химический анализ, фармацевтическое производство, составление композиций, доставка и лечение пациентов, все следуют стандартной практике.
Если не указано иное, термины имеют значения, определенные ниже.
"Антитело" (Ab) должно включать, без ограничения ими, гликопротеин, иммуноглобулин или его антигенсвязывающие части. Антитела специфически связываются с соответствующими антигенами и каждое содержит по меньшей мере две тяжелые (Н) цепи и две легкие (L) цепи, которые соединены друг с другом через дисульфидные связи. Каждая тяжелая цепь содержит вариабельную область тяжелой цепи (VH) и константную область тяжелой цепи. "Константная область тяжелой цепи" или CD антител содержит три домена, называемых как CH1, СН2 и СН3, а также шарнирную область между доменом СН1 и доменом СН2. Каждая легкая цепь содержит вариабельную область легкой цепи (VL) и константную область легкой цепи. Константная область легкой цепи состоит из одного домена CL. Каждая из VH и VL может быть подразделена на гипервариабельные области, называемые "определяющие комплементарность области (CDR)" и промежуточные относительно консервативные области, называемые "каркасные области (FR)". Каждая из VH и VL состоит из трех CDR и четырех FR, расположенных в следующем порядке от амино-конца к карбоксильному концу: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелой и легкой цепи обеспечивают домены, которые взаимодействуют с антигенами.
"Fc-область" (область кристаллизуемого фрагмента) или "Fc-домен" или "Fc" относится к С-концевой части тяжелой цепи, которая опосредует связывание между иммуноглобулином и тканями или факторами хозяина, включая связывание с Fc-рецепторами на различных иммунных клетках (например эффекторных клетках) или с первым компонентом классической системы комплемента (C1q). Таким образом, Fc-область представляет собой полипептид, который образует часть константной области тяжелой цепи антитела, отличную от первого домена константной области иммуноглобулина (домен СН1). Для аллотипов антител IgG, IgA и IgD, Fc-область состоит из двух идентичных белковых фрагментов из доменов СН2 и СН3 двух тяжелых цепей; и в IgM и IgE, Fc-область содержит три константных домена тяжелой цепи (домены СН2-СН3-СН4) в каждой полипептидной цепи. Для IgG, Fc-область содержит шарнирную область между доменами иммуноглобулина СН2 и СН3 и шарнирную область между CH1 и СН2. Несмотря на то, что границы Fc-областей тяжелых цепей иммуноглобулина различны, Fc-области в тяжелых цепях человеческих IgG обычно определяют, как сегмент, охватывающий от положения Р231 до карбоксильного конца тяжелых цепей, пронумерованной в соответствии с EU индексом, таким же, как система нумерации Кабата. Домен СН2 области Fc человеческого IgG простирается примерно от аминокислоты 231 до примерно аминокислоты 340, в то время как домен СН3 расположен на С-конце домена СН2 Fc-области, то есть он простирается примерно от аминокислоты 341 в IgG до примерно аминокислоты 447.
"Полипептидный Fc-фрагмент" относится к фрагменту, содержащему в Fc-области. Полипептидный Fc-фрагмент в данном описании изобретения относится к фрагменту, простирающемуся от аминокислоты 233 до аминокислоты 332 в Fc-области, или к другим фрагментам внутри Fc-области, содержащей указанный фрагмент, такому как домен Fc СН2 или Fc-область.
При использовании здесь "Fc-область" или "полипептидный Fc-фрагмент" может быть природным Fc или модифицированным Fc. Кроме того, "Fc-область" или "полипептидный Fc-фрагмент" может также относиться к такой области в выделенном состоянии, или такой области, представленной в полипептиде белка, содержащего Fc, который также называется "слитый Fc-белок " (например антитело или иммуноадгезин).
"Fc-рецептор" или "FcR" представляет собой рецептор, связывающийся с Fc-областью иммуноглобулина. FcR, связывающиеся с антителами IgG, включают семейство FcγR, содержащее их аллельные варианты и альтернативные варианты сплайсинга. Представители семейства человеческого Fcγ-рецептора включают FcγRI (CD64), FcγRIIA (CD32a), FcγRIIB (CD32b), FcγRIIIA (CD16a), FcγRIIIB (CD16b). При этом FcγRIIB представляет собой единственный ингибирующий Fcγ-рецептор, а все остальные являются активирующими Fcγ-рецепторами. Большинство природных эффекторных клеток совместно экспрессируют один или более активирующих FcγR и ингибирующий FcγRIIB, в то время как клетки естественного киллера (NK) избирательно экспрессируют активирующий Fcγ рецептор (FcγRIII у мышей, FcγRIIIA у людей), но не ингибирующий FcγRIIB у мышей и людей. Эти Fcγ-рецепторы имеют разные молекулярные структуры и, следовательно, разную аффинность к субклассами IgG антител. Среди этих Fcγ-рецепторов, FcγRI представляет собой высокоаффинный рецептор, в то время как FcγRIIA, FcγRIIB и FcγRIIIA являются низко аффинными рецепторами. В этих разных Fcγ-рецепторах наблюдается генетический полиморфизм, что также влияет на аффинность связывания. Наиболее доминантные генетические полиморфизмы включают R131/H131 в FcγRIIA и V158/F158 в FcγRIIIA. Обнаружено, что некоторые из этих полиморфизмов связаны с заболеванием. И реактивность на некоторые терапевтические антитела зависит от присутствия определенных полиморфизмов в Fcγ-рецепторах.
При использовании здесь "последовательность" следует понимать, как охватывающую последовательности, которые по существу идентичны определенной в соответствии с изобретением. Термин "по существу идентичные последовательности" относятся к последовательностям, имеющим идентичность последовательности по меньшей мере 70, 75 или 80%, предпочтительно по меньшей мере 90 или 95%, более предпочтительно по меньшей мере 97, 98 или 99% при оптимальном выравнивании с использованием, например, GAP или BESTFIT и значения штрафа за пробел по умолчанию. Предпочтительно, различающиеся остатки представляют собой консервативные аминокислотные замены. Термин "консервативная аминокислотная замена" относится к замене аминокислотных остатков, имеющих похожую химию (например заряд или гидрофильность) в группе R боковой цепи. Как правило, консервативная аминокислотная замена существенно не изменяет функциональные свойства белка. В случае различия(ий) между двумя или более аминокислотными последовательностями остатка(ов) в консервативной(ых) замене(ах), процент идентичности последовательности или значение подобия может быть скорректировано с учетом консервативности замены. Смотрите, например, Pearson, Methods Mol. Biol. 243: 307-31(1994). Примеры аминокислот, имеющих боковые цепи с аналогичной химией, включают: 1) алифатические боковые цепи, включающие глицин, аланин, валин, лейцин и изолейцин; 2) алифатические гидроксильные боковые цепи, включающие серии и треонин; 3) амид-содержащие боковые цепи, включающие аспарагин и глутамин; 4) ароматические боковые цепи, включающие фенилаланин, тирозин и триптофан; 5) основные боковые цепи, включающие лизин, аргинин и гистидин; 6) кислые боковые цепи, включающие аспарагиновую кислоту и глутаминовую кислоту; и 7) серосодержащие боковые цепи, включающие цистеин и метионин. Предпочтительные консервативные аминокислотные замены включают валин-лейцин-изолецин, фенилаланин-тирозин, лизин-аргинин, аланин-валин, глутамат-аспартат и аспарагин-глутамин. Как отмечалось выше, в дополнение к аминокислотным мутациям, представленным в настоящем изобретении, Fc-область, антитело, Fc-фрагмент или слитый белок в соответствии с настоящим изобретением может дополнительно содержать другие возможные модификации, не раскрытые в настоящем изобретении, при условии, что выполняются описанные выше "по существу идентичные" требования.
Аминокислоты антитела и его фрагмента или домена по изобретению нумеруют в соответствии с нумерационной системой Eu для IgG. Типы мутаций некоторых мутантов, вовлеченных в настоящее изобретение, и их номенклатура, показаны в Таблице 1.
Антитела обычно специфически связываются с соответствующими антигенами с высокой аффинностью (аналогично, белки по изобретению могут также специфически связываться с их молекулами распознавания эпитопа), на что указывает, например, константа диссоциации (KD), равная 10-5-10-11 M или менее. KD выше чем примерно 10-4 М-1 обычно указывает на неспецифическое связывание. В данном описании антитело, "специфически связывающееся с" антигеном, означает, что антитело связывается с этим антигеном или по существу идентичным антигеном с высокой аффинностью, измеренной в виде KD, равной 10-7 М или менее, предпочтительно 10-8 M или менее, более предпочтительно 5×10-9 M или менее, и наиболее предпочтительно 10-8-10-10 М или менее, и не связывается ни с каким нерелевантным антигеном со значительной аффинностью. Антиген является "по существу идентичным" определенному антигену, если он имеют высокую идентичность последовательности, например идентичность последовательности по меньшей мере 80%, по меньшей мере 90%, предпочтительно по меньшей мере 95%, более предпочтительно по меньшей мере 97%, или еще более предпочтительно по меньшей мере 99%.
Иммуноглобулины можно брать из любой широко известной изоформы. Изоформы IgG могут быть подразделены на подклассы у некоторых видов: IgG1, IgG2, IgG3 и IgG4 у человека, IgG1, IgG2A, IgG2B и IgG3 у мышей. Термин "изотип" относится к антителам, кодируемым генами константной области тяжелой цепи (например IgM или IgG1). "Антитела" включают природные и не встречающиеся в природе антитела, моноклональные и поликлональные антитела, химерные и гуманизированные антитела, человеческие и нечеловеческие антитела, полностью синтетические антитела, и одноцепочечные антитела.
"Природный IgG", описанный в настоящем изобретении, относится к таким IgG, которые могут присутствовать в природе, последовательности которых не являются искусственно модифицированными. Следует отметить, что из-за полиморфизма гена, даже натуральные IgG также могут иметь разные мутанты. Любой не искусственно модифицированный IgG в естественном состоянии называется природным IgG, независимо от того, имеет он мутацию или нет.
"Агонистическое антитело" представляет собой антитело, которое связывается с рецептором и активирует его. Примеры такого агонизма включают агонистическое антитело, которое связывается с рецептором суперсемейства фактора некроза опухоли (TNFR) и индуцирует апоптоз клеток, экспрессирующих TNF-рецептор. Анализы определения эффектов, вызывающих апоптоз, описаны в WO 98/51793 и WO 99/37684, которые включены в данный документ посредством ссылки. В конкретном воплощении настоящего изобретения агонистическое анти-CD40 антитело способно повышать противоопухолевый иммунный ответ для опосредованного уничтожения опухолевых клеток посредством связывания с целевой молекулой, передающей сигнал иммуноактивации на поверхности иммунной клетки и активации важного сигнального пути иммуноактивации, контролируемого целевой молекулой. Примеры агонистических антител, которые вошли в клиническое исследование, могут быть указаны в PCT/CN2017/087620.
Термин "агонистическая активность" относится к активности индуцирования некоторых конкретных изменений физиологической активности путем связывания антитела с молекулой антигена и возбуждения молекулы антигена с генерированием сигнала. Молекулы антигена включают рецепторные молекулы и другие молекулы с сигнальными или физиологическими функциями. Указанные конкретные физиологические активности включают, без ограничения ими: пролиферативную активность, активность выживания, активность дифференцировки, транскрипционную активность, мембранно-транспортную активность, аффинность, активность разложения белка, активность фосфорилирования/дефосфорилирования, окислительно-восстановительную активность, активность переноса, активность разложения нуклеиновой кислоты, активность дегидратации, активность индукции клеточной гибели, активность индукции апоптоза и тому подобное.
Термин "родитель" относится к объекту, который модифицируют во время модификации белка. Родитель может быть природным полипептидом, или вариантом, или модифицированной версией природного полипептида. В некоторых воплощениях родительский Fc-фрагмент по настоящему изобретению представляет собой Fc-фрагмент природного IgG.
"Вариант" относится к белку, полученному после модификации родительского белка в результате процесса модификации белка. В частности, варианты могут быть белками, которые получены из родительского белка с помощью мутаций, удалений и/или добавлений аминокислот в родительском белке и сохраняют некоторые или все функции родителя. Предпочтительно, последовательность мутанта в настоящем документе имеет по меньшей мере примерно 80% гомологию с родительской последовательностью, более предпочтительно по меньшей мере примерно 90% гомологию, наиболее предпочтительно по меньшей мере примерно 95% гомологию. Соответственно, используемый здесь термин "Fc вариант" относится к последовательности Fc, которая отличается от родительской Fc-последовательности по меньшей мере одной аминокислотной модификацией. Вариант Fc может содержать только Fc-область, или может присутствовать в контексте антитела, Fc-слияния, выделенного Fc, Fc-области или другого полипептида, который, по существу, кодируется Fc. Вариант Fc может относится к самому полипептиду Fc, к композиции, содержащей вариант полипептида Fc или к аминокислотной последовательности, кодирующей его.
Используемые здесь термины "суперсемейство рецептора фактора некроза опухоли" и "суперсемейство рецептора TNF" оба относятся к рецепторным полипептидам, которые связываются с цитокинами семейства TNF. Как правило, эти рецепторы представляют собой трансмембранные рецепторы типа I, содержащие один или более цистеин-богатых повторов в их внеклеточном домене. Примеры цитокинов семейства TNF включают фактор некроза опухоли-α (TNF-α), фактор некроза опухоли-β (TNF-β или лимфотоксин), лиганд CD30a, лиганд CD27a, лиганд CD40a, лиганд ОХ-40а, лиганд 4-1ВВ, лиганд Аро-1 (также известный, как лиганд Fas или лиганд CD95), лиганд Аро-2 (также известный, как TRAIL), лиганд Аро-3 (также известный, как TWEAK), остеопротегерин (OPG), APRIL, лиганд RANK (также известный, как TRANCE) и TALL-1 (также известный, как BlyS, BAFF или THANK). Примеры рецепторов суперсемейства рецептора TNF включают рецептор фактора некроза опухоли 1 типа (TNFR1), рецептор фактора некроза опухоли 2 типа (TNFR2), рецептор фактора роста нервов р75 (NGFR), В-клеточный поверхностный антиген CD40, Т-клеточный антиген ОХ-40, рецептор Аро-1 (также известный, как Fas или CD95), рецептор Аро-3 (также известный, как DR3, sw1-1, TRAMP и LARD), рецепторы, называемые "трансмембранный активатор и партнер CAML" или "TACI", белок ВСМА, DR4, DR5 (также известный, как Аро-2; TRAIL-R2, TR6, Tango-63, hAPO8, TRICK2 или KILLER), DR6, DcR1 (также известный, как TRID, LIT или TRAIL-R3), DcR2 (также известный, как TRAIL-R4 или TRUNDD), OPG, DcR3 (также известный, как TR6 или М68), CAR1, HVEM (также известный, как ATAR или TR2), GITR, ZTNFR-5, NTR-1, TNFL1, CD30, рецептор лимфотоксина-β (LTBr), рецептор 4-1ВВ и TR9 (ЕР 988,371 А1).
Используемые здесь термины "отношение аффинности к ингибирующему Fcγ-рецептору к аффинности к активирующему Fcγ-рецептору" и "соотношение I/А" оба относятся к соотношению аффинности константной области тяжелой цепи антитела к ингибирующему Fcγ-рецептору (например человеческому FcγRIIB) к его самой высокой аффинности к активирующему Fcγ-рецептору того же вида, например человеческому FcγRI, FcγRIIA, FcγRIIIA, FcγRIIIB.
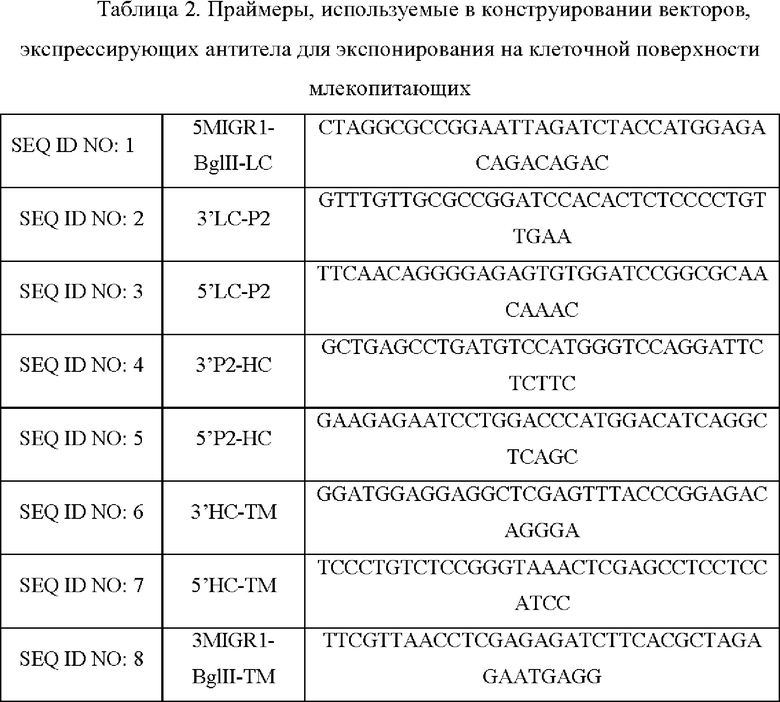
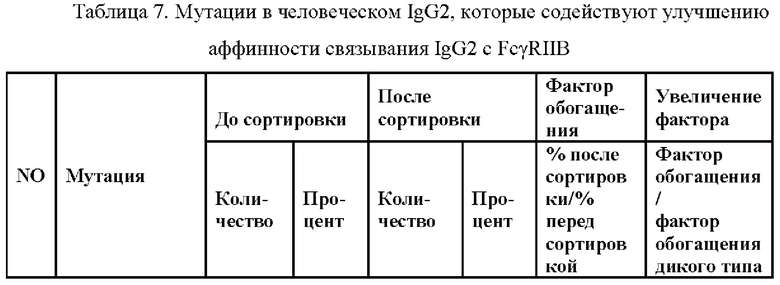
Термин "аффинность" относится к способности двух молекул связываться друг с другом, обычно измеряемой при помощи значения KD. Аффинность здесь также может быть измерена при помощи фактора обогащения (как показано в Таблице 7) или сигнала анализа связывания (как показано на Фиг. 12). Термин "KD" относится к равновесной константе диссоциации взаимодействия между двумя молекулами (например специфического антитела с антигеном или специфического лиганда с рецептором). Термин "фактор обогащения" относится к соотношению процента клеток, экспрессирующих антитело, содержащее конкретную Fc-мутацию после сортировки к такому проценту до сортировки (проанализированному посредством секвенирования второго поколения, как показано в Таблице 7), а сортировка клеток представляет собой сортировку с помощью проточной цитометрии или магнитно-активированную сортировку, предложенную в настоящем изобретении. "Сигнал в анализе связывания" представляет собой значение поглощения в анализе ELISA, предложенном в настоящем изобретении (как показано на Фиг. 12).
"Человеческие" антитела относятся к таким антителам, у которых вариабельные области содержат FR и CDR из человеческих иммуноглобулинов. И антитело может также содержать константную область из человеческого иммуноглобулина, если она присутствует. Человеческое антитело в соответствии с изобретением может включать аминокислотные остатки, не кодируемые последовательностями человеческого иммуноглобулина, такие как мутации, введенные посредством случайного или сайт-направленного мутагенеза in vitro или соматической мутации in vivo. Однако при использовании здесь, термин "человеческое антитело" не предполагает включение таких антител, которые содержат последовательности CDR млекопитающих, не являющихся человеком, (например мышиные), встроенные между человеческими последовательностями каркаса. Термин "человеческое" антитело и "полностью человеческое" антитело используются как синонимы друг друга.
"Антитела" по изобретению включают природные и не встречающиеся в природе антитела, моноклональные и поликлональные антитела, химерные и гуманизированные антитела, человеческие и нечеловеческие антитела и полностью синтетические антитела.
"Гуманизированное" антитело относится к антителу, у которого некоторые аминокислоты, большая часть или все аминокислоты за пределами CDR-доменов, не принадлежащих человеку, заменены соответствующими аминокислотами из человеческого иммуноглобулина. В одном воплощении гуманизированного антитела некоторые, большая часть или все аминокислоты за пределами этих CDR-доменов заменены соответствующими аминокислотами из человеческого иммуноглобулина, а некоторые, большинство или все аминокислоты в одном или более CDR остаются без изменений. Незначительное добавление, делеция, вставка, замена или модификация аминокислоты) приемлемо, при условии, что это изменение не препятствует способности антитела связываться с соответствующим антигеном. "Гуманизированное" антитело сохраняет антиген-связывающую специфичность исходного антитела.
"Химерное антитело" относится к антителу, у которого вариабельная(ые) область(и) происходит(ят) из одного вида, а константная(ые) область(и) из другого, например к антителу, у которого вариабельная(ые) область(и) может(гут) происходить из мышиного антитела, а константная(ые) область(и) из человеческого антитела.
Далее описание проиллюстрировано конкретными примерами, описанными ниже. Следует понимать, что эти примеры являются лишь иллюстративными и не ограничивают объем настоящего описания. В экспериментальных методах без уточнения конкретных условий в следующих примерах, как правило, использовали обычные условия, такие как описаны в Sambrook, Molecular Cloning: A Laboratory Manual (New York: Cold Spring Harbor Laboratory Press, 1989), или следовали рекомендациям производителя. Если не указано иное, проценты и части указывали по массе.
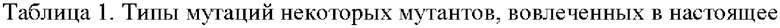
Материалы и методы
Конструирование вектора для экспонирования на поверхности клеток млекопитающего
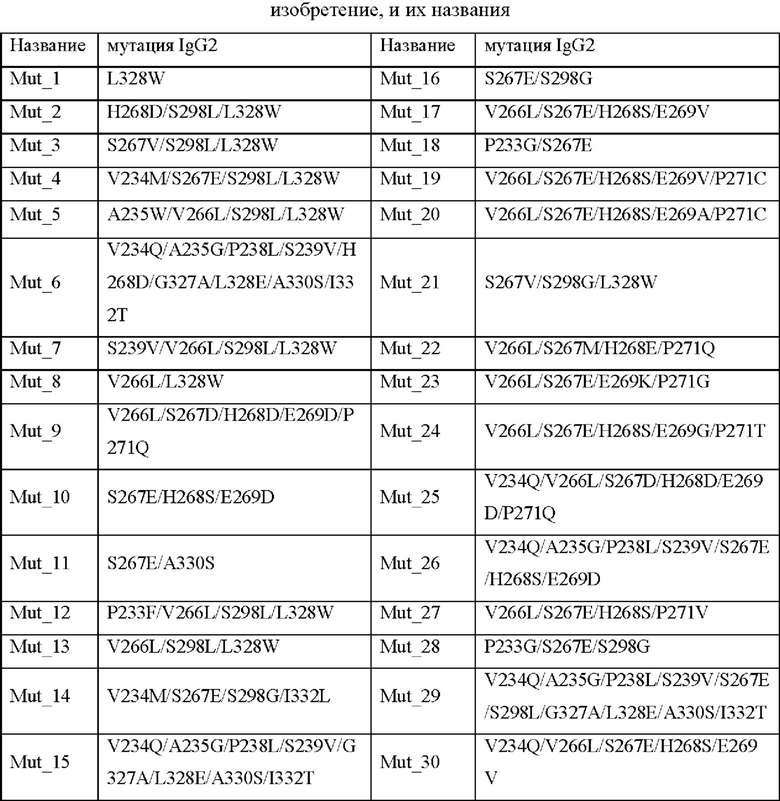
Полноразмерные последовательности легкой и тяжелой цепи человеческого IgG2-антитела к CD40 мыши конструируются на основе ретровирусного вектора MIGRI (Addgene, Pear et al. Blood. 1998 Nov 15. 92(10):3780-92) с помощью набора для многоэтапного клонирования Multi One Step Cloning (Yeasen Biotechnology (Shanghai) Co., Ltd., China). Используемые праймеры показаны в Таблице 2, и конструкция показана на Фиг. 1. В вектор, рестрицированный с помощью рестрикционной эндонуклеазы BglII, вставляли легкую цепь ДНК и тяжелую цепь ДНК (связанные посредством саморасщепляющегося линкера Р2А) полного антитела; конец тяжелой цепи ДНК содержал трансмембранный домен ДНК (последовательность ДНК каждого фрагмента показана в Таблице 3). Плазмида экспрессирует белок GFP при экспрессии человеческого IgG2-антитела. Аминокислотные последовательности поверхностно-экспонированного антитела и его связанной Fc-области показаны в Таблице 4. Конструкцию проверяли секвенированием.





Создание библиотеки Fc-мутантов
Библиотеки точечных мутаций предназначены для введения мутаций с помощью вырожденных праймеров, и были разработаны множественные вырожденные праймеры. Например, вырожденный праймер, используемый для точечной мутации 233 представляет собой CCACCGTGCCCAGCACCANNSGTGGCAGGACCGTCAGTC (SEQ ID NO: 21). Фрагмент библиотеки мутантов и соединительный вектор получали посредством ПЦР, лигировали с помощью набора Multi One Step Cloning Kit (Yeasen Biotechnology (Shanghai) Co., Ltd., China) и трансформировали в DH5α с получением библиотеки мутантов. Для каждой библиотеки отбирали 20 колоний для секвенирования, чтобы подтвердить была ли введена мутация в целевое место.
Метод комбинированной библиотеки мутаций является аналогичным. Праймеры создают в соответствии с типом мутации с обогащением, которое подвергают скринингу в соответствии с библиотекой точечных мутаций. Промежуточную часть вырожденного праймера модифицируют таким образом, чтобы последовательность праймера содержала кодон, кодирующий конкретную аминокислоту, или вырожденный кодон, кодирующий несколько аминокислот, например L328W (TGCAAGGTCTCCAACAAAGGCTGGCCAGCCCCCATCGAGAAAAC, SEQ ID NO: 22), Combine2_1 (ACGTGCGTGGTGGTGGACKNGWBGVASRWSSACCHGGAGGTCCAGTTCAACTGG, SEQ ID NO: 23).
В дополнение к нормальному основанию, R в вышеприведенных праймерах представляет собой A/G, Y представляет С/Т, M представляет А/С, K представляет G/T, S представляет G/C, W представляет A/T, H представляет А/Т/С, В представляет G/T/C, V представляет G/A/C, D представляет G/A/T и N представляет собой A/T/C/G.
Создание стабильно экспрессирующих клеточных линий
Библиотеку плазмиды и хелперной плазмиды Phoenix-Eco (молярное соотношение 2:1) смешивали с реагентом для трансфекции PEI (соотношение по массе 1:5) и добавляли к высеянным на чашки клеткам Phoenix (конфлюентность 80%), заменяли свежую среду через 6 часов и через 48 часов собирали супернатант, содержащий ретровирус. Посеянные на чашки клетки 3Т3 с конфлюентностью 80%, полученные заранее, инфицировали смесью из 50% свежей среды и 50% вышеуказанного ретровирусного супернатанта. Раствор меняли через 24 часа. Через 48 часов могут быть получены клеточные линии, стабильно экспрессирующие антитело.
Анализ с помощью проточной цитометрии клеточных линий, стабильно экспрессирующих антитело
Клетки 3Т3 собирали с помощью расщепления трипсином и получали суспензию одиночных клеток. Примерно 1-5*106 клеток ресуспендировали в 50 мкл буфера FACS (1xPBS, содержащего 0,5% FBS и 2 мМ EDTA), с добавлением PE-F(ab')2 фрагмента козьего античеловеческого IgG (1:500, Jackson ImmunoResearch Laboratories) или биотин-FcγRIIB (1 мкг/мл, Sino Biological) и стрептавидин-АРС (1:500, BD Biosciences). Клетки инкубировали в течение 15 минут на льду, затем дважды промывали буфером FACS и ресуспендировали в 200 мкл буфера FACS и анализировали с помощью проточной цитометрии.
Сортировка клеток с высокой аффинностью к FcγRIIB с помощью проточной цитометрии
Систему окрашивания усиливают в соответствии с вышеуказанным анализом проточной цитометрии и методом окрашивания, и клетки ресуспендируют до конечной концентрации ~1-5*107 клеток/мл перед нанесением. Клетки, экспрессирующие IgG (сильный РЕ флуоресцентный сигнал) и имеющие высокую аффинность к FcγRIIB (сильный АРС флуоресцентный сигнал), сортируют и контролируют, чтобы доля IgG-положительных клеток составляла менее 1%.
Магнитно-активированная сортировка клеток с высокой аффинностью к FcγRIIB и низкой аффинностью к активирующему FcγR (высокое соотношение I/A)
Клетки 3Т3 собирали с помощью расщепления трипсином и получали одноклеточную суспензию. Примерно 1*107 клеток ресуспендировали в 50 мкл буфера MACS (1xPBS, содержащего 0,5% BSA и 2 мМ EDTA) с добавлением биотин-FcγRIIB (1 мкг/мл, Sino Biological) и активирующих FcγR (включающих FcγRI, FcγRIIA131H, FcγRIIA131R, FcγRIIIA158V, FcγRIIIA158F, все по 1 мкг/мл, Shanghai NOVOPROTEIN SCIENTIFIC INC.). Клетки инкубировали в течение 15 минут на льду, а затем дважды промывали буфером MACS и ресуспендировали в 100 мкл буфера MACS. Добавляли двадцать пять мкл анти-биотиновых магнитных гранул и клетки инкубировали в течение 15 минут на льду, а затем один раз промывали буфером MACS, ресуспендировали в 500 мкл и добавляли на LS колонку, помещенную в магнитное поле. Собирали элюат, промывали 3 мл буфера MACS и собирали; затем удаляли LS колонку из магнитного поля и использовали 5 мл буфера MACS для того, чтобы быстро элюировать остальные клетки из сортирующей колонки для сбора положительных клеток, для которых наблюдалось высокое соотношение I/A клеток.
Анализ посредством высокоэффективного секвенирования
Брали примерно 0,1-5*106 клеток целевой клеточной популяции и подвергали клеточному лизису с экстракцией геномной ДНК, выполняли ПЦР (амплификация Fc-фрагмента). Выполняли создание библиотеки и высокоэффективное секвенирование (РЕ 150 или РЕ 250), и примерно 60000-300000 последовательностей были получены для каждого образца. Нуклеотидные последовательности области мутации были извлечены и транслированы в соответствующие аминокислотные последовательности (http://www.cbs.dtu.dk/services/VirtualRibosome/, Rasmus Wernersson. Nucl. Acids Res. 2006 34: W385-W388). Была рассчитана доля каждой мутантной последовательности в каждом образце, где: доля мутантной последовательности = количество мутантной последовательности/общее количество последовательностей.
Очистка и экспрессирование антитела
Перспективный Fc-мутант или новый комбинированный мутант по NGS (секвенирование нового поколения) создают на основе тяжелой цепи антитела к человеческому ОХ40, которую временно трансфицировали в клетки HEK293S вместе с соответствующей легкой цепью для экспрессии белков. Очистку с помощью белка G выполняли для получения разных Fc-мутантных антител, a SDS-PAGE (электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия) использовали для подтверждения того, что структура всех антител является интактной. Последовательность ДНК и последовательность белка антитела к человеческому ОХ40 показаны в Таблице 5 и Таблице 6.




Анализ связывающих свойств мутантного антитела с FcγR посредством ферментного иммуносорбентного анализа (ELISA)
Сто мкл (2 мкг/мл) антитела или его мутанта добавляли к иммуноферментному планшету и оставляли на ночь, затем удаляли супернатант. Планшет блокировали буфером PBS, содержащим 1% BSA, в течение 2 часов и промывали PBST (PBS, содержащий 0,05% Tween 20). Добавляли биотин-меченый внеклеточный доменный белок FcγR (Beijing Sino Biological Co., Ltd) в подходящей концентрации и инкубировали при комнатной температуре в течение 1 часа, затем супернатант удаляли и планшет промывали PBST. Биотин-меченый белок определяли посредством инкубации со стрептавидин-HRP (BD Biosciences) при комнатной температуре в течение 1 часа. Удаляли супернатант и добавляли цветпроявляющий раствор для развития цвета в течение 20-40 минут для определения поглощения при 650 нм (А650).
Анализ иммуноактивационной активности (стимуляции пролиферации Т-клеток) антитела против человеческого ОХ40 другим Fc-мутантным антителом in vitro
Селезенку выделяли из гуманизированных FcγR/OX40 мышей для получения одноклеточной суспензии после лизирования эритроцитов. Выполняли мечение с использованием CFSE (карбоксифлуоресцеин-сукцинимидиловым эфиром). Клетки ресуспендировали в PBS, содержащем 5 мкМ CFSE, до концентрации 5*106/мл и инкубировали при 37°С в течение 15 минут. Затем клетки дважды промывали 5% FBS-содержащим PBS и осаждали при 600g в течение 5 минут, с последующим ресуспендированием клеток в среде для первичной культуры клеток (RPMI + 10% FBS + 1% Pen/Strep + 1% HEPES + 1% пирувата натрия + 0,1% 2МЕ (конечное значение 50 мкМ) + 1% L-глутамина + 1% заменимых аминокислот) до концентрации 3*106/мл. В каждую лунку добавляли 100 мкл клеточной суспензии, то есть 3*105 клеток на лунку. Концентрации антител (к hOX40) разбавляли до 2, 0,2 и 0,02 мкг/мл соответственно, с использованием среды для первичной клеточной культуры, содержащей 0,2 мкг/мл анти-CD3. Сто мкл полученной смеси антител переносили в лунки, содержащие CFSE-меченые гуманизированные FCγR/OX40 клетки селезенки. Двумя группами контролей были: только CD3 группы, содержащие CFSE-меченые клетки и анти-мышиные CD3, но без каких-либо других антител; и CD3+CD28 группы, содержащие CFSE-меченые клетки и анти-мышиные CD3 и 2 мкг/мл анти-мышиного CD28 антитела (Клон 37.51 (RUO), BD Biosciences) (конечные концентрации анти-мышиного CD3 и CD28 составляли 0,1 мкг/мл и 1 мкг/мл соответственно). Клетки инкубировали при 37°С в течение 3 суток в 5% CO2 термостатическом инкубаторе для клеток. После окончания культивирования клетки собирали и определяли количество и пролиферацию CD4+ и CD8+ клеток посредством проточной цитометрии. Пролиферацию Т-клеток анализировали посредством проточной цитометрии: культивированные клетки переносили в 96-луночный планшет с U-образным дном, дважды промывали PBS, центрифугировали при 500g в течение 5 минут, затем удаляли супернатант. Клетки ресуспендировали в 50 мкл буфера FACS (PBS, содержащий 0,5% FBS, 2 мМ EDTA), содержащего РЕ анти-мышиные CD4 (Клон: GK1,5, 1:500, BD) и АРС анти-мышиные CD8a (Клон: 53-6,7, 1:500, BioLegend), инкубировали на льду в темноте в течение 15 минут, затем дважды промывали буфером PBS и ресуспендировали в 200 мкл буфера FACS, содержащего DAPI ((4,6-диамидино-2-фенилиндол)) (0,5 мкг/мл, Invitrogen) и гранулы CountBright Absolute Counting beads (Life Technologies, 2 мкл/образец) и анализировали посредством проточной цитометрии.
В настоящем изобретении, главным образом, предложены последовательности мутантного Fc антитела, которые усиливают взаимодействие человеческого IgG2 с FcγRIIB. При этом в настоящем изобретении также предложен способ скрининга и получения этих мутантов. Как показано на Фиг. 2, Fc-мутанты со свойствами специфической аффинности могут быть отобраны в соответствии с вышеуказанным способом.
Кроме того, специалисты в данной области могут отбирать аминокислотные мутации, которые усиливают различные белок-белковые взаимодействия или взаимодействия белков с другими молекулами в соответствии с вышеуказанным методом скрининга, предложенным в настоящем изобретении; где общий метод скрининга включает:
1) предоставление последовательности родительского белка, введение аминокислотных мутаций в последовательность родительского белка посредством ПЦР;
2) встраивание родительского белка и мутантного белка в экспрессирующий вектор для создания библиотеки мутаций;
3) трансфекция экспрессионного вектора в клетки млекопитающих и экспрессирование родительского белка и мутантного белка на поверхности клеток;
4) инкубация меченого взаимодействующего белка и клетки млекопитающего, и выбор меченых клеток млекопитающих посредством проточной цитометрии или магнитно-активированной сортировки клеток;
5) извлечение ДНК из меченых клеток млекопитающего, секвенирование ДНК и анализ изменения долей последовательностей до и после сортировки; где аминокислотная мутация, доля которой после сортировки значительно выше, чем доля до сортировки, представляет собой аминокислотную мутацию, способную усиливать аффинность связывания между белком и взаимодействующим белком.
Пример 1: Создание библиотеки точечных мутаций IgG2_Fc человеческого антитела
Выбраны несколько сайтов на человеческом IgG2_Fc_СН2, включающие Р233-S239, V266-P271, S298-T299 и G327-I332 (Eu нумерация, см. Фиг. 3 и 4). Аминокислоты в этих сайтах мутированы случайным образом, и каждый сайт содержит 20 типов аминокислот (A, R, D, С, Q, E, H, I, G, N, L, K, М, F, Р, S, Т, W, Y, V) в целом, включая дикий тип. Была создана библиотека плазмид со случайными одноточечными мутациями, соответствующими вышеуказанным четырех областям человеческого IgG2_Fc соответственно (Библиотека1, Библиотека2, Библиотека3, Библиотека4), а также смешанная библиотека из этих четырех библиотек (LibraryMix).
Пример 2: Обогащение клеток после сортировки с помощью проточной цитометрии по сравнению с состоянием до сортировки.
После успешного создания плазмидной библиотеки готовят ретровирус, чтобы инфицировать клетки 3Т3 с получением клеточных линий, стабильно экспрессирующих библиотеки. В настоящем изобретении используют сортировку с помощью проточной цитометрии, чтобы отсортировать клетки, экспрессирующие человеческий IgG2 (выявляемый с помощью анти-человеческого IgG F(ab')2) и связывающий человеческий FcγRIIB. На Фиг. 4 показано, что сортировка с помощью проточной цитометрии может постепенно обогащать клетки с высокой аффинностью связывания с FcγRIIB. Клетки, полученные посредством сортировки с помощью проточной цитометрии для разных раундов библиотеки человеческого IgG2 LibraryMix соответственно анализируют. Анализ методом проточной цитометрии показывает, что доля клеток, связывающихся с FcγRIIB, увеличивается после каждого раунда. Доля после первого раунда составляет 0,90%, а после второго раунда составляет 22,2%, то есть увеличивается в 2,65 раз и в 65,29 раз соответственно, по сравнению с 0,34% человеческого IgG2 дикого типа.
Как показано на Фиг. 5, после двух раундов сортировки доля FcγRIIB-связывающих клеток из Библиотеки1, Библиотеки2, Библиотеки3, Библиотеки4 и БиблиотекиMix, определенная посредством проточной цитометрии, увеличивается до 1,85%, 16,3%, 0,57%, 2,19% и 22,2% соответственно, то есть в 5,44 раз, 47,94 раза, 1,69 раз, 6.44 раз и 65,29 раз выше, чем 0,34% человеческого IgG2 дикого типа.
Пример 3: NGS-анализ типов мутаций IgG2 Fc с повышенной аффинностью связывания с FcγRIIB после сортировки с помощью проточной цитометрии.
Выбирают мутации с соотношением доли последовательности после сортировки к доле до сортировки, увеличенной более чем в два раза по сравнению с человеческим IgG2 дикого типа (фактор обогащения/ фактор обогащения дикого типа >2), то есть мутации человеческого IgG2, которые благоприятны для улучшения аффинности связывания IgG2 с FcγRIIB (по меньшей мере вдвое больше, чем фактор обогащения дикого типа), см. Таблица 7. Например, доля L328W до сортировки составляет 0,39%, а доля после сортировки составляет 12,84%, следовательно, фактор обогащения составляет 33,20, то есть в 22,21 раза больше, чем фактор обогащения дикого типа (1,49).
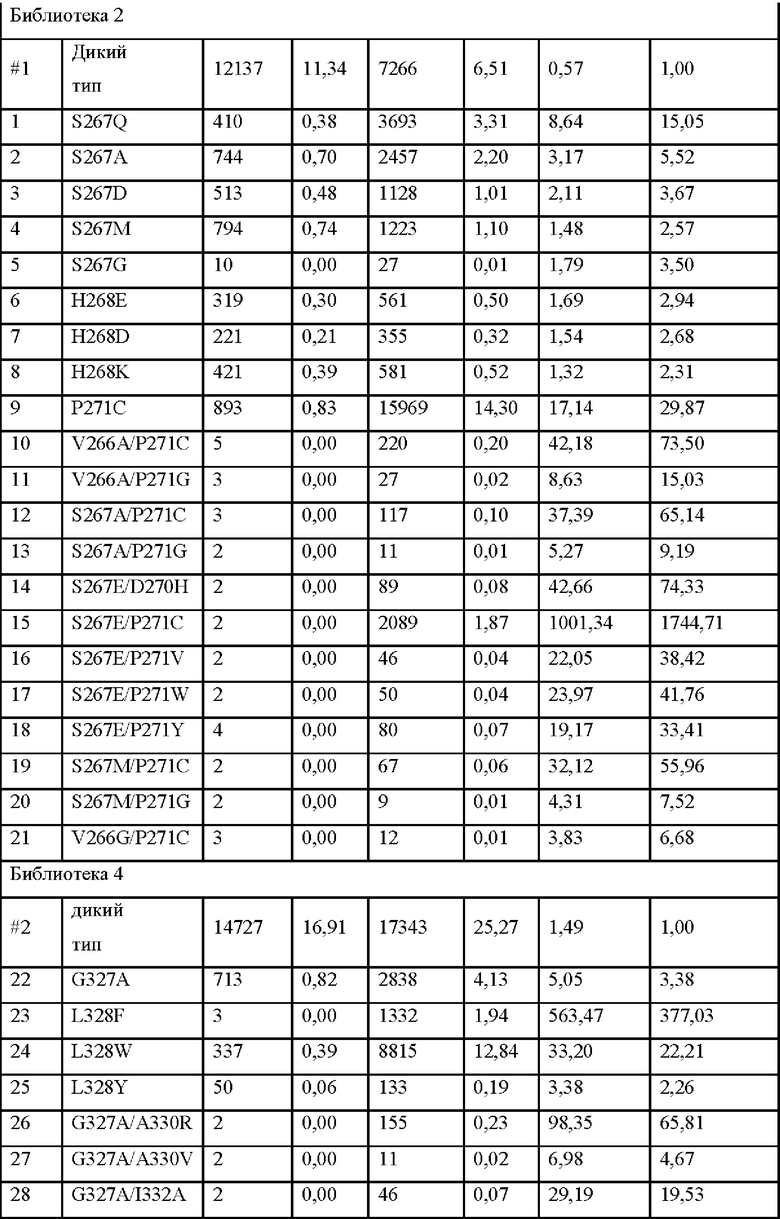
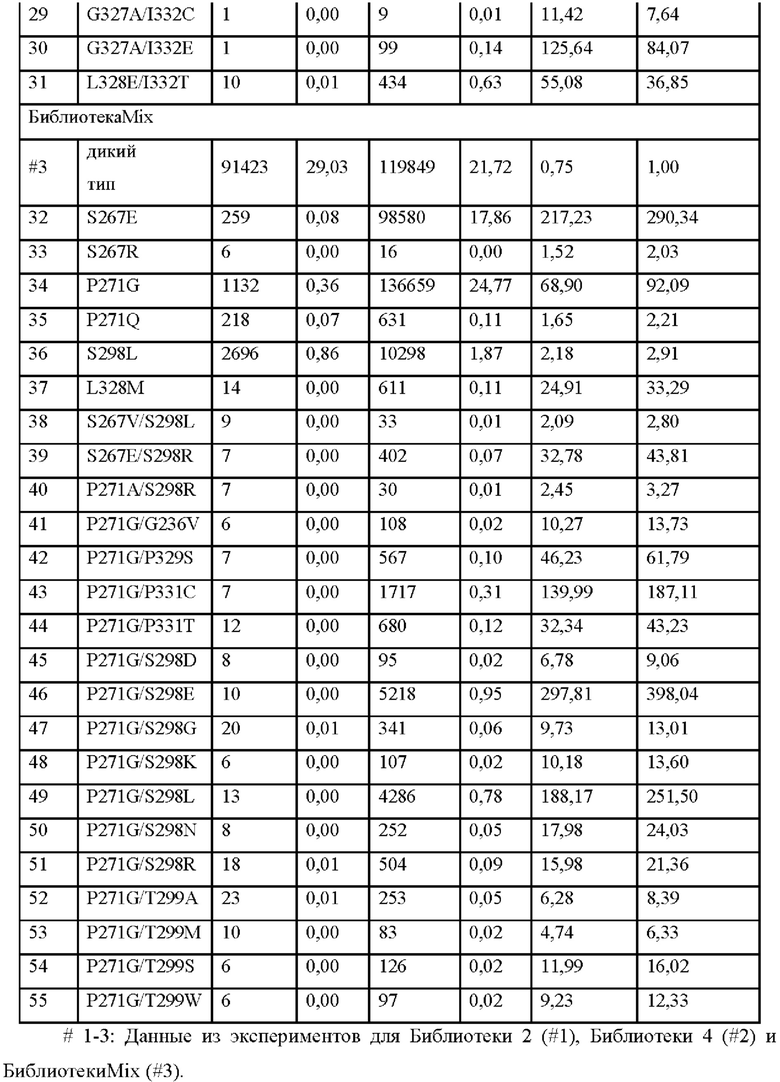
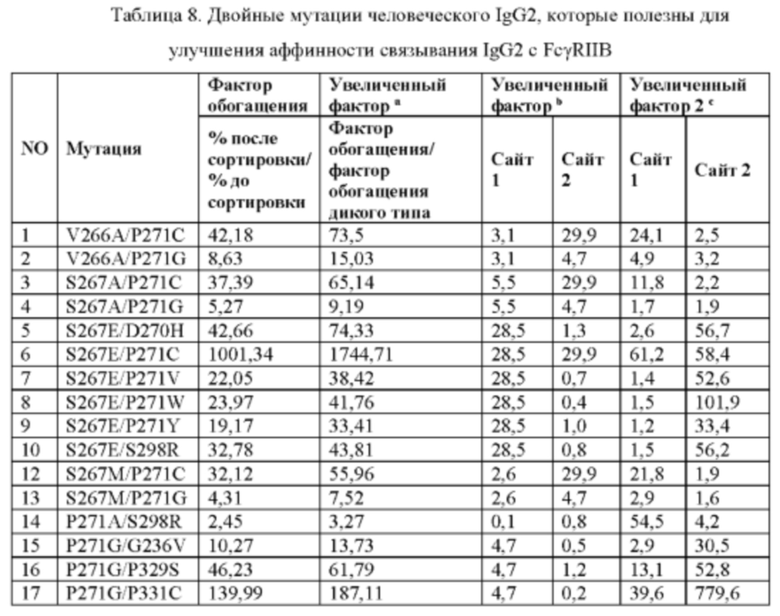
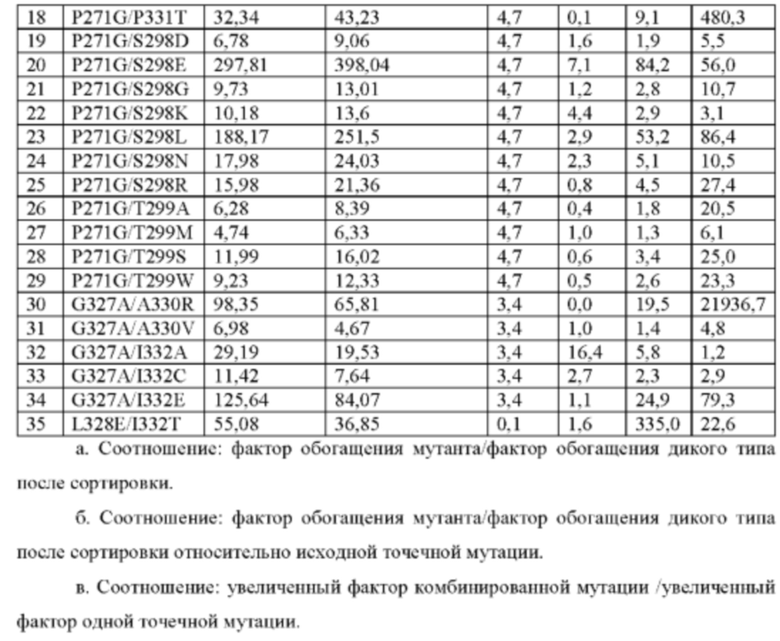
В дополнение к одноточечной мутации также были получены некоторые двойные мутации, при этом соотношения этих аминокислотных мутаций после сортировки с помощью проточной цитометрии к аминокислотным мутациям до сортировки увеличивалось более чем в два раза по сравнению с человеческим IgG2 дикого типа. Комбинация двойной мутации (V266A/P271C или G, S267A/P271C или G, S267E/D270H, S267E/P271C или V или W или Y, S267E/S298R, S267M/P271C или G, P271A/S298R, P271G/G236V, P271G/G329S, P271G/P331C или Т, P271G/S298D или E или G или K или L или N или R, P271G/T299A или M или S или W, G327A/A330R или V, G327A/I332A или С или Е, L328E/I332T, и т.д.) имеет большее увеличение фактора (соотношения), чем его любая точечная мутация, указывая, что обе аминокислоты в комбинации мутации вносят вклад в увеличение аффинности связывания с FcγRIIB. Кроме того, комбинации мутаций, таких как S267V/S298L обеспечивают увеличение фактора, приблизительно равное мутации S298L, которая имеет более высокий фактор, чем S267V, указывая на то, что улучшение комбинации мутаций в основном обязано вкладу S298L, а не другой точечной мутации, как показано в Таблице 8. Следовательно, в дополнении к аминокислотной мутации, предложенной в настоящем изобретении, Fc-область, антитело, Fc-фрагмент или слитый белок по настоящему изобретению могут дополнительно включать другие возможные комбинации или модификации.
Пример 4: Анализ подходящих типов мутантов посредством NGS после магнитно-активированной сортировки клеток
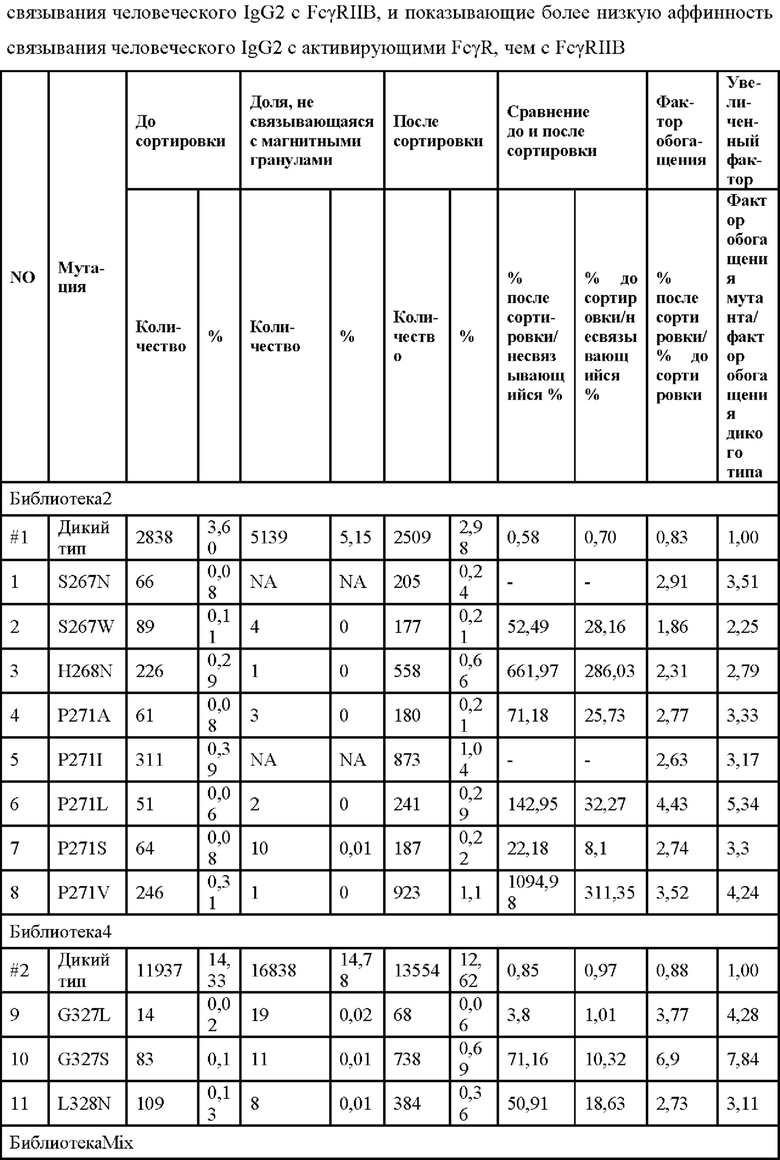
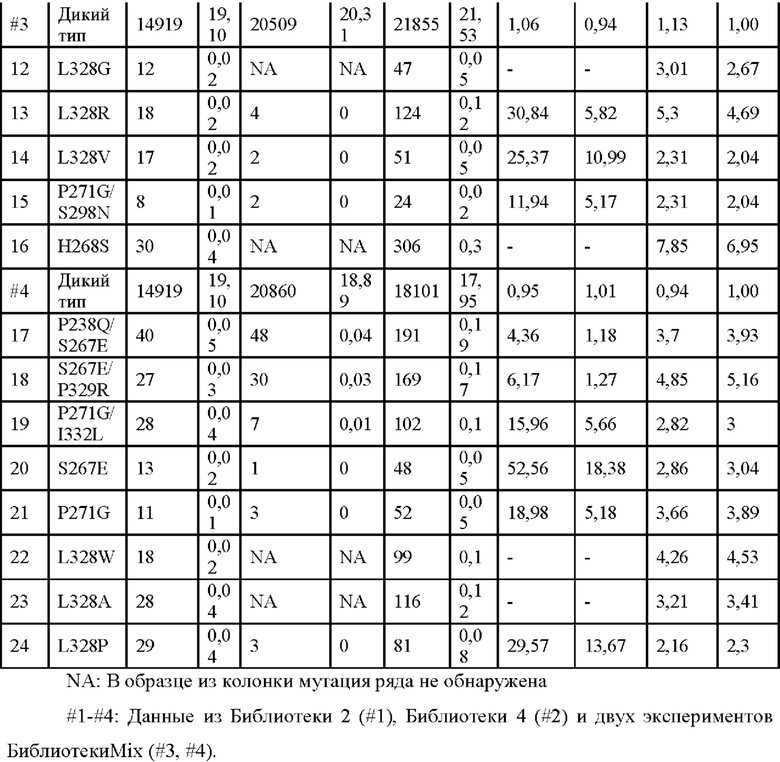
Клетки с высокой аффинностью к FcγRIIB, полученные в результате вышеуказанной сортировки с помощью проточной цитометрии, затем сортировали посредством магнитно-активированной сортировки. Клетки инкубировали со смесью биотин-меченого FcγRIIB и немеченого активирующего FcγR, и затем меченые клетки сортировали с помощью антибиотиновых магнитных гранул. Коэффициенты обогащения после сортировки относительно этой величины до сортировки анализируют посредством NGS. Мутации с более высоким соотношением I/A могут быть отобраны, как показано в Таблице 9. Мутации отбирают в соответствии со следующим критерием: отношение мутаций после сортировки к мутациям до сортировки увеличивается более чем в два раза по сравнению с человеческим IgG2 дикого типа, и доля мутаций уменьшается в той части сортировки, которая не связана с магнитными гранулами (то есть вытекшая жидкость, прошедшая через LS колонку).
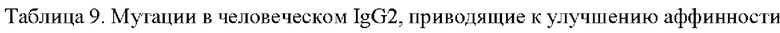
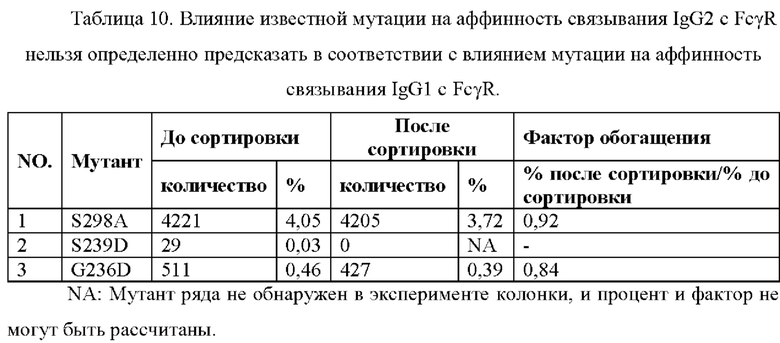
Аффинность человеческого IgG1 к FcγRIIB может быть увеличена с помощью мутации G236D, S239D (Seung Y Chu et al. Molecular Immunology 45 (2008) 3926-3933) и S298A (US 20090042291 A1). Однако в результатах NGS-анализа по настоящему изобретению, доля варианта IgG2, содержащего G236D или S298A, после сортировки не увеличивается, а уменьшается (Таблица 10); доля варианта человеческого IgG2, содержащего S239D до сортировки составляет 0,026% и не обнаруживается после сортировки. Эти результаты показывают, что мутации G236D, S239D и S298A не увеличивают аффинность связывания человеческого IgG2 с FcγRIIB, см. Таблица 10.
Пример 5: Аминокислотные мутации в полипептидных Fc-фрагментах человеческого IgG2, которые могут повышать аффинность к FcγRIIB.
В таблице 11 обобщены аминокислотные мутации, способные усилить аффинность к FcγRIIB, отобранные методом скрининга библиотеки точечных мутаций в соответствии с настоящим изобретением. По сравнению с патентами из предшествующего уровня техники, было обнаружено, что сайты S267G и Р271С по настоящему изобретению оба представляют собой новые типы мутаций в человеческом IgG2, которые могут улучшать аффинность связывания с FcγRIIB. Сайты H268S, L328A и G327A все представляют собой новые типы мутаций в человеческом IgG2, которые улучшают аффинность связывания с FcγRIIB и показывают более низкую аффинность с другим активирующим FcγR, чем с FcγRIIB.

Пример 6: Создание библиотеки комбинированных мутаций человеческого антитела IgG2_Fc
В соответствии с типом Fc-мутации, способным увеличивать аффинность к FcγRIIB (мутация, имеющая фактор обогащения, превышающий более чем в 1 раз дикий тип), отобранной с помощью вышеприведенных библиотек точечных мутаций и результатов высокопроизводительного секвенирования, были разработаны два типа библиотек комбинированных мутаций. Тип I: комбинированные точечные мутации в четырех областях, то есть областях P233-V240, V266-P271, S298-T299 и G327-I332, каждая их которых имеет 0-1 мутацию, и комбинированная мутация содержит 0-4 точечных мутаций. Тип II: комбинированная мутация множественных аминокислот в одной области, то есть области P233-V240, V266-P271, S298-T299 или G327-I332 имеют комбинированные мутации внутри каждой области (соответственно 0-7, 0-6, 0-2 и 0-6 комбинированных мутаций), как показано на Фиг. 6. Размер плазмидной библиотеки составляет 4,67*105.
Пример 7: Обогащение клеток до и после сортировки с помощью проточной цитометрии для библиотеки комбинированных мутаций
В соответствии со скринингом точечных мутаций и результатами высокопроизводительного секвенирования создают библиотеки I и II типа комбинированных мутаций (Пример 6) и библиотеки клеток, экспрессирующих комбинированные мутации. Затем используют проточную цитометрию для сортировки клеток с высокой аффинностью к FcγRIIB за два-три раунда. Как показано на Фиг. 7, после двух раундов сортировки доля клеток библиотеки IgG2_C01 и библиотеки IgG2_C02, определенная посредством проточной цитометрии, которые способны связываться с FcγRIIB, увеличивалась до 9,53% и 26,9% соответственно, что в 41,43 раз и 116,96 раз выше, чем 0,23% человеческого IgG2 дикого типа. IgG2_С01 представляет собой библиотеку комбинированных мутаций (тип I), имеющих не более 1 мутации в каждой из четырех областей P233-V240, V266-P271, S298-T299 и G327-I332; IgG2_C02 представляет собой клеточную библиотеку, полученную посредством комбинирования библиотек комбинированных мутаций (тип II) четырех областей P233-V240, V266-P271, S298-T299 и G327-I332 вместе и перенесения ее в клетки 3Т3.
Как показано на Фиг. 8, после двух раундов сортировки, аффинность связывания клеток из библиотеки Cmix и библиотеки С2 с FcγRIIB значительно увеличивалась, согласно проточной цитометрии. Доля клеток библиотек, которые способны связываться с FcγRIIB, увеличивается после каждого раунда сортировки: Cmix показывает долю клеток, составляющую 1,86% и 28,9%, которые способны связываться с FcγRIIB после первого раунда сортировки и второго раунда сортировки соответственно, что в 246,03 раз и 3822,75 раз выше, чем 0,00756% до сортировки; С2 достигает 6,46% и 28,9%, что в 718,58 раз и 3214,68 раз выше, чем 0,00899% до сортировки. Библиотека Cmix представляет собой библиотеку комбинированных мутаций (тип I) с не более чем одной мутацией в каждой из четырех областей; и библиотека С2 представляет собой библиотеку комбинированных мутаций (тип II) области V266-P271.
Пример 8: NGS-анализ комбинированной мутации IgG2 Fc, показывающий повышение аффинности связывания с FcγRIIB после сортировки с помощью проточной цитометрии.
Для того чтобы подвергнуть скринингу тип IgG2 Fc комбинированной мутации с повышенной аффинностью связывания с FcγRIIB, созданную в настоящем изобретении библиотека комбинированных мутаций, подвергали сортировке с помощью проточной цитометрии для получения клеток с более высокой аффинностью связывания с FcγRIIB, затем с помощью NGS анализируют фактор обогащения для каждого типа мутации после сортировки по сравнению с этим параметром до сортировки. Результат показан в Таблице 12. Мутация, подвергнутая скринингу, имеет более высокий фактор обогащения (после последнего раунда сортировки/до сортировки), или показывает значительное обогащение по меньшей мере в одном раунде сортировки (после указанного раунда сортировки/до указанного раунда сортировки), или обнаруживается только после последнего раунда сортировки. Например, фактор обогащения V266L/S298L/L328W в 21920,33 раз выше, чем у дикого типа (после последнего раунда сортировки/до сортировки); фактор обогащения точечной мутации L328W в 8,78 раз выше, чем у дикого типа (после последнего раунда сортировки/до сортировки); факторы обогащения H268D/S298L/L328W составляют 43,98 (после второго раунда сортировки/до второго раунда сортировки) и 5,95 (после третьего раунда сортировки/до третьего раунда сортировки); фактор обогащения V234M/S267E/S298L/L328W составляет 5,13 (после третьего раунда сортировки/до третьего раунда сортировки); V234Q/A235G/P238L/S239V/G327A/L328E/A330S/I332T определяется только после последнего раунда сортировки.

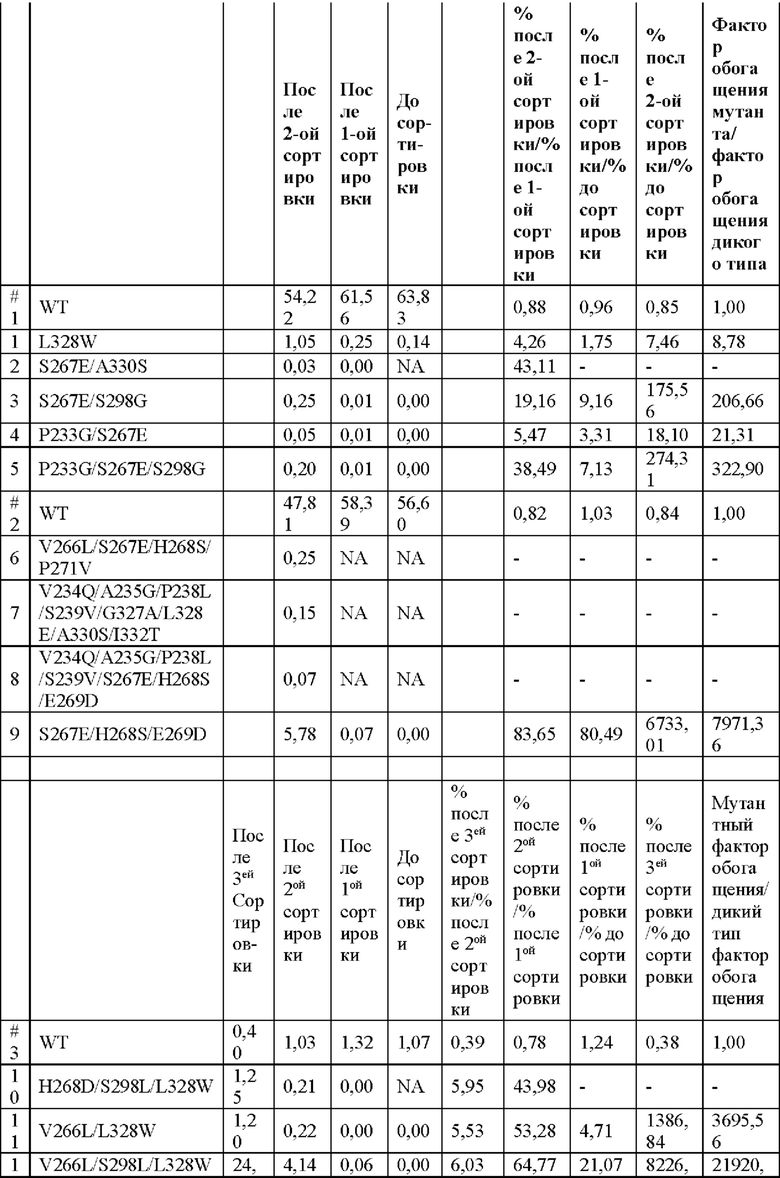
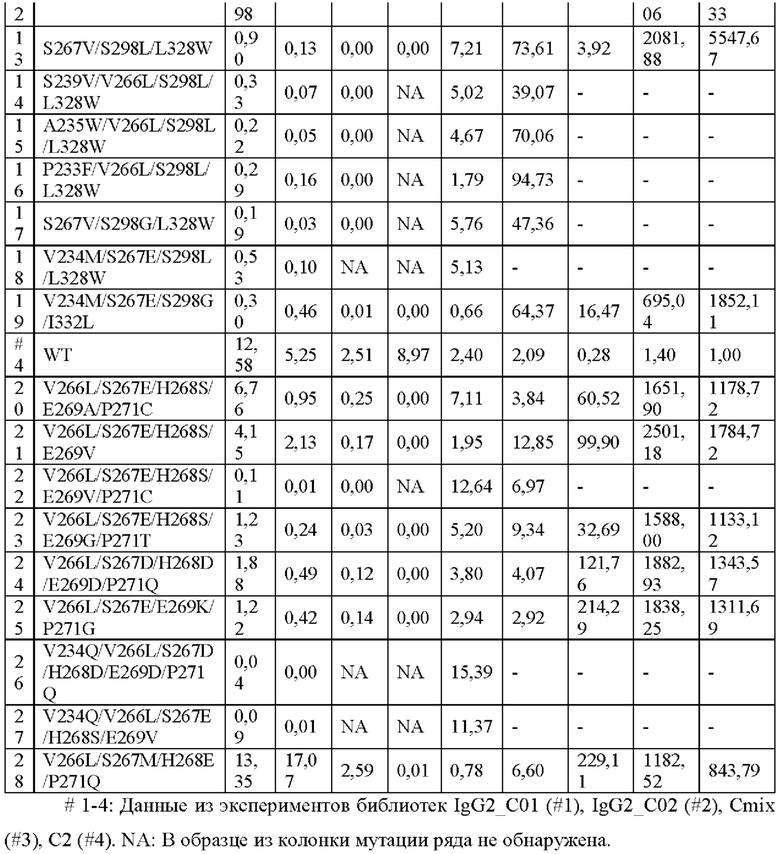
Пример 9: Свойство связывания мутантных антител с FcγR, анализируемые с помощью ферментного иммуносорбентного анализа (ELISA)
На основе предпочтительной Fc одноточечной мутации и комбинированной мутации, отобранной выше с помощью NGS, были созданы новые комбинации Fc-мутаций. Антитела против человеческого ОХ40, содержащие эти новые комбинации Fc-мутаций, экспрессируют и анализируют свойство связывания мутантного антитела с FcγR с помощью ферментного иммуносорбентного анализа (ELISA). На Фиг. 9-14 показана аффинность связывания разных Fc-мутантов с FcγRI, FcγRIIA131H, FcγRIIA131R, FcγRIIB, FcγRIIIA158F и FcγRIIIA158V. Путем определения аффинности связывания IgG1 с каждым FcγR до 1, рассчитывают относительную аффинность связывания каждого мутанта с FcγR (значение поглощения ELISA для связывания мутанта с FcγR, поделенное на значение поглощения ELISA для связывания IgG1 с FcγR) и увеличенный фактор аффинности связывания каждого мутанта с FcγRIIB по сравнению с IgG2 дикого типа (значение поглощения ELISA для связывания мутанта с FcγRIIB, поделенное на ELISA значение поглощения для IgG2 дикого типа с FcγRIIB). Как показано в Таблице 13, увеличение фактора аффинности связывания каждого мутанта с FcγRIIB по сравнению с IgG2 дикого типа составляет от 4,23 до 25,55 раз. Кроме того, рассчитывают соотношение аффинности связывания каждого мутанта с FcγRIIB к аффинности связывания указанного мутанта с FcγRIIA131R (RIIB/RIIAR) и результаты (Таблица 13) показывают, что соотношение RIIB/RIIAR у этих мутантов выше, чем соотношение у дикого типа IgG2 (дикий тип IgG2: 0,34; мутанты: 0,46-3,67).
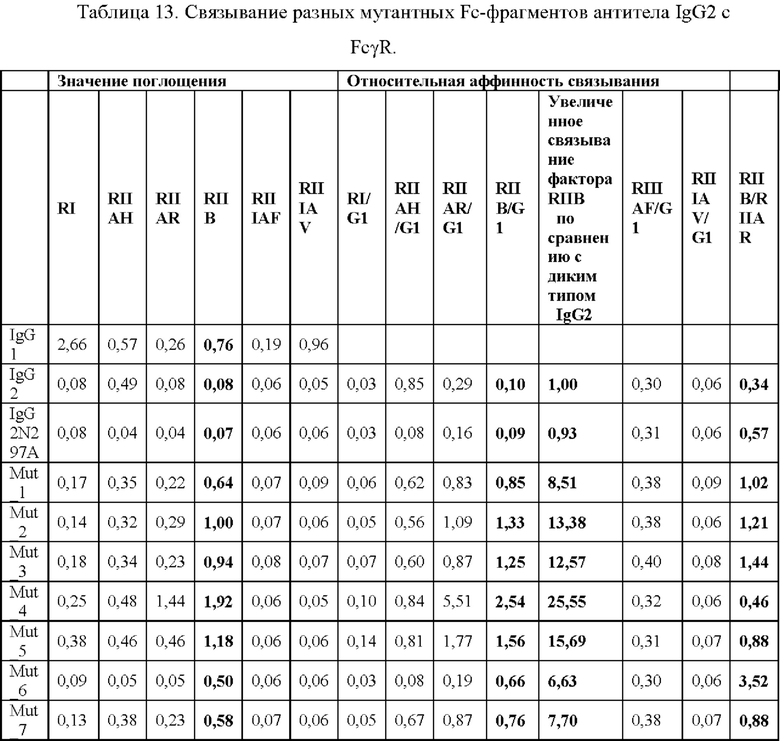
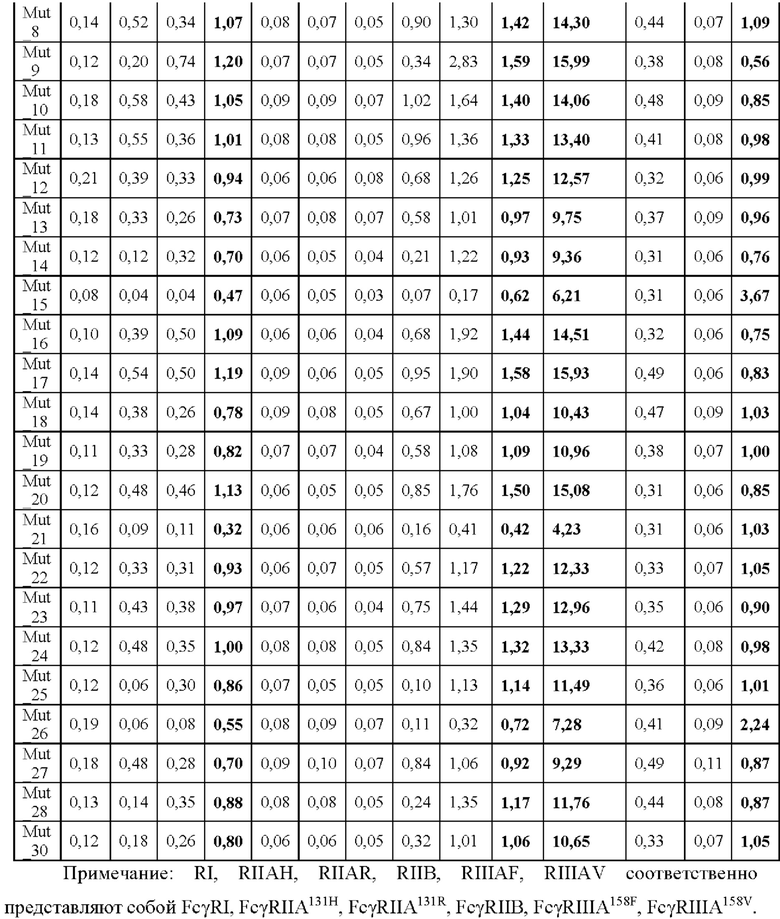
Пример 10: Полезные мутации поддерживают более сильную активность иммуноактивации
Активность иммуноактивации антитела против человеческого ОХ40 (Пример 9), содержащего полезную мутацию, анализируют в гуманизированных мышиных клетках селезенки FCγR/OX40. На Фиг. 16 и 17 показана флуоресцентная интенсивность CFSE и соответствующая гистограмма клеток CD4+, когда концентрация антитела составляет 1 мкг/мл, где низкая флуоресцентная интенсивность CFSE отражает высокую активность, и активность всех выбранных антител лучше, чем активность IgG2 дикого типа. Значения активности разных концентраций антитела в двух экспериментов анализируют вместе. Активность группы только с антителом αCD3 была установлена равной 0, в то время как активность положительной контрольной группы с антителом αCD3 и антителом αCD28 была установлена равной 1. Рассчитывают относительную активность каждого мутантного антитела, а также вычисляют среднее значение. Из таблицы 14 видно, что активность выбранных 30 мутантных антител превосходит активность IgG2 дикого типа, и активность увеличивается от 9,17 до 16,51 раз относительно IgG2 дикого типа.
Пример 11: Влияние известной мутации на способность связывания IgG2 с FcγR не может быть прямо предсказано в соответствии с влиянием этой мутации на способность связывания IgG1 с FcγR.
Аффинность человеческого IgG1 к FcγRIIB может быть увеличена с помощью мутации G236D, S239D (Seung Y Chu et al. Molecular Immunology 45 (2008) 3926-3933) и S298A (US 20090042291 A1). Однако в результате анализа NGS по настоящему изобретению доля варианта IgG2, содержащего G236D или S298A после сортировки, не увеличивается, а уменьшается (Таблица 10); доля варианта человеческого IgG2, содержащего S239D перед сортировкой, составляет 0,026%, и не выявляется после сортировки. Эти результаты демонстрируют, что мутации G236D, S239D и S298A не повышают способность человеческого IgG2 связываться с FcγRIIB, смотрите Таблицу 10.
Кроме того, авторы изобретения также вводили в IgG2 мутации VII (G237D/P238D/H268D/P271G/A330R), способные значительно улучшать аффинность связывания IgG1 с FcγRIIB (F Mimoto et al., Protein Engineering, Design & Selection vol. 26 no. 10 pp.589-598, 2013) с получением IgG2_M2(H268D/P271G), IgG2_M3(H268D/P271G/A330R), IgG2_M4 (G236D/P238D/H268D/P271G) и IgG2_M5(G236D/P238D/H268D/P271G/A330R), где мутации M5 в IgG2 соответствуют мутациям V11 в IgG1. Результаты ELISA на Фиг. 15 показывают, что эти мутанты не обеспечивают IgG2 такой же аффинностью связывания с FcγRIIB, как V11 IgG1.
Следовательно, влияние известной мутации на способность связывания IgG2 с FcγR не может быть прямо предсказано в соответствии с влиянием мутации на способность связывания IgG1 с FcγR.
Каждая ссылка, приведенная в настоящем документе, включена путем ссылки в той же степени, как если бы каждая ссылка была индивидуально включена путем ссылки. Кроме того, следует понимать, что на основе вышеприведенного в описании руководства специалисты в данной области могут осуществлять различные изменения или модификации изобретения и эти эквивалентные формы также подпадают в объем прилагаемой формулы изобретения.
--->
Перечень последовательностей
<110> SHANGHAI JIAO TONG UNIVERSITY SCHOOL OF MEDICINE
<120> Fc-фрагмент антитела, имеющий повышенную аффинность связывания с FcγRIIB
<130> P2020-2571
<150> CN201911223227.1
<151> 2019-12-03
<160> 23
<170> PatentIn version 3.5
<210> 1
<211> 40
<212> DNA
<213> Artificial sequence
<400> 1
ctaggcgccg gaattagatc taccatggag acagacagac 40
<210> 2
<211> 36
<212> DNA
<213> Artificial sequence
<400> 2
gtttgttgcg ccggatccac actctcccct gttgaa 36
<210> 3
<211> 36
<212> DNA
<213> Artificial sequence
<400> 3
ttcaacaggg gagagtgtgg atccggcgca acaaac 36
<210> 4
<211> 36
<212> DNA
<213> Artificial sequence
<400> 4
gctgagcctg atgtccatgg gtccaggatt ctcttc 36
<210> 5
<211> 36
<212> DNA
<213> Artificial sequence
<400> 5
gaagagaatc ctggacccat ggacatcagg ctcagc 36
<210> 6
<211> 36
<212> DNA
<213> Artificial sequence
<400> 6
ggatggagga ggctcgagtt tacccggaga caggga 36
<210> 7
<211> 36
<212> DNA
<213> Artificial sequence
<400> 7
tccctgtctc cgggtaaact cgagcctcct ccatcc 36
<210> 8
<211> 39
<212> DNA
<213> Artificial sequence
<400> 8
ttcgttaacc tcgagagatc ttcacgctag agaatgagg 39
<210> 9
<211> 699
<212> DNA
<213> Artificial sequence
<400> 9
atggagacag acagactcct gctatgggtg ctgctgctct gggtgccagg ctccactggt 60
gacactgtac tgacccagtc tcctgctttg gctgtgtctc caggagagag ggttaccatc 120
tcctgtaggg ccagtgacag tgtcagtaca cttatgcact ggtaccaaca gaaaccagga 180
cagcaaccca aactcctcat ctatctagca tcacacctag aatctggggt ccctgccagg 240
ttcagtggca gtgggtctgg gacagacttc accctcacca ttgatcctgt ggaggctgat 300
gacactgcaa cctattactg tcagcagagt tggaatgatc cgtggacgtt cggtggaggc 360
accaagctgg aattgaaacg aactgtggct gcaccatctg tcttcatctt cccgccatct 420
gatgagcagt tgaaatctgg aactgcctct gttgtgtgcc tgctgaataa cttctatccc 480
agagaggcca aagtacagtg gaaggtggat aacgccctcc aatcgggtaa ctcccaggag 540
agtgtcacag agcaggacag caaggacagc acctacagcc tcagcagcac cctgacgctg 600
agcaaagcag actacgagaa acacaaagtc tacgcctgcg aagtcaccca tcagggcctg 660
agctcgcccg tcacaaagag cttcaacagg ggagagtgt 699
<210> 10
<211> 66
<212> DNA
<213> Artificial sequence
<400> 10
ggatccggcg caacaaactt ctctctgctg aaacaagccg gagatgtcga agagaatcct 60
ggaccc 66
<210> 11
<211> 1383
<212> DNA
<213> Artificial sequence
<400> 11
atggacatca ggctcagctt ggttttcctt gtccttttca taaaaggtgt ccagtgtgag 60
gtgcagctgg tggagtctga tggaggctta gtgcagcctg gaaggtccct aaaactcccc 120
tgtgcagcct caggattcac tttcagtgac tattacatgg cctgggtccg ccaggctcca 180
acgaaggggc tggagtgggt cgcaagcatt agttatgatg gtagtagcac ttactatcga 240
gactccgtga agggccgatt cactatctcc agagataatg caaaaagcac cctatacctg 300
caaatggaca gtctgaggtc tgaggacacg gccacttatt actgcggaag acacagtagc 360
tactttgatt actggggcca aggagtcatg gtcacagtct cgagcgcctc caccaagggc 420
ccatcggtct tccccctggc gccctgctcc aggagcacct ccgagagcac agcggccctg 480
ggctgcctgg tcaaggacta cttccccgaa ccggtgacgg tgtcgtggaa ctcaggcgct 540
ctgaccagcg gcgtgcacac cttcccagct gtcctacagt cctcaggact ctactccctc 600
agcagcgtgg tgaccgtgcc ctccagcaac ttcggcaccc agacctacac ctgcaacgta 660
gatcacaagc ccagcaacac caaggtggac aagacagttg agcgcaaatg ttgtgtcgag 720
tgcccaccgt gcccagcacc acctgtggca ggaccgtcag tcttcctctt ccccccaaaa 780
cccaaggaca ccctcatgat ctcccggacc cctgaggtca cgtgcgtggt ggtggacgtg 840
agccacgaag accccgaggt ccagttcaac tggtacgtgg acggcgtgga ggtgcataat 900
gccaagacaa agccacggga ggagcagttc aacagcacgt tccgtgtggt cagcgtcctc 960
accgttgtgc accaggactg gctgaacggc aaggagtaca agtgcaaggt ctccaacaaa 1020
ggcctcccag cccccatcga gaaaaccatc tccaaaacca aagggcagcc ccgagaacca 1080
caggtgtaca ccctgccccc atcccgggag gagatgacca agaaccaggt cagcctgacc 1140
tgcctggtca aaggcttcta ccccagcgac atcgccgtgg agtgggagag caatgggcag 1200
ccggagaaca actacaagac cacacctccc atgctggact ccgacggctc cttcttcctc 1260
tacagcaagc tcaccgtgga caagagcagg tggcagcagg ggaacgtctt ctcatgctcc 1320
gtgatgcatg aggctctgca caaccactac acgcagaaga gcctctccct gtctccgggt 1380
aaa 1383
<210> 12
<211> 228
<212> DNA
<213> Artificial sequence
<400> 12
ctcgagcctc ctccatccac tgtctccaac atggcgaccg ttgctgttct ggttgtcctt 60
ggagctgcaa tagtcactgg agctgtggtg gcttttgtga tgaagatgag aaggagaaac 120
acaggtggaa aaggagggga ctatgctctg gctccaggct cccagacctc tgatctgtct 180
ctcccagatt gtaaagtgat ggttcatgac cctcattctc tagcgtga 228
<210> 13
<211> 791
<212> PRT
<213> Artificial sequence
<400> 13
Met Glu Thr Asp Arg Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Thr Val Leu Thr Gln Ser Pro Ala Leu Ala Val
20 25 30
Ser Pro Gly Glu Arg Val Thr Ile Ser Cys Arg Ala Ser Asp Ser Val
35 40 45
Ser Thr Leu Met His Trp Tyr Gln Gln Lys Pro Gly Gln Gln Pro Lys
50 55 60
Leu Leu Ile Tyr Leu Ala Ser His Leu Glu Ser Gly Val Pro Ala Arg
65 70 75 80
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asp Pro
85 90 95
Val Glu Ala Asp Asp Thr Ala Thr Tyr Tyr Cys Gln Gln Ser Trp Asn
100 105 110
Asp Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Leu Lys Arg Thr
115 120 125
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
130 135 140
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
145 150 155 160
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
165 170 175
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
180 185 190
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
195 200 205
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
210 215 220
Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Ser Gly Ala Thr Asn Phe
225 230 235 240
Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met
245 250 255
Asp Ile Arg Leu Ser Leu Val Phe Leu Val Leu Phe Ile Lys Gly Val
260 265 270
Gln Cys Glu Val Gln Leu Val Glu Ser Asp Gly Gly Leu Val Gln Pro
275 280 285
Gly Arg Ser Leu Lys Leu Pro Cys Ala Ala Ser Gly Phe Thr Phe Ser
290 295 300
Asp Tyr Tyr Met Ala Trp Val Arg Gln Ala Pro Thr Lys Gly Leu Glu
305 310 315 320
Trp Val Ala Ser Ile Ser Tyr Asp Gly Ser Ser Thr Tyr Tyr Arg Asp
325 330 335
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Ser Thr
340 345 350
Leu Tyr Leu Gln Met Asp Ser Leu Arg Ser Glu Asp Thr Ala Thr Tyr
355 360 365
Tyr Cys Gly Arg His Ser Ser Tyr Phe Asp Tyr Trp Gly Gln Gly Val
370 375 380
Met Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro
385 390 395 400
Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly
405 410 415
Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn
420 425 430
Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln
435 440 445
Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser
450 455 460
Asn Phe Gly Thr Gln Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser
465 470 475 480
Asn Thr Lys Val Asp Lys Thr Val Glu Arg Lys Cys Cys Val Glu Cys
485 490 495
Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe
500 505 510
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
515 520 525
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe
530 535 540
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
545 550 555 560
Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr
565 570 575
Val Val His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
580 585 590
Ser Asn Lys Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr
595 600 605
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg
610 615 620
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
625 630 635 640
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
645 650 655
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser
660 665 670
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
675 680 685
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
690 695 700
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Leu Glu Pro Pro
705 710 715 720
Pro Ser Thr Val Ser Asn Met Ala Thr Val Ala Val Leu Val Val Leu
725 730 735
Gly Ala Ala Ile Val Thr Gly Ala Val Val Ala Phe Val Met Lys Met
740 745 750
Arg Arg Arg Asn Thr Gly Gly Lys Gly Gly Asp Tyr Ala Leu Ala Pro
755 760 765
Gly Ser Gln Thr Ser Asp Leu Ser Leu Pro Asp Cys Lys Val Met Val
770 775 780
His Asp Pro His Ser Leu Ala
785 790
<210> 14
<211> 216
<212> PRT
<213> Artificial sequence
<400> 14
Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
1 5 10 15
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
20 25 30
Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val
35 40 45
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
50 55 60
Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln
65 70 75 80
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly
85 90 95
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro
100 105 110
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
115 120 125
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
130 135 140
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
145 150 155 160
Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
165 170 175
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
180 185 190
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
195 200 205
Ser Leu Ser Leu Ser Pro Gly Lys
210 215
<210> 15
<211> 109
<212> PRT
<213> Artificial sequence
<400> 15
Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
1 5 10 15
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
20 25 30
Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val
35 40 45
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
50 55 60
Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln
65 70 75 80
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly
85 90 95
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys
100 105
<210> 16
<211> 708
<212> DNA
<213> Artificial sequence
<400> 16
atggaaaccc cagcgcagct tctcttcctc ctgctactct ggctcccaga taccaccgga 60
gaaattgtgt tgacgcagtc tccaggcacc ctgtctttgt ctccagggga aagagccacc 120
ctctcctgca gggccagtca gagtgttagc ggcgactact tagcctggta ccagcagaaa 180
cttggccagg ctcccaggct cctcatctat ggtgcatcca tcagggccac tggcatccca 240
gacaggttca gtggcagtgg gtctgggaca gacttcactc tcaccatcag caaactggag 300
cctgaagatt ttgcagtgta ttactgtcag cagtatggta gctcaccgct cactttcggc 360
ggagggacca aggtggagat caaacgaact gtggctgcac catctgtctt catcttcccg 420
ccatctgatg agcagttgaa atctggaact gcctctgttg tgtgcctgct gaataacttc 480
tatcccagag aggccaaagt acagtggaag gtggataacg ccctccaatc gggtaactcc 540
caggagagtg tcacagagca ggacagcaag gacagcacct acagcctcag cagcaccctg 600
acgctgagca aagcagacta cgagaaacac aaagtctacg cctgcgaagt cacccatcag 660
ggcctgagct cgcccgtcac aaagagcttc aacaggggag agtgttga 708
<210> 17
<211> 1392
<212> DNA
<213> Artificial sequence
<400> 17
atgaaacacc tgtggttctt cctcctcctg gtggcagctc ccagatgggt cctgtctcag 60
gtgcagctgc aggagtcggg cccaggactg gtgaagcctt cggggaccct gtcactcacc 120
tgcgctgtct ctggtggctc catcagcagt agtatctggt ggagctgggt ccgccagccc 180
ccagggaagg ggctggaatg gattggggaa atccatcata gtgggaacac caactgcaat 240
ccgtccctca agagtcgagt caccatatca atagacaagt ccaagaacca gttctccctg 300
aaactgacct ctgtgaccgc cgcggacacg gccgtatatt attgtgcgag agcgggaact 360
ggaactacgc ttgactactg gggccaggga accctggtca ccgtctcgag cgcctccacc 420
aagggcccat cggtcttccc cctggcgccc tgctccagga gcacctccga gagcacagcg 480
gccctgggct gcctggtcaa ggactacttc cccgaaccgg tgacggtgtc gtggaactca 540
ggcgctctga ccagcggcgt gcacaccttc ccagctgtcc tacagtcctc aggactctac 600
tccctcagca gcgtggtgac cgtgccctcc agcaacttcg gcacccagac ctacacctgc 660
aacgtagatc acaagcccag caacaccaag gtggacaaga cagttgagcg caaatgttgt 720
gtcgagtgcc caccgtgccc agcaccacct gtggcaggac cgtcagtctt cctcttcccc 780
ccaaaaccca aggacaccct catgatctcc cggacccctg aggtcacgtg cgtggtggtg 840
gacgtgagcc acgaagaccc cgaggtccag ttcaactggt acgtggacgg cgtggaggtg 900
cataatgcca agacaaagcc acgggaggag cagttcaaca gcacgttccg tgtggtcagc 960
gtcctcaccg ttgtgcacca ggactggctg aacggcaagg agtacaagtg caaggtctcc 1020
aacaaaggcc tcccagcccc catcgagaaa accatctcca aaaccaaagg gcagccccga 1080
gaaccacagg tgtacaccct gcccccatcc cgggaggaga tgaccaagaa ccaggtcagc 1140
ctgacctgcc tggtcaaagg cttctacccc agcgacatcg ccgtggagtg ggagagcaat 1200
gggcagccgg agaacaacta caagaccaca cctcccatgc tggactccga cggctccttc 1260
ttcctctaca gcaagctcac cgtggacaag agcaggtggc agcaggggaa cgtcttctca 1320
tgctccgtga tgcatgaggc tctgcacaac cactacacgc agaagagcct ctccctgtct 1380
ccgggtaaat ga 1392
<210> 18
<211> 235
<212> PRT
<213> Artificial sequence
<400> 18
Met Glu Thr Pro Ala Gln Leu Leu Phe Leu Leu Leu Leu Trp Leu Pro
1 5 10 15
Asp Thr Thr Gly Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser
20 25 30
Leu Ser Pro Gly Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser
35 40 45
Val Ser Gly Asp Tyr Leu Ala Trp Tyr Gln Gln Lys Leu Gly Gln Ala
50 55 60
Pro Arg Leu Leu Ile Tyr Gly Ala Ser Ile Arg Ala Thr Gly Ile Pro
65 70 75 80
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Lys Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr
100 105 110
Gly Ser Ser Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
130 135 140
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
145 150 155 160
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
165 170 175
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
180 185 190
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
195 200 205
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
210 215 220
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
225 230 235
<210> 19
<211> 463
<212> PRT
<213> Artificial sequence
<400> 19
Met Lys His Leu Trp Phe Phe Leu Leu Leu Val Ala Ala Pro Arg Trp
1 5 10 15
Val Leu Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys
20 25 30
Pro Ser Gly Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Gly Ser Ile
35 40 45
Ser Ser Ser Ile Trp Trp Ser Trp Val Arg Gln Pro Pro Gly Lys Gly
50 55 60
Leu Glu Trp Ile Gly Glu Ile His His Ser Gly Asn Thr Asn Cys Asn
65 70 75 80
Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Ile Asp Lys Ser Lys Asn
85 90 95
Gln Phe Ser Leu Lys Leu Thr Ser Val Thr Ala Ala Asp Thr Ala Val
100 105 110
Tyr Tyr Cys Ala Arg Ala Gly Thr Gly Thr Thr Leu Asp Tyr Trp Gly
115 120 125
Gln Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
130 135 140
Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala
145 150 155 160
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
165 170 175
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
180 185 190
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
195 200 205
Pro Ser Ser Asn Phe Gly Thr Gln Thr Tyr Thr Cys Asn Val Asp His
210 215 220
Lys Pro Ser Asn Thr Lys Val Asp Lys Thr Val Glu Arg Lys Cys Cys
225 230 235 240
Val Glu Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val
245 250 255
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
260 265 270
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
275 280 285
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
290 295 300
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg Val Val Ser
305 310 315 320
Val Leu Thr Val Val His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
325 330 335
Cys Lys Val Ser Asn Lys Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile
340 345 350
Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
355 360 365
Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
370 375 380
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
385 390 395 400
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser
405 410 415
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
420 425 430
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
435 440 445
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
450 455 460
<210> 20
<211> 99
<212> PRT
<213> Artificial sequence
<400> 20
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
1 5 10 15
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
20 25 30
Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
35 40 45
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
50 55 60
Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp
65 70 75 80
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
85 90 95
Ala Pro Ile
<210> 21
<211> 39
<212> DNA
<213> Artificial sequence
<220>
<221> misc_feature
<222> (19)..(20)
<223> n представляет собой a, c, g или t
<400> 21
ccaccgtgcc cagcaccann sgtggcagga ccgtcagtc 39
<210> 22
<211> 44
<212> DNA
<213> Artificial sequence
<400> 22
tgcaaggtct ccaacaaagg ctggccagcc cccatcgaga aaac 44
<210> 23
<211> 54
<212> DNA
<213> Artificial sequence
<220>
<221> misc_feature
<222> (20)..(20)
<223> n представляет собой a, c, g или t
<400> 23
acgtgcgtgg tggtggackn gwbgvasrws sacchggagg tccagttcaa ctgg 54
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ГИБРИДНЫЕ БЕЛКИ ФРАГМЕНТОВ БЕЛКОВ ЧЕЛОВЕКА ДЛЯ СОЗДАНИЯ УПОРЯДОЧЕННО МУЛЬТИМЕРИЗОВАННЫХ КОМПОЗИЦИЙ ОБЛАСТЕЙ FC ИММУНОГЛОБУЛИНОВ С УСИЛЕННЫМ СВЯЗЫВАНИЕМ С СИСТЕМОЙ КОМПЛЕМЕНТА | 2016 |
|
RU2737378C2 |
| ГИБРИДНЫЕ БЕЛКИ ФРАГМЕНТОВ БЕЛКОВ ЧЕЛОВЕКА ДЛЯ СОЗДАНИЯ УПОРЯДОЧЕННО МУЛЬТИМЕРИЗОВАННЫХ КОМПОЗИЦИЙ ОБЛАСТЕЙ FC ИММУНОГЛОБУЛИНОВ С УСИЛЕННЫМ СВЯЗЫВАНИЕМ С СИСТЕМОЙ КОМПЛЕМЕНТА | 2016 |
|
RU2837284C2 |
| ГИБРИДНЫЕ БЕЛКИ ВАРИАНТА sPD-1—FC | 2019 |
|
RU2785993C2 |
| МУТАНТНЫЕ ВАРИАНТЫ Fc IgG1, ЛИШЕННЫЕ ЭФФЕКТОРНЫХ ФУНКЦИЙ | 2018 |
|
RU2764559C2 |
| АНТИ-PCSK9 АНТИТЕЛО, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2016 |
|
RU2739208C2 |
| СКОНСТРУИРОВАННЫЕ МУЛЬТИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА И ДРУГИЕ МУЛЬТИМЕРНЫЕ БЕЛКИ С АСИММЕТРИЧНЫМИ МУТАЦИЯМИ В ОБЛАСТИ CH2-CH3 | 2018 |
|
RU2804031C2 |
| Терапевтические антитела к CD47 | 2016 |
|
RU2748401C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВАРИАНТОВ FcyRIIB-СПЕЦИФИЧЕСКОЙ Fc-ОБЛАСТИ | 2013 |
|
RU2820161C1 |
| ВАРИАНТЫ FcγRIIB-СПЕЦИФИЧЕСКОЙ Fc-ОБЛАСТИ | 2013 |
|
RU2729831C2 |
| СПОСОБЫ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ, ВКЛЮЧАЮЩИЕ СРЕДСТВА, БЛОКИРУЮЩИЕ CTLA-4 И PD-1 | 2020 |
|
RU2833523C2 |
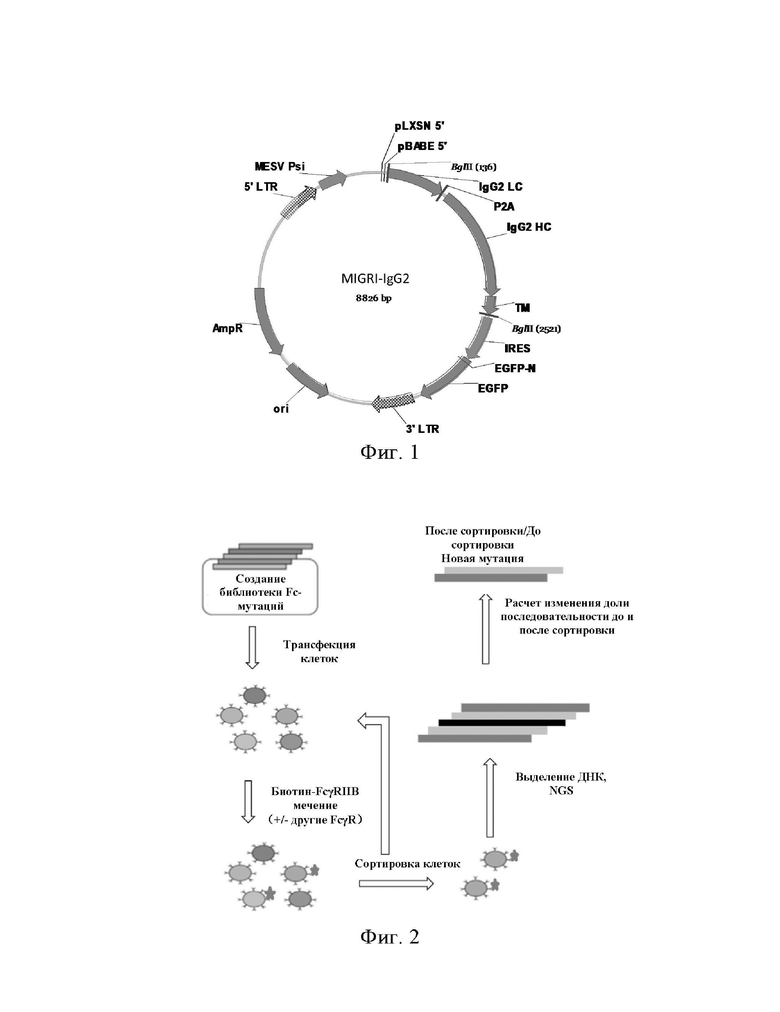
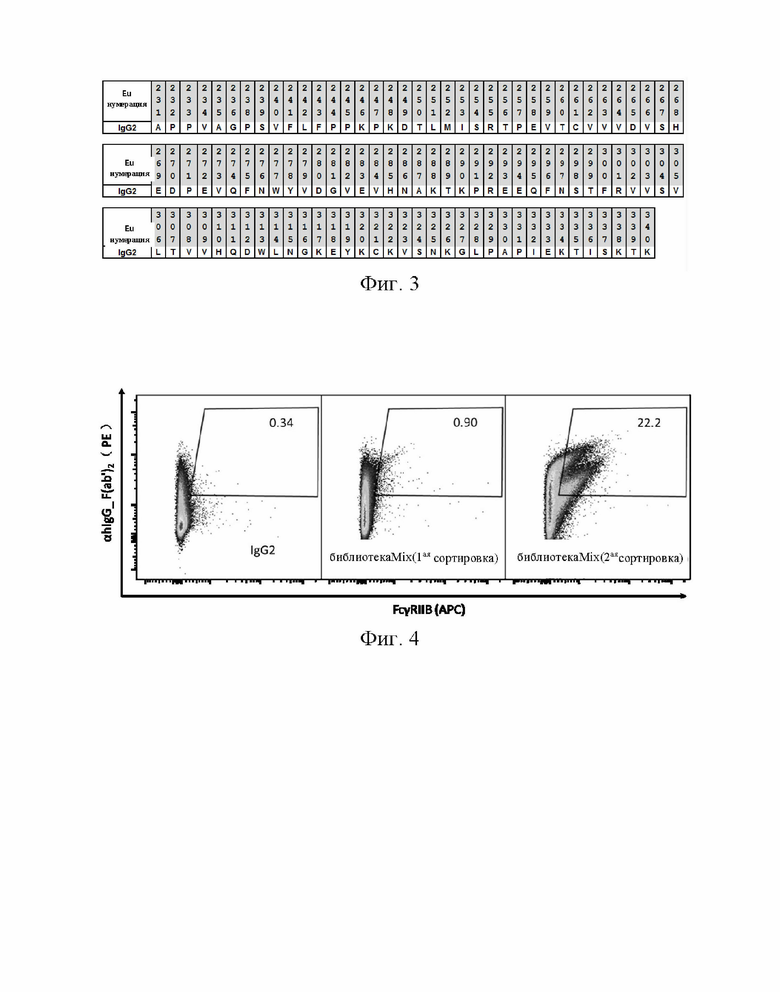
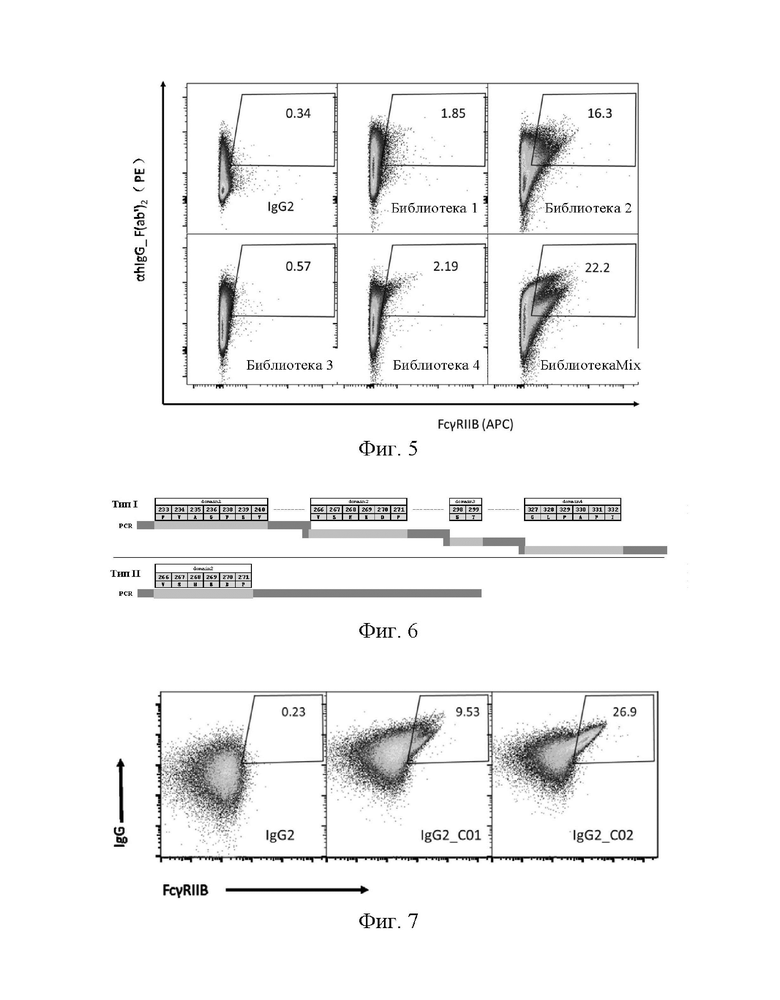
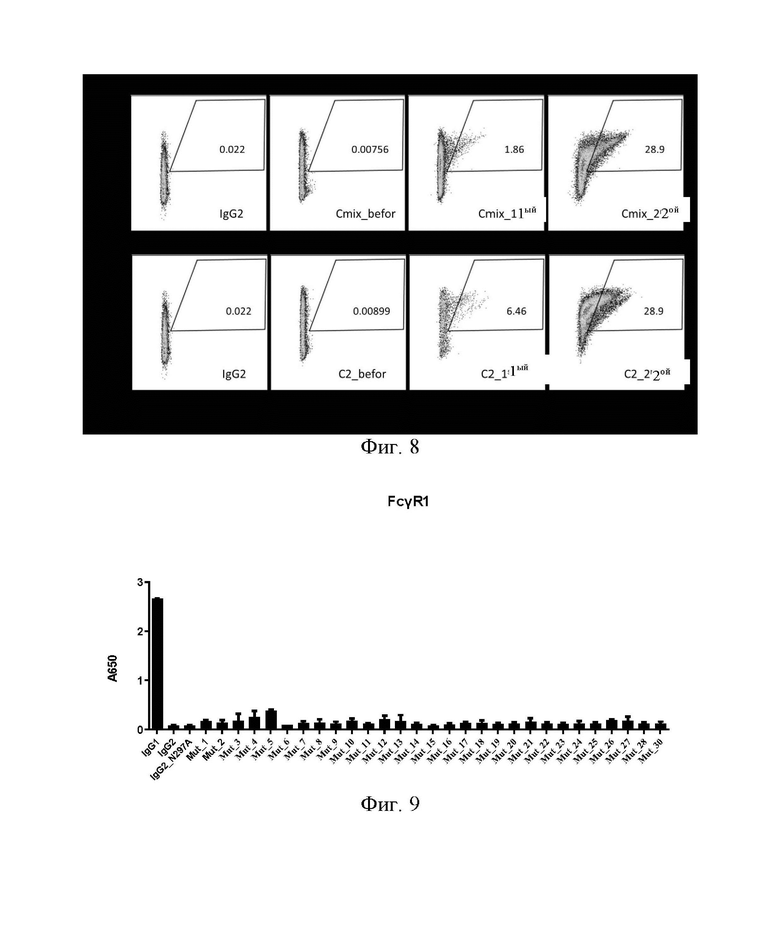
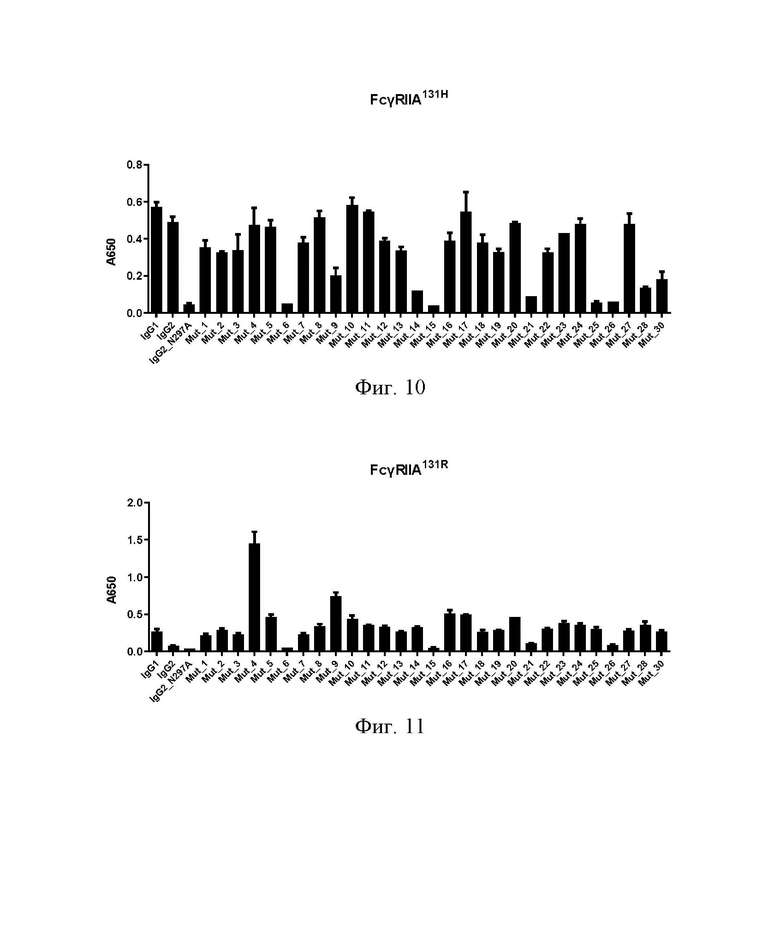
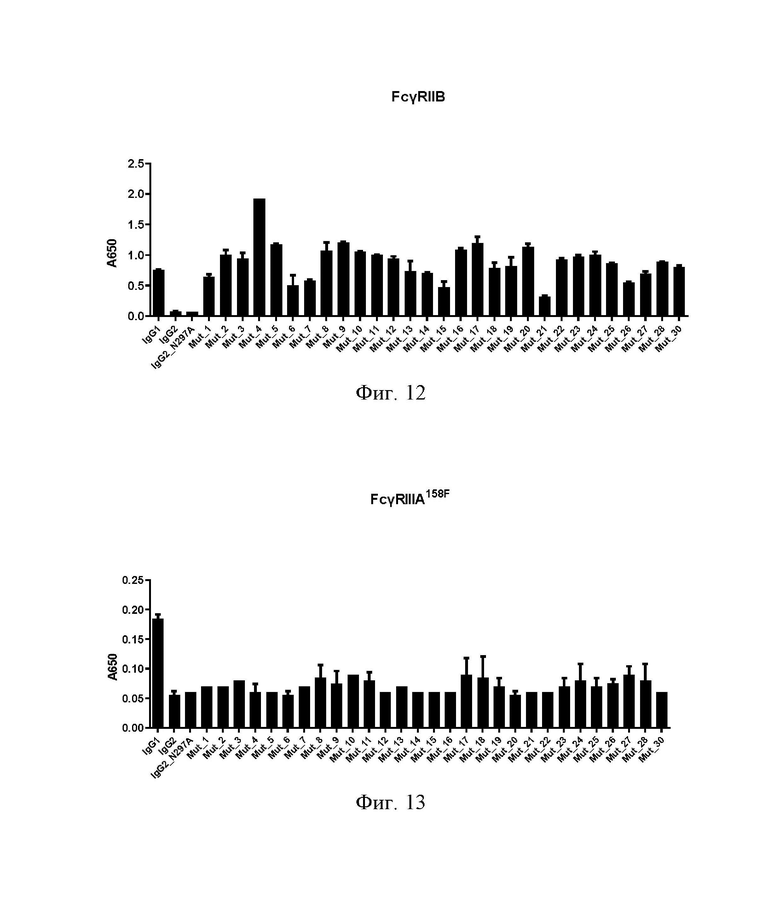
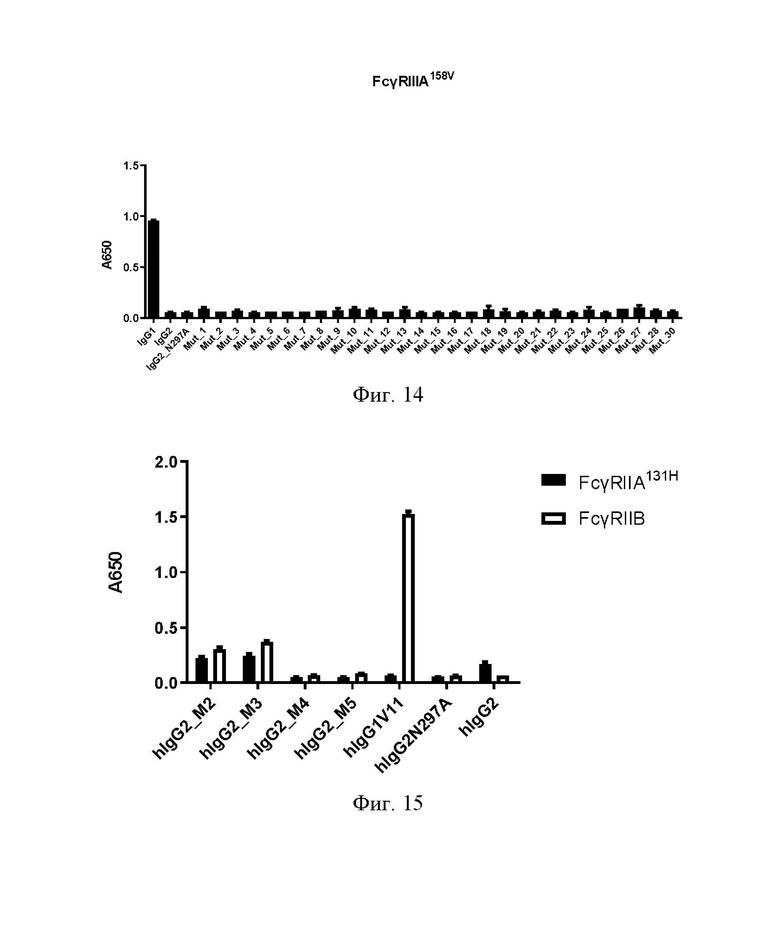
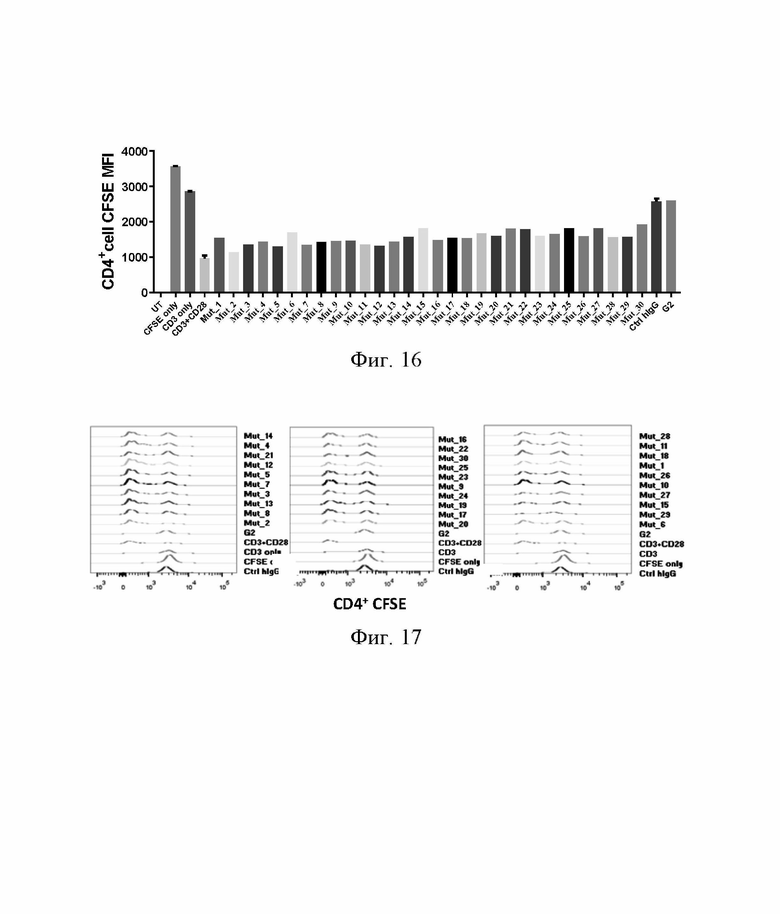
Изобретение относится к области биотехнологии, в частности к мутантному полипептидному Fс-фрагменту, обладающему свойствами повышенной аффинности связывания с FcgRIIB и имеющему аминокислотную последовательность, соответствующую остаткам от положения 233 до положения 332 Fc-области человеческого IgG2 в соответствии с EU нумерацией, а также к мутантной Fc-области иммуноглобулина, обладающей свойствами повышенной аффинности связывания с FcgRIIB и имеющей аминокислотную последовательность от положения 231 до карбоксильного конца тяжелых цепей человеческих IgG2 в соответствии с EU нумерацией. Также раскрыты применение мутантного полипептидного Fс-фрагмента или мутантной Fc-области иммуноглобулина для конструирования агонистической активности антител или слитых белков, выделенный полинуклеотид, экспрессионный вектор, клетка-хозяин, фармацевтическая композиция, способы получения мутантного полипептидного Fс-фрагмента и мутантной Fc-области иммуноглобулина и применение мутантного полипептидного Fс-фрагмента и мутантной Fc-области иммуноглобулина в изготовлении фармацевтической композиции, обладающей повышенной агонистической активностью антитела или слитого белка. Изобретение имеет важное применение в оптимизации агонистической активности антитела. 11 н. и 2 з.п. ф-лы, 17 ил., 14 табл., 11 пр.
1. Мутантный полипептидный Fс-фрагмент, обладающий свойствами повышенной аффинности связывания с FcgRIIB и имеющий аминокислотную последовательность, соответствующую остаткам от положения 233 до положения 332 Fc-области человеческого IgG2 в соответствии с EU нумерацией, как показано в SEQ ID NO: 20, где мутантный полипептидный Fс-фрагмент имеет следующие признаки:
(1) указанный мутантный полипептидный Fс-фрагмент имеет мутацию в положении(ях), выбранном(ых) из группы, состоящей из: L328, H268, S267, P271, G327 или их комбинации, по сравнению с полипептидным Fc-фрагментом дикого типа с SEQ ID NO: 20, где нумерация всех аминокислот основана на Eu нумерации IgG; и
(2) аффинность мутантного полипептидного Fс-фрагмента к FcgRIIB повышена по сравнению с полипептидным Fc-фрагментом дикого типа с SEQ ID NO: 20,
где
мутантный полипептидный Fс-фрагмент имеет мутацию по меньшей мере в одном из L328 и H268 по сравнению с Fc-фрагментом дикого типа, и конкретные мутации в мутантном полипептидном Fс-фрагменте выбраны из одной из группы, состоящей из: L328F, L328Y, L328W, L328E, L328M, L328N, L328G, L328R, L328V, L328A, L328P, H268N, H268K, H268D, H268S, H268E, H268D/S298L/L328W, S267V/S298L/L328W, V234M/S267E/S298L/L328W, A235W/V266L/S298L/L328W, V234Q/A235G/P238L/S239V/H268D/G327A/L328E/A330S/I332T, S239V/V266L/S298L/L328W, V266L/L328W, V266L/S267D/H268D/E269D/P271Q, S267E/H268S/E269D, P233F/V266L/S298L/L328W, V266L/S298L/L328W, V234Q/A235G/P238L/S239V/G327A/L328E/A330S/I332T, V266L/S267E/H268S/E269V, V266L/S267E/H268S/E269V/P271C, V266L/S267E/H268S/E269A/P271C, S267V/S298G/L328W, V266L/S267M/H268E/P271Q, V266L/S267E/H268S/E269G/P271T, V234Q/V266L/S267D/H268D/E269D/P271Q, V234Q/A235G/P238L/S239V/S267E/H268S/E269D, V266L/S267E/H268S/P271V, V234Q/A235G/P238L/S239V/S267E/S298L/G327A/L328E/A330S/I332T, V234Q/V266L/S267E/H268S/E269V и L328E/I332T; где нумерация всех аминокислот основана на Eu нумерации IgG; или
мутантный полипептидный Fс-фрагмент имеет мутацию в S267 по сравнению с Fc-фрагментом дикого типа, и конкретная мутация в мутантном полипептидном Fс-фрагменте выбрана из одной из группы, состоящей из: S267E, S267Q, S267A, S267D, S267M, S267G, S267R, S267V, S267N, S267W, S267E/A330S, S267E/S298G, P233G/S267E, V234M/S267E/S298G/I332L, P233G/S267E/S298G, V266L/S267E/E269K/P271G, P238Q/S267E, S267A/P271C, S267A/P271G, S267E/D270H, S267E/P271C, S267E/P271V, S267E/P271W, S267E/P271Y, S267E/S298R, S267M/P271C, S267M/P271G, S267V/S298L и S267E/P329R; где нумерация всех аминокислот основана на Eu нумерации IgG; или
мутантный полипептидный Fс-фрагмент имеет мутацию в P271 по сравнению с Fc-фрагментом дикого типа, и конкретная мутация в мутантном полипептидном Fс-фрагменте выбрана из одной из группы, состоящей из: P271C, P271G, P271Q, P271A, P271I, P271L, P271S, P271V, P271W, P271Y, V266L/S267E/E269K/P271G, V266A/P271C, V266A/P271G, S267A/P271C, S267A/P271G, S267E/P271C, S267E/P271V, S267E/P271W, S267E/P271Y, S267M/P271C, S267M/P271G, V266G/P271C, P271A/S298R, P271G/G236V, P271G/P329S, P271G/P331C, P271G/P331T, P271G/S298D, P271G/S298E, P271G/S298G, P271G/S298K, P271G/S298L, P271G/S298N, P271G/S298R, P271G/T299A, P271G/T299M, P271G/T299S, P271G/T299W и P271G/I332L; где нумерация всех аминокислот основана на Eu нумерации IgG; или
мутантный полипептидный Fс-фрагмент имеет мутацию в G327 по сравнению с Fc-фрагментом дикого типа, и конкретная мутация в мутантном полипептидном Fс-фрагменте выбрана из одной из группы, состоящей из: G327A, G327L, G327S, G327A/A330R, G327A/A330V, G327A/I332A, G327A/I332C и G327A/I332E; где нумерация всех аминокислот основана на Eu нумерации IgG,
мутантный полипептидный Fс-фрагмент имеет мутацию в S298 по сравнению с Fc-фрагментом дикого типа, и конкретная мутация в мутантном полипептидном Fс-фрагменте представляет собой S298L; где нумерация всех аминокислот основана на Eu нумерации IgG.
2. Мутантный полипептидный Fс-фрагмент по п. 1, где конкретная мутация мутантного полипептидного Fс-фрагмента по сравнению с Fc-фрагментом дикого типа выбрана из одной из группы, состоящей из: H268D/S298L/L328W, S267V/S298L/L328W, V234M/S267E/S298L/L328W, A235W/V266L/S298L/L328W и V234Q/A235G/P238L/S239V/H268D/G327A/L328E/A330S/I332T; где нумерация всех аминокислот основана на Eu нумерации IgG.
3. Мутантная Fc-область иммуноглобулина, обладающая свойствами повышенной аффинности связывания с FcgRIIB и имеющая аминокислотную последовательность от положения 231 до карбоксильного конца тяжелых цепей человеческих IgG2 в соответствии с EU нумерацией, где мутантная Fc-область иммуноглобулина содержит мутантный полипептидный Fс-фрагмент по любому из пп. 1, 2.
4. Применение мутантного полипептидного Fс-фрагмента по любому из пп. 1, 2 или мутантной Fc-области иммуноглобулина по п. 3 для конструирования агонистической активности антител или слитых белков.
5. Выделенный полинуклеотид, который кодирует мутантный полипептидный Fс-фрагмент по любому из пп. 1, 2.
6. Выделенный полинуклеотид, который кодирует мутантную Fc-область иммуноглобулина по п. 3.
7. Экспрессионный вектор, который содержит выделенный полинуклеотид по п. 5 или 6.
8. Клетка-хозяин для экспрессии мутантного полипептидного Fс-фрагмента по любому из пп. 1, 2 или мутантной Fc-области иммуноглобулина по п. 3, которая содержит экспрессионный вектор по п. 7 или имеет полинуклеотид по п. 5 или 6, интегрированный в геном клетки;
или клетка-хозяин экспрессирует мутантный полипептидный Fс-фрагмент по любому из пп. 1-2 или мутантную Fc-область иммуноглобулина по п. 3.
9. Фармацевтическая композиция, обладающая способностью повышать аффинность Fc к FcgRIIB, которая содержит:
(а) мутантный полипептидный Fс-фрагмент по любому из пп. 1, 2 или мутантную Fc-область иммуноглобулина по п. 3; и
(б) фармацевтически приемлемый носитель.
10. Способ получения мутантного полипептидного Fс-фрагмента по любому из пп. 1, 2, включающий стадии:
(1) культивирования клетки-хозяина по п. 8 в подходящих условиях с получением культуры, содержащей указанный мутантный полипептидный Fс-фрагмент; и
11. Способ получения мутантной Fc-области иммуноглобулина по п. 3, включающий стадии:
(1) культивирования клетки-хозяина по п. 8 в подходящих условиях с получением культуры, содержащей указанную мутантную Fc-область иммуноглобулина; и
(2) очистки и/или выделения указанной мутантной Fc-области иммуноглобулина из культуры, полученной на стадии (1).
12. Применение мутантного полипептидного Fс-фрагмента по любому из пп. 1, 2, мутантной Fc-области иммуноглобулина по п. 3, полинуклеотида по п. 5 или 6, экспрессионного вектора по п. 7 и/или клетки-хозяина по п. 8 в изготовлении фармацевтической композиции, обладающей повышенной агонистической активностью антитела или слитого белка.
13. Применение по п. 12, где указанная агонистическая активность полезна для иммунотерапии опухолей, уменьшения воспаления и/или уменьшения аутоиммунных симптомов.
| US 20160122435 A1, 05.05.2016 | |||
| US 7700099 B2, 20.04.2010 | |||
| US 20090042291 A1, 12.02.2009 | |||
| HARGREAVES C.E | |||
| et al., Fcγ receptors: genetic variation, function, and disease, Immunol Rev., 2015, v | |||
| Способ изготовления гибких труб для проведения жидкостей (пожарных рукавов и т.п.) | 1921 |
|
SU268A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| ГУМАНИЗИРОВАННЫЕ АНТИТЕЛА К CD19 И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКОГО, СВЯЗАННОГО С ТРАНСПЛАНТАЦИЕЙ И АУТОИММУННОГО ЗАБОЛЕВАНИЯ | 2007 |
|
RU2495882C2 |
Авторы
Даты
2025-05-12—Публикация
2020-12-03—Подача