Перекрестная ссылка на родственные заявки
[0001] Эта заявка испрашивает приоритет по заявке 62/866810, поданной 26 июня 2019 г. под названием «Готовая лекарственная форма для заместительной ферментотерапии для лечения гомоцистинурии», и заявке 62/983860, поданной 2 марта 2020 г. под названием «Готовая лекарственная форма для ферментотерапии для лечения гомоцистинурии», содержание каждой из которых полностью включено сюда посредством ссылки.
Ссылка на список последовательностей
[0002] Настоящая заявка подается вместе со списком последовательностей в электронной форме. Файл списка последовательностей под названием 2089_1005PCT_SL.txt был создан 26 июня 2020 г. и имеет размер 18401 байт. Информация в электронной форе о списке последовательностей полностью включена сюда посредством ссылки.
Область техники
[0003] Настоящее изобретение относится к композициям и способам для ферментотерапии для лечения гомоцистинурии с использованием описанной здесь готовой лекарственной формы.
Предшествующий уровень техники
Вызванная дефицитом цистатионин-β-синтазы гомоцистинурия (CBSDH), также известная как классическая гомоцистинурия (HCU) или HCU типа 1, является редким заболеванием, поражающим как детей, так и взрослых. CBSDH представляет собой редкое аутосомно-рецессивное метаболическое состояние, характеризующееся избытком соединения гомоцистеина (Hcy) в моче, тканях и плазме из-за снижения или отсутствия активности фермента цистатионин-β-синтазы (CBS) (смотрите Kraus et al., In: Carmel R, Jacobsen DW, eds. Homocysteine in Health and Disease. Cambridge, United Kingdom: Cambridge University Press; 2001:223-243; Sacharow et al., Homocystinuria Caused by Cystathionine Beta-Synthase Deficiency. In: Adam MP, Ardinger HH, Pagon RA, Wallace SE, Bean LJH, Mefford HC, et al, eds. GeneReviewsTM [Интернет]. Seattle (WA): University of Washington, Seattle, 2017; каждый из которых (вышеуказанных документов) полностью включен сюда посредством ссылки).
[0005] Диагноз CBSDH может быть подтвержден с помощью молекулярно-генетического исследования гена CBS, как описано Sacharow и др. CBS представляет собой фермент метаболизма серосодержащей аминокислоты метионина (Met), которая присутствует в белках в пище (смотрите Maclean et al. J Biol Chem. 2012; 287(38):31994-32005, который полностью включен таким образом посредством ссылки). Следовательно, CBSDH также можно диагностировать по определению заметно повышенных концентраций общего метионина в плазме. Эти обнаружения повышения аминокислоты могут быть подтверждены обнаружением снижения активности фермента CBS или обнаружением биаллельных патогенных вариантов гена, кодирующего цистатионин-β-синтазу (смотрите Picker et al., Homocystinuria Caused by Cystathionine Beta-Synthase Deficiency. 2004 Jan 15 [который обновлен 13 ноября 2014 г.] In: Pagon RA, Adam MP, Ardinger HH, et al., eds. GeneReviewsTM [Интернет]. Seattle (WA): University of Washington, Seattle; 1993-2016, который доступен на сайте: ncbi.nlm.nih.gov, который полностью включен таким образом посредством ссылки). Дефицит CBS также приводит к снижению уровней цистатионина (Cth) и цистеина (Cys) (смотрите Veeranki et al. Int J Mol Sci. 2013 Jul 18; 14(7):15074-91, который полностью включен таким образом посредством ссылки).
[0006] CBSDH можно заподозрить на основании следующего (Picker et al. 2014): 1) клинических признаков, включающих эктопию хрусталика (смещение хрусталика в глазу) и/или тяжелую миопию, астенический габитус (высокий и стройный), аномалии скелета, остеопороз с ранним началом и/или тромбоэмболические события, необъяснимую задержку развития/умственную отсталость; 2) скрининга новорожденных на гиперметионинемию или, в частности, положительный по дефициту CBS семейный анамнез, который может привести к идентификации пациентов до появления симптомов (смотрите Yap et al. J Inherit Metab Dis 1998; 21:738-47, который полностью включен таким образом посредством ссылки); и 3) семейного анамнеза. Все эти клинические признаки и возраст появления симптомов у пациентов значительно различаются. Существующие подходы к скринингу обычно не позволяют выявить новорожденных с меньшим дефицитом CBS и выявляют только меньшинство пациентов с более тяжелой CBSDH (смотрите Huemer et al. J Inherit Metab Dis. 2015 Nov; 38(6):1007-19; Yap, Orphanet Encyclopedia [периодическое издание онлайн]. 2005, pages 1-13; Schiff et al. Neuropediatrics. 2012 Dec; 43(6):295-304; каждый из которых полностью включен таким образом посредством ссылки). CBSDH является самым распространенным генетическим нарушением метаболизма серы с распространенностью приблизительно от 1:200000 до 1:335000 во всем мире. В пути метаболизма серы незаменимая аминокислота L-метионин метаболизируется до Hcy, с последующим двухстадийным транссульфурированием сначала до Cth и, наконец, до Cys. CBS, которая катализирует превращение Hcy в Cth, обнаруживается главным образом в печени и почках. Избыток Hcy может быть подвергнут реметилированию в метионин с помощью бетаин-Hcy 5-метилтрансферазы, что также повышает уровень Met в плазме.
[0007] Хотя у некоторых пациентов заболевание диагностируется вскоре после рождения, часто диагноз CBSDH ставится в более позднем возрасте после развития классических клинических симптомов (смотрите Huemer et al. J Inherit Metab Dis. 2015 Nov, 38(6):1007-19; Yap, Orphanet Encyclopedia [периодическое издание онлайн]. 2005, pages 1-13; Huemer et al. J Inherit Metab Dis. 2015 Nov, 38(6):1007-19; Yap, Orphanet Encyclopedia [периодическое издание онлайн]. 2005, pages 1-13; оба из которых полностью включены сюда посредством ссылки). CBSDH характеризуется задержкой развития/умственной отсталостью, эктопией хрусталика и/или тяжелой миопией, аномалиями скелета (чрезмерным ростом и длиной конечностей) и тромбоэмболией. Все эти клинические признаки у пациентов значительно различаются.
[0008] Нормальные уровни общего гомоцистеина (tHcy) варьируются в зависимости от возраста, пола и состояния питания, но, как правило, находятся в диапазоне от 4,5 до 11 мкмоль/л (смотрите Quest Diagnostics Reference Range; questdiagnostics.com, который полностью включен таким образом посредством ссылки). Мужчины, как правило, имеют немного (на 1-2 мкмоль/л) более высокие уровни tHcy, чем женщины, и у пациентов в возрасте от подросткового периода до 80 лет отмечается приблизительно удвоение средних значений (смотрите Refsum et al. Clin Chem 2004;50:3-32, который полностью включен таким образом посредством ссылки). В популяции, получающей соли фолевой кислоты в качестве добавки, верхний предел (97,5%) уровней tHcy составляет приблизительно 12 мкмоль/л у взрослых <65 лет и 16 ммкмоль/л у взрослых старше 65 лет. Многие пациенты с CBSDH имеют тяжелую гипергомоцистеинемию с уровнями общего tHcy, превышающими 100 мкмоль/л, тогда как у других наблюдаются повышения от легкого до повышения до уровня, в несколько раз превышающего норму, (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки). Было обнаружено, что уровни tHcy сильно коррелируют с тяжестью заболевания (смотрите Yap et al. J Inherit Metab Dis 1998; 21:738-747, который полностью включен таким образом посредством ссылки).
[0009] CBSDH характеризуется заболеваниями глаз (эктопией хрусталика и/или тяжелой миопией), костной системы (чрезмерным ростом, длинными конечностями, сколиозом и воронкообразной деформацией грудной клетки), сердечнососудистой системы (тромбоэмболией) и центральной нервной системы (ЦНС) (задержкой развития/умственной отсталостью). Эти клинические признаки проявляются по-разному у пациентов, при этом могут быть вовлечены все системы или только одна. Некоторые пациенты страдают тяжелым полисистемным заболеванием с началом в детстве, тогда как пациенты с менее тяжелым течением заболевания могут оставаться бессимптомными во взрослом возрасте. Без лечения ожидаемая продолжительность жизни у более тяжелых пациентов заметно снижается (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки).
[0010] Исследования показали, что снижение уровней Hcy у пациентов с CBSDH коррелирует с менее тяжелыми проявлениями клинических симптомов (смотрите Yap et al. J Inherit Metab Dis 1998; 21:738-747, который полностью включен таким образом посредством ссылки). Пути, через которые уровни Hcy вызывают повреждение этих систем, описаны в различных местах (например, Ajith et al. Clin Chim Acta 2015; 450:316-321; Sato et al. Bone 2005; 36:721-726; Behera et al. J Cell Physiol 2016, каждый из которых полностью включен таким образом посредством ссылки), и привели к исследованиям также для изучения роли Hcy в общей популяции.
[0011] В настоящее время доступно несколько терапий для лечения CBSDH. Современные терапии нацелены на путь метаболизма серы посредством комбинации одного или более из следующих действий: 1) модификации диеты для снижения потребления белка и/или Met; 2) добавления некоторых или всех следующих веществ: соли фолиевой кислоты, витамина B12, витамина B6; и 3) добавления бетаина в качестве донора метила для усиления ферментативного реметилирования накопленного Hcy в Met. Хотя не было опубликовано исследований качества жизни (QoL) пациентов с CBSDH, было замечено, что пациенты и лица, осуществляющие уход за ними, страдают от психосоциальных последствий соблюдения и принятия строго ограниченной и социально изолирующей диеты и крайне обеспокоены отдаленными медицинскими последствиями заболевания. Многие пациенты сообщают о том, что им не терпится смягчить свои диеты, не ставя под угрозу свои долгосрочные планы на будущее.
[0012] Следовательно, в данной области давно ощущается потребность в способе лечения CBSDH, обладающем большей эффективностью и меньшими негативными эффектами на пациентов, чем существующие терапии.
Краткое изложение сущности настоящего изобретения
[0013] Различные варианты осуществления настоящего изобретения обеспечивают лекарственное вещество, содержащее: (a) выделенный белок цистатионин-β-синтазу (CBS), включающую SEQ ID NO:1; и (b) молекулу ПЭГ, ковалентно связанную с белком CBS. В некоторых вариантах осуществления описанного здесь лекарственного вещества молекула ПЭГ представляет собой ME-200GS.
[0014] Различные варианты осуществления настоящего изобретения обеспечивают фармацевтическую композицию, содержащую лекарственное вещество и фармацевтически приемлемый адъювант, разбавитель или носитель.
[0015] В некоторых вариантах осуществления препарат является лиофилизированным. Различные варианты осуществления настоящего изобретения обеспечивают лиофилизированный препарат, который после восстановления влагосодержания представляет собой восстановленный жидкий препарат, содержащий готовую к применению лекарственную форму в концентрации, составляющей приблизительно 20-30 мг/мл или приблизительно 25 мг/мл, в забуференном фосфатом солевом растворе (PBS); приблизительно 11,4 мМ гидрофосфат натрия; приблизительно 137 мМ хлорид натрия; приблизительно 2,70 мМ хлорид калия; и приблизительно 1,98 мМ дигидроортофосфат калия. Готовая к применению лекарственная форма здесь представляет собой жидкий фармацевтический препарат, содержащий терапевтически эффективное количество лекарственной формы, например, стандартную дозу фармацевтической композиции, включающую лекарственное вещество в виде ПЭГилированного усеченного белка CBS человека с аминокислотной последовательностью SEQ ID NO:1 (например, 20NHS PEG-CBS). Готовая к применению лекарственная форма может поставляться во флаконе или схожем контейнере для облегчения введения субъекту.
[0016] Различные варианты осуществления настоящего изобретения обеспечивают лиофилизированный препарат, который после восстановления влагосодержания представляет собой восстановленный жидкий препарат, содержащий 20-30 мг или приблизительно 25 мг лекарственного вещества; 1 мл воды; 2 мг гидрофосфата натрия (дигидрата); 8 мг хлорида натрия; 0,2 мг хлорида калия; и 0,3 мг дигидроортофосфата калия. В качестве альтернативы, лиофилизированный препарат можно восстановить, чтобы он содержал лекарственное вещество, буфер и наполнитель. В некоторых вариантах осуществления буфер представляет собой 15 мМ фосфат калия. В некоторых вариантах осуществления наполнитель представляет собой 8% (в отношении веса к объему) трегалозу.
[0017] Различные варианты осуществления настоящего изобретения обеспечивают способ лечения гомоцистинурии у субъекта, включающий: введение субъекту терапевтически эффективного количества препарата фармацевтической композиции, описанной здесь.
[0018] В некоторых вариантах осуществления терапевтически эффективное количество представляет собой дозу, выбранную из диапазона от приблизительно 0,25 мг/кг до приблизительно 10 мг/кг. Например, доза составляет приблизительно 0,33 мг/кг, приблизительно 0,66 мг/кг, приблизительно 1,0 мг/кг или приблизительно 1,5 мг/кг. В качестве альтернативы, доза составляет приблизительно 2 мг/кг, приблизительно 7 мг/кг и приблизительно 10 мг/кг. Например, доза может составлять приблизительно 0,5 мг/кг. Альтернативно, терапевтически эффективное количество представляет собой дозу, выбранную из диапазона от приблизительно 5,0 мг/кг до приблизительно 50 мг/кг и от приблизительно 10,0 мг/кг до приблизительно 25 мг/кг. Например, дозу выбирают из группы, состоящей из: приблизительно 0,25 мг/кг, приблизительно 0,33 мг/кг, приблизительно 0,66 мг/кг, приблизительно 1,00 мг/кг, приблизительно 1,50 мг/кг, приблизительно 2,00 мг/кг, приблизительно 3,00 мг/кг, приблизительно 4,00 мг/кг, приблизительно 5,00 мг/кг, приблизительно 6,00 мг/кг, приблизительно 7,00 мг/кг, приблизительно 8,00 мг/кг, приблизительно 9,00 мг/кг, приблизительно 10,0 мг/кг, приблизительно 11,0 мг/кг, приблизительно 12,0 мг/кг, приблизительно 13,0 мг/кг, приблизительно 14,0 мг/кг, приблизительно 15,0 мг/кг, приблизительно 16,0 мг/кг, приблизительно 17,0 мг/кг, приблизительно 18,0 мг/кг, приблизительно 19,0 мг/кг, приблизительно 20,0 мг/кг, приблизительно 21,0 мг/кг, приблизительно 22,0 мг/кг, приблизительно 23,0 мг/кг, приблизительно 24,0 мг/кг, приблизительно 25,0 мг/кг, приблизительно 26,0 мг/кг, приблизительно 27,0 мг/кг, приблизительно 28,0 мг/кг, приблизительно 29,0 мг/кг, приблизительно 30,0 мг/кг, приблизительно 31,0 мг/кг, приблизительно 32,0 мг/кг, приблизительно 33,0 мг/кг, приблизительно 34,0 мг/кг, приблизительно 35,0 мг/кг, приблизительно 36,0 мг/кг, приблизительно 37,0 мг/кг, приблизительно 38,0 мг/кг, приблизительно 39,0 мг/кг, приблизительно 40,0 мг/кг, приблизительно 41,0 мг/кг, приблизительно 42,0 мг/кг, приблизительно 43,0 мг/кг, приблизительно 44,0 мг/кг, приблизительно 45,0 мг/кг, приблизительно 46,0 мг/кг, приблизительно 47,0 мг/кг, приблизительно 48,0 мг/кг, приблизительно 49,0 мг/кг и приблизительно 50,0 мг/кг.
[0019] В некоторых вариантах осуществления способ включает, кроме того, введение субъекту по крайней мере одного вещества, выбранного из группы, состоящей из пиридоксина, витамина B6 и бетаина. В некоторых вариантах осуществления субъект соблюдает диету с ограничением метионина (Met). В некоторых вариантах осуществления способ включает, кроме того, введение антитромбоцитарного средства. В некоторых вариантах осуществления антитромбоцитарное средство представляет собой разжижитель крови варфарин или антикоагулянт. В некоторых вариантах осуществления стадия введения выполняется приблизительно один раз каждые 3 дня. В некоторых вариантах осуществления стадия введения выполняется приблизительно один раз в день. В некоторых вариантах осуществления стадия введения выполняется приблизительно один раз в неделю. В некоторых вариантах осуществления стадию введения повторяют на протяжении приблизительно 6 недель. В некоторых вариантах осуществления стадию введения повторяют на протяжении приблизительно 3 месяцев. В некоторых вариантах осуществления стадию введения повторяют на протяжении приблизительно 6 месяцев. В некоторых вариантах осуществления стадию введения повторяют на протяжении более 6 месяцев. В некоторых вариантах осуществления стадию введения повторяют в течение оставшегося времени жизни субъекта.
[0020] Различные варианты осуществления настоящего изобретения обеспечивают способ снижения уровня гомоцистеина (Hcy) у субъекта, включающий: введение субъекту терапевтически эффективного количества препарата фармацевтической композиции, описанной здесь.
[0021] В некоторых вариантах осуществления уровень Hcy составляет менее приблизительно 80 мкМ после стадии введения. В некоторых вариантах осуществления уровень Hcy снижается вплоть до 10% после стадии введения. В некоторых вариантах осуществления уровень Hcy снижается вплоть до 20% после стадии введения. В некоторых вариантах осуществления уровень Hcy снижается вплоть до 30% после стадии введения. В некоторых вариантах осуществления уровень Hcy снижается вплоть до 40% после стадии введения. В некоторых вариантах осуществления уровень Hcy снижается вплоть до 50% после стадии введения. В некоторых вариантах осуществления уровень Hcy снижается вплоть до 60% после стадии введения. В некоторых вариантах осуществления уровень Hcy снижается вплоть до 70% после стадии введения. В некоторых вариантах осуществления уровень Hcy снижается вплоть до 80% после стадии введения. В некоторых вариантах осуществления уровень Hcy снижается вплоть до 90% после стадии введения. В некоторых вариантах осуществления уровень Hcy находится в диапазоне от приблизительно 10 мкМ до приблизительно 20 мкМ после стадии введения. В некоторых вариантах осуществления уровень Hcy составляет менее 10 мкМ после стадии введения. В некоторых вариантах осуществления уровень Hcy составляет приблизительно 55 мкМ после стадии введения.
[0022] В некоторых вариантах осуществления терапевтически эффективное количество представляет собой дозу, выбранную из диапазона от приблизительно 0,25 мг/кг до приблизительно 10 мг/кг. Например, доза может составлять приблизительно 0,33 мг/кг, приблизительно 0,66 мг/кг, приблизительно 1,0 мг/кг, приблизительно 1,50 мг/кг, приблизительно 2,0 мг/кг, приблизительно 7,0 мг/кг или приблизительно 10 мг/кг. В некоторых вариантах осуществления доза составляет менее 10 мг/кг.
[0023] В некоторых вариантах осуществления способ включает, кроме того, введение субъекту по крайней мере одного вещества, выбранного из группы, состоящей из пиридоксина, витамина B6 и бетаина. В некоторых вариантах осуществления субъект соблюдает диету с ограничением метионина (Met). В некоторых вариантах осуществления способ включает, кроме того, введение антитромбоцитарного средства. В некоторых вариантах осуществления антитромбоцитарное средство представляет собой разжижитель крови варфарин или антикоагулянт. В некоторых вариантах осуществления стадия введения выполняется приблизительно один раз каждые 3 дня. В некоторых вариантах осуществления стадия введения выполняется приблизительно один раз в день. В некоторых вариантах осуществления стадия введения выполняется приблизительно один раз в неделю. В некоторых вариантах осуществления стадию введения повторяют на протяжении приблизительно 6 недель. В некоторых вариантах осуществления стадию введения повторяют на протяжении приблизительно 3 месяцев. В некоторых вариантах осуществления стадию введения повторяют на протяжении приблизительно 6 месяцев. В некоторых вариантах осуществления стадию введения повторяют на протяжении более 6 месяцев. В некоторых вариантах осуществления стадию введения повторяют в течение оставшегося времени жизни субъекта.
[0024] Различные варианты осуществления настоящего изобретения обеспечивают способ повышения уровня цистеина (Cys) у субъекта, включающий: введение субъекту терапевтически эффективного количества препарата фармацевтической композиции, описанной здесь.
[0025] Различные варианты осуществления настоящего изобретения обеспечивают способ повышения уровня цистатионина (Cth) у субъекта, включающий: введение субъекту терапевтически эффективного количества препарата фармацевтической композиции, описанной здесь.
[0026] Различные варианты осуществления настоящего изобретения обеспечивают способ лечения, облегчения или предотвращения негативных клинических последствий, связанных со зрительной системой, костной системой, сердечнососудистой системой и/или центральной нервной системой субъекта, при этом способ включает: введение субъекту терапевтически эффективного количества препарата фармацевтической композиции, описанной здесь.
Краткое описание чертежей
[0027] Вышеизложенные и другие цели, признаки и преимущества станут очевидны из следующего описания конкретных вариантов осуществления настоящего изобретения, как проиллюстрировано на прилагаемых чертежах. Чертежи необязательно должны быть в масштабе; вместо этого акцент делается на иллюстрацию принципов различных вариантов осуществления настоящего изобретения.
[0028] На фиг. 1 представлена блок-схема процесса ПЭГилирования, используемого в некоторых вариантах осуществления, описанных здесь.
[0029] Фиг. 2 представляет собой диаграмму условий входа в исследование с использованием коробки-головоломки для каждого испытания в течение трехдневного периода тестирования.
[0030] На фиг. 3 представлены результаты доклинического исследования на модели гомоцистинурии на мыши с использованием длительного непрерывного лечения 20NHS PEG-CBS (обозначенной на фигуре «PEG CBS C15S») на фоне изменяющегося рациона (рациона со стандартным содержанием метионина («STD»), рациона с высоким содержанием метионина («HMD») и/или рациона с низким или ограниченным содержанием метионина («MRD»).
Подробное описание настоящего изобретения
I. ВВЕДЕНИЕ
[0031] Вызванная дефицитом цистатионин-бета-синтазы гомоцистинурия (CBSDH) характеризуется повышенными уровнями гомоцистеина (Hcy) в плазме, вместе с высокими уровнями Met и сниженными концентрациями цистеина (Cys) (смотрите Yap S. Homocystinuria due to cystathionine beta-synthase deficiency. Orphanet Encyclopaedia [периодическое издание онлайн] 2005; Morris et al. J Inherit Metab Dis 2017; 40:49-74; NORD, Kraus JP. Homocystinuria due to cystathionine beta-synthase deficiency. NORD [периодическое издание онлайн] 2017; каждый из которых полностью включен таким образом посредством ссылки). На сегодняшний день идентифицировано более 180 различных мутаций связанного с CBSDH гена CBS (смотрите Базу данных по мутациям в геноме человека. 2017. Тип ссылки: Интернет-источник. Доступен на сайте: hgmd.cf.ac.uk/ac/index.php, который полностью включен таким образом посредством ссылки). Гомоцистеин (Hcy) представляет собой встречающуюся в природе аминокислоту, которая вместе с серином служит субстратом для фермента CBS. CBS регулирует однонаправленный поток серы от метионина (Met) к цистеину (Cys), действуя на пересечении путей трансметилирования, транссульфурирования и реметилирования (смотрите Maclean et al. J Biol Chem. 2012;287(38):31994-32005, который полностью включен таким образом посредством ссылки). Нативная CBS активируется при связывании аллостерического активатора S-аденозилметионина (SAM) и катализирует реакцию β-замещения, в которой серин конденсируется с Hcy зависимым от пиридоксаль-5'-фосфата (пиридоксина или витамина B6) образом с образованием цистатионина (Cth). Цистатионин-γ-лиаза (CGL), действующая после CBS, использует Cth в качестве субстрата для образования Cys. Таким образом, правильное функционирование CBS важно для регуляции метаболизма Hcy, Met и Cys.
[0032] Тяжесть и проявления признаков и симптомов CBSDH широко варьируются среди пациентов (смотрите Karaca et al. Gene 2014; 534:197-203; Trondle et al. Acta Med Austriaca 2001; 28:145-151; Kluijtmans et al. Am J Hum Genet 1999; 65:59-67; каждый из которых полностью включен таким образом посредством ссылки). У многих пациентов наблюдается тяжелая гипергомоцистеинемия с уровнями общего гомоцистеина (tHcy), превышающими 100 мкмоль/л, тогда как у других отмечаются повышения tHcy в диапазоне от незначительного до повышения до уровня, в несколько раз превышающего норму, (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки). Значительно повышенные уровни tHcy, как правило, коррелируют с более тяжелым течением заболевания, тогда как более низкие уровни, как правило, коррелируют с более легкой формой заболевания. Нормальные уровни tHcy варьируются в зависимости от возраста и состояния питания, но колеблются, как правило, между 10 и 15 мкмоль/л.
[0033] CBSDH обычно классифицируют в зависимости от того, реагирует ли пораженный индивидуум на снижающее уровень общего гомоцистеина (tHcy) лечение пиридоксином (витамином B6), кофактором фермента CBS, необходимым для нормального функционирования CBS (смотрите Mudd et al. Am J Hum Genet 1985; 37: 1-31; Abbott et al. Am J Med Genet 1987; 26:959-969; которые полностью включены таким образом посредством ссылки). В целом, пациенты, которые являются чувствительными к пиридоксину, имеют более низкие уровни tHcy, что приводит к более легкой форме расстройства. У этих пациентов в более позднем возрасте может появиться только один или несколько симптомов CBSDH, и многие из них остаются с не диагностированным заболеванием. Поэтому полагают, что пациенты, которые являются очень чувствительными к пиридоксину, недостаточно представлены в большинстве исследований.
[0034] Ретроспективные исследования показывают, что пациенты с самыми высокими уровнями tHcy (подвергнутые лечению или не подвергнутые лечению) имеют более тяжелые симптомы и в более раннем возрасте (смотрите Yap et al. J Inherit Metab Dis 1998; 21:738-747; Mudd et al. Am J Hum Genet 1985; 37:1-31, оба из которых полностью включены таким образом посредством ссылки). У не подвергнутых лечению индивидуумов с повышенными уровнями tHcy, как правило, наблюдаются задержка развития, тромбоэмболия, тяжелая миопия с последующим смещением хрусталика, переломы типа переломов при остеопорозе, марфаноидный габитус (в частности, удлинение длинных костей) и психические отклонения, в том числе трудности в обучении (смотрите Yap S. Homocystinuria due to cystathionine beta-synthase deficiency. Orphanet Encyclopaedia [периодическое издание онлайн] 2005; Morris et al. J Inherit Metab Dis 2017; 40:49-74; NORD, Kraus JP. Homocystinuria due to cystathionine beta-synthase deficiency. NORD [периодическое издание онлайн] 2017, каждый из которых полностью включен таким образом посредством ссылки). Некоторые пациенты с повышенными уровнями tHcy страдают тяжелым полисистемным заболеванием с началом в детском возрасте. Без лечения ожидаемая продолжительность жизни у более тяжелых пациентов заметно снижается (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки).
[0035] Нормальная плазма человека содержит менее 16 мМ соединений-производных, измеренных как tHcy и состоящих из свободного гомоцистеина (гомоцистеина с восстановленным тиолом) (Hcy-SH или fHcy), дисульфидов (таких как гомоцистеин-цистеин и гомоцистеин) и связанного с белком гомоцистеина (смотрите Ueland; Nord Med 1989; 104:293-298; Mudd et al. N Engl J Med 1995; 333:325; Mudd et al. Arterioscler Thromb Vasc Biol 2000; 20:1704-1706; каждый из которых полностью включен таким образом посредством ссылки). Различие между сульфгидрильной формой (гомоцистеина; Hcy) и дисульфидной формой (гомоцистеина) (смотрите Yap S. Homocystinuria due to cystathionine beta-synthase deficiency. Orphanet Encyclopaedia [периодическое издание онлайн] 2005, который полностью включен таким образом посредством ссылки) важно, поскольку многие патофизиологические эффекты зависят от присутствия сульфгидрильной группы в Hcy (смотрите Yap S. Homocystinuria due to cystathionine beta-synthase deficiency. Orphanet Encyclopaedia [периодическое издание онлайн] 2005; Ueland et al. Nord Med 1989; 104:293-298; Mudd et al. N Engl J Med 1995;333:325; каждый из которых полностью включен таким образом посредством ссылки).
[0036] CBS в основном экспрессируется в печени, поджелудочной железе, почках и головном мозге (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки). Каталитический домен связывает пиридоксаль-5'-фосфат (кофактор, также известный как пиридоксин или витамин B6), а регуляторный домен связывает SAM (аллостерический активатор).
[0037] Недостаточные уровни ферментативной активности CBS блокируют путь транссульфурирования на первой стадии, что приводит к накоплению Hcy, повышению уровней SAH и Met и снижению уровней Cth и Cys. Поскольку клинические данные об этих продуктах нарушенного метаболизма Met, рассмотренные здесь, демонстрируют, что повышенный Hcy (чаще всего измеряемый клинически как tHcy в плазме) наиболее сильно вовлечен в патофизиологию CBSDH.
[0038] Уровни Hcy, превышающие нормальные, модифицируют сульфгидрильные группы в белках, препятствуя правильному сшиванию белков и приводя к структурным аномалиям во многих системах организма. Повышенные уровни Hcy также нарушают внутриклеточную передачу сигналов, что приводит к нарушению функции эндотелия и, в конечном счете, к тромбоэмболиям и сердечнососудистым заболеваниям. При CBSDH накопление Hcy приводит к проявлениям, связанным со зрительной, костной, сердечнососудистой системами, и психологическим проявлениям.
[0039] Иногда диагноз CBSDH подтверждают с помощью молекулярно-генетического исследования гена CBS (смотрите Sacharow et al. Homocystinuria Caused by Cystathionine Beta-Synthase Deficiency. In: Adam MP, Ardinger HH, Pagon RA, Wallace SE, Bean LJH, Mefford HC, et al, editors. GeneReviewsTM [Интернет]. Seattle (WA): University of Washington, Seattle; 1993-2017, который полностью включен таким образом посредством ссылки). Существующие подходы к скринингу обычно не позволяют выявить новорожденных с меньшим дефицитом CBS и выявляют только меньшинство пациентов с более тяжелой CBSDH (смотрите Huemer et al. J Inherit Metab Dis. 2015 Nov; 38(6):1007-19; Yap, Orphanet Encyclopedia [периодическое издание онлайн]. 2005, pages 1-13; Schiff et al. Neuropediatrics. 2012 Dec; 43(6):295-304).
[0040] Предпочтительным измерением для определения уровней Hcy в клинических образцах является tHcy, который включает восстановленный Hcy, а также Hcy, связанный с белком, или в форме дисульфидов. Нормальные уровни tHcy варьируются в зависимости от возраста, пола и состояния питания, но, как правило, находятся в диапазоне от 4,5 до 11 мкМ (стандартном диапазоне QUEST DIAGNOSTICS™). Многие пациенты с CBSDH имеют тяжелую гипергомоцистинурию с уровнями общего tHcy, превышающими 100 мкМ, тогда как у других наблюдаются повышения от легкого до уровня, превышающего норму в несколько раз (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan;40(1):49-74, который полностью включен таким образом посредством ссылки). Уровни tHcy сильно коррелируют с тяжестью заболевания (смотрите Yap et al. J Inherit Metab Dis 1998; 21: 738-47).
[0041] Исследования показали, что снижение уровней Hcy у пациентов с CBSDH коррелирует с менее тяжелыми проявлениями клинических симптомов (смотрите Yap et al. J Inherit Metab Dis 1998; 21: 738-47; Yap et al. Arterioscler Thromb Vasc Biol. 2001 Dec;21(12):2080-5; оба из которых включены таким образом сюда посредством ссылки). Пути, через которые уровни гомоцистеина вызывают повреждение этих систем, описаны в нескольких местах (смотрите Ajith et al. Clin Chim Acta 2015; 450:316-321; Behera et al. J Cell Physiol 99999:1-6, 2016; Saha et al. FASEB J 2016; 30:441-456; которые полностью включены таким образом посредством ссылки) и привели к исследованиям, изучающим роль Hcy в общей популяции, которые выявили значительную патогенную роль Hcy в заболевании.
[0042] Одной из целей лечения описанной здесь готовой лекарственной формой является увеличение активности фермента CBS в кровотоке, что приводит к увеличению контроля метаболизма, тем самым уменьшая клинические проявления заболевания и замедляя или предотвращая дальнейшее ухудшение. Высокомолекулярные соединения, такие как ферменты, обладают ограниченной способностью к проникновению в ткани и поэтому в основном присутствуют в плазме. Эти белки, как правило, сохраняются в кровотоке в течение короткого периода времени, поскольку они удаляются из кровотока с помощью нескольких механизмов (смотрите Vugmeyster et al. World J Biol Chem. 2012; 3(4):73-92, который полностью включен таким образом посредством ссылки). В идеале введенная CBS должна поддерживать высокую активность в плазме в течение времени, достаточного для оказания устойчивого эффекта на метаболизм серосодержащей аминокислоты. Эта цель может быть достигнута путем ПЭГилирования, добавления фрагментов ПЭГ на поверхность белка. ПЭГилирование белков является стратегией, которая получила широкое признание и, как было показано, сводит к минимуму протеолиз, иммунный ответ и антигенность при одновременном повышении стабильности и размера белка и уменьшении удаления почками (смотрите Kang et al. 2009; 14(2):363-380, который полностью включен таким образом посредством ссылки). Описанная здесь готовая лекарственная форма представляет собой ПЭГилированный фермент htCBS C15S, составленный для введения субъекту и предназначенный для подвергания длительному системному воздействию.
А. Клинические проявления гомоцистинурии
[0043] Имеются убедительные доказательства, указывающие на причинно-следственную связь между повышениями уровней tHcy и негативными клиническими последствия в четырех системах, обычно поражаемых у пациентов с CBSDH (зрительной, костной, сердечнососудистой и нервной системах). Эти данные дополнены, кроме того, исследованиями в общей популяции, демонстрирующими сильную связь между умеренно повышенными уровнями tHcy и отрицательными результатами.
1. Глаза
[0044] Поражающие глаза патологии могут быть ранним клиническим признаком CBSDH. У многих индивидуумов развивается смещение хрусталика глаза от центра глазного яблока (эктопия хрусталика). У пораженных индивидуумов также обычно развивается тяжелая миопия (миопия или близорукость) и иридодонез (дрожание окрашенной части глаза). Эктопия хрусталика и миопия обычно развиваются после первого года жизни, а у не подвергнутых лечению индивидуумов - до десятилетнего возраста (смотрите Mudd et al. Am J Hum Genet 1985; 37: 1-31, который полностью включен таким образом посредством ссылки). Другие патологии глаз, которые встречаются реже, включают катаракту, дегенерацию зрительного нерва и глаукому. У некоторых индивидуумов может быть отслоение сетчатки, что может вызвать нечеткость зрения или появление «мушек» в поле зрения (смотрите Burke et al. Br J Ophthalmol, 1989; 73(6): 427-31, который полностью включен таким образом посредством ссылки).
[0045] Повышенные уровни Hcy являются сильным и независимым фактором риска развития осложнений на зрительную систему, в частности смещения хрусталика, у пациентов с CBSDH и в общей популяции (смотрите Mudd et al. Am J Hum Genet 1985; 37: 1-31; Ajith et al., Clin Chim Acta 2015; 450:316-321; Mulvihill et al. J AAPOS 2001; 5:311-315, которые полностью включены таким образом посредством ссылки). Даже при назначении фармакологических вмешательств и диетотерапий у большинства пациентов с CBSDH в конечном итоге возникают осложнения на зрительную систему. Было замечено, что снижение уровней Hcy задерживает и, возможно, предотвращает смещение хрусталика у пациентов с CBSDH (смотрите Yap et al. J Inherit Metab Dis 1998; 21: 738-47, который полностью включен таким образом посредством ссылки).
2. Центральная нервная система
[0046] Задержка развития и проблемы с обучением, такие как умственная отсталость, также могут быть ранними признаками CBSDH, возникающей в возрасте от одного до трех лет (смотрите Screening, Technology and Research in Genetics (STAR-G) Project. 2016. Homocystinuria. Доступен на сайте: newbornscreening.info; National Institutes of Health (NIH), US National Library of Medicine, Genetics Home Reference. Homocystinuria. 2016. ghr.nlm.nih.gov; которые полностью включены таким образом посредством ссылки). Сообщается, что показатель умственного развития (IQ) у индивидуумов с CBSDH колеблется от 10 до 138. Пациенты с самыми высокими уровнями tHcy с большей вероятностью будут иметь более низкий IQ (со средним значением IQ=57 при отсутствии лечения) по сравнению с менее тяжелыми пациентами (со средним значением IQ=79) (смотрите Sacharow et al., Homocystinuria Caused by Cystathionine Beta-Synthase Deficiency. In: Adam MP, Ardinger HH, Pagon RA, Wallace SE, Bean LJH, Mefford HC, et al, editors. GeneReviewsTM [Интернет]. Seattle (WA): University of Washington, Seattle; 1993-2017, который полностью включен таким образом посредством ссылки).
[0047] Судороги возникают у приблизительно 20% не подвергнутых лечению индивидуумов с CBSDH (смотрите Mudd et al. Am J Hum Genet 1985; 37: 1-31, который полностью включен таким образом посредством ссылки). У многих индивидуумов имеются психические проблемы, в том числе расстройство личности, тревога, депрессия, обсессивно-компульсивное поведение и психотические эпизоды (смотрите Sacharow et al. 2017). Также могут встречаться экстрапирамидальные признаки, такие как дистония (смотрите Screening, Technology and Research in Genetics (STAR-G) Project. 2016. Homocystinuria. Доступен на сайте: newbornscreening.info, который полностью включен таким образом посредством ссылки).
[0048] Исследования показали, что ранние снижения уровней Hcy, вызванные диетой с низким содержанием Met, добавками фолиевой кислоты/витамина группы B и/или терапией с использованием пиридоксина и бетаина, могут задержать, а иногда предотвратить или обратить вспять прогрессирование различных неврологических расстройств и обеспечить развитие нормального IQ у пациентов с CBSDH (смотрите El Bashir et al. JIMD Rep 2015; 21:89-95; Yap et al. J Inherit Metab Dis 2001; 24:437-447; которые полностью включены таким образом посредством ссылки). Связи между повышенными уровнями Hcy и связанными с центральной нервной системой (ЦНС) симптомами, включающими умственную отсталость, нейродегенеративные заболевания, судороги, дистонию, психоз, когнитивные расстройства, деменцию и депрессию, в полной мере подтверждены документами у пациентов с CBSDH и в общей популяции (смотрите Abbott et al. Am J Med Genet 1987; 26:959-969; Schimke et al. JAMA 1965; 193:711-719; Herrmann et al. Clin Chem Lab Med 2011; 49:435-441; которые полностью включены таким образом посредством ссылки).
3. Костная система
[0049] У индивидуумов с CBSDH часто развивается ряд аномалий скелета. Пораженные индивидуумы являются часто высокими и стройными с «марфаноидным» габитусом, который включает истончение и удлинение длинных костей (долихостеномелию), колени, которые согнуты внутрь, так что они соприкасаются, когда ноги являются прямыми («вывернутые внутрь колени» или Х-образное искривление ног), сильно изогнутую стопу (полую стопу), аномальное боковое искривление позвоночника (сколиоз), аномально выпирающую грудную клетку (килевидную грудь) или аномально запавшую грудную клетку (впалую грудь). К подростковому возрасту у 50% индивидуумов проявляются признаки остеопороза (смотрите Screening, Technology and Research in Genetics (STAR-G) Project. 2016. Homocystinuria. Доступен на сайте: newbornscreening.info, который полностью включен таким образом посредством ссылки). CBSDH связана с повышенным риском переломов при остеопорозе, что частично может быть связано с низкой минеральной плотностью костей (смотрите Mudd et al. Am J Hum Genet 1985; 37: 1-31; Weber et al. Mol Genet Metab 2016; 117:351-354; которые полностью включены таким образом посредством ссылки).
[0050] В исследовании на 25 ирландских пациентах с CBSDH, наблюдаемых в течение 25 лет, было обнаружено, что риск аномалий скелета был значительно ниже у пациентов в случае удовлетворительного соблюдения схемы понижающего уровень Hcy лечения по сравнению с пациентами, не соблюдающими ее (смотрите Yap et al. J Inherit Metab Dis 1998; 21:738-47, который полностью включен таким образом посредством ссылки).
4. Сердечнососудистая система
[0051] Взаимосвязь между CBSDH и сердечнососудистым заболеванием была впервые продемонстрирована в 1985 году в эпидемиологическом исследовании на пациентах со умеренно-сильно повышенными уровнями Hcy из-за гомозиготной CBSDH (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31, который полностью включен таким образом посредством ссылки). Тромбоэмболия является самым серьезным, часто опасным для жизни осложнением CBSDH и может поражать любой сосуд. Она является основной причиной заболеваемости и ранней смерти у пациентов с CBSDH (смотрите Yap et al. Arterioscler Thromb Vase Biol. 2001 Dec; 21(12):2080-5, который полностью включен таким образом посредством ссылки).
[0052] Риск случаев тромбоэмболии составлял приблизительно 25% в возрасте 16 лет и 50% в возрасте 29 лет. В нескольких сообщениях описывается, как понижающие уровни tHcy лечения, значительно снижают частоту сердечнососудистых событий, основной причины заболеваемости, у пациентов с CBSDH (смотрите Wilcken et al. J Inherit Metab Dis 1997; 20:295-300; Yap et al. Arterioscler Thromb Vasc Biol. 2001 Dec; 21(12):2080-5, которые полностью включены таким образом посредством ссылки). С тех пор ряд других исследований продемонстрировал повышенный риск сердечнососудистых событий, в частности тромбоза вен, у пациентов с CBSDH (смотрите Kelly et al. Neurology 2003; 60:275-279; Magner et al. J Inherit Metab Dis 2011; 34:33-37; которые полностью включены таким образом посредством ссылки).
5. Дополнительные проявления
[0053] У пациентов с CBSDH сообщалось о нескольких дополнительных проявлениях, включающих чрезвычайно тонкую, хрупкую кожу, ломкие волосы, изменение цвета кожи (гипопигментацию) и сыпь на щеках (румянец скул), хотя они встречаются реже. У некоторых индивидуумов могут развиться жировые изменения в печени, выпячивание части кишечника через разрыв брюшной стенки (паховая грыжа) или воспаление поджелудочной железы. Аномальное искривление позвоночника, обращенное выпуклостью назад, (кифоз) и коллапс легкого (спонтанный пневмоторакс) также были зарегистрированы у индивидуумов с CBSDH (смотрите Yap; Orphanet Encyclopedia [периодическое издание онлайн], 2005, pages 1-13, который полностью включен таким образом посредством ссылки).
[0054] Подводя итог, диета с ограничением метионина (MRD) сама по себе является эффективной для коррекции множества симптомов HCU, несмотря на то, что не удается снизить концентрацию Hcy в плазме ниже рекомендуемого уровня, что приводит к повышению тревоги и снижению минерализации костной ткани. С другой стороны, описанная здесь ферментотерапия с использованием 20NHS PEG-CBS снижала концентрации Hcy в плазме ниже примерного порогового уровня, составляющего 100 мкМ, и корректировала все наблюдаемые симптомы HCU. Кроме того, 20NHS PEG-CBS сохраняет свою эффективность при ограничении Met, обеспечивая полностью нормализованный биохимический профиль в плазме. При экстраполяции этих данных на являющихся людьми пациентов результаты авторов настоящего изобретения доказывают, что 20NHS PEG-CBS в качестве единственной пожизненной терапии может быть эффективной для профилактики и коррекции клинических симптомов HCU. Кроме того, лечение 20NHS PEG-CBS должно позволить устранить ограничения Met/ограничения в диете и, таким образом, существенно улучшить качество жизни пациентов с HCU и их семей.
II. КОМПОЗИЦИИ
А. Нативный фермент CBS человека
[0055] Полноразмерный нативный фермент CBS представляет собой тетрамер с четырьмя идентичными мономерами, в котором каждый мономер (размером 63 кДа) организован в три функциональных домена. Первый домен представляет собой N-концевую область из приблизительно 70 аминокислот, которая связывает гем и, как полагают, участвует в ответе на изменения окислительно-восстановительного состояния и/или сворачивании фермента. Второй представляет собой центральный домен, который содержит каталитическое ядро и демонстрирует укладку зависимых от PLP (пиридоксаль-5'-фосфата) ферментов семейства II типа. PLP кофермента глубоко спрятан в расселине между N- и C-концевыми доменами. Третья область представляет собой С-концевой регуляторный домен, состоящий из тандемной пары мотивов CBS, которые при связывании с S-аденозилметионином (SAM) активируют фермент. Удаление регуляторной области приводит к образованию конститутивно активного фермента (смотрите Miles et al. J Biol Chem. 2004 Jul 16; 279(29):29871-4, который полностью включен таким образом посредством ссылки).
[0056] Зависимая от пиридоксаль-5'-фосфата (PLP) укладка фермента CBS содержит гемовую группу. Она катализирует PLP-зависимую реакцию бета-замещения, в которой она конденсирует L-гомоцистеин с L-серином с образованием L-цистатионина. Она аллостерически регулируется при связывании S-аденозил-L-метионина (Ado-Met) с С-концевыми регуляторными доменами, что приводит к конформационной перестройке этих доменов и снятию аутоингибиторного блока. Активация CBS также может быть достигнута путем полного удаления С-концевых регуляторных доменов с образованием конститутивно активной димерной формы фермента (смотрите Miles et al. J Biol Chem. 2004 Jul 16; 279(29):29871-4; Ereno-Orbea et al. Proc Natl Acad Sci USA 111(37), E3845-3852 (2014); каждый из которых полностью включен таким образом посредством ссылки).
[0057] Активное вещество в описанной здесь готовой лекарственной форме представляет собой рекомбинантный усеченный белок CBS человека с заменой цистеина на серин в аминокислотном положении 15 белка (htCBS C15S) по сравнению с аминокислотной последовательностью SEQ ID NO:2 в списке последовательностей настоящего изобретения и SEQ ID NO:2 из WO 2017/083327 (которая полностью включена таким образом посредством ссылки), которая представляет собой нативный белок CBS, который был модифицирован путем добавления полиэтиленгликоля (ПЭГ). Фермент также известен как htCBS C15S. В некоторых вариантах осуществления лекарственное вещество htCBS C15S имеет аминокислотную последовательность SEQ ID NO:1.
[0058] Эта форма фермента обладает высокой склонностью к агрегации, что создает серьезные ограничения для производства и получения CBS человека (hCBS). Была сконструирована ПЭГилированная htCBS C15S (в том числе «20NHS PEG-CBS», определенная здесь), которая образует димеры, а не тетрамеры, которые менее подвержены агрегации. Высокомолекулярные соединения, такие как ферменты, удаляются из кровотока при деградации путем протеолиза и с помощью различных механизмов клиренса (смотрите Vugmeyster et al. World J Biol Chem. 2012; 3(4):73-92, который полностью включен таким образом посредством ссылки). Известно, что ПЭГилирование сводит к минимуму протеолиз и иммуногенность при одновременном увеличении стабильности белка и снижении удаления почками (смотрите Kang et al. 2009; 14(2):363-380, который полностью включен таким образом посредством ссылки). Эти структурные модификации делают описанную здесь готовую лекарственную форму, содержащую ПЭГилированную htCBS C15S, более подходящим кандидатом, чем нативная hCBS, в качестве ферментотерапии (ET) для CBSDH.
[0059] Нативная CBS представляет собой внутриклеточный фермент, и неизвестно о существовании какого-либо механизма для захвата фермента из экстраклеточной среды в его первичное внутриклеточное место приложения действия, тогда как ПЭГилированная htCBS C15S действует экстраклеточно. В отличие от нативной эндогенной CBS, ПЭГилированная htCBS C15S корректирует метаболические нарушения, действуя непосредственно в кровотоке и опосредованно в тканях, и делает это без необходимости S-аденозилметионина (SAM) для активации. Нативный фермент hCBS активируется в клетках при связывании SAM с его С-концевым регуляторным доменом. Однако уровни SAM в кровотоке как у пациентов, так и у здоровых индивидуумов намного ниже уровней, необходимых для активации CBS (смотрите Stabler et al. Metabolism, 2002. 51(8): p. 981-8, который полностью включен таким образом посредством ссылки). Поэтому введение нативной CBS в кровоток было бы неэффективным, так как CBS не активировалась бы. ПЭГилированная htCBS C15S, хотя она остается в кровотоке и не проникает в клетки, была сконструирована таким образом, чтобы обойти необходимость активации с помощью SAM, путем удаления С-концевого регуляторного домена CBS, что сделало фермент конститутивно активным.
B. Ферментотерапия (ET)
[0060] ПЭГилированная htCBS C15S представляет собой ПЭГилированную, усеченную hCBS с заменой цистеина на серин в положении 15 для ET для лечения CBSDH. Эта модификация оптимизирует фермент для образования димеров, а не тетрамеров, и делает его конститутивно активным.
[0061] ПЭГилированная htCBS C15S пополняет недостаточную активность CBS, тем самым снижая уровни гомоцистеина (Hcy) и метионина (Met) в плазме, моче и тканях, повышая уровни цистатионина (Cth) и нормализуя уровни цистеина (Cys) у пациентов с CBSDH. Снижение уровней общего Hcy (tHcy) является текущей целью лечения (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan; 40(l):49-74, который полностью включен таким образом посредством ссылки) и сильно коррелирует с уменьшением клинических последствий (для здоровья зрительной, костной, сердечнососудистой и нервной систем) (Yap; Orphanet Encyclopedia [периодическое издание онлайн] 2005, pages 1-13, который полностью включен таким образом посредством ссылки).
[0062] ПЭГилированная htCBS C15S представляет собой рекомбинантную форму нативного фермента CBS человека, которая продуцируется бактериями E. coli. Последовательность ДНК нативной CBS человека (SEQ ID NO:3 в списке последовательностей настоящего изобретения и SEQ ID NO:1 из WO 2017/083327, которая полностью включена таким образом посредством ссылки) была генетически модифицирована для удаления С-концевого регуляторного участка (аминокислот 414-551) (SEQ ID NO:4 в списке последовательностей настоящего изобретения и SEQ ID NO:3 из WO 2017/083327), образуя усеченную CBS человека. Последовательность ДНК для усеченной CBS человека была, кроме того, модифицирована для введения точечной мутации Т→А в положение 43 кодирующей области ДНК, что привело к замене цистеина на серин в положении 15 транслируемого белка, в результате чего была создана усеченная CBS C15S человека (htCBS C15S) (SEQ ID NO:5 в списке последовательностей настоящего изобретения и SEQ ID NO:13 из WO 2017/083327). Эта замена уменьшает агрегацию и обеспечивает постоянство от партии к партии по сравнению с нативной hCBS.
[0063] Фермент модифицируется, кроме того, в бактериях E. coli во время экспрессии, что приводит к удалению первого Met из белка, как показано в SEQ ID NO:1. После очистки фермент htCBS C15S дополнительно модифицируют путем ПЭГилирования с использованием функционализированных с помощью сложного эфира N-гидроксилсукцинимида фрагментов ПЭГ с М.м. 20 кДа, которые реагируют с первичными аминами на поверхности белка. В среднем приблизительно 5,1 молекулы ПЭГ присоединяются к каждой мономерной единице фермента, образуя гетерогенный димерный продукт со средней молекулярной массой, равной 290 кДа.
C. ПЭГилирование htCBS C15S с получением 20NHS PEG-CBS
[0064] ME-200GS (также называемый метокси-PEG-CO(CH2)3COO-NHS) используется здесь для ПЭГилирования htCBS C15S:

ME-200GS имеет молекулярную массу, равную 290 кДа, и химическое название α-сукцинимидилоксиглутарил-ω-метокси, полиоксиэтилен. ME-200GS нацелен на свободные амины на поверхности htCBS C15S. Между ПЭГ и остатком лизина в htCBS C15S образуется амидная связь. Полученная молекула упоминается в настоящем описании как «20NHS PEG-CBS» и представляет собой ПЭГилированную молекулу цистатионин-бета-синтазы человека, которая является усеченной и имеет мутацию C15S, как представлено в SEQ ID NO:1.
[0065] Фильтрация поперечным потоком (TFF) с отсечением по молекулярной массе=100 кДа и замена буфера в объемном соотношении 1:15 используется для удаления свободного ПЭГ и других примесей, связанных с ПЭГилированием, а впоследствии используется для приготовления против буфера PBS. Ожидается, что все вещества, связанные с процессом, в том числе ионы аммония и другие, имидазол, Triton X-100 и группы NHS, освобождаемые из ПЭГ во время ПЭГилирования, будут присутствовать в следовых количествах после 2 циклов стадии диафильтрации TFF с большим отсечением.
[0066] PEG ME-200GS производится корпорацией NOF в соответствии с требованиями cGMP в соответствии с представленной на фиг. 1 схемой процесса. Все сырье, используемое при производстве продукта ME-200GS, имеет синтетическую или неорганическую природу. Примеси, которые потенциально могут присутствовать в сырье PEG ME-200GS, представляют собой небольшие молекулы.
D. Посттрансляционные модификации
[0067] Для посттрансляционных модификаций могут потребоваться дополнительные биотехнологические стадии для разделения модифицированных и немодифицированных полипептидов, что увеличивает затраты и снижает эффективность производства биологических препаратов. Соответственно, в некоторых вариантах осуществления продукцию полипептидного агента в клетке усиливают путем модуляции экспрессии целевого гена, кодирующего белок, который влияет на посттрансляционную модификацию. В дополнительных вариантах осуществления продукцию биологических агентов повышают путем модуляции экспрессии первого целевого гена, кодирующего белок, который влияет на первую посттрансляционную модификацию, и модуляции экспрессии второго целевого гена, кодирующего белок, который влияет на вторую посттрансляционную модификацию.
[0068] Кроме того, экспрессируемые в прокариотических или эукариотических клетках белки могут подвергаться нескольким посттрансляционным модификациям, которые могут нарушать продукцию и/или структуру, биологическую активность, стабильность, гомогенность и/или другие свойства биологического продукта. Многие из этих модификаций происходят спонтанно во время роста клеток и экспрессии полипептидов и могут происходить в нескольких сайтах, включая остов пептида, боковые цепи аминокислот и N-концы и/или C-концы определенного полипептида. Кроме того, определенный полипептид может содержать несколько различных типов модификаций. Например, белки, экспрессируемые в бактериальных клетках, таких как E. coli, могут подвергаться ацетилированию, удалению гистонов, карбоксилированию и/или дезамидированию (смотрите Yang et al., PNAS 111 (52) E5633-E5642 (2014), который полностью включен таким образом посредством ссылки). Например, белки, экспрессируемые в клетках птиц и млекопитающих, таких как клетки яичника китайского хомячка (СНО), могут подвергаться ацетилированию, карбоксилированию, гамма-карбоксилированию, удалению гистонов, дезамидированию, циклизации N-концевого глутамина и дезамидированию, а также дезамидированию аспарагина.
[0069] В некоторых вариантах осуществления продукцию белка усиливают путем модуляции экспрессии целевого гена, который кодирует белок, участвующий в дезамидировании белка. Белки могут быть подвергнуты дезамидированию несколькими путями, включая циклизацию и дезамидирование N-концевого глутамина и дезамидирование аспарагина. Таким образом, в одном варианте осуществления белок, участвующий в дезамидировании белка, представляет собой амидогидролазу для N-концевого аспарагина. Дезаминирование белков может привести к изменению структурных свойств, снижению эффективности, снижению биологической активности, снижению эффективности, увеличению иммуногенности и/или другим нежелательным свойствам и может быть определено несколькими способами, включающими, но без ограничения этим, разделение белков на основе заряда с помощью, например, ионообменной хроматографии, HPLC (ВЭЖХ), изоэлектрического фокусирования, капиллярного электрофореза, электрофореза в нативном геле, хроматографии с обращенной фазой, хроматографии на основе гидрофобного взаимодействия, аффинной хроматографии, масс-спектрометрии или применения L-изоаспартилметилтрансферазы.
[0070] В некоторых вариантах осуществления белок, влияющий на секрецию белка, представляет собой молекулярный шаперон, выбранный из группы, состоящей из: Hsp40, HSP47 (также называемого ингибитором серпинпептидазы, клада H; белка теплового шока 47), HSP60, Hsp70, HSP90, HSP100, дисульфидизомеразы белков, пептидилпролилизомеразы, калнексина, Erp57 (члена 3 семейства А дисульфидизомераз белков) и BAG 1. В некоторых вариантах осуществления белок, который влияет на секрецию белка, выбран из группы, состоящей из γ-секретазы, p115, белка частицы, распознающей сигнал, (SRP), секретина и киназы (например, MEK).
[0071] Предусматривается, что дальнейшая оптимизация может быть достигнута путем систематического либо добавления, либо удаления нуклеотидов для создания более длинных или более коротких последовательностей и тестирования этих последовательностей, полученных путем передвижения окна более длинного или более короткого размера вверх или вниз по целевой РНК из этой точки. Сочетание этого подхода для создания новых мишеней-кандидатов с тестированием на эффективность эффекторных молекул РНК на основе этих последовательностей-мишеней в анализе ингибирования, известном в данной области техники или описанным здесь, может привести к дальнейшему увеличению эффективности ингибирования. Кроме того, такие оптимизированные последовательности могут быть скорректированы, например, путем введения модифицированных нуклеотидов, как описано здесь документе или известно в данной области техники, путем добавления или изменения выступающего конца или с помощью других модификаций, известных в данной области техники и/или обсуждаемых здесь, для дальнейшей оптимизации молекулы (например, увеличения стабильности в сыворотке или времени полужизни в кровотоке, повышения термостабильность, увеличения трансмембранной доставки, нацеливания на определенное место или тип клеток, увеличения взаимодействия с ферментами пути сайленсинга, увеличения высвобождения из эндосом и т.д.) в качестве ингибитора экспрессии.
E. Стабильность
[0072] Лекарственное вещество или готовая лекарственная форма является стабильным при различных температурах и условиях хранения. В некоторых вариантах осуществления лекарственное вещество или готовая лекарственная форма является стабильным(ой) при хранении при -65°С и -20°С. В качестве альтернативы, лекарственное вещество или готовая лекарственная форма может быть стабильным(ой) при хранении при температуре в диапазоне от приблизительно 2°С до приблизительно 8°С. Альтернативно, лекарственное вещество или готовая лекарственная форма может быть стабильным(ой) при хранении при температуре в диапазоне 25°С±2°С. Например, лекарственное вещество или лекарственный препарат остается стабильным(ой) при температуре от 20°С до 25°С. В некоторых вариантах осуществления лекарственное вещество или готовая лекарственная форма является стабильным(ой) в восстанавливающих условиях. В некоторых вариантах осуществления лекарственное вещество или готовая лекарственная форма является стабильным(ой) в невосстанавливающих условиях. В некоторых вариантах осуществления лекарственное вещество или готовая лекарственная форма остается стабильным(ой) в течение по крайней мере 2 дней, по крайней мере 7 дней, по крайней мере 1 месяца, по крайней мере 2 месяцев, по крайней мере 3 месяцев, по крайней мере 6 месяцев или по крайней мере 12 месяцев. Например, лекарственное вещество или готовая лекарственная форма остается стабильным(ой) при хранении в течение приблизительно 2 дней. Например, лекарственное вещество или готовая лекарственная форма остается стабильным(ой) при хранении в течение приблизительно 7 дней. Например, лекарственное вещество или готовая лекарственная форма остается стабильным(ой) при хранении в течение приблизительно 1 месяца. Например, лекарственное вещество или готовая лекарственная форма остается стабильным(ой) при хранении в течение приблизительно 2 месяцев. Например, лекарственное вещество или готовая лекарственная форма остается стабильным(ой) при хранении в течение приблизительно 3 месяцев. Например, лекарственное вещество или готовая лекарственная форма остается стабильным(ой) при хранении в течение приблизительно 6 месяцев. Например, лекарственное вещество или готовая лекарственная форма остается стабильным(ой) при хранении в течение приблизительно 12 месяцев. Например, лекарственное вещество или готовая лекарственная форма остается стабильным(ой) при хранении в течение приблизительно 18 месяцев.
[0073] В некоторых вариантах осуществления лекарственное вещество или готовая лекарственная форма остается стабильным(ой) при хранении при -65°С вплоть до 18 месяцев. В некоторых вариантах осуществления лекарственное вещество или готовая лекарственная форма остается стабильным(ой) при хранении при температуре от приблизительно 2°С до приблизительно 8°С вплоть до 3 месяцев. В некоторых вариантах осуществления лекарственное вещество или готовая лекарственная форма остается стабильным(ой) при хранении при 25°С±2°С вплоть до 1 месяца.
[0074] В некоторых вариантах осуществления лекарственное вещество или готовая лекарственная форма остается стабильным(ой) в течение по крайней мере 3 циклов замораживания и оттаивания. В некоторых вариантах осуществления лекарственное вещество или готовая лекарственная форма остается стабильным(ой) вплоть до 6 циклов замораживания и оттаивания. Например, лекарственное вещество или готовая лекарственная форма остается стабильным(ой) в течение 5 циклов замораживания и оттаивания. В некоторых вариантах осуществления готовая лекарственная форма является стабильной после выталкивания из шприца.
III ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ
[0075] Описанная здесь готовая лекарственная форма, содержащая ПЭГилированную htCBS C15S, предназначена для восстановления контроля над метаболизмом и уменьшение интенсивности клинических проявлений заболевания путем снижения уровней гомоцистеина и нормализации уровней цистеина у пациентов с CBSDH. htCBS C15S производится с помощью рекомбинантной технологии с использованием E. coli BL21 (DE3), и ее готовят в виде стерильной готовой лекарственной формы в забуференном фосфатом солевом растворе. Готовая лекарственная форма предназначена для введения путем подкожной (SC) инъекции.
[0076] Активность ПЭГилированной htCBS C15S в кровотоке также улучшала или даже полностью нормализовала профили метаболитов в тканях (смотрите WO 2017/083327, которая полностью включена таким образом посредством ссылки). Следовательно, готовая лекарственная форма необязательно должна доставляться в ее природную внутриклеточную среду.
[0077] Готовая лекарственная форма уменьшает накопление токсичного Hcy в кровотоке, моче и тканях пациентов с CBSDH; нормализует уровни Cys в кровотоке и тканях; повышает уровни Cth в кровотоке и тканях; и/или предотвращает, задерживает и/или реверсирует начало проявлений CBSDH. Готовая лекарственная форма обеспечивает по крайней мере одно из этих преимуществ, позволяя пациентам получать удовольствие от нормального питания. На самом деле, повышение активности Cth даже в случае стандартного рациона (например, 4,0 г/кг МЕТ), как было замечено, свидетельствует о повышенной активности готовой лекарственной формы и/или уменьшенном удалении почками.
[0078] Лекарственное вещество 20NHS PEG-CBS готовили в концентрации от 20 до 30 мг/мл или приблизительно 25 мг/мл в забуференном фосфатом солевом растворе (PBS), содержащем гидрофосфат натрия (дигидрат) (11,4 мМ), хлорид натрия (137 мМ), хлорид калия (2,7 мМ) и дигидроортофосфат калия (1,98 мМ), приготовленном с использованием воды для инъекции (WFI). Лекарственное вещество легко растворялось в водном растворе.
[0079] Молекулярная масса лекарственного вещества, рассчитанная по усредненной для каждого изотопа молекулярной массе исходя из SEC/UV/MS, составляет 45,290 кДа для мономера и 90,58 кДа для димера.
[0080] Все партии представляли собой прозрачную жидкость, практически не содержащую видимых частиц, темно-красного цвета. Кроме того, предоставленные результаты электрофореза в SDS-ПААГ, проведенного как в восстанавливающих, так и в невосстанавливающих условиях, и результаты Вестерн-блоттинга соответствовали друг другу для каждой партии. Используя каждый из этих способов, была продемонстрирована характерная, однородная и постоянная картина варианта ПЭГилирования. Сопутствующие лекарственные средства, в том числе антикоагулянты, добавки витаминов и минеральные добавки, бетаин, антидепрессанты, также можно комбинировать с описанной здесь готовой лекарственной формой для повышения эффективности фармацевтической композиции.
IV. ПРЕПАРАТЫ
[0081] Для вышеупомянутых терапевтических применений вводимая доза будет варьироваться в зависимости от используемого соединения, способа введения, желаемого лечения и указанного нарушения. Например, суточная доза соединения по настоящему изобретению при вдыхании может находиться в диапазоне от 0,05 микрограммов на килограмм веса тела (мкг/кг) до 100 микрограммов на килограмм веса тела (мкг/кг). Альтернативно, если соединение вводят перорально, то суточная доза соединения по настоящему изобретению может находиться в диапазоне от 0,01 микрограмма на килограмм веса тела (мкг/кг) до 100 миллиграммов на килограмм веса тела (мг/кг).
[0082] Белок, имеющий аминокислотную последовательность SEQ ID NO:1, который ПЭГилирован с образованием лекарственного вещества, описанного здесь, может использоваться сам по себе, но, как правило, его вводят в форме фармацевтической композиции в сочетании с фармацевтически приемлемым адъювантом, разбавителем или носителем. Таким образом, настоящим изобретением обеспечивается, кроме того, фармацевтическая композиция, содержащая описанное здесь лекарственное вещество в сочетании с фармацевтически приемлемым адъювантом, разбавителем или носителем.
[0083] Фармацевтически приемлемые адъюванты, разбавители или носители, которые могут использоваться в фармацевтических композициях по настоящему изобретению, представляют собой те, которые обычно используются в области приготовления фармацевтических препаратов, и включают, но без ограничения этим, сахара, сахарные спирты, крахмалы, иониты, оксид алюминия, стеарат алюминия, лецитин, сывороточные белки, такие как сывороточный альбумин человека, буферные вещества, такие как фосфаты, глицерин, сорбиновую кислоту, сорбат калия, смеси неполных глицеридов растительных насыщенных жирных кислот, воду, соли или электролиты, такие как сульфат протамина, гидрофосфат натрия, дигидроортофосфат калия, хлорид натрия, соли цинка, коллоидный диоксид кремния, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы, полиэтиленгликоль, карбоксиметилцеллюлозу натрия, полиакрилаты, воски, блоксополимеры полиэтилен-полиоксипропилен, полиэтиленгликоль и шерстный жир (ланолин).
[0084] Фармацевтические композиции по настоящему изобретению могут вводиться перорально, парентерально, с помощью ингаляционного спрея, ректально, назально, трансбуккально, вагинально или через имплантируемый резервуар. В одном варианте осуществления фармацевтическую композицию можно вводить перорально. В одном варианте осуществления фармацевтическую композицию можно вводить подкожно. Фармацевтические композиции по настоящему изобретению могут содержать любые обычные нетоксичные фармацевтически приемлемые адъюванты, разбавители или носители. Используемый здесь термин «парентеральный» включает подкожную, внутрикожную, внутривенную, внутримышечную, интраартикулярную, внутрисуставную, интрастернальную, подоболочечную, внутриочаговую и внутричерепную инъекцию или инфузию.
[0085] Фармацевтические композиции могут быть представлены в форме стерильного инъецируемого препарата, например, в виде стерильной водной или масляной суспензии для инъекций. Суспензия может быть приготовлена в соответствии с методами, известными в данной области техники, с использованием подходящих диспергаторов или смачивающих агентов (таких как, например, Tween 80) и суспендирующих агентов. Стерильный инъецируемый препарат может также представлять собой стерильный инъецируемый раствор или суспензию в нетоксичном парентерально приемлемом адъюванте, разбавителе или носителе, например, в виде раствора в 1,3-бутандиоле. В число приемлемых адъювантов, разбавителей и носителей, которые могут использоваться, входят маннит, вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителя или суспендирующей среды обычно используются стерильные нелетучие масла. Для этой цели может использоваться любое мягкое нелетучее масло, в том числе синтетические моно- или диглицериды. Жирные кислоты, такие как олеиновая кислота и ее производные в виде глицеридов, применимы для приготовления препаратов для инъекций, как и натуральные фармацевтически приемлемые масла, такие как оливковое масло или касторовое масло, особенно в случае их полиоксиэтилированных вариантов. Эти масляные растворы или суспензии могут также содержать разбавитель или диспергатор в виде длинноцепочечного спирта.
[0086] Фармацевтические композиции по настоящему изобретению можно вводить перорально в любой лекарственной форме, приемлемой для перорального применения, включая, но без ограничения этим, капсулы, таблетки, порошки, гранулы и водные суспензии и растворы. Эти лекарственные формы готовят в соответствии с методами, хорошо известными в области приготовления фармацевтических препаратов. В случае таблеток для перорального применения обычно используемые носители включают лактозу и кукурузный крахмал. Также, как правило, добавляют смазывающие агенты, такие как стеарат магния. Для перорального введения в форме капсул применимые разбавители включают лактозу и высушенный кукурузный крахмал. При пероральном введении водных суспензий активный ингредиент объединяют с эмульгаторами и суспендирующими агентами. При желании могут быть добавлены определенные подсластители, и/или ароматизаторы, и/или красители.
[0087] Фармацевтические композиции по настоящему изобретению также могут быть приготовлены в форме суппозиториев для ректального введения. Эти композиции могут быть приготовлены путем смешивания активного ингредиента с подходящим нераздражающим наполнителем, который является твердым при комнатной температуре, но жидким при температуре в прямой кишке и, следовательно, будет плавиться в прямой кишке с высвобождением активного ингредиента. Такие материалы включают, но без ограничения этим, какао-масло, пчелиный воск и полиэтиленгликоли.
[0088] Фармацевтические композиции по настоящему изобретению можно вводить с помощью назального аэрозоля или ингаляции. Такие композиции готовят в соответствии с методами, хорошо известными в области приготовления фармацевтических препаратов, и могут быть приготовлены в виде растворов в физиологическом растворе с использованием бензилового спирта или других подходящих консервантов, активаторов абсорбции для увеличения биодоступности, фторуглеродов и/или других известных солюбилизоторов или диспергаторов, известных в данной области техники.
[0089] Фармацевтические композиции, описанные здесь, могут быть представлены в форме для введения через систему кровообращения, как показано в WO 2015/153102, WO 2016/183482 и WO 2018/009838, каждая из которых полностью включена таким образом посредством ссылки. Белок CBS может кодироваться рекомбинантной нуклеиновой кислотой, экспрессируемой энуклеированными гемопоэтическими клетками (EHC), включающими эритроидные или тромбоидные клетки. Например, эритроидными клетками являются эритроциты, эритроциты или ретикулоциты. Например, тромбоидными клетками являются тромбоциты. В некоторых вариантах осуществления кодируемый белок CBS слит с транслируемым заякоренным в мембране полипептидом. В некоторых вариантах осуществления белок CBS локализован на поверхности EHC. Белок CBS может быть расщеплен для активации фермента в экстраклеточном пространстве. Альтернативно, белок CBS, локализованный внутри, может высвобождаться в экстраклеточное пространство при лизисе EHC. Альтернативно, ферментативная мишень в виде белка CBS может проникать в EHC, а затем выходить через мембрану после изменения. В некоторых вариантах осуществления белок CBS имеет аминокислотную последовательность SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:4 или SEQ ID NO:5 в списке последовательностей настоящего изобретения или SEQ ID NO:2, 3, или 13 из WO 2017/083327 (которая полностью включена таким образом посредством ссылки).
[0090] В зависимости от способа введения фармацевтическая композиция будет содержать от 0,05 до 99% (в весовом отношении), конкретнее, от 0,05 до 80% (в весовом отношении), еще конкретнее от 0,10 до 70% (в весовом отношении), и даже более конкретно от 0,10 до 50% (в весовом отношении) активного ингредиента, при этом все проценты по весу относятся к общей композиции.
[0091] Обычные процедуры для выбора и приготовления подходящих фармацевтических препаратов описаны, например, в «Pharmaceutics - The Science of Dosage Form Design», ME Aulton, Churchill Livingstone, 1988, который полностью включен таким образом посредством ссылки.
[0092] В буферный раствор гидрофосфата натрия (дигидрата), хлорида натрия, хлорида калия и дигидроортофосфата калия лекарственное вещество помещают посредством диафильтрации.
[0093] Готовую лекарственную форму готовят в целевой концентрации, составляющей 20-30 мг/мл или приблизительно 25 мг/мл, в PBS (pH=7,4±0,2). Буфер PBS содержит гидрофосфат натрия (дигидрат) (11,4 мМ), хлорид натрия (137 мМ), хлорид калия (2,7 мМ) и дигидроортофосфат калия (1,98 мМ). В таблице 1 представлены детали состава.
[0094] В таблице 2 приведен примерный состав стандартной дозы готовой лекарственной формы, описанной здесь.
[0095] В некоторых вариантах осуществления готовая лекарственная форма составлена для подвергания субъекта воздействию приблизительно 50 мЕд./мкл. Лиофилизированный препарат может использоваться для введения людям после восстановления влагосодержания.
А. Лиофилизация
[0096] Фармацевтические композиции могут быть представлены в виде лиофилизированного препарата. В некоторых вариантах осуществления лиофилизированный препарат содержит лекарственное вещество, буфер и наполнитель. В некоторых вариантах осуществления после восстановления лиофилизированного препарата в подходящем буфере для восстановления, воде или любом другом фармацевтически приемлемом адъюванте, разбавителе или носителе концентрация лекарственного вещества составляет приблизительно 20-30 мг/мл. В некоторых вариантах осуществления концентрация лекарственного вещества составляет приблизительно 20 мг/мл, приблизительно 21 мг/мл, приблизительно 22 мг/мл, приблизительно 23 мг/мл, приблизительно 24 мг/мл, приблизительно 25 мг/мл, приблизительно 26 мг/мл, приблизительно 27 мг/мл, приблизительно 28 мг/мл, приблизительно 29 мг/мл или приблизительно 30 мг/мл. В некоторых вариантах осуществления концентрация лекарственного вещества составляет приблизительно 25,4 мг/мл. В некоторых вариантах осуществления после восстановления лиофилизированного препарата в подходящем буфере для восстановления, воде или любом другом фармацевтически приемлемом адъюванте, разбавителе или носителе буфер представляет собой фосфат калия в концентрации 15 мМ. В некоторых вариантах осуществления наполнитель представляет собой трегалозу в концентрации 8% (в отношении веса к объему). В некоторых вариантах осуществления препарат содержит сахарозу, так что после восстановления лиофилизированного препарата в подходящем буфере для восстановления, воде или фармацевтически приемлемом адъюванте, разбавителе или носителе концентрация сахарозы составляет 5%. В некоторых вариантах осуществления температура начала распада (Tc, on), определенная с помощью микроскопического исследования лиофилизации, составляет -21°C. В некоторых вариантах осуществления препарат имеет pH 7,5.
[0097] В некоторых вариантах осуществления процесс лиофилизации можно проводить за 48 часов или менее без плавления кристаллической структуры осадка (кека). Процесс лиофилизации можно оптимизировать для настройки одного или более из следующих параметров или свойств, таких как, но без ограничения этим, (i) сокращения времени восстановления лиофилизированного препарата (например, менее 1 минуты), (ii) снижения вязкости для допуска получения более концентрированной готовой лекарственной формы, (iii) включения изотонического буфера для минимизации боли у пациентов и/или (iv) уменьшения де-ПЭГилирования.
[0098] Лиофилизированный препарат может быть приготовлен с использованием следующего протокола. За три дня до приготовления препарата лекарственное вещество (хранящееся при -80°C) в концентрации, составляющей 20-30 мг/мл или приблизительно 25 мг/мл, оттаивают в течение 72 часов при 2-8°C в холодильнике. После оттаивания лекарственное вещество гомогенизируют путем осторожного вращения. Диализ проводят в контролируемых условиях при 2-8°C в течение 24 часов. Используют кассеты для диализа с отсечкой 20 кДа, и буфер заменяют три раза при соотношении объемов, превышающей или равном 1:50 каждый раз. Буфер заменяют через 3 и 6 часов общего времени диализа. Последняя стадия диализа проводится в течение ночи. После диализа препарат извлекают из кассет для диализа и фильтруют с использованием 0,22-мкм фильтра из поливинилидендифторида (PVDF). После фильтрации флаконы наполняют объемом, равным 1,0 мл, в условиях ламинарного потока воздуха.
[0099] Лиофилизацию проводят в лиофилизаторе Epsilon 2-12D опытного образца (Martin Christ, Osterode, Германия). Давление в камере контролируется емкостным датчиком и регулируется вакуумным насосом и регулируемой дозировкой азота.
[0100] После уравновешивания флаконов до 5°C флаконы замораживают до -45°C и уравновешивают в течение еще 5 часов при -45°C. Температура полки устанавливается на -15°C на 31 час при первичной сушке. Вторичную сушку проводят при температуре полки 40°C в течение 2,5 часов. В конце процесса лиофилизации камеру аэрируют азотом до 800 мбар, и флаконы закупоривают, поднимая полки. После закупоривания камеру аэрируют азотом до атмосферного давления. В таблице 3 представлены параметры процесса лиофилизации после оптимизации цикла.
[0101] В процессе лиофилизации контролируются температура продукта, температура полки, температура конденсатора и давление в камере (емкость и датчик Пирани). Температура продукта контролируется датчиками Pt100 (OMEGATM).
V. ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ, НАРУШЕНИЙ ИЛИ СОСТОЯНИЙ
[0102] Индивидуумы с CBSDH, как правило, бессимптомны при рождении, и, если их не лечить, симптомы появляются у этих индивидуумов с течением времени, некоторые уже в младенчестве, многие в подростковом периоде, и, поскольку это заболевание со спектральными симптомами, у некоторых пациентов симптомы появляются только во взрослом возрасте (смотрите Yap, 2005; Mudd et al. Am J Hum Genet 1985; 37:1-31; Morris et al. Guidelines for the diagnosis and management of cystathionine beta-synthase deficiency. J Inherit Metab Dis 2017; 40:49-74; Mudd et al. In: Scriver CL, Beaudet AL, Sly WS, Valle D, eds. The Metabolic and Molecular Basis of Inherited Diseases. 7 ed. New York: McGraw Hill; 2001; 1279-1327, каждый из которых полностью включен таким образом посредством ссылки). Как правило, поражаются четыре основные системы органов: зрительная система (глаза), костная и сердечнососудистая системы, а также ЦНС. Другие органы, такие как печень, поджелудочная железа, желудочно-кишечный тракт и кожа, в том числе волосяные фолликулы, также могут быть поражены (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31; Morris et al. J Inherit Metab Dis 2017; 40:49-74; Muacevic-Katanec et al. Coll Antropol 2011; 35:181-185; Suri et al. J Neurol Sci 2014; 347:305-309, каждый из которых полностью включен таким образом посредством ссылки).
[0103] Накопленные данные показывают, что снижение уровней Hcy может служить показателем успешного применения ферментотерапии (ET) при CBSDH. Это соответствует определению, данному Рабочей группой по биомаркерам NIH-FDA (смотрите FDA-NIH Biomarker Working Group. BEST (Biomarkers, EndpointS, and other Tools) Ресурс [Интернет]. Silver Spring (MD): Food and Drug Administration (US); 2016-. Reasonably Likely Surrogate Endpoint. 2017 Sep 25. В соавторстве с National Institutes of Health (US), Bethesda (MD). ncbi.nlm.nih.gov/books/NBK326791/, который полность включен таким образом посредством ссылки), «фармакодинамического биомаркера/биомаркера ответа, уровень которого изменяется в ответ на воздействие медицинского продукта...» и, более того, маркера, тесно связанного, в случае ET для CBSDH, с механизмом действия лекарственного средства. Следовательно, Hcy в крови или плазме является не только маркером, применимым для фармакодинамических исследований, но также ранее был признан «достаточно вероятным косвенным конечным показателем» гомоцистинурии (HCU).
[0104] В случае младенцев и детей с CBSDH приоритетом является предотвращение осложнений, связанных с CBSDH, и обеспечение надлежащего роста и развития нормального интеллекта (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки). В случае пациентов, диагноз которым был поставлен в более позднем возрасте, целями лечения должны быть предотвращение опасной для жизни тромбоэмболии и минимизация прогрессирования уже выявленных осложнений. Для достижения этих целей биохимические отклонения, связанные с CBSDH, должны быть уменьшены и, если возможно, нормализованы (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки).
[0105] В соответствии с Руководством по диагностике и лечению CBSDH от 2016 г., уровни Hcy должны поддерживаться как можно ближе к норме (на уровне от 10 до 15 мкг/л или ниже). Как правило, это невозможно в случае пациентов с CBSDH, получающих доступное лечение, и поэтому предлагаются желаемые цели: ниже 50 мкмоль/л в случае пациентов с CBSDH, чувствительных к пиридоксину, и ниже 100 мкг/л в случае пациентов, не чувствительных к пиридоксину, (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки). Как отмечалось ранее, пациенты, не чувствительные к пиридоксину, как правило, имеют более высокие уровни Hcy, чем пациенты, чувствительные к пиридоксину. Хотя для пациентов с одним и тем же заболеванием рекомендуются две цели, эти цели были разработаны так, чтобы быть достижимыми, а не оптимизированными, чтобы свести к минимуму осложнения.
[0106] В целом, эффективность длительных лечений, необходимых для контролирования CBSDH, особенно из-за того, что они чаще всего зависят от ограничений в диете и добавок, устанавливается в соответствии с неудовлетворительным или непостоянным соблюдением схемы лечения на протяжении всей жизни. Ферментотерация (ET) для CBSDH позволит избежать многих из этих подводных камней. Ожидается, что за счет компенсации метаболического дефекта при CBSDH с помощью механизма, который не требует серьезного ограничения Met или добавления Cys, с помощью ET будет достигнуто более стойкое снижение Hcy без опасного повышения уровней Met, а также предоставление возможности снять ограничения в диете или нормализовать ее.
[0107] В настоящее время не существует лечения CBSDH, которое устраняло бы лежащие в основе генетические причины заболевания, но общепринятой терапевтической целью является максимально возможное снижение уровня tHcy (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan; 40(1):49-74, который полностью включен таким образом посредством ссылки). Следовательно, современная терапия направлена на коррекцию биохимических отклонений, тем самым снижая риск неблагоприятных клинических проявлений заболевания. Уровни Hcy редко полностью нормализуются с помощью терапий, доступных в настоящее время для пациентов с CBSDH.
[0108] Для достижения целей лечения у большинства пациентов требуется комбинация стратегий. Эти стратегии лечения включают: 1) увеличение остаточной активности CBS путем введения фармакологических доз пиридоксина (витамина B6, кофактора для CBS, наряду с фолиевой кислотой) пациентам, чувствительным к пиридоксину (смотрите Yap et al. Arterioscler Thromb Vasc Biol. 2001 Dec; 21(12):2080-5, который полностью включен таким образом посредством ссылки); 2) снижение метиониновой нагрузки за счет строгого ограничения в диете/белкового ограничения при одновременном дополнении рациона продуктами, выходящим за рамки метаболического блока, и 3) усиление альтернативных метаболических путей для противодействия последствиям дефицита CBS, например, введение бетаина (донора метила) для усиления реметилирования Hcy в Met. В некоторых вариантах осуществления предусмотрены добавки соли фолиевой кислоты и (при необходимости) добавки витамина B12 (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan; 40(1):49-74, который полностью включен таким образом посредством ссылки).
A. Современные терапии для CBSDH
[0109] В некоторых вариантах осуществления пациенты с CBSDH должны получать соответствующие добавки соли фолиевой кислоты и (при необходимости) добавки витамина B12 (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки). Кроме того, пациентов следует лечить с использованием терапии на основе пиридоксина (в случае положительного ответа), дополненной Cys диеты с ограничением Met и/или терапии на основе бетаина. Для достижения целей лечения у большинства пациентов требуется комбинация стратегий.
[0110] Наиболее распространенным назначаемым лечением была комбинация диеты и бетаина с последующим назначение только бетаина и только диеты (смотрите Adam et al. Mol Genet Metab 2013; 110:454-459, который полностью включен таким образом посредством ссылки). По мере того, как пациенты становятся старше 16 лет, им чаще всего назначают только бетаин без диеты, в связи с неудовлетворительным соблюдением взрослыми пациентами диеты с ограничением Met. Однако соблюдение приема бетаина у взрослых является также неудовлетворительным. Медиана потребления белка широко варьировала среди пациентов и резко возрастала с возрастом.
[0111] В соответствии с этими данными в недавнем отчете отмечалось, что только четыре взрослых пациента из 24 пациентов, которым была установлена диета с низким содержанием белка с добавлением конкретных аминокислот, соответствующих CBSDH, следовали этому лечению (смотрите Lorenzini et al. J Inherit Metab Dis. 2017 Oct. 4, который полностью включен таким образом посредством ссылки). Несколько экспертов по CBSDH (Научно-консультативный совет по редким технологиям, состоящий из врачей, являющихся экспертами по CBSDH в США) описали столь же широкую изменчивость в Соединенных Штатах. Из исследования, в котором сравнивались значения tHcy у не подвергнутых лечению и подвергнутых лечению пациентов (25 и 93 пациента, соответственно), был сделан вывод, что между этими двумя группами нет значимых различий (tHcy колеблется от 15,7 до 281,4 и от 4,8 до 312 мкмоль/л, соответственно; медиана значений=125,0 и 119,0 мкмоль/л, соответственно), хотя исследование не предоставило подробностей о схемах лечения пациентов (смотрите Stabler et al. JIMD Rep 2013; 11: 149-163, который полностью включен таким образом посредством ссылки). Эти результаты предполагают все или комбинацию следующих выводов: пациенты или имели гетерогенную картину заболевания, стандартные лечения были неэффективными, и/или соблюдение схемы лечения было неудовлетворительным.
1. Пиридоксин
[0112] После постановки диагноза пациентов проверяют на чувствительность к пиридоксину, кофактору CBS. Введение пиридоксина (витамина B6) в фармакологических дозах увеличивает остаточную активность CBS у индивидуумов, которые, как было установлено, чувствительны к пиридоксину. Определение чувствительности к пиридоксину широко варьируется от учреждения к учреждению, хотя руководство 2016 г., написанное как часть Европейской сети и регистра гомоцистинурии и дефектов метилирования (EHOD), определяло чувствительность к пиридоксину как снижение на 20% уровней tHcy в пределах 6 недель после подвергания воздействию пиридоксина. Как пациенты с сильно повышенными уровнями tHcy, так и пациенты со слегка или умеренно повышенными уровнями tHcy могут быть определены как чувствительные, несмотря на очень разные уровни tHcy. Кроме того, разные лечебные центры по-разному определяют чувствительность к пиридоксину, и поэтому классификация пациентов по уровням tHcy, а не по их чувствительности к пиридоксину, является более соответствующей и строгой. В целом, пациенты, которые являются чувствительными к пиридоксину, имеют некоторую остаточную активность CBS и поэтому более низкие уровни tHcy, что приводит к менее тяжелому течению.
[0113] Пиридоксин, как правило, считается безопасным для пациентов с CBSDH (смотрите Yap; Orphanet Encyclopedia [периодическое издание онлайн] 2005, pages 1-13, который полностью включен таким образом посредством ссылки). Его наиболее часто сообщаемые побочные эффекты включают периферическую невропатию у пациентов, получавших высокие дозы, определяемые как более 900 мг/день (смотрите Schaumburg et al. N Engl J Med 1983; 309:445-448; Ludolph et al. Eur J Pediatr 1993; 152:271; которые полностью включены таким образом посредством ссылки), апноэ и отсутствие реакции у новорожденных, получающих пиридоксин в дозе 500 мг/день (Mudd et al. Am J Hum Genet 1985; 37:1-31, который полностью включен таким образом посредством ссылки) и рабдомиолиз (смотрите Shoji et al. J Inherit Metab Dis 1998; 21:439-440, который полностью включен таким образом посредством ссылки).
[0114] Хотя лечение пиридоксином широко используется, оно обеспечивает умеренное снижение уровней tHcy, и большинство пациентов, которые определены как чувствительные, не способны к значительному снижению, не говоря уже о нормализации, уровней tHcy на одном пиридоксине, поскольку их начальные уровни в несколько раз выше нормы (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan; 40(1):49-74, который полностью включен таким образом посредством ссылки). Помимо длительного лечения пиридоксином, рекомендуется, чтобы пациенты с CBSDH, чувствительные к пиридоксину, также получали соль фолиевой кислоты и, при необходимости, добавку витамина B12.
2. Ограничение в диете
[0115] Ограничения в диете на протяжении всей жизни ранее рекомендовались для всех пациентов с CBSDH (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan; 40(1):49-74; Walter et al. Eur J Pediatr. 1998 Apr; 157 Suppl 2:S71-6, которые полностью включены таким образом посредством ссылки). Рекомендуемая диета крайне ограничена и направлена на снижение потребления Met за счет ограничения содержания белка.
[0116] Основой современной терапии для пациентов с CBSDH является пожизненная низкобелковая диета, включающая всего 5 г натурального белка в день (www.hcunetworkamerica.org), дополненная не включающими Met L-аминокислотами, и, во многих случаях, дополнительный Cys (Yap et al. J Inherit Metab Dis 1998; 21:738-47; Morris et al. J Inherit Metab Dis. 2017 Jan; 40(1):49-74; которые полностью включены таким образом посредством ссылки) дается в дополнение к диете. Строго ограниченная диета состоит из продуктов на основе злаков с низким содержанием метионина, фруктов и овощей с низким содержанием метионина, медицинских продуктов с низким содержанием метионина, масел и сахара. Следует избегать таких продуктов, как мясо, курица, рыба, яйца, молоко, йогурт, сыр, соевые продукты, орехи, бобовые и многие фрукты и овощи, которые содержат умеренное количество Met. Поскольку нативная CBS является ключевым ферментом в метаболизме Met, прием Met, незаменимой аминокислоты, содержащейся во многих пищевых продуктах, приводит к повышению концентраций tHcy в плазме и снижению концентраций последующих метаболитов Cth и Cys.
[0117] Готовые пищевые продукты, выпечка и упакованные пищевые продукты должны строго ограничиваться, поскольку они часто содержат молоко, яйца или муку. Количество белка, необходимое и переносимое каждым пациентом с CBSDH, различно и, вероятно, будет меняться со временем. Это количество корректируется в соответствии с уровнями tHcy, которые контролируются с помощью частых анализов крови (ASIEM Low Protein Handbook for Homocystinuria). Большинству пациентов, находящихся на диетотерапии, также требуется ежедневное потребление малопривлекательной смеси синтетических аминокислот, не включающих Met, для предотвращения вторичной недостаточности питания и для правильного роста у детей и у взрослых для правильного питания (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan; 40(1):49-74; который полностью включен таким образом посредством ссылки).
[0118] Хотя модификации диеты в комбинации с добавкой витамина могут до некоторой степени снизить уровни tHcy у индивидуумов, полностью соблюдающих диету со строгим ограничением, уровни tHcy у большинства пациентов с CBSDH остаются в несколько раз - на несколько порядков выше нормы. Для большинства индивидуумов очень сложно добиться полного соблюдения модификаций диеты на протяжении всей жизни, и возникающие в результате периоды плохого контроля метаболизма имеют кумулятивные вредные эффекты (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan; 40(1):49-74; который полностью включен таким образом посредством ссылки). Соблюдение диеты является часто неудовлетворительным и, как правило, еще больше ухудшается в подростковом и взрослом возрасте (смотрите Walter et al. Eur J Pediatr. 1998 Apr; 157 Suppl 2:S71-6; Schiff et al. Neuropediatrics. 2012 Dec; 43(6):295-304; Garland et al. Paediatr Child Health. 1999 Nov;4(8):557-62; которые полностью включены таким образом посредством ссылки). Более того, употребление в пищу продуктов с высоким содержанием Met не вызывает немедленной негативной физической реакции, что еще больше усугубляет трудности с соблюдением диеты (www.hcunetworkamerica.org). Ограничение приема Met является еще более сложной задачей для детей из-за необходимости обеспечения достаточного количества Met для способствования росту и развитию. Большинству пациентов на диетотерапии также требуется добавка L-аминокислот, обогащенных Cys и не включающих Met, для правильного роста в случае детей и для правильного питания в случае взрослых (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки).
[0119] В недавнем отчете отмечалось, что только четыре взрослых пациента из 24 пациентов, которым была установлена диета с низким содержанием белка с добавлением конкретных аминокислот, соответствующих CBSDH, следовали этому лечению (смотрите Lorenzini et al. J Inherit Metab Dis. (2018) 41:109-115, который полностью включен таким образом посредством ссылки). Несколько экспертов по CBSDH описали столь же широкую изменчивость в Соединенных Штатах.
3. Добавление бетаина
[0120] Проблемы, связанные с терапиями, основанными в основном на диете, обусловили необходимость других подходов к снижению Hcy, в первую очередь добавления бетаина (N, N,N-триметилглицина, продаваемого как CYSTADANE™), вводимого по крайней мере дважды в день. Бетаин редко эффективен в качестве монотерапии (Sakamoto et al. Pediatr Int 2003; 45:333-338, который полностью включен таким образом посредством ссылки) и обычно используется в качестве добавки к пиридоксину и/или диете с ограничением Met (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan; 40(l):49-74; который полностью включен таким образом посредством ссылки).
[0121] Бетаин не устраняет лежащий в основе дефицит CBS, а скорее индуцирует альтернативный путь, приводящий к реметилированию Hcy обратно в Met, и путем коррекции частичного неправильного сворачивания мутантов CBS (смотрите Kopecka et al. J Inherit Metab Dis 2011; 34:39-48, который полностью включен таким образом посредством ссылки). В присутствии бетаина фермент бетаин-гомоцистеин-метилтрансфераза (BHMT) реметилирует Hcy в Met (Singh et al. Genet Med 2004; 6:90-95, который полностью включен таким образом посредством ссылки), тем самым частично снижая уровни Hcy при одновременном повышении и без того сильно повышенных уровней Met. Уровни метаболитов в метаболическом пути после CBS не уменьшаются при введении бетаина, и может потребоваться добавление Cys. Более того, лечение бетаином было связано с аномалиями белого вещества головного мозга - признаком повреждения сосудов головного мозга (Prins et al. Nat Rev Neurol 2015; 11:157-165, который полностью включен таким образом посредством ссылки) - у пациентов с острым отеком головного мозга (Devlin et al. J Pediatr 2004, 144:545-548; Yaghmai et al. Am J Med Genet 2002; 108:57-63; которые полностью включены таким образом посредством ссылки) и без него (Vatanavicharn et al. J Inherit Metab Dis 2008;31 Suppl 3:477-481; Brenton et al. J Child Neurol 2014; 29:88-92; Sasai et al. Tohoku J Exp Med 2015; 237:323-327; которые полностью включены таким образом посредством ссылки).
[0122] Бетаин может быть неприятным на вкус (Walter et al. Eur J Pediatr. 1998 Apr;157 Suppl 2:S71-6, который полностью включен таким образом посредством ссылки) и приводить к неприятному рыбному запаху тела и/или дыхания (смотрите Manning et al. JIMD Rep 2012;5:71-75, который полностью включен таким образом посредством ссылки). Оба эффекта потенциально усугубляются потребностью в высоких дозах (более 6 г/сутки в случае взрослых и детей). В результате соблюдение схемы лечения является неудовлетворительным (смотрите Adam et al. Mol Genet Metab. 2013 Dec; 110(4):454-9; Walter et al. Eur J Pediatr. 1998 Apr;157 Suppl 2:S71-6; Sakamoto et al. Pediatr Int 2003; 45:333-338, которые полностью включены таким образом посредством ссылки).
[0123] Фармацевтический препарат бетаина, CYSTADANE™, был одобрен FDA в 2006 г. и показан для снижения повышенного уровня Hcy в крови при нарушениях в виде гомоцистинурии, включая дефицит CBS, дефицит 5,10-метилентетрагидрофолатредуктазы (MTHFR) и дефекты метаболизма кофактора кобаламина (cbl) (смотрите Recordati. CYSTADANE™ Product Information (PI). 2017. Тип ссылки: источник онлайн, который полностью включен таким образом посредством ссылки).
[0124] Крупнейшее на сегодняшний день исследование по проведению диетотерапии среди пациентов с CBSDH, не чувствительных к пиридоксину, показало, что бетаин был распространенным предпочтительным лечением, особенно в случае пациентов, подростков и взрослых, с поздней постановкой диагноза. Считается, что применение бетаина в качестве основной терапии у 34% пациентов без установления диеты связано с несоблюдением диеты, поскольку нет контролируемых исследований, изучающих долгосрочную эффективность бетаина при приеме без диеты (смотрите Adam et al. Mol Genet Metab 2013;110:454-459, который полностью включен таким образом посредством ссылки). Действительно, при исследовании на модели CBSDH на мыши было установлено, что способность лечения бетаином к значительному понижению уровня tHcy со временем снижалась (смотрите Maclean KN. Betaine treatment of cystathionine b-synthase-deficient homocystinuria; does it work and can it be improved? Dove press 2012; 2:23-33, который полностью включен таким образом посредством ссылки).
4. Антитромбоцитарная терапия
[0125] В дополнение к терапиям, снижающим уровень Hcy, пациентам с плохо контролируемыми уровнями Hcy и/или пациентам с дополнительными факторами риска тромбоза (например, фактором V Лейдена, тромбозом в анамнезе и беременностью) может помочь лечение антитромбоцитарными средствами (например, аспирином, дипиридамолом или клопидогрелем) (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan; 40(1):49-74; который полностью включен таким образом посредством ссылки). Препараты для разжижения крови COUMADIN™ также могут использоваться в случае пациентов с тромбозом вен в анамнезе. Однако антикоагулянты связаны с повышенным риском кровоизлияния в головной мозг, и их применение должно определяться индивидуально для каждого пациента (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan; 40(1):49-74; который полностью включен таким образом посредством ссылки).
5. Клинические результаты современных терапий
[0126] Проявления CBSDH продолжают прогрессировать, при этом классические клинические симптомы достигают различной степени инвалидности, и влияют на качество жизни пораженных индивидуумов. Независимо от возраста, в котором начинается заболевание, утрата биохимического контроля в любом возрасте сопровождается развитием серьезных осложнений, которые могут быть опасными для жизни (смотрите Walter et al. Eur J Pediatr. 1998 Apr; 157 Suppl 2:S71-6), который полностью включен таким образом посредством ссылки).
[0127] Лечение необходимо продолжать на протяжении всей жизни, так как периоды недостаточного контроля метаболизма имеют кумулятивные вредные эффекты, которые могут привести к тяжелым осложнениям и преждевременной смерти (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan; 40(1):49-74, который полностью включен таким образом посредством ссылки).
[0128] Без лечения прогноз CBSDH, не чувствительной к пиридоксину, является плохим, и продолжительность жизни пациентов заметно снижается. Никакие рандомизированные контролируемые испытаний диетотерапии или другой терапии для CBSDH не проводили, так как заболевание было впервые описано в 1962 г. (смотрите Carson et al. Arch Dis Child. 1969 Jun; 44(235):387-92; Gerritsen et al. Biochem Biophys Res Commun. 1962 Dec 19; 9:493-6; которые полностью включены таким образом посредством ссылки). Тем не менее, было опубликовано несколько исследований по данным наблюдений.
[0129] Международное исследование, в ходе которого документировали естественное течение заболевания у 629 не подвергнутых лечению пациентов с CBSDH, показало, что риск осложнений увеличивается с возрастом (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31, который полностью включен таким образом посредством ссылки). Было замечено, что лечение (пиридоксином, диетой с ограничением Met) снижает уровни tHcy в плазме и заметно снижает риск тромбоэмболических событий и смещения хрусталика, хотя отмечали, что соблюдение диеты с ограничением было неудовлетворительным.
[0130] Yap и др. (Arterioscler Thromb Vasc Biol. 2001 Dec;21(12):2080-5) провели международное исследование во множестве центров на 158 подвергнутых лечению пациентах. Частота сердечнососудистых событий была заметно снижена в этой подвергнутой лечению группе по сравнению с исторически установленными контрольными данными Mudd и др. (Am J Hum Genet 1985; 37:1-31, который полностью включен таким образом посредством ссылки). Эта очевидная польза коррелировала с более низкими (но не нормализованными) уровнями tHcy в плазме у пациентов, подвергнутых лечению. Было отмечено, что последовательное соблюдение необходимой схемы очень сложно.
[0131] В целом, несмотря на то, что доступно несколько стратегий лечения CBSDH, они не могут восстановить у большинства пациентов уровни tHcy, близкие к нормальным. Более того, их долгосрочная эффективность устанавливается в соответствии с неудовлетворительным или непостоянным соблюдением схемы лечения на протяжении всей жизни. Поэтому постоянное снижение уровня Hcy трудно поддерживать у пациентов с CBSDH. Лечение описанной здесь готовой лекарственной формой направлено на избегание многих из этих подводных камней. Ожидается, что за счет компенсации метаболического дефекта при CBSDH с помощью механизма, который не требует серьезного ограничения Met или добавления Cys, ферментотерапии (ET) будет достигнуто более стойкое снижение уровня Hcy без опасного повышения уровней Met.
VI. ДОЗИРОВАНИЕ И ВВЕДЕНИЕ
[0132] В некоторых вариантах осуществления готовую лекарственную форму можно вводить субъекту с помощью подкожной (SC), внутривенной (IV) или внутрибрюшинной (IP) инъекции. В одном варианте осуществления готовую лекарственную форму можно вводить субъекту 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, или 20 раз. В другом варианте готовую лекарственную форму вводят более 20 раз. В другом варианте осуществления готовую лекарственную форму вводят более 100 раз. В качестве альтернативы, готовую лекарственную форму можно вводить в течение оставшегося времени жизни субъекта.
[0133] В некоторых вариантах осуществления введение готовой лекарственной формы можно повторять каждые 12 часов, 13 часов, 14 часов, 15 часов, 16 часов, 17 часов, 18 часов, 19 часов, 20 часов, 21 час, 22 часа, 23 часа, ежедневно, каждые 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, каждую неделю, каждые 2 недели, 3 недели и каждый месяц. В некоторых вариантах осуществления введение готовой лекарственной формы осуществляют один раз каждые 3 дня, один раз каждые 2 дня или один раз в день.
[0134] В некоторых вариантах осуществления введение готовой лекарственной формы может представлять собой ряд введений доз, которые разделены минутами, часами, днями или неделями. Например, число доз в ряду может составлять 1, 2, 3, 4, 5 или 6. В качестве неограничивающего примера субъекту вводят 3 дозы с интервалом в 24 часа. В качестве другого неограничивающего примера субъекту вводят 5 доз с интервалом в 12 часов. Субъектом может быть человек.
[0135] В некоторых вариантах осуществления введение готовой лекарственной формы может следовать схеме введения доз в виде рядов доз, в случае которой имеется «окно» между первым рядом и вторым рядом доз. «Окно» между дозами может составлять 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 13 часов, 14 часов, 15 часов, 16 часов, 17 часов, 18 часов, 19 часов, 20 часов, 21 час, 22 часа, 23 часа, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 1 неделю, 2 недели, 3 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, 13 месяцев, 14 месяцев, 15 месяцев, 16 месяцев, 17 месяцев или 18 месяцев. Число доз в ряду может составлять 2, 3, 4, 5 или 6. В качестве неограничивающего примера субъекту может вводиться первый ряд из 5 доз с интервалом в 12 часов, а затем через 14 дней после первой дозы субъекту вводят второй ряд из 5 доз с интервалом в 12 часов. В качестве другого неограничивающего примера субъекту вводят два ряда доз в течение 8 недель, причем первый ряд представляет собой одну дозу дважды в неделю в течение двух недель, а второй ряд доз представляет собой три раза в неделю в течение 6 недель.
[0136] В некоторых вариантах осуществления готовую лекарственную форму можно вводить по крайней мере один раз после того, как субъекту был введен бетаин. Время между введением бетаина и введением готовой лекарственной формы может составлять 1 час, 2 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 13 часов, 14 часов, 15 часов, 16 часов, 17 часов, 18 часов, 19 часов, 20 часов, 21 час, 22 часа, 23 часа, 1 день, 2 дня, 3 дня, 4 дня, 5 дней, 6 дней, 1 неделю, 2 недели, 3 недели, 1 месяц, 2 месяца, 3 месяца, 4 месяца, 5 месяцев, 6 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев, 12 месяцев, 13 месяцев, 14 месяцев, 15 месяцев, 16 месяцев, 17 месяцев или 18 месяцев. В качестве неограничивающего примера готовую лекарственную форму можно вводить через 14 дней после того, как субъекту был введен бетаин. В качестве другого неограничивающего примера субъекту можно вводить две дозы готовой лекарственной формы после того, как субъекту был введен бетаин. В качестве другого неограничивающего примера готовую лекарственную форму можно вводить через 14 или 15 дней после введения бетаина.
[0137] В некоторых вариантах осуществления готовую лекарственную форму можно вводить субъекту в комбинации с бетаином. Комбинацию можно вводить по крайней мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 и 15 раз. В некоторых вариантах осуществления готовую лекарственную форму можно вводить в комбинации с бетаином более 15 раз. Дополнительные комбинированные терапии, которые могут быть назначены пациенту, включают готовую лекарственную форму и по крайней мере одно лечение для снижения уровней tHcy, такое как диета с очень низким содержанием белка/Met и/или витамины/добавки.
[0138] В одном варианте осуществления доза готовой лекарственной формы, вводимая субъекту, может составлять от приблизительно 0,25 мг/кг до приблизительно 10 мг/кг. Например, доза составляет приблизительно 0,33 мг/кг, приблизительно 0,66 мг/кг, 1,0 мг/кг или 1,5 мг/кг. Альтернативно, доза составляет приблизительно 2 мг/кг, приблизительно 7 мг/кг и приблизительно 10 мг/кг. Например, доза может составлять приблизительно 0,5 мг/кг. Альтернативно, терапевтически эффективное количество представляет собой дозу, выбранную из диапазона от приблизительно 5,0 мг/кг до приблизительно 50 мг/кг и от приблизительно 10,0 мг/кг до приблизительно 25 мг/кг. Например, дозу выбирают из группы, состоящей из: приблизительно 0,25 мг/кг, приблизительно 0,33 мг/кг, приблизительно 0,66 мг/кг, приблизительно 1,00 мг/кг, приблизительно 1,10 мг/кг, приблизительно 1,20 мг/кг, приблизительно 1,30 мг/кг, приблизительно 1,40 мг/кг, приблизительно 1,50 мг/кг, приблизительно 1,60 мг/кг, приблизительно 1,70 мг/кг, приблизительно 1,80 мг/кг, приблизительно 1,90 мг/кг, приблизительно 2,00 мг/кг, приблизительно 3,00 мг/кг, приблизительно 4,00 мг/кг, приблизительно 5,00 мг/кг, приблизительно 6,00 мг/кг, приблизительно 7,00 мг/кг, приблизительно 8,00 мг/кг, приблизительно 9,00 мг/кг, приблизительно 10,0 мг/кг, приблизительно 11,0 мг/кг, приблизительно 12,0 мг/кг, приблизительно 13,0 мг/кг, приблизительно 14,0 мг/кг, приблизительно 15,0 мг/кг, приблизительно 16,0 мг/кг, приблизительно 17,0 мг/кг, приблизительно 18,0 мг/кг, приблизительно 19,0 мг/кг, приблизительно 20,0 мг/кг, приблизительно 21,0 мг/кг, приблизительно 22,0 мг/кг, приблизительно 23,0 мг/кг, приблизительно 24,0 мг/кг, приблизительно 25,0 мг/кг, приблизительно 26,0 мг/кг, приблизительно 27,0 мг/кг, приблизительно 28,0 мг/кг, приблизительно 29,0 мг/кг, приблизительно 30,0 мг/кг, приблизительно 31,0 мг/кг, приблизительно 32,0 мг/кг, приблизительно 33,0 мг/кг, приблизительно 34,0 мг/кг, приблизительно 35,0 мг/кг, приблизительно 36,0 мг/кг, приблизительно 37,0 мг/кг, приблизительно 38,0 мг/кг, приблизительно 39,0 мг/кг, приблизительно 40,0 мг/кг, приблизительно 41,0 мг/кг, приблизительно 42,0 мг/кг, приблизительно 43,0 мг/кг, приблизительно 44,0 мг/кг, приблизительно 45,0 мг/кг, приблизительно 46,0 мг/кг, приблизительно 47,0 мг/кг, приблизительно 48,0 мг/кг, приблизительно 49,0 мг/кг и приблизительно 50,0 мг/кг.
[0139] В некоторых вариантах осуществления готовую лекарственную форму вводят субъекту, соблюдающему диету с ограничением метионина. Альтернативно, готовую лекарственную форму вводят субъекту, который не соблюдает диету с ограничением метионина.
[0140] В некоторых вариантах осуществления готовую лекарственную форму можно вводить совместно с другим терапевтическим средством для лечения CBSDH. Используемый здесь термин «совместное введение» означает введение двух или более компонентов. Эти компоненты для совместного введения включают, но без ограничения этим, бетаин или витамин B6. Совместное введение относится к введению двух или более компонентов одновременно или с промежутком времени между введением, составляющим, например, 1 секунду, 5 секунд, 10 секунд, 15 секунд, 30 секунд, 45 секунд, 1 минуту, 2 минуты, 3 минуты, 4 минуты, 5 минут, 6 минут, 7 минут, 8 минут, 9 минут, 10 минут, 11 минут, 12 минут, 13 минут, 14 минут, 15 минут, 16 минут, 17 минут, 18 минут, 19 минут, 20 минут, 21 минуту, 22 минуты, 23 минуты, 24 минуты, 25 минут, 26 минут, 27 минут, 28 минут, 29 минут, 30 минут, 31 минуту, 32 минуты, 33 минуты, 34 минуты, 35 минут, 36 минут, 37 минут, 38 минут, 39 минут, 40 минут, 41 минуту, 42 минуты, 43 минуты, 44 минуты, 45 минут, 46 минут, 47 минут, 48 минут, 49 минут, 50 минут, 51 минуту, 52 минуты, 53 минуты, 54 минуты, 55 минут, 56 минут, 57 минут, 58 минут, 59 минут, 1 час, 1,5 часа, 2 часа, 2,5 часа, 3 часа, 4 часа, 5 часов, 6 часов, 7 часов, 8 часов, 9 часов, 10 часов, 11 часов, 12 часов, 13 часов, 14 часов, 15 часов, 16 часов, 17 часов, 18 часов, 19 часов, 20 часов, 21 час, 22 часа, 23 часа, 1 день, 1,5 дня, 2 дня или 3 дня. В некоторых вариантах осуществления промежуток времени между введением двух или более компонентов превышает 3 дня.
[0141] В некоторых вариантах осуществления готовую лекарственную форму можно применять в качестве парентерального средства для постоянного введения пациентам посредством подкожной (SC) инъекции с начальным интервалом между введения доз - один раз в неделю. Например, еженедельное введение дозы лекарственного средства для 6 доз. В некоторых вариантах осуществления субъект может быть возрастом от 18 до 65 лет. В некоторых вариантах осуществления схожее лечение может быть проведено субъекту в возрасте уже 16 лет.
[0142] В некоторых вариантах осуществления введение выполняется на протяжении 1 дня, 2 дней, 3 дней, 4 дней, 5 дней или 6 дней. В некоторых вариантах осуществления введение выполняется на протяжении 1 недели, 2 недель, 3 недель, 4 недель, 5 недель, 6 недель, 7 недель, 8 недель, 9 недель, 10 недель, 11 недель, 12 недель, 13 недель, 14 недель, 15 недель, 16 недель, 17 недель, 18 недель, 19 недель, 20 недель, 21 недели, 22 недель, 23 недель, 24 недель, 25 недель, 26 недель, 27 недель, 28 недель, 29 недель, 30 недель, 31 недели, 32 недель, 33 недель, 34 недель, 35 недель, 36 недель, 37 недель, 38 недель, 39 недель, 40 недель, 41 недели, 42 недель, 43 недель, 44 недель, 45 недель, 46 недель, 47 недель, 48 недель, 49 недель, 50 недель, 51 недели или 52 недель.
[0143] В некоторых вариантах осуществления готовую лекарственную форму назначают в виде комбинированной терапии с пиридоксином (также называемым витамином B6) и/или антитромбоцитарной терапией.
VII. СТРАТИФИКАЦИЯ ПАЦИЕНТОВ
[0144] В некоторых вариантах осуществления индивидуумы, подходящие для эффективной ферментотерапии с использованием описанной здесь готовой лекарственной формы, включают пациентов с диагнозом CBSDH, на основании подтверждения гомоцистинурии, вызванной генетическим дефицитом CBS, с помощью анализа мутаций гена CBS и уровня tHcy в плазме, превышающего или равного 80 мкМ.
А. Клиническая картина
[0145] В соответствии с Руководством по диагностике и лечению CBSDH, заболевание следует подозревать у детей с тяжелой или быстро прогрессирующей миопатией, смещением хрусталика и/или задержкой развития (смотрите Morris et al. Guidelines for the diagnosis and management of cystathionine beta-synthase deficiency. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки). Исследования также оправданы в случае взрослых с тромбоэмболией и/или смещением хрусталика, но без других симптомов, а также в случае взрослых пациентов с полисистемным заболеванием, в том числе осложнениями на глаза, соединительную ткань, нейропсихиатрическими осложнениями и осложнениями на сердечнососудистую систему (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31; Morris et al. Guidelines for the diagnosis and management of cystathionine beta-synthase deficiency. J Inherit Metab Dis 2017; 40:49-74; Kelly et al. Neurology 2003; 60:275-279, каждый из которых полностью включен таким образом посредством ссылки).
B. Биохимический анализ
[0146] Уровни tHcy в плазме определяют, используя сумму всех свободных и связанных видов гомоцистеина после обработки плазмы восстанавливающим агентом. У здоровых индивидуумов с неизменными пищевыми привычками уровни tHcy остаются относительно постоянными с течением времени (смотрите Refsum et al. Clin Chem 2004; 50:3-32; McKinley et al. Clin Chem 2001;47:1430-1436; каждый из которых полностью включен таким образом посредством ссылки). Однако потребление пищи, богатой белком, может повысить уровни tHcy на приблизительно 10% в течение нескольких часов (смотрите Verhoef et al. Am J Clin Nutr 2005; 82:553-558, который полностью включен таким образом посредством ссылки). Исследование на индивидуумах с гипергомоцистеинемией (tHcy >40 мкмоль/л) показало, что индивидуальные уровни tHcy варьировались вплоть до 25% в течение периода от 4 до 8 месяцев. Однако не было предоставлено никакой информации о разнообразии диет, способах анализа и времени отбора проб, что затрудняло возможность интерпретации данных (смотрите Refsum H, Smith AD, Ueland PM et al. Facts and recommendations about total homocysteine determinations: an expert opinion. Clin Chem 2004; 50:3-32, который полностью включено таким образом посредством ссылки).
[0147] В популяциях без добавления соли фолиевой кислоты соответствующие стандартные верхние пределы составляют приблизительно 15 и 20 мкмоль/л, соответственно. Для подтверждения диагноза CBSDH у новорожденных уровень tHcy в плазме, как предполагается, будет находиться в диапазоне от 50 до более 100 мкмоль/л, а уровень Met в плазме - в диапазоне от 200 до 1500 мкмоль/л (т.е. 3-23 мг/дл) (смотрите Sacharow et al. Homocystinuria Caused by Cystathionine Beta-Synthase Deficiency. GeneReviews 2017, который полностью включен таким образом посредством ссылки). Для подтверждения диагноза CBSDH у не подвергнутого лечению пожилого индивидуума уровень tHcy в плазме, как предполагается, будут выше 100 мкмоль/л, а уровень Met в плазме - выше 50 мкмоль/л (т.е. выше 0,7 мг/дл). Предполагается, что у контрольного новорожденного или пожилого индивидуума уровень tHcy в плазме будет менее 15 мкмоль/л, а уровень Met - от 10 до 40 мкмоль/л (0,2-0,6 мг/дл).
[0148] Уровни Met от высоких до высоконормальных (стандартные диапазоны, как правило, составляют от 40 до 45 и от 12 до 15 мкмоль/л, соответственно) в сочетании с уровнями Cth от низких до низконормальных (стандартные диапазоны от 0,05 до 0,08 и от 0,35 до 0,5 мкмоль/л), соответственно) могут использоваться, чтобы отличить CBSDH от HCU, вызванной генетическими и алиментарными нарушениями реметилирования Hcy (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74; Stabler et al. JIMD Rep 2013; 11:149-163; Bartl et al. Clin Chim Acta 2014; 437:211-217, каждый из которых полностью включен таким образом посредством ссылки). Другое применимое исследование определяет продукцию Cth из Hcy и серина в культивируемых фибробластах с использованием радиоактивных или меченных дейтерием субстратов (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74; Kraus JP. Methods Enzymol 1987; 143:388-394; Smith et al. J Chromatogr B Analyt Technol Biomed Life Sci 2012; 911:186-191, каждый из которых полностью включен таким образом посредством ссылки). Однако ферментный анализ не всегда может отличить отвечающих на пиридоксин и не отвечающих на него индивидуумов, и ферментативная активность может быть нормальной в легких случаях (смотрите Alcaide et al. Clin Chim Acta 2015; 438:261-265, который полностью включен таким образом посредством ссылки). Совсем недавно быстрые стабильные изотопные анализы, измеряющие активность CBS, высвобождаемой из органов в плазму, показали 100% чувствительность у пациентов, не отвечающих на пиридоксин, но только 86% чувствительность у пациентов, ответивших на пиридоксин (смотрите Alcaide et al. Clin Chim Acta 2015; 438:261-265; Krijt et al. J Inherit Metab Dis 2011; 34:49-55, оба из которых полностью включены таким образом посредством ссылки).
C. Молекулярная диагностика
[0149] Молекулярно-генетическое исследование - золотой стандарт диагностического теста на CBSDH - можно проводить либо с помощью исследования одного гена, либо с использованием панели множества генов (смотрите Yap S. Homocystinuria due to cystathionine beta-Synthase deficiency. Orphanet Encyclopaedia [периодическое издание онлайн] 2005; Sacharow SJ, Picker JD, Levy HL. Homocystinuria Caused by Cystathionine Beta-Synthase Deficiency. GeneReviews 2017; Morris et al. J Inherit Metab Dis 2017; 40:49-74; Katsanis et al. Nat. Rev Genet 2013; 14:415-426, каждый из которых полностью включен таким образом посредством ссылки). Индивидуумы с высоким риском наличия определенной мутации CBS должны пройти скрининг с использованием целенаправленного исследования одного гена. Однако это применимо только в отдельных популяциях с распространенной мутацией CBS (например, 93% индивидуумов с CBSDH из Катара несут мутацию p.Arg336Cys; c.1006C>T) и в случае индивидуумов из семей с известным патогенным вариантом. У других пациентов ген CBS можно секвенировать, а анализ делеций/дупликаций в целевом гене проводить только в случае обнаружения одного патогенного варианта или его отсутствия. В качестве альтернативы, одновременное молекулярное исследование множества генов может быть выполнено с использованием панели множества генов. Используемые методы могут включать анализ последовательности, анализ делеций/дупликаций и другие исследования, не основанные на секвенировании, (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки). Как правило, молекулярно-генетическое исследование предназначено для популяций с высоким риском с ограниченным числом распространенных мутаций (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74; Huemer et al. J Inherit Metab Dis 2015; 38:1007-101, каждый из которых полностью включен таким образом посредством ссылки).
D. Тесты на чувствительность к пиридоксину
[0150] Тесты на чувствительность к пиридоксину используются в клинике для определения того, следует ли назначать добавки пиридоксина пациентам с CBSDH. Поскольку разные лечебные центры по-разному определяли чувствительность к пиридоксину (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки), классификация пациентов по уровням tHcy, а не по их чувствительности к пиридоксину, является более точной. Чувствительность к пиридоксину не является показателем контроля метаболизма, а скорее указывает на то, что сохраняется некоторая остаточная активность CBS.
E. Скрининг новорожденных (NBS)
[0151] В общем, тесты на дефицит CBS в ходе NBS проводят путем анализа высушенных капель крови для определения уровней Met. В качестве альтернативы, оценка уровней tHcy, а не Met в высушенных каплях крови для NBS доступна в нескольких центрах по всему миру. Она используется в качестве теста второго уровня для снижения частоты ложноположительных результатов NBS у индивидуумов с высокими уровнями Met (смотрите Turgeon et al. Clin Chem 2010; 56:1686-1695, который полностью включен таким образом посредством ссылки) и не используется для увеличения чувствительности или снижения частоты ложноотрицательных результатов.
VIII. ФЕНОТИПИЧЕСКИЕ ЭФФЕКТЫ
[0152] Ретроспективные исследования показывают пропорциональную связь между уровнями tHcy и последствиями. Пациенты с самыми высокими уровнями tHcy (подвергнутые лечению или подвергнутые лечению) имеют более тяжелые симптомы в более раннем возрасте, тогда как пациенты с более низкими уровнями tHcy демонстрируют меньше симптомов и менее быстро прогрессируют (смотрите Yap S. Homocystinuria due to cystathionine beta-synthase deficiency. Orphanet Encyclopaedia [периодическое издание онлайн] 2005; Mudd et al. Am J Hum Genet 1985; 37:1-31, каждый из которых полностью включен таким образом посредством ссылки). Индивидуумы с повышенными уровнями tHcy, как правило, имеют задержку развития, тромбоэмболию, тяжелую миопию с последующим смещением хрусталика, переломы типа переломов при остеопорозе, марфаноидный габитус (в частности, удлинение длинных костей) и/или психические отклонения, такие как затруднения в учебе (смотрите Yap S. Homocystinuria due to cystathionine beta-synthase deficiency. Orphanet Encyclopaedia [периодическое издание онлайн] 2005; Morris et al. J Inherit Metab Dis 2017; 40:49-74; NORD, Kraus JP. Homocystinuria due to cystathionine beta-synthase deficiency. NORD [периодическое издание онлайн] 2017, каждый из которых полностью включен таким образом посредством ссылки). Отражая спектр последствий дефицита CBS, некоторые пациенты страдают тяжелым полисистемным заболеванием с началом в детском возрасте, тогда как пациенты с менее выраженным повышением уровня Hcy могут оставаться без постановки диагноза во взрослом возрасте (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки). Ожидаемая продолжительность жизни заметно снижается у пациентов с сильно повышенным уровнем Hcy, хотя даже пациенты с умеренно повышенными уровнями tHcy страдают множеством негативных клинических последствий.
[0153] Были получены значительные доказательства, указывающие на причинно-следственную связь между повышенными уровнями tHcy и негативными клиническими последствиями в четырех системах, обычно поражаемых у пациентов с CBSDH (зрительной, костной, сердечнососудистой и нервной системах). В зрительной системе часто наблюдаемые фенотипические эффекты включают: эктопию хрусталика, иридодонез, миопию, а менее часто наблюдаемые фенотипические эффекты включают: глаукому, атрофию зрительного нерва, дегенерацию сетчатки, отслойку сетчатки, катаракту и аномалии роговицы. В костной системе часто наблюдаемые фенотипические эффекты включают: остеопороз, двояковогнутые позвонки, сколиоз, увеличение длины длинных костей, неравномерное расширение метафиза, обусловленные метафизом кости спикулы, аномальный размер/форму эпифизов, линии задержки роста, полую стопу и высокое арочное небо, а менее часто наблюдаемые фенотипические эффекты включают: арахнодактилию, увеличение костей запястья, аномальный костный возраст, килевидную/воронкообразную деформацию грудной клетки, Х-образное искривление ног, кифоз и короткую четвертую пястную кость. В сердечнососудистой системе часто наблюдаемые фенотипические эффекты включают: окклюзии сосудов, румянец на скулах и сетчатое ливедо. В центральной нервной системе часто наблюдаемые фенотипические эффекты включают: умственную отсталость, психические расстройства и экстрапирамидные признаки, а менее часто наблюдаемые фенотипические эффекты включают: судороги и аномальную электроэнцефалограмму. В других системах организма часто наблюдаются следующие фенотипические эффекты: светлые, ломкие волосы, тонкая кожа, жировые изменения в печени, паховая грыжа, миопатия, эндокринные нарушения, снижение факторов свертывания крови и спонтанная перфорация кишечника.
[0154] Наблюдалась сильная взаимосвязь между слегка повышенными уровнями tHcy и негативными последствиями, но данные также показали, что снижение уровней tHcy положительно влияет на клинические проявления. Литература по CBSDH страдает из-за редкости заболевания и последующих небольших исследований, но выигрывает от увеличения клинических результатов в популяции с сильно повышенными уровнями Hcy. И наоборот, исследования в более широкой популяции выигрывают от больших размеров выборки, но страдают от меньших повышений уровней tHcy. Вместе взятые, эти исследования постоянно демонстрируют, что повышенные уровни tHcy сильно предсказывают негативные клинические последствия, и что фармакологические вмешательства для снижения этих уровней полезны.
[0155] Возможный результат лечения CBSDH готовой лекарственной формой, описанной здесь, заключается в снижении концентрации tHcy в плазме до минимально возможных уровней при сохранении более спокойной диеты, включающей более высокие концентрации Met, чем в случае других терапий для CBSDH, и другие незаменимые аминокислоты. В случае младенцев и детей с CBSDH приоритетом является предупреждение осложнений, связанных с CBSDH, и обеспечение надлежащего роста и развития нормального интеллекта (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan; 40(l):49-74, который полностью включен таким образом посредством ссылки). В случае пациентов, которым диагноз поставлен в более позднем возрасте, приоритетом может быть предотвращение опасной для жизни тромбоэмболии и минимизация прогрессирования уже выявленных осложнений. Для достижения этих целей биохимические отклонения, связанные с CBSDH, могут быть уменьшены и, если возможно, нормализованы (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan; 40(l):49-74, который полностью включен таким образом посредством ссылки). Обследование, в котором сравнивались проведения диетотерапии для пациентов с CBSDH в 29 центрах в 8 европейских странах, показало, что в лечебных центрах не было единого мнения относительно целевых диапазонов для уровней tHcy в плазме, при этом медиана рекомендуемого целевого значения составляла менее 55 мкМ и находилась в диапазоне от менее 20 до 100 мкМ в 29 центрах (смотрите Adam et al. Mol Genet Metab. 2013 Dec; l10(4):454-9, который полностью включен таким образом посредством ссылки).
[0156] Пороговое значение, превышающее или равное 80 мкМ, для уровней tHcy для приемлемости для лечения было выбрано здесь во избежание исключения пациентов с предшествующими уровнями tHcy в плазме, составляющими приблизительно 100 мкМ, учитывая индивидуальную вариабельность, составляющую 25%, уровней tHcy в плазме, проверенных с промежутком в несколько месяцев (смотрите Refsum et al. Clin Chem 2004; 50:3-32; Guttormsen et al., J Clin Invest. 1996, 98(9):2174-83; каждый из которых полностью включен таким образом посредством ссылки), чтобы обеспечить уровни, достаточно высокие для обнаружения клинически значимых снижений у небольшого числа пациентов. Составляющая 25% индивидуальная вариабельность уровней tHcy в плазме, проверенных с промежутком в несколько месяцев, (смотрите Refsum et al. Clin Chem 2004; 50:3-32; Guttormsen et al., J Clin Invest. 1996, 98(9):2174-83; каждый из которых полностью включен таким образом посредством ссылки) может быть частично связана со сменами диеты, лекарственных средств или добавок у пациентов с CBSDH с течением времени.
[0157] В отсутствие лечения прогноз для пациентов с CBSDH, не чувствительной к пиридоксину, является мрачным (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74, который полностью включен таким образом посредством ссылки). В 1985 году международное ретроспективное исследование, в ходе которого документировали естественное течение CBSDH у 629 пациентов, путем анализа времени до события перед лечением показало, что 70% пациентов имеют смещение хрусталика к возрасту 10 лет, а у 85% симптомы развиваются к 12 годам (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31; Mudd et al., Skovby F. Disorders of transsulfuration. In: Scriver CL, Beaudet AL, Sly WS, Valle D, eds. The Metabolic and Molecular Basis of Inherited Diseases. 7 ed. New York: McGraw Hill; 2001; 1279-1327, оба из которых полностью включены таким образом посредством ссылки). В целом, у 50% пораженных индивидуумов к 15 годам рентгенологически определялся остеопороз позвоночника, а 23% пациентов, не чувствительных к пиридоксину, (4% чувствительных пациентов) умерли к 30 годам (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31, который полностью включен таким образом посредством ссылки).
[0158] Взятые в целом, имеющиеся данные указывают на то, что современные подходы к лечению CBSDH, включающие ограничительную диету и применение пищевых добавок, являются неэффективными для остановки прогрессирования заболевания у большинства пациентов. Следовательно, существует существенная неудовлетворенная медицинская потребность в идентификации хорошо переносимых терапий, которые будут уменьшать или нормализовать метаболические нарушения при CBSDH и замедлят или остановят прогрессирование клинических проявлений заболевания.
[0159] Наблюдалось причинно-следственная связь между повышенными уровнями Hcy и ключевыми клиническими последствиями CBSDH, включающими осложнения на глаза (в частности, смещение хрусталика), последствия для костной системы (в частности, остеопороз), сердечнососудистые события (в частности, инсульт и заболевание мелких сосудов) и различные последствия для ЦНС (в частности, когнитивной функции). Взаимосвязь между повышенными уровнями tHcy и негативными клиническими последствиями и, наоборот, снижением уровней Hcy и уменьшением клинических последствий дополнительно подтверждается многочисленными исследованиями в общей популяции. В целом, эти клинические данные подчеркивают необходимость ранней диагностики CBSDH и быстрого лечения для снижения уровней Hcy как можно ближе к норме.
[0160] Хотя не было опубликовано исследований качества жизни (QoL) пациентов с CBSDH, в неопубликованных сообщениях указывается на то, что пациенты и лица, осуществляющие уход за ними, страдают от психосоциальных последствий соблюдения и принятия строго ограниченной и социально изолирующей диеты и крайне обеспокоены отдаленными медицинскими последствиями заболевания. Неудивительно, что пациенты стремятся к возможности смягчить свои диеты, не ставя под угрозу их долгосрочные планы на будущее.
[0161] Сильная взаимосвязь между уровнями tHcy и ключевыми клиническими последствиями у пациентов с CBSDH показывает, что изменение уровней tHcy является надежным косвенным маркером комбинации клинических конечных точек при CBSDH. Следовательно, изменения уровней tHcy применимы для (i) мониторинга течения заболевания у пациента в клинике и (ii) прогнозирования клинической пользы от новых терапий в клинических испытаниях, и (ii) прогнозирования эффективности терапии.
[0162] Например, готовая лекарственная форма нормализует или увеличивает гибкость бедренной артерии у субъекта по сравнению с состоянием до введения готовой лекарственной формы субъекту. Например, мыши I278T имеют значительно более низкую гибкость бедренной артерии по сравнению с мышами дикого типа. Диета с ограничением Met может фактически привести к меньшему диаметру бедренной артерии у мышей с I278T по сравнению с обычной диетой как у мышей, получавших готовую лекарственную форму лекарственные продукты, так и у мышей, не получающих ее.
[0163] Исследования, ранее проведенные на 3 моделях заболевания на мышах, продемонстрировали, что htCBS C15S эффективна после системного введения, как описано в WO 2017/083327, которая полностью включена таким образом посредством ссылки. Эти исследования показали составляющее вплоть до 90% снижение экстраклеточного уровня Hcy в плазме и внутриклеточного уровня Hcy в ткани, такой как головной мозг. Было замечено, что введение готовой лекарственной формы приводит к градиенту концентрации с изменением Hcy от более высоких концентраций во внутриклеточном пространстве к более низким концентрациям в экстраклеточном пространстве, где готовая лекарственная форма может его дополнительно процессировать. Экстраклеточная ПЭГилированная htCBS C15S служит «поглотителем» Hcy. В заключение, готовая лекарственная форма восстанавливала контроль над путем метаболизма Met в моделях CBSDH на животных.
[0164] Эти исследования также показали, что подкожное введение доз ПЭГилированной htCBS C15S в моделях CBSDH на мышах корректировало уровни метаболитов, включая повышение уровней Cth и нормализацию уровней Cys. Кроме того, ПЭГилированная htCBS C15S положительно влияла на фенотипическое проявление заболевания у мышей, в том числе выпадение волос на лице, гистологию печени, остеопороз, состав тела, диабетическую ретинопатию (возможно, вторичную по отношению к заболеванию почек) и эритематозную анетодермию и атрофию зрительного нерва из-за окклюзии сосудов сетчатки или неартериальной ишемической нейропатии зрительного нерва, уровни цитокинов и липидов. ПЭГилированная htCBS C15S также спасала мышей с нокаутом (KO) CBS от ранней смерти (смотрите Looker et al. Diabetologia 2003; 46:766-772; Pusparajah et al. Front Physiol 2016; 7:200; Gerth et al. J AAPOS 2008; 12:591-596; Stanger et al. Clin Chem Lab Med 2005; 43:1020-1025; Cahill et al. Am J Ophthalmol 2003; 136:1136-1150; Minniti et al. Eur J Ophthalmol 2014; 24:735-743; каждый из которых полностью включен таким образом посредством ссылки). Также было замечено, что ПЭГилированная htCBS C15S хорошо переносится без каких-либо токсикологических эффектов, отмечаемых при постоянном введении доз в моделях заболевания на животных.
[0165] ПЭГилированная htCBS C15S действует в экстраклеточном пространстве и, как ожидается, снижает концентрации tHcy в плазме независимо от генетики пациентов, сопутствующей терапии или исходного уровня tHcy. Таким образом, подходящая популяция для исследования должна включать как пациентов, чувствительных к пиридоксину, так и пациентов, не чувствительных к нему.
[0166] У здоровых индивидуумов уровни tHcy находятся в диапазоне от приблизительно 5 до 15 мкМ (OECD Environmental Health and Safety Publications. Series on Principles of Good Laboratory Practice and Compliance Monitoring. No. 1 ENV/MC/CHEM(98)17 "Principles of Good Laboratory Practice (пересмотренные в 1997 г.), который полностью включен таким образом посредством ссылки), при этом 98% tHcy находятся в форме дисульфидов или связаны с белком. Только 2% tHcy существует в виде несвязанного, свободного, восстановленного аминотиола, который может служить субстратом для фермента (смотрите EMA: Guideline on bioanalytical method validation, EMEA/CHMP/EWP/192217/2009, ev. 1, 21 July 2011; ATL-15-1419 Atlanbio Study Report «LC-MS/MS determination of cystathionine-D4 as product of the cystathionine β-synthase activity in monkey plasma samples collected during the study 529736»; оба из которых полностью включены таким образом посредством ссылки). С другой стороны пациенты с CBSDH не только имеют уровни в плазме, которые могут достигать 400 мкМ и более, но также демонстрируют резко измененный баланс, при этом уровень восстановленного гомоцистеина достигает 10-25% от значений tHcy.
[0167] В моделях на мышах введение ПЭГилированной htCBS C15S приводило к снижению уровней tHcy вплоть до 90%. Таким образом, начальные уровни восстановленного гомоцистеина, доступные для фермента, (10-25% от общего количества) не могут быть единственными причинами значительного снижения уровней tHcy, которые были зарегистрированы, и ферменту должны стать доступны дополнительные пулы. Например, когда восстановленный Hcy становится дефицитным в результате активности PEG htCBS, баланс между восстановленным Hcy и аддуктами Hcy (в форме связанного с белком Hcy или дисульфидов) в плазме изменяется в сторону образования восстановленного Hcy, который может далее процессироваться ферментом.
А. Осложнения на зрительную систему
[0168] Повышенные уровни Hcy являются сильным и независимым фактором риска осложнений на зрительную систему, в частности смещения хрусталика, у пациентов с CBSDH и в общей популяции. Даже при назначении фармакологических вмешательств и диетотерапий у большинства пациентов с CBSDH в конечном итоге возникают осложнения на глаза. Было установлено, что снижение уровней Hcy задерживает и, возможно, предотвращает смещение хрусталика у пациентов с CBSDH (смотрите Yap S. Homocystinuria due to cystathionine beta-synthase deficiency. Orphanet Encyclopaedia [периодическое издание онлайн] 2005; Mudd et al. Am J Hum Genet 1985; 37:1-31; Martinez-Gutierrez et al. Int Ophthalmol (2011) 31:227-232; Ajith et al. Clin Chim Acta 2015; 450:316-321; Mulvihill et al. J AAPOS 2001; 5:311-315; Marti-Carvajal et al. Cochrane Database Syst Rev 2015;1:CD006612; Sweetser et al. N Engl J Med 2016, 375:1879-1890; Sadiq et al. Semin Ophthalmol 2013; 28:313-320; Wright et al. Homocysteine, folates, and the eye. Eye (Lond) 2008; 22:989-993; Lieberman et al. Am J Ophthalmol 1966, 61:252-255; Harrison et al. Ophthalmology 1998, 105:1886-1890; Ramsey et al. Am J Ophthalmol 1972; 74:377-385; Couser et al. Ophthalmic Genet 2017, 38:91-94; Ghorbanihaghjo et al. Mol Vis 2008, 14:1692-1697; Javadzadeh et al. Mol Vis 2010; 16:2578-2584; Seddon et al. Am J Ophthalmol 2006; 141:201-203; Coral et al. Eye (Lond) 2006; 20:203-207; Axer-Siegel et al. Am J Ophthalmol 2004, 137:84-89; Heuberger et al. Am J Clin Nutr 2002; 76:897-902; Huang et al. Sci Rep 2015; 5:10585; Sen et al. Indian J Clin Biochem 2008; 23:255-257; Yousefi et al. Protein Pept Lett 2013; 20:932-941; Gerth et al. J AAPOS 2008; 12:591-596; Stanger et al. Clin Chem Lab Med 2005, 43:1020-1025; Cahill et al. Am J Ophthalmol 2003, 136:1136-1150; Minniti et al. Eur J Ophthalmol 2014, 24:735-743; Turkcu et al. Medicina (Kaunas) 2013, 49:214-218; Vessani et al. Am J Ophthalmol 2003; 136:41-46; Leibovitch et al. J Glaucoma 2003, 12:36-39; Leibovitzh et al. Medicine (Baltimore) 2016;95:e4858; Micheal et al. Mol Vis 2009; 15:2268-2278; Clement et al. J Glaucoma 2009; 18:73-78; Cumurcu et al. BMC Ophthalmol 2006; 6:6; Bleich et al. J Neural Transm (Vienna) 2002;109:1499-1504; Lee et al. Curr Eye Res 2017; 1-6; Wang et al. Am J Ophthalmol 2004; 137:401-406; Ganapathy et al. Invest Ophthalmol Vis Sci 2009; 50:4460-4470, каждый из которых полностью включен таким образом посредством ссылки). Даже при назначении фармакологических вмешательств и диетотерапий у большинства пациентов с CBSDH в конечном итоге возникают осложнения на глаза. Было установлено, что снижение уровня Hcy задерживает и, возможно, предотвращает смещение хрусталика у пациентов с CBSDH (смотрите Mulvihill et al. J AAPOS 2001; 5:311-315, который полностью включен таким образом посредством ссылки).
[0169] Одним из наиболее постоянно присутствующих и самых ранних проявлений CBSDH является эктопия хрусталика (смещение хрусталика) (смотрите Mulvihill et al. J AAPOS 2001; 5:311-315, который полностью включен таким образом посредством ссылки). Она обычно возникает в возрасте после двух лет и присутствует у приблизительно 50% не подвергнутых лечению, не чувствительных к пиридоксину пациентов к шести годам и у 50% не подвергнутых лечению пациентов, чувствительных к пиридоксину пациентов к 10 годам (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31, который полностью включен таким образом посредством ссылки). Смещение может быть частичным (неполное смещение) или полным, и, хотя оно может происходить книзу или к носу, оно обычно бывает двусторонним (смотрите Mulvihill et al. J AAPOS 2001; 5:311-315; Sweetser et al. N Engl J Med 2016; 375:1879-1890, оба из которых полностью включены таким образом посредством ссылки).
[0170] Смещение хрусталика часто следует за периодом быстро прогрессирующей миопии, что может привести к выраженному астигматизму, монокулярной диплопии и снижению максимально скорректированной остроты зрения (смотрите Sadiq et al. Semin Ophthalmol 2013; 28:313-320, который полностью включен таким образом посредством ссылки). В целом, миопия (диоптрии [D] более 1), как полагают, поражает приблизительно 85% пациентов с CBSDH, а миопия очень высокой степени (более 5D) поражает от 50 до 76% пациентов. Иридодонез (дрожание радужной оболочки после движения глазного яблока) поражает приблизительно 56% пациентов, а сферофакия (небольшой сферический хрусталик, склонный к неполному смещению) поражает 50% пациентов (смотрите Yap S. Homocystinuria due to cystathionine beta-synthase deficiency. Orphanet Encyclopaedia [периодическое издание онлайн] 2005; Mulvihill et al. J AAPOS 2001; 5:311-315, каждый из которых полностью включен таким образом посредством ссылки). Дополнительные осложнения, связанные с CBSDH, включают развитие катаракты, хронический витрит (воспаление стекловидного тела) и хориоретинальное воспаление, блокаду зрачка в случае острой и/или хронической закрытоугольной глаукомы и (у детей) амблиопию (ленивый глаз) (смотрите Sadiq et al. Semin Ophthalmol 2013; 28:313-320, который полностью включен таким образом посредством ссылки).
[0171] Данные длительного ретроспективного исследования на 25 пациентах в возрасте до 24 лет с CBSDH позволяют предположить, что смещение хрусталика можно предотвратить или, по крайней мере, значительно уменьшить и отсрочить у пациентов, у которых уровни tHcy постоянно снижают с раннего возраста (смотрите Yap et al. J Inherit Metab Dis 1998;21:738-747, который полностью включен таким образом посредством ссылки). Раннее понижающее уровень Hcy лечение также было связано со снижением риска общих осложнений на глаза, в том числе усугубления миопии. Подтверждающие данные получены из исследования методом «случай-контроль» на 32 пациентах с CBSDH и 25 сибсах в качестве контролей, в котором раннее понижающее уровень Hcy лечение было связано со значительным уменьшением осложнений на глаза по сравнению с пациентами, которые подвергались лечению в более позднем возрасте или не полностью соблюдали схему лечения (смотрите El Bashir et al. JIMD Rep 2015; 21:89-95, который полностью включен таким образом посредством ссылки).
[0172] Крупнейшее и самое продолжительное на сегодняшний день продольное исследование последствий на здоровье зрительной системы у 25 пациентов с дефицитом кобаламина С, который равно характеризуется повышенными уровнями tHcy, показало, что все из дегенерации желтого пятна, бледности диска зрительного нерва, нистагма, косоглазия и сосудистых изменений присутствует у большинства пациентов.
[0173] Многочисленные исследования пациентов с CBSDH и общей популяции продемонстрировали взаимосвязь между повышенными уровнями Hcy и рядом глазных болезней (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31; Ajith, Clin Chim Acta 2015; 450:316-321; Mulvihill et al. J AAPOS 2001; 5:311-315; Wright et al. Eye (Lond) 2008; 22:989-993, каждый из которых полностью включен таким образом посредством ссылки), включающих миопию и смещение хрусталика (смотрите Yap S. Homocystinuria due to cystathionine beta-synthase deficiency. Orphanet Encyclopaedia [периодическое издание онлайн] 2005; Mudd et al. Am J Hum Genet 1985; 37:1-31; Martinez-Gutierrez et al. Int Ophthalmol 2011; 31:227-232; Suri et al. J Neurol Sci 2014; 347:305-309; Mulvihill et al. J AAPOS 2001; 5:311-315; Lieberman et al. Am J Ophthalmol 1966; 61:252-255; Harrison et al. Ophthalmology 1998; 105:1886-1890; Ramsey et al. Am J Ophthalmol 1972; 74:377-385; Couser et al. Ophthalmic Genet 2017; 38:91-94; каждый из которых полностью включен таким образом посредством ссылки), иридодонез (смотрите Mulvihill et al. J AAPOS 2001; 5:311-315, который полностью включен таким образом посредством ссылки), артериосклероз сетчатки (смотрите Ghorbanihaghjo et al. Mol Vis 2008; 14:1692-1697, который полностью включен таким образом посредством ссылки), возрастную дегенерацию желтого пятна (смотрите Javadzadeh et al. Mol Vis 2010; 16:2578-2584; Seddon et al. Am J Ophthalmol 2006; 141:201-203; Coral et al. Eye (Lond) 2006; 20:203-207; Axer-Siegel et al. Am J Ophthalmol 2004; 137:84-89, каждый из которых полностью включен таким образом посредством ссылки), возрастную макулопатию (AMD) (смотрите Heuberger et al. Am J Clin Nutr 2002; 76:897-902; Huang et al. Sci Rep 2015; 5:10585, оба из которых полностью включены таким образом посредством ссылки), катаракты (смотрите Sen et al. Indian J Clin Biochem 2008; 23:255-257; Yousefi et al. Protein Pept Lett 2013; 20:932-941, оба из которых полностью включены таким образом посредством ссылки), диабетическую ретинопатию (возможно, вторичную по отношению к заболеванию почек) (смотрите Looker et al. Diabetologia 2003; 46:766-772; Pusparajah et al. Front Physiol 2016; 7:200, оба из которых полностью включены таким образом посредством ссылки) и эритематозную анетодермию и атрофию зрительного нерва из-за окклюзии сосудов сетчатки или неартериальной ишемической нейропатии зрительного нерва (смотрите Gerth et al. J AAPOS 2008; 12:591-596; Stanger et al. Clin Chem Lab Med 2005; 43:1020-1025; Cahill et al. Am J Ophthalmol 2003; 136:1136-1150; Minniti et al. Eur J Ophthalmol 2014; 24:735-743; каждый из которых полностью включен таким образом посредством ссылки).
[0174] Ретроспективное исследование 629 пациентов с CBSDH показало, что смещение хрусталика обычно возникает в возрасте после двух лет и присутствует у приблизительно у 50% не подвергнутых лечению пациентов, не чувствительных к пиридоксину, к шести годам и у 50% не подвергнутых лечению пациентов, чувствительных к пиридоксину, в возрасте 10 лет (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31, который полностью включен таким образом посредством ссылки). Крупнейшее и самое продолжительное на сегодняшний день продольное исследование последствий на здоровье зрительной системы у 25 пациентов с дефицитом кобаламина С, который равно характеризуется повышенными уровнями tHcy, показало, что все из дегенерации желтого пятна, бледности диска зрительного нерва, нистагма, косоглазия и сосудистых изменений присутствует у большинства пациентов (смотрите Brooks et al. Ophthalmology. 2016 Mar; 123(3):571-82, который полностью включен таким образом посредством ссылки).
[0175] Многочисленные исследования как пациентов с CBSDH, так и общей популяции продемонстрировали взаимосвязь между повышенными уровнями Hcy и рядом глазных болезней (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31; Ajith TA, Ranimenon. Clin Chim Acta 2015; 450:316-321; Mulvihill et al. J AAPOS 2001; 5:311-315; Wright et al. Eye (Lond) 2008; 22:989-993; каждый из которых полностью включен таким образом посредством ссылки), включающих миопию и смещение хрусталика (смотрите Yap S. Homocystinuria due to cystathionine beta-synthase deficiency. Orphanet Encyclopaedia [периодическое издание онлайн] 2005; Mudd et al. Am J Hum Genet 1985; 37:1-31; Martinez-Gutierrez et al. Int Ophthalmol 2011; 31:227-232; Mulvihill et al. J AAPOS 2001; 5:311-315; Sadiq et al. Semin Ophthalmol 2013; 28:313-320; Lieberman et al. Am J Ophthalmol 1966; 61:252-255; Harrison et al. Ophthalmology 1998; 105:1886-1890; Ramsey et al. Am J Ophthalmol 1972; 74:377-385; Couser et al. Ophthalmic Genet 2017;38:91-94, каждый из которых полностью включен таким образом посредством ссылки), иридодонез (смотрите Mulvihill et al. J AAPOS 2001;5:311-315, который полностью включен таким образом посредством ссылки), артериосклероз сетчатки (смотрите Ghorbanihaghjo et al. Mol Vis 2008; 14:1692-1697, который полностью включен таким образом посредством ссылки), возрастную дегенерацию желтого пятна (смотрите Javadzadeh et al. Mol Vis 2010; 16:2578-2584; Seddon et al. Am J Ophthalmol 2006; 141:201-203; Coral et al. Eye (Lond) 2006; 20:203-207; Axer-Siegel et al. Am J Ophthalmol 2004; 137:84-89; каждый из которых полностью включен таким образом посредством ссылки), возрастную макулопатию (AMD) (смотрите Heuberger et al. Am J Clin Nutr 2002; 76:897-902; Huang et al. Sci Rep 2015; 5:10585, оба из которых полностью включены таким образом посредством ссылки), катаракты (смотрите Sen et al. Indian J Clin Biochem 2008; 23:255-257; Yousefi et al. Protein Pept Lett 2013;20:932-941, оба из которых полностью включены таким образом посредством ссылки), диабетическую ретинопатию (возможно, вторичную по отношению к заболеванию почек) (смотрите Looker et al. Diabetologia 2003; 46:766-772; Pusparajah et al. Front Physiol 2016; 7:200, оба из которых полностью включены таким образом посредством ссылки) и эритематозную анетодермию и атрофию зрительного нерва из-за окклюзии сосудов сетчатки или неартериальной ишемической нейропатии зрительного нерва (смотрите Gerth et al. J AAPOS 2008; 12:591-596; Stanger et al. Clin Chem Lab Med 2005; 43:1020-1025; Cahill et al. Am J Ophthalmol 2003; 136:1136-1150; Minniti et al. Eur J Ophthalmol 2014; 24:735-743; каждый из которых полностью включен таким образом посредством ссылки).
[0176] Исследования, изучающие связь между уровнями Hcy и глаукомой, дали противоречивые результаты. Некоторые показали положительную связь между уровнями Hcy и глаукомой с нормальным давлением, псевдоэксфолиативной глаукомой (PEXG) и первичной открытоугольной глаукомой (POAG), в то время как другие не показали эту связь (смотрите Lieberman et al. Am J Ophthalmol 1966; 61:252-255; Turkcu et al. Medicina (Kaunas) 2013; 49:214-218; Vessani et al. Am J Ophthalmol 2003;136:41-46; Leibovitch et al. J Glaucoma 2003; 12:36-39; Leibovitzh et al. Relationship between homocysteine and intraocular pressure in men and women: A population-based study. Medicine (Baltimore) 2016; 95:e4858; Micheal et al. Mol Vis 2009; 15:2268-2278; Clement et al. J Glaucoma 2009; 18:73-78; Cumurcu et al. BMC Ophthalmol 2006;6:6; Bleich et al. J Neural Transm (Vienna) 2002;109:1499-1504; Lee et al. Curr Eye Res 2017; 1-6; Wang et al. Am J Ophthalmol 2004; 137:401-406; каждый из которых полностью включен таким образом посредством ссылки). Однако утрата ганглиозных клеток сетчатки (RGC) - частое наблюдение у индивидуумов с глаукомой - была продемонстрирована у мышей с эндогенно повышенными уровнями Hcy, вызванными делецией гена CBS, что указывает на вероятную связь между глаукомой и повышенными уровнями tHcy у пациентов с CBSDH (смотрите Ganapathy et al. Invest Ophthalmol Vis Sci 2009; 50:4460-4470, который полностью включен таким образом посредством ссылки).
1. Механизм
[0177] Был предложен ряд механизмов для объяснения эффектов повышенных уровней Hcy на здоровье глаз (смотрите Ajith TA, Ranimenon; Clin Chim Acta 2015;450:316-321, который полностью включен таким образом посредством ссылки). Механизмы, объясняющие эффекты повышенных уровней tHcy, включают нарушение функции эндотелия сосудов, апоптоз ганглиозных клеток сетчатки, изменения экстраклеточного матрикса, снижение активности лизилоксидазы и окислительный стресс, а также прямые цитотоксические и провоспалительные эффекты Hcy, которые, по-видимому, способствуют помутнение хрусталика и повреждению зрительного нерва.
[0178] Возможные механизмы также включают активацию рецептора N-метил-D-аспартата (NMDA), что приводит к притоку кальция в клетку и увеличению продукции активных форм кислорода (ROS), оба из которых способствуют развитию катаракты. Эти изменения, наряду с прямыми цитотоксическими эффектами Hcy, могут вызывать повреждение эндотелия, которое инициирует тромбообразование и апоптоз RGC, что приводит к ретинопатии и глаукоме. Также было показано, что повышенные уровни Hcy повышают уровни асимметричного диметиларгинина (AMDA) и блокируют активность синтазы оксида азота (NOS), тем самым вызывая сужение сосудов и атрофию зрительного нерва за счет снижения уровней оксида азота (NO). Наконец, накопление гомоцистеинилированных белков в сосудистой стенке может запускать продукцию антител против Hcy и воспалительные реакции, что приводит к фагоцитозу, окислительному стрессу, апоптозу RGC и изменениям экстраклеточного матрикса (ECM). В совокупности такие изменения повреждают сосудистую сеть, белки хрусталика и зрительный нерв, что в конечном итоге вызывает нарушение зрительной функции.
[0179] Считается, что у пациентов с CBSDH смещение хрусталика в первую очередь вызвано дегенеративными изменениями волокон пояска, в частности богатых Cys мультидоменных белков ECM, таких как фибриллин-1 (смотрите Sadiq et al. Semin Ophthalmol 2013; 28:313-320; Hubmacher et al. Biochemistry 2011; 50:5322-5332; Hubmacher et al. J Biol Chem 2005; 280:34946-34955; Hubmacher et al. J Biol Chem 2010; 285:1188-1198; каждый из которых полностью включен таким образом посредством ссылки).
[0180] У здоровых людей образование многочисленных внутридоменных дисульфидных связей внутри фибриллина-1 обеспечивает точную укладку белка, необходимую для структурной целостности и функционирования. Нити фибриллина-1 могут затем образовывать межцепочечные дисульфидные связи, что приводит к сборке высокомолекулярных многобелковых агрегатов, известных как микрофибриллы (смотрите Kinsey et al. J Cell Sci 2008; 121:2696-2704; Hubmacher et al. Proc Natl Acad Sci USA 2008; 105:6548-6553, оба из которых полностью включены таким образом посредством ссылки).
[0181] Этот процесс очень зависит от взаимодействия между фибриллином-1 и фибронектином (смотрите Hubmacher et al. Biochemistry 2011; 50:5322-5332, который полностью включен таким образом посредством ссылки). Микрофибриллы образуют каркас для отложения тропоэластина, что является важной стадией образования эластических волокон, таких как волокна, обнаруживаемые в коже, легких, кровеносных сосудах/артериях, связках и глазу (смотрите Hubmacher et al. J Biol Chem 2010; 285:1188-1198, который полностью включен таким образом посредством ссылки). Важность фибриллина-1 иллюстрируют пациенты с синдромом Марфана - состоянием, вызванным мутацией(ями) в гене фибриллина-1, - при котором нарушение функция соединительной ткани связано с такими симптомами, как смещение хрусталика, пролапс органов, остеопороз и гиперподвижность суставов (смотрите Suk et al. J Biol Chem 2004; 279:51258-51265; Collod-Beroud et al. Hum Mutat 2003; 22:199-208, оба из которых полностью включены таким образом посредством ссылки).
[0182] Исследования in vitro показали, что добавление Hcy к фибриллину-1 нарушало образование дисульфидных связей, что, в свою очередь, приводило к аномальной укладке белка, повышенной чувствительности к протеолитической деградации и аномальному образованию ECM (экстраклеточного матрикса) и эластических волокон (смотрите Hubmacher et al. J Biol Chem 2010; 285:1188-1198; Whiteman et al. Antioxid Redox Signal 2006; 8:338-346, оба из которых полностью включены таким образом посредством ссылки). Добавление Hcy к фибробластам кожи человека также было связано с редуцированными формами фибронектина, которые неоптимально связывались с фибриллином-1, тем самым предотвращая образование микрофибрилл (смотрите Hubmacher et al. Biochemistry 2011; 50:5322-5332; Hubmacher et al. J Biol Chem 2010; 285:1188-1198, оба из которых полностью включены таким образом посредством ссылки).
[0183] Помимо смещения (вывиха) хрусталика, дегенерация волокон пояска у пациентов с CBSDH может привести к увеличению кривизны хрусталика, хрусталиковой близорукости, астигматизму, отслоению сетчатки, косоглазию, катарактам и иридодонезу (смотрите Sadiq et al. Semin Ophthalmol 2013; 28:313-320, который полностью включен таким образом посредством ссылки). В отсутствие лечения передний вывих хрусталика может вызвать острый приступ глаукомы со зрачковым блоком. В крайних случаях полное смещение хрусталика связано с увеличением длины глаза по оси, что, возможно, является компенсаторной реакцией на нечеткость зрения (смотрите Mulvihill et al. J AAPOS 2001; 5:311-315, который полностью включен таким образом посредством ссылки).
[0184] Ретроспективное исследование было проведено на 25 случаях CBSDH, выявленных в Ирландии в период с 1971 по 1996 год либо в рамках национальной программы NBS, либо по клинической картине, для изучения эффектов понижающей уровень Hcy терапии на клинические последствия (смотрите Yap et al. J Inherit Metab Dis 1998; 21:738-747, который полностью включен таким образом посредством ссылки). Большинство случаев (24/25) не были чувствительны к пиридоксину. Следовательно, лечение большинства пациентов состояло из не содержащей Met диеты с добавлением Cys, с добавками витамина B12 и соли фолиевой кислоты, если это необходимо. Лечение начинали до 6-недельного возраста пациентов и сравнивали с другой группой, в случае которой лечение начиналось после постановки диагноза, и с одним контрольным пациентом, которого никогда не подвергали лечению. Средний период наблюдения составил 14,3 года (от 2,5 до 23,4) в группах, получавших лечение до 6-недельного возраста, и 14,7 года (от 11,7 до 18,8) для остальных пациентов, что в сумме составило 365,7 пациенто-лет лечения. Из 21 пациента, выявленного с помощью NBS, у 18 не было осложнений во время лечения. Из этих индивидуумов 15/18 имели зрение 20:20, а 3/18 страдали прогрессирующей миопией в течение предыдущих двух лет.
[0185] В соответствии с данными Mudd и др. (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31, который полностью включен таким образом посредством ссылки), смещение хрусталика у индивидуумов с поздней постановкой диагноза возникает в приблизительно двухлетнем возрасте. Смещение хрусталика не было зарегистрировано ни у одного из рано подвергнутых лечению индивидуумов, которые удовлетворительно соблюдали схему терапии. У трех из «рано подвергнутых лечению пациентов» (имеющих самые высокие уровни fHcy) наблюдалось увеличение степени миопии без смещения хрусталика, что, скорее всего, было обусловлено относительно высокими уровнями fHcy в этой небольшой группе пациентов. Это привело авторов к предположению, что прогрессирующая миопия может быть первым признаком, предшествующим смещению хрусталика, неудовлетворительного соблюдения диеты, несмотря на то, что пациент настаивает на обратном. Увеличение степени миопии у этих пациентов подчеркивает, насколько тонким является баланс между нейтральными и негативными клиническими последствия у этих пациентов. У всех поздно выявленных пациентов развилась эктопия хрусталика. Это позволяет предположить, что лечение может отсрочить начало смещения хрусталика, а не предотвратить его.
[0186] Медианные за всю жизнь уровни fHcy в плазме были выше у пациентов с миопией, чем у пациентов без нее (18, 18 и 48 мкмоль/л в сравнение с 11 мкмоль/л, соответственно). Из трех пациентов, выявленных с помощью NBS, у которых развились осложнения в группе, лечение которой было начато после постановки диагноза, все не соблюдали диету. В целом, у 6 из 24 пациентов было смещение хрусталика; из них двое имели рано поставленный диагноз, но не соблюдали диету, а четверо имели поздно поставленный диагноз, в том числе один пациент, который никогда не подвергался лечению. В соответствии с данными Mudd и др. (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31, который полностью включен таким образом посредством ссылки), смещение хрусталика у индивидуумов с поздно поставленным диагнозом (т.е. у пациентов, демонстрирующих осложнения после 2-летнего возраста) возникало приблизительно в двухлетнем возрасте. На момент публикации исследования о смещении хрусталика не сообщил ни один из рано подвергнутых лечению индивидуумов, которые удовлетворительно соблюдали схему терапии.
[0187] Соблюдающие схему лечения пациенты сохраняли свои уровни fHcy на эквивалентных уровнях tHcy, значительно ниже 120 мкмоль/л. Однако на момент публикации все пациенты были моложе 24 лет, и многие из них все еще были педиатрическими пациентами. Было установлено, что соблюдение диеты с ограничением белка быстро ухудшается от подросткового возраста к зрелому возрасту. Описанный выше хрупкий баланс предполагает, что умеренное снижение уровней tHcy, достигнутое этими пациентами, может отсрочить появление симптомов, а не предотвратить их по мере старения этих пациентов.
[0188] Эти результаты (смотрите Yap et al. J Inherit Metab Dis 1998; 21:738-747; Mudd et al. Am J Hum Genet 1985; 37:1-31; каждый из которых полностью включен таким образом посредством ссылки) были подтверждены результатами схожего исследования методом «случай-контроль», проведенного в Катаре, в котором сообщалось об последствиях, включающих нарушение зрения, в 32 случаях CBSDH и у 25 сибсов в качестве контролей (смотрите El Bashir et al. JIMD Rep 2015; 21:89-95), который полностью включен таким образом посредством ссылки). Средний возраст субъектов составлял 11,2 года (диапазон: от 0,6 до 29 лет), и 56% из них были мужчинами. В целом, 9 из 32 случаев (28%) были диагностированы с помощью NBS и подвергнуты лечению в первый месяц жизни. У остальных диагноз был поставлен в возрасте от 14 до 240 месяцев. Уровни tHcy и Met были значительно ниже среди тех, кому диагноз был поставлен с помощью NBS, по сравнению с теми, кого диагностировали клинически. Возможно, это связано с лучшим соблюдением диеты и приема лекарственных средств в раннем возрасте. Ни в одном из 9 случаев, выявленных с помощью NBS, не было проблем со зрением на момент публикации исследования, по сравнению с 18 (78%) в группе с поздно поставленным диагнозом (p<0,001 между группами). Однако, как и в ирландском исследовании 25 пациентов, описанном выше, возраст пациентов в этом исследовании варьировался от 0,6 до 29 лет, и отдаленные осложнения еще не известны.
[0189] Сравнение данных Yap и Naughten (смотрите Yap et al. J Inherit Metab Dis 1998; 21:738-747, который полностью включен таким образом посредством ссылки) с кривыми Каплана-Мейера, полученными Mudd и др., показало, что доля соблюдающих схему лечения, «рано подвергнутых лечению»» пациентов со смещением хрусталика и остеопорозом была значительно ниже, чем ожидалось для не подвергнутых лечению пациентов с CBSDH (p≤0,001).
[0190] Поэтому повышенный уровень Hcy считается сильным и независимым фактором риска осложнений на глаза, в частности смещения хрусталика, у пациентов с CBSDH и в общей популяции (например, как показано в Yap et al. и Mudd et al.Yap et al.). Это подчеркивает необходимость ранней диагностики и лечения CBSDH, а также соблюдения схемы лечения пациентом.
B. Осложнения на костную систему
[0191]. CBSDH связана с повышенным риском переломов при остеопорозе, что может быть частично обусловлено низкой минеральной плотностью костной ткани (смотрите Mudd et al. и Weber et al. Mol Genet Metab 2016; 117:351-354; каждый из которых полностью включен таким образом посредством ссылки).
[0192] Ретроспективный обзор данных в виде амбулаторных карт 19 пациентов с CBSDH за 8 лет показал, что низкая минеральная плотность костной ткани (BMD) была распространена как у детей, так и у взрослых пациентов с CBSDH (смотрите Weber et al.). Это исследование позволило предположить, что прирост костной массы в детстве и подростковом возрасте, критическом периоде для роста костной системы, является недостаточным при CBSDH и может негативно повлиять на достижение максимальной величины костной массы. Это исследование также подчеркнуло, что даже соблюдающие диету пациенты с умеренно повышенными уровнями tHcy, всего в 5 раз превышающими нормальный диапазон, уже страдают от плохих клинических последствий для здоровья костной системе в детстве.
[0193] Согласно Mudd и др., у 80% пациентов с CBSDH развивается остеопороз в возрасте до 30 лет. Более того, повышенные уровни Hcy связаны с повышенным риском переломов при остеопорозе даже у пациентов без CBSDH (смотрите Sato et al. Bone 2005, 36:721-726; van Meurs et al. N Engl J Med 2004; 350:2033-2041; McLean et al. N Engl J Med 2004; 350:2042-2049; каждый из которых полностью включен таким образом посредством ссылки).
[0194] Ретроспективный обзор данных в виде амбулаторных карт 19 субъектов (9 мужчин в возрасте от 3,5 до 49,2 лет), прошедших клиническую денситометрию костной ткани с помощью DXA в период с 2002 по 2010 год, показал, что низкая BMD была распространена как у детей, так и у взрослых пациентов с CBSDH (смотрите Weber et al. Mol Genet Metab 2016;117:351-354, который полностью включен таким образом посредством ссылки). Во время первого DXA-сканирования средняя Z-оценка BMD поясничного отдела позвоночника (LS) составляла -1,2±1,3, а общая Z-оценка BMD тазобедренного сустава составляла -0,89±0,4; обе оценки были значительно ниже 0 (ожидаемой средней Z-оценки в общей популяции) с p=0,002 и 0,02, соответственно. Z-оценка BMD LS при постановке диагноза составляла -1,26±1,4 у пациентов в возрасте до 21 года и -1,06±1,1 у взрослых. В целом, 38% пациентов имели низкую BMD для своего возраста (как определено по Z-оценке ≤-2). Уровни как tHcy, так и Met были положительно связаны с Z-оценкой BMD LS в нескольких моделях линейной регрессии (смотрите Weber et al. Mol Genet Metab 2016; 117:351-354, который полностью включен таким образом посредством ссылки). Средний уровень tHcy у этих 19 индивидуумов составил всего 59,2 мкмоль/л, и большинство из 19 пациентов были детьми. Это исследование предполагает, что прирост костной массы в детстве и подростковом возрасте, критическом периоде для роста костной системы, является недостаточным при CBSDH и может негативно повлиять на достижение максимальной величины костной массы. Это исследование также подчеркнуло, что даже соблюдающие диету пациенты с умеренно повышенными уровнями tHcy, всего в 5 раз превышающими нормальный диапазон, уже страдают от плохих клинических последствий для здоровья костной системы в детстве
[0195] Предыдущие исследования продемонстрировали четкую взаимосвязь между уровнями Hcy и риском переломов в популяциях пожилых людей (смотрите Sato et al. Bone 2005, 36:721-726; van Meurs et al. N Engl J Med 2004; 350:2033-2041; McLean et al. N Engl J Med 2004; 350:2042-2049; каждый из которых полностью включен таким образом посредством ссылки). Результаты двух проспективных популяционных исследований, включавших 2406 субъектов в возрасте ≥55 лет, показали, что скорректированные с учетом возраста и пола риски перелома увеличивались на 30% в случае каждого увеличения уровня tHcy на одно стандартное отклонение (SD) (смотрите van Meurs et al. N Engl J Med 2004; 350:2033-2041; который полностью включен таким образом посредством ссылки). Уровень гомоцистеина в самом верхнем возрастном квартиле был связан с увеличением риска перелома в 1,9 раза. Связи между уровнями гомоцистеина и риском перелома оказались независимыми от минеральной плотности костной ткани и других возможных факторов риска перелома. Повышенный уровень гомоцистеина был сильным и независимым фактором риска переломов при остеопорозе у пожилых мужчин и женщин в общей популяции, схожим по величине с установленными факторами риска переломов и сердечнососудистого заболевания (смотрите van Meurs et al. N Engl J Med 2004; 350:2033-2041; который полностью включен таким образом посредством ссылки). Кроме того, проспективное исследование в США на 825 мужчинах и 1174 женщинах (подисследование испытания HOPE-2) показало, что уровень tHcy в сыворотке крови в самом верхнем квартиле был связан с 1,9-кратным повышением риска переломов костей тазобедренного сустава среди женщин и четырехкратным повышением риска среди мужчин по сравнению с уровнями tHcy в сыворотке в самом нижнем квартиле (смотрите Sawka et al. Arch Intern Med. 2007 Oct 22; 167(19):2136-9, который полностью включен таким образом посредством ссылки). Связь между уровнями tHcy и риском переломов не зависела от BMD и других возможных факторов риска перелома (смотрите van Meurs et al. N Engl J Med 2004; 350:2033-2041; McLean et al. N Engl J Med 2004, 350:2042-2049; Sawka et al. Arch Intern Med. 2007 Oct 22; 167(19):2136-9; каждый из которых полностью включен таким образом посредством ссылки).
[0196] В соответствии с этими результатами исследование на 433 пациентах с инсультом в возрасте старше 65 лет показало, что скорректированные с учетом возраста заболеваемости переломами костей тазобедренного сустава на 1000 человеко-лет увеличивались почти линейно с 2,89 в самых нижних квартилях уровней Hcy до 27,87 в самых верхних квартилях (смотрите Sato et al. Bone 2005; 36:721-726, который полностью включен таким образом посредством ссылки). В совокупности эти результаты позволяет предположить, что повышенные уровни Hcy являются сильным и независимым фактором риска переломов при остеопорозе у пожилых мужчин и женщин.
[0197] Аномалии скелета отсутствуют при рождении и необычны для младенцев и очень маленьких детей (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31, который полностью включен таким образом посредством ссылки). Первыми признаками поражения скелета обычно являются Х-образное искривление ног и полая стопа, с удлинением длинных костей - типичная характеристика синдрома Марфана - часто развивающиеся ближе к половому созреванию (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74); который полностью включен таким образом посредством ссылки). Остеопороз, особенно позвонков и длинных костей, часто встречается у пациентов с CBSDH и может привести к сколиозу/кифозу и/или разрушению тел позвонков (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31; Weber et al. Mol. Genet Metab 2016; 117:351-354; каждый из которых полностью включен таким образом посредством ссылки). Другие относящиеся к скелету проявления могут включать марфаноидные черты лица, причиной которых являются выступающие верхние зубы и высокое небо, а также деформации передней стенки грудной клетки, такие как воронкообразная деформация грудной клетки или килевидная грудь (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74; Sweetser et al. N Engl J Med 2016; 375:1879-1890; Brenton et al. J Bone Joint Surg Br 1972; 54:277-298; каждый из которых полностью включен таким образом посредством ссылки). Из-за этих общих характеристик скелета у синдрома Марфана и CBSDH пациентов с CBSDH иногда неправильно характеризуют как пациентов с синдромом Марфана.
[0198] Исследование на 25 ирландских пациентов с CBSDH, за которым наблюдали в течение 25 лет, показало, что риск остеопороза был значительно ниже у пациентов, выявленных в результате скрининга новорожденных, с хорошим соблюдением схемы понижающего уровень Hcy лечения (диета, витамины и/или бетаин), по сравнению с пациентами, не соблюдающими схему лечения, или пациентами с поздно поставленным диагнозом (смотрите Yap et al. J Inherit Metab Dis 1998; 21:738-747). Подтверждающие доказательства этих результатов были получены в небольшом корейском исследовании на пяти пациентах с CBSDH с хорошим длительным контролем метаболизма. В этом исследовании у пациентов, ранее получавших снижающую уровень Hcy терапию, было меньше аномалий скелета, чем у пациентов с более поздно поставленным диагнозом (смотрите Lim et al. Osteoporos Int 2013, 24:2535-2538, который полностью включен таким образом посредством ссылки). Наконец, в исследовании с использованием модели CBSDH на мыши нормализация уровней tHcy при лечении с использованием ферментотерапии на основе CBS была связана с предотвращением остеопороза (смотрите Majtan et al. Enzyme replacement prevents neonatal death, liver damage, and osteoporosis in murine homocystinuria, FASEB J 2017, который полностью включен таким образом посредством ссылки).
[0199] Точные механизмы, ведущие к низкой BMD и хрупкости скелета у пациентов с CBSDH, до конца не изучены (смотрите Weber et al. Mol Genet Metab 2016; 117:351-354; Lim JS, Lee DH. Changes in bone mineral density and body composition of children with well-controlled homocystinuria caused by CBS deficiency. Osteoporos Int 2013; 24:2535-2538, оба из которых полностью включены таким образом посредством ссылки). Однако многие заболевания соединительной ткани у пациентов с CBSDH напоминают таковые при синдроме Марфана, заболевании соединительной ткани, вызванном мутациями в гене фибриллина-1 и характеризующемся признаками, включающими удлинение длинных костей и переломы типа переломов при остеопорозе (смотрите Hubmacher et al. Biochemistry 2011; 50:5322-5332; Hubmacher et al. J Biol Chem 2010; 285:1188-1198, оба из которых полностью включены таким образом посредством ссылки). Полагают, что повышенные уровни Hcy приводят к хрупкости костей и переломам двумя различными путями (смотрите Behera et al. J Cell Physiol 2016, который полностью включен таким образом посредством ссылки). Первый путь приводит к уменьшению прироста костной массы в детстве и подростковом возрасте из-за нарушения сборки фибриллина. Второй путь приводит к нарушению ремоделирования костей, что приводит к ломкости костей из-за уменьшения образования поперечных связей в коллагене (смотрите Behera et al. J Cell Physiol 2016; Kang et al. J Clin Invest 1973; 52:2571-2578, оба из которых полностью включены таким образом посредством ссылки). В совокупности эти данные позволяют предположить, что прирост костной массы в детстве и подростковом возрасте, критическом периоде для роста скелета, является недостаточным у пациентов с CBSDH, и что это отрицательно влияет на достижение максимального значения костной массы.
[0200] Кроме того, существует сильная взаимосвязь между уровнями Hcy и риском перелома в популяциях пожилых людей (смотрите Sato et al. Bone 2005; 36:721-726; van Meurs et al. N Engl J Med 2004; 350:2033-2041; McLean et al. N Engl J Med 2004; 350:2042-2049; каждый из которых полностью включен таким образом посредством ссылки). Результаты двух международных проспективных популяционных исследований, включавших 2406 субъектов в возрасте от 55 лет и старше, показали, что уровень гомоцистеина в самом верхнем возрастном квартиле был связан с повышением риска переломов в 1,9 раза (смотрите van Meurs et al. N Engl J Med 2004; 350:2033-2041, который полностью включен таким образом посредством ссылки). Повышенный уровень гомоцистеина был сильным и независимым фактором риска переломов при остеопорозе у пожилых мужчин и женщин в общей популяции, схожим по величине с установленными факторами риска для переломов (низкой минеральной плотностью костной ткани, когнитивными расстройствами, недавними падениями) и сердечнососудистого заболевания (смотрите van Meurs et al. N Engl J Med 2004; 350:2033-2041, который полностью включен таким образом посредством ссылки). Кроме того, проспективное исследование на 1999 субъектах в США (подисследование испытания HOPE-2) показало, что уровень tHcy в сыворотке в самом верхнем квартиле был связан с 1,9-кратным увеличением риска переломов костей тазобедренного сустава у женщин и четырехкратным увеличением риска у мужчин, по сравнению с уровнями tHcy в сыворотке в самом нижнем квартиле (смотрите Sawka et al. Arch Intern Med. 2007 Oct 22; 167(19):2136-9, который полностью включен таким образом посредством ссылки). Связи между уровнями tHcy и риском перелома не зависели от BMD и других возможных факторов риска перелома (смотрите van Meurs et al. N Engl J Med 2004; 350:2033-2041; McLean et al. N Engl J Med 2004; 350:2042-2049; Sawka et al. Arch Intern Med. 2007 Oct 22; 167(19):2136-9, каждый из которых полностью включен таким образом посредством ссылки). В соответствии с этими результатами исследование на 433 пациентах с инсультом в возрасте >65 лет показало, что скорректированные с учетом возраста заболеваемости переломами костей тазобедренного сустава на 1000 человеко-лет увеличивались почти линейно с 2,89 в самых нижних квартилях уровней Hcy до 27,87 в самых верхних квартилях (смотрите Sato et al. Bone 2005; 36:721-726, который полностью включен таким образом посредством ссылки). В совокупности эти результаты позволяют предположить, что повышенные уровни Hcy являются сильным и независимым фактором риска переломов при остеопорозе у пожилых мужчин и женщин.
[0201] Точные механизмы, ведущие к низкой BMD и хрупкости скелета у пациентов с CBSDH, до конца не изучены (смотрите Weber et al. Mol Genet Metab 2016; 117:351-354; Lim JS, Lee DH. Changes in bone mineral density and body composition of children with well-controlled homocystinuria caused by CBS deficiency. Osteoporos Int 2013; 24:2535-2538; оба из которых полностью включены таким образом посредством ссылки). Однако многие заболевания соединительной ткани у пациентов с CBSDH напоминают таковые при синдроме Марфана, заболевании соединительной ткани, вызванном мутациями в гене фибриллина-1 и характеризующемся признаками, включающими удлинение длинных костей и переломы типа переломов при остеопорозе (смотрите Brenton et al. J Bone Joint Surg Br 1972; 54:277-298; Hubmacher et al. Biochemistry 2011; 50:5322-5332; Hubmacher et al. J Biol Chem 2010; 285:1188-1198, каждый из которых полностью включен таким образом посредством ссылки).
[0202] У здоровых индивидуумов фибриллин-1 вместе с полимерами коллагена и эластинам собирается для создания экстраклеточного матрикса, архитектурных каркасов для образования костной ткани, гомеостаза и репарации (смотрите Olivieri et al. Fibrogenesis Tissue Repair 2010; 3:24, который полностью включен таким образом посредством ссылки). Исследования показывают, что повышенные уровни tHcy могут приводить к структурным модификациям фрагментов фибриллина-1, которые предотвращают мультимеризацию и приводят к деградации фибриллина-1 (смотрите Hubmacher et al. J Biol Chem 2005; 280:34946-34955; Hubmacher et al. J Biol Chem 2010; 285:1188-1198, оба из которых полностью включены таким образом посредством ссылки). Этот процесс, кроме того, нарушается в результате гомоцистеинилировании фибронектина, которое предотвращает образование комплексов фибронектин-фибриллин, необходимых для мультимеризации фибриллина-1 (смотрите Hubmacher et al. Biochemistry 2011; 50:5322-5332, который полностью включен таким образом посредством ссылки). Такие данные позволяют предположить, что повышенные уровни Hcy оказывают вредный эффект на структуру ECM.
[0203] У здоровых индивидуумов агрегаты фибриллинов (т.е. микрофибриллы) играют важную роль в минерализации кости посредством накопления и активации трансформирующего фактора-бета роста (TGF-бета) и костных морфогенетических белков (BMP) (смотрите Nistala et al. Ann N Y Acad Sci 2010; 1192:253-256; Nistala et al. J Biol Chem 2010; 285:34126-34133, оба из которых полностью включены таким образом посредством ссылки). Нарушение активации TGF-бета и BMP потенциально может способствовать фенотипу скелета, наблюдаемому как при синдроме Марфана, так и при CBSDH, а также может снижать минеральное содержание в костной ткани, как это наблюдается при легких формах CBSDH (смотрите Herrmann et al. Clin Chem 2005; 51:2348-2353, который полностью включен таким образом посредством ссылки). Более того, существуют доказательства in vivo и in vitro, что Hcy может ослаблять прочность костей за счет уменьшения образования поперечных связей в коллагене (смотрите Kang et al. J Clin Invest 1973; 52:2571-2578, который полностью включен таким образом посредством ссылки). В совокупности эти данные позволяют предположить, что прирост костной массы в детстве и подростковом возрасте, критическом периоде для роста скелета, является недостаточным у пациентов с CBSDH, и что это может негативно повлиять на достижение максимального значения костной массы.
[0204] Помимо эффектов на отложение в костях, повышенные уровни Hcy увеличивают скорость ремоделирования костей за счет повышения активности остеокластов (OC) и снижения активности остеобластов (OB) (смотрите Behera et al. J Cell Physiol 2016; Herrmann et al. Clin Chem 2005; 51:2348-2353; Vacek et al. Clin Chem Lab Med 2013; 51:579-590; Vijayan et al. J Endocrinol 2017; 233:243-255, каждый из которых полностью включен таким образом посредством ссылки). Дисбаланс между активностями OB и OC может привести к ломкости костей и увеличению частоты переломов. Полагают, что механизмы, приводящие к опосредованному Hcy снижению активности OB, включают снижение кровотока в костях (следствие снижения доступности NO) (смотрите Tyagi et al. Vasc Health Risk Manag 2011; 7:31-35, который полностью включен таким образом посредством ссылки) и увеличение скоростей апоптоза OB (фиг. 2 и таблицы 14) (смотрите Behera et al. J Cell Physiol 2016; Kim et al. Bone 2006; 39:582-590, оба из которых полностью включены таким образом посредством ссылки). Полагают, что механизмы, приводящие к усилению активности OC, включают повышение уровней внутриклеточных ROS (активных форм кислорода), которые усиливают как дифференцировку OC, так и активность OC за счет повышения активности матриксной металлопротеиназы (MMP) (смотрите Vacek et al. Clin Chem Lab Med 2013; 51:579-590, который полностью включен таким образом посредством ссылки) и подавление апоптоза OC (смотрите Behera et al. J Cell Physiol 2016; Herrmann et al. Clin Chem 2005; 51:2348-2353; Koh et al. J Bone Miner Res 2006; 21:1003-1011, каждый из которых полностью включен таким образом посредством ссылки). Действительно, недавнее исследование на мышах CD1, получавших диету с высоким содержанием Hcy, показало, что кратковременное (7 дней) введение Hcy было связано с уменьшением минеральной плотности тканей (TMD) и увеличением количества OC, тогда как длительное введение Hcy (30 дней) приводило к перепрограммированию OC, апоптозу и минерализации, которые восстанавливали TMD, но нарушали биомеханические свойства ткани (смотрите Vijayan et al. J Endocrinol 2017; 233:243-255, который полностью включен таким образом посредством ссылки).
[0205] Таким образом, повышенные уровни Hcy могут приводить к хрупкости костей и переломам двумя различными путями (смотрите Behera et al. J Cell Physiol 2016, который полностью включен таким образом посредством ссылки). Первый путь приводит к уменьшению прироста костной массы в детстве и подростковом возрасте из-за нарушения структуры ECM и подавления активации фибриллин-1-ассоциированного TGF-бета и BMP. Второй путь приводит к нарушению ремоделирования костной ткани, что приводит к ломкости костей, за счет увеличения активности OC и снижения активности OB.
[0206] Повышенные уровни Hcy связаны с усилением окислительного стресса в микроокружении в костном мозге. Увеличение ROS индуцирует апоптоз остеобластов, тем самым уменьшая возникновение остеобластов. Это усиление окислительного стресса дополнительно снижает доступность NO за счет образования супероксидных анионов, что также может снижать кровоток и ангиогенез в костном мозге. ROS, образующиеся в результате этого процесса, активируют возникновение остеокластов путем слияния моноцитов, что еще больше способствует снижению BMD, приводя к остеопорозу.
[0207] Недавнее исследование на новорожденных мышах с нокаутом (KO) CBS, которых содержали на стандартном корме для грызунов без ограничения Met, показало, что назначение подкожно ферментотерапии на основе CBS, используя рекомбинантную ПЭГилированную усеченную CBS человека (PEG-CBS) в течение 5 месяцев, предотвращало снижение минеральной плотности костной ткани у этих животных, а также могло нормализовать эти показатели у животных, которых подвергали лечению в более позднем возрасте (смотрите Majtan et al. Enzyme replacement prevents neonatal death, liver damage, and osteoporosis in murine homocystinuria. FASEB J 2017, который полностью включен таким образом посредством ссылки). В этом исследовании были предотвращены изменения состава тела, характерные как для модели с нокаутом, так и для пациентов с CBSDH. Как в плазме, так и в тканях нормализовались уровни tHcy и Cys, повышались уровни Cth и улучшались отношения SAM/SAH.
[0208] Подтверждающие данные об эффектах снижения уровней Hcy на последствия для костной системы получены из 25-летнего исследования 25 ирландских пациентов с CBSDH (смотрите Yap et al. J Inherit Metab Dis 1998; 21:738-747, который полностью включен таким образом посредством ссылки). В этом исследовании остеопороз (диагностированный с помощью рентгенологического исследования, а не DXA) присутствовал у одного из трех не соблюдавших схему лечения пациентов, выявленных с помощью NBS, и у одного из четырех пациентов с поздно поставленным диагнозом (в возрасте двух лет). Ни у одного из 18 пациентов, соблюдавших схему раннего лечения (с 6-недельного возраста), признаков остеопороза выявлено не было.
[0209] Небольшое исследование было проведено в Корее на пяти пациентах с CBSDH (3 мальчиках и 3 девочках), у всех из них диагноз был поставлен в молодом возрасте (3 во время NBS и 2 в возрасте 7 лет) с хорошим контролем метаболизма в течение 3,4 лет (смотрите Lim et al. Osteoporos Int 2013; 24:2535-2538, который полностью включен таким образом посредством ссылки). Средний уровень tHcy в плазме при постановке диагноза составлял 34,3±52,6 (от 13 до 78,6) мкмоль/л, средний уровень Met в плазме составлял 716±1347,6 (от 24,3 до 1566) мкмоль/л, и лечение включало диету с низким содержанием Met с добавлением пиридоксина, бетаина и фолиевой кислоты. Определения состава тела и BMD для всех пациентов были в пределах нормы для корейской популяции, и не наблюдалось значительных изменений морфологии скелета с течением времени. У трех пациентов (60%) был небольшой сколиоз пояснично-грудного отдела позвоночника (углы Кобба 7,3°, 7,6° и 10,3°), а у трех пациентов четыре раза регистрировали переломы. Из них два были вызваны спортивной травмой, а один - дорожно-транспортным происшествием. Два случая легкого компрессионного перелома поясничного отдела позвоночника были обнаружены с помощью рентгенографии, и в анамнезе была зарегистрирована сильная боль в спине. У пациентов с ранним диагнозом было меньше аномалий скелета, чем у пациентов с более поздним диагнозом. Однако это исследование показало, что даже у пациентов с рано поставленным диагнозом с помощью NBS, которые соблюдали диетотерапию и имели лишь незначительное-умеренное повышение уровня tHcy, уже в детстве обнаруживались аномалии скелета и множественные переломы.
[0210] В совокупности эти данные свидетельствуют о положительном эффекте раннего понижающего уровень Hcy лечения на последствия для костной системы пациентов с CBSDH. Следует отметить, что у пациентов, соблюдавших схему лечения, уровни tHcy были снижены, но не нормализованы, и хотя у этих пациентов было меньше аномалий скелета, в этой преимущественно молодой группе пациентов были отмечены значительные негативные клинические последствия (остеопороз и переломы).
C. Осложнения на сердечнососудистую систему
[0211] Взаимосвязь между CBSDH и сердечнососудистым заболеванием была впервые продемонстрирована в 1985 г. в эпидемиологическом исследовании на пациентах с умеренно-сильно повышенными уровнями Hcy из-за гомозиготной CBSDH (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31, который полностью включен таким образом посредством ссылки).
[0212] Тромбоэмболия является основной причиной заболеваемости и преждевременной смерти у пациентов с CBSDH (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31; Karaca et al. Gene 2014; 534:197-203; Yap S. J Inherit Metab Dis 2003; 26:259-265, каждый из которых полностью включен таким образом посредством ссылки). Общая частота тромбоэмболических событий у пациентов с CBSDH, не получавших лечения, составляет приблизительно 10% в год (смотрите Cattaneo M. Semin Thromb Hemost 2006; 32:716-723, который полностью включен таким образом посредством ссылки), при этом риск увеличивается после хирургического вмешательства и во время или сразу после беременности (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31; Novy et al. Thromb Haemost 2010; 103:871-873, оба из которых полностью включены таким образом посредством ссылки). Тромбоэмболия может поразить любой кровеносный сосуд, но тромбоз вен (в частности, CSVT (тромбоз мозговых вен и синусов), встречается чаще, чем тромбоз артерий у пациентов с CBSDH (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31; Karaca et al. Gene 2014; 534:197-203; Eslamiyeh et al. Iran J Child Neurol 2015; 9:53-57; Saboul et al. J Child Neurol 2015; 30:107-112, каждый из которых полностью включен таким образом посредством ссылки). Нарушения мозгового кровообращения, особенно CSVT, были описаны у младенцев (смотрите Mahale et al. J Pediatr Neurosci. 2017 Apr-Jun;12(2):206-207, который полностью включен таким образом посредством ссылки); хотя чаще возникают у молодых взрослых (смотрите Yap et al. Arterioscler Thromb Vasc Biol 2001; 21:2080-2085, который полностью включен таким образом посредством ссылки).
[0213] Риск тромбоэмболических событий составлял приблизительно 25% к возрасту 16 лет и 50% к возрасту 29 лет. В 1999 г. Hankey и др. сообщили, что все три генетические причины HCU (CBSDH, дефицит MTHFR и дефицит витамина B12) были связаны с высоким риском преждевременного сердечнососудистого (CV) заболевания, поражающего половину всех гомозиготных индивидуумов к возрасту 30 лет (смотрите Hankey et al. Lancet 1999; 354:407-413, который полностью включен таким образом посредством ссылки). Единственным биохимическим изменением, общим для всех трех нарушений, является повышенный уровень Hcy в сыворотке (часто превышающий 100 мкмоль/л) (смотрите Faeh et al. Swiss Med Wkly 2006; 136:745-756, который полностью включен таким образом посредством ссылки). В нескольких сообщениях описывалось, каким образом понижающее уровень tHcy лечение значительно снижает частоту сердечнососудистых событий, основной причины заболеваемости, у пациентов с CBSDH (смотрите Yap et al. J Inherit Metab Dis 2001; 24:437-447; Wilcken DE, Wilcken B. The natural history of vascular disease in homocystinuria and the effects of treatment. J Inherit Metab Dis 1997; 20:295-300, оба из которых полностью включены таким образом посредством ссылки). С тех пор ряд других исследований продемонстрировал повышенный риск сердечнососудистых событий, в частности тромбоза вен, у пациентов с CBSDH (смотрите Karaca et al. Gene 2014; 534:197-203; Kelly et al. Neurology 2003; 60:275-279; Lussana et al. Thromb Res 2013; 132:681-684; Magner et al. J Inherit Metab Dis 2011; 34:33-37, каждый из которых полностью включен таким образом посредством ссылки).
[0214] Повышенный уровень tHcy в плазме является фактором риска развития сердечнососудистого заболевания и сильным прогностическим фактором смертности у пациентов с ишемической болезнью сердца, как с CBSDH, так и без нее (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31; Karaca et al. Gene 2014; 534:197-203; Kelly et al. Neurology 2003; 60:275-279; Faeh et al. Swiss Med Wkly 2006; 136:745-756; Boushey et al. JAMA 1995; 274:1049-1057; Clarke R et al. JAMA 2002; 288:2015-2022; Hankey et al. Lancet 1999; 354:407-413; Khan et al. Stroke 2008; 39:2943-2949; Graham et al. The European Concerted Action Project. JAMA 1997; 277:1775-1781; Clarke et al. N Engl J Med 1991; 324:1149-1155; Clarke et al. Ir J Med Sci 1992; 161:61-65; Woodward et al. Blood Coagul Fibrinolysis 2006; 17:1-5; Refsum et al. Annu Rev Med 1998; 49:31-62; Yoo et al. Stroke 1998; 29:2478-2483; Selhub et al. N Engl J Med 1995; 332:286-291; Wald et al. BMJ 2002; 325:1202; Bautista et al. J Clin Epidemiol 2002; 55:882-887; Brattstrom et al. Atherosclerosis 1990; 81:51-60; Lussana et al. Thromb Res 2013; 132:681-684; Casas et al. Lancet 2005; 365:224-232; McCully KS. Am J Pathol 1969; 56:111-128; Magner et al. J Inherit Metab Dis 2011; 34:33-37; Wilcken et al. J Clin Invest 1976; 57:1079-1082; Nygard et al. N Engl J Med 1997; 337:230-236; каждый из которых полностью включен таким образом посредством ссылки). Хотя имеется данные о взаимосвязи между уровнями tHcy и риском развития сердечнососудистого заболевания (смотрите Boushey et al. JAMA 1995; 274:1049-1057, каждый полностью включен таким образом посредством ссылки), взаимосвязь между tHcy и инсультом/заболеванием периферических артерий значительно сильнее (смотрите Clarke et al. JAMA 2002; 288:2015-2022; Khan et al. Stroke 2008; 39:2943-2949; Wald et al. BMJ 2002; 325:1202; Casas et al. Lancet 2005; 365:224-232; Brattstrom et al. Haemostasis 1989;19 Suppl 1:35-44, каждый из которых полностью включен таким образом посредством ссылки). Хотя крупные исследования (NORVIT, HOPE-2, VITATOPS) на общей популяции первоначально пришли к выводу, что снижение уровня Hcy оказывает незначительный эффект на основные сердечнососудистые события и рецидив сердечнососудистого заболевания, дальнейший, более конкретный анализ данных ясно показал клиническую пользу от снижения tHcy при инсульте.
[0215] Имеются убедительные доказательства того, что понижение уровня Hcy снижает риск инсульта в общей популяции с умеренно повышенными уровнями tHcy (смотрите Saposnik et al. Stroke 2009; 40:1365-1372; Huo et al. JAMA 2015; 313:1325-1335; Lonn et al. N Engl J Med 2006; 354:1567-1577; Hankey et al. Lancet Neurol 2012; 11:512-520; Spence JD, Lancet Neurol. 2007 Sep;6(9):830-8, каждый из которых полностью включен таким образом посредством ссылки). В исследовании HOPE-2 (смотрите Saposnik et al. Stroke 2009; 40:1365-1372, который полностью включен таким образом посредством ссылки) на 5552 пациентах незначительные снижения уровней tHcy (3 ммоль/л в сравнение с плацебо) приводили к значительному снижению частоты инсульта (снижению относительного риска на 27%, снижению абсолютного риска на 1,3%), что позволяет предположить, что даже небольшие снижения уровней tHcy могут быть полезными. Этот эффект был наиболее выражен у пациентов с исходными уровнями Hcy в верхнем квартиле, снижение абсолютного риска для которых составляло 4,3%. Хотя неясно, влияет ли снижение уровня Hcy на последствия для всей сердечнососудистой системы пациентов с умеренно повышенными уровнями tHcy и без CBSDH (смотрите Marti-Carvajal et al. Cochrane Database Syst Rev 2015; 1:CD006612, который полностью включен таким образом посредством ссылки), его польза для сердечнососудистой системы постоянно демонстрировалась у пациентов с CBSDH (смотрите Yap et al. J Inherit Metab Dis 1998; 21:738-747; Eslamiyeh et al. Iran J Child Neurol 2015; 9:53-57; Saboul et al. J Child Neurol 2015; 30:107-112; Yap et al. Arterioscler Thromb Vasc Biol 2001; 21:2080-2085; Woods et al. BMJ Case Rep 2017; Wilcken et al. J Inherit Metab Dis 1997; 20:295-300; Yap et al. Semin Thromb Hemost 2000; 26:335-340; Ruhoy et al. Pediatr Neurol 2014; 50:108-111, каждый из которых полностью включен таким образом посредством ссылки).
1. Механизм
[0216] Ряд исследований показал, что повышенные уровни Hcy способствуют развитию атеросклероза или тромбоза с помощью связанных с окислительным стрессом механизмов (смотрите Faverzani et al. Cell Mol Neurobiol 2017; Nowak et al. Arterioscler Thromb Vasc Biol 2017;37:e41-e52; Vanzin et al. Mol Genet Metab 2011; 104:112-117; Vanzin et al. Gene 2014; 539:270-274; Vanzin et al. Cell Mol Neurobiol 2015;35:899-911; каждый из который полностью включен таким образом посредством ссылки), включающих активацию посредством NF-κB воспалительных и иммунных реакций (смотрите Rodriguez-Ayala et al. Atherosclerosis 2005; 180:333-340; van Guldener et al. Curr Hypertens Rep 2003; 5:26-31, оба из которых полностью включены в настоящий документ посредством ссылки). Полагают, что причиной срединного (медиального) повреждения, ведущего к тромбозу, является Hcy-опосредованное нарушение функции эндотелия (смотрите Jiang et al. Arterioscler Thromb Vasc Biol 2005; 25:2515-2521; Hossain et al. J Biol Chem 2003; 278:30317-30327; Cai et al. Blood 2000; 96:2140-2148; Zhang et al. J Biol Chem 2001; 276:35867-35874; Papapetropoulos et al. Proc Natl Acad Sci USA 2009; 106:21972-21977; Szabo et al. Br J Pharmacol 2011; 164:853-865; Chiku et al. J Biol Chem 2009; 284:11601-11612; Wang et al. Antioxid Redox Signal 2010; 12:1065-1077; Saha et al. FASEB J 2016; 30:441-456; Ebbing et al. JAMA 2008; 300:795-804; Bonaa et al. N Engl J Med 2006; 354:1578-1588; Marti-Carvajal et al. Cochrane Database Syst Rev 2015;1:CD006612; Celermajer et al. J Am Coll Cardiol 1993; 22:854-858; Rubba et al. Metabolism 1990; 39:1191-1195; каждый из которых полностью включен таким образом посредством ссылки), усиление путей свертывания крови (смотрите Spence JD. Int J Stroke. 2016 Oct;11(7):744-7; Fryer et al. Arterioscler Thromb 1993; 13:1327-1333; Lentz et al. J Clin Invest 1991; 88:1906-1914; каждый из которых полностью включен таким образом посредством ссылки) и увеличение расширения сосудов. Такие протромботические механизмы схожи с теми, которые наблюдаются у пациентов с синдромом Марфана (смотрите Kelly et al. Neurology 2003; 60:275-279; Tripathi P. International Cardiovascular Forum J 2016; 6:13; van Guldener et al. Curr Hypertens Rep 2003; 5:26-31; Hackam et al. JAMA 2003; 290:932-940; Baumbach et al. Circ Res 2002; 91:931-937; Evangelisti et al. Int J Cardiol 2009; 134:251-254; de Valk et al. Stroke 1996; 27:1134-1136, каждый из которых полностью включен таким образом посредством ссылки).
[0217] Причинно-следственная связь между уровнями tHcy и риском развития сердечнососудистых заболеваний, полученная в результате метаанализа данных 27 исследований (более 4000 пациентов), показала градуционный риск атеросклероза коронарных сосудов, сосудов головного мозга и периферических сосудов, так что повышение на 5 мкМ уровня Hcy давало повышенный на 80% риск для женщин и повышенный на 60% риск для мужчин (смотрите Boushey et al. JAMA 1995; 274:1049-1057, который полностью включен таким образом посредством ссылки). Метаанализ данных 30 проспективных или ретроспективных исследований, включающих 5073 случая ишемической болезни сердца (IHD) и 1113 инсультов, показал, что уровень Hcy (приблизительно 3 мкмоль/л), который на 25% ниже обычного (с поправкой на погрешность в виде разбавления регрессии), был связан с на 11% (отношение шансов (OR)=0,89; 95% CI (доверительный интервал) от 0,83 до 0,96) более низким риском IHD и на 19% (OR=0,81; 95% CI от 0,69 до 0,95) более низким риском инсульта (смотрите Clarke R, et al. JAMA 2002; 288:2015-2022, который полностью включен таким образом посредством ссылки).
[0218] Исследование на пациентах с ранее существовавшим сердечнососудистым заболеванием и без него продемонстрировало увеличение, после метиониновой нагрузки, уровня Hcy в плазме (превышающее самые высокие значения у сопоставимых здоровых контрольных субъектов) у 1/21 субъекта с инфарктом миокарда (5%), 14/37 субъектов с аорто-подвздошной болезнью (38%) и 17/53 пациентов с цереброваскулярным заболеванием (32%). Это свидетельствует о том, что связь между уровнями Hcy и заболеванием периферических артерий (PAD) и инсультом значительно сильнее, чем связь между уровнями Hcy и инфарктом миокарда (смотрите Brattstrom et al. Haemostasis 1989; 19 Suppl 1:35-44, который полностью включен таким образом посредством ссылки). Независимая градуционная связь между уровнями Hcy и инсультом была описана в проспективном исследовании, проведенном на британской когорте, состоящей из 457 пациентов с инсультом и 179 контрольных субъектов из того же сообщества (смотрите Khan et al. Stroke 2008; 39:2943-2949). Самые высокие уровни Hcy наблюдались у пациентов с заболеванием мелких сосудов (SVD) (16,2 в сравнение с 11,8 мкмоль/л у контрольных субъектов без инсульта, p<0,001 после поправки на возраст, пол, сердечнососудистые факторы риска, уровни витаминов и функцию почек). В случаях SVD самые высокие уровни Hcy наблюдались у индивидуумов с лакунарным инфарктом с лейкоареозом со сливными очагами гиперинтенсивности. Кроме того, выявлена корреляция между уровнями Hcy и тяжестью лейкоареоза (r=-0,225; p<0,001).
[0219] Эти данные были дополнительно подтверждены исследованием с использованием Менделевской рандомизации, в котором демонстрируется генетическая связь между полиморфизмами MTHFR, регулирующими метаболизм Hcy, и риском инсульта (смотрите Casas et al. Lancet 2005; 365:224-232, который полностью включен таким образом посредством ссылки). Поиск литературы по всем релевантным исследованиям связи между уровнями Hcy и полиморфизмами MTHFR TT и CC для риска инсульта выявил 111 исследований, включающих 15635 индивидуумов без сердечнососудистых заболеваний (CVD). Средневзвешенная разница в уровнях Hcy между гомозиготами ТТ и СС составляла 1,93 мкмоль/л (95% CI от 1,38 до 2,47). Основываясь на результатах предыдущего метаанализа проспективных исследований, в которых повышение уровней Hcy в плазме на 5 мкмоль/л соответствовало OR для инсульта=1,59 (от 1,29 до 1,96), повышение уровней Hcy на 1,93 мкмоль/л у здоровых индивидуумов с генотипом ТТ приведет к ожидаемому для инсульта OR=1,20 (от 1,10 до 1,31) (смотрите Wald et al. BMJ 2002; 325:1202, который полностью включен таким образом посредством ссылки). В соответствии с этим результатом, Khan и др. сообщили о OR=1,26 (от 1,14 до 1,40) для инсульта у гомозигот ТТ по сравнению с гомозиготами СС (р=0,29), независимо от возрастной группы, этнической принадлежности или географического положения. В совокупности эти результаты указывают на причинную роль повышенных уровней Hcy в патогенезе инсульта в общей популяции.
[0220] Является ли умеренное повышение уровня Hcy в сыворотке типичным для пациентов с сердечнососудистым заболеванием из-за гетерозиготной CBSDH, изучали в исследованиях, намного меньших, чем те, которые проводились в общей популяции. Согласно Mudd и др., риск сердечнососудистых событий у пациентов с умеренно повышенными уровнями tHcy из-за гетерозиготной CBSDH (<5% к возрасту 50 лет) схож с таковым в общей популяции (смотрите Mudd et al. Am J Hum Genet 1981; 33:883-893, который полностью включен таким образом посредством ссылки). В соответствии с этим ультразвуковое исследование лиц с гомозиготной и гетерозиготной CBSDH выявило нарушение функции эндотелия в системных артериях гомозиготных детей в возрасте уже четырех лет, тогда как у гетерозиготных взрослых функция эндотелия практически не изменилась (смотрите Celermajer et al. J Am Coll Cardiol 1993; 22:854-858, который полностью включен таким образом посредством ссылки).
[0221] Хотя схожее исследование продемонстрировало признаки преждевременного заболевания артерий как у гомозигот, так и у гетерозигот, у индивидуумов с гомозиготным заболеванием признаки появлялись в гораздо более молодом возрасте (19 лет в сравнение с 45 годами), а тяжесть заболевания была значительно выше (смотрите Rubba et al. Metabolism 1990; 39:1191-1195, который полностью включен таким образом посредством ссылки).
[0222] В целом, наблюдения в случае пациентов с CBSDH соответствовали наблюдениям из предыдущих исследований, при этом риск развития сердечнососудистых заболеваний увеличивался с повышением уровней Hcy (смотрите Boushey et al. JAMA 1995; 274:1049-1057; Clarke et al. JAMA 2002; 288:2015-2022; Khan et al. Stroke 2008; 39:2943-2949; каждый из которых полностью включен таким образом посредством ссылки).
[0223] Эти результаты позволяют предположить, что повышенный уровень Hcy является фактором риска сердечнососудистого заболевания. Кроме того, было установлено, что понижение уровней Hcy значительно снижает риск инсульта в общей популяции и у пациентов с CBSDH.
[0224] Исследования показали, что повышенные уровни Hcy, вызванные CBSDH, могут потенциально способствовать развитию атеросклероза и/или тромбоза с помощью различных механизмов. К ним относятся молекулярные события, такие как индукция окислительного стресса и его последующие эффекты, такие как активация NF-κB (усилителя в виде легкой цепи каппа ядерного фактора активированных В-клеток), фактора транскрипции, регулирующего провоспалительные и другие гены, связанные с повреждением. Различные Hcy-опосредованные эффекты, модулирующие физико-химические свойства сосудистой стенки, такие как те, которые приводят к нарушению функции эндотелия или ригидности артерий, могут способствовать развитию гипертонии, тромбоза или других сердечнососудистых аномалий. Наконец, есть доказательства прямой индукции путей свертывания крови с помощью Hcy, что является более прямым путем, ведущим к тромбозу (смотрите Faverzani et al. Cell Mol Neurobiol 2017; Hainsworth et al. Biochim Biophys Acta 2016; 1862:1008-1017; Ganguly et al. Nutr J 2015; 14:6; Tripathi P. Molecular and biochemical aspects of homocysteine in cardiovascular diseases. International Cardiovascular Forum J 2016; 6:13; Fryer et al. Arterioscler Thromb 1993; 13:1327-1333; каждый из которых полностью включен таким образом посредством ссылки). После краткого описания молекулярных и биохимических механизмов атеросклероза в подразделах ниже будут рассмотрены потенциальные механизмы, ведущие к сердечнососудистым заболеваниям у индивидуумов с повышенным уровнем tHcy, в том числе индивидуумов с CBSDH.
2. Атеросклероз
[0225] Среди наиболее хорошо изученных состояний, ведущих к тромбозу и, следовательно, к закупорке сосудов, относится атеросклероз, прогрессирующее воспалительное заболевание, поражающее коронарное, мозговое и периферическое кровообращение (смотрите Libby et al. Circulation 2005; 111:3481-3488, который полностью включен таким образом посредством ссылки). На его ранних стадиях повреждение сосудов приводит к активации эндотелиальных клеток (TC), рекрутированию моноцитов во внутреннюю оболочку (интиму) и активации макрофагов. Формируется воспалительное атеросклеротическое поражение (жировой слой), состоящее из происходящих из моноцитов, нагруженных липидами макрофагов (пенистых клеток) и Т-лимфоцитов. В результате прогрессирующего накопления липидов образуется липидное ядро, окруженное фиброзным покрытием. На более поздних стадиях активированные макрофаги секретируют ферменты, которые ослабляют фиброзное покрытие, что приводит к разрушению бляшки, кровоизлиянию или тромбозу и ишемическим атакам/острому коронарному синдрому. При разрушении бляшки тканевой фактор подвергается воздействию крови в просвете артерии, что позволяет ему образовывать комплексы с факторами свертывания крови VH/VIIa. Этот процесс инициирует каскад свертывания крови, приводящий к тромбообразованию. Разрушенные бляшки могут привести либо к пристеночному, либо к окклюзионному тромбозу, вызывая, соответственно, частичную или полную закупорку. Пристеночный тромбоз вызывает симптомы ишемии, такие как нестабильная стенокардия, тогда как окклюзионный тромбоз приводит к острым коронарным событиям, таким как инфаркт миокарда и инсульт. Цитокины участвуют во всех стадиях атеросклероза и оказывают сильное влияние на его патогенез (смотрите Ramji et al. Cytokine Growth Factor Rev 2015; 26:673-685, который полностью включен таким образом посредством ссылки). Помимо того, что тромбоз является вторичным по отношению к атеросклерозу, он также может активироваться в отсутствие образования бляшек, например, вследствие мерцательной аритмии или прямой активации каскада свертывания крови.
3. Окислительный стресс
[0226] Исследования на пациентах с повышенными уровнями Hcy показали, что подвергнутые лечению и особенно не подвергнутые лечению пациенты были подвержены окислительному стрессу, о чем свидетельствуют измененные биомаркеры, отражающие окислительное повреждение липидов, белков и ДНК в различных тканях (смотрите Vanzin et al. Mol Genet Metab 2011; 104:112-117; Vanzin et al. Gene 2014; 539:270-274; Vanzin et al. Cell Mol Neurobiol 2015; 35:899-911, каждый из которых полностью включен таким образом посредством ссылки). Окислительный стресс, определяемый как дисбаланс в окислительно-восстановительном гомеостазе, играет ключевую роль в таких сердечнососудистых патологиях, как атеросклероз и связанный с ним тромбоз, в которые вовлечена окислительная модификация липопротеинов низкой плотности, активация эндотелиальных клеток и инициация воспалительных реакций в сосудах (смотрите Nowak et al. Arterioscler Thromb Vasc Biol 2017;37: e41-e52, который полностью включен таким образом посредством ссылки). Окислительный стресс может быть вызван повышенными уровнями ROS (например, супероксидного (O2-) и гидроксильного (HO-) радикалов и перекиси водорода (H2O2)) и/или сниженными уровнями тканевых антиоксидантов (например, супероксиддисмутазы, каталазы и глютатионпероксидазы) (смотрите Faverzani et al. Cell Mol Neurobiol 2017; Nowak et al. Arterioscler Thromb Vasc Biol 2017; 37:e41-e52, оба из которых полностью включены таким образом посредством ссылки). У здоровых индивидуумов ROS образуются как побочные продукты нормального окислительного метаболизма. Однако, кроме того, образование ROS запускается такими факторами риска сердечнососудистых заболеваний, как сигаретный дым, употребление алкоголя, гиперхолестеринемия, гипертония, диабет и повышенный уровень Hcy.
[0227] На молекулярном уровне существует множество путей, через которые Hcy может вызывать повышенный окислительный стресс, некоторые из которых обсуждались ранее. Например, накопление иммуногенных гомоцистеинилированных белков в сосудистой стенке может стимулировать воспаление и, следовательно, образование ROS (O2-) активированными фагоцитами). Другим потенциальным механизмом является индуцированная Hcy активация рецепторов NMDA, запускающая пути передачи сигналов, ведущие к образованию ROS. В эндотелиальных клетках капилляров ЕС сердца Hcy индуцировал повышенные уровни NADPH-оксидазы, ферментов на клеточной поверхности, которые, особенно в активированных клетках, продуцируют высокие уровни O2-. Недавнее исследование (смотрите Chen et al. Sci Rep. 2017 Jul 31; 7(1):6932, который полностью включен таким образом посредством ссылки) позволило предположить, что в ишемизированном мозге крыс Hcy индуцирует митохондриальную дисфункцию с ожидаемым в результате увеличением образования ROS. Также полагают, что Hcy снижает биодоступность полезного вазодилатора NO. O2- реагирует с NO с образованием активных форм азота пероксинитрита, и, действительно, также сообщалось об индуцированном Hcy увеличении нитрования тирозина, индикаторе индуцированного пероксинитритом повреждения белка (смотрите Tyagi et al. Vasc Health Risk Manag 2011; 7:31-35, который полностью включен таким образом посредством ссылки). В более широком значении можно ожидать, что тиол-тиоловые взаимодействия с участием Hcy будут нарушать окислительно-восстановительный статус клеток, например, потенциально снижая доступность восстановленного глютатиона и даже нарушая сборку и укладку белков.
[0228] В исследовании пациентов с CBSDH до и после лечения лечение пиридоксином, добавками соли фолиевой кислоты, бетаина и витамина B12 ослабляло окислительное повреждение липидов у пациентов, но не изменяло содержание сульфгидрильных групп или общий антиоксидантный статус, оба показателя антиоксидантной способности тканей. Тем не менее, отмечалась значительная отрицательная корреляция между содержанием сульфгидрильных групп и уровнями Hcy и положительная корреляция между уровнями продукта перекисного окисления липидов малонового диальдегида и уровнями Hcy. Это позволяет предположить возможную механистическую роль Hcy в окислительном повреждении, наблюдаемом при CBSDH (смотрите Vanzin et al. Mol Genet Metab 2011; 104:112-117, который полностью включен таким образом посредством ссылки). Измененные профили липидов, в частности, снижение уровней липопротеинов высокой плотности и обогащение провоспалительными видами липидов, наблюдались в плазме не подвергнутых лечению и подвергнутых лечению пациентов с CBSDH (смотрите Vanzin et al. Cell Mol Neurobiol 2015; 35:899-911, который полностью включен таким образом посредством ссылки). В другом исследовании сообщалось о значительно большем повреждении ДНК у пациентов с CBSDH, чем у здоровых индивидуумов (смотрите Vanzin et al. Gene 2014; 539:270-274, который полностью включен таким образом посредством ссылки). В совокупности эти данные предполагает вовлечение окислительного стресса в патогенез повреждения сосудов, связанного с повышенным уровнем Hcy. Не было обнаружено корреляции между уровнями Met и какими-либо параметрами, связанными с окислительным стрессом, что позволяет предположить, что Met и его производные вносят небольшой вклад в окислительное повреждение при CBSDH (смотрите Vanzin et al. Mol Genet Metab 2011; 104:112-117, который полностью включен таким образом посредством ссылки).
[0229] Среди множества других молекулярных эффектов окислительный стресс связан с активацией NF-κB, группы факторов транскрипции, регулирующих экспрессию генов провоспалительных факторов, таких как цитокины, которые, как известно, участвуют в инициации и прогрессировании атеросклероза и тромбоза (смотрите Rodriguez-Ayala et al. Atherosclerosis 2005; 180:333-340, который полностью включен таким образом посредством ссылки). Исследования in vitro показали, что обработка эндотелиальных клеток Hcy активирует NF-κB через образование ROS (смотрите van Guldener et al. Curr Hypertens Rep 2003; 5:26-31, который полностью включен таким образом посредством ссылки). Помимо модуляции экспрессии генов, химическая модификация клеточных макромолекул при окислительном стрессе может непосредственно влиять на структуру и функцию сосудистой сети и оказывать другие локальные или системные эффекты, как обсуждается в остальной части раздела.
4. Изменения сосудистой стенки
[0230] Нарушение функции эндотелия обычно определяют как дисбаланс между ассоциированными с эндотелием факторами, модулирующими сократимость и релаксацию сосудов. Среди этих факторов NO или «эндотелиальный релаксирующий фактор» является самым известным, в то время как сероводород (H2S) является другим фактором, описанным совсем недавно (смотрите Jiang et al. Arterioscler Thromb Vasc Biol 2005; 25:2515-2521, который полностью включен таким образом посредством ссылки). В нескольких исследованиях in vitro изучались эффекты Hcy на функцию эндотелия, хотя и с использованием очень высоких уровней Hcy (смотрите Jiang et al. Arterioscler Thromb Vasc Biol 2005; 25:2515-2521; Hossain et al. J Biol Chem 2003; 278:30317-30327; Cai et al. Blood 2000; 96:2140-2148; Zhang et al. J Biol Chem 2001; 276:35867-35874; каждый из которых полностью включен таким образом посредством ссылки). В одном таком исследовании сообщалось об ответе в виде накопления развернутых белков и запрограммированной гибели (в) эндотелиальных клеток(ах) пупочной вены человека (HUVEC), обработанных Hcy, хотя концентрации Hcy были в несколько раз выше, чем у пациентов с сильно повышенными уровнями Hcy (смотрите Zhang et al. J Biol Chem 2001; 276:35867-35874, который полностью включен таким образом посредством ссылки). В других сообщениях Cth-гамма-лиаза (CGL), фермент, участвующий в метаболизме Cth, создавала избыток H2S у пациентов с повышенными уровнями Hcy (смотрите Papapetropoulos et al. Proc Natl Acad Sci USA 2009; 106:21972-21977; Szabo C et al. Br J Pharmacol 2011; 164:853-865; Chiku et al. J Biol Chem 2009; 284:11601-11612, каждый из которых полностью включен таким образом посредством ссылки). Это наблюдение было важным, поскольку сообщалось, что повышенные уровни H2S значительно увеличивают рост сосудов коллатеральных путей кровотока, плотность капилляров и региональный кровоток в тканях (смотрите Wang et al. Antioxid Redox Signal 2010; 12:1065-1077, который полностью включен таким образом посредством ссылки). Однако высокие уровни Hcy (от 0,002 до 2 мМ) не оказывали значительного влияния на пролиферацию эндотелиальных клеток или уровни фосфо-eNOS in vitro (смотрите Saha et al. Cystathionine beta-synthase regulates endothelial function via protein S-sulfhydration. FASEB J 2016; 30:441-456, который полностью включен таким образом посредством ссылки). В целом, эти результаты позволяют предположить возможную роль Hcy в эндотелиальной дисфункции, хотя еще не ясно, влияет ли Hcy непосредственно на эндотелиальные клетки in vivo из-за высоких уровней Hcy, проверенных in vitro.
[0231] В недавнем фармакологическом и генетическом исследовании утрата функции CBS в эндотелиальных клетках (EC) была связана со снижением на 50% клеточного H2S и снижением на 400% глютатиона с сопутствующим повышением клеточных уровней ROS (смотрите Saha et al. FASEB J 2016; 30:441-456, который полностью включен таким образом посредством ссылки). Сайленсинг CBS в EC снижал фенотипические реакции и ответы в виде передачи сигналов на фактор роста эндотелия сосудов (VEGF), и этот эффект усугублялся при уменьшении транскрипции рецептора-2 фактора роста эндотелия сосудов (VEGFR-2) и нейропилина-1 (NRP-1), основных рецепторов, регулирующих эндотелиальные функции, такие как ангиогенез. Подавление транскрипции VEGFR-2 и NRP-1 было опосредовано снижением стабильности фактора транскрипции Sp1, мишени действия в виде сульфгидратирования H2S. Пополнение H2S, но не глютатиона, в ЕС с сайленсингом CBS восстанавливало уровни Sp1 и связывание Sp1 с промотором VEGFR-2, а также увеличивало экспрессию VEGFR-2 и NRP-1 и VEGF-зависимую пролиферацию и миграцию клеток. Это свидетельствует о том, что CBS-опосредованное S-сульфгидратирование белков важно для поддержания здоровья и функционирования сосудов, что подтверждает предыдущие наблюдения, что у пациентов с CBSDH имеется нарушение функции эндотелия (смотрите Celermajer et al. J Am Coll Cardiol 1993; 22:854-858; Rubba et al. Metabolism 1990; 39:1191-1195, оба из которых полностью включены таким образом посредством ссылки), и повышает вероятность того, что пациенты с CBSDH страдают дополнительным и отличным типом повреждения сосудов, в дополнение к типу повреждения сосудов, наблюдаемому у индивидуумов с уровнями Hcy, повышенными по другим причинам.
[0232] Нарушение регуляции эндотелиальной функции или другие эффекты на сократительную способность сосудов могут приводить к отклонениям кровяного давления (BP). Уровень Hcy в плазме был напрямую связан с BP, а снижение уровня Hcy с помощью фолиевой кислоты было связано со снижением BP (смотрите Tripathi P. Molecular and biochemical aspects of homocysteine in cardiovascular diseases. International Cardiovascular Forum J 2016; 6:13; Hackam et al. JAMA 2003; 290:932-940, оба из которых полностью включены в настоящее описание посредством ссылки). Хотя механизмы, приводящие к этим эффектам, были неясны, уровни Hcy более тесно связаны с систолическим, чем с диастолическим BP. Это позволяет предположить, что повышенные уровни Hcy увеличивают ригидность артерий. Степень ригидности артерий во многом определяется количеством и функцией гладкомышечных клеток (SMC), отношением коллагена и эластина в экстраклеточном матриксе (ECM), качеством коллагена и функцией эндотелия (смотрите Tripathi P. Molecular and biochemical aspects of homocysteine in cardiovascular diseases. International Cardiovascular Forum J 2016; 6:13, который полностью включен таким образом посредством ссылки).
[0233] Потенциально, высокие уровни Hcy связаны с увеличенной ригидностью артерий из-за повышенной пролиферации SMC, образования коллагена и образования эластиновых волокон (смотрите van Guldener et al. Curr Hypertens Rep 2003; 5:26-31, который полностью включен таким образом посредством ссылки). Однако также возможно, что Hcy снижает ригидность артерий, нарушая перекрестное сшивание в коллагене. В исследовании, проведенном на карликовых свиньях, индуцированное диетой повышение уровня Hcy приводило к «синдрому мегаартерий» с гиперпульсацией артерий, систолической (но не диастолической) гипертензией и длительной реактивной гиперемией проводящих артерий с дилатацией аорты (смотрите van Guldener et al. Homocysteine and blood pressure. Curr Hypertens Rep 2003; 5:26-31, который полностью включен таким образом посредством ссылки). Также наблюдалась фрагментация эластичного слоя артериальной стенки, коррелирующая с ригидностью аорты.
[0234] В соответствии с этими данными проведенное на мышах с CBSDH и без нее исследование показало, что площадь поперечного сечения стенки сосуда была значительно больше у мышей CBS+/-, которых кормили, используя контрольную диету, (437±22 мкм2), и мышей CBS+/+ (442±36 мкм2) и мышей CBS+/- (471± 46 мкм2), которых кормили, используя диету с высоким содержанием Met, по сравнению с мышами CBS+/+ (324±18 мкм2), которых кормили, используя контрольную диету (p<0,05) (смотрите Baumbach et al. Structure of cerebral arterioles in cystathionine beta-synthase-deficient mice. Circ Res 2002; 91:931-937, который полностью включен таким образом посредством ссылки).
[0235] Во время максимальной вазодилатации кривые расширяемости мозговых артериол мышей CBS+/- на контрольном рационе и мышей CBS+/+ и CBS+/- на рационе с высоким содержанием Met, были смещены вправо от кривой для мышей CBS+/+ на контрольной диете. Это указывало на то, что расширение мозговых артериол было больше у мышей с повышенными уровнями tHcy в плазме. Эти результаты позволяют предположить, что повышенные уровни Hcy индуцируют гипертрофию сосудов головного мозга и изменяют механику сосудов головного мозга, причем оба эффекта потенциально способствуют повышению частоты тромбозов, например, инсульта, даже при отсутствии атеросклероза (смотрите Baumbach et al. Circ Res 2002; 91:931-937, который полностью включен таким образом посредством ссылки).
[0236] Дальнейшее подтверждение эффектов повышенного уровня Hcy на вазодилатацию получено в исследовании на 5 итальянских пациентах с CBSDH и уровнями tHcy в диапазоне от 193,6 до 342 мкмоль/л (смотрите Evangelisti et al. Int J Cardiol 2009; 134:251-254, который полностью включен таким образом посредством ссылки). У пациентов были выявлены признаки пролапса клапана сердца легкой степени и/или регургитации и появление соединительной ткани.
5. Тромбоз
[0237] Повышенные уровни Hcy связаны с более высоким риском тромбоза глубоких вен, тромбоза венозных синусов головного мозга и тромбоза вен сетчатки (смотрите Spence JD. Lancet Neurol. 2007 Sep;6(9):830-8, который полностью включен таким образом посредством ссылки), хотя во многих исследованиях не удалось найти связь с риском инфаркта миокарда. В соответствии с этими результатами дополнительные, хотя и небольшие исследования позволяют предположить, что CBSDH связана с тромбозом, но необязательно с атеросклерозом. Визуализация сосудов у пациентов с семейной гиперхолестеринемией (FH) и CBSDH показала, что, в то время как у пациентов с FH наблюдалось диффузное и очаговое утолщение сонных артерий и нарушение функция эндотелия, приводящие к снижению кровотока, у пациентов с CBSDH редко были бляшки в их сонных артериях, и они были схожими со здоровыми контрольными субъектами по показателю как толщины комплекса интима-медиа (IMT), так и скорости кровотока в средней мозговой артерии (смотрите Rubba et al. Stroke 1994; 25:943-950, который полностью включен таким образом посредством ссылки). Это исследование предполагает, что типичные атеросклеротические поражения могут необязательно предшествовать тромботическим событиям при CBSDH, и что срединное повреждение, ведущее к тромбозу, также может быть вызвано расширением артерий.
[0238] Подтверждение этого наблюдения получено из исследования, в котором распространенность атеросклероза сонных и бедренных артерий (определяемую по IMT и лодыжечно-плечевому индексу) у 13 пациентов с ферментативно доказанной гетерозиготной CBSDH сравнивали с таковой у 12 здоровых субъектов с нормальной Met-нагрузкой по результатам проверки (смотрите de Valk et al. Stroke 1996; 27: 1134-1136, который полностью включен таким образом посредством ссылки). Значимых различий между группами по средним значениям IMT, распределению частоты IMT или IMT в каждом из пяти артериальных сегментов не наблюдалось. Эти результаты могут объяснить тем фактом, что гетерозиготные индивидуумы были слишком молоды (все возрастом <50 лет) для развития структурных изменений сосудов. Однако эти данные также предполагают, что повышенные уровни Hcy могут в первую очередь влиять на каскад свертывания крови, по крайней мере, у более молодых пациентов. Действительно, в описании симптомов у трех неродственных пациентах с CBSDH было обнаружено, что у одного пациента случился инсульт из-за внутрипросветного тромбоза, а у другого пациента была сердечная или артериальная тромбоэмболия, также без признаков краниоцервикального атеросклероза (смотрите Kelly et al. Neurology 2003; 60:275-279, который полностью включен таким образом посредством ссылки).
[0239] В соответствии с этими наблюдениями, добавление Hcy к эндотелиальным клеткам (EC) HUVEC и CV1 необратимо инактивировало антикоагулянты, белок С и тромбомодулин (смотрите Lentz et al. J Clin Invest 1991; 88:1906-1914, который полностью включен таким образом посредством ссылки). Более того, добавление Hcy к культивируемым EC человека повышало активность прокоагулянта-тканевого фактора в зависимости от времени и концентрации (смотрите Fryer et al. Arterioscler Thromb 1993; 13:1327-1333, который полностью включен в настоящее описание посредством ссылки).
[0240] В обоих исследованиях Hcy усиливал пути свертывания крови посредством механизма, вовлекающего его свободную сульфгидрильную группу. В совокупности эти данные подтверждают гипотезу о том, что нарушения в механизмах свертывания крови в сосудах способствуют повышению риска развития сердечнососудистых заболеваний у пациентов с CBSDH, и что это может играть более раннюю роль у пациентов с CBSDH, до того, как эффекты Hcy на атеросклероз станут очевидными.
[0241] Снижение уровней Hcy в плазме снижает риск развития осложнений на сердечнососудистую систему, в частности инсульта, у пациентов с CBSDH и в общей популяции.
[0242] Недавние анализы обнаружили сильную связь в общей популяции между повышенным уровнем tHcy и риском инсульта (смотрите Saposnik et al. Stroke 2009; 40:1365-1372; Spence JD. Homocysteine lowering for stroke prevention: Unravelling the complexity of the evidence. Int J Stroke. 2016 Oct; 11(7):744-7; Hankey et al. Lancet Neurol 2012; 11:512-520, каждый из которых полностью включен таким образом посредством ссылки).
[0243] В прошлом польза от вмешательств для снижения Hcy у пациентов с повышенными уровнями Hcy казалась неоднозначными, при этом некоторые исследования показывали снижение риска развития сердечнососудистых заболеваний (смотрите Yap et al. J Inherit Metab Dis 1998; 21:738-747; Yap et al. Arterioscler Thromb Vasc Biol 2001; 21:2080-2085; Wilcken et al. J Inherit Metab Dis 1997; 20:295-300; Yap et al. Semin Thromb Hemost 2000; 26:335-340; Saposnik et al. Stroke 2009; 40:1365-1372; Huo et al. JAMA 2015; 313:1325-1335; Hankey et al. Lancet Neurol 2012; 11:512-520, каждый из которых полностью включен таким образом посредством ссылки), а другие не показали пользы (смотрите Marti-Carvajal et al. Cochrane Database Syst Rev 2015;1:CD006612; Ebbing et al. JAMA 2008; 300:795-804; Bonaa et al. N Engl J Med 2006; 354:1578-1588; Liem et al. Heart 2005; 91:1213-1214; Toole et al. JAMA 2004; 291:565-575; B vitamins in patients with recent transient ischemic attack or stroke in the VITAmins TO Prevent Stroke (VITATOPS) trial: a randomized, double-blind, parallel, placebo-controlled trial (смотрите Lancet Neurol 2010; 9:855-865; Albert et al. JAMA 2008; 299:2027-2036, каждый из которых полностью включен таким образом посредством ссылки). Во многих из этих исследований проверяли вмешательства с использованием витаминов, в первую очередь добавление витаминов группы В (B6 и B12) и соли фолиевой кислоты, для снижения уровня Hcy. Следовательно, результаты исследования зависели от искажающих результаты факторов, таких как проживание субъектов в регионах, в которых практикуется обогащение солью фолиевой кислотой, наличие почечной дисфункции, делающей их более уязвимыми к токсичности кобаламина, наличие дефицита витамина B12, связанного с плохой абсорбцией, что относительно часто встречается у пожилых людей, или нахождение на антитромбоцитарных препаратах. В этих недавних анализах учитывались эти искажающие результаты факторы, и был сделан вывод, что при учете таких ключевых переменных повышенный уровень tHcy увеличивает риск инсульта в общей популяции (смотрите Mudd et al. Arterioscler Thromb Vasc Biol 2000; 20:1704-1706; Spence JD. Int J Stroke. 2016 Oct;11(7):744-7; Spence JD, Clin Chem Lab Med. 2013 Mar 1; 51(3):633-7, каждый из которых полностью включен таким образом посредством ссылки).
[0244] Понижающая уровень Hcy терапия снижает риск инсульта даже у индивидуумов без CBSDH. В испытании HOPE-2 (Heart Outcomes Prevention Evaluation 2) 5522 взрослых в возрасте ≥55, лет с сердечнососудистым заболеванием или сахарным диабетом в анамнезе и с по крайней мере одним дополнительным фактором риска развития сердечнососудистого заболевания, были рандомизированы для приема витаминных добавок (фолиевой кислоты, витамина B6 и витамина B12) или плацебо в течение 5 лет (смотрите Saposnik et al. Stroke 2009; 40:1365-1372, который полностью включен таким образом посредством ссылки). Средние исходные концентрации Hcy составляли 11,5 мкмоль/л в обеих группах, и пациенты, ежедневно принимавшие витаминную добавку, содержащую >0,2 мг фолиевой кислоты, на исходном уровне были исключены из исследования. В целом, снижение уровня Hcy (в среднем на 3,0 мкмоль/л по сравнению с плацебо) было связано со значительным снижением относительного риска инсульта на 27% (абсолютное снижение на 1,3%) (HR=0,75; 95% CI от 0,59 до 0,97) и незначительным снижением относительного риска ишемического инсульта (HR=0,81; 95% CI, от 0,60 до 1,09) и геморрагического инсульта (HR=0,80; 95% CI, 0,32-2,02). При анализе подгрупп относительный риск инсульта был больше всего снижен среди пациентов с исходными уровнями Hcy в самых верхних квартилях (снижение абсолютного риска на 4,3%). Наибольшая польза от лечения отмечалась у пациентов в возрасте <69 лет, проживающих в регионах, в которых продукты не обогащались фолиевой кислотой, и у тех, кто не получал антитромбоцитарные или гиполипидемические препараты на момент включения в исследование. Таким образом, в испытании HOPE-2 сообщалось о снижении заболеваемостью инсультом у индивидуумов, получавших витамины группы В, по сравнению с плацебо (относительный риск (HR)=0,75; 95% CI от 0,59 до 0,97), тогда как риск инфаркта миокарда был одинаковым в обеих группах лечения (RR=0,98; 95% CI от 0,85 до 1,14) (смотрите Saposnik et al. Stroke 2009; 40:1365-1372; Lonn E, Yusuf S, Arnold MJ et al. Homocysteine lowering with folic acid and B vitamins in vascular disease. N Engl J Med 2006; 354:1567-1577, оба из которых полностью включены таким образом посредством ссылки).
[0245] В соответствии с результатами испытания HOPE-2, в результате субанализа испытания VITATOPS, в котором 8164 пациента с недавно перенесенным инсультом или транзиторной ишемической атакой были рандомизированы для двойного слепого лечения витаминами группы В или плацебо в среднем в течение 3,4 лет, установили, что витамины группы В значительно снижали основной составной исход (инсульт, инфаркт миокарда или смерть от сердечнососудистых причин) среди пациентов, не получавших антитромбоцитарную терапию на исходном уровне (17% в сравнение с 21% в группе плацебо; HR=0,76, 0,60-0,96). Не наблюдалось значительного эффекта витаминов группы В у индивидуумов, получающих антитромбоцитарную терапию (смотрите Hankey et al. Antiplatelet therapy and the effects of B vitamins in patients with previous stroke or transient ischemic attack: a post-hoc sub-analysis of VITATOPS, a randomized, placebo-controlled trial. Lancet Neurol 2012; 11:512-520, который полностью включен таким образом посредством ссылки). В этом исследовании уровни tHcy значительно снижались с 12,4-13,7 мкмоль/л на исходном уровне до 9,9-10,5 мкмоль/л после витаминотерапии, независимо от того, получали ли пациенты антитромбоцитарную терапию (p<0,0001 для обеих групп лечения) (смотрите Hankey et al. Lancet Neurol 2012; 11:512-520, который полностью включен таким образом посредством ссылки).
[0246] Полагают, что каскады воспалительных реакций вносят вклад в патогенез ишемического инсульта. В отчете Framingham Offspring Study на 3224 участниках (смотрите Shoamanesh et al. Neurology. 2016 Sep;87(12):1206-11, который полностью включен таким образом посредством ссылки) пришли к заключению, что повышенные уровни tHcy и трех других маркеров воспаления были тесно связаны с риском ишемического инсульта и увеличивали прогностическую способность оценки профиля риска инсульта по Фрамингеской шкале.
[0247] Метаанализ данных исследований VISP и VITATOPS показал, что у пациентов с нормальной функцией почек, ранее не подвергавшихся воздействию высоких доз цианокобаламина, наблюдалась значительная польза от витаминотерапии, включающей цианокобаламин в высоких дозах (0,78, 0,67-0,90; взаимодействие p=0,03), тогда как витаминотерапия, включающая цианокобаламин (форму витамина группы B) в высоких дозах, не влияла на риск инсульта у индивидуумов с нарушением функции почек (RR=1,04, 95% CI от 0,84 до 1,27) (смотрите Spence JD. Lancet Neurol. 2007 Sep; 6(9):830-8, который полностью включен таким образом посредством ссылки). Эти результаты свидетельствуют о потенциально искажающих эффектах цианокобаламина, известного своей нефротоксичностью, связанных с накоплением цианидов у пациентов со значительным нарушением функции почек (смотрите Spence JD, Clin Chem Lab Med. 2013 Mar 1;51(3):633-7, который полностью включен таким образом посредством ссылки). В соответствии с этим, в исследовании DIVINe (Diabetic Intervention with Vitamins in Nephropathy) витамины группы В в высоких дозах, в том числе цианокобаламин в количестве 1000 мкг, были вредными, усиливая снижение eGFR (установленной скорости клубочковой фильтрации) (смотрите Spence JD. Int J Stroke. 2016 Oct; 11(7):744-7; House et al. JAMA 2010; 303: 1603-1609, оба из которых полностью включены таким образом посредством ссылки). В совокупности такие данные подтверждают применение не являющихся цианидсодержащими витаминов группы В, таких как метилкобаламин, вместо цианокобаламина, для снижения уровней Hcy у индивидуумов с высоким риском инсульта, особенно с почечной недостаточностью.
[0248] Токсичность цианокобаламина и цианида, кроме того, рассматривалась в предыдущих испытаниях как искажающие факторы при наличии почечной недостаточности по результатам CSPPT (China Stroke Primary Prevention Trial (смотрите Huo et al. JAMA. 2015 Apr 7; 313(13):1325-35, который полностью включен таким образом посредством ссылки)). Польза от лечения, продемонстрированная в случае почечной недостаточности при CSPPT, противоречила отсутствию пользы, отмечаемому в исследованиях DIVINe, VISP и VITOPS, вероятно, из-за лечения цианокобаламином в последнем исследовании.
[0249] Поскольку в Китае обогащение солью фолиевой кислоты до сих пор не внедрено, эффект добавления фолиевой кислоты на снижение уровней tHcy мог быть изучен там в большой популяции. CSPPT представляло собой рандомизированное двойное слепое исследование, проведенное на 20702 взрослых с гипертонией, но без инсульта или инфаркта миокарда в анамнезе, в котором было продемонстрировано, что фолиевая кислота значительно снижает риск первого инсульта (2,7 в сравнение с 3,4% без фолиевой кислоты, HR=0,79; 95% CI от 0,68 до 0,93), первого ишемического инсульта (2,2 в сравнение с 2,8% без фолиевой кислоты, HR=0,76; 95% CI от 0,64 до 0,91) и составных сердечнососудистых событий (смерти от сердечнососудистых событий, инфаркта миокарда и инсульта; 3,1% в сравнение с 3,9% без фолиевой кислоты, HR=0,80; 95% CI от 0,69 до 0,92). Напротив, между двумя группами не было значимых различий в риске геморрагического инсульта, смертности по всем причинам или частоте нежелательных явлений. В подисследовании CSPPT (смотрите Xu et al. JAMA Intern Med. 2016 Oct 1; 176(10):1443-1450, который полностью включен таким образом посредством ссылки), оба субъекта с почечной недостаточностью или без нее (eGFR ниже 60 мл/мин/1,73 м2) получили пользу от фолиевой кислоты, и подисследование, кроме того, подтвердило, что в группе, получавшей фолиевую кислоту, наблюдалось гораздо большее падение уровня Hcy в сыворотке, чем в группе, не получавшей фолиевую кислоту (1,9 в сравнение с 0,2 мкмоль/л, соответственно, p<0,001).
[0250] В Кокрановском обзоре 2017 г. (смотрите Martí-Carvajal et al. Cochrane Database Syst Rev. 2017 Aug 17;8:CD006612, который полностью включен таким образом посредством ссылки), в котором анализируются 15 рандомизированных контролируемых испытаний, включающих 74422 участника, сообщалось о небольшом различии в эффекте снижения уровня Hcy с помощью витаминов группы В на инсульт, но отсутствии эффектов на инфаркт миокарда, смерть по любой причине или неблагоприятные явления. По сравнению с плацебо/стандартной терапией вмешательства, снижающие уровень Hcy, были связаны со снижением частоты инсультов с несмертельным или смертельным исходом (4,33% в сравнение с 5,1% для контрольной группы; RR=0,90, 95% CI от 0,82 до 0,99), но не влияли на частоту инфарктов миокарда с несмертельным или смертельным исходом (7,1% в сравнение с 6,0% для плацебо; относительный риск (RR)=1,02, 95% CI от 0,95 до 1,10) или смерти по любой причине (11,7% в сравнение с 12,3% для плацебо; RR=1,01, 95% CI от 0,96 до 1,06) в общей популяции. Этот обзор представлял собой обновление трех более ранних версий (2009, 2013 и 2015), в которых ранее был сделан вывод об отсутствии доказательств, подтверждающих эффекты снижающих уровень Hcy вмешательств на сердечнососудистые события, хотя в обзоре 2015 года указывалось на незначительную тенденцию к снижению частоты инсульта (смотрите Marti-Carvajal Cochrane Database Syst Rev 2015;1:CD006612, который полностью включен таким образом посредством ссылки). Сила доказательств эффекта вмешательств, снижающих уровень Hcy, на инсульт становилась больше по мере того, как стали доступны дополнительные испытания.
[0251] В исследованиях, включенных в обзор, использовались различные схемы добавления витаминов в качестве понижающей уровень Hcy терапии (смотрите Martí-Carvajal et al. Cochrane Database Syst Rev. 2017 Aug 17; 8:CD006612, который полностью включен таким образом посредством ссылки). Обзор 2017 года добавил три новых испытания к обзору 2015 года. Из общего числа в 10 испытаниях использовали пиридоксин плюс витамины B9 (соль фолиевой кислоты) и B12, в пяти - только витамин B9, а в одном из 10 использовали 5-метилтетрагидрофолат вместо фолиевой кислоты. Некоторые испытания включали сопутствующие лекарственные средства (как в контрольной группе, так и в группе, получавшей витамины), 7 испытаний с гиполипидемическими средствами и одно с антигипертензивными средствами. В целом, понижающее уровень Hcy лечение приводило к относительно небольшому снижению средних уровней tHcy. Кроме того, три исследования были проведены на популяции, обогащенной фолиевой кислотой, и два - на смешанной популяции (некоторые субъекты получали обогащенную пищу, а другие - нет), что могло замаскировать эффекты в виде снижения уровня Hcy. Принимая во внимание искажающие факторы, которые могут повлиять на такие исследования, неудивительно, что в более ранних обзорах не было выявлено каких-либо значительных эффектов схем витаминотерапии на сердечнососудистые события, а в последнем обзоре сообщалось лишь об умеренных эффектах на инсульт. Также следует отметить, что многие потенциальные причины повышенных уровней Hcy не были изучены в исследованиях, включенных в Кокрановский обзор (смотрите Marti-Carvajal et al. Cochrane Database Syst Rev 2015;1:CD006612, который полностью включен таким образом посредством ссылки). Могут быть дополнительные факторы, влияющие на патофизиологию риска развития сердечнососудистого заболевания у пациентов с CBSDH и в более молодом возрасте, чем в общей популяции. Примечательно, что даже умеренные снижения уровней Hcy в значительной степени связаны со снижением риска инсульта.
[0252] Интересный вопрос, вытекающий из нескольких из этих анализов, заключается в том, почему некоторые исследования показали эффект уровней Hcy на инсульт, но не на инфаркт миокарда. В связи с этим вопросом Spence (смотрите Spence JD. Lancet Neurol. 2007 Sep; 6(9):830-8, который полностью включен таким образом посредством ссылки) указал на ключевые различия между инфарктом миокарда и инфарктом головного мозга, при этом инфаркт головного мозга тесно связан с тромбозом/эмболией, но тромбоз in situ является вторичным по отношению к разрушению бляшки в коронарной артерии почти во всех случаях инфаркта миокарда. Поэтому Spence пришел к выводу, что значительная часть инсультов связана с тромботическими процессами, которые могут быть связаны с повышением уровня tHcy.
[0253] Повышенные уровни tHcy могут быть важны не только при кардиоэмболическом инсульте, но также при атероэмболическом и лакунарном инфаркте. Исследование на пожилых пациентах с фибрилляцией предсердий, получавших антикоагулянтную терапию, показало, что высокие уровни tHcy (>90-ого процентиля) были связаны с 4,7-кратным увеличением ишемических осложнений (смотрите Poli et al. J Am Coll Cardiol 2009; 54:999-1002, который полностью включен таким образом посредством ссылки). Другое исследование на пациентах с криптогенным ишемическим инсультом показало, что у пациентов с открытым овальным окном (фактором риска инфаркта головного мозга) уровни tHcy в плазме были значительно выше, чем у пациентов без него (8,9±3 в сравнение с 7,9±2,6 мкмоль/л, соответственно; p=0,021) (смотрите Ozdemir et al. J Neurol Sci 2008; 275:121-127, который полностью включен таким образом посредством ссылки). При рассмотрении таких данных Spence (смотрите Spence JD. Homocysteine lowering for stroke prevention: Unravelling the complexity of the evidence. Int J Stroke. 2016 Oct; 11(7):744-7, который полностью включен таким образом посредством ссылки) сделал предположение, что Hcy в первую очередь влияет на образование эритроцитарного тромба (фибриновой полимерной сетки с захваченными эритроцитами, которая образуется в условиях стаза), но что лакунарный инфаркт и бляшки в сонных артериях также в значительной степени связаны с tHcy, поскольку уровни tHcy также были значительно выше у пациентов с микроэмболами при транскраниальной допплерографии (16,2 против 10,1 ммоль/л), и большинство таких микроэмболов, как полагают, представляют собой агрегаты тромбоцитов, количество которых снижается с помощью двойной антитромбоцитарной терапии (смотрите Spence JD. Homocysteine lowering for stroke prevention: Unravelling the complexity of the evidence. Int J Stroke. 2016 Oct; 11(7):744-7, который полностью включен таким образом посредством ссылки).
[0254] В исследовании, проведенном на 32 пациентах с CBSDH (в возрасте от 9 до 66 лет), подвергнутых лечение пиридоксином, фолиевой кислотой и гидроксокобаламином, в общей сложности 539 пациенто-лет, зарегистрировано два сердечнососудистых события (одна эмболия легочной артерии со смертельным исходом и один инфаркт миокарда) во время лечения (смотрите Wilcken et al. J Inherit Metab Dis 1997; 20:295-300, который полностью включен таким образом посредством ссылки). Согласно эпидемиологическому исследованию, проведенному Mudd и др., за тот же период времени без лечения можно было бы ожидать 21 событие (RR=0,09 (95% CI от 0,02 до 0,38); p=0,0001). Во втором исследовании, проведенном на 84 пациентах из трех стран в возрасте от 2,5 до 70 лет, зарегистрировано пять случаев эмболии вен (VE) в течение 1314 пациенто-лет лечения, одна эмболия легочной артерии, два инфаркта миокарда и два случая аневризмы брюшной аорты (смотрите Yap et al. Semin Thromb Hemost 2000; 26:335-340, который полностью включен таким образом посредством ссылки). Согласно Mudd и др. (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31, который полностью включен таким образом посредством ссылки) у не подвергнутых лечению пациентов можно было бы ожидать 53 случая VE RR=0,091 (95% CI от 0,043 до 0,190); р<0,001).
[0255] Доказательства, подтверждающие эти результаты, получены из крупного международного, проводимого во множестве центров исследования по данным наблюдений 158 пациентов с CBSDH (смотрите Yap et al. Arterioscler Thromb Vase Biol 2001; 21:2080-2085, который полностью включен таким образом посредством ссылки), большинство в возрасте от 10 до 30 лет. В этом исследовании наблюдали за 17 сердечнососудистыми событиями у 12 подвергнутых лечению индивидуумов, тремя случаями эмболии легочной артерии, двумя случаями инфаркта миокарда, пятью случаями тромбоза глубоких вен, тремя нарушениями мозгового кровообращения, одной транзиторной ишемической атакой, одним тромбозом сагиттального синуса и двумя аневризмами брюшной аорты. Без лечения в схожей популяции можно было бы ожидать 112 сердечнососудистых события (RR=0,09 (95% PI от 0,036 до 0,228); p<0,0001). Это исследование также подчеркивает, что даже подвергнутые лечению и тщательно наблюдаемые молодые взрослые пациенты с CBSDH страдают от плохих клинических последствий по сравнению с общей популяцией.
[0256] Повышенные уровни tHcy в плазме является фактором риска развития сердечнососудистого заболевания и сильным прогностическим фактором смертности у пациентов с CAD (ишемической болезнью сердца), как с CBSD, так и без нее (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31; Karaca et al. Gene 2014; 534:197-203; Kelly et al. Neurology 2003; 60:275-279; Faeh et al. Swiss Med Wkly 2006; 136:745-756; Boushey et al. JAMA 1995; 274:1049-1057; Clarke et al. JAMA 2002; 288:2015-2022; Hankey et al. Lancet 1999; 354:407-413; Khan et al. Stroke 2008; 39:2943-2949; Graham et al. JAMA 1997; 277:1775-1781; Clarke et al. N Engl J Med 1991; 324:1149-1155; Clarke et al. Ir J Med Sci 1992; 161:61-65; Woodward et al. Blood Coagul Fibrinolysis 2006; 17:1-5; Refsum et al. Annu Rev Med 1998; 49:31-62; Yoo et al. Stroke 1998; 29:2478-2483; Selsun et al. N Engl J Med 1995; 332:286-291; Wald et al. BMJ 2002; 325:1202; Bautista et al. J Clin Epidemiol 2002; 55:882-887; Brattstrom et al. Atherosclerosis 1990; 81:51-60; Lussana et al. Thromb Res 2013; 132:681-684; Casas et al. Lancet 2005; 365:224-232; McCully KS. Am J Pathol 1969; 56:111-128; Magner et al. J Inherit Metab Dis 2011; 34:33-37; Wilcken et al. J Clin Invest 1976; 57:1079-1082; Nygard et al. N Engl J Med 1997; 337:230-236, каждый из которых полностью включен таким образом посредством ссылки).
[0257] Из доказательств причинно-следственной связи между уровнями tHcy и риском развития сердечнососудистых заболеваний (смотрите Boushey et al. JAMA 1995; 274:1049-1057, который полностью включен таким образом посредством ссылки), самые сильные взаимосвязи были продемонстрированы между уровнем tHcy и инсультом или PAD (смотрите Clarke et al. JAMA 2002; 288:2015-2022; Khan et al. Stroke 2008; 39:2943-2949; Wald et al. BMJ 2002; 325:1202; Casas et al. Lancet 2005; 365:224-232; Brattstrom et al. Haemostasis 1989;19 Suppl 1:35-44, каждых из которых полностью включен таким образом посредством ссылки), в том числе у пациентов с гомозиготными и гетерозиготными мутациями CBS (смотрите Rubba et al. Metabolism 1990; 39:1191-1195, который полностью включен таким образом посредством ссылки).
[0258] Механизмы, потенциально связывающие повышенный уровень Hcy с повреждением сосудов, разнообразны и сложны. Несколько исследований выявили вовлечение окислительного стресса (смотрите Faverzani et al. Cell Mol Neurobiol 2017; Nowak et al. Arterioscler Thromb Vasc Biol 2017;37: e41-e52; Vanzin et al. Mol Genet Metab 2011; 104:112-117; Vanzin et al. Gene 2014; 539:270-274; Vanzin et al. Lipid, Cell Mol Neurobiol 2015; 35:899-911, каждый из которых полностью включен таким образом посредством ссылки), в том числе за счет активации через NF-κB воспалительной/иммунной реакции (смотрите Rodriguez-Ayala et al. Atherosclerosis 2005; 180:333-340; van Guldener et al. Curr Hypertens Rep 2003; 5:26-31, оба из которых полностью включены таким образом посредством ссылки). Хотя такие воспалительные процессы характерны для атеросклероза, типичные атеросклеротические поражения необязательно должны предшествовать тромботическим событиям у пациентов с CBSDH (смотрите Rubba et al. Stroke 1994; 25:943-950; de Valk et al. Stroke 1996; 27:1134-1136, оба из которых полностью включены таким образом посредством ссылки). Вместо этого полагают, что срединное повреждение, ведущее к тромбозу, вызвано Hcy-опосредованным нарушением функции эндотелия (смотрите Marti-Carvajal et al. Cochrane Database Syst Rev 2015;1:CD006612; Celermajer et al. J Am Coll Cardiol 1993; 22:854-858; Rubba et al. Metabolism 1990; 39:1191-1195; Jiang et al. Arterioscler Thromb Vasc Biol 2005; 25:2515-2521; Hossain et al. J Biol Chem 2003; 278:30317-30327; Cai et al. Blood 2000; 96:2140-2148; Zhang et al. J Biol Chem 2001; 276:35867-35874; Papapetropoulos et al. Proc Natl Acad Sci USA 2009; 106:21972-21977; Szabo et al. Br J Pharmacol 2011; 164:853-865; Chiku et al. J Biol Chem 2009; 284:11601-11612; Wang et al. Antioxid Redox Signal 2010; 12:1065-1077; Saha S, et al. FASEB J 2016; 30:441-456; Ebbing et al. JAMA 2008; 300:795-804; Bonaa et al. N Engl J Med 2006; 354:1578-1588, каждый из которых полностью включен таким образом посредством ссылки), усилением путей свертывания крови (смотрите Spence JD. Int J Stroke. 2016 Oct; 11(7):744-7; Fryer et al. Arterioscler Thromb 1993; 13:1327-1333; Lentz et al. J Clin Invest 1991; 88:1906-1914, каждый из которых полностью включен таким образом посредством ссылки) и увеличением расширения сосудов, которые схожи с тромботическими процессами, подразумеваемыми у пациентов с синдромом Марфана (смотрите Kelly et al. Neurology 2003; 60:275-279; Tripathi P. Molecular and biochemical aspects of homocysteine in cardiovascular diseases. International Cardiovascular Forum J 2016; 6:13; van Guldener et al. Curr Hypertens Rep 2003; 5:26-31; Hackam et al. JAMA 2003; 290:932-940; Baumbach et al. Circ Res 2002; 91:931-937; Evangelisti et al. Int J Cardiol 2009; 134:251-254; de Valk et al. Stroke 1996; 27:1134-1136, каждый из которых полностью включен таким образом посредством ссылки). В соответствии с исследованиями нарушения функции эндотелия у пациентов с CBSDH, фармакологические и генетические исследования выявили участие CBS-опосредованной S-сульфгидратации белков в поддержании здоровья и функции сосудов (смотрите Celermajer et al. J Am Coll Cardiol 1993; 22:854-858; Rubba et al. Metabolism 1990; 39:1191-1195, оба из которых полностью включены таким образом посредством ссылки). Таким образом, вполне вероятно, что механизмы повреждения сосудов у пациентов с CBSDH более разнообразны, чем в общей популяции с сердечнососудистыми заболеваниями.
[0259] Имеется большое число данных о том, что снижение уровня Hcy полезно для снижения риска инсульта у индивидуумов с CBSDH и без нее (смотрите Saposnik et al. Stroke 2009; 40:1365-1372; Huo et al. JAMA 2015; 313:1325-1335; Lonn et al. N Engl J Med 2006; 354:1567-1577; Hankey et al. Lancet Neurol 2012; 11:512-520; Spence JD. Lancet Neurol. 2007 Sep; 6(9):830-8; каждый из который полностью включен таким образом посредством ссылки). Хотя средние исходные уровни Hcy были относительно низкими в исследованиях, проведенных на общей популяции, снижение частоты инсульта в значительной степени коррелировало с вмешательствами для снижения уровня Hcy, указывая на пользу даже небольших снижений уровней tHcy.
[0260] Обновленные обзоры соответствующих испытаний подтверждают благоприятные воздействия понижающего уровень Hcy лечения на инсульт (смотрите Martí-Carvajal et al. Cochrane Database Syst Rev. 2017 Aug 17; 8:CD006612, который полностью включен таким образом посредством ссылки). Искажающие результаты факторы, таких как обогащение солью фолиевой кислоты, наличие дефицита витамина B12 или нарушения функции почек, делающие пациентов уязвимыми к высокой дозе цианокобаламина, или прием субъектами антитромбоцитарных препаратов, сделали неясными результаты испытаний. Недавние анализы показали, что при учете таких факторов связь между уровнем tHcy и риском инсульта была сильной в общей популяции (смотрите Spence JD, Clin Chem Lab Med. 2013 Mar 1; 51(3):633-7, который полностью включен таким образом посредством ссылки). Однако важно, что у пациентов с CBSDH с гораздо более высокими уровнями tHcy, чем в общей популяции, была последовательно продемонстрировано польза для здоровья сердечнососудистой системы от снижения Hcy (смотрите Yap et al. J Inherit Metab Dis 1998; 21:738-747; Eslamiyeh et al. Iran J Child Neurol 2015; 9:53-57; Saboul et al. J Child Neurol 2015; 30:107-112; Yap et al. Arterioscler Thromb Vasc Biol 2001; 21:2080-2085; Woods et al. BMJ Case Rep 2017;2017; Wilcken et al. J Inherit Metab Dis 1997; 20:295-300; Yap et al. Semin Thromb Hemost 2000; 26:335-340; Ruhoy et al. Pediatr Neurol 2014; 50:108-111, каждый из который полностью включен таким образом посредством ссылки).
[0261] Эти данные свидетельствуют о том, что повышенный уровень Hcy является фактором риска развития сердечнососудистого заболевания, особенно инсульта, у пациентов с CBSDH и без нее, и что риска развития сердечнососудистых или цереброваскулярных заболеваний можно снизить посредством длительной Hcy-снижающей терапии.
[0262] Тромбоэмболия является основной причиной заболеваемости и преждевременной смерти у пациентов с CBSDH (смотрите Mudd et al. Am J Hum Genet 1985; 37: 1-31; Karaca et al. Gene 2014; 534: 197-203; Yap S. J Inherit Metab Dis 2003; 26:259-265, каждый из которых полностью включен таким образом посредством ссылки). Общая частота тромбоэмболических событий у пациентов с CBSDH, не подвергнутой лечения, составляет приблизительно 10% в год (смотрите Cattaneo M. Semin Thromb Hemost 2006; 32:716-723, который полностью включен таким образом посредством ссылки), при этом риск возрастает после хирургического вмешательства и во время или сразу после беременности (смотрите Mudd et al. Am J Hum Genet 1985; 37: 1-31; Novy et al. Thromb Haemost 2010; 103:871-873, оба из которых полностью включены таким образом посредством ссылки). Тромбоэмболия может поразить любой кровеносный сосуд, но тромбоз вен (в частности, тромбоз мозговых вен и синусов (CSVT)) встречается чаще, чем тромбоз артерий у пациентов с CBSDH (смотрите Mudd et al. Am J Hum Genet 1985; 37: 1-31; Karaca et al. al. Gene 2014; 534: 197-203; Eslamiyeh et al. Iran i Child Neurol 2015; 9:53-57; Saboul et al. J Child Neurol 2015; 30: 107-112, каждый из которых полностью включен таким образом посредством ссылки).
[0263] Исследование на 629 не подвергнутых лечению пациентах с CBSDH показало, что из наблюдаемых 253 сердечнососудистых событий (возникших у 158 пациентов) 81 (32%) были нарушениями мозгового кровообращения, 130 (51%) поражениями периферических вен (из них 32 привели к эмболии легочной артерии), 10 (4%) привели к инфаркту миокарда (MI), 28 (11%) были поражениями периферических артерий, и четыре (2%) не попали ни в одну из этих категорий (смотрите Mudd et al. Am J Hum Genet 1985; 37: 1-31, который полностью включен таким образом посредством ссылки). Нарушения мозгового кровообращения, особенно CSVT, были описаны у младенцев (смотрите Mahhale et al. J Pediatr Neurosci. 2017 Apr-Jun; 12(2):206-207, который полностью включен таким образом посредством ссылки), хотя чаще они возникают у молодых взрослых (смотрите Yap et al. Arterioscler Thromb Vase Biol 2001; 21:2080-2085, который полностью включен таким образом посредством ссылки). Сообщалось, что цереброваскулярные события лишь косвенно связаны с категорией пациентов с реакцией на пиридоксин.
[0264] Риск сердечнососудистых событий составлял приблизительно 30% у пациентов в возрасте <20 лет, увеличиваясь до 50% к возрасту 30 лет. Однако симптомы могут возникать в любом возрасте, и тромбоз со смертельным исходом был описан у младенцев уже в возрасте 6 месяцев (смотрите Cardo et al. Dev Med Child Neurol 1999; 41:132-135, который полностью включен таким образом посредством ссылки). После 10-летнего возраста ожидается одно сердечнососудистое событие в 25 лет. Как правило, первыми признаками CBSDH у детей являются умственная отсталость, проявляющаяся задержкой развития в течение первого или второго года жизни, и/или смещение хрусталика/миопия высокой степени. Напротив, у взрослых чаще возникают сердечнососудистые события.
D. Влияния диеты на фенотипические эффекты
[0265] В некоторых вариантах осуществления мышей I278T, модель HCU на мыши, использовали для оценки длительного воздействия ферментотерапии для HCU с использованием 20NHS PEG-CBS на клинические конечные точки, относящиеся к являющимся людьми пациентам. Эффективность 20NHS PEG-CBS на фоне нормального потребления метионина (REG) и диеты с ограничением Met (MRD), а также только MRD. Лечение 20NHS PEG-CBS может привести к снижению концентрации гомоцистеина в плазме на 90% и коррекции обучения/познания, нарушения функции эндотелия, гемостаза, минерализации костей и фенотипов состава тела, связанных с HCU. В некоторых вариантах осуществления лечение 20NHS PEG-CBS на фоне MRD-диеты нормализовало уровень Hcy в плазме. Было замечено, что только MRD-диета снижает уровень Hcy в плазме на 67% и корректирует фенотип HCU у мышей I278T. Однако MRD-диета повышала тревогу и снижала минеральное содержание в костной ткани как у мышей I278T, так и у контрольных мышей дикого типа. Таким образом, 20NHS PEG-CBS очень эффективна для лечения HCU у субъектов на фоне нормального потребления Met или диеты с ограничением Met. Фактически, ферментотерапия с использованием 20NHS PEG-CBS на фоне нормального потребления Met работает одинаково или дает лучшие результаты по сравнению с диетой с ограничением Met.
E. Неврологические осложнения
[0266] Исследования показали, что ранние снижения уровней Hcy, вызванные диетой с низким содержанием Met, добавками фолиевой кислоты/витамина группы B и/или терапией с использованием пиридоксина и бетаина, могут предотвратить, а иногда и обратить вспять прогрессирование различных неврологических расстройств и обеспечивать нормальное развитие IQ у пациентов с CBSDH (смотрите El Bashir et al. JIMD Rep 2015; 21:89-95; Yap et al. J Inherit Metab Dis 2001; 24:437-447; Mech AW, Farah A. Correlation of clinical response with homocysteine reduction during therapy with reduced B vitamins in patients with MDD who are positive for MTHFR C677T or A1298C polymorphism: a randomized, double-blind, placebo-controlled study. J Clin Psychiatry 2016; 77:668-671; Grobe H. Eur J Pediatr 1980; 135:199-203; каждый из которых полностью включен таким образом посредством ссылки). Дополнительные доказательства представлены в исследованиях конкретных случаев у пациентов с CBSDH, у которых значительные снижения, даже нормализация, уровней Hcy приводили к полной или частичной коррекции последствий для здоровья ЦНС (смотрите Yap et al. J Inherit Metab Dis 2001; 24:437-447; Brenton et al. J Child Neurol 2014; 29:88-92; Rezazadeh et al. Child Neurol Open 2014; 1:2329048X14545870; Kaeser et al. J Neurol Neurosurg Psychiatry 1969; 32:88-93; Colafrancesco et al. Eur J Pediatr 2015; 174:1263-1266; Yokoi et al. Pediatr Int 2008; 50:694-695; Li et al. Pathology 1999; 31:221-224, каждый из которых полностью включен таким образом посредством ссылки).
[0267] Связи между повышенными уровнями Hcy и связанными с ЦНС симптомами, включающими умственную отсталость, нейродегенеративные заболевания, судороги, дистонию, психоз, когнитивные расстройства, деменцию и депрессию, полностью подтверждены документами у пациентов с CBSDH и в общей популяции (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74; Abbott et al. Am J Med Genet 1987; 26:959-969; Mudd et al. Disorders of transsulfuration. In: Scriver CL, Beaudet AL, Sly WS, Valle D, eds. The Metabolic and Molecular Basis of Inherited Diseases. 7 ed. New York: McGraw Hill; 2001;1279-1327; Hidalgo et al. Eur Child Adolesc Psychiatry 2014; 23:235-238; Smith et al. PLoS One 2010; 5:e12244; Seshadri et al. N Engl J Med 2002; 346:476-483; Bottiglieri et al. J Neurol Neurosurg Psychiatry 2000; 69:228-232; Bjelland et al. Arch Gen Psychiatry 2003; 60:618-626; Tolmunen et al. Am J Clin Nutr 2004; 80:1574-1578; Kaeser et al. J Neurol Neurosurg Psychiatry 1969; 32:88-93; Golimbet et al. Psychiatry Res 2009; 170:168-171; Clarke et al. Arch Neurol 1998; 55:1449-1455; Permoda-Osip et al. Neuropsychobiology 2014; 69:107-111; Oliveira et al. BMJ Case Rep 2016; 2016; Troen et al. Proc Natl Acad Sci USA 2008; 105:12474-12479; Sudduth et al. J Cereb Blood Flow Metab 2013; 33:708-715; Hainsworth et al. Biochim Biophys Acta 2016; 1862:1008-1017; Herrmann et al. Clin Chem Lab Med 2011; 49:435-441; Kim et al. J Nutr 2007; 137:2093-2097; Selhub et al. Am J Clin Nutr 2000; 71:614S-620S; McCaddon et al. Dement Geriatr Cogn Disord 2001; 12:309-313; Smallwood et al. Neuropathol Appl Neurobiol 2012; 38:337-343; Beydoun et al. BMC Public Health 2014; 14:643; Gortz et al. J Neurol Sci 2004; 218:109-114; Health Quality O. Vitamin B12 and cognitive function: an evidence-based analysis. Ont.Health Technol.Assess.Ser.13 (23), 1e45. 2013. Тип ссылки: Интернет-источник; Salagre et al. Eur Psychiatry 2017; 43:81-91, каждый из которых полностью включен таким образом посредством ссылки). Полагают, что механизмы, ведущие к расстройствам ЦНС у индивидуумов с повышенными уровнями Hcy, включают опосредованное tHcy повреждение нейронов (смотрите Mudd et al. Disorders of transsulfuration. In: Scriver CL, Beaudet AL, Sly WS, Valle D, eds. The Metabolic and Molecular Basis of Inherited Diseases. 7 ed. New York: McGraw Hill; 2001; 1279-1327; Hainsworth et al. Biochim Biophys Acta 2016; 1862:1008-1017; Stefanello et al. Metab Brain Dis 2007; 22:172-182; Toborek et al. Atherosclerosis 1995; 115:217-224, каждый из которых полностью включен таким образом посредством ссылки), повреждение эндотелия сосудов, вызванное Hcy-опосредованным окислительным стрессом (смотрите Vivitsky et al. Am J Physiol Regul IntegrComp Physiol 2004;287: R39-R46, который полностью включен таким образом посредством ссылки), потерю нейронов (смотрите Yeganeh et al. J Mol Neurosci 2013; 50:551-557; Heider et al. J Neural Transm Suppl 2004;1-13, оба из которых полностью включены таким образом посредством ссылки), и ослабление активности нейронной сети (смотрите Gortz et al. J Neurol Sci 2004; 218:109-114, который полностью включен таким образом посредством ссылки). Считается, что депрессия и судороги, по крайней мере частично, вызваны Hcy-опосредованными снижениями уровней аденозина в головном мозге с последующими снижениями уровней норадреналина и дофамина (смотрите Mech et al. J Clin Psychiatry 2016; 77:668-671; Domagala et al. Thromb Res 1997; 87:411-416; Vivitsky et al. Am J Physiol Regul IntegrComp Physiol 2004; 287:R39-R46; Folstein et al. Am J Psychiatry 2007; 164:861-867, каждый из которых полностью включен таким образом посредством ссылки).
[0268] Эти данные продемонстрировали сильную корреляцию между уровнями Hcy и повышенным риском расстройств ЦНС у пациентов с CBSDH. Ранняя понижающая уровень Hcy терапия необходима для нормального развития детей с ранним началом CBSDH, а также для коррекции или ослабления расстройств ЦНС у пациентов с диагнозом CBSDH, поставленным в более позднем возрасте.
[0269] В результате исследования на 63 пациентах с CBSDH установили, что у 51% были психические расстройства, включающие тревогу и эпизодическую депрессию (10%), хронические поведенческие расстройства (например, агрессию и злоупотребление наркотиками или алкоголем) (17%), хроническое обсессивно-компульсивное расстройство (5%) и расстройства личности (19%) (смотрите Abbott et al. Am J Med Genet 1987; 26:959-969, который полностью включен таким образом посредством ссылки). Психоз может признаком, имеющимся в подростковом возрасте (смотрите Hidalgo et al. Eur Child Adolesc Psychiatry 2014; 23:235-238, который полностью включен таким образом посредством ссылки).
[0270] В отсутствие лечения приблизительно 90% пациентов, не чувствительных к пиридоксину, испытывают трудности в обучении (смотрите Mudd et al. Am J Hum Genet 1985; 37:1-31, который полностью включен таким образом посредством ссылки), при этом IQ, как правило, находится в диапазоне от 10 до 138, со средним значением=57 у индивидуумов, не чувствительных к пиридоксину, по сравнению с 79 у не подвергнутых лечению, чувствительных к пиридоксину пациентов, и 105 у подвергнутых лечению, чувствительных к пиридоксину пациентов с удовлетворительным соблюдением схемы лечения (смотрите Yap et al. J Inherit Metab Dis 2001; 24:437-447, который полностью включен таким образом посредством ссылки). Судороги возникают у 20% нечувствительных пациентов к 12 годам, и сообщалось о нескольких случаях двигательных нарушений, не связанных с инфарктом в базальных ганглиях, включая полимиоклонию, дистонию и болезнь Паркинсона (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74; Rezazadeh et al. Child Neurol Open 2014; 1:2329048X14545870, оба из которых полностью включены таким образом посредством ссылки).
[0271] Связь между CBSDH и нейропсихиатрическими симптомами была впервые описана Schimke и др. в 1965 г. (смотрите Schimke et al. JAMA 1965; 193:711-719, который полностью включен таким образом посредством ссылки). Эта связь позже была подтверждена исследованием, в котором сообщается о психопатологии у более чем 50% пациентов с дефицитом CBS (смотрите Abbott et al. Am J Med Genet 1987; 26:959-969, который полностью включен таким образом посредством ссылки). С тех пор многочисленные эпидемиологические исследования показали положительную дозозависимую взаимосвязь между даже небольшими повышениями уровней tHcy в плазме и риском расстройств ЦНС, включающих умственную отсталость и нейродегенеративные заболевания (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74; Seshadri et al. N Engl J Med 2002; 346:476-483; Clarke et al. Arch Neurol 1998; 55:1449-1455; Hainsworth et al. Biochim Biophys Acta 2016; 1862:1008-1017; Herrmann et al. Clin Chem Lab Med 2011; 49:435-441; Kim J et al. J Nutr 2007; 137:2093-2097; Selhub et al. Am J Clin Nutr 2000; 71:614S-620S; McCaddon et al. Dement Geriatr Cogn Disord 2001; 12:309-313; Smallwood et al. Neuropathol Appl Neurobiol 2012; 38:337-343; Beydoun et al. BMC Public Health 2014; 14:643; каждый из которых полностью включен таким образом посредством ссылки). В целом, у пациентов с сильно повышенными уровнями Hcy (от 50 до 200 мкМ/л), как правило, отмечалась острая дисфункция нейронов, включая судороги и психоз, тогда как более умеренные уровни Hcy (от 15 до 50 мкМ/л) связаны с когнитивным расстройством и деменцией (смотрите Mudd et al. Disorders of transsulfuration. In: Scriver CL, Beaudet AL, Sly WS, Valle D, eds. The Metabolic and Molecular Basis of Inherited Diseases. 7 ed. New York: McGraw Hill; 2001;1279-1327; Gortz et al. J Neurol Sci 2004; 218:109-114, оба из которых полностью включены таким образом посредством ссылки).
[0272] Повышенный уровень Hcy широко признан надежным и независимым фактором риска когнитивного расстройства (смотрите Smith et al. PLoS One 2010; 5:e12244; Seshadri et al. N Engl J Med 2002; 346:476-483, оба из которых полностью включены таким образом посредством ссылки), начала деменции (смотрите Health Quality O. Vitamin B12 and cognitive function: an evidence-based analysis. Ont.Health Technol.Assess.Ser.13 (23), 1e45. 2013. Тип ссылки: Интернет-источник, который полностью включен таким образом посредством ссылки) и болезни Альцгеймера (смотрите Seshadri et al. N Engl J Med 2002; 346:476-483, который полностью включен таким образом посредством ссылки). Кроме того, было показано, что повышенные уровни Hcy (>15 мкмоль/л) присутствуют у вплоть до 90% пациентов с депрессией (смотрите Bottiglieri et al. J Neurol Neurosurg Psychiatry 2000; 69:228-232; Bjelland et al. Arch Gen Psychiatry 2003; 60:618-626, оба из которых полностью включены таким образом посредством), при этом у мужчин в верхнем тертиле по уровням tHcy более чем в два раза выше вероятность страдания депрессией, чем у мужчин в самом нижнем тертиле (смотрите Tolmunen et al. Am J Clin Nutr 2004; 80:1574-1578, который полностью включен таким образом посредством ссылки). Повышенный уровень Hcy обычно регистрируется в случаях шизофрении, рассеянного склероза, болезни Паркинсона, фибромиалгии/синдрома хронической усталости (смотрите Kaeser et al. J Neurol Neurosurg Psychiatry 1969; 32:88-93; Golimbet et al. Psychiatry Res 2009; 170:168-171; Clarke et al. Arch Neurol 1998; 55:1449-1455; каждый из которых полностью включен таким образом посредством ссылки) и повторяющейся дистонии без цереброваскулярного заболевания (смотрите Sinclair et al. Mov Disord 2006; 21:1780-1782, который полностью включен таким образом посредством ссылки). Была описана возможная связь между полиморфизмом T833C гена CBS и биполярным расстройством (смотрите Permoda-Osip et al. Neuropsychobiology 2014; 69:107-111, который полностью включен таким образом посредством ссылки), а недавний метаанализ показал взаимосвязь между повышенными уровнями Hcy и манией/эутимией у индивидуумов с биполярным расстройством (смотрите Salagre et al. Eur Psychiatry 2017; 43:81-91, который полностью включен таким образом посредством ссылки). Первый известный случай периферической невропатии, связанной с CBSDH, был недавно описан у 18-летнего мужчины с CBSDH (смотрите Oliveira et al. BMJ Case Rep 2016;2016, который полностью включен таким образом посредством ссылки), а случай психоза со смертельным исходом был описан у 17-летнего мужчины с ранее не диагностированной CBSDH (смотрите Hidalgo et al. Eur Child Adolesc Psychiatry 2014; 23:235-238, который полностью включен таким образом посредством ссылки).
[0273] Прямые доказательства взаимосвязи между уровнями Hcy и деменцией получены в исследованиях на животных, в которых введение Hcy было связано с развитием патологических изменений головного мозга (смотрите Troen et al. Proc Natl Acad Sci U S A 2008; 105:12474-12479; Sudduth et al. J Cereb Blood Flow Metab 2013; 33:708-715, каждый из которых полностью включен таким образом посредством ссылки). В первом таком исследовании у самцов мышей C57BL6/J с повышенными уровнями Hcy (индуцированными диетой с недостатком витамина группы B) были значительно нарушены пространственное обучение и память, со значительным разрежением капилляров в гиппокампе без сопутствующего глиоза или нейродегенерации (смотрите Troen et al. Proc Natl Acad Sci U S A 2008; 105:12474-12479, который полностью включен таким образом посредством ссылки). Общая длина капилляров в гиппокампе обратно коррелировала с латентными периодами (задержками) выхода из водного лабиринта Морриса (r= -0,757, p<0,001) и с уровнем tHcy в плазмы (r= -0,631, p<0,007). У мышей, которых кормили, используя богатую Met диету, наблюдались схожие, но менее выраженные эффекты. Эти данные свидетельствуют о том, что повышенные уровни Hcy связаны с разрежением капилляров в головном мозге, приводящим к когнитивному расстройству в отсутствие или в случае предшествующей нейродегенерации. Это может объяснить связь между повышенными уровнями Hcy и снижением когнитивных функций у людей.
[0274] Во втором исследовании здоровых мышей кормили, используя диету с недостатком соли фолиевой кислоты, витаминов B6 и B12 и с добавлением Met, для индуцирования умеренно повышенных уровней Hcy (tHcy в плазме 82,93±3,56 мкмоль/л). У этих мышей были нарушения пространственной памяти, что оценивалось с помощью двухдневного водного лабиринта с радиальными рукавами (смотрите Sudduth et al. J Cereb Blood Flow Metab 2013; 33:708-715, который полностью включен таким образом посредством ссылки). МРТ и гистологическое исследование выявили значительную частоту микрокровоизлияний. Также наблюдались нейровоспаление и повышенная экспрессия и активность MMP2 и MMP9, обоих ферментов, участвующих в патогенезе мозгового кровоизлияния. Это предполагает связь между повышенными уровнями Hcy и сосудистой деменцией, например, при болезни Альцгеймера.
[0275] У людей изменения в белом веществе (признак повреждения сосудов) часто связаны с повышенными уровнями Hcy как у индивидуумов с CBSDH (смотрите El Bashir et al. JIMD Rep 2015; 21:89-95; Vatanavicharn et al. J Inherit Metab Dis 2008;31 Suppl 3:477-481; Brenton et al. J Child Neurol 2014; 29:88-92; Ruhoy et al. Pediatr Neurol 2014; 50:108-111; каждый из которых полностью включен таким образом посредством ссылки), так и без CBSDH (смотрите Hogervorst et al. Arch Neurol 2002; 59:787-793; Kloppenborg et al. Neurology 2014; 82:777-783; каждый из которых полностью включен таким образом посредством ссылки). Однако эти изменения не всегда связаны с признаками инсульта. Кроме того, визуализирующие исследования головного мозга пациентов с CBSDH часто показывают признаки атрофии или закупорки вен (смотрите Vatanavicham et al. J Inherit Metab Dis 2008; 31 Suppl 3:477-481, который полностью включен таким образом посредством ссылки).
[0276] Сканирование показывает диффузный симметричный анормальный увеличенный сигнал белого вещества в подкорковых структурах головного мозга и, в меньшей степени, белого вещества, находящего глубже, в полушариях головного мозга, в первую очередь теменно-затылочной области
1. Механизм
[0277] Точные механизмы, с помощью которых повышенные уровни Hcy влияют на здоровье нервной системы, неизвестно. Несколько исследований на животных показали связь между повышенными уровнями tHcy и нейротоксичностью, а также сопутствующими нервными и психическими нарушениями.
[0278] Раннее исследование показало, что очень высокие внутрибрюшинные дозы Hcy индуцировали генерализованный судорожный статус - эпилептический припадок у крыс с индуцированными кобальтом поражениями двигательной области коры головного мозга (смотрите Mudd et al. Disorders of transsulfuration. In: Scriver CL, Beaudet AL, Sly WS, Valle D, eds. The Metabolic and Molecular Basis of Inherited Diseases. 7 ed. New York: McGraw Hill; 2001; 1279-1327, который полностью включен таким образом посредством ссылки). Припадки усиливались при добавлении Met и витамина группы B, и были некоторые доказательства синергетических эффектов пиридоксаль-5'-фосфата и Hcy в отношении блокирования постсинаптических рецепторов гамма-аминомасляной кислоты. Более того, подвергание тканей неокортекса грызунов воздействию Hcy приводило к захвату аденозина в форме AdoHcy (смотрите Heinecke et al. J Biol Chem 1987; 262:10098-10103, который полностью включен таким образом посредством ссылки). Авторы заявили, что аденозин является преимущественно депрессантом при действиях в головном мозге, и что судорожные состояния и психические изменения, связанные с высокими уровнями Hcy, могут быть опосредованы сниженными уровнями аденозина в головном мозге.
[0279] Hcy связан как с нейротоксичностью, так и с морфологическими изменениями в головном мозге (смотрите Hainsworth et al. Biochim Biophys Acta 2016; 1862:1008-1017, который полностью включен таким образом посредством ссылки). Например, исследования на крысах и кроликах показали, что повреждение нейронов было вызвано Hcy-опосредованными повышениями уровней веществ, реагирующих с тиомасляной кислотой (TEARS), индикаторов окислительного стресса (смотрите Stefanello et al. Metab Brain Dis 2007; 22:172-182; Toborek et al. Atherosclerosis 1995; 115:217-224, оба из которых полностью включены таким образом посредством ссылки). Схожие повышения уровней TBARS в плазме также наблюдалось у людей после перорально назначенной Met-нагрузки (смотрите Domagala et al. Thromb Res 1997; 87:411-416, который полностью включен таким образом посредством ссылки). Более того, исследование на модели повышенных уровней Hcy на мыши свидетельствовало о том, что клеточное повреждение, вызванное окислительным стрессом, может усиливаться у пациентов с CBSDH, поскольку снижения уровней Cys приводит к низким уровням глютатиона в нейронах, важного антиоксиданта, синтезируемого из глутамата, Cys и глицина (смотрите Vivitsky et al. Am J Physiol Regul IntegrComp Physiol 2004;287: R39-R46, который полностью включен таким образом посредством ссылки).
[0280] Инъекция Hcy in vivo в левый желудочек головного мозга крыс вызывала дозозависимую гибель нейронов (смотрите Yeganeh et al. J Mol Neurosci 2013; 50:551-557, который полностью включен таким образом посредством ссылки), а инкубации нейронов тегментума (покрышки) среднего мозга крыс с Hcy приводили к меньшему количеству и более коротким дофаминергическим нейритам (смотрите Heider et al. J Neural Transm Suppl 2004; 1-13, который полностью включен таким образом посредством ссылки). В обоих исследованиях эффекты Hcy ослаблялись совместным введением Hcy с антагонистами NMDA и метаботропными глутаматными рецепторами, что позволяет предположить опосредованный глутаматными рецепторами путь для Hcy-индуцирумого повреждения нейронов. Дополнительные доказательства этого пути получены из исследования, в котором введение Hcy приводило к дозозависимому перекисному окислению липидов в синаптосомах головного мозга крыс (смотрите Jara-Prado et al. Neurotox Res 2003; 5:237-243, который полностью включен таким образом посредством ссылки). И снова эффекты ингибировались введением антагониста рецептора NMDA.
[0281] Исследование на спонтанно активных нейронах коры головного мозга эмбрионов крыс показало, что уровни Hcy, превышающие диапазон для сильно повышенных уровней Hcy, вызывали дозозависимое подавление активности нейронной сети (смотрите Gortz et al. J Neurol Sci 2004; 218:109-114, который полностью включен таким образом посредством ссылки). Эффекты, наблюдаемые в этом исследовании, не были клинически значимыми, поскольку такие завышенные уровни Hcy никогда не достигаются у пациентов с CBSDH. Однако умеренные повышения уровней гомоцистеинсульфокислоты и гомоцистеиновой кислоты (окисленных форм Hcy, часто обнаруживаемых у пациентов с повышенными уровнями Hcy) оказывали схожий эффект. В каждом случае повреждение нейронной сети ингибировалось 2-амино-5-фосфоновалериановой кислотой, что снова указывает на то, что рецептор NMDA является медиатором этого Hcy-индуцируемого нарушения функции нейронов. Эти результаты позволяют предположить, что дисфункция нейронов, связанная с повышенными уровнями Hcy, вероятно, вызвана окисленными формами Hcy, а не самим Hcy.
[0282] Отсутствие умственной отсталости, судорог и других расстройств ЦНС у пациентов с синдромом Марфана и другими заболеваниями соединительной ткани позволяет предположить, что неврологические расстройства у пациентов с CBSDH не вызваны недостатками ни фибриллина, ни коллагена (смотрите Mudd et al. Disorders of transsulfuration. In: Scriver CL, Beaudet AL, Sly WS, Valle D, eds. The Metabolic and Molecular Basis of Inherited Diseases. 7 ed. New York: McGraw Hill; 2001; 1279-1327, который полностью включен таким образом посредством ссылки). У пациентов с CBSDH, не подвергнутых лечению, повышенные уровни SAM и сниженные уровни SAH ингибируют реакции трансметилирования, необходимые для синтеза миелина, что приводит к дальнейшему повреждению нервов (смотрите Mudd et al. Disorders of transsulfuration. In: Scriver CL, Beaudet AL, Sly WS, Valle D, eds. The Metabolic and Molecular Basis of Inherited Diseases. 7 ed. New York: McGraw Hill; 2001; 1279-1327, который полностью включен таким образом посредством ссылки). Снижение синтеза миелина также может быть вызвано низкими уровнями серина у пациентов с CBSDH из-за повышенных скоростей реметилирования (смотрите Orendac et al. J Inherit Metab Dis 2003; 26:761-773, который полностью включен таким образом посредством ссылки). Наконец, метаболизм Hcy играет ключевую роль в синтезе моноаминов, предоставляя метильные группы для образования норадреналина и дофамина (смотрите Mech et al. J Clin Psychiatry 2016; 77:668-671; Folstein et al. Am J Psychiatry 2007; 164:861-867, оба из которых полностью включены таким образом посредством ссылки). Действительно, «гомоцистеиновая гипотеза депрессии» (смотрите Folstein et al. Am J Psychiatry 2007; 164:861-867, который полностью включен таким образом посредством ссылки) утверждает, что низкие уровни норадреналина и дофамина, возникающие в результате повышенных уровней Hcy, являются основной причиной депрессии.
[0283] Электронная микроскопия биоптатов головного мозга крыс показала цереброваскулярные структурные изменения у животных, которых кормили, используя диету с высоким содержанием Hcy в течение 8 недель. Эти изменения были связаны с высокими уровнями tHcy в плазме (смотрите Lee et al. J Nutr 2005; 135:544-548, который полностью включен таким образом посредством ссылки). Потребление фолиевой кислоты с пищей в течение следующих 8 недель снижало уровни tHcy в плазме до нормальных уровней и значительно уменьшало частоту повреждения сосудов. Это свидетельствует о том, что снижение уровня Hcy с использованием добавок фолиевой кислоты может уменьшить вредные эффекты на эндотелий сосудов экспериментально индуцированных повышенных уровней Hcy.
[0284] Исследование, разработанное для оценки эффективности и безопасности сокращенных витаминов группы В в качестве монотерапии у взрослых с большим депрессивным расстройством (MDD) и CBSDH, из-за по крайней мере одного полиморфизма MTHFR (N=330), показало, что лечение комбинацией сокращенных витаминов группы В значительно снижало уровни tHcy у 131 пациента, подвергнутого лечению (82,4%), (среднее снижение в этой подгруппе составило 25%; p<0,001), тогда как у пациентов, получавших плацебо, наблюдалось небольшое повышение уровней tHcy (смотрите Mech et al. J Clin Psychiatry 2016; 77:668-671, который полностью включен таким образом посредством ссылки). Подвергнутые лечению пациенты в среднем имели 12-балльное снижение по шкале оценки депрессии Монтгомери-Асберга (MADRS) к неделе 8, а 42% достигали полной ремиссии (p<0,001). Дальнейшее клиническое улучшение коррелировало со значительным снижением уровней tHcy у большинства ответивших на лечение. Хотя это исследование не проводилось на пациентах с CBSDH, оно продемонстрировало явную пользу от снижения Hcy у индивидуумов с депрессией, что подтверждает «гомоцистеиновую гипотезу депрессии гипотезу» (смотрите Folstein et al. Am J Psychiatry 2007; 164:861-867, который полностью включен таким образом посредством ссылки).
[0285] Польза понижающей уровень Hcy терапии у индивидуумов с психическими симптомами, связанными с CBSDH, была впервые продемонстрирована в исследовании 12 пациентов с поздно поставленным диагнозом (смотрите Grobe H. Eur J Pediatr 1980; 135:199-203, который полностью включен таким образом посредством ссылки). Трое из этих пациентов никогда не лечились эффективно и имели серьезные психологические расстройства с преждевременной смертью. Остальные 8 пациентов были в возрасте от 1 до 26 лет (в среднем 13 лет), и у всех были психические симптомы, включающие раздражительность, ADHD (синдром дефицита внимания и гиперактивности), апатию и психоз. Лечение пиридоксином или диетой с низким содержанием Met с добавлением L-цистеина в течение 2-9 лет сопровождалось поразительным улучшением поведения и интеллектуального развития, что коррелировало с биохимической нормализацией. Авторы подчеркнули необходимость лечения всех пациентов, независимо от возраста на момент постановки диагноза и предшествующего лечения, из-за обратимости и улучшения последствий, связанных с CBSDH, наблюдаемых в их исследовании.
[0286] Более свежие данные из ирландской программы скрининга были использованы для сравнения умственных способностей 23 нечувствительных к пиридоксину индивидуумов с CBSDH (339 пациенто-лет лечения) с таковыми у 10 здоровых сибсов в качестве контролей (смотрите Yap et al. J Inherit Metab Dis 2001; 24:437-447, который полностью включен таким образом посредством ссылки). Из 23 идентифицированных пациентов у 19 была диагностирована CBSDH с помощью NBS, и их лечили в раннем возрасте (в пределах 6 недель после рождения), у двух CBSDH выявили поздно (в возрасте 2,2 и 2,9 года), а двоих не подвергали лечению на момент оценки. Всех пациентов лечили смесью синтетических аминокислот, не содержащей Met, с добавлением цистеина, с добавками витамина B12 и фолиевой кислоты, по мере необходимости. Бетаин использовался в течение последних 5 лет в качестве дополнения к лечению у пациентов, рано подвергнутых лечению, которые стали неудовлетворительно соблюдать диету, а также у всех пациентов с поздно выявленной CBSDH.
[0287] В целом, 13 из 19 пациентов в группе рано начатого лечения (средний возраст 14,4 года; диапазон от 4,4 до 24,9) соблюдали схему лечения (что определялось по медиане уровня fHcy в плазмы в течение жизни <11 мкмоль/л) и не имели осложнений, в то время как у остальных 6 (средний возраст 19,9 лет, диапазон от 13,8 до 25,5 лет), которые неудовлетворительно соблюдали схему лечения, развились осложнения. Среднее значение IQ по полной шкале (FIQ) составило 105,8 (диапазон: от 84 до 120) в группе соблюдающих схему лечения пациентов по сравнению с 80,8 (диапазон: от 40 до 103) в группе неудовлетворительно соблюдавших схему лечения пациентов. Контрольная группа (n=10) со средним возрастом=19,4 года (диапазон: от 9,7 до 32,9) лет имела среднее значение FIQ=102 (диапазон: от 76 до 116). Два поздно выявленных пациента в возрасте 18,9 и 18,8 лет имели значение FIQ, равное 80 и 102, соответственно, в то время как два не подвергнутых лечению пациента в возрасте 22,4 и 11,7 лет имели значение FIQ, равное 52 и 53, соответственно. Не было никаких значимых различий между соблюдающими схему лечения, рано подвергнутыми лечению индивидуумами и их здоровыми родными братьями и сестрами (сибсами) (в качестве контроля), за исключением FIQ, который был значительно выше у здоровых сибсов (p=0,0397). Несмотря на относительно небольшое количество, эти результаты свидетельствуют о том, что рано начатое лечение с хорошим биохимическим контролем предотвращает умственную отсталость.
[0288] Схожие результаты были получены в исследовании методом «случай-контроль, в котором сообщалось о последствиях для развития нервной системы, образования и когнитивных функций в 32 случаях CBSDH и 25 сибсов из контрольной группы в Катаре (смотрите El Bashir et al. JIMD Rep 2015; 21:89-95, который полностью включен таким образом посредством ссылки). Средний возраст субъектов этого исследования составлял 11,2 года (диапазон: от 0,6 до 29 лет), 56% из них были мужчинами. По сравнению с не пораженными болезнью сибсами больные индивидуумы имели более низкий общий IQ (особенно по показателю кратковременной памяти, количественного мышления и визуально-пространственных областей), и у значительного числа случаев в виде подростков и взрослых были сопутствующие заболевания, а также поведенческие и эмоциональные проблемы. Из них 9 случаев (28%) CBSDH были выявлены с помощью NBS и подвергнуты лечению в первый месяц жизни. Остальным диагноз был поставлен в возрасте от 14 до 240 месяцев. Уровни tHcy и Met во время лечения были значительно ниже у пациентов, выявленных с помощью NBS, чем у тех, диагноз которым был поставлен клинически, возможно, из-за лучшего соблюдения диеты и приема лекарственных средств в раннем возрасте. Значимая разница в IQ наблюдалась между рано и клинически выявленными пациентами. Хотя различия в языковых областях, посещении специальных школ и доступе к дополнительной поддержке в классе не были статистически значимыми между группами, в «клинически выявленной» группе затруднений было явно больше.
[0289] Хотя число исследованных здесь пациентов невелико, наблюдается заметная разница между детьми, диагноз которым был поставлен при рождении, и теми, диагноз которым был поставлен в момент начала хождения. Средний уровень tHcy, составляющий 115 мкмоль/л в клинически диагностированной группе, был связан с плохими клиническими последствиями и очень низким IQ.
[0290] Дополнительные доказательства пользы понижающей уровень Hcy лечения при психопатологии у пациентов с CBSDH получены из ретроспективного обзора данных в виде амбулаторных карт всех пациентов с HCU, поступивших в Бостонскую детскую больницу с 1963 г. (неопубликованные данные любезно предоставлены M. Almuqbil, et al.). Всего было выявлено 19 пациентов с HCU, трое из которых были исключены из анализа из-за возможно искажающего результаты наличия метилмалоновой ацидемии (также связанной с психологическими проблемами) в дополнение к CBSDH. Из оставшихся 16 пациентов 7 (6 с CBSDH и один с недостаточностью кобаламина (Cbl)) удовлетворительно соблюдали схему раннего лечения (четыре только на диете, двое на диете плюс бетаин и один на Cbl). Шесть из этих пациентов не имели явных психических симптомов, кроме легкого когнитивного расстройства. Напротив, 9 пациентов (7 с CBSDH, нечувствительной к пиридоксину, и двое с недостатком CblG) неудовлетворительно или не всегда соблюдали схему лечения (двое на бетаине и диете, один только на диете, трое на витаминах группы В и двое на фолиевой кислоте и бетаине). Все 7 пациентов с CBSDH и неудовлетворительным соблюдением схемы лечения имели психические проблемы, включающие депрессию (n=4), параноидальные состояния (n=2), паранойю и бредовый психоз (n=1), тревогу и дисрегуляцию настроения (n=1) и ADHD (синдром дефицита внимания и гиперактивности), которые уменьшались при хорошем контроле метаболизма (n=1). Два случая с недостатком CblG были заметно встревоженными или взволнованными. Возраст, пол и уровни способностей к познанию, по-видимому, не были значимо различны между психически больными и здоровыми индивидуумами. Эти результаты позволяют предположить, что хороший контроль метаболизма (снижение Hcy и/или Met) может отсрочить и, возможно, предотвратить появление психических и поведенческих расстройств у пациентов с CBSDH. Однако исследование не установило, приводит ли плохо контролируемая CBSDH к психопатологии, или же коморбидность с самой психопатологией препятствует результату в виде удовлетворительного соблюдения схемы лечения.
[0291] Связи между повышенными уровнями Hcy и связанными с ЦНС симптомами, включающие умственную отсталость, нейродегенеративные заболевания, судороги, дистонию, психоз, когнитивные расстройства, деменцию и депрессию, полностью подтверждены документами у индивидуумов с CBSDH и без нее (смотрите Morris et al. J Inherit Metab Dis 2017; 40:49-74; Abbott et al. Am J Med Genet 1987; 26:959-969; Mudd et al. Disorders of transsulfuration. In: Scriver CL, Beaudet AL, Sly WS, Valle D, eds. The Metabolic and Molecular Basis of Inherited Diseases. 7 ed. New York: McGraw Hill; 2001;1279-1327; Hidalgo et al. Eur Child Adolesc Psychiatry 2014; 23:235-238; Schimke et al. JAMA 1965; 193:711-719; Smith et al. PLoS One 2010;5: e12244; Seshadri et al. N Engl J Med 2002; 346:476-483; Bottiglieri et al. J Neurol Neurosurg Psychiatry 2000; 69:228-232; Bjelland et al. Arch Gen Psychiatry 2003; 60:618-626; Tolmunen et al. Am J Clin Nutr 2004; 80:1574-1578; Kaeser et al. J Neurol Neurosurg Psychiatry 1969; 32:88-93; Golimbet et al. Psychiatry Res 2009; 170:168-171; Clarke et al. Arch Neurol 1998; 55:1449-1455; Sinclair et al. Mov Disord 2006; 21:1780-1782; Permoda-Osip et al. Neuropsychobiology 2014; 69:107-111; Oliveira et al. BMJ Case Rep 2016;2016; Troen et al. Proc Natl Acad Sci USA 2008; 105:12474-12479; Sudduth et al. J Cereb Blood Flow Metab 2013; 33:708-715; Hainsworth et al. Biochim Biophys Acta 2016; 1862:1008-1017; Herrmann et al. Clin Chem Lab Med 2011; 49:435-441; Kim et al. J Nutr 2007; 137:2093-2097; Selhub et al. Am J Clin Nutr 2000; 71:614S-620S; McCaddon et al. Dement Geriatr Cogn Disord 2001; 12:309-313; Smallwood et al. Neuropathol Appl Neurobiol 2012; 38:337-343; Beydoun et al. BMC Public Health 2014; 14:643; Gortz et al. J Neurol Sci 2004; 218:109-114; Health Quality O. Vitamin B12 and cognitive function: an evidence-based analysis. Ont.Health Technol. Assess.Ser.13 (23), 1e45. 2013. Тип ссылки: Интернет-источник; Salagre et al. Eur Psychiatry 2017; 43:81-91, каждый из которых полностью включен таким образом посредством ссылки). Полагают, что механизмы, ведущие к расстройствам ЦНС у индивидуумов с повышенными уровнями Hcy, включают опосредованное tHcy повреждение нейронов (смотрите Mudd et al. Disorders of transsulfuration. In: Scriver CL, Beaudet AL, Sly WS, Valle D, eds. The Metabolic and Molecular Basis of Inherited Diseases. 7 ed. New York: McGraw Hill; 2001;1279-1327; Hainsworth et al. Biochim Biophys Acta 2016; 1862:1008-1017; Stefanello et al. Metab Brain Dis 2007; 22:172-182; Toborek et al. Atherosclerosis 1995; 115:217-224, каждый из которых полностью включен таким образом посредством ссылки), повреждение эндотелия сосудов, вызванное Hcy-опосредованным окислительным стрессом (смотрите Vivitsky et al. Am J Physiol Regul IntegrComp Physiol 2004;287: R39-R46, который полностью включен таким образом посредством ссылки), потерю нейронов (смотрите Yeganeh et al. J Mol Neurosci 2013; 50:551-557; Heider et al. J Neural Transm Suppl 2004; 1-13, оба из которых полностью включены таким образом посредством ссылки) и ослабление активности нейронной сети (смотрите Gortz et al. J Neurol Sci 2004; 218:109-114, который полностью включен таким образом посредством ссылки). Считается, что депрессия и судороги, по крайней мере частично, вызваны Hcy-опосредованными снижениями уровней аденозина в головном мозге с последующими снижениями уровней норадреналина и дофамина (смотрите Mech et al. J Clin Psychiatry 2016; 77:668-671; Domagala et al. Thromb Res 1997; 87:411-416; Vivitsky et al. Am J Physiol Regul IntegrComp Physiol 2004;287: R39-R46; Folstein et al. Am J Psychiatry 2007; 164:861-867; каждый из которых полностью включен таким образом посредством ссылки).
[0292] Многочисленные исследования, как на моделях CBSDH на животных (смотрите Lee et al. J Nutr 2005; 135:544-548; 135:544-548, который полностью включен таким образом посредством ссылки), так и на пациентах с CBSDH (смотрите El Bashir et al. JIMD Rep 2015; 21:89-95; Yap et al. J Inherit Metab Dis 2001; 24:437-447; Mech et al. J Clin Psychiatry 2016; 77:668-671; Grobe H. Eur J Pediatr 1980; 135:199-203, каждый из которых полностью включен таким образом посредством ссылки), показали, что ранние снижения уровней Hcy, индуцированные диетой с низким содержанием Met, добавками фолиевой кислоты/витамина группы B и/или терапией с использованием пиридоксина/бетаина, могут предотвратить, а иногда и обратить вспять, прогрессирование различных неврологических расстройств. Дополнительные доказательства представлены в ряде из 6 исследований конкретных случаев у пациентов с CBSDH, у которых значительное снижение, даже нормализация, уровней Hcy приводило к полной или частичной коррекции последствий для здоровья ЦНС (смотрите Yap et al. J Inherit Metab Dis 2001; 24:437-447; Brenton et al. J Child Neurol 2014; 29:88-92; Rezazadeh et al. Child Neurol Open 2014; 1:2329048X14545870; Kaeser et al. J Neurol Neurosurg Psychiatry 1969; 32:88-93; Colafrancesco et al. Eur J Pediatr 2015; 174:1263-1266; Yokoi et al. Pediatr Int 2008; 50:694-695; Li et al. Pathology 1999; 31:221-224, каждый из которых полностью включен таким образом посредством ссылки).
[0293] Эти данные демонстрируют сильную корреляцию между уровнями Hcy и повышенным риском расстройств ЦНС у пациентов с CBSDH и в общей популяции. Ранняя понижающая уровень Hcy терапия необходима для нормального развития детей с ранним началом CBSDH, а также для коррекции или ослабления расстройств ЦНС у пациентов с диагнозом CBSDH, поставленным в более позднем возрасте.
IX ОПРЕДЕЛЕНИЯ
[0294] Используемые в этом описании формы единственного числа «a», «an» и «the» включают ссылки во множественном числе, если контекст явно не диктует иное.
[0295] Если представлен диапазон значений, подразумевается, что каждое промежуточное значение между верхним и нижним пределом этого диапазона и любое другое указанное или промежуточное значение в указанном диапазоне включено в описание и конкретно раскрыто. Например, если указан диапазон от 1 мкм до 8 мкм, подразумевается, что также явно раскрыты 2 мкм, 3 мкм, 4 мкм, 5 мкм, 6 мкм и 7 мкм, а также ряд значений, больших или равных 1 мкм, и ряд значений, меньших или равных 8 мкм
[0296] Используемый здесь термин «совместно вводимые» или «совместное введение» означает введение двух или более терапевтических компонентов, включая фармацевтическую композицию.
[0297] Используемый здесь термин «готовая лекарственная формат» относится к лекарственной форме фармацевтической композиции, включающей лекарственное вещество в виде ПЭГилированного усеченного белка CBS человека с аминокислотной последовательностью SEQ ID NO: 1 (например, 20NHS PEG-CBS).
[0298] Используемый здесь термин «лекарственное вещество» относится к ПЭГилированному белку CBS с аминокислотной последовательностью SEQ ID NO:1 (например, 20NHS PEG-CBS).
[0299] Используемый здесь термин «негативное клиническое последствие» относится к нежелательному фенотипическому эффекту, возникающему вследствие заболевания, нарушения или состояния.
[0300] Используемый здесь термин «рекомбинантный», при его использовании в отношении, например, клетки, нуклеиновой кислоты, полипептида, экспрессионной кассеты или вектора, относится к материалу или материалу, соответствующему природной или нативной форме материала, который был модифицирован путем введения нового фрагмента или изменения существующего фрагмента, или идентичному ему, но образованному или полученному из синтетических материалов. Например, рекомбинантные клетки экспрессируют гены, которые не обнаруживаются в природной (нерекомбинантной) форме клетки, (т.е. «экзогенные нуклеиновые кислоты») или экспрессируют природные гены, которые в других обстоятельствах экспрессируются на другом уровне, как правило, недостаточно экспрессируются или вообще не экспрессируются.
[0301] Рекомбинантные методы могут включать, например, использование рекомбинантной нуклеиновой кислоты, такой как кДНК, кодирующая белок или антисмысловую последовательность, для встраивания в экспрессионную систему, такую как экспрессионный вектор; полученную конструкцию вводят в клетку, и клетка экспрессирует нуклеиновую кислоту и белок, в соответствующем случае. Рекомбинантные методы также включают лигирование нуклеиновых кислот с кодирующими или промоторными последовательностями из разных источников в одну экспрессионную кассету или вектор для экспрессии слитого белка, конститутивной экспрессии белка или индуцируемой экспрессии белка.
[0302] Используемые здесь термины «субъект», «индивидуум» или «пациент» используются здесь взаимозаменяемо и относятся к позвоночному, предпочтительно к млекопитающему. Млекопитающие включают людей, но без ограничения этим.
[0303] Используемый здесь термин «связанный (ассоциированный)» относится к совпадению с развитием или проявлением заболевания, состояния или фенотипа. Связь (ассоциация) может быть обусловлена, но без ограничения этим, генами, ответственными за функции «домашнего хозяйства», изменение которых может обеспечить основу для ряда заболеваний и состояний, тех, которые являются частью пути, вовлеченного в конкретное заболевание, состояние или фенотип, и тех, которые косвенно способствуют проявлению заболевания, состояния или фенотипа.
[0304] Используемый здесь термин «фармацевтически приемлемый наполнитель» или «фармацевтически приемлемый носитель» относится к наполнителю, который необязательно может быть включен в композиции по настоящему изобретению и который не вызывает значительных неблагоприятных токсикологических эффектов у пациента. В частности, в данном случае это относится к наполнителю, который можно вводить в организм являющегося млекопитающим субъекта в сочетании с активным соединением (здесь ПЭГилированной htCBS или «20NHS PEG-CBS») без значительных неблагоприятных токсикологических эффектов для субъекта.
[0305] Используемые здесь термины «адъювант», «разбавитель» или «носитель» означают любое вещество, само не являющееся терапевтическим средством, используемое в качестве носителя для доставки терапевтического средства и подходящее для введения субъекту, например млекопитающему, или добавляемое в фармацевтическую композицию для улучшения ее свойств при обращении или хранении, или для обеспечения или облегчения формирования стандартной дозы композиции в отдельное изделие, такое как капсула или таблетка, подходящее для перорального введения. Термины «адъювант», «разбавитель» или «носитель» охватывают «наполнители», в том числе «фармацевтически приемлемые наполнители», «носители», «растворители» и т.п., как эти термины здесь используются. Наполнители и носители включают любые такие материалы, известные в данной области техники, например, любую жидкость, гель, растворитель, жидкий разбавитель, солюбилизатор и т.п., которые нетоксичны и не взаимодействуют с другими компонентами композиции вредным образом. Введение может означать пероральное введение, ингаляцию, энтеральное введение, кормление или инокуляцию с помощью внутривенной инъекции. Наполнители могут включать стандартные фармацевтические наполнители, а также могут включать любые компоненты, которые можно использовать для приготовления пищевых продуктов и напитков для потребления людьми и/или животными, кормовых смесей или приманок или других пищевых продуктов.
[0306] Используемый здесь термин «лекарственное средство» или «фармакологически активный агент», или любой другой аналогичный термин означает любой химический или биологический материал или соединение, в том числе пептиды, подходящий для введения способами, ранее известными в данной области техники, и/или способами, описанными в настоящем изобретении, который вызывает желаемый биологический или фармакологический эффект, который может включать, но без ограничения этим, (1) профилактический эффект на организм и предотвращение нежелательного биологического эффекта, например предотвращение инфекции, (2) облегчение состояния, вызванного заболеванием, например, облегчение боли или воспаления, вызванного(ой) заболеванием, и/или (3) облегчение, уменьшение или полное устранение заболевания из организма. Эффект может быть местным, например, обеспечение местного обезболивающего эффекта, или он может быть системным. Это описание не относится к новым проникающим веществам или к новым классам активных агентов. Скорее, оно ограничивается способом доставки агентов или проникающих веществ, которые существуют в уровне техники или которые могут быть позже установлены в качестве активных агентов и которые подходят для доставки в соответствии с настоящим изобретением.
[0307] Используемый здесь термин «приблизительно», в частности, в отношении данного количества, предназначен для охвата отклонений плюс или минус пять процентов.
[0308] Используемые здесь термины «фармакологически эффективное количество» или «терапевтически эффективное количество» в отношении композиции по настоящему изобретению относятся к нетоксичному, но достаточному количеству активного агента (или композиции, содержащей активный агент) для обеспечения желательного уровня в кровотоке или в месте действия (например, внутриклеточно) у субъекта, подлежащего лечению, и/или для обеспечения желаемого физиологического, биофизического, биохимического, фармакологического или терапевтического ответа, такого как уменьшение интенсивности проявлений гомоцистинурии. Требуемое точное количество будет варьироваться от субъекта к субъекту и будет зависеть от многочисленных факторов, таких как активный агент, активность композиции, используемое устройство для доставки, физические характеристики композиции, предполагаемое применение пациентом (т.е. число доз, вводимых в день), а также касающихся пациента соображений, таких как вид, возраст и общее состояние здоровья субъекта, тяжесть состояния, подлежащего лечению, дополнительные лекарственные средства, принимаемые субъектом, способ введения и т.п. Эти факторы и соображения могут быть без труда определены специалистом в данной области техники на основании представленной здесь информации. Соответствующее «эффективное» количество в любом отдельном случае может быть определено специалистом со средним уровнем компетентности в данной области техники, используя рутинное экспериментирование, на основании представленной здесь информации.
[0309] Используемый здесь термин «нуклеиновая кислота» может быть в форме РНК или в форме ДНК и включать информационную РНК, синтетические РНК и ДНК, кДНК и геномную ДНК. ДНК может быть двухцепочечной или одноцепочечной, и, если она является одноцепочечной, может быть кодирующей цепью или некодирующей (антисмысловой, комплементарной) цепью.
[0310] Используемый здесь термин «мутант» представляет собой мутантный белок, разработанный или сконструированный для изменения свойств или функций, связанных с гликозилированием, стабилизацией белка и/или связыванием лиганда.
[0311] Используемые здесь термины «природный (нативный)» или «дикий тип» по отношению к данной клетке, полипептиду, нуклеиновой кислоте, признаку или фенотипу относятся к форме, в которой они обычно встречаются в природе.
[0312] Используемые здесь термины «белок», «полипептид», «олигопептид» и «пептид» имеют свое обычное значение и используются взаимозаменяемо для обозначения полимера, состоящего из по крайней мере двух аминокислот, ковалентно связанных амидной связью, независимо от длины или посттрансляционной модификации (например, гликозилирования, фосфорилирования, липидирования, миристилирования, убиквитинирования и т.д.). Кроме того, описанные здесь полипептиды не ограничиваются определенной длиной. В это определение включены D- и L-аминокислоты и смеси D- и L-аминокислот. Этот термин также не относится к модификациям полипептида после его экспрессии, например, гликозилированию, ацетилированию, фосфорилированию и т.п., а также к другим модификациям, известным в данной области техники, как встречающимся в природе, так и не встречающимся в природе, или не исключает их. Полипептид может быть целым белком или его подпоследовательностью. Полипептиды также могут относиться к аминокислотным подпоследовательностям, включающим эпитопы, т.е. антигенные детерминанты, в значительной степени ответственные за иммуногенные свойства полипептида и способные вызывать иммунный ответ.
[0313] Используемый здесь термин «положение, соответствующее» и т.п. относится к представляющему интерес положению (т.е. номеру основания или остатка) в молекуле нуклеиновой кислоты или белке относительно положения в другой эталонной молекуле нуклеиновой кислоты или белке. Соответствующие положения можно определить путем сравнения и совмещения последовательностей для максимизации числа совпадающих нуклеотидов или остатков, например, таким образом, чтобы идентичность между последовательностями составляла более 90%, более 95%, более 96%, более 97%, более 98% или более 99%. Затем представляющему интерес положению присваивается номер, присвоенный в эталонной молекуле нуклеиновой кислоты. Например, если конкретный полиморфизм в гене-X встречается в нуклеотиде 2073 SEQ ID NO:X, для идентификации соответствующего нуклеотида в другой аллели или изоляте, последовательности совмещают, а затем идентифицируют положение, которое совмещается с 2073. Поскольку различные аллели могут иметь разную длину, положение, обозначающее 2073, может быть не нуклеотидом 2073, а вместо этого находиться в положении, которое «соответствует» этому положению в эталонной последовательности.
[0314] Используемый здесь термин «длительное введение» относится к введению фермента CBS, htCBS или мутанта htCBS (например, с мутацией C15S), конъюгированного с фрагментом ПЭГ, в течение периода времени, составляющего 6 недель или дольше.
[0315] Используемый здесь термин «непрерывное введение» относится к повторяющемуся введению фермента CBS, htCBS или мутанта htCBS (например, с мутацией C15S), конъюгированного с фрагментом ПЭГ, в ходе исследования посредством подкожной инъекции или имплантированного осмотического насоса.
[0316] Здесь описаны способы лечения гомоцистинурии с помощью ферментотерапии (ET) с использование описанной здесь готовой лекарственной формы, включающей ПЭГилированный усеченный белок CBS человека с мутацией, приводящей к замене цистеина в положении 15 аминокислоты на серин.
[0317] Подробности одного или более вариантов осуществления настоящего изобретения изложены в сопроводительном описании ниже. Хотя любые материалы и способы, подобные или эквивалентные тем, что здесь описаны, могут быть использованы на практике или при тестировании настоящего изобретения, теперь будут описаны предпочтительные материалы и способы. Другие признаки, цели и преимущества настоящего изобретения будут очевидны из описания. В описании формы единственного числа также включают множественное число, если контекст явно не диктует иное. Кроме особо оговоренных случаев, все технические и научные термины, используемые здесь, имеют то же значение, в котором они обычно понимаются специалистом со средним уровнем компетентности в области техники, к которой относится это изобретение. В случае конфликта настоящее описание имеет преимущественную силу.
[0318] Настоящее изобретение дополнительно проиллюстрировано следующими неограничивающими примерами.
ПРИМЕРЫ
Пример 1. Экспериментальные протоколы
A. Ферментация
[0319] Экспрессионный вектор, содержащий последовательность, кодирующую усеченную CBS человека, трансформировали в бактерии E.coli Bl-21 (DE3), и бактерии из устойчивых к канамицину клонов выращивали в 5 мл среды Луриа-Бертани (LB) с 30 мкг/мл канамицина в течение ночи при 37°C на ротационном шейкере со скоростью 275 об./мин. Один мл ночной культуры добавляли к 100 мл среды Terrific Broth (TB) с 30 мкг/мл канамицина и выращивали в течение ночи. Затем 10 мл прекультуры добавляли к 1 л среды TB, содержащей 0,001% тиамина-HCl, pH 8,0, 0,0025% пиридоксина-HCl, pH 8,0, 0,3 мМ δ-ALA, pH 8,0, 150 мкМ хлорида железа, 30 мкг/мл канамицина. Затем культуру выращивали при 30°C на ротационном шейкере со скоростью 275 об./мин до тех пор, пока ОП600 не достигала значения, составляющего приблизительно 0,6-0,7, и экспрессию белка индуцировали добавлением 1 мМ IPTG. Ферментацию продолжали еще 16 часов. Клетки собирали центрифугированием при относительной центробежной силе (ref), равной 6000, в течение 10 минут при 4°C, промывали охлажденным на льду 0,9% NaCl, повторно центрифугировали, как описано выше, и замораживали при -80°C. Затем добавляли буфер для лизиса (20 мМ NaH2PO4, pH 7,2, 40 мМ NaCl, 0,1 мМ PLP) к клеточному осадку, и последний гомогенизировали в гомогенизаторе Даунса и обрабатывали лизоцимом (конечная концентрация=2 мг/мл), инкубировали в течение 1 часа при 4°C на качающейся платформе, обрабатывали ультразвуком для снижения вязкости и центрифугировали при ref=53000. Затем супернатант, содержащий растворимую фракцию, хранили при -80°C.
[0320] Планы по оптимизации и масштабированию были разработаны для установления процесса ферментации для экспрессии CBS на высоком уровне, количеств и профилей добавления к средам добавок, таких как 5-аминолевулиновая кислота (ALA), тиамин (витамин B1), пиридоксина HC1 и/или хлорид железа, С-источника и их начальных условий и условий подачи, температуры, рН, а также условий индукции (концентрации индуктора и продолжительности периода индукции).
[0321] Наивысшая плотность клеток и наилучшие уровни экспрессии были достигнуты при использовании минимальной солевой среды (С-источник: глицерин), дополненной в общей сложности 0,05 г/л B6 и 0,5 г/л ALA в течение периода индукции 24 часа при 30°С.
[0322] В конце ферментации (EOF) была достигнута плотность клеток при 600 нм (OD600), составляющая приблизительно 110±10, что соответствовало сырому весу, составляющему приблизительно 90±10 г/л. Титр CBS в процессе ферментации составлял приблизительно 2,5-3,0 г CBS/л, как определено с помощью радиоактивного и колориметрического анализов активности.
B. Очистка
[0323] Целевое извлечение по показателю общей ферментативной активности очищенного фермента из клеточного лизата составляло 30% при условии, что потребуются по крайней мере три стадии хроматографии. Разработанный процесс оценивали в масштабе колонки для захвата объемом 60 мл.
1. Стадия захвата
[0324] Анионообменную хроматографию (AEX) использовали в качестве первой стадии захвата при получении рекомбинантного CBS. Затем элюат доочищали для дальнейшей очистки путем захвата на смоле DEAE-Sepharose при рН, близком к нейтральному, с последующим линейным градиентом KH2PO4. DEAE-Sepharose является слабым обменником, что означает, что заряд системы зависел от рН окружающей среды. Таким образом, pH тесно связан с динамической связывающей способностью (DBC) смолы. Снижение pH при связывании до 6,4 не снижало эффективность стадии захвата. Время загрузки составляло приблизительно 30 минут, если для разведения клеточной пасты использовали 5 объемов буфера для растворения - разрушения.
[0325] Промывку выполняли для объема 10 колонок с загрузочной способностью, близкой к определенному максимуму=7 г/л CBS (что эквивалентно DBC, составляющей приблизительно 35 г общего белка на л смолы). Элюирование проводили в условиях проводимости для элюирования - 16 мСм/см в присутствии 120 мМ NaCl.
[0326] Было обнаружено, что извлечение составляет приблизительно 90%, если клеточный экстракт загружали в течение узкого промежутка времени. В зависимости от титра CBS в клеточном экстракте в результате этой стадии захвата был достигнут коэффициент очистки, составляющий приблизительно 3,5.
2. Аффинная хроматография с иммобилизованным металлом (IMAC)
[0327] При IMAC, также называемой аффинной хроматографией с иммобилизованным металлом Co2+, с ионами цинка (Zn), используется селективность связывания для ортогонального разделения CBS и белка клетки-хозяина (HCP). Наблюдали коэффициент очистки, составляющий приблизительно 2,5.
[0328] Стадия элюирования включала 11 мМ имидазол в сочетании с обессоливанием фракции CBS. Концентрация хлорида натрия снижалась с 400 мМ (при загрузке/промывке) до 50 мМ в буфере для элюирования. В ходе мелкомасштабной проверки смогли установить, что проводимость оказывает большое влияние на сам характер элюирования. Например, CBS можно было элюировать только чистой водой, без имидазола. Стабильность CBS повышали за счет увеличения количества хлорида натрия в буфере для элюирования. При равной 150 мМ концентрации хлорида натрия характер элюирования лишь слегка изменялся.
[0329] Используя HEPES в качестве буферной системы, можно было измерить DBC, составляющую 12-15 г/л. Кроме того, стабильность образца увеличилась не только в отношении осаждения, но и уменьшилась деградация. При добавлении DEAE деградация была остановлена при использовании буфера HEPES, в отличие от используемой в настоящее время фосфатной буферной системы. При увеличении масштаба DEAE и сульфат аммония добавлялись сразу после завершения элюирования, что должно препятствовать деградации. Кроме того, последующую доочистку проводили как можно быстрее, чтобы время инкубации в этом состоянии было коротким. Элюирующий при IMAC пул загружали в колонку для хроматографии на основе гидрофобных взаимодействий (HIC) в течение 3 часов для доочистки.
3. Стадия доочистки
[0330] Разделение на заключительной хроматографической стадии очистки CBS было основано на гидрофобном взаимодействии. Основная колонка отделяла представляющий интерес CBS от большей части HCP за счет различий в условиях элюирования. Большая часть HCP сильнее связывается с HIC, чем CBS, что указывает на то, что CBS является менее гидрофобным, чем большинство остальных HCP.
[0331] По сравнению с IMAC, HIC характеризуется низким разделением по связыванию (менее 10%). Более 90% остающихся примесей HCP было отделено от HIC на стадии элюирования. Извлечение CBS из HIC составляло приблизительно 95%. DBC составляла от приблизительно 16 г/л до приблизительно 18 г/л. Эффективность этой стадии доочистки была достаточно большой. pH для стадии элюирования был между 6 и 8. Буферная система (фосфатная или 20 мМ HEPES) не оказывала заметного влияния.
[0332] Коэффициент очистки на этой стадии доочистки составлял приблизительно 1,1 из-за низкого содержания остаточных HPC внутри загрузки, что было типичным для конечной стадии хроматографии. Степень чистоты конечной CBS между всеми выполненными последующими производственными процессами была одинаково высокой, что указывает на то, что эта стадия доочистки компенсировала различные степени примесей внутри загрузки.
[0333] Можно выполнить адаптацию, чтобы адаптировать стадии процесса к существующему оборудованию и позволить позже увеличить объем ферментации до 100 л для производства. Для обеспечения надежного качества продукта EDTA (например, 10 мМ) может добавляться на нескольких стадиях процесса для предотвращения деградации продукта, вызванной металлопротеазами.
C. ПЭГилирование
[0334] Реакция ПЭГилирования вела себя как реакция второго порядка с ингибированием, индуцированным продуктом. Поскольку гидролиз в NHS-PEG не может быть причиной ингибирования реакции, а конечная картина ПЭГилирования достигалась через 4 часа ПЭГилирования, наблюдали, что оставшийся (приблизительно 50%) NHS-PEG все еще остается активным. Интересно, что добавление дополнительного количества NHS-PEG в реакционную смесь увеличивало степень ПЭГилирования. Концентрация CBS в реакционной смеси составляла 8 г/л для получения желаемой картины ПЭГилирования без увеличения отношения NHS-PEG к CBS в отсутствие DMSO.
D. Данные и статистический анализ
[0335] В таблице 4 представлены подробные сведения о программном обеспечении, аналитических инструментах и алгоритмах, используемых для анализа данных в приведенных здесь примерах.
[0336] Все хроматограммы были просмотрены аналитиком, чтобы убедиться, что форма хроматографического пика и интеграция пиков являются удовлетворительными. Данные, переданные вручную, были перепроверены на фоне исходных данных, которые являются частью необработанных данных исследования. Критерии приемлемости цикла были установлены до анализа на основе результатов калибровочных стандартов, контроля качества и контроля качества холостого опыта. Данные представлены как среднее значение±стандартная ошибка среднего (SEM).
[0337] Статистический анализ был проведен с использованием дисперсионного анализа (ANOVA), а затем критерия множественных сравнений Тьюки для определения значимости.
E. Анализ активности CBS, основанный на превращении радиоактивно меченного Ser.
[0338] CBS катализирует реакцию β-замещения, в которой серин (Ser) конденсируется с Hcy зависимым от пиридоксаль-5'-фосфата (PLP) образом с образованием Cth. Активность фермента CBS определяли с помощью радиоизотопного анализа с использованием 14C-меченого Ser в качестве субстрата.
[0339] 14L-Ser+L-Hcy → 14C-L-Cth+H2O.
[0340] Аликвоту объемом 7 мкл (всего 420 нг) чистой 20NHS PEG-CBS в буфере для разведения (0,1 М Tris-HCl при pH 8,6, содержащем 1 мМ DTT, 10 мкМ PLP и 0,5 мг/мл бычьего сывороточного альбумина (BSA)) или 7 мкл плазмы (разведение не требуется для образцов D25 и D27) добавляли к 88 мкл реакционной смеси (0,1 М Tris-HCl при pH 8,6, содержащей 10 мМ L-Ser, 0,5 мМ PLP, 0,5 мг/мл BSA и 0,3 мкКи L-[14C(U)]-Ser). Образцы уравновешивали до 37°С путем инкубации в водяной бане в течение 5 мин. Реакцию инициировали с использованием 5 мкл 0,2 М Hcy (конечная концентрация 10 мМ) и инкубировали еще 30 мин при 37°С.
[0341] Начало анализа и отбор образцов полученной смеси сдвигали так, чтобы время каждой реакции составляло точно 30 минут. Для отделения радиоактивного продукта (Cth) от меченого субстрата (Ser) использовали нисходящую бумажную хроматографию. Чтобы остановить реакцию, смесь для анализа охлаждали в ледяной бане, и аликвоту объемом 20 мкл пипеткой наносили на бумагу для хроматографии CHR степени 3 (Whatman, GE Healthcare, Pittsburgh, PA, США) для разделения. 14C-Cth, образовавшийся в ходе реакции, отделяли от 14C-Ser с помощью элюирования в течение ночи смесью 2-пропанол:муравьиная кислота:H2O (75:5,7:18,9 по объему). Стандарт, содержащий смесь Cth и Ser, помещали вместе с образцами на каждую сторону хроматографической бумаги. Хроматографическую бумагу сушили, и стандартные дорожки окрашивали кислым раствором нингидрина. Участки каждой дорожки с образцом, содержащие меченый Cth, вырезали, погружали в 5 мл сцинтилляционного коктейля Opti-flour (PerkinElmer, North Billerica, MA, США) и подсчитывали в сцинтилляционном счетчике Beckman LS-3801. Образец без фермента использовали в качестве холостой пробы для контроля фоновой радиоактивности, которая вычиталась из подсчета в каждом образце. Для чистого фермента в качестве контроля, значения удельной активности CBS представляли в единицах фермента (количестве фермента, которое 1 мкмоль Cth/ч) на мг CBS (т.е. Ед./мг белка). Для образцов плазмы значения активности представляли в миллиединицах (количестве фермента, которое образует 1 нмоль Cth/ч) на мкл плазмы (т.е. мЕд./мл плазмы).
[0342] Эти маточные растворы с номинальным значением=25 мг/мл (24,8-26,7 мг/мл в забуференном фосфатом солевом растворе, рН 7,4 (PBS)) хранили в виде аликвот при -80°С. В каждый день обработки готовили одноразовые свежие растворы фермента путем разведения маточных растворов в PBS до конечных концентраций, равных 1 мг/мл, и вводили мышам в дозе, составляющей 7,5 мг/кг. Объемы, инъецируемые для введения целевой дозы, рассчитывали на основе веса в указанные дни. Любой раствор, оставшийся после завершения инъекций в этот день, выбрасывали.
F. Вестерн-блоттинг
[0343] Готовую лекарственную форму инъецировали четырем мышам I278T-/-, и кровь собирали через 24 часа после первой инъекции и через 72 часа после последней инъекции, чтобы использовать их в качестве контроля. Образцы плазмы D25 и D27 от всех групп в примере 5 анализировали с помощью Вестерн-блоттинга для выявления возможного деПЭГилирования in vivo. Образцы плазмы (4 мкл на дорожку) наносили на градиентные (4%-20%) гели MiniProtean TGX (Bio-Rad, Hercules, CA, США), и белки разделяли с помощью электрофореза в денатурирующих, восстанавливающих условиях. Маркеры молекулярной массы (Precision Plus Protein Dual Color Standard, Bio-Rad) и аликвоты каждого препарата (150-500 нг на дорожку) обрабатывали аналогичным образом и подвергали электрофорезу вместе с образцами плазмы. После электрофоретического разделения полосы белков переносили на мембраны из PVDF (BioRad). Отдельные мембраны блокировали в течение ночи при 4°C в растворе для блокирования (5% обезжиренном молоке в PBS с 0,02% Tween 20). Затем мембраны промывали и инкубировали с кроличьим поликлональным антителом против hCBS (Orphan Technologies UCD Kraus lab серия # R2B2, антисывороткой, разведенной в растворе для блокирования в 5000 раз) в течение 1 часа. Затем мембраны промывали и инкубировали с антителами против кроличьего IgG, конъюгированными с пероксидазой хрена (HRP) (Jackson Laboratories, Bat Harbor, ME, США, 5000-кратно разведенными раствором для блокирования) в течение 30 минут. После промывки мембран полосы визуализировали путем инкубации с хемилюминесцентным субстратом (SuperSignal West Pico, ThermoFisher Scientific, Waltham, MA, США) в течение 5 минут с последующим захватом сигнала на прозрачной синей рентгеновской пленке (CL-Xposure Film, ThermoFisher Scientific). Проявленные пленки сканировали с помощью планшетного сканера (Perfection V550 Photo Color Scanner, Epson, Long Beach, CA, США).
G. Химикаты
[0344] Если не указано иное, все материалы были приобретены у Sigma или Fisher Scientific. L-[U-14C]-серин был получен от Perkin Elmer Life Sciences.
H. Сбор и анализ плазмы
[0345] Для сбора крови в пробирки BD Microtainer PST с гепарином лития (Becton, Dickinson and Company, NJ, США) использовали одноразовый ланцет для сбора крови из поднижнечелюстной вены. Затем пробирки центрифугировали при 10000хg в течение 5 мин с последующим переносом плазмы в пробирки на 1,5 мл и хранением при -80°C. Метаболиты серосодержащей аминокислоты в плазме определяли с помощью жидкостной хроматографии с разведением стабильных изотопов и тандемной масс-спектрометрией (LC-MS/MS), как описано в другом месте.
I. Исследования на животных
[0346] Исследования проводили с использованием линии мышей с нокаутом CBS, экспрессирующих мутантный трансген I278T CBS человека (мышей I278T CBS -/- (I278T -/-)). Родительская пара гетерозиготных трансгенных мышей I278T на фоне C57BL6 была предоставлена Dr. Warren Kruger (Fox Chase Cancer Center, Philadelphia, PA, США). У мышей нокдаун мышиного гена CBS, и они также экспрессируют человеческий CBS I278T под контролем промотора гена металлотионеина (смотрите Wang, et al. (2005) Hum Mol Genet 14, 2201-2208, который полностью включен таким образом посредством ссылки). Мутантный фермент обладает приблизительно 2-3% активности CBS WT, так что экспрессия трансгена спасает от неонатальной смертности, обычно наблюдаемой у гомозиготных по нокауту CBS мышей (смотрите Watanabe et al. (1995) Proceedings of the National Academy of Sciences USA 92, 1585-1589; Maclean et al. (2010) Molecular Genetics and Metabolism 101, 163-171; каждый из которых полностью включен таким образом посредством ссылки). Если не указано иное, животных содержали на стандартном облученном прессованном корме для грызунов (Teklad 2920X, Envigo, Indianapolis, IN, США).
[0347] Для получения CBS-гомозиготных трансгенных животных для исследования, гомозиготных или гетерозиготных самцов скрещивали с гетерозиготными самками для получения пометов, содержащих CBS-гомозиготных (-/-) детенышей, помимо других генотипов, все из которых экспрессируют трансген I278T. Родительским парам и новорожденным мышам давали цинк (25 мМ сульфат цинка в питьевой воде) для индукции экспрессии трансгена. Гомозиготная линия (I278T-/-) с фенотипом гомоцистинурии (HCU) служит в качестве модели для CBSDH, тогда как другие полученные генотипы в данном исследовании не использовались (смотрите Wang, et al. (2005) Hum Mol Genet 14, 2201-2208, который полностью включен таким образом посредством ссылки).
[0348] Все процедуры с животными, использованные в этом исследовании, были рассмотрены и одобрены University of Colorado-Denver IACUC, который придерживается всех федеральных, государственных и местных законов, правил и политик. University of Colorado-Denver является учреждением, аккредитованным AAALAC (№ 00235), застрахованным Службой общественного здравоохранения (№ A 3269-01) и лицензированным Министерством сельского хозяйства США (№ 84-R-0059). Процедуры с участием мышей проводились в соответствии с одобренным IACUC протоколом № -49414(03)1E.
[0349] Мышей размножали и генотипировали в учреждении, в котором работают авторы настоящего изобретения, как описано ранее в Wang, et al. (2005) Hum Mol Genet 14, 2201-2208, который полностью включен таким образом посредством ссылки. Родительские пары содержались на прессованной стандартной пище 2920X (Envigo, CA, США) и воде, содержащей 25 мМ ZnCl2, для индукции экспрессии трансгена и, таким образом, спасения I278T-гомозиготных детенышей от неонатальной гибели. После отнятия от груди в возрасте 21 дня I278T-гомозиготных мышей и их родных братьев и сестер дикого типа распределяли в одну из восьми групп. В возрасте 24 дней мышей переводили на рацион с определенным аминокислотным составом либо с нормальным (Envigo TD.170063, 4% Met; группы A, B, C и D), либо с ограниченным содержанием метионина (Envigo TD.l 10591, 0,5% Met; группы E, F, G и H). В дополнение к новому рациону в день 24 мышам также вводили подкожно носитель PBS (группам A, C, E и G) или 10 мг/кг 20NHS PEG-CBS (группам B, D, F и H) 3 раза в неделю (понедельник, среду, пятницу) до возраста 22 недели. Мышей еженедельно взвешивали с использованием веса для расчета объемов инъекций 20NHS PEG-CBS в течение недели.
J. Хранение и препараты фермента
[0350] 20NHS PEG-CBS в жидком препарате использовали для исследования стабильности, проведенного в соответствии с cGMP, как здесь описано, и из этого исследования были получены следующие образцы: контрольный фермент или «контрольный препарат» (T0-80C), которые хранили при температуре ниже -65°C, и образцы ферментов, подвергнутые инкубации в условиях ускоренного исследования стабильности при 25°C в течение 2 дней (T2D-25C), 1 месяца (T1M-25C) и 6 месяцев (T6M-25C).
Пример 2. Определение снижения уровня ПЭГилирования в препаратах в виде готовой лекарственной формы
[0351] Препараты в виде готовой лекарственной формы с различной степенью деПЭГилирования были созданы для ускоренного исследования стабильности, проводимого в условиях «надлежащей производственной практики» (GMP) для готовой лекарственной формы, путем инкубации готовой лекарственной формы при 25°C в течение двух дней, одного месяца или шести месяцев. Контрольный образец хранили в рекомендуемом диапазоне температур, т.е. ниже -65°С.
[0352] Различия в ПЭГилировании между препаратами подтверждали с помощью высокоэффективной жидкостной хроматографии с обращенной фазой (RP-HPLC). Выделено десять высокоПЭГилированных и менее ПЭГилированных форм, а также CBS без ПЭГилирования и кофактора в виде гема (P10), высвобождающегося при денатурации фермента. Степень деПЭГилирования в каждом образце определяли путем сравнения относительных площадей пиков, соответствующих различно ПЭГилированным или полностью деПЭГилированным формам. Результаты RP-HPLC представлены в таблице 5. «CBS» представляет собой нативный (немодифицированный) фермент, а остальные пики - препараты с разной степенью ПЭГилирования.
[0353] Анализ с помощью RP-HPLC показал, что по сравнению с контрольным образцом в препаратах, подвергнутых инкубации течение 1 месяца и, даже больше, в течение 6 месяцев при 25°C наблюдалось значительное де-ПЭГилирование. Как показано в таблице 5, эти образцы продемонстрировали более высокую долю пиков, соответствующих менее ПЭГилированным формам (например, P3), и, соответственно, меньшее количество пиков для более ПЭГилированных форм (например, P6 и P7). Кроме того, пик, соответствующий немодифицированной (или полностью деПЭГилированной) CBS, был наиболее заметен в препарате, подвергнутом инкубации в течение шести месяцев. Однако в препарате, подвергнутом инкубации при 25°C в течение 2 дней, распределение различно ПЭГилированных форм было более схожим с таковым для контрольного фермента, который всегда хранился при температуре, которая ниже или равна -65°C.
Пример 3. Эффективность препаратов со сниженными уровнями ПЭГилирования у мышей
[0354] Для оценки биологической эквивалентности готовой лекарственной формы и ее деПЭГилированных препаратов эффективность анализировали на мышах I278T CBS-/- (I278T-/-), модели, повторяющей биохимические последствия CBSDH, т.е. отклонения уровней метаболитов метионина (Met) в плазме, в том числе повышенный уровень гомоцистеина (Hcy) и пониженный уровень цистеина (Cys). Аминотиолы (общие Cys и Hcy) в плазме и остальные аминокислоты, а также SAM и SAH измеряли с помощью LC-MS/MS (ЖХ-МС/МС), как описано в Arning et al. (2016) Methods Mol Biol 1378, 255-262, который полностью включен таким образом посредством ссылки.
[0355] Мыши I278T CBS-/- (I278T-/-) лишены мышиного гена CBS и экспрессируют мутантный I278T ген CBS человека, несущий наиболее часто встречающуюся патогенную мутацию у пациентов с CBSDH. Эти мыши проявляют приблизительно 2%-3% активности CBS дикого типа и имеют фенотип гомоцистинурии (HCU) (смотрите Wang, et al. (2005) Hum Mol Genet 14, 2201-2208, который полностью включен таким образом посредством ссылки). Он включает повышения уровней Hcy, Met и S-аденозилгомоцистеина (SAH) как в плазме, так и в тканях и сопутствующее снижение уровней Cth и Cys в плазме. Эта линия мышей была первоначально получена от профессора Warren D. Kruger в Fox Chase Cancer Center (Philadelphia, PA, США).
[0356] Для проверки эффективности использовали как самцов, так и самок взрослых мышей I278T-/-, которых содержали на стандартном (REG) рационе. В начале исследования мышей делили на четыре группы, соответствующие четырем препаратам. Кровь собирали для измерений на исходном уровне за по крайней мере одну неделю до введения дозы. Кровь собирали из поднижнечелюстной вены находящихся в сознании исследуемых животных с помощью одноразового ланцета, предназначенного для отбора образцов из поднижнечелюстной вены, в пробирки для приготовления плазмы с гепарином лития и гелем (Greiner Bio-One, Monroe, NC, США или их эквивалентом от других поставщиков). Плазму собирали из образцов крови после центрифугирования при 1200xg в течение 10 мин и хранили при -80°C в пробирках объемом 1,5 мл до проведения анализа.
[0357] Начиная с дня 1 (D1), мыши получали три подкожных (SC) инъекции, каждая по 7,5 мг/кг, в неделю (в понедельник, среду и пятницу) соответствующего препарата, соответствующего их экспериментальной группе.
[0358] Лечение продолжалось в течение 24 дней. Днями инъекции препаратов были D1, D3, D5, D8, D10, D12, D15, D17, D19, D22 и D24. Кровь собирали по крайней мере один раз в неделю, через 24 часа после инъекции, а также через 72 часа после последней инъекции. В дополнение к сбору на исходном уровне (D0) образцы крови отбирали в D2, D11, D18, D25 и D27. Плазму готовили из всех образцов крови сразу после сбора и хранили в виде замороженных аликвот до проведения анализа. Аликвоту каждого образца анализировали на метаболиты Met, тогда как аликвоты некоторых (D25 и D27) образцов также анализировали на активность CBS, как описано в примере 4. Анализировали метаболиты Met: Hcy, Cth, Cys, Met, Bet, диметилглицин (DMG), глицин (Gly), серин (Ser), S-аденозилметионин (SAM) и S-аденозилгомоцистеин (SAH). Если не указано иное, результаты для обоих полов объединяли.
[0359] Препараты сравнивали на основании их способности повышать при подкожной инъекции уровни анализируемых метаболитов Met в плазме. Кроме того, на тех же мышах исследовали деПЭГилирование препаратов in vivo.
[0360] В дополнение к отбору образцов крови на исходном уровне (D0) его выполняли в D2, D11, D18, D25 и D27. Плазму готовили из всех образцов крови сразу после сбора и хранили в виде аликвот в замороженном виде до проведения анализа. Аликвоту каждого образца анализировали на метаболиты Met, тогда как аликвоты некоторых (D25 и D27) образцов также анализировали на активность CBS. Отобранные аликвоты (D2 и D27) также анализировали с помощью Вестерн-блоттинга для оценки деПЭГилирования 20NHS PEG-CBS in vivo.
[0361] У пациентов с CBSDH уровни Hcy и часто Met в плазме и тканях являются высокими, в то время как уровни Cth и Cys являются низкими. Мыши I278T-/- на стандартном рационе имеют повышенные уровни Hcy и сниженные уровни Cys в плазме, таким образом повторяя ключевые аспекты нарушения регуляции метаболизма, наблюдаемого у пациентов с CBSDH (смотрите Wang, et al. (2005) Hum Mol Genet 14, 2201-2208, который полностью включен таким образом посредством ссылки). Среди метаболитов, анализируемых в этом исследовании, Hcy в плазме является маркером, который чаще всего отслеживают клинически (смотрите Morris et al. (2017) J Inherit Metab Dis 40, 49-74, который полностью включен таким образом посредством ссылки).
[0362] Уровни Hcy, Cys, Cth и Met в плазме (среднее значение±стандартная ошибка среднего) представлены в таблице 6.
[0363] Как показано в таблице 6 уровни Hcy в плазме у мышей I278T-/- были очень высокими (≥450 мкМ в D0) и существенно снижались в пределах 24 часов от первой инъекции, независимо от препарата. Препарат, подвергнутый инкубации при 25°С в течение одного месяца (Т1М-25С), подвергшийся существенному деПЭГилированию, проявлял эффективность, эквивалентную таковой контрольного препарата, хранившегося при температуре ниже -65°С (Т0-80С), и препарата, подвергнутого инкубации в течение 2 дней при 25°С (T2D-25С). Статистический анализ общих эффектов показал, что препарат, подвергнутый инкубации в течение 6 месяцев, (T6M-25C) был значительно менее эффективен, исходя из уровней Hcy, чем другие препараты (p<0,00501). В день 27 уровни Hcy оставались ниже, чем в D0 для двух других препаратов (p<0,01). Препарат, подвергнутый инкубации в течение 6 месяцев (T6M-25C), напротив, все еще оставался эффективным, но значительно менее эффективным, чем другие (p<0,01), в результате чего уровни Hcy в плазме составляли приблизительно 200 мкМ по сравнению с 88-145 мкМ в других трех группах. Через 72 часа после последней инъекции уровни Hcy частично повышались, но еще не возвращались к уровням у не подвергнутых лечению мышей (p<0,01 в D27 по сравнению с D0 для контрольного препарата (Т0-80С) и препарата, подвергнутого инкубации в течение 2 дней, (T2D-25C), но незначимые различия отмечались для препаратов, подвергнутых инкубации в течение 1 месяца (T1M-25C) и 6 месяцев (T6M-25C)). Эти результаты согласуются с предыдущими фармакодинамическими исследованиями (Majtan et al. Life Sci 200, 15-25 (2018), который полностью включен таким образом посредством ссылки).
[0364] Статистический анализ общих эффектов показал, что препарат, подвергнутый инкубации в течение 6 месяцев, оказывал значительно меньший эффект на уровни Cys, чем другие препараты (p<0,001). Уровни Cys в плазме, подавленные у мышей в качестве модели CBSDH, нормализовались (приблизительно 200-250 мкМ) всеми препаратами, кроме препарата, подвергнутого инкубации в течение шести месяцев (T6M-25C). Повышенные уровни Cys возвращались к исходному уровню в течение 72 часов после окончания схемы осуществления инъекций.
[0365] Несмотря на высокую вариабельность, уровни Cth в плазме повышались при лечении всеми препаратами, что согласуется с наблюдениями, что все препараты обладали каталитической активностью CBS. Поэтому препарат, подвергнутый инкубации в течение шести месяцев, (T6M-25C), скорее всего, будет иметь различия в фармакокинетике, а не в фармакодинамике по сравнению с тремя другими препаратами.
[0366] Уровни Met в плазме не демонстрировали заметных закономерностей в ответ на лечения, что согласуется с предыдущими наблюдениями, что уровни Met в плазме отражали в первую очередь потребление Met с пищей у мышей в качестве модели CBSDH, с лечением 20NHS PEG-CBS или без него (Majtan et al. J Inherit Metab Dis 41 (Suppl 1), S56 (2018). Статистический анализ не показал значимых различий в уровнях Cth между четырьмя препаратами.
[0367] В дополнение к Hcy, Cys, Cth и Met, несколько других аналитов были включены в панель метаболитов, и уровни этих метаболитов не показали значимых различий между группами. Дополнительные аналиты представлены в таблице 7.
SAH
[0368] Как показано в Таблице 7 (и как указано в таблице 6), T0-80C относится к контрольному препарату, T2D-25C относится к препаратам, подвергнутым инкубации в течение 2 дней при -25°С, T1M-25C относится к препаратам, подвергнутым инкубации в течение 1 месяца при 25°С, а T6M-25C относится к препаратам, подвергнутым инкубации в течение 6 месяцев при 25°С. Результаты RP-HPLC показали, что значительное де-ПЭГилирование произошло в 20NHS PEG-CBS, подвергнутой инкубации in vitro при 25°С в течение 1 месяца, и даже больше при инкубации в течение 6 месяцев. Тем не менее, лечение мышей I278T-/- всеми четырьмя препаратами приводило к резкому снижению уровней Hcy в плазме, хотя в случае наиболее значительно деПЭГилированного образца (препарата, подвергнутого инкубации течение 6 месяцев при 25°С) это снижение было значительно менее выраженным (p<0,01). Так же уровни Cys в плазме повышались всеми препаратами, хотя снова препарат, подвергнутый инкубации в течение 6 месяцев при 25°С, был значительно менее эффективным (p<0,001), чем другие. Все образцы, собранные в период лечения, продемонстрировали повышенные, хотя и вариабельные, уровни в плазме Cth, продукта, образуемого каждым препаратом из его субстрата Hcy, по сравнению с исходными уровнями (D0). Это указывало на то, что все препараты были каталитически активными, что согласуется с измерениями удельной активности, проведенными на препаратах перед инъекцией. Лечение не оказывало существенного влияния на уровни Met в плазме, что согласуется с предыдущими, полученными авторами настоящего изобретения данными, что уровни Met, по-видимому, в основном зависят от приема пищи, а не от лечения готовыми лекарственными формами, и тем фактом, что все мыши находились на стандартной рационе на протяжении всего исследования. Все лечения приводили к повышению активности CBS в плазме, но у мышей, получавших препарат, подвергнутый инкубации в течение 6 месяцев при 25°С, активность была значительно ниже (p<0,01) по сравнению с другими группами. Таким образом, лечение самым деПЭГилированным препаратом приводила к более низкой ферментативной активности в плазме, что приводило к более низкой эффективности in vivo, в то время как два других препарата, подвергнутых инкубации при 25°С, были столь же эффективными, как и контрольные образцы. Примечательно, что подвергнутый инкубации в течение одного месяца препарат, который был значительно деПЭГилирован по сравнению с контролем, продемонстрировал схожую с контролем эффективность. Уровни де-ПЭГилирования, наблюдаемые после инкубации в течение 2 дней, 1 месяца или 6 месяцев, вероятно, будут достигаться только в условиях ускоренного исследования стабильности и крайне маловероятно возникнут в клинических условиях.
Пример 4. Ферментативная активность препаратов с пониженным уровнем ПЭГилирования
[0369] Через 24 и 72 часа после последней инъекции измеряли активность CBS в плазме, т.е. каталитическую активность препаратов в образцах плазмы, собранных в дни 25 и 27.
[0370] Используя колориметрический анализ, описанный в Kayastha et al. Anal Biochem 193(2), 200-203 (1991), который полностью включен таким образом посредством ссылки, результаты исследования стабильности показали отсутствие потери удельной активности CBS (200±100 Ед./мг белка для партии) в течение 6-месячного инкубационного периода, при этом активности, измеренные для контроля, подвергнутых инкубации в течение 2 дней, 1 месяца и 6 месяцев препаратов, составляли 145, 204, 170 и 205 Ед./мг, соответственно.
[0371] Также был проведен другой анализ активности CBS, основанный на превращении меченного радиоактивным изотопом Ser, как описано в примере 1. Измерения активности CBS представлены в таблице 8.
мкл]
мкл]
[0372] На основании полученных данных деПЭГилирование in vivo не было значительным. Кроме того, при ускорении in vitro до уровней в подвергнутом инкубации препарате, включительно, деПЭГилирование, как было замечено, не влияло на активность CBS или эффективность in vivo.
[0373] В соответствии с увеличением метаболитов Met все препараты приводили к повышению активности CBS в плазме во всех группах, хотя наблюдалось, что препарат, подвергнутый инкубации в течение 6 месяцев, имел значительно более низкую активность, чем другие, в день 25 (p<0,04), но не в день 27. Снова, значительное де-ПЭГилирование в препарате, подвергнутом инкубации в течение 1 месяца, не влияло на уровни активности CBS в плазме, достигнутые in vivo, при этом результаты были сравнимыми с результатами в случае контроля.
[0374] Удельные активности контроля, препарата, подвергнутого инкубации в течение 2 дней, препарата, подвергнутого инкубации в течение 1 месяца, и препарата, подвергнутого инкубации в течение 6 месяцев, составляли 2324,11, 1714,19, 1786,08 и 1318,76 Ед./мг белка, соответственно, при анализе с использованием того же метода, отслеживающего превращение радиоактивного Ser. Подвергнутый инкубации в течение одного месяца препарат (Т1М-25С), значительно деПЭГилированный по сравнению с контролем, проявлял схожую с контролем активность.
Пример 5. Анализ с помощью Вестерн-блоттинга деПЭГилирования in vivo
[0375] Для оценки того, подвергалась ли готовая лекарственная форма деПЭГилированию in vivo, аликвоты плазмы мышей в качестве модели CBSDH, получавших контроль, анализировали с помощью Вестерн-блоттинга. В день 2 картина ПЭГилирования в образцах плазмы была схожей с таковой в случае контроля перед инъекцией, при этом неПЭГилированный фермент не обнаруживался, и не наблюдалась явная тенденция к большему количеству менее ПЭГилированных полос. В день 27, со сбором через 72 часа после последней инъекции, у всех мышей были обнаружены небольшие повышения неПЭГилированного фермента. Однако изменение картины ПЭГилирования было незначительным по сравнению с материалом до инъекции, а соотношения между различными полосами были приблизительно такими же в день 27, как и в день 2. Так же деПЭГилирование in vivo было минимальным для других препаратов, даже несмотря на то, что перед инъекцией препараты, подвергнутые инкубации в течение 1 месяца и 6 месяцев, по данным RP-HPLC продемонстрировали значительные уровни деПЭГилированного фермента, в том числе немодифицированной CBS, особенно в случае препарата, подвергнутого инкубации в течение 6 месяцев. Возможно, что эти наиболее деПЭГилированные формы подвергались деградации или выводились быстрее после инъекции, поэтому они не присутствовали в образцах плазмы, проанализированных с помощью Вестерн-блоттинга. Схожие анализы трех других препаратов также показали минимальное де-ПЭГилирование после их введения in vivo.
Пример 6. Сравнение эффективности длительного лечения 20NHS PEG-CBS с рационом с ограничением Met
[0376] Нарушение регуляции метаболизма серосодержащей аминокислоты является ключевой особенностью фенотипа HCU как у являющихся людьми пациентов, так и у моделей заболевания на мышах. Устойчивое улучшение или восстановление контроля над метаболизмом являются ключевыми аспектами успешного лечения (смотрите Morris et al. (2017) J Inherit Metab Dis 40, 49-74; Majtan et al. (2017) FASEB J 31, 5495-5506; Majtan et al. (2018) Enzyme Replacement Therapy Ameliorates Multiple Symptoms of Murine Homocystinuria. Molecular therapy: the Journal of the American Society of Gene Therapy 26, 834-844; каждый из которых полностью включен таким образом посредством ссылки). Начиная с 4-недельного возраста, мышей содержали на рационах с нормальным (REG) или ограниченным (MRD) содержанием метионина, и они получали подкожные инъекции либо PBS в качестве носителя, либо 10 мг/кг 20NHS PEG-CBS три раза в неделю до окончания исследования в 22-недельном возрасте. В таблице 9 представлены уровни метаболитов серосодержащей аминокислоты в плазме у мышей в возрасте 18 недель. Представлены репрезентативные краткие характеристики концентраций общего гомоцистеина, общего цистеина, цистатионина, метионина и отношения SAM/SAH в плазме. Исследуемые группы, описанные и проанализированные в этом и последующих примерах здесь, суммированы следующим образом:
[0377] WT (REG+PBS) относится к мышам дикого типа на обычном рационе, получающим подкожную инъекцию PBS;
[0378] WT (REG+20 NHS PEG-CBS) относится к мышам дикого типа на обычном рационе, получающим подкожную инъекцию 20NHS PEG-CBS;
[0379] I278T (REG+PBS) относится к мышам I278T на обычном рационе, получающим подкожную инъекцию PBS;
[0380] I278T (REG+20NHS PEG-CBS) относится к мышам I278T на обычном рационе, получающим подкожную инъекцию 20NHS PEG-CBS;
[0381] WT (MRD+PBS) относится к мышам дикого типа на рационе с ограничением Met, получающим подкожную инъекцию PBS;
[0382] WT (MRD+20NHS PEG-CBS) относится к мышам дикого типа на рационе с ограничением Met, получающим подкожную инъекцию 20NHS PEG-CBS;
[0383] I278T (MRD+PBS) относится к мышам I278T на рационе с ограничением Met, получающим подкожную инъекцию PBS; и
[0384] I278T (MRD+20NHS PEG-CBS) относится к мышам I278T на рационе с ограничением Met, получающим подкожную инъекцию 20NHS PEG-CBS.
SAM/SAH
[0385] Как показано в таблице 9, у мышей дикого типа, независимо от рациона или лечения, уровни Hcy в плазме находились в диапазоне значений для нормальных здоровых мышей (приблизительно 16 мкМ). Однако у мышей I278T на REG-рационе, получающих носитель, уровни Hcy в плазме были значительно повышенными по сравнению с контролем (423 мкМ, p<0,001). На MRD-рационе уровни Hcy в плазме были значительно ниже (140 мкМ, т.е. снижение на 67%), но все же оставались заметно повышенными по сравнению с контролями (p<0,001). Лечение с помощью 20NHS PEG-CBS значительно снижало уровни Hcy в плазме мышей I278T на REG-рационе до 41 мкМ (снижение на 90%, p<0,001) и полностью их нормализовало до 14 мкМ у мышей на MRD-рационе (p<0,001) по сравнению с мышами I278T, которым инъецировали носитель. Уровни Cys в плазме были почти в 3 раза ниже у мышей I278T на REG-рационе, получающих носитель, по сравнению с контролями (105 в сравнение с 295 мкМ, p<0,001) и в пределах нормы во всех остальных группах. В соответствии с его ролью продукта реакции, катализируемой 20NHS PEG-CBS, уровни Cth в плазме были повышенными у всех мышей, получающих лечение 20NHS PEG-CBS, по сравнению с их аналогами, которым инъецировали носитель. Повышение уровня Cth в плазме зависело от концентрации Hcy, ограничивающего субстрата, достигая 76 и 18 мкМ у мышей I278T на REG-рационе и MRD-рационе, соответственно (p<0,001). 20NHS PEG-CBS сохраняла свою эффективность даже тогда, когда концентрации субстрата были очень низкими, на что указывало в приблизительно 8 раз более высокие уровни Cth в плазме контролей, подвергнутых лечению 20NHS PEG-CBS, по сравнению с теми, кто получал носитель. Уровни Met в плазме были выше во всех группах на REG-рационе, чем на MRD-рационе. Однако уровни Met в плазме у мышей I278T на MRD-рационе были схожими с таковыми у контролей на REG-рационе (51 в сравнение с 52 мкМ, p=не уточнено) и нормализовались при лечении 20NHS PEG-CBS (30 мкМ, p<0,001). Отношение SAM к SAH, отражающее способность к метилированию, было существенно сниженным у мышей I278T на REG-рационе (0,12) и частично повышенным на MRD-рационе (1,77) по сравнению с соответствующими контролями (3,29 и 3,84 у мышей WT на REG-рационе и MRD-рационе, соответственно; p<0,001). При лечении 20NHS PEG-CBS отношения SAM/SAH значительно улучшались и полностью нормализовались у мышей I278T на REG-рационе (2,26, p<0,001) и MRD-рационе (4,01, p<0,001), соответственно. В целом, различия между группами, описанными здесь, для момента времени W18 соответствовали тем, которые наблюдались в течение всего курса исследования.
[0386] В руководствах по лечению HCU, вызванной дефицитом CBS, рекомендуется поддерживать концентрацию общего Hcy в плазме ниже 50 и 100 мкМ у пациентов, которые являются полностью чувствительными и нечувствительными к пиридоксину, соответственно (смотрите Morris et al. (2017) J Inherit Metab Dis 40, 49-74, который полностью включен таким образом посредством ссылки). В исследовании авторов настоящего изобретения мыши I278T не смогли достичь этого целевого уровня даже при содержании на рационе со строгим ограничении Met, получая в 8 раз меньше Met, чем в случае стандартного рекомендуемого потребления для мышей (0,5 г/кг и 4 г/кг Met в MRD-рационе и REG-рационе, соответственно). За исключением начального образца, взятого в возрасте 6 недель, уровни Hcy в плазме колебались между 121-195 мкМ у мышей I278T на MRD-рационе во время исследования. Используя ту же модель на мыши, что и в Gupta et al. (2014) Cystathionine beta-synthase-deficient mice thrive on a low-methionine diet. FASEB J 28, 781-790, который полностью включен таким образом посредством ссылки, было установлено, что схожий MRD-рацион, содержащий 0,5 г/кг Met, снижает уровень Hcy в сыворотке до 81 мкМ у 34-недельных мышей I278T. Разница может быть связана с возрастом мышей и продолжительностью их содержания на рационе. Напротив, уровни Hcy в плазме мышей I278T, которые находили на REG-рационе и были подвергнуты лечению 20NHS PEG-CBS, варьировали в диапазоне 26-41 мкМ, за исключением последнего образца, взятого в возрасте 22 недель. Кроме того, введение 20NHS PEG-CBS мышам I278T на MRD-рационе полностью нормализовало уровень Hcy в плазме ниже 15 мкМ. Эти данные свидетельствуют о том, что, в отличие от ферментотерапии (ET), даже строгое ограничение Met не может привести уровни Hcy в плазме к терапевтическим целевым значениям у мышей с HCU. Если желательна полная нормализация метаболизма, потребуется комбинация ЕТ с некоторым уровнем ограничения Met для достижения этой цели.
[0387] Эти результаты являются доказательством того, что полная нормализация метаболизма не требуется для достижения коррекции фенотипа HCU, и, таким образом, по-видимому, существует пороговый эффект, когда речь идет о проявлении фенотипа HCU у мышей. На самом деле модели менее тяжелой HCU на мышах с уровнями Hcy в плазме между 170 и 300 мкМ имели фенотип гораздо менее тяжелой HCU (смотрите Gupta et al. (2009)). Mouse models of cystathionine beta-synthase deficiency reveal significant threshold effects of hyperhomocysteinemia. FASEB J 23, 883-893, который полностью включен таким образом посредством ссылки) или не демонстрировали клинические симптомы HCU (смотрите Majtan et al. (2018) Human mutation 39, 210-218, который полностью включен таким образом посредством ссылки). По-видимому, этот порог применим к являющимся людьми пациентам, а также к подвергнутым лечению пациентам с HCU, которые показали снижение риска и частоты сердечнососудистых событий, несмотря на неспособность достичь нормализации метаболизма (смотрите Wilcken et al. (1997) Journal of Inherited Metabolic Disease 20, 295-300; Yap et al. (2000) Vascular complications of severe hyperhomocysteinemia in patients with homocystinuria due to cystathionine beta-synthase deficiency: effects of homocysteine-lowering therapy. Seminars in thrombosis and hemostasis 26, 335-340; Yap et al. (2001) Vascular outcome in patients with homocystinuria due to cystathionine beta-synthase deficiency treated chronically: a multicenter observational study. Arteriosclerosis, thrombosis, and vascular biology 21, 2080-2085; каждый из которых полностью включен таким образом посредством ссылки).
Пример 7. Опосредованная потоком вазодилатация (FMD)
[0388] Мыши I278T страдают нарушением функции эндотелия, а тромбоэмболия является основной причиной заболеваемости и ранней смерти пациентов с HCU (смотрите Majtan et al. (2018) Human mutation 39, 210-218, который полностью включен таким образом посредством ссылки). Поскольку наличие нарушения функции эндотелия тесно связано с риском развития сердечнососудистых заболеваний в бедренной артерии исследуемых мышей оценивали эндотелий-зависимую опосредованную потоком вазодилатацию (FMD) (не представленные данные). Эндотелий-зависимую опосредованную потоком вазодилатацию осуществляли, как описано в (смотрите Schuler et al. (2014) Measurement of endothelium-dependent vasodilation in mice--brief report. Arteriosclerosis, thrombosis, and vascular biology 34, 2651-2657, который полностью включен таким образом посредством ссылки), мышей анестезировали изофлураном (3% для индукции и 1,5% для поддержания) Температуру тела поддерживали на уровне 37±1°C с помощью подогреваемого стола для осмотра, который также был снабжен электродами для снятия ЭКГ, и контролировали, используя ректальный термометр. Задние конечности выбривали и покрывали теплым гелем для ультразвуковой обработки. Ультразвуковой датчик прикрепляли к стереотаксическому держателю и вручную совмещали с бедренной веной, видимой в верхней части внутренней поверхности бедра, высокочастотную платформу визуализации Vevo 2100 с высоким разрешением, оснащенную линейным микросканирующим преобразователем с частотой 30-70 МГц (Fujifilm VisualSonics, Toronto, ON, Канада), использовали для визуализации бедренных артерий у мышей. Сосудистый окклюдер (Docx, Ukiah, CA, США) помещали вокруг нижней конечности для вызова окклюзии дистального отдела задней конечности в качестве триггера ишемии. Как только было получено четкое изображение стенки сосуда, и зарегистрированы базовые показания, эксперимент начинали с надувания сосудистого окклюдера в течение 5 минут. После ишемии задней конечности манжету сдували, и измерения диаметра бедренной артерии (FA) постоянно регистрировали в течение 5 минут с 30-секундными интервалами. Диаметр бедренной артерии на полученных изображениях определяли вручную в автономном режиме.
[0389] Для определения эффектов длительного введения готовой лекарственной формы на клинические симптомы HCU у мышей, мышам I278T (+/+ и -/-) на рационе с ограничением Met (MRD) вводили либо носитель (PBS), либо 20NHS PEG-CBS в дозе 10 мг/кг (готовой лекарственной формы) три раза в неделю до возраста 22 недели. Мыши находились на одном из двух рационов: 1) стандартном рационе (REG) с 4,0 г/кг Met или 2) рационе с ограничением Met (MRD) с 0,5 г/кг Met. Мышей делили на следующие группы: А (+/+,REG, PBS); В (+/+, REG, готовая лекарственная форма); C (-/-, REG, PBS); D (-/-, REG, готовая лекарственная форма); E (+/+, MRD, PBS); F (+/+, MRD, готовая лекарственная форма); G (-/-, MRD, готовая лекарственная форма); H (-/-, MRD, готовая лекарственная форма).
[0390] У мышей I278T отмечали значительную потерю гибкости бедренной артерии (т.е. ригидность артерии) по сравнению с контрольной группой (+/+) в случае лечения лекарственным средством, нормализирующим фенотип. Отмечали, что диаметр бедренной артерии на исходном уровне T0 был меньше у мышей на MRD-рационе, чем у мышей на REG-рационе. После регистрации исходных значений 5-минутная окклюзия без кровотока вызывала реактивную гиперемию, характеризующуюся временным увеличением диаметра артерий перед возвращением к исходному уровню. В таблице 10 представлен диаметр бедренной артерии мышей на REG-рационе или MRD-рационе, оцененный у 19-недельных мышей.
[0391] Как показано в таблице 10, у мышей 1278T на REG-рационе, получавших носитель, явно наблюдалось нарушение эндотелиальной функции, на что указывало значительно меньшее максимальное расширение бедренной артерии в моменты времени - 60 и 90 секунд (в обоих случаях 216 мкм) после 5-минутной ишемии по сравнению с контролями (238 и 235 мкм, p<0,001), а также с мышами I278T на том же рационе, но получающими лечение 20NHS PEG-CBS (в обоих случаях 232 мкм, p<0,01). Получающие носитель мыши I278T на REG-рационе продемонстрировали значительно уменьшенный ответ по сравнению со всеми другими группами. Напротив, ни у одной из мышей на MRD-рационе не было признаков нарушения эндотелиальной функции, и они демонстрировали нормальную сосудистую реакцию на ишемию в случае лечения 20NHS PEG-CBS и без него.
[0392] Отмечали, что лечение мышей I278T на MRD-рационе нормализовало диаметр бедренной артерии до того же уровня, что и у мышей на REG-рационе.
Пример 8. Модель вызванного химическим повреждением сонной артерии тромбоза (CITM )
[0393] Измерения на модели вызванного химическим повреждением сонной артерии тромбоза (CITM) проводили, как описано в Marchi et al. (2012) Thrombosis and hemostasis 108, 516-526, который полностью включен таким образом посредством ссылки. Мышей анестезировали путем внутрибрюшинной инъекции комбинации кетамина (в дозе для индукции - 80-100 мг/кг, затем 10-20 мг/кг/ч для поддержания) и ксилазина (в дозе для индукции - 8-16 мг/кг, затем 1-2 мг/кг/ч для поддержания), и температуру тела поддерживали на уровне 36-38°C с помощью грелки и контролировали с помощью ректального термометра. Трахею обнажали и канюлировали, и животных искусственно вентилировали воздухом и дополнительным кислородом. Обнажали общие сонные артерии, и исходный поток контролировали с помощью доплеровского датчика потока 0,5 PBS (Transonic Systems, Ithaca, NY, США). Для повреждения артерии на сонную артерию на 1 минуту накладывали фильтровальную бумагу Whatman размером 1×1 мм, смоченную 10% раствором хлорида железа. Кровоток в сосуде контролировали и регистрировали вплоть до 20 минут, используя ультразвуковой датчик. Время до окклюзии (TTO) определяли как время между введением FeCl3 и отсутствием потока в течение 1 минуты. Кровь брали из нижней полой вены в шприц, промытый 3,2% раствором цитрата натрия, и превращали в плазму с низким содержанием тромбоцитов с помощью центрифугирования при 5000хg в течение 10 мин. В конце процедуры мышей подвергали эвтаназии путем вывиха шейных позвонков с последующей двусторонней торакотомией. В таблице 11 представлены результаты, полученные на модели вызванного химическим повреждением сонной артерии тромбоза (CITM). Время до стойкой окклюзии сонной артерии после химического повреждения, вызванного 10% FeCl3, определяли у 22-недельных мышей. Только мыши I278T, которые находились на REG-рационе и получали носитель, продемонстрировали значительное увеличение времени до окклюзии, тогда как диетотерапия с использованием MRD и/или лечение 20NHS PEG-CBS нормализовали этот параметр до контрольных уровней. «CBS» в таблице 11 представляет собой 20NHS PEG-CBS.
[0394] У мышей I278T наблюдалась задержка экспериментального тромбоза, который нормализовался при любом лечении. Для оценки того, проявляют ли мыши I278T протромботический фенотип, и если да, как рацион и ферментотерапия повлияют на него, индуцировали экспериментальный тромбоз общей сонной артерии, используя 10% FeCl3. У мышей I278T, которым инъецировали носитель, на REG-рационе отмечалось значительно большее время до стойкой окклюзии, чем в других группах (10 минут 59 секунд), что указывает на то, что, в отличие от пациентов с HCU, у мышей I278T не проявляется протромботический фенотип и, кроме того, демонстрировались значительные задержки тромбообразования по сравнению с контролями (8 минут 42 секунды, p<0,05). Интересно, что лечение мышей I278T с помощью 20NHS PEG-CBS (8 минут 49 секунд) или диетотерапия с использованием MRD (7 минут 34 секунды) нормализовало время до окклюзии до значений, наблюдаемых в контроле.
[0395] Тромбоэмболия является основной причиной заболеваемости и смертности при HCU (смотрите Mudd, et al. (2001) Disorders of transsulfuration. In The Metabolic and Molecular Bases of Inherited Disease (Scriver, C. R., Beaudet, A. L., Sly, W. S., Valle, D., Childs, B., Kinzler, K., and Vogelstein, B., eds) pp. 2007-2056, McGraw-Hill, New York; Morris et al. (2017) J Inherit Metab Dis 40, 49-74; каждый из которых полностью включен таким образом посредством ссылки), однако мыши I278T на REG-рационе, получающие плацебо, не проявляли склонности к тромбозу, несмотря на значительное нарушение эндотелиальной функцию. Об аналогичном открытии сообщалось ранее с использованием той же модели I278T на мыши (смотрите Dayal et al. (2012) Blood 119, 3176-3183, который полностью включен таким образом посредством ссылки), а также для мышей с полным нокаутом CBS (смотрите Maclean et al. (2010) Molecular Genetics and Metabolism 101, 163-171; который полностью включен таким образом посредством ссылки).
[0396] Как нарушение эндотелиальной функцию, так и парадоксально увеличенное время до окклюзии нормализовались у мышей I278T на MRD-рационе или на REG-рационе, но получающих 20NHS PEG-CBS. Эти результаты означают, что, несмотря на отсутствие гиперкоагуляции у мышей I278T, ограничение Met или введение 20NHS PEG-CBS могут быть эффективными в коррекции патологического гемостаза, наблюдаемого в других моделях HCU на мышах и, что более важно, у являющихся людьми пациентов.
Пример 9. Исследования поведения
[0397] Во всех исследованиях поведения от экспериментатора скрывали сведения о генотипе, рационе и лечении мышей. Задание в тесте «открытое поле» исследует аспекты поведения типа состояния тревоги (смотрите Prut et al. (2003) European journal of pharmacology 463, 3-33, который полностью включен таким образом посредством ссылки). Мыши свободно исследовали открытую коробку (44×44×24 см), при отслеживании их сверху в течение 10-минутного испытания. Перед началом испытания центр и периметр были отмечены, используя программное обеспечение для отслеживания животных (Ethovision XT, Noldus, Wageningen, Нидерланды). Программное обеспечение использовалось для определения времени, проведенного в центре по сравнению с периферией, а также пройденного расстояния.
[0398] Задание с использованием коробки-головоломки выполнялось, как описано ранее у Ben Abdallah et al. (2011) Experimental neurology 227, 42-52, который полностью включен таким образом посредством ссылки, мышам давали 3 минуты, чтобы войти в целевую коробку (15×28×28 см). Если мышь не попадала в целевую коробку, ее поощрял и направлял экспериментатор. Крытая целевая коробка примыкала к хорошо освещенной открытой арене (58х28х28 см). Вход в целевую коробку начинался как дверной проем (испытание 1), затем был заменен тоннелем (испытания 2, 3, 4), затем тоннель был засыпан опилками (испытания 5, 6, 7), а затем засыпанный тоннель был закрыт небольшим прямоугольным куском картона (испытания 8, 9). Каждая мышь подвергалась девяти испытаниям в течение 3 дней. Первый день состоял из испытаний 1-3, второй день состоял из испытаний 4-6, а испытания 7-9 выполнялись в день 3.
[0399] Для проверки когнитивной функции более высокого порядка проводили тест на решение задач, в котором от мышей требовалось выполнение задач избегания опасности возрастающей сложности в течение ограниченного периода времени. Арена с коробкой-головоломкой была спроектирована с использованием белой коробки PLEXIGLAS™, разделенной черным барьером на два отсека: стартовую и целевую зоны. Мышей помещали в ярко освещенную стартовую зону, и было замечено, что они предпочитали меньшую крытую/темную целевую зону, доступ к которой осуществляется через узкий тоннель. Тесты состояли из девяти испытаний, распределенных на протяжении трех дней подряд, в течение которых мышей обучали преодолевать препятствия в тоннеле, чтобы получить доступ к целевой зоне. Препятствия были трех видов и варьировались от легких до средних и сложных. Таблица 12 представляет собой сводку испытаний 1-9 (T1-T9).
[0400] Любое лечение мышей I278T улучшает их способность к обучению и познание, но ограничение Met увеличивает тревогу. Задержка развития и различные психические симптомы распространены среди пациентов с HCU. Сначала был проведен тест «открытое поле» для оценки уровня тревоги и двигательной активности у исследуемых мышей. В таблице 13 и таблице 14 представлены результаты теста «открытое поле». В таблице 13 представлено пройденное расстояние для каждой группой мышей.
[0401] В таблице 14 представлено время, проведенное в центре, для каждой группы мышей.
[0402] Не наблюдалось значительного влияния лечения 20NHS PEG-CBS на уровень тревоги или двигательную активность как контрольных мышей, так и мышей I278T. Однако мыши на MRD-рационе, независимо от генотипа, прошли на арене для тестирования значительно большее расстояние (p<0,01) и находились в более тревожном состоянии, поскольку они проводили меньше времени в центре арены (p<0,001) по сравнению с мышами на REG-рационе. Хотя пол мыши и инъекции носителя PBS или 20NHS PEG-CBS не оказывали какого-либо значительного влияния на поведение мышей, REG- (закрашенные символы) и MRD-рационы (незакрашенные символы) приводили к изменениям в передвижении и уровне тревоги как у мышей дикого типа, так и у мышей I278T.
[0403] Во-вторых, когнитивную/исполнительную функцию исследуемых мышей оценивали в исследовании с использованием коробки-головоломки (фиг. 2), в котором мыши должны добраться до темной целевой коробки, чтобы избежать ярко освещенной арены. В таблице 15 представлено время до достижения целевой коробки у мышей WT и I278T на одном из двух рационов, получающих либо носитель, либо 20NHS PEG-CBS. Этот результат позволил оценить способности решать задачи (испытания с № 2, 5 и 8) и обучаемость/кратковременную память (испытания с № 3, 6 и 9). Кроме того, повторение на следующий день обеспечило измерение долговременной памяти (испытания с № 4 и 7).
[0404] Доступ к целевой коробке усложняли с каждым испытанием, как указано в таблице 15, в которой представлено время в секундах, необходимое в каждом из 9 испытаний для мышей в исследуемых группах, чтобы добраться до целевой коробки. Среднее значение и стандартная ошибка среднего (SEM) были рассчитаны для результатов, представленных в таблице 15 (не представленные данные). Контрольные мыший на одном из двух рационов, получающие либо носитель, либо 20NHS PEG-CBS, выполняли тест сходно без признаков когнитивного расстройства. С другой стороны, мыши I278T на REG-рационе продемонстрировали значительно худшее выполнение, что указывает на когнитивное расстройство, по сравнению с мышами на MRD-рационе или контролями (p<0,001). При лечении 20NHS PEG-CBS мыши I278T выполняли тест так же, как и контрольные мыши, на обоих рационах.
[0405] У мышей I278T, которые находились на REG-рационе и получали инъекции PBS, наблюдались когнитивные расстройства по сравнению с мышами I278T, которые находились на MRD-рационе и получали инъекции PBS, и мышами на REG- и MRD-рационах, которым вводили готовую лекарственную форму. Вывод подтверждался неспособностью мышей на REG-рационе, получавших инъекции PBS, вовремя достигать целевой коробки, когда сложность задачи возрастала (т.е. испытания 5-10). Не наблюдалось значимых различий во времени достижения целевой коробки между мышами, которым вводили готовую лекарственную форму, на REG-рационе или на MRD-рационе.
[0406] У пациентов с HCU распространено многие психологические и психиатрические состояния, такие как психоз, обсессивно-компульсивное расстройство, депрессия и расстройства поведения/личности (смотрите Abbott et al. (1987) American Journal of Medical Genetics 26, 959-969, который полностью включен таким образом посредством ссылки). Кроме того, индивидуумы с HCU имеют много недостатков развития и познавательные затруднения, при этом значительное число случаев неспособно к обучению и имеет более низкий IQ (смотрите El Bashir et al. JIMD reports 21, 89-95, который полностью включен таким образом посредством ссылки). Проведенное авторами настоящего изобретения исследование поведения мышей показало, что этот фенотип действительно повторяется у мышей I278T, демонстрирующих когнитивное расстройство при их содержании на REG-рационе и получении ими носителя по сравнению с контролями и мышами I278T, которых содержали на MRD-рационе или подвергали лечению 20NHS PEG-CBS (фиг. 2 и таблица 15). Насколько известно авторам настоящего изобретения, это первое сообщение о таком фенотипе и его успешной коррекции в какой-либо модели вызванной дефицитом CBS HCU на мыши. Кроме того, мыши продемонстрировали значительно повышенный уровень активности и тревоги при их содержании на MRD-рационе по сравнению с мышами на REG-рационе.
[0407] У мышей I278T, получающих носитель, на REG-рационе были значительно нарушены когнитивные функции по сравнению с мышами на MRD-рационе, на что указывало большее время до достижения целевой коробки (таблица 15). Однако мыши I278T, которым инъецировали 20NHS PEG-CBS, на REG-рационе выполняли тест схоже с контролями или мышами I278T на MRD-рационе (таблица 15). Сплошные линии с закрашенными символами и пунктирные линии со незакрашенными символами обозначают мышей на REG- и MRD-рационах, соответственно. Точки на всех графиках представляют собой средние значения, а «усы» показывают среднеквадратические отклонения (SD).
[0408] Эти особенности поведения, вероятно, не связаны с HCU, поскольку она поражала мышей независимо от генотипа и лечения 20NHS PEG-CBS. Было установлено, что депривация незаменимых аминокислот, включая ограничение Met, ощущается в передней грушевидной области коры, и последующая передача глутаматергических сигналов влияет на поведение мышей (смотрите Anthony et al. (2013) Detection of amino acid deprivation in the central nervous system. Current opinion in clinical nutrition and metabolic care 16, 96-101, который полностью включен таким образом посредством ссылки). Глутамат является основным нейромедиатором возбуждения в центральной нервной системе, что может объяснить повышенную двигательную активность, уровень беспокойства и тревоги.
Пример 10. Двухэнергетическая рентгеновская абсорбциометрия (DEXA)
[0409] Плотность костей и состав тела оценивали у мышей, подвергнутых анестезии (с использованием комбинации 60 мг/кг кетамина и 15 мг/кг ксилазина в PBS, вводимой внутрибрюшинно), используя сканер GE Lunar PIXImus (Lunar Corp., Madison, WI,, США). Мышей помещали на лоток животом вниз и сканировали от шеи вниз за исключением хвоста. После сканирования, мышей помещали обратно в их клетки для восстановления.
[0410] Ограничение Met ухудшает минерализацию костей и состав тела, тогда как лечение 20NHS PEG-CBS нормализует фенотип мышей I278T на REG-рационе. Среди клинических симптомов, наблюдаемых у пациентов с HCU, присутствуют худоба, низкий индекс массы тела и остеопороз (смотрите Mudd et al. (2001) Disorders of transsulfuration. In The Metabolic and Molecular Bases of Inherited Disease (Scriver, C. R., Beaudet, A. L., Sly, W. S., Valle, D., Childs, B., Kinzler, K., and Vogelstein, B., eds) pp. 2007-2056, McGraw-Hill, New York, который полностью включен таким образом посредством ссылки). Таким образом, мышей исследовали, используя DEXA, для оценки минерального содержания в их костях и состава их тела. В таблице 16 представлены результаты оценки с помощью DEXA минерализации костей и состава тела. Сканирования DEXA проводили, когда мыши достигали возраста 22 недель. Таблица 16 включает минеральное содержание в костях, массу жировой ткани и массу нежировых тканей.
[0411] На REG-рационе минеральное содержание в костях (BMC) было значительно ниже у мышей I278T, получающих носитель, по сравнению с контролями (0,33 в сравнение с 0,39 г, p<0,001), в то время как лечение 20NHS PEG-CBS полностью нормализовало его (0,4 в сравнение с 0,4 г, p=не уточнено). На MRD-рационе все группы продемонстрировали равное BMC (0,34-0,36 г), которое было значительно сниженным по сравнению с контролями на REG-рационе (p<0,05) и схожим с таковым у мышей I278T, которым вводили носитель, на REG-рационе. На REG-рационе мыши I278T, получающие носитель, были значительно худее мышей в других группах, в частности, имели меньше жировой ткани (2,63 в сравнение с 4,24 г, p<0,01) и массу нежировой ткани (13,81 в сравнение с 16,97 г, p<0,001), чем контроли. Лечение 20NHS PEG-CBS нормализовало состав тела мышей I278T на REG-рационе. На MRD-рационе величина массы жировой ткани была сопоставимой во всех группах и схожей с таковой у контролей или у мышей I278T, подвергнутых лечению 20NHS PEG-CBS, на REG-рационе. Точно так же величина массы нежировой ткани была схожей во всех группах на MRD-рационе (14,71-16,02 г), но значительно ниже по сравнению с контролями и мышами I278T, подвергнутыми лечению 20NHS PEG-CBS, на REG-рационе (p<0,05).
[0412] Аномалии скелета и дефекты соединительной ткани являются самыми заметными клиническими симптомами у пациентов с HCU (смотрите Mudd et al. (2001) Disorders of transsulfuration. In The Metabolic and Molecular Bases of Inherited Disease (Scriver, C. R., Beaudet, A. L., Sly, W. S., Valle, D., Childs, B., Kinzler, K., and Vogelstein, B., eds) pp. 2007-2056, McGraw-Hill, New York, который полностью включен таким образом посредством ссылки). Остеопороз, часто связанный со сколиозом, и низкий индекс массы тела являются типичными проявлениями у не подвергнутых лечению пациентов или пациентов с поздно поставленным диагнозом независимо от тяжести заболевания (смотрите Mudd et al. (2001) Disorders of transsulfuration. In The Metabolic and Molecular Bases of Inherited Disease (Scriver, C. R., Beaudet, A. L., Sly, W. S., Valle, D., Childs, B., Kinzler, K., and Vogelstein, B., eds) pp. 2007-2056, McGraw-Hill, New York; Parrot et al. (2000) J Inherit Metab Dis 23, 338-340; каждый из которых полностью включен таким образом посредством ссылки). Снижение минерализации костной ткани, низкое содержание жировой ткани и низкий общий вес были обнаружены у KO и I278T (смотрите Majtan et al. (2017) FASEB J 31, 5495-5506; Gupta et al. (2009) FASEB J 23, 883-893; Majtan et al. (2018) Enzyme Replacement Therapy Ameliorates Multiple Symptoms of Murine Homocystinuria. Molecular therapy: the journal of the American Society of Gene Therapy 26, 834-844; каждый из которых полностью включен таким образом посредством ссылки), но не у модели HCU на мыши HO (смотрите Majtan et al. (2018) Human mutation 39, 210-218; который полностью включен таким образом посредством ссылки). Как показано в таблице 16, эти данные, а также эффективность 20NHS PEG-CBS в нормализации этого фенотипа, были подтверждены у мышей I278T на REG-рационе, получающих носитель. С другой стороны, строгое ограничение Met приводило к снижению минерализации костной ткани, меньшей величине массы нежировой ткани и нормальной-увеличенной величине массы жировой ткани у всех мышей на MRD-рационе, независимо от генотипа и лечения, по сравнению с мышами дикого типа на REG-рационе. За исключением жировой массы, MRD-рацион по существу давал общую картину, очень похожую на таковую у не подвергнутых лечению мышей I278T на REG-рационе, получающих носитель. Ранее было установлено, что MRD-рацион является очень эффективным в коррекции фенотипа HCU у мышей I278T, в том числе минерализации костной ткани (смотрите Gupta et al. (2014) FASEB J 28, 781-790; Kruger et al. (2016) Annals of the New York Academy of Sciences 1363, 80-90; каждый из которых полностью включен таким образом посредством ссылки).
Пример 11. Причина смерти мышей с HCU на рационе с высоким содержанием Met
[0413] Данные на мышах показали, что строгое ограничение Met у пациентов с HCU может привести к нежелательному результату. Наблюдалось, что самки мышей HO, но не самцы мышей HO, внезапно умирали после перехода на рацион с высоким содержанием метионина (HMD), который включал 8,2 г МЕТ на кг пищи. Для анализа причины смерти взрослых самок мышей HO сажали на HMD-рацион, мышей в подростковом возрасте I278T - на HMD-рацион, REG-рацион (4,0 г Met на кг пищи) или REG+0,1/0,2/0,4% Met в воде. За мышами ежедневно следили, регулярно взвешивали и брали кровь. Свеженайденные тушки животных подвергались вскрытию и гистологическому анализу.
[0414] Мыши были разделены на 6 групп (A-F). Группа А состояла из 7 самок мышей HO на HMD-рационе. Группа B состояла из одного самца мыши I278T и одной самки мыши I278T на HMD-рационе. Группа C состояла из одного самца мыши I278T и одной самки мыши I278T на REG-рационе и с добавлением 0,4% Met. Группа D состояла из одного самца мыши I278T и двух самок мышей I278T на REG-рационе с добавлением 0,2% Met. Группа E состояла из одного самца мыши I278T и одной самки мыши I278T на REG-рационе и с добавлением 0,1% Met. Группа F состояла из одной самки мыши I278T и двух самцов мышей I278T на REG-рационе. Контроли для вскрытия всех трудов включали четырех самок мышей HO; двух самцов и двух самок взрослых мышей I278T и WT, 2 самок мышей в подростковом возрасте I278T и трех самцов и трех самок мышей в подростковом возрасте I278T и WT. Все контроли при вскрытии трупов находились на стандартном рационе (STD).
[0415] Три из семи самок мышей НО на HMD-рационе умерли между днем 11 и днем 18. Эти мыши не росли, и потеря веса или увеличение веса полностью прекратились. При содержании на HMD-рационе наблюдали существенное увеличение уровней как Hcy, так и Met, тогда как уровень Cys все время оставался низким. Предварительные гистологические данные показали дегенерацию фолликулов в яичниках, экзокринную поджелудочную железу с сапонификацией, вакуолями, и многоочаговую минерализацию в сердечной мышце, мозговой слой с мертвыми нейронами, дисплазию вилочковой железы с выраженным апоптозом Т-лимфоцитов, стеатоз печени, воспаление и фиброз.
[0416] В случае мышей I278T наблюдалось увеличение уровня Hcy в плазме у мышей, получающих добавки Met в воде, а не в пище. Наблюдалось увеличение Met в плазме аналогично Hcy, но в зависимости от потребления Met, за исключением контрольных мышей на REG-рационе. Предварительные гистологические данные для мышей I278T показали экзокринную поджелудочную железу с фиброзом и воспалением, воспаление печени, стеатоз, дегенерацию волосяных фолликулов и кишечного эпителия, дисплазию вилочковой железы с выраженным апоптозом Т-лимфоцитов и кровь в двенадцатиперстной кишке.
[0417] Измеряли вес тела и уровни метаболитов с течением времени. Также выполняли вскрытие всех трупов и гистологическое исследование под оптическим микроскопом.
Пример 12. Исследование токсичности на отличных от человека приматах (NHP)
[0418] Токсичность описанной здесь готовой лекарственной формы определяли после подкожного (SC) введения один раз каждые 3 дня и один раз каждый день до NHP в течение 26 недель.
[0419] Группы из 8 самцов и самок яванских макак получали подкожные инъекции носителя (PBS) в качестве контроля или готовой лекарственной формы (объем дозы=приблизительно 0,4 мл/кг) в соответствии со следующей схемой исследования. Максимальная доза в этом исследовании представляет собой максимально возможную дозу на основе максимально достижимой концентрации 20NHS PEG-CBS в препарате и максимального объема дозы, который можно безопасно ввести макакам путем подкожной инъекции на постоянной основе (смотрите Gad et al. Int J Toxicol. 2016 Mar-Apr; 35(2):95-178, который полностью включен таким образом посредством ссылки). Диапазон доз охватывает диапазон предполагаемых терапевтических доз (от 0,5 до 7 мг/кг). Максимальная доза определялась с учетом вязкости препарата для подкожной инъекции, рекомендуемых объемов для постоянных инъекций в случае макак и прогнозируемого времени воздействия на макак по сравнению с людьми. В таблице 17 представлены подробности для групп лечения 1-6.
[0420] Оценка токсичности основывалась на смертности; клинических наблюдениях; весе тела и температуре; кровяном давлении; потреблении качественной пищи; офтальмологических наблюдениях; физикальном, неврологическом и респираторном обследованиях; ЭКГ; и клинической и анатомической патологии. Образцы крови были собраны для анализов метаболитов и активности, анализов комплемента (CH50), ADA и антител против ПЭГ, а также токсикологического анализа.
[0421] Никаких связанных с готовой лекарственной формой изменений интервала PR, продолжительности QRS, интервала QT, скорректированного интервала QT (QTc) или частоты сердечных сокращений не наблюдалось во время фазы введения доз ни у одной из групп. Во время качественной оценки ЭКГ никакие нарушения ритма или качественные изменения ЭКГ не были связаны с готовой лекарственной формой.
[0422] Никаких связанных с готовой лекарственной формой эффектов на клиническую патологию, вес органов, макроскопические данные не наблюдалось ни при одном запланированном умерщвлении. Все животные дожили до запланированного умерщвления. Кроме того, ни для одной из доз не были сделаны связанные с готовой лекарственной формой клинические наблюдения; не отмечалось связанное с готовой лекарственной формой изменение веса тела, набор веса тела или увеличение кровяного давления; или изменение в нейроповеденческих наблюдениях, температуре тела или дыхании.
[0423] Таким образом, учитывая всю базу данных по безопасности 20NHS PEG-CBS, не ожидается, что вакуолизация, связанная с ПЭГ, будет представлять собой риск в исследованиях на людях. Данные по токсикологии повторных доз у яванских макак в сочетании с данными по безопасности на различных моделях CBSDH на мышах после повторного введения доз в течение до 6 месяцев считаются соответствующими и достаточными для обоснования начальной дозы и повышения дозы для человека в клиническом испытании.
[0424] Места подкожных инъекций наблюдали во время описанного выше исследования. Минимальные-незначительные периваскулярные мононуклеарные инфильтраты в одном или более мест подкожных инъекций наблюдались в NHP с инъекцией готовой лекарственной формы в повторной дозе.
Пример 13. Лечение гомоцистинурии у людей
[0425] Для анализа лечения гомоцистинурии у людей будет проводиться двойное слепое рандомизированное плацебо-контролируемое исследование, состоящее из двух частей, на пациентах с генетически подтвержденной CBSDH. Подходящие пациенты будут включены и рандомизированы в соотношении получающих готовую лекарственную форму пациентов/плацебо -3:1. Когорты будут включать пациентов в возрасте от 16 до 65 лет, включительно, с генетическим подтверждением CBSDH и повышенными уровнями tHcy в плазме, превышающими или равными 80 мкМ. Согласно Руководству по диагностике и лечению CBSDH от 2016 г., уровни tHcy должны поддерживаться как можно ближе к норме (на уровне 10-15 мкМ или ниже) и, безусловно, ниже 100 мкМ (смотрите Morris et al. J Inherit Metab Dis. 2017 Jan;40(1):49-74, который полностью включен таким образом посредством ссылки). Критерий включения, относящийся к уровням tHcy, превышающим или равным 80 мкМ, позволяет включить пациентов с типичными уровнями, равными 100 мкМ, признавая ежедневную изменчивость и изменчивость анализа. В качестве альтернативы, уровень tHcy, превышающий или равный 30 мкМ, может использоваться для определения пациента с CBSDH.
[0426] Готовая лекарственная форма будет поставляться в виде 1 мл стерильного раствора лекарственного вещества с концентрацией 25±3 мг/мл, помещенного в одноразовый флакон объемом 2 мл. Лечение будет длиться 12 недель с сигнальным дозированием и будет делиться на период дозирования и период вымывания исследуемого лекарственного средства (готовой лекарственной формы или плацебо).
[0427] Исследуемое лекарственное средство (готовая лекарственная форма или плацебо) будет вводиться с помощью подкожной инъекции. Инъекция будет выполняться в плечи, живот, бедра или ягодицы, как это будет определено лицом, выполняющим инъекцию. Максимальный объем в каждое место инъекции будет составлять 2 мл или в соответствии со стандартными процедурами учреждения.
[0428] Планируется, что три уровня доз будут оцениваться последовательно в трех последовательных когортах. Когорта для каждого уровня дозы будет включать четырех субъектов: три субъекта будут рандомизированы для получения активного лекарственного средства (20NHS PEG-CBS), а один субъект будет рандомизирован для получения плацебо (соотношение рандомизации активный агент/плацебо - 3:1). Исследуемое лекарственное средство будет вводиться подкожно еженедельно. Каждой когорте будут вводить следующие дозы:
Когорте 1: 0,33 мг/кг;
Когорте 2: 0,66 мг/кг; и
Когорте 3: 1,0 мг/кг.
[0429] Период дозирования будет состоять из 6 еженедельных доз исследуемого лекарственного средства с последующим 6-недельным периодом, в течение которого исследуемое лекарственное средство не вводят. Исследование с пролонгированным периодом дозирования, используя приведенный ниже протокол, будет проводиться дольше 12 недель.
[0430] Во время недели 1 в день 1 каждый субъект госпитализируется в клинический центр в качестве стационарного пациента минимум на 24 часа, в течение которых он/она подвергается мониторингу безопасности до и после введения дозы (основных показателей состояния организма, ЭКГ в 12 отведениях), забору крови для лабораторных параметров безопасности, забору крови для фармакокинетических (PK)/фармакодинамических (PD) оценок и уровней антител (только до введения дозы) с последующим первым введением исследуемого лекарственного средства.
[0431] Забор крови для PK/PD оценок и последующий мониторинг безопасности, основных показателей состояния организма, ЭКГ в 12 отведениях, и оценки побочных эффектов (AE) или тяжелых побочных эффектов (SAE), а также забор крови для лабораторных параметров безопасности также будут выполняться, начиная с дня 2. Образцы крови и образцы пятен крови при проколе пальца будут браться перед введением дозы (0 часов), а также через 2, 4, 8, 12 часов (в день 1) и 24 часа (день 2, перед выпиской) после введения исследуемого лекарственного средства в центре. В центре будут проводиться исследовательские оценки tHcy при проколе пальца по DBS и пятен крови на PSD. Также будут проводиться клинические оценки и другие оценки безопасности.
[0432] В день 3 субъект вернется в центр для забора крови или PK/PD оценок (48-часового отбора проб), исследовательских оценок tHcy при проколе пальца по DBS и пятен крови на PSD и последующего мониторинга безопасности - AE или SAE, основных показателей состояния организма, ЭКГ в 12 отведениях, и забора крови для лабораторных параметров безопасности.
[0433] В дни 4, 5, 6 и 7 субъект подвергается осмотрам на дому, проводимым посещающим его квалифицированным медицинским работником для последующего мониторинга безопасности - любых AE или SAE, основных показателей состояния организма, и забора крови для лабораторных параметров безопасности и PK/PD оценок (через 72 [день 4], 96 [день 5], 120 [день 6] и 144 [день 7] часов после введения исследуемого лекарственного средства. При показании в соответствии с каким-либо сигналом/проблемой, связанной с безопасностью, субъект будет проинструктирован осуществить внеплановое посещение центра для полной оценки.
[0434] Во время недель со 2 по 5 каждый субъект будет еженедельно посещать центр для введения исследуемого лекарственного средства, оценок безопасности, иммуногенности (только на неделе 3), отборов проб крови для фармакокинетических/фармакокинетических оценок и исследовательских оценок tHcy при проколе пальца на глубокую стимуляцию головного мозга (DBS) и энергетическую спектральную плотность (PSD) при посещениях 4, 5, 6 и 7.
[0435] Период вымывания будет начинаться в день 36 после завершения периода введения доз исследуемого лекарственного средства. Мониторинг безопасности, а также последовательные фармакокинетические/фармакокинетические оценки будут проводиться в течение этого периода. Каждого субъекта будет еженедельно посещать на дому посещающий его медицинский работник, с последующим одним посещением центра по завершении 6 недель вымывания. Оценки в течение этого периода включают мониторинг безопасности, основных показателей состояния организма, и забор крови для обычных лабораторных анализов, PK, PD и иммуногенности. Исследовательские оценки tHcy в крови при проколе пальца по DBS и пятен крови на PSD будут проводиться в клиническом центре во время последнего визита в период вымывания.
[0436] Что касается безопасности, начальная доза, составляющая 0,33 мг/кг один раз в неделю, в приблизительно 30 раз ниже, чем NOAEL в NHP (т.е. 10 мг/кг каждые 3 дня). Запланированная максимальная доза, составляющая 1,0 мг/кг, в приблизительно 10 раз ниже, чем NOAEL в NHP. Таким образом, диапазон запланированных доз в протоколе обеспечивает большой запас прочности.
[0437] Помимо соображений безопасности, экстраполяция фармакокинетических/фармакокинетических данных от мышей, крыс и NHP показывает, что запланированные дозы и интервалы позволят достичь терапевтически значимых концентраций в плазме пациентов с CBSDH. Фармакологические исследования на мышах показывают, что воздействие приблизительно 50 мЕд./мкл после однократной инъекции было эффективным. Экстраполяции фармакокинетических/фармакокинетических данных от людей показывают, что доза 0,33 мг/кг дважды в неделю или 0,66 мг/кг еженедельно достигнет этого эффективного уровня через 6 недель введения доз. Экстраполированный/прогнозируемый период полувыведения у человека составляет 175 часов или 7,3 дня.
Пример 14. Предварительные результаты клинического исследования фазы ½
[0438] Предварительные результаты продолжающегося исследования фазы 1/2 - обследование пациентов в возрасте от 12 до 65 лет, включительно, с HCU в документально подтвержденном анамнезе, вторичной по отношению к генетическому дефициту CBS, с уровнями общего гомоцистеина (tHcy), превышающими/равными 80 мкМ - (как подробно описано в примере 13), подтверждают эффективность составляющих 1 мг/кг доз 20NHS PEG-CBS, вводимых один или два раза в неделю при воздействии в течение периода до 1 года, до 6 месяцев, до 45 дней или до 1 месяца, как у детей, так и у взрослых в качестве пациентов. Исследования демонстрируют хороший профиль безопасности с низкой угрозой безопасности и низкой иммуногенностью. Например, большинство TEAE (побочных эффектов, возникающих при лечении) были легкими, а некоторые - умеренными. У пациента было зарегистрировано только 1 SAE (значительный побочный эффект); пациент пропустил 1 дозу 20NHS PEG-CBS и возобновил введение доз без проблем.
[0439] Наблюдали умеренную иммуногенность. Наблюдаемые титры антител против лекарственного средства (ADA) были схожими с титрами до введения дозы, за исключением 1 пациента, с максимальным титром=4100. Более того, обнаруженные антитела не являются нейтрализующими на основании результатов фармакокинетического исследования. Наблюдаемые титры антител против ПЭГ были схожими с титрами до введения дозы и также не являются нейтрализующими на основании результатов фармакокинетического исследования. Эти результаты лучше, чем в случае сравнительных ферментотерапий, например, Palynziq, которые показали титры ADA=1000000 через 3 месяца и титры антител против ПЭГ=~10000 через 1 месяц. При других ферментотерапиях обычно наблюдаются титры ≥1000.
[0440] Предварительные результаты демонстрируют среднее снижение до приблизительно 50% от исходных уровней tHcy на неделе 1 и неделе 6 (при дозе 1 мг/кг один или два раза в неделю) в 3 из 4 демаскированных когорт (при этом 1 из 4 когорт получала плацебо-контроль и не получала активную готовую лекарственную форму). Ежедневный отбор образцов в течение недели 1 и недели 6 показал снижение на приблизительно 40-60% уровней tHcy по сравнению с исходными уровнями в 3 из 4 демаскированных когорт (при этом 1 из 4 когорт получала плацебо-контроль и не получала активной готовой лекарственной формы). Наблюдаемая максимальная эффективность (в 1 из 4 демаскированных когорт) приводила к падению уровней tHcy у 2/3 пациентов до приблизительно 50 мкМ с исходных уровней, составляющих от приблизительно 100 мкМ до приблизительно 200 мкМ. Уровни 20NHS PEG-CBS тесно коррелировали со снижениями tHcy для каждого пациента. Усовершенствованные модели предсказывают, что вводимая дважды в неделю доза (1 или 1,5 мг/кг) более чем удвоит наблюдаемую максимальную эффективность и достигнет устойчивых уровней tHcy.
[0441] Результаты демонстрируют, что 20NHS PEG-CBS, вводимая субъектам в соответствии с описанными выше способами, является активным и стабильным в плазме (в отличие от нативного фермента) и резко снижает повышенные уровни tHcy (внутриклеточные и в плазме), независимо от лежащей в основе патологии.
Пример 15. 20NHS PEG-CBS позволяет смягчить рацион и прекратить введение бетаина в модели гомоцистинурии на мыши.
[0442] Доклинические исследования на модели гомоцистинурии на мыши демонстрируют, что длительное непрерывное лечение (например, до 16 недель) с использованием 20NHS PEG-CBS значительно снижает и/или нормализует уровни tHcy независимо от рациона. Как показано на фиг. 3, у мышей НО на стандартном метиониновом рационе («STD») уровни tHcy были повышенными (например, выше 100 мкМ) даже при введении бетаина. Введение 20NHS PEG-CBS резко снижало или нормализовало уровни tHcy даже после отмены бетаина.
[0443] Мышей НО использовали для подсчета ключевых биохимических показателей гомоцистинурии у являющихся людьми субъектов. Как самцов, так и самок мышей HO использовали и содержали, если не указано иное, на стандартном полноценном рационе (STD, полноценный рацион Teklad 2920X, с 5,0 г/кг Met и 3,0 г/кг цистеина). Мышей делили на три группы: A, B и C. Группа A оставалась на STD до недели 10. Группы B и C были помещены на рацион с высоким содержанием Met (HMD, обогащенный Met рацион с заданным аминокислотным составом TD.01084, 8,2 г/кг Met и 3,5 г/кг цистеина) и рацион с ограничением Met (MRD, рацион с ограничением Met и с заданным аминокислотным составом TD.110591, 0,5 г/кг Met и 3,5 г/кг цистеина), соответственно, до недели 10. Три группы содержались на этих рационах в течение первых 2 недель без дополнительных лечений. (Смерти мышей в группе B в течение этого периода потребовали включения в исследование дополнительных мышей для завершения исследования.) Мыши продолжали находиться на указанных рационах, а также получали бетаин (2% (в отношении веса к объему) в питьевой воде) с недели 3 по неделю 5. Мышей, продолжающих находиться на рационах и получающих бетаин, также подвергали лечению 20NHS PEG-CBS (7,5 мг/кг подкожно, 3 раза в неделю), начиная с недели 6. Введение бетаина затем прекращали, начиная с недели 9, тогда как лечение 20NHS PEG-CBS продолжали до конца исследования (недели 16). Смена рациона выполнялась следующим образом: смена № 1 (неделя 11 - неделя 12), группы A, B и C переходили на HMD, MRD и STD, соответственно; смена № 2 (неделя 13 - неделя 14), группы A, B и C переходили на MRD, STD и HMD, соответственно; смена № 3 (неделя 15 - неделя 16), группы A, B и C возвращались обратно на свои исходные рационы, STD, HMD и MRD, соответственно. Кровь собирали 1-3 раза в неделю на протяжении всего исследования, и анализировали уровни в плазме метаболитов, в том числе Hcy, Met и Cys. Образцы крови собирали из поднижнечелюстной вены находящихся в сознании животных с помощью одноразового ланцета, предназначенного для подчелюстного забора образцов, в пробирки с гепарином лития Capiject T-MLHG (Terumo Medical Corporation, Somerset, NJ, США). Плазму собирали из образцов крови после центрифугирования при 1200xg в течение 10 мин и хранили при -80°C в пробирках объемом 1,5 мл. Аминотиолы (общие Cys и Hcy) в плазме и оставшиеся аминокислоты, а также SAM и SAH, измеряли с помощью LC-MS/MS, как описано в Arning and Bottiglieri, Clinical Applications of Mass Spectrometry in Biomolecular Analysis, U. Garg, Editor. 2016, Springer: Seacaucus, NJ. p. 255-262, содержание которого в его полном объеме включено сюда посредством ссылки. Применяли факторный ANOVA (дисперсионный анализ), а затем апостериорный критерий HSD Тьюки. Значения p<0,05 считались статистически значимыми.
[0444] Как показано на фиг. 3, уровни Hcy в плазме резко менялись по сравнению с исходными уровнями (~95-166 мкМ) у мышей на STD-рационе, в соответствии с уровнями Met в соответствующих рационах. Таким образом, после перехода только на MRD-рацион уровни Hcy снижались до ~26-56 мкМ, тогда как HMD-рацион увеличивал уровни Hcy до более чем 400 мкМ. Бетаин нормализовал уровни Hcy (≤16 мкМ) у мышей на MRD-рационе, но был лишь частично эффективным и неэффективным у мышей на HMD- и STD-рационах, соответственно. Это наблюдение поддерживает практику лечения HCU комбинацией бетаина и ограничением Met. У мышей на HMD- или STD-рационе, все еще получающих бетаин, введение 20NHS PEG-CBS резко снижало уровни Hcy до ~22-55 мкМ. Важно отметить, что когда введение бетаина прекращали, но продолжали лечение 20NHS PEG-CBS, эти низкие уровни Hcy оставались стабильными, а уровни у мышей на MRD-рационе оставались нормальными. Кроме того, Hcy в плазме также оставался на этих низких стабильных уровнях при смене рациона, даже когда мышей на MRD-рационе переводили на STD- или HMD-рацион.
[0445] Уровни Met в плазме повышались в приблизительно 2 раза у мышей НО на HMD-рационе и еще больше, вплоть до 7 раз, при добавлении бетаина (не представленные данные). Это, наряду с повышением уровня Hcy, вероятно, вносило вклад в высокую смертность в группе B, особенно в случае самок. Значительно повышенный уровень Met, наблюдаемый в случае введения бетаина у мышей на HMD-рационе, согласовывался с тем фактом, что Met, наряду с диметилглицином (DMG), является продуктом реакции между бетаином и Hcy, катализируемой бетаин-гомоцистеинметилтрансферазой (BHMT). Соответственно, уровни DMG также были самыми высокими в группе B, что согласуется с повышенной доступностью субстрата Hcy для BHMT в этой группе.
[0446] Лечение 20NHS PEG-CBS, при добавлении к введению бетаина, было высокоэффективным в снижении уровней Met в плазме в группе B до значений, сравнимых с таковыми в группах A и C. Снова, эти низкие уровни Met поддерживались лечением 20NHS PEG-CBS, даже после отмены бетаина и последующей смены рациона. Другое интересное наблюдение заключалось в том, что уровни DMG в группе B снижались приблизительно наполовину, когда лечение 20NHS PEG-CBS назначали вместе с бетаином (не представленные данные). Это позволило предположить, что 20NHS PEG-CBS эффективно конкурирует с бетаином за Hcy.
[0447] Хотя уровни Cys в плазме у мышей НО составляют приблизительно половину от уровней у контрольных мышей дикого типа (~200 мкМ), они полностью нормализовались (~226-236 мкМ) у мышей НО на MRD-рационе (не представленные данные). Бетаин сам по себе не изменял уровни Cys ни в одной из групп, но добавление 20NHS PEG-CBS частично приводило к полной нормализации уровней Cys у мышей на HMD-рационе (~152-219 мкМ) и STD-рационе (~156-195 мкМ). Хотя на протяжении всего исследования наблюдались значительные колебания, уровни Cys, нормализованные с помощью 20NHS PEG-CBS, по-видимому, не зависели от исключения бетаина или последующей смены рациона. В соответствии с ее каталитической активностью 20NHS PEG-CBS повышала уровни Cth во всех группах, особенно в группах, начинающихся с STD- или HMD-рациона, что предполагает корреляцию между уровнями Hcy и Cth, хотя и с большими колебаниями (не представленные данные).
[0448] Также следили за отношением S-аденозилметионина (SAM) к S-аденозилгомоцистеину (SAH) (не представленные данные). По сравнению с другими группами отношение SAM/SAH было значительно выше у мышей в группе C, несколько снижаясь при лечении 20NHS PEG-CBS. В группах A и B лечение 20NHS PEG-CBS вызывало умеренное увеличение отношения SAM/SAH. Во время лечения 20NHS PEG-CBS отношение SAM/SAH во всех группах было одинаковым, хотя до смены рациона оно было несколько выше в группе C.
[0449] В целом, в присутствии бетаина лечение 20NHS PEG-CBS значительно снижало уровни Met у мышей HO, которых кормили HMD, и уровни Hcy у мышей, которых кормили HMD или STD. У мышей HO на MRD-рационе одного бетаина было достаточно для нормализации уровня Hcy в плазме. 20NHS PEG-CBS, но не бетаин, нормализовал уровни Cys у мышей на STD- или HMD-рационе. После исключения бетаина одной 20NHS PEG-CBS было достаточно для сохранения этих улучшений метаболизма, даже когда потребление Met менялось путем смены рациона. Это наблюдение, наряду с изменениями уровней DMG, указывало на то, что добавление бетаина не дает дополнительных преимуществ при совместном введении с 20NHS PEG-CBS.
Пример 16. Получение и анализ лиофилизированных препаратов 20NHS PEG-CBS
[0450] Различные препараты 20NHS PEG-CBS тестировали для идентификации составов, которые приводили к (i) уменьшению времени лиофилизации, (ii) уменьшению времени восстановления, (iii) снижению вязкости и/или (iv) уменьшению деПЭГилирования 20NHS PEG-CBS. 20NHS PEG-CBS в концентрации 25,4 мг/мл в 25 мМ фосфате калия, 5% сахарозе при pH 7,5, как описано ниже, использовали для приготовления препаратов, описанных в таблице 18.
[0451] Активные препараты анализировали до лиофилизации (здесь называемые «Т-жидкостью»), а также после лиофилизации (здесь называемые «Т-Lyo» и «Т0» исследования стабильности). Впоследствии лиофилизированный материал помещали на исследование стабильности на срок вплоть до 3 месяцев (T3M) при 5°С, 25°С/60% относительной влажности и 40°С/75% относительной влажности. Стабильность лиофилизированных препаратов также проверяли через один месяц (TIM).
A. Приготовление образца
[0452] За три дня до приготовления препарата 20NHS PEG-CBS (25,4 мг/мл в 25 мМ фосфате калия, 5% сахарозе, pH 7,5) вынимали из морозильной камеры (-80°С) и оттаивали в течение 72 часов в холодильнике при температуре 5°С. После оттаивания 20NHS PEG-CBS в концентрации 25,4 мг/мл в 25 мМ фосфате калия, 5% сахарозе, pH 7,5 гомогенизировали путем осторожного вращения. Препараты получали путем диализа в контролируемых условиях при 5°С в течение 24 часов с использованием кассет для диализа с отсечкой 20 кДа и трех замен буфера при объемном соотношении ≥1:45 каждый раз (3300 мл буфера на замену). Буфер заменяли через 3 и 6 часов общего времени диализа, последнюю стадию диализа проводили в течение ночи. После диализа препараты извлекали из кассет для диализа с последующим анализом рН, осмоляльности и концентрации белка. Было обнаружено, что для всех препаратов концентрация белка находится в пределах спецификаций 20-30 мг/мл. Для препарата F3, описанного в таблице 18, маточный раствор 10% (в отношении веса к объему) полисорбата 80 (PS80) добавляли в диализируемый материал до достижения его конечной концентрации=0,01% (в отношении веса к объему).
B. Лиофилизация
[0453] Лиофилизацию препаратов проводили с использованием лиофилизатора Epsilon 2-12D опытного образца (RND-FD02, Martin Christ, Германия). Перед началом первичной сушки все препараты объединяли в одном лиофилизаторе. Вакуум в процессе лиофилизации контролировали емкостным датчиком. Оптимизированный процесс лиофилизации обобщен в таблице 19. После уравновешивания флаконов до 5°С флаконы замораживали до -45°С и уравновешивали в течение еще 5 часов при -45°С. Температуру полки устанавливали на -15°С на 31 час при первичной сушке. Вторичную сушку проводили при температуре полки 40°С в течение 2,5 часов. В конце процесса лиофилизации камеру аэрировали азотом до 800 мбар, и флаконы закупоривали, поднимая полки. После закупорки камеру аэрировали азотом до атмосферного давления.
C. Восстановление влагосодержания лиофилизированных препаратов
[0454] Лиофилизированные продукты восстанавливали с использованием воды высокой степени очистки. Объем восстановления определяли гравиметрически как потерю веса при лиофилизации. Время восстановления определяли как время до достижения полного восстановления лиофилизированного продукта после добавления жидкости. Поведение при восстановлении оценивали, в основном, по пенообразованию. Было определено время восстановления для всех препаратов на протяжении исследования стабильности. В целом, время восстановления колебалось от 54 секунд до 4,75 минут. Между препаратами не наблюдалось значимых различий во времени восстановления, за исключением препарата F5, для достижения полного восстановления которого требовалось больше времени. Кроме того, все препараты продемонстрировали сопоставимое пенообразование от умеренного до сильного уровня.
D. Анализ лиофилизированных препаратов
[0455] Оценивали внешний вид лиофилизированных препаратов в Т0 исследования стабильности. Принимаемые во внимание параметры включали компактность осадка (кека), контакт со стенками флакона, форму осадка, цвет и общий вид. Все препараты со структурой кека имели хороший внешний вид, будучи плотными и коричневатыми по своей природе. Кроме того, наблюдалась небольшая вертикальная усадка кристаллического осадка. F1, F3 и F6 продемонстрировали несколько незначительных трещин внутри кека, в то время как кеки всех других препаратов оказались неповрежденными. В целом, существенных различий между препаратами не наблюдалось. Внешний вид кека не изменялся после одного месяца исследования стабильности ни при одном из исследуемых условий хранения. Оценка внешнего вида подгруппы препаратов (F1, F3 и F7) через три месяца также не выявила каких-либо изменений внешнего вида.
[0456] Флаконы проверяли на наличие или отсутствие видимых частиц при осторожном ручном круговом перемешивании в течение 5 секунд на белом фоне и в течение 5 секунд на черном фоне в соответствии с Европейской фармакопеей (9-е издание; монография 2.9.20) при 2000-3750 люкс. Было обнаружено, что все препараты не содержат видимых белковых частиц и характеризуются интенсивным окрашиванием. Более того, некоторые образцы были классифицированы как вязкие растворы или проявляли склонность к улавливанию пузырьков воздуха.
[0457] Значение рН препаратов измеряли калиброванным рН-метром (SevenCompact™ SC S210-B, Mettler Toledo AG, Schwerzenbach, Швейцария), используя электрод нормальной ионной силы (InLab™ Micro Pro ISM) для небольших объемов образцов. Анализы рН проводили для всех препаратов до лиофилизации, а также в ходе исследования стабильности. Для всех образцов были измерены значения рН в пределах указанного в спецификации диапазона рН 7,5±0,3.
[0458] Осмоляльность образцов измеряли методом понижения точки замерзания, используя осмометр Gonotec OSMOMAT 3000 (Gonotec GmbH, Германия). Осмоляльность лиофилизированных препаратов сравнивали со значениями осмоляльности 20NHS PEG-CBS (25,4 мг/мл в 25 мМ фосфате калия, 5% сахарозе, pH 7,5). Сопоставимые значения осмоляльности были получены до и после лиофилизации.
[0459] Концентрацию белка во всех препаратах анализировали с помощью УФ-спектроскопии до лиофилизации, а также в ходе исследования стабильности. Все полученные концентрации белка находились в пределах спецификации 20-30 мг/мл. При сравнении концентраций белка до и после лиофилизации для всех препаратов отмечалась разница ≤5%. Следовательно, анализ как концентрации белка, так и осмоляльности указывает на точное определение потери воды во время лиофилизации.
[0460] Измерения вязкости проводили, используя реометр Kinexus ultraplus (Malvern Instruments, Соединенное Королевство (Великобритании и Северной Ирландии)). Определенная вязкость препаратов находилась в диапазоне от ~18 до 27 мПа*с (таблица 25). Не наблюдалось влияние времени хранения или температуры на вязкость. Однако при сравнении препаратов были определены в значительной степени разные вязкости. При сравнении значений вязкости с результатами УФ-спектроскопии была очевидна корреляция вязкости раствора с концентрацией белка.
[0461] Мутность препаратов измеряли, используя нефелометр NEPHLA (Dr. Lange, Германия). В целом, низкая мутность была получена для всех препаратов после приготовления, а также в ходе исследования стабильности. Значимой разницы между препаратами не наблюдалось. Два образца, хранившиеся при 2-8°С (F2 и F4), продемонстрировали большую мутность, чем соответствующие образцы, хранившиеся при 25°С или 40°С. Эти повышенные значения, вероятно, являются артефактом измерения.
[0462] Цвет препаратов в жидкости также оценивали, используя спектральный колориметр (LICO 690 Professional, Соединенное Королевство). Все образцы, независимо от момента времени и состава препарата, были классифицированы как наиболее близкие к R1 по красной шкале.
[0463] Количественную оценку и визуализацию невидимых невооруженным глазом частиц (~1-100 мкм), а также дифференциацию капель силиконового масла и белковых частиц проводили с использованием микропотоковой визуализации (MFI). Были определены концентрации частиц ≥2 мкм, определенные с помощью MFI. В целом, очень низкие концентрации частиц были определены для всех препаратов, условий хранения и моментов времени. Четких тенденций изменений содержания частиц в ходе исследования стабильности выявлено не было.
[0464] Высокоэффективную гель-хроматографию (HP-SEC) проводили после приготовления препаратов, а также во все моменты времени определения стабильности после восстановления лиофилизированных образцов. В целом, все образцы продемонстрировали высокое содержание PEG-CBS и отсутствие увеличения содержания неПЭГилированной молекулы на протяжении всего исследования стабильности.
[0465] Для всех образцов также выполняли высокоэффективную жидкостную хроматографию с обращенной фазой. На хроматограмме были идентифицированы десять различимых пиков, которые были названы от пика 1 до пика 10 с увеличением времени удержания. Здесь наблюдалось уменьшение относительных площадей пиков 6-9 и увеличение относительных площадей пиков 1-4.
[0466] Поведение замороженных препаратов в вакууме анализировали с помощью микроскопического исследования лиофилизации (FDSC 196, Resultec, Германия). Измерения в ходе микроскопического исследования лиофилизации (FDM) проводили для Т-жидкости (препарата перед лиофилизацией) для того, чтобы отрегулировать параметры процесса лиофилизации в соответствии с температурами начала распада (Tc, on). Определенные значения Tc, on находились в диапазоне от -22°С до -14°С. Таким образом, ни один из препаратов не продемонстрировал распад при температурах выше -25°С, соответствующих заданной температуре полок во время первичной сушки цикла лиофилизации.
[0467] В заключение, семь препаратов были проверены в отношении времени их восстановления, вязкости, а также стабильности после хранения при 2-8°С, 25°С и 40°С в течение до трех месяцев. Что касается времени восстановления кека и вязкости образца, не было замечено существенных различий ни между препаратами, ни между моментами времени анализа. Для кеков продукта F5 было определено значительно большее время восстановления по сравнению с другими кандидатами. Все образцы, хранившиеся при температуре 2-8°С или 25°С, продемонстрировали в целом хорошую стабильность. Однако в условиях хранения при 40°С были выявлены некоторые различия между препаратами. Например, анализ с помощью HP-SEC показал снижение относительного содержания PEG-CBS в случае препаратов F2, F4 и F6 в сочетании с повышением относительного содержания пика 1 после хранения в течение одного месяца. Анализ с помощью RP-HPLC (ОФ-ВЭЖХ) показал уменьшение относительных площадей пиков 6-9, сопровождающееся увеличением относительных площадей пиков 1-4 препаратов F2 и F5. Таким образом, образцы, подвергшиеся стадии модификации во время замораживания, в целом оказались менее стабильными, чем образцы без стадии модификации во время замораживания.
[0468] Среди протестированных препаратов препараты F1, F3 и F7 продемонстрировали очень высокую стабильность во всех условиях хранения (за некоторыми исключениями). В итоге, препараты F1, F3 и F7 показали сравнительно хорошие результаты среди них и во всех моментах времени анализа.
Пример 17. Анализ и оптимизация параметров процесса лиофилизации
[0469] Описанный в примере 16 препарат F1, состоящий из 15 мМ фосфата калия, 8% трегалозы, pH 7,5, использовали для оптимизации процесса лиофилизации. Ожидаемые результаты оптимизированной лиофилизации включают (i) сокращение времени цикла лиофилизации без расплавления кека, (ii) сокращение времени восстановления и (iii) уменьшение де-ПЭГилирования 20NHS PEG-CBS.
[0470] Оптимизацию процесса лиофилизации проводили в ходе трех последовательных циклов лиофилизации при различных параметрах процесса. В частности, (i) время первичной сушки (PD), (ii) температура PD и (iii) время вторичной сушки (SD) варьировались между циклами. Целью цикла 1 была оптимизация параметров первичной сушки, в то время как в цикле 2 основное внимание уделялось характеристике вторичной сушки, а цикл 3 был нацелен на сокращение времени процесса до менее 48 часов.
[0471] Три последовательных цикла лиофилизации выполняли в лиофилизаторе Epsilon 2-12D опытного образца. Давление в камере контролировали с помощью емкостного датчика и регулировали вакуумным насосом и регулируемой дозировкой азота.
сек)
(°C)
мин)
[0472] Лиофилизированные препараты, полученные в результате оптимизированного процесса лиофилизации, оценивали с помощью аналитических методов, описанных здесь.
[0473] Лиофилизированные осадки после сушки подвергали визуальной оценке. Принимаемые во внимание параметры включали компактность осадка, контакт со стенками флакона, форму осадка, цвет и общий вид. Анализ лиофилизированных образцов показал хороший внешний вид с плотной структурой и коричневатой окраской.
[0474] Содержание воды в лиофилизированных осадках определяли с использованием кулонометрического титратора Карла Фишера Aqua 40.00 (Analytik Jena GmbH). Отмечали низкое остаточное содержание влаги во всех образцах.
[0475] Дифференциальную сканирующую калориметрию (DSC) на приборе Mettler Toledo DSC1_943 (Mettler Toledo, Германия) проводили для измерения температуры стеклования (Tg), кристаллизации и эндотермического плавления лиофилизированных продуктов. В целом, результаты варьировались от 111°C до 117°C, что указывает на стабильные результирующие осадки. Перед анализом с помощью визуального осмотра, определения мутности, УФ-спектроскопии, HP-SEC и RP-HPLC (ОФ-ВЭЖХ) лиофилизированное содержимое флаконов восстанавливали. Для восстановления содержимого флаконов использовали воду. Наблюдаемое время восстановления было коротким и сравнимым, в пределах от ~1 до ~1,5 минут. После восстановления лиофилизированный продукт продемонстрировал умеренное-сильное пенообразование.
[0476] Визуальный осмотр проводили на наличие или отсутствие видимых частиц при осторожном ручном круговом перемешивании в течение 5 секунд на белом фоне и в течение 5 секунд на черном фоне в соответствии с Европейской фармакопеей (9-е издание; монография 2.9.20) при 2000-3750 люкс. Осмотр проводился независимо двумя обученными экспертами. Ни в одном из проанализированных образцов, независимо от условий процесса, не было обнаружено видимых частиц. Все растворы оказались окрашенными и вязкими. Кроме того, после восстановления в некоторых случаях были обнаружены пузырьки воздуха.
[0477] Для измерений мутности использовали нефелометр NEPHLA (Dr. Lange, Düsseldorf, Германия), работающий на длине волны 860 нм и регистрирующий под углом 90°. Очень низкие мутности были получены для всех образцов на протяжении всего исследования. Изменение различных технологических параметров циклов оптимизации не повлияло на мутность препарата.
[0478] УФ-спектроскопию выполняли с использованием прибора C Technologies SoloVPE. Все концентрации белка находились в пределах спецификаций 20-30 мг/мл. Для большинства измерений наблюдалась небольшая тенденция к более высокой концентрации белка после лиофилизации и восстановления (T-Lyo) по сравнению с T-Liquid. Более высокое поглощение в случае образцов T-Lyo всех трех циклов могло быть результатом рассеяния света, например, вызванного пузырьками воздуха, которые также наблюдались при визуальном осмотре.
[0479] На протяжении всего исследования были определены сопоставимые профили HP-SEC с высоким содержанием PEG-CBS от 93 до 95%. Ни в одном из образцов не было обнаружено деПЭГилированной CBS. Следовательно, измененные параметры процесса лиофилизации не повлияли на ПЭГилирование образцов и не привели к образованию новых форм, обнаруживаемых с помощью HP-SEC. В соответствии с профилями HP-SEC измененные условия процесса лиофилизации также не оказали влияния на картину ПЭГилирования.
[0480] Концентрацию белка определяли, используя GPBT1198 с длиной волны 280 нм. Содержание свободного ПЭГ определяли с помощью RP-HPLC GPBT3078. Не наблюдалось явных изменений концентрации белка в образцах до и после лиофилизации, а также между образцами из флаконов, находящихся в центральных и краевых положениях. При сравнении образцов до и после лиофилизации существенных изменений содержания свободного ПЭГ и активности не выявлено. Таким образом, оптимизированные параметры цикла лиофилизации не оказали отрицательного влияния на анализируемые показатели качества продукта.
[0481] В заключение, процесс лиофилизации был успешно оптимизирован путем регулирования параметров замораживания, PD и SD. Оптимизированный процесс характеризуется существенно сокращенным временем цикла ≤48 часов. Ни один из примененных способов анализа твердого или жидкого состояния не показал нанесение процессом оптимизации ущерба качеству продукта. Кроме того, сравнение краевых и центральных положений флаконов в цикле 3 показало, что продукт устойчив к неравномерности температур продуктов в партии во время PD.
Пример 18. Оценка параметров последующего процесса очистки
[0482] Альтернативные последующие процессы очистки фермента цистатионин-β-синтазы (CBS) выполняли в крупном масштабе с целью повышения выхода и извлечения из существующего процесса. Биомассу получали с помощью периодической ферментации с подпиткой (ферментации с высокой плотностью клеток) в минимальной среде в масштабе 10 л. При сборе биомассу отделяли от среды с помощью центрифугирования, ресуспендировали в буфере для лизиса и разрушали посредством гомогенизации под высоким давлением. После отделения клеточного экстракта от клеточного дебриса с помощью центрифугирования супернатант, содержащий CBS, осветляли с помощью ряда глубинных фильтраций, а затем использовали в качестве исходного материала для последующего ряда хроматографий, включающего (i) анионообменную хроматографию (AEX) в качестве стадии захвата, используя HiTrap DEAE Sepharose FF (GE), (ii) аффинную хроматографию с иммобилизованным металлом (IMAC) (с заряженной Zn2+ средой) в качестве промежуточной стадии с использованием Chelating Sepharose FF (GE) и (iii) хроматографию на основе гидрофобного взаимодействия (HIC) в качестве стадии доочистки с использованием Butyl-S Sepharose 6 FF (GE). После диафильтрации с использованием фильтрации поперечным потоком (TFF) очищенной CBS проводили ПЭГилирование. Для составления ПЭГилированную CBS подвергали диафильтрации и снова концентрировали с помощью TFF. В альтернативных процессах использовали осаждение с использованием PEI (0,35%) клеточного лизата, замену буферной системы с фосфатной на HEPES и замену Triton X-100 на Tween™20.
А. Ферментация
[0483] Для получения биомассы, необходимой для оптимизации и масштабирования процесса очистки, были проведены две последовательные 10-литровые периодические ферментации с подпиткой в минимальной среде. Для всех циклов масштабирования использовали биомассу, полученную в ферментере 2 (объем сбора: 9,2 л; биомасса: 1791 г).
B. Увеличение масштаба последующего процесса очистки
[0484] Процесс очистки 1 включал одну или более из следующих стадий: (i) сбор клеток, (ii) ресуспендирование клеток, (iii) разрушение клеток, (iv) осаждение с использованием полиэтиленимина (PEI), (v) центрифугирование, (vi) стерилизацию фильтрованием, (vii) захват с использованием DEAE Sepharose FF с третьей стадией промывки для замены фосфатного буфера обратно на HEPES, (viii) промежуточную стадию с использованием Chelating Sepharose FF, заряженной ионами цинка, (ix) стадию доочистки с использованием Butyl-S Sepharose 6 FF, (x) TFF, (xi) ПЭГилирование.
[0485] Процесс очистки 2 включал одну или более из следующих стадий: (i) сбор клеток, (ii) ресуспендирование клеток, (iii) разрушение клеток, (iv) центрифугирование, (v) глубинную фильтрацию, (vi) стерилизацию фильтрованием, (vii) захват с использованием DEAE Sepharose FF, (viii) промежуточную стадию с использованием Chelating Sepharose FF, заряженной ионами цинка, (ix) стадию доочистки с использованием Butyl-S Sepharose 6 FF со второй стадией промывки, включенной для замены HEPES-буфера обратно на фосфатный буфер, и стадией разведения, включенной во избежание осаждения CBS, (x) TFF, (xi) ПЭГилирование.
C. Стадия захвата
[0486] После разрушения клеток посредством гомогенизации под высоким давлением проводили осаждение с использованием PEI с последующей стерильной фильтрацией. Общее извлечение CBS на стадии захвата составило 58,1% (5,4 г CBS; 2,5 г/л CBS). Общее содержание белка в элюированном пуле захвата составило 7,5 г. Извлечение CBS и выход процесса очистки 2a были подтверждены (извлечение 85,1%; 5,4 г CBS; 2,6 г/л CBS) и выше, чем в процессе очистки 1 (извлечение 47,7%; 5,3 г CBS; 1,03 г/л CBS). В целом, осаждение с использованием PEI и повторная замена буфера в колонке не оказали очевидных негативных эффектов на выход.
D. Промежуточная стадия
[0487] Элюированный пул захвата хранили в течение ночи при температуре от 4°C до 8°C и дополнительно обрабатывали в день 2 процесса на промежуточной стадии с использованием Chelating Sepharose FF, заряженной ионами цинка.
E. Стадия доочистки
[0488] Промежуточный элюированный пул разводили 20 мМ буфером HEPES для получения концентрации CBS, составляющей приблизительно 1,6 г/л. Впоследствии добавляли 10 мМ EDTA для хранения в течение ночи при температуре от 4°C до 8°C. В день 3 процесса перед загрузкой в колонку для доочистки добавляли сульфат аммония (конечная концентрация: 1,4 М).
[0489] В проточном потоке не был определен сигнал поглощения, т.е. не было белка и не было вымывания CBS. Определяли профиль элюирования в процессе очистки.
[0490] Процесс очистки давал степень извлечения CBS=92,9% или выше. Из-за предварительного разведения промежуточного элюированного пула не было эффекта концентрирования, и не наблюдалось осаждение CBS на колонке для доочистки, что приводило к увеличению извлечения на приблизительно 8%. Общее извлечение CBS составило 38,7% или более для всех проверенных процессов очистки. Элюированный пул подвергали диафильтрации против буфера для ПЭГилирования и концентрировали до 40 г/л CBS с помощью TFF (Vivaflow 200, 50 кДа, PES). С TFF-ретентатом был проведен всесторонний анализ для определения качества CBS.
F. ПЭГилирование
[0491] Небольшой объем (1 мл) TFF-ретентата ПЭГилировали в небольшом масштабе и анализировали с помощью электрофореза в SDS-ПААГ, HPLC (SE-, RP- и AEX-) и IEF и сравнивали с эталонным стандартом PEG-CBS. Кинетику ПЭГилирования контролировали с помощью SE-HPLC (одно измерение каждые четыре-пять часов) и определяли относительное время удержания=tR (PEG-CBS)/tR(CBS) x 100%, где tR представляет собой время удержания соответствующих форм. Если относительное время удержания (представленное как целое число) превышало 85%, это указывало на необходимость добавления дополнительного количества ПЭГ. Относительное время удержания через 4,3 часа составило 82,4%, т.е. ниже порогового значения=85%. Поэтому никакого дополнительного ПЭГ не добавляли. После 24-часового ПЭГилирования относительное время удержания составило 82,8%.
Эквиваленты и объем
[0492] Специалисты в данной области техники осознают или смогут установить, используя не более чем обычные эксперименты, множество эквивалентов конкретных вариантов осуществления в соответствии с описанным здесь изобретением. Объем настоящего изобретения, как предполагается, не ограничивается вышеприведенным описанием, а вернее изложен в прилагаемой формуле изобретения.
[0493] В формуле изобретения такие артикли, как «a», «an» и «the», могут означать один или более чем один, если не указано иное или иным образом не следует из контекста. Формула изобретения или описания, которые включают «или» между одним или более членов группы, считаются соответствующими, если один, более чем один или все члены группы присутствуют, используются или иным образом имеют отношение к данному продукту или процессу, если не указано иное или иным образом следует из контекста. Описание включает варианты осуществления, в которых ровно один член группы присутствует, используется или иным образом имеет отношение к данному продукту или процессу. Описание включает варианты осуществления, в которых более одного члена или вся группа членов присутствует, используется или иным образом имеет отношение к данному продукту или процессу.
[0494] Также отмечается, что термин «содержащий (включающий)» является открытым и допускает, но не требует включения(е) дополнительных элементов или стадий. Когда термин «содержащий» используется здесь, термин «состоящий из» также охватывается и раскрывается.
[0495] Там, где даны диапазоны, включены конечные точки. Кроме того, следует понимать, что, если не указано иное или иное не следует из контекста и понимания специалиста со средним уровнем компетентности в данной области техники, значения, представленные в виде диапазонов, могут принимать любое конкретное значение или поддиапазон в пределах указанных диапазонов в различных вариантах осуществления настоящего изобретения, до десятых долей нижнего предела диапазона, если из контекста явно не следует иное.
[0496] Кроме того, следует понимать, что любой конкретный вариант осуществления настоящего изобретения, относящийся к известному уровню техники, может быть явно исключен из любого одного или более пунктов формулы изобретения. Поскольку считается, что такие варианты осуществления известны специалисту со средним уровнем компетентности в данной области техники, они могут быть исключены, даже если исключение в явной форме здесь не указано. Любой конкретный вариант осуществления композиций по настоящему изобретению (например, любой антибиотик, терапевтический или активный ингредиент, любой способ производства, любой способ применения и т.д.) может быть исключен из любого одного или более пунктов формулы изобретения по любой причине, независимо от того, связан ли он с существованием предшествующего уровня техники.
[0497] Следует понимать, что слова, которые были использованы, являются словами описания, а не ограничения, и что изменения могут быть внесены в рамках прилагаемой формулы изобретения без отклонения от истинного объема и сущности настоящего изобретения в его более широких аспектах.
[0498] Хотя настоящее изобретение было описано достаточно подробно и с некоторыми подробностями в отношении нескольких описанных вариантов осуществления, не предполагается, что оно должно ограничиваться какими-либо такими подробностями или вариантами осуществления или каким-либо конкретным вариантом осуществления, но оно должно толковаться со ссылками на прилагаемую формулу изобретения, чтобы обеспечить самое широкое из возможных толкований такой формулы изобретения с учетом предшествующего уровня техники и, следовательно, чтобы эффективно охватить предполагаемый объем настоящего изобретения.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ТРАВИР ТЕРАПЬЮТИКС СВИТЗЕРЛЭНД ГМБХ
ДЗЕ РИДЖЕНТС ОФ ДЗЕ ЮНИВЕРСИТИ ОФ КОЛОРАДО, Э БОДИ КОРПОРЕЙТ
<120> ГОТОВАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ФЕРМЕНТОТЕРАПИИ ДЛЯ ЛЕЧЕНИЯ ГОМОЦИСТИНУРИИ
<130> 2089.1005PCT
<140> PCT/USXXXX/XXXXXX
<141> 2020-06-26
<150> 62/983,860
<151> 2020-03-02
<150> 62/866,810
<151> 2019-06-26
<160> 5
<170> Патент в версии 3.5
<210> 1
<211> 412
<212> Белок
<213> Homo sapiens
<400> 1
Pro Ser Glu Thr Pro Gln Ala Glu Val Gly Pro Thr Gly Ser Pro His
1 5 10 15
Arg Ser Gly Pro His Ser Ala Lys Gly Ser Leu Glu Lys Gly Ser Pro
20 25 30
Glu Asp Lys Glu Ala Lys Glu Pro Leu Trp Ile Arg Pro Asp Ala Pro
35 40 45
Ser Arg Cys Thr Trp Gln Leu Gly Arg Pro Ala Ser Glu Ser Pro His
50 55 60
His His Thr Ala Pro Ala Lys Ser Pro Lys Ile Leu Pro Asp Ile Leu
65 70 75 80
Lys Lys Ile Gly Asp Thr Pro Met Val Arg Ile Asn Lys Ile Gly Lys
85 90 95
Lys Phe Gly Leu Lys Cys Glu Leu Leu Ala Lys Cys Glu Phe Phe Asn
100 105 110
Ala Gly Gly Ser Val Lys Asp Arg Ile Ser Leu Arg Met Ile Glu Asp
115 120 125
Ala Glu Arg Asp Gly Thr Leu Lys Pro Gly Asp Thr Ile Ile Glu Pro
130 135 140
Thr Ser Gly Asn Thr Gly Ile Gly Leu Ala Leu Ala Ala Ala Val Arg
145 150 155 160
Gly Tyr Arg Cys Ile Ile Val Met Pro Glu Lys Met Ser Ser Glu Lys
165 170 175
Val Asp Val Leu Arg Ala Leu Gly Ala Glu Ile Val Arg Thr Pro Thr
180 185 190
Asn Ala Arg Phe Asp Ser Pro Glu Ser His Val Gly Val Ala Trp Arg
195 200 205
Leu Lys Asn Glu Ile Pro Asn Ser His Ile Leu Asp Gln Tyr Arg Asn
210 215 220
Ala Ser Asn Pro Leu Ala His Tyr Asp Thr Thr Ala Asp Glu Ile Leu
225 230 235 240
Gln Gln Cys Asp Gly Lys Leu Asp Met Leu Val Ala Ser Val Gly Thr
245 250 255
Gly Gly Thr Ile Thr Gly Ile Ala Arg Lys Leu Lys Glu Lys Cys Pro
260 265 270
Gly Cys Arg Ile Ile Gly Val Asp Pro Glu Gly Ser Ile Leu Ala Glu
275 280 285
Pro Glu Glu Leu Asn Gln Thr Glu Gln Thr Thr Tyr Glu Val Glu Gly
290 295 300
Ile Gly Tyr Asp Phe Ile Pro Thr Val Leu Asp Arg Thr Val Val Asp
305 310 315 320
Lys Trp Phe Lys Ser Asn Asp Glu Glu Ala Phe Thr Phe Ala Arg Met
325 330 335
Leu Ile Ala Gln Glu Gly Leu Leu Cys Gly Gly Ser Ala Gly Ser Thr
340 345 350
Val Ala Val Ala Val Lys Ala Ala Gln Glu Leu Gln Glu Gly Gln Arg
355 360 365
Cys Val Val Ile Leu Pro Asp Ser Val Arg Asn Tyr Met Thr Lys Phe
370 375 380
Leu Ser Asp Arg Trp Met Leu Gln Lys Gly Phe Leu Lys Glu Glu Asp
385 390 395 400
Leu Thr Glu Lys Lys Pro Trp Trp Trp His Leu Arg
405 410
<210> 2
<211> 551
<212> Белок
<213> Homo sapiens
<400> 2
Met Pro Ser Glu Thr Pro Gln Ala Glu Val Gly Pro Thr Gly Cys Pro
1 5 10 15
His Arg Ser Gly Pro His Ser Ala Lys Gly Ser Leu Glu Lys Gly Ser
20 25 30
Pro Glu Asp Lys Glu Ala Lys Glu Pro Leu Trp Ile Arg Pro Asp Ala
35 40 45
Pro Ser Arg Cys Thr Trp Gln Leu Gly Arg Pro Ala Ser Glu Ser Pro
50 55 60
His His His Thr Ala Pro Ala Lys Ser Pro Lys Ile Leu Pro Asp Ile
65 70 75 80
Leu Lys Lys Ile Gly Asp Thr Pro Met Val Arg Ile Asn Lys Ile Gly
85 90 95
Lys Lys Phe Gly Leu Lys Cys Glu Leu Leu Ala Lys Cys Glu Phe Phe
100 105 110
Asn Ala Gly Gly Ser Val Lys Asp Arg Ile Ser Leu Arg Met Ile Glu
115 120 125
Asp Ala Glu Arg Asp Gly Thr Leu Lys Pro Gly Asp Thr Ile Ile Glu
130 135 140
Pro Thr Ser Gly Asn Thr Gly Ile Gly Leu Ala Leu Ala Ala Ala Val
145 150 155 160
Arg Gly Tyr Arg Cys Ile Ile Val Met Pro Glu Lys Met Ser Ser Glu
165 170 175
Lys Val Asp Val Leu Arg Ala Leu Gly Ala Glu Ile Val Arg Thr Pro
180 185 190
Thr Asn Ala Arg Phe Asp Ser Pro Glu Ser His Val Gly Val Ala Trp
195 200 205
Arg Leu Lys Asn Glu Ile Pro Asn Ser His Ile Leu Asp Gln Tyr Arg
210 215 220
Asn Ala Ser Asn Pro Leu Ala His Tyr Asp Thr Thr Ala Asp Glu Ile
225 230 235 240
Leu Gln Gln Cys Asp Gly Lys Leu Asp Met Leu Val Ala Ser Val Gly
245 250 255
Thr Gly Gly Thr Ile Thr Gly Ile Ala Arg Lys Leu Lys Glu Lys Cys
260 265 270
Pro Gly Cys Arg Ile Ile Gly Val Asp Pro Glu Gly Ser Ile Leu Ala
275 280 285
Glu Pro Glu Glu Leu Asn Gln Thr Glu Gln Thr Thr Tyr Glu Val Glu
290 295 300
Gly Ile Gly Tyr Asp Phe Ile Pro Thr Val Leu Asp Arg Thr Val Val
305 310 315 320
Asp Lys Trp Phe Lys Ser Asn Asp Glu Glu Ala Phe Thr Phe Ala Arg
325 330 335
Met Leu Ile Ala Gln Glu Gly Leu Leu Cys Gly Gly Ser Ala Gly Ser
340 345 350
Thr Val Ala Val Ala Val Lys Ala Ala Gln Glu Leu Gln Glu Gly Gln
355 360 365
Arg Cys Val Val Ile Leu Pro Asp Ser Val Arg Asn Tyr Met Thr Lys
370 375 380
Phe Leu Ser Asp Arg Trp Met Leu Gln Lys Gly Phe Leu Lys Glu Glu
385 390 395 400
Asp Leu Thr Glu Lys Lys Pro Trp Trp Trp His Leu Arg Val Gln Glu
405 410 415
Leu Gly Leu Ser Ala Pro Leu Thr Val Leu Pro Thr Ile Thr Cys Gly
420 425 430
His Thr Ile Glu Ile Leu Arg Glu Lys Gly Phe Asp Gln Ala Pro Val
435 440 445
Val Asp Glu Ala Gly Val Ile Leu Gly Met Val Thr Leu Gly Asn Met
450 455 460
Leu Ser Ser Leu Leu Ala Gly Lys Val Gln Pro Ser Asp Gln Val Gly
465 470 475 480
Lys Val Ile Tyr Lys Gln Phe Lys Gln Ile Arg Leu Thr Asp Thr Leu
485 490 495
Gly Arg Leu Ser His Ile Leu Glu Met Asp His Phe Ala Leu Val Val
500 505 510
His Glu Gln Ile Gln Tyr His Ser Thr Gly Lys Ser Ser Gln Arg Gln
515 520 525
Met Val Phe Gly Val Val Thr Ala Ile Asp Leu Leu Asn Phe Val Ala
530 535 540
Ala Gln Glu Arg Asp Gln Lys
545 550
<210> 3
<211> 1656
<212> ДНК
<213> Homo sapiens
<400> 3
atgccgtcag aaaccccgca ggcagaagtg ggtccgacgg gttgcccgca ccgtagcggt 60
ccgcattctg caaaaggcag tctggaaaaa ggttccccgg aagataaaga agccaaagaa 120
ccgctgtgga ttcgtccgga cgcaccgtca cgctgtacct ggcagctggg tcgtccggca 180
agcgaatctc cgcatcacca tacggctccg gcgaaaagtc cgaaaattct gccggatatc 240
ctgaagaaaa ttggtgacac cccgatggtt cgtatcaaca aaatcggcaa aaaattcggt 300
ctgaaatgcg aactgctggc taaatgtgaa tttttcaatg cgggcggttc cgtgaaagat 360
cgtatctcac tgcgcatgat tgaagatgct gaacgcgacg gcaccctgaa accgggtgat 420
acgattatcg aaccgacctc tggcaacacg ggtatcggtc tggcactggc ggcggcagtc 480
cgtggttatc gctgcattat cgtgatgccg gaaaaaatga gctctgaaaa agttgatgtc 540
ctgcgtgctc tgggcgcgga aattgttcgt accccgacga atgcccgctt cgacagtccg 600
gaatcccatg tgggtgttgc atggcgcctg aaaaacgaaa tcccgaattc gcacattctg 660
gatcagtatc gtaacgctag caatccgctg gcgcattacg ataccacggc cgacgaaatc 720
ctgcagcaat gtgatggcaa actggacatg ctggtcgctt ctgtgggtac cggcggtacc 780
attacgggca tcgcgcgtaa actgaaagaa aaatgcccgg gctgtcgcat tatcggtgtg 840
gatccggaag gcagtattct ggcggaaccg gaagaactga accagaccga acaaaccacg 900
tatgaagttg aaggcatcgg ttacgatttt attccgaccg tcctggatcg cacggtggtt 960
gacaaatggt tcaaaagcaa tgacgaagaa gcctttacct tcgcacgtat gctgatcgct 1020
caggaaggtc tgctgtgcgg tggttcagca ggttcgacgg tcgcagtggc agttaaagct 1080
gcgcaggaac tgcaagaagg tcaacgttgt gtcgtgattc tgccggattc tgttcgcaac 1140
tacatgacca aatttctgag tgaccgttgg atgctgcaaa aaggcttcct gaaagaagaa 1200
gatctgaccg agaaaaaacc gtggtggtgg cacctgcgcg tgcaggaact gggtctgtcc 1260
gcaccgctga ccgttctgcc gaccatcacg tgcggccata cgattgaaat cctgcgtgaa 1320
aaaggttttg atcaggcccc ggttgtcgac gaagcaggcg tgattctggg tatggttacc 1380
ctgggtaaca tgctgagttc cctgctggcg ggcaaagtgc aaccgagcga tcaggttggt 1440
aaagtcatct acaaacaatt caaacagatt cgtctgaccg atacgctggg ccgcctgtcg 1500
cacatcctgg aaatggacca tttcgcgctg gttgtgcacg aacagattca ataccatagc 1560
accggcaaat catcgcagcg ccaaatggtc tttggtgtcg tgacggccat tgatctgctg 1620
aatttcgtgg ccgcacaaga acgtgaccag aaataa 1656
<210> 4
<211> 413
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический полипептид
<400> 4
Met Pro Ser Glu Thr Pro Gln Ala Glu Val Gly Pro Thr Gly Cys Pro
1 5 10 15
His Arg Ser Gly Pro His Ser Ala Lys Gly Ser Leu Glu Lys Gly Ser
20 25 30
Pro Glu Asp Lys Glu Ala Lys Glu Pro Leu Trp Ile Arg Pro Asp Ala
35 40 45
Pro Ser Arg Cys Thr Trp Gln Leu Gly Arg Pro Ala Ser Glu Ser Pro
50 55 60
His His His Thr Ala Pro Ala Lys Ser Pro Lys Ile Leu Pro Asp Ile
65 70 75 80
Leu Lys Lys Ile Gly Asp Thr Pro Met Val Arg Ile Asn Lys Ile Gly
85 90 95
Lys Lys Phe Gly Leu Lys Cys Glu Leu Leu Ala Lys Cys Glu Phe Phe
100 105 110
Asn Ala Gly Gly Ser Val Lys Asp Arg Ile Ser Leu Arg Met Ile Glu
115 120 125
Asp Ala Glu Arg Asp Gly Thr Leu Lys Pro Gly Asp Thr Ile Ile Glu
130 135 140
Pro Thr Ser Gly Asn Thr Gly Ile Gly Leu Ala Leu Ala Ala Ala Val
145 150 155 160
Arg Gly Tyr Arg Cys Ile Ile Val Met Pro Glu Lys Met Ser Ser Glu
165 170 175
Lys Val Asp Val Leu Arg Ala Leu Gly Ala Glu Ile Val Arg Thr Pro
180 185 190
Thr Asn Ala Arg Phe Asp Ser Pro Glu Ser His Val Gly Val Ala Trp
195 200 205
Arg Leu Lys Asn Glu Ile Pro Asn Ser His Ile Leu Asp Gln Tyr Arg
210 215 220
Asn Ala Ser Asn Pro Leu Ala His Tyr Asp Thr Thr Ala Asp Glu Ile
225 230 235 240
Leu Gln Gln Cys Asp Gly Lys Leu Asp Met Leu Val Ala Ser Val Gly
245 250 255
Thr Gly Gly Thr Ile Thr Gly Ile Ala Arg Lys Leu Lys Glu Lys Cys
260 265 270
Pro Gly Cys Arg Ile Ile Gly Val Asp Pro Glu Gly Ser Ile Leu Ala
275 280 285
Glu Pro Glu Glu Leu Asn Gln Thr Glu Gln Thr Thr Tyr Glu Val Glu
290 295 300
Gly Ile Gly Tyr Asp Phe Ile Pro Thr Val Leu Asp Arg Thr Val Val
305 310 315 320
Asp Lys Trp Phe Lys Ser Asn Asp Glu Glu Ala Phe Thr Phe Ala Arg
325 330 335
Met Leu Ile Ala Gln Glu Gly Leu Leu Cys Gly Gly Ser Ala Gly Ser
340 345 350
Thr Val Ala Val Ala Val Lys Ala Ala Gln Glu Leu Gln Glu Gly Gln
355 360 365
Arg Cys Val Val Ile Leu Pro Asp Ser Val Arg Asn Tyr Met Thr Lys
370 375 380
Phe Leu Ser Asp Arg Trp Met Leu Gln Lys Gly Phe Leu Lys Glu Glu
385 390 395 400
Asp Leu Thr Glu Lys Lys Pro Trp Trp Trp His Leu Arg
405 410
<210> 5
<211> 413
<212> Белок
<213> Искусственная последовательность
<220>
<223> Описание искусственной последовательности: синтетический
полипептид усеченной C15S-мутантной CBS человека
<400> 5
Met Pro Ser Glu Thr Pro Gln Ala Glu Val Gly Pro Thr Gly Ser Pro
1 5 10 15
His Arg Ser Gly Pro His Ser Ala Lys Gly Ser Leu Glu Lys Gly Ser
20 25 30
Pro Glu Asp Lys Glu Ala Lys Glu Pro Leu Trp Ile Arg Pro Asp Ala
35 40 45
Pro Ser Arg Cys Thr Trp Gln Leu Gly Arg Pro Ala Ser Glu Ser Pro
50 55 60
His His His Thr Ala Pro Ala Lys Ser Pro Lys Ile Leu Pro Asp Ile
65 70 75 80
Leu Lys Lys Ile Gly Asp Thr Pro Met Val Arg Ile Asn Lys Ile Gly
85 90 95
Lys Lys Phe Gly Leu Lys Cys Glu Leu Leu Ala Lys Cys Glu Phe Phe
100 105 110
Asn Ala Gly Gly Ser Val Lys Asp Arg Ile Ser Leu Arg Met Ile Glu
115 120 125
Asp Ala Glu Arg Asp Gly Thr Leu Lys Pro Gly Asp Thr Ile Ile Glu
130 135 140
Pro Thr Ser Gly Asn Thr Gly Ile Gly Leu Ala Leu Ala Ala Ala Val
145 150 155 160
Arg Gly Tyr Arg Cys Ile Ile Val Met Pro Glu Lys Met Ser Ser Glu
165 170 175
Lys Val Asp Val Leu Arg Ala Leu Gly Ala Glu Ile Val Arg Thr Pro
180 185 190
Thr Asn Ala Arg Phe Asp Ser Pro Glu Ser His Val Gly Val Ala Trp
195 200 205
Arg Leu Lys Asn Glu Ile Pro Asn Ser His Ile Leu Asp Gln Tyr Arg
210 215 220
Asn Ala Ser Asn Pro Leu Ala His Tyr Asp Thr Thr Ala Asp Glu Ile
225 230 235 240
Leu Gln Gln Cys Asp Gly Lys Leu Asp Met Leu Val Ala Ser Val Gly
245 250 255
Thr Gly Gly Thr Ile Thr Gly Ile Ala Arg Lys Leu Lys Glu Lys Cys
260 265 270
Pro Gly Cys Arg Ile Ile Gly Val Asp Pro Glu Gly Ser Ile Leu Ala
275 280 285
Glu Pro Glu Glu Leu Asn Gln Thr Glu Gln Thr Thr Tyr Glu Val Glu
290 295 300
Gly Ile Gly Tyr Asp Phe Ile Pro Thr Val Leu Asp Arg Thr Val Val
305 310 315 320
Asp Lys Trp Phe Lys Ser Asn Asp Glu Glu Ala Phe Thr Phe Ala Arg
325 330 335
Met Leu Ile Ala Gln Glu Gly Leu Leu Cys Gly Gly Ser Ala Gly Ser
340 345 350
Thr Val Ala Val Ala Val Lys Ala Ala Gln Glu Leu Gln Glu Gly Gln
355 360 365
Arg Cys Val Val Ile Leu Pro Asp Ser Val Arg Asn Tyr Met Thr Lys
370 375 380
Phe Leu Ser Asp Arg Trp Met Leu Gln Lys Gly Phe Leu Lys Glu Glu
385 390 395 400
Asp Leu Thr Glu Lys Lys Pro Trp Trp Trp His Leu Arg
405 410
<---
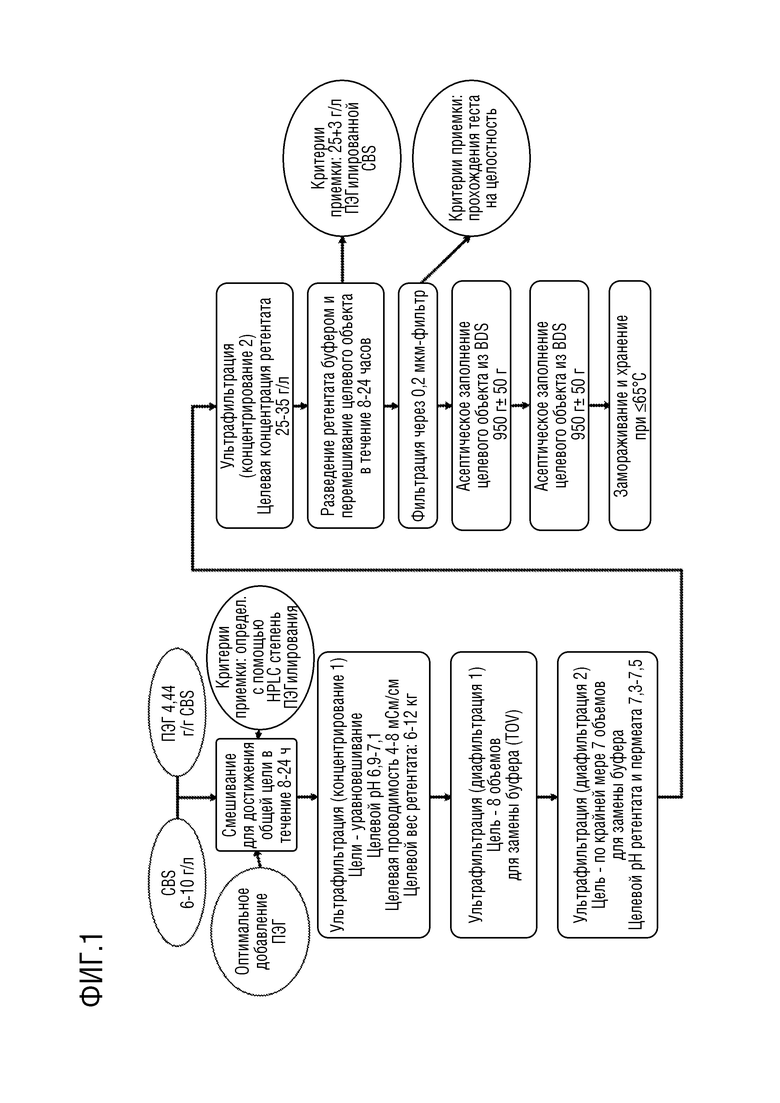
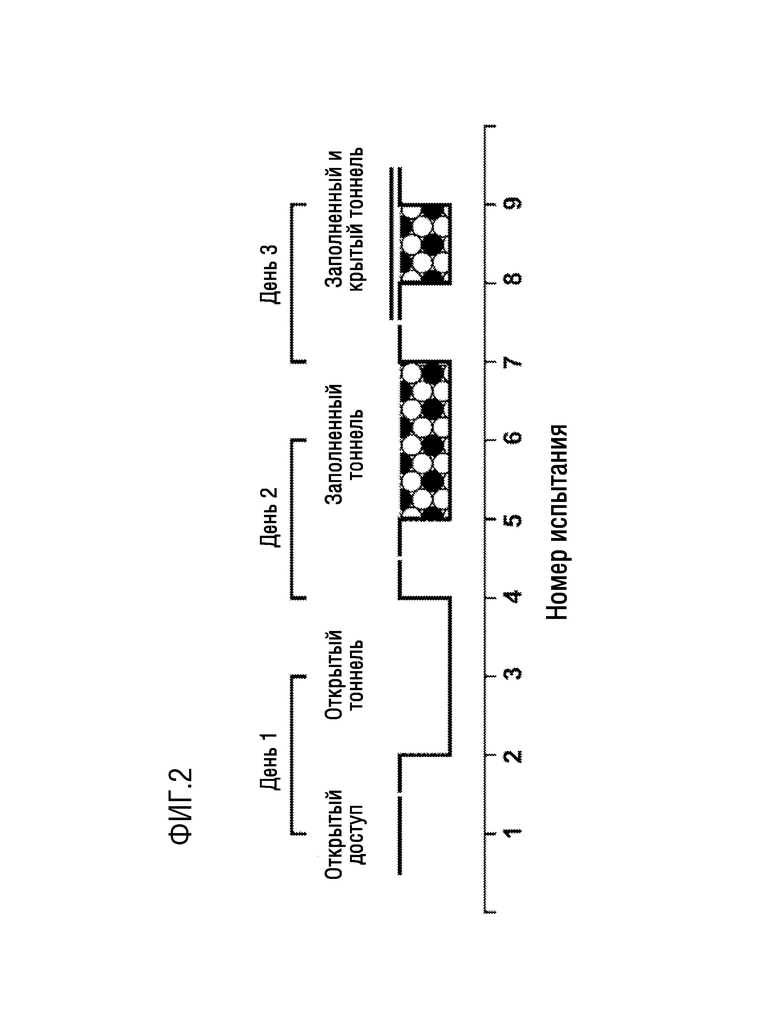
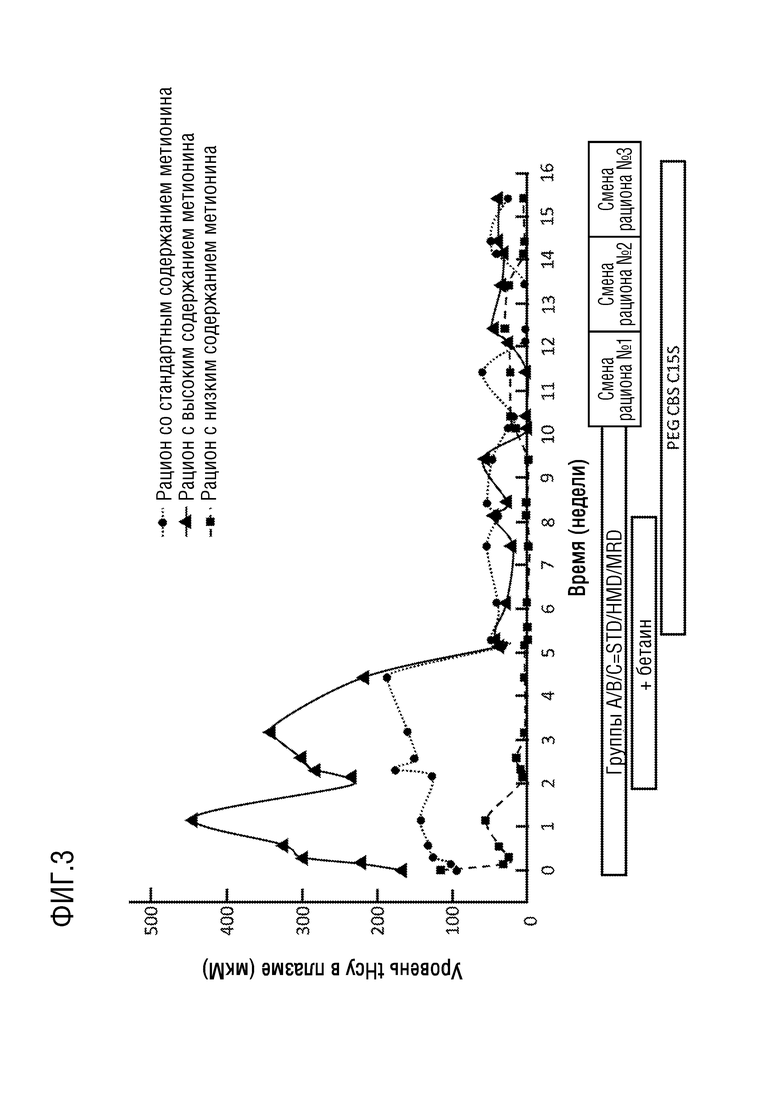
Изобретение относится к препаратам, содержащим ПЭГилированный белок цистатионин-β-синтазы (CBS), и их использованию в лечении гомоцистинурии. Предложен лиофилизированный препарат лекарственного вещества для лечения гомоцистинурии у субъекта, содержащий лекарственное вещество, содержащее выделенный белок CBS, содержащий SEQ ID NO: 1, и по меньшей мере одну молекулу ПЭГ массой 20 кДа, ковалентно связанную с белком CBS, 15 мМ фосфата калия и 8% (мас./об.) трегалозы. Также предложен восстановленный жидкий препарат для лечения гомоцистинурии у субъекта. Указанный препарат используют для снижения уровня гомоцистеина (Hcy) или повышения уровней цистеина (Cys) и/или цистатионина (Cth) у нуждающегося в этом субъекта, а также для лечения гомоцистинурии у нуждающегося в этом субъекта. Изобретение обеспечивает эффективное лечение гомоцистинурии. 9 н. и 57 з.п. ф-лы, 3 ил., 19 табл., 18 пр.
1. Лиофилизированный препарат лекарственного вещества для лечения гомоцистинурии у субъекта, содержащий:
(i) лекарственное вещество, содержащее выделенный белок цистатионин-β-синтазы (CBS), содержащий SEQ ID NO: 1, и по меньшей мере одну молекулу ПЭГ массой 20 кДа, ковалентно связанную с белком CBS;
(ii) 15 мМ фосфата калия и
(iii) 8% (мас./об.) трегалозы.
2. Лиофилизированный препарат по п. 1, где молекула ПЭГ представляет собой ME-200GS.
3. Лиофилизированный препарат по п. 1, где лекарственное вещество получено или может быть получено с использованием метокси-ПЭГ-СО(СН2)3СОО-NHS для ПЭГилирования белка CBS.
4. Восстановленный жидкий препарат для лечения гомоцистинурии у субъекта, содержащий:
(i) лекарственное вещество в концентрации 20-30 мг/мл, где лекарственное вещество содержит выделенный белок цистатионин-β-синтазы (CBS), содержащий SEQ ID NO: 1, и по меньшей мере одну молекулу ПЭГ массой 20 кДа, ковалентно связанную с белком CBS;
(ii) 15 мМ фосфата калия и
(iii) 8% (мас./об.) трегалозы.
5. Восстановленный жидкий препарат по п. 4, в котором количество лекарственного вещества составляет 25 мг.
6. Восстановленный жидкий состав по п. 4, дополнительно содержащий 1 мл воды.
7. Восстановленный жидкий препарат по п. 4, в котором молекула ПЭГ представляет собой ME-200GS.
8. Восстановленный жидкий препарат по п. 4, где лекарственное вещество получено или может быть получено с использованием метокси-ПЭГ-СО(СН2)3СОО-NHS для ПЭГилирования белка CBS.
9. Способ лечения гомоцистинурии у субъекта, включающий введение субъекту терапевтически эффективного количества восстановленного жидкого препарата по любому из пп. 4-8.
10. Способ по п. 9, в котором терапевтически эффективное количество представляет собой дозу, выбранную из диапазона от 0,25 до 10 мг/кг.
11. Способ по п. 9, где восстановленный жидкий препарат предназначен для введения лекарственного вещества в дозе менее 10 мг/кг.
12. Способ по п. 10, в котором доза составляет 0,33 мг/кг.
13. Способ по п. 10, в котором доза составляет 0,66 мг/кг.
14. Способ по п. 10, в котором доза составляет 1,0 мг/кг.
15. Способ по п. 10, в котором доза составляет 1,5 мг/кг.
16. Способ по любому из пп. 9-15, который включает, кроме того, введение субъекту по крайней мере одного вещества, выбранного из группы, состоящей из пиридоксина, витамина B6 и бетаина.
17. Способ по любому из пп. 9-16, в котором субъект соблюдает диету с ограничением метионина (Met).
18. Способ по любому из пп. 9-17, который включает, кроме того, введение антитромбоцитарного средства.
19. Способ по п. 18, в котором антитромбоцитарное средство представляет собой разжижитель крови варфарин или антикоагулянт.
20. Способ по любому из пп. 9-19, в котором стадия введения выполняется один раз каждые 3 дня.
21. Способ по любому из пп. 9-19, в котором стадия введения выполняется один раз в день.
22. Способ по любому из пп. 9-19, в котором стадия введения выполняется один раз в неделю.
23. Способ по любому из пп. 9-22, в котором стадию введения повторяют на протяжении 6 недель.
24. Способ по любому из пп. 9-22, в котором стадию введения повторяют на протяжении 3 месяцев.
25. Способ по любому из пп. 9-22, в котором стадию введения повторяют на протяжении 6 месяцев.
26. Способ по любому из пп. 9-22, в котором стадию введения повторяют на протяжении более 6 месяцев.
27. Способ по любому из пп. 9-22, в котором стадию введения повторяют в течение оставшегося времени жизни субъекта.
28. Способ снижения повышенного уровня гомоцистеина (Hcy) у субъекта, включающий введение субъекту терапевтически эффективного количества восстановленного жидкого препарата по любому из пп. 4-8.
29. Способ по п. 28, в котором уровень Hcy составляет менее 80 мкМ после стадии введения.
30. Способ по п. 28, в котором уровень Hcy снижается вплоть до 10% после стадии введения.
31. Способ по п. 28, в котором уровень Hcy снижается вплоть до 20% после стадии введения.
32. Способ по п. 28, в котором уровень Hcy снижается вплоть до 30% после стадии введения.
33. Способ по п. 28, в котором уровень Hcy снижается вплоть до 40% после стадии введения.
34. Способ по п. 28, в котором уровень Hcy снижается вплоть до 50% после стадии введения.
35. Способ по п. 28, в котором уровень Hcy снижается вплоть до 60% после стадии введения.
36. Способ по п. 28, в котором уровень Hcy снижается вплоть до 70% после стадии введения.
37. Способ по п. 28, в котором уровень Hcy снижается вплоть до 80% после стадии введения.
38. Способ по п. 28, в котором уровень Hcy снижается вплоть до 90% после стадии введения.
39. Способ по любому из пп. 28-38, в котором уровень Hcy находится в диапазоне от 10 до 20 мкМ после стадии введения.
40. Способ по любому из пп. 28-38, в котором уровень Hcy составляет менее 10 мкМ после стадии введения.
41. Способ по любому из пп. 28-38, в котором уровень Hcy составляет 55 мкМ после стадии введения.
42. Способ по любому из пп. 28-41, в котором терапевтически эффективное количество представляет собой дозу, выбранную из диапазона от 0,25 до 10 мг/кг.
43. Способ по п. 42, в котором доза составляет 0,33 мг/кг.
44. Способ по п. 42, в котором доза составляет 0,66 мг/кг.
45. Способ по п. 42, в котором доза составляет 1,0 мг/кг.
46. Способ по п. 42, в котором доза составляет 1,5 мг/кг.
47. Способ по п. 42, в котором доза составляет 7,0 мг/кг.
48. Способ по п. 42, в котором доза составляет 10 мг/кг.
49. Способ по п. 42, в котором доза составляет менее 10 мг/кг.
50. Способ по любому из пп. 28-49, который включает, кроме того, введение субъекту по крайней мере одного вещества, выбранного из группы, состоящей из пиридоксина, витамина B6 и бетаина.
51. Способ по любому из пп. 28-50, в котором субъект соблюдает диету с ограничением метионина (Met).
52. Способ по любому из пп. 28-51, который включает, кроме того, введение антитромбоцитарного средства.
53. Способ по п. 52, в котором антитромбоцитарное средство представляет собой разжижитель крови варфарин или антикоагулянт.
54. Способ по любому из пп. 28-53, в котором стадия введения выполняется один раз каждые 3 дня.
55. Способ по любому из пп. 28-53, в котором стадия введения выполняется один раз в день.
56. Способ по любому из пп. 28-53, в котором стадия введения выполняется один раз в неделю.
57. Способ по любому из пп. 28-53, в котором стадию введения повторяют на протяжении 6 недель.
58. Способ по любому из пп. 28-53, в котором стадию введения повторяют на протяжении 3 месяцев.
59. Способ по любому из пп. 28-53, в котором стадию введения повторяют на протяжении 6 месяцев.
60. Способ по любому из пп. 28-53, в котором стадию введения повторяют на протяжении более 6 месяцев.
61. Способ по любому из пп. 25-50, в котором стадию введения повторяют в течение оставшегося времени жизни субъекта.
62. Способ повышения сниженного уровня цистеина (Cys) у субъекта, страдающего от гомоцистинурии, включающий введение субъекту терапевтически эффективного количества восстановленного жидкого препарата по любому из пп. 4-8.
63. Способ повышения сниженного уровня цистатионина (Cth) у субъекта, страдающего от гомоцистинурии, включающий введение субъекту терапевтически эффективного количества препарата фармацевтической композиции по любому из пп. 4-8.
64. Способ лечения, облегчения или предотвращения негативных клинических последствий гомоцистинурии, связанных со зрительной системой, костной системой, сердечно-сосудистой системой и/или центральной нервной системой субъекта, при этом способ включает введение субъекту терапевтически эффективного количества восстановленного жидкого препарата по любому из пп. 4-8.
65. Применение лиофилизированного препарата лекарственного вещества по любому из пп. 1-3 в способе лечения гомоцистинурии, где терапевтически эффективное количество восстановленного жидкого препарата на основе лиофилизированного препарата, содержащего:
(i) лекарственное вещество в концентрации 20-30 мг/мл;
(ii) 15 мМ фосфата калия и
(iii) 8% (мас./об.) трегалозы,
вводят человеку.
66. Применение лиофилизированного лекарственного препарата лекарственного вещества по любому из пп. 1-3 для приготовления восстановленного жидкого лекарственного препарата, где после восстановления восстановленный жидкий лекарственный препарат содержит:
(i) лекарственное вещество в концентрации 20-30 мг/мл, причем лекарственное вещество содержит выделенный белок цистатионин-β-синтазы (CBS), содержащий SEQ ID NO: 1, и по меньшей мере одну молекулу ПЭГ массой 20 кДа, ковалентно связанную с белком CBS;
(ii) 15 мМ фосфата калия и
(iii) 8% (мас./об.) трегалозы.
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| US 10046036 B2, 14.08.2018 | |||
| MAJTAN T | |||
| et al | |||
| Engineering and Characterization of an Enzyme Replacement Therapy for Classical Homocystinuria | |||
| Biomacromolecules | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| БАРАНОВ А.А | |||
| и др | |||
| Гомоцистинурия у детей | |||
| Вопросы современной педиатрии | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
Авторы
Даты
2025-05-14—Публикация
2020-06-26—Подача