ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет согласно предварительной заявке на патент США № 62/887400, поданной 15 августа 2019 г., предварительной заявке на патент США № 62/903187, поданной 20 сентября 2019 г., и предварительной заявке на патент США № 62/962668, поданной 17 января 2020 г., раскрытия каждой из которых настоящим включены посредством ссылки во всей своей полноте.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит перечень последовательностей, который был подан в электронном виде в формате ASCII и настоящим включен посредством ссылки во всей своей полноте. Указанная ASCII-копия, созданная 12 августа 2020 г., имеет название 2020-08-12_01183-0073-00PCT_seq_listing.txt, и ее размер составляет 128000 байтов.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Отдельные популяции Т-клеток модулируют иммунную систему для поддержания иммунного гомеостаза и толерантности. Например, регуляторные Т-клетки (Treg) предупреждают ненадлежащие ответы иммунной системы путем предупреждения патологической аутореактивности, тогда как цитотоксические Т-клетки нацеливаются на инфицированные клетки и/или раковые клетки и разрушают их. В некоторых случаях модулирование различных популяций Т-клеток представляет собой вариант лечения заболевания или показания. В некоторых случаях этому способствует наличие дополнительных средств или способов в комбинированной терапии.
Соответственно, в одном аспекте в данном документе представлены способы лечения рака у субъекта, включающие введение субъекту конъюгата IL-2 в комбинации с одним или несколькими ингибиторами контрольных точек иммунного ответа.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В данном документе в определенных вариантах осуществления описаны способы лечения рака. Охватываются следующие варианты осуществления.
Вариант осуществления A1 представляет собой способ лечения рака у нуждающегося в этом субъекта, включающий введение субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких ингибиторов контрольных точек иммунного ответа, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (I):
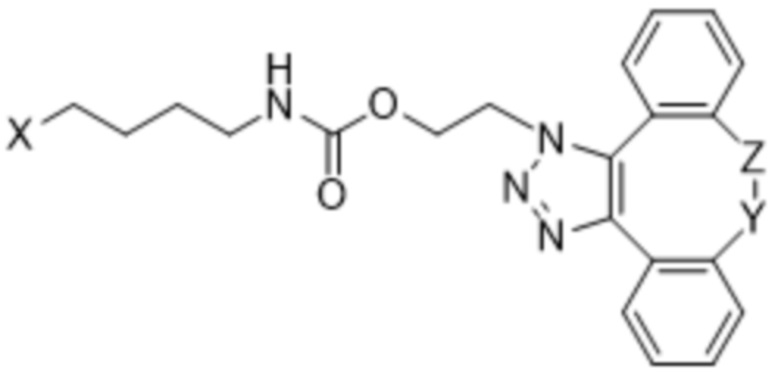
Формула (I);
где:
Z представляет собой CH2, и Y представляет собой 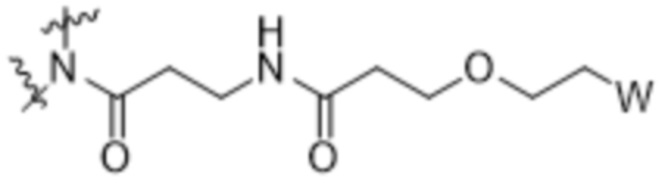 ;
;
Y представляет собой CH2, и Z представляет собой  ;
;
Z представляет собой CH2, и Y представляет собой 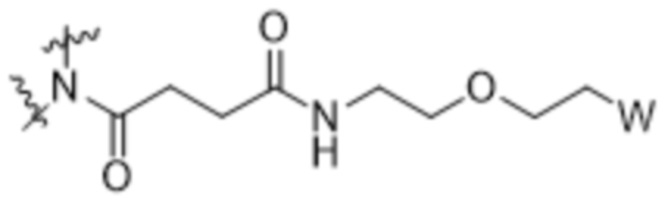 ; или
; или
Y представляет собой CH2, и Z представляет собой 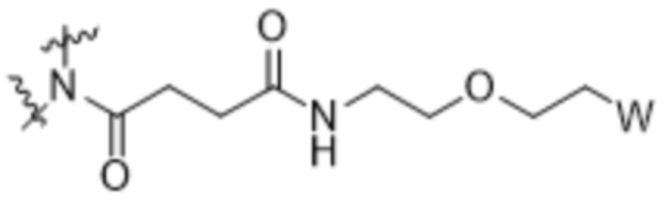 ;
;
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа;
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
где положение структуры формулы (I) в SEQ ID NO: 3 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71.
Вариант осуществления A2 представляет собой способ согласно варианту осуществления A1, где в конъюгате IL-2 Z представляет собой CH2, и Y представляет собой  .
.
Вариант осуществления A3 представляет собой способ согласно варианту осуществления A1, где в конъюгате IL-2 Y представляет собой CH2, и Z представляет собой  .
.
Вариант осуществления A4 представляет собой способ согласно варианту осуществления A1, где в конъюгате IL-2 Z представляет собой CH2, и Y представляет собой  .
.
Вариант осуществления A5 представляет собой способ согласно варианту осуществления A1, где в конъюгате IL-2 Y представляет собой CH2, и Z представляет собой  .
.
Вариант осуществления A6 представляет собой способ согласно любому из вариантов осуществления A1-A5, где в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 25 кДа, 30 кДа или 35 кДа.
Вариант осуществления A7 представляет собой способ согласно варианту осуществления A6, где в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 30 кДа.
Вариант осуществления A8 представляет собой способ согласно любому из вариантов осуществления A1-A7, где в конъюгате IL-2 положение структуры формулы (I) в SEQ ID NO: 3 представляет собой P64.
Вариант осуществления A9 представляет собой способ согласно варианту осуществления A1, где структура формулы (I) имеет структуру формулы (X) или формулы (XI) или представляет собой смесь формулы (X) и формулы (XI):
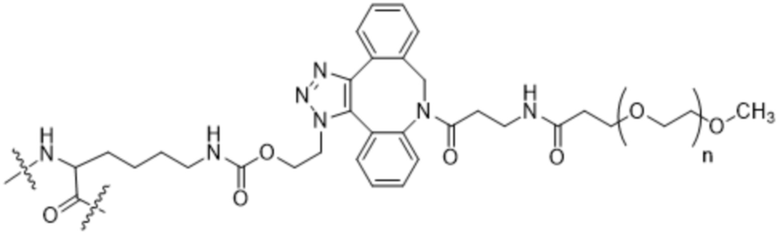
Формула (X);
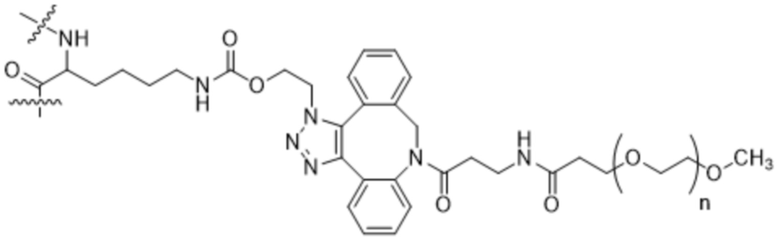
(XI);
где:
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
волнистыми линиями указаны ковалентные связи с аминокислотными остатками в SEQ ID NO: 3, которые не заменены.
Вариант осуществления A10 представляет собой способ согласно варианту осуществления A9, где в конъюгате IL-2 положение структуры формулы (X) или формулы (XI) в SEQ ID NO: 3 представляет собой P64.
Вариант осуществления A11 представляет собой способ согласно вариантам осуществления A9 или A10, где в конъюгате IL-2 n представляет собой такое целое число, что -(OCH2CH2)n-OCH3 имеет молекулярную массу, составляющую приблизительно 25 кДа, 30 кДа или 35 кДа.
Вариант осуществления A12 представляет собой способ согласно варианту осуществления A11, где в конъюгате IL-2 n представляет собой такое целое число, что -(OCH2CH2)n-OCH3 имеет молекулярную массу, составляющую приблизительно 30 кДа.
Вариант осуществления A13 представляет собой способ согласно варианту осуществления A1, где структура формулы (I) имеет структуру формулы (XII) или формулы (XIII) или представляет собой смесь формулы (XII) и формулы (XIII):
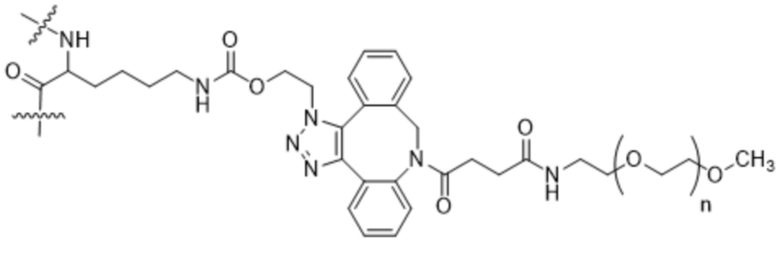
Формула (XII);
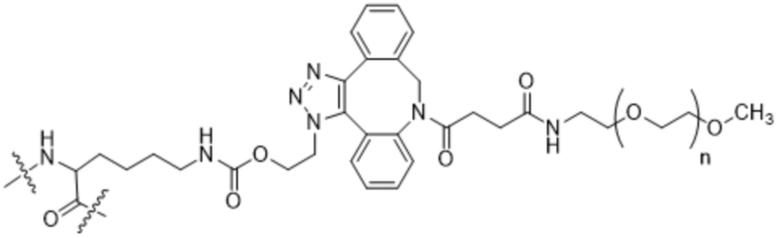
(XIII);
где:
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
волнистыми линиями указаны ковалентные связи с аминокислотными остатками в SEQ ID NO: 3, которые не заменены.
Вариант осуществления A14 представляет собой способ согласно варианту осуществления A13, где в конъюгате IL-2 положение структуры формулы (XII) или формулы (XIII) в SEQ ID NO: 3 представляет собой P64.
Вариант осуществления A15 представляет собой способ согласно вариантам осуществления A13 или A14, где в конъюгате IL-2 n представляет собой такое целое число, что -(OCH2CH2)n-OCH3 имеет молекулярную массу, составляющую приблизительно 25 кДа, 30 кДа или 35 кДа.
Вариант осуществления A16 представляет собой способ согласно варианту осуществления A15, где в конъюгате IL-2 n представляет собой такое целое число, что -(OCH2CH2)n-OCH3 имеет молекулярную массу, составляющую приблизительно 30 кДа.
Вариант осуществления A17 представляет собой способ лечения рака у нуждающегося в этом субъекта, включающий введение субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких ингибиторов контрольных точек иммунного ответа, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 50, где [AzK_L1_PEG30кДа] имеет структуру формулы (IV) или формулы (V) или представляет собой смесь структур формулы (IV) и формулы (V):
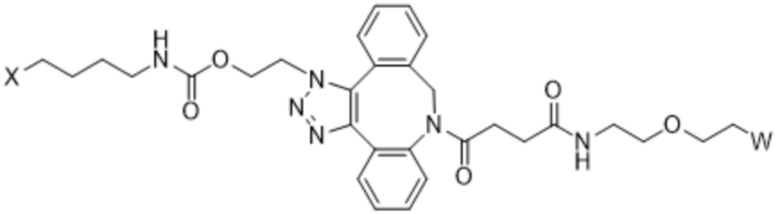
Формула (IV);
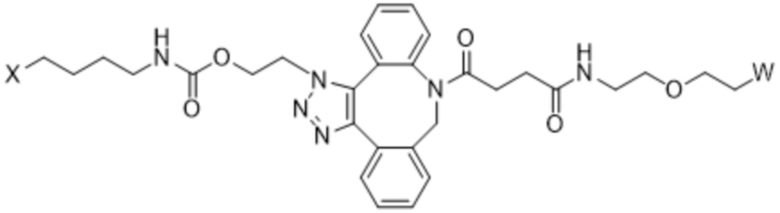
Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа;
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку.
Вариант осуществления A18 представляет собой способ согласно варианту осуществления A17, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 25 кДа, 30 кДа или 35 кДа.
Вариант осуществления A19 представляет собой способ согласно варианту осуществления A18, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления A20 представляет собой способ лечения рака у нуждающегося в этом субъекта, включающий введение субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких ингибиторов контрольных точек иммунного ответа, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 50, где [AzK_L1_PEG30кДа] имеет структуру формулы (XII) или формулы (XIII) или представляет собой смесь структур формулы (XII) и формулы (XIII):

Формула (XII);

(XIII);
где:
n представляет собой такое целое число, что -(OCH2CH2)n-OCH3 имеет молекулярную массу, составляющую приблизительно 30 кДа; и
волнистыми линиями указаны ковалентные связи с аминокислотными остатками в SEQ ID NO: 50, которые не заменены.
Вариант осуществления A21 представляет собой способ согласно любому из вариантов осуществления A1-A20, где один или несколько ингибиторов контрольных точек иммунного ответа представляют собой один или несколько ингибиторов PD-1.
Вариант осуществления A22 представляет собой способ согласно варианту осуществления A21, где один или несколько ингибиторов PD-1 выбраны из пембролизумаба, ниволумаба и цемиплимаба.
Вариант осуществления A23 представляет собой способ согласно варианту осуществления A22, где один или несколько ингибиторов PD-1 представляют собой пембролизумаб.
Вариант осуществления A24 представляет собой способ согласно варианту осуществления A22, где один или несколько ингибиторов PD-1 представляют собой ниволумаб.
Вариант осуществления A25 представляет собой способ согласно любому из вариантов осуществления A1-A24, где рак выбран из почечноклеточной карциномы (RCC), немелкоклеточного рака легкого (NSCLC), плоскоклеточного рака головы и шеи (HNSCC), классической лимфомы Ходжкина (cHL), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), уротелиальной карциномы, рака с микросателлитной нестабильностью, рака с микросателлитной стабильностью, рака желудка, рака ободочной кишки, рака ободочной и прямой кишки (CRC), рака шейки матки, гепатоцеллюлярной карциномы (HCC), карциномы из клеток Меркеля (MCC), меланомы, мелкоклеточного рака легкого (SCLC), рака пищевода, плоскоклеточной карциномы пищевода (ESCC), глиобластомы, мезотелиомы, рака молочной железы, трижды негативного рака молочной железы, рака предстательной железы, кастрационно-резистентного рака предстательной железы, метастатического кастрационно-резистентного рака предстательной железы или метастатического кастрационно-резистентного рака предстательной железы с дефектами ответа на повреждение ДНК (DDR), рака мочевого пузыря, рака яичника, опухолей с мутационной нагрузкой от умеренной до низкой, плоскоклеточной карциномы кожи (CSCC), плоскоклеточного рака кожи (SCSC), опухолей с экспрессией PD-L1 от низкой до отсутствующей, опухолей, распространяющихся системно в печень и CNS за пределы их первичного анатомического участка происхождения, и диффузной крупноклеточной В-клеточной лимфомы.
Вариант осуществления A26 представляет собой способ согласно любому из вариантов осуществления A1-A25, где конъюгат IL-2 вводят субъекту один раз в неделю, один раз в две недели, один раз в три недели, один раз в 4 недели, один раз в 5 недель, один раз в 6 недель, один раз в 7 недель или один раз в 8 недель.
Вариант осуществления A27 представляет собой способ согласно любому из вариантов осуществления A1-A26, где конъюгат IL-2 вводят субъекту путем внутривенного введения.
Вариант осуществления A28 представляет собой способ согласно любому из вариантов осуществления A1-A27, где конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Лучшее понимание признаков и преимуществ настоящего изобретения будет достигнуто посредством ссылки на следующее подробное описание, в котором изложены иллюстративные варианты осуществления, в которых используются принципы настоящего изобретения, и прилагаемые графические материалы, на которых представлено следующее.
На фиг. 1 показан график противоопухолевой активности соединения A, дозы которого вводятся IV по схеме QWx3, из исследования 1 в примере 11. Черные стрелки обозначают дни введения доз соединения A.
На фиг. 2 показан график объемов опухоли для соединения A, дозы которого вводятся IV по схеме QWx3, из исследования 1 в примере 11.
На фиг. 3 показаны объемы опухоли в день 15 после обработки для каждого животного, получавшего обработку путем введения доз соединения A QWx3, из исследования 1 в примере 11. Черные стрелки обозначают дни введения доз соединения A.
На фиг. 4 показаны объемы опухоли в день 15 после обработки для каждого животного, которому вводили дозы соединения A Q2Wx2, из исследования 1 в примере 11.
На фиг. 5 показаны кривые среднего роста опухоли при обработке мышей с помощью среды-носителя, 6 мг/кг соединения A в качестве средства монотерапии, антитела к PD-1 в качестве средства монотерапии и комбинации 6 мг/кг соединения A и антитела к PD-1 из исследования 2 в примере 11. Черные стрелки обозначают дни введения доз соединения A.
На фиг. 6 показан график данных о % TGI в день 15 после обработки в группе, получавшей обработку с помощью комбинации соединения A и антитела к PD-1, по сравнению с группами, получавшими обработку с помощью среды-носителя, соединения A в отдельности или антитела к PD-1 в отдельности, из исследования 2 в примере 11. *p < 0,05, **p < 0,01 и ***p < 0,01; в сравнении с контрольной средой-носителем. ┴p < 0,05 в сравнении с антителом к PD-1. #p < 0,05 в сравнении с соединением A. Данные представляют средний объем опухоли ± SEM (14 мышей/группа).
На фиг. 7 показан график кривых выживаемости Каплана-Мейера для групп обработки из исследования 2 в примере 11. *p < 0,05 в сравнении с контрольной средой-носителем. ┴p < 0,05 в сравнении с антителом к PD-1. #p < 0,05 в сравнении с соединением A.
На фиг. 8 представлены кривые среднего роста опухоли при введении доз соединения A в качестве средства монотерапии при 1 мг/кг, 3 мг/кг, 6 мг/кг и 9 мг/кг в исследовании 3 в примере 11. Данные представляют средний объем опухоли ± SEM (14 мышей/группа; за исключением 12 мышей/группа для 9 мг/кг соединения A). Черные стрелки обозначают дни введения доз соединения A.
На фиг. 9 представлены индивидуальные объемы опухоли в день 15 после обработки из исследования 3 в примере 11. Данные представляют индивидуальные объемы опухоли; также показано среднее значение ± SEM и % TGI по сравнению с контрольной средой-носителем. ***p < 0,01 в сравнении с контрольной средой-носителем.
На фиг. 10 показан график кривых выживаемости Каплана-Мейера для групп обработки, получавших обработку с помощью среды-носителя (контроль), антитела к PD-1 в отдельности, соединения A в отдельности и комбинации соединения A и антитела к PD-1. *p < 0,05 в сравнении с контрольной средой-носителем из исследования 3 в примере 11. ┴p < 0,05 в сравнении с антителом к PD-1. #p < 0,05 в сравнении с соединением A.
На фиг. 11A и фиг. 11B показаны графики иллюстративных уровней цитокинов для IL-2 и IL-2_P65[AzK_L1_PEG30кДа]-1 в отдельности и в комбинации с ниволумабом (Nivo) или пембролизумабом (Pem) для одного донора из примера 12. На фиг. 11A показан график уровней IFN-гамма, IL-8, IL-6, TNF-альфа, IL-4 и IL-5. На фиг. 11B показан график уровней IL-6, TNF-альфа и IL-5.
На фиг. 12 показано высвобождение интерферона гамма в анализе реакции смешанной культуры лимфоцитов (MLR) для комбинации соединения B (IL-2_P65[AzK_L1_PEG30кДа]-1) и пембролизумаба согласно примеру 13.
На фиг. 13 и фиг. 14 показано высвобождение интерферона гамма в анализе реакции смешанной культуры лимфоцитов (MLR) для комбинации соединения B (IL-2_P65[AzK_L1_PEG30кДа]-1) и ниволумаба согласно примеру 13.
На фиг. 15 показаны фармакокинетические свойства соединения B из примера 14.
На фиг. 16A-16D показано количество pSTAT5+ клеток среди CD8+ T-клеток периферической крови, CD8+ T-клеток памяти, NK-клеток и Treg-клеток соответственно после введения соединения B согласно примеру 14.
На фиг. 17A-17G показана активация Ki67 в популяциях CD8+ T-, NK- и Treg-клеток с помощью соединения B согласно примеру 14.
На фиг. 18A-18D показаны анализы образцов опухоли (уровни CD8+ T-клеток, NK-клеток и Treg-клеток и соотношение CD8+/Treg) после обработки с помощью соединения B согласно примеру 14.
На фиг. 19 показано разнообразие TCR после обработки с помощью соединения B и антитела к PD-1 мыши согласно примеру 15.
На фиг. 20 показана клональность TIL в зависимости от доли T-клеток после указанных обработок (например, с помощью соединения B и/или антитела к PD-1 мыши) согласно примеру 15.
На фиг. 21 показана клональность T-клеток после обработки с помощью соединения B по сравнению с контрольной средой-носителем согласно примеру 15.
На фиг. 22 показана тепловая карта экспрессии в образцах опухоли из CT26 в день 8 после обработки с помощью контроля (среды-носителя), соединения B (6 мг/кг), антитела к PD-1 мыши (10 мг/кг) или комбинации соединения B и антитела к PD-1 мыши (N=10 мышей на группу) из примера 16.
На фиг. 23A-23C показаны ключевые экспрессионные репортеры состояния микроокружения опухоли после обработки с помощью соединения B согласно примеру 16: анализ инфильтрации активированных CD8+ эффекторных Т-клеток и эффекторных T-клеток памяти и цитолитических NK-клеток. CTL=контроль (среда-носитель); соед. B=соединение B; aPD1=антитело к PD-1 мыши; соед. B aPD1=комбинация соединения B и антитела к PD-1 мыши.
На фиг. 24A-24B показан профилирующий анализ уровней экспрессии генов сигнатуры интерферона γ в ответ на терапию согласно примеру 16. CTL=контроль (среда-носитель); соед. B=соединение B; aPD1=антитело к PD-1 мыши; соед. B aPD1=комбинация соединения B и антитела к PD-1 мыши.
На фиг. 25 и фиг. 26 показана оценка выживаемости и роста опухоли у повторно стимулированных животных без опухолей согласно примеру 17.
На фиг. 27A и фиг. 27B показано, что соединение B способствует общему увеличению количества T-клеток памяти (CD3+), в том числе CD8+ T-клеток памяти, в периферической крови у повторно стимулированных мышей согласно примеру 17.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Следует понимать, что изложенное выше общее описание и следующее подробное описание являются исключительно иллюстративными и пояснительными и не ограничивают никакой заявляемый объект изобретения. В той мере, в которой какой-либо материал, включенный в данный документ посредством ссылки, не соответствует прямому содержанию настоящего раскрытия, прямое содержание имеет преимущественную силу.
Определения
Если не указано иное, все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понимается специалистом в области техники, к которой принадлежит заявляемый объект изобретения. В настоящей заявке использование единственного числа предусматривает множественное число, если специально не указано иное. Следует отметить, что используемые в описании и прилагаемой формуле изобретения формы единственного числа включают ссылки на множественное число, если контекстом явно не предписывается иное. В настоящей заявке использование "или" означает "и/или", если не указано иное. Кроме того, использование термина "включающий", а также других форм, таких как "включать", "включает" и "включенный", не является ограничивающим.
Ссылка в настоящем описании на "некоторые варианты осуществления", "вариант осуществления", "один вариант осуществления" или "другие варианты осуществления" означает, что конкретные признак, структура или характеристика, описанные в связи с вариантами осуществления, включены в по меньшей мере некоторые варианты осуществления, но не обязательно во все варианты осуществления настоящего изобретения.
Используемые в данном документе диапазоны и количества могут быть выражены как "приблизительно" конкретное значение или диапазон. "Приблизительно" также включает точное количество. Следовательно, "приблизительно 5 мкл" означает "приблизительно 5 мкл", а также "5 мкл". Как правило, термин "приблизительно" включает количество, которое, как ожидается, будет находиться в пределах экспериментальной погрешности, как, например, в пределах 15%, 10% или 5%.
Заголовки разделов, используемые в данном документе, предназначены исключительно для организационных целей и не должны толковаться как ограничивающие описываемый объект изобретения.
Термин "или" используется во включающем смысле, эквивалентном "и/или", если контекстом явно не предписывается иное.
Используемые в данном документе термины "индивидуум (индивидуумы)", "субъект (субъекты)" и "пациент (пациенты)" означают любое млекопитающее. В некоторых вариантах осуществления млекопитающее является человеком. В некоторых вариантах осуществления млекопитающее является отличным от человека. Ни один из терминов не требует ситуаций и не ограничен ситуациями, которые характеризуются наблюдением (например, постоянным или периодическим) медицинского работника (например, врача, дипломированной медсестры, практикующей медсестры, фельдшера, санитара или работника хосписа).
Используемый в данном документе термин "значительный" или "в значительной степени" в отношении аффинности связывания означает изменение аффинности связывания цитокина (например, полипептида IL-2), достаточное для влияния на связывание цитокина (например, полипептида IL-2) с рецептором-мишенью. В некоторых случаях термин относится к изменению на по меньшей мере 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или больше. В некоторых случаях термин означает изменение в по меньшей мере 2 раза, 3 раза, 4 раза, 5 раз, 6 раз, 7 раз, 8 раз, 9 раз, 10 раз, 50 раз, 100 раз, 500 раз, 1000 раз или больше.
В некоторых случаях термин "значительный" или "в значительной степени" в отношении активации одной или нескольких популяций клеток посредством цитокинового сигнального комплекса означает изменение, достаточное для активации популяции клеток. В некоторых случаях изменение для активации популяции клеток измеряется как активность передачи сигнала рецепторами. В таких случаях может быть представлено значение EC50. В других случаях может быть представлено значение ED50. В дополнительных случаях может быть представлена концентрация или доза цитокина.
Используемый в данном документе термин "активность" относится к количеству цитокина (например, полипептида IL-2), требуемому для достижения целевого эффекта. В некоторых случаях термин "активность" относится к количеству цитокина (например, полипептида IL-2), требуемому для активации цитокинового рецептора-мишени (например, рецептора IL-2). В других случаях термин "активность" относится к количеству цитокина (например, полипептида IL-2), требуемому для активации популяции клеток-мишеней. В некоторых случаях активность измеряется как ED50 (эффективная доза 50) или доза, требуемая для достижения 50% от максимального эффекта. В других случаях активность измеряется как ЕС50 (эффективная концентрация 50) или доза, требуемая для достижения целевого эффекта у 50% популяции.
Используемый в данном документе термин "неприродная аминокислота" относится к аминокислоте, отличной от одной из 20 встречающихся в природе аминокислот. Иллюстративные неприродные аминокислоты описаны в Young et al., "Beyond the canonical 20 amino acids: expanding the genetic lexicon", J. of Biological Chemistry 285(15): 11039-11044 (2010), раскрытие которой включено в данный документ посредством ссылки.
Термин "антитело" в данном документе используется в самом широком смысле и охватывает различные структуры антител, в том числе без ограничения моноклональные антитела, поликлональные антитела, полиспецифические антитела (например, биспецифические антитела) и фрагменты антител, при условии, что они проявляют желаемую антигенсвязывающую активность. "Фрагмент антитела" относится к молекуле, отличной от интактного антитела, которая содержит часть интактного антитела, связывающую антиген, с которым связывается интактное антитело. Примеры фрагментов антител включают без ограничения Fv, Fab, Fab', Fab’-SH, F(ab')2; диатела; линейные антитела; одноцепочечные молекулы антител (например, scFv) и полиспецифические антитела, образованные из фрагментов антител. В некоторых вариантах осуществления антиген представляет собой EGFR.
Используемый в данном документе термин "моноклональное(моноклональные) антитело(антитела)" относится к антителу, полученному из популяции по сути однородных антител, т. е. отдельные антитела, составляющие популяцию, являются идентичными и/или связывают один и тот же эпитоп, за исключением возможных вариантов антител, например, содержащих встречающиеся в природе мутации или появляющихся в ходе получения препарата на основе моноклональных антител, при этом такие варианты обычно присутствуют в незначительных количествах. В отличие от препаратов на основе поликлональных антител, которые обычно содержат различные антитела, направленные против различных детерминант (эпитопов), каждое моноклональное антитело из препарата на основе моноклональных антител направлено против одной детерминанты на антигене. Таким образом, модификатор "моноклональное" указывает на характер антитела как полученного из по сути однородной популяции антител и не должен толковаться как требующий получения антитела каким-либо конкретным способом. Например, моноклональные антитела, которые должны применяться в соответствии с настоящим изобретением, могут быть получены с помощью ряда методик, в том числе без ограничения гибридомного способа, способов рекомбинантных ДНК, способов фагового дисплея и способов с использованием трансгенных животных, содержащих все локусы иммуноглобулинов человека или их часть, при этом такие способы и другие иллюстративные способы получения моноклональных антител описаны в данном документе.
Как используется в данном документе, "нуклеотид" относится к соединению, содержащему нуклеозидный фрагмент и фосфатный фрагмент. Иллюстративные природные нуклеотиды включают без ограничения аденозинтрифосфат (ATP), уридинтрифосфат (UTP), цитидинтрифосфат (CTP), гуанозинтрифосфат (GTP), аденозиндифосфат (ADP), уридиндифосфат (UDP), цитидиндифосфат (CDP), гуанозиндифосфат (GDP), аденозинмонофосфат (AMP), уридинмонофосфат (UMP), цитидинмонофосфат (CMP) и гуанозинмонофосфат (GMP), дезоксиаденозинтрифосфат (dATP), дезокситимидинтрифосфат (dTTP), дезоксицитидинтрифосфат (dCTP), дезоксигуанозинтрифосфат (dGTP), дезоксиаденозиндифосфат (dADP), тимидиндифосфат (dTDP), дезоксицитидиндифосфат (dCDP), дезоксигуанозиндифосфат (dGDP), дезоксиаденозинмонофосфат (dAMP), дезокситимидинмонофосфат (dTMP), дезоксицитидинмонофосфат (dCMP) и дезоксигуанозинмонофосфат (dGMP). Иллюстративные природные дезоксирибонуклеотиды, которые содержат дезоксирибозу в качестве сахарного фрагмента, включают dATP, dTTP, dCTP, dGTP, dADP, dTDP, dCDP, dGDP, dAMP, dTMP, dCMP и dGMP. Иллюстративные природные рибонуклеотиды, которые содержат рибозу в качестве сахарного фрагмента, включают ATP, UTP, CTP, GTP, ADP, UDP, CDP, GDP, AMP, UMP, CMP и GMP.
Как используется в данном документе, "основание" или "нуклеиновое основание" относится к по меньшей мере части нуклеозида или нуклеотида (нуклеозид и нуклеотид охватывают рибо- или дезоксирибонуклеотидные варианты), являющейся нуклеиновым основанием, которая в некоторых случаях может содержать дополнительные модификации сахарной части нуклеозида или нуклеотида. В некоторых случаях термин "основание" также используется для обозначения всего нуклеозида или нуклеотида (например, "основание" может быть встроено с помощью ДНК-полимеразы в ДНК или с помощью РНК-полимеразы в РНК). Однако термин "основание" не следует интерпретировать как обязательно представляющий весь нуклеозид или нуклеотид, если этого не требует контекст. В представленных в данном документе химических структурах основания или нуклеинового основания показано только основание нуклеозида или нуклеотида, а сахарный фрагмент и необязательно какие-либо фосфатные остатки опущены для ясности. Как используется в представленных в данном документе химических структурах основания или нуклеинового основания, волнистая линия представляет соединение с нуклеозидом или нуклеотидом, при этом сахарная часть нуклеозида или нуклеотида может быть дополнительно модифицирована. В некоторых вариантах осуществления волнистая линия представляет присоединение основания или нуклеинового основания к сахарной части нуклеозида или нуклеотида, такой как пентоза. В некоторых вариантах осуществления пентоза представляет собой рибозу или дезоксирибозу.
В некоторых вариантах осуществления нуклеиновое основание обычно представляет собой часть нуклеозида, являющуюся гетероциклическим основанием. Нуклеиновые основания могут встречаться в природе, могут быть модифицированы, могут не иметь сходства с природными основаниями и/или могут быть синтезированы, например, путем органического синтеза. В определенных вариантах осуществления нуклеиновое основание содержит любой атом или группу атомов в нуклеозиде или нуклеотиде, где атом или группа атомов способны взаимодействовать с основанием другой нуклеиновой кислоты с использованием или без использования водородных связей. В определенных вариантах осуществления неприродное нуклеиновое основание не является производным природного нуклеинового основания. Следует отметить, что неприродные нуклеиновые основания не обязательно обладают основными свойствами, однако для простоты они называются нуклеиновыми основаниями. В некоторых вариантах осуществления при упоминании нуклеинового основания "(d)" указывает на то, что нуклеиновое основание может быть присоединено к дезоксирибозе или рибозе, тогда как "d" без скобок указывает на то, что нуклеиновое основание присоединено к дезоксирибозе.
Как используется в данном документе, "нуклеозид" представляет собой соединение, содержащее фрагмент, являющийся нуклеиновым основанием, и сахарный фрагмент. Нуклеозиды включают без ограничения нуклеозиды, встречающиеся в природе (обнаруживаемые в ДНК и РНК), нуклеозиды, лишенные основания, модифицированные нуклеозиды и нуклеозиды, имеющие миметические основания и/или сахарные группы. Нуклеозиды включают нуклеозиды, содержащие любое разнообразие заместителей. Нуклеозид может представлять собой гликозидное соединение, образованное посредством гликозидной связи между основанием нуклеиновой кислоты и восстанавливающей группой сахара.
Используемый в данном документе термин "аналог" химической структуры относится к химической структуре, которая сохраняет существенное сходство с исходной структурой, хотя она не может быть легко получена синтетическим путем из исходной структуры. В некоторых вариантах осуществления аналог нуклеотида представляет собой неприродный нуклеотид. В некоторых вариантах осуществления аналог нуклеозида представляет собой неприродный нуклеозид. Родственная химическая структура, которая легко получается синтетическим путем из исходной химической структуры, называется "производной".
Хотя различные признаки настоящего изобретения могут быть описаны в контексте одного варианта осуществления, эти признаки также могут быть представлены отдельно или в любой подходящей комбинации. И наоборот, хотя настоящее изобретение может быть описано в данном документе в контексте отдельных вариантов осуществления для ясности, настоящее изобретение также может быть реализовано в одном варианте осуществления.
Конъюгаты IL-2
Цитокины включают в себя семейство клеточных сигнальных белков, таких как хемокины, интерфероны, интерлейкины, лимфокины, факторы некроза опухоли и другие факторы роста, играющие роль в клеточном гомеостазе врожденной и адаптивной иммунной системы. Цитокины продуцируются иммунными клетками, такими как макрофаги, В-лимфоциты, Т-лимфоциты и тучные клетки, эндотелиальными клетками, фибробластами и различными стромальными клетками. В некоторых случаях цитокины модулируют баланс между гуморальными и клеточными иммунными ответами.
Интерлейкины представляют собой сигнальные белки, которые модулируют развитие и дифференцировку Т- и В-лимфоцитов, клеток моноцитарной линии дифференцировки, нейтрофилов, базофилов, эозинофилов, мегакариоцитов и гемопоэтических клеток. Интерлейкины продуцируются хелперными CD4 T- и B-лимфоцитами, моноцитами, макрофагами, эндотелиальными клетками и другими резидентными в тканях клетками.
Интерлейкин 2 (IL-2) представляет собой плейотропный цитокин 1 типа, структура которого содержит пучок из четырех α-спиралей с молекулярной массой 15,5 кДа. Форма-предшественник IL-2 имеет длину 153 аминокислотных остатка, при этом первые 20 аминокислот образуют сигнальный пептид, а остатки 21-153 образуют зрелую форму. IL-2 продуцируется главным образом CD4+ T-клетками после стимуляции антигеном и в меньшей степени CD8+ клетками, естественными клетками-киллерами (NK) клетками и естественными Т-клетками-киллерами (NKT), активированными дендритными клетками (DC) и тучными клетками. Передача сигнала, опосредованная IL-2, происходит посредством взаимодействия со специфическими комбинациями субъединиц рецептора IL-2 (IL-2R) IL-2Rα (также известной как CD25), IL-2Rβ (также известной как CD122) и IL-2Rγ (также известной как CD132). При взаимодействии IL-2 с IL-2Rα образуется комплекс рецептора IL-2 "с низкой аффинностью" с Kd, составляющей приблизительно 10-8 M. При взаимодействии IL-2 с IL-2Rβ и IL-2Rγ образуется комплекс рецептора IL-2 "с промежуточной аффинностью" с Kd, составляющей приблизительно 10-9 M. При взаимодействии IL-2 со всеми тремя субъединицами IL-2Rα, IL-2Rβ и IL-2Rγ образуется комплекс рецептора IL-2 "с высокой аффинностью" с Kd, составляющей приблизительно > 10-11 M.
В некоторых случаях при передаче сигнала, опосредованной IL-2, посредством комплекса IL-2Rαβγ "с высокой аффинностью" модулируется активация и пролиферация регуляторных Т-клеток. Регуляторные Т-клетки или CD4+CD25+Foxp3+ регуляторные T-клетки (Treg) опосредуют поддержание иммунного гомеостаза путем подавления эффекторных клеток, таких как CD4+ Т-клетки, CD8+ Т-клетки, В-клетки, NK-клетки и NKT-клетки. В некоторых случаях Treg-клетки образуются в тимусе (tTreg-клетки) или их образование индуцируется из "необученных" Т-клеток в периферической крови (pTreg-клетки). В некоторых случаях Treg-клетки считаются медиаторами периферической толерантности. И действительно, в одном исследовании перенос истощенных по CD25 CD4+ Т-клеток периферической крови вызывал ряд аутоиммунных заболеваний у "голых" мышей, тогда как совместный перенос CD4+CD25+ Т-клеток подавлял развитие аутоиммунитета (Sakaguchi, et al., "Immunologic self-tolerance maintained by activated T cells expressing IL-2 receptor alpha-chains (CD25)", J. Immunol. 155(3): 1151-1164 (1995), раскрытие которой включено в данный документ посредством ссылки). При увеличении популяции Treg-клеток отрицательно регулируется пролиферация эффекторных Т-клеток и подавляются аутоиммунитет и Т-клеточные противоопухолевые ответы.
При передаче сигнала, опосредованной IL-2, посредством комплекса IL-2Rβγ "с промежуточной аффинностью" модулируется активация и пролиферация CD8+ эффекторных T-клеток (Teff), NK-клеток и NKT-клеток. CD8+ Teff-клетки (также известные как цитотоксические Т-клетки, Тс-клетки, цитотоксические Т-лимфоциты, CTL, киллерные Т-клетки, цитолитические Т-клетки, Tcon или Т-клетки-киллеры) представляют собой Т-лимфоциты, которые распознают и уничтожают поврежденные клетки, раковые клетки и клетки, инфицированные патогенами. NK- и NKT-клетки представляют собой типы лимфоцитов, которые, подобно CD8+ Teff-клеткам, нацеливаются на раковые клетки и клетки, инфицированные патогенами.
В некоторых случаях передача сигнала, опосредованная IL-2, используется для модулирования Т-клеточных ответов и, следовательно, для лечения рака. Например, IL-2 вводят в высокодозовой форме, чтобы индуцировать размножение популяций Teff-клеток для лечения рака. Однако высокодозовый IL-2, кроме того, приводит к сопутствующей стимуляции Treg-клеток, которые ослабляют противоопухолевые иммунные ответы. Высокодозовый IL-2 также индуцирует токсические нежелательные явления, опосредованные привлечением в сосудистую сеть клеток, экспрессирующих альфа-цепь IL-2R, включая клетки врожденной иммунной системы 2 типа (ILC-2), эозинофилы и эндотелиальные клетки. Это приводит к эозинофилии, синдрому повышенной проницаемости капилляров и синдрому повышенной проницаемости сосудов (VLS).
Адоптивная клеточная терапия позволяет врачам эффективно использовать собственные иммунные клетки пациента для борьбы с такими заболеваниями, как пролиферативное заболевание (например, рак), а также инфекционное заболевание. В данном документе в некоторых вариантах осуществления раскрываются способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где одно или несколько дополнительных средств могут включать в себя один или несколько ингибиторов контрольных точек иммунного ответа.
В некоторых вариантах осуществления в данном документе описаны конъюгаты интерлейкина 2 (IL-2). В некоторых вариантах осуществления в данном документе описаны иллюстративные полипептиды, показанные в таблице 1. В некоторых вариантах осуществления конъюгаты IL-2, описанные в данном документе, представлены в качестве примера в таблице 1.
(Homo sapiens)
(зрелая форма)
(Homo sapiens)
(предшественник)
№ доступа в NCBI: AAB46883.1
X=сайт, содержащий неприродную аминокислоту.
[AzK]=N6-((2-азидоэтокси)-карбонил)-L-лизин с регистрационным номером согласно Химической реферативной службе 1167421-25-1.
[AzK_PEG]=N6-((2-азидоэтокси)-карбонил)-L-лизин, стабильно конъюгированный с PEG с помощью DBCO-опосредованной клик-химии с образованием соединения, содержащего структуру формулы (II) или формулы (III). Например, если указано, PEG5кДа обозначает линейную цепь полиэтиленгликоля со средней молекулярной массой 5 килодальтонов, кэппированную метоксигруппой. Соотношение региоизомеров, образующихся в результате клик-реакции, составляет приблизительно 1:1 или более 1:1. Термин "DBCO" означает химический фрагмент, содержащий дибензоциклооктиновую группу, как, например, содержащий соединение mPEG-DBCO, проиллюстрированное на схеме 1 в примере 2. Иллюстративная структура группы метокси-PEG проиллюстрирована в структуре mPEG-DBCO на схеме 1 в примере 2.
[AzK_L1_PEG]=N6-((2-азидоэтокси)-карбонил)-L-лизин, стабильно конъюгированный с PEG с помощью DBCO-опосредованной клик-химии с образованием соединения, содержащего структуру формулы (IV) или формулы (V). Например, если указано, PEG5кДа обозначает линейную цепь полиэтиленгликоля со средней молекулярной массой 5 килодальтонов, кэппированную метоксигруппой. Соотношение региоизомеров, образующихся в результате клик-реакции, составляет приблизительно 1:1 или более 1:1. Термин "DBCO" означает химический фрагмент, содержащий дибензоциклооктиновую группу, как, например, содержащий соединение mPEG-DBCO, проиллюстрированное на схеме 1 в примере 2.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (I):

Формула (I);
где:
Z представляет собой CH2, и Y представляет собой  ;
;
Y представляет собой CH2, и Z представляет собой  ;
;
Z представляет собой CH2, и Y представляет собой  ; или
; или
Y представляет собой CH2, и Z представляет собой  ;
;
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку.
Здесь и по всему данному документу термин "конъюгат IL-2" охватывает фармацевтически приемлемые соли, сольваты и гидраты указанной структуры.
Здесь и по всему данному документу структура формулы (I) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты. В некоторых вариантах осуществления структура формулы (I) или любые ее вариант осуществления или видоизменение представлены в виде ее фармацевтически приемлемой соли. В некоторых вариантах осуществления структура формулы (I) или любые ее вариант осуществления или видоизменение представлены в виде ее сольвата. В некоторых вариантах осуществления структура формулы (I) или любые ее вариант осуществления или видоизменение представлены в виде ее гидрата. В некоторых вариантах осуществления структура формулы (I) или любые ее вариант осуществления или видоизменение представлены в виде свободного основания.
В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 Z представляет собой CH2, и Y представляет собой  . В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 Y представляет собой CH2, и Z представляет собой
. В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 Y представляет собой CH2, и Z представляет собой  . В некоторых вариантах осуществления способа, описанного в данном документе, Z представляет собой CH2, и Y представляет собой
. В некоторых вариантах осуществления способа, описанного в данном документе, Z представляет собой CH2, и Y представляет собой  . В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 Z представляет собой CH2, и Y представляет собой
. В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 Z представляет собой CH2, и Y представляет собой  . В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 Y представляет собой CH2, и Z представляет собой
. В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 Y представляет собой CH2, и Z представляет собой  . Здесь и по всему данному документу варианты осуществления Z и Y также охватывают их фармацевтически приемлемые соль, сольват или гидрат.
. Здесь и по всему данному документу варианты осуществления Z и Y также охватывают их фармацевтически приемлемые соль, сольват или гидрат.
В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 20 кДа и 30 кДа. В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 10 кДа. В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 15 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, при этом в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 20 кДа. В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 25 кДа. В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 30 кДа. В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 35 кДа. В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 40 кДа. В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 45 кДа. В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 50 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, при этом в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 60 кДа.
В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 положение структуры формулы (I) в аминокислотной последовательности конъюгата IL-2 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71, где положение структуры формулы (I) в аминокислотной последовательности конъюгата IL-2 относится к положениям в SEQ ID NO: 3. В некоторых вариантах осуществления способа, описанного в данном документе, в конъюгате IL-2 положение структуры формулы (I) в аминокислотной последовательности конъюгата IL-2 выбрано из F41, E61 и P64, где положение структуры формулы (I) в аминокислотной последовательности конъюгата IL-2 относится к положениям в SEQ ID NO: 3.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 15-19, где [AzK_PEG] имеет структуру формулы (II) или формулы (III) или представляет собой смесь формулы (II) и формулы (III):

Формула (II);
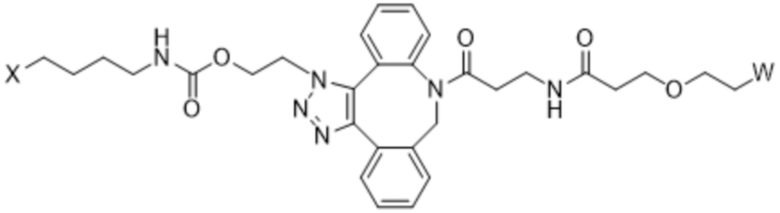
Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку.
В некоторых вариантах осуществления конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
Здесь и по всему данному документу структура формулы (II) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты. Здесь и по всему данному документу структура формулы (III) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты.
В некоторых вариантах осуществления [AzK_PEG] представляет собой смесь формулы (II) и формулы (III).
В некоторых вариантах осуществления [AzK_PEG] имеет структуру формулы (II):

Формула (II)
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 15. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 16. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 17. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 18. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 19. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления W в структуре формулы (II) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления [AzK_PEG] имеет структуру формулы (III):

Формула (III)
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 15. В некоторых вариантах осуществления W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 16. В некоторых вариантах осуществления W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 17. В некоторых вариантах осуществления W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 18. В некоторых вариантах осуществления W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 19. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (III) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления способов, раскрытых в данном документе, применяют конъюгат IL-2, имеющий аминокислотную последовательность, выбранную из любой из SEQ ID NO: 15, 16, 17, 18 и 19, где [AzK_PEG] содержит группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 15, 16, 17, 18 и 19, где [AzK_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 15, 16, 17, 18 и 19, где [AzK_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 10 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 15, 16, 17, 18 и 19, где [AzK_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 15 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 15, 16, 17, 18 и 19, где [AzK_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 20 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 15, 16, 17, 18 и 19, где [AzK_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 25 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 15, 16, 17, 18 и 19, где [AzK_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 30 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 15, 16, 17, 18 и 19, где [AzK_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 35 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 15, 16, 17, 18 и 19, где [AzK_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 40 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 15, 16, 17, 18 и 19, где [AzK_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 45 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 15, 16, 17, 18 и 19, где [AzK_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 50 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 15, 16, 17, 18 и 19, где [AzK_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 60 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 15, 16, 17, 18 и 19, где [AzK_PEG] содержит группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа, и где группа PEG представляет собой группу метокси-PEG, линейную группу метокси-PEG или разветвленную группу метокси-PEG.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 20-24, где [AzK_PEG5кДа] имеет структуру формулы (II) или формулы (III) или представляет собой смесь формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 20. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 21. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 22. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 23. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 24.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором [AzK_PEG5кДа] имеет структуру формулы (II):

Формула (II)
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 20. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 21. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 22. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 23. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 24.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором [AzK_PEG5кДа] имеет структуру формулы (III):

Формула (III);
или ее фармацевтически приемлемых соли, сольвата или гидрата. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 20. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 21. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 22. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 23. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 24.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 25-29, где [AzK_PEG30кДа] имеет структуру формулы (II) или формулы (III) или представляет собой смесь структур формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку.
В некоторых вариантах осуществления конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 25. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 26. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 27. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 28. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 29.
В некоторых вариантах осуществления в способах, раскрытых в данном документе, применяют конъюгат IL-2, в котором [AzK_PEG30кДа] имеет структуру формулы (II):

Формула (II);
или ее фармацевтически приемлемых соли, сольвата или гидрата. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 25. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 26. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 27. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 28. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 29.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором [AzK_PEG30кДа] имеет структуру формулы (III):

Формула (III)
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 25. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 26. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 27. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 28. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 29.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 15-19, где [AzK_PEG] представляет собой смесь структур формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку.
В некоторых вариантах осуществления конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG] в конъюгате IL-2, составляет приблизительно 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG] в конъюгате IL-2, составляет более 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG] в конъюгате IL-2, составляет менее 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W представляет собой линейную или разветвленную группу PEG. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W представляет собой линейную группу PEG. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W представляет собой разветвленную группу PEG. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W представляет собой группу метокси-PEG. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором группа метокси-PEG является линейной или разветвленной. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором группа метокси-PEG является линейной. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором группа метокси-PEG является разветвленной.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 20-24, где [AzK_PEG5кДа] представляет собой смесь структур формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или ее фармацевтически приемлемых соли, сольвата или гидрата.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG5кДа] в конъюгате IL-2, составляет приблизительно 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG5кДа] в конъюгате IL-2, составляет более 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG5кДа] в конъюгате IL-2, составляет менее 1:1.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 25-29, где [AzK_PEG30кДа] представляет собой смесь структур формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или ее фармацевтически приемлемых соли, сольвата или гидрата.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG30кДа] в конъюгате IL-2, составляет приблизительно 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG30кДа] в конъюгате IL-2, составляет более 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG30кДа] в конъюгате IL-2, составляет менее 1:1.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, описанный в данном документе, содержащий структуру формулы (II) или формулы (III) или смесь формулы (II) и формулы (III), где W представляет собой линейную или разветвленную группу PEG. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (II) или формулы (III) представляет собой линейную группу PEG. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (II) или формулы (III) представляет собой разветвленную группу PEG. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (II) или формулы (III) представляет собой группу метокси-PEG. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (II) или формулы (III) представляет собой группу метокси-PEG, которая является линейной или разветвленной. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором группа метокси-PEG в структуре формулы (II) или формулы (III) является линейной. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором группа метокси-PEG в структуре формулы (II) или формулы (III) является разветвленной.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 40-44, где [AzK_L1_PEG] имеет структуру формулы (IV) или формулы (V) или представляет собой смесь формулы (IV) и формулы (V):
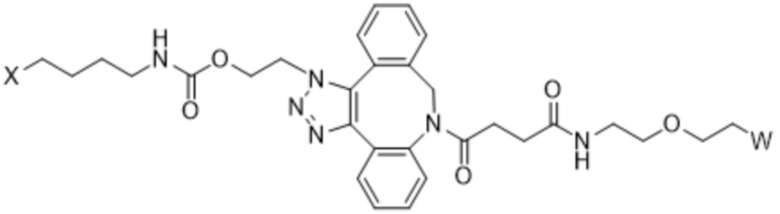
Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Здесь и по всему данному документу структура формулы (IV) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты. Здесь и по всему данному документу структура формулы (V) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором [AzK_L1_PEG] представляет собой смесь формулы (IV) и формулы (V).
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором [AzK_L1_PEG] имеет структуру формулы (IV):
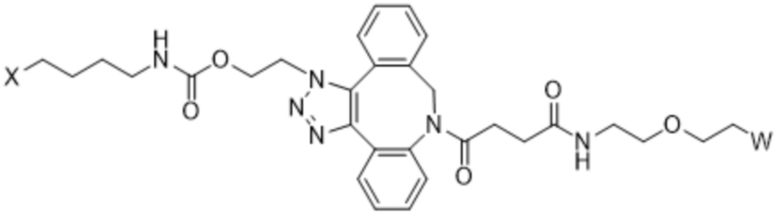
Формула (IV)
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 40. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 41. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 42. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 43. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 44. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором [AzK_L1_PEG] имеет структуру формулы (V):

Формула (V)
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 40. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 41. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 42. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 43. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 40, 41, 42, 43 и 44, где [AzK_L1_PEG] содержит группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 40, 41, 42, 43 и 44, где [AzK_L1_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 40, 41, 42, 43 и 44, где [AzK_L1_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 10 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 40, 41, 42, 43 и 44, где [AzK_L1_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 15 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 40, 41, 42, 43 и 44, где [AzK_L1_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 20 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 40, 41, 42, 43 и 44, где [AzK_L1_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 25 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 40, 41, 42, 43 и 44, где [AzK_L1_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 30 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 40, 41, 42, 43 и 44, где [AzK_L1_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 35 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 40, 41, 42, 43 и 44, где [AzK_L1_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 40 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 40, 41, 42, 43 и 44, где [AzK_L1_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 45 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 40, 41, 42, 43 и 44, где [AzK_L1_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 50 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 40, 41, 42, 43 и 44, где [AzK_L1_PEG] содержит группу PEG, имеющую среднюю молекулярную массу 60 кДа. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность, выбранную из любой из SEQ ID NO: 40, 41, 42, 43 и 44, где [AzK_L1_PEG] содержит группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа, и где группа PEG представляет собой группу метокси-PEG, линейную группу метокси-PEG или разветвленную группу метокси-PEG.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 45-49, где [AzK_L1_PEG5кДа] имеет структуру формулы (IV) или формулы (V) или представляет собой смесь формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку.
В некоторых вариантах осуществления конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 45. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 46. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 47. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 48. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 49.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором [AzK_L1_PEG5кДа] имеет структуру формулы (IV):

Формула (IV);
или ее фармацевтически приемлемых соли, сольвата или гидрата. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 45. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 46. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 47. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 48. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 49.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором [AzK_L1_PEG5кДа] имеет структуру формулы (V):

Формула (V)
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 45. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 46. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 47. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 48. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 49.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 50-54, где [AzK_L1_PEG30кДа] имеет структуру формулы (IV) или формулы (V) или представляет собой смесь структур формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 50. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 51. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 52. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 53. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 54.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором [AzK_L1_PEG30кДа] имеет структуру формулы (IV):

Формула (IV);
или ее фармацевтически приемлемых соли, сольвата или гидрата. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 50. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 51. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 52. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 53. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 54.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором [AzK_L1_PEG30кДа] имеет структуру формулы (V):

Формула (V)
В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 50. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 51. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 52. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 53. В некоторых вариантах осуществления конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 54.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 40-44, где [Azk_L1_PEG] представляет собой смесь структур формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или ее фармацевтически приемлемых соли, сольвата или гидрата.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG] в конъюгате IL-2, составляет приблизительно 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG] в конъюгате IL-2, составляет более 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG] в конъюгате IL-2, составляет менее 1:1.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 45-49, где [AzK_L1_PEG5кДа] представляет собой смесь структур формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или ее фармацевтически приемлемых соли, сольвата или гидрата.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG5кДа] в конъюгате IL-2, составляет приблизительно 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG5кДа] в конъюгате IL-2, составляет более 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG5кДа] в конъюгате IL-2, составляет менее 1:1.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 50-54, где [AzK_L1_PEG30кДа] представляет собой смесь структур формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или ее фармацевтически приемлемых соли, сольвата или гидрата.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG30кДа] в конъюгате IL-2, составляет приблизительно 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG30кДа] в конъюгате IL-2, составляет более 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG30кДа] в конъюгате IL-2, составляет менее 1:1.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 10 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 15 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 20 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 25 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 35 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 40 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 45 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 50 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 55 кДа. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу PEG, имеющую среднюю молекулярную массу 60 кДа.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, описанный в данном документе, содержащий структуру формулы (IV) или формулы (V) или смесь формулы (IV) и формулы (V), где W представляет собой линейную или разветвленную группу PEG. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой линейную группу PEG. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой разветвленную группу PEG. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу метокси-PEG. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором W в структуре формулы (IV) или формулы (V) представляет собой группу метокси-PEG, которая является линейной или разветвленной. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором группа метокси-PEG в структуре формулы (IV) или формулы (V) является линейной. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором группа метокси-PEG в структуре формулы (IV) или формулы (V) является разветвленной.
Что касается конъюгатов IL-2, применяемых в способах, описанных в данном документе, иллюстративная структура группы метокси-PEG проиллюстрирована в структуре mPEG-DBCO на схеме 1 в примере 2. Иллюстративные структуры группы метокси-PEG проиллюстрированы в приведенных ниже структурах mPEG-DBCO:
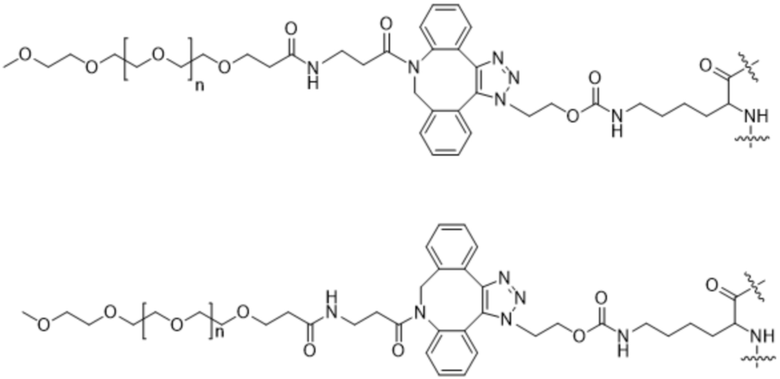
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 представляет собой конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VI) или формулы (VII) или смесью формулы (VI) и формулы (VII):
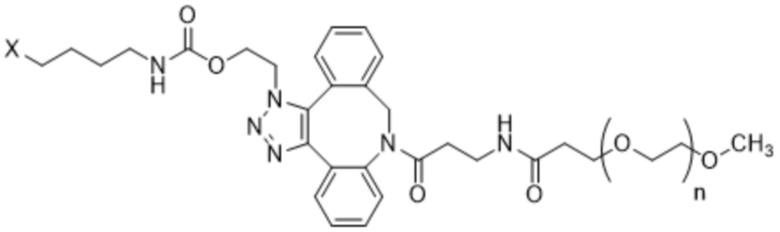
Формула (VI),
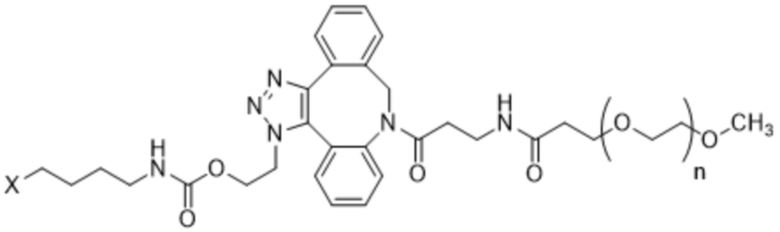
Формула (VII),
где:
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
X имеет структуру  ,
,
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку.
В некоторых вариантах осуществления конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
Здесь и по всему данному документу структура формулы (VI) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты. Здесь и по всему данному документу структура формулы (VII) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты.
В некоторых вариантах осуществления n в соединениях формулы (VI) и формулы (VII) находится в диапазоне от приблизительно 5 до приблизительно 4600, или от приблизительно 10 до приблизительно 4000, или от приблизительно 20 до приблизительно 3000, или от приблизительно 100 до приблизительно 3000, или от приблизительно 100 до приблизительно 2900, или от приблизительно 150 до приблизительно 2900, или от приблизительно 125 до приблизительно 2900, или от приблизительно 100 до приблизительно 2500, или от приблизительно 100 до приблизительно 2000, или от приблизительно 100 до приблизительно 1900, или от приблизительно 100 до приблизительно 1850, или от приблизительно 100 до приблизительно 1750, или от приблизительно 100 до приблизительно 1650, или от приблизительно 100 до приблизительно 1500, или от приблизительно 100 до приблизительно 1400, или от приблизительно 100 до приблизительно 1300, или от приблизительно 100 до приблизительно 1250, или от приблизительно 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575. В некоторых вариантах осуществления n в соединениях формулы (VI) и формулы (VII) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71, где положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 относится к положениям в SEQ ID NO: 3. В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71. В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение K34. В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение F41. В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение F43. В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение K42. В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение E61. В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение P64. В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение R37. В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение T40. В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение E67. В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение Y44. В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение V68. В некоторых вариантах осуществления положение структуры формулы (VI), формулы (VII) или смеси формулы (VI) и формулы (VII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение L71.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (VI) и количества структуры формулы (VII), составляющих общее количество конъюгата IL-2, составляет приблизительно 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (VI) и количества структуры формулы (VII), составляющих общее количество конъюгата IL-2, составляет более 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (VI) и количества структуры формулы (VII), составляющих общее количество конъюгата IL-2, составляет менее 1:1.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VI) или формулы (VII) или смесью формулы (VI) и формулы (VII), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71, и где n представляет собой целое число от 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575. В некоторых вариантах осуществления n в соединениях формулы (VI) и формулы (VII) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VI) или формулы (VII) или смесью формулы (VI) и формулы (VII), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (VI) и формулы (VII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137 и 1249.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VI) или формулы (VII) или смесью формулы (VI) и формулы (VII), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (VI) и формулы (VII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VI) или формулы (VII) или смесью формулы (VI) и формулы (VII), где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором n в соединениях формулы (VI) и формулы (VII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VI) или формулы (VII) или смесью формулы (VI) и формулы (VII), где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (VI) и формулы (VII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В некоторых вариантах осуществления n в структурах формулы (VI) и формулы (VII) представляет собой такое целое число, что молекулярная масса фрагмента PEG находится в диапазоне от приблизительно 1000 дальтонов до приблизительно 200000 дальтонов, или от приблизительно 2000 дальтонов до приблизительно 150000 дальтонов, или от приблизительно 3000 дальтонов до приблизительно 125000 дальтонов, или от приблизительно 4000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 90000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 80000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 65000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 60000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 30000 дальтонов.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VI) или формулы (VII) или смесью формулы (VI) и формулы (VII), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов, приблизительно 50000 дальтонов, приблизительно 60000 дальтонов, приблизительно 70000 дальтонов, приблизительно 80000 дальтонов, приблизительно 90000 дальтонов, приблизительно 100000 дальтонов, приблизительно 125000 дальтонов, приблизительно 150000 дальтонов, приблизительно 175000 дальтонов или приблизительно 200000 дальтонов.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VI) или формулы (VII) или смесью формулы (VI) и формулы (VII), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов или приблизительно 50000 дальтонов.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 представляет собой конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX):
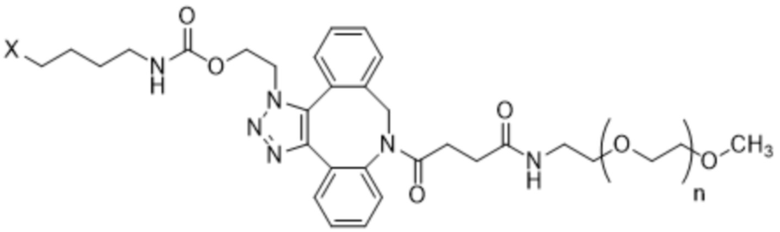
Формула (VIII),
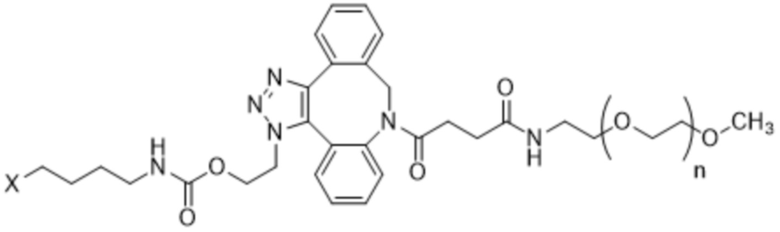
Формула (IX),
где:
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
X имеет структуру  ,
,
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку.
В некоторых вариантах осуществления конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
Здесь и по всему данному документу структура формулы (VIII) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты. Здесь и по всему данному документу структура формулы (IX) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты.
В некоторых вариантах осуществления n в соединениях формулы (VIII) и формулы (IX) находится в диапазоне от приблизительно 5 до приблизительно 4600, или от приблизительно 10 до приблизительно 4000, или от приблизительно 20 до приблизительно 3000, или от приблизительно 100 до приблизительно 3000, или от приблизительно 100 до приблизительно 2900, или от приблизительно 150 до приблизительно 2900, или от приблизительно 125 до приблизительно 2900, или от приблизительно 100 до приблизительно 2500, или от приблизительно 100 до приблизительно 2000, или от приблизительно 100 до приблизительно 1900, или от приблизительно 100 до приблизительно 1850, или от приблизительно 100 до приблизительно 1750, или от приблизительно 100 до приблизительно 1650, или от приблизительно 100 до приблизительно 1500, или от приблизительно 100 до приблизительно 1400, или от приблизительно 100 до приблизительно 1300, или от приблизительно 100 до приблизительно 1250, или от приблизительно 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575. В некоторых вариантах осуществления n в соединениях формулы (VIII) и формулы (IX) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71, где положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 относится к положениям в SEQ ID NO: 3. В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71. В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение K34. В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение F41. В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение F43. В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение K42. В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение E61. В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение P64. В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение R37. В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение T40. В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение E67. В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение Y44. В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение V68. В некоторых вариантах осуществления положение структуры формулы (VIII), формулы (IX) или смеси формулы (VIII) и формулы (IX) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение L71.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (VIII) и количества структуры формулы (IX), составляющих общее количество конъюгата IL-2, составляет приблизительно 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (VIII) и количества структуры формулы (IX), составляющих общее количество конъюгата IL-2, составляет более 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (VIII) и количества структуры формулы (IX), составляющих общее количество конъюгата IL-2, составляет менее 1:1.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71, и где n представляет собой целое число от 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575. В некоторых вариантах осуществления n в соединениях формулы (VIII) и формулы (IX) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (VIII) и формулы (IX) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137 и 1249.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (VIII) и формулы (IX) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX), где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (VIII) и формулы (IX) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX), где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (VIII) и формулы (IX) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 представляет собой конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG находится в диапазоне от приблизительно 1000 дальтонов до приблизительно 200000 дальтонов, или от приблизительно 2000 дальтонов до приблизительно 150000 дальтонов, или от приблизительно 3000 дальтонов до приблизительно 125000 дальтонов, или от приблизительно 4000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 90000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 80000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 65000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 60000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 30000 дальтонов.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов, приблизительно 50000 дальтонов, приблизительно 60000 дальтонов, приблизительно 70000 дальтонов, приблизительно 80000 дальтонов, приблизительно 90000 дальтонов, приблизительно 100000 дальтонов, приблизительно 125000 дальтонов, приблизительно 150000 дальтонов, приблизительно 175000 дальтонов или приблизительно 200000 дальтонов. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов или приблизительно 50000 дальтонов.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (X) или формулы (XI) или смесью формулы (X) и формулы (XI):

Формула (X);

Формула (XI);
где:
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
волнистыми линиями указаны ковалентные связи с аминокислотными остатками в SEQ ID NO: 3, которые не заменены.
Здесь и по всему данному документу структура формулы (X) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты. Здесь и по всему данному документу структура формулы (XI) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты. В некоторых вариантах осуществления конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (X) и формуле (XI) предусматривает рацемическую смесь, предусматривает смесь, обогащенную (R), предусматривает смесь, обогащенную (S), предусматривает по сути (R), предусматривает по сути (S), предусматривает (R) или предусматривает (S). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (X) и формуле (XI) предусматривает рацемическую смесь. В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (X) и формуле (XI) предусматривает смесь, обогащенную (R). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (X) и формуле (XI) предусматривает смесь, обогащенную (S). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (X) и формуле (XI) предусматривает по сути (R). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (X) и формуле (XI) предусматривает по сути (S). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (X) и формуле (XI) предусматривает (R). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (X) и формуле (XI) предусматривает (S).
В некоторых вариантах осуществления n в соединениях формулы (X) и формулы (XI) находится в диапазоне от приблизительно 5 до приблизительно 4600, или от приблизительно 10 до приблизительно 4000, или от приблизительно 20 до приблизительно 3000, или от приблизительно 100 до приблизительно 3000, или от приблизительно 100 до приблизительно 2900, или от приблизительно 150 до приблизительно 2900, или от приблизительно 125 до приблизительно 2900, или от приблизительно 100 до приблизительно 2500, или от приблизительно 100 до приблизительно 2000, или от приблизительно 100 до приблизительно 1900, или от приблизительно 100 до приблизительно 1850, или от приблизительно 100 до приблизительно 1750, или от приблизительно 100 до приблизительно 1650, или от приблизительно 100 до приблизительно 1500, или от приблизительно 100 до приблизительно 1400, или от приблизительно 100 до приблизительно 1300, или от приблизительно 100 до приблизительно 1250, или от приблизительно 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575. В некоторых вариантах осуществления n в соединениях формулы (X) и формулы (XI) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
В некоторых вариантах осуществления положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71, где положение структуры формулы (X), формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 относится к положениям в SEQ ID NO: 3. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71. В некоторых вариантах осуществления положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение K34. В некоторых вариантах осуществления положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение F41. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение F43. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение K42. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение E61. В некоторых вариантах осуществления положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение P64. В некоторых вариантах осуществления положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение R37. В некоторых вариантах осуществления положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение T40. В некоторых вариантах осуществления положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение E67. В некоторых вариантах осуществления положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение Y44. В некоторых вариантах осуществления положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение V68. В некоторых вариантах осуществления положение структуры формулы (X) или формулы (XI) или смеси формулы (X) и формулы (XI) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение L71.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (X) и количества структуры формулы (XI), составляющих общее количество конъюгата IL-2, составляет приблизительно 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (X) и количества структуры формулы (XI), составляющих общее количество конъюгата IL-2, составляет более 1:1. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором соотношение количества структуры формулы (X) и количества структуры формулы (XI), составляющих общее количество конъюгата IL-2, составляет менее 1:1.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (X) или формулы (XI) или смесью формулы (X) и формулы (XI), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71, и где n представляет собой целое число от 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575. В некоторых вариантах осуществления n в соединениях формулы (VI) и формулы (VII) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (X) или формулы (XI) или смесью формулы (X) и формулы (XI), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (X) и формулы (XI) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137 и 1249.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (X) или формулы (XI) или смесью формулы (X) и формулы (XI), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (X) и формулы (XI) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (X) или формулы (XI) или смесью формулы (X) и формулы (XI), где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления в способах применяют конъюгат IL-2, в котором n в соединениях формулы (X) и формулы (XI) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (X) или формулы (XI) или смесью формулы (X) и формулы (XI), где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (X) и формулы (XI) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В некоторых вариантах осуществления n в структурах формулы (X) и формулы (XI) представляет собой такое целое число, что молекулярная масса фрагмента PEG находится в диапазоне от приблизительно 1000 дальтонов до приблизительно 200000 дальтонов, или от приблизительно 2000 дальтонов до приблизительно 150000 дальтонов, или от приблизительно 3000 дальтонов до приблизительно 125000 дальтонов, или от приблизительно 4000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 90000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 80000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 65000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 60000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 30000 дальтонов.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (X) или формулы (XI) или смесью формулы (X) и формулы (XI), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов, приблизительно 50000 дальтонов, приблизительно 60000 дальтонов, приблизительно 70000 дальтонов, приблизительно 80000 дальтонов, приблизительно 90000 дальтонов, приблизительно 100000 дальтонов, приблизительно 125000 дальтонов, приблизительно 150000 дальтонов, приблизительно 175000 дальтонов или приблизительно 200000 дальтонов.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (X) или формулы (XI) или смесью формулы (X) и формулы (XI), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов или приблизительно 50000 дальтонов.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 представляет собой конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XII) или формулы (XIII) или смесью формулы (XII) и формулы (XIII):

Формула (XII);

Формула (XIII);
где:
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
волнистыми линиями указаны ковалентные связи с аминокислотными остатками в SEQ ID NO: 3, которые не заменены.
Здесь и по всему данному документу структура формулы (XII) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты. Здесь и по всему данному документу структура формулы (XIII) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты. В некоторых вариантах осуществления конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XII) и формуле (XIII) предусматривает рацемическую смесь, предусматривает смесь, обогащенную (R), предусматривает смесь, обогащенную (S), предусматривает по сути (R), предусматривает по сути (S), предусматривает (R) или предусматривает (S). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XII) и формуле (XIII) предусматривает рацемическую смесь. В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XII) и формуле (XIII) предусматривает смесь, обогащенную (R). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XII) и формуле (XIII) предусматривает смесь, обогащенную (S). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XII) и формуле (XIII) предусматривает по сути (R). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XII) и формуле (XIII) предусматривает по сути (S). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XII) и формуле (XIII) предусматривает (R). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XII) и формуле (XIII) предусматривает (S).
В некоторых вариантах осуществления n в соединениях формулы (XII) и формулы (XIII) находится в диапазоне от приблизительно 5 до приблизительно 4600, или от приблизительно 10 до приблизительно 4000, или от приблизительно 20 до приблизительно 3000, или от приблизительно 100 до приблизительно 3000, или от приблизительно 100 до приблизительно 2900, или от приблизительно 150 до приблизительно 2900, или от приблизительно 125 до приблизительно 2900, или от приблизительно 100 до приблизительно 2500, или от приблизительно 100 до приблизительно 2000, или от приблизительно 100 до приблизительно 1900, или от приблизительно 100 до приблизительно 1850, или от приблизительно 100 до приблизительно 1750, или от приблизительно 100 до приблизительно 1650, или от приблизительно 100 до приблизительно 1500, или от приблизительно 100 до приблизительно 1400, или от приблизительно 100 до приблизительно 1300, или от приблизительно 100 до приблизительно 1250, или от приблизительно 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575. В некоторых вариантах осуществления n в соединениях формулы (XII) и (XIII) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71, где положение структуры формулы (XII), формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 относится к положениям в SEQ ID NO: 3. В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71. В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение K34. В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение F41. В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение F43. В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение K42. В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение E61. В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение P64. В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение R37. В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение T40. В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение E67. В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение Y44. В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение V68. В некоторых вариантах осуществления положение структуры формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение L71.
В некоторых вариантах осуществления соотношение количества структуры формулы (XII) и количества структуры формулы (XIII), составляющих общее количество конъюгата IL-2, составляет приблизительно 1:1. В некоторых вариантах осуществления соотношение количества структуры формулы (XII) и количества структуры формулы (XIII), составляющих общее количество конъюгата IL-2, составляет более 1:1. В некоторых вариантах осуществления соотношение количества структуры формулы (XII) и количества структуры формулы (XIII), составляющих общее количество конъюгата IL-2, составляет менее 1:1.
В некоторых вариантах осуществления в данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XII) или формулы (XIII) или смесью формулы (XII) и формулы (XIII), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71, и где n представляет собой целое число от 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575. В некоторых вариантах осуществления n в соединениях формулы (XII) и формулы (XIII) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XII) или формулы (XIII) или смесью формулы (XII) и формулы (XIII), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (XII) и формулы (XIII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137 и 1249.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XII) или формулы (XIII) или смесью формулы (XII) и формулы (XIII), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (XII) и формулы (XIII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XII) или формулы (XIII) или смесью формулы (XII) и формулы (XIII), где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (XII) и формулы (XIII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XII) или формулы (XIII) или смесью формулы (XII) и формулы (XIII), где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления n в соединениях формулы (XII) и формулы (XIII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В некоторых вариантах осуществления n в структурах формулы (XII) или формулы (XIII) или смеси формулы (XII) и формулы (XIII) представляет собой такое целое число, что молекулярная масса фрагмента PEG находится в диапазоне от приблизительно 1000 дальтонов до приблизительно 200000 дальтонов, или от приблизительно 2000 дальтонов до приблизительно 150000 дальтонов, или от приблизительно 3000 дальтонов до приблизительно 125000 дальтонов, или от приблизительно 4000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 90000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 80000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 65000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 60000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 30000 дальтонов.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XII) или формулы (XIII) или смесью формулы (XII) и формулы (XIII), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов, приблизительно 50000 дальтонов, приблизительно 60000 дальтонов, приблизительно 70000 дальтонов, приблизительно 80000 дальтонов, приблизительно 90000 дальтонов, приблизительно 100000 дальтонов, приблизительно 125000 дальтонов, приблизительно 150000 дальтонов, приблизительно 175000 дальтонов или приблизительно 200000 дальтонов. В данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XII) или формулы (XIII) или смесью формулы (XII) и формулы (XIII), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов или приблизительно 50000 дальтонов.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких ингибиторов PD-1, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом аминокислотный остаток в E61 или P64 в конъюгате IL-2 заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX):

Формула (VIII);

(IX);
где:
n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 15000 дальтонов до приблизительно 60000 дальтонов; и
X имеет структуру  ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку.
В некоторых вариантах осуществления конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
В некоторых вариантах осуществления аминокислотный остаток в E61 в конъюгате IL-2 заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX), и при этом n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов. В некоторых вариантах осуществления n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 30000 дальтонов. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой пембролизумаб, ниволумаб или цемиплимаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой пембролизумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой ниволумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой цемиплимаб.
В некоторых вариантах осуществления аминокислотный остаток в P64 в конъюгате IL-2 заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX), и при этом n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов. В некоторых вариантах осуществления n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 30000 дальтонов. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой пембролизумаб, ниволумаб или цемиплимаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой пембролизумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой ниволумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой цемиплимаб.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких ингибиторов PD-1, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом аминокислотный остаток в E61 или P64 в конъюгате IL-2 заменен структурой формулы (VI) или формулы (VII) или смесью формулы (VI) и формулы (VII):

Формула (VI);

(VII);
где:
n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 15000 дальтонов до приблизительно 60000 дальтонов; и
X имеет структуру  ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку.
В некоторых вариантах осуществления конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
В некоторых вариантах осуществления аминокислотный остаток в E61 в конъюгате IL-2 заменен структурой формулы (VI) или формулы (VII) или смесью формулы (VI) и формулы (VII), и при этом n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов. В некоторых вариантах осуществления n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 30000 дальтонов. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой пембролизумаб, ниволумаб или цемиплимаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой пембролизумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой ниволумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой цемиплимаб.
В некоторых вариантах осуществления аминокислотный остаток в P64 в конъюгате IL-2 заменен структурой формулы (VI) или формулы (VII) или смесью формулы (VI) и формулы (VII), и при этом n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов. В некоторых вариантах осуществления n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 30000 дальтонов. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой пембролизумаб, ниволумаб или цемиплимаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой пембролизумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой ниволумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой цемиплимаб.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 представляет собой конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 1, SEQ ID NO: 3 или SEQ ID NO: 4, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен цистеином, ковалентно связанным с группой PEG. В некоторых вариантах осуществления группа PEG имеет молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа. В некоторых вариантах осуществления группа PEG имеет молекулярную массу 5 кДа. В некоторых вариантах осуществления группа PEG имеет молекулярную массу 10 кДа. В некоторых вариантах осуществления группа PEG имеет молекулярную массу 15 кДа. В некоторых вариантах осуществления группа PEG имеет молекулярную массу 20 кДа. В некоторых вариантах осуществления группа PEG имеет молекулярную массу 25 кДа. В некоторых вариантах осуществления группа PEG имеет молекулярную массу 30 кДа. В некоторых вариантах осуществления группа PEG имеет молекулярную массу 35 кДа. В некоторых вариантах осуществления группа PEG имеет молекулярную массу 40 кДа. В некоторых вариантах осуществления группа PEG имеет молекулярную массу 45 кДа. В некоторых вариантах осуществления группа PEG имеет молекулярную массу 50 кДа. В некоторых вариантах осуществления группа PEG имеет молекулярную массу 60 кДа. В некоторых вариантах осуществления конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, и по меньшей мере один аминокислотный остаток в конъюгате IL-2, который заменен цистеином, выбран из K34, T36, R37, T40, F41, K42, F43, Y44, E60, E61, E67, K63, P64, V68, L71 и Y106. В некоторых вариантах осуществления конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, и по меньшей мере один аминокислотный остаток в конъюгате IL-2, который заменен цистеином, выбран из K34, T40, F41, K42, Y44, E60, E61, E67, K63, P64, V68 и L71. В некоторых вариантах осуществления конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 4, и по меньшей мере один аминокислотный остаток в конъюгате IL-2, который заменен цистеином, выбран из K35, T37, R38, T41, F42, K43, F44, Y45, E61, E62, E68, K64, P65, V69, L72 и Y107.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 представляет собой конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, в которой по меньшей мере один отличный от лизина остаток заменен лизином, содержащим линкер и водорастворимый полимер. В некоторых вариантах осуществления водорастворимый полимер представляет собой группу PEG.
В некоторых вариантах осуществления конъюгат IL-2 содержит группу PEG, ковалентно связанную посредством невысвобождаемой связи. В некоторых вариантах осуществления конъюгат IL-2 содержит невысвобождаемую ковалентно связанную группу PEG.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 имеет SEQ ID NO: 3, где отличная от лизина аминокислота в конъюгате IL-2 заменена остатком лизина, и где остаток лизина содержит один или несколько водорастворимых полимеров и ковалентный линкер. В некоторых вариантах осуществления остаток лизина расположен в области K34-Y106 в SEQ ID NO: 3. В некоторых вариантах осуществления остаток лизина расположен в K34. В некоторых вариантах осуществления остаток лизина расположен в F41. В некоторых вариантах осуществления остаток лизина расположен в F43. В некоторых вариантах осуществления остаток лизина расположен в K42. В некоторых вариантах осуществления остаток лизина расположен в E61. В некоторых вариантах осуществления остаток лизина расположен в P64. В некоторых вариантах осуществления остаток лизина расположен в R37. В некоторых вариантах осуществления остаток лизина расположен в T40. В некоторых вариантах осуществления остаток лизина расположен в E67. В некоторых вариантах осуществления остаток лизина расположен в Y44. В некоторых вариантах осуществления остаток лизина расположен в V68. В некоторых вариантах осуществления остаток лизина расположен в L71.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 имеет SEQ ID NO: 3, где отличная от лизина аминокислота в конъюгате IL-2 заменена остатком лизина, и где остаток лизина содержит один или несколько водорастворимых полимеров и ковалентный линкер. В некоторых вариантах осуществления остаток лизина расположен в области K34-Y106 в SEQ ID NO: 3. В некоторых вариантах осуществления остаток лизина расположен в K34. В некоторых вариантах осуществления остаток лизина расположен в F41. В некоторых вариантах осуществления остаток лизина расположен в F43. В некоторых вариантах осуществления остаток лизина расположен в K42. В некоторых вариантах осуществления остаток лизина расположен в E61. В некоторых вариантах осуществления остаток лизина расположен в P64. В некоторых вариантах осуществления остаток лизина расположен в R37. В некоторых вариантах осуществления остаток лизина расположен в T40. В некоторых вариантах осуществления остаток лизина расположен в E67. В некоторых вариантах осуществления остаток лизина расположен в Y44. В некоторых вариантах осуществления остаток лизина расположен в V68. В некоторых вариантах осуществления остаток лизина расположен в L71.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 представляет собой вариант интерлейкина-2 (IL-2), где отличная от лизина аминокислота в аминокислотной последовательности варианта IL-2 заменена аминокислотой, содержащей (a) лизин; (b) ковалентный линкер и (3) один или несколько водорастворимых полимеров. В некоторых вариантах осуществления один или несколько водорастворимых полимеров содержат группу PEG.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 представляет собой конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XIV) или формулы (XV) или смесью формулы (XIV) и формулы (XV):
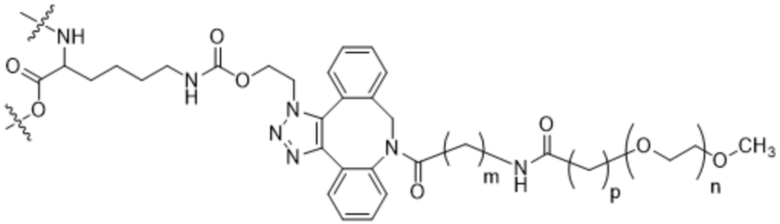
Формула (XIV);
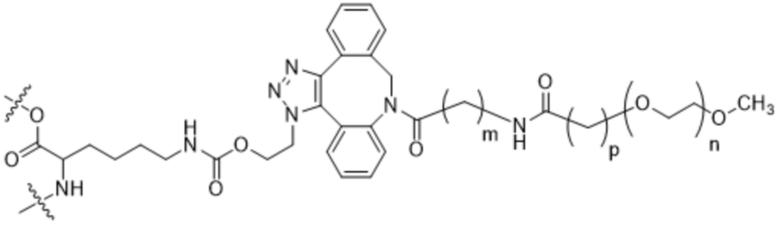
Формула (XV);
где:
m представляет собой целое число от 0 до 20;
p представляет собой целое число от 0 до 20;
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
волнистыми линиями указаны ковалентные связи с аминокислотными остатками в SEQ ID NO: 3, которые не заменены.
Здесь и по всему данному документу структура формулы (XIV) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты. Здесь и по всему данному документу структура формулы (XV) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты. В некоторых вариантах осуществления конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XIV) и формуле (XV) предусматривает рацемическую смесь, предусматривает смесь, обогащенную (R), предусматривает смесь, обогащенную (S), предусматривает по сути (R), предусматривает по сути (S), предусматривает (R) или предусматривает (S). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XIV) и формуле (XV) предусматривает рацемическую смесь. В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XIV) и формуле (XV) предусматривает смесь, обогащенную (R). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XIV) и формуле (XV) предусматривает смесь, обогащенную (S). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XIV) и формуле (XV) предусматривает по сути (R). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XIV) и формуле (XV) предусматривает по сути (S). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XIV) и формуле (XV) предусматривает (R). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XIV) и формуле (XV) предусматривает (S).
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, в которой m в соединениях формулы (XIV) и формулы (XV) составляет от 0 до 20, или от 1 до 18, или от 1 до 16, или от 1 до 14, или от 1 до 12, или от 1 до 10, или от 1 до 9, или от 1 до 8, или от 1 до 7, или от 1 до 6, или от 1 до 5, или от 1 до 4, или от 1 до 3, или от 1 до 2. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 1. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 2. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 3. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 4. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 5. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 6. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 7. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 8. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 9. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 10. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 11. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 12. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 13. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 14. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 15. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 16. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 17. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 18. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 19. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 20.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, в которой р в соединениях формулы (XIV) и формулы (XV) составляет от 1 до 20, или от 1 до 18, или от 1 до 16, или от 1 до 14, или от 1 до 12, или от 1 до 10, или от 1 до 9, или от 1 до 8, или от 1 до 7, или от 1 до 6, или от 1 до 5, или от 1 до 4, или от 1 до 3, или от 1 до 2. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 1. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 2. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 3. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 4. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 5. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 6. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 7. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 8. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 9. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 10. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 11. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 12. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 13. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 14. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 15. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XIV) и формулы (XV) равняется 16. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 17. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 18. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 19. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, p в соединениях формулы (XIV) и формулы (XV) равняется 20.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, в которой n в соединениях формулы (XIV) и формулы (XV) находится в диапазоне от приблизительно 5 до приблизительно 4600, или от приблизительно 10 до приблизительно 4000, или от приблизительно 20 до приблизительно 3000, или от приблизительно 100 до приблизительно 3000, или от приблизительно 100 до приблизительно 2900, или от приблизительно 150 до приблизительно 2900, или от приблизительно 125 до приблизительно 2900, или от приблизительно 100 до приблизительно 2500, или от приблизительно 100 до приблизительно 2000, или от приблизительно 100 до приблизительно 1900, или от приблизительно 100 до приблизительно 1850, или от приблизительно 100 до приблизительно 1750, или от приблизительно 100 до приблизительно 1650, или от приблизительно 100 до приблизительно 1500, или от приблизительно 100 до приблизительно 1400, или от приблизительно 100 до приблизительно 1300, или от приблизительно 100 до приблизительно 1250, или от приблизительно 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, в которой m в соединениях формулы (XIV) и формулы (XV) представляет собой целое число от 1 до 6, p представляет собой целое число от 1 до 6, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m представляет собой целое число от 2 до 6, p представляет собой целое число от 2 до 6, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m представляет собой целое число от 2 до 4, p представляет собой целое число от 2 до 4, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 1, p равняется 2, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 2, p равняется 2, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 3, p равняется 2, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 4, p равняется 2, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 5, p равняется 2, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 6, p равняется 2, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 7, p равняется 2, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 8, p равняется 2, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 9, p равняется 2, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 10, p равняется 2, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 11, p равняется 2, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 11, p равняется 2, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 2, p равняется 2, и n представляет собой целое число, выбранное из 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, в которой n в соединениях формулы (XIV) и формулы (XV) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV) или формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71, где положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 относится к положениям в SEQ ID NO: 3. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение K34. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение F41. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение F43. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение K42. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение E61. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение P64. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение R37. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение T40. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение E67. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение Y44. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение V68. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XIV), формулы (XV) или смеси формулы (XIV) и формулы (XV) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение L71.
В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, соотношение количества структуры формулы (XIV) и количества структуры формулы (XV), составляющих общее количество конъюгата IL-2, составляет приблизительно 1:1. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, соотношение количества структуры формулы (XIV) и количества структуры формулы (XV), составляющих общее количество конъюгата IL-2, составляет более 1:1. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, соотношение количества структуры формулы (XIV) и количества структуры формулы (XV), составляющих общее количество конъюгата IL-2, составляет менее 1:1.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 представляет собой конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XIV) или формулы (XV) или смесью формулы (XIV) и формулы (XV), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71, и где n представляет собой целое число от 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, n в соединениях формулы (XIV) и формулы (XV) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 представляет собой конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XIV) или формулы (XV) или смесью формулы (XIV) и формулы (XV), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, n в соединениях формулы (XIV) и формулы (XV) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137 и 1249.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XIV) или формулы (XV) или смесью формулы (XIV) и формулы (XV), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, n в соединениях формулы (XIV) и формулы (XV) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 представляет собой конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XIV) или формулы (XV) или смесью формулы (XIV) и формулы (XV), где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, n в соединениях формулы (XIV) и формулы (XV) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XIV) или формулы (XV) или смесью формулы (XIV) и формулы (XV), где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, n в соединениях формулы (XIV) и формулы (XV) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XIV) или формулы (XV) или смесью формулы (XIV) и формулы (XV), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG находится в диапазоне от приблизительно 1000 дальтонов до приблизительно 200000 дальтонов, или от приблизительно 2000 дальтонов до приблизительно 150000 дальтонов, или от приблизительно 3000 дальтонов до приблизительно 125000 дальтонов, или от приблизительно 4000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 90000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 80000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 65000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 60000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 30000 дальтонов.
В данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XIV) или формулы (XV) или смесью формулы (XIV) и формулы (XV), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов, приблизительно 50000 дальтонов, приблизительно 60000 дальтонов, приблизительно 70000 дальтонов, приблизительно 80000 дальтонов, приблизительно 90000 дальтонов, приблизительно 100000 дальтонов, приблизительно 125000 дальтонов, приблизительно 150000 дальтонов, приблизительно 175000 дальтонов или приблизительно 200000 дальтонов.
В данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XIV) или формулы (XV) или смесью формулы (XIV) и формулы (XV), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов или приблизительно 50000 дальтонов.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XIV) или (XV) или смесью (XIV) и (XV), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, m представляет собой целое число от 1 до 6, p представляет собой целое число от 1 до 6, и n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формул (XIV) и (XV) m равняется 2, p равняется 2, и n представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137 и 1249.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XIV) или формулы (XV) или смесью формулы (XIV) и формулы (XV), где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из E61 и P64, и где m представляет собой целое число от 1 до 6, p представляет собой целое число от 1 до 6, и n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 2, p равняется 2, и n представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XIV) или формулы (XV) или смесью формулы (XIV) и формулы (XV), где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где m представляет собой целое число от 1 до 6, p представляет собой целое число от 1 до 6, и n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 2, p равняется 2, и n представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XIV) или формулы (XV) или смесью формулы (XIV) и формулы (XV), где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где m представляет собой целое число от 1 до 6, p представляет собой целое число от 1 до 6, и n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XIV) и формулы (XV) m равняется 2, p равняется 2, и n представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XVI) или формулы (XVII) или смесью формулы (XVI) и формулы (XVII):
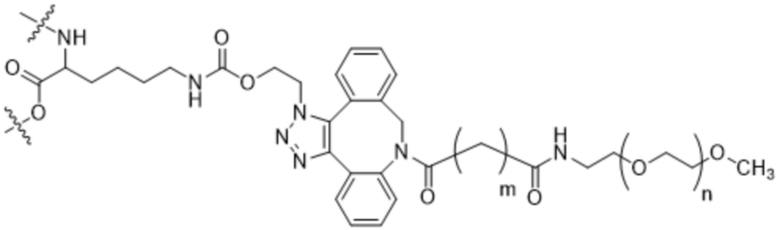
Формула (XVI);
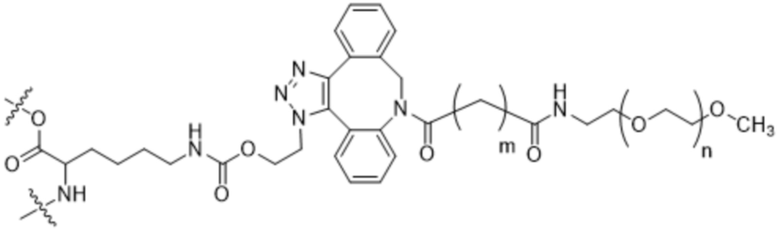
Формула (XVII);
где:
m представляет собой целое число от 0 до 20;
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
волнистыми линиями указаны ковалентные связи с аминокислотными остатками в SEQ ID NO: 3, которые не заменены.
Здесь и по всему данному документу структура формулы (XVI) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты. Здесь и по всему данному документу структура формулы (XVII) охватывает ее фармацевтически приемлемые соли, сольваты или гидраты. В некоторых вариантах осуществления конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XVI) и формуле (XVII) предусматривает рацемическую смесь, предусматривает смесь, обогащенную (R), предусматривает смесь, обогащенную (S), предусматривает по сути (R), предусматривает по сути (S), предусматривает (R) или предусматривает (S). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XVI) и формуле (XVII) предусматривает рацемическую смесь. В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XVI) и формуле (XVII) предусматривает смесь, обогащенную (R). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XVI) и формуле (XVII) предусматривает смесь, обогащенную (S). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XVI) и формуле (XVII) предусматривает по сути (R). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XVI) и формуле (XVII) предусматривает по сути (S). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XVI) и формуле (XVII) предусматривает (R). В некоторых вариантах осуществления стереохимическая конфигурация хирального центра в формуле (XVI) и формуле (XVII) предусматривает (S).
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, в которой m в соединениях формулы (XVI) и формулы (XVII) составляет от 1 до 20, или от 1 до 18, или от 1 до 16, или от 1 до 14, или от 1 до 12, или от 1 до 10, или от 1 до 9, или от 1 до 8, или от 1 до 7, или от 1 до 6, или от 1 до 5, или от 1 до 4, или от 1 до 3, или от 1 до 2. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 1. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 2. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 3. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 4. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 5. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 6. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 7. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 8. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 9. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 10. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 11. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 12. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 13. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 14. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 15. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 16. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 17. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 18. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 19. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, m в соединениях формулы (XVI) и формулы (XVII) равняется 20.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, в которой n в соединениях формулы (XVI) и формулы (XVII) находится в диапазоне от приблизительно 5 до приблизительно 4600, или от приблизительно 10 до приблизительно 4000, или от приблизительно 20 до приблизительно 3000, или от приблизительно 100 до приблизительно 3000, или от приблизительно 100 до приблизительно 2900, или от приблизительно 150 до приблизительно 2900, или от приблизительно 125 до приблизительно 2900, или от приблизительно 100 до приблизительно 2500, или от приблизительно 100 до приблизительно 2000, или от приблизительно 100 до приблизительно 1900, или от приблизительно 100 до приблизительно 1850, или от приблизительно 100 до приблизительно 1750, или от приблизительно 100 до приблизительно 1650, или от приблизительно 100 до приблизительно 1500, или от приблизительно 100 до приблизительно 1400, или от приблизительно 100 до приблизительно 1300, или от приблизительно 100 до приблизительно 1250, или от приблизительно 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, в которой m в соединениях формулы (XVI) и формулы (XVII) представляет собой целое число от 1 до 6, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m представляет собой целое число от 2 до 6, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m представляет собой целое число от 2 до 4, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 1, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 2, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 3, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 4, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 5, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 6, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 7, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 8, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 9, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 10, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 11, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 12, и n представляет собой целое число, выбранное из 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 2, и n представляет собой целое число, выбранное из 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136 и 1137.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, в которой n в соединениях формулы (XVI) и формулы (XVII) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71, где положение структуры формулы (I) в аминокислотной последовательности конъюгата IL-2 относится к положениям в SEQ ID NO: 3. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение K34. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение F41. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение F43. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение K42. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение E61. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение P64. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение R37. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение T40. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение E67. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение Y44. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение V68. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, положение структуры формулы (XVI) или формулы (XVII) или смеси формулы (XVI) и формулы (XVII) в аминокислотной последовательности конъюгата IL-2 под SEQ ID NO: 3 представляет собой положение L71.
В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, соотношение количества структуры формулы (XVI) и количества структуры формулы (XVII), составляющих общее количество конъюгата IL-2, составляет приблизительно 1:1. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, соотношение количества структуры формулы (XVI) и количества структуры формулы (XVII), составляющих общее количество конъюгата IL-2, составляет более 1:1. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, соотношение количества структуры формулы (XVI) и количества структуры формулы (XVII), составляющих общее количество конъюгата IL-2, составляет менее 1:1.
В некоторых вариантах осуществления в способах применяют конъюгат IL-2, содержащий аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2, замененный структурой формулы (XVI) или формулы (XVII) или смесью формулы (XVI) и формулы (XVII), выбран из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71, и где n представляет собой целое число от 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, n в соединениях формулы (XVI) и формулы (XVII) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
В некоторых вариантах осуществления в данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2, замененный структурой формулы (XVI) или формулы (XVII) или смесью формулы (XVI) и формулы (XVII), выбран из F41, F43, K42, E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, n в соединениях формулы (XVI) и формулы (XVII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137 и 1249.
В некоторых вариантах осуществления в данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2, замененный структурой формулы (XVI) или формулы (XVII) или смесью формулы (XVI) и формулы (XVII), выбран из E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, n в соединениях формулы (XVI) и формулы (XVII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
В некоторых вариантах осуществления в данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2, замененный структурой формулы (XVI) или формулы (XVII) или смесью формулы (XVI) и формулы (XVII), который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, n в соединениях формулы (XVI) и формулы (XVII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В некоторых вариантах осуществления в данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2, замененный структурой формулы (XVI) или формулы (XVII) или смесью формулы (XVI) и формулы (XVII), который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, n в соединениях формулы (XVI) и формулы (XVII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В некоторых вариантах осуществления в данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XVI) или формулы (XVII) или смесью формулы (XVI) и формулы (XVII), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG находится в диапазоне от приблизительно 1000 дальтонов до приблизительно 200000 дальтонов, или от приблизительно 2000 дальтонов до приблизительно 150000 дальтонов, или от приблизительно 3000 дальтонов до приблизительно 125000 дальтонов, или от приблизительно 4000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 90000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 80000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 65000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 60000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 30000 дальтонов.
В данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XVI) или формулы (XVII) или смесью формулы (XVI) и формулы (XVII), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов, приблизительно 50000 дальтонов, приблизительно 60000 дальтонов, приблизительно 70000 дальтонов, приблизительно 80000 дальтонов, приблизительно 90000 дальтонов, приблизительно 100000 дальтонов, приблизительно 125000 дальтонов, приблизительно 150000 дальтонов, приблизительно 175000 дальтонов или приблизительно 200000 дальтонов. В данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XVI) или формулы (XVII) или смесью формулы (XVI) и формулы (XVII), где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов или приблизительно 50000 дальтонов.
В некоторых вариантах осуществления в данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2, замененный структурой формулы (XVI) или формулы (XVII) или смесью формулы (XVI) и формулы (XVII), выбран из F41, F43, K42, E61 и P64, m представляет собой целое число от 1 до 6, и n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 2, и n представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137 и 1249.
В некоторых вариантах осуществления в данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2, замененный структурой формулы (XVI) или формулы (XVII) или смесью формулы (XVI) и формулы (XVII), выбран из E61 и P64, и где m представляет собой целое число от 1 до 6, и n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 2, и n представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
В некоторых вариантах осуществления в данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2, замененный структурой формулы (XVI) или формулы (XVII) или смесью формулы (XVI) и формулы (XVII), который заменен, представляет собой E61, и где m представляет собой целое число от 1 до 6, и n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 2, и n представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В некоторых вариантах осуществления в данном документе описаны конъюгаты IL-2, содержащие аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2, замененный структурой формулы (XVI) или формулы (XVII) или смесью формулы (XVI) и формулы (XVII), представляет собой P64, и где m представляет собой целое число от 1 до 6, и n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909. В некоторых вариантах осуществления конъюгата IL-2, описанного в данном документе, в соединениях формулы (XVI) и формулы (XVII) m равняется 2, и n представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910. В некоторых вариантах осуществления n составляет от приблизительно 500 до приблизительно 1000. В некоторых вариантах осуществления n составляет от приблизительно 550 до приблизительно 800. В некоторых вариантах осуществления n составляет приблизительно 681.
В некоторых вариантах осуществления в данном документе описан способ лечения пролиферативного заболевания или состояния у нуждающегося в этом субъекта, который включает введение субъекту терапевтически эффективного количества (a) конъюгата цитокина (например, конъюгата IL-2), описанного в таблице 1, и (b) одного или нескольких дополнительных средств. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 1-98. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 1-84. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 15-29. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 40-54. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 55-69. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 70-84. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 85-98. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 1. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 2. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 3. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 4. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 5. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 6. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 7. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 8. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 9. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 10. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 11. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 12. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 13. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 14. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 15. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 16. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 17. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 18. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 19. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 20. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 21. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 22. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 23. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 24. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 25. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 26. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 27. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 28. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 24. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 25. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 26. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 27. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 28. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 29. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 30. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 31. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 32. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 33. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 34. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 35. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 36. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 37. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 38. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 39. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 40. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 41. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 42. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 43. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 44. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 45. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 46. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 47. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 48. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 49. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 50. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 51. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 52. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 53. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 54. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 55. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 56. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 57. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 58. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 59. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 60. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 61. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 62. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 63. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 64. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 65. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 66. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 67. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 68. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 69. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 70. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 71. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 72. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 73. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 74. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 75. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 76. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 77. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 78. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 79. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 80. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 81. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 82. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 83. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 84. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 85. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 86. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 87. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 88. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 89. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 90. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 91. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 92. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 93. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 94. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 95. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 96. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 97. В некоторых вариантах осуществления конъюгат IL-2 содержит SEQ ID NO: 98.
В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (I). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (II). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (III). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (IV). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (V). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (VI). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (VII). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (VIII). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (IX). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (X). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (XI). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (XII). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (XIII). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (XIV). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (XV). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (XVI). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (XV). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (XVI). В некоторых вариантах осуществления конъюгат IL-2 содержит структуру формулы (XVII).
В некоторых вариантах осуществления конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 86, 88, 90, 92, 94, 96 и 98. В любом из этих вариантов осуществления структура формулы (I) или какого-либо ее видоизменения, как, например, формулы (II) - формулы (XVII) или какого-либо ее видоизменения, встроена в сайт, содержащий неприродную аминокислоту.
В некоторых вариантах осуществления в данном документе описаны конъюгаты IL-2, модифицированные в положении аминокислоты. В некоторых случаях модификация представляет собой замену на природную аминокислоту. В некоторых случаях модификация представляет собой замену на неприродную аминокислоту. В некоторых случаях в данном документе описан выделенный и модифицированный полипептид IL-2, который содержит по меньшей мере одну неприродную аминокислоту. В некоторых случаях полипептид IL-2 характеризуется приблизительно 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичностью последовательности c любой из SEQ ID NO: 3-84. В некоторых случаях полипептид IL-2 характеризуется приблизительно 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% идентичностью последовательности c любой из SEQ ID NO: 3-98.
В некоторых случаях конъюгат IL-2 дополнительно содержит дополнительную мутацию. В некоторых случаях дополнительная мутация находится в положении аминокислоты, выбранном из K35, T37, R38, T41, F42, K43, F44, Y45, E61, E62, E68, K64, P65, V69, L72 и Y107. В таких случаях аминокислота конъюгирована с дополнительным конъюгирующим фрагментом для увеличения периода полужизни в сыворотке крови, стабильности или их комбинации. В качестве альтернативы перед связыванием с дополнительным конъюгирующим фрагментом аминокислоту вначале подвергают мутации по типу замены на природную аминокислоту, такую как лизин, цистеин, гистидин, аргинин, аспарагиновая кислота, глутаминовая кислота, серин, треонин или тирозин; или на неприродную аминокислоту.
В некоторых случаях группа PEG не ограничена конкретной структурой. В некоторых случаях PEG является линейным (например, кэппированным на конце, например, алкокси-PEG или бифункциональным PEG), разветвленным или многолучевым (например, вилкообразным PEG или PEG, присоединенным к полиольной сердцевине), имеет дендритную (или звездообразную) архитектуру, при этом каждый из них имеет или не имеет одну или несколько разрушаемых связей. Более того, внутренняя структура водорастворимого полимера может быть организована в виде любого количества различных повторяющихся паттернов и может быть выбрана из группы, состоящей из гомополимера, чередующегося сополимера, статистического сополимера, блок-сополимера, чередующегося триполимера, статистического триполимера и блок-триполимера.
Как правило, PEG будут содержать ряд мономеров (OCH2CH2) [или мономеров (CH2CH2O), в зависимости от того, как определяется PEG]. Используемое в данном документе количество повторяющихся звеньев обозначается индексом "n" в "(OCH2CH2)n". Таким образом, значение (n) обычно попадает в один или несколько из следующих диапазонов: от 2 до приблизительно 3400, от приблизительно 100 до приблизительно 2300, от приблизительно 100 до приблизительно 2270, от приблизительно 136 до приблизительно 2050, от приблизительно 225 до приблизительно 1930, от приблизительно 450 до приблизительно 1930, от приблизительно 1200 до приблизительно 1930, от приблизительно 568 до приблизительно 2727, от приблизительно 660 до приблизительно 2730, от приблизительно 795 до приблизительно 2730, от приблизительно 795 до приблизительно 2730, от приблизительно 909 до приблизительно 2730 и от приблизительно 1200 до приблизительно 1900. Для любого указанного полимера, для которого известна молекулярная масса, можно определить количество повторяющихся звеньев (т. е. "n"), разделив общую средневесовую молекулярную массу полимера на молекулярную массу повторяющегося мономера.
В некоторых случаях PEG представляет собой кэппированный на конце полимер, то есть полимер, имеющий по меньшей мере один конец, кэппированный относительно инертной группой, такой как низшая C1-6алкоксигруппа или гидроксильная группа. Если полимер представляет собой PEG, например, можно применять метокси-PEG (обычно называемый mPEG), который является линейной формой PEG, где один конец полимера представляет собой метоксигруппу (-OCH3), тогда как другой конец представляет собой гидроксильную или другую функциональную группу, которая необязательно может быть химически модифицирована.
В некоторых вариантах осуществления группа PEG, содержащаяся в конъюгатах IL-2, раскрытых в данном документе, представляет собой линейную или разветвленную группу PEG. В некоторых вариантах осуществления группа PEG представляет собой линейную группу PEG. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу PEG. В некоторых вариантах осуществления группа PEG представляет собой группу метокси-PEG. В некоторых вариантах осуществления группа PEG представляет собой линейную или разветвленную группу метокси-PEG. В некоторых вариантах осуществления группа PEG представляет собой линейную группу метокси-PEG. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу метокси-PEG. В некоторых вариантах осуществления группа PEG представляет собой линейную или разветвленную группу PEG, имеющую среднюю молекулярную массу от приблизительно 100 дальтонов до приблизительно 150000 дальтонов. Иллюстративные диапазоны включают, например, средневесовые молекулярные массы в диапазоне от более 5000 дальтонов до приблизительно 100000 дальтонов, в диапазоне от приблизительно 6000 дальтонов до приблизительно 90000 дальтонов, в диапазоне от приблизительно 10000 дальтонов до приблизительно 85000 дальтонов, в диапазоне от более 10000 дальтонов до приблизительно 85000 дальтонов, в диапазоне от приблизительно 20000 дальтонов до приблизительно 85000 дальтонов, в диапазоне от приблизительно 53000 дальтонов до приблизительно 85000 дальтонов, в диапазоне от приблизительно 25000 дальтонов до приблизительно 120000 дальтонов, в диапазоне от приблизительно 29000 дальтонов до приблизительно 120000 дальтонов, в диапазоне от приблизительно 35000 дальтонов до приблизительно 120000 дальтонов и в диапазоне от приблизительно 40000 дальтонов до приблизительно 120000 дальтонов. Иллюстративные средневесовые молекулярные массы группы PEG включают значения, составляющие приблизительно 100 дальтонов, приблизительно 200 дальтонов, приблизительно 300 дальтонов, приблизительно 400 дальтонов, приблизительно 500 дальтонов, приблизительно 600 дальтонов, приблизительно 700 дальтонов, приблизительно 750 дальтонов, приблизительно 800 дальтонов, приблизительно 900 дальтонов, приблизительно 1000 дальтонов, приблизительно 1500 дальтонов, приблизительно 2000 дальтонов, приблизительно 2200 дальтонов, приблизительно 2500 дальтонов, приблизительно 3000 дальтонов, приблизительно 4000 дальтонов, приблизительно 4400 дальтонов, приблизительно 4500 дальтонов, приблизительно 5000 дальтонов, приблизительно 5500 дальтонов, приблизительно 6000 дальтонов, приблизительно 7000 дальтонов, приблизительно 7500 дальтонов, приблизительно 8000 дальтонов, приблизительно 9000 дальтонов, приблизительно 10000 дальтонов, приблизительно 11000 дальтонов, приблизительно 12000 дальтонов, приблизительно 13000 дальтонов, приблизительно 14000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 22500 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов, приблизительно 50000 дальтонов, приблизительно 55000 дальтонов, приблизительно 60000 дальтонов, приблизительно 65000 дальтонов, приблизительно 70000 дальтонов, приблизительно 75000 дальтонов, приблизительно 80000 дальтонов, приблизительно 90000 дальтонов, приблизительно 95000 дальтонов и приблизительно 100000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную группу PEG, имеющую среднюю молекулярную массу, раскрытую выше. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу PEG, имеющую среднюю молекулярную массу, раскрытую выше. В некоторых вариантах осуществления группа PEG, содержащаяся в конъюгатах IL-2, раскрытых в данном документе, представляет собой линейную или разветвленную группу PEG, имеющую определенную молекулярную массу ± 10%, или 15%, или 20%, или 25%. Например, в объем настоящего изобретения включены конъюгаты IL-2, содержащие группу PEG, имеющую молекулярную массу 30000 Да ± 3000 Да, или 30000 Да ± 4500 Да, или 30000 Да ± 6000 Да.
В некоторых вариантах осуществления группа PEG, содержащаяся в конъюгатах IL-2, раскрытых в данном документе, представляет собой линейную или разветвленную группу PEG, имеющую среднюю молекулярную массу от приблизительно 5000 дальтонов до приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную или разветвленную группу PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 5500 дальтонов, приблизительно 6000 дальтонов, приблизительно 7000 дальтонов, приблизительно 7500 дальтонов, приблизительно 8000 дальтонов, приблизительно 9000 дальтонов, приблизительно 10000 дальтонов, приблизительно 11000 дальтонов, приблизительно 12000 дальтонов, приблизительно 13000 дальтонов, приблизительно 14000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 22500 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов, приблизительно 50000 дальтонов, приблизительно 55000 дальтонов, приблизительно 60000 дальтонов, приблизительно 65000 дальтонов, приблизительно 70000 дальтонов, приблизительно 75000 дальтонов, приблизительно 80000 дальтонов, приблизительно 90000 дальтонов, приблизительно 95000 дальтонов и приблизительно 100000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную или разветвленную группу PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 10000 дальтонов, приблизительно 20000 дальтонов, приблизительно 30000 дальтонов, приблизительно 50000 дальтонов или приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную или разветвленную группу PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 30000 дальтонов, приблизительно 50000 дальтонов или приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную группу PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 10000 дальтонов, приблизительно 20000 дальтонов, приблизительно 30000 дальтонов, приблизительно 50000 дальтонов или приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 10000 дальтонов, приблизительно 20000 дальтонов, приблизительно 30000 дальтонов, приблизительно 50000 дальтонов или приблизительно 60000 дальтонов.
В некоторых вариантах осуществления группа PEG, содержащаяся в конъюгатах IL-2, раскрытых в данном документе, представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу от приблизительно 5000 дальтонов до приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 5500 дальтонов, приблизительно 6000 дальтонов, приблизительно 7000 дальтонов, приблизительно 7500 дальтонов, приблизительно 8000 дальтонов, приблизительно 9000 дальтонов, приблизительно 10000 дальтонов, приблизительно 11000 дальтонов, приблизительно 12000 дальтонов, приблизительно 13000 дальтонов, приблизительно 14000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 22500 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов, приблизительно 50000 дальтонов, приблизительно 55000 дальтонов, приблизительно 60000 дальтонов, приблизительно 65000 дальтонов, приблизительно 70000 дальтонов, приблизительно 75000 дальтонов, приблизительно 80000 дальтонов, приблизительно 90000 дальтонов, приблизительно 95000 дальтонов и приблизительно 100000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 10000 дальтонов, приблизительно 20000 дальтонов, приблизительно 30000 дальтонов, приблизительно 50000 дальтонов или приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 30000 дальтонов, приблизительно 50000 дальтонов или приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 10000 дальтонов, приблизительно 20000 дальтонов, приблизительно 30000 дальтонов, приблизительно 50000 дальтонов или приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 10000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 20000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 30000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 50000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG, содержащаяся в конъюгатах IL-2, раскрытых в данном документе, представляет собой линейную группу метокси-PEG, имеющую определенную молекулярную массу ± 10%, или 15%, или 20%, или 25%. Например, в объем настоящего изобретения включены конъюгаты IL-2, содержащие линейную группу метокси-PEG, имеющую молекулярную массу 30000 Да ± 3000 Да, или 30000 Да ± 4500 Да, или 30000 Да ± 6000 Да.
В некоторых вариантах осуществления группа PEG, содержащаяся в конъюгатах IL-2, раскрытых в данном документе, представляет собой разветвленную группу метокси-PEG, имеющую среднюю молекулярную массу от приблизительно 5000 дальтонов до приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 5500 дальтонов, приблизительно 6000 дальтонов, приблизительно 7000 дальтонов, приблизительно 7500 дальтонов, приблизительно 8000 дальтонов, приблизительно 9000 дальтонов, приблизительно 10000 дальтонов, приблизительно 11000 дальтонов, приблизительно 12000 дальтонов, приблизительно 13000 дальтонов, приблизительно 14000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 22500 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов, приблизительно 50000 дальтонов, приблизительно 55000 дальтонов, приблизительно 60000 дальтонов, приблизительно 65000 дальтонов, приблизительно 70000 дальтонов, приблизительно 75000 дальтонов, приблизительно 80000 дальтонов, приблизительно 90000 дальтонов, приблизительно 95000 дальтонов и приблизительно 100000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 10000 дальтонов, приблизительно 20000 дальтонов, приблизительно 30000 дальтонов, приблизительно 50000 дальтонов или приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 30000 дальтонов, приблизительно 50000 дальтонов или приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 10000 дальтонов, приблизительно 20000 дальтонов, приблизительно 30000 дальтонов, приблизительно 50000 дальтонов или приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов, приблизительно 10000 дальтонов, приблизительно 20000 дальтонов, приблизительно 30000 дальтонов, приблизительно 50000 дальтонов или приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 5000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 10000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 20000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 30000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 50000 дальтонов. В некоторых вариантах осуществления группа PEG представляет собой разветвленную группу метокси-PEG, имеющую среднюю молекулярную массу, составляющую приблизительно 60000 дальтонов. В некоторых вариантах осуществления группа PEG, содержащаяся в конъюгатах IL-2, раскрытых в данном документе, представляет собой разветвленную группу метокси-PEG, имеющую определенную молекулярную массу ± 10%, или 15%, или 20%, или 25%. Например, в объем настоящего изобретения включены конъюгаты IL-2, содержащие разветвленную группу метокси-PEG, имеющую молекулярную массу 30000 Да ± 3000 Да, или 30000 Да ± 4500 Да, или 30000 Да ± 6000 Да.
В некоторых вариантах осуществления иллюстративные группы PEG включают без ограничения линейный или разветвленный дискретный PEG (dPEG) от Quanta BioDesign, Ltd; линейные, разветвленные или вилкообразные PEG от Nektar Therapeutics и Y-образные производные PEG от JenKem Technology.
Химия конъюгации
Химия конъюгации
Различные реакции конъюгации применяют для конъюгации линкеров, конъюгирующих фрагментов и неприродных аминокислот, встроенных в цитокиновые пептиды, описанные в данном документе. Такие реакции конъюгации часто совместимы с водными условиями, как, например, "биоортогональные" реакции. В некоторых вариантах осуществления реакции конъюгации опосредуются химическими реагентами, такими как катализаторы, свет или реакционноспособные химические группы, обнаруживаемые в линкерах, конъюгирующих фрагментах или в неприродных аминокислотах. В некоторых вариантах осуществления реакции конъюгации опосредуются ферментами. В некоторых вариантах осуществления применяемая в данном документе реакция конъюгации описана в Gong, Y., Pan, L. Tett. Lett. 2015, 56, 2123. В некоторых вариантах осуществления применяемая в данном документе реакция конъюгации описана в Chen, X.; Wu. Y-W. Org. Biomol. Chem. 2016, 14, 5417. Раскрытие каждого из этих литературных источников включено в данный документ посредством ссылки.
В некоторых вариантах осуществления, описанных в данном документе, описанная в данном документе реакция конъюгации включает в себя реакцию 1,3-диполярного циклоприсоединения. В некоторых вариантах осуществления реакция 1,3-диполярного циклоприсоединения включает в себя реакцию азида и фосфина ("клик"-реакцию). В некоторых вариантах осуществления реакция конъюгации катализируется медью. В некоторых вариантах осуществления описанная в данном документе реакция конъюгации приводит к получению цитокинового пептида, содержащего линкер или конъюгирующий фрагмент, присоединенный посредством триазола. В некоторых вариантах осуществления описанная в данном документе реакция конъюгации включает в себя реакцию азида с напряженным олефином. В некоторых вариантах осуществления описанная в данном документе реакция конъюгации включает в себя реакцию азида с напряженным алкином. В некоторых вариантах осуществления описанная в данном документе реакция конъюгации включает в себя реакцию азида с циклоалкином, например, DBCO.
В некоторых вариантах осуществления, описанных в данном документе, описанная в данном документе реакция конъюгации включает в себя реакцию, представленную на схеме S1, где X представляет собой положение в конъюгате IL-2, содержащее неприродную аминокислоту, как, например, в любой из SEQ ID NO: 5, 6, 7, 8, 9, 30, 31, 32, 33 и 34.
Схема S1
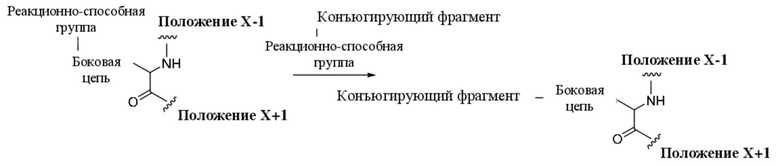
В некоторых вариантах осуществления конъюгирующий фрагмент включает в себя водорастворимый полимер. В некоторых вариантах осуществления реакционноспособная группа включает в себя алкин или азид.
В некоторых вариантах осуществления, описанных в данном документе, описанная в данном документе реакция конъюгации включает в себя реакцию, представленную на схеме S2, где X представляет собой положение в конъюгате IL-2, содержащее неприродную аминокислоту, как, например, в любой из SEQ ID NO: 5, 6, 7, 8, 9, 30, 31, 32, 33 и 34.
Схема S2

В некоторых вариантах осуществления, описанных в данном документе, описанная в данном документе реакция конъюгации включает в себя реакцию, представленную на схеме S3, где X представляет собой положение в конъюгате IL-2, содержащее неприродную аминокислоту, как, например, в любой из SEQ ID NO: 5, 6, 7, 8, 9, 30, 31, 32, 33 и 34.
Схема S3
 ,
,
В некоторых вариантах осуществления, описанных в данном документе, описанная в данном документе реакция конъюгации включает в себя реакцию, представленную на схеме S4, где X представляет собой положение в конъюгате IL-2, содержащее неприродную аминокислоту, как, например, в любой из SEQ ID NO: 5, 6, 7, 8, 9, 30, 31, 32, 33 и 34.
Схема S4
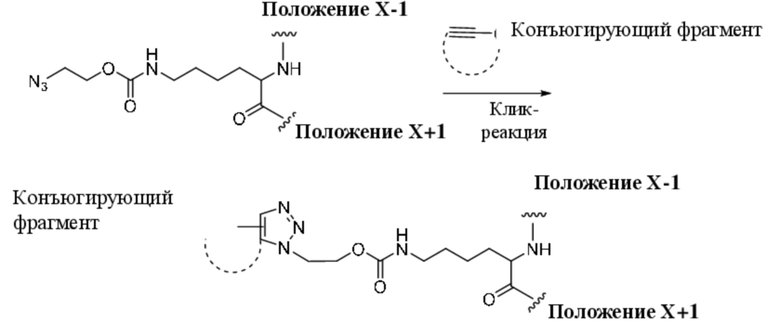
В некоторых вариантах осуществления, описанных в данном документе, описанная в данном документе реакция конъюгации включает в себя реакцию циклоприсоединения между азидным фрагментом, таким как фрагмент, содержащийся в белке, содержащем аминокислотный остаток, полученный из N6-((2-азидоэтокси)-карбонил)-L-лизина (AzK), и напряженным циклоалкином, таким как полученный из DBCO, который представляет собой химический фрагмент, содержащий дибензоциклооктиновую группу. Группы PEG, содержащие фрагмент DBCO, являются коммерчески доступными или могут быть получены способами, известными средним специалистам в данной области. Иллюстративная реакция показана на схемах S5 и S6.
Схема S5
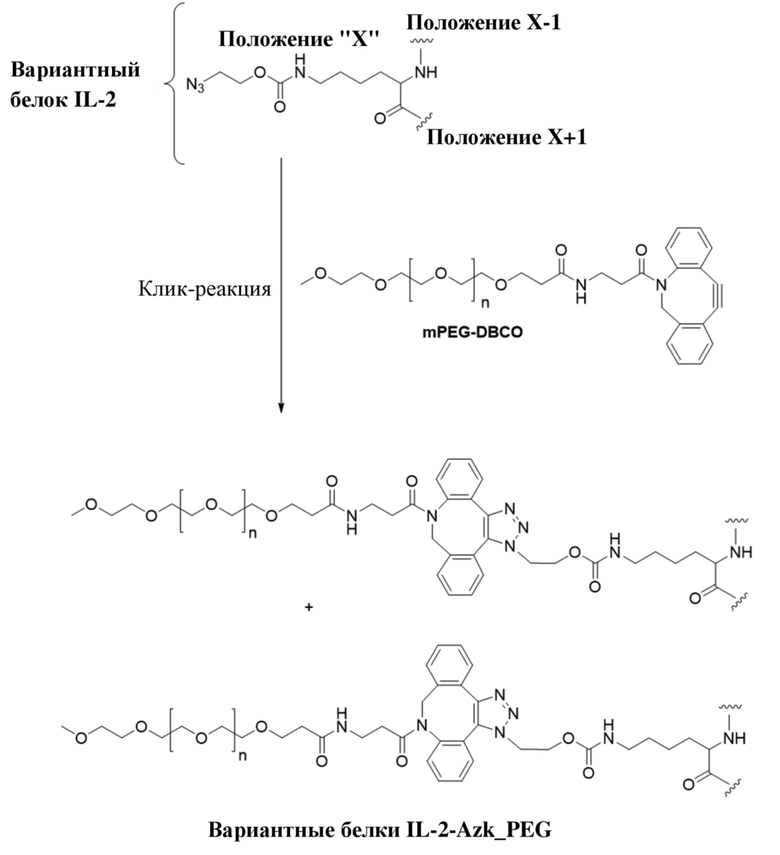
Схема S6
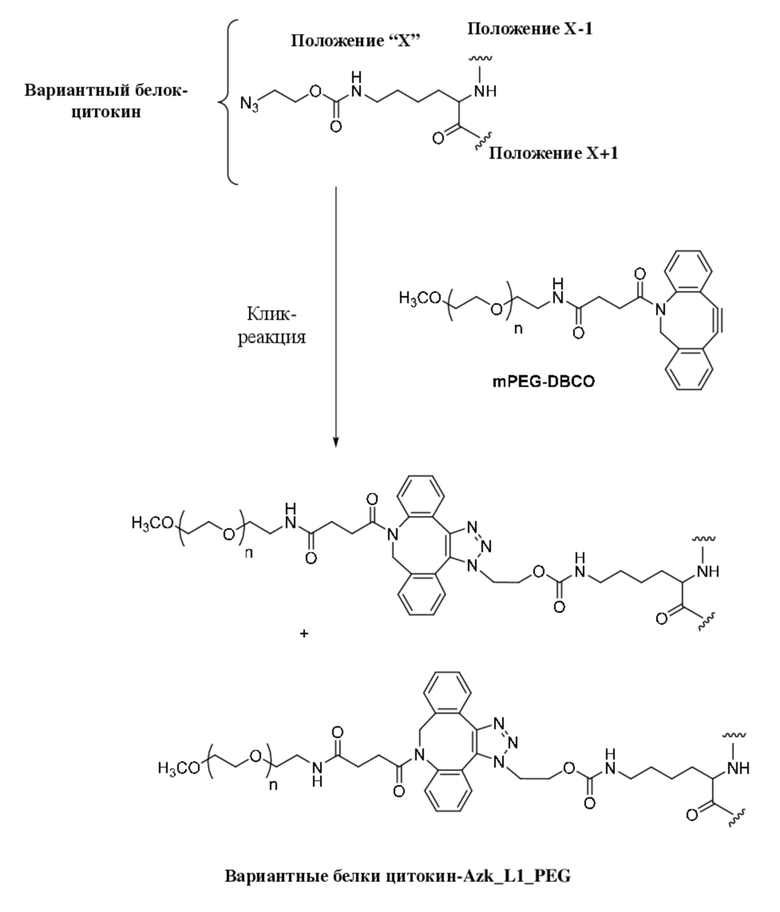
С помощью реакций конъюгации, таких как клик-реакция, описанная в данном документе, можно получать один региоизомер или смесь региоизомеров. В некоторых случаях соотношение региоизомеров составляет приблизительно 1:1. В некоторых случаях соотношение региоизомеров составляет приблизительно 2:1. В некоторых случаях соотношение региоизомеров составляет приблизительно 1,5:1. В некоторых случаях соотношение региоизомеров составляет приблизительно 1,2:1. В некоторых случаях соотношение региоизомеров составляет приблизительно 1,1:1. В некоторых случаях соотношение региоизомеров составляет более 1:1.
Получение цитокиновых полипептидов
В некоторых случаях конъюгаты IL-2, описанные в данном документе, содержащие мутацию по типу замены на природную аминокислоту либо мутацию по типу замены на неприродную аминокислоту, получают рекомбинантным путем или синтезируют химическим способом. В некоторых случаях конъюгаты IL-2, описанные в данном документе, получают рекомбинантным путем, например, в системе клеток-хозяев либо в бесклеточной системе. В любом из вариантов осуществления или видоизменений, описанных в данном документе, аминокислота может представлять собой L-аминокислоту или D-аминокислоту. В некоторых вариантах осуществления аминокислота представляет собой L-аминокислоту. В других вариантах осуществления аминокислота представляет собой D-аминокислоту.
В некоторых случаях конъюгаты IL-2 получают рекомбинантным путем с применением системы клеток-хозяев. В некоторых случаях клетка-хозяин представляет собой эукариотическую клетку (например, клетку млекопитающего, клетки насекомых, дрожжевые клетки или растительную клетку) или прокариотическую клетку (например, грамположительную бактерию или грамотрицательную бактерию). В некоторых случаях эукариотическая клетка-хозяин представляет собой клетку-хозяина, являющуюся клеткой млекопитающего. В некоторых случаях клетка-хозяин, являющаяся клеткой млекопитающего, относится к стабильной линии клеток или линии клеток, которая содержит представляющий интерес генетический материал, встроенный в ее собственный геном, и обладает способностью экспрессировать продукт генетического материала после многих поколений клеточного деления. В других случаях клетка-хозяин, являющаяся клеткой млекопитающего, относится к транзиентной линии клеток или линии клеток, которая не содержит представляющий интерес генетический материал, встроенный в ее собственный геном, и не обладает способностью экспрессировать продукт генетического материала после многих поколений клеточного деления.
Иллюстративные клетки-хозяева, являющиеся клетками млекопитающих, включают линию клеток 293T, линию клеток 293A, линию клеток 293FT, клетки 293F, клетки 293H, клетки A549, клетки MDCK, клетки CHO DG44, клетки CHO-S, клетки CHO-K1, клетки Expi293F™, линию клеток Flp-In™ T-REx™ 293, линию клеток Flp-In™-293, линию клеток Flp-In™-3T3, линию клеток Flp-In™-BHK, линию клеток Flp-In™-CHO, линию клеток Flp-In™-CV-1, линию клеток Flp-In™-Jurkat, клетки FreeStyle™ 293-F, клетки FreeStyle™ CHO-S, линию клеток GripTite™ 293 MSR, линию клеток GS-CHO, клетки HepaRG™, линию клеток T-REx™ Jurkat, клетки Per.C6, линию клеток T-REx™-293, линию клеток T-REx™-CHO и линию клеток T-REx™-HeLa.
В некоторых вариантах осуществления эукариотическая клетка-хозяин представляет собой клетку-хозяина, являющуюся клеткой насекомого. Иллюстративная клетка-хозяин, являющаяся клеткой насекомого, включает клетки S2 Drosophila, клетки Sf9, клетки Sf21, клетки High Five™ и клетки expresSF+®.
В некоторых вариантах осуществления эукариотическая клетка-хозяин представляет собой дрожжевую клетку-хозяина. Иллюстративные дрожжевые клетки-хозяева включают штаммы дрожжей Pichia pastoris (K. phaffii), такие как GS115, KM71H, SMD1168, SMD1168H и X-33, и штамм дрожжей Saccharomyces cerevisiae, такой как INVSc1.
В некоторых вариантах осуществления эукариотическая клетка-хозяин представляет собой растительную клетку-хозяина. В некоторых случаях растительные клетки включают клетку водоросли. Иллюстративные линии растительных клеток включают штаммы Chlamydomonas reinhardtii 137c или Synechococcus elongatus PPC 7942.
В некоторых вариантах осуществления клетка-хозяин представляет собой прокариотическую клетку-хозяина. Иллюстративные прокариотические клетки-хозяева включают BL21, Mach1™, DH10B™, TOP10, DH5α, DH10Bac™, OmniMax™, MegaX™, DH12S™, INV110, TOP10F', INVαF, TOP10/P3, ccdB Survival, PIR1, PIR2, Stbl2™, Stbl3™ или Stbl4™.
В некоторых случаях подходящие молекулы полинуклеиновой кислоты или векторы для получения полипептида IL-2, описанного в данном документе, включают любые подходящие векторы, полученные из эукариотического либо прокариотического источника. Иллюстративные молекулы полинуклеиновой кислоты или векторы включают векторы, полученные из источника, относящегося к бактериям (например, E. coli), насекомым, дрожжам (например, Pichia pastoris, K. phaffii), водорослям или млекопитающим. Бактериальные векторы включают, например, pACYC177, pASK75, векторы серии pBAD, векторы серии pBADM, векторы серии pET, векторы серии pETM, векторы серии pGEX, pHAT, pHAT2, pMal-c2, pMal-p2, векторы серии pQE, pRSET A, pRSET B, pRSET C, серию pTrcHis2, pZA31-Luc, pZE21-MCS-1, pFLAG-ATS, pFLAG-CTS, pFLAG-MAC, pFLAG-Shift-12c, pTAC-MAT-1, pFLAG-CTC или pTAC-MAT-2.
Векторы насекомых включают, например, pFastBac1, pFastBac DUAL, pFastBac ET, pFastBac HTa, pFastBac HTb, pFastBac HTc, pFastBac M30a, pFastBac M30b, pFastBac M30c, pVL1392, pVL1393, pVL1393 M10, pVL1393 M11, pVL1393 M12, векторы FLAG, такие как pPolh-FLAG1 или pPolh-MAT2, или векторы MAT, такие как pPolh-MAT1 или pPolh-MAT2.
Дрожжевые векторы включают, например, вектор Gateway® pDEST™ 14, вектор Gateway® pDEST™ 15, вектор Gateway® pDEST™ 17, вектор Gateway® pDEST™ 24, вектор Gateway® pYES-DEST52, вектор доставки Gateway® pBAD-DEST49, вектор pAO815 Pichia, вектор pFLD1 Pichia pastoris (K. phaffii), вектор pGAPZ A, B и C Pichia pastoris (K. phaffii), вектор pPIC3.5K Pichia, вектор pPIC6 A, B и C Pichia, вектор pPIC9K Pichia, pTEF1/Zeo, дрожжевой вектор pYES2, дрожжевой вектор pYES2/CT, дрожжевой вектор pYES2/NT A, B и C или дрожжевой вектор pYES3/CT.
Векторы водорослей включают, например, вектор pChlamy-4 или вектор MCS.
Векторы млекопитающих включают, например, векторы транзиентной экспрессии или векторы стабильной экспрессии. Иллюстративные векторы транзиентной экспрессии млекопитающих включают p3xFLAG-CMV-8, pFLAG-Myc-CMV-19, pFLAG-Myc-CMV-23, pFLAG-CMV-2, pFLAG-CMV-6a, b,c, pFLAG-CMV-5.1, pFLAG-CMV-5a, b,c, p3xFLAG-CMV-7.1, pFLAG-CMV-20, p3xFLAG-Myc-CMV-24, pCMV-FLAG-MAT1, pCMV-FLAG-MAT2, pBICEP-CMV-3 или pBICEP-CMV-4. Иллюстративные векторы стабильной экспрессии млекопитающих включают pFLAG-CMV-3, p3xFLAG-CMV-9, p3xFLAG-CMV-13, pFLAG-Myc-CMV-21, p3xFLAG-Myc-CMV-25, pFLAG-CMV-4, p3xFLAG-CMV-10, p3xFLAG-CMV-14, pFLAG-Myc-CMV-22, p3xFLAG-Myc-CMV-26, pBICEP-CMV-1 или pBICEP-CMV-2.
В некоторых случаях для получения цитокинового полипептида (например, IL-2), описанного в данном документе, применяют бесклеточную систему. В некоторых случаях бесклеточная система содержит смесь цитоплазматических и/или ядерных компонентов из клетки и подходит для синтеза нуклеиновых кислот in vitro. В некоторых случаях в бесклеточной системе используются компоненты прокариотических клеток. В других случаях в бесклеточной системе используются компоненты эукариотических клеток. Синтез нуклеиновых кислот достигается в бесклеточной системе, например, на основе клетки дрозофилы, яйца Xenopus, архей или клеток HeLa. Иллюстративные бесклеточные системы включают систему на основе экстракта S30 E. coli, систему S30 E. coli T7 или PURExpress®, XpressCF и XpressCF+.
Бесклеточные системы трансляции содержат различные компоненты, как, например, плазмиды, мРНК, ДНК, тРНК, синтетазы, факторы высвобождения, рибосомы, белки-шапероны, факторы инициации и элонгации трансляции, природные и/или неприродные аминокислоты и/или другие компоненты, применяемые для экспрессии белка. Такие компоненты необязательно модифицированы для улучшения выхода, увеличения скорости синтеза, увеличения качества белкового продукта или встраивания неприродных аминокислот. В некоторых вариантах осуществления цитокины, описанные в данном документе, синтезируют с применением бесклеточных систем трансляции, описанных в US 8778631; US 2017/0283469; US 2018/0051065; US 2014/0315245 или US 8778631. В некоторых вариантах осуществления бесклеточные системы трансляции предусматривают модификацию факторов высвобождения или даже удаление одного или нескольких факторов высвобождения из системы. В некоторых вариантах осуществления бесклеточные системы трансляции содержат пониженную концентрацию протеазы. В некоторых вариантах осуществления бесклеточные системы трансляции содержат модифицированные тРНК с переназначенными кодонами, используемыми для кодирования неприродных аминокислот. В некоторых вариантах осуществления синтетазы, описанные в данном документе, предназначенные для встраивания неприродных аминокислот, применяются в бесклеточных системах трансляции. В некоторых вариантах осуществления тРНК предварительно нагружают неприродными аминокислотами с помощью ферментативных или химических способов перед добавлением в бесклеточную систему трансляции. В некоторых вариантах осуществления компоненты для бесклеточной системы трансляции получают из модифицированных организмов, таких как модифицированные бактерии, дрожжи или другой организм.
В некоторых вариантах осуществления цитокиновый полипептид (например, IL-2) получают в виде формы с циклической перестановкой с помощью экспрессионной системы хозяина либо с помощью бесклеточной системы.
Получение цитокинового полипептида, содержащего неприродную аминокислоту
В настоящем изобретении можно использовать ортогональный или расширенный генетический код, в котором один или несколько конкретных кодонов, присутствующих в последовательности нуклеиновой кислоты цитокинового полипептида (например, IL-2), предназначены для кодирования неприродной аминокислоты, чтобы ее можно было генетически встроить в цитокин (например, IL-2) с использованием ортогональной пары тРНК-синтетаза/тРНК. Ортогональная пара тРНК-синтетаза/тРНК способна загружать тРНК неприродной аминокислотой и способна встраивать эту неприродную аминокислоту в полипептидную цепь в соответствии с кодоном.
В некоторых случаях кодон представляет собой кодон "янтарь", "охра", "опал" или квадруплетный кодон. В некоторых случаях кодон соответствует ортогональной тРНК, которая будет применяться для переноса неприродной аминокислоты. В некоторых случаях кодон представляет собой "янтарь". В других случаях кодон представляет собой ортогональный кодон.
В некоторых случаях кодон представляет собой квадруплетный кодон, который может быть декодирован ортогональной рибосомой ribo-Q1. В некоторых случаях квадруплетный кодон является таким, как проиллюстрировано в Neumann, et al., "Encoding multiple unnatural amino acids via evolution of a quadruplet-decoding ribosome", Nature, 464(7287): 441-444 (2010), раскрытие которой включено в данный документ посредством ссылки.
В некоторых случаях кодон, используемый в настоящем изобретении, представляет собой перекодированный кодон, например, синонимичный кодон или редкий кодон, который заменен альтернативным кодоном. В некоторых случаях перекодированный кодон является таким, как описано в Napolitano, et al., "Emergent rules for codon choice elucidated by editing rare arginine codons in Escherichia coli," PNAS, 113(38): E5588-5597 (2016). В некоторых случаях перекодированный кодон является таким, как описано в Ostrov et al., "Design, synthesis, and testing toward a 57-codon genome", Science 353(6301): 819-822 (2016). Раскрытие каждого из этих литературных источников включено в данный документ посредством ссылки.
В некоторых случаях используются неприродные нуклеиновые кислоты, что приводит к встраиванию одной или нескольких неприродных аминокислот в цитокин (например, IL-2). Иллюстративные неприродные нуклеиновые кислоты включают без ограничения урацил-5-ил, гипоксантин-9-ил (I), 2-аминоаденин-9-ил, 5-метилцитозин (5-me-C), 5-гидроксиметилцитозин, ксантин, гипоксантин, 2-аминоаденин, 6-метил- и другие алкильные производные аденина и гуанина, 2-пропил- и другие алкильные производные аденина и гуанина, 2-тиоурацил, 2-тиотимин и 2-тиоцитозин, 5-галогенурацил и цитозин, 5-пропинилурацил и цитозин, 6-азоурацил, цитозин и тимин, 5-урацил (псевдоурацил), 4-тиоурацил, 8-галоген-, 8-амино-, 8-тиол-, 8-тиоалкил-, 8-гидроксил- и другие 8-замещенные аденины и гуанины, 5-галоген-, в частности 5-бром-, 5-трифторметил- и другие 5-замещенные урацилы и цитозины, 7-метилгуанин и 7-метиладенин, 8-азагуанин и 8-азааденин, 7-деазагуанин и 7-деазааденин, а также 3-деазагуанин и 3-деазааденин. Представлены определенные неприродные нуклеиновые кислоты, такие как 5-замещенные пиримидины, 6-азапиримидины и N-2-замещенные пурины, N-6-замещенные пурины, O-6-замещенные пурины, 2-аминопропиладенин, 5-пропинилурацил, 5-пропинилцитозин, 5-метилцитозин, те, которые увеличивают стабильность образования дуплекса, универсальные нуклеиновые кислоты, гидрофобные нуклеиновые кислоты, смешанные нуклеиновые кислоты, нуклеиновые кислоты увеличенного размера, фторированные нуклеиновые кислоты, 5-замещенные пиримидины, 6-азапиримидины и N-2-, N-6- и О-6-замещенные пурины, включая 2-аминопропиладенин, 5-пропинилурацил и 5-пропинилцитозин, 5-метилцитозин (5-me-C), 5-гидроксиметилцитозин, ксантин, гипоксантин, 2-аминоаденин, 6-метил-, другие алкильные производные аденина и гуанина, 2-пропил- и другие алкильные производные аденина и гуанина, 2-тиоурацил, 2-тиотимин и 2-тиоцитозин, 5-галогенурацил, 5-галогенцитозин, 5-пропинил- (-C≡C-CH3-) урацил, 5-пропинилцитозин, другие алкинильные производные пиримидиновых нуклеиновых кислот, 6-азоурацил, 6-азоцитозин, 6-азотимин, 5-урацил (псевдоурацил), 4-тиоурацил, 8-галоген-, 8-амино-, 8-тиол-, 8-тиоалкил-, 8-гидроксил- и другие 8-замещенные аденины и гуанины, 5-галоген-, в частности 5-бром-, 5-трифторметил-, другие 5-замещенные урацилы и цитозины, 7-метилгуанин, 7-метиладенин, 2-F-аденин, 2-аминоаденин, 8-азагуанин, 8-азааденин, 7-деазагуанин, 7-деазааденин, 3-деазагуанин, 3-деазааденин, трициклические пиримидины, феноксазинцитидин ([5,4-b][1,4]бензоксазин-2(3Н)-он), фенотиазинцитидин (1Н-пиримидо[5,4-b][1,4]бензотиазин-2(3H)-он), G-зажимы, феноксазинцитидин (например, 9-(2-аминоэтокси)-H-пиримидо[5,4-b][1,4]бензоксазин-2(3H)-он), карбазолцитидин (2H-пиримидо[4,5-b]индол-2-он), пиридоиндолцитидин (H-пиридо[3’,2’:4,5]пирроло[2,3-d]пиримидин-2-он), те, в которых пуриновое или пиримидиновое основание заменено другими гетероциклами, 7-деазааденин, 7-деазагуанозин, 2-аминопиридин, 2-пиридон, азацитозин, 5-бромцитозин, бромурацил, 5-хлорцитозин, хлорированный цитозин, циклоцитозин, цитозин-арабинозид, 5-фторцитозин, фторпиримидин, фторурацил, 5,6-дигидроцитозин, 5-йодцитозин, гидроксимочевина, йодурацил, 5-нитроцитозин, 5-бромурацил, 5-хлорурацил, 5-фторурацил и 5-йодурацил, 2-аминоаденин, 6-тиогуанин, 2-тиотимин, 4-тиотимин, 5-пропинилурацил, 4-тиоурацил, N4-этилцитозин, 7-деазагуанин, 7-деаза-8-азагуанин, 5-гидроксицитозин, 2’-дезоксиуридин, 2-амино-2’-дезоксиаденозин и те, которые описаны в патентах США №№ 3687808; 4845205; 4910300; 4948882; 5093232; 5130302; 5134066; 5175273; 5367066; 5432272; 5457187; 5459255; 5484908; 5502177; 5525711; 5552540; 5587469; 5594121; 5596091; 5614617; 5645985; 5681941; 5750692; 5763588; 5830653 и 6005096; WO 99/62923; Kandimalla et al., (2001) Bioorg. Med. Chem. 9:807-813; The Concise Encyclopedia of Polymer Science and Engineering, Kroschwitz, J.I., Ed., John Wiley & Sons, 1990, 858-859; Englisch et al., Angewandte Chemie, International Edition, 1991, 30, 613; и Sanghvi, Chapter 15, Antisense Research and Applications, Crooke and Lebleu Eds., CRC Press, 1993, 273-288. Дополнительные модификации оснований можно найти, например, в патенте США № 3687808; Englisch et al., Angewandte Chemie, International Edition, 1991, 30, 613; и Sanghvi, Chapter 15, Antisense Research and Applications, страницы 289-302, Crooke and Lebleu ed., CRC Press, 1993. Раскрытие каждого из этих литературных источников включено в данный документ посредством ссылки.
Неприродные нуклеиновые кислоты, содержащие различные гетероциклические основания и различные сахарные фрагменты (и аналоги сахаров), доступны в данной области техники, и нуклеиновые кислоты в некоторых случаях содержат одно или несколько гетероциклических оснований, отличных от основных пяти компонентов-оснований встречающихся в природе нуклеиновых кислот. Например, гетероциклическое основание включает в некоторых случаях урацил-5-ильные, цитозин-5-ильные, аденин-7-ильные, аденин-8-ильные, гуанин-7-ильные, гуанин-8-ильные, 4-аминопирроло[2,3-d]пиримидин-5-ильные, 2-амино-4-оксопирроло[2,3-d]пиримидин-5-ильные, 2-амино-4-оксопирроло[2,3-d]пиримидин-3-ильные группы, где пурины присоединены к сахарному фрагменту нуклеиновой кислоты по положению 9, пиримидины по положению 1, пирролопиримидины по положению 7, а пиразолопиримидины по положению 1.
В некоторых вариантах осуществления аналоги нуклеотидов также модифицированы по фосфатному фрагменту. Модифицированные фосфатные фрагменты включают без ограничения фрагменты с модификацией в связи между двумя нуклеотидами и включают, например, фосфотиоат, хиральный фосфотиоат, фосфодитиоат, фосфотриэфир, аминоалкилфосфотриэфир, метил- и другие алкилфосфонаты, включая 3’-алкиленфосфонат и хиральные фосфонаты, фосфинаты, фосфорамидаты, включая 3’-аминофосфорамидат и аминоалкилфосфорамидаты, тионофосфорамидаты, тионоалкилфосфонаты, тионоалкилфосфотриэфиры и боранофосфаты. Следует понимать, что эти фосфатные или модифицированные фосфатные связи между двумя нуклеотидами образованы посредством 3’-5’-связи или 2’-5’-связи, и связь характеризуется инвертированной полярностью, как например, с 3’-5’ на 5’-3’ или с 2’-5’ на 5’-2’. Также включены различные соли, смешанные соли и формы свободных кислот. В многочисленных патентах США изложена идея получения и применения нуклеотидов, содержащих модифицированные фосфаты, и они включают без ограничения 3687808; 4469863; 4476301; 5023243; 5177196; 5188897; 5264423; 5276019; 5278302; 5286717; 5321131; 5399676; 5405939; 5453496; 5455233; 5466677; 5476925; 5519126; 5536821; 5541306; 5550111; 5563253; 5571799; 5587361 и 5625050, раскрытия каждого из которых включены в данный документ посредством ссылки.
В некоторых вариантах осуществления неприродные нуклеиновые кислоты включают 2’,3’-дидезокси-2’,3’-дидегидронуклеозиды (PCT/US2002/006460), 5’-замещенные производные ДНК и РНК (PCT/US2011/033961; Saha et al., J. Org Chem., 1995, 60, 788-789; Wang et al., Bioorganic & Medicinal Chemistry Letters, 1999, 9, 885-890; и Mikhailov et al., Nucleosides & Nucleotides, 1991, 10(1-3), 339-343; Leonid et al., 1995, 14(3-5), 901-905; и Eppacher et al., Helvetica Chimica Acta, 2004, 87, 3004-3020; PCT/JP2000/004720; PCT/JP2003/002342; PCT/JP2004/013216; PCT/JP2005/020435; PCT/JP2006/315479; PCT/JP2006/324484; PCT/JP2009/056718; PCT/JP2010/067560) или 5’-замещенные мономеры, полученные в виде монофосфата с модифицированными основаниями (Wang et al., Nucleosides Nucleotides & Nucleic Acids, 2004, 23 (1 & 2), 317-337). Раскрытие каждого из этих литературных источников включено в данный документ посредством ссылки.
В некоторых вариантах осуществления неприродные нуклеиновые кислоты содержат модификации в 5’-положении и 2’-положении сахарного кольца (PCT/US94/02993), как, например, 5’-CH2-замещенные 2’-O-защищенные нуклеозиды (Wu et al., Helvetica Chimica Acta, 2000, 83, 1127-1143 и Wu et al., Bioconjugate Chem. 1999, 10, 921-924). В некоторых случаях неприродные нуклеиновые кислоты содержат нуклеозидные димеры с амидной связью, которые были получены для встраивания в олигонуклеотиды, где 3’-связанный нуклеозид в димере (5’-3’) содержит 2’-OCH3 и 5’-(S)-CH3 (Mesmaeker et al., Synlett, 1997, 1287-1290). Неприродные нуклеиновые кислоты могут содержать 2’-замещенные 5’-CH2- (или O-) модифицированные нуклеозиды (PCT/US92/01020). Неприродные нуклеиновые кислоты могут содержать 5’-метиленфосфонатные мономеры и димеры ДНК и РНК (Bohringer et al., Tet. Lett., 1993, 34, 2723-2726; Collingwood et al., Synlett, 1995, 7, 703-705; и Hutter et al., Helvetica Chimica Acta, 2002, 85, 2777-2806). Неприродные нуклеиновые кислоты могут содержать 5’-фосфонатные мономеры, имеющие 2’-замещение (US2006/0074035), и другие модифицированные 5’-фосфонатные мономеры (WO1997/35869). Неприродные нуклеиновые кислоты могут содержать 5’-модифицированные метиленфосфонатные мономеры (EP614907 и EP629633). Неприродные нуклеиновые кислоты могут содержать аналоги 5’- или 6’-фосфонатных рибонуклеозидов, содержащие гидроксильную группу в 5’- и/или 6’-положении (Chen et al., Phosphorus, Sulfur and Silicon, 2002, 777, 1783-1786; Jung et al., Bioorg. Med. Chem., 2000, 8, 2501-2509; Gallier et al., Eur. J. Org. Chem., 2007, 925-933; и Hampton et al., J. Med. Chem., 1976, 19(8), 1029-1033). Неприродные нуклеиновые кислоты могут содержать 5’-фосфонатные дезоксирибонуклеозидные мономеры и димеры, имеющие 5’-фосфатную группу (Nawrot et al., Oligonucleotides, 2006, 16(1), 68-82). Неприродные нуклеиновые кислоты могут содержать нуклеозиды, имеющие 6’-фосфонатную группу, в которой 5’- и/или 6’-положение является незамещенным или замещенным тио-трет-бутильной группой (SC(CH3)3) (и ее аналогами); метиленаминогруппой (CH2NH2) (и ее аналогами) или цианогруппой (CN) (и ее аналогами) (Fairhurst et al., Synlett, 2001, 4, 467-472; Kappler et al., J. Med. Chem., 1986, 29, 1030-1038; Kappler et al., J. Med. Chem., 1982, 25, 1179-1184; Vrudhula et al., J. Med. Chem., 1987, 30, 888-894; Hampton et al., J. Med. Chem., 1976, 19, 1371-1377; Geze et al., J. Am. Chem. Soc, 1983, 105(26), 7638-7640; и Hampton et al., J. Am. Chem. Soc, 1973, 95(13), 4404-4414). Раскрытие каждого из этих литературных источников включено в данный документ посредством ссылки.
В некоторых вариантах осуществления неприродные нуклеиновые кислоты также содержат модификации сахарного фрагмента. В некоторых случаях нуклеиновые кислоты содержат один или несколько нуклеозидов, где сахарная группа была модифицирована. Такие нуклеозиды с модифицированным сахаром способны придавать повышенную стабильность к действию нуклеаз, увеличенную аффинность связывания или некоторые другие полезные биологические свойства. В определенных вариантах осуществления нуклеиновые кислоты содержат химически модифицированный рибофуранозный кольцевой фрагмент. Примеры химически модифицированных рибофуранозных колец предусматривают без ограничения добавление замещающих групп (в том числе 5’- и/или 2’-замещающих групп); соединение мостиком двух атомов кольца с образованием бициклических нуклеиновых кислот (BNA), замену атома кислорода рибозильного кольца на S, N(R) или C(R1)(R2) (R=H, C1-C12алкил или защитная группа) и их комбинации. Примеры химически модифицированных сахаров можно найти в WO2008/101157, US2005/0130923 и WO2007/134181, раскрытия каждой из которых включены в данный документ посредством ссылки.
В некоторых случаях модифицированная нуклеиновая кислота содержит модифицированные сахара или аналоги сахаров. Таким образом, в дополнение к рибозе и дезоксирибозе сахарный фрагмент может представлять собой пентозу, дезоксипентозу, гексозу, дезоксигексозу, глюкозу, арабинозу, ксилозу, ликсозу или циклопентильную группу, представляющую собой "аналог" сахара. Сахар может быть представлен в пиранозильной или фуранозильной форме. Сахарный фрагмент может представлять собой фуранозид рибозы, дезоксирибозы, арабинозы или 2’-O-алкилрибозы, и сахар может быть присоединен к соответствующим гетероциклическим основаниям в [альфа] либо в [бета]-аномерной конфигурации. Модификации сахара предусматривают без ограничения аналоги 2’-алкокси-РНК, аналоги 2’-амино-РНК, 2’-фтор-ДНК и химерные формы 2’-алкокси- или амино-РНК/ДНК. Например, модификация сахара может предусматривать 2’-O-метилуридин или 2’-O-метилцитидин. Модификации сахара предусматривают 2’-O-алкилзамещенные дезоксирибонуклеозиды и 2’-O-этиленгликоль-подобные рибонуклеозиды. Известно получение этих сахаров или аналогов сахаров и соответствующих "нуклеозидов", где такие сахара или аналоги присоединены к гетероциклическому основанию (основанию нуклеиновой кислоты). Модификации сахара также могут быть получены и объединены с другими модификациями.
Модификации сахарного фрагмента включают природные модификации рибозы и дезоксирибозы, а также неприродные модификации. Модификации сахара включают без ограничения следующие модификации в 2’-положении: OH; F; O-, S- или N-алкил; O-, S- или N-алкенил; O-, S- или N-алкинил или O-алкил-O-алкил, где алкил, алкенил и алкинил могут представлять собой замещенный или незамещенный C1-C10алкил или C2-C10алкенил и -алкинил. 2’-Модификации сахара также включают без ограничения -O[(CH2)nO]mCH3, -O(CH2)nOCH3, -O(CH2)nNH2, -O(CH2)nCH3, -O(CH2)nONH2 и -O(CH2)nON[(CH2)nCH3)]2, где n и m составляют от 1 до приблизительно 10.
Другие модификации в 2’-положении включают без ограничения низший C1-C10алкил, замещенный низший алкил, алкарил, аралкил, O-алкарил, O-аралкил, SH, SCH3, OCN, Cl, Br, CN, CF3, OCF3, SOCH3, SO2CH3, ONO2, NO2, N3, NH2, гетероциклоалкил, гетероциклоалкарил, аминоалкиламино, полиалкиламино, замещенный силил, РНК-расщепляющую группу, репортерную группу, интеркалятор, группу для улучшения фармакокинетических свойств олигонуклеотида или группу для улучшения фармакодинамических свойств олигонуклеотида, а также другие заместители с аналогичными свойствами. Аналогичные модификации также могут быть осуществлены в других положениях в сахаре, в частности в 3’-положении сахара в 3’-концевом нуклеотиде или в олигонуклеотидах с 2’-5’-связями и в 5’-положении 5’-концевого нуклеотида. Модифицированные сахара также включают сахара, которые содержат модификации по мостиковому атому кислорода кольца, такие как CH2 и S. Нуклеотиды с аналогами сахаров также могут содержать миметики сахаров, такие как циклобутильные фрагменты вместо пентофуранозильного сахара. Существует множество патентов США, в которых изложена идея получения таких модифицированных сахарных структур и в которых подробно излагается и описывается ряд модификаций оснований, как, например, патенты США №№ 4981957; 5118800; 5319080; 5359044; 5393878; 5446137; 5466786; 5514785; 5519134; 5567811; 5576427; 5591722; 5597909; 5610300; 5627053; 5639873; 5646265; 5658873; 5670633; 4845205; 5130302; 5134066; 5175273; 5367066; 5432272; 5457187; 5459255; 5484908; 5502177; 5525711; 5552540; 5587469; 5594121, 5596091; 5614617; 5681941 и 5700920, каждый из которых включен в данный документ посредством ссылки во всей своей полноте.
Примеры нуклеиновых кислот, имеющих модифицированные сахарные фрагменты, включают без ограничения нуклеиновые кислоты, содержащие замещающие группы 5’-винил, 5’-метил (R или S), 4’-S, 2’-F, 2’-OCH3 и 2’-O(CH2)2OCH3. Заместитель в 2’-положении также может быть выбран из аллила, амино, азидо, тио, O-аллила, O-(C1-C10алкила), OCF3, O(CH2)2SCH3, O(CH2)2-O-N(Rm)(Rn) и O-CH2-C(=O)-N(Rm)(Rn), где каждый Rm и Rn независимо представляет собой H или замещенный или незамещенный C1-C10алкил.
В определенных вариантах осуществления нуклеиновые кислоты, описанные в данном документе, содержат одну или несколько бициклических нуклеиновых кислот. В определенных таких вариантах осуществления бициклическая нуклеиновая кислота содержит мостик между 4’- и 2’-атомами рибозильного кольца. В определенных вариантах осуществления нуклеиновые кислоты, представленные в данном документе, содержат одну или несколько бициклических нуклеиновых кислот, где мостик образует 4’-2’-бициклическую нуклеиновую кислоту. Примеры таких 4’-2’-бициклических нуклеиновых кислот включают без ограничения одну из формул: 4’-(CH2)-O-2’ (LNA); 4’-(CH2)-S-2’; 4’-(CH2)2-O-2’ (ENA); 4’-CH(CH3)-O-2’ и 4’-CH(CH2OCH3)-O-2’ и их аналогов (см. патент США № 7399845); 4’-C(CH3)(CH3)-O-2’ и ее аналогов (см. WO2009/006478, WO2008/150729, US2004/0171570, патент США № 7427672, Chattopadhyaya et al., J. Org. Chem., 209, 74, 118-134 и WO2008/154401). Также см., например: Singh et al., Chem. Commun., 1998, 4, 455-456; Koshkin et al., Tetrahedron, 1998, 54, 3607-3630; Wahlestedt et al., Proc. Natl. Acad. Sci. U. S. A., 2000, 97, 5633-5638; Kumar et al., Bioorg. Med. Chem. Lett., 1998, 8, 2219-2222; Singh et al., J. Org. Chem., 1998, 63, 10035-10039; Srivastava et al., J. Am. Chem. Soc., 2007, 129(26) 8362-8379; Elayadi et al., Curr. Opinion Invens. Drugs, 2001, 2, 558-561; Braasch et al., Chem. Biol, 2001, 8, 1-7; Oram et al., Curr. Opinion Mol. Ther., 2001, 3, 239-243; патенты США №№ 4849513, 5015733, 5118800, 5118802, 7053207, 6268490, 6770748, 6794499, 7034133, 6525191, 6670461 и 7399845; международные публикации №№ WO2004/106356, WO1994/14226, WO2005/021570, WO2007/090071 и WO2007/134181; публикации заявок на патент США №№ US2004/0171570, US2007/0287831 и US2008/0039618; предварительные заявки на патент США №№ 60/989574, 61/026995, 61/026998, 61/056564, 61/086231, 61/097787 и 61/099844; а также международные заявки №№ PCT/US2008/064591, PCT US2008/066154, PCT US2008/068922 и PCT/DK98/00393, раскрытия каждого из которых включены в данный документ посредством ссылки.
В определенных вариантах осуществления нуклеиновые кислоты содержат связанные нуклеиновые кислоты. Нуклеиновые кислоты могут быть связаны друг с другом с помощью любой связи между нуклеиновыми кислотами. Два основных класса групп, связывающих между собой нуклеиновые кислоты, определяются наличием или отсутствием атома фосфора. Иллюстративные фосфорсодержащие связи между нуклеиновыми кислотами включают без ограничения фосфодиэфирные, фосфотриэфирные, метилфосфонатные, фосфорамидатные и фосфотиоатные (P=S). Иллюстративные не содержащие фосфор группы, связывающие между собой нуклеиновые кислоты, включают без ограничения метиленметилимино (-CH2-N(CH3)-O-CH2-), тиодиэфирную (-O-C(O)-S-), тионокарбаматную (-O-C(O)(NH)-S-); силоксановую (-O-Si(H)2-O-) и N, N*-диметилгидразиновую (-CH2-N(CH3)-N(CH3)). В определенных вариантах осуществления связи между нуклеиновыми кислотами, имеющие хиральный атом, можно получать в виде рацемической смеси, в виде отдельных энантиомеров, например, алкилфосфонатов и фосфотиоатов. Неприродные нуклеиновые кислоты могут содержать одну модификацию. Неприродные нуклеиновые кислоты могут содержать несколько модификаций в одном из фрагментов или между различными фрагментами.
Модификации фосфатного остова в нуклеиновой кислоте включают без ограничения метилфосфонат, фосфотиоат, фосфорамидат (мостиковый или немостиковый), фосфотриэфир, фосфодитиоат, дитиофосфат и боранофосфат и могут применяться в любой комбинации. Также можно применять другие нефосфатные связи.
В некоторых вариантах осуществления модификации остова (например, метилфосфонатные, фосфотиоатные, фосфорамидатные и фосфодитиоатные межнуклеотидные связи) могут придавать иммуномодулирующую активность модифицированной нуклеиновой кислоте и/или повышать ее стабильность in vivo.
В некоторых случаях фосфорсодержащее производное (или модифицированная фосфатная группа) присоединено к сахарному фрагменту или фрагменту, являющемуся аналогом сахара, и может представлять собой монофосфат, дифосфат, трифосфат, алкилфосфонат, фосфотиоат, фосфодитиоат, фосфорамидат или т.п. Иллюстративные полинуклеотиды, содержащие модифицированные фосфатные связи или нефосфатные связи, можно найти в Peyrottes et al., 1996, Nucleic Acids Res. 24: 1841-1848; Chaturvedi et al., 1996, Nucleic Acids Res. 24:2318-2323; и Schultz et al., (1996) Nucleic Acids Res. 24:2966-2973; Matteucci, 1997, "Oligonucleotide Analogs: an Overview" в Oligonucleotides as Therapeutic Agents, (Chadwick and Cardew, ed.), John Wiley and Sons, New York, NY; Zon, 1993, "Oligonucleoside Phosphorothioates" в Protocols for Oligonucleotides and Analogs, Synthesis and Properties, Humana Press, pp. 165-190; Miller et al., 1971, JACS 93:6657-6665; Jager et al., 1988, Biochem. 27:7247-7246; Nelson et al., 1997, JOC 62:7278-7287; патенте США № 5453496 и Micklefield, 2001, Curr. Med. Chem. 8: 1157-1179, раскрытия каждого из которых включены в данный документ посредством ссылки.
В некоторых случаях модификация остова включает замену фосфодиэфирной связи альтернативным фрагментом, таким как анионная, нейтральная или катионная группа. Примеры таких модификаций включают анионную межнуклеозидную связь; фосфорамидатную модификацию N3’-P5’; боранофосфатную ДНК; проолигонуклеотиды; нейтральные межнуклеозидные связи, такие как метилфосфонаты; ДНК с амидной связью; метилен(метилиминовые) связи; формацетальные и тиоформацетальные связи; остовы, содержащие сульфонильные группы; морфолиновые олигонуклеотиды; пептидные нуклеиновые кислоты (PNA) и положительно заряженные дезоксирибонуклеиновые гуанидиновые (DNG) олигонуклеотиды (Micklefield, 2001, Current Medicinal Chemistry 8: 1157-1179, раскрытие которой включено в данный документ посредством ссылки). Модифицированная нуклеиновая кислота может содержать химерный или смешанный остов, содержащий одну или несколько модификаций, например, комбинацию фосфатных связей, такую как комбинация фосфодиэфирных и фосфотиоатных связей.
Заместители для фосфата включают, например, короткоцепочечные алкильные или циклоалкильные межнуклеозидные связи, смешанные гетероатомные и алкильные или циклоалкильные межнуклеозидные связи или одну или несколько короткоцепочечных гетероатомных или гетероциклических межнуклеозидных связей. Они включают те, которые имеют морфолиновые связи (образованные частично из сахарной части нуклеозида); силоксановые остовы; сульфидные, сульфоксидные и сульфоновые остовы; формацетильные и тиоформацетильные остовы; метиленформацетильные и тиоформацетильные остовы; алкенсодержащие остовы; сульфаматные остовы; метилениминовые и метиленгидразиновые остовы; сульфонатные и сульфонамидные остовы; амидные остовы и другие, имеющие смешанные составляющие части из N, O, S и CH2. В многочисленных патентах США раскрыто получение и применение этих типов замен фосфата, и они включают без ограничения патенты США №№ 5034506; 5166315; 5185444; 5214134; 5216141; 5235033; 5264562; 5264564; 5405938; 5434257; 5466677; 5470967; 5489677; 5541307; 5561225; 5596086; 5602240; 5610289; 5602240; 5608046; 5610289; 5618704; 5623070; 5663312; 5633360; 5677437 и 5677439, раскрытия каждого из которых включены в данный документ посредством ссылки. В случае с заместителем для нуклеотида также следует понимать, что можно заменять как сахарный, так и фосфатный фрагменты нуклеотида, например, с помощью связи амидного типа (аминоэтилглицина) (PNA). В патентах США №№ 5539082; 5714331 и 5719262 изложена идея получения и применения молекул PNA, и каждый из них включен в данный документ посредством ссылки. См. также Nielsen et al., Science, 1991, 254, 1497-1500. Также возможно связать другие типы молекул (конъюгатов) с нуклеотидами или аналогами нуклеотидов, чтобы усилить, например, поглощение клеткой. Конъюгаты могут быть химически связаны с нуклеотидом или аналогами нуклеотидов. Такие конъюгаты включают без ограничения липидные фрагменты, такие как холестериновый фрагмент (Letsinger et al., Proc. Natl. Acad. Sci. USA, 1989, 86, 6553-6556), холиновую кислоту (Manoharan et al., Bioorg. Med. Chem. Let., 1994, 4, 1053-1060), простой тиоэфир, например, гексил-S-тритилтиол (Manoharan et al., Ann. KY. Acad. Sci., 1992, 660, 306-309; Manoharan et al., Bioorg. Med. Chem. Let., 1993, 3, 2765-2770), тиохолестерин (Oberhauser et al., Nucl. Acids Res., 1992, 20, 533-538), алифатическую цепь, например, додекандиоловые или ундециловые остатки (Saison-Behmoaras et al., EM5OJ, 1991, 10, 1111-1118; Kabanov et al., FEBS Lett., 1990, 259, 327-330; Svinarchuk et al., Biochimie, 1993, 75, 49-54), фосфолипид, например, ди-гексадецил-рац-глицерин или 1-ди-O-гексадецил-рац-глицеро-S-H-фосфонат триэтиламмония (Manoharan et al., Tetrahedron Lett., 1995, 36, 3651-3654; Shea et al., Nucl. Acids Res., 1990, 18, 3777-3783), цепь полиамина или полиэтиленгликоля (Manoharan et al., Nucleosides & Nucleotides, 1995, 14, 969-973) или адамантануксусную кислоту (Manoharan et al., Tetrahedron Lett., 1995, 36, 3651-3654), пальмитиловый фрагмент (Mishra et al., Biochem. Biophys. Acta, 1995, 1264, 229-237) или октадециламиновый или гексиламинокарбонилоксихолестериновый фрагмент (Crooke et al., J. Pharmacol. Exp. Ther., 1996, 277, 923-937). В многочисленных патентах США изложена идея получения таких конъюгатов, и они включают без ограничения патенты США №№ 4828979; 4948882; 5218105; 5525465; 5541313; 5545730; 5552538; 5578717; 5580731; 5580731; 5591584; 5109124; 5118802; 5138045; 5414077; 5486603; 5512439; 5578718; 5608046; 4587044; 4605735; 4667025; 4762779; 4789737; 4824941; 4835263; 4876335; 4904582; 4958013; 5082830; 5112963; 5214136; 5082830; 5112963; 5214136; 5245022; 5254469; 5258506; 5262536; 5272250; 5292873; 5317098; 5371241; 5391723; 5416203; 5451463; 5510475; 5512667; 5514785; 5565552; 5567810; 5574142; 5585481; 5587371; 5595726; 5597696; 5599923; 5599928 и 5688941. Раскрытие каждого из этих литературных источников включено в данный документ посредством ссылки.
В некоторых случаях неприродные нуклеиновые кислоты дополнительно образуют неприродные пары оснований. Иллюстративные неприродные нуклеотиды, способные к образованию неприродной пары оснований ДНК или РНК (UBP) в условиях in vivo, включают без ограничения TAT1, dTAT1, 5FM, d5FM, TPT3, dTPT3, 5SICS, d5SICS, NaM, dNaM, CNMO, dCNMO и их комбинации. В некоторых вариантах осуществления неприродные нуклеотиды включают:
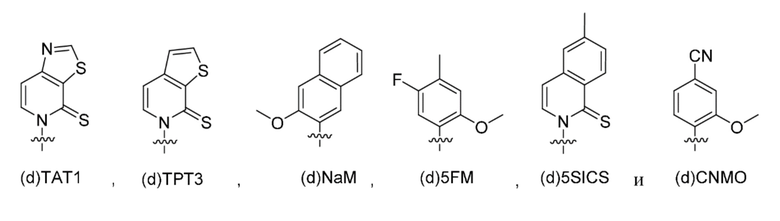
Иллюстративные неприродные пары оснований включают (d)TPT3-(d)NaM; (d)5SICS-(d)NaM; (d)CNMO-(d)TAT1; (d)NaM-(d)TAT1; (d)CNMO-(d)TPT3 и (d)5FM-(d)TAT1.
Другие примеры неприродных нуклеотидов, способных образовывать неприродные UBP, которые можно применять для получения конъюгатов IL-2, раскрытых в данном документе, можно найти в Dien et al., J Am Chem Soc., 2018, 140:16115-16123; Feldman et al., J Am Chem Soc, 2017, 139:11427-11433; Ledbetter et al., J Am Chem Soc., 2018, 140:758-765; Dhami et al., Nucleic Acids Res. 2014, 42:10235-10244; Malyshev et al., Nature, 2014, 509:385-388; Betz et al., J Am Chem Soc., 2013, 135:18637-18643; Lavergne et al., J Am Chem Soc. 2013, 135:5408-5419; и Malyshev et al. Proc Natl Acad Sci USA, 2012, 109:12005-12010, раскрытия каждого из которых включены в данный документ посредством ссылки. В некоторых вариантах осуществления неприродные нуклеотиды включают:
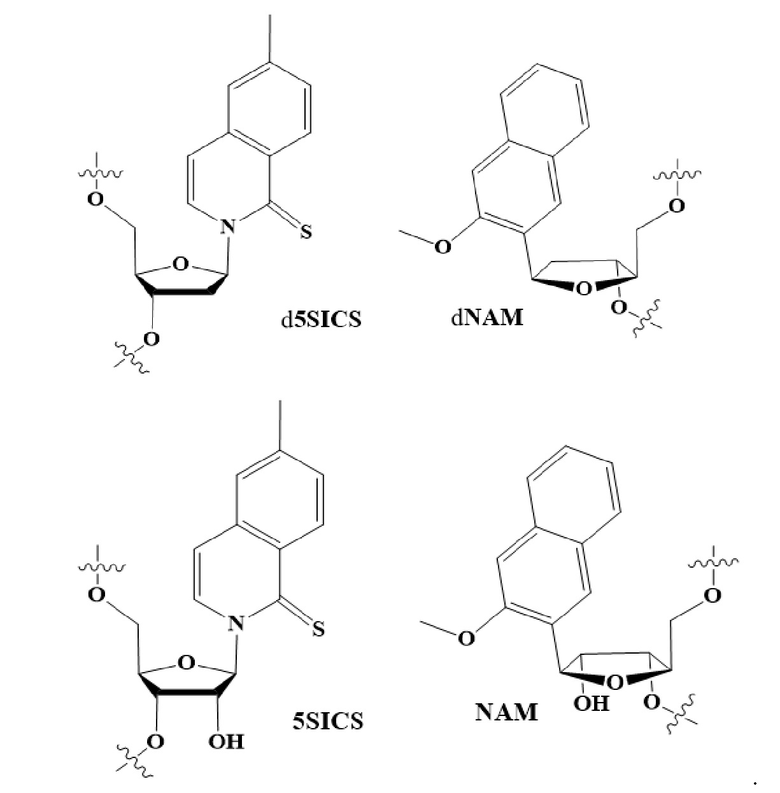
В некоторых вариантах осуществления неприродные нуклеотиды, которые можно применять для получения конъюгатов IL-2, раскрытых в данном документе, можно получить из соединения формулы
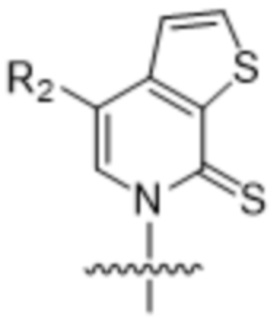
где R2 выбран из группы, состоящей из водорода, алкила, алкенила, алкинила, метокси, метантиола, метанселено, галогена, циано и азидо; и
волнистой линией указана связь с рибозилом или 2’-дезоксирибозилом, где 5’-гидроксигруппа рибозильного или 2’-дезоксирибозильного фрагмента находится в свободной форме, необязательно связана с монофосфатной, дифосфатной или трифосфатной группой или включена в РНК или ДНК или в аналог РНК или аналог ДНК.
В некоторых вариантах осуществления неприродные нуклеотиды, которые можно применять для получения конъюгатов IL-2, раскрытых в данном документе, можно получить из соединения формулы
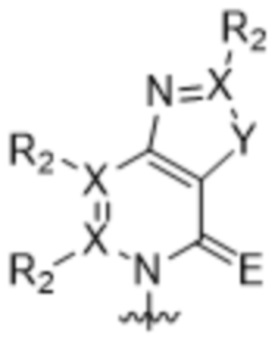
где:
каждый X независимо представляет собой углерод или азот;
R2 отсутствует, если X представляет собой азот, и присутствует, если X представляет собой углерод, и независимо представляет собой водород, алкил, алкенил, алкинил, метокси, метантиол, метанселено, галоген, циано или азид;
Y представляет собой серу, кислород, селен или вторичный амин;
E представляет собой кислород, серу или селен; и
волнистой линией указана точка связывания с рибозильным, дезоксирибозильным или дидезоксирибозильным фрагментом или его аналогом, где рибозильный, дезоксирибозильный или дидезоксирибозильный фрагмент или его аналог находится в свободной форме, соединен с монофосфатной, дифосфатной, трифосфатной, α-тиотрифосфатной, β-тиотрифосфатной или γ-тиотрифосфатной группой или включен в РНК или ДНК или в аналог РНК или аналог ДНК.
В некоторых вариантах осуществления каждый Х представляет собой углерод. В некоторых вариантах осуществления по меньшей мере один X представляет собой углерод. В некоторых вариантах осуществления один X представляет собой углерод. В некоторых вариантах осуществления по меньшей мере два X представляют собой углерод. В некоторых вариантах осуществления два X представляют собой углерод. В некоторых вариантах осуществления по меньшей мере один X представляет собой азот. В некоторых вариантах осуществления один X представляет собой азот. В некоторых вариантах осуществления по меньшей мере два X представляют собой азот. В некоторых вариантах осуществления два X представляют собой азот.
В некоторых вариантах осуществления Y представляет собой серу. В некоторых вариантах осуществления Y представляет собой кислород. В некоторых вариантах осуществления Y представляет собой селен. В некоторых вариантах осуществления Y представляет собой вторичный амин.
В некоторых вариантах осуществления E представляет собой серу. В некоторых вариантах осуществления E представляет собой кислород. В некоторых вариантах осуществления Е представляет собой селен.
В некоторых вариантах осуществления R2 присутствует, если X представляет собой углерод. В некоторых вариантах осуществления R2 отсутствует, если X представляет собой азот. В некоторых вариантах осуществления каждый R2 в тех случаях, когда он присутствует, представляет собой водород. В некоторых вариантах осуществления R2 представляет собой алкил, такой как метил, этил или пропил. В некоторых вариантах осуществления R2 представляет собой алкенил, такой как -CH2=CH2. В некоторых вариантах осуществления R2 представляет собой алкинил, такой как этинил. В некоторых вариантах осуществления R2 представляет собой метокси. В некоторых вариантах осуществления R2 представляет собой метантиол. В некоторых вариантах осуществления R2 представляет собой метанселено. В некоторых вариантах осуществления R2 представляет собой галоген, такой как хлор, бром или фтор. В некоторых вариантах осуществления R2 представляет собой циано. В некоторых вариантах осуществления R2 представляет собой азид.
В некоторых вариантах осуществления E представляет собой серу, Y представляет собой серу, и каждый X независимо представляет собой углерод или азот. В некоторых вариантах осуществления E представляет собой серу, Y представляет собой серу, и каждый Х представляет собой углерод.
В некоторых вариантах осуществления неприродные нуклеотиды, которые можно применять для получения конъюгатов IL-2, раскрытых в данном документе, можно получить из
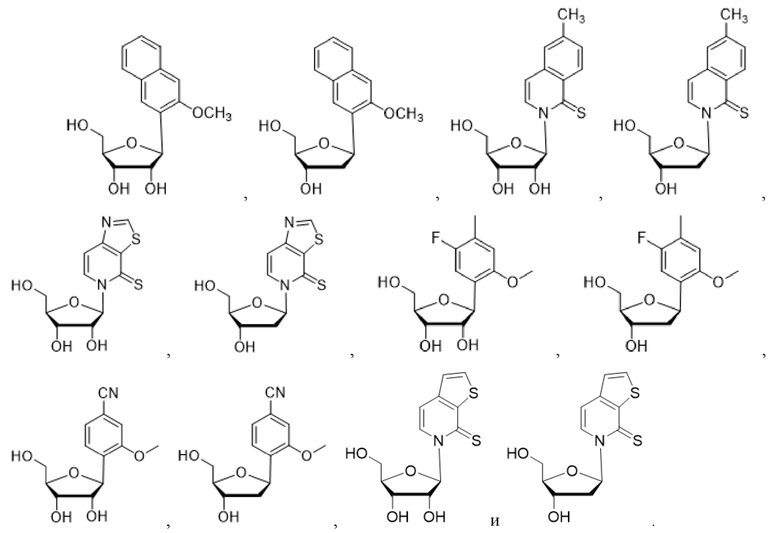
В некоторых вариантах осуществления неприродные нуклеотиды, которые можно применять для получения конъюгатов IL-2, раскрытых в данном документе, включают
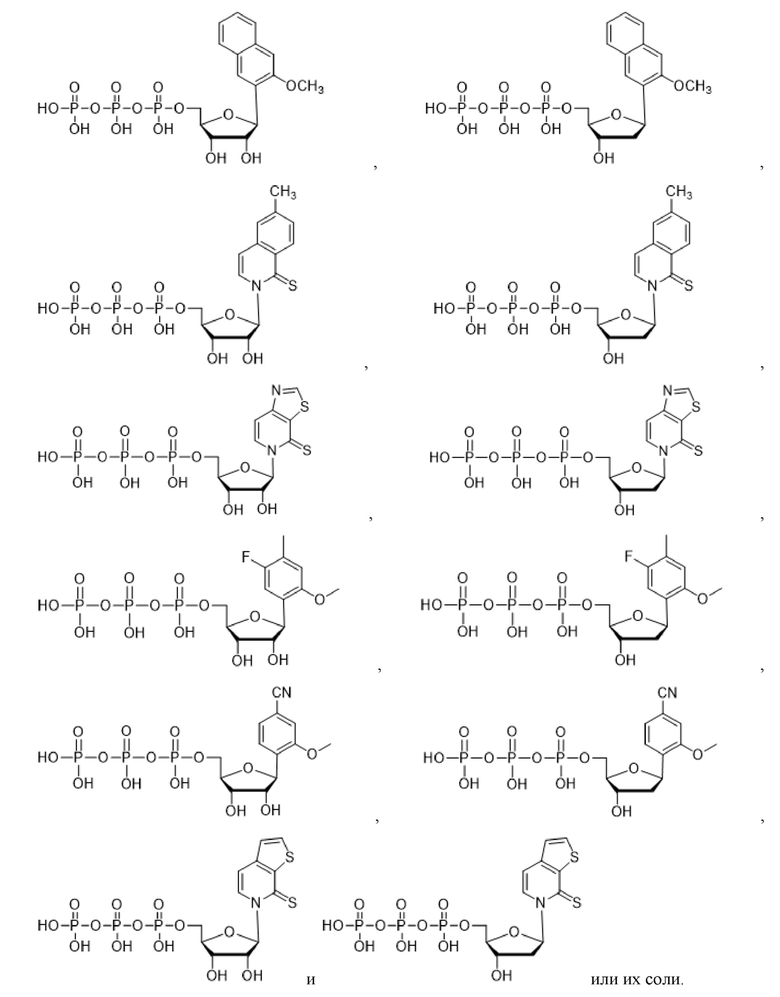
В некоторых вариантах осуществления неприродная пара оснований образует неприродную аминокислоту, описанную в Dumas et al., "Designing logical codon reassignment - Expanding the chemistry in biology", Chemical Science, 6: 50-69 (2015), раскрытие которой включено в данный документ посредством ссылки.
В некоторых вариантах осуществления неприродная аминокислота встраивается в цитокин (например, полипептид IL) с помощью синтетического кодона, содержащего неприродную нуклеиновую кислоту. В некоторых случаях неприродная аминокислота встраивается в цитокин с помощью ортогональной пары модифицированная синтетаза/тРНК. Такие ортогональные пары содержат неприродную синтетазу, которая способна загружать неприродную тРНК неприродной аминокислотой, при этом минимизируя загрузку а) других эндогенных аминокислот на неприродную тРНК и b) неприродных аминокислот на другие эндогенные тРНК. Такие ортогональные пары содержат тРНК, которые способны загружаться с помощью неприродной синтетазы, избегая при этом загрузки a) другими эндогенными аминокислотами с помощью эндогенных синтетаз. В некоторых вариантах осуществления такие пары идентифицированы из различных организмов, таких как источники, относящиеся к бактериям, дрожжам, археям или людям. В некоторых вариантах осуществления ортогональная пара синтетаза/тРНК содержит компоненты из одного организма. В некоторых вариантах осуществления ортогональная пара синтетаза/тРНК содержит компоненты из двух различных организмов. В некоторых вариантах осуществления ортогональная пара синтетаза/тРНК содержит компоненты, которые до модификации способствуют трансляции двух различных аминокислот. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную аланинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную аргининсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную аспарагинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную синтетазу аспарагиновой кислоты. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную цистеинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную глутаминсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную синтетазу глутаминовой кислоты. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную аланин/глицинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную гистидинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную лейцинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную изолейцинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную лизинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную метионинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную фенилаланинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную пролинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную серинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную треонинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную триптофансинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную тирозинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную валинсинтетазу. В некоторых вариантах осуществления ортогональная синтетаза представляет собой модифицированную фосфосеринсинтетазу. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для аланина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для аргинина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для аспарагина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для аспарагиновой кислоты. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для цистеина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для глутамина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для глутаминовой кислоты. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для аланина/глицина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для гистидина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для лейцина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для изолейцина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для лизина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для метионина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для фенилаланина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для пролина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для серина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для треонина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для триптофана. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для тирозина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для валина. В некоторых вариантах осуществления ортогональная тРНК представляет собой модифицированную тРНК для фосфосерина.
В некоторых вариантах осуществления неприродная аминокислота встраивается в цитокин (например, полипептид IL) с помощью пары аминоацил-тРНК-синтетаза (aaRS или RS)/тРНК. Иллюстративные пары aaRS-тРНК включают без ограничения пары aaRS Methanococcus jannaschii (Mj-Tyr)/тРНК, пары TyrRS E. coli (Ec-Tyr)/тРНКCUA B. stearothermophilus, пары LeuRS E. coli (Ec-Leu)/тРНКCUA B. stearothermophilus и пары пирролизил-тРНК. В некоторых случаях неприродная аминокислота встраивается в цитокин (например, в полипептид IL) с помощью пары Mj-TyrRS/тРНК. Иллюстративные UAA, которые можно встраивать с помощью пары Mj-TyrRS/тРНК, включают без ограничения пара-замещенные производные фенилаланина, такие как п-аминофенилаланин и п-метоксифенилаланин; мета-замещенные производные тирозина, такие как 3-аминотирозин, 3-нитротирозин, 3,4-дигидроксифенилаланин и 3-йодтирозин; фенилселеноцистеин; п-борфенилаланин и о-нитробензилтирозин.
В некоторых случаях неприродная аминокислота встраивается в цитокин (например, в полипептид IL) с помощью пары Ec-Tyr/тРНКCUA или Ec-Leu/тРНКCUA. Иллюстративные UAA, которые можно встраивать с помощью пары Ec-Tyr/тРНКCUA или Ec-Leu/тРНКCUA, включают без ограничения производные фенилаланина, содержащие бензофеноновые, кетоновые, йодидные или азидные заместители; O-пропаргилтирозин; α-аминокаприловую кислоту, O-метилтирозин, O-нитробензилцистеин и 3-(нафталин-2-иламино)-2-аминопропановую кислоту.
В некоторых случаях неприродная аминокислота встраивается в цитокин (например, в полипептид IL) с помощью пары пирролизил-тРНК. В некоторых случаях PylRS получена из архебактерии, например, из метаногенной архебактерии. В некоторых случаях PylRS получена из Methanosarcina barkeri, Methanosarcina mazei или Methanosarcina acetivorans. Иллюстративные UAA, которые можно встраивать с помощью пары пирролизил-тРНК, включают без ограничения амид- и карбаматзамещенные лизины, такие как 2-амино-6-((R)-тетрагидрофуран-2-карбоксамидо)гексановая кислота, N-ε-D-пролил-L-лизин и N-ε-циклопентилоксикарбонил-L-лизин; N-ε-акрилоил-L-лизин; N-ε-[(1-(6-нитробензо[d][1,3]диоксол-5-ил)этокси)карбонил]-L-лизин и N-ε-(1-метилциклопроп-2-ен-карбоксамидо)лизин. В некоторых вариантах осуществления конъюгаты IL-2, раскрытые в данном документе, могут быть получены путем применения тРНК M. mazei, которая селективно нагружается неприродной аминокислотой, такой как N6-((2-азидоэтокси)-карбонил)-L-лизин (AzK), с помощью пирролизил-тРНК-синтетазы M. barkeri (MbPylRS). Средним специалистам в данной области известны и другие способы, как, например, способы, раскрытые в Zhang et al., Nature 2017, 551(7682): 644-647, раскрытие которой включено в данный документ посредством ссылки.
В некоторых случаях неприродная аминокислота встраивается в цитокин, описанный в данном документе (например, в полипептид IL), с помощью синтетазы, раскрытой в US 9988619 и US 9938516, раскрытия каждого из которых включены в данный документ посредством ссылки.
Клетку-хозяина, в которую вводят раскрытые в данном документе конструкции или векторы, культивируют или поддерживают в подходящей среде таким образом, что продуцируются тРНК, тРНК-синтетаза и представляющий интерес белок. Среда также содержит неприродную(неприродные) аминокислоту(аминокислоты), так что в представляющий интерес белок встраивается(встраиваются) неприродная(неприродные) аминокислота(аминокислоты). В некоторых вариантах осуществления в клетке-хозяине также присутствует переносчик нуклеозидтрифосфатов (NTT) из бактерии, растения или водоросли. В некоторых вариантах осуществления конъюгаты IL-2, раскрытые в данном документе, получают путем использования клетки-хозяина, которая экспрессирует NTT. В некоторых вариантах осуществления переносчик нуклеотидов/нуклеозидтрифосфатов, используемый в клетке-хозяине, может быть выбран из TpNTT1, TpNTT2, TpNTT3, TpNTT4, TpNTT5, TpNTT6, TpNTT7, TpNTT8 (T. pseudonana), PtNTT1, PtNTT2, PtNTT3, PtNTT4, PtNTT5, PtNTT6 (P. tricornutum), GsNTT (Galdieria sulphuraria), AtNTT1, AtNTT2 (Arabidopsis thaliana), CtNTT1, CtNTT2 (Chlamydia trachomatis), PamNTT1, PamNTT2 (Protochlamydia amoebophila), CcNTT (Caedibacter caryophilus), RpNTT1 (Rickettsia prowazekii). В некоторых вариантах осуществления NTT выбран из PtNTT1, PtNTT2, PtNTT3, PtNTT4, PtNTT5 и PtNTT6. В некоторых вариантах осуществления NTT представляет собой PtNTT1. В некоторых вариантах осуществления NTT представляет собой PtNTT2. В некоторых вариантах осуществления NTT представляет собой PtNTT3. В некоторых вариантах осуществления NTT представляет собой PtNTT4. В некоторых вариантах осуществления NTT представляет собой PtNTT5. В некоторых вариантах осуществления NTT представляет собой PtNTT6. Другие NTT, которые могут быть использованы, раскрыты в Zhang et al., Nature 2017, 551(7682): 644-647; Malyshev et al. Nature 2014 (509(7500), 385-388; и Zhang et al. Proc Natl Acad Sci USA, 2017, 114:1317-1322, раскрытия каждого из которых включены в данный документ посредством ссылки.
Ортогональная пара тРНК-синтетаза/тРНК загружает тРНК неприродной аминокислотой и встраивает неприродную аминокислоту в полипептидную цепь в соответствии с кодоном. Иллюстративные пары aaRS-тРНК включают без ограничения пары aaRS Methanococcus jannaschii (Mj-Tyr)/тРНК, пары TyrRS E. coli (Ec-Tyr)/тРНКCUA B. stearothermophilus, пары LeuRS E. coli (Ec-Leu)/тРНКCUA B. stearothermophilus и пары пирролизил-тРНК. Другие пары aaRS-тРНК, которые могут быть использованы в соответствии с настоящим изобретением, включают пары, полученные из M. mazei, пары, описанные в Feldman et al., J Am Chem Soc., 2018 140:1447-1454; и Zhang et al. Proc Natl Acad Sci USA, 2017, 114:1317-1322, раскрытия каждого из которых включены в данный документ посредством ссылки.
В некоторых вариантах осуществления представлены способы получения конъюгатов IL-2, раскрытых в данном документе, в клеточной системе, которая экспрессирует NTT и тРНК-синтетазу. В некоторых вариантах осуществления, описанных в данном документе, NTT выбран из PtNTT1, PtNTT2, PtNTT3, PtNTT4, PtNTT5 и PtNTT6, а тРНК-синтетаза выбрана из Methanococcus jannaschii, TyrRS E. coli (Ec-Tyr)/B. stearothermophilus и M. mazei. В некоторых вариантах осуществления NTT представляет собой PtNTT1, а тРНК-синтетаза получена из Methanococcus jannaschii, TyrRS E. coli (Ec-Tyr)/B. stearothermophilus или M. mazei. В некоторых вариантах осуществления NTT представляет собой PtNTT2, а тРНК-синтетаза получена из Methanococcus jannaschii, TyrRS E. coli (Ec-Tyr)/B. stearothermophilus или M. mazei. В некоторых вариантах осуществления NTT представляет собой PtNTT3, а тРНК-синтетаза получена из Methanococcus jannaschii, TyrRS E. coli (Ec-Tyr)/B. stearothermophilus или M. mazei. В некоторых вариантах осуществления NTT представляет собой PtNTT3, а тРНК-синтетаза получена из Methanococcus jannaschii, TyrRS E. coli (Ec-Tyr)/B. stearothermophilus или M. mazei. В некоторых вариантах осуществления NTT представляет собой PtNTT4, а тРНК-синтетаза получена из Methanococcus jannaschii, TyrRS E. coli (Ec-Tyr)/B. stearothermophilus или M. mazei. В некоторых вариантах осуществления NTT представляет собой PtNTT5, а тРНК-синтетаза получена из Methanococcus jannaschii, TyrRS E. coli (Ec-Tyr)/B. stearothermophilus или M. mazei. В некоторых вариантах осуществления NTT представляет собой PtNTT6, а тРНК-синтетаза получена из Methanococcus jannaschii, TyrRS E. coli (Ec-Tyr)/B. stearothermophilus или M. mazei.
В некоторых вариантах осуществления конъюгаты IL-2, раскрытые в данном документе, могут быть получены в клетке, такой как E. coli, содержащей (a) переносчик нуклеотидтрифосфатов PtNTT2 (включая усеченный вариант, в котором первые 65 аминокислотных остатков полноразмерного белка удалены), (b) плазмиду, содержащую двухнитевой олигонуклеотид, который кодирует вариант IL-2, имеющий желаемую аминокислотную последовательность, и который содержит неприродную пару оснований, содержащую первый неприродный нуклеотид и второй неприродный нуклеотид, для обеспечения наличия кодона в желаемом положении, в которое будет встроена неприродная аминокислота, такая как N6-((2-азидоэтокси)-карбонил)-L-лизин (AzK), (c) плазмиду, кодирующую тРНК, полученную из M. mazei, которая содержит неприродный нуклеотид для обеспечения наличия распознаваемого антикодона (для кодона варианта IL-2) вместо своей нативной последовательности, и (d) плазмиду, кодирующую пирролизил-тРНК-синтетазу, полученную из M. barkeri (MbPylRS), которая может представлять собой ту же плазмиду, которая кодирует тРНК, или другую плазмиду. Кроме того, в некоторых вариантах осуществления клетка дополнена дезоксириботрифосфатами, содержащими одно или несколько неприродных оснований. Кроме того, в некоторых вариантах осуществления клетка дополнена риботрифосфатами, содержащими одно или несколько неприродных оснований. Кроме того, в некоторых вариантах осуществления клетки дополнены одной или несколькими неприродными аминокислотами, такими как N6-((2-азидоэтокси)-карбонил)-L-лизин (AzK). В некоторых вариантах осуществления двухнитевой олигонуклеотид, который кодирует аминокислотную последовательность желаемого варианта IL-2, содержит кодон AXC, например, в положении 34, 37, 40, 41, 42, 43, 44, 61, 64, 68 или 71 последовательности, которая кодирует белок, имеющий SEQ ID NO: 3, или в положении 35, 38, 41, 42, 43, 45, 62, 65, 69 или 72 последовательности, которая кодирует белок, имеющий SEQ ID NO: 4, где X представляет собой неприродный нуклеотид. В некоторых вариантах осуществления клетка дополнительно содержит плазмиду, которая может представлять собой плазмиду для экспрессии белка или другую плазмиду, которая кодирует ген ортогональной тРНК из M. mazei, которая содержит антикодон GYT, соответствующий AXC, вместо своей нативной последовательности, где Y представляет собой неприродный нуклеотид, который является комплементарным неприродному нуклеотиду в кодоне и может быть таким же, как он, или отличаться от него. В некоторых вариантах осуществления неприродный нуклеотид в кодоне отличается от неприродного нуклеотида в антикодоне и комплементарен ему. В некоторых вариантах осуществления неприродный нуклеотид в кодоне является таким же, как неприродный нуклеотид в антикодоне. В некоторых вариантах осуществления первый и второй неприродные нуклеотиды, составляющие неприродную пару оснований в двухнитевом олигонуклеотиде, могут быть получены из 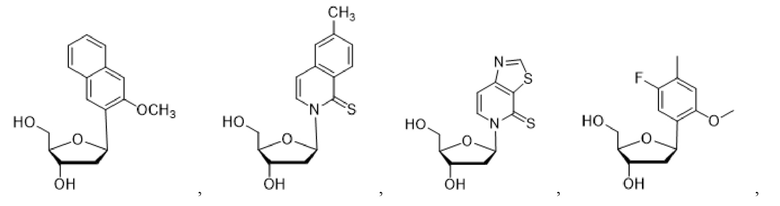
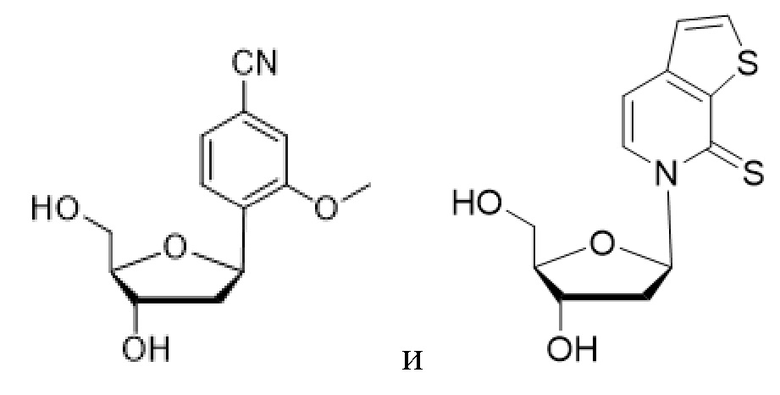 . В некоторых вариантах осуществления первый и второй неприродные нуклеотиды, составляющие неприродную пару оснований в двухнитевом олигонуклеотиде, могут быть получены из
. В некоторых вариантах осуществления первый и второй неприродные нуклеотиды, составляющие неприродную пару оснований в двухнитевом олигонуклеотиде, могут быть получены из 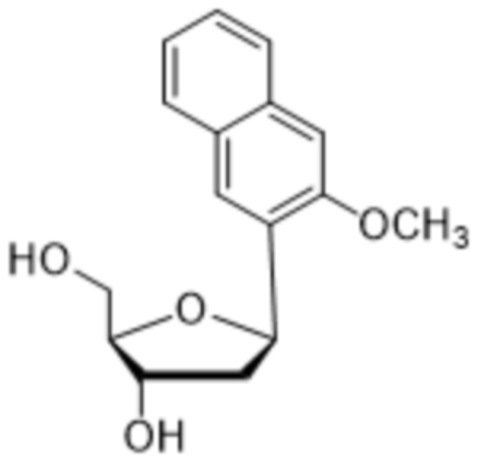 и
и 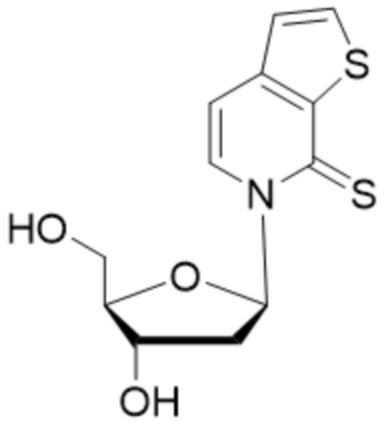 . В некоторых вариантах осуществления первый и второй неприродные нуклеотиды, составляющие неприродную пару оснований в двухнитевом олигонуклеотиде, могут быть получены из
. В некоторых вариантах осуществления первый и второй неприродные нуклеотиды, составляющие неприродную пару оснований в двухнитевом олигонуклеотиде, могут быть получены из  и
и 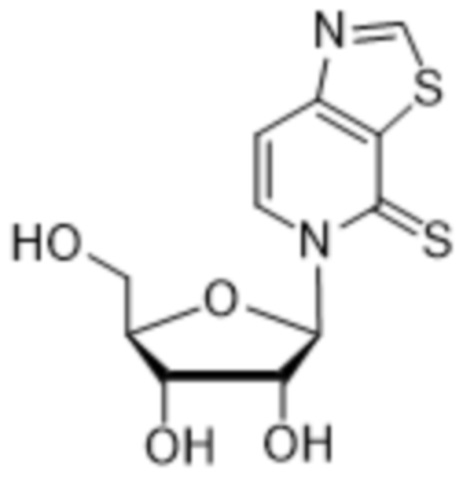 . В некоторых вариантах осуществления трифосфаты первого и второго неприродных нуклеотидов включают
. В некоторых вариантах осуществления трифосфаты первого и второго неприродных нуклеотидов включают 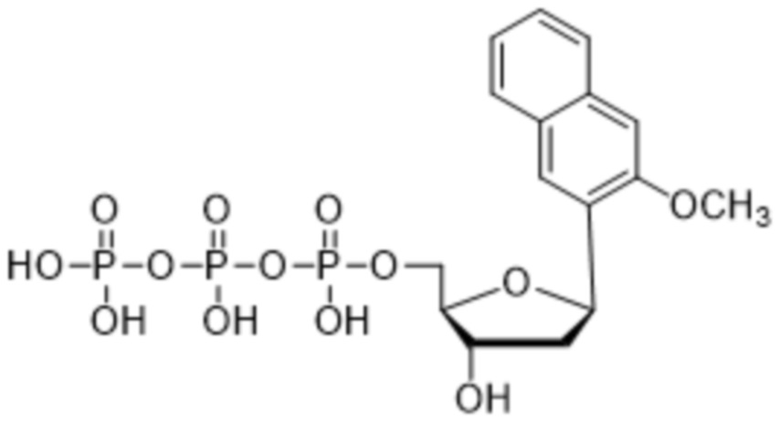 ,
, 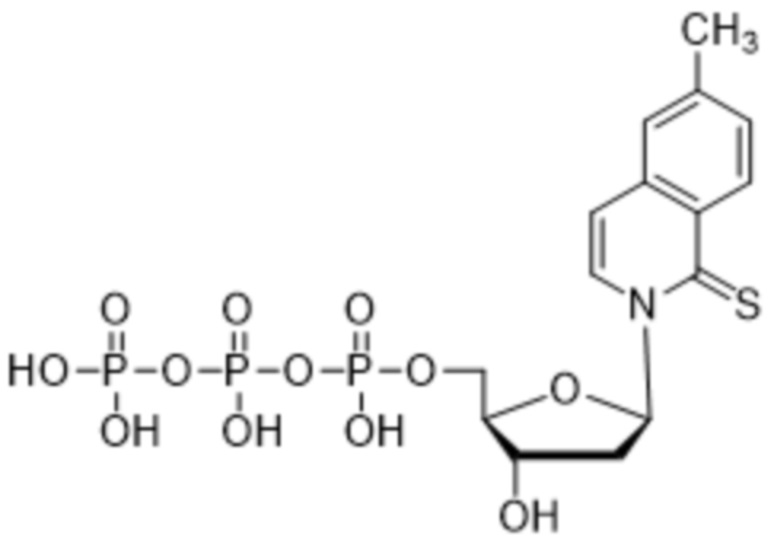 и
и 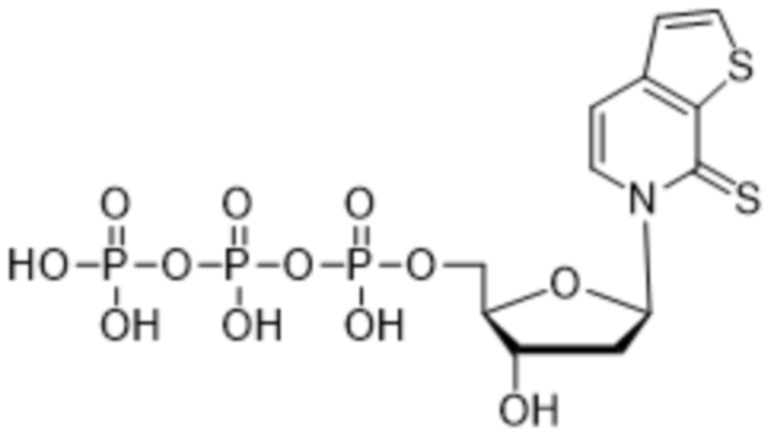 или их соли. В некоторых вариантах осуществления трифосфаты первого и второго неприродных нуклеотидов включают
или их соли. В некоторых вариантах осуществления трифосфаты первого и второго неприродных нуклеотидов включают  и
и  или их соли. В некоторых вариантах осуществления трифосфаты первого и второго неприродных нуклеотидов включают
или их соли. В некоторых вариантах осуществления трифосфаты первого и второго неприродных нуклеотидов включают  и
и 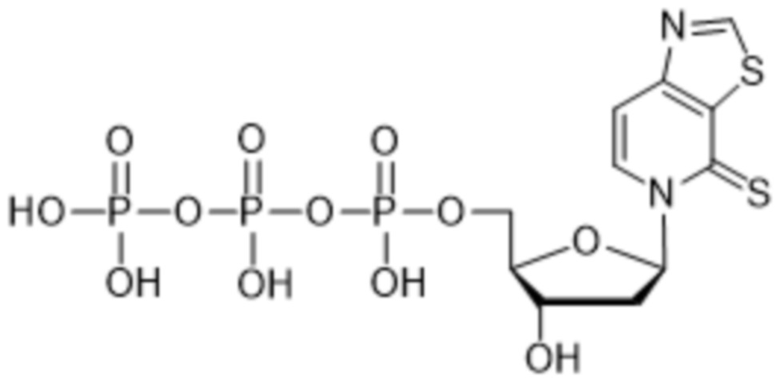 или их соли. В некоторых вариантах осуществления мРНК, полученная из двухнитевого олигонуклеотида, содержащего первый неприродный нуклеотид и второй неприродный нуклеотид, может содержать кодон, содержащий неприродный нуклеотид, полученный из
или их соли. В некоторых вариантах осуществления мРНК, полученная из двухнитевого олигонуклеотида, содержащего первый неприродный нуклеотид и второй неприродный нуклеотид, может содержать кодон, содержащий неприродный нуклеотид, полученный из 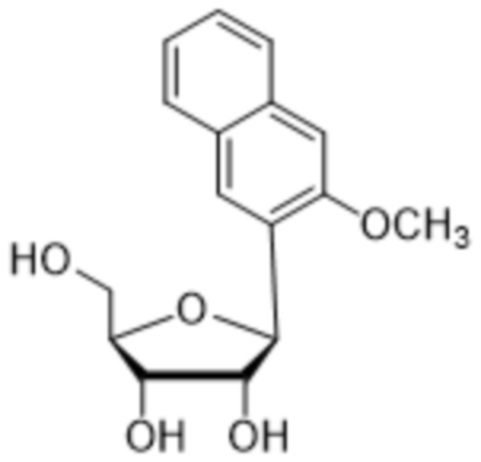 ,
, 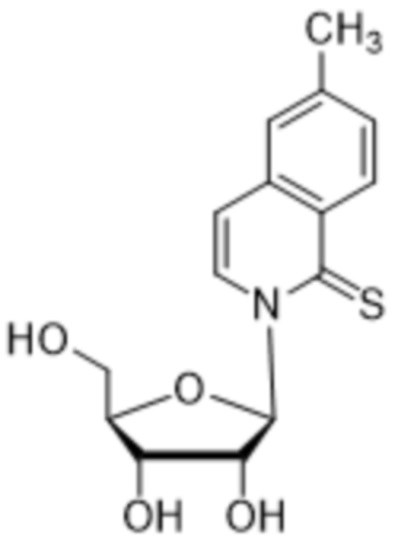 ,
, 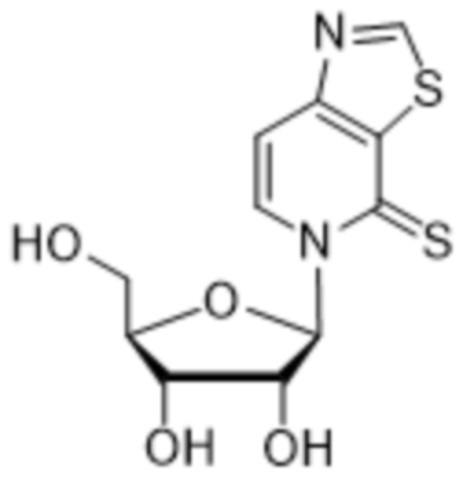 ,
, 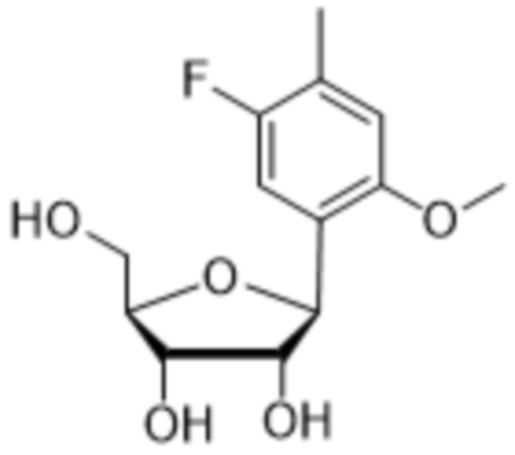 ,
, 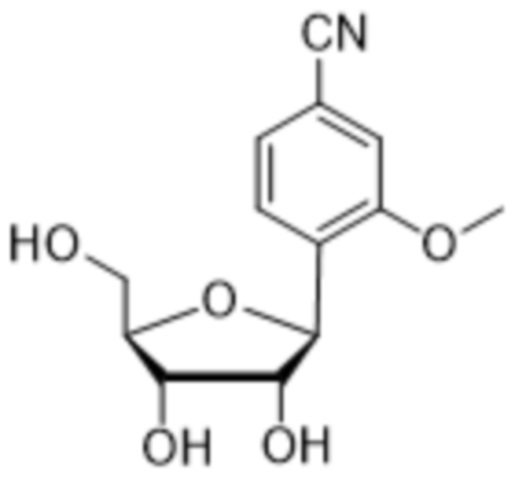 и
и 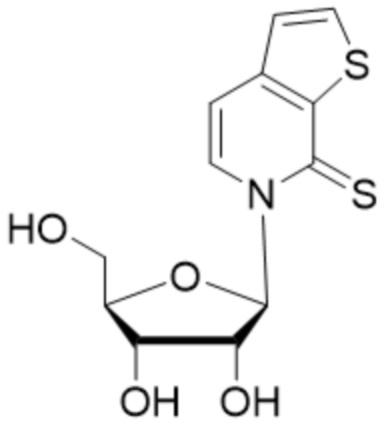 . В некоторых вариантах осуществления тРНК M. mazei может содержать антикодон, содержащий неприродный нуклеотид, который распознает кодон, содержащий неприродный нуклеотид мРНК. Антикодон в тРНК M. mazei может содержать неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления тРНК M. mazei может содержать антикодон, содержащий неприродный нуклеотид, который распознает кодон, содержащий неприродный нуклеотид мРНК. Антикодон в тРНК M. mazei может содержать неприродный нуклеотид, полученный из  ,
,  ,
,  ,
,  ,
,  и
и  . В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления тРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления тРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления тРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления тРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления тРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления тРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления тРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления тРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления тРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления тРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления тРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления тРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из  , а тРНК содержит неприродный нуклеотид, полученный из
, а тРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из  , а тРНК содержит неприродный нуклеотид, полученный из
, а тРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из  , а тРНК содержит неприродный нуклеотид, полученный из
, а тРНК содержит неприродный нуклеотид, полученный из  . В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из
. В некоторых вариантах осуществления мРНК содержит неприродный нуклеотид, полученный из  , а тРНК содержит неприродный нуклеотид, полученный из
, а тРНК содержит неприродный нуклеотид, полученный из  . Клетку-хозяина культивируют в среде, содержащей соответствующие питательные вещества и дополненной (a) трифосфатами дезоксирибонуклеозидов, содержащими одно или несколько неприродных оснований, которые необходимы для репликации плазмиды(плазмид), кодирующей(кодирующих) ген цитокина и несущей(несущих) кодон, (b) трифосфатами рибонуклеозидов, содержащими одно или несколько неприродных оснований, необходимых для транскрипции (i) мРНК, соответствующей последовательности, кодирующей цитокин, и содержащей кодон, содержащий одно или несколько неприродных оснований, и (ii) тРНК, содержащей антикодон, содержащий одно или несколько неприродных оснований, и (c) неприродной(неприродными) аминокислотой(аминокислотами), которые должны быть встроены в полипептидную последовательность представляющего интерес цитокина. Затем клетки-хозяева поддерживают в условиях, обеспечивающих экспрессию представляющего интерес белка.
. Клетку-хозяина культивируют в среде, содержащей соответствующие питательные вещества и дополненной (a) трифосфатами дезоксирибонуклеозидов, содержащими одно или несколько неприродных оснований, которые необходимы для репликации плазмиды(плазмид), кодирующей(кодирующих) ген цитокина и несущей(несущих) кодон, (b) трифосфатами рибонуклеозидов, содержащими одно или несколько неприродных оснований, необходимых для транскрипции (i) мРНК, соответствующей последовательности, кодирующей цитокин, и содержащей кодон, содержащий одно или несколько неприродных оснований, и (ii) тРНК, содержащей антикодон, содержащий одно или несколько неприродных оснований, и (c) неприродной(неприродными) аминокислотой(аминокислотами), которые должны быть встроены в полипептидную последовательность представляющего интерес цитокина. Затем клетки-хозяева поддерживают в условиях, обеспечивающих экспрессию представляющего интерес белка.
Полученный в результате экспрессируемый белок, содержащий AzK, может быть очищен способами, известными средним специалистам в данной области, а затем может быть проведена его реакция с алкином, таким как DBCO, содержащим цепь PEG, имеющую желаемую среднюю молекулярную массу, раскрытую в данном документе, в условиях, известных средним специалистам в данной области, с получением конъюгатов IL-2, раскрытых в данном документе. Средним специалистам в данной области известны и другие способы, как, например, способы, раскрытые в Zhang et al., Nature 2017, 551(7682): 644-647; WO 2015157555; WO 2015021432; WO 2016115168; WO 2017106767; WO 2017223528; WO 2019014262; WO 2019014267; WO 2019028419 и WO2019/028425, раскрытия каждой из которых включены в данный документ посредством ссылки.
Полученный в результате экспрессируемый белок, содержащий одну или несколько неприродных аминокислот, например, AzK, может быть очищен способами, известными средним специалистам в данной области, а затем может быть проведена его реакция с алкином, таким как DBCO, содержащим цепь PEG, имеющую желаемую среднюю молекулярную массу, раскрытую в данном документе, в условиях, известных средним специалистам в данной области, с получением конъюгатов IL-2, раскрытых в данном документе. Средним специалистам в данной области известны и другие способы, как, например, способы, раскрытые в Zhang et al., Nature 2017, 551(7682): 644-647; WO 2015157555; WO 2015021432; WO 2016115168; WO 2017106767; WO 2017223528; WO 2019014262; WO 2019014267; WO 2019028419 и WO2019/028425, раскрытия каждой из которых включены в данный документ посредством ссылки.
В качестве альтернативы цитокиновый полипептид (например, IL-2), содержащий неприродную(неприродные) аминокислоту(аминокислоты), получают посредством введения в клетку-хозяина описанных в данном документе конструкций нуклеиновых кислот, содержащих тРНК и аминоацил-тРНК-синтетазу и содержащих представляющую интерес последовательность нуклеиновой кислоты с одним или несколькими ортогональными (стоп-)кодонами в рамке считывания. Клетку-хозяина культивируют в среде, содержащей соответствующие питательные вещества и дополненной (a) трифосфатами дезоксирибонуклеозидов, содержащими одно или несколько неприродных оснований, требуемых для репликации плазмиды(плазмид), кодирующей(кодирующих) ген цитокина и несущей(несущих) новый кодон и антикодон, (b) трифосфатами рибонуклеозидов, требуемыми для транскрипции мРНК, соответствующей (i) последовательности цитокина, содержащей кодон, и (ii) ортогональной тРНК, содержащей антикодон, и (c) неприродной(неприродными) аминокислотой(аминокислотами). Затем клетки-хозяева поддерживают в условиях, обеспечивающих экспрессию представляющего интерес белка. Неприродная(неприродные) аминокислота(аминокислоты) встраивается(встраиваются) в полипептидную цепь в соответствии с неприродным кодоном. Например, одна или несколько неприродных аминокислот встраиваются в цитокиновый полипептид (например, IL-2). В качестве альтернативы две или более неприродные аминокислоты могут встраиваться в цитокиновый полипептид (например, IL-2) в двух или более сайтах белка.
После продуцирования в клетке-хозяине цитокинового полипептида (например, IL-2), в который встроена(встроены) неприродная(неприродные) аминокислота(аминокислоты), он может быть экстрагирован из нее с помощью ряда методик, известных из уровня техники, в том числе ферментативного, химического и/или осмотического лизиса и физического разрушения. Цитокиновый полипептид (например, IL-2) может быть очищен с помощью стандартных методик, известных из уровня техники, таких как препаративная ионообменная хроматография, гидрофобная хроматография, аффинная хроматография, или посредством любой другой подходящей методики, известной средним специалистам в данной области.
Подходящие клетки-хозяева могут включать бактериальные клетки (например, E. coli, BL21(DE3)), но в наиболее подходящем случае клетки-хозяева являются эукариотическими клетками, например, клетками насекомых (например, представителя рода Drosophila, такого как Drosophila melanogaster), дрожжевыми клетками, клетками нематод (например, C. elegans), клетками мышей (например, Mus musculus) или млекопитающих (такими как клетки яичника китайского хомячка (CHO) или клетки COS, клетки человека 293T, клетки HeLa, клетки NIH/3T3 и клетки эритролейкоза мыши (MEL)) или клетками человека или другими эукариотическими клетками. Другие подходящие клетки-хозяева известны специалистам в данной области. В подходящем случае клетка-хозяин представляет собой клетку млекопитающего, такую как клетка человека, или клетку насекомого. В некоторых вариантах осуществления подходящие клетки-хозяева предусматривают E. coli.
Другими подходящими клетками-хозяевами, которые в целом можно использовать в вариантах осуществления настоящего изобретения, являются клетки, упомянутые в разделе "Примеры". Векторную ДНК можно вводить в клетки-хозяева с помощью традиционных методик трансформации или трансфекции. Используемые в данном документе термины "трансформация" и "трансфекция" предназначены для обозначения ряда хорошо известных методик введения чужеродной молекулы нуклеиновой кислоты (например, ДНК) в клетку-хозяина, в том числе соосаждения фосфатом кальция или хлоридом кальция, трансфекции, опосредованной DEAE-декстраном, липофекции или электропорации. Подходящие способы трансформации или трансфекции клеток-хозяев хорошо известны из уровня техники.
При создании линий клеток обычно предпочтительно получать стабильные линии клеток. Например, известно, что в случае стабильной трансфекции клеток млекопитающих в зависимости от применяемых вектора экспрессии и методики трансфекции только небольшая часть клеток может интегрировать чужеродную ДНК в свой геном. Для идентификации и отбора этих интегрантов в клетки-хозяева вместе с представляющим интерес геном обычно вводят ген, который кодирует селектируемый маркер (например, для устойчивости к антибиотикам). Предпочтительные селектируемые маркеры включают маркеры, которые придают устойчивость к лекарственным средствам, таким как G418, гигромицин или метотрексат. Молекулы нуклеиновой кислоты, кодирующие селектируемый маркер, можно вводить в клетку-хозяина в том же векторе или можно вводить в отдельном векторе. Клетки, стабильно трансфицированные введенной молекулой нуклеиновой кислоты, можно идентифицировать посредством отбора по чувствительности к лекарственному средству (например, клетки, которые содержат встроенный ген селектируемого маркера, выживают, тогда как другие клетки погибают).
В одном варианте осуществления описанные в данном документе конструкции интегрируются в геном клетки-хозяина. Преимущество стабильной интеграции состоит в том, что достигается однородность между отдельными клетками или клонами. Еще одно преимущество состоит в возможности осуществления отбора лучших продуцентов. Соответственно, желательно создавать стабильные линии клеток. В другом варианте осуществления описанными в данном документе конструкциями трансфицируют клетку-хозяина. Преимущество трансфекции клетки-хозяина конструкциями состоит в том, что показатели выхода белка могут быть увеличены до максимума. В одном аспекте описана клетка, содержащая конструкцию нуклеиновой кислоты или вектор, описанные в данном документе.
Дополнительные средства
В некоторых вариантах осуществления в данном документе описан способ лечения пролиферативного заболевания или состояния у нуждающегося в этом субъекта, который включает введение субъекту терапевтически эффективного количества конъюгата цитокина (например, конъюгата IL-2), описанного в данном документе. В некоторых вариантах осуществления в данном документе описан способ лечения рака у нуждающегося в этом субъекта, который включает введение субъекту терапевтически эффективного количества конъюгата цитокина (например, конъюгата IL-2), описанного в данном документе, в комбинации с одним или несколькими дополнительными средствами. В некоторых вариантах осуществления в данном документе описан способ лечения рака у нуждающегося в этом субъекта, который включает введение субъекту терапевтически эффективного количества конъюгата цитокина (например, конъюгата IL-2), описанного в данном документе, в комбинации с одним или несколькими ингибиторами контрольных точек иммунного ответа.
В некотором варианте осуществления одно или несколько дополнительных средств включают в себя один или несколько ингибиторов контрольных точек иммунного ответа, выбранных из ингибиторов PD-1. В некотором варианте осуществления одно или несколько дополнительных средств включают в себя один или несколько ингибиторов PD-1. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 выбраны из пембролизумаба, ниволумаба, цемиплимаба, ламбролизумаба, AMP-224, синтилимаба, торипалимаба, камрелизумаба, тислелизумаба, достарлимаба (GSK), PDR001 (Novartis), MGA012 (MacroGenics/Incyte), GLS-010 (Arcus/WuXi), AGEN2024 (Agenus), цетрелимаба (Janssen), ABBV-181 (Abbvie), AMG-404 (Amgen), BI-754091 (Boehringer Ingelheim), CC-90006 (Celgene), JTX-4014 (Jounce), PF-06801591 (Pfizer) и генолимзумаба (Apollomics/Genor BioPharma). В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой пембролизумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой ниволумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой цемиплимаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой ламбролизумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой AMP-224. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой синтилимаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой торипалимаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой камрелизумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой тислелизумаб.
В некоторых вариантах осуществления одно или несколько дополнительных средств включают в себя ингибиторы контрольных точек иммунного ответа, выбранные из ингибиторов PD-L1. В некоторых вариантах осуществления один или несколько ингибиторов PD-L1 выбраны из атезолизумаба, авелумаба и дурвалумаба, ASC22 (Alphamab/Ascletis), CX-072 (CytomX), CS1001 (CStone), косибелимаба (Checkpoint Therapeutics), INCB86550 (Incyte) и TG-1501 (TG Therapeutics). В некоторых вариантах осуществления один или несколько ингибиторов PD-L1 представляют собой атезолизумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-L1 представляют собой авелумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-L1 представляют собой дурвалумаб. В некоторых вариантах осуществления один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов CTLA-4. В некоторых вариантах осуществления один или несколько ингибиторов CTLA-4 выбраны из тремелимумаба, ипилимумаба и AGEN-1884 (Agenus). В некоторых вариантах осуществления один или несколько ингибиторов CTLA-4 представляют собой тремелимумаб. В некоторых вариантах осуществления один или несколько ингибиторов CTLA-4 представляют собой ипилимумаб.
В некоторых вариантах осуществления одно или несколько дополнительных средств включают в себя ингибиторы контрольных точек иммунного ответа, выбранные из ингибиторов CTLA-4. В некоторых вариантах осуществления ингибитор CTLA-4 выбран из тремелимумаба и ипилимумаба. В некоторых вариантах осуществления ингибитор CTLA-4 представляет собой тремелимумаб. В некоторых вариантах осуществления ингибитор CTLA-4 представляет собой ипилимумаб.
Способы лечения
В данном документе описаны способы лечения рака у нуждающегося в этом субъекта, включающие введение субъекту эффективного количества (a) конъюгата IL-2, описанного в данном документе, и (b) одного или нескольких дополнительных средств. В некоторых вариантах осуществления в данном документе описаны способы лечения рака у нуждающегося в этом субъекта, включающие введение субъекту эффективного количества (a) конъюгата IL-2, описанного в данном документе, и (b) одного или нескольких ингибиторов контрольных точек иммунного ответа.
Типы рака
В данном документе описаны способы лечения рака у субъекта, включающие введение нуждающемуся в этом субъекту эффективного количества конъюгата IL-2, описанного в данном документе. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, рак у субъекта выбран из почечноклеточной карциномы (RCC), немелкоклеточного рака легкого (NSCLC), плоскоклеточного рака головы и шеи (HNSCC), классической лимфомы Ходжкина (cHL), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), уротелиальной карциномы, рака с микросателлитной нестабильностью, рака с микросателлитной стабильностью, рака желудка, рака шейки матки, гепатоцеллюлярной карциномы (HCC), карциномы из клеток Меркеля (MCC), меланомы, мелкоклеточного рака легкого (SCLC), рака пищевода, глиобластомы, мезотелиомы, рака молочной железы, трижды негативного рака молочной железы, рака предстательной железы, кастрационно-резистентного рака предстательной железы, метастатического кастрационно-резистентного рака предстательной железы или метастатического кастрационно-резистентного рака предстательной железы с дефектами ответа на повреждение ДНК (DDR), рака мочевого пузыря, рака яичника, опухолей с мутационной нагрузкой от умеренной до низкой, плоскоклеточной карциномы кожи (CSCC), плоскоклеточного рака кожи (SCSC), опухолей с экспрессией PD-L1 от низкой до отсутствующей, опухолей, распространяющихся системно в печень и CNS за пределы их первичного анатомического участка происхождения, и диффузной крупноклеточной В-клеточной лимфомы.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, рак у субъекта выбран из почечноклеточной карциномы (RCC), немелкоклеточного рака легкого (NSCLC), уротелиальной карциномы, меланомы, карциномы из клеток Меркеля (MCC) и плоскоклеточного рака головы и шеи (HNSCC). В одном варианте осуществления рак представляет собой почечноклеточную карциному (RCC). В одном варианте осуществления рак представляет собой немелкоклеточный рак легкого (NSCLC). В одном варианте осуществления рак представляет собой уротелиальную карциному. В одном варианте осуществления рак представляет собой меланому. В одном варианте осуществления рак представляет собой карциному из клеток Меркеля (MCC). В одном варианте осуществления рак представляет собой плоскоклеточный рак головы и шеи (HNSCC).
В некоторых вариантах осуществления представлены способы, описанные в данном документе, где одно или несколько дополнительных средств включают в себя один или несколько ингибиторов контрольных точек иммунного ответа.
В некоторых вариантах осуществления один или несколько ингибиторов контрольных точек иммунного ответа выбраны из группы, состоящей из ингибиторов PD-1, ингибиторов PD-L1, ингибиторов PD-L2, ингибиторов CTLA-4, агонистов OX40 и агонистов 4-1BB.
В некоторых вариантах осуществления один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов PD-1. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 выбраны из пембролизумаба, ниволумаба, цемиплимаба, ламбролизумаба, AMP-224, синтилимаба, торипалимаба, камрелизумаба, тислелизумаба, достарлимаба (GSK), PDR001 (Novartis), MGA012 (Macrogenics/Incyte), GLS-010 (Arcus/WuXi), AGEN2024 (Agenus), цетрелимаба (Janssen), ABBV-181 (Abbvie), AMG-404 (Amgen), BI-754091 (Boehringer Ingelheim), CC-90006 (Celgene), JTX-4014 (Jounce), PF-06801591 (Pfizer) и генолимзумаба (Apollomics/Genor BioPharma). В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой пембролизумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой ниволумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой цемиплимаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой ламбролизумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой AMP-224. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой синтилимаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой торипалимаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой камрелизумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-1 представляют собой тислелизумаб.
В некоторых вариантах осуществления один или несколько ингибиторов PD-L1 выбраны из атезолизумаба, авелумаба и дурвалумаба, ASC22 (Alphamab/Ascletis), CX-072 (CytomX), CS1001 (CStone), косибелимаба (Checkpoint Therapeutics), INCB86550 (Incyte) и TG-1501 (TG Therapeutics). В некоторых вариантах осуществления один или несколько ингибиторов PD-L1 представляют собой атезолизумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-L1 представляют собой авелумаб. В некоторых вариантах осуществления один или несколько ингибиторов PD-L1 представляют собой дурвалумаб. В некоторых вариантах осуществления один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов CTLA-4. В некоторых вариантах осуществления один или несколько ингибиторов CTLA-4 выбраны из тремелимумаба, ипилимумаба и AGEN-1884 (Agenus). В некоторых вариантах осуществления один или несколько ингибиторов CTLA-4 представляют собой тремелимумаб. В некоторых вариантах осуществления один или несколько ингибиторов CTLA-4 представляют собой ипилимумаб.
В некоторых вариантах осуществления один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов CTLA-4. В некоторых вариантах осуществления ингибитор CTLA-4 выбран из тремелимумаба и ипилимумаба. В некоторых вариантах осуществления ингибитор CTLA-4 представляет собой тремелимумаб. В некоторых вариантах осуществления ингибитор CTLA-4 представляет собой ипилимумаб.
В некоторых вариантах осуществления рак имеет форму солидной опухоли. В некоторых вариантах осуществления рак имеет форму опухоли жидких тканей.
В некоторых вариантах осуществления конъюгат IL-2 вводят субъекту до введения субъекту одного или нескольких дополнительных средств. В некоторых вариантах осуществления одно или несколько дополнительных средств вводят субъекту до введения субъекту конъюгата IL-2. В некоторых вариантах осуществления конъюгат IL-2 и одно или несколько дополнительных средств вводят субъекту одновременно.
В некоторых вариантах осуществления способ дополнительно включает введение субъекту терапевтически эффективного количества одного или нескольких ингибиторов сигнального пути фактора роста клеток эндотелия сосудов (VEGF) или мишени рапамицина у млекопитающих (mTOR) в дополнение к одному или нескольким ингибиторам контрольных точек. В некоторых вариантах осуществления субъекту вводят один или несколько ингибиторов сигнального пути VEGF. В некоторых вариантах осуществления один или несколько ингибиторов сигнального пути VEGF выбраны из группы, состоящей из ингибиторов тирозинкиназного (TKI) рецептора фактора роста клеток эндотелия сосудов (VEGFR) и моноклональных антител к VEGF. В некоторых вариантах осуществления один или несколько ингибиторов сигнального пути VEGF выбраны из одного или нескольких TKI VEGFR. В некоторых вариантах осуществления один или несколько TKI VEGFR выбраны из группы, состоящей из кабозантиниба, акситиниба, пазопаниба, сунитиниба или сорафениба. В некоторых вариантах осуществления один или несколько TKI VEGFR представляют собой кабозантиниб. В некоторых вариантах осуществления один или несколько TKI VEGFR представляют собой акситиниб. В некоторых вариантах осуществления один или несколько TKI VEGFR представляют собой пазопаниб. В некоторых вариантах осуществления один или несколько TKI VEGFR представляют собой сунитиниб. В некоторых вариантах осуществления где один или несколько TKI VEGFR представляют собой сорафениб. В некоторых вариантах осуществления один или несколько ингибиторов сигнального пути VEGF выбраны из одного или нескольких моноклональных антител к VEGF. В некоторых вариантах осуществления одно или несколько моноклональных антител к VEGF представляют собой бевацизумаб.
В некоторых вариантах осуществления один или несколько ингибиторов mTOR выбраны из группы, состоящей из рапамицина, эверолимуса, темсиролимуса, ридафоролимуса и дефоролимуса. В некоторых вариантах осуществления один или несколько ингибиторов mTOR представляют собой рапамицин. В некоторых вариантах осуществления один или несколько ингибиторов mTOR представляют собой эверолимус. В некоторых вариантах осуществления один или несколько ингибиторов mTOR представляют собой темсиролимус. В некоторых вариантах осуществления один или несколько ингибиторов mTOR представляют собой ридафоролимус. В некоторых вариантах осуществления один или несколько ингибиторов mTOR представляют собой дефоролимус. В некоторых вариантах осуществления рак у субъекта представляет собой почечноклеточную карциному (RCC).
В некоторых вариантах осуществления способы дополнительно включают введение субъекту терапевтически эффективного количества одного или нескольких ингибиторов поли-ADP-рибозополимеразы (PARP) в дополнение к одному или нескольким ингибиторам контрольных точек. В некоторых вариантах осуществления ингибиторы PARP выбраны из группы, состоящей из олапариба, нирапариба, рукапариба, талазопариба, велипариба, CEP-9722 и E7016. В некоторых вариантах осуществления ингибитор PARP представляет собой олапариб. В некоторых вариантах осуществления ингибитор PARP представляет собой нирапариб. В некоторых вариантах осуществления ингибитор PARP представляет собой рукапариб. В некоторых вариантах осуществления ингибитор PARP представляет собой талазопариб. В некоторых вариантах осуществления ингибитор PARP представляет собой велипариб. В некоторых вариантах осуществления ингибитор PARP представляет собой CEP-9722. В некоторых вариантах осуществления ингибитор PARP представляет собой E7016.
В некоторых вариантах осуществления способы дополнительно включают введение субъекту терапевтически эффективного количества нестероидного антиандрогенного соединения (NSAA) в дополнение к одному или нескольким ингибиторам контрольных точек. В некоторых вариантах осуществления NSAA представляет собой флутамид, нилутамид, бикалутамид, топилутамид, апалутамид или энзалутамид. В некоторых вариантах осуществления NSAA представляет собой флутамид. В некоторых вариантах осуществления NSAA представляет собой нилутамид. В некоторых вариантах осуществления NSAA представляет собой бикалутамид. В некоторых вариантах осуществления NSAA представляет собой топилутамид. В некоторых вариантах осуществления NSAA представляет собой апалутамид. В некоторых вариантах осуществления NSAA представляет собой энзалутамид.
В некоторых вариантах осуществления способы дополнительно включают введение субъекту терапевтически эффективного количества одного или нескольких ингибиторов поли-ADP-рибозополимеразы (PARP) и нестероидного антиандрогенного соединения (NSAA) в дополнение к одному или нескольким ингибиторам контрольных точек, где ингибиторы PARP и NSAA могут быть независимо выбраны из изложенных выше.
В некоторых вариантах осуществления одно или несколько дополнительных средств дополнительно включают в себя одно или несколько химиотерапевтических средств в дополнение к одному или нескольким ингибиторам контрольных точек. В некоторых вариантах осуществления одно или несколько химиотерапевтических средств включают в себя одно или несколько химиотерапевтических средств на основе платины. В некоторых вариантах осуществления одно или несколько химиотерапевтических средств включают в себя карбоплатин и пеметрексед. В некоторых вариантах осуществления одно или несколько химиотерапевтических средств включают в себя карбоплатин и наб-паклитаксел. В некоторых вариантах осуществления одно или несколько химиотерапевтических средств включают в себя карбоплатин и доцетаксел. В некоторых вариантах осуществления рак у субъекта представляет собой немелкоклеточный рак легкого (NSCLC).
В некоторых вариантах осуществления одно или несколько дополнительных средств представляют собой одно или несколько химиотерапевтических средств. В некоторых вариантах осуществления одно или несколько химиотерапевтических средств включают в себя одно или несколько химиотерапевтических средств на основе платины. В некоторых вариантах осуществления у субъекта имеется положительный результат тестирования на вирус папилломы человека (HPV) до введения конъюгата IL-2 и одного или нескольких дополнительных средств. В некоторых вариантах осуществления рак у субъекта представляет собой плоскоклеточный рак головы и шеи (HNSCC). В некоторых вариантах осуществления способ дополнительно предусматривает положительный результат тестирования субъекта на вирус папилломы человека (HPV+) с последующим введением конъюгата IL-2 и одного или нескольких дополнительных средств.
Введение
В некоторых вариантах осуществления после введения конъюгата IL-2 и одного или нескольких дополнительных средств субъект испытывает ответ, измеряемый с помощью иммуноопосредованных критериев оценки ответа солидных опухолей (iRECIST).
В некоторых вариантах осуществления ответ представляет собой полный ответ, частичный ответ или стабилизацию заболевания. В некоторых вариантах осуществления конъюгат IL-2 вводят субъекту путем внутривенной, подкожной, внутримышечной, интрацеребральной, интраназальной, внутриартериальной, внутрисуставной, внутрикожной, интравитреальной, внутрикостной инфузии, внутрибрюшинного или интратекального введения. В некоторых вариантах осуществления конъюгат IL-2 вводят субъекту путем внутривенного, подкожного или внутримышечного введения. В некоторых вариантах осуществления конъюгат IL-2 вводят субъекту путем внутривенного введения. В некоторых вариантах осуществления конъюгат IL-2 вводят субъекту путем подкожного введения. В некоторых вариантах осуществления конъюгат IL-2 вводят субъекту путем внутримышечного введения.
В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в неделю, один раз в две недели, один раз в три недели, один раз в 4 недели, один раз в 5 недель, один раз в 6 недель, один раз в 7 недель, один раз в 8 недель, один раз в 9 недель, один раз в 10 недель, один раз в 11 недель, один раз в 12 недель, один раз в 13 недель, один раз в 14 недель, один раз в 15 недель, один раз в 16 недель, один раз в 17 недель, один раз в 18 недель, один раз в 19 недель, один раз в 20 недель, один раз в 21 неделю, один раз в 22 недели, один раз в 23 недели, один раз в 24 недели, один раз в 25 недель, один раз в 26 недель, один раз в 27 недель или один раз в 28 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в неделю. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в две недели. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в три недели. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 4 недели. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 5 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 6 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 7 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 8 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 9 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 10 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 11 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 12 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 13 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 14 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 15 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 16 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 17 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 18 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 19 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 20 недель. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 21 неделю. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 22 недели. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 23 недели. В некоторых вариантах осуществления эффективное количество конъюгата IL-2 вводят нуждающемуся в этом субъекту один раз в 24 недели.
В некоторых вариантах осуществления количество указанного средства, которое соответствует такому количеству, варьируется в зависимости от таких факторов, как конкретное соединение, тяжесть заболевания, индивидуальные характеристики (например, масса) субъекта или хозяина, нуждающегося в лечении, но тем не менее обычно определяется способом, известным из уровня техники, в соответствии с конкретными обстоятельствами, относящимися к конкретному случаю, включающими, например, конкретное вводимое средство, путь введения и субъекта или хозяина, получающего лечение. В некоторых случаях желаемая доза в целях удобства представлена в виде однократной дозы или разделенных доз, вводимых одновременно (или в течение короткого периода времени) или с соответствующими интервалами, например, в виде двух, трех, четырех или более частей дозы в день.
В некоторых вариантах осуществления способы включают введение дозы конъюгата IL-2 нуждающемуся в этом субъекту в диапазоне дозы от 1 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 2 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 4 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 6 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 8 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 10 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 12 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 14 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 16 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 18 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 20 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 22 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 24 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 26 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 28 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 32 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 34 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 36 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 40 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 45 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 50 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 55 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 60 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 65 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 70 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 75 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 80 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 85 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 90 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 95 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 100 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 110 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 120 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 130 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 140 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 150 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 160 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 170 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 180 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта, или от приблизительно 190 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта. Вышеупомянутые диапазоны являются лишь предположительными, поскольку количество переменных, относящихся к индивидуальному режиму лечения, велико, и существенные отклонения от этих рекомендуемых значений не являются редкостью. Такие дозы изменяются в зависимости от ряда переменных, не ограничивающихся активностью применяемого соединения, заболеванием или состоянием, подлежащим лечению, способом введения, потребностями отдельного субъекта, тяжестью заболевания или состояния, подлежащего лечению, и мнением практикующего специалиста. В некоторых вариантах осуществления токсичность и терапевтическую эффективность таких терапевтических режимов определяют с помощью стандартных фармацевтических процедур в культурах клеток или у экспериментальных животных, включая без ограничения определение LD50 (дозы, летальной для 50% популяции) и ED50 (дозы, терапевтически эффективной для 50% популяции). Соотношение доз для токсического и терапевтического эффектов представляет собой терапевтический индекс и выражается в виде соотношения между LD50 и ED50. Предпочтительными являются соединения, демонстрирующие высокие терапевтические индексы. Данные, полученные в анализах культур клеток и в исследованиях на животных, используются при составлении диапазона доз для применения у человека. Доза таких соединений предпочтительно находится в пределах диапазона циркулирующих концентраций, который включает ED50 с минимальной токсичностью. Доза варьируется в пределах этого диапазона в зависимости от используемой лекарственной формы и используемого пути введения.
В некоторых вариантах осуществления способы включают введение дозы конъюгата IL-2 нуждающемуся в этом субъекту в дозе, составляющей приблизительно 1 мкг конъюгата IL-2 на кг массы тела субъекта или приблизительно 2 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 4 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 6 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 8 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 10 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 12 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 14 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 16 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 18 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 20 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 22 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 24 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 26 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 28 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 30 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 32 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 34 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 36 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 38 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 40 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 42 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 44 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 46 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 48 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 50 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 55 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 60 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 65 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 70 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 75 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 80 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 85 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 90 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 95 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 100 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 110 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 120 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 130 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 140 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 150 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 160 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 170 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 180 мкг конъюгата IL-2 на кг массы тела субъекта, приблизительно 190 мкг конъюгата IL-2 на кг массы тела субъекта или приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта. Вышеупомянутые диапазоны являются лишь предположительными, поскольку количество переменных, относящихся к индивидуальному режиму лечения, велико, и существенные отклонения от этих рекомендуемых значений не являются редкостью. Такие дозы изменяются в зависимости от ряда переменных, не ограничивающихся активностью применяемого соединения, заболеванием или состоянием, подлежащим лечению, способом введения, потребностями отдельного субъекта, тяжестью заболевания или состояния, подлежащего лечению, и мнением практикующего специалиста. В некоторых вариантах осуществления токсичность и терапевтическую эффективность таких терапевтических режимов определяют с помощью стандартных фармацевтических процедур в культурах клеток или у экспериментальных животных, включая без ограничения определение LD50 (дозы, летальной для 50% популяции) и ED50 (дозы, терапевтически эффективной для 50% популяции). Соотношение доз для токсического и терапевтического эффектов представляет собой терапевтический индекс и выражается в виде соотношения между LD50 и ED50. Предпочтительными являются соединения, демонстрирующие высокие терапевтические индексы. Данные, полученные в анализах культур клеток и в исследованиях на животных, используются при составлении диапазона доз для применения у человека. Доза таких соединений предпочтительно находится в пределах диапазона циркулирующих концентраций, который включает ED50 с минимальной токсичностью. Доза варьируется в пределах этого диапазона в зависимости от используемой лекарственной формы и используемого пути введения.
В некоторых вариантах осуществления дополнительное средство можно вводить в дозе и с использованием режима введения доз, которые были определены как безопасные и эффективные для этого дополнительного средства. Например, пембролизумаб можно вводить нуждающемуся в этом субъекту согласно способам, описанным в данном документе, в дозе, составляющей приблизительно 200 мг, каждые 3 недели. В другом примере ниволумаб можно вводить нуждающемуся в этом субъекту согласно способам, описанным в данном документе, в дозе, составляющей приблизительно 240 мг, каждые 2 недели или в дозе, составляющей приблизительно 480 мг, каждые 4 недели. В другом примере цемиплимаб можно вводить нуждающемуся в этом субъекту согласно способам, описанным в данном документе, в дозе, составляющей приблизительно 350 мг, в виде внутривенной инфузии в течение 30 минут каждые 3 недели. В другом примере атезолизумаб можно вводить субъекту согласно способам, описанным в данном документе, в дозе 840 мг каждые 2 недели, 1200 мг каждые 3 недели или 1680 мг каждые 4 недели. В другом примере авелумаб можно вводить субъекту согласно способам, описанным в данном документе, в дозе 800 мг каждые 2 недели. В другом примере дурвалумаб можно вводить субъекту согласно способам, описанным в данном документе, в дозе 10 мг на кг массы тела субъекта каждые 2 недели. В другом примере ипилимумаб можно вводить субъекту для лечения меланомы согласно способам, описанным в данном документе, в дозе, составляющей приблизительно 3 мг на кг массы тела субъекта в течение 90 минут каждые три недели в общей сложности в количестве 4 доз или приблизительно 10 мг на кг массы тела субъекта в течение 90 минут в общей сложности в количестве 4 доз, а затем 10 мг на кг массы тела субъекта на протяжении до 3 лет. При почечноклеточной карциноме на поздней стадии ипилимумаб можно вводить согласно способам, описанным в данном документе, в дозе 1 мг на кг массы тела субъекта в течение 30 минут.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не требует наличия отделения интенсивной терапии или квалифицированных специалистов в области сердечно-легочной медицины или интенсивной терапии. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не требует наличия отделения интенсивной терапии или квалифицированных специалистов в области сердечно-легочной медицины или интенсивной терапии. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не требует наличия отделения интенсивной терапии. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не требует наличия квалифицированных специалистов в области сердечно-легочной медицины или интенсивной терапии.
Эффекты введения
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости сосудов у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости сосудов 2 степени, 3 степени или 4 степени у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости сосудов 2 степени у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости сосудов 3 степени у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости сосудов 4 степени у субъекта.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает потерю сосудистого тонуса у субъекта.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает транссудацию белков и жидкости плазмы крови во внесосудистое пространство у субъекта.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает гипотензию и снижение перфузии органов у субъекта.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает нарушение функции нейтрофилов у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает снижение хемотаксиса у субъекта.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не ассоциировано с увеличенным риском диссеминированной инфекции у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, диссеминированная инфекция представляет собой сепсис или бактериальный эндокардит. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, диссеминированная инфекция представляет собой сепсис. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, диссеминированная инфекция представляет собой бактериальный эндокардит. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, субъект получает лечение любых предсуществующих бактериальных инфекций до введения конъюгата IL-2. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, субъект получает лечение с помощью антибактериального средства, выбранного из оксациллина, нафциллина, ципрофлоксацина и ванкомицина, до введения конъюгата IL-2.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не приводит к усугублению предсуществующего или первоначально проявляющегося аутоиммунного заболевания или воспалительного нарушения у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не приводит к усугублению предсуществующего или первоначально проявляющегося аутоиммунного заболевания у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не приводит к усугублению предсуществующего или первоначально проявляющегося воспалительного нарушения у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, аутоиммунное заболевание или воспалительное нарушение у субъекта выбрано из болезни Крона, склеродермии, тиреоидита, воспалительного артрита, сахарного диабета, окулобульбарной тяжелой миастении, серповидного IgA-гломерулонефрита, холецистита, церебрального васкулита, синдрома Стивенса-Джонсона и буллезного пемфигоида. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой болезнь Крона. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой склеродермию. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой тиреоидит. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой воспалительный артрит. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой сахарный диабет. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой окулобульбарную тяжелую миастению. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой серповидный IgA-гломерулонефрит. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой холецистит. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой церебральный васкулит. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой синдром Стивенса-Джонсона. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой буллезный пемфигоид.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает изменения психического состояния, затруднения речи, корковую слепоту, атаксию конечностей или походки, галлюцинации, возбуждение, притупление чувствительности или кому у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает судороги у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не противопоказано субъектам, у которых имеется подтвержденное судорожное расстройство.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости капилляров у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости капилляров 2 степени, 3 степени или 4 степени у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости капилляров 2 степени у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости капилляров 3 степени у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости капилляров 4 степени у субъекта.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает снижение среднего артериального кровяного давления у субъекта после введения конъюгата IL-2 субъекту. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает гипотензию у субъекта после введения конъюгата IL-2 субъекту. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не приводит к тому, что субъект испытывает систолическое кровяное давление ниже 90 мм рт. ст. или снижение систолического давления на 20 мм рт. ст. от исходного уровня после введения конъюгата IL-2 субъекту.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает отек у субъекта после введения конъюгата IL-2 субъекту. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает нарушение функции почек или печени у субъекта после введения конъюгата IL-2 субъекту.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает эозинофилию у субъекта после введения конъюгата IL-2 субъекту. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не приводит к тому, что количество эозинофилов в периферической крови у субъекта превышает 500 на мкл после введения конъюгата IL-2 субъекту. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не приводит к тому, что количество эозинофилов в периферической крови у субъекта превышает 500 на мкл - 1500 на мкл после введения конъюгата IL-2 субъекту. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не приводит к тому, что количество эозинофилов в периферической крови у субъекта превышает 1500 на мкл - 5000 на мкл после введения конъюгата IL-2 субъекту. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не приводит к тому, что количество эозинофилов в периферической крови у субъекта превышает 5000 на мкл после введения конъюгата IL-2 субъекту. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не противопоказано субъектам, находящимся на режиме лечения психотропными лекарственными средствами.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не противопоказано субъектам, находящимся на режиме лечения нефротоксическими, миелотоксическими, кардиотоксическими или гепатотоксическими лекарственными средствами. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не противопоказано субъектам, находящимся на режиме лечения аминогликозидами, средствами цитотоксической химиотерапии, доксорубицином, метотрексатом или аспарагиназой. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не противопоказано субъектам, которые получают лечение в комбинированных режимах, предусматривающих противоопухолевые средства. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, противоопухолевое средство выбрано из дакарбазина, цисплатина, тамоксифена и интерферона альфа.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 субъекту не вызывает одно или несколько нежелательных явлений 4 степени у субъекта после введения конъюгата IL-2 субъекту. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, одно или несколько нежелательных явлений 4 степени выбраны из гипотермии; шока; брадикардии; желудочковой экстрасистолии; ишемии миокарда; обморока; кровоизлияния; предсердной аритмии; флебита; AV-блокады второй степени; эндокардита; перикардиального выпота; периферической гангрены; тромбоза; нарушения со стороны коронарных артерий; стоматита; тошноты и рвоты; аномалии функциональных проб печени; желудочно-кишечного кровоизлияния; гематемезиса; геморрагического поноса; нарушения со стороны желудочно-кишечного тракта; прободения кишечника; панкреатита; анемии; лейкопении; лейкоцитоза; гипокальциемии; увеличения уровня щелочной фосфатазы; увеличения концентрации азота мочевины в крови (BUN); гиперурикемии; увеличения концентрации небелкового азота (NPN); респираторного ацидоза; сонливости; возбуждения; нейропатии; параноидной реакции; спазма; большого эпилептического припадка; делирия; астмы; отека легких; гипервентиляции; гипоксии; кровохарканья; гиповентиляции; пневмоторакса; мидриаза; нарушения со стороны зрачка; аномалии функции почек; почечной недостаточности и острого канальцевого некроза. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 группе субъектов не вызывает одно или несколько нежелательных явлений 4 степени у более чем 1% субъектов после введения конъюгата IL-2 субъектам. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, одно или несколько нежелательных явлений 4 степени выбраны из гипотермии; шока; брадикардии; желудочковой экстрасистолии; ишемии миокарда; обморока; кровоизлияния; предсердной аритмии; флебита; AV-блокады второй степени; эндокардита; перикардиального выпота; периферической гангрены; тромбоза; нарушения со стороны коронарных артерий; стоматита; тошноты и рвоты; аномалии функциональных проб печени; желудочно-кишечного кровоизлияния; гематемезиса; геморрагического поноса; нарушения со стороны желудочно-кишечного тракта; прободения кишечника; панкреатита; анемии; лейкопении; лейкоцитоза; гипокальциемии; увеличения уровня щелочной фосфатазы; увеличения концентрации азота мочевины в крови (BUN); гиперурикемии; увеличения концентрации небелкового азота (NPN); респираторного ацидоза; сонливости; возбуждения; нейропатии; параноидной реакции; спазма; большого эпилептического припадка; делирия; астмы; отека легких; гипервентиляции; гипоксии; кровохарканья; гиповентиляции; пневмоторакса; мидриаза; нарушения со стороны зрачка; аномалии функции почек; почечной недостаточности и острого канальцевого некроза.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 группе субъектов не вызывает одно или несколько нежелательных явлений у более чем 1% субъектов после введения конъюгата IL-2 субъектам, где одно или несколько нежелательных явлений выбраны из язвы двенадцатиперстной кишки; некроза кишечника; миокардита; наджелудочковой тахикардии; перманентной или транзиторной слепоты на фоне неврита зрительного нерва; транзиторной ишемической атаки; менингита; отека головного мозга; перикардита; аллергического интерстициального нефрита и трахеопищеводной фистулы.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение эффективного количества конъюгата IL-2 группе субъектов не вызывает одно или несколько нежелательных явлений у более чем 1% субъектов после введения конъюгата IL-2 субъектам, где одно или несколько нежелательных явлений выбраны из злокачественной гипертермии; остановки сердца; инфаркта миокарда; легочной эмболии; инсульта; прободения кишечника; печеночной или почечной недостаточности; тяжелой депрессии, приводящей к суициду; отека легких; остановки дыхания; дыхательной недостаточности.
В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение конъюгата IL-2 субъекту приводит к увеличению количества CD8+ T- и NK-клеток в периферической крови у субъекта без увеличения количества CD4+ регуляторных T-клеток в периферической крови у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение конъюгата IL-2 субъекту приводит к увеличению количества CD8+ T- и NK-клеток в периферической крови у субъекта без увеличения количества эозинофилов в периферической крови у субъекта. В некоторых вариантах осуществления способа лечения рака, описанного в данном документе, введение конъюгата IL-2 субъекту приводит к увеличению количества CD8+ T- и NK-клеток в периферической крови у субъекта без увеличения количества внутриопухолевых CD8+ T- и NK-клеток у субъекта и без увеличения количества внутриопухолевых CD4+ регуляторных T-клеток у субъекта.
Фармацевтические композиции и составы
В данном документе описаны фармацевтические композиции, содержащие эффективное количество конъюгата IL-2, описанного в данном документе, и одно или несколько фармацевтически приемлемых наполнителей.
В некоторых вариантах осуществления фармацевтическую композицию и составы, содержащие конъюгат цитокина (например, конъюгат IL-2), описанный в данном документе, вводят субъекту посредством нескольких путей введения, включая без ограничения парентеральный, пероральный, трансбуккальный, ректальный, подъязычный или трансдермальный пути введения. В некоторых случаях парентеральное введение включает внутривенную, подкожную, внутримышечную, интрацеребральную, интраназальную, внутриартериальную, внутрисуставную, внутрикожную, интравитреальную, внутрикостную инфузию, внутрибрюшинное или интратекальное введение. В некоторых случаях фармацевтическая композиция составлена для местного введения. В других случаях фармацевтическая композиция составлена для системного введения. В некоторых вариантах осуществления фармацевтические композицию и составы, описанные в данном документе, вводят субъекту посредством внутривенного, подкожного и внутримышечного введения. В некоторых вариантах осуществления фармацевтическую композицию и составы, описанные в данном документе, вводят субъекту посредством внутривенного введения. В некоторых вариантах осуществления фармацевтическую композицию и составы, описанные в данном документе, вводят субъекту посредством введения. В некоторых вариантах осуществления фармацевтическую композицию и составы, описанные в данном документе, вводят субъекту посредством внутримышечного введения.
В некоторых вариантах осуществления фармацевтические составы включают без ограничения водные жидкие дисперсии, самоэмульгирующиеся дисперсии, твердые растворы, липосомальные дисперсии, аэрозоли, твердые лекарственные формы, порошки, составы с немедленным высвобождением, составы с контролируемым высвобождением, быстроплавкие составы, таблетки, капсулы, пилюли, составы с отсроченным высвобождением, составы с пролонгированным высвобождением, составы с пульсирующим высвобождением, составы в виде множества частиц (например, составы на основе наночастиц) и составы со смешанным немедленным и контролируемым высвобождением.
В некоторых вариантах осуществления фармацевтические составы содержат носитель или материалы-носители, выбранные на основании совместимости с композицией, раскрытой в данном документе, и характеристик профиля высвобождения желаемой лекарственной формы. Иллюстративные материалы-носители включают, например, связующие вещества, суспендирующие средства, разрыхляющие средства, заполнители, поверхностно-активные вещества, солюбилизаторы, стабилизаторы, смазывающие вещества, смачивающие средства, разбавители и т.п. Фармацевтически совместимые материалы-носители включают без ограничения аравийскую камедь, желатин, коллоидный диоксид кремния, глицерофосфат кальция, лактат кальция, мальтодекстрин, глицерин, силикат магния, поливинилпирролидон (PVP), холестерин, сложные эфиры холестерина, казеинат натрия, соевый лецитин, таурохолевую кислоту, фосфатидилхолин, хлорид натрия, фосфат трикальция, фосфат дикалия, целлюлозу и конъюгаты целлюлозы, сахара, стеароиллактилат натрия, каррагинан, моноглицерид, диглицерид, прежелатинизированный крахмал и т.п. См., например, Remington: The Science and Practice of Pharmacy, Nineteenth Ed (Easton, Pa.: Mack Publishing Company, 1995), Hoover, John E., Remington's Pharmaceutical Sciences, Mack Publishing Co., Easton, Pennsylvania 1975, Liberman, H.A. and Lachman, L., Eds., Pharmaceutical Dosage Forms, Marcel Decker, New York, N.Y., 1980, и Pharmaceutical Dosage Forms and Drug Delivery Systems, Seventh Ed. (Lippincott Williams & Wilkins 1999), раскрытия каждого из которых включены в данный документ посредством ссылки.
В некоторых случаях фармацевтическая композиция составлена в виде иммунолипосомы, которая содержит совокупность конъюгатов IL-2, непосредственно или опосредованно связанных с липидным бислоем липосом. Иллюстративные липиды включают без ограничения жирные кислоты; фосфолипиды; стерины, такие как холестерины; сфинголипиды, такие как сфингомиелин; гликосфинголипиды, такие как ганглиозиды, глобозиды и цереброзиды; аминные поверхностно-активные вещества, такие как стеарил-, олеил- и линолеиламины. В некоторых случаях липид включает в себя катионный липид. В некоторых случаях липид включает в себя фосфолипид. Иллюстративные фосфолипиды включают без ограничения фосфатидную кислоту ("PA"), фосфатидилхолин ("PC"), фосфатидилглицерин ("PG"), фосфатидилэтаноламин ("PE"), фосфатидилинозитол ("PI") и фосфатидилсерин ("PS"), сфингомиелин (в том числе сфингомиелин головного мозга), лецитин, лизолецитин, лизофосфатидилэтаноламин, цереброзиды, диарахидоилфосфатидилхолин ("DAPC"), дидеканоил-L-альфа-фосфатидилхолин ("DDPC"), диэлаидоилфосфатидилхолин ("DEPC"), дилауроилфосфатидилхолин ("DLPC"), дилинолеоилфосфатидилхолин, димиристоилфосфатидилхолин ("DMPC"), диолеоилфосфатидилхолин ("DOPC"), дипальмитоилфосфатидилхолин ("DPPC"), дистеароилфосфатидилхолин ("DSPC"), 1-пальмитоил-2-олеоилфосфатидилхолин ("POPC"), диарахидоилфосфатидилглицерин ("DAPG"), дидеканоил-L-альфа-фосфатидилглицерин ("DDPG"), диэлаидоилфосфатидилглицерин ("DEPG"), дилауроилфосфатидилглицерин ("DLPG"), дилинолеоилфосфатидилглицерин, димиристоилфосфатидилглицерин ("DMPG"), диолеоилфосфатидилглицерин ("DOPG"), дипальмитоилфосфатидилглицерин ("DPPG"), дистеароилфосфатидилглицерин ("DSPG"), 1-пальмитоил-2-олеоилфосфатидилглицерин ("POPG"), диарахидоилфосфатидилэтаноламин ("DAPE"), дидеканоил-L-альфа-фосфатидилэтаноламин ("DDPE"), диэлаидоилфосфатидилэтаноламин ("DEPE"), дилауроилфосфатидилэтаноламин ("DLPE"), дилинолеоилфосфатидилэтаноламин, димиристоилфосфатидилэтаноламин ("DMPE"), диолеоилфосфатидилэтаноламин ("DOPE"), дипальмитоилфосфатидилэтаноламин ("DPPE"), дистеароилфосфатидилэтаноламин ("DSPE"), 1-пальмитоил-2-олеоилфосфатидилэтаноламин ("POPE"), диарахидоилфосфатидилинозитол ("DAPI"), дидеканоил-L-альфа-фосфатидилинозитол ("DDPI"), диэлаидоилфосфатидилинозитол ("DEPI"), дилауроилфосфатидилинозитол ("DLPI"), дилинолеоилфосфатидилинозитол, димиристоилфосфатидилинозитол ("DMPI"), диолеоилфосфатидилинозитол ("DOPI"), дипальмитоилфосфатидилинозитол ("DPPI"), дистеароилфосфатидилинозитол ("DSPI"), 1-пальмитоил-2-олеоилфосфатидилинозитол ("POPI"), диарахидоилфосфатидилсерин ("DAPS"), дидеканоил-L-альфа-фосфатидилсерин ("DDPS"), диэлаидоилфосфатидилсерин ("DEPS"), дилауроилфосфатидилсерин ("DLPS"), дилинолеоилфосфатидилсерин, димиристоилфосфатидилсерин ("DMPS"), диолеоилфосфатидилсерин ("DOPS"), дипальмитоилфосфатидилсерин ("DPPS"), дистеароилфосфатидилсерин ("DSPS"), 1-пальмитоил-2-олеоилфосфатидилсерин ("POPS"), диарахидоилсфингомиелин, дидеканоилсфингомиелин, диэлаидоилсфингомиелин, дилауроилсфингомиелин, дилинолеоилсфингомиелин, димиристоилсфингомиелин, сфингомиелин, диолеоилсфингомиелин, дипальмитоилсфингомиелин, дистеароилсфингомиелин и 1-пальмитоил-2-олеоилсфингомиелин.
В некоторых случаях фармацевтические составы дополнительно содержат средства, регулирующие pH, или буферные средства, которые включают кислоты, такие как уксусная, борная, лимонная, молочная, фосфорная и хлористоводородная кислоты, основания, такие как гидроксид натрия, фосфат натрия, борат натрия, цитрат натрия, ацетат натрия, лактат натрия и трис-гидроксиметиламинометан, и буферы, такие как цитрат/декстроза, бикарбонат натрия и хлорид аммония. Такие кислоты, основания и буферы включают в количестве, требуемом для поддержания pH композиции в приемлемом диапазоне.
В некоторых случаях фармацевтический состав содержит одну или несколько солей в количестве, требуемом для приведения осмоляльности композиции в приемлемый диапазон. Такие соли включают соли, содержащие катионы натрия, калия или аммония и хлоридные, цитратные, аскорбатные, боратные, фосфатные, бикарбонатные, сульфатные, тиосульфатные или бисульфитные анионы, при этом подходящие соли включают хлорид натрия, хлорид калия, тиосульфат натрия, бисульфит натрия и сульфат аммония.
В некоторых вариантах осуществления фармацевтические составы содержат без ограничения сахара, такие как трегалоза, сахароза, маннит, мальтоза, глюкоза, или соли, такие как фосфат калия, цитрат натрия, сульфат аммония, и/или другие средства, такие как гепарин, для увеличения растворимости и стабильности полипептидов in vivo.
В некоторых случаях фармацевтические составы дополнительно содержат разбавитель, который применяют для стабилизации соединений, поскольку он способен обеспечить более стабильную среду. Соли, растворенные в буферных растворах (которые также способны обеспечивать контроль или поддержание pH), используют в качестве разбавителей в данной области техники, в том числе без ограничения забуференный фосфатом физиологический раствор. В некоторых случаях разбавители увеличивают объем композиции для облегчения прессования или для создания достаточного объема для получения однородной смеси для заполнения капсул. Такие соединения могут включать, например, лактозу, крахмал, маннит, сорбит, декстрозу, микрокристаллическую целлюлозу, такую как Avicel®, двухосновный фосфат кальция, дигидрат фосфата дикальция, фосфат трикальция, фосфат кальция, безводную лактозу, высушенную распылением лактозу, прежелатинизированный крахмал, прессуемый сахар, такой как Di-Pac® (Amstar), маннит, гидроксипропилметилцеллюлозу, ацетат-стеарат гидроксипропилметилцеллюлозы, разбавители на основе сахарозы, кондитерский сахар, моногидрат одноосновного сульфата кальция, дигидрат сульфата кальция, тригидрат лактата кальция, декстраты, гидролизованные сухие вещества зерновых культур, амилозу, порошковую целлюлозу, карбонат кальция, глицин, каолин, маннит, хлорид натрия, инозит, бентонит и т.п. В некоторых вариантах осуществления конъюгаты IL-2, раскрытые в данном документе, могут применяться в фармацевтических составах, содержащих гистидин, сорбит и полисорбат 80 или любую их комбинацию, дающую стабильный состав, и могут вводиться нуждающимся в этом субъектам. В одном варианте осуществления конъюгаты IL-2, раскрытые в данном документе, могут быть представлены в виде готового лекарственного препарата в подходящем контейнере, таком как флакон, в следующем виде: конъюгат IL-2 (от приблизительно 2 мг до приблизительно 10 мг); L-гистидин (от приблизительно 0,5 мг до приблизительно 2 мг); гидрохлорид L-гистидина (от приблизительно 1 мг до приблизительно 2 мг); сорбит (от приблизительно 20 мг до приблизительно 80 мг) и полисорбат 80 (от приблизительно 0,1 мг до приблизительно 0,2 мг); с достаточным количеством воды для инъекции для получения жидкого состава, подходящего для применения в раскрытых способах.
В некоторых случаях фармацевтические составы содержат разрыхляющие средства или разрыхлители для облегчения разрушения или распада вещества. Термин "распад" включает как растворение, так и диспергирование лекарственной формы при контакте с желудочно-кишечным соком. Примеры разрыхляющих средств включают крахмал, например, природный крахмал, такой как кукурузный крахмал или картофельный крахмал, прежелатинизированный крахмал, такой как National 1551 или Amijel®, или крахмалгликолят натрия, такой как Promogel® или Explotab®, целлюлозу, такую как продукт из древесины, кристаллическая метилцеллюлоза, например, Avicel®, Avicel® PH101, Avicel® PH102, Avicel® PH105, Elcema® P100, Emcocel®, Vivacel®, Ming Tia® и Solka-Floc®, метилцеллюлоза, кроскармеллоза или сшитая целлюлоза, такая как сшитая натрий-карбоксиметилцеллюлоза (Ac-Di-Sol®), сшитая карбоксиметилцеллюлоза или сшитая кроскармеллоза, сшитый крахмал, такой как крахмалгликолят натрия, сшитый полимер, такой как кросповидон, сшитый поливинилпирролидон, альгинат, такой как альгиновая кислота или соль альгиновой кислоты, такая как альгинат натрия, глину, такую как Veegum® HV (алюмосиликат магния), камедь, такую как агар, гуаровая камедь, камедь рожкового дерева, камедь карайи, пектин или трагакантовая камедь, крахмалгликолят натрия, бентонит, природную губку, поверхностно-активное вещество, смолу, такую как катионообменная смола, цитрусовую пульпу, лаурилсульфат натрия, лаурилсульфат натрия в комбинации с крахмалом и т.п.
В некоторых случаях фармацевтические составы содержат заполнители, такие как лактоза, карбонат кальция, фосфат кальция, двухосновный фосфат кальция, сульфат кальция, микрокристаллическая целлюлоза, целлюлозный порошок, декстроза, декстраты, декстран, крахмалы, прежелатинизированный крахмал, сахароза, ксилит, лактит, маннит, сорбит, хлорид натрия, полиэтиленгликоль и т.п.
Смазывающие вещества и вещества, способствующие скольжению, также необязательно включают в фармацевтические составы, описанные в данном документе, для предупреждения, снижения или ингибирования адгезии или трения материалов. Иллюстративные смазывающие вещества включают, например, стеариновую кислоту, гидроксид кальция, тальк, стеарилфумарат натрия, углеводород, такой как минеральное масло, или гидрогенизированное растительное масло, такое как гидрогенизированное соевое масло (Sterotex®), высшие жирные кислоты и их соли щелочных металлов и щелочноземельных металлов, таких как алюминий, кальций, магний, цинк, стеариновую кислоту, стеараты натрия, глицерин, тальк, воски, Stear-O-Wet®, борную кислоту, бензоат натрия, ацетат натрия, хлорид натрия, лейцин, полиэтиленгликоль (например, PEG-4000) или метоксиполиэтиленгликоль, такой как Carbowax™, олеат натрия, бензоат натрия, глицерилбегенат, полиэтиленгликоль, лаурилсульфат магния или натрия, коллоидный диоксид кремния, такой как Syloid™, Cab-O-Sil®, крахмал, такой как кукурузный крахмал, кремнийорганическое масло, поверхностно-активное вещество и т.п.
Пластификаторы включают соединения, применяемые для размягчения микроинкапсулирующего материала или пленочных покрытий, чтобы сделать их менее хрупкими. Подходящие пластификаторы включают, например, полиэтиленгликоли, такие как PEG 300, PEG 400, PEG 600, PEG 1450, PEG 3350 и PEG 800, стеариновую кислоту, пропиленгликоль, олеиновую кислоту, триэтилцеллюлозу и триацетин. Пластификаторы также могут функционировать в качестве диспергирующих средств или смачивающих средств.
Солюбилизаторы включают такие соединения, как триацетин, триэтилцитрат, этилолеат, этилкаприлат, лаурилсульфат натрия, докузат натрия, витамин E-TPGS, диметилацетамид, N-метилпирролидон, N-гидроксиэтилпирролидон, поливинилпирролидон, гидроксипропилметилцеллюлозу, гидроксипропилциклодекстрины, этанол, н-бутанол, изопропиловый спирт, холестерин, соли желчных кислот, полиэтиленгликоль 200-600, гликофурол, транскутол, пропиленгликоль и диметилизосорбид и т.п.
Стабилизаторы включают такие соединения, как любые антиоксидантные средства, буферы, кислоты, консерванты и т.п. Иллюстративные стабилизаторы включают гидрохлорид L-аргинина, трометамин, альбумин (человеческий), лимонную кислоту, бензиловый спирт, фенол, дигидрат бифосфата динатрия, пропиленгликоль, метакрезол или м-крезол, ацетат цинка, полисорбат-20 или Tween® 20 или трометамол.
Суспендирующие средства включают такие соединения, как поливинилпирролидон, например, поливинилпирролидон K12, поливинилпирролидон K17, поливинилпирролидон K25 или поливинилпирролидон K30, coполимер винилпирролидона и винилацетата (S630), полиэтиленгликоль, например, полиэтиленгликоль, который может иметь молекулярную массу от приблизительно 300 до приблизительно 6000, или от приблизительно 3350 до приблизительно 4000, или от приблизительно 7000 до приблизительно 5400, натрий-карбоксиметилцеллюлоза, метилцеллюлоза, гидроксипропилметилцеллюлоза, ацетат-стеарат гидроксиметилцеллюлозы, полисорбат-80, гидроксиэтилцеллюлоза, альгинат натрия, камеди, такие как, например, трагакантовая камедь и аравийская камедь, гуаровая камедь, ксантаны, в том числе ксантановая камедь, сахара, целлюлозные соединения, такие как, например, натрий-карбоксиметилцеллюлоза, метилцеллюлоза, натрий-карбоксиметилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксиэтилцеллюлоза, полисорбат-80, альгинат натрия, полиэтоксилированный сорбитанмонолаурат, полиэтоксилированный сорбитанмонолаурат, повидон и т.п.
Поверхностно-активные вещества включают такие соединения, как лаурилсульфат натрия, докузат натрия, Tween 60 или 80, триацетин, витамин E-TPGS, сорбитанмоноолеат, полиоксиэтиленсорбитанмоноолеат, полисорбаты, полоксамеры, соли желчных кислот, глицерилмоностеарат, сополимеры этиленоксида и пропиленоксида, например, Pluronic® (BASF), и т.п. Дополнительные поверхностно-активные вещества включают полиоксиэтиленированные глицериды жирных кислот и растительные масла, например, полиоксиэтилен(60)-модифицированное гидрогенизированное касторовое масло, а также алкиловые эфиры и алкилфениловые эфиры полиоксиэтилена, например, октоксинол 10, октоксинол 40. Иногда поверхностно-активные вещества включают для повышения физической стабильности или для других целей.
Средства, повышающие вязкость, включают, например, метилцеллюлозу, ксантановую камедь, карбоксиметилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, ацетат-стеарат гидроксипропилметилцеллюлозы, фталат гидроксипропилметилцеллюлозы, карбомер, поливиниловый спирт, альгинаты, аравийскую камедь, хитозаны и их комбинации.
Смачивающие средства включают такие соединения, как олеиновая кислота, глицерилмоностеарат, сорбитанмоноолеат, сорбитанмонолаурат, олеат триэтаноламина, полиоксиэтиленсорбитанмоноолеат, полиоксиэтиленсорбитанмонолаурат, докузат натрия, олеат натрия, лаурилсульфат натрия, докузат натрия, триацетин, Tween 80, витамин E-TPGS, соли аммония и т.п.
В некоторых случаях фармацевтическую композицию, содержащую конъюгат IL-2 (такой как конъюгат IL-2 формул (I-XVII)) и ингибитор контрольных точек иммунного ответа, вводят в виде состава, содержащего оба лекарственных средства. В некоторых случаях весовое процентное соотношение конъюгата IL-2 и ингибитора контрольных точек иммунного ответа или наоборот составляет от 10:1 до 1:10. В некоторых случаях весовое процентное соотношение конъюгата IL-2 и ингибитора контрольных точек иммунного ответа или наоборот составляет от 7:1 до 1:2. В некоторых случаях весовое процентное соотношение конъюгата IL-2 и ингибитора контрольных точек иммунного ответа или наоборот составляет от 5:1 до 1:5. В некоторых случаях весовое процентное соотношение конъюгата IL-2 и ингибитора контрольных точек иммунного ответа или наоборот составляет от 3:1 до 1:3. В некоторых случаях весовое процентное соотношение конъюгата IL-2 и ингибитора контрольных точек иммунного ответа или наоборот составляет приблизительно 10:1, или приблизительно 9:1, приблизительно 8:1, приблизительно 7:1, приблизительно 6:1, приблизительно 5:1, приблизительно 4:1, приблизительно 3:1, приблизительно 2:1, или приблизительно 1:1. В некоторых случаях весовое процентное соотношение конъюгата IL-2 и ингибитора контрольных точек иммунного ответа или наоборот составляет от 10:1 до 1:1, от 7:1 до 2:1, от 5:1 до 1:1 или от 3:1 до 1:1.
В определенных вариантах осуществления комбинацию ингибитора контрольных точек иммунного ответа (такого как ингибитор PD-1) и конъюгата IL-2 (такого как конъюгаты формул (I-XVII)), описанного в данном документе, вводят в виде чистого химического соединения. В других вариантах осуществления комбинацию ингибитора контрольных точек иммунного ответа и конъюгата IL-2, описанного в данном документе, объединяют с фармацевтически подходящим или приемлемым носителем (также называемым в данном документе фармацевтически подходящим (или приемлемым) наполнителем, физиологически подходящим (или приемлемым) наполнителем или физиологически подходящим (или приемлемым) носителем), выбранным, исходя из выбранного пути введения и стандартной фармацевтической практики, как описано, например, в Remington: The Science and Practice of Pharmacy (Gennaro, 21st Ed. Mack Pub. Co., Easton, PA (2005), раскрытие которой включено в данный документ посредством ссылки). В некоторых вариантах осуществления каждый из ингибитора контрольных точек иммунного ответа и конъюгата IL-2, описанного в данном документе, вводят в виде отдельных композиций. В некоторых вариантах осуществления отдельные композиции на основе ингибитора контрольных точек иммунного ответа и/или конъюгата IL-2, описанного в данном документе, объединяют с подходящим или приемлемым наполнителем. В некоторых вариантах осуществления ингибитор контрольных точек иммунного ответа и конъюгат IL-2, описанный в данном документе, вводят в виде одной объединенной композиции.
В данном документе представлены фармацевтические композиции, содержащие конъюгат IL-2, описанный в данном документе, и ингибитор контрольных точек иммунного ответа вместе с одним или несколькими фармацевтически приемлемыми носителями. Носитель(носители) (или наполнитель(наполнители)) являются приемлемыми или подходящими, если носитель совместим с другими ингредиентами композиции и не вреден для лица, получающего композицию (т.e. субъекта или пациента). В определенных вариантах осуществления ингибитор контрольных точек иммунного ответа и конъюгат IL-2, описанный в данном документе, являются по сути чистыми в том смысле, что они содержат менее чем приблизительно 5%, или менее чем приблизительно 1%, или менее чем приблизительно 0,1% других органических малых молекул, таких как непрореагировавшие промежуточные соединения или побочные продукты синтеза, которые образуются, например, на одной или нескольких стадиях способа синтеза. В некоторых случаях фармацевтические композиции содержат ингибитор контрольных точек иммунного ответа и конъюгат IL-2, описанный в данном документе, и один или несколько фармацевтически приемлемых наполнителей. В некоторых случаях фармацевтические композиции, содержащие ингибитор контрольных точек иммунного ответа и конъюгат IL-2, описанный в данном документе, или их комбинацию, содержат (в качестве неограничивающего примера) такие наполнители, как 0,9% хлорид натрия для инъекций согласно USP, дегидратированный спирт, dl-альфа-токоферол, безводная лимонная кислота, полисорбат 80, полиэтиленгликоль 400, пропиленгликоль, бензиловый спирт, цитрат натрия, сульфит натрия, Cremophor EL, альбумин или любая их комбинация. В некоторых случаях фармацевтические композиции содержат наночастицы. В некоторых случаях фармацевтические композиции содержат другие наполнители, традиционно используемые в инъекционных композициях. В некоторых случаях фармацевтические композиции содержат контрастное средство, содействующее визуализации доставки фармацевтической композиции. В некоторых случаях фармацевтические композиции содержат жидкость, суспензию, раствор или гель. В некоторых случаях фармацевтические композиции, содержащие ингибитор контрольных точек иммунного ответа и конъюгат IL-2, описанный в данном документе, или их комбинацию, являются инъекционными. В некоторых случаях фармацевтические композиции содержат наполнители, которые солюбилизируют ингибитор контрольных точек иммунного ответа и конъюгат IL-2, описанный в данном документе, или их комбинацию. В другом варианте осуществления фармацевтические композиции, содержащие ингибитор контрольных точек иммунного ответа и конъюгат IL-2, описанный в данном документе, представлены в лекарственной форме для парентерального введения, которая содержит один или несколько фармацевтически приемлемых наполнителей или носителей. В некоторых случаях фармацевтические композиции, содержащие ингибитор контрольных точек иммунного ответа и конъюгат IL-2, описанный в данном документе, или их комбинацию, являются инъекционными. В случае составления фармацевтических композиций для внутривенной, кожной или подкожной инъекции активный ингредиент находится в форме парентерально приемлемого водного раствора, который является апирогенным и характеризуется подходящими pH, изотоничностью и стабильностью. Специалисты в данной области хорошо умеют получать подходящие растворы с использованием, например, изотонических сред-носителей, таких как хлорид натрия для инъекций, раствор Рингера для инъекций или раствор Рингера с лактатом для инъекций. В некоторых вариантах осуществления включены консерванты, стабилизаторы, наполнители, буферы, антиоксиданты и/или другие добавки.
Наборы/готовые изделия
В определенных вариантах осуществления в данном документе раскрыты наборы и готовые изделия для применения с одним или несколькими способами и композициями, описанными в данном документе. Такие наборы содержат носитель, упаковку или контейнер, который разделен на отсеки для размещения одного или нескольких контейнеров, таких как флаконы, пробирки и т.п., при этом каждый из контейнеров содержит один из отдельных элементов, которые должны применяться в способе, описанном в данном документе. Подходящие контейнеры включают, например, бутылки, флаконы, шприцы и тестовые пробирки. В одном варианте осуществления контейнеры изготовлены из ряда материалов, таких как стекло или пластик.
Набор обычно содержит этикетки с перечнем содержимого и/или инструкциями по применению, а также вкладыши в упаковке с инструкциями по применению. Также обычно включается набор инструкций.
В одном варианте осуществления этикетка находится на контейнере или связана с ним. В одном варианте осуществления этикетка находится на контейнере, когда буквы, числа или другие символы, образующие этикетку, прикреплены, отформованы или вытравлены на самом контейнере, при этом этикетка связана с контейнером, когда она находится внутри вместилища или держателя, в котором также удерживается контейнер, например, в виде вкладыша в упаковке. В одном варианте осуществления этикетка используется для обозначения того, что содержимое должно применяться для конкретного терапевтического применения. На этикетке также представлены указания по применению содержимого, как, например, в способах, описанных в данном документе.
В определенных вариантах осуществления фармацевтические композиции представлены в упаковке или дозирующем устройстве, которые содержат одну или несколько стандартных лекарственных форм, содержащих соединение, представленное в данном документе. Упаковка, например, содержит металлическую фольгу или пластиковую пленку, как, например, блистерная упаковка. В одном варианте осуществления к упаковке или дозирующему устройству прилагаются инструкции по введению. В одном варианте осуществления к упаковке или дозирующему устройству также прилагается уведомление, связанное с контейнером, в форме, предписанной государственным органом, регулирующим изготовление, применение или продажу фармацевтических препаратов, при этом данное уведомление отражает одобрение органом формы лекарственного средства для введения человеку или животным. Такое уведомление, например, представляет собой этикетку для лекарственных средств, одобренную Управлением США по контролю качества пищевых продуктов и лекарственных средств, или одобренный листок-вкладыш для продукта. В одном варианте осуществления композиции, содержащие соединение, представленное в данном документе, составленные в совместимом фармацевтическом носителе, также получают, помещают в соответствующий контейнер и маркируют для лечения указанного состояния.
Иллюстративные варианты осуществления
Далее настоящее изобретение описывается с помощью следующих вариантов осуществления. Признаки каждого из вариантов осуществления комбинируются с любым из других вариантов осуществления, где это уместно и осуществимо на практике.
Вариант осуществления 1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (I):

Формула (I);
где:
Z представляет собой CH2, и Y представляет собой  ;
;
Y представляет собой CH2, и Z представляет собой  ;
;
Z представляет собой CH2, и Y представляет собой  ; или
; или
Y представляет собой CH2, и Z представляет собой  ;
;
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
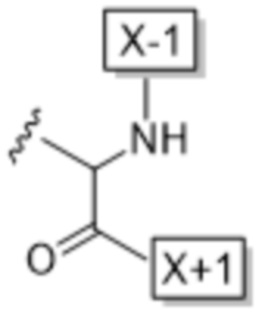 ;
;
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 1.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (I):

Формула (I);
где:
Z представляет собой CH2, и Y представляет собой  ;
;
Y представляет собой CH2, и Z представляет собой  ;
;
Z представляет собой CH2, и Y представляет собой  ; или
; или
Y представляет собой CH2, и Z представляет собой  ;
;
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 2. Способ согласно вариантам осуществления 1 или 1.1, где в конъюгате IL-2 Z представляет собой CH2, и Y представляет собой  .
.
Вариант осуществления 3. Способ согласно вариантам осуществления 1 или 1.1, где в конъюгате IL-2 Y представляет собой CH2, и Z представляет собой  .
.
Вариант осуществления 4. Способ согласно вариантам осуществления 1 или 1.1, где в конъюгате IL-2 Z представляет собой CH2, и Y представляет собой  .
.
Вариант осуществления 5. Способ согласно вариантам осуществления 1 или 1.1, где в конъюгате IL-2 Z представляет собой CH2, и Y представляет собой  .
.
Вариант осуществления 6. Способ согласно вариантам осуществления 1 или 1.1, где в конъюгате IL-2 Y представляет собой CH2, и Z представляет собой  .
.
Вариант осуществления 7. Способ согласно вариантам осуществления 1 или 1.1, где в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 20 кДа и 30 кДа.
Вариант осуществления 8. Способ согласно вариантам осуществления 1 или 1.1, где в конъюгате IL-2 или его фармацевтически приемлемых соли, сольвате или гидрате группа PEG имеет среднюю молекулярную массу 10 кДа, 20 кДа или 30 кДа.
Вариант осуществления 9. Способ согласно вариантам осуществления 1 или 1.1, где в конъюгате IL-2 группа PEG имеет среднюю молекулярную массу 30 кДа.
Вариант осуществления 10. Способ согласно вариантам осуществления 1 или 1.1, где в конъюгате IL-2 положение структуры формулы (I) в аминокислотной последовательности конъюгата IL-2 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71.
Вариант осуществления 11. Способ согласно вариантам осуществления 1 или 1.1, где в конъюгате IL-2 положение структуры формулы (I) в аминокислотной последовательности конъюгата IL-2 выбрано из F41, E61 и P64.
Вариант осуществления 12. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 15-19, где [AzK_PEG] имеет структуру формулы (II) или формулы (III) или представляет собой смесь формулы (II) и формулы (III):

Формула (II);
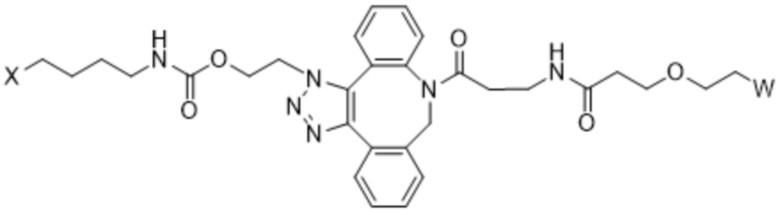
Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 12.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 15-19, где [AzK_PEG] имеет структуру формулы (II) или формулы (III) или представляет собой смесь формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 13. Способ согласно вариантам осуществления 12 или 12.1, где [AzK_PEG] представляет собой смесь формулы (II) и формулы (III).
Вариант осуществления 14. Способ согласно вариантам осуществления 12 или 12.1, где [AzK_PEG] имеет структуру формулы (II):

Формула (II);
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 15. Способ согласно варианту осуществления 14, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 15.
Вариант осуществления 16. Способ согласно варианту осуществления 15, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 17. Способ согласно варианту осуществления 16, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 18. Способ согласно варианту осуществления 17, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 19. Способ согласно варианту осуществления 17, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 20. Способ согласно вариантам осуществления 12 или 12.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 16.
Вариант осуществления 21. Способ согласно варианту осуществления 20, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 22. Способ согласно варианту осуществления 21, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 23. Способ согласно варианту осуществления 22, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 24. Способ согласно варианту осуществления 22, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 25. Способ согласно вариантам осуществления 12 или 12.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 17.
Вариант осуществления 26. Способ согласно варианту осуществления 25, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 27. Способ согласно варианту осуществления 26, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 28. Способ согласно варианту осуществления 27, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 29. Способ согласно варианту осуществления 27, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 30. Способ согласно вариантам осуществления 12 или 12.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 18.
Вариант осуществления 31. Способ согласно варианту осуществления 30, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 32. Способ согласно варианту осуществления 31, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 33. Способ согласно варианту осуществления 32, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 34. Способ согласно варианту осуществления 32, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 35. Способ согласно вариантам осуществления 12 или 12.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 19.
Вариант осуществления 36. Способ согласно варианту осуществления 35, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 37. Способ согласно варианту осуществления 36, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 38. Способ согласно варианту осуществления 37, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 39. Способ согласно варианту осуществления 37, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 40. Способ согласно вариантам осуществления 12 или 12.1, где [AzK_PEG] имеет структуру формулы (III):

Формула (III);
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 41. Способ согласно варианту осуществления 40, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 15.
Вариант осуществления 42. Способ согласно варианту осуществления 41, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 43. Способ согласно варианту осуществления 42, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 44. Способ согласно варианту осуществления 43, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 45. Способ согласно варианту осуществления 43, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 46. Способ согласно вариантам осуществления 12 или 12.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 16.
Вариант осуществления 47. Способ согласно варианту осуществления 46, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 48. Способ согласно варианту осуществления 47, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 49. Способ согласно варианту осуществления 48, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 50. Способ согласно варианту осуществления 48, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 51. Способ согласно вариантам осуществления 12 или 12.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 17.
Вариант осуществления 52. Способ согласно варианту осуществления 51, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 53. Способ согласно варианту осуществления 52, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 54. Способ согласно варианту осуществления 53, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 55. Способ согласно варианту осуществления 53, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 56. Способ согласно вариантам осуществления 12 или 12.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 18.
Вариант осуществления 57. Способ согласно варианту осуществления 56, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 58. Способ согласно варианту осуществления 57, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 59. Способ согласно варианту осуществления 58, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 60. Способ согласно варианту осуществления 58, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 61. Способ согласно вариантам осуществления 12 или 12.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 19.
Вариант осуществления 62. Способ согласно варианту осуществления 61, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 63. Способ согласно варианту осуществления 62, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 64. Способ согласно варианту осуществления 63, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 65. Способ согласно варианту осуществления 63, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 66. Способ согласно любому из вариантов осуществления 1-65, где W представляет собой линейную или разветвленную группу PEG.
Вариант осуществления 67. Способ согласно любому из вариантов осуществления 1-65, где W представляет собой линейную группу PEG.
Вариант осуществления 68. Способ согласно любому из вариантов осуществления 1-65, где W представляет собой разветвленную группу PEG.
Вариант осуществления 69. Способ согласно любому из вариантов осуществления 1-65, где W представляет собой группу метокси-PEG.
Вариант осуществления 70. Способ согласно варианту осуществления 69, где группа метокси-PEG является линейной или разветвленной.
Вариант осуществления 71. Способ согласно варианту осуществления 70, где группа метокси-PEG является линейной.
Вариант осуществления 72. Способ согласно варианту осуществления 70, где группа метокси-PEG является разветвленной.
Вариант осуществления 73. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 20-24, где [AzK_PEG5кДа] имеет структуру формулы (II) или формулы (III) или представляет собой смесь формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа; и
X имеет структуру
 ;
;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 73.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 20-24, где [AzK_PEG5кДа] имеет структуру формулы (II) или формулы (III) или представляет собой смесь формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 74. Способ согласно вариантам осуществления 73 или 73.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 20.
Вариант осуществления 75. Способ согласно вариантам осуществления 73 или 73.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 21.
Вариант осуществления 76. Способ согласно вариантам осуществления 73 или 73.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 22.
Вариант осуществления 77. Способ согласно вариантам осуществления 73 или 73.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 23.
Вариант осуществления 78. Способ согласно вариантам осуществления 73 или 73.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 24.
Вариант осуществления 79. Способ согласно вариантам осуществления 73 или 73.1, где [AzK_PEG5кДа] имеет структуру формулы (II):

Формула (II);
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 80. Способ согласно варианту осуществления 79, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 20.
Вариант осуществления 81. Способ согласно варианту осуществления 79, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 21.
Вариант осуществления 82. Способ согласно варианту осуществления 79, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 22.
Вариант осуществления 83. Способ согласно варианту осуществления 79, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 23.
Вариант осуществления 84. Способ согласно варианту осуществления 79, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 24.
Вариант осуществления 85. Способ согласно вариантам осуществления 73 или 73.1, где [AzK_PEG5кДа] имеет структуру формулы (III):

Формула (III);
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 86. Способ согласно варианту осуществления 85, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 20.
Вариант осуществления 87. Способ согласно варианту осуществления 85, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 21.
Вариант осуществления 88. Способ согласно варианту осуществления 85, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 22.
Вариант осуществления 89. Способ согласно варианту осуществления 85, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 23.
Вариант осуществления 90. Способ согласно варианту осуществления 85, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 24.
Вариант осуществления 91. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 25-29, где [AzK_PEG30кДа] имеет структуру формулы (II) или формулы (III) или представляет собой смесь структур формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа; и
X имеет структуру
 ;
;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 91.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 25-29, где [AzK_PEG30кДа] имеет структуру формулы (II) или формулы (III) или представляет собой смесь структур формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 92. Способ согласно вариантам осуществления 91 или 91.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 25.
Вариант осуществления 93. Способ согласно вариантам осуществления 91 или 91.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 26.
Вариант осуществления 94. Способ согласно вариантам осуществления 91 или 91.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 27.
Вариант осуществления 95. Способ согласно вариантам осуществления 91 или 91.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 28.
Вариант осуществления 96. Способ согласно вариантам осуществления 91 или 91.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 29.
Вариант осуществления 97. Способ согласно вариантам осуществления 91 или 91.1, где [AzK_PEG30кДа] имеет структуру формулы (II):

Формула (II);
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 98. Способ согласно варианту осуществления 97, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 25.
Вариант осуществления 99. Способ согласно варианту осуществления 97, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 26.
Вариант осуществления 100. Способ согласно варианту осуществления 97, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 27.
Вариант осуществления 101. Способ согласно варианту осуществления 97, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 28.
Вариант осуществления 102. Способ согласно варианту осуществления 97, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 29.
Вариант осуществления 103. Способ согласно вариантам осуществления 91 или 91.1, где [AzK_PEG30кДа] имеет структуру формулы (III):

Формула (III);
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 104. Способ согласно варианту осуществления 103, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 25.
Вариант осуществления 105. Способ согласно варианту осуществления 103, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 26.
Вариант осуществления 106. Способ согласно варианту осуществления 103, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 27.
Вариант осуществления 107. Способ согласно варианту осуществления 103, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 28.
Вариант осуществления 108. Способ согласно варианту осуществления 103, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 29.
Вариант осуществления 109. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 15-19, где [AzK_PEG] представляет собой смесь структур формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 109.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 15-19, где [AzK_PEG] представляет собой смесь структур формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 110. Способ согласно вариантам осуществления 109 или 109.1, где соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG] в конъюгате IL-2, составляет приблизительно 1:1.
Вариант осуществления 111. Способ согласно вариантам осуществления 109 или 109.1, где соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG] в конъюгате IL-2, составляет более 1:1.
Вариант осуществления 112. Способ согласно вариантам осуществления 109 или 109.1, где соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG] в конъюгате IL-2, составляет менее 1:1.
Вариант осуществления 113. Способ согласно любому из вариантов осуществления 109-112, где W представляет собой линейную или разветвленную группу PEG.
Вариант осуществления 114. Способ согласно любому из вариантов осуществления 109-112, где W представляет собой линейную группу PEG.
Вариант осуществления 115. Способ согласно любому из вариантов осуществления 109-112, где W представляет собой разветвленную группу PEG.
Вариант осуществления 116. Способ согласно любому из вариантов осуществления 109-112, где W представляет собой группу метокси-PEG.
Вариант осуществления 117. Способ согласно варианту осуществления 116, где группа метокси-PEG является линейной или разветвленной.
Вариант осуществления 118. Способ согласно варианту осуществления 117, где группа метокси-PEG является линейной.
Вариант осуществления 119. Способ согласно варианту осуществления 117, где группа метокси-PEG является разветвленной.
Вариант осуществления 120. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 20-24, где [AzK_PEG5кДа] представляет собой смесь структур формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа; и
X имеет структуру
 ;
;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 120.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 20-24, где [AzK_PEG5кДа] представляет собой смесь структур формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 121. Способ согласно вариантам осуществления 120 или 120.1, где соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG5кДа] в конъюгате IL-2, составляет приблизительно 1:1.
Вариант осуществления 122. Способ согласно вариантам осуществления 120 или 120.1, где соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG5кДа] в конъюгате IL-2, составляет более 1:1.
Вариант осуществления 123. Способ согласно вариантам осуществления 120 или 120.1, где соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG5кДа] в конъюгате IL-2, составляет менее 1:1.
Вариант осуществления 124. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 25-29, где [AzK_PEG30кДа] представляет собой смесь структур формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа; и
X имеет структуру
 ;
;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 124.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 25-29, где [AzK_PEG30кДа] представляет собой смесь структур формулы (II) и формулы (III):

Формула (II);

Формула (III);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 125. Способ согласно вариантам осуществления 124 или 124.1, где соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG30кДа] в конъюгате IL-2, составляет приблизительно 1:1.
Вариант осуществления 126. Способ согласно вариантам осуществления 124 или 124.1, где соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG30кДа] в конъюгате IL-2, составляет более 1:1.
Вариант осуществления 127. Способ согласно вариантам осуществления 124 или 124.1, где соотношение количества структуры формулы (II) и количества структуры формулы (III), составляющих общее количество [AzK_PEG30кДа] в конъюгате IL-2, составляет менее 1:1.
Вариант осуществления 128. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 40-44, где [AzK_L1_PEG] имеет структуру формулы (IV) или формулы (V) или представляет собой смесь формулы (IV) и формулы (V):

Формула (IV);
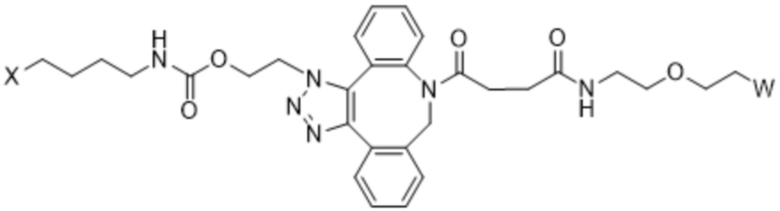
Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 128.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 40-44, где [AzK_L1_PEG] имеет структуру формулы (IV) или формулы (V) или представляет собой смесь формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 129. Способ согласно вариантам осуществления 128 или 128.1, где [AzK_L1_PEG] представляет собой смесь формулы (IV) и формулы (V).
Вариант осуществления 130. Способ согласно вариантам осуществления 128 или 128.1, где [AzK_L1_PEG] имеет структуру формулы (IV):

Формула (IV);
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 131. Способ согласно вариантам осуществления 128 или 128.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 40.
Вариант осуществления 132. Способ согласно варианту осуществления 131, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 133. Способ согласно варианту осуществления 132, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 134. Способ согласно варианту осуществления 133, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 135. Способ согласно варианту осуществления 133, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 136. Способ согласно вариантам осуществления 128 или 128.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 41.
Вариант осуществления 137. Способ согласно варианту осуществления 136, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 138. Способ согласно варианту осуществления 137, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 139. Способ согласно варианту осуществления 138, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 140. Способ согласно варианту осуществления 138, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 141. Способ согласно вариантам осуществления 128 или 128.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 42.
Вариант осуществления 142. Способ согласно варианту осуществления 141, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 143. Способ согласно варианту осуществления 142, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 144. Способ согласно варианту осуществления 143, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 145. Способ согласно варианту осуществления 143, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 146. Способ согласно вариантам осуществления 128 или 128.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 43.
Вариант осуществления 147. Способ согласно варианту осуществления 146, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 148. Способ согласно варианту осуществления 147, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 149. Способ согласно варианту осуществления 148, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 150. Способ согласно варианту осуществления 148, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 151. Способ согласно вариантам осуществления 128 или 128.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 44.
Вариант осуществления 152. Способ согласно варианту осуществления 151, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 153. Способ согласно варианту осуществления 152, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 154. Способ согласно варианту осуществления 153, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 155. Способ согласно варианту осуществления 153, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 156. Способ согласно вариантам осуществления 128 или 128.1, где [AzK_L1_PEG] имеет структуру формулы (V):
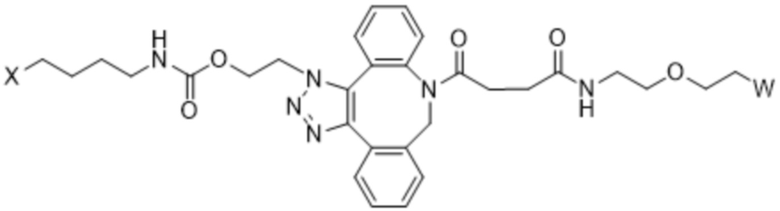
Формула (V);
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 157. Способ согласно варианту осуществления 156, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 40.
Вариант осуществления 158. Способ согласно варианту осуществления 156, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 159. Способ согласно варианту осуществления 158, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 160. Способ согласно варианту осуществления 159, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 161. Способ согласно варианту осуществления 159, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 162. Способ согласно варианту осуществления 156, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 41.
Вариант осуществления 163. Способ согласно варианту осуществления 162, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 164. Способ согласно варианту осуществления 163, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 165. Способ согласно варианту осуществления 164, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 166. Способ согласно варианту осуществления 164, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 167. Способ согласно варианту осуществления 156, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 42.
Вариант осуществления 168. Способ согласно варианту осуществления 167, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 169. Способ согласно варианту осуществления 168, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 170. Способ согласно варианту осуществления 169, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 171. Способ согласно варианту осуществления 169, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 172. Способ согласно варианту осуществления 156, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 43.
Вариант осуществления 173. Способ согласно варианту осуществления 172, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 174. Способ согласно варианту осуществления 173, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 175. Способ согласно варианту осуществления 174, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 176. Способ согласно варианту осуществления 174, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 177. Способ согласно варианту осуществления 156, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 44.
Вариант осуществления 178. Способ согласно варианту осуществления 177, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа и 30 кДа.
Вариант осуществления 179. Способ согласно варианту осуществления 178, где W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа и 30 кДа.
Вариант осуществления 180. Способ согласно варианту осуществления 179, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа.
Вариант осуществления 181. Способ согласно варианту осуществления 179, где W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа.
Вариант осуществления 182. Способ согласно любому из вариантов осуществления 128-181, где W представляет собой линейную или разветвленную группу PEG.
Вариант осуществления 183. Способ согласно любому из вариантов осуществления 128-181, где W представляет собой линейную группу PEG.
Вариант осуществления 184. Способ согласно любому из вариантов осуществления 128-181, где W представляет собой разветвленную группу PEG.
Вариант осуществления 185. Способ согласно любому из вариантов осуществления 128-181, где W представляет собой группу метокси-PEG.
Вариант осуществления 186. Способ согласно варианту осуществления 185, где группа метокси-PEG является линейной или разветвленной.
Вариант осуществления 187. Способ согласно варианту осуществления 186, где группа метокси-PEG является линейной.
Вариант осуществления 188. Способ согласно варианту осуществления 186, где группа метокси-PEG является разветвленной.
Вариант осуществления 189. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 45-49, где [AzK_L1_PEG5кДа] имеет структуру формулы (IV) или формулы (V) или представляет собой смесь формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа; и
X имеет структуру
 ;
;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 189.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 45-49, где [AzK_L1_PEG5кДа] имеет структуру формулы (IV) или формулы (V) или представляет собой смесь формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 190. Способ согласно вариантам осуществления 189 или 189.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 45.
Вариант осуществления 191. Способ согласно вариантам осуществления 189 или 189.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 46.
Вариант осуществления 192. Способ согласно вариантам осуществления 189 или 189.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 47.
Вариант осуществления 193. Способ согласно вариантам осуществления 189 или 189.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 48.
Вариант осуществления 194. Способ согласно вариантам осуществления 189 или 189.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 49.
Вариант осуществления 195. Способ согласно вариантам осуществления 189 или 189.1, где [AzK_L1_PEG5кДа] имеет структуру формулы (IV):

Формула (IV);
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 196. Способ согласно варианту осуществления 195, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 45.
Вариант осуществления 197. Способ согласно варианту осуществления 195, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 46.
Вариант осуществления 198. Способ согласно варианту осуществления 195, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 47.
Вариант осуществления 199. Способ согласно варианту осуществления 195, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 48.
Вариант осуществления 200. Способ согласно варианту осуществления 195, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 49.
Вариант осуществления 201. Способ согласно вариантам осуществления 189 или 189.1, где [AzK_L1_PEG5кДа] имеет структуру формулы (V):

Формула (V);
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 202. Способ согласно варианту осуществления 201, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 45.
Вариант осуществления 203. Способ согласно варианту осуществления 201, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 46.
Вариант осуществления 204. Способ согласно варианту осуществления 201, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 47.
Вариант осуществления 205. Способ согласно варианту осуществления 201, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 48.
Вариант осуществления 206. Способ согласно варианту осуществления 201, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 49.
Вариант осуществления 207. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 50-54, где [AzK_L1_PEG30кДа] имеет структуру формулы (IV) или формулы (V) или представляет собой смесь структур формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа; и
X имеет структуру
 ;
;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 207.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 50-54, где [AzK_L1_PEG30кДа] имеет структуру формулы (IV) или формулы (V) или представляет собой смесь структур формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа; и
X имеет структуру
 ;
;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 208. Способ согласно вариантам осуществления 207 или 207.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 50.
Вариант осуществления 209. Способ согласно вариантам осуществления 207 или 207.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 51.
Вариант осуществления 210. Способ согласно вариантам осуществления 207 или 207.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 52.
Вариант осуществления 211. Способ согласно вариантам осуществления 207 или 207.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 53.
Вариант осуществления 212. Способ согласно вариантам осуществления 207 или 207.1, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 54.
Вариант осуществления 213. Способ согласно вариантам осуществления 207 или 207.1, где [AzK_L1_PEG30кДа] имеет структуру формулы (IV):

Формула (IV);
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 214. Способ согласно варианту осуществления 213, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 50.
Вариант осуществления 215. Способ согласно варианту осуществления 213, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 51.
Вариант осуществления 216. Способ согласно варианту осуществления 213, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 52.
Вариант осуществления 217. Способ согласно варианту осуществления 213, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 53.
Вариант осуществления 218. Способ согласно варианту осуществления 213, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 54.
Вариант осуществления 219. Способ согласно вариантам осуществления 207 или 207.1, где [AzK_L1_PEG30кДа] имеет структуру формулы (V):

Формула (V);
или ее фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 220. Способ согласно варианту осуществления 219, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 50.
Вариант осуществления 221. Способ согласно варианту осуществления 219, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 51.
Вариант осуществления 222. Способ согласно варианту осуществления 219, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 52.
Вариант осуществления 223. Способ согласно варианту осуществления 219, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 53.
Вариант осуществления 224. Способ согласно варианту осуществления 219, где конъюгат IL-2 имеет аминокислотную последовательность под SEQ ID NO: 54.
Вариант осуществления 225. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 40-44, где [Azk_L1_PEG] представляет собой смесь структур формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 225.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 40-44, где [Azk_L1_PEG] представляет собой смесь структур формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 226. Способ согласно вариантам осуществления 225 или 225.1, где соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG] в конъюгате IL-2, составляет приблизительно 1:1.
Вариант осуществления 227. Способ согласно вариантам осуществления 225 или 225.1, где соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG] в конъюгате IL-2, составляет более 1:1.
Вариант осуществления 228. Способ согласно вариантам осуществления 225 или 225.1, где соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG] в конъюгате IL-2, составляет менее 1:1.
Вариант осуществления 229. Способ согласно любому из вариантов осуществления 225-228, где W представляет собой линейную или разветвленную группу PEG.
Вариант осуществления 230. Способ согласно любому из вариантов осуществления 225-228, где W представляет собой линейную группу PEG.
Вариант осуществления 231. Способ согласно любому из вариантов осуществления 225-228, где W представляет собой разветвленную группу PEG.
Вариант осуществления 232. Способ согласно любому из вариантов осуществления 225-228, где W представляет собой группу метокси-PEG.
Вариант осуществления 233. Способ согласно варианту осуществления 232, где группа метокси-PEG является линейной или разветвленной.
Вариант осуществления 234. Способ согласно варианту осуществления 233, где группа метокси-PEG является линейной.
Вариант осуществления 235. Способ согласно варианту осуществления 233, где группа метокси-PEG является разветвленной.
Вариант осуществления 236. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 45-49, где [AzK_L1_PEG5кДа] представляет собой смесь структур формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа; и
X имеет структуру
 ;
;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 236.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 45-49, где [AzK_L1_PEG5кДа] представляет собой смесь структур формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 5 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 237. Способ согласно вариантам осуществления 236 или 236.1, где соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_ PEG5кДа] в конъюгате IL-2, составляет приблизительно 1:1.
Вариант осуществления 238. Способ согласно вариантам осуществления 236 или 236.1, где соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_PEG5кДа] в конъюгате IL-2, составляет более 1:1.
Вариант осуществления 239. Способ согласно вариантам осуществления 236 или 236.1, где соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG5кДа] в конъюгате IL-2, составляет менее 1:1.
Вариант осуществления 240. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 50-54, где [AzK_L1_PEG30кДа] представляет собой смесь структур формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа; и
X имеет структуру
 ;
;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 240.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под любым из SEQ ID NO: 50-54, где [AzK_L1_PEG30кДа] представляет собой смесь структур формулы (IV) и формулы (V):

Формула (IV);

Формула (V);
где:
W представляет собой группу PEG, имеющую среднюю молекулярную массу 30 кДа; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 241. Способ согласно вариантам осуществления 240 или 240.1, где соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG30кДа] в конъюгате IL-2, составляет приблизительно 1:1.
Вариант осуществления 242. Способ согласно вариантам осуществления 240 или 240.1, где соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG30кДа] в конъюгате IL-2, составляет более 1:1.
Вариант осуществления 243. Способ согласно вариантам осуществления 240 или 240.1, где соотношение количества структуры формулы (IV) и количества структуры формулы (V), составляющих общее количество [AzK_L1_PEG30кДа] в конъюгате IL-2, составляет менее 1:1.
Вариант осуществления 244. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VI) или (VII) или смесью (VI) и (VII):

Формула (VI),

(VII),
где:
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
X имеет структуру  ,
,
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 244.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VI) или (VII) или смесью (VI) и (VII):

Формула (VI),

(VII),
где:
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 245. Способ согласно вариантам осуществления 244 или 244.1, где n в соединениях формулы (VI) и (VII) находится в диапазоне от приблизительно 5 до приблизительно 4600, или от приблизительно 10 до приблизительно 4000, или от приблизительно 20 до приблизительно 3000, или от приблизительно 100 до приблизительно 3000, или от приблизительно 100 до приблизительно 2900, или от приблизительно 150 до приблизительно 2900, или от приблизительно 125 до приблизительно 2900, или от приблизительно 100 до приблизительно 2500, или от приблизительно 100 до приблизительно 2000, или от приблизительно 100 до приблизительно 1900, или от приблизительно 100 до приблизительно 1850, или от приблизительно 100 до приблизительно 1750, или от приблизительно 100 до приблизительно 1650, или от приблизительно 100 до приблизительно 1500, или от приблизительно 100 до приблизительно 1400, или от приблизительно 100 до приблизительно 1300, или от приблизительно 100 до приблизительно 1250, или от приблизительно 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575.
Вариант осуществления 246. Способ согласно вариантам осуществления 244 или 244.1, где n в соединениях формулы (VI) и (VII) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
Вариант осуществления 247. Способ согласно любому из вариантов осуществления 244-246, где положение структуры формулы (VI), формулы (VII) или смеси формул (VI) и (VII) в аминокислотной последовательности конъюгата IL-2 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71.
Вариант осуществления 248. Способ согласно варианту осуществления 247, где положение структуры формулы (VI), формулы (VII) или смеси формул (VI) и (VII) в аминокислотной последовательности конъюгата IL-2 представляет собой K34.
Вариант осуществления 249. Способ согласно варианту осуществления 247, где положение структуры формулы (VI), формулы (VII) или смеси формул (VI) и (VII) в аминокислотной последовательности конъюгата IL-2 представляет собой F41.
Вариант осуществления 250. Способ согласно варианту осуществления 247, где положение структуры формулы (VI), формулы (VII) или смеси формул (VI) и (VII) в аминокислотной последовательности конъюгата IL-2 представляет собой F43.
Вариант осуществления 251. Способ согласно варианту осуществления 247, где положение структуры формулы (VI), формулы (VII) или смеси формул (VI) и (VII) в аминокислотной последовательности конъюгата IL-2 представляет собой K42.
Вариант осуществления 252. Способ согласно варианту осуществления 247, где положение структуры формулы (VI), формулы (VII) или смеси формул (VI) и (VII) в аминокислотной последовательности конъюгата IL-2 представляет собой E61.
Вариант осуществления 253. Способ согласно варианту осуществления 247, где положение структуры формулы (VI), формулы (VII) или смеси формул (VI) и (VII) в аминокислотной последовательности конъюгата IL-2 представляет собой P64.
Вариант осуществления 254. Способ согласно варианту осуществления 247, где положение структуры формулы (VI), формулы (VII) или смеси формул (VI) и (VII) в аминокислотной последовательности конъюгата IL-2 представляет собой R37.
Вариант осуществления 255. Способ согласно варианту осуществления 247, где положение структуры формулы (VI), формулы (VII) или смеси формул (VI) и (VII) в аминокислотной последовательности конъюгата IL-2 представляет собой T40.
Вариант осуществления 256. Способ согласно варианту осуществления 247, где положение структуры формулы (VI), формулы (VII) или смеси формул (VI) и (VII) в аминокислотной последовательности конъюгата IL-2 представляет собой E67.
Вариант осуществления 257. Способ согласно варианту осуществления 247, где положение структуры формулы (VI), формулы (VII) или смеси формул (VI) и (VII) в аминокислотной последовательности конъюгата IL-2 представляет собой Y44.
Вариант осуществления 258. Способ согласно варианту осуществления 247, где положение структуры формулы (VI), формулы (VII) или смеси формул (VI) и (VII) в аминокислотной последовательности конъюгата IL-2 представляет собой V68.
Вариант осуществления 259. Способ согласно варианту осуществления 247, где положение структуры формулы (VI), формулы (VII) или смеси формул (VI) и (VII) в аминокислотной последовательности конъюгата IL-2 представляет собой L71.
Вариант осуществления 260. Способ согласно любому из вариантов осуществления 244-259, где соотношение количества структуры формулы (VI) и количества структуры формулы (VII), составляющих общее количество конъюгата IL-2, составляет более 1:1.
Вариант осуществления 261. Способ согласно любому из вариантов осуществления 244-259, где соотношение количества структуры формулы (VI) и количества структуры формулы (VII), составляющих общее количество конъюгата IL-2, составляет менее 1:1.
Вариант осуществления 262. Способ согласно вариантам осуществления 244 или 244.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 263. Способ согласно вариантам осуществления 244 или 244.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и n представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137 и 1249.
Вариант осуществления 264. Способ согласно вариантам осуществления 244 или 244.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 265. Способ согласно варианту осуществления 264, где n в соединениях формулы (VI) и (VII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
Вариант осуществления 266. Способ согласно вариантам осуществления 244 или 244.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 267. Способ согласно варианту осуществления 266, где n в соединениях формулы (VI) и (VII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
Вариант осуществления 268. Способ согласно варианту осуществления 266, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 500 до приблизительно 1000.
Вариант осуществления 269. Способ согласно варианту осуществления 266, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 550 до приблизительно 800.
Вариант осуществления 270. Способ согласно варианту осуществления 267, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n равняется 681.
Вариант осуществления 271. Способ согласно вариантам осуществления 244 или 244.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 272. Способ согласно варианту осуществления 271, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n в соединениях формулы (VI) и (VII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
Вариант осуществления 273. Способ согласно варианту осуществления 271, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 500 до приблизительно 1000.
Вариант осуществления 274. Способ согласно варианту осуществления 273, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 550 до приблизительно 800.
Вариант осуществления 275. Способ согласно варианту осуществления 271, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n равняется 681.
Вариант осуществления 276. Способ согласно вариантам осуществления 244 или 244.1, где n представляет собой такое целое число, что молекулярная масса фрагмента PEG находится в диапазоне от приблизительно 1000 дальтонов до приблизительно 200000 дальтонов, или от приблизительно 2000 дальтонов до приблизительно 150000 дальтонов, или от приблизительно 3000 дальтонов до приблизительно 125000 дальтонов, или от приблизительно 4000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 90000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 80000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 65000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 60000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 30000 дальтонов.
Вариант осуществления 277. Способ согласно вариантам осуществления 244 или 244.1, где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов, приблизительно 50000 дальтонов, приблизительно 60000 дальтонов, приблизительно 70000 дальтонов, приблизительно 80000 дальтонов, приблизительно 90000 дальтонов, приблизительно 100000 дальтонов, приблизительно 125000 дальтонов, приблизительно 150000 дальтонов, приблизительно 175000 дальтонов или приблизительно 200000 дальтонов.
Вариант осуществления 278. Способ согласно вариантам осуществления 244 или 244.1, где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов или приблизительно 50000 дальтонов.
Вариант осуществления 279. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VIII) или (IX) или смесью (VIII) и (IX):

Формула (VIII),

(IX),
где:
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
X имеет структуру  ,
,
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 279.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (VIII) или (IX) или смесью (VIII) и (IX):

Формула (VIII),

(IX),
где:
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 280. Способ согласно вариантам осуществления 279 или 279.1, где n в соединениях формулы (VIII) и (IX) находится в диапазоне от приблизительно 5 до приблизительно 4600, или от приблизительно 10 до приблизительно 4000, или от приблизительно 20 до приблизительно 3000, или от приблизительно 100 до приблизительно 3000, или от приблизительно 100 до приблизительно 2900, или от приблизительно 150 до приблизительно 2900, или от приблизительно 125 до приблизительно 2900, или от приблизительно 100 до приблизительно 2500, или от приблизительно 100 до приблизительно 2000, или от приблизительно 100 до приблизительно 1900, или от приблизительно 100 до приблизительно 1850, или от приблизительно 100 до приблизительно 1750, или от приблизительно 100 до приблизительно 1650, или от приблизительно 100 до приблизительно 1500, или от приблизительно 100 до приблизительно 1400, или от приблизительно 100 до приблизительно 1300, или от приблизительно 100 до приблизительно 1250, или от приблизительно 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575.
Вариант осуществления 281. Способ согласно вариантам осуществления 279 или 279.1, где n в соединениях формулы (VIII) и (IX) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
Вариант осуществления 282. Способ согласно любому из вариантов осуществления 279-281, где положение структуры формулы (VIII), формулы (IX) или смеси формул (VIII) и (IX) в аминокислотной последовательности конъюгата IL-2 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71.
Вариант осуществления 283. Способ согласно варианту осуществления 282, где положение структуры формулы (VIII), формулы (IX) или смеси формул (VIII) и (IX) в аминокислотной последовательности конъюгата IL-2 представляет собой K34.
Вариант осуществления 284. Способ согласно варианту осуществления 282, где положение структуры формулы (VIII), формулы (IX) или смеси формул (VIII) и (IX) в аминокислотной последовательности конъюгата IL-2 представляет собой F41.
Вариант осуществления 285. Способ согласно варианту осуществления 282, где положение структуры формулы (VIII), формулы (IX) или смеси формул (VIII) и (IX) в аминокислотной последовательности конъюгата IL-2 представляет собой F43.
Вариант осуществления 286. Способ согласно варианту осуществления 282, где положение структуры формулы (VIII), формулы (IX) или смеси формул (VIII) и (IX) в аминокислотной последовательности конъюгата IL-2 представляет собой K42.
Вариант осуществления 287. Способ согласно варианту осуществления 282, где положение структуры формулы (VIII), формулы (IX) или смеси формул (VIII) и (IX) в аминокислотной последовательности конъюгата IL-2 представляет собой E61.
Вариант осуществления 288. Способ согласно варианту осуществления 282, где положение структуры формулы (VIII), формулы (IX) или смеси формул (VIII) и (IX) в аминокислотной последовательности конъюгата IL-2 представляет собой P64.
Вариант осуществления 289. Способ согласно варианту осуществления 282, где положение структуры формулы (VIII), формулы (IX) или смеси формул (VIII) и (IX) в аминокислотной последовательности конъюгата IL-2 представляет собой R37.
Вариант осуществления 290. Способ согласно варианту осуществления 282, где положение структуры формулы (VIII), формулы (IX) или смеси формул (VIII) и (IX) в аминокислотной последовательности конъюгата IL-2 представляет собой T40.
Вариант осуществления 291. Способ согласно варианту осуществления 282, где положение структуры формулы (VIII), формулы (IX) или смеси формул (VIII) и (IX) в аминокислотной последовательности конъюгата IL-2 представляет собой E67.
Вариант осуществления 292. Способ согласно варианту осуществления 282, где положение структуры формулы (VIII), формулы (IX) или смеси формул (VIII) и (IX) в аминокислотной последовательности конъюгата IL-2 представляет собой Y44.
Вариант осуществления 293. Способ согласно варианту осуществления 282, где положение структуры формулы (VIII), формулы (IX) или смеси формул (VIII) и (IX) в аминокислотной последовательности конъюгата IL-2 представляет собой V68.
Вариант осуществления 294. Способ согласно варианту осуществления 282, где положение структуры формулы (VIII), формулы (IX) или смеси формул (VIII) и (IX) в аминокислотной последовательности конъюгата IL-2 представляет собой L71.
Вариант осуществления 295. Способ согласно любому из вариантов осуществления 279-294, где соотношение количества структуры формулы (VIII) и количества структуры формулы (IX), составляющих общее количество конъюгата IL-2, составляет более 1:1.
Вариант осуществления 296. Способ согласно любому из вариантов осуществления 279-294, где соотношение количества структуры формулы (VIII) и количества структуры формулы (IX), составляющих общее количество конъюгата IL-2, составляет менее 1:1.
Вариант осуществления 297. Способ согласно вариантам осуществления 279 или 279.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 298. Способ согласно вариантам осуществления 279 или 279.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и n представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137 и 1249.
Вариант осуществления 299. Способ согласно вариантам осуществления 279 или 279.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 300. Способ согласно варианту осуществления 299, где n в соединениях формулы (VIII) и (IX) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
Вариант осуществления 301. Способ согласно вариантам осуществления 279 или 279.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 302. Способ согласно варианту осуществления 300, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n в соединениях формулы (VIII) и (IX) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
Вариант осуществления 303. Способ согласно вариантам осуществления 279 или 279.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 500 до приблизительно 1000.
Вариант осуществления 304. Способ согласно варианту осуществления 303, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 550 до приблизительно 800.
Вариант осуществления 305. Способ согласно варианту осуществления 302, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n равняется 681.
Вариант осуществления 306. Способ согласно вариантам осуществления 279 или 279.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 307. Способ согласно вариантам осуществления 279 или 279.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n в соединениях формулы (VIII) и (IX) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
Вариант осуществления 308. Способ согласно вариантам осуществления 279 или 279.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 500 до приблизительно 1000.
Вариант осуществления 309. Способ согласно вариантам осуществления 279 или 279.1, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 550 до приблизительно 800.
Вариант осуществления 310. Способ согласно варианту осуществления 307, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n равняется 681.
Вариант осуществления 311. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (X) или (XI) или смесью (X) и (XI):

Формула (X),

(XI),
где:
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
волнистыми линиями указаны ковалентные связи с аминокислотными остатками в SEQ ID NO: 3, которые не заменены.
Вариант осуществления 312. Способ согласно варианту осуществления 311, где n в соединениях формулы (X) и (XI) находится в диапазоне от приблизительно 5 до приблизительно 4600, или от приблизительно 10 до приблизительно 4000, или от приблизительно 20 до приблизительно 3000, или от приблизительно 100 до приблизительно 3000, или от приблизительно 100 до приблизительно 2900, или от приблизительно 150 до приблизительно 2900, или от приблизительно 125 до приблизительно 2900, или от приблизительно 100 до приблизительно 2500, или от приблизительно 100 до приблизительно 2000, или от приблизительно 100 до приблизительно 1900, или от приблизительно 100 до приблизительно 1850, или от приблизительно 100 до приблизительно 1750, или от приблизительно 100 до приблизительно 1650, или от приблизительно 100 до приблизительно 1500, или от приблизительно 100 до приблизительно 1400, или от приблизительно 100 до приблизительно 1300, или от приблизительно 100 до приблизительно 1250, или от приблизительно 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575.
Вариант осуществления 313. Способ согласно варианту осуществления 311, где n в соединениях формулы (X) и (XI) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
Вариант осуществления 314. Способ согласно любому из вариантов осуществления 311-313, где положение структуры формулы (X), формулы (XI) или смеси формул (X) и (XI) в аминокислотной последовательности конъюгата IL-2 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71.
Вариант осуществления 315. Способ согласно варианту осуществления 314, где положение структуры формулы (X), формулы (XI) или смеси формул (X) и (XI) в аминокислотной последовательности конъюгата IL-2 представляет собой K34.
Вариант осуществления 316. Способ согласно варианту осуществления 314, где положение структуры формулы (X), формулы (XI) или смеси формул (X) и (XI) в аминокислотной последовательности конъюгата IL-2 представляет собой F41.
Вариант осуществления 317. Способ согласно варианту осуществления 314, где положение структуры формулы (X), формулы (XI) или смеси формул (X) и (XI) в аминокислотной последовательности конъюгата IL-2 представляет собой F43.
Вариант осуществления 318. Способ согласно варианту осуществления 314, где положение структуры формулы (X), формулы (XI) или смеси формул (X) и (XI) в аминокислотной последовательности конъюгата IL-2 представляет собой K42.
Вариант осуществления 319. Способ согласно варианту осуществления 314, где положение структуры формулы (X), формулы (XI) или смеси формул (X) и (XI) в аминокислотной последовательности конъюгата IL-2 представляет собой E61.
Вариант осуществления 320. Способ согласно варианту осуществления 314, где положение структуры формулы (X), формулы (XI) или смеси формул (X) и (XI) в аминокислотной последовательности конъюгата IL-2 представляет собой P64.
Вариант осуществления 321. Способ согласно варианту осуществления 314, где положение структуры формулы (X), формулы (XI) или смеси формул (X) и (XI) в аминокислотной последовательности конъюгата IL-2 представляет собой R37.
Вариант осуществления 322. Способ согласно варианту осуществления 314, где положение структуры формулы (X), формулы (XI) или смеси формул (X) и (XI) в аминокислотной последовательности конъюгата IL-2 представляет собой T40.
Вариант осуществления 323. Способ согласно варианту осуществления 314, где положение структуры формулы (X), формулы (XI) или смеси формул (X) и (XI) в аминокислотной последовательности конъюгата IL-2 представляет собой E67.
Вариант осуществления 324. Способ согласно варианту осуществления 314, где положение структуры формулы (X), формулы (XI) или смеси формул (X) и (XI) в аминокислотной последовательности конъюгата IL-2 представляет собой Y44.
Вариант осуществления 325. Способ согласно варианту осуществления 314, где положение структуры формулы (X), формулы (XI) или смеси формул (X) и (XI) в аминокислотной последовательности конъюгата IL-2 представляет собой V68.
Вариант осуществления 326. Способ согласно варианту осуществления 314, где положение структуры формулы (X), формулы (XI) или смеси формул (X) и (XI) в аминокислотной последовательности конъюгата IL-2 представляет собой L71.
Вариант осуществления 327. Способ согласно любому из вариантов осуществления 311-326, где соотношение количества структуры формулы (X) и количества структуры формулы (XI), составляющих общее количество конъюгата IL-2, составляет более 1:1.
Вариант осуществления 328. Способ согласно любому из вариантов осуществления 311-326, где соотношение количества структуры формулы (X) и количества структуры формулы (XI), составляющих общее количество конъюгата IL-2, составляет менее 1:1.
Вариант осуществления 329. Способ согласно варианту осуществления 311, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 330. Способ согласно варианту осуществления 311, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и n представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137 и 1249.
Вариант осуществления 331. Способ согласно варианту осуществления 311, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 332. Способ согласно варианту осуществления 330, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и где n в соединениях формулы (X) и (XI) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
Вариант осуществления 333. Способ согласно варианту осуществления 311, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 334. Способ согласно варианту осуществления 311, где n в соединениях формулы (X) и (XI) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
Вариант осуществления 335. Способ согласно варианту осуществления 311, где n составляет от приблизительно 500 до приблизительно 1000.
Вариант осуществления 336. Способ согласно варианту осуществления 335, где n составляет от приблизительно 550 до приблизительно 800.
Вариант осуществления 337. Способ согласно варианту осуществления 332, где n равняется 681.
Вариант осуществления 338. Способ согласно варианту осуществления 311, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 339. Способ согласно варианту осуществления 311, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n в соединениях формулы (X) и (XI) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
Вариант осуществления 340. Способ согласно варианту осуществления 311, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 500 до приблизительно 1000.
Вариант осуществления 341. Способ согласно варианту осуществления 340, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 550 до приблизительно 800.
Вариант осуществления 342. Способ согласно варианту осуществления 339, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n равняется 681.
Вариант осуществления 343. Способ согласно варианту осуществления 311, где n представляет собой такое целое число, что молекулярная масса фрагмента PEG находится в диапазоне от приблизительно 1000 дальтонов до приблизительно 200000 дальтонов, или от приблизительно 2000 дальтонов до приблизительно 150000 дальтонов, или от приблизительно 3000 дальтонов до приблизительно 125000 дальтонов, или от приблизительно 4000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 90000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 80000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 65000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 60000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 30000 дальтонов.
Вариант осуществления 344. Способ согласно варианту осуществления 311, где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов, приблизительно 50000 дальтонов, приблизительно 60000 дальтонов, приблизительно 70000 дальтонов, приблизительно 80000 дальтонов, приблизительно 90000 дальтонов, приблизительно 100000 дальтонов, приблизительно 125000 дальтонов, приблизительно 150000 дальтонов, приблизительно 175000 дальтонов или приблизительно 200000 дальтонов.
Вариант осуществления 345. Способ согласно варианту осуществления 311, где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов или приблизительно 50000 дальтонов.
Вариант осуществления 346. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен структурой формулы (XII) или (XIII) или смесью (XII) и (XIII):

Формула (XII),

(XIII),
где:
n представляет собой целое число в диапазоне от приблизительно 2 до приблизительно 5000; и
волнистыми линиями указаны ковалентные связи с аминокислотными остатками в SEQ ID NO: 3, которые не заменены.
Вариант осуществления 347. Способ согласно варианту осуществления 346, где n в соединениях формулы (XII) и (XIII) находится в диапазоне от приблизительно 5 до приблизительно 4600, или от приблизительно 10 до приблизительно 4000, или от приблизительно 20 до приблизительно 3000, или от приблизительно 100 до приблизительно 3000, или от приблизительно 100 до приблизительно 2900, или от приблизительно 150 до приблизительно 2900, или от приблизительно 125 до приблизительно 2900, или от приблизительно 100 до приблизительно 2500, или от приблизительно 100 до приблизительно 2000, или от приблизительно 100 до приблизительно 1900, или от приблизительно 100 до приблизительно 1850, или от приблизительно 100 до приблизительно 1750, или от приблизительно 100 до приблизительно 1650, или от приблизительно 100 до приблизительно 1500, или от приблизительно 100 до приблизительно 1400, или от приблизительно 100 до приблизительно 1300, или от приблизительно 100 до приблизительно 1250, или от приблизительно 100 до приблизительно 1150, или от приблизительно 100 до приблизительно 1100, или от приблизительно 100 до приблизительно 1000, или от приблизительно 100 до приблизительно 900, или от приблизительно 100 до приблизительно 750, или от приблизительно 100 до приблизительно 700, или от приблизительно 100 до приблизительно 600, или от приблизительно 100 до приблизительно 575, или от приблизительно 100 до приблизительно 500, или от приблизительно 100 до приблизительно 450, или от приблизительно 100 до приблизительно 350, или от приблизительно 100 до приблизительно 275, или от приблизительно 100 до приблизительно 230, или от приблизительно 150 до приблизительно 475, или от приблизительно 150 до приблизительно 340, или от приблизительно 113 до приблизительно 340, или от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 340 до приблизительно 795, или от приблизительно 341 до приблизительно 682, или от приблизительно 568 до приблизительно 909, или от приблизительно 227 до приблизительно 1500, или от приблизительно 225 до приблизительно 2280, или от приблизительно 460 до приблизительно 2160, или от приблизительно 460 до приблизительно 2050, или от приблизительно 341 до приблизительно 1820, или от приблизительно 341 до приблизительно 1710, или от приблизительно 341 до приблизительно 1250, или от приблизительно 225 до приблизительно 1250, или от приблизительно 341 до приблизительно 1250, или от приблизительно 341 до приблизительно 1136, или от приблизительно 341 до приблизительно 1023, или от приблизительно 341 до приблизительно 910, или от приблизительно 341 до приблизительно 796, или от приблизительно 341 до приблизительно 682, или от приблизительно 341 до приблизительно 568, или от приблизительно 114 до приблизительно 1000, или от приблизительно 114 до приблизительно 950, или от приблизительно 114 до приблизительно 910, или от приблизительно 114 до приблизительно 800, или от приблизительно 114 до приблизительно 690, или от приблизительно 114 до приблизительно 575.
Вариант осуществления 348. Способ согласно варианту осуществления 346, где n в соединениях формулы (XII) и (XIII) представляет собой целое число, выбранное из 2, 5, 10, 11, 22, 23, 113, 114, 227, 228, 340, 341, 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137, 1249, 1250, 1251, 1362, 1363, 1364, 1476, 1477, 1478, 1589, 1590, 1591, 1703, 1704, 1705, 1817, 1818, 1819, 1930, 1931, 1932, 2044, 2045, 2046, 2158, 2159, 2160, 2271, 2272, 2273, 2839, 2840, 2841, 2953, 2954, 2955, 3408, 3409, 3410, 3976, 3977, 3978, 4544, 4545 и 4546.
Вариант осуществления 349. Способ согласно любому из вариантов осуществления 346-348, где положение структуры формулы (XII), формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 выбрано из K34, F41, F43, K42, E61, P64, R37, T40, E67, Y44, V68 и L71.
Вариант осуществления 350. Способ согласно варианту осуществления 349, где положение структуры формулы (XII), формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 представляет собой K34.
Вариант осуществления 351. Способ согласно варианту осуществления 349, где положение структуры формулы (XII), формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 представляет собой F41.
Вариант осуществления 352. Способ согласно варианту осуществления 349, где положение структуры формулы (XII), формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 представляет собой F43.
Вариант осуществления 353. Способ согласно варианту осуществления 349, где положение структуры формулы (XII), формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 представляет собой K42.
Вариант осуществления 354. Способ согласно варианту осуществления 349, где положение структуры формулы (XII), формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 представляет собой E61.
Вариант осуществления 355. Способ согласно варианту осуществления 349, где положение структуры формулы (XII), формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 представляет собой P64.
Вариант осуществления 356. Способ согласно варианту осуществления 349, где положение структуры формулы (XII), формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 представляет собой R37.
Вариант осуществления 357. Способ согласно варианту осуществления 349, где положение структуры формулы (XII), формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 представляет собой T40.
Вариант осуществления 358. Способ согласно варианту осуществления 349, где положение структуры формулы (XII), формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 представляет собой E67.
Вариант осуществления 359. Способ согласно варианту осуществления 349, где положение структуры формулы (XII), формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 представляет собой Y44.
Вариант осуществления 360. Способ согласно варианту осуществления 349, где положение структуры формулы (XII), формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 представляет собой V68.
Вариант осуществления 361. Способ согласно варианту осуществления 349, где положение структуры формулы (XII), формулы (XIII) или смеси формул (XII) и (XIII) в аминокислотной последовательности конъюгата IL-2 представляет собой L71.
Вариант осуществления 362. Способ согласно любому из вариантов осуществления 346-361, где соотношение количества структуры формулы (XII) и количества структуры формулы (XIII), составляющих общее количество конъюгата IL-2, составляет более 1:1.
Вариант осуществления 363. Способ согласно любому из вариантов осуществления 346-361, где соотношение количества структуры формулы (XII) и количества структуры формулы (XIII), составляющих общее количество конъюгата IL-2, составляет менее 1:1.
Вариант осуществления 364. Способ согласно варианту осуществления 346, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 365. Способ согласно варианту осуществления 346, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и n представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909, 910, 1021, 1022, 1023, 1135, 1136, 1137 и 1249.
Вариант осуществления 366. Способ согласно варианту осуществления 346, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из E61 и P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 367. Способ согласно варианту осуществления 365, где аминокислотный остаток в SEQ ID NO: 3, который заменен, выбран из F41, F43, K42, E61 и P64, и где n в соединениях формулы (XII) и (XIII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
Вариант осуществления 368. Способ согласно варианту осуществления 346, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой E61, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 369. Способ согласно варианту осуществления 346, где n в соединениях формулы (XII) и (XIII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
Вариант осуществления 370. Способ согласно варианту осуществления 346, где n составляет от приблизительно 500 до приблизительно 1000.
Вариант осуществления 371. Способ согласно варианту осуществления 370, где n составляет от приблизительно 550 до приблизительно 800.
Вариант осуществления 372. Способ согласно варианту осуществления 369, где n равняется 681.
Вариант осуществления 373. Способ согласно варианту осуществления 346, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 450 до приблизительно 800, или от приблизительно 454 до приблизительно 796, или от приблизительно 454 до приблизительно 682, или от приблизительно 568 до приблизительно 909.
Вариант осуществления 374. Способ согласно варианту осуществления 346, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n в соединениях формулы (XII) и (XIII) представляет собой целое число, выбранное из 454, 455, 568, 569, 680, 681, 682, 794, 795, 796, 908, 909 и 910.
Вариант осуществления 375. Способ согласно варианту осуществления 346, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 500 до приблизительно 1000.
Вариант осуществления 376. Способ согласно варианту осуществления 375, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n представляет собой целое число от приблизительно 550 до приблизительно 800.
Вариант осуществления 377. Способ согласно варианту осуществления 374, где аминокислотный остаток в SEQ ID NO: 3, который заменен, представляет собой P64, и где n равняется 681.
Вариант осуществления 378. Способ согласно варианту осуществления 346, где n представляет собой такое целое число, что молекулярная масса фрагмента PEG находится в диапазоне от приблизительно 1000 дальтонов до приблизительно 200000 дальтонов, или от приблизительно 2000 дальтонов до приблизительно 150000 дальтонов, или от приблизительно 3000 дальтонов до приблизительно 125000 дальтонов, или от приблизительно 4000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 100000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 90000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 80000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 70000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 65000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 60000 дальтонов, или от приблизительно 5000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 6000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 7000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 8500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 9500 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 10000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 15000 дальтонов до приблизительно 30000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 50000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 45000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 35000 дальтонов, или от приблизительно 20000 дальтонов до приблизительно 30000 дальтонов.
Вариант осуществления 379. Способ согласно варианту осуществления 346, где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов, приблизительно 50000 дальтонов, приблизительно 60000 дальтонов, приблизительно 70000 дальтонов, приблизительно 80000 дальтонов, приблизительно 90000 дальтонов, приблизительно 100000 дальтонов, приблизительно 125000 дальтонов, приблизительно 150000 дальтонов, приблизительно 175000 дальтонов или приблизительно 200000 дальтонов.
Вариант осуществления 380. Способ согласно варианту осуществления 346, где n представляет собой такое целое число, что молекулярная масса фрагмента PEG составляет приблизительно 5000 дальтонов, приблизительно 7500 дальтонов, приблизительно 10000 дальтонов, приблизительно 15000 дальтонов, приблизительно 20000 дальтонов, приблизительно 25000 дальтонов, приблизительно 30000 дальтонов, приблизительно 35000 дальтонов, приблизительно 40000 дальтонов, приблизительно 45000 дальтонов или приблизительно 50000 дальтонов.
Вариант осуществления 381. Способ согласно любому из вариантов осуществления 1-380, где одно или несколько дополнительных средств представляют собой один или несколько ингибиторов контрольных точек иммунного ответа, выбранных из группы, состоящей из ингибиторов PD-1, ингибиторов PD-L1, ингибиторов PD-L2, ингибиторов CTLA-4, агонистов OX40 и агонистов 4-1BB.
Вариант осуществления 382. Способ согласно варианту осуществления 381, где один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов PD-1.
Вариант осуществления 383. Способ согласно варианту осуществления 382, где один или несколько ингибиторов PD-1 выбраны из пембролизумаба, ниволумаба, цемиплимаба, ламбролизумаба, AMP-224, синтилимаба, торипалимаба, камрелизумаба, тислелизумаба, достарлимаба (GSK), PDR001 (Novartis), MGA012 (Macrogenics/Incyte), GLS-010 (Arcus/WuXi), AGEN2024 (Agenus), цетрелимаба (Janssen), ABBV-181 (Abbvie), AMG-404 (Amgen), BI-754091 (Boehringer Ingelheim), CC-90006 (Celgene), JTX-4014 (Jounce), PF-06801591 (Pfizer) и генолимзумаба (Apollomics/Genor BioPharma).
Вариант осуществления 384. Способ согласно варианту осуществления 383, где один или несколько ингибиторов PD-1 представляют собой пембролизумаб.
Вариант осуществления 385. Способ согласно варианту осуществления 383, где один или несколько ингибиторов PD-1 представляют собой ниволумаб.
Вариант осуществления 386. Способ согласно варианту осуществления 383, где один или несколько ингибиторов PD-1 представляют собой цемиплимаб.
Вариант осуществления 387. Способ согласно варианту осуществления 383, где один или несколько ингибиторов PD-1 представляют собой ламбролизумаб.
Вариант осуществления 388. Способ согласно варианту осуществления 383, где один или несколько ингибиторов PD-1 представляют собой AMP-224.
Вариант осуществления 389. Способ согласно варианту осуществления 383, где один или несколько ингибиторов PD-1 представляют собой синтилимаб.
Вариант осуществления 390. Способ согласно варианту осуществления 383, где один или несколько ингибиторов PD-1 представляют собой торипалимаб.
Вариант осуществления 391. Способ согласно варианту осуществления 383, где один или несколько ингибиторов PD-1 представляют собой камрелизумаб.
Вариант осуществления 392. Способ согласно варианту осуществления 383, где один или несколько ингибиторов PD-1 представляют собой тислелизумаб.
Вариант осуществления 393. Способ согласно варианту осуществления 381, где один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов PD-L1.
Вариант осуществления 394. Способ согласно варианту осуществления 393, где один или несколько ингибиторов PD-L1 выбраны из атезолизумаба, авелумаба, дурвалумаба, ASC22 (Alphamab/Ascletis), CX-072 (CytomX), CS1001 (CStone), косибелимаба (Checkpoint Therapeutics), INCB86550 (Incyte) и TG-1501 (TG Therapeutics).
Вариант осуществления 395. Способ согласно варианту осуществления 394, где один или несколько ингибиторов PD-L1 представляют собой атезолизумаб.
Вариант осуществления 396. Способ согласно варианту осуществления 394, где один или несколько ингибиторов PD-L1 представляют собой авелумаб.
Вариант осуществления 397. Способ согласно варианту осуществления 394, где один или несколько ингибиторов PD-L1 представляют собой дурвалумаб.
Вариант осуществления 398. Способ согласно варианту осуществления 381, где один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов CTLA-4.
Вариант осуществления 399. Способ согласно варианту осуществления 398, где один или несколько ингибиторов CTLA-4 выбраны из тремелимумаба, ипилимумаба и AGEN-1884 (Agenus).
Вариант осуществления 400. Способ согласно варианту осуществления 399, где один или несколько ингибиторов CTLA-4 представляют собой тремелимумаб.
Вариант осуществления 401. Способ согласно варианту осуществления 399, где один или несколько ингибиторов CTLA-4 представляют собой ипилимумаб.
Вариант осуществления 402. Способ согласно любому из вариантов осуществления 1-401, где рак у субъекта выбран из почечноклеточной карциномы (RCC), немелкоклеточного рака легкого (NSCLC), плоскоклеточного рака головы и шеи (HNSCC), классической лимфомы Ходжкина (cHL), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), уротелиальной карциномы, рака с микросателлитной нестабильностью, рака с микросателлитной стабильностью, рака желудка, рака шейки матки, гепатоцеллюлярной карциномы (HCC), карциномы из клеток Меркеля (MCC), меланомы, мелкоклеточного рака легкого (SCLC), рака пищевода, глиобластомы, мезотелиомы, рака молочной железы, трижды негативного рака молочной железы, рака предстательной железы, кастрационно-резистентного рака предстательной железы, метастатического кастрационно-резистентного рака предстательной железы или метастатического кастрационно-резистентного рака предстательной железы с дефектами ответа на повреждение ДНК (DDR), рака мочевого пузыря, рака яичника, опухолей с мутационной нагрузкой от умеренной до низкой, плоскоклеточной карциномы кожи (CSCC), плоскоклеточного рака кожи (SCSC), опухолей с экспрессией PD-L1 от низкой до отсутствующей, опухолей, распространяющихся системно в печень и CNS за пределы их первичного анатомического участка происхождения, и диффузной крупноклеточной В-клеточной лимфомы.
Вариант осуществления 403. Способ согласно варианту осуществления 402, где рак у субъекта выбран из почечноклеточной карциномы (RCC), немелкоклеточного рака легкого (NSCLC), уротелиальной карциномы и меланомы.
Вариант осуществления 404. Способ согласно любому из вариантов осуществления 1-403, где конъюгат IL-2 вводят нуждающемуся в этом субъекту один раз в неделю, один раз в две недели, один раз в три недели, один раз в 4 недели, один раз в 5 недель, один раз в 6 недель, один раз в 7 недель или один раз в 8 недель.
Вариант осуществления 405. Способ согласно варианту осуществления 404, где конъюгат IL-2 вводят нуждающемуся в этом субъекту один раз в неделю, один раз в две недели или один раз в три недели.
Вариант осуществления 406. Способ согласно варианту осуществления 405, где конъюгат IL-2 вводят нуждающемуся в этом субъекту один раз в две недели.
Вариант осуществления 407. Способ согласно варианту осуществления 405, где конъюгат IL-2 вводят нуждающемуся в этом субъекту один раз в три недели.
Вариант осуществления 408. Способ согласно любому из вариантов осуществления 1-407, где введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости сосудов у субъекта.
Вариант осуществления 409. Способ согласно варианту осуществления 408, где введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости сосудов 2 степени, 3 степени или 4 степени у субъекта.
Вариант осуществления 410. Способ согласно варианту осуществления 409, где введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости сосудов 2 степени у субъекта.
Вариант осуществления 411. Способ согласно варианту осуществления 409, где введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости сосудов 3 степени у субъекта.
Вариант осуществления 412. Способ согласно варианту осуществления 409, где введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости сосудов 4 степени у субъекта.
Вариант осуществления 413. Способ согласно любому из вариантов осуществления 1-412, где введение эффективного количества конъюгата IL-2 субъекту не вызывает потерю сосудистого тонуса у субъекта.
Вариант осуществления 414. Способ согласно любому из вариантов осуществления 1-413, где введение эффективного количества конъюгата IL-2 субъекту не вызывает транссудацию белков и жидкости плазмы крови во внесосудистое пространство у субъекта.
Вариант осуществления 415. Способ согласно любому из вариантов осуществления 1-414, где введение эффективного количества конъюгата IL-2 субъекту не вызывает гипотензию и снижение перфузии органов у субъекта.
Вариант осуществления 416. Способ согласно любому из вариантов осуществления 1-415, где введение эффективного количества конъюгата IL-2 субъекту не вызывает нарушение функции нейтрофилов у субъекта.
Вариант осуществления 417. Способ согласно любому из вариантов осуществления 1-415, где введение эффективного количества конъюгата IL-2 субъекту не вызывает снижение хемотаксиса у субъекта.
Вариант осуществления 418. Способ согласно любому из вариантов осуществления 1-417, где введение эффективного количества конъюгата IL-2 субъекту не ассоциировано с увеличенным риском диссеминированной инфекции у субъекта.
Вариант осуществления 419. Способ согласно варианту осуществления 418, где диссеминированная инфекция представляет собой сепсис или бактериальный эндокардит.
Вариант осуществления 420. Способ согласно варианту осуществления 419, где диссеминированная инфекция представляет собой сепсис.
Вариант осуществления 421. Способ согласно варианту осуществления 419, где диссеминированная инфекция представляет собой бактериальный эндокардит.
Вариант осуществления 422. Способ лечения рака у субъекта согласно любому из вариантов осуществления 1-421, где субъект получает лечение любых предсуществующих бактериальных инфекций до введения конъюгата IL-2.
Вариант осуществления 423. Способ согласно варианту осуществления 422, где субъект получает лечение с помощью антибактериального средства, выбранного из оксациллина, нафциллина, ципрофлоксацина и ванкомицина, до введения конъюгата IL-2.
Вариант осуществления 424. Способ согласно любому из вариантов осуществления 1-423, где введение эффективного количества конъюгата IL-2 субъекту не приводит к усугублению предсуществующего или первоначально проявляющегося аутоиммунного заболевания или воспалительного нарушения у субъекта.
Вариант осуществления 425. Способ согласно варианту осуществления 424, где введение эффективного количества конъюгата IL-2 субъекту не приводит к усугублению предсуществующего или первоначально проявляющегося аутоиммунного заболевания у субъекта.
Вариант осуществления 426. Способ согласно варианту осуществления 424, где введение эффективного количества конъюгата IL-2 субъекту не приводит к усугублению предсуществующего или первоначально проявляющегося воспалительного нарушения у субъекта.
Вариант осуществления 427. Способ согласно варианту осуществления 424, где аутоиммунное заболевание или воспалительное нарушение у субъекта выбрано из болезни Крона, склеродермии, тиреоидита, воспалительного артрита, сахарного диабета, окулобульбарной тяжелой миастении, серповидного IgA-гломерулонефрита, холецистита, церебрального васкулита, синдрома Стивенса-Джонсона и буллезного пемфигоида.
Вариант осуществления 428. Способ согласно варианту осуществления 427, где аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой болезнь Крона.
Вариант осуществления 429. Способ согласно варианту осуществления 427, где аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой склеродермию.
Вариант осуществления 430. Способ согласно варианту осуществления 427, где аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой тиреоидит.
Вариант осуществления 431. Способ согласно варианту осуществления 427, где аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой воспалительный артрит.
Вариант осуществления 432. Способ согласно варианту осуществления 427, где аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой сахарный диабет.
Вариант осуществления 433. Способ согласно варианту осуществления 427, где аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой окулобульбарную тяжелую миастению.
Вариант осуществления 434. Способ согласно варианту осуществления 427, где аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой серповидный IgA-гломерулонефрит.
Вариант осуществления 435. Способ согласно варианту осуществления 427, где аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой холецистит.
Вариант осуществления 436. Способ согласно варианту осуществления 427, где аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой церебральный васкулит.
Вариант осуществления 437. Способ согласно варианту осуществления 427, где аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой синдром Стивенса-Джонсона.
Вариант осуществления 438. Способ согласно варианту осуществления 427, где аутоиммунное заболевание или воспалительное нарушение у субъекта представляет собой буллезный пемфигоид.
Вариант осуществления 439. Способ согласно любому из вариантов осуществления 1-438, где введение эффективного количества конъюгата IL-2 субъекту не вызывает изменения психического состояния, затруднения речи, корковую слепоту, атаксию конечностей или походки, галлюцинации, возбуждение, притупление чувствительности или кому у субъекта.
Вариант осуществления 440. Способ согласно любому из вариантов осуществления 1-439, где введение эффективного количества конъюгата IL-2 субъекту не вызывает судороги у субъекта.
Вариант осуществления 441. Способ согласно любому из вариантов осуществления 1-440, где введение эффективного количества конъюгата IL-2 субъекту не противопоказано субъектам, у которых имеется подтвержденное судорожное расстройство.
Вариант осуществления 442. Способ согласно любому из вариантов осуществления 1-441, где введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости капилляров у субъекта.
Вариант осуществления 443. Способ согласно варианту осуществления 442, где введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости капилляров 2 степени, 3 степени или 4 степени у субъекта.
Вариант осуществления 444. Способ согласно варианту осуществления 443, где введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости капилляров 2 степени у субъекта.
Вариант осуществления 445. Способ согласно варианту осуществления 443, где введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости капилляров 3 степени у субъекта.
Вариант осуществления 446. Способ согласно варианту осуществления 443, где введение эффективного количества конъюгата IL-2 субъекту не вызывает синдром повышенной проницаемости капилляров 4 степени у субъекта.
Вариант осуществления 447. Способ согласно любому из вариантов осуществления 1-446, где введение эффективного количества конъюгата IL-2 субъекту не вызывает снижение среднего артериального кровяного давления у субъекта после введения конъюгата IL-2 субъекту.
Вариант осуществления 448. Способ согласно любому из вариантов осуществления 1-447, где введение эффективного количества конъюгата IL-2 субъекту не вызывает гипотензию у субъекта после введения конъюгата IL-2 субъекту.
Вариант осуществления 449. Способ согласно варианту осуществления 448, где введение эффективного количества конъюгата IL-2 субъекту не приводит к тому, что субъект испытывает систолическое кровяное давление ниже 90 мм рт. ст. или снижение систолического давления на 20 мм рт. ст. от исходного уровня после введения конъюгата IL-2 субъекту.
Вариант осуществления 450. Способ согласно любому из вариантов осуществления 1-449, где введение эффективного количества конъюгата IL-2 субъекту не вызывает отек у субъекта после введения конъюгата IL-2 субъекту.
Вариант осуществления 451. Способ согласно любому из вариантов осуществления 1-450, где введение эффективного количества конъюгата IL-2 субъекту не вызывает нарушение функции почек или печени у субъекта после введения конъюгата IL-2 субъекту.
Вариант осуществления 452. Способ согласно любому из вариантов осуществления 1-451, где введение эффективного количества конъюгата IL-2 субъекту не вызывает эозинофилию у субъекта после введения конъюгата IL-2 субъекту.
Вариант осуществления 453. Способ согласно варианту осуществления 452, где введение эффективного количества конъюгата IL-2 субъекту не приводит к тому, что количество эозинофилов в периферической крови у субъекта превышает 500 на мкл после введения конъюгата IL-2 субъекту.
Вариант осуществления 454. Способ согласно варианту осуществления 452, где введение эффективного количества конъюгата IL-2 субъекту не приводит к тому, что количество эозинофилов в периферической крови у субъекта превышает 500 на мкл - 1500 на мкл после введения конъюгата IL-2 субъекту.
Вариант осуществления 455. Способ согласно варианту осуществления 452, где введение эффективного количества конъюгата IL-2 субъекту не приводит к тому, что количество эозинофилов в периферической крови у субъекта превышает 1500 на мкл - 5000 на мкл после введения конъюгата IL-2 субъекту.
Вариант осуществления 456. Способ согласно варианту осуществления 452, где введение эффективного количества конъюгата IL-2 субъекту не приводит к тому, что количество эозинофилов в периферической крови у субъекта превышает 5000 на мкл после введения конъюгата IL-2 субъекту.
Вариант осуществления 457. Способ согласно любому из вариантов осуществления 1-456, где введение эффективного количества конъюгата IL-2 субъекту не противопоказано субъектам, находящимся на режиме лечения психотропными лекарственными средствами.
Вариант осуществления 458. Способ согласно любому из вариантов осуществления 1-457, где введение эффективного количества конъюгата IL-2 субъекту не противопоказано субъектам, находящимся на режиме лечения нефротоксическими, миелотоксическими, кардиотоксическими или гепатотоксическими лекарственными средствами.
Вариант осуществления 459. Способ согласно варианту осуществления 458, где введение эффективного количества конъюгата IL-2 субъекту не противопоказано субъектам, находящимся на режиме лечения аминогликозидами, средствами цитотоксической химиотерапии, доксорубицином, метотрексатом или аспарагиназой.
Вариант осуществления 460. Способ согласно любому из вариантов осуществления 1-459, где введение эффективного количества конъюгата IL-2 субъекту не противопоказано субъектам, которые получают лечение в комбинированных режимах, предусматривающих противоопухолевые средства.
Вариант осуществления 461. Способ согласно варианту осуществления 460, где противоопухолевое средство выбрано из дакарбазина, цисплатина, тамоксифена и интерферона альфа.
Вариант осуществления 462. Способ согласно любому из вариантов осуществления 1-461, где введение эффективного количества конъюгата IL-2 субъекту не вызывает одно или несколько нежелательных явлений 4 степени у субъекта после введения конъюгата IL-2 субъекту.
Вариант осуществления 463. Способ согласно варианту осуществления 462, где одно или несколько нежелательных явлений 4 степени выбраны из гипотермии; шока; брадикардии; желудочковой экстрасистолии; ишемии миокарда; обморока; кровоизлияния; предсердной аритмии; флебита; AV-блокады второй степени; эндокардита; перикардиального выпота; периферической гангрены; тромбоза; нарушения со стороны коронарных артерий; стоматита; тошноты и рвоты; аномалии функциональных проб печени; желудочно-кишечного кровоизлияния; гематемезиса; геморрагического поноса; нарушения со стороны желудочно-кишечного тракта; прободения кишечника; панкреатита; анемии; лейкопении; лейкоцитоза; гипокальциемии; увеличения уровня щелочной фосфатазы; увеличения концентрации азота мочевины в крови (BUN); гиперурикемии; увеличения концентрации небелкового азота (NPN); респираторного ацидоза; сонливости; возбуждения; нейропатии; параноидной реакции; спазма; большого эпилептического припадка; делирия; астмы; отека легких; гипервентиляции; гипоксии; кровохарканья; гиповентиляции; пневмоторакса; мидриаза; нарушения со стороны зрачка; аномалии функции почек; почечной недостаточности и острого канальцевого некроза.
Вариант осуществления 464. Способ согласно любому из вариантов осуществления 1-463, где введение эффективного количества конъюгата IL-2 группе субъектов не вызывает одно или несколько нежелательных явлений 4 степени у более чем 1% субъектов после введения конъюгата IL-2 субъектам.
Вариант осуществления 465. Способ согласно варианту осуществления 464, где одно или несколько нежелательных явлений 4 степени выбраны из гипотермии; шока; брадикардии; желудочковой экстрасистолии; ишемии миокарда; обморока; кровоизлияния; предсердной аритмии; флебита; AV-блокады второй степени; эндокардита; перикардиального выпота; периферической гангрены; тромбоза; нарушения со стороны коронарных артерий; стоматита; тошноты и рвоты; аномалии функциональных проб печени; желудочно-кишечного кровоизлияния; гематемезиса; геморрагического поноса; нарушения со стороны желудочно-кишечного тракта; прободения кишечника; панкреатита; анемии; лейкопении; лейкоцитоза; гипокальциемии; увеличения уровня щелочной фосфатазы; увеличения концентрации азота мочевины в крови (BUN); гиперурикемии; увеличения концентрации небелкового азота (NPN); респираторного ацидоза; сонливости; возбуждения; нейропатии; параноидной реакции; спазма; большого эпилептического припадка; делирия; астмы; отека легких; гипервентиляции; гипоксии; кровохарканья; гиповентиляции; пневмоторакса; мидриаза; нарушения со стороны зрачка; аномалии функции почек; почечной недостаточности и острого канальцевого некроза.
Вариант осуществления 466. Способ согласно любому из вариантов осуществления 1-465, где введение эффективного количества конъюгата IL-2 группе субъектов не вызывает одно или несколько нежелательных явлений у более чем 1% субъектов после введения конъюгата IL-2 субъектам, где одно или несколько нежелательных явлений выбраны из язвы двенадцатиперстной кишки; некроза кишечника; миокардита; наджелудочковой тахикардии; перманентной или транзиторной слепоты на фоне неврита зрительного нерва; транзиторной ишемической атаки; менингита; отека головного мозга; перикардита; аллергического интерстициального нефрита и трахеопищеводной фистулы.
Вариант осуществления 467. Способ согласно любому из вариантов осуществления 1-466, где введение эффективного количества конъюгата IL-2 группе субъектов не вызывает одно или несколько нежелательных явлений у более чем 1% субъектов после введения конъюгата IL-2 субъектам, где одно или несколько нежелательных явлений выбраны из злокачественной гипертермии; остановки сердца; инфаркта миокарда; легочной эмболии; инсульта; прободения кишечника; печеночной или почечной недостаточности; тяжелой депрессии, приводящей к суициду; отека легких; остановки дыхания; дыхательной недостаточности.
Вариант осуществления 468. Способ согласно любому из вариантов осуществления 1-467, где введение конъюгата IL-2 субъекту приводит к увеличению количества CD8+ T- и NK-клеток в периферической крови у субъекта без увеличения количества CD4+ регуляторных T-клеток в периферической крови у субъекта.
Вариант осуществления 469. Способ согласно любому из вариантов осуществления 1-468, где введение конъюгата IL-2 субъекту приводит к увеличению количества CD8+ T- и NK-клеток в периферической крови у субъекта без увеличения количества эозинофилов в периферической крови у субъекта.
Вариант осуществления 470. Способ согласно любому из вариантов осуществления 1-469, где введение конъюгата IL-2 субъекту приводит к увеличению количества внутриопухолевых CD8+ T- и NK-клеток у субъекта без увеличения количества внутриопухолевых CD4+ регуляторных T-клеток у субъекта.
Вариант осуществления 471. Способ согласно любому из вариантов осуществления 1-470, где введение эффективного количества конъюгата IL-2 субъекту не требует наличия отделения интенсивной терапии или квалифицированных специалистов в области сердечно-легочной медицины или интенсивной терапии.
Вариант осуществления 472. Способ согласно варианту осуществления 471, где введение эффективного количества конъюгата IL-2 субъекту не требует наличия отделения интенсивной терапии.
Вариант осуществления 473. Способ согласно варианту осуществления 471, где введение эффективного количества конъюгата IL-2 субъекту не требует наличия квалифицированных специалистов в области сердечно-легочной медицины или интенсивной терапии.
Вариант осуществления 474. Способ согласно любому из вариантов осуществления 1-473, где рак имеет форму солидной опухоли.
Вариант осуществления 475. Способ согласно любому из вариантов осуществления 1-473, где рак имеет форму опухоли жидких тканей.
Вариант осуществления 476. Способ согласно любому из вариантов осуществления 381-475, где конъюгат IL-2 вводят субъекту до введения субъекту одного или нескольких ингибиторов контрольных точек иммунного ответа.
Вариант осуществления 477. Способ согласно любому из вариантов осуществления 381-475, где один или несколько ингибиторов контрольных точек иммунного ответа вводят субъекту до введения субъекту конъюгата IL-2.
Вариант осуществления 478. Способ согласно любому из вариантов осуществления 381-475, где конъюгат IL-2 и один или несколько ингибиторов контрольных точек иммунного ответа вводят субъекту одновременно.
Вариант осуществления 479. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 1, SEQ ID NO: 3 или SEQ ID NO: 4, при этом по меньшей мере один аминокислотный остаток в конъюгате IL-2 заменен цистеином, ковалентно связанным с группой PEG.
Вариант осуществления 480. Способ согласно варианту осуществления 479, где группа PEG имеет молекулярную массу, выбранную из 5 кДа, 10 кДа, 15 кДа, 20 кДа, 25 кДа, 30 кДа, 35 кДа, 40 кДа, 45 кДа, 50 кДа и 60 кДа.
Вариант осуществления 481. Способ согласно варианту осуществления 479, где группа PEG имеет молекулярную массу 5 кДа.
Вариант осуществления 482. Способ согласно варианту осуществления 479, где группа PEG имеет молекулярную массу 10 кДа.
Вариант осуществления 483. Способ согласно варианту осуществления 479, где группа PEG имеет молекулярную массу 15 кДа.
Вариант осуществления 484. Способ согласно варианту осуществления 479, где группа PEG имеет молекулярную массу 20 кДа.
Вариант осуществления 485. Способ согласно варианту осуществления 479, где группа PEG имеет молекулярную массу 25 кДа.
Вариант осуществления 486. Способ согласно варианту осуществления 479, где группа PEG имеет молекулярную массу 30 кДа.
Вариант осуществления 487. Способ согласно варианту осуществления 479, где группа PEG имеет молекулярную массу 35 кДа.
Вариант осуществления 488. Способ согласно варианту осуществления 479, где группа PEG имеет молекулярную массу 40 кДа.
Вариант осуществления 489. Способ согласно варианту осуществления 479, где группа PEG имеет молекулярную массу 45 кДа.
Вариант осуществления 490. Способ согласно варианту осуществления 479, где группа PEG имеет молекулярную массу 50 кДа.
Вариант осуществления 491. Способ согласно варианту осуществления 479, где группа PEG имеет молекулярную массу 60 кДа.
Вариант осуществления 492. Способ согласно любому из вариантов осуществления 479-491, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, и по меньшей мере один аминокислотный остаток в конъюгате IL-2, который заменен цистеином, выбран из K34, T36, R37, T40, F41, K42, F43, Y44, E60, E61, E67, K63, P64, V68, L71 и Y106.
Вариант осуществления 493. Способ согласно любому из вариантов осуществления 479-491, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, и по меньшей мере один аминокислотный остаток в конъюгате IL-2, который заменен цистеином, выбран из K34, T40, F41, K42, Y44, E60, E61, E67, K63, P64, V68 и L71.
Вариант осуществления 494. Способ согласно любому из вариантов осуществления 479-491, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 4, и по меньшей мере один аминокислотный остаток в конъюгате IL-2, который заменен цистеином, выбран из K35, T37, R38, T41, F42, K43, F44, Y45, E61, E62, E68, K64, P65, V69, L72 и Y107.
Вариант осуществления 495. Способ согласно любому из вариантов осуществления 479-494, где одно или несколько дополнительных средств представляют собой один или несколько ингибиторов контрольных точек иммунного ответа, выбранных из группы, состоящей из ингибиторов PD-1, ингибиторов PD-L1, ингибиторов PD-L2, ингибиторов CTLA-4, агонистов OX40 и агонистов 4-1BB.
Вариант осуществления 496. Способ согласно варианту осуществления 495, где один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов PD-1.
Вариант осуществления 497. Способ согласно варианту осуществления 496, где один или несколько ингибиторов PD-1 выбраны из пембролизумаба, ниволумаба, цемиплимаба, ламбролизумаба, AMP-224, синтилимаба, торипалимаба, камрелизумаба, тислелизумаба, достарлимаба (GSK), PDR001 (Novartis), MGA012 (Macrogenics/Incyte), GLS-010 (Arcus/WuXi), AGEN2024 (Agenus), цетрелимаба (Janssen), ABBV-181 (Abbvie), AMG-404 (Amgen), BI-754091 (Boehringer Ingelheim), CC-90006 (Celgene), JTX-4014 (Jounce), PF-06801591 (Pfizer) и генолимзумаба (Apollomics/Genor BioPharma).
Вариант осуществления 498. Способ согласно варианту осуществления 495, где один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов PD-L1.
Вариант осуществления 499. Способ согласно варианту осуществления 498, где один или несколько ингибиторов PD-L1 выбраны из атезолизумаба, авелумаба, дурвалумаба, ASC22 (Alphamab/Ascletis), CX-072 (CytomX), CS1001 (CStone), косибелимаба (Checkpoint Therapeutics), INCB86550 (Incyte) и TG-1501 (TG Therapeutics).
Вариант осуществления 500. Способ согласно варианту осуществления 495, где один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов CTLA-4.
Вариант осуществления 501. Способ согласно варианту осуществления 500, где один или несколько ингибиторов CTLA-4 выбраны из тремелимумаба, ипилимумаба и AGEN-1884 (Agenus).
Вариант осуществления 502. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, в которой по меньшей мере один отличный от лизина остаток заменен лизином, содержащим линкер и водорастворимый полимер.
Вариант осуществления 503. Способ согласно варианту осуществления 502, где водорастворимый полимер представляет собой группу PEG.
Вариант осуществления 504. Способ согласно вариантам осуществления 502 или 503, где одно или несколько дополнительных средств представляют собой один или несколько ингибиторов контрольных точек иммунного ответа, выбранных из группы, состоящей из ингибиторов PD-1, ингибиторов PD-L1, ингибиторов PD-L2, ингибиторов CTLA-4, агонистов OX40 и агонистов 4-1BB.
Вариант осуществления 505. Способ согласно варианту осуществления 504, где один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов PD-1.
Вариант осуществления 506. Способ согласно варианту осуществления 505, где один или несколько ингибиторов PD-1 выбраны из пембролизумаба, ниволумаба, цемиплимаба, ламбролизумаба, AMP-224, синтилимаба, торипалимаба, камрелизумаба, тислелизумаба, достарлимаба (GSK), PDR001 (Novartis), MGA012 (Macrogenics/Incyte), GLS-010 (Arcus/WuXi), AGEN2024 (Agenus), цетрелимаба (Janssen), ABBV-181 (Abbvie), AMG-404 (Amgen), BI-754091 (Boehringer Ingelheim), CC-90006 (Celgene), JTX-4014 (Jounce), PF-06801591 (Pfizer) и генолимзумаба (Apollomics/Genor BioPharma).
Вариант осуществления 507. Способ согласно варианту осуществления 506, где один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов PD-L1.
Вариант осуществления 508. Способ согласно варианту осуществления 507, где ингибиторы PD-L1 выбраны из атезолизумаба, авелумаба, дурвалумаба, ASC22 (Alphamab/Ascletis), CX-072 (CytomX), CS1001 (CStone), косибелимаба (Checkpoint Therapeutics), INCB86550 (Incyte) и TG-1501 (TG Therapeutics).
Вариант осуществления 509. Способ согласно варианту осуществления 508, где один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов CTLA-4.
Вариант осуществления 510. Способ согласно варианту осуществления 509, где один или несколько ингибиторов CTLA-4 выбраны из тремелимумаба, ипилимумаба и AGEN-1884 (Agenus).
Вариант осуществления 511. Способ согласно любому из вариантов осуществления 1-510, где конъюгат IL-2 содержит группу PEG, ковалентно связанную посредством невысвобождаемой связи.
Вариант осуществления 512. Способ согласно любому из вариантов осуществления 11-511, где конъюгат IL-2 содержит невысвобождаемую ковалентно связанную группу PEG.
Вариант осуществления 513. Способ согласно любому из вариантов осуществления 1-512, где после введения конъюгата IL-2 и одного или нескольких дополнительных средств субъект испытывает ответ, измеряемый с помощью иммуноопосредованных критериев оценки ответа солидных опухолей (iRECIST).
Вариант осуществления 514. Способ согласно варианту осуществления 513, где ответ представляет собой полный ответ, частичный ответ или стабилизацию заболевания.
Вариант осуществления 515. Способ согласно любому из вариантов осуществления 1-514, где конъюгат IL-2 вводят субъекту путем внутривенной, подкожной, внутримышечной, интрацеребральной, интраназальной, внутриартериальной, внутрисуставной, внутрикожной, интравитреальной, внутрикостной инфузии, внутрибрюшинного или интратекального введения.
Вариант осуществления 516. Способ согласно варианту осуществления 515, где конъюгат IL-2 вводят субъекту путем внутривенного, подкожного или внутримышечного введения.
Вариант осуществления 517. Способ согласно варианту осуществления 515, где конъюгат IL-2 вводят субъекту путем внутривенного введения.
Вариант осуществления 518. Способ согласно варианту осуществления 515, где конъюгат IL-2 вводят субъекту путем подкожного введения.
Вариант осуществления 519. Способ согласно варианту осуществления 515, где конъюгат IL-2 вводят субъекту путем внутримышечного введения.
Вариант осуществления 520. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 представляет собой конъюгат IL-2, имеющий SEQ ID NO: 3, где отличная от лизина аминокислота в конъюгате IL-2 заменена остатком лизина, и где остаток лизина содержит один или несколько водорастворимых полимеров и ковалентный линкер.
Вариант осуществления 521. Способ согласно варианту осуществления 520, где остаток лизина расположен в области K34-Y106 в SEQ ID NO: 3.
Вариант осуществления 522. Способ согласно варианту осуществления 521, где остаток лизина расположен в K34.
Вариант осуществления 523. Способ согласно варианту осуществления 521, где остаток лизина расположен в F41.
Вариант осуществления 524. Способ согласно варианту осуществления 521, где остаток лизина расположен в F43.
Вариант осуществления 525. Способ согласно варианту осуществления 521, где остаток лизина расположен в K42.
Вариант осуществления 526. Способ согласно варианту осуществления 521, где остаток лизина расположен в E61.
Вариант осуществления 527. Способ согласно варианту осуществления 521, где остаток лизина расположен в P64.
Вариант осуществления 528. Способ согласно варианту осуществления 521, где остаток лизина расположен в R37.
Вариант осуществления 529. Способ согласно варианту осуществления 521, где остаток лизина расположен в T40.
Вариант осуществления 530. Способ согласно варианту осуществления 521, где остаток лизина расположен в E67.
Вариант осуществления 531. Способ согласно варианту осуществления 521, где остаток лизина расположен в Y44.
Вариант осуществления 532. Способ согласно варианту осуществления 521, где остаток лизина расположен в V68.
Вариант осуществления 533. Способ согласно варианту осуществления 521, где остаток лизина расположен в L71.
Вариант осуществления 534. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких дополнительных средств, где конъюгат IL-2 представляет собой вариант интерлейкина-2 (IL-2), где отличная от лизина аминокислота в аминокислотной последовательности варианта IL-2 заменена аминокислотой, содержащей (a) лизин; (b) ковалентный линкер и (3) один или несколько водорастворимых полимеров.
Вариант осуществления 535. Способ согласно любому из вариантов осуществления 520-534, где один или несколько водорастворимых полимеров содержат группу PEG.
Вариант осуществления 536. Способ согласно варианту осуществления 535, где группа PEG представляет разветвленную или линейную группу PEG.
Вариант осуществления 537. Способ согласно любому из вариантов осуществления 520-536, где одно или несколько дополнительных средств представляют собой один или несколько ингибиторов контрольных точек иммунного ответа, выбранных из группы, состоящей из ингибиторов PD-1, ингибиторов PD-L1, ингибиторов PD-L2, ингибиторов CTLA-4, агонистов OX40 и агонистов 4-1BB.
Вариант осуществления 538. Способ согласно варианту осуществления 537, где один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов PD-1.
Вариант осуществления 539. Способ согласно варианту осуществления 538, где один или несколько ингибиторов PD-1 выбраны из пембролизумаба, ниволумаба, цемиплимаба, ламбролизумаба, AMP-224, синтилимаба, торипалимаба, камрелизумаба, тислелизумаба, достарлимаба (GSK), PDR001 (Novartis), MGA012 (Macrogenics/Incyte), GLS-010 (Arcus/WuXi), AGEN2024 (Agenus), цетрелимаба (Janssen), ABBV-181 (Abbvie), AMG-404 (Amgen), BI-754091 (Boehringer Ingelheim), CC-90006 (Celgene), JTX-4014 (Jounce), PF-06801591 (Pfizer) и генолимзумаба (Apollomics/Genor BioPharma).
Вариант осуществления 540. Способ согласно варианту осуществления 539, где один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов PD-L1.
Вариант осуществления 541. Способ согласно варианту осуществления 540, где ингибиторы PD-L1 выбраны из атезолизумаба, авелумаба, дурвалумаба, ASC22 (Alphamab/Ascletis), CX-072 (CytomX), CS1001 (CStone), косибелимаба (Checkpoint Therapeutics), INCB86550 (Incyte) и TG-1501 (TG Therapeutics).
Вариант осуществления 542. Способ согласно варианту осуществления 541, где один или несколько ингибиторов контрольных точек иммунного ответа выбраны из ингибиторов CTLA-4.
Вариант осуществления 543. Способ согласно варианту осуществления 542, где ингибиторы CTLA-4 выбраны из тремелимумаба, ипилимумаба и AGEN-1884 (Agenus).
Вариант осуществления 544. Способ согласно любому из вариантов осуществления 381-543, где способ дополнительно включает введение субъекту терапевтически эффективного количества одного или нескольких ингибиторов сигнального пути фактора роста клеток эндотелия сосудов (VEGF) или мишени рапамицина у млекопитающих (mTOR).
Вариант осуществления 545. Способ согласно варианту осуществления 544, где субъекту вводят один или несколько ингибиторов сигнального пути VEGF.
Вариант осуществления 546. Способ согласно варианту осуществления 545, где один или несколько ингибиторов сигнального пути VEGF выбраны из группы, состоящей из ингибиторов тирозинкиназного (TKI) рецептора фактора роста клеток эндотелия сосудов (VEGFR) и моноклональных антител к VEGF.
Вариант осуществления 547. Способ согласно варианту осуществления 546, где один или несколько ингибиторов сигнального пути VEGF выбраны из одного или нескольких TKI VEGFR.
Вариант осуществления 548. Способ согласно варианту осуществления 547, где один или несколько TKI VEGFR выбраны из группы, состоящей из кабозантиниба, акситиниба, пазопаниба, сунитиниба или сорафениба.
Вариант осуществления 549. Способ согласно варианту осуществления 548, где один или несколько TKI VEGFR представляют собой кабозантиниб.
Вариант осуществления 550. Способ согласно варианту осуществления 548, где один или несколько TKI VEGFR представляют собой акситиниб.
Вариант осуществления 551. Способ согласно варианту осуществления 548, где один или несколько TKI VEGFR представляют собой пазопаниб.
Вариант осуществления 552. Способ согласно варианту осуществления 548, где один или несколько TKI VEGFR представляют собой сунитиниб.
Вариант осуществления 553. Способ согласно варианту осуществления 548, где один или несколько TKI VEGFR представляют собой сорафениб.
Вариант осуществления 554. Способ согласно варианту осуществления 546, где один или несколько ингибиторов сигнального пути VEGF выбраны из одного или нескольких моноклональных антител к VEGF.
Вариант осуществления 555. Способ согласно варианту осуществления 554, где один или несколько моноклональных антител к VEGF представляют собой бевацизумаб.
Вариант осуществления 556. Способ согласно варианту осуществления 544, где один или несколько ингибиторов mTOR выбраны из группы, состоящей из рапамицина, эверолимуса, темсиролимуса, ридафоролимуса и дефоролимуса.
Вариант осуществления 557. Способ согласно варианту осуществления 556, где один или несколько ингибиторов mTOR представляют собой рапамицин.
Вариант осуществления 558. Способ согласно варианту осуществления 556, где один или несколько ингибиторов mTOR представляют собой эверолимус.
Вариант осуществления 559. Способ согласно варианту осуществления 556, где один или несколько ингибиторов mTOR представляют собой темсиролимус.
Вариант осуществления 560. Способ согласно варианту осуществления 556, где один или несколько ингибиторов mTOR представляют собой ридафоролимус.
Вариант осуществления 561. Способ согласно варианту осуществления 556, где один или несколько ингибиторов mTOR представляют собой дефоролимус.
Вариант осуществления 562. Способ согласно любому из вариантов осуществления 544-561, где рак у субъекта представляет собой почечноклеточную карциному (RCC).
Вариант осуществления 563. Способ согласно варианту осуществления 562, где один или несколько TKI VEGFR представляют собой акситиниб или кабозантиниб.
Вариант осуществления 564. Способ согласно варианту осуществления 562, где один или несколько TKI VEGFR представляют собой кабозантиниб.
Вариант осуществления 565. Способ согласно любому из вариантов осуществления 381-543, где одно или несколько дополнительных средств дополнительно включают в себя одно или несколько химиотерапевтических средств.
Вариант осуществления 566. Способ согласно варианту осуществления 565, где одно или несколько химиотерапевтических средств включают в себя одно или несколько химиотерапевтических средств на основе платины.
Вариант осуществления 567. Способ согласно варианту осуществления 565, где одно или несколько химиотерапевтических средств включают в себя карбоплатин и пеметрексед.
Вариант осуществления 568. Способ согласно варианту осуществления 565, где одно или несколько химиотерапевтических средств включают в себя карбоплатин и наб-паклитаксел.
Вариант осуществления 569. Способ согласно варианту осуществления 565, где одно или несколько химиотерапевтических средств включают в себя карбоплатин и доцетаксел.
Вариант осуществления 570. Способ согласно любому из вариантов осуществления 565-569, где рак у субъекта представляет собой немелкоклеточный рак легкого (NSCLC).
Вариант осуществления 571. Способ согласно любому из вариантов осуществления 1-570, где одно или несколько дополнительных средств представляют собой одно или несколько химиотерапевтических средств.
Вариант осуществления 572. Способ согласно варианту осуществления 571, где одно или несколько химиотерапевтических средств включают в себя одно или несколько химиотерапевтических средств на основе платины.
Вариант осуществления 573. Способ согласно любому из вариантов осуществления 1-572, где у субъекта имеется положительный результат тестирования на вирус папилломы человека (HPV) до введения конъюгата IL-2 и одного или нескольких дополнительных средств.
Вариант осуществления 574. Способ согласно варианту осуществления 572, где рак у субъекта представляет собой плоскоклеточный рак головы и шеи (HNSCC).
Вариант осуществления 575. Способ согласно любому из вариантов осуществления 1-572, дополнительно предусматривающий положительный результат тестирования субъекта на вирус папилломы человека (HPV+) с последующим введением конъюгата IL-2 и одного или нескольких дополнительных средств.
Вариант осуществления 576. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких ингибиторов PD-1, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом аминокислотный остаток в E61 или P64 в конъюгате IL-2 заменен структурой формулы (VIII) или (IX) или смесью (VIII) и (IX):

Формула (VIII),

(IX),
где:
n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 15000 дальтонов до приблизительно 60000 дальтонов; и
X имеет структуру  ,
,
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 576.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких ингибиторов PD-1, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом аминокислотный остаток в E61 или P64 в конъюгате IL-2 заменен структурой формулы (VIII) или (IX) или смесью (VIII) и (IX):

Формула (VIII),

(IX),
где:
n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 15000 дальтонов до приблизительно 60000 дальтонов; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 577. Способ согласно вариантам осуществления 576 или 576.1, где аминокислотный остаток в E61 в конъюгате IL-2 заменен структурой формулы (VIII) или (IX) или смесью (VIII) и (IX), и где n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов.
Вариант осуществления 578. Способ согласно варианту осуществления 577, где n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 30000 дальтонов.
Вариант осуществления 579. Способ согласно вариантам осуществления 577 или 578, где один или несколько ингибиторов PD-1 представляют собой пембролизумаб или ниволумаб.
Вариант осуществления 580. Способ согласно варианту осуществления 579, где один или несколько ингибиторов PD-1 представляют собой пембролизумаб.
Вариант осуществления 581. Способ согласно варианту осуществления 579, где один или несколько ингибиторов PD-1 представляют собой ниволумаб.
Вариант осуществления 582. Способ согласно вариантам осуществления 576 или 576.1, где аминокислотный остаток в P64 в конъюгате IL-2 заменен структурой формулы (VIII) или (IX) или смесью (VIII) и (IX), и где n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов.
Вариант осуществления 583. Способ согласно варианту осуществления 582, где n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 30000 дальтонов.
Вариант осуществления 584. Способ согласно вариантам осуществления 582 или 583, где один или несколько ингибиторов PD-1 представляют собой пембролизумаб или ниволумаб.
Вариант осуществления 585. Способ согласно варианту осуществления 584, где один или несколько ингибиторов PD-1 представляют собой пембролизумаб.
Вариант осуществления 586. Способ согласно варианту осуществления 584, где один или несколько ингибиторов PD-1 представляют собой ниволумаб.
Вариант осуществления 587. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких ингибиторов PD-1, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом аминокислотный остаток в E61 или P64 в конъюгате IL-2 заменен структурой формулы (VI) или (VII) или смесью (VI) и (VII):

Формула (VI),

(VII),
где:
n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 15000 дальтонов до приблизительно 60000 дальтонов; и
X имеет структуру  ,
,
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 587.1. Способ лечения рака у субъекта, включающий введение нуждающемуся в этом субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких ингибиторов PD-1, где конъюгат IL-2 содержит аминокислотную последовательность под SEQ ID NO: 3, при этом аминокислотный остаток в E61 или P64 в конъюгате IL-2 заменен структурой формулы (VI) или (VII) или смесью (VI) и (VII):

Формула (VI),

(VII),
где:
n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 15000 дальтонов до приблизительно 60000 дальтонов; и
X имеет структуру
 ;
;
X-1 указывает точку присоединения к предыдущему аминокислотному остатку; и
X+1 указывает точку присоединения к следующему аминокислотному остатку;
или их фармацевтически приемлемых соли, сольвата или гидрата.
Вариант осуществления 588. Способ согласно вариантам осуществления 587 или 587.1, где аминокислотный остаток в E61 в конъюгате IL-2 заменен структурой формулы (VI) или (VII) или смесью (VI) и (VII), и где n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов.
Вариант осуществления 589. Способ согласно варианту осуществления 588, где n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 30000 дальтонов.
Вариант осуществления 590. Способ согласно вариантам осуществления 588 или 589, где один или несколько ингибиторов PD-1 представляют собой пембролизумаб или ниволумаб.
Вариант осуществления 591. Способ согласно варианту осуществления 590, где один или несколько ингибиторов PD-1 представляют собой пембролизумаб.
Вариант осуществления 592. Способ согласно варианту осуществления 590, где один или несколько ингибиторов PD-1 представляют собой ниволумаб.
Вариант осуществления 593. Способ согласно вариантам осуществления 587 или 587.1, где аминокислотный остаток в P64 в конъюгате IL-2 заменен структурой формулы (VI) или (VII) или смесью (VI) и (VII), и где n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 20000 дальтонов до приблизительно 40000 дальтонов.
Вариант осуществления 594. Способ согласно варианту осуществления 593, где n представляет собой такое целое число, что молекулярная масса группы PEG составляет от приблизительно 30000 дальтонов.
Вариант осуществления 595. Способ согласно вариантам осуществления 593 или 594, где один или несколько ингибиторов PD-1 представляют собой пембролизумаб или ниволумаб.
Вариант осуществления 596. Способ согласно варианту осуществления 595, где один или несколько ингибиторов PD-1 представляют собой пембролизумаб.
Вариант осуществления 597. Способ согласно варианту осуществления 595, где один или несколько ингибиторов PD-1 представляют собой ниволумаб.
Вариант осуществления 598. Способ согласно любому из вариантов осуществления 1-597, где конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
Вариант осуществления 599. Конъюгат IL-2 для применения в способе согласно любому из вариантов осуществления 1-598.
Вариант осуществления 600. Применение конъюгата IL-2 для изготовления лекарственного препарата для лечения рака в соответствии со способом согласно любому из вариантов осуществления 1-598.
ПРИМЕРЫ
Данные примеры представлены исключительно в иллюстративных целях и не ограничивают объем представленной в данном документе формулы изобретения.
В каждом из соединений, раскрытых в примерах 2-8, используется SEQ ID NO: 4 и фрагмент [AzK_PEG], где положение замененной аминокислоты в конъюгате IL-2 относится к положениям в SEQ ID NO: 4.
Например, соединение, обозначенное как "P65_5кДа" в таблицах 3A и 3B, получали посредством способов, аналогичных тем, которые раскрыты в примере 2, где вначале получали белок, имеющий SEQ ID NO: 4, в которой пролин в положении 65 был заменен на N6-((2-азидоэтокси)-карбонил)-L-лизин (AzK) (SEQ ID NO: 10). Затем проводили реакцию AzK-содержащего белка в условиях клик-химии с DBCO, содержащим линейную группу метокси-PEG, имеющую среднюю молекулярную массу 5 кДа, с получением продукта, имеющего SEQ ID NO: 20, содержащую формулу (II), формулу (III) или смесь формул (II) и (III), где W представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу 5 кДа.
В другом примере соединение, обозначенное как "P65_30кДа" в таблицах 3A и 3B, которое использовали в примере 4, примере 5, примере 6 и примере 11 (также называемое "IL-2_P65[AzK_PEG30кДа]" в примере 11 и называемое в примере 11 и в графических материалах "соединение A"), получали вначале посредством получения белка, имеющего SEQ ID NO: 4, в которой пролин в положении 65 был заменен на N6-((2-азидоэтокси)-карбонил)-L-лизин (AzK) (SEQ ID NO: 10). Затем проводили реакцию AzK-содержащего белка в условиях клик-химии с DBCO, содержащим линейную группу метокси-PEG, имеющую среднюю молекулярную массу 30 кДа, с получением продукта, имеющего SEQ ID NO: 25, содержащего формулу (II), формулу (III) или смесь формул (II) и (III), где W представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу 30 кДа. Соединение также может быть определено как соединение, содержащее аминокислотную последовательность под SEQ ID NO: 4, в которой пролин в положении 65 (P65) заменен структурой формулы (VI) или (VII) или смесью (VI) и (VII), и при этом n представляет собой такое целое число, что группа PEG имеет молекулярную массу, составляющую приблизительно 30 кДа. Соединение также может быть определено как соединение, содержащее аминокислотную последовательность под SEQ ID NO: 4, в которой пролин в положении 65 (P65) заменен структурой формулы (X) или (XI) или смесью (X) и (XI), и при этом n представляет собой такое целое число, что группа PEG имеет молекулярную массу, составляющую приблизительно 30 кДа.
В другом примере соединение, обозначенное как "E62_5кДа" в таблицах 3A и 3B, получали вначале посредством получения белка, имеющего SEQ ID NO: 4, в которой глутаминовая кислота в положении 62 была заменена на N6-((2-азидоэтокси)-карбонил)-L-лизин AzK (SEQ ID NO: 11). Затем проводили реакцию AzK-содержащего белка в условиях клик-химии с DBCO, содержащим линейную группу метокси-PEG, имеющую среднюю молекулярную массу 5 кДа, с получением продукта, имеющего SEQ ID NO: 21, содержащую формулу (II), формулу (III) или смесь формул (II) и (III), где W представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу 5 кДа.
В другом примере соединение, обозначенное как "E62_30кДа" в таблицах 3A и 3B, а также используемое в примере 4, получали вначале посредством получения белка, имеющего SEQ ID NO: 4, в которой глутаминовая кислота в положении 62 была заменена на N6-((2-азидоэтокси)-карбонил)-L-лизин (AzK) (SEQ ID NO: 11). Затем проводили реакцию AzK-содержащего белка в условиях клик-химии с DBCO, содержащим линейную группу метокси-PEG, имеющую среднюю молекулярную массу 30 кДа, с получением продукта, имеющего SEQ ID NO: 26, содержащего формулу (II), формулу (III) или смесь формул (II) и (III), где W представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу 30 кДа. Соединение также может быть определено как соединение, содержащее аминокислотную последовательность под SEQ ID NO: 4, в которой глутаминовая кислота в положении 62 (E62) заменена структурой формулы (VI) или (VII) или смесью (VI) и (VII), и при этом n представляет собой такое целое число, что группа PEG имеет молекулярную массу, составляющую приблизительно 30 кДа. Соединение также может быть определено как соединение, содержащее аминокислотную последовательность под SEQ ID NO: 4, в которой глутаминовая кислота в положении 62 (E62) заменена структурой формулы (X) или (XI) или смесью (X) и (XI), и при этом n представляет собой такое целое число, что группа PEG имеет молекулярную массу, составляющую приблизительно 30 кДа.
В другом примере соединение, обозначенное как "K35_30кДа" и используемое в примере 8, получали вначале посредством получения белка, имеющего SEQ ID NO: 4, в которой лизин в положении 35 был заменен на N6-((2-азидоэтокси)-карбонил)-L-лизин (AzK) (SEQ ID NO: 14). Затем проводили реакцию AzK-содержащего белка в условиях клик-химии с DBCO, содержащим линейную группу метокси-PEG, имеющую среднюю молекулярную массу 30 кДа, с получением продукта, имеющего SEQ ID NO: 29, содержащего формулу (II), формулу (III) или смесь формул (II) и (III), где W представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу 30 кДа. Соединение также может быть определено как соединение, содержащее аминокислотную последовательность под SEQ ID NO: 4, в которой лизин в положении 35 (K35) заменен структурой формулы (VI) или (VII) или смесью (VI) и (VII), и при этом n представляет собой такое целое число, что группа PEG имеет молекулярную массу, составляющую приблизительно 30 кДа. Соединение также может быть определено как соединение, содержащее аминокислотную последовательность под SEQ ID NO: 4, в которой лизин в положении 35 (K35) заменен структурой формулы (X) или (XI) или смесью (X) и (XI), и при этом n представляет собой такое целое число, что группа PEG имеет молекулярную массу, составляющую приблизительно 30 кДа.
В примерах 9 и 10 использовали соединение "IL-2_P65_[AzK_L1_PEG30кДа]-1", которое содержит SEQ ID NO: 50, в которой пролин в положении 64 заменен на AzK_L1_PEG30кДа, где AzK_L1_PEG30кДа определен как структура формулы (IV) или формулы (V) или смесь формул (IV) и (V) и линейная цепь mPEG массой 30 кДа. Соединение IL-2_P65[AzK_L1_PEG30кДа]-1 также определено как соединение, содержащее SEQ ID NO: 3, в которой остаток пролина в положении 64 (P64) заменен структурой формулы (VIII) или (IX) или смесью (VIII) и (IX), и при этом n представляет собой такое целое число, что молекулярная масса группы PEG составляет приблизительно 30 кДа. Соединение IL-2_P65[AzK_L1_PEG30кДа]-1 также определено как соединение, содержащее SEQ ID NO: 3, в которой остаток пролина в положении 64 (P64) заменен структурой формулы (XII) или (XIII) или смесью (XII) и (XIII), и при этом n представляет собой такое целое число, что молекулярная масса группы PEG составляет приблизительно 30 кДа. Соединение IL-2_P65[AzK_L1_PEG30кДа]-1 также упоминается в примерах 12 и последующих и в графических материалах как "соединение B". Соединение получали посредством способов, аналогичных тем, которые раскрыты в примере 2, где вначале получали белок, имеющий SEQ ID NO: 3, в которой пролин в положении 64 был заменен на N6-((2-азидоэтокси)-карбонил)-L-лизин AzK (SEQ ID NO: 35). Затем проводили реакцию AzK-содержащего белка в условиях клик-химии с DBCO, содержащим линейную группу метокси-PEG, имеющую среднюю молекулярную массу 30 кДа.
В примере 11 использовали соединение "IL-2_P65[AzK_PEG30кДа]" (также называемое в данном документе "P65_30кДа"), которое было таким, как описано выше.
ПРИМЕР 1
Анализы димеризации киназных и цитокиновых рецепторов
Обращение с клетками
Обеспечивали размножение линий клеток PathHunter из замороженных исходных культур в соответствии со стандартными процедурами. Клетки высевали в общем объеме 20 мкл в 384-луночные микропланшеты с белыми стенками и инкубировали в течение соответствующего периода времени перед тестированием.
Формат агонистов
Для определения агонистов клетки инкубировали с образцом для индукции ответа. Осуществляли промежуточное разбавление исходных растворов образцов для получения 5Х образца в буфере для анализа. Приблизительно 5 мкл 5X образца добавляли к клеткам и инкубировали при 37°C в течение 6-16 часов в зависимости от анализа. Концентрация среды-носителя составляла 1%.
Детектирование сигнала
Сигнал в анализе генерировали путем однократного добавления 12,5 или 15 мкл (50% об./об.) коктейля детекторных реагентов PathHunter для анализов агонистов и антагонистов соответственно с последующим инкубированием в течение одного часа при комнатной температуре. В некоторых анализах активность выявляли с использованием высокочувствительного детекторного реагента (набор PathHunter Flash) с целью улучшения эффективности анализа. В ходе данных анализов в лунки добавляли равный объем детекторного реагента (25 или 30 мкл) с последующим инкубированием в течение одного часа при комнатной температуре. Прочитывание микропланшетов проводили после генерирования сигнала с помощью прибора PerkinElmer EnVisionTM для детектирования хемилюминесцентного сигнала.
Анализ данных
Активность соединений анализировали с использованием пакета для анализа данных CBIS (ChemInnovation, Калифорния). Для анализов в режиме агонизма процент активности рассчитывали по следующей формуле:
% активности=100% x (среднее RLU тестируемого образца - среднее RLU контрольной среды-носителя) / (среднее MAX RLU контрольного лиганда - среднее RLU контрольной среды-носителя).
Для анализов в режиме антагонизма процент ингибирования рассчитывали по следующей формуле:
% ингибирования=100% x (1 - (среднее RLU тестируемого образца - среднее RLU контрольной среды-носителя) / (среднее RLU контроля EC80 - среднее RLU контрольной среды-носителя)).
ПРИМЕР 2
Клеточный скрининг для идентификации пегилированных соединений IL-2 без взаимодействия с IL-2Rα
Функциональному анализу подвергали иллюстративные конъюгаты IL-2: K35, F42, K43, E62 и P65. Конъюгаты IL-2 экспрессировали в виде телец включения в E. coli посредством способов, раскрытых в данном документе, при этом получали экспрессионные плазмиды, кодирующие белок с желаемой аминокислотной последовательностью, которые содержали (a) неприродную пару оснований, содержащую первый неприродный нуклеотид и второй неприродный нуклеотид, для обеспечения наличия кодона в желаемом положении, в которое встраивали неприродную аминокислоту N6-((2-азидоэтокси)-карбонил)-L-лизин (AzK), и соответствующего антикодона в тРНК, (b) плазмиду, кодирующую тРНК, полученную из Pyl M. mazei , которая содержит неприродный нуклеотид для обеспечения наличия соответствующего антикодона вместо своей нативной последовательности, (c) плазмиду, кодирующую пирролизил-тРНК-синтетазу, полученную из M. barkeri (MbPylRS), и (d) N6-((2-азидоэтокси)-карбонил)-L-лизин (AzK). Двухнитевой олигонуклеотид, который кодирует аминокислотную последовательность желаемого варианта IL-2, содержал кодон AXC, например, в положении 34, 37, 40, 41, 42, 43, 44, 61, 64, 68 или 71 последовательности, которая кодирует белок, имеющий SEQ ID NO: 3, или в положении 35, 38, 41, 42, 43, 45, 62, 65, 69 или 72 последовательности, которая кодирует белок, имеющий SEQ ID NO: 4, где X представляет собой неприродный нуклеотид, раскрытый в данном документе. В некоторых вариантах осуществления клетка дополнительно содержит плазмиду, которая может представлять собой плазмиду для экспрессии белка или другую плазмиду, которая кодирует ген ортогональной тРНК из M. mazei, которая содержит антикодон GYT, соответствующий AXC, вместо своей нативной последовательности, где Y представляет собой неприродный нуклеотид, раскрытый в данном документе, и может быть таким же, как неприродный нуклеотид в кодоне, или отличаться от него. X и Y выбраны из неприродных нуклеотидов dTPT3, dNaM и dCNMO, раскрытых в данном документе. Экспрессируемый белок очищали и подвергали рефолдингу с использованием стандартных процедур перед сайт-специфическим пегилированием AzK-содержащего продукта IL-2 с помощью DBCO-опосредованной клик-химии без использования меди для стабильного ковалентного присоединения фрагментов mPEG к AzK (схема 1).
Схема 1. Иллюстративный синтез вариантов интерлейкина с AzK_PEG (где n обозначает число повторяющихся звеньев PEG). Реакция фрагмента AzK с алкинильным фрагментом DBCO может давать один региоизомерный продукт или смесь региоизомерных продуктов.
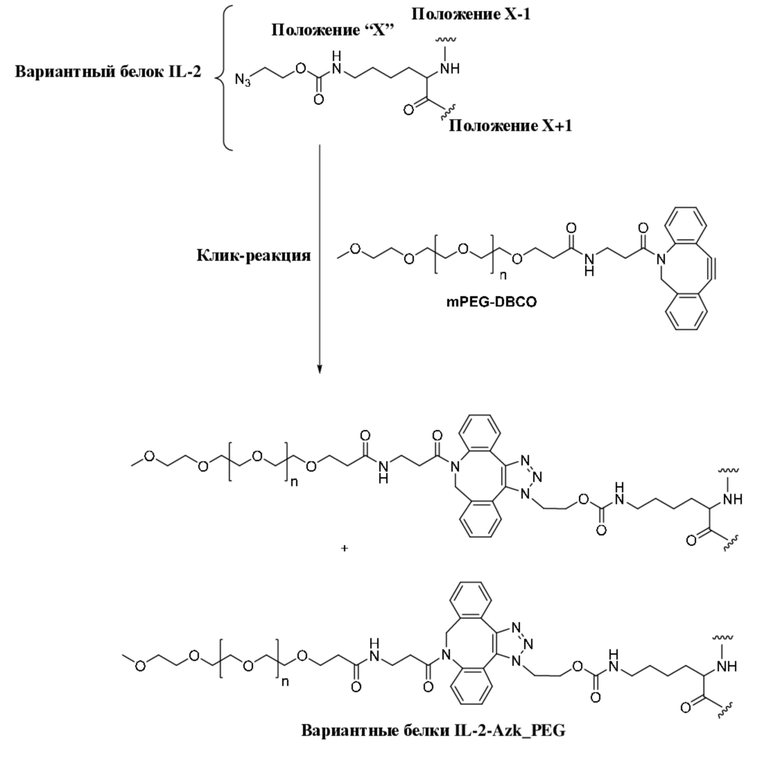
Конъюгаты IL-2 подвергали скринингу в отношении функциональной активности в DiscoverX (Фримонт, Калифорния) с использованием анализа цитокиновых рецепторов IL-2 PathHunter. В данном анализе используют рекомбинантную линию клеток U2OS человека, которая экспрессирует субъединицы β (IL-2Rβ) и γ (IL-2Rγ) рецептора IL-2, каждая из которых слита с половиной разделенного репортерного фермента β-галактозидазы. Дополнительно конструировали вторую линию клеток для экспрессии субъединицы IL-2Rα. Параллельное тестирование с этими двумя линиями клеток позволяет оценить активацию варианта рецептора IL-2αβγ, а также базального комплекса βγ. Активность агониста IL-2 в рецепторном комплексе IL-2βγ стимулирует димеризацию рецептора и восстановление репортерной β-галактозидазы, что приводит к образованию хемилюминесцентного сигнала. Анализ проводили в режиме агонизма для определения EC50 каждого тестируемого препарата, а сравнение профилей кривой зависимости доза-ответ между положительными и отрицательными по IL2Rα типами клеток позволяет определить вклад IL2Rα в наблюдаемую активность.
В таблице 2 показаны данные по ЕС50 для агонизма рецептора IL-2 при клеточном скрининге пегилированных конъюгатов IL-2 с 10 кДа (за исключением указанных случаев)
EC50 (нМ)
EC50 (нМ)
Биохимические взаимодействия пегилированного IL-2 с субъединицами рецептора IL-2 человека
Кинетические параметры взаимодействий пегилированного соединения IL-2 с субъединицами рецептора IL-2 человека измеряли с использованием поверхностного плазмонного резонанса (SPR) в Biosensor Tools LLC (Солт-Лейк-Сити, Юта). Для этих исследований внеклеточные домены IL-2Rα (Sino Biological, № 10165-H02H) и β (Sino Biological, № 10696-H02H), слитые с Fc IgG1 человека, захватывали на поверхности сенсорного чипа CM4, покрытого белком А, от Biacore. Эти поверхности зондировали в двух повторностях в серии двукратных разведений, начиная с 2 мкM нативного IL-2 (IL-2 дикого типа; Thermo № PHC0021), P65_30кДа, P65_5кДа, E62_30кДа либо E62_5кДа, с использованием прибора Biacore 2000 SPR. Тестируемые образцы вводили на 60 секунд для обеспечения измерения ассоциации, а затем только буфер (промывочный) на 30 секунд для измерения диссоциации. Единицы ответа (RU, ось Y) наносили на график в зависимости от времени (с, ось X).
Чтобы оценить эффект α-субъединицы рецептора IL-2 в отношении связывания IL-2 с β, α захватывали в приблизительно двукратном избытке по сравнению с β. На эти поверхности наносили нативный IL-2 (IL-2 дикого типа), P65_30кДа, P65_5кДа, E62_30кДа или E62_5кДа в серии трехкратных разведений, начиная с 2,5 мкМ. Данные о связывании аппроксимировали моделью взаимодействия 1:1, которая включала объемный сдвиг, и извлеченные кинетические параметры обобщенно представлены в таблице 3A и таблице 3B. Как показано в таблице 3A и таблице 3B, низкомолекулярные PEG устраняют взаимодействие с IL2R-альфа, но оказывают менее выраженный неспецифический эффект в отношении взаимодействия с IL2R-бета.
Определение профиля иммунного ответа ex vivo для соединений IL-2 в образцах РВМС, полученных из системы удаления первичных лейкоцитов человека (LRS)
Для определения того, как разная рецепторная специфичность IL-2 P65_30кДа, K64_30кДа, K43_30кДа, K35_30кДа и F42_30кДа влияет на активацию субпопуляций первичных иммунных клеток, осуществляли определение профиля зависимости "концентрация-ответ" для активации лимфоцитов в образцах мононуклеарных клеток периферической крови (PBMC) человека, полученных из LRS, с помощью многоцветной проточной цитометрии. Эти исследования осуществляли в PrimityBio LLC (Фримонт, Калифорния). Свежие образцы, полученные из LRS, обрабатывали с помощью нативного IL-2, IL-2 P65_30кДа, K64_30кДа, K43_30кДа, K35_30кДа и F42_30кДа в серии 5-кратных разведений, начиная с наивысшей концентрации 30 мкг/мл. После 45-минутного инкубирования образцы фиксировали и окрашивали антителами для выявления фосфорилированной формы фактора транскрипции STAT5 (pSTAT5), являющегося маркером вышележащего привлечения и активации сигнальных комплексов рецептора IL-2, а также панели поверхностных маркеров для отслеживания образования pSTAT5 в специфических субпопуляциях T-клеток и естественных клеток-киллеров (NK). Панель окрашивания для исследования методом проточной цитометрии образцов PBMC, полученных из LRS, включает маркеры эффекторных Т-клеток (Teff: CD3+, CD4+, CD8+, CD127+), NK-клеток (CD3-, CD16+) и регуляторных Т-клеток (Treg: CD3+, CD4+, CD8-, IL-2Rα+, CD127-1).
Данные проточной цитометрии анализировали в отношении активации различных субпопуляций Т- и NK-клеток в режиме зависимости "концентрация-ответ", считывая накопление pSTAT5 после обработки с помощью нативного IL-2. Вследствие Treg-специфической экспрессии IL-2Rα нативный IL-2 демонстрировал увеличенную активность стимуляции pSTAT5 в Treg по сравнению с CD8 Teff- и NK-клетками. По сравнению с нативным соединением пегилированные варианты демонстрировали умеренно сниженную активность в отношении популяций CD8 T-клеток и NK-клеток, но показывали дифференциальное снижение активности в Treg-клетках, экспрессирующих IL-2Rα, по сравнению с нативным IL-2.
В таблице 4 представлена EC50 зависимости доза-ответ для передачи сигнала, опосредованной pSTAT5 (EC50), в образцах из LRS человека или для пролиферации CTTL-2 при обработке указанным вариантом IL-2.
N.D.=не определено.
Значения EC50 (пг/мл) рассчитывали по кривым зависимости доза-ответ, полученным из графиков MFI.
ПРИМЕР 3
PEG и замена остатков способствуют фармакологическим свойствам вариантов, не связанным с альфа-субъединицей
Для определения того, как PEG и замена остатков влияют на фармакологические свойства IL-2 E62, не связанные с альфа-субъединицей, осуществляли определение профиля зависимости "концентрация-ответ" для активации лимфоцитов в образцах мононуклеарных клеток периферической крови (PBMC) человека, полученных из LRS, с помощью многоцветной проточной цитометрии. Эти исследования осуществляли в PrimityBio LLC (Фримонт, Калифорния). Свежие образцы, полученные из LRS, обрабатывали с помощью нативного IL-2, E62K либо E62_30кДа в серии 5-кратных разведений, начиная с наивысшей концентрации 30 мкг/мл. После 45-минутного инкубирования образцы фиксировали и окрашивали антителами для выявления фосфорилированной формы фактора транскрипции STAT5 (pSTAT5), являющегося маркером вышележащего привлечения и активации сигнальных комплексов рецептора IL-2, а также панели поверхностных маркеров для отслеживания образования pSTAT5 в специфических субпопуляциях T-клеток и естественных клеток-киллеров (NK). Панель окрашивания для исследования методом проточной цитометрии образцов PBMC, полученных из LRS, включает маркеры CD4, CD4+ центральных клеток памяти, CD4+ эффекторных клеток памяти, CD4+ Т-клеток памяти, CD4+ "необученных" T-клеток, CD4+ T-клеток, CD8, CD8+ центральных клеток памяти, CD8+ эффекторных клеток памяти, CD8+ T-клеток памяти, CD8+ "необученных" T-клеток, CD8+ T-клеток, NK-клеток и регуляторных T-клеток.
ПРИМЕР 4
PK/PD-исследования у мышей C57BL/6, ранее не участвовавших в экспериментах (E3826-U1704) и несущих опухоль из B16-F10 (E3826-U1803)
Планы исследования обобщенно представлены в таблице 5 и таблице 6, при этом дозу рассчитывали, исходя из массы белкового компонента, не включая массу фрагмента PEG. Образцы терминальной крови собирали посредством пункции сердца в указанные моменты времени. Исследование E3826-U1704 включало 13 моментов времени (0,13, 0,25, 0,5, 1, 2, 4, 8, 12, 24, 48, 72, 96 и 120 ч.) с умерщвлением 3 мышей в каждый момент времени, а исследование E3826-U1803 включало 9 моментов времени (2, 8, 12, 24, 48, 72, 120, 168 и 240 ч.) с умерщвлением 4-7 мышей в каждый момент времени. Плазму крови и клетки крови (в обоих исследованиях) и опухоли в исследовании E3826-U1803 собирали для PK- и PD-анализов.
Биологический анализ образцов плазмы крови осуществляли с использованием сертифицированного ELISA-анализа IL-2 человека (Abcam, Кембридж, Великобритания). Концентрации альдеслейкина, E62_30кДа и P65_30кДа и внутреннего стандарта в образцах, полученных из плазмы крови, определяли посредством ELISA-анализа. Анализ данных PK осуществляли в NW Solutions (Сиэтл, Вашингтон). Данные PK импортировали в Phoenix WinNonlin v6.4 (Certara/Pharsight, Принстон, Нью-Джерси) для анализа. Данные о средних групповых значениях концентрации в плазме крови в зависимости от времени анализировали с помощью некомпартментных методов с использованием модели IV болюсного введения.
В исследовании E3826-U1704 как P65_30кДа, так и E62_30кДа демонстрируют лучший PK-профиль по сравнению с альдеслейкином, что обобщенно представлено в таблице 7. После однократной IV болюсной дозы альдеслейкина Tmax наблюдалась через 0,03 ч. после введения дозы (первый момент времени измерения после введения дозы), а средние концентрации в плазме крови поддавались измерению в течение до 4 ч. после введения дозы. После однократного IV болюсного введения дозы P65_30кДа и E62_30кДа Tmax наблюдалась через 0,03 ч. после введения дозы, а средние концентрации в плазме крови поддавались измерению в течение до 120 ч. после введения дозы (последний момент времени измерения). В отдельном исследовании после IV введения дозы E62_5кДа Tmax наблюдалась через 0,133 ч. после введения дозы, а средние концентрации в плазме крови поддавались измерению в течение до 12 ч. после введения дозы.
Воздействие, определенное на основании Cmax и AUC0-t, было следующим: P65_30кДа > E62_30кДа >> E62_5кДа > альдеслейкин. E62_5кДа с более низкомолекулярным PEG характеризовался PK-профилем, близким к rIL-2 (таблица 7). Воздействие P65_30кДа в 5,5 и 200 раз превышало воздействие альдеслейкина при определении на основании Cmax и AUC0-t соответственно. Кроме того, P65_30кДа демонстрировал 23-кратное увеличение t1/2 (13,3 ч. в сравнении с 0,57 ч.) и приблизительно 198-кратное снижение CL (6,58 в сравнении с 1300 мл/ч./кг) по сравнению с альдеслейкином. Как для P65_30кДа, так и для E62_30кДа объем распределения (82,4 и 92,3 мл/кг соответственно) был в приблизительно 4,2-4,7 раза сниженным по сравнению с альдеслейкином и сходным с объемом крови у мыши (85 мл/кг [Boersen 2013]). Это свидетельствует о том, что P65_30кДа и E62_30кДа распределяются главным образом в системном кровотоке.
Примечание: R2 представляет собой параметр критерия согласия для конечной фазы каждого профиля зависимости концентрации от времени.
Все параметры приведены с точностью до 3 значащих цифр.
ПРИМЕР 5
Фармакодинамические наблюдения в компартменте периферической крови
Фосфорилирование STAT5 и индукцию пролиферации клеток (ранний молекулярный маркер Ki-67 и количества клеток) использовали в качестве фармакодинамических показателей для оценки фармакологического профиля P65_30кДа относительно его фармакокинетических характеристик. PD-маркер pSTAT5 показал хорошую корреляцию с PK как для P65_30кДа, так и для альдеслейкина в CD8+ эффекторных Т-клетках (таблица 7). Стойкое повышение уровня pSTAT5 наблюдалось как в NK-, так и в CD8+Т-клетках в течение до 72 ч. и до 24 ч. в Treg. Индукция pSTAT5 возвращалась к исходному уровню спустя всего 2 ч. у мышей, получавших дозу альдеслейкина. Фосфорилирование STAT5 приводило к пролиферативным ответам (72-120 ч.) CD8+ эффекторных Т-клеток и NK-клеток, но не Treg. Фенотипический анализ CD8+ эффекторных Т-клеток выявил значительное размножение CD44+ клеток памяти в данной популяции.
Фармакодинамические наблюдения в опухолевом компартменте у мышей C57BL/6, несущих опухоль из B16-F10 (E3826-U1803)
В таблице 8 показана концентрация лекарственного средства в плазме крови и в опухоли после однократной дозы 3 мг/кг P65_30кДа у мышей, несущих опухоль из B16-F10, при этом дозу рассчитывали, исходя из массы белкового компонента, не включая массу фрагмента PEG. Период полужизни в опухоли вдвое превышал период полужизни в плазме крови (24,4 в сравнении с 12,6), что указывает на то, что P65_30кДа проникает в опухоль и сохраняется в опухоли. Хвостовые части кривых пересекаются, показывая, что из плазмы крови выведение происходит быстрее, чем из опухоли (данные не показаны). Соотношение AUC в опухоли:плазме крови составляло 9,7% и 8,4% для доз 1 и 3 мг/кг соответственно.
Исследование MTD на мышах Balb/c E3826-U1802
Исследование диапазона доз P65_30кДа выполняли на самках мышей Balb/c, ранее не участвовавших в экспериментах, в Crown Biosciences, Inc. (Сан-Диего, Калифорния). План исследования показан в таблице 9, при этом дозу рассчитывали, исходя из массы белкового компонента, не включая массу фрагмента PEG. Образцы крови отбирали из поднижнечелюстной вены в 8 моментов времени (0,25, 1, 4, 12, 24, 34, 48 и 72 ч.). Как плазму крови, так и клетки крови собирали для PK- и PD-анализов.
Все образцы плазмы крови анализировали в отношении цитокинов IL-2 человека, а также IL-2, TNF-α, IFNγ, IL-5 и IL-6 мыши, используя коммерчески доступные наборы для ELISA.
# Для оценивания PK/PD использовали только дозу 0,3 мг/кг P65_30кДа.
Токсикологические наблюдения в исследовании MTD с использованием мышей Balb/c
Основной формой токсичности, ассоциированной с высокодозовым альдеслейкином, является синдром повышенной проницаемости сосудов и ассоциированный с ним синдром высвобождения цитокинов (CRS). Для оценивания потенциала данного эффекта у мышей осуществляли однократное IV введение P65_30кДа в дозах в диапазоне доз от 0,01 до 5,0 мг/кг (таблица 9), при этом дозу рассчитывали, исходя из массы белкового компонента, не включая массу фрагмента PEG. Осуществляемыми анализами были гематологический анализ, гистопатологический анализ, анализ массы органов и анализ цитокинов. При гематологическом, гистопатологическом анализе или анализе массы тела не наблюдались аномалии по сравнению с мышами, обработанными контрольной средой-носителем, как для P65_30кДа, так и для альдеслейкина. Что касается анализа цитокинов, наблюдалось, что альдеслейкин повышал уровни IL-5 в плазме крови, начиная с дозы 1 мг/кг до 5 мг/кг. В случае с P65_30кДа умеренное увеличение уровня IL-5 (но меньшее по сравнению с альдеслейкином) наблюдалось только при дозе 5 мг/кг. Транзиторное повышение уровней IFNγ в системном кровотоке наблюдалось как для альдеслейкина, так и для P65_30 кДа.
ПРИМЕР 6
PK/PD у макаков-крабоедов - исследование № 20157276
Фармакокинетический и фармакодинамический профили P65_30кДа оценивали у макаков-крабоедов, ранее участвовавших в экспериментах, после введения однократной внутривенной дозы 0,3 мг/кг, при этом дозу рассчитывали, исходя из массы белкового компонента, не включая массу фрагмента PEG. Исследование проводили в Charles River Laboratories, Inc. (Рино, Невада), а анализ данных PK осуществляли в NW Solutions (Сиэтл, Вашингтон). Образцы крови собирали до введения дозы и в 15 моментов времени (через 0,5, 1, 2, 4, 8, 12, 24, 36, 48, 72, 120, 144, 168, 192 и 240 ч. после введения дозы). Как плазму крови, так и клетки крови собирали для PK- и PD-анализов. Выбранные моменты времени использовали для анализа PK, PD, популяции клеток и гематологического анализа.
Все образцы плазмы крови анализировали в отношении IL-2 человека (PK-показатели) с использованием коммерчески доступных наборов для ELISA.
В таблице 10 показаны PK-параметры P65_30кДа у макака-крабоеда.
После введения однократной IV болюсной дозы Tmax наблюдалась через 0,5 ч. после введения дозы (первый момент времени измерения после введения дозы), а средние концентрации в плазме крови поддавались измерению в течение до 168 ч. после введения дозы (последнее измерение). t1/2 и AUC для P65_30кДа составляли 13,6 ч. и 121000 ч.*нг/мл соответственно.
Гематологические параметры у макаков-крабоедов - исследование № 20157276
Для гематологических параметров моменты времени оценивания соответствуют дню -1 до введения дозы и дням 1, 3, 6, 8, 10, 12, 14, 17, 19, 21 после введения дозы.
ПРИМЕР 7
Определение профиля иммунного ответа ex vivo для иллюстративных соединений IL-2 в образцах РВМС, полученных из системы удаления первичных лейкоцитов человека (LRS)
Для определения того, как разная рецепторная специфичность иллюстративных соединений IL-2 влияет на активацию субпопуляций первичных иммунных клеток, осуществляли определение профиля зависимости "концентрация-ответ" для активации лимфоцитов в образцах мононуклеарных клеток периферической крови (PBMC) человека, полученных из LRS, с помощью многоцветной проточной цитометрии. Конъюгаты из таблицы 12 синтезировали с помощью модификации SEQ ID NO: 1. Эти исследования осуществляли в PrimityBio LLC (Фримонт, Калифорния). Первичные лимфоциты, полученные из образцов LRS человека, обрабатывали серией разведений иллюстративных соединений IL-2 и определяли количественно на основании передачи сигнала, опосредованной pSTAT5, в каждом типе лимфоцитарных клеток с использованием панели, показанной в таблице 11.
Данные проточной цитометрии анализировали в отношении активации различных субпопуляций Т- и NK-клеток в режиме зависимости "концентрация-ответ", считывая накопление pSTAT5 после обработки с помощью иллюстративного варианта IL-2 K9_30кДа.
В таблице 12 показана EC50 зависимости доза-ответ для передачи сигнала, опосредованной pSTAT5 (EC50), в образцах из LRS человека или для пролиферации CTTL-2 при обработке указанным вариантом IL-2.
Treg
*Изменение активности в Treg по сравнению с нативным IL-2 (IL-2 дикого типа) анализировали в каждом отдельном эксперименте.
Значения EC50 (пг/мл) рассчитывали по кривым зависимости доза-ответ, полученным из графиков MFI.
ПРИМЕР 8
PK-исследование на мышах C57BL/6
Подробности эксперимента обобщенно представлены в таблице 13, при этом дозу рассчитывали, исходя из массы белкового компонента, не включая массу фрагмента PEG.
Оценивали фармакокинетические свойства иллюстративного пегилированного соединения IL-2 K35_30кДа при двух уровнях дозы. Лиофилизированный тестируемый препарат восстанавливали в PBS, и девяти самцам мышей C57BL/6 вводили дозы 0,3 и 3 мг/кг посредством внутривенной инъекции в хвостовую вену для каждой дозовой группы (см. подробности сбора ниже). Образцы крови собирали через 0,08, 0,25, 0,5, 1, 2, 4, 8, 12 и 24 ч. после введения дозы. Набор для ELISA hIL-2 от Abcam (ab100566), который не характеризуется перекрестной реактивностью с нативным IL-2 мыши, использовали для выявления и количественной оценки тестируемых препаратов. Для введения поправки на специфичные для ELISA различия в чувствительности выявления нативных и пегилированных соединений с помощью данного набора строили калибровочные кривые нативного IL-2 и исследуемого препарата K35_30кДа с использованием буфера для разбавления тестируемого препарата, при этом данные анализировали относительно соответствующих калибровочных кривых. Представленные на графике данные представляют среднее значение и SEM для трех отдельных образцов (биологических повторностей), описанных выше, а PK-параметры для тестируемых препаратов K35_30кДа были извлечены и обобщенно представлены в таблице 14.
ПРИМЕР 9
Определение характеристик связывания с IL-2R-альфа и IL-2R-бета человека
Исследование выполняли для определения характеристик связывания иллюстративного конъюгата IL-2 IL-2_P65[AzK_L1_PEG30кДа]-1 с IL-2R-альфа и IL-2R-бета человека. Соединение IL-2_P65[AzK_L1_PEG30кДа]-1 было таким, как описано ранее, и содержало SEQ ID NO: 50, в которой пролин в положении 64 заменен на AzK_L1_PEG30кДа, где AzK_L1_PEG30кДа определен как структура формулы (IV) или формулы (V) или смесь формулы (IV) и формулы (V) и линейная цепь mPEG массой 30 кДа. Соединение IL-2_P65[AzK_L1_PEG30кДа]-1 также определено как соединение, содержащее SEQ ID NO: 3, в которой остаток пролина в положении 64 (P64) заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX), и при этом n представляет собой такое целое число, что молекулярная масса группы PEG составляет приблизительно 30 кДа. Соединение IL-2_P65[AzK_L1_PEG30кДа]-1 также определено как соединение, содержащее SEQ ID NO: 3, в которой остаток пролина в положении 64 (P64) заменен структурой формулы (XII) или формулы (XIII) или смесью формулы (XII) и формулы (XIII), и при этом n представляет собой такое целое число, что молекулярная масса группы PEG составляет приблизительно 30 кДа.
Соединение получали посредством способов, аналогичных тем, которые раскрыты в примере 2, где вначале получали белок, имеющий SEQ ID NO: 3, в которой пролин в положении 64 был заменен на N6-((2-азидоэтокси)-карбонил)-L-лизин AzK (SEQ ID NO: 35). Затем проводили реакцию AzK-содержащего белка в условиях клик-химии с DBCO, содержащим линейную группу метокси-PEG, имеющую среднюю молекулярную массу 30 кДа. Вкратце, IL-2, используемый для биоконъюгации, экспрессировали в виде телец включения в E. coli посредством способов, раскрытых в данном документе, с использованием (a) экспрессионной плазмиды, кодирующей (i) белок с желаемой аминокислотной последовательностью, ген которого содержит первую неприродную пару оснований для обеспечения наличия кодона в желаемом положении, в которое встраивали неприродную аминокислоту N6-((2-азидоэтокси)-карбонил)-L-лизин (AzK), и (ii) тРНК, полученную из Pyl M. mazei, ген которой содержит второй неприродный нуклеотид для обеспечения наличия соответствующего антикодона вместо своей нативной последовательности; (b) плазмиды, кодирующей пирролизил-тРНК-синтетазу, полученную из M. barkeri (MbPylRS), (c) AzK и (d) усеченного варианта переносчика нуклеотидтрифосфатов PtNTT2, в котором первые 65 аминокислотных остатков полноразмерного белка были удалены. Двухнитевой олигонуклеотид, который кодирует аминокислотную последовательность варианта IL-2, содержал кодон AXC в качестве кодона 64 в последовательности, которая кодирует белок, имеющий SEQ ID NO: 3, в которой P64 заменен на неприродную аминокислоту, описанную в данном документе. Плазмида, кодирующая ген ортогональной тРНК из M. mazei, содержала антикодон GYT, соответствующий AXC, вместо своей нативной последовательности, где Y представляет собой неприродный нуклеотид, раскрытый в данном документе. X и Y выбраны из неприродных нуклеотидов dTPT3 и dNaM, раскрытых в данном документе. Экспрессируемый белок экстрагировали из телец включения и подвергали рефолдингу с использованием стандартных процедур перед сайт-специфическим пегилированием AzK-содержащего продукта IL-2 с помощью DBCO-опосредованной клик-химии без использования меди для стабильного ковалентного присоединения фрагментов mPEG (линейной группы метокси-PEG, имеющей среднюю молекулярную массу 30 кДа) к AzK (как представлено на схеме S6 выше).
Образцы тестируемого препарата, связывающиеся с IL-2R-альфа. Образцы тестируемого препарата в растворе тестировали в отношении связывания с поверхностями с рецептором IL-2R-альфа. Данные об ответе обрабатывали путем вычитания сигналов от эталонной поверхности без рецептора, а также среднего значения для введений буфера с использованием Scrubber-2 (BioLogic Software Pty Ltd). Ответы на серию концентраций rhIL-2 глобально аппроксимировали моделью взаимодействия 1:1 с включением стадии массопереноса. Сводная информация о константах связывания представлена в таблице 15.
Захват Fc-меченного IL-2R-бета на сенсорном чипе CM4, покрытом белком. Сенсорный чип CM4 вставляли в оптический биосенсор Biacore 4000, и инструмент трижды подвергали первоначальной обработке рабочим буфером HBS-P (HBS-P представляет собой 1X HBS-N с добавлением 0,005% Tween-20). Сочетание с белком A проводили с использованием стандартных условий сочетания с NHS/EDC. IL-2R-бета-Fc растворяли в воде до концентрации 0,1 мг/мл, а затем разбавляли 1/1000 рабочим буфером HBS-P. IL-2R-бета-Fc вводили в течение разных периодов времени для создания 2 поверхностей с разной плотностью рецепторов (~ 750 RU и 1500 RU, данные не показаны).
Определение характеристик образцов, связывающихся с IL-2R-бета. Образцы тестируемого препарата в растворе тестировали в отношении связывания с поверхностями с рецептором IL-2R-бета. Данные об ответе обрабатывали путем вычитания сигналов от эталонной поверхности без рецептора, а также среднего значения для введений буфера с использованием Scrubber-2 (BioLogic Software Pty Ltd). Ответы на образцы rhIL-2 (2-кратные разведения наивысшей концентрации 4 мкМ) и IL-2_P65[AzK_L1_PEG30кДа]-1 (2-кратные разведения наивысшей концентрации 8 мкМ), тестируемые в двух повторностях, глобально аппроксимировали моделью взаимодействия 1:1 с включением стадии массопереноса. Сводная информация о константах связывания представлена в таблице 15.
Результаты. His-меченный IL-2R-альфа захватывали при различных плотностях на сенсорном чипе с NTA, нагруженной никелем, в биосенсорной системе Biacore SPR. Fc-меченный IL-2R-бета захватывали при различных плотностях на сенсорном чипе CM4, покрытом белком А. Данные об ответе аппроксимировали моделью взаимодействия 1:1 для определения констант связывания для каждого взаимодействия. Рекомбинантный IL-2 человека (rhIL-2) связывался с IL-2R альфа с аффинностью ~ 11 нМ, тогда как связывание образцов IL-2_P65[AzK_L1_PEG30кДа]-1 с IL-2R-альфа было невозможно выявить. RhIL-2 связывался с IL-2R-бета с аффинностью ~ 700 нМ, а IL-2_P65[AzK_L1_PEG30кДа]-1 связывался с IL-2R-бета с аффинностью ~ 3 мкМ при данных условиях тестирования.
ПРИМЕР 10
Проводили исследование для определения активности и дифференциальной специфичности для типа клеток у IL-2_P65[AzK_L1_PEG30кДа]-1 в сравнении с рекомбинантным интерлейкином-2 человека (hIL-2) в отношении активности передачи сигнала, опосредованной фосфорилированной формой фактора транскрипции STAT5 (pSTAT5), в типах первичных иммунных клеток человека. Соединение IL-2_P65[AzK_L1_PEG30кДа]-1 было таким, как описано ранее, и содержало SEQ ID NO: 50, в которой пролин в положении 64 заменен на AzK_L1_PEG30кДа, где AzK_L1_PEG30кДа определен как структура формулы (IV) или формулы (V) или смесь формулы (IV) и формулы (V) и линейная цепь mPEG массой 30 кДа. Соединение IL-2_P65[AzK_L1_PEG30кДа]-1 также определено как соединение, содержащее SEQ ID NO: 3, в которой остаток пролина в положении 64 (P64) заменен структурой формулы (VIII) или формулы (IX) или смесью формулы (VIII) и формулы (IX), и при этом n представляет собой такое целое число, что молекулярная масса группы PEG составляет приблизительно 30 кДа. Соединение IL-2_P65[AzK_L1_PEG30кДа]-1 также определено как соединение, содержащее SEQ ID NO: 3, в которой остаток пролина в положении 64 (P64) заменен структурой формулы (XII) или формулы (XIII) или смесью формулы (XII) и формулы (XIII), и при этом n представляет собой такое целое число, что молекулярная масса группы PEG составляет приблизительно 30 кДа. Соединение получали посредством способов, аналогичных тем, которые раскрыты в примере 2, где вначале получали белок, имеющий SEQ ID NO: 3, в которой пролин в положении 64 был заменен на N6-((2-азидоэтокси)-карбонил)-L-лизин AzK (SEQ ID NO: 35). Затем проводили реакцию AzK-содержащего белка в условиях клик-химии с DBCO, содержащим линейную группу метокси-PEG, имеющую среднюю молекулярную массу 30 кДа.
Способы обработки образцов PBMC человека. Исходные растворы IL-2 (контроль, 1 мг/мл) и IL-2_P65[AzK_L1_PEG30кДа]-1 ("партия 1": 1,27 мг/мл; "партия 2": 2,29 мг/мл) хранили в виде исходных растворов, замороженных при -20°C.
Партию 1 и партию 2 соединений IL-2_P65[AzK_L1_PEG30кДа]-1 разбавляли в PBS, а IL-2 разбавляли с помощью PBS+0,1% BSA с получением 10X исходных растворов. Концентрация 10X исходного раствора IL-2 составляла 5 мкг/мл, а концентрация исходных растворов GLP-1 и GLP-2 составляла от 6 до 300 мкг/мл в зависимости от эксперимента. 10X исходные растворы разбавляли c последовательными 5-кратными разведениями для проведения подбора дозы по 10 точкам. Наивысшая доза IL-2 составляла 5 мкг/мл, а для исходных растворов партии 1 и партии 2 - от 6 до 300 мкг/мл в зависимости от эксперимента. 10 мкл каждого исходного раствора добавляли к 90 мкл образцов клеток для достижения конечной наивысшей дозы 500 нг/мл для IL-2 и от 0,6 до 30 мкг/мл для каждой из партии 1 и партии 2.
Стимуляция образцов. Для стимуляции 10 мкл представленной выше подобранной дозы добавляли к 90 мкл образца крови, предварительно уравновешенного до 37°C. Образцы инкубировали при 37°C в течение 45 минут. В конце периода инкубирования эритроциты лизировали, и клетки одновременно фиксировали следующим образом:
100 мкл клеток переносили в 900 мкл буфера BD для лизиса/фиксации (Beckton Dickinson, № по каталогу 558049) и сразу же перемешивали вихревым способом. BD для лизиса/фиксации получали путем разбавления исходного раствора 1:5 водой для культивирования клеток непосредственно перед добавлением. Образцы инкубировали в течение 10 минут при комнатной температуре, затем центрифугировали при 450 x g в течение 5 минут для осаждения клеток. Осажденные клетки промывали с помощью PBS+0,5% BSA и хранили при -37°C до анализа.
Протокол окрашивания
Стадия 1. Клетки размораживали при комнатной температуре. Стадия 2. Добавляли реагент для блокирования Fc-рецепторов (TruStain FcX™). Стадия 3. Инкубировали при комнатной температуре в течение 5 минут. Стадия 4. Добавляли следующие антитела из таблицы 16.
Стадия 5. Инкубировали в течение 20 минут при комнатной температуре. Стадия 6. Клетки промывали два раза с помощью PBS+0,5% BSA. Стадия 7. Клетки пермеабилизировали путем добавления 10 объемов метанола на один объем клеток. Стадия 8. Клетки инкубировали в течение 10 минут при 4°C. Стадия 9. Промывали с помощью PBS. Стадия 10. Клетки промывали с помощью PBS с 0,5% BSA. Стадия 11. Добавляли реагент для блокирования Fc-рецепторов (TruStain FcX™). Стадия 12. Добавляли следующую панель окрашивания после пермеабилизации из таблицы 17.
Проточная цитометрия и анализ данных. Образцы прогоняли на приборе Becton Dickinson Fortessa и LSR II с пятью лазерами (372 нМ, 405 нМ, 488 нМ, 561 нМ и 640 нМ). Приборы были оснащены 20 детекторами, предусматривающими параметры рассеяния. Инструменты регулярно калибровали с использованием гранул Becton Dickinson Cytometer Setup & Tracking. 96-луночные планшеты, содержащие окрашенные образцы, анализировали при менее чем 8000 клеток/секунда с использованием высокопроизводительного приспособления для отбора образцов из 96-луночных планшетов.
Данные экспортировали как файлы.fcs на сетевой диск и подвергали компенсации для учета избытка флуорофоров, а файлы.fcs аннотировали. Затем проводили гейтирование данных, содержащихся в файлах.fcs. Клетки вначале гейтировали по синглетам с использованием FSC-A по FSC-H, чтобы исключить любые агрегаты или дублеты. В данном гейте клетки гейтировали по прямому рассеянию от среднего до высокого (FSC-A) и боковому рассеянию (SSC-A), чтобы исключить эритроциты, дебрис и гранулоциты. Затем Т-клетки гейтировали как CD3+ CD56/16-отрицательную популяцию на 3-ей панели. NK-клетки идентифицировали как CD3-отрицательную популяцию с высоким уровнем CD56/16 на 3-ей панели. Затем Т-клетки разделяли на CD4+ Т-клетки и CD8+ Т-клетки. Затем Treg-клетки гейтировали из CD4+ Т-клеток как популяцию CD25hi x C127lo.
Статистические данные и построение графиков для выведения значений EC50. Медианную интенсивность флуоресценции (MFI) для каждого из популяции клеток, донора и обработки соединением рассчитывали по сигналу в канале, выявляющем фосфорилирование. Статистические данные анализировали с помощью Spotfire. В Spotfire данные наносили на логарифмическую шкалу для доз соединения и линейную шкалу для считываемых показателей MFI. Эти данные аппроксимировали с использованием 4-параметрического уравнения логистической регрессии. ЕС50 рассчитывали как точку перегиба кривой.
Результаты. Образцы IL-2 человека и IL-2_P65[AzK_L1_PEG30кДа]-1 разбавляли и тестировали в трех повторностях в отношении каждого из трех отдельных доноров, как описано выше. Расчетные значения полумаксимальной эффективной концентрации (ЕС50) указаны в таблице 19. Результаты демонстрируют, что IL-2_P65[AzK_L1_PEG30кДа]-1 является высокоактивным агонистом передачи сигнала от рецептора IL-2 в лимфоцитах человека. Как согласуется с предыдущими исследованиями связывания in vitro, которые показали, что IL-2_P65[AzK_L1_PEG30кДа]-1 специфично взаимодействует с субъединицей IL-2Rβ, а не с IL2Rα, он продемонстрировал специфичное снижение активности передачи сигнала в Treg-клетках, активность в которых зависит от взаимодействия с IL-2Rα, по сравнению с Teff- и NK-клетками, которые не характеризуются конститутивной экспрессией IL-2Rα на высоких уровнях.
Данные представляют собой среднее значение ± стандартная ошибка среднего (SEM), рассчитанное при тестировании образцов в трех повторностях от трех независимых доноров.
*IL-2_P65[AzK_L1_PEG30кДа]-1.
ПРИМЕР 11
Применение соединения A в комбинации с ингибитором контрольных точек при обработке мышей Balb/c, несущих опухоль из CT-26 Соединение IL-2_P65[AzK_PEG30кДа] (также называемое в данном документе "P65_30кДа", а в графических материалах - "соединение A") получали согласно способам, раскрытым в данном документе, вначале посредством получения белка, имеющего SEQ ID NO: 4, в которой пролин в положении 65 был заменен на N6-((2-азидоэтокси)-карбонил)-L-лизин (AzK) (SEQ ID NO: 10). Затем проводили реакцию AzK-содержащего белка в условиях клик-химии с DBCO, содержащим линейную группу метокси-PEG, имеющую среднюю молекулярную массу 30 кДа, с получением продукта, имеющего SEQ ID NO: 25, содержащего формулу (II), формулу (III) или смесь формулы (II) и формулы (III), где W представляет собой линейную группу метокси-PEG, имеющую среднюю молекулярную массу 30 кДа. Соединение также может быть определено как соединение, содержащее аминокислотную последовательность под SEQ ID NO: 4, в которой пролин в положении 65 (P65) заменен структурой формулы (VI) или формулы (VII) или смесью формулы (VI) и формулы (VII), и при этом n представляет собой такое целое число, что группа PEG имеет молекулярную массу, составляющую приблизительно 30 кДа. Соединение также может быть определено как соединение, содержащее аминокислотную последовательность под SEQ ID NO: 4, в которой пролин в положении 65 (P65) заменен структурой формулы (X) или формулы (XI) или смесью формулы (X) и формулы (XI), и при этом n представляет собой такое целое число, что группа PEG имеет молекулярную массу, составляющую приблизительно 30 кДа.
Исследования соединения А в качестве средства монотерапии и в комбинации с антителом к PD-1 проводили на самках мышей Balb/c. Для исследований 1 и 2 самок мышей Balb/c в возрасте 6-8 недель со средней массой от 16 г до 21 г приобретали у Jackson Laboratories (Сакраменто, Калифорния). Для исследования 3 самок мышей Balb/c в возрасте 7-8 недель со средней массой от 18 до 22 г приобретали для HD Biosciences у Taconic Biosciences. Криогенно консервированные флаконы с клетками рака ободочной кишки CT-26 приобретали в Американской коллекции тканевых культур (ATCC, Манассас, Вирджиния). Клетки размораживали и культивировали в соответствии с протоколом производителя. В день инокуляции опухолевых клеток клетки промывали в бессывороточной среде, подсчитывали и повторно суспендировали в холодной бессывороточной среде при концентрации 250000 (исследования 1 и 2) или 300000 (исследование 3) жизнеспособных клеток на 0,1 мл. Клетки CT-26 (0,1 мл) инъецировали подкожно в бока отдельных мышей, и обеспечивали рост опухолей.
В исследованиях 1 и 2, в которых применяли комбинацию соединения А и антитела к PD-1, применяемым антителом было антитело к PD-1 мыши (BioXCell; RMP1-14), а контрольным антителом было антитело изотипа IgG1 (BioXCell; № по каталогу BP0089, № партии 2A3). В исследовании 3, в котором применяли антитело к PD-1, применяемым антителом было антитело к PD-1 мыши (BioXCell; № по каталогу BP0146, RMP1-14, № партии 695318A1), а контрольным антителом было антитело изотипа IgG1 (BioXCell; № по каталогу BP0089, № партии 2A3).
Лиофилизированное соединение А восстанавливали в виде 10 мг/мл исходного раствора с помощью 0,1 М уксусной кислоты. Затем его дополнительно разбавляли до рабочей концентрации с помощью 1х забуференного фосфатом физиологического раствора (PBS). Соединение восстанавливали и разбавляли за час до введения дозы животным и выдерживали на льду до введения дозы. Лиофилизированное соединение хранили при -80°C до применения. Среду-носитель хранили при 4°C.
Осуществляли три отдельных исследования эффективности с использованием мышей Balb/c, несущих опухоль из CT-26. План исследования 1, в котором соединение А оценивали в отношении дозозависимой эффективности в качестве средства монотерапии, представлен в таблице 19. Планы исследований 2 и 3, в которых оценивали эффективность соединения А в комбинации с антителом к PD-1, представлены в таблице 20 и таблице 21 соответственно. Путь введения соединения А был внутривенным (IV). IV введение доз мышам осуществляли через хвостовую вену. Антитело вводили внутрибрюшинно (IP). Все средства вводили с учетом индивидуальной массы тела каждого животного, полученной непосредственно перед каждым введением дозы. Ниже описаны подробности режима введения доз.
IV=внутривенное; QWx3=один раз в неделю в общей сложности в количестве 3 доз; Q2Wx2=один раз в 2 недели в общей сложности в количестве 2 доз.
изотипический контроль IgG
BIWx3=два раза в неделю в течение 3 недель в общей сложности в количестве 6 доз; IP=внутрибрюшинное; IV=внутривенное; QWx3=один раз в неделю в общей сложности в количестве 3 доз.
изотипический
контроль IgG
антитело к PD-1
антитело к PD-1
антитело к PD-1
BIWx3=два раза в неделю в течение 3 недель в общей сложности в количестве 6 доз; IP=внутрибрюшинное; IV=внутривенное; QWx3=один раз в неделю в общей сложности в количестве 3 доз; Q2Wx2=один раз в 2 недели в общей сложности в количестве 2 доз.
В исследовании 1 мышей, несущих опухоль из CT-26, обрабатывали средой-носителем IV один раз в неделю в общей сложности в количестве 3 доз (QWx3) или соединением A при 0,3, 1 или 3 мг/кг IV один раз в неделю в общей сложности в количестве трех доз (QWx3) либо один раз в 2 недели в общей сложности в количестве 2 доз (Q2Wx2), начиная в день 4 после инокуляции опухолевых клеток, когда средний объем опухоли составлял ~ 80 мм3.
В исследовании 2 мышей, несущих опухоль из CT-26, обрабатывали в день 5 после инокуляции опухолевых клеток, когда средний объем опухоли составлял ~ 80 мм3. Осуществляли введение дозы среды-носителя IV QWx3+изотипического контроля IgG IP, или соединения A при 3 или 6 мг/кг IV по схеме введения доз QWx3, или антитела к PD-1 при 10 мг/кг IP, или комбинации соединения A при 6 мг/кг IV QWx3+антитела к PD-1 при 10 мг/кг IP. IP введение доз антитела во всех случаях осуществляли два раза в неделю в течение 3 недель в общей сложности в количестве 6 доз (BIWx3).
В исследовании 3 мышей, несущих опухоль из CT-26, обрабатывали в день 7 после инокуляции опухолевых клеток, когда средний объем опухоли составлял ~ 70 мм3. Осуществляли введение дозы среды-носителя IV QWx3+изотипического контроля IgG IP BIWx3; или соединения A при 1, 3, 6 или 9 мг/кг IV по схеме введения доз QWx3, или антитела к PD-1 при 10 мг/кг IP BIWx3; или комбинации соединения A при 1, 3 или 6 мг/кг IV QWx3+антитела к PD-1 при 10 мг/кг IP BIWx3.
Сводная информация обо всех трех исследованиях показана в таблице 22. Животных обследовали ежедневно в отношении клинических признаков. Согласно указаниям IACUC животных гуманно умерщвляли, когда опухоли вырастали до более 2000 мм3 в объеме, или наблюдалось продолжающееся ухудшение их состояния, или демонстрировались явные признаки сильного дистресса и/или боли.
Выживаемость каждой мыши отслеживали в течение более 100 дней, после чего выживших животных без опухолей в исследованиях 2 и 3 включали в продолжение исследования с повторной стимуляцией в течение двух циклов с интервалом в 2 месяца. В частности, животных без опухолей подвергали повторной стимуляции путем инокуляции того же типа опухолевых клеток (CT-26) в нижнюю часть противоположного бока. Контрольными животными были соответствующие по возрасту мыши, ранее не участвовавшие в экспериментах, которым параллельно инокулировали такое же количество опухолевых клеток CT-26 в нижнюю часть противоположного бока.
Рост опухоли отслеживали с помощью измерений цифровым штангенциркулем каждые 3-4 дня до конца исследования. Объем опухоли рассчитывали как ширина2 x длина/2, где ширина представляет собой наименьшее измерение, а длина представляет собой наибольшее измерение. Необработанные данные об объеме опухоли представлены в отчетах об исследовании.
Данные о среднем объеме опухоли для каждой группы откладывали на графике в зависимости от времени с планками стандартной ошибки среднего (SEM). Кроме того, индивидуальные данные об объеме опухоли за последний день перед умерщвлением животных откладывали на графике вместе со средним значением и планкой SEM для изучения распределения данных.
Статистический анализ данных об объеме опухоли за последний день до умерщвления животных осуществляли с использованием GraphPad Prism v.7.0. Данные анализировали в отношении значимости с использованием одностороннего ANOVA. Попарные сравнения проводили с использованием процедур критерия Тьюки (2-стороннего). Сообщали о p-значении для каждого отдельного сравнения.
Процент ингибирования роста опухоли (% TGI) в каждой группе обработки в сравнении с контрольной группой рассчитывали следующим образом:
[(контроль - контроль на исходном уровне) - (обработка - обработка на исходном уровне)]/(контроль - контроль на исходном уровне) x 100%.
Выживаемость каждой мыши регистрировали, и строили график Каплана-Мейера, чтобы показать выживаемость по группам обработки, и значимость оценивали с помощью логарифмического рангового критерия (Кокса-Мантеля). Выживаемость отслеживали в течение более 100 дней после начала обработки в исследованиях № 1, № 2 и № 3, а также на протяжении двух циклов повторной стимуляции у выживших мышей без опухолей в исследованиях № 2 и № 3. Анализы осуществляли с использованием GraphPad Prism версии 7.0.
[доза антителаa]
(мг/кг)
% TGI рассчитывали в день 15 (исследование 1) и день 17 (исследования 2 и 3).
Результаты представляют собой среднее значение ± SEM.
QWx3=один раз в неделю в общей сложности в количестве 3 доз; Q2Wx2=один раз в 2 недели в общей сложности в количестве 2 доз; TGI=ингибирование роста опухоли. * p < 0,05 в сравнении с контрольной средой-носителем; ** p < 0,05 в сравнении со средствами монотерапии (соединением A или антителом); *** p < 0,001 в сравнении со средой-носителем или антителом изотипического контроля; # p < 0,01 в сравнении с антителом изотипического контроля.
В исследовании 1 соединение А оценивали в отношении дозозависимой эффективности в качестве средства монотерапии у самок мышей Balb/c, несущих развившиеся подкожные опухоли ободочной кишки из CT-26. Исследование формально завершали в день 15 после начала обработки в соответствии с гуманной конечной точкой, установленной IACUC, когда некоторые опухоли в контрольной группе достигали объема более 2000 мм3. На фиг. 1 показано изменение среднего объема опухоли с течением времени для групп, получавших обработку путем введения доз QWx3 соединения А. На фиг. 2 показаны объемы опухоли в день 15 после обработки для каждого животного, получавшего обработку путем введения доз QWx3 соединения А. На фиг. 3 показано изменение среднего объема опухоли с течением времени для групп, получавших обработку путем введения доз Q2Wx2 соединения А. На фиг. 4 показаны объемы опухоли в день 15 после обработки для каждого животного, которому вводили дозы Q2Wx2 соединения А.
При схеме введения доз QWx3 соединение A демонстрировало дозозависимую противоопухолевую активность в режиме монотерапии, в результате чего % TGI по сравнению с контрольной средой-носителем составлял 31%, 19% и 52% для дозовых групп 0,3, 1 и 3 мг/кг соответственно. Аналогичным образом, при схеме введения доз Q2Wx2 соединение A демонстрировало дозозависимую противоопухолевую активность в режиме монотерапии, в результате чего % TGI по сравнению с контрольной средой-носителем составлял 20%, 27% и 45% для дозовых групп 0,3, 1 и 3 мг/кг соответственно. Однако при обеих схемах введения доз только для дозы 3 мг/кг наблюдалась статистическая значимость (p < 0,05) по сравнению с контрольной средой-носителем. Обе схемы введения доз демонстрировали сопоставимую противоопухолевую активность. Поэтому для последующих исследований в этой мышиной модели выбирали схему введения доз QWx3.
На фиг. 1, 3, 5 и 8 черные стрелки обозначают дни введения доз соединения A. Данные на фиг. 1 и 3 представляют собой кривые среднего роста опухоли при введении доз QWx3 и введении доз Q2Wx2 соединения A; черные стрелки обозначают дни введения доз соединения A. Данные на фиг. 2 и 4 представляют индивидуальный объем опухоли и средний объем опухоли ± стандартная ошибка среднего (SEM) (10 мышей/группа) в день 15 после обработки при введении доз QWx3 и Q2Wx2 соединения A. Данные представляют индивидуальные объемы опухоли; также показано среднее значение ± SEM и % TGI по сравнению с контрольной средой-носителем.
Данные на фиг. 3 представляют средний объем опухоли ± стандартная ошибка среднего (SEM) (10 мышей/группа) у животных при введении доз Q2Wx2 соединения A. Данные на фиг. 4 представляют данные об индивидуальном и среднем объеме опухоли в день 15 после обработки при введении доз Q2Wx2 соединения A. * p < 0,05 в сравнении с контрольной средой-носителем в день 15.
Проводили два отдельных исследования (исследования 2 и 3) на мышах, несущих опухоль ободочной кишки из CT-26, для оценивания соединения A в качестве средства монотерапии и в комбинации с антителом к PD-1 мыши, являющимся ингибитором контрольных точек. Диапазоны доз соединения А в этих исследованиях перекрывались, при этом в исследовании 3 диапазон доз был шире. В обоих исследованиях соединение А вводили QWx3, и антитело на том же уровне дозы вводили BIWx3.
В исследовании 2 оценивали противоопухолевую активность соединения A в качестве средства монотерапии при 3 и 6 мг/кг (QWx3) у самок мышей Balb/c, несущих развившиеся подкожные опухоли ободочной кишки из CT-26. Кроме того, оценивали противоопухолевую активность комбинации при IV введении доз соединения A при 6 мг/кг (QWx3) и антитела к PD-1 при 10 мг/кг IP (BIWx3). % TGI рассчитывали в день 15 после начала обработки, поскольку некоторые опухоли в группе, получавшей контрольную среду-носитель, достигали объема более 2000 мм3. Тем не менее, за животными в группах обработки, которые демонстрировали полную регрессию опухоли, следили путем измерений опухоли с частотой один или два раза в неделю.
Соединение A демонстрировало противоопухолевую активность в режиме монотерапии, в результате чего % TGI по сравнению с контрольной средой-носителем составлял 56,3% и 35,6% для дозовых групп 3 и 6 мг/кг соответственно. В исследовании комбинации мышей, несущих опухоль из CT-26, обрабатывали IV соединением A при 6 мг/кг QWx3, или IP антителом к PD-1 BIWx3, или комбинацией по тем же схемам введения доз, начиная через 5 дней после инокуляции опухолевых клеток, когда средний объем опухоли составлял ~ 80 мм3. На фиг. 5 показаны кривые среднего роста опухоли при обработке мышей с помощью среды-носителя, 6 мг/кг соединения A в качестве средства монотерапии, антитела к PD-1 в качестве средства монотерапии и комбинации 6 мг/кг соединения A и антитела к PD-1. Данные на фиг. 5 представляют средний объем опухоли ± SEM (14 мышей/группа). Верхние стрелки обозначают дни введения доз соединения А, а нижние стрелки обозначают дни введения доз антитела к PD-1. Противоопухолевая активность комбинации была значимо повышенной по сравнению с соединением А или антителом к PD-1 в отдельности (p < 0,05). Данные о % TGI показаны на фиг. 6 и демонстрируют значительные противоопухолевые эффекты в день 15 после обработки в группе, получавшей обработку с помощью комбинации соединения А и антитела к PD-1, по сравнению с группами, получавшими обработку с помощью среды-носителя, соединения A в отдельности или антитела к PD-1 в отдельности (35,6% для группы, получавшей соединение A в отдельности; 44,1% для группы, получавшей антитело к PD-1 в отдельности; и 74,6% для группы, которой вводили комбинацию соединения A и антитела к PD-1). Данные представляют индивидуальные объемы опухоли; также показано среднее значение ± SEM и % TGI по сравнению с контрольной средой-носителем. *p < 0,05, **p < 0,01 и ***p < 0,01; в сравнении с контрольной средой-носителем. ┴p < 0,05 в сравнении с антителом к PD-1. #p < 0,05 в сравнении с соединением A. Медианные значения продолжительности выживания в группах показаны на фиг. 7 и составляли 17, 27, 27,5 и 38 дней для групп, получавших контроль, соединение A, антитело к PD-1 и соединение A+антитело к PD-1 соответственно. Медианная продолжительность выживания в группе, получавшей комбинацию, была значимо большей, чем в группах, получавших обработку с помощью как соединения A (p < 0,05), так и антитела к PD-1 (p < 0,05) в качестве средств монотерапии. Через 98 дней после обработки в каждой из дозовых групп, получавших соединение A и антитело к PD-1, выживало без опухоли только 1 из 14 животных (7%), тогда как в группе, получавшей комбинацию, выживали без опухолей 4 из 14 животных (29%). Данные на фиг. 7 представляют кривые выживаемости Каплана-Мейера для групп обработки. *p < 0,05 в сравнении с контрольной средой-носителем. ┴p < 0,05 в сравнении с антителом к PD-1. #p < 0,05 в сравнении с соединением A.
В исследовании 3 противоопухолевую активность соединения А в качестве средства монотерапии оценивали на самках мышей Balb/c, несущих SC опухоли ободочной кишки из CT-26, в более широком диапазоне доз (1, 3, 6 и 9 мг/кг) по сравнению с исследованием 2 при той же схеме IV введения доз QWx3. Данные на фиг. 8 представляют кривые среднего роста опухоли при введении доз соединения A в качестве средства монотерапии при 1 мг/кг, 3 мг/кг, 6 мг/кг и 9 мг/кг. Данные представляют средний объем опухоли ± SEM (14 мышей/группа; за исключением 12 мышей/группа для 9 мг/кг соединения A). Черные стрелки обозначают дни введения доз соединения A. Соединение A, дозы которого вводили в отдельности при 1 мг/кг, 3 мг/кг, 6 мг/кг и 9 мг/кг, также демонстрировало дозозависимую противоопухолевую активность, в результате чего % TGI по сравнению с контрольной средой-носителем составлял 29,8%, 58,8%, 86,2% и 84,8% для дозовых групп 1, 3, 6 и 9 мг/кг соответственно (фиг. 9). % TGI рассчитывали в день 15 после начала обработки, поскольку некоторые опухоли в группе, получавшей контрольную среду-носитель, достигали более 2000 мм3. Тем не менее, за животными в группах обработки, которые демонстрировали полную регрессию опухоли, следили путем измерений опухоли с частотой один или два раза в неделю. Данные на фиг. 9 представляют индивидуальные объемы опухоли в день 15 после обработки. Данные представляют индивидуальные объемы опухоли; также показано среднее значение ± SEM и % TGI по сравнению с контрольной средой-носителем. ***p < 0,01 в сравнении с контрольной средой-носителем. Наиболее низкая доза (1 мг/кг) не демонстрировала статистически значимую противоопухолевую активность, тогда как в остальных 3 дозовых группах наблюдалась статистическая значимость (p < 0,001) по сравнению с группой, получавшей обработку средой-носителем. Данные также показывали, что % TGI у двух групп, получавших высокую дозу (6 мг/кг и 9 мг/кг), были сходными, что указывает на то, что максимальная противоопухолевая активность достигалась при дозе 6 мг/кг. В дозовой группе 9 мг/кг 2 из 14 животных были обнаружены мертвыми после потери > 15% массы тела в результате обработки.
В фазе исследования комбинации соединение A вводили в дозе 1, 3 или 6 мг/кг (QWx3) с антителом к PD-1 при 10 мг/кг IP (BIWx3). Мышей, несущих опухоль из CT-26, обрабатывали IV соединением A при 1, 3, 6 или 9 мг/кг QWx3, или IP антителом к PD-1 BIWx3, или комбинацией по тем же схемам введения доз, начиная через 7 дней после инокуляции опухолевых клеток, когда средний объем опухоли составлял ~ 70 мм3. Следует отметить, что в группе, получавшей 9 мг/кг соединения A в качестве средства монотерапии, двух животных обнаружили мертвыми после потери > 15% массы тела, и их не включали в анализ. При использовании комбинации 1 мг/кг соединения A+антитело к PD-1 не наблюдалась аддитивная противоопухолевая активность, исходя из данных о выживаемости. Через несколько дней после обработки с помощью соединения А в группе, получавшей антитело к PD-1, выживало 1 из 14 животных (7%), тогда как в группе, получавшей 3 мг/кг средства монотерапии, выживало 0 животных. Однако в группе, получавшей 3 мг/кг соединения A+антитело к PD-1, выживало 2 из 14 животных (14%) до дней получения соединения A. Как показано на фиг. 10, комбинация 6 мг/кг соединения А+антитело к PD-1 приводила к продлению выживаемости по сравнению с каждым средством монотерапии в отдельности. Медианные значения продолжительности выживания составляли 21, 35, 24,5 и 49 дней для групп, получавших контрольную среду-носитель, соединение A (6 мг/кг), антитело к PD-1 (10 мг/кг) и соединение A+антитело к PD-1 (6 мг/кг соединения A и 10 мг/кг антитела к PD-1) соответственно. Медианная продолжительность выживания в группе, получавшей комбинацию, была значимо большей, чем в группах, получавших обработку с помощью соединения A и антитела к PD-1 (p < 0,05) в качестве средств монотерапии. В частности, через несколько дней после обработки с помощью соединения А в группе, получавшей 6 мг/кг соединения A, выживало 0 животных, тогда как в группе, получавшей антитело к PD-1, выживало без опухоли только 1 из 14 животных (7%). Однако в группе, получавшей комбинацию, выживали без опухолей 5 из 14 (36%) животных (p < 0,05). Данные на фиг. 10 представляют кривые выживаемости Каплана-Мейера для групп обработки. *p < 0,05 в сравнении с контрольной средой-носителем. ┴p < 0,05 в сравнении с антителом к PD-1. #p < 0,05 в сравнении с соединением A.
ПРИМЕР 12
Анализ высвобождения цитокинов из цельной крови
Образцы цельной крови человека от 6 здоровых доноров инкубировали с серией титров IL-2_P65[AzK_L1_PEG30кДа]-1 (соединения B) или IL-2 в отдельности или в комбинации с PEM ("Pembro" или пембролизумабом) или NIVO (ниволумабом) в течение 24 ч. Цитокины, высвободившиеся из цельной крови после обработки в надосадочную жидкость, измеряли с использованием набора U-PLEX Meso Scale Discovery (MSD) для шести аналитов (IFN-γ, IL-4, IL-5, IL-6, IL-8, TNF-α).
Протокол
Кровь в пробирках с гепарином от 6 здоровых доноров получали из службы донорской крови Научно-исследовательского института Скриппс (TSRI; Сан-Диего, Калифорния). Образцы тестировали в день сбора; от доноров 1-3 в один день, а от доноров 4-6 - на другой день.
Цельную кровь человека инкубировали с различными концентрациями IL-2_P65[AzK_L1_PEG30кДа]-1, а также 90 мкг/мл пембролизумаба или 127 мкг/мл ниволумаба (ожидаемыми значениями Cmax клинической дозы).
Цельную кровь вначале разбавляли в 2 раза средой RPMI 1640. Объем 180 мкл предварительно разбавленной цельной крови высевали в 96-луночный планшет для культуры тканей. Затем в аналитический планшет добавляли 20 мкл соединений в 10х конечной тестируемой концентрации. Условия тестирования включали серийное титрование IL-2_P65[AzK_L1_PEG30кДа]-1 (4,5 мкг/мл, 1,5 мкг/мл, 0,8 мкг/мл, 0,45 мкг/мл и 0,2 мкг/мл) или IL-2 (0,8 мкг/мл, 0,45 мкг/мл, 0,2 мкг/мл, 0,1 мкг/мл и 0,03 мкг/мл) и серийное титрование IL-2_P65[AzK_L1_PEG30кДа]-1 либо IL-2 в комбинации с 90 мкг/мл PEM или 127 мкг/мл NIVO. Кроме того, включали положительные и отрицательные контроли для демонстрации чувствительности и специфичности анализа: 100 мкг/мл предварительно покрывающего антитела мыши Ultra LEAF к CD3 человека использовали в качестве положительных контролей для анализа. 50 мкг/мл предварительно покрывающего IgG1 мыши Ultra LEAF изотипа κ представляет собой изотипический контроль для упомянутого выше антитела к CD3 человека. Буфер для составления IL-2_P65[AzK_L1_PEG30кДа]-1 в отдельности был отрицательным контролем для анализа. Отсутствие обработки также служило отрицательным контролем для анализа.
После добавления соединения(соединений) в лунку кровь инкубировали при 37°C. После центрифугирования образцов надосадочную жидкость собирали через 24 ч. после обработки и хранили при -80°C до анализа. Цитокины человека (IFN-γ, TNF-α, IL-8, IL-6, IL-5, IL-4), высвободившиеся в анализе, определяли количественно с помощью набора U-PLEX MSD. Нижний предел выявления для анализа указан в приведенной ниже таблице. Предел выявления каждого планшета сообщается в программном обеспечении MSD Discovery Workbench. Предел выявления немного отличается для каждого планшета.
Материалы
Результаты
L-2_P65[AzK_L1_PEG30кДа]-1 и IL-2 индуцировали дозозависимую индукцию IFN-γ при 24-часовой обработке, но не индуцировали значительного высвобождения других 5 цитокинов (IL4, IL5, IL8, TNFa, IL6), тестируемых в данном анализе. В комбинации с Pem либо с Nivo как IL-2_P65[AzK_L1_PEG30кДа]-1, так и IL-2 (R&D) не вызывали значительного изменения профиля цитокинов (IFN-γ, IL-4, IL-5, IL-8, TNF-α, IL-6), тестируемых в данном исследовании. Данные по отдельным донорам указаны в таблицах 24-32. Иллюстративные графики для одного донора показаны на фиг. 11A-11B.
BDL=ниже предела выявления.
мкг/мл
BDL=ниже предела выявления.
мкг/мл
(культуральная среда)
контроль IgG4
BDL=ниже предела выявления.
Данные по каждому донору (например, D1-D6) нормализовали относительно его конкретного значения с буфером для составления. ND=не определено.
Данные по каждому донору (например, D1-D6) нормализовали относительно его конкретного значения с буфером для составления.
BDL=ниже предела выявления.
(мкг/
мл)
"Соединение B" представляет собой IL-2_P65[AzK_L1_PEG30кДа]-1. Данные по каждому донору (например, D1-D6) нормализовали относительно его конкретного значения с буфером для составления. BDL=ниже предела выявления.
(мкг/мл)
"Соединение B" представляет собой IL-2_P65[AzK_L1_PEG30кДа]-1. Данные по каждому донору (например, D1-D6) нормализовали относительно его конкретного значения с буфером для составления.
(мкг/мл)
"Соединение B" представляет собой IL-2_P65[AzK_L1_PEG30кДа]-1. BDL=ниже предела выявления.
ПРИМЕР 13
Анализ реакции смешанной культуры аллогенных лимфоцитов человека (MLR)
Анализ реакции смешанной культуры аллогенных лимфоцитов человека (MLR) применяли для оценивания способности соединения B (IL-2_P65[AzK_L1_PEG30кДа]-1) усиливать активацию TCR в качестве средства монотерапии и в комбинации с ингибитором контрольных точек (ниволумабом или пембролизумабом) в качестве модели цитолитического ответа на опухолевые клетки, презентирующие специфические антигены или неоантигены.
Для каждого прогона анализа использовали мононуклеарные клетки периферической крови (МНК) от двух нормальных здоровых доноров. Моноцитарные DC создавали путем культивирования моноцитов, выделенных из PBMC с использованием набора для отрицательного отбора моноцитов (StemCell), in vitro в течение 7 дней, что предусматривало добавление 1500 МЕ/мл IL-4 и 1500 МЕ/мл GM-CSF. Культуральную среду заменяли в дни 3 и 5. Моноцитарные DC собирали в день 7. В этот день CD4+ T-клетки выделяли у другого донора с помощью набора для отрицательного отбора (StemCell). CD4+ Т-клетки (1×105) и аллогенные моноцитарные DC (1×104) совместно культивировали в 96-луночных титрационных микропланшетах в присутствии диапазона концентраций соединения B (0,005-100 мкг/мл) в отдельности или с 5, 50 или 500 нг/мл ниволумаба, пембролизумаба или изотипического контроля IgG. Каждый прогон организовывали в 3 повторностях для каждого условия обработки. Через 5 дней совместного культивирования секрецию IFN-γ в надосадочных жидкостях культуры анализировали с использованием набора для твердофазного иммуноферментного анализа (ELISA) (Abcam; № по каталогу Ab46025). Уровни IFN-γ после воздействия комбинации соединения B и пембролизумаба показаны на фиг. 12. Уровни IFN-γ после воздействия комбинации соединения B и ниволумаба показаны на фиг. 13 и 14. Для получения данных, показанных на фиг. 13, применяли клинический чистый ниволумаб, а для получения данных, показанных на фиг. 14, применяли ниволумаб, чистый для исследований (SelleckChem). Результаты демонстрировали, что соединение B, ниволумаб и пембролизумаб, применяемые в качестве средств монотерапии, индуцировали высвобождение IFN-γ зависимым от концентрации образом. Удивительно, но комбинация (a) соединения B и ниволумаба и (b) соединения B и пембролизумаба демонстрировала синергический эффект в анализе MLR. Данные, показанные на фиг. 12, 13 и 14, представляют среднее значение для 3 повторностей ± стандартная ошибка среднего от одной пары доноров.
ПРИМЕР 14
Соединение B индуцирует экспрессию Ki67 в CD8+ T-, NK- и Treg-клетках, но приводит к размножению только CD8+ T- и NK-клеток, но не Treg, в периферической крови и в опухолях из CT-26
Для оценивания фармакокинетических (PK) и фармакодинамических (PD) свойств соединения В самкам мышей Balb/c (в возрасте 6-8 недель, со средней массой 16-22 г, Jackson Laboratories или Taconic Biosciences) подкожно в область бока инокулировали опухолевые клетки CT-26 (ATCC). Рост опухоли отслеживали путем измерения опухолей три раза в неделю. Когда объемы опухолей достигали примерно 150 мм3, мышей рандомизировали в контрольную группу и группу обработки. После IV введения однократной дозы 3 мг/кг соединения B мышам, несущим опухоль из CT-26, образцы терминальной крови и опухоли собирали в день 0 (через 2 ч., 8 ч. и 12 ч.), день 1 (N=3 мыши в каждый момент времени), дни 2, 3, 5, 7, 10 и через 12 дней после введения дозы (N=4 мыши в каждый момент времени). Образцы плазмы крови и опухоли анализировали в отношении соединения B с помощью анализа ELISA.
Фармакокинетический анализ
Опухоль разделяли на две половины, и одну половину взвешивали и замораживали в жидком азоте для PK-анализа опухоли. Замороженные образцы опухоли гомогенизировали с помощью буфера для лизиса (1 таблетка ингибитора протеаз (SIGMA, № по каталогу 4693159001) в 10 мл 1x PBS). Каждые 0,1 г ткани смешивали с 0,4 мл буфера для лизиса. В каждую пробирку для сбора тканей добавляли гранулу из нержавеющей стали размером 5 мм (Qiagen, № по каталогу 69989) перед гомогенизацией с помощью TissueLyser II (Qiagen) при 20 Гц в течение 20 секунд. После гомогенизации лизат опухоли осаждали путем центрифугирования, а надосадочную жидкость собирали для PK-анализа соединения B.
Как показано на фиг. 15, воздействие соединения B на опухоль составляло примерно 4% от воздействия на плазму крови (AUC0-t 429000 и 15900 ч.•нг/мл для плазмы крови и опухоли соответственно). t1/2 в опухоли почти в два раза превышал t1/2 в плазме крови (19,9 ч. и 9,8 ч. в опухоли и плазме крови соответственно), что указывает на то, что соединение B распределяется в опухоли и сохраняется там на протяжении более длительного времени по сравнению с компартментом крови.
Фармакодинамический анализ
Проточная цитометрия. Для фенотипирования иммунных клеток цельной крови образцы крови лизировали и фиксировали сразу после сбора терминальной крови. Вкратце, образцы крови обрабатывали 20 объемами предварительно нагретого 1x буфера для лизиса/фиксации (BD Phosflow™, № по каталогу 558049) в соответствии с протоколом производителя. Перед окрашиванием антителами суспензии клеток блокировали реагентом для блокирования Fc-рецепторов (антителом к CD16/32 TruStain FcX, BioLegend). После блокирования клетки вначале окрашивали на следующие маркеры клеточной поверхности: антителом к CD3 мыши, конъюгированным с Ax488 (17A2), антителом к CD4 мыши, конъюгированным с Bv786 (RM4-5), антителом к CD8а мыши, конъюгированным с Bv711 (53-6.7), антителом к CD49b мыши, конъюгированным с Bv421 (DX5), биотинилированным антителом к CD25 мыши (REA568), антителом к CD335 мыши, конъюгированным с Bv605 (29A1.4). Затем клетки пермеабилизировали предварительно охлажденным до 4°C метанолом (Fisher Chemical, A412-4) и подвергали внутриклеточному окрашиванию антителом к FoxP3 мыши, конъюгированным с РЕ (FJK-16s), антителом к Ki67, конъюгированным с PerCP-eFluor710, и антителом к Pstat5, конъюгированным с Ax647 (Py694), а также антителом к CD44, конъюгированным с PEcy7 (IM7), и конъюгатом BUV395-стрептавидин для биотина. Образцы прочитывали с использованием BD LSRFortessa, при этом анализ проводили с помощью программного обеспечения FlowJo.
CD8 клетки идентифицировали как CD3+CD8a+. Treg-клетки идентифицировали как CD3+CD4+CD25+FoxP3+. Естественные клетки-киллеры гейтировали по CD3-CD335+CD49b+. CD8 клетки памяти оценивали как CD3+CD8+CD44hi.
FACS опухоли. Суспензию отдельных клеток образцов мышиных опухолей получали путем измельчения опухолей до небольших фрагментов и расщепления с помощью набора для диссоциации мышиных опухолей MACS (Miltenyi, 130-096-730) в соответствии с протоколом производителя. Живые клетки идентифицировали с помощью фиксируемого красителя для определения жизнеспособности eFluor 780 (eBioscience, 65-0865-14). Суспензию клеток блокировали антителом к CD16/32 мыши (TruStain FcX, BioLegend, № по кат. 101319), после чего проводили окрашивание на маркеры клеточной поверхности. Затем клетки фиксировали и пермеабилизировали с помощью реагента для фиксации/пермеабилизации и окрашивания FoxP3/факторов транскрипции (eBioscience, № по кат. 00-5521-00), а затем окрашивали на внутриклеточные маркеры. Антитела, применяемые для поверхностных антигенов, представляли собой антитело к CD45 мыши, конъюгированное с PEcy7 (30-F11), антитело к CD3e мыши, конъюгированное с BUV395 (17A2), антитело к CD4 мыши, конъюгированное с BV510 (GK1.5), антитело к CD8a, конъюгированное с PE-eF610 (53-6.7), антитело к CD335 мыши, конъюгированное с BV605 (29A1.4), антитело к CD25 мыши, конъюгированное с AF700 (PC61), антитело к CD49b мыши, конъюгированное с APC (DX5). Антитела для внутриклеточных антигенов представляли собой антитело к FoxP3, конъюгированное с PE (FJK-16s), и антитело к Ki67, конъюгированное с AF488 (11F6). Популяцию CD8 клеток идентифицировали как CD3+CD8+, а популяцию NK-клеток определяли как CD3-CD335+CD49b+. Treg-клетки гейтировали по CD3+CD4+CD25+FoxP3+. События регистрировали с помощью BD LSRFortessa и анализировали с помощью программного обеспечения FlowJo.
Результаты. Образцы крови и опухоли анализировали в отношении PD-показателей в субпопуляциях клеток (CD8+ T-, NK- и Treg-клеток), включающих уровни внутриклеточного фосфорилированного STAT5 (pSTAT5, маркера занятости рецепторов и ранней передачи сигнала), Ki67 (маркера пролиферации клеток) и количества CD8+ T-, NK- и Treg-клеток. pSTAT5 в различных типах клеток измеряли только в крови.
Мыши, несущие опухоль из CT-26, которым вводили дозу 3 мг/кг соединения B, демонстрировали стойкую индукцию pSTAT5 в периферической крови в популяциях CD8+ T-клеток, CD8+ T-клеток памяти, NK- и Treg-клеток. Процентная доля pSTAT5+ клеток среди CD8+ Т-клеток периферической крови (фиг. 16A) и CD8+ Т-клеток памяти (фиг. 16B) достигала пикового значения через 2 ч. после введения дозы, оставалась повышенной до примерно 48 ч. и возвращалась к исходному уровню через 72 ч. Среди NK-клеток (фиг. 16C) доля pSTAT5+ клеток постепенно увеличивалась после введения дозы, достигая пикового значения через 48 ч., и возвращалась к исходному уровню через 120 ч. Индукция pSTAT5+ в Treg-клетках (фиг. 16D) происходила согласно картине, сходной с таковой в CD8+ T-клетках.
После индукции pSTAT5 соединение B индуцировало значительную активацию Ki67 во всех трех популяциях клеток (в CD8+ T-, NK- и Treg-клетках) в одинаковой степени с дня 1 по день 7 (p < 0,05) перед возвращением в день 10 к уровням, соответствующим контрольной среде-носителю (фиг. 17A-17F). Как показано на фиг. 17A и фиг. 17B, активация Ki67 с помощью соединения B приводила к значительным пролиферативным ответам CD8+ Т-клеток с 3 по 12 день (p < 0,05 по сравнению с контролем). Фенотипический анализ CD8+ Т-клеток выявил значительное размножение CD44+ клеток памяти в этой популяции в течение того же периода времени. В отличие от CD8+ Т-клеток, соединение В индуцировало максимальное размножение NK-клеток через 3 дня после введения дозы, которое оставалось повышенным в день 5 (p < 0,05 по сравнению с контролем) перед возвращением в день 7 к уровням, соответствующим обработке контрольной средой-носителем (фиг. 17C и фиг. 17D). В отличие от CD8+ как T-, так и NK-клеток, соединение B вызывало только очень кратковременное размножение Treg-клеток на значительно сниженном уровне (только 2,5% по сравнению с 15-25% для CD8+ T- и NK-клеток) в день 3 после введения дозы (фиг. 17E и 17F). Размножение CD8+ T-клеток и отсутствие значительного размножения субпопуляции CD4+ Treg-клеток приводило к прогрессирующему увеличению соотношения CD8+ T/Treg, достигающему пикового значения в день 7 в дозовой группе 3 мг/кг (фиг. 17G).
Анализ образцов опухоли выявил, что через 7 дней после обработки с помощью соединения В как CD8+ Т-клетки, так и NK-клетки значительно размножились в опухоли (p < 0,05 по сравнению с контролем), и их численность оставалась повышенной до дня 10 (фиг. 18A-18B). Однако в ответ на соединение B популяция Treg-клеток в опухоли не демонстрировала значительное размножение по сравнению со средой-носителем с течением времени (фиг. 18C). Размножение CD8+ T-клеток и отсутствие размножения субпопуляции CD4+ Treg-клеток приводило к прогрессирующему увеличению соотношения CD8+ T/Treg, достигающему пикового значения в день 7 в дозовой группе 3 мг/кг (фиг. 18D).
Краткий итог. У мышей, несущих опухоль из CT-26, соединение B при 3 мг/кг индуцировало активацию pSTAT5 в периферической крови во всех типах иммунных клеток, включая CD8+ T-, CD8+ клетки памяти, NK- и Treg-клетки, что указывает на привлечение рецепторного комплекса IL-2Rβ/γ. Кроме того, соединение B индуцировало маркер пролиферации Ki-67 во всех этих типах клеток при данной дозе, но пролиферация наблюдалась только в CD8+ T- и NK-клетках. Это приводило к соотношению CD8/Treg, составляющему примерно 20 при данной дозе в периферической крови. Хотя воздействие соединения B на опухоль составляло примерно 4% от воздействия на плазму крови, оно сохранялось в опухоли в два раза дольше, что приводило к соотношению CD8 T/Treg, достаточному для демонстрации ингибирования роста опухоли. При более высоких дозах 6 и 9 мг/кг наблюдалось более значительное ингибирование роста опухоли, что приводило к регрессии опухоли.
ПРИМЕР 15
Соединение B увеличивает долю внутриопухолевых Т-клеток и разнообразие TCR в мышиных опухолях из CT-26
Эффект соединения В в качестве средства монотерапии и в комбинации с антителом к PD-1 в отношении репертуара Т-клеток изучали с использованием мышей, несущих опухоль из CT-26. Самкам мышей Balb/c (в возрасте 6-8 недель, со средней массой 16-22 г, Jackson Laboratories или Taconic Biosciences) подкожно в область бока инокулировали опухолевые клетки CT-26 (ATCC), и рост опухоли отслеживали путем измерения опухолей три раза в неделю. Когда опухоли достигали примерно 180 мм3, мышей (N=4 для каждой группы) рандомизировали в следующие группы: контроль (среда-носитель для соединения B+изотипический контроль), соединение B (однократная IV доза 6 мг/кг в день 0), антитело к PD-1 мыши (10 мг/кг, две дозы в дни 0 и 3, IP) или комбинация соединение B+антитело к PD-1. Образцы крови и опухоли собирали до введения дозы и в дни 5, 8, 12 и 16 после введения дозы и хранили при -80°C до анализа. Образцы анализировали в отношении доли внутриопухолевых Т-клеток и разнообразия TCR (Adaptive Biotechnologies, Сиэтл, Вашингтон). Осуществляли секвенирование TCR в инфильтрирующих Т-клетках с помощью ImmunoSEQ™.
Ко дню 8 опухоли из CT-26, обработанные с помощью 6 мг/кг соединения B в отдельности или в комбинации с антителом к PD-1 мыши, демонстрировали значительно более низкую клональность репертуара TCR, определенную с помощью апостериорного критерия Дьюнна, по сравнению с группами, получавшими среду-носитель либо антитело к PD-1 в отдельности (p=0,005). Клональность оценивали количественно по степени моно- или олигоклонального доминирования в репертуаре путем измерения формы распределения частоты клонов. Клональное разнообразие определяли путем снижения объема выборки до минимального количества матриц. Как согласуется с клональностью, в дни 5 и 8 разнообразие TCR демонстрировало противоположную тенденцию и было более высоким в группах, получавших обработку с помощью соединения B или комбинации соединение+антитело к PD-1 (p < 0,05) (фиг. 19). В количественных показателях репертуара Т-клеток в день 12 или 16 не наблюдалась значительная разница при обработке с помощью соединения В или комбинации с антителом к PD-1.
Как показано на фиг. 20, секвенирование TCR также демонстрировало, что соединение В повышает долю лимфоцитов, инфильтрирующих опухоль (TIL), в отдельности или в комбинации с антителом к PD-1 (p < 0,05). Анализ образцов периферической крови в день 8 выявил, что соединение В также значительно уменьшало (p=0,001) клональность Т-клеток по сравнению с контрольной средой-носителем, что согласуется с наблюдениями, сделанным в опухоли (фиг. 21).
ПРИМЕР 16
Соединение B перепрограммирует микроокружение опухоли из CT-26 на высокую активность Teff, индукцию IFN-γ и экспрессию лигандов-контрольных точек
Образцы опухоли из CT-26 из исследования, описанного выше в примере 15, также профилировали с помощью секвенирования мРНК (OminiSeq, Буффало, Нью-Йорк) и анализировали с помощью GeneCentric (парк "Исследовательский треугольник", Северная Каролина) для идентификации клеточных и молекулярных сигнатур инфильтрации и активации лимфоцитов. Данные представлены в виде тепловой карты экспрессии в образцах опухоли из CT26 в день 8 после обработки с помощью контроля (среды-носителя), соединения B (6 мг/кг), антитела к PD-1 мыши (10 мг/кг) или комбинации соединения B и антитела к PD-1 мыши (N=10 мышей на группу). Все сигнатуры и отдельные гены показаны с p-значениями < 0,05 согласно K-W (за исключением PD-L1, p=0,23). Иммунная активация, индуцированная обработкой с помощью соединения B и антитела к PD1, представлена в виде тепловых карт на основании значений, полученных с использованием центрированных к медиане значений log2 экспрессии генов, составляющих различные иммунные сигнатуры, и отдельных генов. Также создавали диаграммы размаха, показывающие уровни экспрессии отдельных сигнатур иммунной активации или отдельных генов. По этим диаграммам размаха проводили попарные сравнения между контрольной группой и группами обработки в дни 8 и 12, и p-значения показаны, когда p-значения согласно критерию суммы рангов Уилкоксона составляли < 0,05. Тепловые карты и диаграммы размаха строили с помощью программы R версии 3.5.3. На диаграммах размаха показаны нижний квартиль, медиана и верхний квартиль данных об экспрессии. "Усы" на диаграммах показывают полное распределение данных об экспрессии. Номенклатура, представленная на фиг. 22, соответствует ортологичным генам человека.
Верхний ряд тепловой карты на фиг. 22 показывает, что через 8 дней после однократной дозы соединения B опухоли из CT26 были инфильтрированы активированными CD8+ эффекторными Т-клетками и Т-клетками памяти, а также CD56dim (цитолитический фенотип) NK-клетками. Численность этих популяций клеток еще больше повышалась в случае с комбинацией с антителом к PD-1. Центрированные к среднему значения log2 уровней экспрессии (фиг. 23) показывают, что соединение В значимо (p < 0,05) повышало количество активированных CD8+ Т-клеток и CD8+ Т-клеток памяти в этих опухолях по сравнению с уровнями до введения дозы, тогда как комбинация соединения В и антитела к PD-1 значимо повышала количество CD56dim NK-клеток по сравнению с уровнем до введения дозы или контролем (p < 0,01). Как показано на фиг. 22, соединение В индуцировало несколько маркеров ответа на IL-2 и активации Т-клеток, в том числе три цепи рецептора IL-2 CD28, 4-1BB и CD40. Кроме того, обработка с помощью соединения В приводила к повышению экспрессии ингибирующих рецепторов-контрольных точек PD-1 и CTLA4, а также лигандов PD-1 PD-L1 и PD-L2. Соединение B также индуцировало гены, сообщающие о высвобождении IFN-γ и активации сигнальных путей IFN-γ (фиг. 24A).
Для конструирования сигнатуры ответа на соединение B у мышей, несущих опухоль CT-26, проводили контролируемый анализ для идентификации дифференциально экспрессируемых генов (FDR < 0/01) между животными, получавшими обработку с помощью контрольной среды-носителя и получавшими обработку с помощью соединения B, в день 8 после обработки. Профили экспрессии генов сопоставляли в выборках мышей, получавших обработку с помощью соединения B в день 8 и получавших контрольную среду-носитель в день 8, с использованием анализов значимости. Множественные сравнения корректировали с использованием уровня ложноположительных результатов (FDR=0,01). Гены ранжировали по p-значению, скорректированному по FDR, а соответствующая кратность изменения указана в таблице 35. Кратность изменения больше единицы указывает на более высокую экспрессию генов в группе, получавшей обработку с помощью соединения B; кратность изменения меньше единицы указывает на более высокую экспрессию генов в контрольной группе.
Сорок два из 43 наиболее дифференциально экспрессируемых генов использовали для прототипа PRS на соединение B. Ген GT(ROSA)26 исключали из прототипа PRS, поскольку этот ген используется в качестве локуса нокина у мыши. Осуществляли вызовы прототипа с помощью соединения B и проводили сравнение между контрольной группой и группами обработки соединением B и антителом к PD1. Осуществляли попарные сравнения PRS между контрольной группой и группами обработки для дней 8 и 12, которые представляли в виде диаграмм размаха (фиг. 24A). Показаны р-значения, полученные с помощью парного критерия суммы рангов Уилкоксона (р-значение < 0,05). С помощью программы R версии 3.5.3 строили диаграммы размаха, показывающие нижний квартиль, медиану и верхний квартиль данных об экспрессии. "Усы" на диаграммах показывают медиану плюс-минус 1,5-кратный межквартильный размах (IQR) или данные о минимуме/максимуме экспрессии, если минимум/максимум находятся в пределах 1,5-кратного IQR.
Сорок два гена характеризовались повышенной экспрессией под действием соединения B в день 8 по сравнению с контролем. Двадцать три человеческих ортолога, показанных в таблице 35, использовали для создания прототипа сигнатуры ответа. Как показано подчеркнутым текстом в таблице 35, выявили несколько генов с известными биологическими свойствами, связанными с IL-2. Для соединения B в качестве средства монотерапии и в комбинации с антителом к PD-1 мыши наблюдались значительные вызовы сигнатуры по сравнению с мышами, получавшими обработку с помощью среды-носителем (ФИГ. 24B).
ПРИМЕР 17
Соединение В способствует формированию стойких ответов с участием Т-клеток памяти, предотвращая рост опухоли из CT-26 у выживших животных, стимулированных путем повторной инъекции клеток CT-26
В примере 15 7 мышей оставались без опухолей в день 100 и включали по 1 животному в каждой из групп, получавших соединение B при 3 мг/кг, соединение B при 6 мг/кг и антитело к PD-1, и 4 животных из группы, получавшей комбинацию соединение B при 6 мг/кг+антитело к PD-1. Этим 7 мышам и 7 контрольным мышам, ранее не участвовавшим в экспериментах, параллельно инокулировали одинаковое количество опухолевых клеток CT-26 в день 121 (исследование № 2). Как показано на фиг. 25, ни у одной из 7 мышей, ранее получавших обработку с помощью соединения B, антитела к PD-1 или их комбинации, не развивались опухоли, тогда как у всех контрольных животных росли опухоли, что указывает на формирование устойчивых популяций Т-клеток памяти в ответ на первоначальные обработки. Через два месяца в день 181 7 получавшим обработку животным без опухолей, которые выжили после первой повторной стимуляции, вместе с 7 контрольными мышами снова инокулировали опухолевые клетки CT-26. И в этот раз также у 7 получавших обработку животных без опухолей не развивались опухоли, тогда как у контрольных животных опухоли росли (фиг. 25). 7 животных без опухолей дожили до дня 202, когда исследование было прекращено.
Эксперимент с повторной стимуляцией повторяли с выжившими животными в дополнительном исследовании (исследование № 3). В общей сложности 9 выживших мышей без опухолей (по 1 животному в каждой из групп, получавших соединение B при 9 мг/кг и антитело к PD-1, 2 животных из группы, получавшей комбинацию соединение B при 3 мг/кг+антитело к PD-1, и 5 животных из группы, получавшей комбинацию соединение B при 6 мг/кг+антитело к PD-1) с полной регрессией опухоли в день 102 повторно стимулировали путем подкожной инокуляции опухолевых клеток CT-26. Также параллельно проводили инокуляцию дополнительным 10 контрольным мышам, ранее не участвовавшим в экспериментах. Как показано на фиг. 26, ни у одного из 9 животных не развивались опухоли, что указывает на формирование устойчивых популяций Т-клеток памяти в ответ на первоначальную обработку. В отличие от этого, у всех 10 контрольных животных развивались опухоли. Через два месяца в день 163 осуществляли вторую повторную стимуляцию у тех же 9 животных, которые выжили после первой стимуляции; дополнительные 9 животных, ранее не участвовавших в экспериментах, служили контролем. Как и в случае с первой повторной стимуляцией, у 9 выживших животных не развивались опухоли, что подтверждает устойчивость ответов с участием Т-клеток памяти после первоначальных обработок, тогда как у контрольных животных опухоли росли (фиг. 26). 9 животных без опухолей дожили до дня 184, когда исследование было прекращено.
Для определения способности соединения В способствовать стойкому ответу с участием Т-клеток памяти через 60 дней после второй повторной стимуляции у 7 выживших мышей из исследования № 2 собирали образцы крови. FACS-анализ образцов крови в отношении экспрессии клеток памяти выявил, что соединение В способствует формированию устойчивой иммунологической памяти против опухолей из CT-26, что наблюдается в виде общего увеличения количества Т-клеток памяти в периферической крови (CD3+), в том числе CD8+ Т-клеток памяти (ФИГ. 27A-27B).
Краткий итог. Анализ TIL в опухолях, обработанных с помощью 6 мг/кг соединения B, выявил увеличение репертуара T-клеток и количества активированных CD8+ T-клеток (в том числе эффекторных Т-клеток памяти) и NK-клеток, а также уровня экспрессии сигнатур IFNγ, которые индуцируют лиганды-контрольные точки. Терапия, направленная на контрольные точки иммунного ответа, широко применялась и демонстрировала эффективность в отношении растущего количества форм рака, в том числе метастатической меланомы и почечноклеточной карциномы (Hodi F.S. et al., N. Engl. J. Med. (2010) 363(8):711-723; Topalian S.L. et al., N. Engl. J. Med. (2012) 366(26):2443-2454; Wolchok J.D. et al., N. Engl. J. Med. (2013) 369(2):122-133; Sharma P. et al. Cell (2015) 161(2):205-214; Alsaab H.O. et al., Frontiers in Pharmacology (2017) 8:561, 1-15; Pardoll D.M. Nat. Rev. Cancer (2016) 12(4): 252-264). Однако частота полного ответа все еще остается довольно низкой. Ингибиторы контрольных точек устраняют ограничения, присущие дисфункциональным цитотоксическим Т-лимфоцитам, и примируют их, а средства цитокиновой терапии, такие как IL-2, могут активировать их и вызывать их пролиферацию. Кроме того, терапевтические средства на основе IL-2 могут обеспечивать размножение и активацию Fc+ лимфоцитов, таких как NK-клетки. Таким образом, ингибиторы контрольных точек и IL-2 в комбинации дополняют друг друга, опосредуя эффекты в отношении иммунных ответов для улучшения противоопухолевых ответов. В современных исследованиях комбинированная обработка с помощью соединения B и антитела к PD-1 приводила к преимуществу в выживаемости по сравнению с каждым средством в режиме монотерапии благодаря увеличению как разнообразия, так и клональности активированных цитотоксических CD8+ T- и NK-клеток. Более того, мыши без опухолей, получавшие обработку с помощью соединения B или комбинации, имели устойчивую популяцию Т-клеток памяти. Это приводило к отторжению опухолевых клеток у выживших мышей после повторных стимуляций теми же опухолевыми клетками в двух случаях с разницей в 2 месяца, при этом первую повторную стимуляцию осуществляли через 100 дней после последней обработки с помощью соединения B, антитела к PD-1 или комбинации.
Хотя в данном документе были показаны и описаны предпочтительные варианты осуществления настоящего изобретения, специалистам в данной области будет очевидно, что такие варианты осуществления представлены только в качестве примера. Многочисленные видоизменения, модификации и замены теперь будут очевидны специалистам в данной области без отступления от настоящего изобретения. Следует понимать, что различные альтернативы вариантам осуществления настоящего изобретения, описанным в данном документе, можно использовать при осуществлении настоящего изобретения на практике. Подразумевается, что нижеследующая формула изобретения определяет объем настоящего изобретения, и что способы и структуры в пределах объема данной формулы изобретения и их эквиваленты охвачены ею. Раскрытия всех патентов и научной литературы, цитируемых в данном документе, явным образом включены в данный документ посредством ссылки во всей своей полноте.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> SYNTHORX, INC.
<120> ВИДЫ ИММУНООНКОЛОГИЧЕСКОЙ КОМБИНИРОВАННОЙ ТЕРАПИИ
С ПРИМЕНЕНИЕМ КОНЪЮГАТОВ IL-2
<130> 01183-0073-00PCT
<150> US 62/887,400
<151> 2019-08-15
<150> US 62/903,187
<151> 2019-09-20
<150> US 62/962,668
<151> 2020-01-17
<160> 98
<170> PatentIn версия 3.5
<210> 1
<211> 133
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> другой_признак
<223> IL-2 (Homo sapiens) (зрелая форма)
<400> 1
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 2
<211> 153
<212> БЕЛОК
<213> Homo sapiens
<220>
<221> другой_признак
<223> IL-2 (Homo sapiens) (предшественник)
<400> 2
Met Tyr Arg Met Gln Leu Leu Ser Cys Ile Ala Leu Ser Leu Ala Leu
1 5 10 15
Val Thr Asn Ser Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu
20 25 30
Gln Leu Glu His Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile
35 40 45
Asn Asn Tyr Lys Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe
50 55 60
Tyr Met Pro Lys Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu
65 70 75 80
Glu Glu Leu Lys Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys
85 90 95
Asn Phe His Leu Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile
100 105 110
Val Leu Glu Leu Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala
115 120 125
Asp Glu Thr Ala Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe
130 135 140
Cys Gln Ser Ile Ile Ser Thr Leu Thr
145 150
<210> 3
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетический: альдеслейкин
<400> 3
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 4
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_C125S
<400> 4
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 5
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65X
<220>
<221> другой_признак
<222> (65)..(65)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 5
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Xaa Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 6
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62X
<220>
<221> другой_признак
<222> (62)..(62)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 6
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 7
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42X
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 7
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 8
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43X
<220>
<221> другой_признак
<222> (43)..(43)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 8
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 9
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35X
<220>
<221> другой_признак
<222> (35)..(35)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 9
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 10
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK]
<220>
<221> другой_признак
<222> (65)..(65)
<223> Xaa представляет собой [AzK]
<400> 10
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Xaa Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 11
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK]
<220>
<221> другой_признак
<222> (62)..(62)
<223> Xaa представляет собой [AzK]
<400> 11
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 12
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK]
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK]
<400> 12
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 13
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK]
<220>
<221> другой_признак
<222> (43)..(43)
<223> Xaa представляет собой [AzK]
<400> 13
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 14
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK]
<220>
<221> другой_признак
<222> (35)..(35)
<223> Xaa представляет собой [AzK]
<400> 14
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 15
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK_PEG]
<220>
<221> другой_признак
<222> (65)..(65)
<223> Xaa представляет собой [AzK_PEG]
<400> 15
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Xaa Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 16
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK_PEG]
<220>
<221> другой_признак
<222> (62)..(62)
<223> Xaa представляет собой [AzK_PEG]
<400> 16
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 17
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK_PEG]
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK_PEG]
<400> 17
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 18
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK_PEG]
<220>
<221> другой_признак
<222> (43)..(43)
<223> Xaa представляет собой [AzK_PEG]
<400> 18
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 19
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK_PEG]
<220>
<221> другой_признак
<222> (35)..(35)
<223> Xaa представляет собой [AzK_PEG]
<400> 19
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 20
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK_PEG5кДа]
<220>
<221> другой_признак
<222> (65)..(65)
<223> Xaa представляет собой [AzK_PEG5кДа]
<400> 20
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Xaa Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 21
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK_PEG5кДа]
<220>
<221> другой_признак
<222> (62)..(62)
<223> Xaa представляет собой [AzK_PEG5кДа]
<400> 21
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 22
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK_PEG5кДа]
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK_PEG5кДа]
<400> 22
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 23
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK_PEG5кДа]
<220>
<221> другой_признак
<222> (43)..(43)
<223> Xaa представляет собой [AzK_PEG5кДа]
<400> 23
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 24
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK_PEG5кДа]
<220>
<221> другой_признак
<222> (35)..(35)
<223> Xaa представляет собой [AzK_PEG5кДа]
<400> 24
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 25
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK_PEG30kD]
<220>
<221> другой_признак
<222> (65)..(65)
<223> Xaa представляет собой [AzK_PEG30kD]
<400> 25
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Xaa Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 26
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK_PEG30kD]
<220>
<221> другой_признак
<222> (62)..(62)
<223> Xaa представляет собой [AzK_PEG30kD]
<400> 26
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 27
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK_PEG30kD]
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK_PEG30kD]
<400> 27
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 28
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK_PEG30kD]
<220>
<221> другой_признак
<222> (43)..(43)
<223> Xaa представляет собой [AzK_PEG30kD]
<400> 28
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 29
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK_PEG30kD]
<220>
<221> другой_признак
<222> (35)..(35)
<223> Xaa представляет собой [AzK_PEG30kD]
<400> 29
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 30
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65X-1
<220>
<221> другой_признак
<222> (64)..(64)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 30
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Xaa
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 31
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62X-1
<220>
<221> другой_признак
<222> (61)..(61)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 31
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 32
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42X-1
<220>
<221> другой_признак
<222> (41)..(41)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 32
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 33
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43X-1
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 33
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 34
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35X-1
<220>
<221> другой_признак
<222> (34)..(34)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 34
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 35
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK]-1
<220>
<221> другой_признак
<222> (64)..(64)
<223> Xaa представляет собой [AzK]
<400> 35
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Xaa
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 36
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK]-1
<220>
<221> другой_признак
<222> (61)..(61)
<223> Xaa представляет собой [AzK]
<400> 36
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 37
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK]-1
<220>
<221> другой_признак
<222> (41)..(41)
<223> Xaa представляет собой [AzK]
<400> 37
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 38
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK]-1
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK]
<400> 38
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 39
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK]-1
<220>
<221> другой_признак
<222> (34)..(34)
<223> Xaa представляет собой [AzK]
<400> 39
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 40
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK_L1_PEG]-1
<220>
<221> другой_признак
<222> (64)..(64)
<223> Xaa представляет собой [AzK_L1_PEG]
<400> 40
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Xaa
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 41
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK_L1_PEG]-1
<220>
<221> другой_признак
<222> (61)..(61)
<223> Xaa представляет собой [AzK_L1_PEG]
<400> 41
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 42
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK_L1_PEG]-1
<220>
<221> другой_признак
<222> (41)..(41)
<223> Xaa представляет собой [AzK_L1_PEG]
<400> 42
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 43
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK_L1_PEG]-1
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK_L1_PEG]
<400> 43
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 44
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK_L1_PEG]-1
<220>
<221> другой_признак
<222> (34)..(34)
<223> Xaa представляет собой [AzK_L1_PEG]
<400> 44
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 45
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK_L1_PEG5кДа]-1
<220>
<221> другой_признак
<222> (64)..(64)
<223> Xaa представляет собой [AzK_L1_PEG5kD]
<400> 45
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Xaa
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 46
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK_ L1_PEG5kD]-1
<220>
<221> другой_признак
<222> (61)..(61)
<223> Xaa представляет собой [AzK_L1_PEG5kD]
<400> 46
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 47
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK_ L1_PEG5kD]-1
<220>
<221> другой_признак
<222> (41)..(41)
<223> Xaa представляет собой [AzK_L1_PEG5kD]
<400> 47
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 48
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK_ L1_PEG5kD]-1
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK_L1_PEG5kD]
<400> 48
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 49
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK_ L1_PEG5kD]-1
<220>
<221> другой_признак
<222> (34)..(34)
<223> Xaa представляет собой [AzK_L1_PEG5kD]
<400> 49
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 50
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK_ L1_PEG30kD]-1
<220>
<221> другой_признак
<222> (64)..(64)
<223> Xaa представляет собой [AzK_L1_PEG30kD]
<400> 50
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Xaa
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 51
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK_ L1_PEG30kD]-1
<220>
<221> другой_признак
<222> (61)..(61)
<223> Xaa представляет собой [AzK_L1_PEG30kD]
<400> 51
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 52
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK_ L1_PEG30kD]-1
<220>
<221> другой_признак
<222> (41)..(41)
<223> Xaa представляет собой [AzK_L1_PEG30kD]
<400> 52
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 53
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK_ L1_PEG30kD]-1
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK_L1_PEG30kD]
<400> 53
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 54
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK_ L1_PEG30kD]-1
<220>
<221> другой_признак
<222> (34)..(34)
<223> Xaa представляет собой [AzK_L1_PEG30kD]
<400> 54
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 55
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK_L1_PEG]-2
<220>
<221> другой_признак
<222> (65)..(65)
<223> Xaa представляет собой [AzK_L1_PEG]
<400> 55
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Xaa Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 56
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK_L1_PEG]-2
<220>
<221> другой_признак
<222> (62)..(62)
<223> Xaa представляет собой [AzK_L1_PEG]
<400> 56
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 57
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK_L1_PEG]-2
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK_L1_PEG]
<400> 57
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 58
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK_L1_PEG]-2
<220>
<221> другой_признак
<222> (43)..(43)
<223> Xaa представляет собой [AzK_L1_PEG]
<400> 58
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 59
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK_L1_PEG]-2
<220>
<221> другой_признак
<222> (35)..(35)
<223> Xaa представляет собой [AzK_L1_PEG]
<400> 59
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 60
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK_L1_PEG5кДа]-2
<220>
<221> другой_признак
<222> (65)..(65)
<223> Xaa представляет собой [AzK_L1_PEG5kD]
<400> 60
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Xaa Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 61
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK_ L1_PEG5kD]-2
<220>
<221> другой_признак
<222> (62)..(62)
<223> Xaa представляет собой [AzK_L1_PEG5kD]
<400> 61
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 62
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK_ L1_PEG5kD]-2
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK_L1_PEG5kD]
<400> 62
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 63
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK_ L1_PEG5kD]-2
<220>
<221> другой_признак
<222> (43)..(43)
<223> Xaa представляет собой [AzK_L1_PEG5kD]
<400> 63
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 64
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK_ L1_PEG5kD]-2
<220>
<221> другой_признак
<222> (35)..(35)
<223> Xaa представляет собой [AzK_L1_PEG5kD]
<400> 64
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 65
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK_ L1_PEG30kD]-2
<220>
<221> другой_признак
<222> (65)..(65)
<223> Xaa представляет собой [AzK_L1_PEG30kD]
<400> 65
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Xaa Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 66
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK_ L1_PEG30kD]-2
<220>
<221> другой_признак
<222> (62)..(62)
<223> Xaa представляет собой [AzK_L1_PEG30kD]
<400> 66
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 67
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK_ L1_PEG30kD]-2
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK_L1_PEG30kD]
<400> 67
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 68
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK_ L1_PEG30kD]-2
<220>
<221> другой_признак
<222> (43)..(43)
<223> Xaa представляет собой [AzK_L1_PEG30kD]
<400> 68
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 69
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK_ L1_PEG30kD]-2
<220>
<221> другой_признак
<222> (35)..(35)
<223> Xaa представляет собой [AzK_L1_PEG30kD]
<400> 69
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 70
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK_PEG]-1
<220>
<221> другой_признак
<222> (64)..(64)
<223> Xaa представляет собой [AzK_PEG]
<400> 70
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Xaa
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 71
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK_PEG]-1
<220>
<221> другой_признак
<222> (61)..(61)
<223> Xaa представляет собой [AzK_PEG]
<400> 71
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 72
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK_PEG]-1
<220>
<221> другой_признак
<222> (41)..(41)
<223> Xaa представляет собой [AzK_PEG]
<400> 72
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 73
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK_PEG]-1
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK_PEG]
<400> 73
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 74
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK_PEG]-1
<220>
<221> другой_признак
<222> (34)..(34)
<223> Xaa представляет собой [AzK_PEG]
<400> 74
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 75
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK_ PEG5kD]-1
<220>
<221> другой_признак
<222> (64)..(64)
<223> Xaa представляет собой [AzK_PEG5кДа]
<400> 75
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Xaa
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 76
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK_PEG5кДа]-1
<220>
<221> другой_признак
<222> (61)..(61)
<223> Xaa представляет собой [AzK_PEG5кДа]
<400> 76
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 77
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK_PEG5кДа]-1
<220>
<221> другой_признак
<222> (41)..(41)
<223> Xaa представляет собой [AzK_PEG5кДа]
<400> 77
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 78
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK_PEG5кДа]-1
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK_PEG5кДа]
<400> 78
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 79
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK_PEG5кДа]-1
<220>
<221> другой_признак
<222> (34)..(34)
<223> Xaa представляет собой [AzK_PEG5кДа]
<400> 79
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 80
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_P65[AzK_PEG30kD]-1
<220>
<221> другой_признак
<222> (64)..(64)
<223> Xaa представляет собой [AzK_PEG30kD]
<400> 80
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Xaa
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 81
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E62[AzK_PEG30kD]-1
<220>
<221> другой_признак
<222> (61)..(61)
<223> Xaa представляет собой [AzK_PEG30kD]
<400> 81
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Xaa Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 82
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F42[AzK_PEG30kD]-1
<220>
<221> другой_признак
<222> (41)..(41)
<223> Xaa представляет собой [AzK_PEG30kD]
<400> 82
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Xaa Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 83
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K43[AzK_PEG30kD]-1
<220>
<221> другой_признак
<222> (42)..(42)
<223> Xaa представляет собой [AzK_PEG30kD]
<400> 83
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Xaa Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 84
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_K35[AzK_PEG30kD]-1
<220>
<221> другой_признак
<222> (34)..(34)
<223> Xaa представляет собой [AzK_PEG30kD]
<400> 84
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Xaa Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Ser Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 85
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F44X
<220>
<221> другой_признак
<222> (44)..(44)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 85
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Xaa Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 86
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_F44X-1
<220>
<221> другой_признак
<222> (43)..(43)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 86
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Xaa Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 87
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_R38X
<220>
<221> другой_признак
<222> (38)..(38)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 87
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Xaa Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 88
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_R38X-1
<220>
<221> другой_признак
<222> (37)..(37)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 88
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Xaa Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 89
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_T41X
<220>
<221> другой_признак
<222> (41)..(41)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 89
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Xaa Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 90
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_T41X-1
<220>
<221> другой_признак
<222> (40)..(40)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 90
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Xaa Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 91
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E68X
<220>
<221> другой_признак
<222> (68)..(68)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 91
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Xaa Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 92
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_E68X-1
<220>
<221> другой_признак
<222> (67)..(67)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 92
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Xaa Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 93
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_Y45X
<220>
<221> другой_признак
<222> (45)..(45)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 93
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Xaa Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 94
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_Y45X-1
<220>
<221> другой_признак
<222> (44)..(44)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 94
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Xaa Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 95
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_V69X
<220>
<221> другой_признак
<222> (69)..(69)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 95
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Xaa Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 96
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_V69X-1
<220>
<221> другой_признак
<222> (68)..(68)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 96
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Xaa Leu Asn Leu Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<210> 97
<211> 133
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_L72X
<220>
<221> другой_признак
<222> (72)..(72)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 97
Ala Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His
1 5 10 15
Leu Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys
20 25 30
Asn Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys
35 40 45
Lys Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys
50 55 60
Pro Leu Glu Glu Val Leu Asn Xaa Ala Gln Ser Lys Asn Phe His Leu
65 70 75 80
Arg Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu
85 90 95
Lys Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala
100 105 110
Thr Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile
115 120 125
Ile Ser Thr Leu Thr
130
<210> 98
<211> 132
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Синтетическая: IL-2_L72X-1
<220>
<221> другой_признак
<222> (71)..(71)
<223> Xaa представляет собой любую неприродную аминокислоту
<400> 98
Pro Thr Ser Ser Ser Thr Lys Lys Thr Gln Leu Gln Leu Glu His Leu
1 5 10 15
Leu Leu Asp Leu Gln Met Ile Leu Asn Gly Ile Asn Asn Tyr Lys Asn
20 25 30
Pro Lys Leu Thr Arg Met Leu Thr Phe Lys Phe Tyr Met Pro Lys Lys
35 40 45
Ala Thr Glu Leu Lys His Leu Gln Cys Leu Glu Glu Glu Leu Lys Pro
50 55 60
Leu Glu Glu Val Leu Asn Xaa Ala Gln Ser Lys Asn Phe His Leu Arg
65 70 75 80
Pro Arg Asp Leu Ile Ser Asn Ile Asn Val Ile Val Leu Glu Leu Lys
85 90 95
Gly Ser Glu Thr Thr Phe Met Cys Glu Tyr Ala Asp Glu Thr Ala Thr
100 105 110
Ile Val Glu Phe Leu Asn Arg Trp Ile Thr Phe Cys Gln Ser Ile Ile
115 120 125
Ser Thr Leu Thr
130
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНЪЮГАТЫ ИНТЕРЛЕЙКИНА 10 И ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2829811C1 |
| КОНЪЮГАТЫ IL-2 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2829327C2 |
| КОМПОЗИЦИИ IL-12, НАЦЕЛЕННЫЕ НА EDB | 2019 |
|
RU2758143C1 |
| МУТАНТЫ FIMH E. COLI И ИХ ПРИМЕНЕНИЕ | 2021 |
|
RU2831010C1 |
| БИОЛОГИЧЕСКИЕ МАТЕРИАЛЫ ДЛЯ МОДУЛЯЦИИ ИММУННЫХ ОТВЕТОВ | 2017 |
|
RU2770060C2 |
| КОНЪЮГАТЫ АНТИТЕЛА И ЛЕКАРСТВЕННОГО СРЕДСТВА, СОДЕРЖАЩИЕ МОДУЛЯТОР СПЛАЙСИНГА НА ОСНОВЕ ГЕРБОКСИДИЕНА, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2820607C2 |
| ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ КОНЪЮГАТА ТРОЙНОГО АГОНИСТА ДЛИТЕЛЬНОГО ДЕЙСТВИЯ, ОБЛАДАЮЩЕГО АКТИВНОСТЯМИ В ОТНОШЕНИИ ВСЕХ ИЗ РЕЦЕПТОРОВ ГЛЮКАГОНА /GLP-1/GIP, ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ ЛЕГКОГО | 2020 |
|
RU2829342C1 |
| НОВЫЕ ПОЛИПЕПТИДЫ СО СПЕЦИФИЧЕСКИМ СВЯЗЫВАНИЕМ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2723034C2 |
| ПРОЛЕКАРСТВЕННЫЕ КОМПОЗИЦИИ НА ОСНОВЕ ГИДРОГЕЛЯ ПОПЕРЕЧНО-СШИТОЙ ГИАЛУРОНОВОЙ КИСЛОТЫ И СПОСОБЫ | 2018 |
|
RU2812787C2 |
| ВАРИАНТ ЧЕЛОВЕЧЕСКОГО ИНТЕРЛЕЙКИНА-2 ИЛИ ЕГО ПРОИЗВОДНОЕ | 2019 |
|
RU2799437C2 |
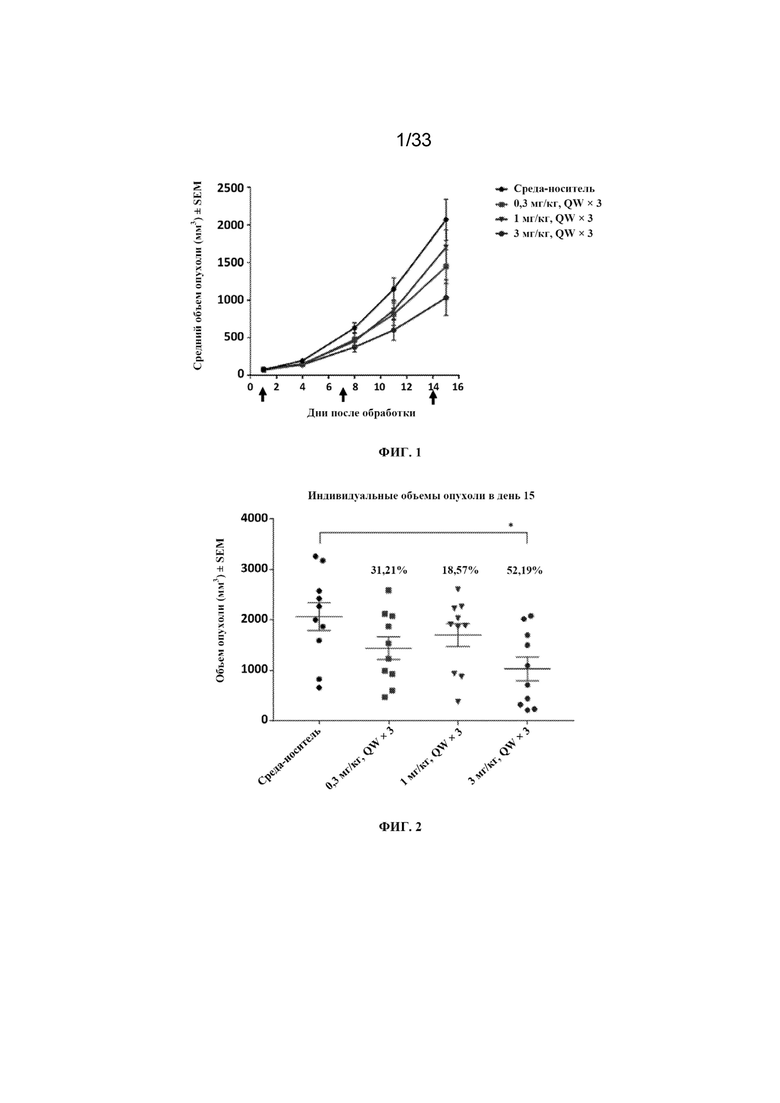
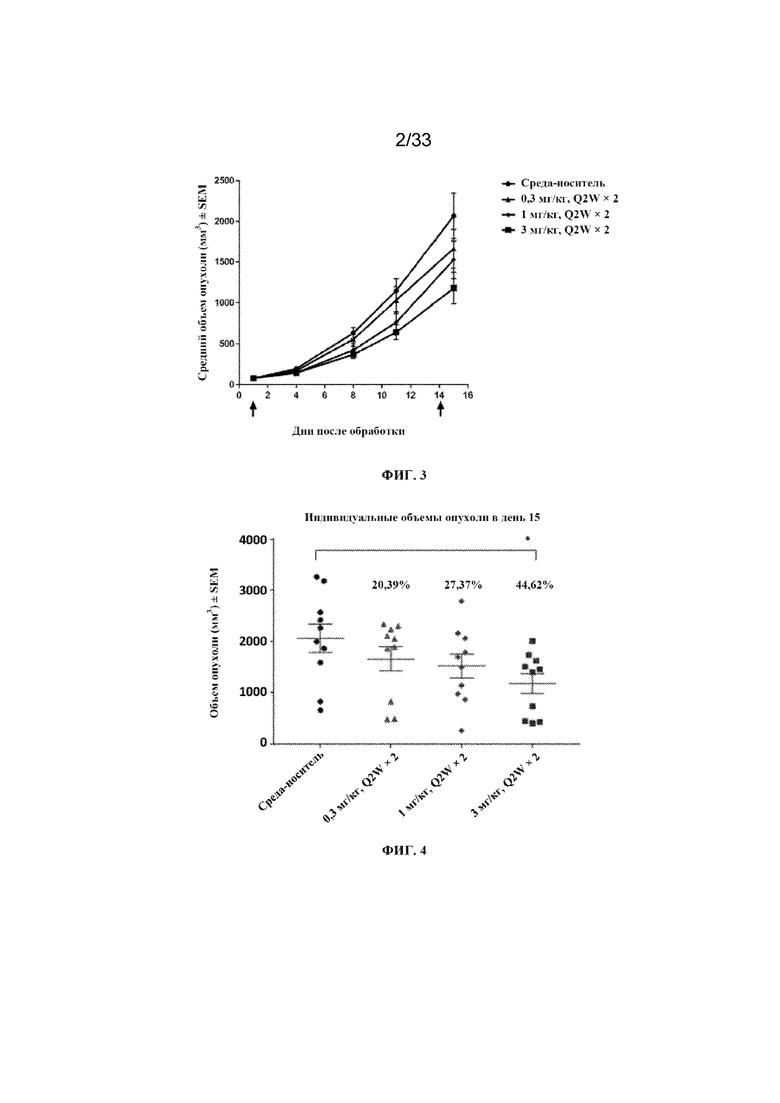
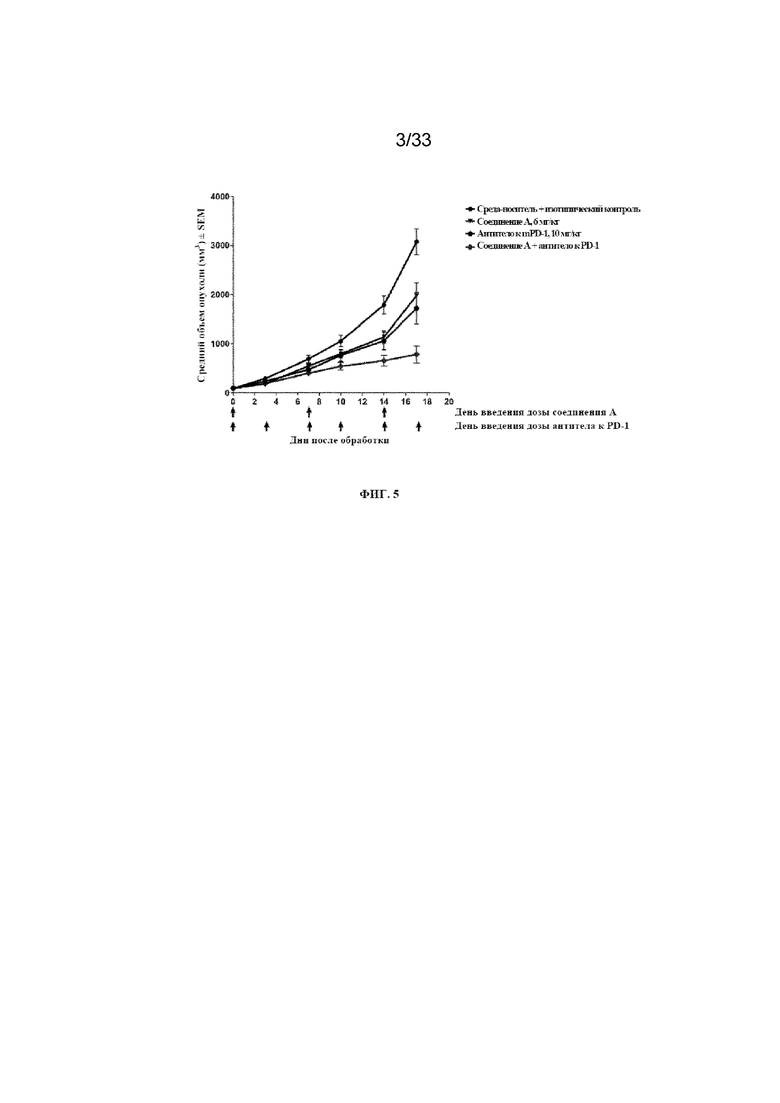

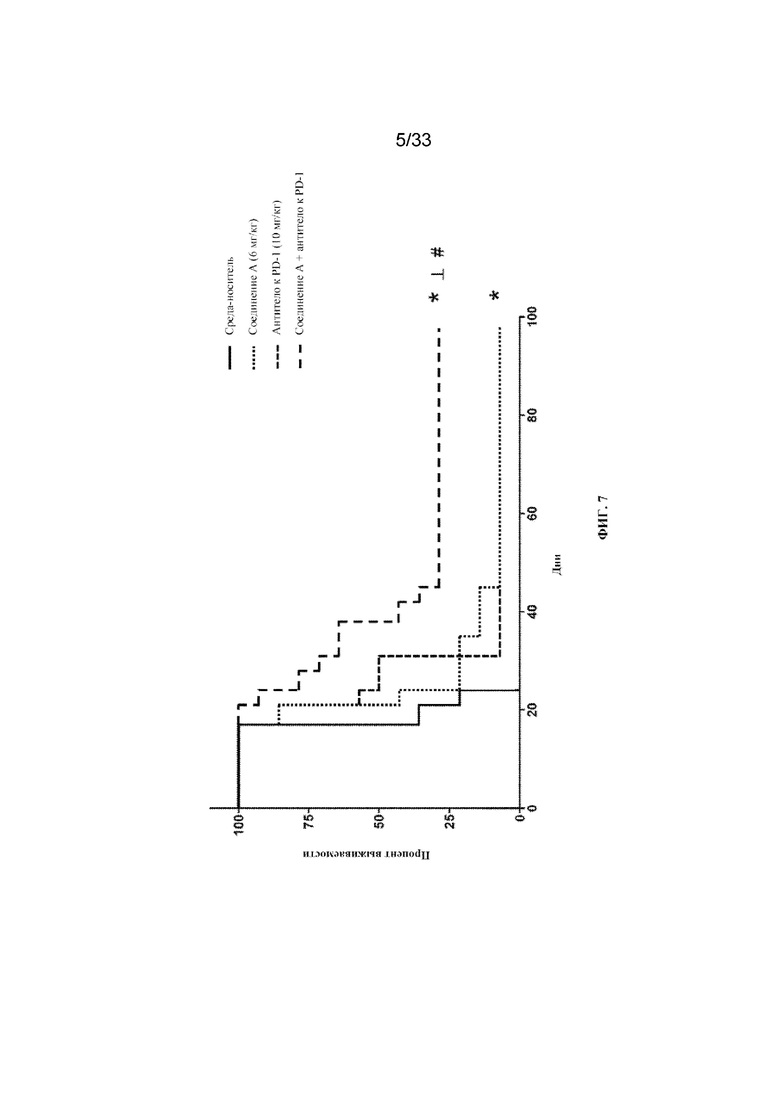
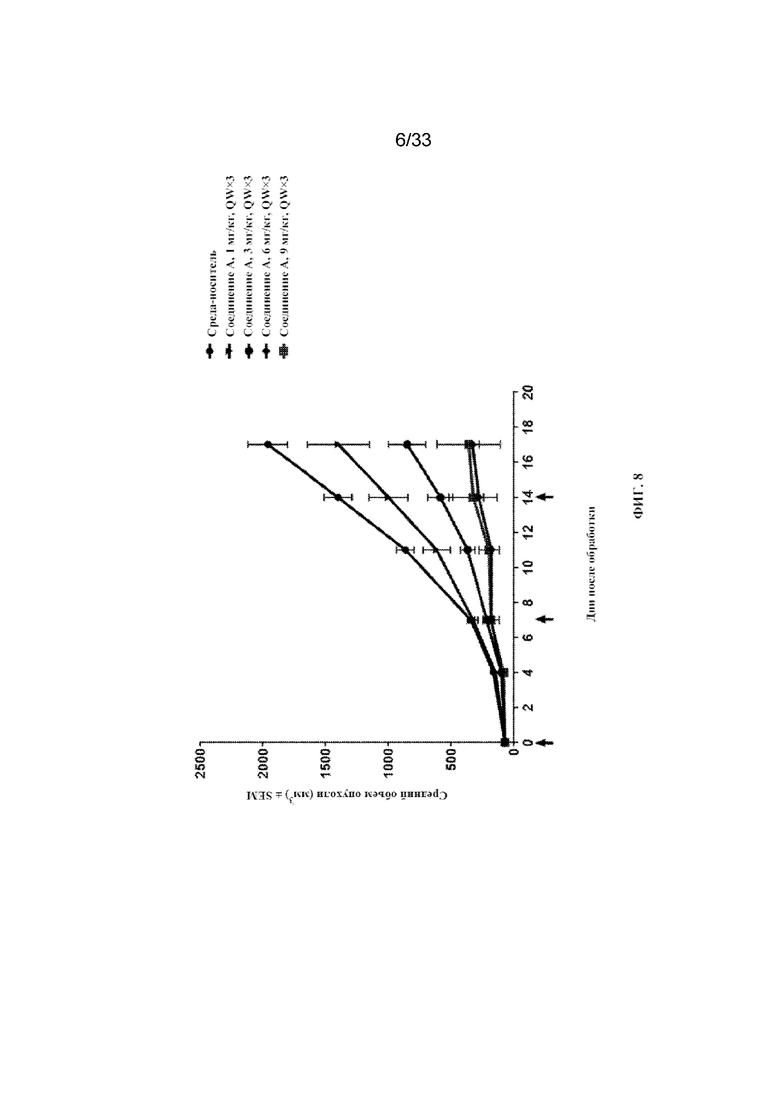
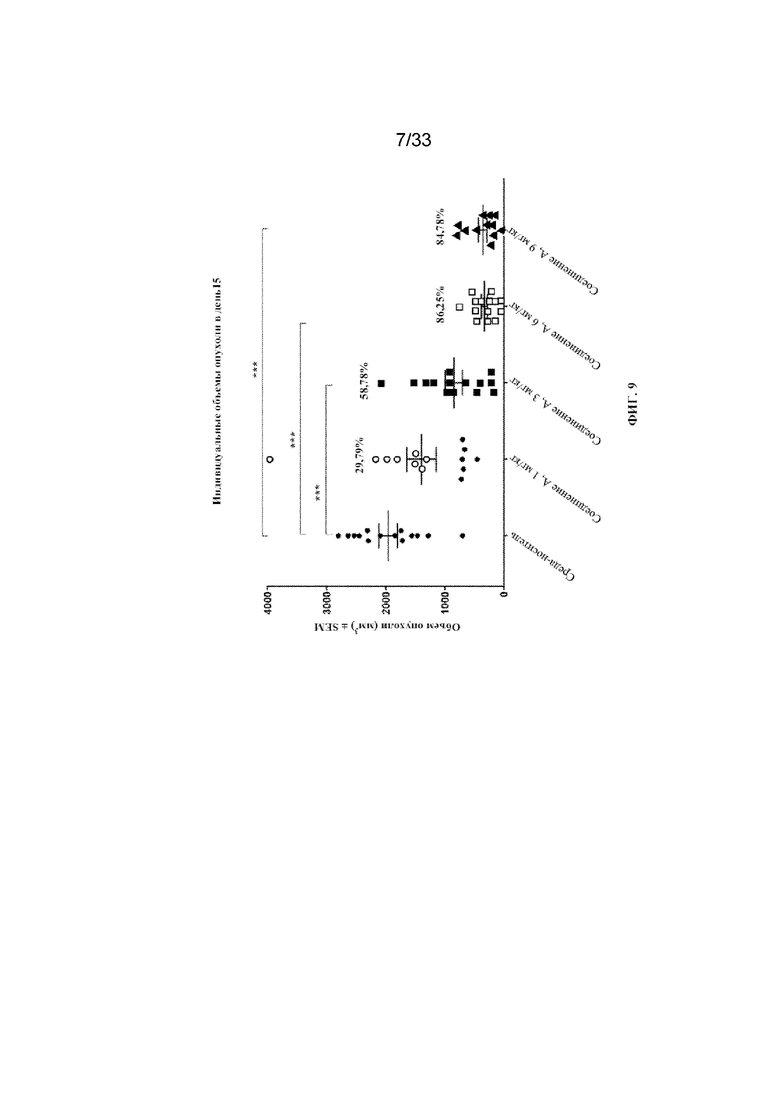
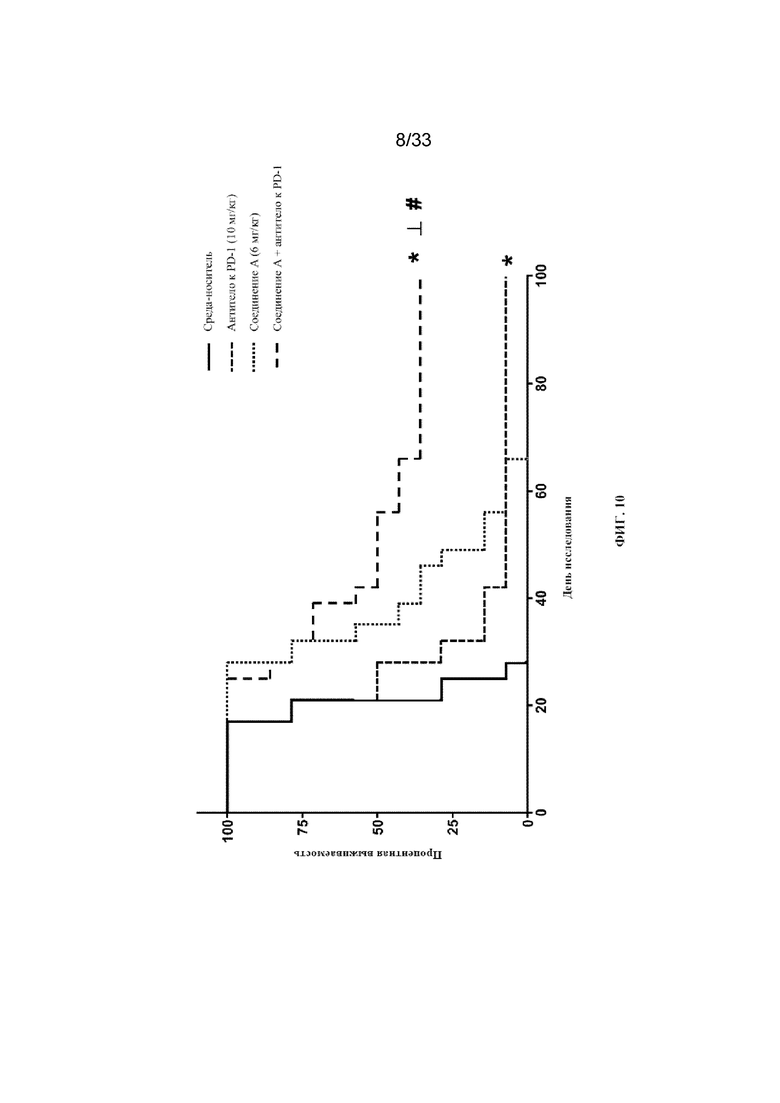
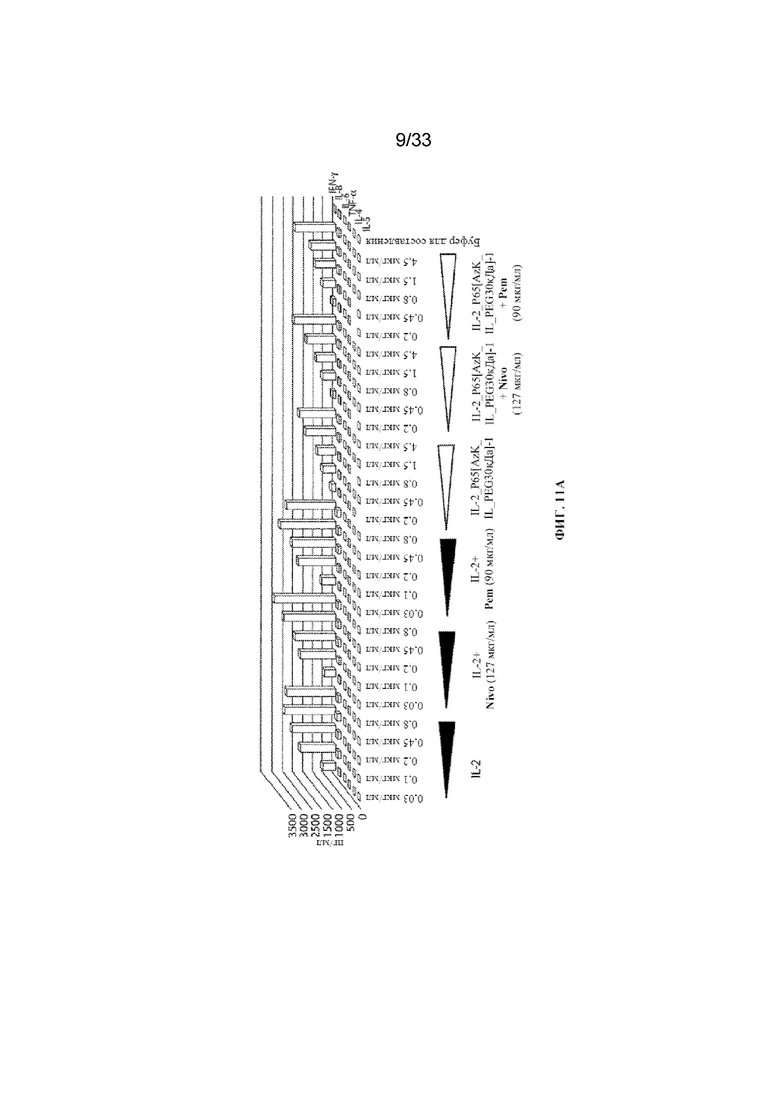
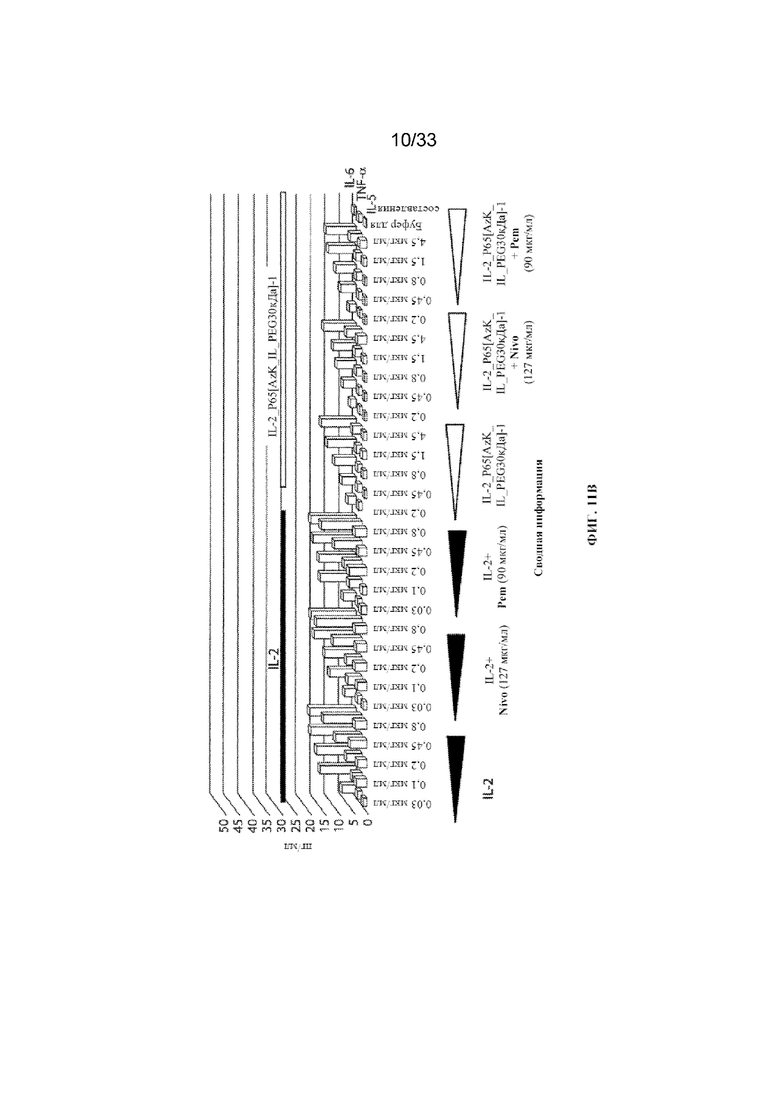
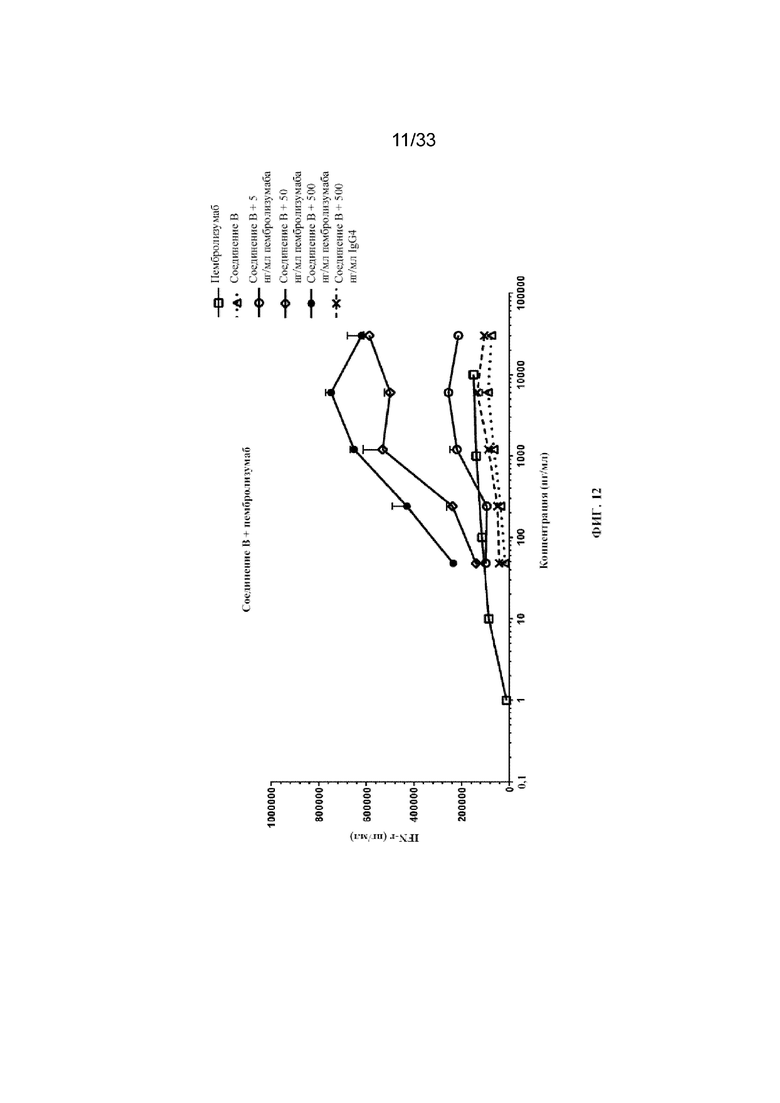
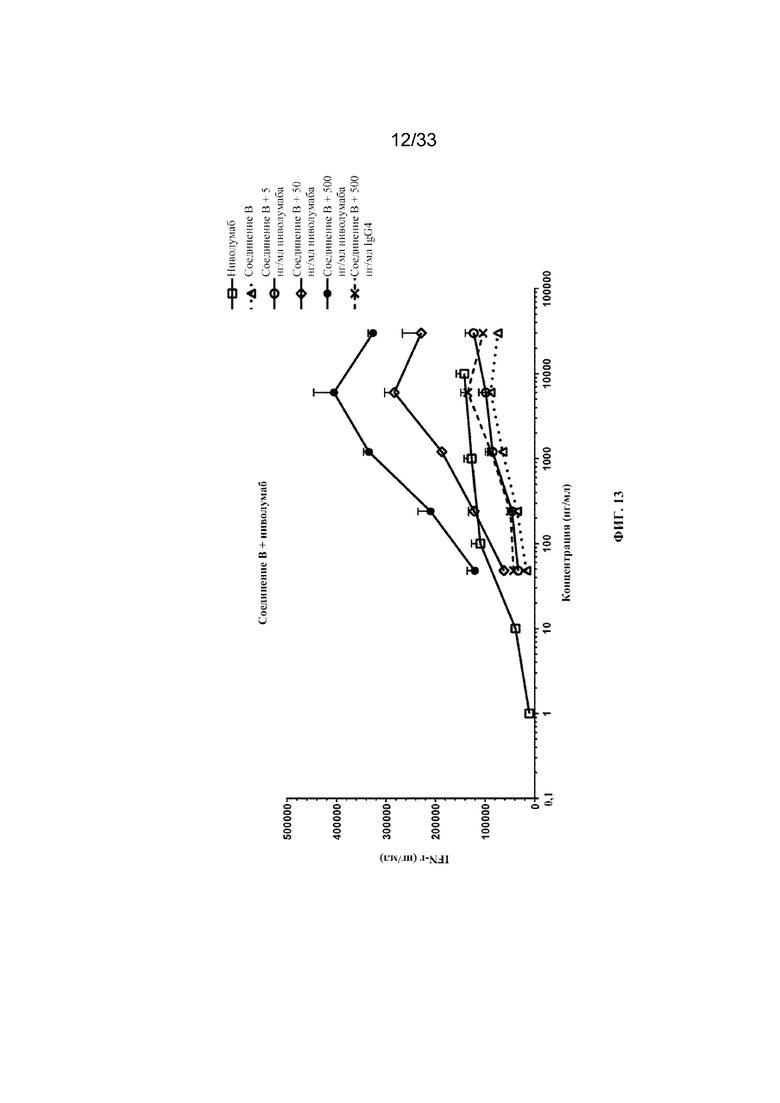
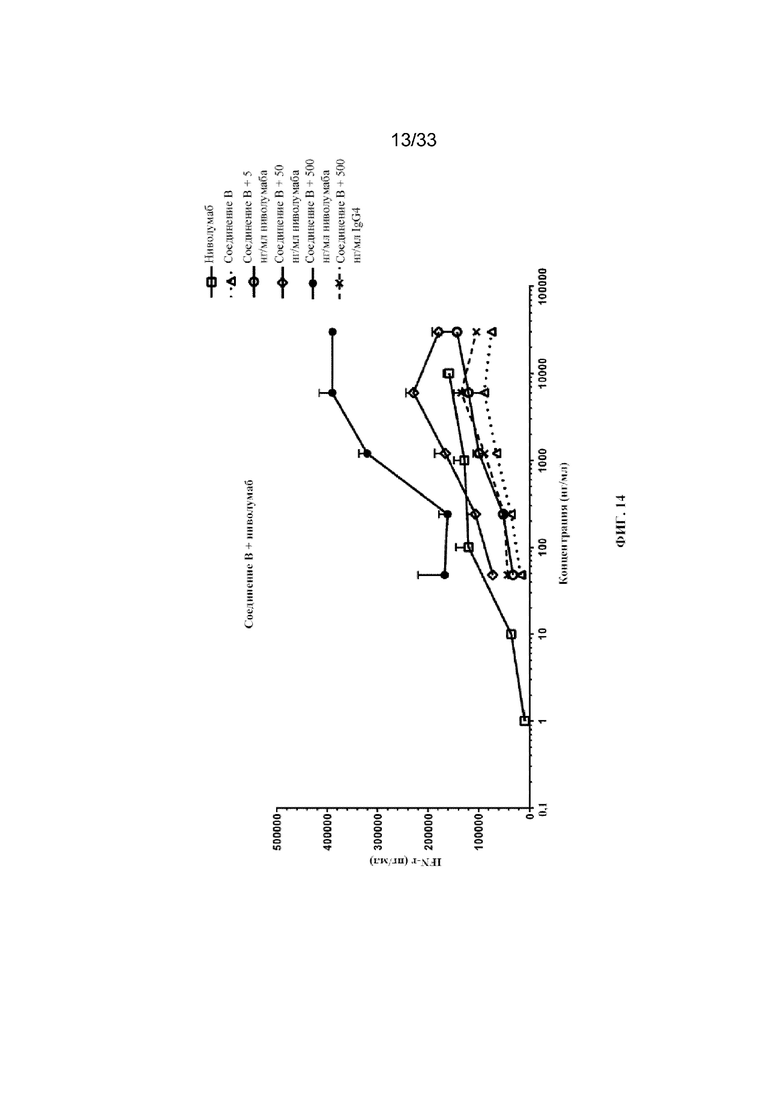
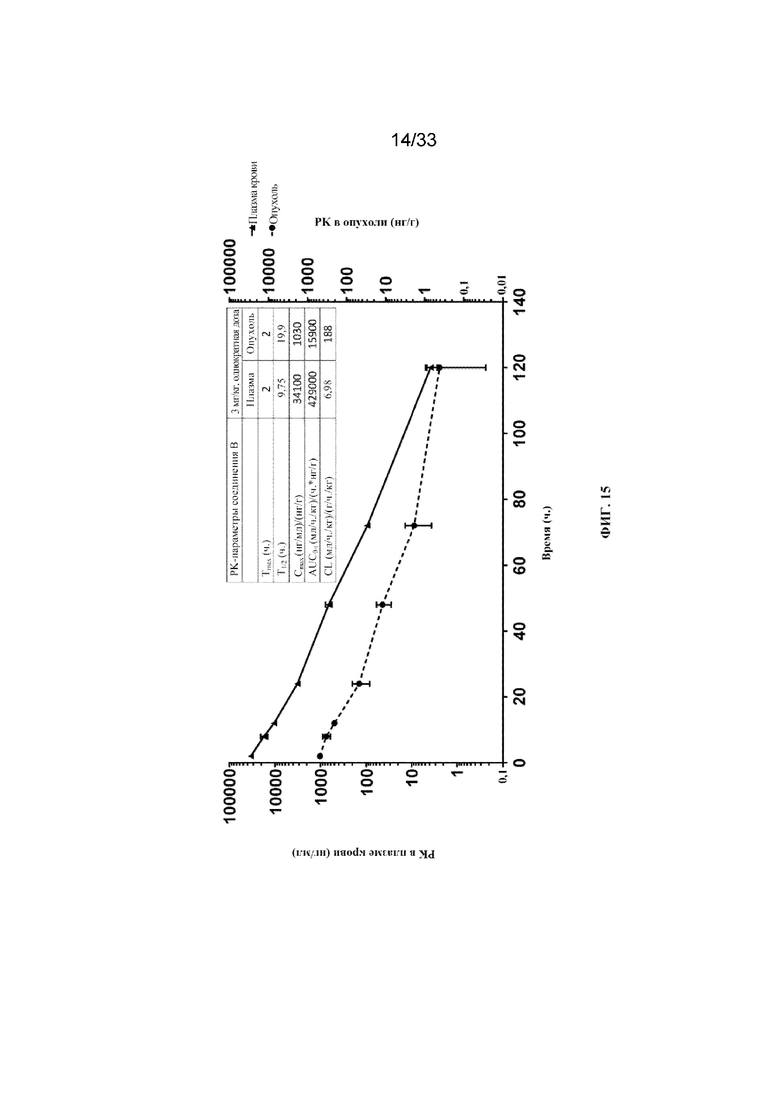
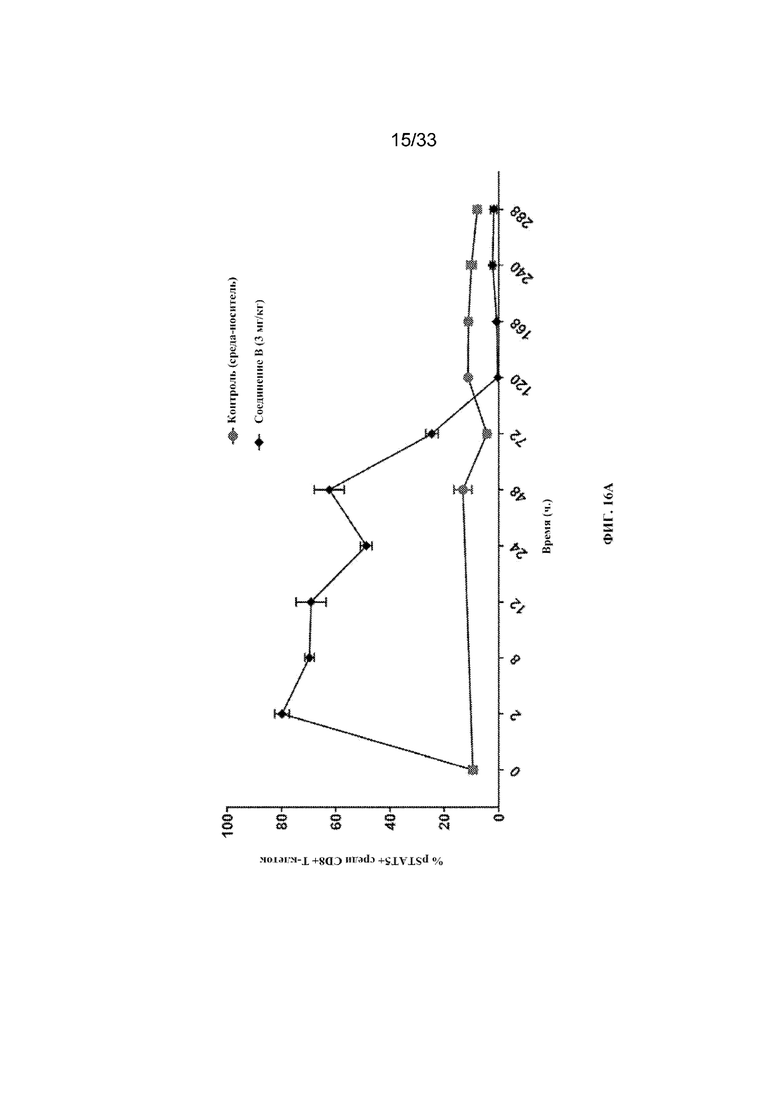
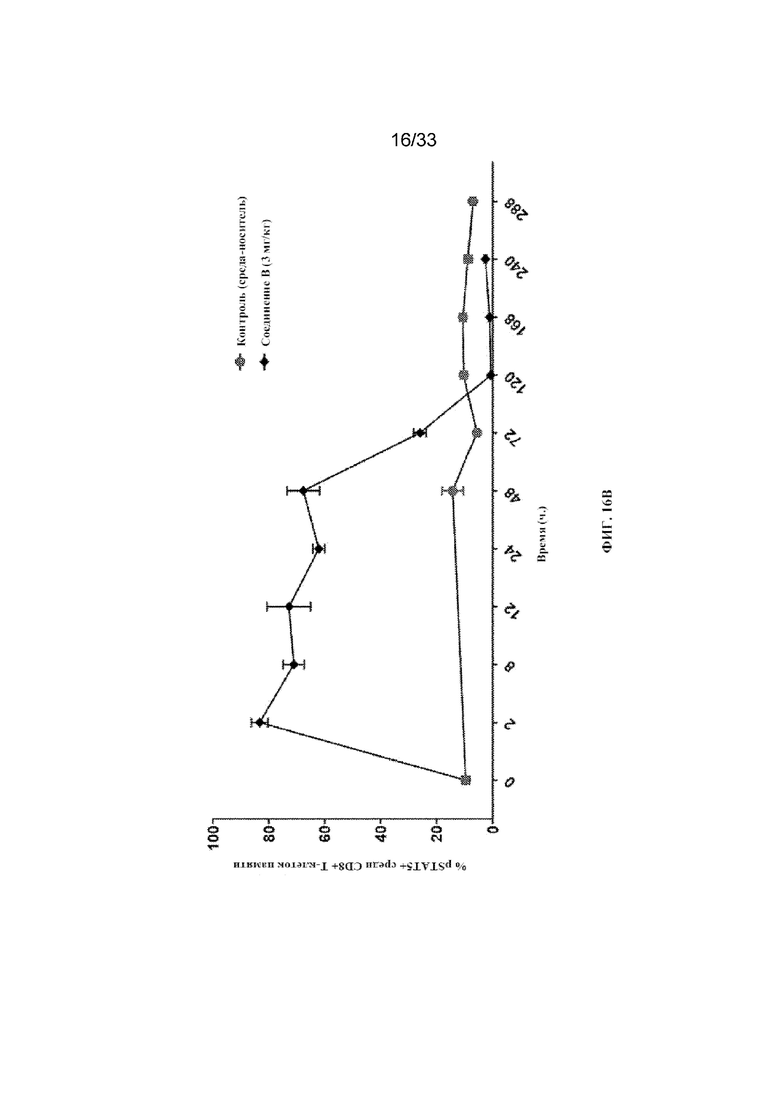
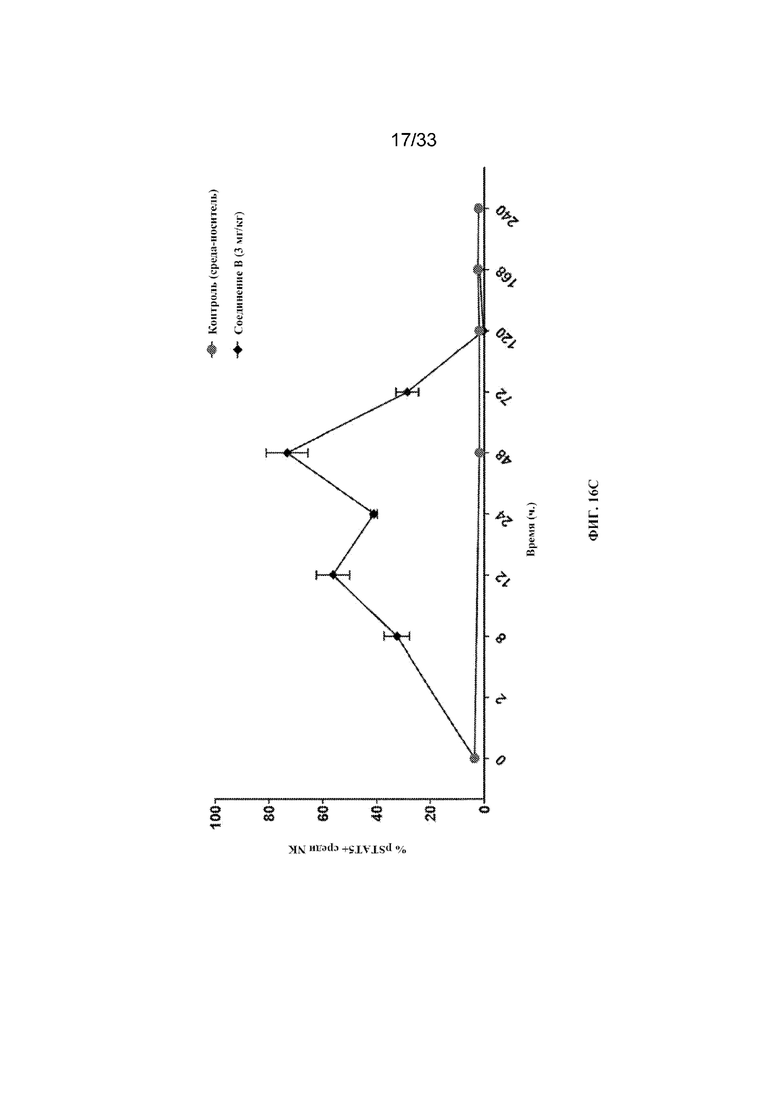
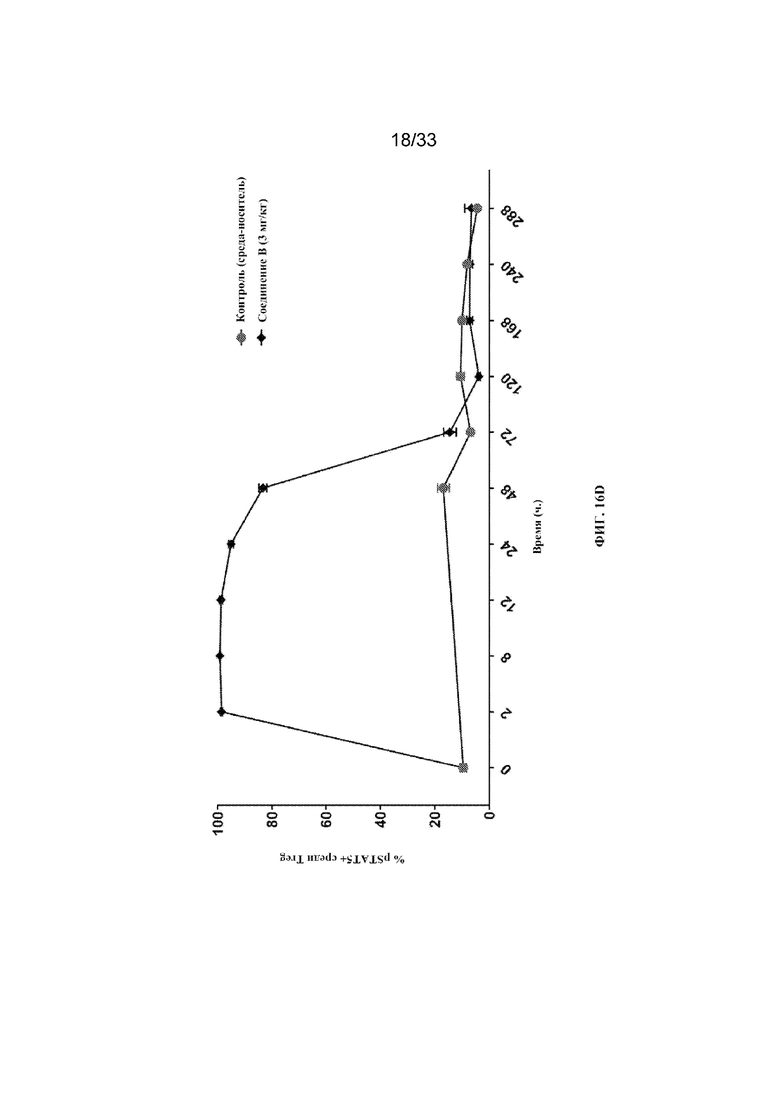
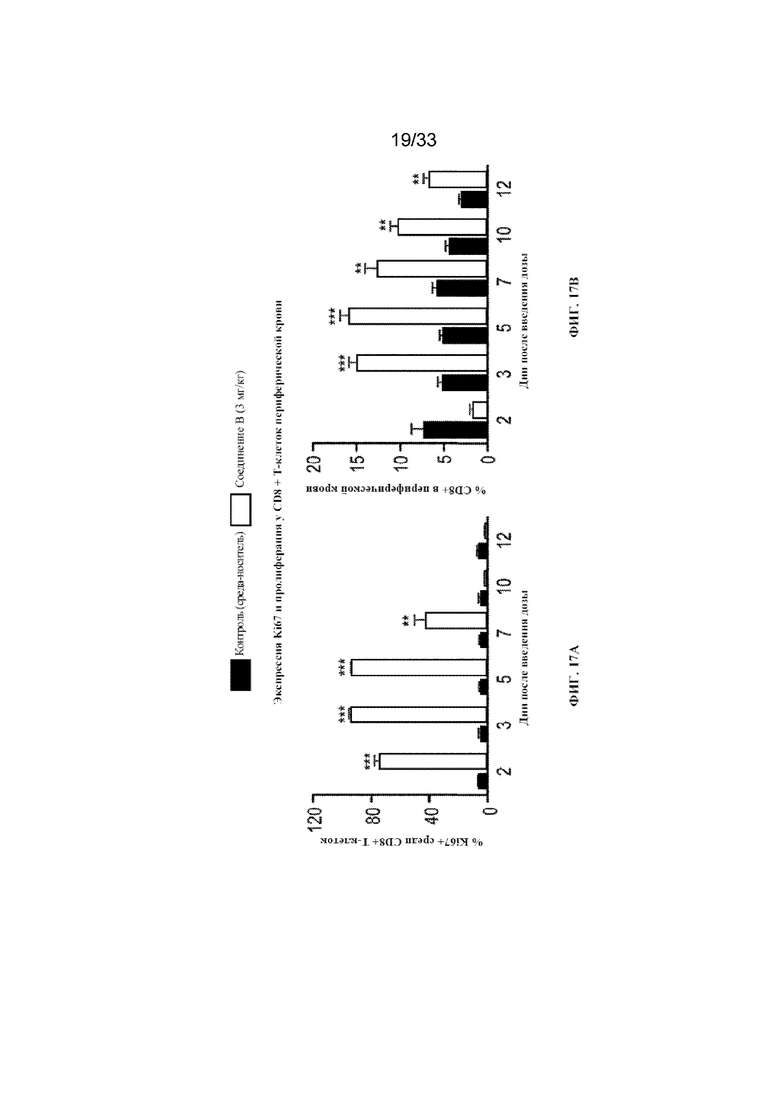
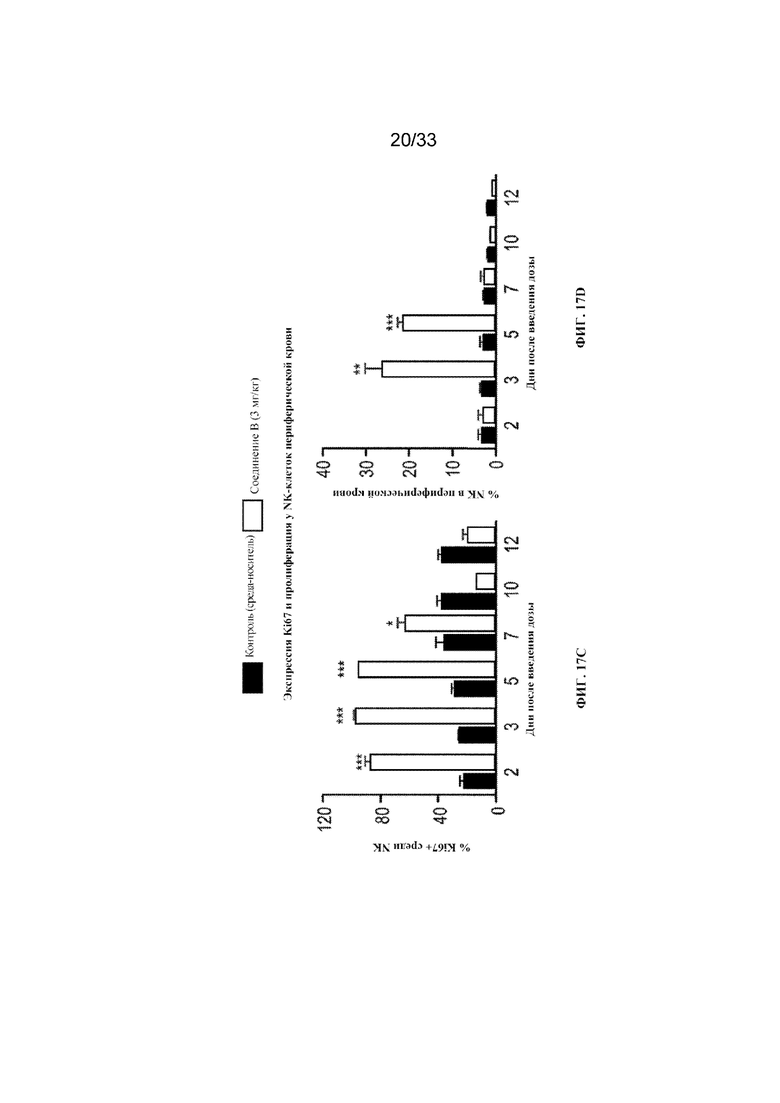
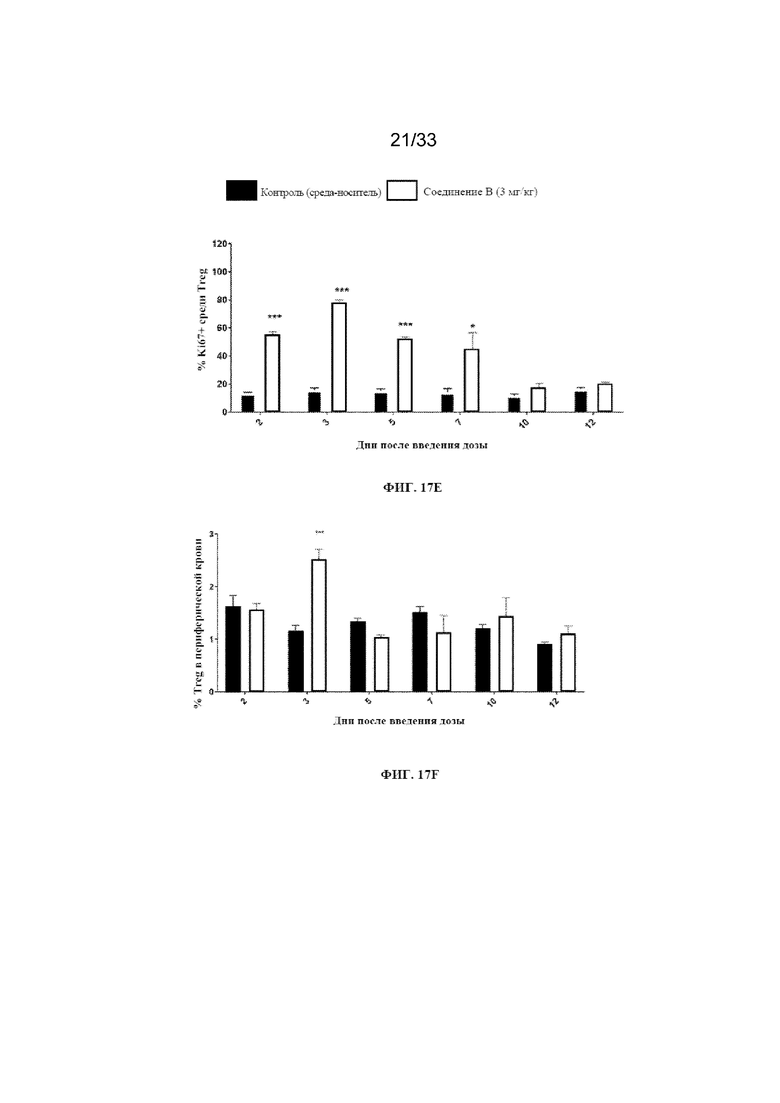
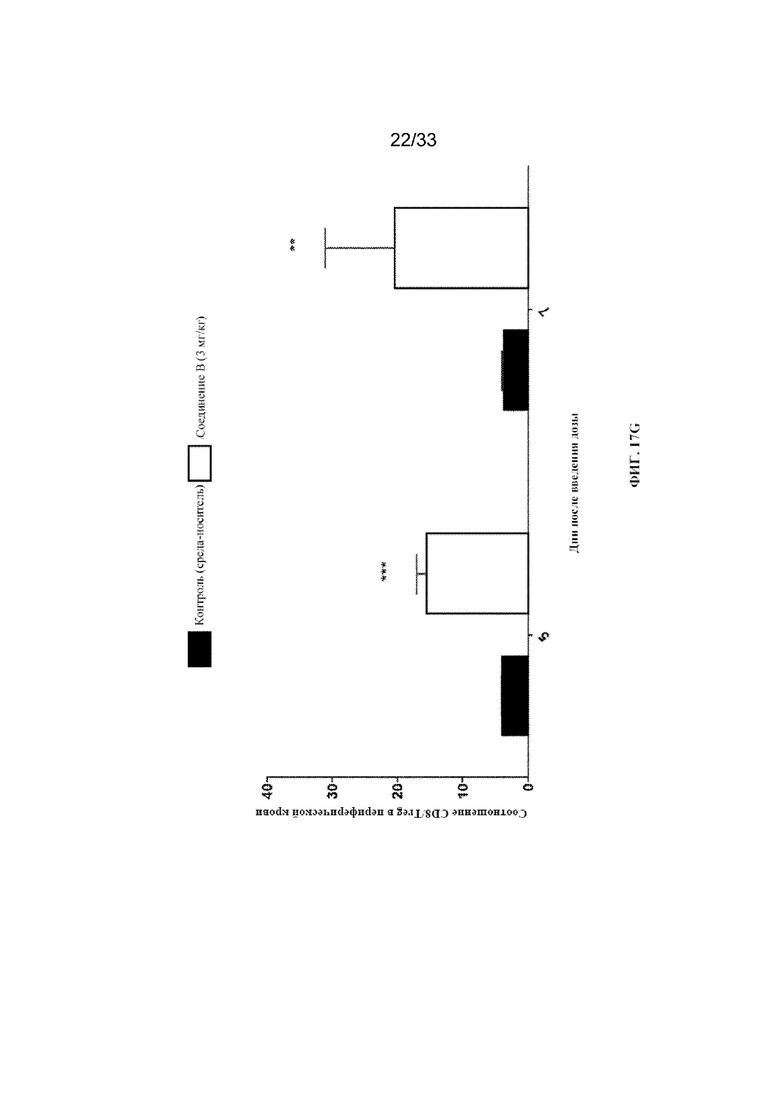
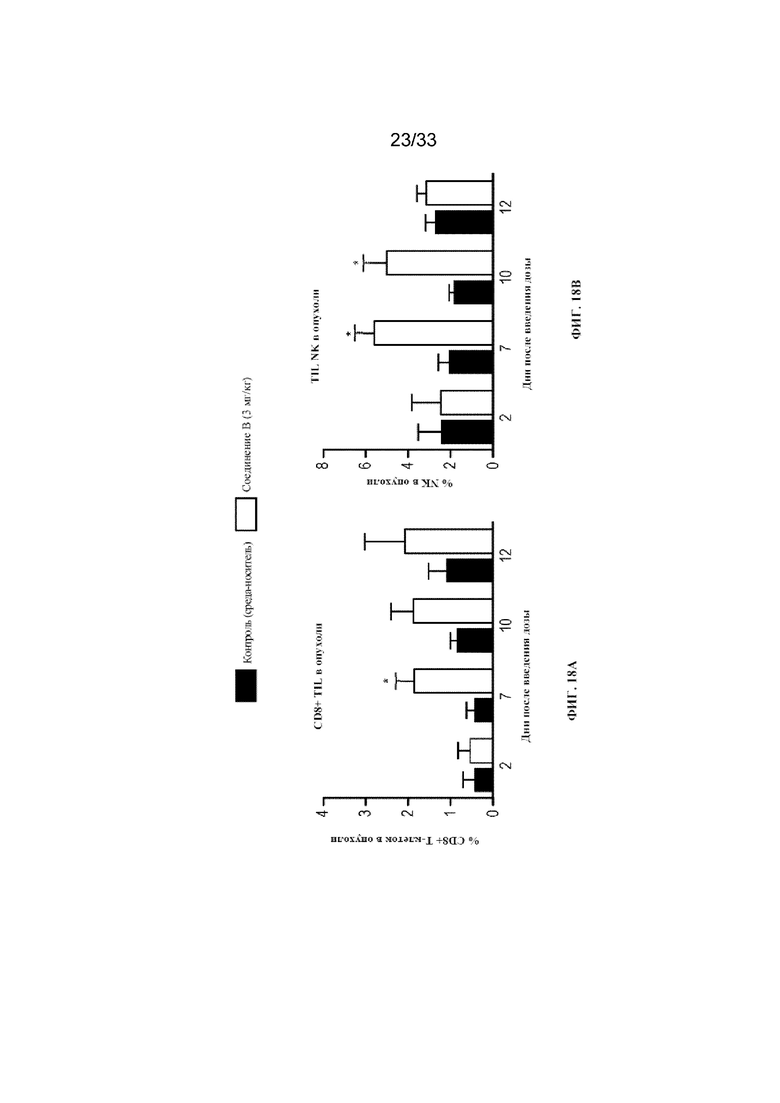
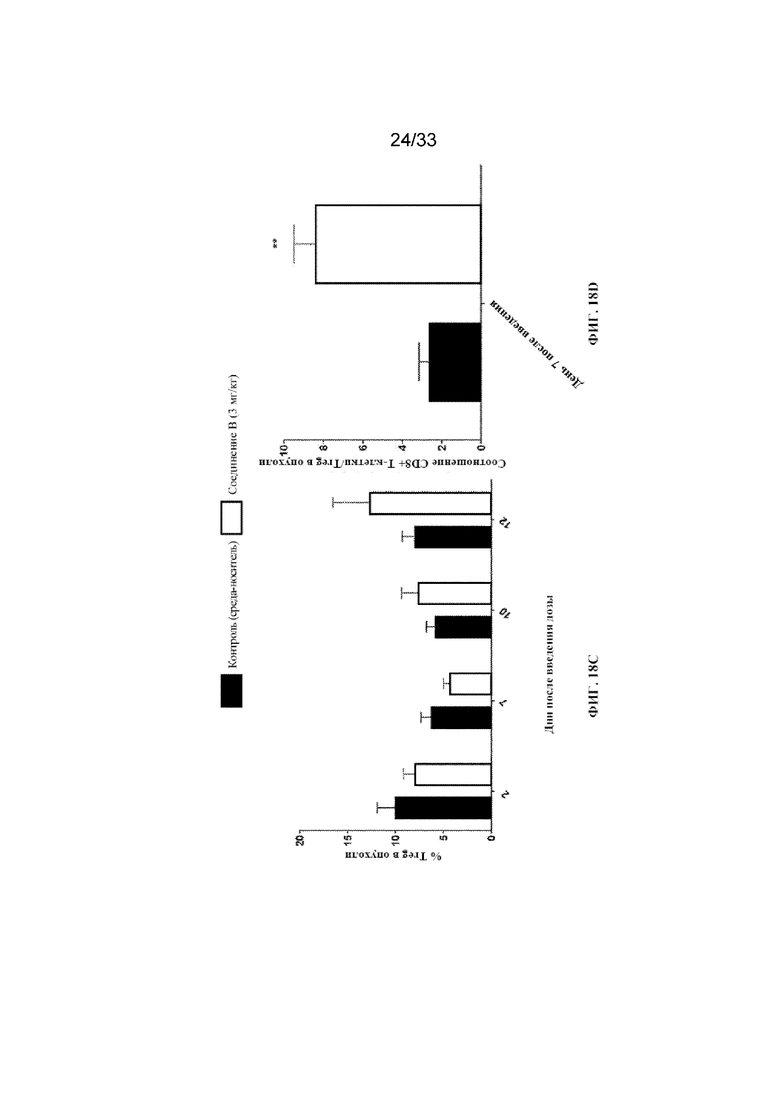
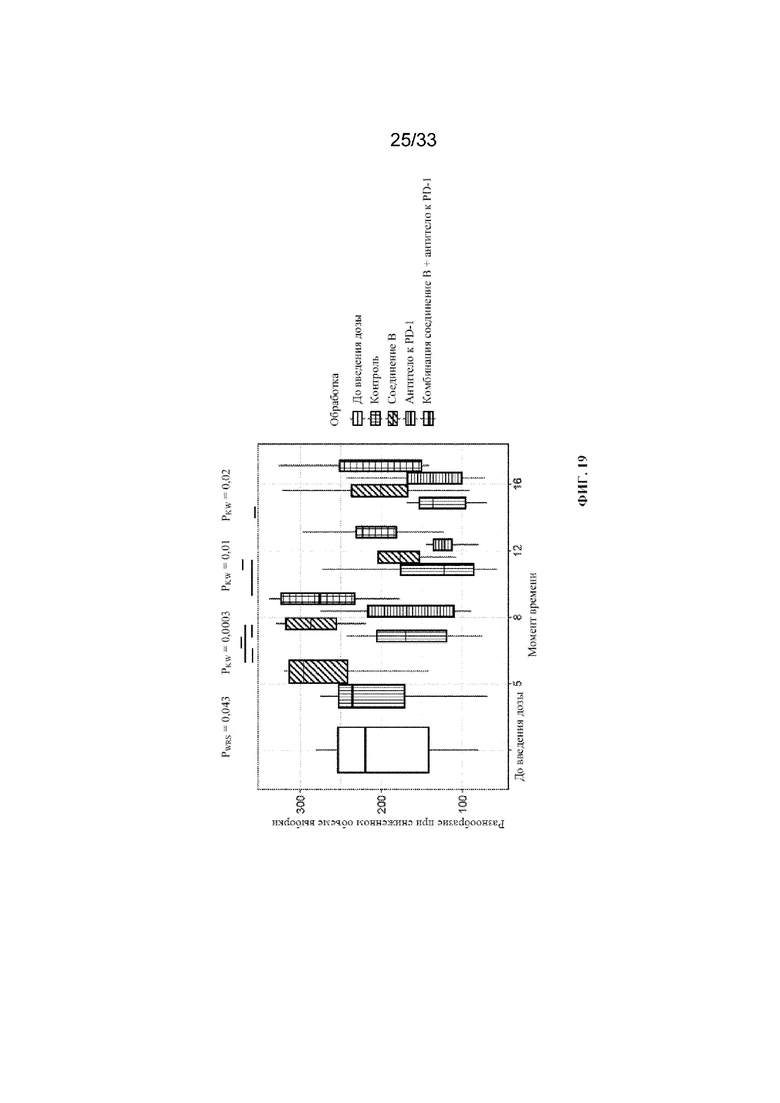
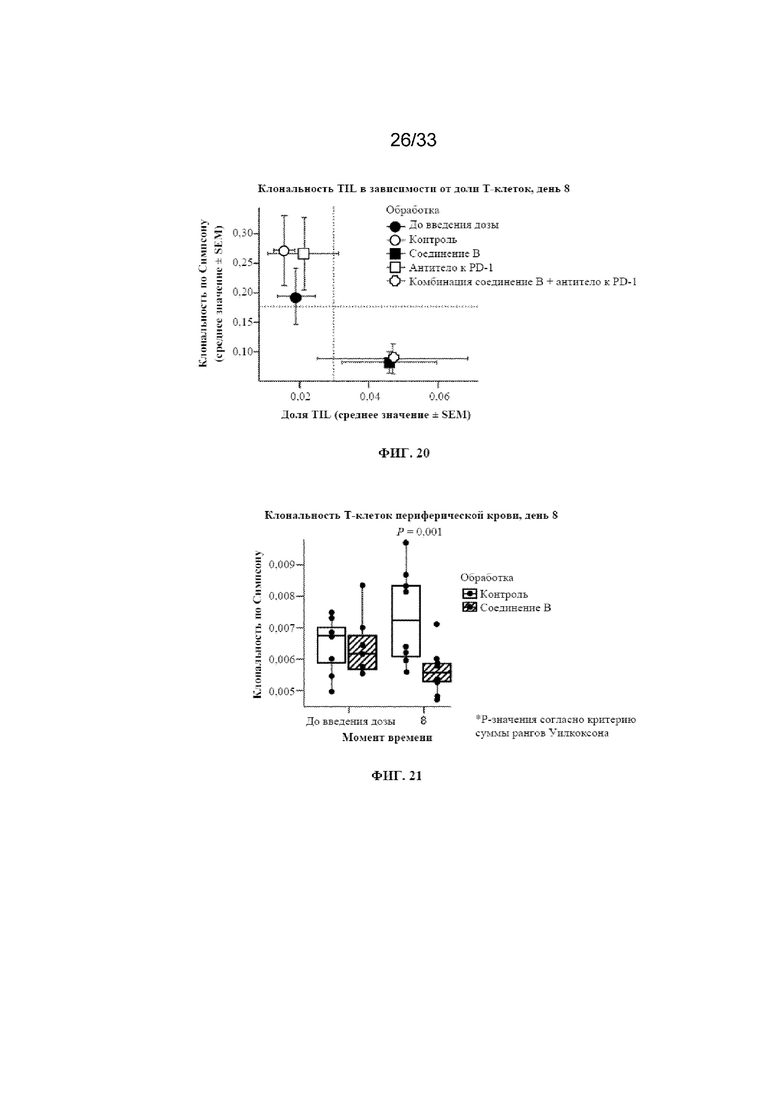
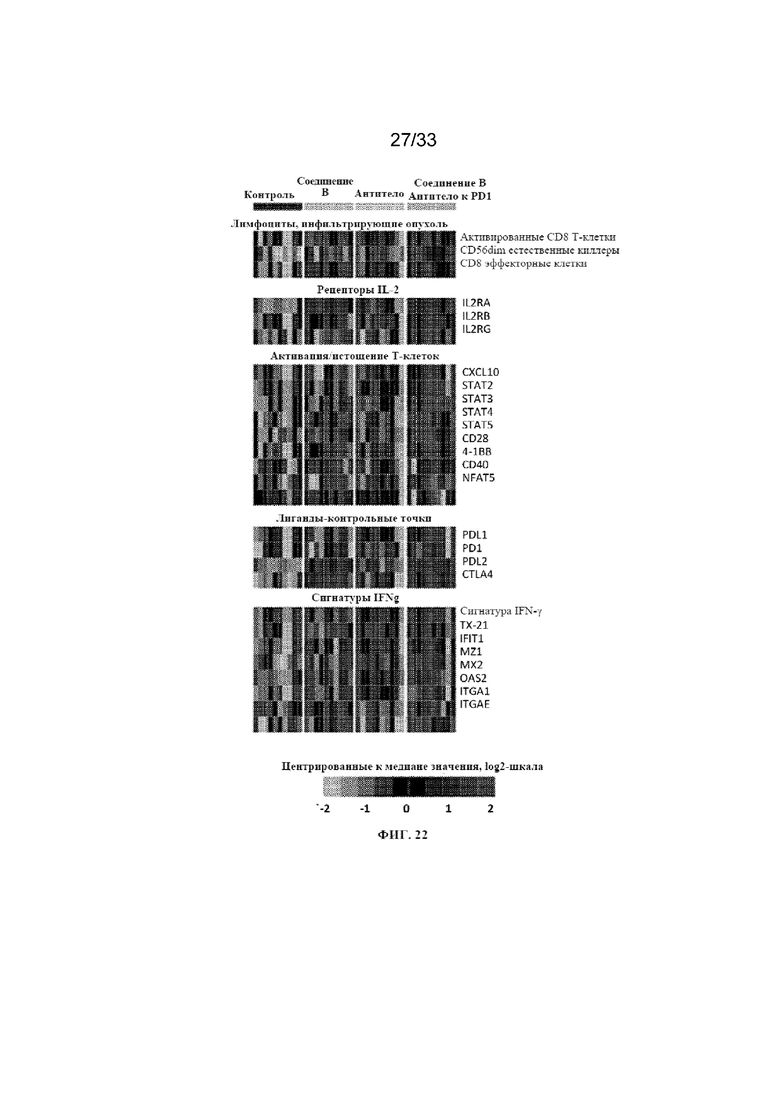

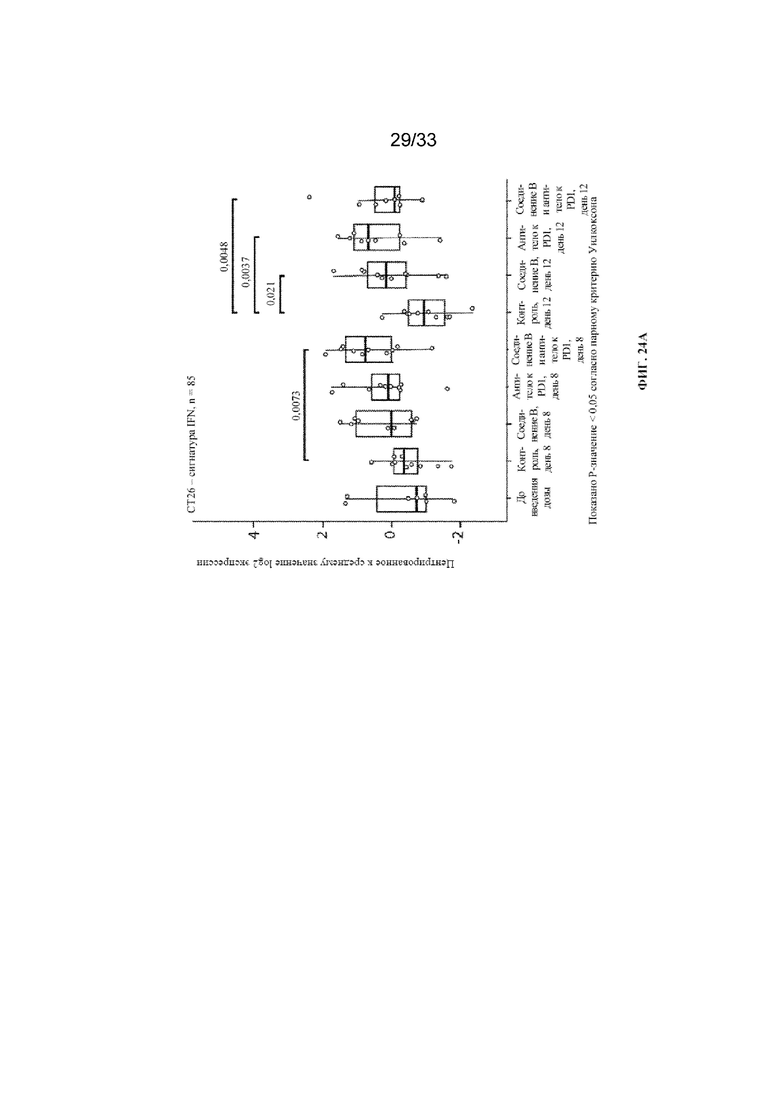
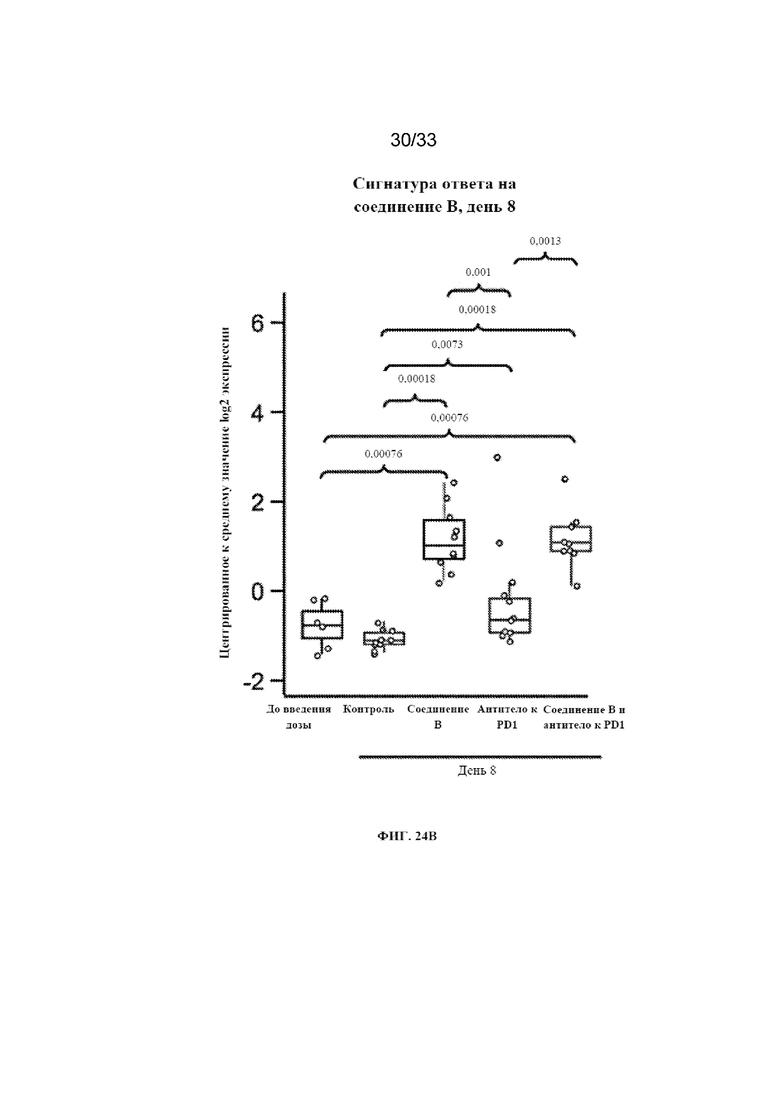
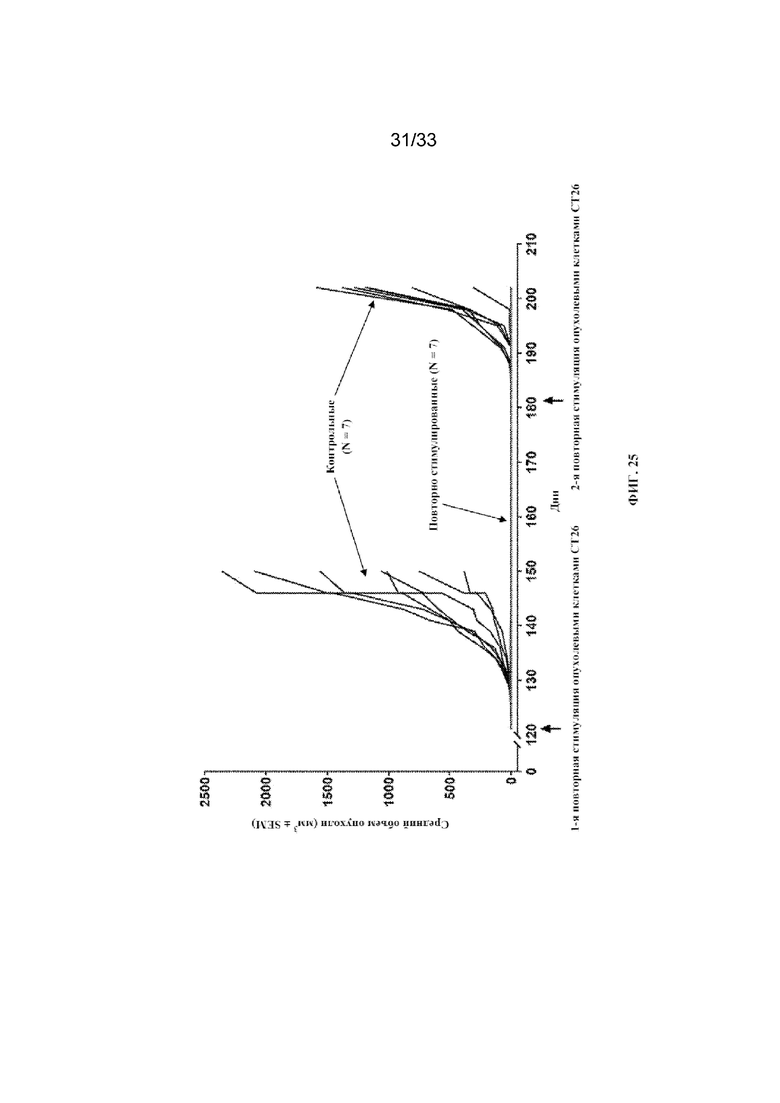
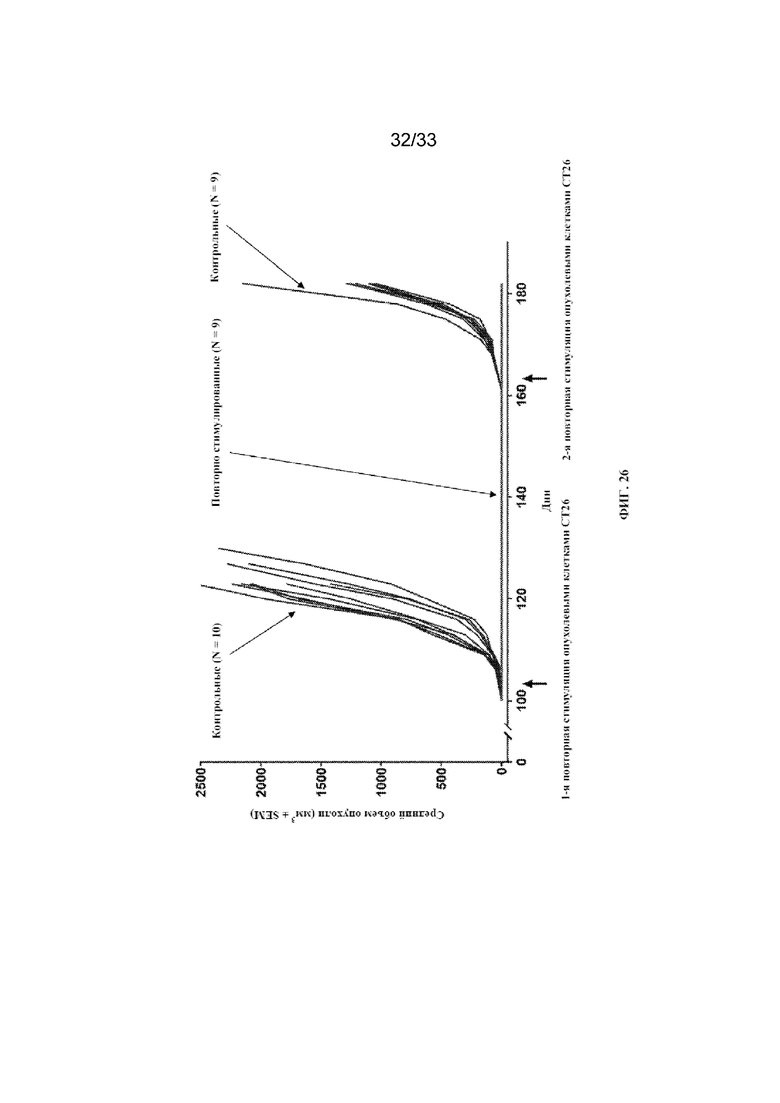
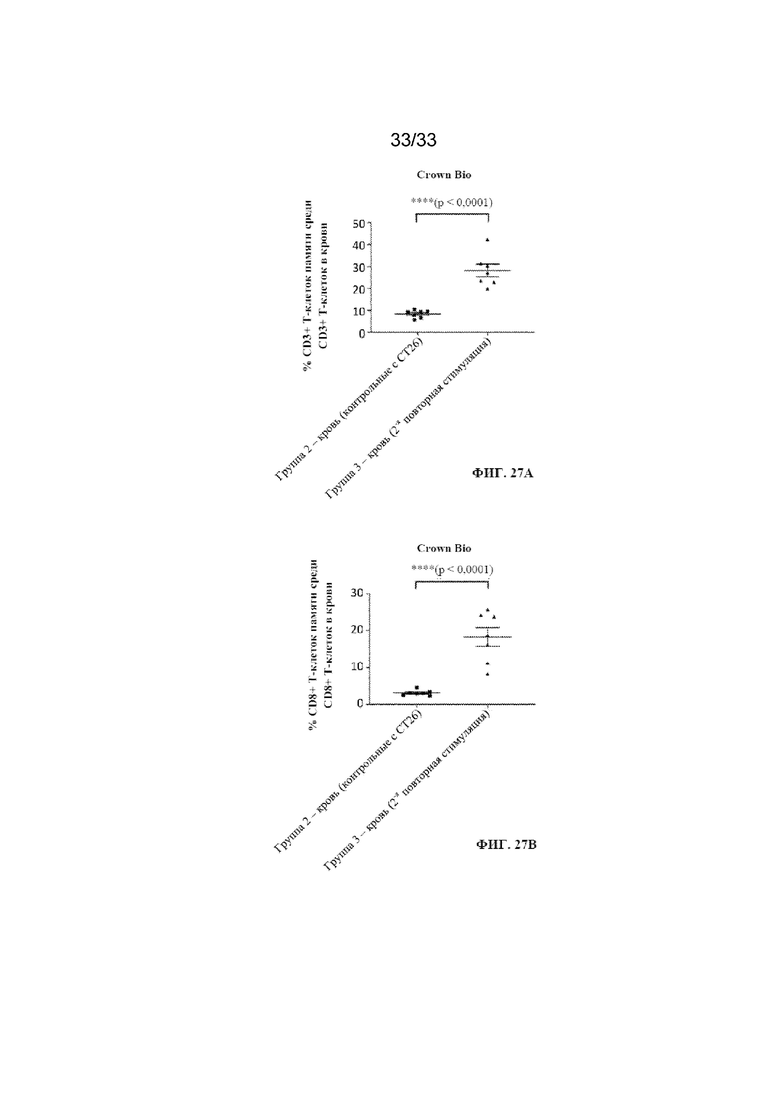
Настоящее изобретение относится к области биотехнологии и может быть использовано в медицине. Предложен способ иммунотерапии различных пролиферативных заболеваний, включающий введение субъекту комбинации конъюгата IL-2 с DBCO–ПЭГ и анти-PD-1 антитела. В материалах настоящей заявки показано преимущество применения конъюгата IL-2 в комбинации с ингибитором PD-1 для лечения рака по сравнению с применением указанных терапевтических агентов по отдельности. 17 з.п. ф-лы, 27 ил., 35 табл., 17 пр.
1. Способ лечения рака у нуждающегося в этом субъекта, включающий введение субъекту терапевтически эффективного количества (a) конъюгата IL-2 и (b) одного или нескольких ингибиторов PD-1, где:
(i) конъюгат IL-2 содержит аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 50, в которой остается [AzK_L1_PEG30кДа] из SEQ ID NO: 50, где [AzK_L1_PEG30кДа] имеет структуру формулы (XII);
(ii) конъюгат IL-2 содержит аминокислотную последовательность, которая по меньшей мере на 95% идентична аминокислотной последовательности SEQ ID NO: 50, в которой остается [AzK_L1_PEG30кДа] из SEQ ID NO: 50, где [AzK_L1_PEG30кДа] имеет структуру формулы (XIII); или
(iii) конъюгат IL-2 вводят в виде фармацевтической композиции, содержащей смесь, где смесь содержит конъюгат IL-2 (i) и конъюгат IL-2 (ii),
где формула (XII) и формула (XIII) представлены ниже:
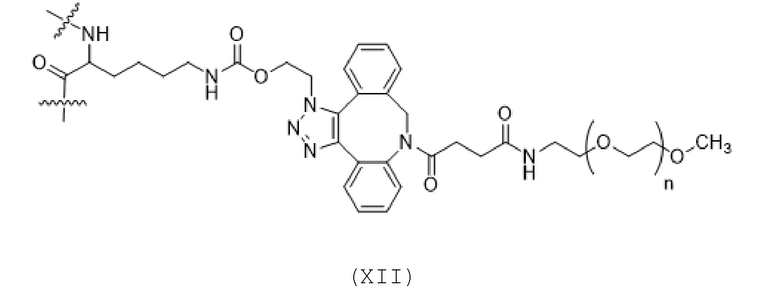
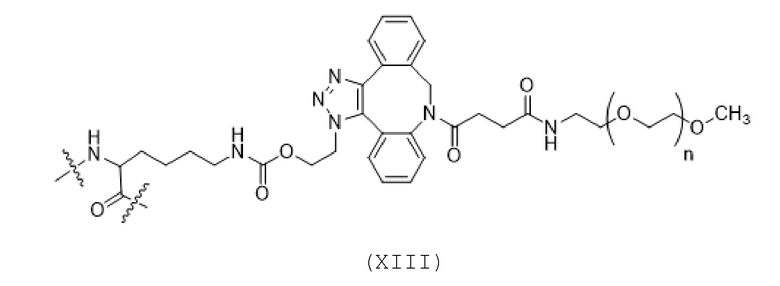
где:
n представляет собой такое целое число, что ПЭГ, имеющий структуру -(OCH2CH2)n-OCH3, имеет молекулярную массу, составляющую приблизительно 30 кДа; и
волнистыми линиями указаны ковалентные связи с первыми предшествующими аминокислотными остатками и первыми последующими аминокислотными остатками, соответственно, в SEQ ID NO: 50.
2. Способ по п. 1, где один или несколько ингибиторов PD-1 представляют собой пембролизумаб, ниволумаб или цемиплимаб.
3. Способ по п. 2, где один или несколько ингибиторов PD-1 представляют собой пембролизумаб.
4. Способ по п. 2, где один или несколько ингибиторов PD-1 представляют собой ниволумаб.
5. Способ по п. 2, где один или несколько ингибиторов PD-1 представляют собой цемиплимаб.
6. Способ по любому из пп. 1-5, где рак выбран из почечноклеточной карциномы (RCC), немелкоклеточного рака легкого (NSCLC), плоскоклеточного рака головы и шеи (HNSCC), классической лимфомы Ходжкина (cHL), первичной медиастинальной крупноклеточной В-клеточной лимфомы (PMBCL), уротелиальной карциномы, рака с микросателлитной нестабильностью, рака с микросателлитной стабильностью, рака желудка, рака ободочной кишки, рака ободочной и прямой кишки (CRC), рака шейки матки, гепатоцеллюлярной карциномы (HCC), карциномы из клеток Меркеля (MCC), меланомы, мелкоклеточного рака легкого (SCLC), рака пищевода, плоскоклеточной карциномы пищевода (ESCC), глиобластомы, мезотелиомы, рака молочной железы, трижды негативного рака молочной железы, рака предстательной железы, кастрационно-резистентного рака предстательной железы, метастатического кастрационно-резистентного рака предстательной железы или метастатического кастрационно-резистентного рака предстательной железы с дефектами ответа на повреждение ДНК (DDR), рака мочевого пузыря, рака яичника, опухолей с мутационной нагрузкой от умеренной до низкой, плоскоклеточной карциномы кожи (CSCC), плоскоклеточного рака кожи (SCSC), опухолей, распространяющихся системно в печень и CNS за пределы их первичного анатомического участка происхождения, и диффузной крупноклеточной В-клеточной лимфомы.
7. Способ по п. 6, где рак выбран из немелкоклеточного рака легкого (NSCLC), классической лимфомы Ходжкина (cHL), плоскоклеточного рака головы и шеи (HNSCC), рака ободочной кишки, рака ободочной и прямой кишки (CRC) и меланомы.
8. Способ по п. 6, где рак выбран из рака ободочной кишки.
9. Способ по любому из пп. 1-8, где конъюгат IL-2 вводят субъекту один раз в неделю, один раз в две недели, один раз в три недели, один раз в 4 недели, один раз в 5 недель, один раз в 6 недель, один раз в 7 недель или один раз в 8 недель.
10. Способ по любому из пп. 1-8, где конъюгат IL-2 вводят субъекту один раз в неделю.
11. Способ по любому из пп. 1-8, где конъюгат IL-2 вводят субъекту один раз в две недели.
12. Способ по любому из пп. 1-8, где конъюгат IL-2 вводят субъекту один раз в три недели.
13. Способ по любому из пп. 1-12, где конъюгат IL-2 вводят субъекту путем внутривенного введения.
14. Способ по любому из пп. 1-12, где конъюгат IL-2 вводят субъекту путем подкожного введения.
15. Способ по любому из пп. 1-14, где конъюгат IL-2 представляет собой фармацевтически приемлемые соль, сольват или гидрат.
16. Способ по любому из пп. 1-15, где конъюгат IL-2 вводят в дозе от приблизительно 10 мкг конъюгата IL-2 на кг массы тела субъекта до приблизительно 200 мкг конъюгата IL-2 на кг массы тела субъекта.
17. Способ по любому из пп. 1-16, где конъюгат IL-2 содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности SEQ ID NO: 50, в которой остается [AzK_L1_PEG30кДа] из SEQ ID NO: 50.
18. Способ по любому из пп. 1-16, где конъюгат IL-2 содержит аминокислотную последовательность SEQ ID NO: 50.
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
| GUPTA V | |||
| et al., Protein PEGylation for cancer therapy: bench to bedside, J | |||
| Cell Commun | |||
| Signal., 2019, v | |||
| Насос | 1917 |
|
SU13A1 |
| TANG A | |||
| et al., The challenges and molecular approaches surrounding interleukin-2-based therapeutics in cancer, Cytokine X, 2019, v | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| SAMBI M | |||
| et | |||
Авторы
Даты
2025-05-20—Публикация
2020-08-14—Подача