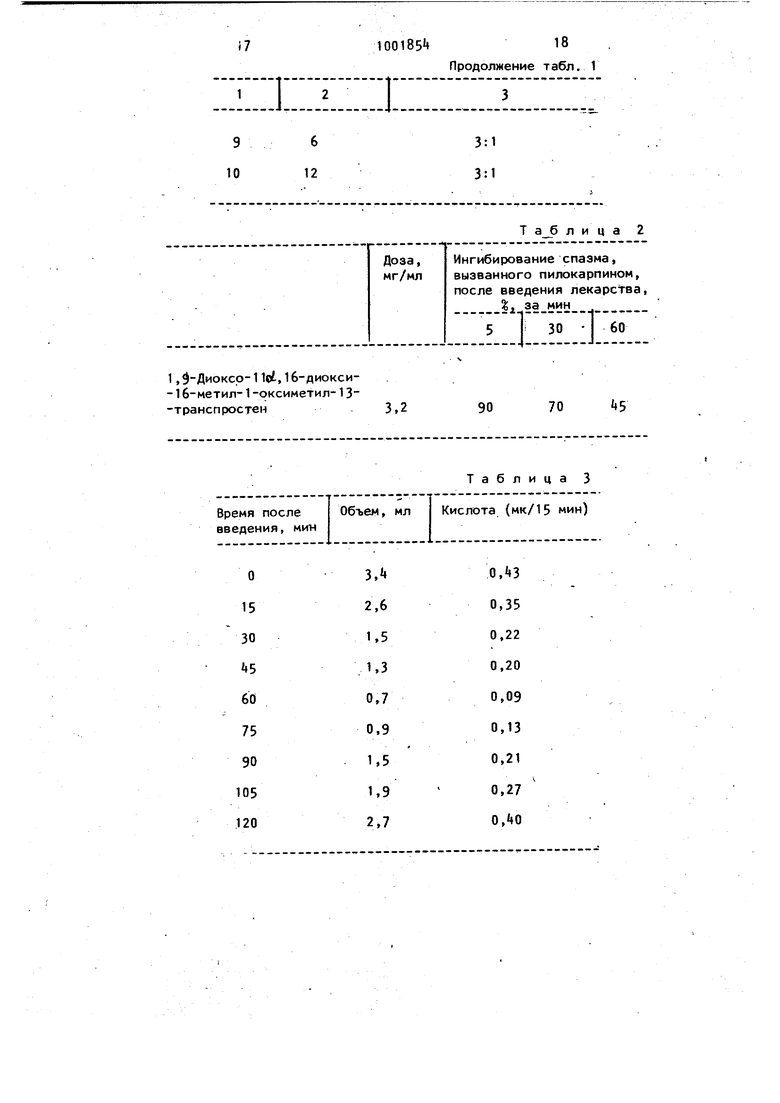
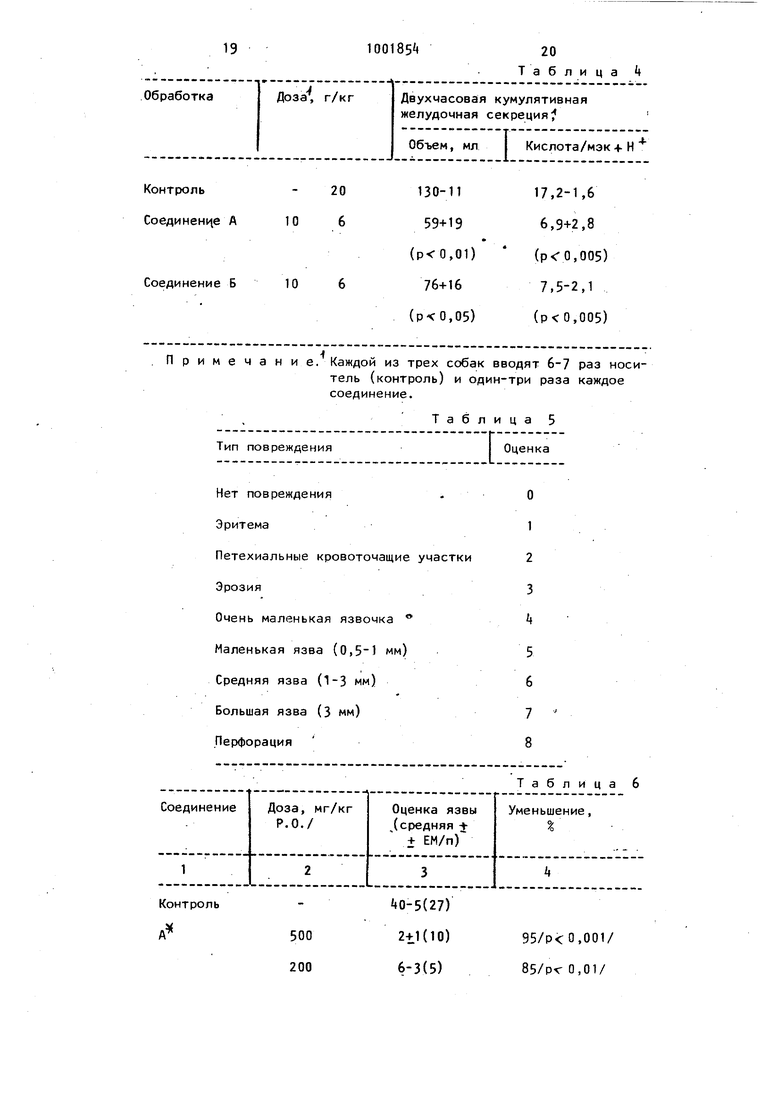
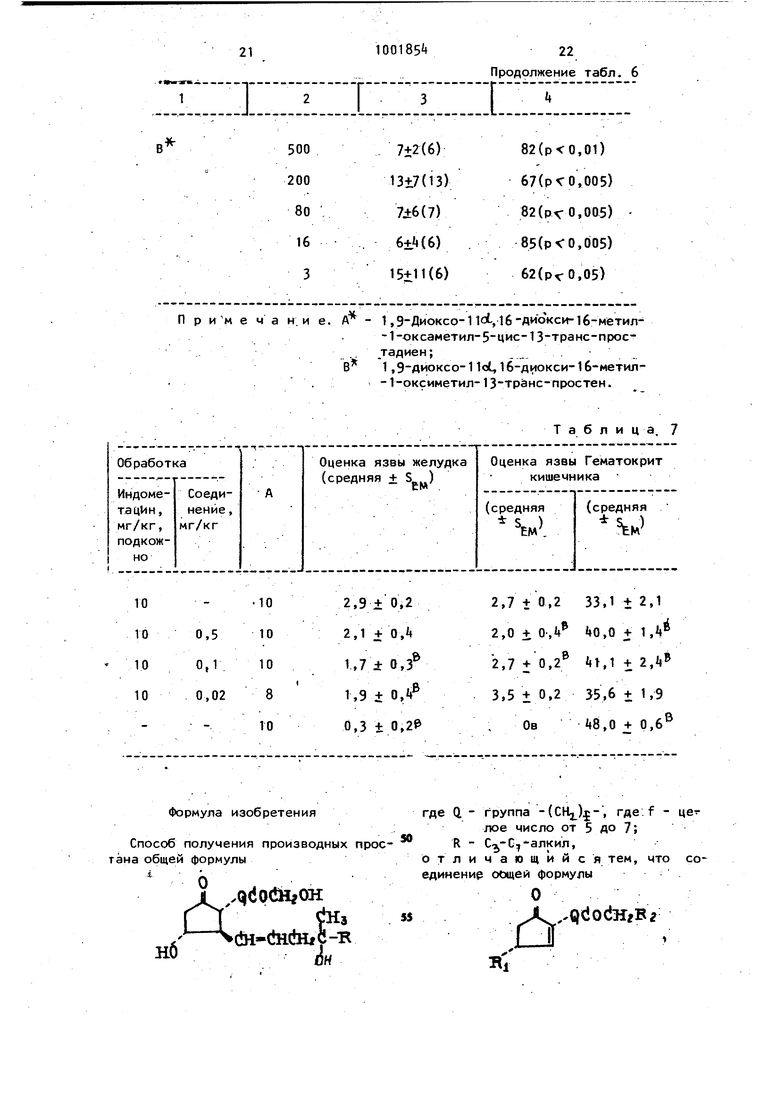
(5) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПРОСТАНА Изобретение относится к способу получения новых производных простан общей формулы О ... ;qdociH OH ЬЛ. -ciHdHjf|-K бн где Q - группа -(СНз)-, где f -цел число от 5 до 7; R С -С- -ллкйл, обладающий фар макологической активностью. Известен способ получения метило вого эфира 11-диоксипростагландина заключающийся в том, что 2-(6-Kapi6o метоксигексил)циклопент-2-енон подвергают взаимодействию с литийкупра том формулы .Iduf /г с последующим отщеплением защитной, группы 1 3Цельизобретения - разработка способа получения новых фармакологически активныхпроизводных простана общей формулы ( 1). Поставленная цель достигается тем, что согласно способу, основанному на использовании реакции получения производных простана общей формулы ( 1 ), соединение общей формулы ..р ОС1Нг,В2 (|7) где Q имеет указанные значения; К.-гидроксил или низшая алкоксигруппа;R -низшая алкоксигпуппа, подвергают взаимодействию с литийкупратом общей формулы
djHyClscl-du-clH-dii- clHgC де R и R. имеют указанные значения, и в полученном рацемическом или опти чески активном соединении общей формулыЛ .QdodHgE, г т ч ciH ciHdH ci-E С где Q, R, R, имеют указанные зн . чения, удаляют защитные группы с последующи выделением целевого продукта. Производные простана общей формулы (|) обладают потенциальной активностью как гипотенсивные, антиязвенные агенты, используются для лечения желудочной гиперсекреции и эрозии же лудка, обеспечивая защиту против уль церогенных и других желудочных затру нений, вызванных различными нестеро-идными противовоспалительными агента и, например, индометацин, аспирин и фенилбутазон, как бронхорасширяющие, противовоспалительные, абортивные родовспомогательные средства, контро лирующие оплодотворяющие агенты и ре гуляторы центральной нервной системы В сельском хозяйстве используются ка регулятор течки у коров и других домашних животных. Пример 1. Получение 4-метил- -окси-1 октина. К перемешиваемой суспензии амальгамы, полученной из 6,2.г магния и 50 мг хлористой ртути, суспендирован ной при температуре кипения в 60 мл .эфира, добавляют раствор смеси, сос. тоящий из 26 г 2-гексанона и 29,8 г бромистого пропаргйла в 65 мл эфира в течение 60 мин. После предваритель ного нагревания с обратным холодильником в течение 30 мин, полученную смесь охлаждают до О С и обрабатывают 35 мл насыщенного раствора хлорис того аммония. Смесь разбавляют эфиром и фильтруют через целит. Фильтрат промывают рассолом, сушат карбонатом калия и концентрируют. Остаток перегоняют и получают вышеуказанный продукт. П р и м 6 р 2. Получение 4-метил-4-триметилсилокси- 1-октина.
.4
(in)
:R
Li
К перемешиваемому раствору 2k г 4-метил-)-окси-1-октена и 33,3 г имидазола в 130 мл Диметилформамида при 5С добавляют 2 мл хлортриметилсилана в течение 5 мин. Раствор перемешивают при комнатной температуре 17ч и затем добавляют 600 мл гексана и 250 мл ледяной. воДы. Гексановую фазу отделяют и промывают последовательно водой и рассолом. Раствор сушат сульфатом магния и выпаривают, получают жидкость. П р и м е р 3- Получение 4-метил-4-триметилсилокси-1-(три-Н-бутил-станнил)-транс-1-октена. Перемешиваемую смесь 20 г 4-метил-4-триметилсилокси-1-октина , 28 мл три-И-бутилоловогидрида и 50 мл азобисизобутиронитрила в атмосфере азота нагревают до . После того, как начавшаяся экзотермическая реакция затихает, смесь нагревают при один час. Полученный продукт выделяют из реационной смеси. П р и м е р 4.. Получение 1-(1-метокси-1-метилэтокси)-8-Сз(-метркси-1-метилэтокси)3 -5-оксо-1-циклопентен-1-ил-2-октанона. К перемешиваемому раствору 31,2 г (130 моль) 1-гидрокси-8-(3 гидрокси -5 оксо-1-циклопентен-1-ил)-2-октанона в 190 мл , высушенного над молекулярными ситами, добавляют 7 мл 2-метоксипропена с последующим добавлением 0,1 мл соляной кислоты. Поддерживают температуру 25°С охлаждением на водяной бане. Через 30 мин по данным тонкослойной хроматограф.ии в этилацетате исходное вещество не обнаруживается. Присутствуют мелкие пятна с R.EO,5 и 0,6; большое пятно с RX 0,78. Через час добавляют еще 0,1 мл дихлоруксусной кислоты. После того, как общее реакционное время составит 2 ч, раствор разбавляют 650 мл гексана. Раствор промывают 50 мл насыщенного NaHCO-i (рассолом) , сушат (, .) и добавляют 0,05 мл пиридина. Растворители удаляют, получают А8, г (97) вещества. ПМР (СОСЦ),(Г : 7,06 (м, 1Н, СНОН); i,92 (1Н, СНО); it,00 (с, 2Н, ); 3,22 (с, ЗН, ОСН); 3,18 (с, ЗН, 5 . . OCHj); 2,62, 2,0, 2,l6 (м, 6Н, CMj,S 1,36 (м, 20H, , CHjS). ИК (четкий): 5830 мм, Примерз. Получение триметил силил-2-триметилсилоксиацетата. К раствблу 15 г (0,197 моль) гликолевой кислоты в 50 мл сухого пиридина приливают 32,3 г. (0,2 мол1 1.1, 1 ,3 гексаметилдисилазина. После перемешивания в течение 15 мин добав ляют по каплям 10,86 г (0,1 моль) три метилсилилхлорида. Смесь перемешивают 1 ч и затем фильтруют от белого осадка, который промывают петролейным эфиром. Фильтрат и промывные воды концентрируют при пониженном давлении при 30°С. Остаток перегоняют (ВЗВб с) 15 мин, получают 38 г продукта. П р и м е р 6. Получение три-триметилсилилоксиэтилена. К раствору 50,98 г (0,316 моль) 1., гексаметилдисилазина в .250 мл тетрагидрофурана добавляют при перемешивании в атмосфере аргона при по каплям 133,3 мл (0,) 2,4-М-Н-бутиллития в гексане. Затем раствор выдерживают при в течение 30 мин. Раствор охлаждают до и 58,7 г триметилсилил-2-триметилсилоксиацетата добавляют по каплям После перемешивания в течение 30 мин 3,2 г (0, моль) триметилсилилхлорида добавляют в течение 10 мин, раствору дают нагреться до комнатной температуры в течение 30 мин. Растворитель удаляют при пониженном давлении Остаток смешивают с равным объемом петролейного эфира и фильтруютот суспензии хлорида лития. Растворитель удаляют и остаток перегоняют (70-75 С уЦ мин), получают 6,б5 г продукта. Примеру. Получение 2-С6-(хлорформил)гексил -циклопент-2-ен-1-она. К суспензии 1,9 г ( 0,08 моль гид рида натрия в 100 мл тетрагидрофурана добавляют при перемешивании под ар гоном по каплям раствор 17 г (0,08 моль) 2-(6-кapбoкcигeкcил)-циклoпeнт-2-eн-oнa в 160 мл тетрагидрофурана. Затем смесь перемешивают 1 ч 15 мин, охлаждают до и добавляют 13 мл окс,алилхлорида. Смесь перемешивают при 0°С в течение 30 мин и при комнатной температуре 30 мин. Раствор разбавляют 500 мл эфира и фильтруют через целит. Растворитель удаляют из фильтрата и остаток дважды экстрагиру ют горячим гексаном. Гексан удаляют, получают 16 г продукта. П р и м е р 8.. Получение 2-(8-гидрокси-7 оксо-октил)-цикг1Опент-2-ен-1-она. Смесь 6,3 г 2- 6-(хлорформил)гексил -циклопент-2-ен-1-она и 16 г трис-триметилсилилоксиэтилена перемешивают под аргоном при 90-100 С в течение 1 ч. К ЭТОЙ смеси добавляют 25 мл диоксана и 10 мл 0, соляной кислоты. Смесь нагревают при 8оС в течение 30 мин. Смесь вливают в pacqoл и экстрагируют эфиром. Эфирнмй раствор промывают насыщенным .бикарбонатом натрия и сушат сульфатом магния. Растворитель удаляют и остаток хроматографируют на сухой колонке селикагеля, элюируя эфиром, содержащим 2% уксусной кислоты, получают 1,7 г прэдукта (Rf 0,5). П р им е р 9. Получение 1,9 диокco-11Q 1б-диокси-1б-метил-1-оксиметил-13 транс-простена. А. К перемешиваемому раствору г (150 моль винилолова, из которых 120 моль являются траяс-изомером) Е-1 -три-Н-бутилстаннил- -метил- -три- метилсилилокси-1-октана в 120 мл тетрагидрофурана при вначале добавляют 60 мл 2,0 МН -бутиллития в гексане в течение 5 мин, чтобы температура была менее . Полученный раствор светло-янтарного цвета за 10 мин нагревают до и поддерживают эту температуру в течение 2 ч. Затем раствор снова охлаждают до -7оС для использования в методике по пункту С. хорошо перемешиваемому раствору пентина меди (17,25 г, 132ммоль) добавляют мл (около 3,1 г или 26 ммоль) свежеперегнанного триамида гексаметилфосфора. Спустя 20 мин добавляют 300 мл эфира. Полученный прозрачный светло-желтый раствор охлаждают до за 60 мин. С. К раствору виниллития, полученному по пункту А при , добавляют предварительно охлажденный раствор комплекса меди, полученногопо пункту В, с помощью иглы сдвойным наконечником за 10 мин, чтобы температура; не поднималась выше -65 С. Полученный, раствор светло-янтарного цвета перемешивают при в течение 60 мин. D. К перемешиваемому раствору, полученному по пункту С при , вначале добавляют раствор 23,07 г (60,0 ммоль) 1-(1-метокси-1-метилэтокси) -8-f 3- (мето.кси-1 -метилэтокси) -5-оксо-1-циклопент-1-ил32-октанона в 50 мл эфира за 10 мин так, чтобы температура не снижалась ниже -б5 С. Шприц и ампулу с мембраной промывают 10 мл эфира. Спустя 5 мин раствор светло-янтарного цвета нагревают до за 10 мин. Раствор перемешивают при ,С в течение 1,5 ч, а затем нагревают до за 30 мин, после чего снова охлаждают до -78°С. Ре акцию- прекращают, добавляют раствор ,4 мл (около ммоль) ледяной уксусной кислоты в 100 мл эфира. Образовавшийся осадок перемешивают магнит ной мешалкой. E.Полученную смесь перемешивают с 750 мл эфира и ледяной смесью 480 мл 1 н. НС1 и 240 мл насыщенного МНлС1. Полученную смесь интенсивно перемешивают при в течение 5 мин Водные фазы выделяют и экстрагируют 350 мл эфира. Объединенные органические фазы промывают последовательно 2 раза по мл ледяной 1 н. НС1, мл полунасыщенного рассола, 24 О мл смеси 1:1 насыщенный рассол/насыщенный NaHCOo, 2kQ мл полунасыщенного солевого раствора и 3 раза - насыщенным рассолом. Раствор высушивают суль фатом магния, фильтруют через небольшой слой целита и концентрируют в вакууме при , получают 108 г подвижной свет)ю-желтой жч дкости. F.Продукты, полученные по пункту Е, в этом опыте (60 ммоль; 108 г) и в аналогичном опыте (57,7 моль; 103 г) объединяют. Полученное вещество (211 г) обрабатывают раствором, полученным из мл ледяной кислоты, 70 мл тетрагидрофурана и 235 мл воды. Полученный раствор перемешивают при в течение 60 мин. В смесь добавляют 600 мл толуола. Затем в роторном испарителе при температуре око ло ЗСРС отгоняют брО мл дистиллята. Колбу с раствором присоединяют к стан дартной вакуумной установке для перегонки с приемником, охлаждаемым смесью сухой лед-ацетон. Полученный раст вор разбавляют 600 мл толуола. Затем отгоняют 600 мл дистиллята при И давлении 0,1 мл водн. ст. Раствор разбавляют 600 мл толуола и затем концентрируют до объема около 1000мл Полученный раствор разбавляют 600 мл толуола (всего используют 2700 мл толуола) . Полученный раствор выпаривают, получают 19 г смеси бесцветного| тетрабутилолова и масла цвета темного янтаря. G. Вещество, полученное по пункту F, помещают сверху на слой силикагеля Mallinckrodt АГ СС- (385 г) в стеклянной колонке размером 5,830см Колонку промывают 2500 мл гексана для удаления оловосодержащего соединения, а затем 000 мл этилацетата, чтобы извлечь все нерастворимое в гексане вещество, находящееся в колбе и на боковых стенках колонки с силикагелем в верхней части. При испарении первых 3250 см элюата этилацетата получают 77, г янтарного масла. После испарения последних 750 см элюата получают 0,1 г янтарного масла (всего 77,5 г). Н. Хроматография. В колонку диаметром 5, см,, заполненную смесью гептанэтилацетат (2:1), помещают 970 г силикагеля марки Mallincrodt АГ СС-7. Колонку оставляют на ночь. Эту колонку (размеры ее 5,-98 см) используют для очистки большей части продукта по пункту С (71 г). Полученное вещество (71 г) растворяют в смеси гертан-этилацетат (2:1), 250 мл и 50 мл этилацетата, необходимого для получения раствора. Раствор проявляют на описанной колонке. Элюирование проводят при небольшом избыточном давлении азота для достижения скорости потока около 3 л/ч. Фракции, выходящие из колонки, исследуют методом тех, используя систему растворителя 20:1 этилацетат-метанол. Пластины, проявляют, запыляют раствор 2 ,А-динитробензола, а затем раствор ацетата меди (2) и нагревают. Колонку элюируют смесями гептанэтилацетат в последовательности, приведенной в табл. 1. Собранные фракции объема около 1500-2000 мл исследуют с помощью ТСХ. Выделяют продукт, полученный промыванием смесями, соответствующих составов (6-10 в табл. 1) в количестве 16,9 г. Соединения общей формулы (1) являются более специфическими по силе действия, вызывают простагландиноподобные биологические реакций и/или имеют значительно большую длительность биологической активности. Например, 11-диокси-ПГЕ соединения общей формулы (|) относительно слабо стимулируют гладкую мускулатуру, ViMeют увеличенную стабильность и удлиненный срок действия. По сравнению с известными простагландинами соединений общей формулы (I) можно эффективно вводить орально, подъязычно, интравагинально, внутримышечно или подкожно инъекциями или инфузиями. Это облегчает поддержание равномерных уровней соединений в теле более елабыми, короткими или маленькими дозами и делает возможным введение препарата самим пациентом. Соединения общей формулы (1) используют как бронхорасширяющие агенты для лечения астмы и хронических бронхитов в виде аэрозолей от 10 г до 10 мг/мл фармацевтически пригодного жидкого носителя). По сравнению с природными простагландинами ПГА и ПГЕ эти соединения, в частности, отличает продолжительность действия. ПГЕ и ПГА соединения .используют для уменьшения и контроля избыточной желудочной секреции, в результате чего уменьшается или устоаняется желудочная эрозия или образование желудочно-кишечной язвы и ускоряется вылечивание язв, уже име ющихся в желудочно-кишечном тракте. Для этой цели соединения впрыскивают или вводят инфузией внутривенно, подкожно или внутримышечно (доза инфузии от 0,1 до 500 мг/кг веса тела в минуту; общая дневная доза инъекции или инфу зии от 0,1 до 20 мг/кг веса тела). Эти соединения применяют в сочетании с различными нестероидными противовоспалительными агентами, такими как аспирин, фенилбутазон, индометацин и т.п. , чтобы свести к минимуму ульцерогенные действия последних. ПГЕ и ПГА соединения общей формулы (I) стимулируют эпидермальную пролиферацию и кератинизацию, благодаря чему ускоряют заживление поврежденной кожи, например при ожоге, ранении или хирургической операции. Кроме того, ПГА соединения способствуют быстрому прирастанию пересаженной кожи. I- , Для этих целей предпочтительно местное применение соединений на или вблизи участка, где желателен рост клеток и образование кератина, в виде аэрозольной жидкости, микронизированного порошка для распыления изотонического водного раствора (в случае влажных перевязок) или в виде крема, лосьона и мази в сочетании с обычными разбавителями. В некоторых случаях когда имеются значительные потери жидкости (экстенсивные ожоги или потери кожи по другим причинам) эффективными являются внутривенная инъекция или инфузия, отдельно или в сочетании с обычными инфузиями-крови, плазмы или их заменителей. Возможно также введение подкожное или внутримышечное, оральное, подъязычное, буккальное или вагинальное. Вблизи участка применяют влажные повязки при ожогах кожи второй и/или третьей степени площадью 5-25 см использованием изотонического водного раствора соединения. Простагландины применяют в сочетании с антибиотиками, в частности гентамицином, неомицином, полимиксином В, бацитрацином, стрептомицином и окситетрациклином; с другими антибактериальными препаратами, такими как Солянокислый мафенид, сульфадиазин, фуразолийхлорид и нитрофуразон; и с кортикостероидами, такими как гидрокортизон, преднизолон, метилпреднизолон и фторпреднизолон, каждое из них используется в обычных для их индивидуального применения концентрациях. ПГА соединения, их производные и соли повышают приток крови кепочкам, увеличивают объем и содержание электролита в моче, поэтому их применяют для снятия почечной дисфункции, особенно в случаях затрудненного непарного почечного притока крови, например почечно-печеночного синдрома. В случае избыточной или несоответствующей секреции гормона АДН диуретичес-i кое действие этих соединений еще более высокое. Вазопрессивное действие этих соединений проявляется в анефретическом состоянии. ПГЕ соединения используются как местные сосудорасширяющие препараты, а также при необходимости ингибировать скопление тромбоцитов, чтобы снизить их адгезионный характер, снять и предохранить образование тромбов. Эти соединения применяют, например, для лечения и предупреждения инфарктов миокарда и послеоперационного тромбоза. Соединения вводят внутривенно, подкожно, внутримышечно и в виде стерильных имплантатов продолжительного действия. Для быстрой реакции, особенно в состоянии беременности, предпочтительным является внутривенный способ введения. Исполь-. 1110 зуют дозы от 0,005 до 20 мг/кг веса тела в день. Ингибирование скопления тромбоцитов in vitro осуществляют по следующей методике. Человеческую плазму, богатую протеином, инкубируют с модифицированным раствором тирода (0-50%). ПГЕ соединения вводят в различных концентрациях и после :5 мин инкубации добавляют такой агрегирующий агент, как аденозиндифосфат или коллаген. Изменение оптической плотности (светорассечение) регистрируют глазом и отмечают ингиби рование (-) и отсутствие ингибирования (+). Испытуемые соединения считаются активными, если они ингибируют скопление тромбоцитов, вызванное аденозиндифосфатом или коллагеном в концентрации 0,025 мг/мл или менее, в течение мин. Например, 1 ,9-диоксо-15 окси-1-оксиметилен-13 транс-простен показывает ингибирование скопления тромбоцитов, вызванного как аденозиндифосфатом, так и коллагеном, при концентрации 0,025 мг/мл. ПГЕ соединения оказывают бронхорасширяющее действие, как определено в тексте с использованием анестезированных собак с искусственным дыханием и испытывающих непрерывный респираторный спазм, вызванный пилокарпином . Используют дворняжек любого пола, весящих кг. Им вводят подкожно солянокислый морфин(1,5 мг/кг). Внутривенную перфузию (объем) хлоразола начинают через полчаса после инъекции морфина таким образом, чтобы в течение 15 мин ввести 60 мг/кг. В течение всего эксперимента поддерживают непрерывную перфузию 10 мг/кгСобаке делают искусственное дыхание с помощью Стерлинг-насоса со скоростью 20 вдохов в минуту. Объем устанав ливают в соответствии с весом животного. Все измерения выполняют на собаках, положенных навзничь на подогреваемый V-образный стол. Получают кураризацию сукцинилхолинхлоридом, используя исходную инъекцию 3 мг/кг в течение 3 мин с последующей непрерывной перфузией 0,1 мл/кг мин. Респираторный спазм инициируют на чальной инъекцией 400 мг/кг солянокислого пилокарпина 5 мин. Возможно уве личение или уменьшение дозы солянокислого пилокарпина в зависимости от наблюдаемого действия на сопротивле54ние воздушного пути. Перед началом непрерывной перфузии солянокислого пилокарпина отсрочку 15 мин наблюдают при дозе 4 мгк/кг мин, чтобы поддержать постоянный спазм во время испытания. Вводят металлическую канюлю и закрепляют после трахеотомии. Катетеризуют для впрыскивания различных агентов две головные и две бедренные вены. Бедренную артерию катетеризуют, чтобы измерить системное давление крови. Пищеводный баллон (11- 2,5 см) вводят в нижнюю треть азофага для измерения эндорагического давления. Измерение потока воздуха осуществляют с помощью пневматахографа Флейша, связанного с трахейной трубкой. Транслегочное давление измеряют следующим образом. Трахейную канюлю аксиальной трубкой из нержавеющей стали (1,5 мм), которая закрыта на конце и защищена на расстоянии 2,5 см от конца канюли. В последнем сегменте просверлены три полости диаметром 1 мм. Трубка, используемая для измерения трахеального давления, связана с одной или двумя камерами дифференциального датчика Санборн 2б7 В/С. Другая камера связана с пищеводным баллоном с помощью полиэтиленового катетера такой же длины и характеристик, как и у баллона. Воздушный поток из пневмотахографа Флейша измеряют при помощи дифференциального датчика Санборн 270. Объем вдох-выдох получают электронным интегрированием сигнала потока с использованием PC интегратора. Системное и легочное давление крови регистрируют с помощью датчика давления Санборн В/С или 1280 В. Все эти параметры регистрируются на полиграфе Санборна. Транслегочное давление и объем вдоха-выдоха представляют в прямоугольных координатах на осциллоскопе. Испытуемы соединения вводят аэрозольным путем. Микрораспыпительный респиратор Бёрдд Марк 7 соединяют с металлической канюлей сразу после пневмотахографа. Струя испытуемого соединения в аэрозоле Р вытекает под давлением 2 кг/см, попадая в микрораспылитель как раз во время одного цикла вдыхания. .Мирокраспылитель установлен на респираторной трубке во время порыва струи. Взвешивают непосредственно до и после введения, что.13 100 бы определить количество .введенного испытуемого соединения. В табл. 2 показан процент инг1 ирования спазма, вызванного пилокарпином, для некоторых соединений по изоб ретению. Каждой собаке вводят примерно 50 мг раствора. - . Используют неанестезированных беспородных собак, весом 10-15 кг. Живот ные имеют хирургически выполненный мешок, не содержащий нервов, который осушают под действием силы тяжести через титановую канюлю. Эти животные приучены стоять спокойно в опоре Павлова. Желудочную секрецию стимулируют с очень низкой скоростью, давая стабильную секрецию ( от максимальной с кислым фосфатом гистамина, 3050 г/кг«ч). При такой стимуляции стабильный выход желудочного секрета может поддерживаться в течение 3ч. Во -время изучения секреции постоян но собирают желудочный сок,и создают объединенную 15-мийутную коллекцию. Определяют собранный объем, рН и титруемую кислотность. Кислоту определяют титрованием аликвота желудочного обравца 0,1 н. раствором едкого натра до рН 7,0, используя автоматический титратор. Лекарства вводят на основе субмакс мальной стимуляции желудочной секреции результаты сравниваются с контрольными исследованиями секреции без использования лекарства. Лекарство вводят оральным путем в главный желудок. Этот путь легко осуществим и не допускает скоплений желудочного сока. Например, одно из ПГЕ соединений 1 ,Э Диоксо-1 lol., 16-ДИОКСИ-16-метил-1-оксиметил-5-цис-13-транс-простадиенвводят в желудок одной из собак дозой 100 мг/кг. Объем и титруемая кислотность желудочного сока после введения 1 00 Mf/к приведены в табл. 3 (средние величины четырех испытаний на одну собаку), Секреция желудочной кислоты в фистуле собаки. Трем беспородным собакам (20-32 кг вставляют канйли из нержавеющей стали в наиболее зависимую часть брюшного желудка и выводят наружу через живот для сбора желудочных секретов. Собаки приучены стоять спокойно в опоре Павлова и во время последующего изучения секреции находятся в сознании Действие 1,9 Яиоксо-1 Ы, 1б-диокси-16-метил-1-оксиметил-13 транс-простена (А) и 1,9 Диоксо-По1-, 16-диoкcиr 16-метил-1-оксиметил-5 цис-13 транс-простадиена (Б) на секрецию желудочной кислоты а в приготовленной фистуле собаки показано в табл. Л (после 26 ч поста секреция желудочной кислотгы субмаксимально стимулирована, .начинается через Бмин после введения лекарства, используется постоянная внутривенная инфузия кислого фосф1та гистамина - 0 г/кг/ч). Вызы.вание язв. Самцов крыс Спарг-Дайлей Дер шд (лаборатория Локк-Эрикон, Майвуд, Иллинойс), весящих 150-200 г, заставляют поститься и обеспечивают питьевой водой за 16-19 ч до начала испытания. Крысам орально вводят соединение или носитель (приблизительно 0,5 мл}, а затем сажают в клетки типа Волльмана. Через 5 мин после введения лекарства животных погружают (хвостом вниз) до уровня плеч в водяную баню температурой на 100 мин. В конце этого животных обезглавливают н их желудочки быстро вырезают с примерно 5 мм каждого эзофага и двенадцатиперстной кишки. Срезанный под тупым углом желудок вскрывают по наибольшей кривизне, начиная с верхушки рубца через железистую слизистую в привратник желудка и открывают кусочек двенадцатиперстной кишки вдоль края. Обрезки удаляют из желудка, промывая солевым раствором при комнатной температуре и осторожно промокают его марлей или фильтровальной бумагой. Затем желудок раскладывают слизистой вверх на регистрационной карте или другом аналогичном материале. Оценка повреждения Подсчитывают повреждения с помощью освещенного увеличительного стекла (для общего подсчета повреждений). Отметка для каждого повреждения дана в табл. 5Очень большие (по площади) неперфорированные язвы часто видны, имеют диаметр больше 3 мм и оценены как кратные 7. Например, язва диаметром 3 мм имеет площадь 7,1 мм . Язва размером 9 мм, имеет площадь 36 мм и, следовательно, является эквивалентом 5-и язвам с оценкой 7. 1510 Действие простагландинов на язвы, вызванные стрессом (погружением) у крыс, показано в табл. 6. Вызванные индометацином язвы у крыс Самцов крыс Вистар (Ройал Харт, Нью Хёмптон, Н.И), весящих г, распределяют на контрольную и обрабатываемые группы (5 крыс в группе) и каждую крысу сажают в клетку. Период испытания 52 ч. В течение первых 33 ч крысам дают в избытке пищу и питьевую воду, но затем заставляют поститься в течение ночи перед умерщвлением. Индометацин суспендируют (А мг/мл) в 1, растворе крахмала в фосфатном буфере (КфБ.Р). 115,57 растворяют в количестве 10 мг/мл в этаноле, а затем разбавляют в КфБР до концентра ции 0,1 мг/мл или до более низкой кон центрации, какая требуется. Суспензию индометацина вводят подкожно (10 мг/кг суспензию простагландина дают в количестве 0,5 мг/кг или менее на день О и 1. Крысы получают только одну дозу простагландина и индометацина в день спустя 2, 6 ч их убивают хлороформом. Желудки вырезают, вскрывают по наибольшей кривизне и осторожно промывают а чашке с водой. Затем их раскладывают слизистой вверх и прикалывают к одинаковым корковым пластинам размером 2,5 дюйма в диаметре, пронумерованным на обороте. Желудки произвольно оценивают в со ответствии со следующей шкалой (Ю): 0- норма; 1- петехиальные кровоточащие участки или очень маленькие язвочки; 2- одна или две маленькие язвочки или кровоточащая эрозия; 3- большие площади кровоточащей эрозии или язв малого размера; - массивные площади кровоточащей эрозии или много язв, главным образом больших. Кишки также удаляют и исследуют на ичие язв, которые оцениваются в соетствии со шкалой, приведенной ни0- норма; 1- слизистая тонкая, петехиальные кровотечения; 2- свищи, когда кишки надуваются воздухом; 3 малые язвы. Кишки более хрупкие, чем нормальные, разрывы вдоль линии прикреплений брыжейки, при удалении; 4 - много больших перфорированных язв, слипания, кишки кровоточащие и очень хрупкие, легко прорезаются- и не могут быть удалены без повреждений. Сортировка. Действие 1,9 Диоксо-1 lei, 16-диокси-метил-1-окси-метил-13-транс-проса на язвы, вызванные индометациу крыс, показано в табл. 7Таблица









7 8
1:1 Этилацетат-гептан
3:2 2:1 1 О
15 30 60 75 90
105 120
0, 0,35 0,22 0,20 0,09 0,13 0,21 0,27 0, :i:;: ::::i;::::i:::::::::i:::;:::: 9 63:1 10 123:1 , -Диокср-1Ы, 16 яиокси16-метил-1-оксиметил-13транспростен3,29070 tS Время после Объем, мл Кислота (мк/15 мин) введения, митн Продолжение табл. 1 Т лица 2 Доза, Ингибирование спазма, мг/мл вызванного пилокарпином, после введения лекарства, %j: 5 J 30 60 ТаблицаЗ Обработка Доза, г/кг Двухчасовая Контроль - 20 130-11 Соединение А 10 6 59+19 Соединение Б 10 6 76+16 . Примечание. Каждой из трех собак тель (контроль) и оди соединение. Тип повреждения Нет поврежденияЭритемаПетехиальные кровоточащиеучастки Эрозия Очень маленькая язвочка Маленькая язва (0,5-1 мм) Средняя язва (1-3 мм) Большая язва (З мм) Перфорация « I BBflBHKIM ««. « Доза, мг/кг Соединение P.O./
Контроль
500 200 желудочная с Объем, мл (,01) (,05) Табл Оценка язвы средняя :}: + ЕМ/п)
,001/ 85/Рг 0,01/ Таблица кумулятивная екреция I Кис лота/мэк-f Н 17,2-1,6 6,9+2,8 (,005) 7,5-2,1 (,005) вводят 6-7 раз носин-три раза каждое ица 5 Оценка О 1 . 2 3 k 5 6 7 8 «IH «.. .«н Таблицаб Уменьшение, Примечание. А В. Формула изобретениягде Способ получения производных простана общей формулыот 1.един ,хЧ({0(йгОН J .yaiS 55 (1н-(1н(н с-11
Таблица, 7 ; 1,9-Диоксо-11 A,l6-Диoкcи-16-мeтил-1-оксаметил-5 цис-13 транс-прос тадиен;. 1,9-Диoкco-11ol,16-диoкcи-16-мeтил-1-оксиметил-13 транс-простен. Q, группа {СН)-, rfle.f - цег лое число от 5 до 7; R - С -С -алкил, личающийся тем, что соение оощей формулы . . О - . : А ,Q(JO( Г ц 1
231001851 2 4
где Q имеет указанные значения; R -низшая алкоксигруппа,
R -гидроксил или низшая алкокси- подвергают взаимодействию с литийкупгруппа;ратом общей формулы
{
(i3H7Cieci-( | LL где Ли R имеют указанные значения, и в полученном рацемическом или оптически активном 1 соединении общей формулыI оНпгНт R JI хЧСи1,лглг Г л СНз 4fJH( - J{, .L
Нз ( 4
9 где Q, R, R и R. имеют указанные знаЮчения, удаляют защитные группы с последующим выделением-целевого продукта. Источники информации принятые во внимaниJe при экспертизе ,5 1. Kluge A.F. et al. Synthesis of Prostaglandins Models and Prostaglandins bv Conjugate Add.ltion of a Functionalized Organocopper Reagent.-tj. Am. Chem. Soc., 1972, v. ЭЦ, p. 782.
Авторы
Даты
1983-02-28—Публикация
1978-12-08—Подача