(5) СПОСОБ ПОЛУЧЕНИЯ -ЗАМЕЩЕННЫХ ПРОИЗВОДНЫХ ИМИДАЗОЛИД 1Н-2-ОНА 31 .) 5(3 Фенилметокси- -метоксифeнил)-мeтилeнj-2,,-имидaзoлидинoн. 24,23 г (100 ммоль) 2-фенилметокс -4-метоксибензальдегида и 10,01 г гидантоина (100 ммоль) нагревают в смеси 38 мл безводной уксусной кисло ты е 19)5 г безводного ацетата натрия, при встряхивании, при 140 С. Полученный прозрачный раствор при 15В-1б2 С кипятят 2,5 ч при действии обратного холодильника, затем охлаждают и выливают в250 млледяной воды. Полученная смола примерно через 30 мин выделяет кристаллы. Кристаллы отфильтровывают, промывают дважды 50 мл воды, дважды 50 мл этанола и, в заключение, дважды 50 мл простого эфира. Получают 14,75 г (45,5) продукта, т.пл. 249-251С. Элементный анализ. Вычислено, : С 66,66; Н 4,97; N 8,64. (Мол.мо 324,34) Найдено,%: С 66,33; Н 5,22; N 8,45. S} 5-L(З-Фенилметокси-4-метоксифенил)-метил -2,4-имидазолидинон. 34,43 г полученного продукта (100 ммоль), суспендируют в 200 мл воды. К суспензии добавляют 43 мл 10 Н. раствора гидрата окиси натрия. Затем в реакционную смесь при вносят при перемешивании в течение 45 мин 342 г 2%-ной амальгамы натрия Во время добавления температуру выдерживают на уровне 50-58°С, применяя охлаждение льдом. Полученный про зрачный раствор совместно с амальгамой натрия перемешивают дополнительно 45 мин при 50с. После этого раст вор декантируют от ртути, ртуть дваж ды промывают 30 мл воды. Объединенны водные фазы охлаждают до минус 10 С и затем подкисляют 60 мл концентрированнои хлористоводородной кислоты при перемешивании, обращая при этом внимание на то, чтобы температура не превышала +50°С. После 10 мин выдерж ки выпавшие в осадок кристаллы отфильтровывают и дважды промывают 100 мл воды о Отфильтрованный продукт растворяют в 350 мл хлороформа и про мывают раствором бикарбоната натрия до нейтральной реакции. Раствор высушивают над безводным сульфатом маг ния и упаривают в вакууме. К остатку добавляют 300 мл бензола и снова упа 56 4 ривают. Остаток после упаривания растирают с 80 мл эфира, после 30 мин выдержки отфильтровывают кристаллы и промывают 30 мл эфира. Получают 23,62 г (72,41) продукта, т.пл. 147-149°С. Элементный анализ. ВычисленоД: С 66,25; Н 5,5б; N 8,58 Н (Мол.м. 326,35) Найдено Д: С 66,25; Н 5,6l;N 8,39 S ) (3-Фенилметокси- -метоксифенил)-метил т 2-имидазолидинон. 19)0 г (500 ммоль) литийалюминийгидрида растворяют в 250 мл безводного эфира. К раствору добавляют малыми порциями в течение 30 мин 32,6 г (100 ммоль) продукта, полученного согласно примеру 16. Во время добавления суспензию кипятят при действии обратного холодильника. Затем к суспензии добавляют при перемешивании в течение 30 мин 250 мл безводного тетрагидрофурана. При добавлении тетрагидрофуран.а суспензия бурно вскипает и поэтому время от времени должна охлаждаться. По окончании добавления реакционную смесь дополнительно кипятят 30 мин при действии обратного холодильника. Избь1точное количество литийалюминийгидрида разлагают при охлаждении посредством добавления 100 мл этилацетата, после-чего реакционную смесь при перемешивании выливаЪт в 1200 мл ледяной воды. Смесь подкисляют 200 мл конц. хлористоводородной кислоты, после чего четыре раза экстрагируют 500 мл хлороформа„ Объединенные органические фазы промывают 100 мл воды, высушивают над безводным сульфатом магния и упаривают в вакууме, К смолообразному остатку добавляют 300 мл бензола и снова выпаривают о Маслообразный остаток смешивают с 100 мл эфира, при этом выпадают кристаллы, которые после 30 мин выдержки отфильтровывают и дважды промывают 50 мл эфира. Получают 26,03 г продукта (83,4), Топл. 154-1.57С (после перекристаллизации из изопропанола продукт имеет т.пл. 15б-158 С). Элементный анализ. Вычислено,%: С 69,21; Н 6,45; N 8,97. Н. , (Мол.м. 312,37) Н 6,58; Найдено,%: С 69,28; N 8,85 Пример 2. -С(3 Циклопентил окси- -метоксифенил)-метил -2-имидазолидинон. а) 3 Циклопентилокси-4-метоксибензальдегид. 15,22 г (100 ммоль) изованилина растворяют в 125 мл диметилсульфокси да. К раствору добавляют 27 г безвод ного порошкообразного карбоната калия. Суспензию перемешивают при 60 30 мин, затем в течение 1 ч добавляю 12,9 мл (120 ммоль) циклопентилброми да, причем температуру выдерживает на уровне . При этой температуре суспензию перемешивают еще 8 ч, зате охлаждают до 25°С и выливают в 500 м воды. Водную эмульсию раза экстр.агируют 10 мл эфира. Объединенные эф ные фазы дважды промывают в 20 мл .1 н. раствора гидрата окиси натрия, высушивают над безводным сульфатом магния и упаривают. Остаток смешивают с 100 мл бензола и снова упари вают.. Оставшееся масло фракционирую в вакууме. , , Получают 20,65 г (Э,0%) продукта т.кип. 136-138°С (0,01 мм рт.ст). Элементный анализ. Вычислено,: С 70,89; Н 7,32 С . (Мол.м. 220,28) . Найдено,: С 70,78; Н 7,27. 5-С{3 Циклопентилокси- -меток сифенил)-метилен -2,А-имидазолидиндион. 22,03 г (100 ммоль) полученного .продукта (пример 2а) подвергают ре:акции обмена с 10,01 г (100 ммоль) гидантоина аналогично примеру Id. Получают 13,95 г (k6,%} продукта, т.пл. 223-225°С. Элементный анализ. Вычислено,: С 63,57; И 6,00; N 9,26 . C(,H gNi04 (Мол.м. 302,33) Найдено,: С 63,15; Н 5,93; N 9,1 ё ) 5-Г(3 Циклопентилокси- -меток сифенил)-метилЗ-2,|-имидазолидиндион Исходят из 30,23 г (100 ммоль) по лученного продукта (пример 25) и работают аналогично примеру 1. Получают 20,82 г (68,51) продукта т.пл. 1А9-151°С. Элементный анализ. Вычислено,: С 63,1t; Н 6,б2; N 9,20 ЧЬ (Мол.м. 30i,35) Найдено,%: С 63,15;. Н 6, N 9,0 2.) -ПЗ Циклопенти1-|окси-Ц-метоксифенил)-метил1-2-имидазолидинона Исходят из30,3 г (100 ммоль) полученного продукта (пример 2 ) и работают аналогично примеру 1-0. Получают 21,05 г (72-,5) продукта, т.пл. 110-113 С (после перекристаллизации из ацетона т.пл. С). Элементный анализ. Вычислено,%: С 66,18; Н 7, N 9,65 , (Мол.м. 290,37-) Найдено,%: С 66,10; Н 7,80;N Э,62 ПримерЗ-гQ ) (3-Oкcи-4-мeтoкcифeнил)-мeтилJ-2-имидазолидинон. 31, г (100 ммоль) продукта, полученного аналогично примеру 1-S, растворяют в смеси 300 мл тетрагидрофурана и 150 мл метанола при температуре кипения. Раствор гидрируют в присутствии 3 г 10%-ного палладия на активированном угле при (в течение 75 мин потребляется 100 ммоль водорода). Катализатор отфильтровы вают и трижды промывают смесью 100 мл хлороформа и 100 мл метанола при температуре кипения. Фильтрат объединяют с промывной жидкостью и упаривают. К остатку после упаривания добавляют 300 мл бензола и продолжают упаривание. Остаток смешивают с 100 мл эфира, выделившиеся кристаллы после 30 мин выдержки отфильтровывают и промывают 50 мл эфира. Получают 20,38 г (91,5%) продукта т.пл. 192-202 С (после перекристаллизации из метанола 20б-208°С). d ) - (З-Циклопентилокси-4-метоксифенил)-метилЗ-2-имидазолидинон. 27,22 г (100 ммоль) полученного продукта (пример За) растворяют в 220 мл диметилоульфоксида. К раствору добавляют 27 г порошкообразного безводного карбоната калия, Суспензию перемешивают при }G мин. Затем в течение 60 мин прибавляют 12,9 г (120 ммоль) циклопентилбромида, причем температуру выдерживают на уровне 60°С, Далее суспензию перемешивают дополнительно 20 ч при 60 С, охлаждают до 2 С и выливают в 800 мл воды. Водную эмульсию экстрагируют А раза по 00 мл хлороформ;а. Объединенные органические фазы дважды промывают 50 мл 1 н. раствора гидрата окиси натрия, высушивают над безводным сульфатоммагния, затем упаривают, Маслообразный остаток смешивают с .200 мл бензола и вновь упаривают. Остаток после упаривания смешивают с 150 мл эфира, выпавший кристаллический продукт после 30 мин выдержки от фильтровывают и промывают 5Q мл эфира., Получают 21,30 г (73,%) продукта т.пл. 10 -1tJ7 C (после перекристаллизации из ацетона 115-11б С). Продукт на основании присущих ему физических показателей идентичен продукту, полученному согласно примеру 1 U Пример о Получение лечебного препарата. Таблетки, пригодные для приема внутрь через рот и служащие фармацевтическим целям, содержащие по 10 м биологически-активного вещества, имеют следующий состав, г: С(3 Циклопентилокси-4-мeтoкcифeнил)-мeтилJ-2-имидазолидинон 0,010 Крахмал пшеничный 0, Молочный сахар0,037 Карбоксиметилцеллюлоза0,006 Тальк0,005 Средний вес одной таблетки составляет О,100 г. Понижающее аппетит действие исследуют на крысах вида CFY следующим образом. Подопытных животных лишают корма на 2Ц Ц, затем дают через рот соединения и спустя полчаса- после этого дают корм до полного насыщения. Изме-ряют количество принятого корма в последующие 5 ч. Определяют также изменение веса животных и съеденное ими количество твердого, гранулированного корма, соответственно осахаренного молока или картофельных хлопьев, затем по полученным данным- выясняют значение показателя ED-50. Полученные результаты представлены в -Таблице.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения пептидов или их солей | 1977 |
|
SU664560A3 |
| Способ получения производных 2-фенил-3-ароилбензотиофена или их солей | 1976 |
|
SU701539A3 |
| СПОСОБ ПОЛУЧЕНИЯ АЗОТСОДЕРЖАЩИХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИПРИЕМЛЕМЫХ СОЛЕЙ | 1990 |
|
RU2026296C1 |
| Способ получения производных пиридо (1,2-а) пиримидина или их фармацевтически приемлемых солей или их оптически активных изомеров | 1978 |
|
SU999973A3 |
| Способ получения пептидов или их уксуснокислых солей | 1977 |
|
SU691082A3 |
| Способ получения производных цис-4-фенил-1,2,3,4-тетрагидро-1-нафтиламина или их солей | 1980 |
|
SU1014467A3 |
| Способ получения @ -лактамов (его варианты) | 1981 |
|
SU1272981A3 |
| Способ получения 4а-арил-цис-декагидроизохинолинов | 1975 |
|
SU682126A3 |
| Способ получения производных пиридо/1,2-а/пиримидинов или их солей,или их оптически активных изомеров | 1978 |
|
SU906379A3 |
| ПРОЛЕКАРСТВА 3-АЦИЛ-2-ОКСИНДОЛ-1-КАРБОКСАМИДОВ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2124514C1 |

Д-Амфетин, Атедрон, Бензедрин, тилбензолэтанамин-сульфат
Мазиндол (Сандоз) , санорекс, теренак: 5 ( -хлорфенил)-2,5 Дигидро-ЗН-имидазо (2, 1-С1 -изоиндол-ол.
Фенфлюрамин (Сервье): пондеракс, пондерал, пондимин: ОЬ-М-эти Тс -метил-3(трифторметил)-бензоэтанамин- гидрохлорид.
Хлорфентермин (Уорнер-Ламберт), пре-сат, дезопимон,(1,о -диметил- -хлор-бензоэтанамии-гидрохлорид. 1а:Г - (3 Циклопентилокси-4-метч
оксифенил)-метил -2-ииидазолидинон.
X:ED(j- - така доза (при введении через рЬт), при которой крысы после Zt ч голодания в течение 5 ч поедают половинное количество корма в сравнении с контрольными, или же прирост их веса становится наполовину меньшим, чем у контрольных крыс.
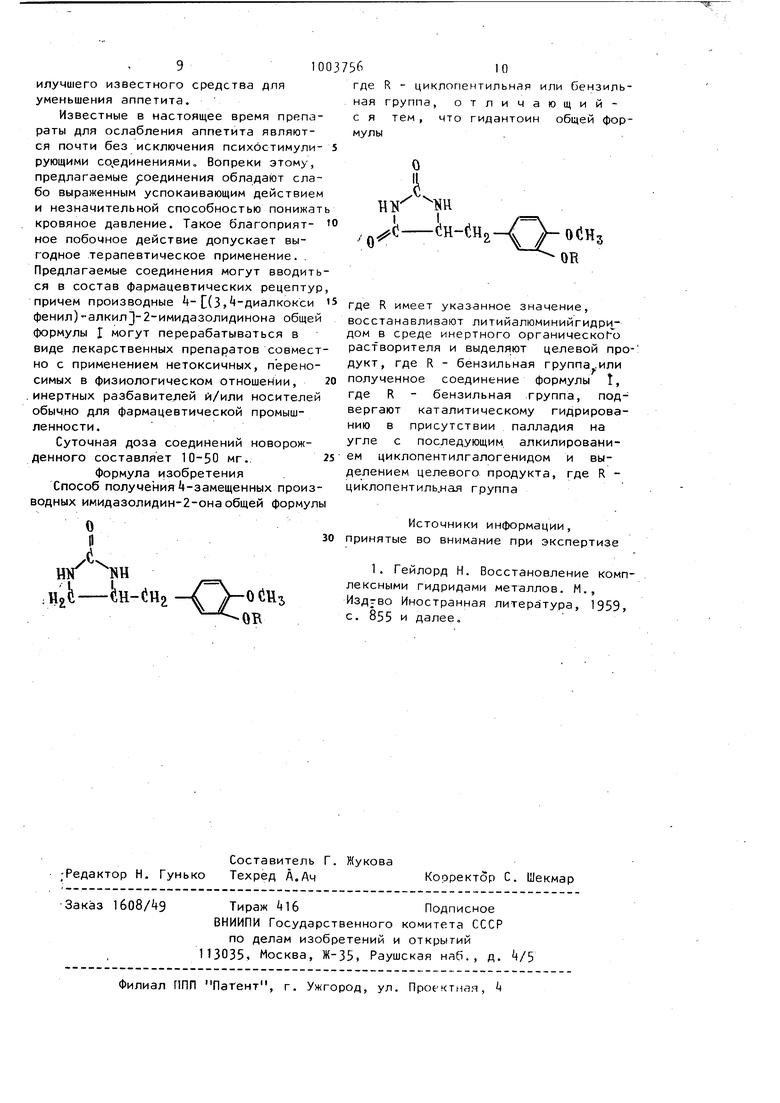
Из данныхтаблицы следует, что соединение 1а общей формулы 1 проявляет лучшее понижающее аппетит действие в сравнении с известными соединениями с таким же направлением действия. Терапевтический индекс данного соединения оказался лучшим, чем у наилучшего известного средства для уменьшения аппетита. Известные в настоящее время препараты для ослабления аппетита являются почти без исключения психостимулирующими соединениями. Вопреки этому, предлагаемые роединения обладают слабо выраженным успокаивающим действием и незначительной способностью понижат кровяное давление. Такое благоприятнов побочное действие допускает выгодное терапевтическое применение. . Предлагаемые соединения могут вводить ся в состав фармацевтических рецептур причем производные 4-(3,4-диалкокси фенил)алкил -2-имидазолидинона общей формулы I могут перерабатываться в виде лекарственных препаратов совмест но с применением нетоксичных, переносимых в физиологическом отношении, . инертных разбавителей ft/или носителей обычно для фармацевтической промышленности. Суточная доза соединений новорожденного составляет 10-50 мг.. Формула изобретения Способ получения 4-замещенных производных имидазолидин-2-онаобщей формулы (iU-(5H2 где R - циклопентильная или бензильная группа, отличающийс я тем , что гидантоин общей формулы (iH-dH где R имеет указанное значение, восстанавливают литийалюминийгидри дом в среде инертного органического pacfвopитeля и выделяют целевой продукт, где R - бензильная группа .или полученное соединение формулы 1, где R - бензильная группа, подвергают каталитическому гидрированию в присутствии палладия на угле с последующим алкилированием циклопентилгалогенидом и выделением целевого продукта, где R циклопентиль.ная группа Источники информации, принятые во внимание при экспертизе 1. Гейлорд Н. Восстановление комплексными гидридами металлов. М., Издтво Иностранная литература, 1959, с. 855 и далее
Авторы
Даты
1983-03-07—Публикация
1979-10-31—Подача