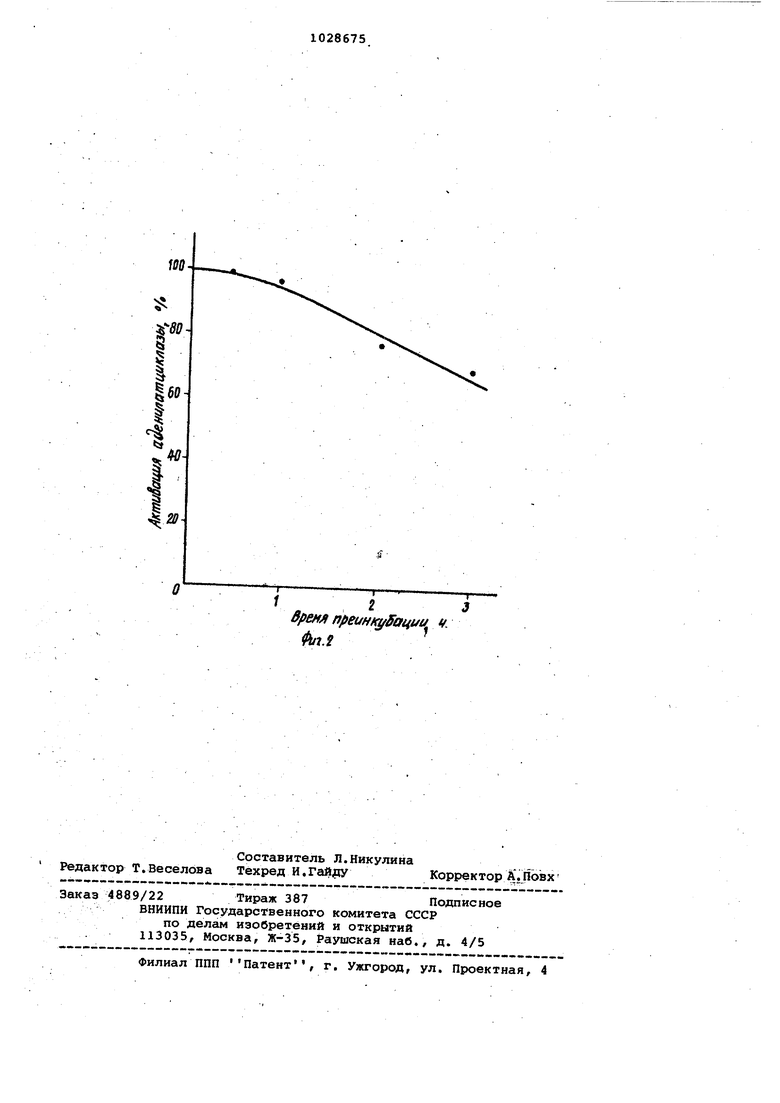
Изобретение относится к новому химическому соединению соли - N-х ацетилгидразон оксогуанозин-5-три фосфата (оксо-ГТФ) формулы А S nrV ,-P-O-P-O-CKi Чт у -Э1Н1 НО-Р-0 и OLi nw НО ОН для специфического ингибирования аденилатциклаэной активности, стим лируемой гуаниловыми нуклеотидами Данное соединение является специфическим регулятором аденилатцик лазной системы и может быть исполь зовано в биохимических исследованиях для изучения строения и механизма действия данного фермента, а также в медицине для изменения в клетках различных тканей уровня циклического аденозин-3, 5-монофосфата, который является продукто аденилатциклаз,ной реакции и играет роль регулятора многих биохимических процессов. Известен N-изоникотиноилгидразо оксо-ГТФ til. НО-Р-0-Р-О-Р-О-СНONO ONQ ONQ Однакоэто соединение не содержит реакцирнноспособной группиров и не оказывает ингибирунхцего действия на аденилатциклазную активность, стимулируемую гуаниловыми нуклеотидами. Цель изобретения - изыскание нового соедияения, позволяющего ра ширить ассортимент специфических регуляторов аденилатциклазной акти 1|ОСТИ. Поставленная цель Достигается свойствами нового соединения - ли тиевой соли N-хлорацетйлгидразона оксогуанозин-5 -трифосфата формулы (I), которое является специфическим ингибитором аденилатциклазной активности, стимулируемой гуаниловыми нуклеотидами. . Соединение формулы (J) получается синтезом, основанным на известной реакции диальдегидных производных, полученных периодатнвм окислением нуклеотидов, с моноацилгидразидами Г23-И заключаквдимся во взаимодействии окисленного периодатом натрия ГТФ (оксо-ГТФ) с хлоргидратом N-хлорацетилгидразида в литий-ацетатном буфере (рН 5). Пример. Литиевая соль N-хлорацетилгидразона оксо-ГТФ. 176,5 мг (0,825 ммоль) периодата натрия растворяют в 2 мл воды,добавляют 400 мг (0,75 ммоль) тетранатриевой соли гуанозин-5 -трифосфата. и полученный раствор перемешивают 1 ч при 4°С, защищая его от доступа света. После этого к реакционной смеси прибавляют 0,5 мл этйленгликоля и оставляют на 30 мин. Далее раствор при наносят.на колонку с сефадексом G-10 (2-75 см), уравновешенньм водой. Элюцию оксо-ГТФ проводят водой. Фракции, обладающие поглощением npk 260 нм и не содержащие примеси иодат-ионов ( -I- ЗНаО) , объединяют и упаривают досуха при пониженном давлении и температуре водяной бани 35 С. Остаток растворяют в 2 мл 0,25 М литий-ацетатного буфера (рН 5) и при охлаждении до 4°С добавляют 116 мг (0,8 ммоль) хлоргидрата Ы хлорацетилгидразида. Раствор перемещивают 2 ч при 4°С и обрабатывают 20 мл охлажденного этанола. Выпавший осадок центрифугируют, промывают этанолсад и высушивают в вакууме над пятиокисью фосфора. Получают 235 мг литиевой соли N-хлорацетилгидразона, оксо-ГТФ. Выхог 47%. Найдено, %: С 21,92; Н 2,95; Р 13,77; се 5,10. , Н бСеНтО уР,,-,. НгО Вычислено, %: G 21,66; Н 2,73; т 13,96; С 5,33. Соединение охрактеризовано хроматографической подвижностью при тонкослойной хроматографии на пластинках с полиэтилёниминцеллюлозой в 1 М jpacTBOpe хлористоголития R 0,04 и на пластинках SiPufoP в системе диоксан-аммиак-вода (6:4:1) R.j 0,15. Соединение охарактеризовано элект-, ррфоретической подвижностью при высоковольтном электрофорезе на бумаге 1 в 0,05 М литий-ацетатном буфере (рН 3,7) -, Б относительно ГМФ 2,0 в 0,05 М цитратном буфере (рН 6,5) - Е относительно ,8.. Соединение обладает характерным для гуаниловых нуклеотидов УФ-спектP° S-ь - 252 нм,, ,1 10 М см (РН.7). . Ингибированне аденилатциклазной активности, стимулируемой гуаниловыми нуклеотидами, изучают следующим образом. Мембранный препарат аденилатцикла зы СКФ 4.6.1.1. АТФ-пирофосфатлиаза (циклизующая) (АЦ) из хвос тового ядрг. мозга быка известными ме тодами. Активность фермента определя ют по образованию Р-цАМФ (цикличес кий аденозин-3, 3 -монофосфат) из Р АТФ. (30 Ки/ммоль) . Ингибирование N-хлорацетилгидразоном оксо-ГТФ стимуляции реакции синтеза цАМФ под действием гуанилил5-метилендифосфоната проводят в стандартных условиях при . Преин кубацию N-хлорацетилгидразона оксоГТФ в концентрации 10 М с мембранны препаратом АЦ проводят в течение раз личных интервалов времени в 20 мМ на трийборатном буфере (рН 8,0), содержащем 0,1 мМ ЭГТА (этиленбис-(оксиэтиленнитрило)-тетрауксусная кислота) , 1 мМ дитиотрейтол, 10 мМ MgCj и 8 мг/мл белка мембран. Преинкубаци останавливают 50-кратньм разведением тем же буфером, охлажденнЕФ до . После этого пробы центрифугируют 10 мин при 10000 об/мин и осадок мем бран суспендируют в среде разведением до концентрации белка 8 мг/мл. Me браны, преинкубированные в отсутствие N-хлорацетилгидразона оксо-ГТФ, обрабатывают аналогично. Затем проводят активацию АЦ добавлением вод- ного раствора гуанилил-5-метилендифосфоната до концентрации БЧО Ми после преинкубации с активатором в течение 15 мин при определяют количество Р-цАМФ, образукацегося за б мин при . Для этого 25 мкл смеси обработанного мембранного препарата добавляют к 25 мкл среды ин кубации, содержащей 100 мМ трис-НСе (рН 8,0) , .20 ММ Мдева, 2 мМ ЭГТА, 4 мМ цАМФ, 0,2 мМ АТФ, 40 мМ теофиллина, 2 мг/мл креатинкиназы, 40 мМ креатинфосфата АТФ ;(250000 имп/мин.). Защитный эффект гуанилил-5-метилендифосфоната от действия N-хлорацетилгидразона оксоГТФ наблюдают после добавления водного раствора гyaнилил-5-мeтилeндиJ фосфоната до концентрации 210 М к среде преинкубации, содержащей - мембранный препарат АЦ (конечный объем пробы 20 мкл), и выщерживания в течение 15 мин при 37°С, Здтем добавляют 5 мкл 510 М раство:ра N-хлорацетилгидразона оксо-ГТФ и (преинкубируют в течение различных интервалов времени при 20°С, после чего определяют образование Р-цАМФ по указанной методике. Активация мембранного препарата АЦ с помощью гуанйлил-5-метилендифосфоната в концентрации М приводит к увеличению активности фермента в 3,5 раза по сравнению с базальным уровнем активности. Ингибирование фермента определяют по следугадей формуле: . 100%, где И - стимулированная гуанилил-5 метилендифосфонатом активность АЦ после обработки N-хлорацетилгидразоном оксоГТФ;а - стимулированная гуанилил-5 метилендифосфонатом активность АЦ; б - базальная активность АЦ. На фиг.1 показана зависимость активации аденилатциклазы, стимулировацной гуанилил-5 -метилендифосфо-, натом (0,5 мМ, 15 мин, ), от времени предварительной инкубации, фермента с N-хлорацетилгидразоном оксо-ГТФ (1 мМ, 22°С) ; на .фиг.2 зависимость активации сленилатциклазы от времени преинкубации N-хлорацетилгидразона оксо-ГТФ (1 мМ, ) с ферментом, предварительно активированным гуанилил-5- метилендифосфонатом (0,2 мМ, 15 мин, 37С) . Как следует из фиг.1, за 3 ч преинкубации с N-Хлорацетилгидразоном.оксо-ГТФ АЦ практически полностью утрачивают способность к стимуляции гуанилил-5-метилендифосфонатом. При этом эффект увеличивается с течением времени, что говорит о необратимом связывании N-хлорацетилгидразона с одним из компонентов АЦ-системы. При предварительной преинкубации мембран с.гуанилил-5цетилендифосфонатсм с последующей обработкой N-хлорацетилгидразоном оксо-ГТФ ингибирующий эффект заметно снижается (фиг.2), что указывает на. специфическое взаимодействие предлагаемого соединения с ГТФ-связьшающим центром аденилатциклазной системы, в результате чего утрачивается способность АЦ к регуляции гуаниловыми нуклеотидами.
/2Э
Вренл nfieuHKifgotft/u v.
Фи.

Литиевая соль N-хлорацетилгидразона оксогуанозин-5-трифосфата ф01Ж1улы (I)О 6 О О II Я В йПГ J но-р-0-Р-о-р-о-сн, .t I . f . i . 1 OLl OU OLl 1,0, для специфического ингибирования аденилатциклаэнрй активности, стимулируемой гуаниловыми нуклеотидами. уевкщ 
| i | |||
| Spiegee A.M., Dovms R,W., Aurbach Jr.G.D, Separation of a Gua- nine HucCeofci 5e ReguEatory Unit Erom The AdenyCate CycPase Сотрвех With GTi Affinity Ghrcaraatography.-Journal of Cycftlc Nuc eotide Research, 5, 3-17 |
Авторы
Даты
1983-07-15—Публикация
1981-08-17—Подача