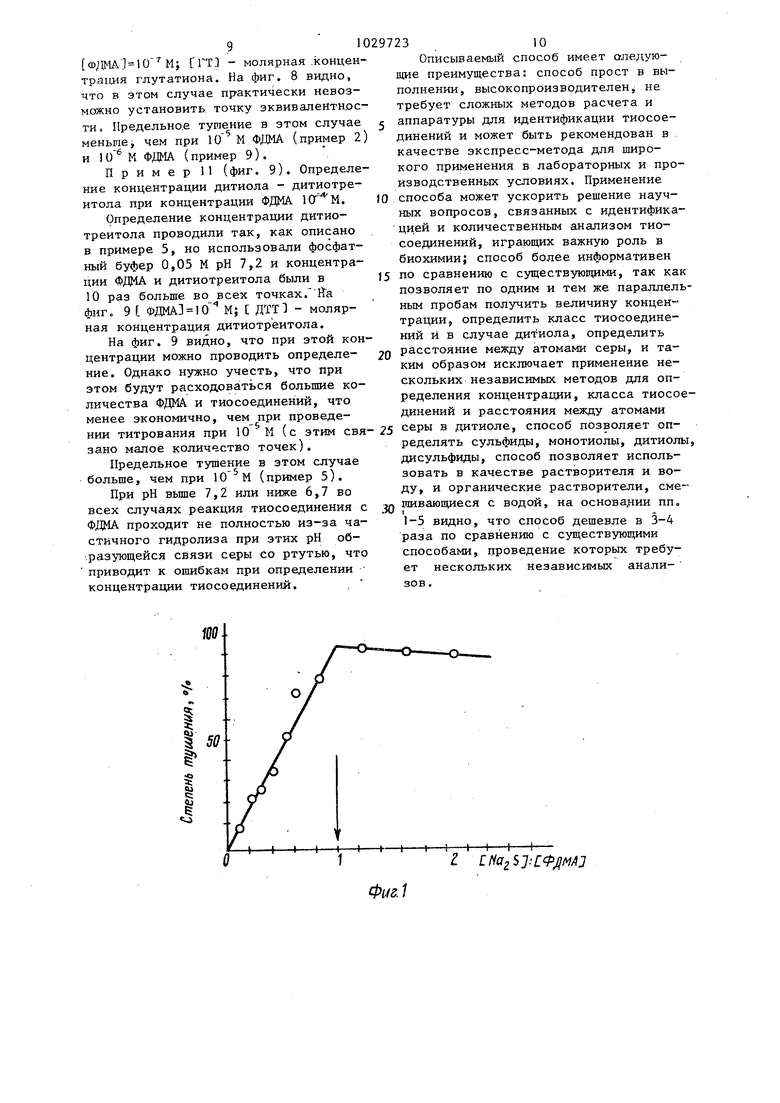
Изобретение относится к области аналитической химии, преимущественно аналитической биохимии, и может быть использовано как экспресс-анализ в лабораторных и производственны условиях для определения концентраци растворимых в воде или растворителях смешивающихся с водой, сульфидов, ор ганических тиолов, дитиолов, дисуль фидов, а также одновременно для отнес-ения анализируемого тиосоединения к одному из перечисленных классов и определения расстояния между атомами серы в растворе в случае дитиолов, В аналитической химии и биохимии часто ставится задача определения класса и количественного содержания перечисленных тиосоединений. Однако сзпцествующие до настоящего времени способы трудоемки, не позволяют сделать различие между этими классами тиосоединений и в ряде случаев непригодны при анализе этих соединений Известен спектрофотометрический способ Бойера, основанный на измерении прироста оптической плотности в области 250-255 нм,которьй происходит при присоединении п-меркурибензо ата к SH-группам. Недостатками этого способа является: невозможность определения тиолов, сильно поглощающих при 250255 нм, невозможность применения в присутствии примесей (например, N-ме тилформамида), поглощающих при 250 нм; невозможность определения тиосоединений при концентрации их ме нее -З- 10 М. Известен также амперометрический способ, основанный на измерении ионной проводимости в электрох-имической ячейке раствора тиола, титруемого раствором AgNOo, 5 . когда все SH-группы блокируются, в растворе появляются свободные ионы металла и, как следствие, диффузионный ток. Чувствительность способа - 0,11 мкмоля тиосоединения. К недостаткам этого способа относятся невысокая чувствительность и способность меркаптидов серебра дополнительно связывать ионы Ag с образованием комплексов типа t(RS-Ag)Agl . Образование таких комплексов объясняет завьшенные результаты при титровании цистеина и других соединений. Известен способ, основанный на измерении тушения флуоресценции флуоресцеин димеркуриацетата (ФДМА) при 32 его реакции с дисульфидами в/ щелочной среде. За реакцию тушения ответственно, в частности, образование ковалентной связи между ртутью и атомами серы. Степень тушения связывают с количеством дисульфидных групп. Недостатки этого способа следующие. возможность определения этим способом только концентрации дисульфидов в белках, т,ко калибровочная зависимость рассчитана только на это; невозможность выполнения количественных измерений в присутствии тушащих флуоресценцию ФДМАпримесей. К недостаткам этого способа относится также проведение реакции в сильно щелочной средеS что способствует освобождению в белках каких-то дополнительных групп, которые тушат флуоресценцию и мешает точному количественному определению дисульфидов. Все перечисленные способы не позволяют дифференцировать классы тиосоединений и определять расстояние между атомами серы в случае дитиолов. Ближайшим к изобретению по сущности и достигаемому эффекту является фпуориметрический способ определения тиосоединений в нейтральной среде, включающий измерение степени тушения флуоресценции флуоресцеиндимеркуриацетата (ФДМА) при его реакции с тиосоединением. Способ основан на измерении тушения флуоресценции ФДМА при его реакции с монотиолом при рН 7,4, За реакцию тушения ответственно образование ковалентной связи между ртутью и атомами серы. По данному способу при рН 14 определяют также дисульфиды или смесь дисульфидов с монотиолами По указанному способу для определения концентрации монотиолов в стеклянный стакан вносят 1,5 мл раствора ФДМА, 0,1-1,5 мл исследуемого образца, 1,5 мл 0,05 М трис-НС1буфера (для создания рН 7,4). Конечный объем доводят до 4,5 мл бидистиллированной водой. Параллельно ставят контрольную пробу, в которой объем образца компенсируют водой. После инкубации в течение 15-20 мин по интенсивности тушения флуоресценции при рН 7j4 определяют количество SH-групп по калибровочной кривой. Калибровочная кривая строится по восстановленному глутатиону в параллельных пробах при повьшгении мольного соотношения глутатиона и ФДМА от О до 1. Максимальная относительная ошибка 2-4%. Недостатками прототипа являются: невозможность определения концентрации дитиолов и сульфидов, так как калибровочная кривая рассчитана толь ко на анализ монотиолов, невозможность определения по этому способу класса тиосоединения, а также расстояния между атомами серы дитиола в растворе. Реакция проводится только в водной среде, анализ монотиолов не по методу параллельных проб, а по единичной точке. Определение концентрации тиосоеди нений в одной пробе при отношении монотиола к ФДМА, меньшем 1, является серьезным недостатком способа, так как вид калибровочной кривой зависит от класса тиосоединения, и при анализе тиосоединений неизвестного класса ( монотиолы, дитиолы, сульфиды нельзя определить концентрацию. Цель изобретения - расширение класса определяемых тиосоединений, как водорастворимых, так и растворимых в органических растворителях, смешивающихся с водой, одновременное определение концентрации тиосоединений и определение расстояния между атомами серы в случае дитиолов Поставленная цель достигается тем, что при флуориметрическом определении тиосоединений в нейтральной среде способом, включающим измерение степени тушения флуоресценции флуоресцеиндимеркуриацетата () при его реакции с тиосоединениями, реакцию ФДМА с тиосоединением проводят при концентрации ФДМА 10 -10моль/л степень тушения флуоресценции ФЩА. измеряют, сравнивая флуоресценцию ФДМА с флуоресценцией в пробах, в кб торые добавляют тиосоединение в моль ном соотношении от 0,05 до 5 к ФДМА, строят зависимость степени тушения флуоресценции от объема прибавленного соединения и по точке эквиваленткости, соответствующей излому в указанной зависимости, определяют концентрацию и судят о классе тиосоединений и расстоянии между атомами серы в дитиолах. Способ осуществляют следующим образом. ФДМА растворяют в 1,5 мл 0,01 н. раствора NaOH в воде, прибавляют для нейтрализации 1,5 мл 0,5 М (моль/л)фосфатного буфера рН 7,0, фильтруют полученный раствор. Разводят раствор ФДМА до 10 0,05 М фосфатным буфером рН 7,0. В 10 пробирок разливают ФДМА (по 0,3 мл в каждую пробирку), раствор тиосоединения в 0,05 М фосфатном буфере прибавляют в пробирки № 2-10 возрастающими дозами: например, начиная с или 0,1 мл и увеличивая объем дозы на 0,1 мл - от 0,1 мэля до 3-5 молей тиосоединения на моль ФДМА. Затем доводят объем раствора в пробирках № 1-10 до 3 мл 0,05 М фосфатным буфером рН 7,0, и через 15-20 мин записывают спектр флуоресценции ФДМА на спектрофлуориметре (например, Aminco-Bowman) при возбуждении 450 нм. В случае тиосоединений, не растворимых в воде и растворимых в органических растворителях, смешивающихся с водой {например, в спирте или N-метилформамиде), после прибавления тиосоединения в этом растворителе в пробирки № 2-10, во все пробирки (N 1-10) прибавляют зтот раствори-, тель до его объема в пробирке № 10, затем доводят общий объем в пробирках № 1-10 до 3 мл 0,05 М фосфатным буфером рН 7,0 и записывают спектр флуоресценции. Тушение флуоресценции и в том, и в другом случае оценивают по уменьшению интенсивности флуоресценции в точке максимума фпуоресценции. Строят график зависимости степени тушения (%) от объема (мл) .тиосоединения в пробе. Степень тушения (%) рассчитывают по формуле где 1 - интенсивность флуоресценции ФДМА в контроле (проба № 1); I - интенсивность; флуоресценции в Опытной пробе (пробы (Р 2-10). Точка эквивалентности соответствует излому зависимости степени тущения флуоресценции от объема тиосоединения в пробе. Концентрацию тиосоедине;ния в точке эквивалентности определяют по формуле: Т -У ФДМА1 -V, где 1 Т1 и ( - молярные концентрации тиосоединения и ФДМА соответственно; V и V - объемы (мл) тиосоединения и ФДМА соответственно. 51 На фиг, 1-9 изображены зависимости степени тушения флуоресценции от объема тиосоединений (фиг. 1-5, 7-9) и от расстояния между атомами серы в дитиолах (фиг. 6). Так.как анализируемые тиосоединения нестойки при хранении в растворе в присутствии воздуха5 то в случае примеров № 1-6, 9-11 концентрацию ис ходного анализируемого тиосоединения определяли параллельно по методу Бой ера. Поэтому на фиг. 1-5, 7-9 для большей наглядности отложены не мл тиосоединения, а отношение молярной концентрации тиосоединения, определенной по методу Бойера, к молярной концентрации ФДМА, На оси ординат от ложена степень тушения в %. Стрелками показаны точки эквивалентности. Пример 1 (фиг. 1). Определение концентрации сульфида Na. Кристаллы Na,jS9HgO марки х.ч. вы сушивали в течение суток в вакуумэксикаторе над NaOH. Непосредственно перед анализом готовили 10М раствор . в 0,05 М фосфатном буфере рН 7,2. Определение концентрации про водили как описано в методике, но при рН 7 5 2 и в 8 пар аплельных пробах На фиг ФДМА К; - молярная концентрация . И р и м е р 2 (фиг. 2). Определе ние концентрации монотиола - восстановленного глутатиона. Восстановленный глутатион фирмы Reonal хроматографически гомогенный хранили в вакуумированном сосуде на холоде. Непосредственно перед ана лизом готовили 10М раствор глутатиона в 0,05 М фосфатном буфере рН 7,0. Определение концентрации проводили, как описано в методике при рН 7,0, но в 12 параллельных пробах. На фиг. 2 ФДМАТ 10М; моляр ная концентрация глутатиона. И р и м е р (фиг. З). Определение концентрации монотиола-2-меркаптоэта нола в присутствии этилового спирта. 2-Меркаптоэтанол фирмы Fluka 98% чистоты ( 1,115) разводили этиловым спиртом до концентрации 10 М. Определение концентра1 ;ии проводили, как описано в методике, в присутствии этилового спирта, в 8 па раллельных пробах, но использовали 0,05 М фосфатный буфер рН 6,7. На фиг. 3 1 ФДМА СМЭ1 - молярная концентрация меркаптрэтанола. 3 П р и м е р 4 (фиг. 4).Определение концентрации дитиола - дитиотреитола. Дитиотреитол фирмы Serva растворяли в 0,05 М фосфатном буфере рН 7,0. Определение концентрации проводили как описано в методике при рН 7,0. На фиг. Фда1А1 ИГ М; t ДТТ1 молярная концентрация дитиотреитола. П р и м е р 5. (фиго 5). Определение концентрации дитиола - дигидролипоевой кислоты в присутствии этилового спирта. Использовали 10 м раствор дигидролипоевой кислоты в спирте, приготовленный в атмосфере Аг. В связи с легкостью окисления дигидролипоевой кислоты во время отбора проб пипеткой через раствор пропускали Аг. Определение концентрации проводили, как описано в методике, в присутствии этилового спирта, но использовали 0,05 М фосфатный буфер рН 6,7. На фиг. 5 ДПЖ1 - молярная концентрация дигидролипоевой кислоты. П р и м е р 6. Определение концентрации дисульфида - липоевой кислоты. Концентрацию раствора липоевой кислоты фирмы Fluka определяли после ее восстановления в дигидролипоевую кислоту боргйдридом натрия. Определение концентрации дигидролипоевой кислоты проводили, как описано в примере 5 (фиг, 5). Получена зависимость, аналогичная фиг. 5. П р и м е р 7, Определение концентрации дитиола-дитиотреитола в присутствии N-метилформамида. Определение концентрации дитиотреитола проводили, как описано в примере 5, но вместо этилового спирта использовали К-метилформамид. Получена зависимость, аналогичная фиг. 4. П р и м е р 8 (фиг. 6). Определение-класса тиосоединений, и в случае дитиолов - расстояния между атомами серы в растворе. По данным примеров 1-5, повторенных 3 раза, нашли, что каждому классу тиосоединений соответствует в точке эквивалентности определенная степень тушения флуоресценции ФДМА. В случае сульфидов степень тушения флуоресценции 10 М ФДОА в точке эквивалентности составляет 85-95%, монотиолов 45-55%, дитиолов 65-80%, По данным примеров 1-5, повторенных 3 раза, построили график зависимости средней из 3 опытов степени ту шения в точке эквивалентности от рас стояния в растворе между атомами сер в точках присоединения ФДМА, в А (фиг. 6), Цифры возле точек на фиг.6 соответствуют следующим тиосоединениям: 1 - сульфид натрия; 2 - дитиотреитол; 3 - дигидролипоевая кислота; 4, 5 - монотиолы - восстановленный тлутатион и меркаптозтанол. Расстояние между атомами серы (в точках присоединения ФДМА) в растворе в дитиотреитоле и дигидролипоевой кислоте, модифицированных ФДМА, равны соответственно 4 А и 4,5 А, определили из их моделей по Стюарту-Бриглебу. В случае на фиг. 6 отложено расстояние (1,6 А) между точками присоединения ФДМА к , опрёде ленное также из модели по СтюартуБриглебу, Из фиг. 6 видно, что при расстоянии более 9,5 А между атомами серы в растворе дополнительного по сравнению с монотиолами (точки 4, 5) тушения наблюдаться не будет, По фиг. 6 можно определять расстояние между атомами серы дитиолов в растворе, если оно не превышает 9,5 А. В основе этого определения ле жит обнаруженное в данной работе уменьшение квантового выхода ФДМА (т.е. уменьшение интенсивности флуоресценции) за счет взаимодействия молекул ФДМА, связанных сульфидом или дитиолом, видимо, в результате возможно изменение квантового выхода флуоресценции за счет образования пары молекул ФДМА. Параллельно с уменьшением интенсивности флуоресценции ФДМА при реакции с сульфидом или дитиолом происходит смещение мак симума флуоресценции ФДМА от 520 нм на несколько нм в сторону коротких волн; параллельно происходит уменьшение интенсивности и изменение формы линии в спектре поглощения ФДМА. Известно, что алифатические соеди нения легко принимают в растворе свернутую конформацию, и расстояние между атомами серы в растворе будет определяться легкостью сворачивания молекулы. Это наглядно проявляется в случае дитиотреитола и дигидролипо евой кислоты. Последняя, имея лишь 3 СН j - группы между атомами серы, судя по модели по Стюарту-Бриглебу, не может присоединить 2 молекулы ФДМА в свернутой конформации, и в случае этого соединения расстояние между атомами серы в растворе больше, чем в случае дитиотреитола, имеющего 4 СНд-группы, которые могут присое- , динить 2 молекулы ФДМА в свернутой конформации. Калибровочные зависимости, аналогичные фиг. 6 можно сделать для всей области концентраций ФДМА, при которой возможно определение концентрации (10-10 М) .Однако, как будет показано ниже в примерах 9-11, нужно учитьшать, что предельное тушение зависит не только от класса тиосоединения, но и от концентрации ФДМА в точке эквивалентности. П р и м е р 9 (фиг. 7). Определение концентрации восстановленного глутатиона при концентрации ФДМА . Определение концентрации проводили, как описано в примере 2 (фиг. 2), в фосфатном буфере 0,05 М рН 7,0 в 11 параллельных пробах за тем исключением, что во всех точках концентрации ФДМА и глутатиона были в 10 раз меньше. Сплошная лииия на фиг. 7 измерения сделаны через 15 мин поел смешивания; прерывистая линия - че рез-4 ч. Из фиг. 7 видно, что и при зтой концентрации ФДМА реакция доходит до конца и за 15 мин: через 4 ч наблюдается не дополнительное тушение, а некоторое возгорание флуоресценции. На фиг. 7 СФДЬ1А 10 М; ГТТ- молярная концентрация глутатиона. Видно, что точка эквивалент- кости в этом случае выявляется хуже, чем в случае 1О М ФДМА (пример 2). Тушение в точке эквивалентности в этом случае меньше, чем при 10 М ФДМА (пример 2). Пример 10 (фиг. 8). Определение концентрации восстановленного глутатиона при концентрации ФДМА . Определение концентрации восстановленного глутатиона проводили, как описано в примере 2 (фиг. 2), в фосфатном буфере рН 7,0, в 8 параллельиых пробах, но во всех точках концентрации ФДОА и глутатиона бьши в 100 раз.меньше. На фиг. В 1ФДМАЗ 10 М; trTl - молярная концентрахщя глутатиона. Сплошная линия измерения сделаны через 5 мин после смешивания; прерывистая линия - через 4 ч. На оси ординат отложен процент остаточной флуоресценции: : 100.
ФДМА.1 М; ГГТ - молярная .концентраиля глутатиона. На фиг. 8 видно, что в этом случае практически невозможно установить точку эквивалентности . Предельно.е тушение в этом случае меньшеi чем при 10 М ФДМА (пример 2 и 10 К ФДМА (пример 9),
Пример П (фиг. 9). Определение концентрации дитиола - дитиотреитола при концентрации ФДМА. 10 М,
Определение концентрации дитиотреитола проводили так, как описано в примере 5, но использовали фосфатный буфер 0,05 М рН 7,2 и концентрации ФДМА и дитиотреитола были в 10 раз больше во всех точках. fe фиг. 9 t ФДМА М; ДТТ:1 - молярная концентрация дитиотреитола.
На фиг. 9 видно, что при этой концентрации можно проводить определение. Однако нужно учесть, что при этом будут расходоваться большие количества ФДМА и тиосоединений, что менее экономично, чем при проведении титрования при 10 М (с этим связано малое количество точек).
Предельное тушение в этом случае больше, чем при 10 М (пример 5).
При рН вьше 7,2 или ниже 6,7 во всех случаях реакция тиосоединения с ФДМА проходит не полностью из-за частичного гидролиза при этих рН образующейся связи серы со ртутью, что приводит к ошибкам при определении концентрации тиосоединений.
Описываемый способ имеет оледующие преимущества: способ прост в выполнении, высокопроизводителенj не требует сложных методов расчета и аппаратуры для идентификации тиосоединений и может быть рекомендован в качестве экспресс-метода для широкого применения в лабораторных и производственных условиях. Применение способа может ускорить решение научных вопросов, связанных с идентификаци.ей и количественным анализом тиосоединений, играющих важную роль в биохимии; способ более информативен
5 по сравненшо с существующими, так как позволяет по одним и тем же параллельным пробам получить величину концен трации, определить класс тиосоединений и в случае дитиола, определить
Q расстояние между атомами серы, и таким образом исключает применение нескольких независимых методов для определения концентрации, класса тиосоединений и расстояния между атомами
5 серы в дитиоле, способ позволяет определять сульфиды, монотиолы, дитиолы, дисульфиды, способ позволяет использовать в качестве растворителя и воду, и органические растворители, смешивающиеся с водой, на ocнoвa ии пп.
1-5 видно, что способ дешевле в 3-4 раза по сравнению с с тцествующими способами, проведение которых требует нескольких независимых анализов.
50
г
I I I
70I бд
0
«о
50
К7
4-46 8 W 1Z Фкг.б



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ ХРОНИЧЕСКОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ | 2004 |
|
RU2281090C2 |
| Способ количественного определения @ -аминокислот | 1986 |
|
SU1361477A1 |
| КОМПОЗИЦИЯ С АНТИОКСИДАНТНЫМИ СВОЙСТВАМИ И СПОСОБ ЛЕЧЕНИЯ БОЛЕЗНЕЙ МЛЕКОПИТАЮЩИХ | 2002 |
|
RU2280448C2 |
| Способ определения гликозилированных белков крови | 1986 |
|
SU1465766A1 |
| СПЕЦИФИЧЕСКИЙ РЕГУЛЯТОР АКТИВНОСТИ НУКЛЕОТИД-ЗАВИСИМЫХ ФЕРМЕНТОВ | 1997 |
|
RU2130490C1 |
| Способ определения активности глутатионтрансферазы | 1990 |
|
SU1759874A1 |
| Способ определения активности глутатионпероксидазы в эритроцитах | 1984 |
|
SU1282003A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КАРБЕНИЦИЛЛИНА В РАСТВОРЕ | 1991 |
|
RU2028143C1 |
| Способ определения активности моноаминоксидазы в тромбоцитах | 1982 |
|
SU1049810A1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕЧЕННОГО ТРИТИЕМ ТРОМБОКСАНА B | 1990 |
|
SU1732514A1 |

ФЛУОРИМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ ТИОСОЕДИНЕНИЙ в нейтральной среде, включающий измерение степени тушения дхпуоресценции флуоресцеиндимеркуриацетата (ФДМА) при его реакции с тиосоединением, отличающийся тем, что, с целью расширения класса определяемых тиосоединений, как водорастворимых, таки растворимых в органических растворителях, смешиваю1чихся с водой, одновременного определения концентрации класса тиосоединений и расстояния между атомами серы в случае дитиолов, реакцию ФДМА с тиосоединением проводят при концентрации ФДМА 10 1 о моль/л, степень тушения флуорес(Л С ценции ФДМА измеряют сравнивая флуоресценцию ФДМА с флуоресценцией в пробах, в которые добавляют тиосоединение в мольном соотношении от S 0,05 до 5 ФДМА, строят зависимость степени тушения флуоресценции от объема прибавленного соединения и по точке эквивалентности, соответствующей излому в указанной зависимости, Ю СО определяют концентрацию и судят о классе тиосоединений и расстоянии v между атомами серы в дитиолах. N3
| Воуег P.D | |||
| Spectrophotometric investigation of reactions of protein sulfhydril groups with organic mercury compounds J | |||
| Am | |||
| Chem | |||
| Soc | |||
| Устройство для автоматического пуска в ход регистрирующих механизмов в самопишущих приборах | 1925 |
|
SU1954A1 |
| Аппарат, предназначенный для летания | 0 |
|
SU76A1 |
| УСТРОЙСТВО ДЛЯ РАДИОПРИЕМА | 1925 |
|
SU4331A1 |
| Торчинский Ю.М | |||
| Сульфгидрильные и дисульфидные группы белков | |||
| - М | |||
| Наука, 1971, с | |||
| Приспособление для подачи воды в паровой котел | 1920 |
|
SU229A1 |
| Karush F., а.о An | |||
| Assay Method for Bisulfide Groups Ъу Fluorescence Qunchung | |||
| Analyt | |||
| Biochem | |||
| Прибор для заливки свинцом стыковых рельсовых зазоров | 1925 |
|
SU1964A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Облицовка комнатных печей | 1918 |
|
SU100A1 |
| Миронов Г.П | |||
| и др | |||
| Чувствительный флуориметрический метод определения SH и S-S групп при их совместном | |||
| присутствии | |||
| Вопросы медицинской химии, 1971, т | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| Пуговица | 0 |
|
SU83A1 |
Авторы
Даты
1987-09-30—Публикация
1981-09-29—Подача