Изобретение относится к способам получения биологически активных соединений, меченных радиоактивными изотопами.
Тромбоксан (ТХ) В2 является стабильным продуктом гидролиза очень лабильного в водных растворах (t1/2 = 30 c), соединения ТХА2, метаболита арахидоновой кислоты (АК), обладающего широким спектром биологической активности (стимулирует агрегацию тромбоцитов, вызывает сокращение гладко-мышечной мускулатуры дыхательных путей и кровеносных сосудов).
Меченный тритием ТХВ2 используется в РИА-наборах для определения эндогенного ТХВ2. Чувствительность этого метода тем выше, чем выше молярная радиоактивность препарата [3H] ТХВ2. Так, использование [3H] ТХВ2 с молярной радиоактивностью 120 Ки/ммоль и больше позволяет определять до нескольких пикограммов ТХВ2 на пробу (каталог фирмы "Amersham" на 1990).
Структурные формулы тромбоксана В2 и его предшественников:
Арахидоновая кислота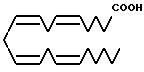
Тромбоксан А2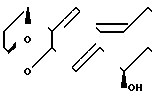


Тромбоксан В2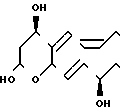

 OH
OH
Сведения о способе получения меченного тритием тромбоксана В2 в патентной документации отсутствуют, но есть данные о получении [1-14C] ТХВ2 в научной литературе - прототип.
В этой работе в качестве ферментного препарата используются тромбоциты человека, полученные следующим образом. Кровь от здоровых доноров, которые в течение недели не принимали аспирин или другие противовоспалительные препараты, центрифугируют 15 мин при 200g. В полученной богатой тромбоцитами плазме определяют количество тромбоцитов, после чего тромбоциты освобождают центрифугированием при 800g в течение 15 мин и суспендируют в таком объеме трис-солевого буфера (рН 7,4), чтобы концентрация тромбоцитов равнялась 109 клеток/мл. Затем 1 мл суспензии тромбоцитов предынкубируют 2 мин при 37о и инкубируют в течение 5 мин при той же температуре с различными концентрациями [1-14C] АК с молярной радиоактивностью 54 Ки/моль (1, 5, 10, 50, 100 мкМ). Реакцию останавливают добавлением 20 объемов смеси хлороформметанол (2: 1, v/v). Экстрагированные продукты реакции фракционируют с помощью колоночной хроматографии (0,5 Г Biosil-A). Фракции, содержащие различные метаболиты [1-14C] АК, анализируют с помощью ТСХ в системе растворителей СНСl3: CH3OH: CH3COOH: H2O (90: 8: 1: 0,8; v/v/v/v) и сканирования радиоактивности радиохроматосканером, а также с использованием радиогазхроматографии. Выход [1-14C] ТХВ2 и его молярную радиоактивность определяют методами РИА и по разведению [2H8] ТХВ2 с использованием совмещенной газхроматографии-масспектрометрии. Полученные результаты представлены в таблице.
Наибольший выход [1-14C] ТХВ2, равный 13% , достигается при концентрации [1-14C] АК 10 мкМ. Молярная радиоактивность целевого продукта снижается при этом на 33% .
Основными недостатками прототипа являются низкий выход [1-14C] ТХВ2 и значительное снижение молярной радиоактивности относительно исходной [1-14C] АК при ее концентрациях 10-100 мкМ.
Целью изобретения является получение меченного тритием ТХВ2 с высокой молярной радиоактивностью, повышение выхода и качества целевого продукта за счет увеличения молярной радиоактивности.
Цель достигается выделением и частичной очисткой ПГН-синтетазы из везикулярных желез барана и ТХ-синтетазы из тромбоцитов человека 1; инкубацией [3H] АК с концентрацией 10-100 мкМ с частично очищенным препаратом ПГН-синтетазы при соотношении 0,3-3,3 мкмоль [3H] АК на 1 мг ПГН-синтетазы (40-400 нмоль [3H] АК (на единицу активности ПГН-синтетазы2) в течение не более 4 мин, после чего добавляют препарат частично очищенной ТХ-синтетазы до концентрации 0,11-0,55 мГ/мл и инкубируют 25-40 мин при 25оС.
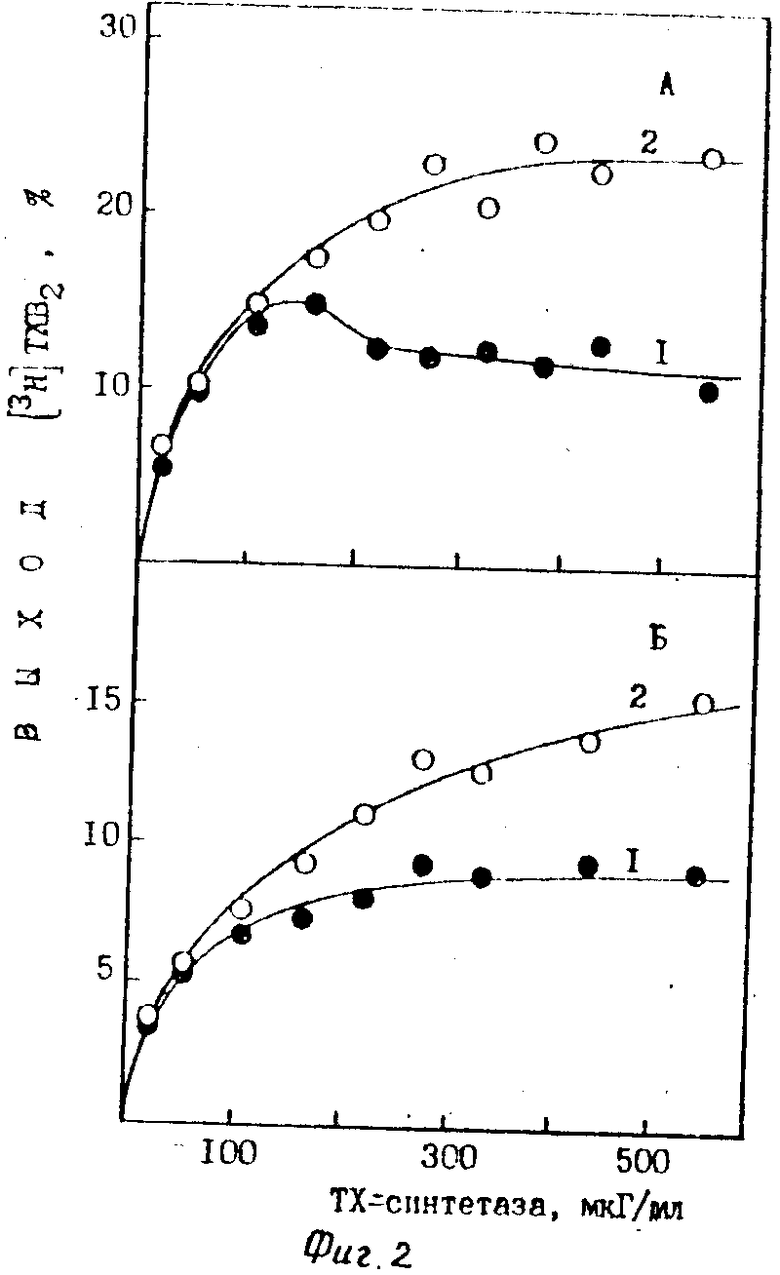
Изобретение поясняется фиг. 1-5, где на фиг. 1 - зависимость выхода [3H] ТХВ2 (кривые 1 и 2) и степени превращения [3H] АК (кривые 3 и 4) от концентрации ПГН-синтетазы при τ = 0 (кривые 1 и 3) и τ = 1 мин (кривые 2 и 4): А - начальная концентрация [3H] АК 25 мкМ, Б - 100 мкМ; концентрация препарата ТХ-синтетазы 220 мкГ/мл. Условия проведения эксперимента (среда инкубации (СИ): L-адреналин 2 мМ, гемин 2 мкМ; 20 мМ калий-фосфатный буфер (рН 7,4); температура СИ 25оС; на фиг. 2 - зависимость выхода [3H] ТХВ2 от концентрации ТХ-синтетазы при τ = 0 (кривая 1) и τ = 1 мин (кривая 2): А - начальная концентрация [3H] АК 25 мкМ; Б - 100 мкМ; концентрация ПГН-синтетазы 30 мкГ/мл. СИ как на фиг. 1; на фиг. 3 - зависимость выхода [3H] ТХВ2 от начальной концентрации [3H] АК при τ = 0 (кривая 1) и τ = 1 мин (кривая 2). Концентрация ПГН-синтетазы 30 мкГ/мл, ТХ-синтетазы 380 мкГ/мл. СИ как на фиг. 1, на фиг. 4 - зависимость выхода [3H] ТХВ2 от величины τ. Начальная концентрация [3H] АК 25 мкМ, концентрация ПГН-синтетазы 30 мкГ/мл, ТХ-синтетазы 220 мкГ/мл. СИ как на фиг. 1; на фиг. 5 - кинетика накопления [3H] ТХВ2 (кривые 1 и 2) и расходования [3H] АК (кривые 3 и 4) при τ = 0 (кривые 1 и 3) и τ = 1 мин (кривые 2 и 4). Начальная концентрация [3H] АК 25 мкМ, концентрация ПГН-синтетазы 15 мкГ/мл и ТХ-синтетазы 380 мкГ/мл. СИ как на фиг. 1.
Сущность изобретения заключается в использовании двух очищенных ферментов (не содержащих эндогенные полиненасыщенные жирные кислоты), которые последовательно (через определенное время) вводят в реакционную смесь, содержащую [3H] АК.
Оптимизацию синтеза [3H] ТХВ2 проводят относительно выхода [3H] ТХВ2, рассчитанного, исходя из радиоактивности взятой в реакцию [3H] АК.
Препарат ПГН-синтетазы получают из везикулярных жезел барана путем измельчения желез гомогенизатором, осаждения микросомальной фракции центрифугированием, солюбилизации мембранных белков неионным детергентом Tween-20, фракционирования на колонке с DEAE-целлюлозой.
Препарат ТХ-синтетазы получают из осажденных при фракционировании крови тромбоцитов человека путем разрушения клеток ультразвуком, выделения микросомальной фракции центрифугированием, солюбилизации неионным детергентом Triton X-100, хроматографии на колонке с DEAE-целлюлозой.
Для определения оптимальных условий синтеза [3H] ТХВ2 устанавливают зависимость выхода [3H] ТХВ2 от концентрации препаратов ПГН-синтетазы (фиг. 1А и 1Б) и ТХ-синтетазы (фиг. 2А и 2Б), начальной концентрации [3H] АК4 (фиг. 3), величины τ (фиг. 4) и времени инкубации (фиг. 5).
Все эксперименты проводят в калийфосфатном буфере с рН 7,4. Реакцию начинают добавлением в реакционную смесь, содержащую [3H] АК, препарата ПГН-синтетазы или смеси препаратов ПГН-синтетазы и ТХ-синтетазы, а останавливают добавлением раствора лимонной кислоты (до рН 3). Время между добавлением к реакционной смеси ПГН-синтетазы и ТХ-синтетазы и ТХ-синтетазы обозначают τ .
Варьирование концентрации ПГН-синтетазы при постоянной концентрации ТХ-синтетазы (0,22 мГ/мл), двух концентрациях [3H] АК (25 и 100 мкМ) и двух значениях τ (0 и 1 мин) показывает, что концентрация ПГН-синтетазы, при которой выход [3H] ТХВ2 достигает предельных значений, существенно не зависит от перечисленных параметров (фиг. 1А и 1Б). При этом выход [3H] ТХВ2 при τ = 1 мин был в 1,3-1,4 раза выше, чем при τ = 0, и достигал 20-21% для концентрации [3H] АК 25 мкМ и 13-14% - для 100 мкМ.
Существенное увеличение выхода [3H] ТХВ2 при τ = 1 мин (по сравнению с выходом при τ = 0) наблюдается при варьировании концентрации ТХ-синтетазы в условиях сохранения постоянной концентрации ПГН-синтетазы (фиг. 2А и 2Б). Соотношение выходов [3H] ТХВ2 при τ = 1 мин и τ = 0 увеличивается пропорционально увеличению концентрации ТХ-синтетазы и достигает значений 1,6-2.
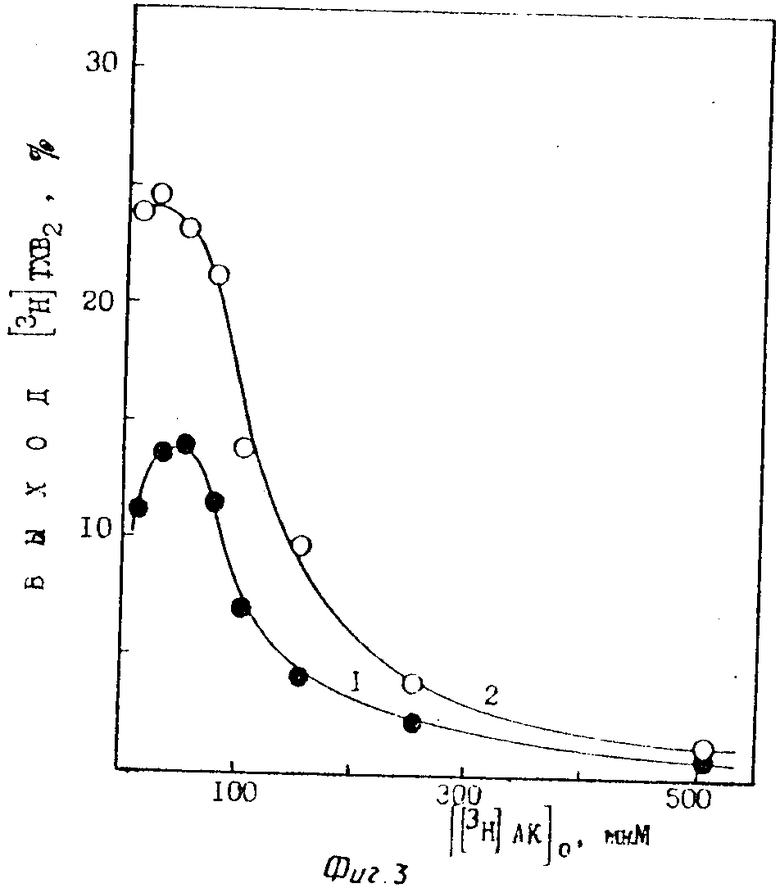
При варьировании начальных концентраций [3H] АК от 10 до 500 мкМ максимальный выход [3H] ТХВ2 21-25% для τ = 1 мин и 12-14% для τ = 0 достигается при 10-75 мкМ [3H] АК (фиг. 3). При дальнейшем увеличении концентрации [3H] АК происходит резкое снижение выхода конечного продукта при практически неизменном соотношении выходов при τ = 1 мин и τ = 0, равном 1,8-2 для каждой выбранной концентрации [3H] АК.
На фиг. 4 представлена зависимость выхода [3H] ТХВ2 при τ≥ 0 относительно выхода [3H] ТХВ2 при τ= 0 ([[3H] ТХВ2] ∞τ/[[3H] ТХВ2] ∞τ ). Максимальное увеличение выхода [3H] ∞τТХВ2 наблюдается при τ = 1 мин. При увеличении τ ( τ> 1 мин) происходит резкое снижение выхода: при τ = 15 мин выход [3H] ТХВ2 равен примерно 1/2 выхода при τ = 0.
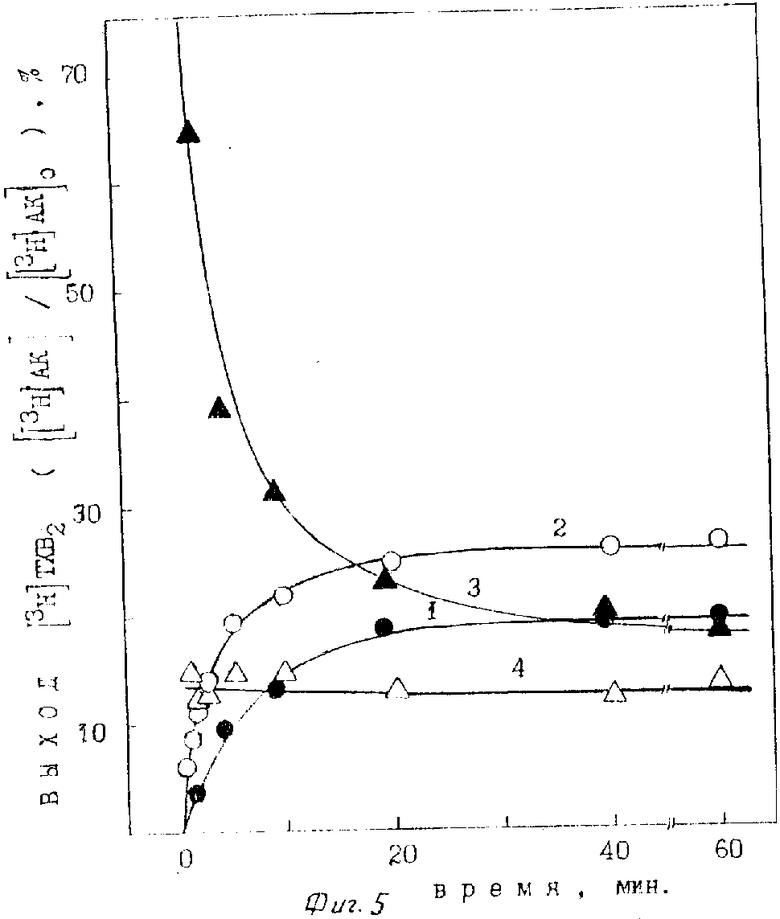
Как следует из фиг. 5, скорость образования [3H] ТХВ2 после добавления в реакционную смесь ТХ-синтетазы при τ = 1 мин в 4 раза выше, чем в случае τ = 0. Предельный выход конечного продукта достигается через 25-40 мин инкубации [3H] АК со смесью ПГН-синтетазы и ТХ-синтетазы при 25оС.
Определение молярных радиоактивностей [3H] ТХВ2, полученного при различных концентрациях исходных [3H] АК и ТХ-синтетазы, с помощью ВЭЖХ бромфенацилового эфира, меченного тритием тромбоксана, показывает, что ее значения не зависят от изменения перечисленных параметров и составляют 85-90% от молярной радиоактивностей исходной жирной кислоты.
Таким образом, обнаружен эффект существенного увеличения выхода [3H] ТХВ2 при последовательном добавлении ПГН-синтетазы и ТХ-синтетазы к реакционной смеси, содержащей [3H] АК, через определенный промежуток времени τ , причем оптимальное значение τ равно 1 мин.
Из приведенных результатов видно, что соотношение выходов [3H] ТХВ2 при τ = 1 мин и τ = 0 при варьировании концентраций ТХ-синтетазы и [3H] АК зависит только от концентрации препарата ТХ-синтетазы. Поэтому обнаруженный эффект может быть связан с неспецифической сорбцией исходной [3H] АК на примесных белках, а также известным фактом ингибирования ТХ-синтетазной активности эйкозаполиеновыми кислотами. В случае τ > 0 и при избытке ПГН-синтетазы оба эти ограничения становятся несущественными за счет быстрого превращения исходной [3H] АК в лабильный промежуточный продукт, обладающий меньшей способностью сорбироваться на белках и не вызывающий ингибирование ТХ-синтетазы.
В этой связи возникают определенные требования к используемым для синтеза [3H] ТХВ2 препаратам ферментов: максимальная степень очистки (или удельная активность) и отсутствие примесей полиненасыщенных жирных кислот (включая АК и ТК), которые могут приводить к ингибированию ТХ-синтетазы, а также к разбавлению их радиоактивномеченых аналогов и, как следствие, к снижению молярной радиоактивности конечного продукта.
Использование частично очищенных (по предлагаемым методикам) препаратов ПГН-синтетазы и ТХ-синтетазы позволяет в отличие от использования цельных клеток, клеточных гомогенатов и мембранных препаратов максимально снизить или предотвратить полностью действие перечисленных отрицательных факторов.
Таким образом, инкубации [3H] АК с концентрацией 10-15 мкМ с очищенным препаратом ПГН-синтетазы (1,67 мкмоль [3H] АК на 1 мГ ПГН-синтетазы или 200 нмоль меченой кислоты на 1Е ПГН-синтетазы) в присутствии L-адреналина (2 мМ) и гемина (2 МкМ) в калийфосфатном буфере (рН 7,4) при 25оС в течение 1 мин с последующим добавлением очищенного препарата ТХ-синтетазы (0,35-0,5 мГ/мл или 0,05-0,07 Е/мл) и продолжение инкубации в течение 25-40 мин при тех же условиях приводит к образованию [3H] ТХВ2 с выходом 24-25% .
Как уже отмечалось, основными недостатками способа-прототипа являются низкий выход и значительное снижение молярной радиоактивности целевого продукта - [1-14C] ТХВ2. Сравнение предлагаемого способа со способом-прототипом показывает, что эти недостатки связаны, главным образом, с использованием в качестве ферментного препарата изолированных тромбоцитов человека. Наблюдаемое снижение молярной радиоактивности [1-14C] ТХВ2 на 28-33% по сравнению с исходной [1-14C] АК при ее концентрациях 10 мкм и выше связано со стимуляцией тромбоцитов, приводящей к высвобождению эндогенной АК, которая наряду с [1-14C] АК вовлекается в реакции ферментативного синтеза ТХВ2.
Получение [3H] ТХВ2 с использованием предлагаемого способа позволяет увеличить химический выход целевого продукта в 1,8-2 раза по сравнению со способом-прототипом. При этом снижение молярной радиоактивности (на 10-15% ) связано только с высвобождением атомов трития при внутримолекулярных структурных перегруппировках, сопровождающих превращение [3H] АК в [3H] ТХВ2.
П р и м е р. 1. Получение препарата ПГН-синтетазы.
100 Г везикулярных желез барана (-60оС) помещают в 200 мл 50 мМ трис HCl буфера (рН 8), содержащего 10 мМ Na2EDTA, 1 мМ диэтилдитиокарбамат (DEDTC) и 0,1% (w/v) Tween-20, измельчают до гомогенного состояния с помощью Waring Comm. blender (10 раз по 15 с с интервалом 30 с) и центрифугируют 30 мин при 4500g. Полученный супернатант (около 230 мл) фильтруют через четыре слоя марли и центрифугируют 90 мин при 95˙103g. Осадок (микросомальная фракция) суспендируют в 20 мМ калий-фосфатном буфере (рН 7,4), содержащем 2 мМ Na2EDTA и 0,5 мМ DEDTC, с использованием стеклянного гомогенизатора с тефлоновым пестиком, доводят объем суспензии буфера до 180 мл и повторно центрифугируют 90 мин при 95˙103g. Полученный осадок ресуспендируют в 20 мМ калий-фосфатном буфере (рН 7,4) с 0,5 мМ DETA и 0,1 мМ дитиотреитолом (DTT) (буфер А), добавляют 9 мл 10% (w/v) Tween-20, доводят объем до 60 мл буфером А и центрифугируют 120 мин при 95˙103g. Супернатант (около 50 мл), содержащий ПГН-синтетазную активность, отбирают и наносят на колонку с DEAE-целлюлозной (2,5˙30 см), уравновешенную в буфере А, содержащем 0,1% w/v Lubrol PX. Фракцию несвязавшихся с DEAE-целлюлозой белков собирают с используют в дальнейшем в качестве частично очищенного препарата ПГН-синтетазы. Все операции при выделении фермента проводят при температуре +4оС.
В результате приведенной процедуры получают 75 мл препарата ПГН-синтетазы с концентрацией белка 0,9 мГ/мл и специфической активностью 8,3 мкмоль арахидоновой кислоты (АК) в 1 мин на 1 мГ белка (25оС, 50 мМ трис-буфер, рН 8).
2. Получение препарата тромбоксансинтетазы.
К 60 Г осажденных центрифугированием тромбоцитов человека (получены на Центральной станции переливания крови, Москва), которые хранили до использования при -60оС, добавляют 20 мл 20 мМ калий-фосфатного буфера (рН 7,4), содержащего 10 мМ Na2˙EDTA, 0,1 мМ дитиотреитол (DTT) и 1,15% KCl (буфер Б), гомогенизируют в Waring Comm. bleuder (10 раз по 30 с с промежутками в 30 с), обрабатывают ультразвуком 20 раз по 5 с с промежутками в 25 с (22 Гц; амплитуда 14-16 единиц между пиками). Полученный таким образом клеточный гомогенат (около 250 мл) центрифугируют 25 мин при 4000g, после чего супернатант (около 180 мл) рецентрифугируют 90 мин при 90˙103g. Осадок (микросомальная фракция) суспендируют в буфере Б, доводят объем до 180 мл и центрифугируют 90 мин при 90˙103g. Полученные в осадке микросхемы ресуспендируют в 20 мМ калий-фосфатном буфере, содержащем 1 мМ Na2˙EDTA, 0,5 мМ DTT, 10% глицерина и 1% Lubrol PX, доводят объем до 90 мл, выдерживают 1 ч при +4оС и центрифугируют 120 мин при 90˙103g. К 80 мл полученного супернатанта (фракция солюбилизированного детергентом фермента) добавляют 16 мл 0,2 М калий-фосфатного буфера и 25-30 мл DEAE-целлюлозы ("Whafman"), уравновешенной в 50 мМ калий-фосфатном буфере (рН 7,4), содержащем 1 мМ Na2EDTA, 0,1 мМ DTT, 10% (v/v) глицерина, (буфер В) и выдерживают 30 мин при +4оС с перемешиванием. Несвязавшуюся с DEAE-целлюлозой фракцию, содержащую тромбоксансинтетазную активность, отделяют центрифугированием (15 мин при 3500g). Оставшийся в осадке гель повторно суспендируют в 25-30 мл буфера В, выдерживают 10 мин при +4оС и центрифугируют.
В результате получают 75 мл препарата тромбоксансинтетазы с концентрацией белка 1,09 мГ/мл и специфической активностью 0,13 мкмоль ПГН2 в 1 мин на 1 мГ белка (25оС, 20 мМ калий-фосфатный буфер, рН 7,4).
3. Получение [3H] ТХВ2.
К раствору 2,8 ГБк (0,5 мкмоль) [5,6,8,9,11,12,14,15(n)-3H] арахидоновой кислоты с молярной радиоактивностью 5,6 ПБк/моль в 100 мкл этилового спирта добавляют 0,5 мл 0,2 М калий-фосфатного буфера (рН 7,4), 3,87 мл деионизированной воды, 100 мкл 100 мМ раствора L-адреналина, 100 мкл 100 мкМ раствора гемина (Fe+3-протопорфирина IX), предынкубируют 5 мин при 25оС и добавляют 330 мкл препарата ПГН-синтетазы. Через 1 мин инкубации при 25оС с интенсивным перемешиванием добавляют смесь препарата тромбоксансинтетазы (3,5 мл) и 20 мМ калий-фосфатного буфера (рН 7,4) (1,5 мл), предварительно выдержанную 5 мин при 25оС, и продолжают инкубацию в течение 30 мин. Затем добавляют 2М раствора лимонной кислоты (до рН 3) и экстрагируют продукты реакции этилацетатом (3˙30 мл). При этом в экстракте оказывается не менее 90% от исходной радиоактивности. Экстракт сушат безводным сульфатом натрия, фильтруют, упаривают и растворяют в метаноле. Выход [3H] ТХВ2 определяют с помощью ТСХ продуктов реакции в системе растворителей А - хлороформ: метанол: уксусная кислота (90: 9: 1, v/v/v). Распределение радиоактивных продуктов по пластинке определяют с помощью радиохроматосканера. Очистку [3H] ТХВ2 осуществляют с помощью препаративной ТСХ на силикагельных пластинках "Силуфол" (ЧСФР) в системе растворителей А. [3H] ТХВ2 элюируют с пластинки этилацетатом (3˙3 мл), затем растворитель упаривают и вещество растворяют в 10 мл этанола.
Получают 0,65 ГБк [3H] ТХВ2 (24% ) с молярной радиоактивностью 4,95 ПБк/моль и радиохимической чистотой 98% .
1 Описание методов выделения и очистки ПГН-синтетазы и ТХ-синтетазы и характеристики полученных препаратов ферментов приведены в примере.
2 За единицу активности (Е) ПГН-синтетазы принимают количество фермента, способное превращать 1 мкмоль АК за 1 мин при 25оС в трис-буфере (рН 8).
4 Во всех случаях концентрации [3H] АК определяется в расчете на объем реакционной смеси после добавления препарата ТХ-синтетазы ( τ > 0) или смеси двух ферментов ( τ = 0). (56) Febs Lett. , 1983, V. 157, N 1, p. 173-178.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МЕЧЕННОГО ТРИТИЕМ ТРОМБОКСАНА B | 1990 |
|
SU1732513A3 |
| СПОСОБ ПОЛУЧЕНИЯ МЕЧЕННОГО ТРИТИЕМ ПРОСТАГЛАНДИНА F | 1990 |
|
SU1774660A1 |
| СПОСОБ ПОЛУЧЕНИЯ КРАТНОМЕЧЕННЫХ ТРИТИЕМ ПРОСТАГЛАНДИНОВ ТИПА E ИЛИ ИХ ПРОИЗВОДНЫХ ТИПА A, B, F, ИЛИ МЕТИЛОВЫХ ЭФИРОВ ПРОСТАГЛАНДИНОВ ТИПА J | 1988 |
|
SU1646252A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОСТАГЛАНДИНА F | 1990 |
|
RU1774659C |
| Способ определения активности простагландин-синтетазы в тромбоцитах | 1988 |
|
SU1506358A1 |
| Способ определения типа течений шизофрений | 1989 |
|
SU1608582A1 |
| Способ получения производных пиридина | 1984 |
|
SU1391500A3 |
| ПРОИЗВОДНЫЕ БЕНЗОЛАЛКАНОВОЙ КИСЛОТЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2110512C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРАНСПОРТНОЙ РИБОНУКЛЕИНОВОЙ КИСЛОТЫ (ТРНК) ИЗ ПРЕПАРАТА СУММАРНОЙ ТРНК ПЛАЦЕНТЫ ЧЕЛОВЕКА | 1992 |
|
RU2034292C1 |
| СПОСОБ БЫСТРОЙ НОРМАЛИЗАЦИИ ОБМЕНА АРАХИДОНОВОЙ КИСЛОТЫ В ТРОМБОЦИТАХ У БОЛЬНЫХ АРТЕРИАЛЬНОЙ ГИПЕРТОНИЕЙ С МЕТАБОЛИЧЕСКИМ СИНДРОМОМ | 2007 |
|
RU2330652C1 |


Изобретение относится к способам получения биологически активных соединений, меченных радиоактивными изотопами, и может быть использовано для получения меченного тритием тромбоксана B2. Целью изобретения является повышение выхода и качества целевого продукта за счет увеличения молярной радиоактивности. Цель достигается выделением и частичной очисткой ПГН-синтетазы из везикулярных желез барана и тромбоцитов человека; инкубацией [3H]-арахидоновой кислоты с концентрацией 10 - 100 мкМ с частично очищенным препаратом простагландин Н-синтетазы (ПГН) при соотношении 0,3 - 3,3 мкмоль [3H] ЛК на 1 мГ ПГН-синтетазы в течение не более 4 мин, после чего добавляют препарат частично очищенной ТХ-синтетазы до концентрации 0,11 - 0,545 мГ/мл и инкубируют 25 - 40 мин при 25С. 1 табл. , 5 ил.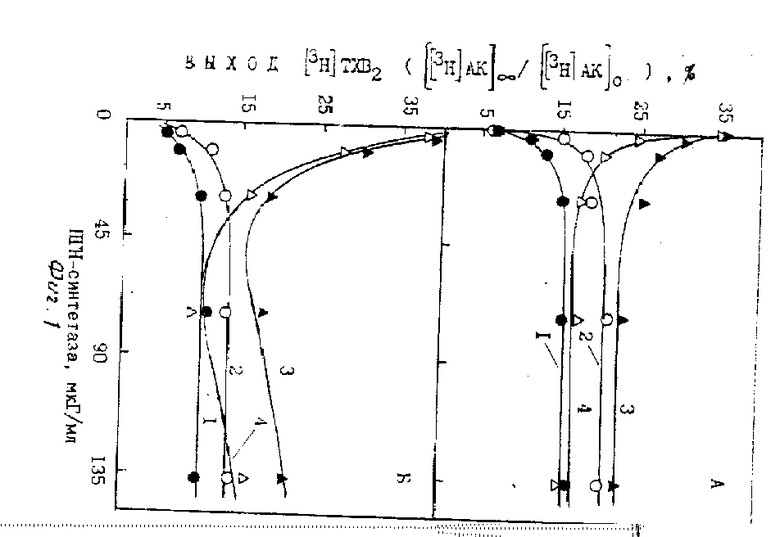
Авторы
Даты
1994-03-15—Публикация
1990-08-20—Подача