о
00
о 00 ел
Э5
Изобретение относится к способам i получения 2 гидроксиалкиловых эфиров |гликолей, которые могут найти примеМнение в качестве неионогенных поверх:ностно-активных веществ для получения моющих средств, эмульгаторов и др.
Известен способ получения алкоксилированных спиртов и гликолевых эфиров реакцией окисей олефинов со спиртами и гликолями. 8 качестве катализаторов применяют кислые катализатоipbf крекинга типа алюмосиликатов или ;катализаторы гидрирования на носителях Cl.
Недостатком этого способа являетс :полумение 17 18 масД продукта димеризации окисей, что уменьшает выход продуктов прямого присоединения спиртов или гликолей к окисям и ухудшает качество продуктов.
Наиболее близким по технической сущности к предлагаемому является способ получения, продукта реакции эпоксида с органическим соединением, содержащим реакционноспособный во дород, напри мер этанола с п МОЛЯМИ окисиэтиленаJ путем взаимодействия органического соединения содержащего реакционноспособный водород, и эпоксида в присутствии 0,001-5 катализатора, взятого в группе, состоящей из фторбората натрия, перхлората магния, кальция, маргзнца, никеля и цинка, при 80200°С tz.
Недостатком известного способа является низкая селективность, что приводит к получению смесиj содержащей- от Ц0% и выше продуктов конденсации органических соединений с полимерными формами исходных эпокси.дов.
Цель изобретения - увеличение селектизкости процесса.
Поставленная цель достигается способом получения 2-гидроксиалкиловых эфиров этиленгликоля или полиэтиленгликоля взаимодействием эпоксида с соответстеующим спиртом при 80-200 С в присутствии катализатора, S качестве -которого используют борфторид цинкэ, исходного эпоксида 1,2-окиси додецена или 1|,2-окисй
CH5(CH2)g CH-CHg OCHr-CHHrO-CHg CB2-OH,
он
тетр здецена и спирта - полиэтиленгликолЯд этиленгликоля или его эфиров.
Проведение процесса таким образом дает возможность увеличить селективность и получить мономерный продукт с содержанием его до 99.
П ример1, В стеклянный реактор с мешалкой и пробоотборником, снабженный рубашкой для нагревающей
жидкости, подаваемой от термостата, загружают 15 г диэтиленгликоля 9 г 1,2-окиси додецена, нагревают реакционную смеСь до 100 С и вводят 0,091 г гидрата борфтористого цинка, содержащего i,5 мае. : основного вещества. Через 8 мин реакционная масса гомогенизируется; нагревание продолжают 0 течение 70 мин. За ходом реакции следят, отбирая через
пробоотборник пробы и анализируя их на содержание окиси. Результаты опыта представлены в табл, 1.
Т а б л и ц а 1
Полученный продукт промывают 101-ным раствором поваренной соли при. 90-95 для отделения диэтиленгликоля с водной фазой, промывку повторяют 3 раза, объем раствора хлористого натрия соответствует половине объема органической фазы, оставшейся после-каждой промывки. Затем . органическую фазу охлаждают до и растворяют в 100 мл ацетона, засыпают а раствор безводный сульфат натрия для удаления воды и через 1020 ч отгоняют ацетон В результате получают 13j5 г бесцветной прозрачной жидкости с гидроксильным числом 383 мг КОН/Г.
Таким образом, получают неполный 2-гидроксидодециловый эфир диэтиленгликоля формулы
3. 1030356л
расчетное гидроксильное число кото-хроматографии на,пластинках Siluрого равно 387 мг КОН/г. Выход 86%. fol в смесях растворителей бензолот теоретического. Значительные поте-ацетон, взятых в отношении 1:1, и ри обусловлены частичной растворимое-этиловый спирт-вода, взятых в отноше тью полученного гидроксиэфира в воде. 10:1, обнаружено только по одноОбразования продуктов полимеризации му пятну, что доказывает индивидуальокиси нет, так как эти продукты об-ность полученного продукта, ладают худшей растворимостью в воде
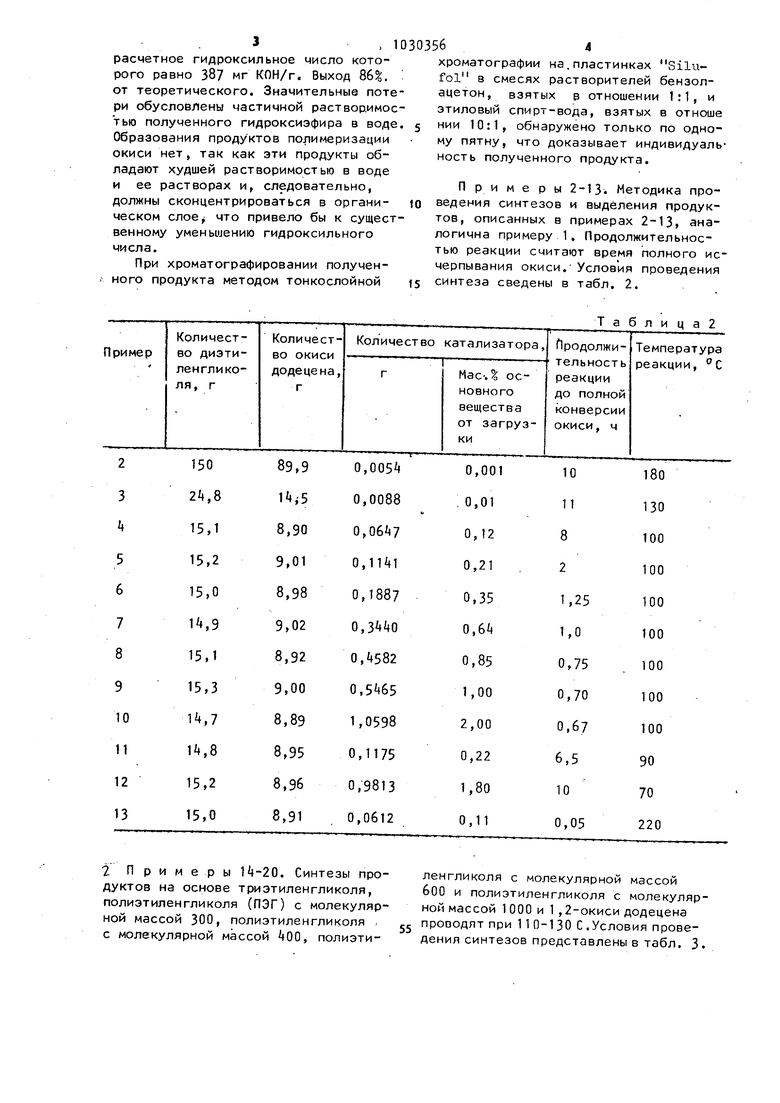
и ее растворах и, следовательно.Примеры 2-13. Методика продолжны сконцентрироваться в органи- foведения синтезов и выделения продукческом слое что привело бы к сущест-тов, описанных в примерах 2-13, анавенному уменьшению гидроксильногологична примеру 1. Продолжительносчисла. реакции считают время полного исПри хроматографировании получен-черпывания окиси. Условия проведения
ного продукта методом тонкослойной fsсинтеза сведены в табл. 2.
Таблица2



| название | год | авторы | номер документа |
|---|---|---|---|
| Водоразбавляемое термореактивное связующее для катофоретических покрытий | 1982 |
|
SU1358787A3 |
| Способ получения оксидов высших олефинов | 1987 |
|
SU1439967A1 |
| РАДИАЦИОННО ОТВЕРЖДАЕМЫЕ, СПОСОБНЫЕ ДИСПЕРГИРОВАТЬСЯ В ВОДЕ ПОЛИУРЕТАН(МЕТ)АКРИЛАТЫ | 2013 |
|
RU2648994C2 |
| Способ получения полиуретановых эластомеров, пригодных для изготовления слоистого покрытия поверхностей | 1973 |
|
SU597341A3 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОЭМУЛЬГИРУЕМЫХ ПОЛИУРЕТАНАКРИЛАТОВ | 2014 |
|
RU2656392C2 |
| Способ получения сшивающего компонента для содержащего гидроксильные группы и/или первичные и/или вторичные аминогруппы связующего для электропогружных лаков на основе аминополиолов | 1986 |
|
SU1475485A3 |
| СПОСОБ ПОЛУЧЕНИЯ ГЛИЦИДИЛОВЫХ ЭФИРОВ ПОЛИ(ОКСИАЛКИЛЕН)ГЛИКОЛЕЙ | 1995 |
|
RU2084454C1 |
| Термопластичная полимерная композиция | 1990 |
|
SU1821480A1 |
| Способ получения гидроксилсодержащих моно- или полисульфидов | 1977 |
|
SU802276A1 |
| ПРИМЕНЕНИЕ, ПРИ НЕОБХОДИМОСТИ, ОКИСЛЕННЫХ ПРОСТЫХ ТИОЭФИРОВ АЛКОКСИЛАТОВ СПИРТА В МОЮЩИХ И ЧИСТЯЩИХ СРЕДСТВАХ | 2012 |
|
RU2597014C2 |
СПОСОБ ПОЛУЧЕНИЯ 2-ГИДРОКСИАЛКИЛОВЫХ ЭФИРОВ ЭТИЛЕНГЛИКОЛЯ ИЛИ ПОЛИЭТИЛЕНГЛИКОЛЯ взаимодействием эпоксида с соответствующим спиртом при 80-200°С 8 присутствии катализатора, отли чаю. щий с я тем, что, с целью увеличения селективности процесса, в качестве катализатора используют борфторйд цинка, исходного эпоксида - 1,2-окись додецеиа или 1,2-окись тетрадецена ив качестве сИирта - полиэтиленгликоль, этиленгликоль или его эфиры.
2 Приме р ы 1}-20. Синтезы продуктов на основе триэтиленгликоля, полиэтиленгликоля (ПЭГ) с молекулярной массой 300, полиэтиленгликоля„ с молекулярной массой lOO, полиэтиленгликоля с молекулярной массой бОО и полиэтиленгликоля с молекулярной массой 1 000 и 1 ,2-окиси додецена проводят при 11 0-130 С .Условия проведения синтезов представлены в табл. 3.
Лвнгликоль
После проведения конденсации реакционную массу отмывают раствором поваренной соли, выделяют как описано в примере 1 и анаИндивидуальность состава полученных продуктов так же, как и в предыдущих примерах, подтверждается методом тонкослойной хроматографии. Таким образом,получают неполные 2гидроксидодециловые эфиры полиэтиленгликолей общей формулы R -сн- (скп(::н2о),,н он
Твбпица)
1,5
110
0,083 t30
Ь5 НО
0,75 НО
1,75
но
лизируют на содержание гидроксильных групп. Результаты анализа полученных продуктов представ.лены в табл. k. .Таблица де. R алкильный радикал с 10 атомами углерода; п - -число оксиэтильных звеньев (от 3 до 23). |(рисутствие полимеров химимеским а;|апнзс,м не. обнаруживается, содержание основного вещества близко к 100°, Дяй сравнения в табл. приведены рбсчетнь№ гидроксильные числа для. 710 продуктов Конденсации на основе диче ра OKv-си додецена. Из этих да,нных( следует, что присутствие димеризованных окисей, а.тем более продуктов с высокЬй степенью полимеризации окисей, привело бы к значительному уменьшению гидроксильного числа, легко обнаруживаемого химическим анализом. П р им е р 21. Загружают ПЭГ-400 в реактор в количестве 25 г; загрузка 1,2-окиси тетрадецена - 3 г. После нагрева реакционной массы до 90 С в реактор вводят 0,202 г гидрата Zn(BF4 )2. с содержанием цинка 18 (0,0363 г). Расчетное гидроксильное число продукта присоединения ПЭГ- 00 к 1,2-окиси тетрадецена равно 183 мг КОН/Г. Получают неполный 2-гидрокситетрадециловый эфир нонаэтиленгликоля формулы СНЛСН9)-СН-СН9-О-(СН9 С51оО)Л П -5 /У П риме р 2.. В стеклянный реактор загружают 25,8 г метилцеллозольва, что составляет 0,33 моль основного вещества и 6 г 1,2-окиси додецена, что составляет 0,335 моль осHoBHoVo вещества. Нагревают смесь до и вводят 0,526 г гидрата ZnCBFx).. Через мин окись полностью вступает в реакцию. При хроМатографировании полученного продук«юр I
Пример { Формула гидроксиалкилоаого эфира лолиэтиленгликоля ,6 ,7 18 19 20
Т а б л и ц а 5
Т.пл., ®С Н5-(сн4-у1-сНг(о-сн2-сКг)б;5 СН5-(СН2)9 СН-СН2-(ОСН2-СН2)ОН CHf(CH8)(0-CH2-CH2) ОН. Г(СНг)а- ;Н СЯ5г{о-СН2-СНг)ОН ОН Г((0-СН,-СНг) - (СН«)и (« СНг CH,)g - он .од 6 та методом тонкослойной хроматографии на пластинках Silufol в смеси ацетона и бензола., взятых в отношении 1:1, обнаружено только одно пятно; что доказывает индивидуальность полученного вещества. Гидроксильное число продукта - 206 мг КОН/г, рас7 считанное гидроксильное число составляет 209 мг КОН/Г. Получен 2-гидроксидодецилметилгликолевый эфир формулы ,.CH,)g-CH -CHj-CH,-осн.. он П риме р23. В стеклянный реактор загружают Й, г неполного иуравьинокислого эфира диэтиленгликояя, .что составляет 0,107 моль основного вещества и 20,3 г 1,2-окиси додецена, что составляет 0,107 моль основного вещества,, Нагревают смесь до , добавляют 0,4 г.гидрата Zn(BF). Полное израсходование окиси достигается за 60 мин, Хроматографирование полученного продукта на пластинках 11с;,-т,,„т11 .,. „ .,.., ., К -Silufol смесью ацетона и бензола в отношении 1:1 показывает индивидуальность полученного вещества. Гидроксильное число продукта 17б мг КОН/г, расчетное гидроксильное число 173 мг КОН/г. Получен смешанный 2-гидроксидодецилформилгликолевый эфир формулы СНз-(СН2.)9-СН-СН,-0-СНйгСНйгО-С, плавле ия веществ, плавящихся в доступных для обычных лабораторных измерений условиях, приведена в табл. .5. (-6,5)-{-Ь.9) (-6.5)-(-6,9) 1,5-1,8 .19-20 Зб-37 5 2.9-3.3
,91030356 10
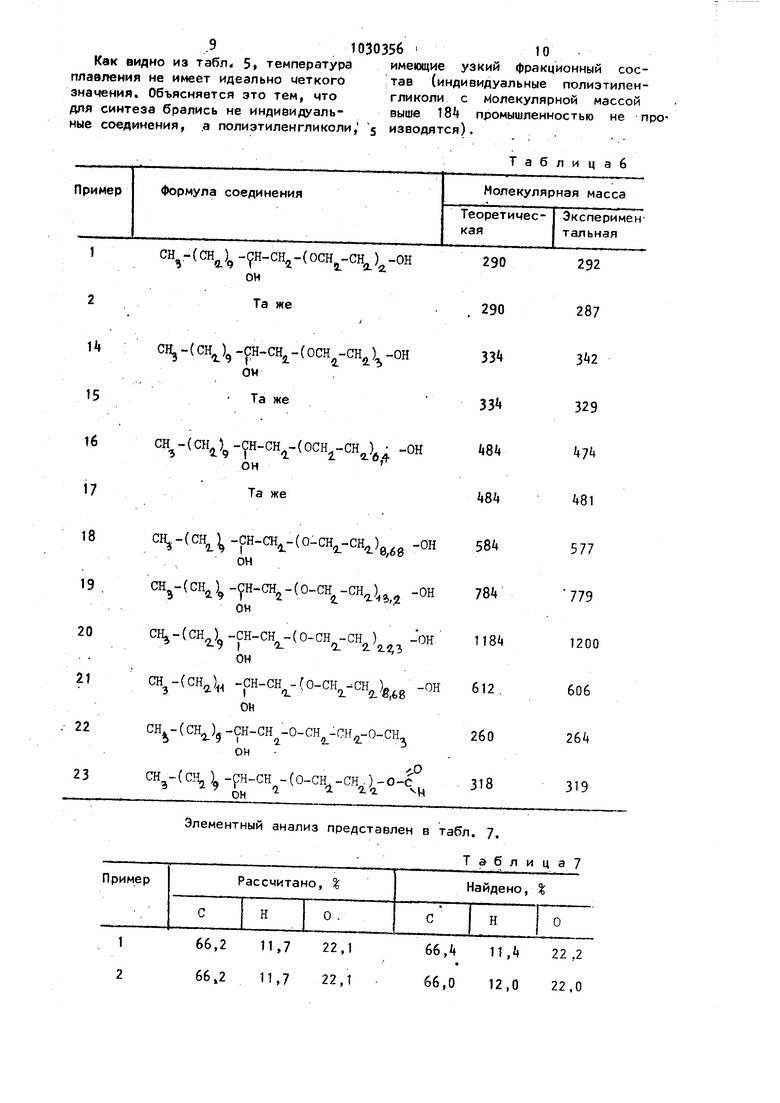
Как видно из табл. 5 температура имещие узкий фракционный сосплавления не имеет идеально меткого тав (индивидуальные полиэтилензначения. Объясняется это тем, что гликоли с Молекулярной массой для синтеза брались не Индиейдуаль- выше 18 промышленностью не проные соединения, ,а полиэтиленгликоли, 5 изводятся).
66,2 11,7 22,1
1 2 11,7 22,1
Таблицаб
66,4 11, 22,2
66,0 12,0 22,0
11
Таким образом, предлагаемый способ не содержащие по данным химического позволяет получить мономерные произ- 30 анализа продуктов полимеризации эпокводные эпоксидов и органических сое- ;сидов, и увеличить скорость . продинений с активными атомами водорода, цесса.
12
1030356 Продолжение табл. 7
Авторы
Даты
1983-07-23—Публикация
1980-12-30—Подача