

| название | год | авторы | номер документа |
|---|---|---|---|
| Производные 5-оксибензофурана, обладающие местноанестезирующим, противоаритмическим, противофибрилляторным, противосудорожным и противокаталептическим действием | 1982 |
|
SU1045584A1 |
| Арилоксиметильные производные 3-карбэтокси-4-диметиламинометил-5-оксибензофурана, обладающие анальгезирующим, противокаталептическим, противосудорожным, противоаритмическим, противофибрилляторным действием и увеличивающие объемную скорость мозгового кровотока | 1982 |
|
SU1050258A1 |
| 3-[2′ 5′ -ДИМЕТОКСИБЕНЗОИЛ]-5-ОКСИБЕНЗОФУРАН, ОБЛАДАЮЩИЙ АНТИАНГИНАЛЬНОЙ И ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ | 1978 |
|
SU1135157A1 |
| Гидрохлориды производных 2-карбэтокси-4-оксибензофурана, обладающие стимулирующим действием на мозговое кровообращение, гипотоническим действием на гладкую мускулатуру и антикаталептическим действием | 1982 |
|
SU1063058A1 |
| АНТИАРИТМИЧЕСКОЕ СРЕДСТВО | 1983 |
|
RU2068261C1 |
| ПРОИЗВОДНЫЕ БЕНЗИЛАМИДА 4-ОКСИМАСЛЯНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ МЕСТНО-АНЕСТЕЗИРУЮЩУЮ, АНТИАРИТМИЧЕСКУЮ, АНТИАНГИАЛЬНУЮ И АНТИНЕКРОТИЧЕСКУЮ АКТИВНОСТЬ | 1988 |
|
SU1601984A1 |
| ГИДРОХЛОРИД 3-(2,5- ДИМЕТОКСИБЕНЗОИЛ) -4- ДИМЕТИЛАМИНОМЕТИЛ -5-ОКСИ-6- БРОМБЕНЗОФУРАНА, ОБЛАДАЮЩИЙ АНАЛЬГЕТИЧЕСКИМ, МЕСТНОАНЕСТЕЗИРУЮЩИМ, ПРОТИВОСУДОРОЖНЫМ, ПРОТИВОАРИТМИЧЕСКИМ, СТИМУЛИРУЮЩИМ КОРОНАРНЫЙ, МОЗГОВОЙ И ПОЧЕЧНЫЙ КРОВОТОК ДЕЙСТВИЯМИ | 1989 |
|
SU1681502A1 |
| КОМПОЗИЦИЯ АМИНОКИСЛОТ С МИКРОЭЛЕМЕНТАМИ, ОБЛАДАЮЩАЯ ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ | 1999 |
|
RU2173553C2 |
| 4,6-Бисаминометильные производные 5-оксибензофурана, обладающие местноанестезирующим, антиаритмическим и спазмолитическим действием | 1977 |
|
SU677325A1 |
| Соли мезидидов @ -пиперидинкарбоновых кислот, обладающие местноанестезирующей, антиаритмической и антифибрилляторной активностью, и мезидиды @ -пиперидинкарбоновых кислот в качестве промежуточных продуктов для синтеза солей мезидидов @ -пиперидинкарбоновых кислот | 1983 |
|
SU1120654A1 |

а g
vp
где R имеет указанные значения, с первичным или вторичным амином общей формулы 3
RH.
где R имеет указанные значения, в среде неполярного растворителя, предпочтительно бензола, и образующееся основание обрабатывают соляной кислотой.
Структура соединений общей формулы 1 доказана спектральны1 и данными и подтверждена данными элементного анализа.
Пример. Получение гидрохлорида 2-карбэтокси-3-аллиламинометил-4-оксибензофурана (1а)..
Смесь 10,23 г(р.ОЗ моль) 2-карбэтоксиЗ-бромметил-4-ацетоксибенЗофурана, 6,85 г
(0,12 моль) аллиламина и 50 мл бензола вЫ держивают при 20-25°С 5-6 ч. Выделившийся осадок отфильтровывают. Маточный раствор промывают водой, сушат над сульфатом магния и упаривают. Остаток растворяют в ацетоне (50 мл), в раствор добавляют концентрированной соляной кислоты до рН 4-5. При охлаждении выпадают кристаллы. Выпавщий осадок отфильтровывают, промывают ацетоном и сушат.
Получают 4.02 г (43%) гидрохлорида 2карбэтоксй-З-аллиламинометил-4-оксибенгзофурана а еиде бесцветных кристаллов, растворимых в воде и спирте, т.разл. 194196°С (зтиловый спирт).
Найдено, %: С 58,00: Н 5.80.- N 4.БО; С 11,48.
СшН1бС1МО4.
Вычислено, %: С 57,79; Н 5,82.- N 4,49; С1 11.37.
В условиях.аналогичных примеру, получают соединения 1 б. 1 в. выход и физико-химические характеристики которых даны в табл.1.
Эти соединения представляют собой
бесцветные кристаллические вещества, устойчи.вые на воздухе, растворимые в воде и спирте.
УФтспектры этих соединений характеризуются двумя максимумами поглощения,
находящимися при 248-250 и 304-305 tffA.
В ИК-спектрах соединений общей фор мулы 1 имеются полосы поглощения в области И700-1720 и 3400-3430 см, указывающие на наличие сяожнозфирной и
гйдроксильной групп.
Опыты поставлень на здоровых лабораторных, животных, достигших половой зрелости.
Токсичность при однократном введении
определяли на 75 белых мышах обоего пола массой 18-25 г при внутрибрюшинном введении соединений. Показатели токсичности вычислены по Беренсу.
Противоаритмические свойства выявляли на модели аконитиновой аритмии в опытах на 50 крысах в сравнении с новохаинамидом и кордароном...
Первый из них был взят для сравнения как широко известный препарат, апробирОванный а эксперименте в клинике, Кордерон, как и соединений общей формулы t, йвляется производным бензофурана, про являющим при этом тот же характер деист
ВИЯ, ..
Противофибрилляторное действие иселедовали в опытах tia 16 кошках, у которых фибрилляцию желудочков сердца вызывали с помощью прямоугольного электричес.кого импульса длительностью 100 см б уязвимый период электрокардиограммы. Порог фиб рилляции определяли до введения соединений и затем после внутривенного введений их через 5,15,30 и 40 мин.
. Результаты исследований. Токсичность соединений при однократном введении мышам представлена в табл,2. Токсическив4Е(0зы вызывали угнетение мышей.
Из табл,2 следует, что соединение 1в б 2,5 раза менее токсично, чем корларст, ЛД50 которого при &нут|зибрюши«н0м eee дении составляет 35В «г/кг, ив 8 раз менее токсично новокаинами/:, УЩт 140 мгМг, Соединения 1а и t€ также менее 1йекс1лч«ы чем Новокаинамид
Результаты по исследованиш ярэтй&сгаритмической акшвмости представлен - в табл.3.
. Как видно из табл,3,151ротивоаритм1 цеская активность соединений Ши fQ в дозах 10% ЛДбо соответствует таковой новокаинамида, взятого в дозе 20% ЛДео, и кощарона, используемого в оптимальной дозе Ш мг/кг. Более высокие дозы нарушают овентрикулярную проводимость. Соединение 1а оказалось активнее препаратов,
Физико-химические характеристики соединений общей формулы 1
взятых АЛЯ сравнения; оно восстанавливало нарушенный ритм у 8 крыс из 10, тогда как новокаинамид и кордарон только у двух, В дозе 10% ЛДбо соединение 1а повышало порог фибрилляции желудочков сердца кошек в 1,7 раза.
При сопоставлении противоаритмической активности соединений (1а. 16 и 1в) с известными соединениями А и Б и противоаритмическими препаратами кордароном и никотинамидом установлено., что соединения Тб и 1в по активности нaxo/Iяtcя на уровне кордарона и новокаинамида, а соединение 1а превосходит соединения А и Б, Так. соединение ta оказывает протиеоаритмическое действие у 8 крыс из 10, а извест«ые соединения А и Б - у Б крыс из 10 и у 7 из 40 соответственно.
Следует отметить, что соединение 1а обладает также и противофибрипляторнбй активностью, которая менее выражена по сравнению с ранее описанными соединениями А и Б.
Кроме того, следует отмет «ть, что соединения общей формулы I эпачитель+1О менее токсичны, чем известные соединения А и &.
Так, ЛДбб соединений 1а, 1би 1всоставляег соответственно 121,$; 176,0 и 890,0 мг/кг, а ЛДзо известмы х соединений А и Б соответственно составляет 5t,0 и 135,0 мг/кг.
Таким образом, соединения общей формулы t по своему биологическому действию сопоставимы с известными соединениями аналогичной структуры и, кроме того, они Менее токсичны.
(56) Авторское свидетельство СССР Мг 3412453/23-04 кл. С 07 D 307/81; С 07 D 307/84, 26.03.82 непу6л«куемое).
Табяица 1
.ш
wei
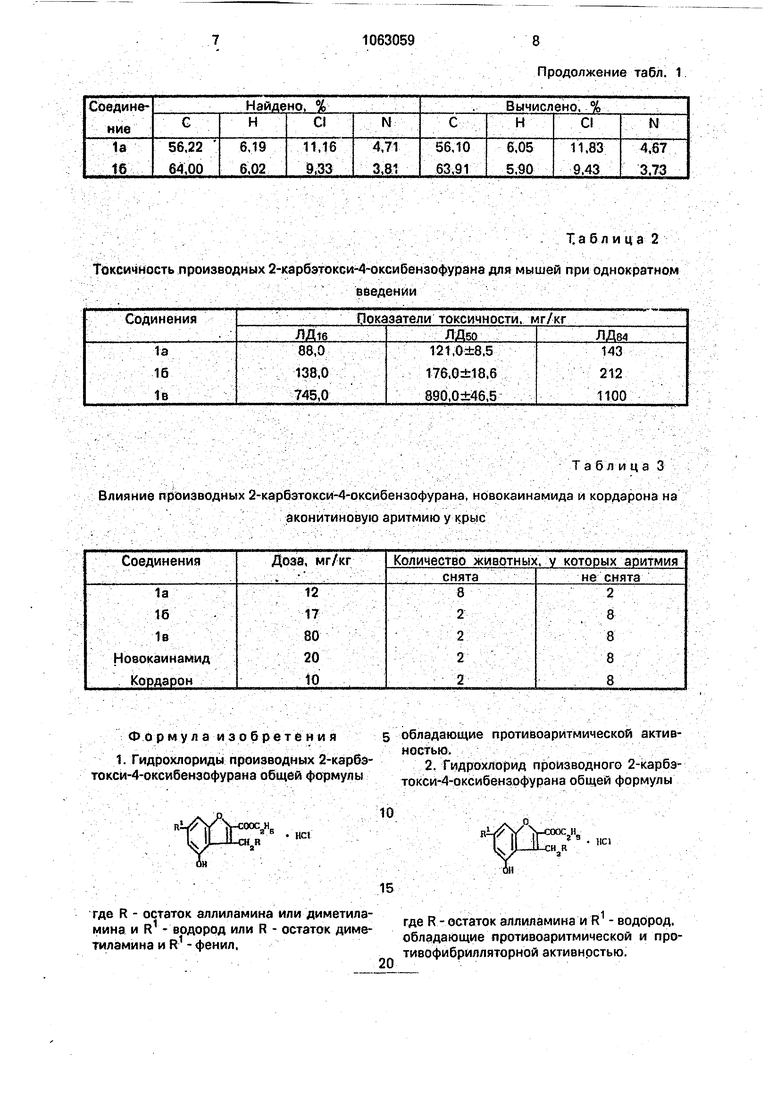
t&n....- V .. . . ..., . ,-:. - - .. Та б л и ц а 2 ; .Токсичность производных 2-карбэтокси-4 оксиббнзофуранд для мышей при однократном
,. ; ./ вйер нт :/ „ - г- . : , л ,,,
...:.,.;, . ; :..,.:,J.; / . . :, ,.-; ; . абЛИ ц а 3
Влияние производных 2-карбзтокси-4-оксибензофурана, Нбвокаинамида и кордарона на
аконитиНовую аритмию у крыс
Продолжение табл. 1
Авторы
Даты
1993-10-30—Публикация
1982-05-06—Подача