1
Изобретение относится к новому химическому соединению, а именно к гептапептиду формулы
Val-Tyr-Ile-His-Pro-Phe-Arg (1 обладающему способностью ингибировать миотропное действие брадикинина, которое может найти применение в экспериментальной биологии , и медицине.
Брадикинин играет существенную роль в воспалительных процессах. Биологические эффекты брадикинина - увеличение проницаемости сосудов, болевое действие, миотропное действие на гладкую мускулатуру и т.д.5 физиологически существенные в острых процессах, нежелательны в хронических воспалениях и в случае ожогов.
Известен структурньш аналог брадикинина - октапептид формулы
835602
Arg-Pro-Pro-Gly-Phe-Ser-Pro-Leu, обладающий способностью ингибиро-г вать миотропное действие брадикинина. Однако его биологическая ак5 тивность недостаточна для создания на его основе медицинских препаратов, ингибирующих миотропное действие брадикинина.
О Цель изобретения - расширение арсенала средств, ингибирующих мидтропное действие брадикинина.
Цель достигается гептапептидом формулы
15 Val-Tyr-Ile-His-Pro-Phe-Arg
Синтез гептапептида формулы 1 осуществляют известными методами путем конденсации отдельных пептид20 ных фрагментов азидным методом согласно нижеприведенной схеме:



| название | год | авторы | номер документа |
|---|---|---|---|
| Циклический аналог ангиотензина,обладающий способностью ингибировать прессорное и миотропное действие ангиотензина | 1981 |
|
SU1067796A1 |
| Способ получения пептидов | 1978 |
|
SU845773A3 |
| СПОСОБ ПОЛУЧЕНИЯ БУСЕРЕЛИНА И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ЕГО ПОЛУЧЕНИЯ | 2010 |
|
RU2442791C1 |
| Способ получения метиловых эфиров октапептидов | 1981 |
|
SU1041030A3 |
| Способ получения полипептидов или их солей | 1977 |
|
SU910116A3 |
| Способ получения октапептидов | 1981 |
|
SU993816A3 |
| КОНЪЮГАТЫ АНТИТЕЛА И ЛЕКАРСТВЕННОГО СРЕДСТВА (ADC) И КОНЪЮГАТЫ АНТИТЕЛА И ПРОЛЕКАРСТВА (APDC), СОДЕРЖАЩИЕ ФЕРМЕНТАТИВНО РАСЩЕПЛЯЕМЫЕ ГРУППЫ | 2016 |
|
RU2751512C2 |
| Циклические аналоги каллидина и других пахикининов,обладающие пролонгированным гипотензивным действием в сочетании с низкой или полностью отсутствующей миотропной активностью | 1978 |
|
SU1219587A1 |
| ЛИНКЕРЫ НА ОСНОВЕ СУЛЬФОМАЛЕИМИДА И СООТВЕТСТВУЮЩИЕ КОНЪЮГАТЫ | 2019 |
|
RU2815199C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИПСИХОТИЧЕСКОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2411248C2 |

Гептапептид формулы Val-Tyr-Ile-His-Pro-Phe-Arg обладающий способностью ингибировать миотропное действие брадикинина. сл эо со :л 35
Z - бензилоксикарбонил;
Вое -- трет.-бутилоксикарбонил;
Bzl - бензил;
BzlNOg - п-нитробензил;
NOj нитрогруппа;
Me - метил;
NP - п-нитрофенил
В синтезе были использованы производные аминокислот фирмы Реанал (ВНР). Все аминокислоты L-конфигурации.
Температуру плавления синтезированных соединений определяют в открытых капилярах без исправления. Гмогенность полученных с оединений контролируют с помощью тонкослойной хроматографии (ТСХ) и методом ЯМР. тех осуществляют на пластинках с силикагелем фирмы Мерк (ФРГ) с следующих системах:
А хлороформ - метанол - уксусая кислота (85:10:5);
Б - хлороформ - этанол - н-бутанол - этилацетат - вода (10:6:4:3:1);
В - хлороформ - этанол - изопропанол - этилацетат - вода (10:6:4:3: l) ;
Г - хлороформ - этанол - вода (40:47:5);
Д - хлороформ - метанол - уксусная кислота - вода (12.0:41 f6:6);
Е - эт1 шацетат - пиридин - уксусная кислота - вода (5:3:1:2);
Ж - пиридин - н-бутанол - уксусная кислота - вода (10:15:3:12).
Электрофоретическая подвижность оединений приведена по отношению
к гистидину ( Е „,g на бумаге FN -15 в 5 н (рН 1,9) уксусной кислоте.
Аминокислотный состав определяют на анализаторе Liquimat III фирмы Kontron (ФРГ).
Пример . Получение гептапептида формулы .
-Tyr(Bzl)-Ile-His(Bzl)-Pro-Ome (ll)
К охлажденному до раствору 20,74 г (40 ммоль) гидразида бензилоксикарбонил-валил-0-бензил-тирозина в 300 мл ДМФЛ добавляет 53,3 мл (160 ммоль) 3 н раствора хлористого водорода в этилацетате, 4,61 мл (40 ммоль) трет.-бутилнитрита в 10 мл ДМОЛ и выдерживают 30 мин при -20°С и 10 мин при -5 С. Затем реакционную смесь охлаждают до -40°С и прибавляют охлажденный до -10 С раствор 16,56 мл (120 ммол триэтиламина в 30 мл ДМФЛ и при -20 С раствор I метилового эфира изолейцил-N -бензил-гистидина, полученный добавлением 11,04 мл (80 ммоль) триэтиламина к охлажденному до раствору 21,7 г (40 ммоль) дихлоргидрата метилового эфира изолейцил-N -бензил-гистидина в 200 мл ДМФЛ (.осадок хлоргидрата триэтиламина удаляют фильтрацией) .
Реакционную смесь вьщерживают при +4 С 24 ч, частично упаривают, остаток выливают в 300 мл смеси, состоящей из насыщенного раствора хлористого натрия и 5%-ного раствор бисульфата натрия (2:1), Выпавший осадок отфильтровывают, промывают водой и высушивают в вакууме над PjOy/KOH.
Выход 34,4 г (90%), т.пл. 179182°С.л -32 ( ДМФЛ). ,22 (Л); 0,71 (Б); 0,81 (Б).
Вос-РЬе-Лг§(1ГО2)-ОБ21К02 (Ш
К охлажденному до раствору 7,82 г (20 ммоль) хлоргидрата п-ниробензилового эфира М -нитро-аргинина в 50 мл ДМФЛ добав,ляют .2,76 мл (20 ммоль) триэтиламина, 1,36 г (20 ммоль) имидазола в 10 мл ДМФЛ и 8 г (20 ммоль) п-нитрофенилового эфира трет-бутилоксикарбонш1-фенш1аланина в 50 мл ДМФЛ, Затем реакцио
ную смесь перемешивают при комнатной температуре 48 ч, вЬшивают в 5%-ный раствор бисульфата натрия и экстрагируют этилацетатом.
Этилацетатный экстракт промьшают водой, 5%-ным раствором бикарбоната натрия, водой и упаривают. Остаток растирают с эфиром, отфильтровьшают и сушат в вакууме над . Выход 10,9 г (91%).
К раствору 9,56 г (10 ммоль) метилового эфира бензилоксикарбонил-валил-О-бензил-тирозил-изолей ;;цил-М -бензил-гистидилпролина (П)
в 200 мл ДМФА добавляют 5 мл (100 ммоль) гидразина.
Реакционную смесь вьщерживают при комнатной температуре 48 ч и выливают в 1000 мл насыщенного
раствора хлористого натрия, вьтавший осадок отфильтровьгеают, промывают водой и сушат в вакууме над
P OS/KOH.
Выход 9,1 г (95%).Rг 0,45 (Л); 0,38 (Б); 0,70 (Д).
(V)
НС1-H-Phe-Arg(N0,)-OBzlNO,
К раствору 10,5 г (19 ммоль) ТТТ в 100 мл этипацетата добавляют 19 мл (76ммоль) 4 н,раствора хлористого водорода в этилацетате. Реакционную смесь выдерживают при 20°С 30 мин, упаривают в вакууме, остаток растирают с эфиром, осадок отфильтровывают и сушат в вакууме . над .
Выход 9,9 г (99%).o -6,2 ( СНзСООН);Я, 0,20 (Л); 0,31 (Б); 0,48 (Г);
Z-Val-Tyr(Bzl)-Ile-Hi8(Bzl)-Pr6-Phe-Лrg(NOг)-OBzlN02(VI)
К охлажденному до -20с раствору 1,91 г (2 ммоль) IV в 50 мл ДМФЛ добавляют 2,67 мл (8 ммоль) 3 н.раствора хлористого водорода в этилацетате, 0,23 мл (2 ммоль) трет.-бутилнитрита в 3 мл ДМФА и выдер живают 30 мин при -20 С и 10 мин при -5 С. Затем реакционную смесь охлаждают до и прибавляют охлажденный до раствор 1,1 мл (8 ммол триэтиламина в 5 мл ДМФА и при -20 С раствор п-нитробензилового эфира фенилаланил-N -нитроаргинина, полученный добавлением 0,28 мл (2 ммоль) триэтиламина к охлажденному до О С раствору 1,08 г (2 ммоль V в 20 мл ДМФА. Реакционную смесь выдерживаютпри 24 ч, выливают в смесь, состоящую из 150 мл насыщенного раствора хлористого натрия и 50 мл 5%-ного раствора бисульфата натрия. Выпавший осадок отфильтровывают, промывают водой и сушат в вакууме над Выход 2,5 г (87%). т.пл. 125127°С, -34,0°/С 1;:ДМФА/; ,90 (Б); 0,53 (В); 0,68 (Г). 6. Валил-тирозил-изолейцил-гистидил-пролил-фенилаланил-аргининVal-Tyr-Ile-His-Pro-Phe-Arg (I) К раствору 0,5 г (0,35 ммоль) VI в смеси метанол-уксусная кислотавода (5:l:l) прибавляют 0,2 г палладиевой черни и гидрируют 24 ч. Затем катализатор отфильтровывают, фильтра упаривают, остаток растирают с эфиром, осадок отфильтровывают и очищают на колонке с целлюлозой СМ-50, элюент-градиентный раствор ацетата аммония. После очистки йродукт лиофилизуют. Выход О,, 14 г (44%) -24,0° ( СН,СООН);R , 0,80 (Е); 0,77 (Ж); , Аминокислотный анализ: Val 0,95 (1); Тур 0,90 (1)1 Не 1,0 (1); His 0,89 (1); Pro 0,97 (1); Phe 0,96 (1); Arg 0,87 (), Биологическая активность описываемого гептапептида изучена в опытах in vitro и in vivo. В опытах in vitro изучена миотропная активность а в опытах in vivo - влияние на артериальное давление наркотизированных крыс и на депрессорный эффект брадикинина, В качестве стандартного препарата использовали триацетат брадикинина фирмы Реанал (ВНР). 1. Определение миотропной активности, Миотропная активность описываемого гептапептида изучена в опытах in vitro по известной методике путем регистрации изотонических сокращений изолированных маток (uterus) крыс. Для регистрации использован модифицированный прибор ВИ6-5МА. Агонистические и антагонистические свойства гептапептида формулы 1 изучены в,диапазоне концентраций -10 М. Определены параметры, характеризующие взаимодействие вещества с рецептором (л- внутренняя активность, рД - показатель специф чecкoгo агонистического сродства, рА2 - показатель специфического антагонистического сродства). Время предварительной экспозиции органов изучаемым соединением при исследовании его влияния на миотропнь Й эффект брадикинина составляет 3 мин. При расчетекумулятивных кривых концентрация - эффект (КККЭ) каждая точка или значение определены из 6 опытов ± стандартцая ошибка ,05. Полученные результаты представлены в таблице и на фиг. 1 и 2. Влияние гептапептида 1 на миотропное действие брадикинина териальное давление. Белых крыс обоего пола весом 180-200 г наркотизируют 25%-ньгм раствором уретана из расчета 0,5 мл/100 г веса. Артериальное давление регистрируют из общей сонной артерии при помощи трансдюсера (Bentley Trantec Pressure Transducer) на двухканальном ре7
гистрирующем приборе Gemini (Италия) . Вещество вводят в бедренную вену в виде инъекции в объеме 0,1 мл/200 г в дозах 0,5500 мкг/кг. Влияние на депрессорный эффект брадикинина изучают путем его введения в дозах 5-500 мкг за 1 мин до введении брадикинина.
Токсичность описываемого соединения определена на мышах.
В результате проведенных исследований установлено, что в опытах invitro на изолированной матке крысы гептапептид формулы 1 проявляет миотропную активность, характеризующуюся следующими параметрами: ot 0,52.tO,09, рДг 7,00+0,27, а в концентрации 10М конкурентно ингибирует миотропньш эффект брадикинина ,18±0,29, что почти на два порядка выше, чем у известного антагониста брадикинипа 835608
Arg-Pro-Pro-Gly-Phe-Ser-Pro-Leu (,3).
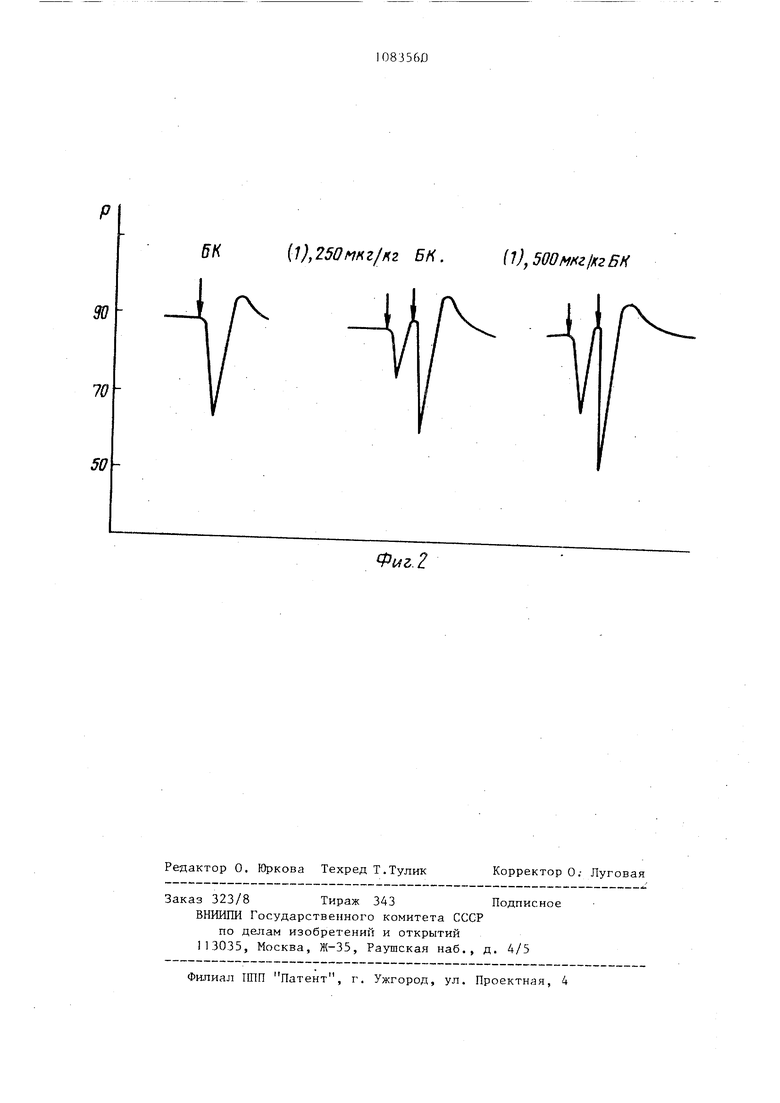
. В опытах in vivo на наркотизированных уретаном крысах при внутри5 венном введении исследуемое соединение в дозах до 250 мкг/кг не оказывает влияния на артериальное давление и не влияет на депрессорный эффект брадикинина. В дозе 500 мкг/кг 10 оно проявляет эквидепрессорный с брадикинином эффект, а также незначительйо потенцирует депрессоркый эффект последнего,
ЛД 5р гептапептида формулы 1 сос15 тавляет 175±15 мг/кг.
Таким образом, описываемое соединение обладает выраженной способностью конкуретно блокировать рецепторы брадикинина в экстравазальных 20 гладкомышечных тканях без существенного влияния на гипотензивное действие брадикинина.
(l),250i KzlH2 БН.{1),500м/ г1/(гБН
5К
90
70
50
Фиг. 2
| Regoli D., Barabe J., Pharmacology of bradykinin and related kinins, Pharmacol | |||
| Rev., 3, 1 |
Авторы
Даты
1986-01-30—Публикация
1982-05-26—Подача