2.Способ получения химически мо-дифицироваиного носителя на основе кремнезема, включающий обработку кремнезема J - глицидилоксипропилтриэтоксисиланом до содержания на поверхности носителя эпоксидных групп в количестве 15-1000 мкмоль/г, Отличающийся тем, что
обработанный у-глицйдиоксипропилтриэтоксисиланом кремнезем дополнительно обрабатывают тиоцинатом щелочного металла или тиомочевиной в количестве 20 - 100 моль на 1 моль эпоксигрупп в среде апротонного растворителя при 50100°С.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ХИРАЛЬНОЙ ПЛАНАРНОЙ ПЛАСТИНЫ ДЛЯ ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИИ ОПТИЧЕСКИХ ИЗОМЕРОВ | 2012 |
|
RU2545315C2 |
| Способ получения модифицированного кремнеземного носителя для иммобилизации биоспецифических лигандов | 1987 |
|
SU1477439A1 |
| Модифицированный полимерами макропористый кремнезем в качестве носителя для дисульфидно-обменной ковалентной хроматографии белков и способ его получения | 1977 |
|
SU687081A1 |
| Способ получения иммобилизованного катализатора гидросилилирования | 1977 |
|
SU743717A1 |
| Способ получения тиолсодержащих сорбентов | 1978 |
|
SU771106A1 |
| СУБСТРАТ ДЛЯ ИММОБИЛИЗАЦИИ ФУНКЦИОНАЛЬНЫХ ВЕЩЕСТВ И СПОСОБ ПРИГОТОВЛЕНИЯ ДАННОГО СУБСТРАТА | 2011 |
|
RU2602901C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННОЙ УРЕАЗЫ | 2004 |
|
RU2294369C2 |
| Способ получения активированных носителей | 1977 |
|
SU859372A1 |
| Способ получения носителя для иммобилизации органических соединений | 1982 |
|
SU1153975A1 |
| СПОСОБ ПОЛУЧЕНИЯ КРЕМНЕЗЕМАЛЬДЕГИДОВ | 2009 |
|
RU2400468C1 |
1.Химически модифицированный носитель на основе кремнезема с диаметрами пор 10-250 нм, содержащий на поверхности группы формулы -(с1Нг)з-0- Нг-с1н-енг для иммобилизации биологически активных соединений. (Л со -vj ел СП 00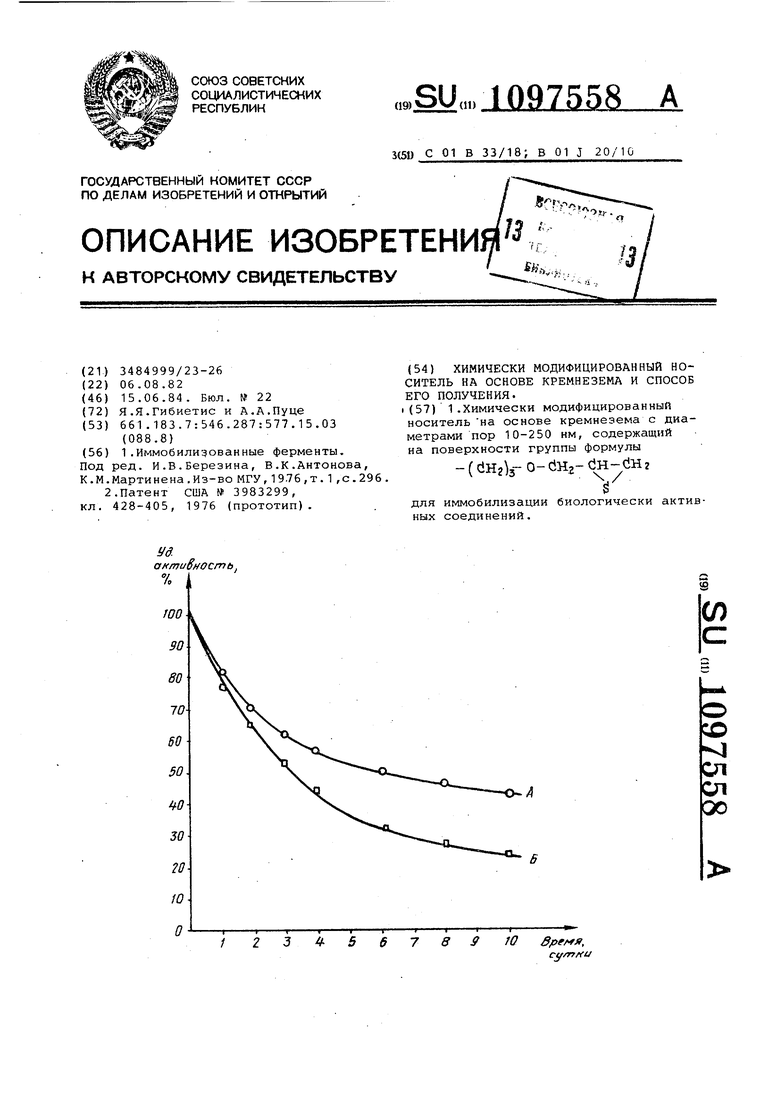

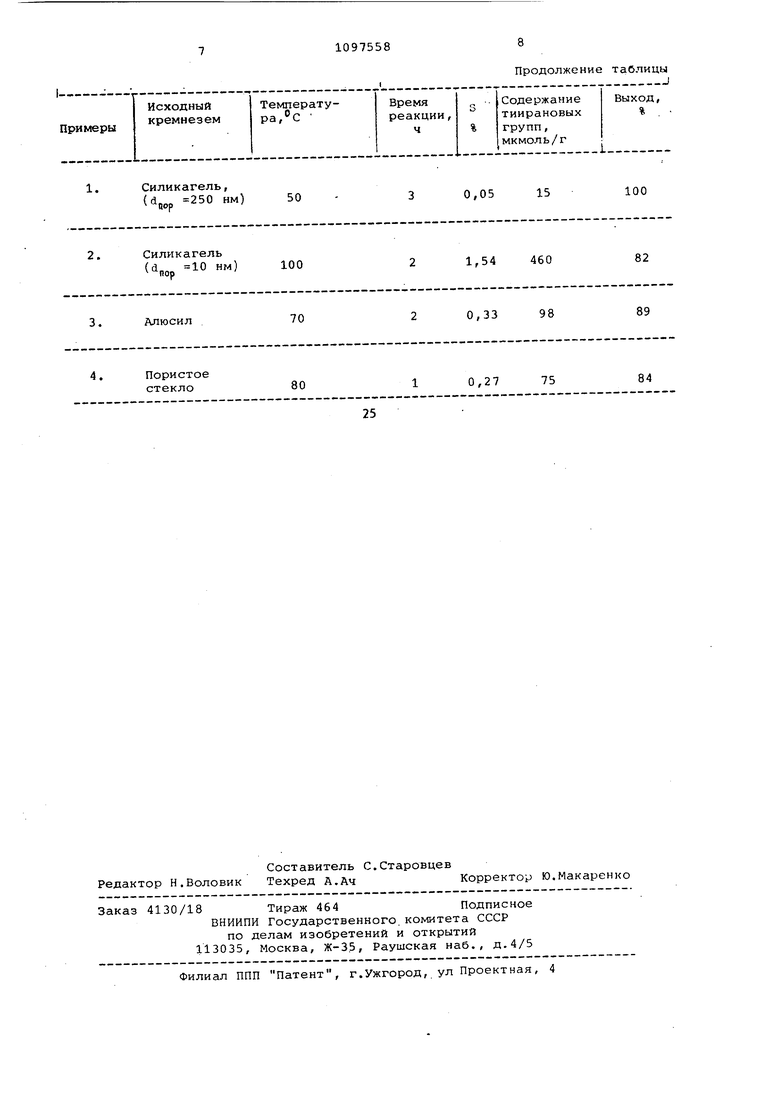
Изобретение относится к способу получения химически модифицированных кремнеземных носителей и может быть использовано для иммобилизации биологически активных соединений ферментов, их ингибиторов, кофакторов . Известны модифицированные органи ческими соединениями кремнеземные носители, используемые для иммобили зации биологически активных веществ Однако известные носители предна значены для иммобилизации соединени содержащих лишь определенные функци нальные группы и во многих случаях их необходимо дополнительно активировать. Наиболее близким к предлагаемому iявляется носитель 2J на основе мак .ропористого кремнезема,- содержащий поверхности группы формулы -(ЙНг),- О-ЙНг- dH- ОН 5 / . Указанное соединение привито к поверхности кремнезема гидролитичес ски прочной системой связей 5 Si -О - Si - С. Эпоксидные группы носителя способны реагировать с функциональными группами ( - ОН,- NHg - SH) биологически активных молекул что определяет возможность использо вания данного носителя для иммобилизации широкого набора ферментов, ингибиторов и др. Носитель с привитыми эпоксигруппами получают обработкой кремнезема раствором у -глицидилоксипропилтриэтоксисилана в воде или органическом растворителе 2 . Однако при иМ14обилиэации на данном носителе биологически активных молекул, содержащих тиольные группы, помимо эффекта иммобилизации наблюдается потеря биологической активноети. При этом полученные препараты им мобилизованных биологически активных молекул данного химического строения под воздействием кислорода быстро те ряют свою активность, так как тиольные группы легко окисляются кислоро-, дом. При обычных условиях иммобилизации (водный раствор, воздух), а также при хранении готового продукта, иммобилизируемое вещество (или иммобилизованное на носителе вещество) соприкасается с кислородом, что и приводит к потере их биологической активности. Для избежания данного нежелательного явления, процесс иммобилизации биологически активных молекул, содержащих тиольные группы, на носителе известного строения обычно осуществляют в Инертной атмосфере или в присутствии восстанавливающих агентов 2-меркаптоэтанрла, дитиотреитола. Последние снижают выход и загрязняют целевой продукт. Цель изобретения - получение химически модифицированного носителя на основе кремнезема для иммобилизации биологических соединений, в том числе биологически активных молекул, со/держащих тиольные группы. Поставленная цель достигается тем, что химически модифицированный носитель на основе кремнезема с диаметрами пор 10-250 нм, содержащей на поверхности группы формулы (еНг)з-0- 2Нг-Сн-йНг ля иммобилизации биологически акивных соединений. Способ получения химически модиицированного носителя на основе ремнезема, включающий обработку ремнезема -глицидилоксипропилтритоксисиланом до содержания на поерхности носителя эпоксидных групп количестве 15-1000 мкмоль/г обработанный у-глицидилоксипропилтритоксисиланом кремнезем дополнительно обрабатывают тиоцинатом щелочного еталла или тиомочевиной в кпли«естве 20-100 моль на 1 моль эпоксигрупп, в среде апротонного растворителя при 50-100°с Сущность способа заключается в iTOM, что носитель, содержащий на inosepxHOCTH эпоксидные группы в количестве 15-1000 мкмоль/г обрабатывают в соответствии со схемой Р-((1Нг)з- 0-dH2-«iH-dH2 + )2 О «- Р-{ЙНг)з-0-с Нг-с5н-ОН+ О-СйШг), т «f J р где Р - кремнезем; tt - щелочной металл. Носитель общей формулы (1) получ ют с выходов 80-100% в зависимости от структуры кремнеземной матрицы и условий реакции. Носитель представляет собой макропористый кремнеземный материал, с держащий на поверхности тиирановой группы в количестве 15-460 мкмоль/г носителя. Тиирановые группы носител как и эпоксидные группы, способны реагировать с нуклеофильными функци ональными группами биологически активных молекул, что приводит к иммо билизации последних. Иммобилизация протекает по следу щей схеме Р-( ОНг)з- 5Нг-Ь НЫ-3- . i - Р-(с н4-0- Нг-ЙН-бНг-У-Ъ где Р - кремнезем; 8 - молекула биологически акти ного вещества; Ч - О, NH, S. Таким образом, в процессе иммоби лизации биологически активных молекул на носителе общей формулы (1) образуются свободные тиольные группы. Образование этих групп позволяе использовать носитель для иммобилиз ции активных молекул, содержащих ти ольные группы: свободные тиольные группы, находящиеся на поверхности носителя, служат в качестве восстанавливающего агента. Полученный модифицированный кремнеземный носитель общей формулы (1) в процессе иммобилизации исполняет две функции: матрицы для иммобилизации и восстанавливающего аген та. Способ получения носителя осуществляется следующим образом. Обработку исходного носителя, со держащего эпокси-группы, проводят избытком тиоцината щелочного метгшла или тиомочевины (на 1 моль эпоксидных групп исходного вещества используют 20-100 молей соответствующего агента), обработку исходного вещества проводят в среде полярного апротонного растворителя, например диметилформамида (ДМФА), диметилсульфоксида (ДМСО) и др., при 50 100°С. При-мольном соотношении тиоцината щелочного металла или тиомочевины к эпоксигруппам меньше чем 20:1 снижается выход реакции, соотношение больше чем 100:1 нецелесообразно. При температуре меньше 50 С значительно увеличивается время проведения реакции. При температуре выше протекают побочные реакции, приводящие к разрушению тиирановых групп. Применение протонного растворителя приводит к раскрытию тиирановых групп до тиольных. Полученный модифицированный кремнеземный носитель общей формулы (1) представляет собой белое вещество в форме гранул сферической или нерегулярной (JjOpNttJ, нерастворимое в воде и органических растворителях, которое разлалается в концентрированных щелочах и в растворе фтористого водорода. Структура нового соединения подхвержена элементным анализом, титриметрическим определением тиоэпоксидных групп. Пример. 10,О г силохрома С-80, модифицированного -глицидилоксипропилтриэтоксисиланом и содержащего 130 мкмоль/г эпоксидных групп, суспендируют в 50 мл диметилформамида (ДМФА) и при перемешивании добавляют раствор реагента, содержащего 5,8 г (60 моль) тиоцината калия в 50 мл ДМФА (соотношение 50:1). Перемешивают при 80 С в течение 2ч, фильтруют. Нерастворимый продукт промывают последовательно ДМФА, холод-, ной водой и ацетоном до полного удаления растворимых компонентов. Сушат в вакуумэксикаторе 5 ч. Получают 10,0 целевого продукта. Найдено, % : 5-0,38 Вычислено,%: S - 0,35 Содержание титрируемых тиопоксидных групп 112 мкмоль/г. Выход по функциональным группам 93%. Пример2. По примеру 1 осуществляют синтез носителя, изменяя температуру реакции, соотношение реагентов и тип исходного кремнеземного носителя. В таблице представлены характерно тики носителей в зависимости от ус.поВИЙ обработки (тип и количество реагента, температура, растворитель, время реакции).
; Примерз, 1,0г модифицированного носителя, полученного по примеру 1, суспендируют в 10 )уш фосфатного буферного раствора (рН 7,6) в котором растворено 10 мкмоль трилона Б, смесь встряхивают 15 мин. Добавляют 100 мг трипсина, растворенного в 10 мл буферного раствора, и выдерживают смесь в течение суток -при 5°С, периодически встряхивая. Продукт фильтруют, промывают фосфатным буферным раствором и дистиллированной водой. Продукт содержит 38 мг белка на 1 г сухого веса, удельная активность иммобилизованного трипсина 42 ед/г..
Пример4. 50 мг уреазы в бикарбонатном буфере (10 мл 0,05 М, рН 8,6) инкубируют с 5,0 модифицированного кремнеземного носителя, полученного по примеру 1, при 2-5°С в течение 2 сут. Продукт фильтруют, промывают буферным раствором с добавлением 0,5 М NaCl. Продукт содержит 8 мг/г белка, удельная активность 70 ед/г,
И р и М е р 5. Образец препарата, полученного по примеру 4, инкубируют -в фосфатном буферном растворе .(0,01 М, рН 7,5) при 15°С, В аналоги1. Силикагель,
(пор 250 нм)
15
(d,p 10 нм) 570
110
Алюсил
Пористое
БС(НП2)2
90 стекло
ных условиях инкубируют уреазу, иммобилизованную на носителе, полученного по прототипу. Через определенные промежутки времени определяют уреазную активность препарата.
На чертеже изображена зависимость удельной активности уреазы от времени хранения.
Кривая А описывает изменение удел ной активности уреазы, иммобилизованной на предлагаемом носителе, кривая Б уреазы иммобилизованной на носителе - прототипе.
Таким образом, предлагаемый носитель за счет возникновения тиольных групп при иммобилизации соединений позволяет получать препараты иммобилзованных биологически активных веществ более устойчивые к окислению и сохраняющие свою активность на высоком уровне длительное время.
Технико-экономическая эффективность изобретения состоит в том, что использование предлагаемого носителя для И1 мобилизации биологически активных соединений позволит расширить ассортимент иммобилизованных препаратов, в частности биологически активных веществ, содержащих тиольные группы.
100
ДМФА
KSCH
20
ДМФА
WaSCN
50
ДМФА
KSCN
50
ДМСО
1, Силикагель,
{d,p 250 нм) 50
Продолжение таблицы
J
100
0,05 15
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Под ред | |||
| И.В.Березина, В.К.Антонова, К.М.Мартинена,Из-во МГУ, 19.76, т | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Солесос | 1922 |
|
SU29A1 |
| Способ получения сульфокислот из нефтяных масел | 1911 |
|
SU428A1 |
| Уд | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
Авторы
Даты
1984-06-15—Публикация
1982-08-06—Подача