1
изобретение относится к химии органических изоцианатов и их производных, а именно - к способам разделения смесей 2,4- и 2,6-толуилендиизоцианатов (ТДИ), которые являются продуктами многотоннажного производства и представляют собой важнейшее сырье для синтеза полиуретанов.
Свойства полимерных материалов существенно зависят от строения используемых для их получения мономеров, В связи с этим огромное значение имеет проблема выделения чистых 2,4- и 2,6-ТДИ.
Известен способ разделения смеси этих диизоцианатов, заключающийся в использовании их различной реакционной способности при взаимодействий с сухим хлористым водородом. Образующийся в первую очередь осадок 2,4-карбамилхлорида отфильтровывается, а из раствора выделяется 2,6-изомер О .
Недостатком этого способа является ограниченная избирательность реакции, вследствие чего невозможно получить чистый 2,6-ТДИ. Последний получается только с примесью 2,4-ТДИ.
Известен также способ разделения смеси 2,4- и 2,6-ТДИ методом парциальной кристаллизации 2,
Недостатком способа является невозможность получения чистых изомеров. 2,4-ТДИ вьщеляется с примесью 2,5% 2,6-ТДИ, а 2,6-ТДИ содержит до 7% 2,4-ТДИ.
Наиболее близким к предлагаемому по технической сущности и достигаемому результату является способ разеления смеси 2,6-ТДИ с помощью трет-бутилового спирта. Способ заключается в том, что смесь 2,4- и 2,6-ТДИ состава 65:35 обрабатывают трет-бутиловым спиртом в расчете на 2,4-ТДИ. Так как изоцианатная группа в положении 4 более реакционоспособна, чем в положениях 2 и 6, в первую очередь спирт реагирует 2,4-ТДИ. Реакция протекает при . Непрореагировавший 2,6-ТДИ тгоняется в вакууме и его выход сотавляет 35% .
К недостаткам известного способа относится малая избирательность реакции Трет-бутилового спирта со сме СЬЮ 2,4- и 2,6-ТДИ, так как наряду
1172972
с 2,4-изомаром в реакцию со спиртом вступает часть 2,6-ТДИ и получается не чистьй .2,6-ТДИ, а смесь 2,6- и 2,4-ТДИ состава 84:16; выделение
5 одного из изомеров (а именно 2,), тогда как 2,4-ТДИ остается связанным в виде уретана и невысокий выход целевого продукта.
Целью изобретения является повы0 шение селективности процесса и увеличение выхода обоих изомеров.
Поставленная цель достигается предлагаемым способом разделения 2,4- и 2,6-толуилендиизоцианатов,
15 который состоит в том, что смесь 2,4- и 2,6-трлуилендиизоцианатов обрабатьшают Н,Л-дизамещенными трихлорацетамидинами общей формулы
С1зС
(О
Ч X
X
где X - диметиламино-, диэтиламиНО-, дипропиламино-, дибутиламино-, морфолино-, пиперидино-группы, в среде петролейного эфира или уайтспирита, или керосина при температуре от -5 до 20С, после чего образовавшуюся Ы-(4-метил-З-изоцианатофенил)-N-(1-диалкйламино-2,2,2-трихлорэтилиден) мочевину общей формулы .../Г СС1з
шз-рьт-с-к с „„ лсо о
где X имеет указанные значения, отделяют из реакционной массы, из
остатка упариванием с последующей перегонкой выделяют 2,6-изомер, затем замещенную мочевину общей формулы И обрабатывают сухим хлористым водородом в среде органического растворителя при 80-1 , вьтавший при этом солянокислый l,N-диaлкилтрихлорацетамидин отфильтровывают и из фильтрата выпариванием с после-. дующей перегонкой выделяют 2,4-толуилендиизоцианат.
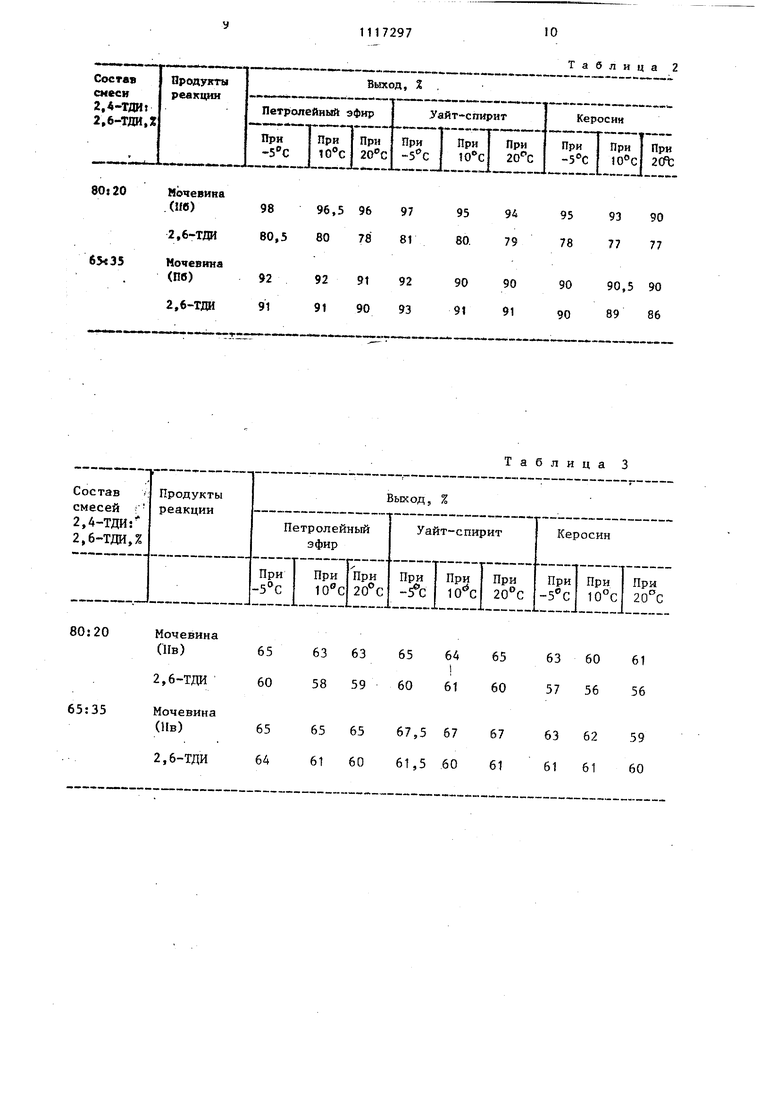
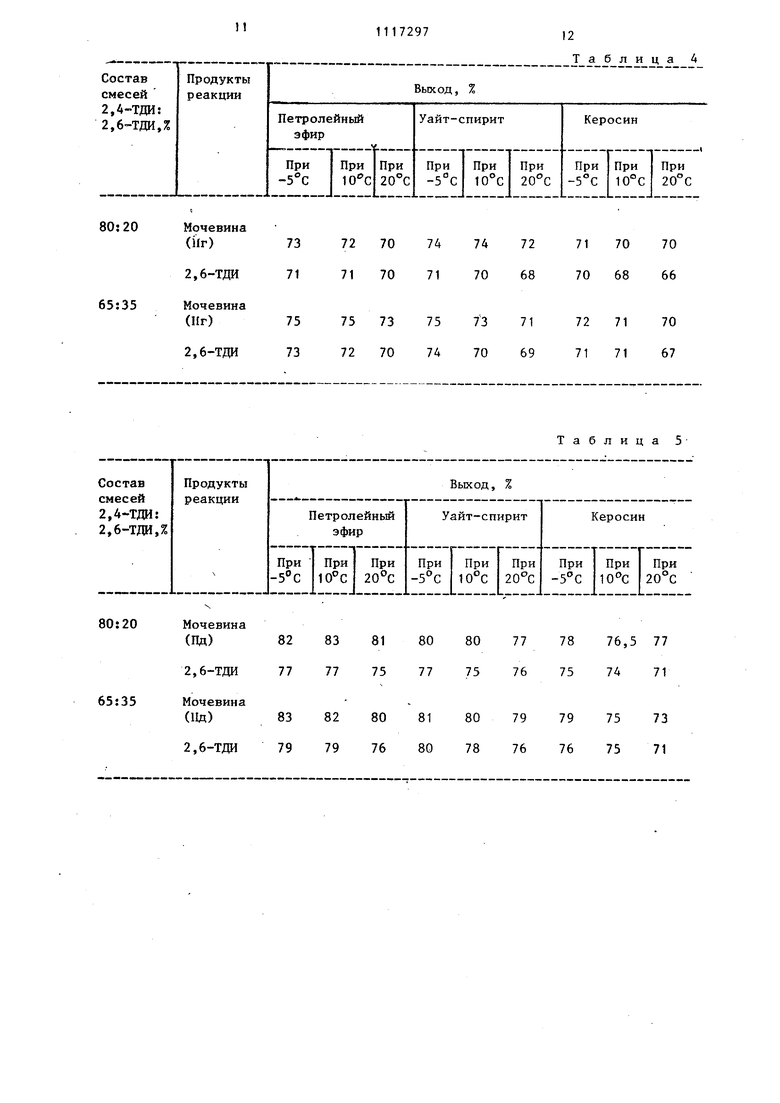
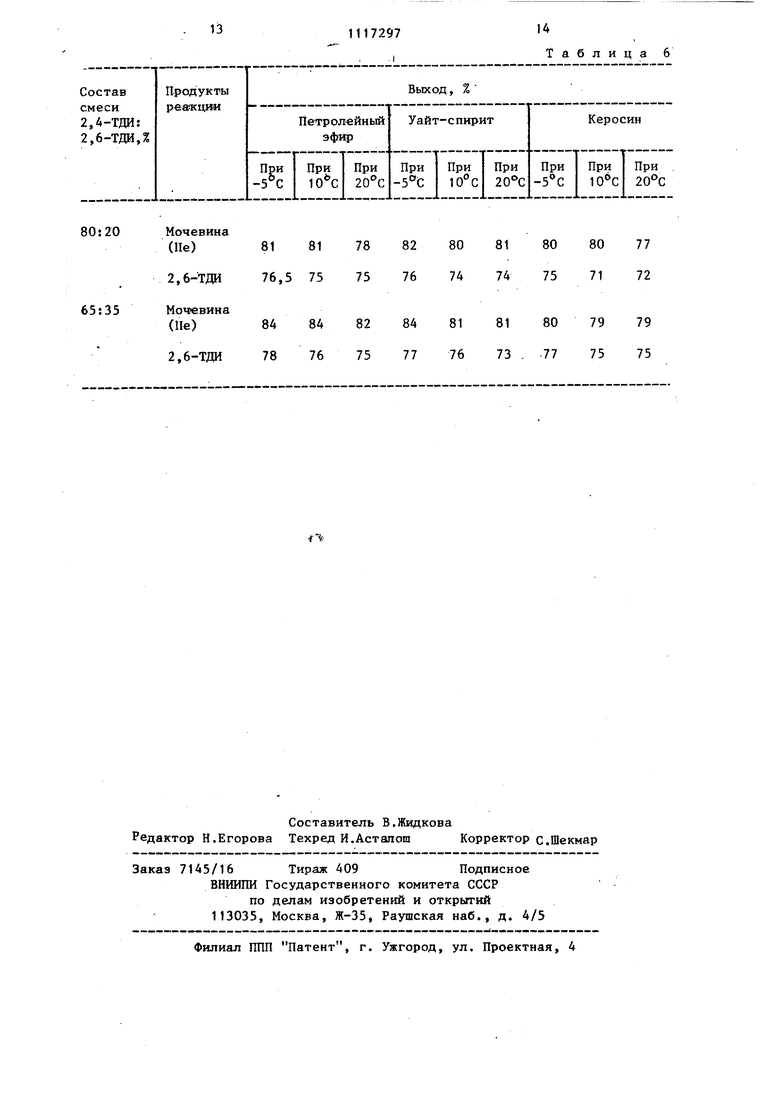
Трихлорацетамидины реагируют только с 2.,4-ТДИ и дают кристаллические мочевины общей формулы И, которые легко отделяются фильтрованием. Непрореагировавший 2,6-ТДИ выделяется из фильтрата перегонкой в вакууме с выходом 60-91%. 2,6-ТДИ не вступает в реакцию с амидинамн . формулы 1 ни при повышенных температурах, ни при использовании избытка амидинов. Мочевины формулы И после отделения 2,6-ТДИ растворяют в органическом растворителе (толуол, ксилол, хлорбензол) и обрабатывают хлористы водородом. При этом количественно выпадает осадок хлоргидрата диалкил(циклоапкил)трихлорацетамидина, который отделяют фильтрованием, а из фильтрата перегонкой в вакууме с выходом 68-90% вьщеляют 2,4-ТДИ. Из хлористоводородных солей .N,N-Диалкил(циклоалкил)трихлораце тамидинов обычным способом при обработке водными растворами соды или поташа можно легко получить их свободные основания. Выход регенерированных таким образом амидинов формулы 1 достигает 80%. Чистота полученных 2,6- и 2,4-ТД подтверждается данными ИК- и ПМР-сп ктроскопии. Пример 1. Обработка смесей 2,4- и 2,6-ТДИ Н,М-диметилтрихлорацетамидином, вьщеление 2,6-ТДИ и М -(4-метил-3-изоцианатофенил)-М-(1-диметиламино-2,2,2-трихлорэ тилййей)мочевины (Иа). Раствор 34,8 г (0,2 моль) смеси 2,4- и 2,6-ТДИ состава 80:20 или 65:35 в 250 мл органического растворителя, (петролейного эфира, уайт спирита, керосина), помещают в реак тор, снабженный механической мешалкой, капельной воронкой, и в течение 2,5 ч при перемешивании и охлаж дении ледяной водой прибавляют к нему раствор соответственно 30,3 г (0,16 моль) или 24,6 г (0,13 моль) Н,М-диметилтрихлорацетамидина в 70 того же растворителя, после чего ох лаждение снимают. Реакционную смесь оставляют при 20-25 0 на 12 ч. Выпавший осадок отфильтровывают, промьшают петролейным эфиром и сушат. Получают соответственно 47,1 г (81% или 39,23 (83%)N -(4-метил-З-изо цианатофенил)-Н-(1-диметиламино-2,2 2-трихлорэтилиден) мочевины (Под с т. пл. 93-95°С. Найдено, %: С 42,90; Н 3,99; N 14,97. С1ДО.,. Вычислено, %: С 42,93; Н 3,61, N 15,40. Фильтрат упаривают в вакууме водоструйного насоса, остаток перего74няют, выделяя соответственно 26,3 г (74%) или 46,0 г (75,5%) 2,6-ТДИ. Т. кип. 124-126 С (12 мм рт.ст.) 1° 1,5709. Выходы мочевины (На) и 2,6-ТДИ приведены в табл. 1. Пример 2. Обработка смесей 2,4- и 2,6-ТДИ К, N-диэтшттрихлорацетамидином (1 б), вьщеление 2,6-ТДИ и N -(4-метил-З-изоцианатофенил)-N-(1-диэтиламино-2,2,2-трихлорэтилиден)-мочевины (П). По методике, приведенной в примере 1, раствор 34,8 г (0,2 моль) смеси 2,4- и 2,6-ТДИ состава 80:20 или 65:35 обрабатывают Н,М-дизт11птрихлорацетамидином соответственно 35,7 г (0,16 моль) или 28,3 г (0,13 моль)„ Получают соответственно 28,6 г (80,5%) или 55,5 г (91%) 2,6-ТДИ с Т..КИП. П9-121°С (10 мм рт.ст.), Hjj 1,5711, а также 61,4 г (98%) или 46,8 г (92%) N -(-метил-3-изоцианатофенил)-М-(1-диэтиламино-2,2,2-трихлорэтилидей)мочевины с т.пл. 114-118°С (см. табл. 2). Найдено, %: С 45,50; Н 4,41, N 14,47 C. Вычислено,%: С 46,00; Н 4,37; 14,30. Пример 3. Обработка смесей 2,4- и 2,6-ТДИ М,Ы-дипроп1штрихлорацетамидином (1 в), вьщеление 2,6-ТДИ и N-(4-метил-3-изоцианатофенил)НЧ-(1-дипропиламино-2,2,2-трихлорэтиЛ1щен)мочевины (Ив) . По методике, приведенной в примере 1, раствор 34,8 г (0,2 моль) смеси 2,4- и 2,6-ТДИ состава 80:20 или 65:35 обрабатывают N ,N-дипpoпIlлтрихлорацетамидином соответственно 39,3 г (0,16 моль) или 31,9 г (0,13 моль). Получают соответственно 21,3 г (60%) или 39,0 г (64%) 2,6-ТДИ с т.кип. 122-123°С (11 мм рт.ст.). 1, 5707, а также 43,65 г (65%) или 36,6 г (67%)N-(4-метил-З-изоцианатофенил)- N-(1-дипропиламино 2,2,2-трихлорэтилиден)мочевины с т.пл. 92-94°С (см. табл. 3). . Найдено, %: С 48,52, Н 5,39, N 13,61 С„Н,С1 V,. Вычислено, %: С 48,65; Н 5,04; N 13,35. Пример 4. Обработка смесей 2,4- и 2,6-ТДИ N ,(Я-дибутилтрихлорацетамидином (1 ), вьщеление 2, и Н-(4-метил-3-иэоцианатофенил)N -(1-дибутиламино-2,2,2-трихлорэтилиден)мочевины (lit) . По методике, приведенной в примере 1, раствор 34,8 г (0,2 моль) смеси 2,4- и 2,6-ТДИ состава 80:20 или 65:35 обрабатьюают N,Н-дибутилтрихлорацетамидином соответственно 43,8 г (0,16моль) или 35,6 г (0,13 моль). Получают соответственно 25,23 г (71%) или 45,1 г (73%) 2,6-ТДИ с т.кип. 119-121°С (10 мм рт.ст), h|f 1,5708,а также 52.3 г (73Г%) или 43,7 г (75%). М-(4-метил3-изоцианатофенил)- N -(1-дибутиламино-2,2,2-трихлорэтилиден) мочевины с т.пл. 78-80°С (см. табл. 4), Найдено, %: С 51,27; Н 5,83; N 12,65. С . Вычислено, %: С 50,97; Н 5,63; N.12,51. Пример 5. Обработка смесей 2,4- и 2,6-ТДИ морфолинотрихлорацетамидином (13) выделение 2,6-ТДИ и М-(метил-3-изоцианатофенил)-Ы-(1-морфолино-2,2,2 трихлорэтилиден) мочевины (ИЭ). По методике, приведенной в примере 1, раствор 34,8 г (0,2 моль) смеси 2,4- и 2,6-ТДИ состава 80:20 или 65:35 обрабатьшают морфолинотрихлорацетамидином соответственно 37,0 г (0,16 моль) или 30,1 г (0,13 моль). Получают соответственно 27,4 г (77%) или 48,16 г (79%) 2,6-ТДИ.с т.кип. 120-124с (11 мм pT.CT.),n|f 1,5698, а также 53,2 г (82%) или 43,8 г (83% N-(4-метил-З-изоцианатофенил)-N-(1-морфолино-2,2,2-трихлорэтилиден) мо чевины с т.пл. 100-102 С (см. табл.5 Найдено, %: С 44,77; Н 4,21; N 13,66. C,j.H,5C ,. Вычислено, %: С 44,41; Н 3,73| N 13,8t. Пример 6. Обработка смесей 2,4- и 2,6-ТДИ пиперидинотрихлорацетамидином (1е), выделение 2,6-ТДИ и N-(метил-3-изоцианатофенил)-N(1пиперидино-2,2, 2-трихлорэтили,цен) мо чевины (Пе). По методике, приведенной в при11ере 1, раствор 34,8 г (0,2 моль) смеси 2,4- и 2,6-ТДИ состава 80:20 или 65:35 обрабатывают пиперидинотрихлорацетамидином соответственно 36,72 г (0,16 моль) или 29,8 г (0,13 моль). Получают соответственно 27,19 г (76,5%) или 47,55 г (7&%) 2,6-ТДИ с т.кип. 121-124°С. 11 мм pT.cT.),n2j1,5704,а также52,3г (81%) или 44,1 г (84%) Ы-(4 метил-3-изоцианатофенил) М -(1-пиперидино-2,2,2-трихлорэтилиден) мочевины с т.пл. 112-П4 С (см. табл. 6). Найдено, %: С 47,61; Н 4,32; N 13,84. CieH-nCbN Вычислено, %: С 47,60; Н 4,25; N 13,88. Пример 7. Выделение 2,4-ТДИ из N - ( 4-метил-З-изоцианатофенил) - |V-(1-диметиламино-2,2,2 -трихлорэтилиден) мочевины (lid) . В реактор, снабженный обратным холодильником механической мешалкой и барботером, помещают 54,5 г (О,15 моль)N-(4-метил-З-изоцианатофенил)- N-(1-димeтшIaминo-2,2,2-трихлорэтилиден) мочевины в 400 мл безводного органического растворителя (толуола, хлорбензола, ксилола). При нагревании (80-110°С) и перемешивании становится гомогенной и через нее в течение 1 ч пропускают интенсивный ток сухого хлористого водорода. При этом в осадок количественно вьшадает солянокисльй Н,М-диметилтрихлорацетамидин. Суспензию охлаждают до 20-25 0 и фильтруют на пористом фильтре. Фильтрат упаривают, остаток перегоняют в вакууме, получая 20,2 г (77%) 2,4-ТДИ с т.кип. 133-135 0 (18 мм рт.ст), 1,5666. Пример 8. Вьщеление 2,4-ТДИ из J(4-мeтшI-3-изoциaнaтoфeнил)-N-(1-диэтиламино 2,2,2 -трихлорэтютиден) мочевины (П ). По методике, приведенной в примере 7, обрабатывают хлористым водородом 58,8 г (0,15 моль) N -(4-метил-Зизоцианатофенил) -N-(1-диэтил-2,252-трихлорэтш:иден) мочевины. Получают 23,5 г (90%) 2,4-ТДИ с т.кип. 122 124С (12 мм рт.ст), n|f 1,5661. Пример 9. Вьщеление 2,4-ТДИ из N -(4-метил-3-изоцианатофенил) - N-(1 ДИпропиламино-2,2,2 -трихлорзтилиден) мочевины (Пе). По методике, приведенной в примее 7, обрабатывают хлористьм водороом 63,0 г (0,15 моль)N -(4-метш1-3-изоцианатофенил)-N -(1-дипропиламино-2,2,2-трихлорэтилиден) мочевины. Получают 18,8 г (72%) 2,4-ТДИ с т.кип: 123-125°С (12 мм рт.ст), 1,5663. Пример 10. Вьщеление 2,4-ТД из Н-(4-метил-3-изоцианатофенил-(Ч Н(1-дибутиламико-2,2,2-трихлорэтилиден) мочевины (П ). По методике, приведенной в примере 7, обрабатывают хлористым водородом 67,2 г (0,15 моль)N-(4-мeтил-3-изoциaнaтoфeншl) -N-( 1-дибутилам но-2,2,2-трихлорэтилиден) мочевины. Получают 19,9 г (76%) 2,4-ТДИ с т.кип. 130-132°С (17 мм рт.ст), п 1,5663. Пример 11. Выделение 2,4-ТД из N -(4-мeтил-3-изoциaнaтoфeнил)-N-( 1 -морфолино- 2,2,2-трихлорэтйлидеи) мочевины (НЭ). По методике, приведенной в примере 7, обрабатывают хлористым водородом 60,9 г (0,15 моль)N -(4-мeтил-3-изoциaнaтoфeнил)- М-(1-морфолино-2,2,2-трихлорэтш11Вден) мочевины. Получают 19,8 г (76%) 2,4-ТДИ с т.кип. (17 мм рт.ст), г 1,5662. Пример 12. Вьщеление 2,4-ТД из N -(4-метил-3-изоцианатофенил)-Н - (1 -пиперидино-2,2,2-тршшорэ тилиде)мочевины (Не). По методике, приведенной в примере 7, обрабатывают хлористым водо7родом 60,6 г (0,15 моль)N -(4-метил-3-изоцианатофенил)-М-(1-пиперидино-2,2,2-трихлорэтилиден) мочевины. Получают 17,8 г (68%) 2,4-ТДИ -с т.кип. 121-122°С (11 мм рт.ст), t.j, 1,5661. В примерах 7-12 в качестве растэорителей брались толуол, хлорбензол, ксилол. Данная реакция представляет собой диссоциацию мочевин (1«на 2,4-ТДИ и соответствующий амидин, которьм связьшается хлористым водородом в соль. Диссоциация начинается при , но по мере уменьшения концентрации исходной мочевины значительно замедляется Полнота реакции достигается при 110°С. Используемые растворители: толуол, хлорбензол, ксилол очень близки по природе, поэтому замена одного на другой в данной реакции не оказывает влияния на выходы продуктов. Таким образом, предлагаемьм способ впервые позволил разделить на чистые изомеры смеси 2,4- и 2,6-ТДИ состава 80:20 и 65:35, которые являются продуктами многотоннажного производства. Способ характеризуется простотой, высокой селективностью, доступностью реагентов и применяемых растворителей, высоким выходом целевых продуктов, а также возможностью регенерации применяемых реагентов.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения диалкиловых эфиров 2-(2,2-дихлорвинил)малоновой кислоты | 1987 |
|
SU1549946A1 |
| Способ получения N-[2-(4-фторфенил)-1-метил]-этил-N-метил-N-пропиниламина в виде рецемата или L-изомера, или их солей | 1986 |
|
SU1609443A3 |
| АЛКИЛЗАМЕЩЕННЫЕ ЦИКЛИЧЕСКИЕ АМИНЫ В КАЧЕСТВЕ СЕЛЕКТИВНЫХ ЛИГАНДОВ D3-ДОПАМИНА | 1997 |
|
RU2185372C2 |
| Способ получения триацетонамина | 1974 |
|
SU692557A3 |
| Гербицидно-антидотная композиция | 1981 |
|
SU1478990A3 |
| Способ получения моно- и/илидиАМиНОАлКЕНОВ | 1976 |
|
SU802263A1 |
| Способ получения 1,3-дикетооктагидроизохинолинов | 1975 |
|
SU574153A3 |
| Способ получения @ -алкоксиметил- @ -( @ , @ -дихлорвинил)-ацетоуксусного эфира или @ -алкоксиметил- @ -( @ , @ -дихлорвинил)-ацетилацетона | 1984 |
|
SU1198055A1 |
| Способ получения N-/2,2,2-трихлорэтилиден/арилсульфамидов | 1979 |
|
SU899543A1 |
| ТРИЦИКЛИЧЕСКИЕ АЗОТСОДЕРЖАЩИЕ СОЕДИНЕНИЯ И ПРОИЗВОДНЫЕ ТЕТРАГИДРОХИНОЛИНА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1991 |
|
RU2023712C1 |

Мочевина (На)
81 74
8079
2,6-ТДИ
7371
Мочевина (Па)
83 75,5
8081
2,6-тда
7371
Таблица 1
80 74
79 70
78 77
80 74 73,5 71
80 71
80 72
80 71
78 72
80 74
61 60 61,5 60
64
2,6-ТДИ
Таблица 2
61
61 61
60 Мочевина (Пд) 8283818080 2,6-ТДИ 7777757715 Мочевина (11д) 8382808180 2,6-ТДИ 7979768078
Таблица А
Таблица 5 777876,577 76757471 79797573 76767571
Таблица 6
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ коррекции подкожных мягких тканей человека | 2024 |
|
RU2831012C1 |
| Прибор для периодического прерывания электрической цепи в случае ее перегрузки | 1921 |
|
SU260A1 |
| Реактивная дисковая турбина | 1925 |
|
SU1958A1 |
| Прибор для периодического прерывания электрической цепи в случае ее перегрузки | 1921 |
|
SU260A1 |
| Приспособление для изготовления в грунте бетонных свай с употреблением обсадных труб | 1915 |
|
SU1981A1 |
| Прибор для периодического прерывания электрической цепи в случае ее перегрузки | 1921 |
|
SU260A1 |
| Водоотводчик | 1925 |
|
SU1962A1 |
Авторы
Даты
1984-10-07—Публикация
1982-08-06—Подача