Изобретение относится к усовершенствованному способу получения 3™ -хлорпиридииа, который используют в качестве полупродукта в органическом синтезе, в сельском хозяйстве з качестна и п ибитора нитрификации азотных удобрений. Наиболее близким к изобретению по технической сущности и достигаемому результату является способ получения 3-хлорпиридина хлорированием газообразнымхлором в присутствии катализатора А1С1., при нагревании до SO-ISO C в течение 13 ч. С повышением температуры хлорированйя до 130С вых.од 3-хлорпиридина составляет 35% С J Однако выход 3-хлорпиридина. невысок (30-35%), требуется использование газообразного хлора и используется 2,5-кратный избыток безводного хлористого алюминия. Целью изобретения является повышение выхода целевого продукта и упрощение процесса. Поставленная цель достигается тем что согласно способу получения 3 -хлорпиридина, заключающемуся в том что пиридин хлорируют эквимолярным количеством хлористого сульфуриЛа в присутствии катализатора, представляющего собой хлорид Fe. In, Sn, Sb, Zn или Hg при 50-55 0 в течение 10-15 ч. Предпочтительно, количество катализатора составляет 5-10% от исходно го пиридина. Хлорирование пиридина в течение времени большего или. меньшего, чем оптимальном интервале приводит .к сн жению выхода, к такому же результату приводит-понижение температуры процесса, а при температуре выше происходит разложение хлористого сульфурила. Увеличение количества катализато ра не приводит к изменению выхода. Пример 1. Хлорирование пири дина хлористьгм сульфурилом в отсутс вии катализатора. К раствору г (0,16 моль),пиридина в 50 мл четыреххлористого уг лерода при охлаждении добавляют 10 мл или 1б,7г (0,12 .моль) сульфурилхлорида. Смесь нагревают до 50- 55С и выдерживают при этой темпера туре 7-15 ч, охлаящают, нейтрализую водной щелочью до рН 10 и экстраги532руют четыреххлористым углеродом и эфиром 320 мл а- Объединенные выТЯЖК.И сушат над , отфильтровывают от твердого сушителя и перегоняют через ректификационную колонну (16 т:,т.) .Получают 7,0т непрореагировавшего пиридина с интервал-ом температур -112-120 0, п , 1 ,.510, . Фракция с интервалом температуры кипения 140-150 С состоит из 3 хлорпи ридина 0,5 г (3%) п 1,531. и.0,10 г (0,4%) 355-дихлорпиридина п 1,5540, т.пл., 63°С. Строение 3-хлор и 3,5-дихлорпиридина доказано по идентичности lio тех и ИК-спектру с образцами известного строения. Совпадение времени вькода в газожидкостной хроматографии свидетелей пиридина 3-хлор- и 3,5-дихлорпиридинов с продуктами реакции также подтверждает идентичность анализируемых соединений . Пример 2. Хлорирование пиридина .хлористым сульфурилом в-присутствии катализаторов - солей р- и d-элементов периодической системы. Менделеева. 2.1.Хлорирование пиридина в когшлексе-с хлористым индием. Смесь 17 г комплекса состава и 20 мл хлористого сульфурила в 50 мл четыреххлористого углерода при перемешивании нагревают в течение 24 ч при 50-55 С, После охлаждения до комнатной температуры реакционную смесь нейтрализуют водной щелочью до рН 10 и далее экстрагируют СС 3-20 и эфи-. ром , Обьединенные экстракты сушат над твердым Na2SO и .подвергаЮт фракционной перегонке. Основная фракция перегналась при 100-110°, п|5 1,5061. Идентичность по ТСХ- и ИК-спектру с пиридином свир;етельствует, что в указанных условиях.пиридин в комплексе не хлорируется. В аналогичных условиях хлорирование пиридина в комплексе в течение 15 и 7 ч также не приводит к успеху. 2.2.Хпорирование пиридина в прис.утствии каталитических количеств треххлористого индия. К 12,5 г (0,516 моль) пирилина и Зг (5% от общего веса) безводной соли .в 50 .мл четыреххлористого углерода при охлаждении добавляют 10 мл или 16,7 г (О,, 12 моль) сульфурилхлорида Смесь нагревают до 503 . 55С и выдерживают при йтой темпера туре в течение 15 ч -и далее выделение и характеристика продуктов реакции как в примерах 1, 2,1. Выход 3-хлорпиридина 9,9 г 55%) .п 1.5309 т.кип. . 2.2.1.Хлорирование пиридина в аВалогичной, что и в примере 2.2. ме тодике, но ,прй нагревании реакционной смеси в течение 24 ч выход 3хлорпиридина понижается и составляет 23%. 2.2.2.Хлорирование пиридина в аналогичной примеру 2;2. методике, но при нагревании реакционной смеси в течение 7 ч выход 3-хлорпиридина достигает2,7 г (15%). 2.2.3.Хлорирование пиридина в аналогичных примеру 2.2. условиях, но при нагревании реакционной смеси в течение 10 ч выход целевого продук та 6,7 г (37,2%). . .4. Хлорирование пиридина в условиях примера 2.2., но с увеличением количества применяемого катализатора до 10% и 20% от рбщего веса реакционной среды не влияет на выход целевого продукта. ; 2.2.5. Хлорирование пиридина в ус ловиях примера 2.2., но при 0-35С выход 3-хлорпиридина достигает 5%. С повьшением температуры процесса выше 55 С происходит разложение хлористого сульфурила на Cf и S02 . . 2.2.6. Хлорирование пиридина .хлористым сульфурилом в условиях примера 2.2., но при молярном их соотноше 534 , НИИ 0,16: 0,20, соответственно выход 3-хлорпиридина 3,1 г (17%). Пример 3. Хлорирование пиридина хлористым сульфурилом в присутстВИИ каталитических количеств солей ри d-элементов периодической системы Менделеева. К раствору 12,5 г (0,16 моль) пиридина и 3 г (5%) соли р- и d-элементов (таблица) в 50 мл четыреххлористого углерода при охлаждении добавляют 10 мл или г (0,12 моль) суль1фурилхлорида и далее проводят процесс аналогично примеру 2.2. Для газожидкостной хроматографии проводят отгонку растворителя и остаток подвергают количественному анализу на содержание пиридина, 3-хлор- и полихлорпиридинов с целью более корректорного анализа продуктов реакции и, следовательно, достоверного определения каталитического эффекта солей d- и р-элементов. Экспериментальные данные по хлорированию пиридина суммированы в таблице. Таким образом, из данных таблицы следует, что пиридин гладко гапогенируется в присутствии 5-10% каталитических количествхлоридов Af, Fe, In, Sn, Zn, Hg. По сравнению с известным способом предлагаемьй способ обладает следующими преимуществами: повьппение выхода 3-хлорпйридина до 63%; замена газообразного хлора на хлористый судьфурил.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения хлорпиридинов | 1977 |
|
SU652177A1 |
| СПОСОБ ПОЛУЧЕНИЯ о^-ХЛОРПРОШОНОВОЙ. кислоты | 1979 |
|
SU825495A1 |
| Способ получения однохлористой серы | 1980 |
|
SU874606A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТИЛ-4-ГАЛОГЕН-ФЕНОКСИАЦЕТАТОВ ТРИС-(2-ГИДРОКСИЭТИЛ)АММОНИЯ (2-МЕТИЛ-4-ГАЛОГЕН-ФЕНОКСИАЦЕТОКСИПРОТАТРАНОВ) | 2009 |
|
RU2427568C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТА-ХЛОРБЕНЗОИЛХЛОРИДА | 1992 |
|
RU2041199C1 |
| Способ получения 2-хлор-5-[ @ -(2 @ ,4 @ -ди-трет-амилфенокси)-бутироиламино]-анилида @ -хлорпивалоилуксусной кислоты | 1988 |
|
SU1574591A1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕНЗИЛХЛОРИДА | 2005 |
|
RU2291144C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-ДИФЕНИЛФОСФОРИЛ-N′-АЛКИЛ (C-C) МОЧЕВИН | 2006 |
|
RU2296768C1 |
| Способ получения м-феноксибензальдегида | 1977 |
|
SU816397A3 |
| Способ получения 2,6-дихлор-4-нитроанилина | 1982 |
|
SU1033494A1 |
1. СПОСОБ ПОЛУЧЕНИЯ 3-ХЛОРПИРИДИНА жидкофазным хлорированием пиридина в присутствии катализатора при нагревании, отличающийс я тем, что, с целью повышения выхода целевого продукта и упрощения процесса, хлорирование пиридина проводят эквимолярным количеством хлористого сульфурила, в качестве катализатора используют хлориды А{, Fe, In, Sn, Zn или Hg и процесс ведут в течение 10-15 ч при 30-55 с. 2. Способ ПОП.1, отличающийся тем, что количество катализатора составляет 5-10% от исходного пиридина.
4,7 1,8 2,9
Ь5 6,1
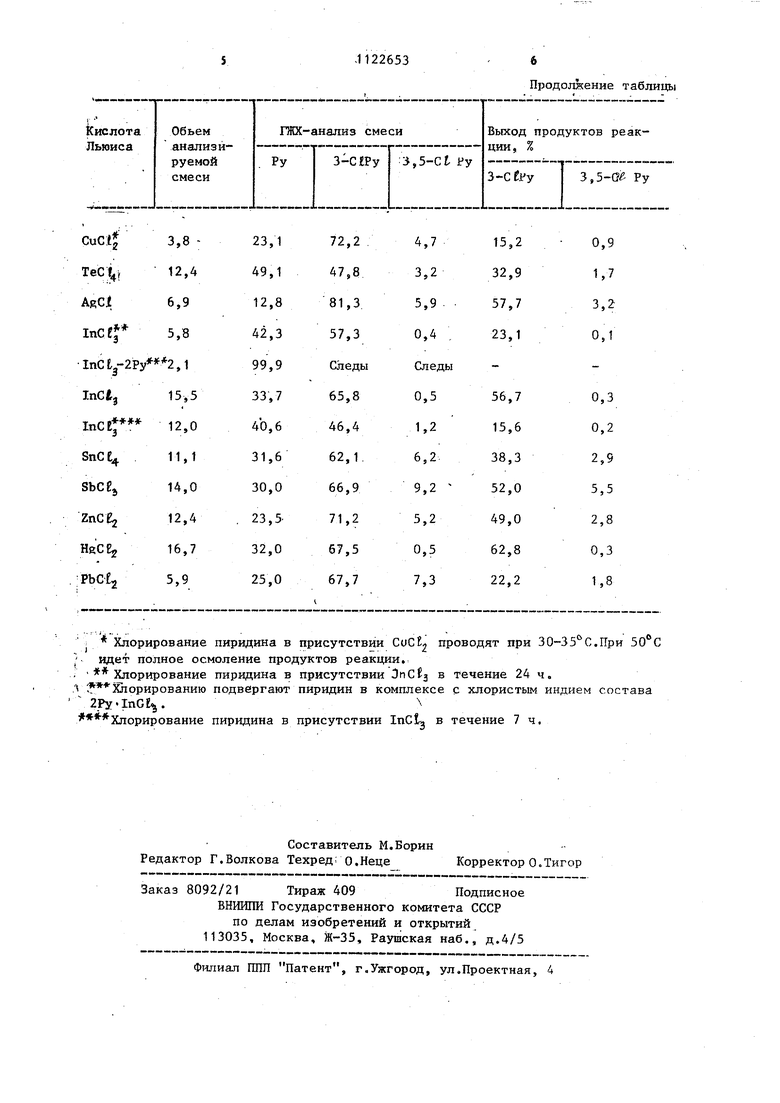
Хлорирование пиридина в присутствии СоСВ проводят при ЗО-ЗЗ С.При
/ идет полное осмоление продуктов реакции.
- Хлорирование пиридина в присутствии OnCfj в течение 24 ч. Л 51орированию подвергают пиридин в комплексе с хлористым индием состава .1пСЦ.
Хлорирование пиридина в присутствии InCt в течение 7 ч.
6
Продолжение таблицы
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Pearson D.E., Hargrove W.W., Chow J.K.T | |||
| The Swamping Effect | |||
| The halogenation оБ Pyridines.- Journal ob organic Chemistry, 1961, v.26, p.789-792 (прототип) | |||
Авторы
Даты
1984-11-07—Публикация
1983-06-16—Подача