3 .. перемешивании при комнатной .температуре прибавляют 20%-ный водный раствор трихлорида железа. Перемешивание реакционной смеси продолжают в течение 2 ч, затем отделяют осадок, промывают водой и высушивают. Получают синие кристаллы,- выход 0,7 г (46%), т.пл. 250°С (разложение) .
Найденоi%: С34,56; Н 1,16, С1 34,91; N 8,81{ S 10,42.
Вычислено,%: С 34,92; Н 0,98; С1 34,36; N 9,05; S 10,36.
ИК-спектр в нуйоле, т) , см : 1633 ( хинона), 1631 (тиазольное кольцо), 1534().
УФ-спектр в этаноле, я , нм (): 318 (13800), 597 (4700).
Пример 2. 2-(2-Мет1шамино-5-тиазолил)-3,5,6-трихлор-1,4-бензохинон.
Смесь 0,9 г (0,003 моль) ,Nг(диэтилaминoвинип) -3,5,6-трихлор-1,4-бензохинона, 0,27 г (0,003 моль)N -метилтиомочевины и 1 мл конц.соляной кислоты в 30 мл диоксана. кипятят 2 ч. Охлаждают, осадок отделяют, растворяют в 2 мл ДМФА и к раствору прибавляют 10 мл 20%-ного водного раствора трихлорид железа. Перемешивают 2 ч, затем отделяют осадок, щ омывают водой и высушивают. Получают темно-синие кристаллы, выход 0,75 г (41%), т.пл. 250 С (разложение),
Найдено,%: С1 32,31; N 8,85; S 10,47.
.
Вычислено,%: Cl 32,87-, N 8,66; S 9,91.
ИК-спектр в нуйоле, , см : 1662, 1645 ( хинона), 1604 (тиазольное кольцо), 1512 ().
УФ-спектр в эталоне,Jrnax (): 324 (12800), 620 (5400).
Пример 3. 2-(2-Фениламино-5-тиазолил)-3,5,6-трихлор-1,4-бензохинон.
а). Смесь 0,9 г (0,003 моль) 2- 2-N, N- (диэтиламиновинил) -, 5,6-трихлор-1,4-бензохинона, 0,6 г (0,003 моль) N-фенилтиомочевины и .1 мл конд.соляной кислоты в 30 мл диоксана кипятят 2 ч. После охлаждения осадок отделяют, растворяют в 8 МП ДМФА и к раствору приливают 20 мл 20%-ного водного раствора -трихлорида железа. Реакционнзто смесь
31874А
перемешивают при комнатной температуре 2 ч, затем отделяют осадок, промывают водой и высушивают. Получают темно-синие кристаллы. Выход 0,7 г (63%), т.пл. 25.0°С (раЬложе ние).
Найдено,%: С1 27,48; N S 8,39.
C,5H C1 N202S
Вычислено,%: Cl 27,60; N 7,27; S 8,30.
ИК-спектр в нуйоле, - , 1682 ( хинона), 1630 (тиазольное кольцо), 1538 ().
б). Смесь 0,56 г (0,002 моль) ,Ы-(диметиламиновинил)3 -3,5,6-трихлор-1,4-бензохинона, 0,30 г (0,002 моль) N-фенилтиомочевнны и 1 мл конд.соляной кислоты в 20 МП диоксана кипятят около 2 ч. Охлаждают, .осадок отделяют, затем растворяют в 5 мл ДМФА и к раствору при перемешивании прибавляют 10 мп 20%ного водного раствора трихлорида железа. Продолжают перемешивание реакционной смеси в течение 2 ч, затем отделяют осадок, промывают водой и высушивают. Выход 0,2 т (26%), т.пл. 250 С (разложение).
Данные ЛК-спектра и элементного анализа соответствуют образцу, полученному по методу а).
Пример 4. 2-(2-Ацетилами но-5-тиазолш1)-2,5,6-трихлор-1,4-бензохинон..
35Смесь 0,9 г (0,003 моль) ,N-(диэтилaминoвинил)J -3,5 6-трихлор-1,4-бензохинона, 0,36 г (0,003 моль) N-ацетилтиомочевины и 1 мл конц.соляной кислоты в 30 мл 0 диоксана кипятят 2 ч. Реакционную смесь охлаждают, затем прибавляют 50-60 МП гексана. Выпавший осадок отфильтровьгоают, растворяют в В мл ДМФА и к р.аствору при перемешива45 нрш прибавляют 20 мп 20%-ного водного раствора трихлорида железа. Реакщюннзто смесь перемешивают при комнатной температуре 2 ч, затем отделяют осадок, промывают водой 50 и высутпивают. Получают темно-т})иолетовые кристаллы, вьпсод 0,4 г.(40%), т.пл. (разложение).
Найдено,%:с 36,76, Н 1,63; С1 30,15; N 8,54,- S 9,77. . 55 . C,,HjCl,
Вычислено,%: С 37,16; Н 1,42; С1 29,92j N 7,88; S 9,00, S ИК-спектр в нуйоле, , 1677 (), 1637 (тиазольное кольцо 1548 (). УФ-спектр в этаноле, .та нм {): 392 (17000), 513 (3400). Пример 5. 2-(2-Аллиламино-5-тиазсшип)-3,5 6-трихлор-1,4-бензохинон. Смесь 0,9 г (0,003 м№ь) ,Nr(диэтипaминoвинил)J -3,5,6-трихлор-1,4-бензохинона, О,35 г (0,003 моль) N-аллилтиомочевины и 1 МП конц. НС1 в 30 мл диоксана кипятят 2 ч, затем растворитель упари вагот в вакууме до объема около 10 м и прибавляют в реакционную смесь 20 мл гексана. Выпавший осадок отде ляют, растворяют в 5-6 мл ДМФА и йри перемешивании прибавляет 20 мл 20%-ного водного раствора трихлорид железа. Реакционную смесь перемешивают 2 ч, затем отделяют осадок. По лучают синие кристаллы, выход О,5 г (50%), т.пл. (разложение) . 4 Найдено,%: G 41,10, Н 2,14, С1 30,24,- N 8,10,- S 9,50. Cj2HjCl N202S Вычислено,%-: С 41,19, Н 2,02, С1 30,43, N 8,02, S 9,16. ИК-спектр в нуйоле, - , см : 1683 ( хинона), 1618 (тиазольное кольцо), 1532 () . При проведении способа при температуре ниже температуры кипения смеси скорость реакции замедляется, что ведет к уменьшению выхода промежуточного гидрохинона, а следовательно, и целевого продукта. Таким образом, предлагаемьй способ позволяет получить новые производные 2-аминотиазола, содержащие в 5-ом положении остаток трихлор-1,4-бензохинона, которые могут найти применение в качестве промеж5точных соединений для создания веществ, обладающих повышенной электропроводностью или фоточувствительностью, из доступных исходных соединений с хорошими выходами.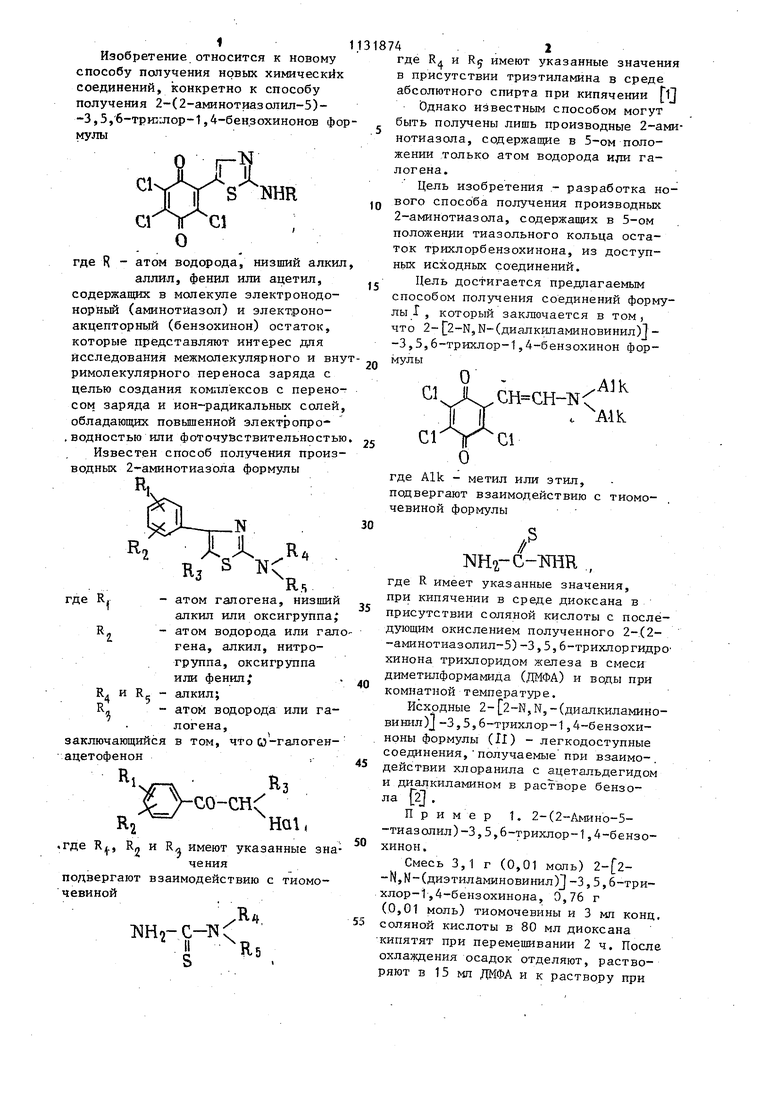


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2-(2-аминотиазолил-5)-3,5,6-трихлор-1,4-бензохинонов | 1984 |
|
SU1188169A1 |
| АЙ БИБЛИОТЕКА1*"? Гм | 1970 |
|
SU262893A1 |
| ХИНОНОВЫЕ ПРОИЗВОДНЫЕ | 1992 |
|
RU2054412C1 |
| Способ получения амидов цианкарбоновых кислот (способ Станкявичюса) | 1989 |
|
SU1625872A1 |
| НОВЫЕ ОПТИЧЕСКИ АКТИВНЫЕ 4-ГИДРОКСИ-2-АЗА-9,10-АНТРАХИНОНЫ, ОБЛАДАЮЩИЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2436775C1 |
| Способ получения хиноновых производных | 1985 |
|
SU1807985A3 |
| Производные пиримидо-[4,5- @ ] [1,4]-бензоксазепина и способ их получения | 1977 |
|
SU671271A1 |
| Способ получения 6-аминометилпиримидо /4,5-в/ /1,4/ тиазинов | 1972 |
|
SU445283A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,7-БИС[2-(ДИЭТИЛАМИНО)ЭТОКСИ]ФЛОУРЕНОНА ДИГИДРОХЛОРИДА | 1994 |
|
RU2076097C1 |
| 1-Ацетил-2-(2 @ ,4 @ -диметоксифенил)-3-(4 @ -R-фенил)-1,2,3,4-тетрагидрохиназолиноны-4, проявляющие противовоспалительную активность | 1982 |
|
SU1063049A1 |
СПОСОБ ПОЛУЧЕНИЯ 2- 2-АМИНЬТИАЗОЛИЛ-5)-3,5,6-ТРИКЛОР-1,4-БЕНЗОХИНОНОВ формулы О где R - атом водорода, низший алкил, аллил, фенил или ацетил, отл и чающийся тем, что 2- N-(диалкиламиновинил )J -3,5,6-трихлор-1,4-бензохинон формулы ОЛ1К ClvJkxCH CH- c: ii V сг-лЛс о где Alk метил или этил, подвергают взаимодействию с тиомочевиной формулы § (Л , где R имеет указанные значения, при кипячении в среде диоксана в присутствии соляной кислоты с последующим окислением полученного 2-
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Патент CUIA № 3775423, KJi | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Приспособление для склейки фанер в стыках | 1924 |
|
SU1973A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| D.Buckley et al | |||
| Syntheses of Substituted Amino- and arainovinylquinones | |||
| - J | |||
| Chem | |||
| Soc, 1957, | |||
Авторы
Даты
1984-12-30—Публикация
1983-12-13—Подача