подвергают взаимодействию с производным пиперидина общей формулы R где R, R Ир имеют указанные значения, в инертном органическом растворителе и целевбй продукт вьщеляют в свободном виде или в виде соли с фармацевтически приемлемой кислотой, или. в виде цис- или транс-изомера . Приоритет по признакам:15.07.81 - R - низший алкил; Я - атом водовода, низший алкил; . R - атом водорода, Alk - низший алкандиил; А - - CHj - CHj-, - С С -, - С N -, присоединенный к атому S углеродным атомом, где R, R и R каждый независимо выбирают из группы, состоящей из водорода или низшего алкила, и где R и R могут также дополнять насьш1енное или несасыщенное 5- или 6-членное карбоциклическое кольцо. Q - Аг - С О, 138032 где или где рой С или чис или где Аг - фенил или фенил, замещенный атомом галогена, Q - радикал формулы R - атом водорода или низший алкил; 1.04.82 - R2 - арил; - низший алкил, - группа формулы Х-Аг, в котоX является членом, выбранным из - ОН, /С (О - низший алкил)2 С . (CH2)g, где R - целое 0 о, равное 2 или 3, или C N-OH5 г - фенил или фенил, замещенный а.томом галогена, Q - радикал формулы R3 R атом водорода или низший алкил; атом галогена.














Способ получения производных бициклического пиримидин-5-она общей формулы I N. Ri R3 R Q низший алкил; , атом водорода, низший алкил или арил; . R - атом водорода или низгаий алкил; Alk - низший алкандиил Л - двутсвалентный радикал формулы . С или - С N - С ; R присоединенный к атому S углеродным атомом, где R, R и R каждый независимо выбирают из группы, состоящей из водорода и низшего алкила, и где R и R могут также дополнять насыр;енное или ненасыщенное 5- или 6-членное карбоциклическое кольцо; Q - группа формулы X - Аг, в которой X является членом, выбранным из О, СН - ОН, С

Изобретение относится к способу получения новых производных бициклического пиримидин-5-онё общей формулы
/ Vn
( -VT 11
Л
А УТ - О
где R - низший алкил,
R - атом водорода, низйнй алкил или арил;
атом водорода или низший
алкил,. низший алкандиил;
двухвалентньш радикал формулыСН2 -,, -СН2 -, -С-С-
,4
или
10
присоединенный к атому S углеродным .атомом, где R и R и В каждый не ависимо выбирают из группы, состояная, пропанднкарбоновая кислота, этандикарбоновая (2)-2-этендикарбоновая, (R)-2-этандикарбоновая, 2-оксиэтандикарбоновая, 2,3-диокси-этандикарбоновая, 2-окси-1,2,3-пропантрикарбоновая, бензойная, З-фенил-2-акриловая, ос-фенолуксус}ная, метансульфо-, этансульфо-, бен золсульфо-, 4-метилбензолсульфо-, циклогексансульфо-, 2-океибензойная, 4-амино-2-оксибензойная кислоты и подобные им. И наоборот, полученные соли можно превратить путем обработки щелочью в свободные основания. Ряд промежуточных продуктов и исходных материалов, использованных в указанных способах, являются известными соединениями, другие могут быть получены по известным в Данной отрасли техники способам получения сходных, соединений, способы си теза некоторых из них приведены далее. Промежуточные продукты формулы II возможно получать посредством превращения гидроксильной группы со ответствующих спиртов, например, проводя реакцию спиртов с хлористым тионилом, сульфурилхлоридом, пентабромидом фосфора, хлорокисью фосфора, 4-метил-бензил-хлористым суль фонилом и подобными им. Получение промежуточных продукто Пример 1. Смесь 40 ч 4-метил-2-тиазоламина, 30 ч, З-ацетил-4,5-дигидро-2(ЗН)-фуранона и 225 ч метилбензола перемешивают и нагревают с обратным холодильником 2,5 ч совместно с 0,6 ч. хлористоводородной кислоты. После охлаждения до комнатной температуры добавляют 170 ч. фосфорил-хлорида, Массу постепенно нагревают приблизительно до 110 С и перемешивают дополнитель но 2 ч при этой температуре. Реакционную смесь выпаривают и остаток выпивают на измельченньй лед. Добавляют гидрат окиси аммония до достижения рН 8. Продукт экстрагиру ют трихлорметаном. Экстракт высушивают, фильтруют и выпаривают. Остаток очищают колоночной хроматографи ей над силикагелем с применением смеси трихлорметана с метанолом (95:5 по объему) в качестве средства для отмьтки из адсорбента. Чистые фракции собирают и растворитель выпаривают. Остаток кристаллизуют из смеси 2,2 -оксибиспропана и 2-прапанола, что дает 19,3 ч. 6-(2-хлорэтил)-3,7-диметил-5Н-тиазолоСЗ,2-а)пиримидин-5-она (промежуточный 1 продукт)„ Аналогичным образом получает также 6-(2-хлорэтил)-2,3-дигидро-7-метил-5Н-тиазоло(3,2-а)пиримидин-5-он (промежуточный 2 продукт) и 3-(2-хлорэтил)-758-дигидро-2-метил-4Н, 6Н-циклопента(4,5), тиазоло(3, ;2-а)пиримидин-4-он. То пл. 11Я°С (промежуточный 3 продукт), Пример 2. Смесь 75 ч. 2- . -бензотиазоламина, 76 ч. 3-ацетил-4,5-дигидро-2(ЗН)-фуранона, 2,4 ч. 12-н хлористоводородной кислоты и 270 ч. метилбензола перемеривают и нагревают с обратным холодильником 2 ч с применением водоотделителя, Реакционную смесь охлаждают и добавляют 323 ч. фосфорилхлорида при 20-25 С, Все вместе постепенно /Ч нагревают до 110 Си продолжают перемешивание 2 ч при этой температуре. Растворитель выпаривают и остаток вьшивают на смесь измельченного льда с гидратом окиси аммония. Продукт экстрагируют трихлормеааном. Экстракт высушивают, фильтруют и выпаривают. Остаток очищапэт колоночной хроматографией над силикагелем, применяя для отмывки из адсорбента смесь трихлорметана с метанолом (92:8 по объему). Чистые фракции собирают и растворитель вьтаривают. Остаток кристаллизуют из смеси 2-пропанола с 2,2 -оксибиспропаном, что дает 39 ч, 3-(2-хлорэтил)-2-метил-4Н-пиридо(2,1-б)бензатиазол-4-он т. пл, 144 С.(промежуточный 4 продукт), . . Аналогичным образом получают так- е 6-(2-хлорэтил)-2-, 7-диметш1-5Н1,3,4-тиадиазоло(3,2-а)пиримидин-5-он; т, пл, 118 С (промежуточный 5 продукт) и 6-(2-хлорэтил)-7-метил-5Н-тиазоло-(3,2-а)пиримидин-5-он (промежуточный 6 продукт), Пример Зо Смесь 30 ч, 4-окси-2-меркапто-6-метш1-5-пиримидинэтанола, 6,8 ч. гидрата окиси натрия, 15 ч. бикарбоната натрия и 100 ч, 2-пропанона перемешивают при комнатной температуре, затем добавяют 180 ч. тетрагидрофурана и 170. ч. воды. Далее добавляют сразу 25 ч, З-хлор-2-бутанона и 0,2 ч. Ы,Ы,Ы-триэтилбеизолэтанамина-хлоридэ и все вместе перемешивают и нагревают 1 ч при 60 С. Перемепшвание продолжают всю ночь при комнатной температуре. Реакционную смесь фильтруют и фильтрат высаливают. Органическую фазу отделяют, высушивают, фильтруют и вьшаривают, что дает 36 ч. 5-(2-оксиэтил)-6-метил-2 (1 -метил-2-оксопропил) тио -4-(ЗН)пиримидинона в виде маслообраз ного остатка (промежуточньш 7 продукт) . .Пример 4. Смесь 30 ч. 4-ок си-2-меркапто-6-метил-5-пиримидинэтанола, 25 ч. карбоната калия, 270 ч. N,N-димeтилaцeтaмидa и 75 ч воды перемешивают при комнатной тем пературе и добавляют 36 ч. 1,3-дибромпропана сразу, температура повышается до 50 Со Все вместе перем шивают всю ночь при комнатной температуре. Реакционную смесь выпаривают, к остатку добавляют воду. Твердый продукт промЬшают водой и ; высушивают в вакууме при , что дает 21 ч. (58%) 3,4-дигидро-7 -(2-оксиэтил)-8-метил-2А, бН-пирим до(2,1-б) (1,3) тиазин-6-она; т.пл. 155°С (промежуточный продукт Аналоничным образом получают та же 2,3-дигидро-6-(2-оксиэтил)-7-ме тил-5Н-тиазоло-(3,2-а)пиримидин-5-он} т. пл. 148,7°С (промежуточный 9 продукт), П р и м е р 5. Смесь 20 ч. 3,4 -дигидро-7-(2-оксизтил)-8-метил-2Н -6Н-пиримидо(2,1-6)(1,3)тиазин-6-она, 50 ч. уксусной кислоты и 180 ч„ бромистоводородной кислоты в виде 67%-ного раствора уксусной кислоты перемешивают и нагревают с обратным холодильником. Перемеши вание продолжают всю ночь при температуре кипения. Реакционную смес вьтаривают и твердый остаток расти рают в 2-пропаноне. Продукт отфиль ровывают и высушивают, что дает 24 ч. (100%) 7-(2-бромэтил)-3,4-дигидро-8-метил-2Н,бН-пиримчдо(2, -б)-(1,3)тиазин-6-он-моногидробромид$ т. пл. 215 С,(промежуточньй 10 продукт). Аналогичным образом получают та же 6-(2-бромэтил)-2-3-дигидро-7 метил-5Н-тиаз оло-(3,2-а)пиримидйн -5-oн-мoнoгйдpoбpoмид т. пл. 237,2 .G, (промежуточный 11 продукт) Пример 6. Смесь 36 ч. 5-(2-оксиэтил)-6-метил-2- ( 1-метил-2-оксопррпил)(ЗН)-пиримидинона и 240 ч. 60%-ного раствора бромистоводородной кислоты в уксусной кислоте перемешивают и нагревают 4 ч при 90 С. Реакционную смесь вьтаривают и остаток суспендируют в 400 ч. 2-пропанона. Твердый продукт отфильтровывают, промьтают 2-пропаноном и высушивают, что дает 44 ч. 6-(2-бромзтил)-2,3,7-триметш1-5Н-тиазола(3,2-а)пиримидин-5-, -она моногидробромида, т.пл. (промежуточный 12 продукт). Пример 7. К перемепаиваемому и нагреваемому с обратньш холодильником комплексному соединению Гриньяра, предварительно приготовленному исходя из. 14,6 ч магния и l05 ч. 1-бром-4-фторбензола в 450 ч. -оксибисэтана, добавляют по каплям раствор 94 ч. 4-фенил-1-(фенилчетил)-4-пиперидинкарбоногидрохлорида в 360 ч, метилбензола. Около 250 ч. 1,1 -оксибисэтана перегоняют при внутренней температуре 60-65 С. Мутный раствор перемешивают и нагревают с обратным холодильником 5 ч. Реакционную смесь разлагают насыщенным раствором хлорида аммония в воде. Слои разделяют и органическую фазу высушивают, фильтруют и выпаривают. Маслянистый остаток кипятят в разбавленном растворе хлористоводородной кислоты. После охлаждения реакционную массу подщелачивают гидратом окиси аммония и экстрагируют трихлорметаном. Экстракт высушивают, фильтруют и выпаривают. Остаток .кристаллизуют из смеси 2-пропанола с 2,2 -оксибиспропаном, что дает 91 -ч. (81%) (4-фторфенил) { 4-фенил-1-(фенш1метил)-4-пиперидинил метанона; т. пл. 147,6 С (промежуточный 13 продукт). Следуя способу Гриньяра, получают также (4-фторфенил)4-метил-1-(фенилметил)-4-пиперидинил метанон в виде маслянистого остатка (щЮмежуточ- ный 14 продукт). Пример 8. К перемешиваемой смеси ,79 ч. (4.-фторфенил) 4-фенил-1 - (фенйлметил) -4-пиперидинилДметаног на и 630 чо метлпбензола добавляют по каплям 32 ч, этил-карбонохлоридата при комнатной температуре, ffo окончании продолжают перемешивание 5 ч при температуре кипения. Реакционную смесь вьшаривают и (хлорметил) бензол отгоняют в вакууме (насос) . Маслянистый остаток очищают колоночной хроматографией над силикагелем с применением в качестве средства для отмывки из адсорбента смесь трихлорметана с метанолом (982 по объему). Чистые фракции соб рают, и растворитель вьшаривают. Остаток кристаллизуют из смеси 2,2-оксибиспропана с небольшим количес вом петролейного эфира, что дает 35,5 ч. этил А(-4-фторбензоил)-4-фенил-Т-пиперидинкарбоксилата;т.пл. 91,7 С (промежуточный 15 продукт). Аналогичным обпазом получают так же этил 4-(4-фторбензоил)-4-метил-1 -пиперидинкарбоксилат в виде остатк (промежуточный 16 продукт) Пример 9. Смесь 14 ч. этил ,4-(4-фторбензоил)-4-фенил-1-пиперидинкарбоксилата и 150 ч. 48%-ного водного раствора бромистоводородно кислоты перемешивают и нагревают с обратным холодильником 30 мин. Реак ционную смесь разбавляют 100 ч. вод и реакционную массу оставляют при перемешивании до охлаждения до комнатной температуры. Выпавший в осадок продукт отфильтровывают (фильтрат 1 откладывают), промывают метилбензолом и перемешивают в 2-пропа,ноне. Снова отфильтровывают (фильтрат Г1 откладывают) и высушивают, что дает первую фракцию, состоящую из 4,3 ч, (4-фторфенил)(4-фенил-4-пиперидинил)метанона-гидробромида полугидрата.. Фильтрат Г и II вьтаривают и остаток твердого вещества перемешивают в 4-метш1-2-пентаноне. Продукт отфильтровывают и высушивают, что дает вторую фракцию, состоящую из 6,2 ч. (4-фторфеннл) (4-фенил-4-пиперидинил)-метанона гидробромида гемигидрата; т. пл. 173,4 С. Общий выход 73% (промежуточный 17 продукт Аналогичным образом получают также (4-фторфенш1) (4-метил-4-пиперидинил)метанон гидробромид (промежуточный 18 продукт). П р и т е р 10. К перемешиваемо смеси 100 ч. пиридина, 53 ч. 5-фтор -1Н-индола и 270 ч. бензола добавляют по каплям 57 ч. хлористого бензоила. По окончании продолжают перемешивание всю ночь при комнатной температуре. Реакционную смесь выливают в разбавленный раствор хлористоводородной кислоты и разделяют слои. Органическую фазу высушивают, фильтруют и вьтаривают. Остаток дважды очищают колоночной хроматографией над силикагелем. Для отмывки из адсорбента используют смесь трихлорметана с метанолом (95:5 по объему)о Чистые фракции собирают и растворитель выпаривают, что дает 80 ч. 1-бензоил-4-(5-фтор-1Н-индол-3-ил)-1,4-дигидропиридина в виде остатка (промежуточный 19 продукт). Аналогичным образом получают также 1-бензоил-1,4-дигидро-4-(1Н-ИНдол-3-ил)-3-метилпиридин в качестве маслообразного остатка (промежуточньш 20 продукт). Пример 11. Смесь 65 ч. 1-бензоил-4-(5-фтор-1Н-индол-3-ил)-1,4-дигидропиридина и 270 ч. N,N-диметилацетамида гидрируют при нормальном- давлении при комнатной температуре 10 ч. катализатора в виде 10%-ного палладия на активированном угле. После поглощения вычисленного количества водорода катализатор отфильтровывают и фильтрат выпаривают. Остаток выливают на воду и проДУкт экстрагируют 4-метил-2-пентаноном.,Экстракт высушивают, фильтруют и выпаривают. Остаток очшцают колоночной хроматографией пац силикагелем, применяя смесь трихлорметана с метанолом (95:5 по объему) для отмывки из адсорбента. Чистые фракции собирают и растворитель вьтаривают, что дает 5 ч. 1-бензоил-4-(5-фтор-1Н-индол-3-ил)пиперидина в виде остатка (промежуточный 21 продзкт) . Аналогичным образом получают также цис-1-бензоил-4-(1Н-индол-3-нп)-3-метилпиперидин; т. пл. 230,7 С (промежуточный 22 продукт). Пример 12. Смесь 21 ч. цис-1-бензоил-4-(1Н-индол-3-ил)-3-метилпиперидина, 60 ч. гидрата окиси калия 385 ч. 1,2-этандиола и 80 ч, воды перемешивают и нагревают с обратным холодильником (около 130 С) всю ночь. После охладцения на время добавляют около 200 ч. воды, причем
продукт кристаллизуется. Все вместе дополнительно охлаждают, твердый продукт отфильтровывают, промывают большим количеством воды и 2,2 -оксибиспропаном, затем высушивают Выход 11,2 ч. (80%) цис-3-(3-метил-4-пиперидинил)-1Н-индол Хпромежутоный 23 продукт).
Аналогичным образом получают также 5-фтор 3-(4-пиперидинил)-1Ниндол (промежуточный 24 продукт).
Получение целевых соединений.
Пример 13. Смесь 3,3 ч. 6-(2-хлорэтил)-2,З-дигидро-7-метил-5Н-тйазола(3,2-а)пиримидин-5-она, 3 ч. (4-фторфенил) (Д-пиперидинил)метанонгидрохлорида, 8 ч. карбоната натрия и 120 1. 4-метил-2-пентанона перемешивают при температуре кипения с обратным холодильником в течение 20 ч , используя водоотделитель. Реакционную смесь фильтруют в горячем виде над Hyflo, а затем фильтровальную лепешку промывают трихлормётаном. Полученный фильтрат вьшаривают. Остаток очищают на хроматографической колонке с силикагелем, используя смесь трихлорметана и метанола (95:5 по объему) в качестве элюента. Чистые франкции собирают и элюент выпаривают. Остаток кристаллизуют из смеси 2-пропанона и 2,2-оксибиспропана, получая 2 ч. 6-Г2- 4-(4-фторбензоил)-1-пиперидинил этш1 -2,3-дигидро-7-метил-5Н-тиазоло(3,2-а)пиримидин-5-она, т.пл.165,6°С (соединение 1), выход
40%. ; ,
Аналогичным образом получают 7-{2- 4-(А-фторбензоил)-1-пипериди|нил зтш1 -3,4-дигидро-8-метил 2Н, 6Н-пиримидо 2,1 -в D d тиазин-6-он J т. пл. 165,2°С (соединение 2); выход 52% и 3,4-дигидро-7 2-(4-1H-Индoл-3-шl) -1 -пиперидянилД-зтил -8 -метил-2Н-бН-йиримидо(2,1-в)(1,3)тизин-6-oHj т. пл. 227,1 С (соединение 3), выход 42%.
Пример 14. Смесь 3,75 ч. 6-(2-хлорэтил)-3,7-диметил-5Н-тиазо лс1-(3,2-а)пиримидин-5-она; 3,6 ч. (4-фторфенил)(4-пиперидинил) мета- нонгидрохлорида, 12 ч. карбоната натрия, 0,1 ч. иодида калия и 200 ч 4-метил-2-пентанона перемешивают и кипятят с обратным холодильником в течение 22 ч, используя водоотделитель. Реакционную смесь фильтруют в горячем виде на Hyflo и полученный фильтрат вьтаривают. Остат очищают с помощью хроматографической колонки на силикагеле, используя смесь трихлорметана и метанол (90:10 по объему) в качестве злюент
Чистые фракции собирают и элюент выпаривают. Полученный остаток кристаллизуют из смеси ацетонитри- ла и 2,2 -оксибиспропана, получая 5 ч. (4-фторбензоил)-1-пиI перидинил этил -3,7-диЬ1етил-5Н-тиазоло(3,2-а)пиримидин-5-она; т. пл.
Тем же способом,используя эквиj валентные количества соответствующи исходных материалов получают:
(4-фторбензоил)-1-пиперидинил} этил1-7-метил-5Н-тиазоло (3,2-а)пиримидин-5-он{ т.пл. 147,9 С (соединение 5), выход 22%;
3-Г2- 4-(4-фторбензоил)-1-пипер идинил э тил1-2-метил-4Н-пйримидо(2,1-в)бензотиазол-4-он; т.пл.175,4 (соединение 6), выход 33%,
6- Гз- 4- (4-фторбензоил) -1 -пиперидинил этил 5(-2, 7-диметил-5Н-1,3,4-тиодиазоло(3,2-а)пиримидин-5-он; т.пл. 198,2с (соединение 7), выход 51%;
3-Г2- 4-(4-фторбензоил)-1-пипе- ридинилД 3тилЛ -7,8-дигидро -2-метил-4Н, . 6Н-циклопента (4,5) тиазоло ,2-а пиримидин-4-он; т. пл. 183,8 195.8С (соединение 8),. выход 42%, 6-Г2- 4-(4-фторбензоил)-4-мeтил-.1-пипepидинил зтил -7-мeтил-5H-тиaзoлo (3 ,2-а)пиримидин-5-она моногидрохлорид т. пл. 177, (соединени 9), выход 45%;
(4-фторбензоил)-4-фенил-1-пиперидиншт этил -7-метил-5Нтиазоло(3,2-а)пиримидин-5-он; т. пл 161,1с (соединение 10), выход 53/5.
Пример 15. Смесь 3,75 ч. 6- (2-хлорзтил)-3,7-диметил-5Н-тиазО ло(3,2-а)пиримидин-5-она, 3 ч. 3-(4-пиперидинил)-1Н-индола, 10 ч. карбоната натрия; 0,1 ч. иодида калия и 200 ч. 4-метил-2-пентанона перемешивают и кипятят с обратным холодильником в течение 20 ч с водоотделителем. Затем реакционную смесь фильтруют в горячем виде на Hyflo и полученный фильтрат выпаривают. Остаток очищают на хроматографической колонке с силикагелем, используя смесь трихлорметана и 13 метанол (90:10 по объему) в качестве элюента,. Чистые фракции собирают и элюент выпаривают. Остаток кристаллизуют из этанола, получая 3,25 ч. 6-((1Н-индол-3-ил)-1-пиперидинил -э ,7-диметил-5Н-тиаэоло(3,2-а) пиримидин-5-она, т. пл. 274, (соединение 11), выход 53%. Тем же способом, используя эквивалентные количества соответствующих исходных материалов получают: (1Н-индол-3-ил)-1-пиперидинйлДэтил1-7-метил-5Н-тиазоло(3,2-а)пиримидин-5-он; т. пл. 218,5 (соединение 12), выход 45% 3- 2- 4- (1 Н-индол-3-ил) -1 -пиперидинил этил -2-метил-4Н-пиримидио(2,1-в)бензотиазол-4-он| т. пл. 274,9°С (соединение 13), выход 50% 4-(1 Н-индол-3-ил)-1-пиперидинил этил -2,7-диметил-5Н-1,3., 4-тиадиазоло(3.,2-а)пиримидин-5-он/ т. пл. 260,1°С (соединение 14), выход 7 7%I . 2,3-дигидро-6-.( 1 Н-индол-3-ил)-1-пиперидинил |этил -7 -метил -5Н-тиазоло(3,2-а)пиримидин-5-он т. Пл. 238,2-241,7°С (с разложением (соединение 15), выкод 55%J 2-метйл-З- (.2- 4-метил (1 Н-индол-3-ил)-1-пиперидинил -зтил -4Н-ПИримидо(2,1-в)бензотиазол-4-он т.пл.270, (соединение 16), выход 76%; , 7,8-дигидро-З- 2- 4-(1Н-индол-3 -ил)-1-пиперидинил1-этил -2-метил-4Н, бН-циклопента(4,5)тиазоло(3,2 -а)пиримидин-4-он; т. пл. 242,9°С (соединение 17), выход 69%; 3,7-диметил-6- 2- 4-(2-метил-1Н -индол-3-ил)-1-пиперидинил этил -5Н-тиазоло(3,2-а)пиримидин-5-он, т. пл. 187,9-188,7°С (соединение 1 выход 48%, 7-метил-6- 2- 4-(2-метил-1 Н-индол-3-ил)-1-пиперидинил2 -этил|-5Нтиазоло (3,2-а)пиримидин-5-он, т. пл. 170, (соединение 19), вы ход 12%, 6-j2- С4-(5-ФТОР-1 Н-индол-3-ил)-1-пиперидинилЗ ,7-диметил-5Н-тиазоло(3,2-а)пиримидин-5-он т. пл. 270,6°С (соединение 20), выход 50% i6- 2-14-(5-хлрр-1Н-индол-3-ил)-1-пиперидинил}-этилЧ-7-метил-5Н-тиазоло(3.,2-а)пиримидин-5-он 2Т.ПЛ.224,бС (соединение 21), ход 20%J р( (5-фторо-1 Н-индол-3-ил )-1-пиперидинил этил -7-метил-5Н-:тиазоло(3,2-а)пиримидин-5-он1 т.пл.. 244, (соединение 22), выход 51%, цис-2,3-ДИГИДРО-6-С2- 4 -(1Н-индол-З-ил)-Зметил-1-пиперидинил этил -7-метил-5Н-тиазола(3,2-а)пиримидин-5-он; т. пл. 234, (соединение 23), выход 61%. Пример 16. Смесь 5,85 ч, 6-(2-бромэтил)-2,3,7-триметил-5Н-тиазоло(3,2-а)пиримидин-5-он моногидробромида, 4 ч. (4-фторфенил)(4-пиперидинил)метаноногидрохлорида, 10 чо карбоната натрия, 3 ч. 30% раствора метилата натрия и 240 ч. 4-метил-2-пентанона перемешивают и кипятят с обратным холодильником в течение 20 ч, используя водоотделитель. Реакционную смесь фильтруют в горячем виде на Hyflo и полученный фильтрат выпаривают. Остаток очищают на хроматографической колонке с силикагёлем, используя смесь трихлорметана и метанола (95:5 по объему) в.качестве элюента. Чистые фракции собирают и элюент выпаривают. Остаток кристаллизуют из смеси ацетонитрила и 2,2 -оксибиспропана (3:1 по объему), получая 1 ч. (4-фторбензоил)-1-пиперидинил этилЯ-2,3,7-триметил-5Н-тиазоло(3,2-а)пиримидин-5-она; т. пл. 159, (соединение 24), выход 14%. Аналогичным образом получают: 6- (1Н-индол-3-ил)-1-пиперидинил} э тил} -2,3, 7-триметил-5Н-Тиазоло(3,2-а)пиримидин-5-он т. пл. 240,2®С (соединение 25), вькод 30%, 6-Г2-Г4-(4-фторфенил оксиметил)-1-пипepидинилJ-этилJ-3,7-диметил75Н-тиазоло(3,2-а)пиримидин-5-он т. пл. 138, (соединение 26), выход 27%; (4-фторфенил оксиметил).-1-пиперидинил -этил -3,4-дигидро-8-метил-2Н, бН-пиримидо(2,1-в)(1,3-тиазин-6-он),т„ пл. 174,1C (соеинение 27), выход 52%. П р и м е р . 17. Перемешиваемую и подогреваемую суспензию 4 ч. -12- 4- (1 Н-индол-3-ил) -1 -пиперидиилЗ ,7-диметил-5Н-тиаз оло3,2-а)пиримидин-5-она в 80 ч. эта- I ола подкисляют фосфорной кислотой.
60 ч. воды добавляют ji все кипятят. Нерастворившуюся часть отфильтровывают, полученному фильтрату дают возможность кристаллизоваться. Полученный продукт отфильтровывают и сушат, получая 4,5 ч (80%) (IH-индол-З-ил)1-пиперидинил2этш14-3,7 -дкметил 5Н-тиазоло(3,2-а)пири шдин-5-oнфocфaт (2;3) моногидрата т. пл. ZlAjA c (соединение 28), выход 80%.
Тем же способом получают:
6-Г2- 4-(1 Н-индол-3-ил) -1-пиперидннил} , Т-гдиметил-ЗН-тиазоло (3, 2-а)пиримидин-5-он сульфат (1:1) моногидрат т. пл. 244,3 С (соединение 29), выход 80%,
(IH-индол-З-ил)-1-пиперидинил этил1-3,7-диметш1-5Н-тиазоло(3,2-а)пиримидин-5-он-2-окси-1,2,3-пропантрнкарбоксилат (2:1) моногидрат т. пл. 190,5 С (соединение 30), выход 25Z;
/+/-6 ((IH-индол-З-ил)-1-пиперидинил 1этил -3,7-диметш1-511-тиазоло(3,2-а)пиримидин-5-он(К-/К, )-2,3-диоксибутандионат (2:1) моног здрат; т. пл. 177, (соединение 31), внход 40%;
6-f2- 4-(1Н-ичдол-3-ил)-1-пиперидинш1 этилЯ-3,7-диметил-5Н-тиазоло(3,2-а)пиримидин-5-ок(2)-2-бутандионат (1:1); т. пл. 150, (соединение 32), выход 35%. .
При мер 18. Смесь 6,8 ч. 6-(2-бромэтил)-2,З-дигидро-7-метил-5Н-тиазоло(3,2-а)пиримйдин-5-оиа, 3,15 ч, б( -(4- орофенил)-4-пиперидинметакопа; 4,8 ч. карбоната нат1тя; 0,1 ч, иодида калия и 200 ч, ;4-метил-2-пентанона перемешивают
:и кипятят с ОбраТНЫМ ХОЛОДИЛЬНИКОМ в
течение 24 ч. Реакционную смесь охлаждают, прс швают 50 ч. воды, сушат, 4 «пьтруют и выпаривают. Остаток очищают на хроматографической колонке, иа сипикагеле, используя смесь трихлорметана н метанола (90:10 по объему) в качестве элюента. Чистые / фракции собирают и элюент выпаривают. Остаток отверждают при растирании в ацетЬнитриле о Продзкт отфильтровыва, дважды промывают ацетонитрилом и сушат, получая 2,5 ч. (42%) (4-фторфенш1 оксиьютил)-1-пиперидинил}этил -2,3-дигид, ро-7 метш1 5Н-тиазоло(3,2-а)пирими8032 16
дин-5-она, т. пл. 204, (соедине чние 33), выход 42%.
Аналогичным образом получают ЦИС1 -6-f2-{4-(1Н-индол-З-ил)-3-метил-15 -пиперидинил -этил -3,7-диметил-5Н-тиазоло(3,2-а)пиримидин-5-он; т. пл. 212,8 С (соединение 34), выход 18%.
Пример 19. Смесь 9,3 ч. (бромэтил)-3,7-диметил-5Нтиазоло(3,2-а)пиримидин-5-он моногидробромида 6,5 ч. (4-фторофенил)-1,3-диоксрлан-2-ил пиперидина; 10,2 ч. карбоната натрия и 120 ч. 4-метил-2-пентанона перемешивают и кипятят с обратным холодильником в течение ночи. Реакционную смесь охлаждают и добавляют воду. Спои разделяют. Органическую фазу сушат, фильтруют и выпаривают. Остаток очищают на хроматограчической колонке на силикагеле, используя смесь трихлорметана и метанола (98:2 по объему) в качестве эяюеята. Чистые фракции собирают и элюент выпаривают. Остаток перекристаллизовывают из 2,2-оксибиспропана. Полученный продукт фильтруют.и суаат, получая 4 ч. (35%) 6-|2- 4-(2-)40 -фторфенш13-1,3-диоксалан-2-ил(-1-пиперидинил)этил}-3,7-диметил-5Н-тиазоло(3,2-а)пиримидин-5-она/ т. пл. 140 С (соединение 35), выход 35%.
Пример 20. Смесь %3 ч. 6-f2-С4-(4-фторбензоил)-1-пиперидиннлЗ-этил -З,7-да метил-5Н-тиазоло(3,2-а)пиримидин-5-она, 10 ч.
0 1,1, 1 -(метилидентрис/окси)трисэтана, 4 ч. 4-метилбензолсульфокислоты и 80 ч. этанола перемешивают и кипятят с обратным холодильнике, в течение 72 ч. После охлаждения
5 вводят газообразный аммиак. Образ пощийся осадок отфильтровывают и ползгченный фильтрат вьтаривают. Остаток очищают на хроматографической колонке на силикагеле, используя
0 смесь трихлорметана и этаньла (ЯОг Щ по объему) в качестве элюента. Чистые фракции собирают и элюент вы:Паривают. Остаток далее очищают хроматографически с обращенной фазой
5 на Li Chroprep. R Р 18, используя бмесь воды, содержащей 0,5% ацетата аммония, и метанол, содержащий О,tZ , Л-(11-метш1этил)-2-пропанамина (15:85
по объему), в качестве элюента. Чистые фракции собирают и элюент выпаривают. Остаток кристаллизуют из 2,2-оксибиспропана, получая 0,, 6-Г2- А-(диэтокси)4-фторфенилЗметил{1-пиперидинил) ,7-димётил-5Н-тиазоло (3,2-а) пиримидин-5-она Jг. пло 115,6®С (соединение 36), вы- . асод 6%. .
Пример 21. Смесь из 4 ч. 6-Г2- 4-(Д-фторбензоил)-1-пиперидинил2этап1-2,3-дигидро-7-метил-5Н-тиазрла(3,2-а)-пиримидин-5-она-, 0,7 ч. гидроксиламин-гидрохлорида; 1 ч. Н,Ы-диэтш1-этан-амина и 20 Чо этанола перемешивают и нагревают с обратным холодильником в течение 5 ч. Реакционную смесь вьшаривают и остаток перемешивают с водой. Продукт экстрагируют дихлорметаном. Экстракт высушивают, фильтруют и выпаривают. Остаток вьщеляют на хроматографической колонке на силикагеле с использованием смеси трихлорметана и метанола (95:5 объемн.) в качестве элюента. Первую фракцию L(E)-изомер собирают и элюент выпаривают. Остаток выкристаллизовывают из 2-пропанола с получением 1 ч. (24%) (Е)-6-((4-фторфенил) (гидроКси-имино)-метил -(1-пиперидинил) -3 ,3-дигидро-7-метил5Н-тиазоло-(3,2-а) пиримидин-5-она, т. пл. 214,1°С..
Вторую фракцию (2)-изомера собирают и элюент выпаривают. Остаток выкристаллизовывают из 2-пропанЬла с получением 0,2 ч. (4,6%) (2)(4-фторфенил) (гидрокси-имин.о)-мвтил1-( 1-пиперидинил) -этил -2,3-дигидро-7-метил-5Н-тиазоло-,2-а)пиридидин-5-она; т. пл. 220,8°С.- ,
Соединения формулы Г или их фармацевтически пригодные соли - продукты присоединения кислот - обладают выраженной психотропной, антигистаминной и антисеротонивной активностью.
Активность соединения в качестве психотропньк средств доказывается опытными данными испытаний с апоморфином (АЛО), триптамином (ТРИ) и норэпинефрином ,(НОР) на крысах и Г испытания с АПО на собаках. Испытания проводят согласно активным ме- . тодикам. Опытные данные даны в табл„ t..
Испытание с АПО, ТРИ и НОР на крысах. Подопытных животных (взрослые самцы крыс породы Wistav вес 240 + 10 г после продолжавшейся
всю ночь вьщержки без пищи обраба, тывают посредством подкожных инъекций (1 мл/100 г) водным раствором исследуемого соединения (время нулевой отсчет) и помещают в изолированные клетки для наблюдения. Через 30 мин (отсчет времени - 80 мин) вводят внутривенно 1,25 мг/кг апоморфина-гидрохлорида (АПО), после чего крыс наблюдают в течение 1 ч для выявления волнения, беспокойства, стереотипного жевания. К концу 1-часового периода (отсчет времени 90 мин) тем же животным вводят внутривенно 40 мг/кг ТРИ и -отмечают типичные припадки по типу апоплексического удара. Двумя часами позже после начала предварительной обработки (отсчет времени 120 мин) те же животные подвергаются внутривенной инъекции НОР (1,25 мг/кг), . после чего наблюдают возможную смертность за время до 60 мин.
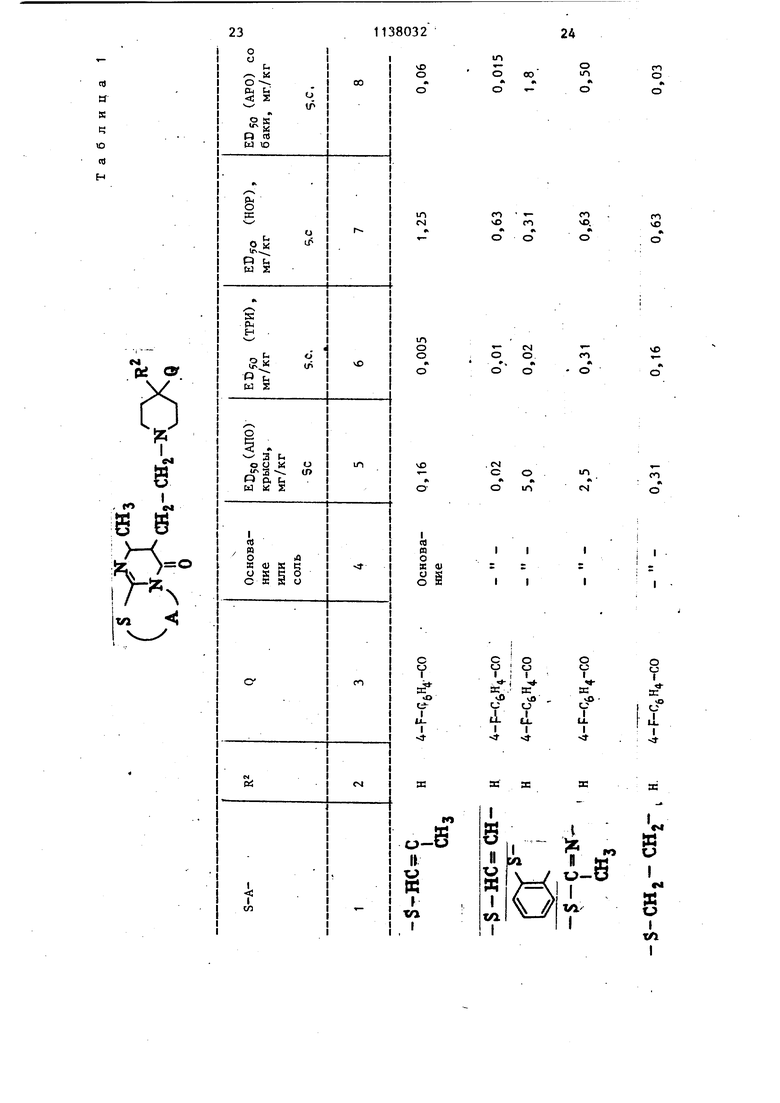
В табл. 1 приведены значения BDjg у р°яда соединений. Показатель
EDgg в том виде, как он здесь используется, .представляет дозу, которая защищает 50% животных от явлений вызванных действием АПО, ТРИ или НОР.
Испытание с АПО на собаках.(АПОсобака). Соединения, указанные в табл. 1, вводят подкожно гончим собакам при различных дозировках, после чего спустя 1 ч животные под-
вергаются лечению стандартной
дозой АПО 0,31 мг/кг, вводимой подкожно .
В табл. 1 приведены значения для ряда соединений. Показатель ED
й
в том смысле, в каком он здесь используется, представляет дозу, которая защищает 50% животных от рвоты.
Сила действия соединений в качестве антагонистов серотонина видна
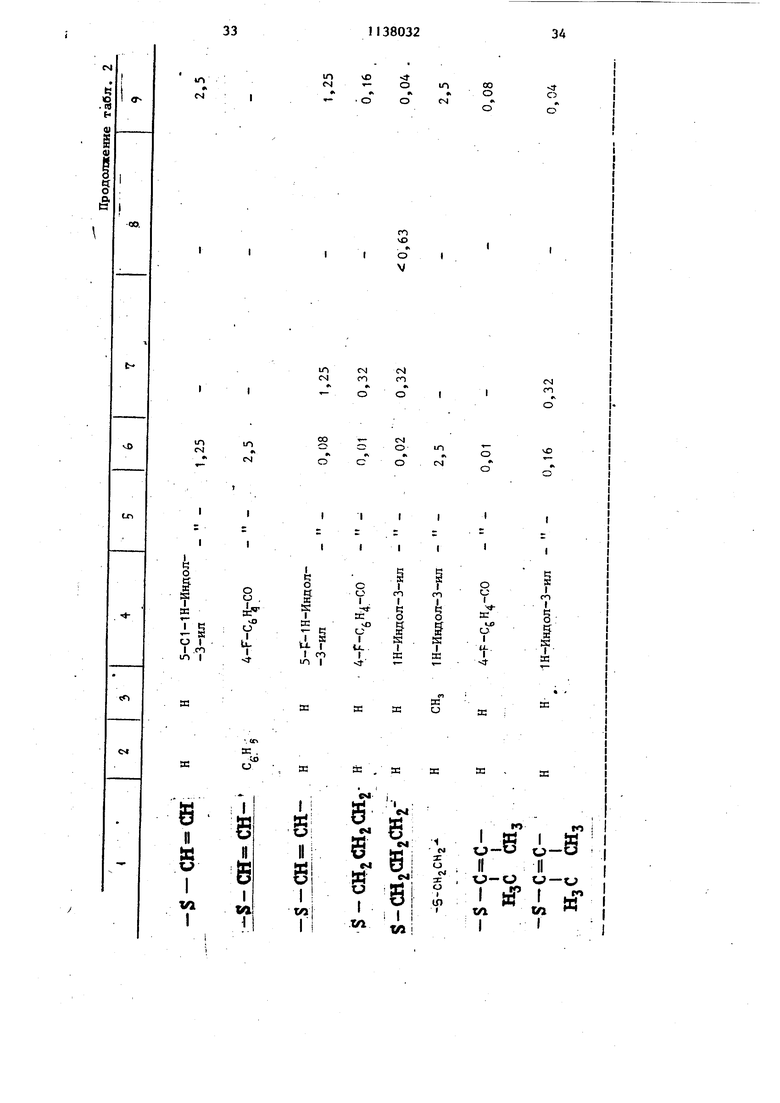
по результатам,полученным при последунщих испытаниях, при которых исследовалось их антагонистическое действие на применение серотонина. Результаты испытаний на действия, вызывающие повреждение желудка (повреждения вызывались искусственно, действием соединения 48/80). Соединение 48/80 (смесь олигомеров, полученных конденсацией 4-метокси-Н-метилбензолэтанамина с формальдеги дом) представляет сильнодействующее средство, способствукщее вьщепению вазоактивных аминов из эндогенных резервов, например гистамина или се ротонина. У крыс, инъекционированных соединением 48/80, проявляются согласуемые измненения кровоснаб-. женйя у различных сосудистых образо ваний: цианоз ушных раковин « конеч ностей четко выявляются в пределах 5 мин после инъекции соединения, крысы погибают от шока в пределах 30 мин. Шок, за которым следует гибель, может быть устранен, если крыс предварительно обрабатывают с .лечебной целью классическим Н-1 антагонистом. Однако стимулирующие воздействия на желудочную секрецию остаются ненарушенными, так что у крыс, обработанных с лечебной целью соединением 48/80 и защищенных от шока антагонистом Н-1, могут появляться все признаки интенсивного действия желудочных желез. Широ кое вскрытие погибших животных пока зывает наличие расширенных желудков с ненормальным содержимым, а также грубых, нервных, блестящих, красных бляшек по всей слизистой оболочке, соответствующей участкам с распавшимися железами. Ряд известных антагонистов серотонина такие, как метисергид, ципрогептадин, цинансерин и др., полностью предотвращает цианоз ушных раковин и периферических участков, а также повреждений ; железистых участков желудка и его необычное расширение. В табл.. 2 приведен ряд соединени общей формулы Г соответствукицие им дозы, при которых расЕШрение желудка полностью отсутствует у 50% подопытных крыс (значенияED50 )« I Антагонистическа я активность в отношении действия протомина на артерию, расположенную ближе к хвостеному концу тела крысы. Лля проверочного испытания используют хвостовые артерии предварительно вьщержан ных без корма самцов крыс (210-235 г). Из Каждой артерии получают две спиральные полосы длиной 5-6 см и шириной 2 мм, которые монтируют в вертикальном положении в 1QO мп ванны для органов, содержащей обработанный .кислородом раствор Krebs-Hehse betа. Сокращения, меньшие максимальных получают посредством., добавления одиночных дозировок серотонина (40 нг/мл) нанограммы к ванне для органов в течение 2 мин, каждый раз с интервалом 10 мин, амплитуду сокращения измеряют до добавления лекарства и в течение 5 мин после. После вымывания антагонист снова добавляют 3 раза, чтобы убедиться восстанавливаются и нормализуются ли сокращения. В табл. 2 показаны значения показателя ряда соединений формулы Г , а также их пригодных в фармацевтическом отношении солей, полученных при указанном испытании. В связи с этим, значения ЕВуд представляют мин1жальные, концентрации бирлогически активного соединения, при которых амплитуда сокрар;ения Снижается по меньшей мере на 50% против нормального ее значения. Ингибирование вызванного серотонином сокращения трахеи у морской свинки. Кольца трахей длиной 5 мм, полученные у морских свинок (400500 г), вьщержанных без корма в течение ночи, суспензируют с предварительной нагрузкой 2 г в 100 г ванны, представляющей растор Тирода, газированный смесью 95% кислорода и 5% углекислого газа (). Сокращения регистрируют изометрически. К жидкости, образующей ванну, добавляют с 30 мин интервалами по шарику серотонина 0,31 мг/л (время контакта 8 мин) до и после 30 мин инкуба1р1онного периода при единичной концентрации антагониста.-ОтветHyib реакцию в присутствии антагониста сравнивают с ответной реакцией, наблк давшейся до добавления антагониста (препарат становился непри- . годным для исследований зависимости время - активность). Значения, как показано в табл. 2, представляют собой концентрации антагониста, при которых действие его оснижается . на 50%. Эффективность действия соединений в качестве антагонистов гистамина становится очевидной по рёзультатам. Защита крыс от гибели, вызываемой действием соединения 48/80. Соединение. 48/80, представляющее ..рмесь
олигомеров, полученных конденсацией 4-метокси-М-метил-фенетиламина с формальдегилом, изйестное сильнодействующее средство, высвобождающее гистамин, ЗаиЕИтное действие в отношении гибельного резкого ослабления кровообращения, вызываемого соединением 48/80, представляется простым способом количественной оценки противогистаминного действия иcпытye «лx соединений. Для опытов используют самцов крыс породы Wistar весом 240-260 г, рожденных от родителей, находящихся в родстве между собой. После вьщержки без корма в течение ночи крыс переносят в кондиционированные помещения для дальнейшей обработки (21 j-1 С, относительная влажность 65+5%) .
Крыс обрабатывают путем подкожных инъекций или скармливают испытуемое соединение, или чистый растворитель (О,9-ный раствор хлорида натрия). Через 1ч после такой обработки вводят внутривенно соединение 48/80, свежерастворенное в воде при дозировке 0,5 мг/кг (0,2 мл/100 веса тела).
При контрольных опытах среди 250 животньк, обработанных раствором, которым вводят путем инъекций стандартную дозу соединения 48/80, выживают не бсшее 2,8% животных спустя 4ч. Поэтому такие контрольные опыты рассматриваются как надежный критерий оценки защитного действия при введении лекарства с лечебной целью
3222
В табл. 2 приведены значения KDjo для ряда соединений формулы I и их пригодных в фармацевтическом отношении солей, полученные при указанном
испытании. В данном случае значения ED50 представляют минимальные дозы соединений,, водимых с лечебной целью подкожным путем, причем 50% крыс оказываются защищенными от гибели в результате воздействия соединения 48/80. Благодаря фармакологическим действиям, присущим соединениям общей формулы F или их солям с фармацевтически пригодной кислотой их можно использовать для лечения психотропных заболеваний, а также для лечения целого ряда заболеваний, при которых высвобождение серотонина
имеет решающее значение (блокирование вызнанных серотонином сокращений бронхиальных тканей, артерий и вен), Соединения могут также использоваться в качестве средств успокаивакщих, снимающих ощущение тревоги, нервного напряжения, противоагрессивных, защищающих мускулы и сердечно-сосудистую систему. Следовательно, соединения и соли оказываются пригодными для защиты теплокровных животных, например, в стрессовых ситуациях, возникакядих, в частности, во время транспортировки и т,п. Дополнительно соединения
полезны в качестве защитных
средств при шоковых состояниях, вызванных эндотоксином, а также средства против поноса.
nJ
я
s t;
Ю П)
H
ем
01
tf Я
ч
ю nt
н
о
чО О
m чс
. м
г
о
о
00
с
ОО О
t
ш
о
CN
ю
CN
П с
п
о
33
Ж
го
;.-Г|
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ГИБКИЙ ЭЛЕКТРОНАГРЕВАТЕЛЬ | 1992 |
|
RU2006187C1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ получения производных пиперазина или пиперидина или их солей | 1977 |
|
SU683621A3 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1985-01-30—Публикация
1982-06-24—Подача