сх со оа 9д ..Изобретение относится к новому х мическому соединению, а именно к пе хлорату 2,6-ди-п-метоксифенил-4-фенилэтинилпирИЛИЯ формулы рССбНб СНзО С104 ОШз который является импрегнатором в то кослойной хроматографии, и может найти применение при анализе сложны липидных смесей в клинической и лабораторной практике. Цель изобретения - поиск новых веществ в ряду солей 2,6-диарил-4фенилэтинилпирилия, обладающих новы .свойствхэм импрегнаторов в тонкослой ной хроматографии. Пример 1. Перхлорат 2,6-ди -П-метоксифенил-4-фенилэтинилпирили Металлируют 2,0 г (0,02 моль) фе нилацетилена бутиллитием в абсолютном эфире .в атмосфере аргона при 34 35°С в течение 1,5 ч. К образовавше муся фенилацетилениду лития добавляют 3,9 г (0,01 моль) перхлората 2,6-ди-п-метоксифенилпирилия, перемешивают при кипячении 30 мин до по ного растворения добавленного перхлората. Реакционную смесь обрабаты вают насыщенным раствором хлорида аммония, эфирный .слой отделяют, суш сульфатом натрия и прибавляют 0,03 моль ацетилперхлората. Выход перхлората 2,6-ди-п-метоксифенил-4-фенилэтинилпирилия 65-70%, Т.пл.20 . ИК-спектр в вазелиновом масле, 2210 (), 1620, 1610 (ароматич.), 1270 (С-О-С), 1100 (Сfop. ПМР-спектр в трифторуксусной кис лоте, внутренний эталон ГМСД,сЛ,М.д 3,45 (с, 6Н, 2 ОСНз), 6,42-8,0 (м. 13Н, ароматические протоны). Найдено, %: С 65,07; Н 4,87; 7,39. Вычислено, %:С 65,79; Н 4,29; С1 7,Л9. Перхлорат 2,6-ди- -метоксифенил-4-фенилэтиншширилия представляет собой ярко-красные кристаллы, имею цие в растворе оранжево-желтую люминесцёнцин), не изменяющуюся под действием света. Разделение и индикацию липидных смесей осуществляют следующим образом. Перхлорат 2,6-ди-п-метоксифенил-4-фенилэтилпирилия вводят в силикагель и проводят разделение липидной смеси в системе растворителей, не растворяющей импрегнатор. После разделения смеси липидов по прохождению фронта растворителя пластины сушат на на воздухе при любом освещении. Индикацию разделенных фракций осуществляют в ультрафиолетовом свете (вариант я), либо после кратковременной обработки парами иода также в ультрафиолетовом свете (вариант б ), либо визуально после проявления белых пятен на общем окрашенном фоне (вариант 6 ). Разделение фракций характеризуется хроматоГрафической подвижностью R,T.e. отношением длины пробега фракции (j.) к длине пробега всего фронта растворителей () Rh Pj/f; шириной фракции d , т.е. величиной пятна, измеренной вдоль линии пробега растворителей; наличием диффузной зоны - хвоста С. Пример 2. Разделение стандартных веществ в силикагеле с предлагаемым и известным импрегнаторами, нитратом серебра и без них. A.Готовят суспензию 4 г силикагеля в 8 мл 0,1%-ного хлороформного раствора перхлората 2,.6-ди-И-метоксифенил-4-фенилэтинилпирилия и выливают ее на пластину из стекла 9x12 см. После испарения хлороформа пластина готова к употреблению. Б. По известной методике готовят суспензию 4 г силикагеля в 10 мл 10%-ного водного раствора нитрата серебра и выпивают ее на такую же пластину. Пластину с суспензией сушат 12-18 ч при комнатной темггературе и активируют 1 ч при 105с. Все процессы проводят в темноте. После остывания пластина готова к употреблению. B.Готовят такую же пластину без импрегнатора. Для этого 4 г силикагеля суспендируют в 8 мл хлороформа или в 10 мл дистиллированной воды, наносят суспензию на пластину и сушат при комнатной температуре и активируют при 1 ч. На стартовую линию каждой пластины (А, В и Б) наносят в ВИДР точечных пятен диаметром не более 3 мм по 5 мкг раствора стандартного вещества (кефалина, холестерина, пальмитиново кислоты, трйолеина, этилстеарата) в хлороформе. Содержание лйпида 10 мкг Разделение фракций проводят в систем растворителей петролейный эфир: диэтиловый эфир: ледяная уксусная кислота 90:10:1. По прохождению фронта растворителя пластины вынимают, подсушивают на воздухе и обнаруживают фракции на пластинах Б и В после сжи гания липидов 50%-ной серной кислоты, а на пластине А в ультрафиолетовом свете после кратковременной обработки парами иода (вариант 5 ). Ра ная обработка вызвана тем, что пластины Б и В не флуоресцируют в ультра фиолетовом свете и не дают визуального проявления пятен липидов без об работки, а сжигание липидов на пластине А серной кислотой невозможно за счет реакции импрегнатора с кислотой Индикация липидов в парах иода на пластине с нитратом серебра также невозможна из-за реакции импрегнатора с иодом, и дает общее пожелтени пластины без проявления пятен липидов.. , Стандартные вещества дают на хроматограммах четко очерченные пятна без диффузных зон, что объясняется их высокой очисткой и однородностью. Поэтому разделение стандартных веществ характеризуют только двумя показателями RK и d. Результаты определения приведены в табл. 1. Как видно из табл. 1, стандартные вещества дают после разгона также одно пятно и на пластинах с предлагаемым импрегнатором. Величина RP стандартных веществ при этом не изменяется, т.е. характеристики веществ остаются прежними. Применение перхлората 2,6-ди-п-метоксифенил-4-фенилэтинилпирилия дает возможность сократить щирину фракций по сравнени с нитратом серебра в среднем на 0,7 мм. Неизмейность Rr при сокращении размеров фракции свидетельствует о повышении точности разделения. Пример 3. Разделение эвкалиптового масла в тонком слое силикагеля, импрегнированного перхлорато 2,6-ди-п-метоксифенилэтилпирилия. Готовят пластины аналогично примеру 2 (А и Б). На стартовую линию наносят в виде точечного пятна пробу содержащую 10-100 мкг липидов, а также растворы стандартных веществ,служащих для идентификации фракций пробы. Проводят разделение липидов в смеси растворителей, приведенной выше . Пластины высушивают на воздухе и обнаруживают пятна липидов одним из вариантов «. 5 или в. В табл. 2 приведены значения Кл и d, а также с - наличие (+) или отсутствие (-) диффузной зоны - хвоста. Эвкалиптовое масло на силикагеле без импрегнатора дает не более четырех фракций на фоне общей диффузной зоны так как в отличие от стандартных веществ природные смеси липидов обладают большой неоднородностью и содержат минорные компоненты, которые и дают хвосты. Из табл. 2 видно, что использование в качестве импрегнатора перхлората 2,6-ди-п-метоксифенш1-4-фенилэтинилпирилия позволяет не только сократить ширину разделяемых фракций на 0,7 мм в среднем, но и устранить образование хвостов, т.е. размытых зон, препятствующих четкой индикации пятен, вместо них обнаруживаются минорные компоненты в виде тонких четко очерченных пятен. Кроме того, повьпиается четкость хроматографического разделения, так как обнаруживаются, помимо основных, минорные фракции, не улавливаемые нитратом серебра, которые дают хвосты . Как видно из вариантов « и 5, возможно использование предлагаемого импрегнатора для индикации без дополнительной обработки как в ультрафиолетовом, так и при обычном све.те, т.е. импрегнатор является одновременно и индикатором. Пример 4. Подбор оптимальных для разделения липидов концентраций перхлората 2,6-ди-п-метоксифенил-4-фенилэтинилпирилия. Аналогично примеру 2 (А) готовят пластины, импрегнированные веществом общей формулы в различных концентрациях (табл. 3). Хлороформные растворы стандартных веществ в одинаковых количествах наносят на стартовую линию в виде точечных пятен на все пластины и разгоняют их в приведенной системе растворителей. После разделения пятна липидов обнаруживают по варианту б, как наиболее чувствительному. Результаты определения приведены в табл. 3, где знаком (+) об значено наличие пятна, а знаком (-) его отсутствие. Из табл. 3 видно, что четкое раз деление фракций при использовании перхлората 2 6-ди-п-метоксифенил-4-фенилэтинилпирилия происходит при минимальной концентрации 0,05% и вьше, тогда как концентрация нитрата серебра в тех же условиях состав ляет 10%. Таким образом, рабочая концентра ция перхлората 2,6-ди-п-метоксифенил-А-фенилэтинилпирилия в 200 раз меньше концентрации используемого нитрата серебра. Повьшение концентрации предлагаемого импрегнатора (выше 0,1%) нецелесообразно, так ка она не влияет на результаты определения (интенсивность окраски и люминесценции фона в интервале 0,51,0% достаточна для индикации фракций липидов по всем вариантам а- б) Концентрация не оказываетвидимого влияния на свойства импрегнатора. Пример 5. Определение времени визуального проявления пятен Липидов на пластинах, импрегниро-, ванных перхлоратом 2,6-ди-Ь-метокси фенил-4-фенилэтинилпирилия. Аналогично примеру 2 (А) готовят пластины, импрегнированные предлага мым соединением концентрации- 0,1%, наносят на стартовую линию пробы стандартных веществ, разделяют в си теме растворителей и оставляют для визуального обнаружения пятен при комнатной температуре. Результаты. определения приведены в табл. 4. Для нитрата серебра обнаружение пят в таких условиях невозможно. Как видно из табл. 4, проявлени пятен липидов всех классов заканчи вается через 8 ч, а большинство пя тен через 7 ч,. Некоторые фракции пр являются уже через 5 ч. Поэтому, в зависимости от определяемого класса липидов для визуального обнаружения достаточно 5 - 8 ч. Пример 6. Определение чувствительности способа с использованием перхлората 2,6-ди-п-метоксифенил-4-фенилэтйнилпирилия в качестве импрегнатора - индикатора. Аналогично примеру 2 (А и Б) гото- вят пластины,. импрегнированные предлагаемым соединением общей формулы и . нитратом серебра и наносят на стартовую линию растворы стандартных веществ с различным их содержанием. После разделения в системе растворителей проводят обнаружение пятен липидов. Результаты определения приведены в табл. 5. Как видно из табл. 5 чувствительность определения с использованием импрегнатора - соединения общей формулы, как индикатора не уступает известному AgNOj для свободных жирных кислот и их эфиров и превосходят его в два раза для фосфолипидов, триглицеридов и холестерина. Таким образом, по сравнению с наилучшим из применяемых импрегнаторов нитратом серебра при использовании Импрегнатора перхлората 2,6-ди-г -метоксифенил-4-фенилэтинилпирилияотпадает необходимость соблюдать определенные условия освещения; повышается точность хроматографического разделения: в среднем на 0,7 мм сокращается ширина фракций и устраняется образование диффузных зон хвостов при неизменной величине Rn; появляется возможность определения фракций как без дополнительной обработки (визуально в обычном или ультрафиолетовом свете), так и с кратковременной обработкой в парах иода. Кроме того, использование предлагаемого импрегнатора позволяет заменить дефицитный для народного хозяйства нитрат серебра. Перхлорат 2,б-ди-п-метоксифенил-4-фенш1этинилпирилия может использоваться в медицине для анализа сложных липидных смесей, а также в органической и аналитической химии.
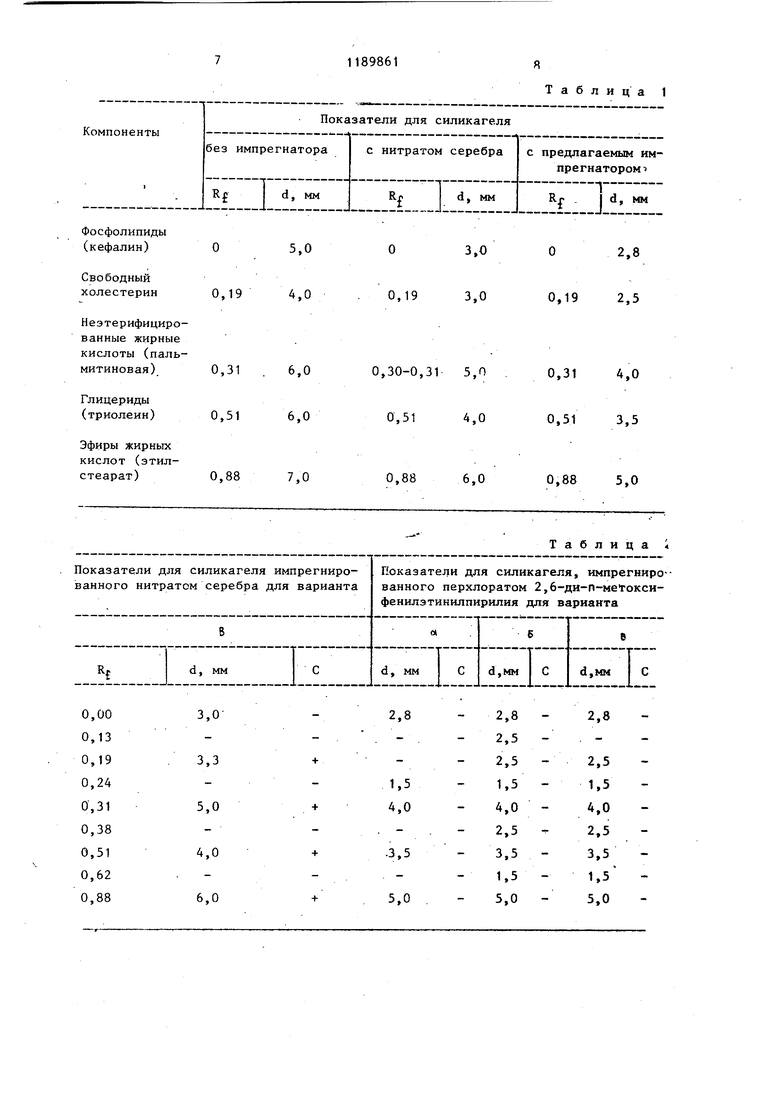
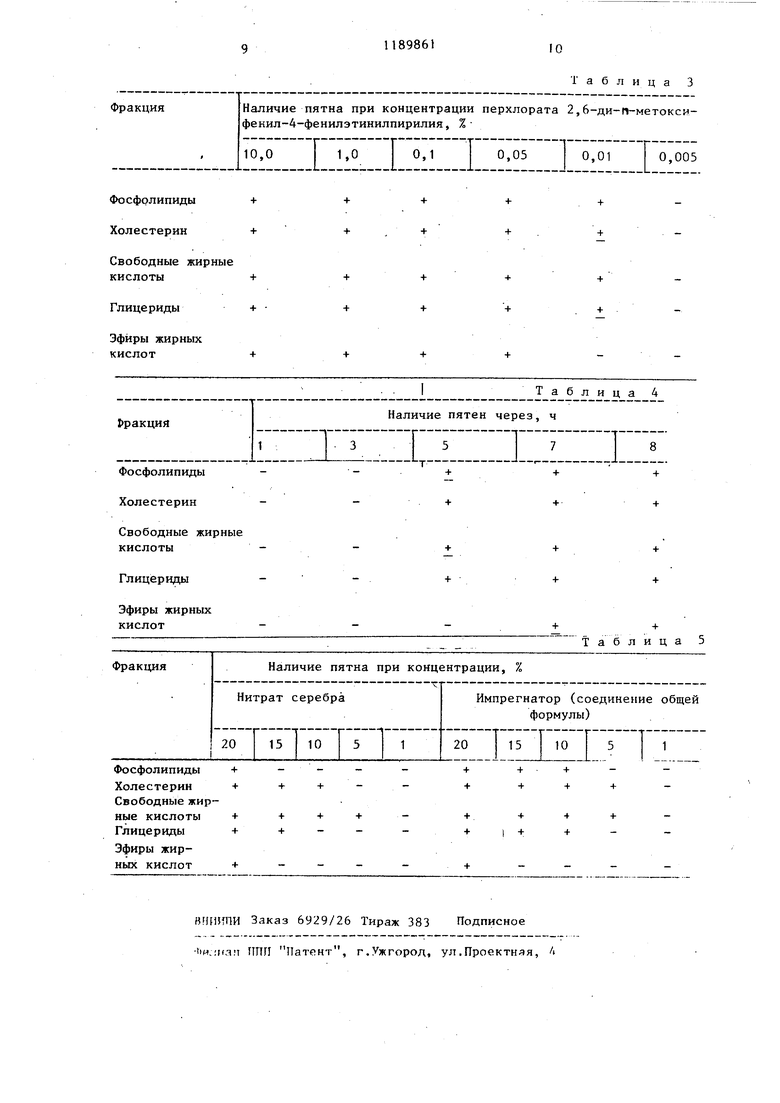
Таблица 1


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ индикации микроколичеств липидов | 1981 |
|
SU991304A1 |
| Перхлораты пиримидо [1,2-а] бензимидазолия в качестве флуоресцентных красителей растительных тканей и микроорганизмов | 1982 |
|
SU1051091A1 |
| Реагент для фотометрического определения анионных синтетических поверхностно-активных веществ | 1981 |
|
SU1008652A1 |
| Способ определения монометиланилина в углеводородных топливах | 2015 |
|
RU2609864C1 |
| Способ количественного определения группового состава липидов | 1980 |
|
SU1010554A1 |
| Способ получения арахидоновой кислоты | 1983 |
|
SU1132947A1 |
| Способ получения арахидоновой кислоты | 1977 |
|
SU897766A1 |
| Способ определения фоксима в секционном материале | 1984 |
|
SU1196772A1 |
| Способ определения соединений,содержащих катион-1,1-диметил-4,4-дипиридиния | 1982 |
|
SU1062600A1 |
| Способ диагностики диффузного гломерулонефрита | 1979 |
|
SU924572A1 |
Перхлорат 2,6-ди-п-метоксифенип-4-фенилэтинилпирилия формулы CECCgHs СНзО как импрегнатор в тонкослойной хроматографии. Vi
Таблица
Фосфрлипиды
Холестерин
Свободные жирные
кислоты
Глицериды
Эфйры жирных
кислот
Свободные жирные кислоты
Глицериды
Эфиры жирных кислот
Таблица 3
+
Таблица 5
| Кирхнер Ю | |||
| Тонкослойная хроматография | |||
| - М.: Мир, 1981, с | |||
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
Авторы
Даты
1985-11-07—Публикация
1984-06-28—Подача