Изобретение относится к новым химическим соединениям, а именно диалкилди- циклогексил-18-краун-6, которые находят применение как экстрагенты в процессах извлечения и разделения металлов.
Целью изобретения является увеличение экстракционных свойств в ряду производных дициклогексил-18-краун-6.
Пример. I. Получение 4-изопропил- циклогексанола.
Смесь 27,2 г (0,2 моль) 4-изопропилфе- нола и 3 г промышленного сплавного Nt-AI- Ti-катализатора в 200 мл изопропилового спирта помещают в стальной автоклав на 0,5 л и гидрируют при 170°С при перемешивании и давлении 70 атм в течение 3 ч до поглощения 0,6 М водорода. После охлаждения катализатор отфильтровывают и отгоняют изопропиловый спирт. Остаток представляет собой жидкость, которая по данным ГЖХ является конечным продуктом с чистотой 99,5%. Получено 28,1 г4-изопро- пилциклогексанола, выход 98,4%; т.кип. Юб-ЮВ С/ЗО мм рт.ст. 1,4660, 0,922.
Аналогично каталитическим гидрированием соответствующего 4-алкилфенола получают 4-бутилциклогексанол, 4-изопен- тилциклогексанол, 4-гексилциклогексанол, 4-октилциклогексанол, 4-децилциклогекса- нол, 4-додецилциклогексанол.
II.Получение 4-изопропилциклогексе- на.
Смесь 27 г 4-изопропилциклогексанола и 15 мл 85%-ной фосфорной кислоты помещают в колбу, соединенную с нисходящим холодильником,, и создают в системе вакуум (ост. давление 30 мм рт.ст.). Смесь нагревают до кипения и выдерживают до прекращения отгонки воды и 4-изопропил- циклогексана. От полученного дистиллята отделяют нижний водный слой, верхний слой сушат надСаСЬ и перегоняют.
Получено 21,7 г 4-изопропилциклогек- сана, выход 92,1%,т.кип. 125-127°С, йодное число 203 (теор. 204,7).
Аналогично при дегидратации соответствующего 4-алкилциклогексанола получают 4-бутилциклогексен, 4-изопен- тилциклогексен, 4-гексилциклогексен, 4-ок- тилциклогексен, 4-децилциклогексен, 4-додецилциклогексен.
III.Получение 4-изопропилциклогексан- диола-1,2.
К 18.6 г4-изопропилциклогексена и при перемешивании и охлаждении медленно приливают смесь, состоящую из 18,8 г ледяной уксусной кислоты. 18,8 г 30%-ной Н202 и 2 г концентрированной серной кислоты. Скорость приливания регулируют так. чтобы
температура оставалась в пределах 20- 25°С. Затем смесь нагревают 3 ч при 45°С, после охлаждения нейтрализуют раствором гидроокиси натрия и экстрагируют продукт
реакции эфиром. Растворитель отгоняют, остаток перегоняют в вакууме.
Получено 14,8 г 4-изопропилциклогек- сандиола-1,2, выход 62,4%, т.кип. 104- 106°С/2 мм рт.ст.
0 Найдено,%: С 68,43: Н 11,39. CgHieOa.
Вычислено,%: С 68,31; Н 11,47. Анал огично при гидроксилировании соответствующего 4-алкилциклогексена пол5 учают 4-бутилциклогександиол-1,2;
4-изопентилциклогександиол-1.2; 4-гексилциклогександиол-1,2; 4-октилциклогександиол-1,2; 4-додецилциклогександиол-1,2.
Смесь 22,8 г 4-изопропилпирокатехина
0 и 2,5 г промышленного сплавного NI-AI-TI- катализатора в 200 мл изопропилового спирта помещают в 0,5 л стальной автоклав и гидрируют при 160°С при перемешивании и давлении 80 атм в течение 5 ч до поглоще5 ния 0,45 М водорода. После охлаждения катализатор отфильтровывают и отгоняют изопропиловый спирт. Остаток по данных ГЖХ представляет собой конечный продукт с чистотой 99,1%.
0 Получают 23,4 г 4-изопропилциклогек- сандиола-1,2, выход 97,8%. т.кип. 104- 106°С/2 мм рт.ст.
IV. Получение ди(2-оксиэтилового)-эфи- ра 4-изопропилциклогександиола-1,2.
5 Смесь 15,8 г 4-изопропилциклогексан- диола-1,2 32,2 г этиленхлоргидрина, 1,6 г 18-краун-6 и 100 мл 40%-ного водного раствора КОН при интенсивном перемешивании нагревают в закрытом сосуде при 40°С
0 в течение 8 ч. После охлаждения добавляют 130 мл воды для полного растворения осадка, органический слой отделяют, водную фазу экстрагируют два раза по 30 мл эфира. Органические растворы объединяют, про5 мывают 25 мл 3%-ного раствора соляной кислоты и три раза по 100 мл воды. Отгоняют эфир, остаток перегоняют в вакууме.
Получают 14,9 г ди(2-оксиэтилового) эфира 4-изопропилцклоге«диола-1,2 (1а),
0 выход 60,6%, т.кип. 131-133°С/0,1 мм рт.ст. Найдено,%: С 63,24; Н 10,71.
С1зН2б04
Вычислено,%: С 63,38; Н 10,64.
Аналогично при применении в качестве 5 катализатора дициклогексил-18-краун-6 (ДЦГ18К6), 2,3 г получен целевой продукт с выходом 65,3%.
Аналогично путем взаимодействия соответствующего 4-алкилциклогександиола- 1,2 с этиленхлоргидрином в присутствии
щелочи в условиях мбжфазмого катализа краун-эфирами получают ди(2-оксиэтило- вые) эфиры 4-6утилциклогександиола-1,2 (16), 4-изопентилциклогександиола-1,2 {1в), 4-гексилциклогександиола-1,2 (1г), 4-октил- циклогександиола-1,2 {1д), 4-децилциклр- гександиола-1,2 (1е), 4-додецилцикло- гександиола-1.2 (1ж),
V.Получение ди(2-хлорэтилового) эфира 4-изопропилциклогександиола-1,2 (II а).
Смесь 12.3 г ди(2-оксиэтилового) эфира 4-изопропилциклогександиола-1,2, 5U мл бензола и 8,7 г пиридина нагревают до кипения и прикапывают при перемешивании в течение 3 ч 13,1 мл хлористого тионила, затем кипятят смесь в течение 8 ч. После охлаждения прикапывают при перемешивании раствор .1,5 мл концентрированной соляной кислоты в 5 мл воды. Органический слой промывают водой и отгоняют бензол. Остаток представляет собой жидкость, которая является по данным ГЖХ конечным продуктом с чистотой 94,5%.
Получено 13,8 г ди(2-хлорэтилового) эфира 4-изопропилциклогександиола-1,2 (II а), выход 92,2%, содержание С123,6% (теор. 25,03%). Аналогично получают ди(2-хлорэ- тиловые) зфиры 4-бутилциклргександиола- 1,2 (II б), 4-пентилциклогександиола-1,2 (II в), 4-гексилциклогександиола-1,2 (II г), 4-ок- тилциклогександиола-1,2 (II д), 4-децилцик- логександиоЛа-1,2 (II е), 4-додецилцикло- гександиола-1,2 (II ж).:
VI.Получение диизопропилдициклогек- сил-18-краун-6.
Смесь 5,5 г соединения 1а, 6,8 г соединения II а, 0,4 г 18-краун-б и 25.мл 40%-ного водного раствора КОН нагревают при интенсивном перемешивании при 80°С в течение 7 ч. После охлаждения добавляют 40 мл воды для полного растворения осадка, органический слой отделяют, водную фазу экстрагируют два раза по 10 мл хлороформа. Органические растворы объединяют, промывают 10 мл 3%-ного раствора соляной кислоты и три раза по 50 мл водой. Отгоняют хлороформ, продукт реакции очищают колоночной хроматографией на окиси алюминия (элюент гексан-хлороформ-аце- тон 6:1:1).
Получено 5,5 г диизопропилдициклогек- сил-18-краун-6 (соединение I). выход 53,5%.
Найдено,%: С 68,25; Н 10.71.
С2бН480б
Вычислено,%: С 68,38; Н 10.59.
ИК-спектр; vc-o-c 1106 см отсутствуют валентные колебания гидроксильной группы в области 3650-3200 см
Аналогично при применении в качестве катализатора 0,6 г соединения I получено соединение I с выходом 59,6%.
Аналогично конденсацией соединения 5 (16) с соединением (Мб) получают дибутилди- циклгексил-18-краун-6 (соед.Н) с выходом 56,2% при применении в качестве катализатора соединения II.
Найдено, %; С 69,26,- Н 10.88.
0С28Н5206
Вычислено,%: С 69,38: Н 10.81.
ИК-спектр: Vc-o-o 1105 cм отсутствуют валентные колебания гидроксильной группы в области 3650-3200 см 5 Аналогично конденсацией соединения (М в) с соединением (II в) получают диамил- дициклогексил-18-краун-6 (соед. И д) с выходом 47,6% при применении в качестве катализатора 18-краун-6 и с выходом 55,5% 0 лри применении в качестве катализатора соединения (II).
Найдено,%: С 70,33: Н 11.08.
СзоНБбОа
Вычислено.%: С 70,27: Н 11,01. 5 ИК-спектр: vc-o-o 1108 см отсутствуют валентные колебания гидроксильной группы в области 3650-3200 см
Аналогично конденсацией соединения (I г) с соединением (11 г) получают дигексил- 0 дИциклогексил-18-краун-6 (соединения )с выходом 46,5% при применении в качестве катализатора 18-краун-6 и с выходом 54,9% при применении в качестве катализатора соединения IV. 5 Найдено,%: С 71,01: Н 11,28.
С21НбоОб
Вычислено,%: С71,07; Н 1,18.
ИК-спектр: vc-o-c 1107 см отсутствуют валентные колебания гидроксильной груп- 0 пы в области 3650-3200 см
Аналогично при конденсации соединения (I д) с соединением (Ид) получен диок- тилдициклогексил-18-краун-6 (соед.V) с выходом 51,2% при применении в качестве 5 катализатора соединения V.
Найдено,%: С 72,31; Н 11,40.
СзбНбвОб
Вычислено,%: с 72,44; Н 11,48.
ИК-спектр; vc-o-c 11,06 cм отсутству- 0 ют валентные колебания гидроксильной группы в области 3650-3200 см .
Аналогично конденсацией соединения
(I е) с соединением (II е) получают дидецилдициклогексил-18-краун-6 (соед. VI) с выхо5 дом 44,2% (катализатор 18-краун-6) и с
выходом 52,4% (катализатор соединения VI).
Найдено,%: С 73,49; Н 11,81.
С40Н7бОб
Вычислено,%: С 73,57; Н 11.73.
ИК-спектр: vc-o-c 1110 см отсутствуют валентные колебания гидроксильной группы в области 3650-3200 см . При конденсации соединения (I ж) с соединением (И ж) получен дидодецилдициклогбксил-18-Kpia- ун-6 (соед. VII) с выходом 46,4% (катализатор 18-краун-6) и с выходом 50,8% (катализатор соед. VII).
Найдено,%: С 74,73; Н 11,82.
СддНадОб
Вычислено.%: С 74,52; Н 11.94.
ИК-спектр: vc-o-c 1109 см отсутствуют валентные колебания ОН-группы в области 3650-3200 см
Экстракционные свойства диалкилди- циклогексил-18-краун-6 (соединения l-Vli).
Результаты сравнения зкстракцирниых свойств соединений l-Vll с дициклогексил- 18-краун-6 представлены в табл.1.
Из представленных табличных данных следует, что краун-эфиры с алкильными заместителями в циклогексильном кольце обладают более высокой экстракционной способностью по сравнению с Незамещенным дициклогексил-18-краун-6.
В табл.2 представлена зависимость распределения металлов от концентрации
Сопоставление экстракции катионов металлов из 1.5 М азотной кислоты 0,05 М растворами производных 18-1сраун-6 в хлороформе. Исходный водн«р1й раствор содержит по 0,01 М каждого из катионов
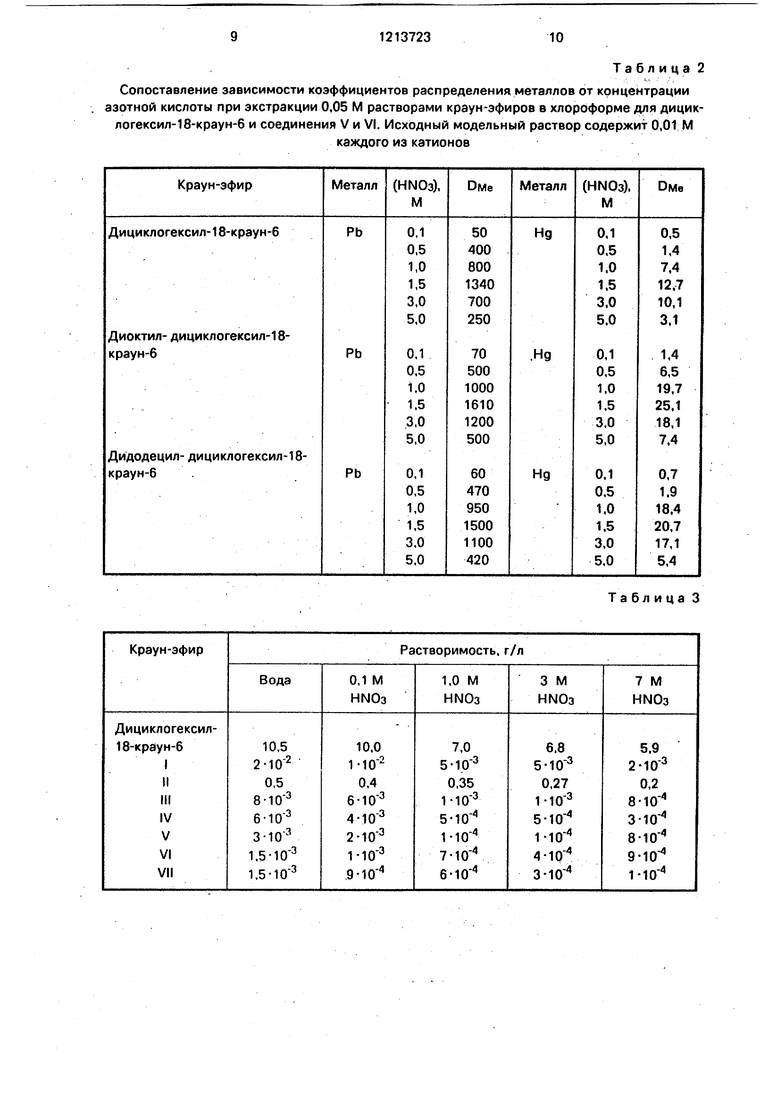
азотной кислоты при экстракции 0,05 М растворами краун-эфиров в хлороформе.
Таким образом, зависимости коэффициентов распределения от концентрации азотной кислоты носят экстремальный характер с максимумом экстракции при 1,5 М азотной кислоты.
В табЛ.З представлено сопоставление растворимости краун-эфиров в воде и растворах азотной кислоты различной концентрации.
Представленные в табл.3 данные свидетельствуют о том, что введение в циклогек- сильное кольцо алкильных радикалов с
длиной цепи от СзН до Ci2H25 вызывает снижение (более чем в 10000 раз) растворимости краун-зфиров в водных растворах по сравнению с дициклогексил-18-краун-6. Это означает, что потери экстрагентов в
процессах извлечения металлов снижаются с 10 кг на 1 м перерабатываемого раствора до 2-3 г/м. Это является преимуществом диалкилдициклогексил-18-краун-6 по сравнению с незамещенным аналогом
дициклогексил-18-краун-6.
(56) Авторское свидетельство СССР М: 931778, кл. С 22 В 26 Л О, 1981.
Таблица 1
Т а б л и ц а 2
Сопоставление зависимости коэффициентов распределения металлов от концентрации
азотной кислоты при экстракции 0,05 М растворами краун-эфиров в хлороформе для дициклогексил-18-краун-6 и соединения V и VI. Исходный модельный раствор содержит 0,01 М
каждого из катионов
Таблица 3
Формула иэрбретен ия
Диалкилдициклогексил-18-краун-б общей формулы
YV
Cui; I йвп I viin
Техред М;Моргентал
Корре
Тираж НПО Поиск Роспатента 113035, Москва, Ж-35. Раушская наб., 4/5
Подп
Производственно-издательский комбинат Патент, г. Ужгород, ул.Гагарина, 101
где R - изо-пропил, н-бутил, изо-пентил, н- гексил, н-октил, н-децил, н-додецил. как экстрагенты калия, ртути, железа, свинца, индия, таллия, галлия и стронция из растворов.
Корректор с. Патрушева
., 4/5
Подписное


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения диалкиловых эфиров полиэтиленгликолей | 1979 |
|
SU876635A1 |
| Способ получения 4-алкокси-2-оксифенонов | 1979 |
|
SU883000A1 |
| Способ получения макроциклических полиэфиров | 1981 |
|
SU996415A1 |
| Способ разделения цис-син-цис- и цис-анти-цис-изомеров дициклогексил-18-краун-6 | 1981 |
|
SU1014237A1 |
| Способ получения производных 2,5,8,15,18,21-гексаоксатрицикло/20,4,0,09,14/ гексакозана | 1981 |
|
SU981318A1 |
| Способ очистки краун-эфиров-производных краун-6 | 1982 |
|
SU1065415A1 |
| Способ получения ацетильных производных бензокраун-эфиров | 1987 |
|
SU1482919A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИС-1,2-ДИ-(АЛКИЛСЕЛЕНО)ЭТЕНОВ | 1991 |
|
SU1833615A3 |
| Способ получения высших нитроалканов | 1980 |
|
SU918291A1 |
| Способ получения макроциклического комплексообразователя, способного образовывать комплексы с щелочными и щелочноземельными металлами в среде органического растворителя | 1988 |
|
SU1689377A1 |
Диалкипдицикпогексип-18-краун-6 общей формулы, R где R изо-пропил н-бутиа изопентид н-гексид н-октия н-децид н-додецид как экарагенты капиа ртути, железа, свинца, индия, таллия, галлия и стронция из растворов.

Авторы
Даты
1993-12-30—Публикация
1984-01-02—Подача