I
Изобретение относится к способу получения новых бензофуранбензо-(в) тиофен- или нафталинкарбонозых 1сис- лот общей формулы.
где У, который присоединен к кольцу А, означает -СООН или
X - О, 5 или ,
Е, присоединен к атому углерода кольца В, означает водород, галоид, алкил С,-С4 или - 5 (С -С -алкил)i
К, который присоединен к атому углерода кольца В, означает
N N-CHr
или (3-пиридил)-Z ,
где Z - группа , СО или 5 , или их фармацевтически приемлемых солей, которые могут быть использованы в качестве терапевтических агентов, например, при лечении тромбоза, ише- мической болезни сердца, сердечных приступов, переходного ишенического приступа, мигрени, заболеваний периферических сосудов, сосудистых . , осложнений диабета, рака и эндокси- нового шока.
Цель изобретения - синтез новых соединений, обладающих ценными свойствами.
Получение новых соединений формул (1) иллюстрируется следующими примерами. Все температуры указаны в с.
Пример 1. 2-(1-имидaзoлил- мeтил)-3-мeтилбeнзo(в)тиoфeн-6-кapбo нoвaя кислота, (i) 6-бром-2-гидрок- симетил-3-метилбензоСв)тиофен
Раствор н-бутил-лития в гексане (13,2 мл 1,55 М раствора) добавляют каплями к перемешиваемому раствору 2,6-дибром-3-метилбензо(в)тиофена (6,60 г) в сухом эфире (150 мл) при 0°С в атмосфере сухого азота и смесь перемешивают при О С в течение 30 мин, Затем порциями добавляют параформалЬ дегид (0,71 г) и смесь перемешивают при О .С в течение 3 ч. Добавляют воду и разделяют слои. Эфирный слой промывают водой, сушат () и упаривают с получением масла, которое хроматографируют на силикагеле. Элюирование хлороформом дает вначале некоторое количество примесей, а затем чистый продукт. Упаривание
2172562
содержащих продукт фракций дает твердое вещество, которое перекристалли- зовывают из этилацетата/бензина (т.кип. 60-80 С) с получением 6-бром- 5 2-гидроксилметил-3-метилбензо(в)тио- фена (3,20 г), т.пл. 95-9б с.
Найдено, %: С 46,97; Н 3,49
С,„Н,Вг.05
Рассчитано, %: С 46,70, Н 3,53. 10 (ii)6-бpoм-2-xлopмeтил-3-мeтил- бeнзo(в)тиoфeн
Тионилхлорид (2,0 мл) добавляют каплями к перемешиваемому раствору 6-бром-2-гидроксиметил-3-метилбензо- (5 (в)тиофена (3,60 г) и пиридина (3 капли) в хлороформе (80 мл). Раствор перемешивают при комнатной температуре в течение 1 ч, затем . промывают водой, раствором бикарбона- 20 та натрия и сушат (). Упаривание растворителя дает количественный выход 6-бром-2-хлорметил-3-метилбен- зо(в)тиофена. Проба, перекристаллизованная из бензина (т.кип. 40-60 с), 25 имеет т.пл. 92-93.
Найдено, %: С 43,51 Н 3,00
C gHgBrCeS
Рассчитано, %: С 43,58, Н 2,92
(i i i )6-бром-2-(1-имидазолилме- 30 тш1)-3-метилбензо(в) тиофен
Обработка 6-бром-2-хлорметил-3- мeт шбeнзo(в)тиoфeнa имидазолом и бикарбонатом натрия по методике примера 4 (п)дает 6-бром-2-(1-ими- , дазолилметил)-3-метилбензо(в)тиофен. Т.пл. 138-139 (из этилацетата) бензина, т.пл. 60-80 .
Найдено, %: С 50,49, Н 3,57, N9,19
C,,,5
Рассчитано, %: С 50,82, Н 3,61, N 9,12
(11)2-(1-имидазолилметил)-3-ме- тилбензо(в)тиофен-6-карбонитрил
Смесь 6-бром-2-(1-имидазолилметил ) -3-метилбензо (в) тиофена (1,01 г) и цианида меди (I) (1,80 г) в N,М-диметилформамиде (20 мл) нагревают при кипении с обратным холодильником в течение 22 ч, а затем охлаждают и выливают в воду. Твердое вещество отфильтровывают, промывают водой, а затем суспендируют в смеси концентрированного водного
раствора аммиака (100 мл) и этилацетата (150 мл) и смесь перемешивают, пока не исчезнет твердое вещество, Отделяют органическийг слой, промыва312
ют водой, осушают () и упари- ; вают. Остаток перекристаллиэовывают из этилацетата/бензина (т,кип. 60- 80 С) с получением 2-( 1-имкдазолил- метил)-3-метилбензо(в)тиофен-6-кар- бонитрила (0,58), т.пл. 154-155°.
Найдено, %: С 66,04; Н 4,50; N 16,61
СнН.,5
Рассчитано, %: С 66,37, Н 4,38j N 16,59
(у)2-(1-имидазолилметил)-3-метил- бензо(в)тиофен 6-карбоновая кислота
Смесь 2-(1-имидазолилметил)-3- метилбензо(в)тиофен-карбонитрила (0,40 г), гидроокиси натрия (0,20 г) этанола (2 мл) и воды (20 мл) на- гревают при кипении с обратным холодильником в течение 24 ч. Раствор упаривают и остаток растворяют в воде и раствор подкисляют уксусной кислотой. Твердое вещество отфильтровывают и очищают повторным растворением в разбавленном растворе гидроокиси натрия, фильтрованием и под- кислением фильтрата уксусной кислотой. Твердое вещество отфильтровывают, промывают водой и сушат с получением 2-(1-имидазолилметил)-3-ме- тилбензо(в)-тиофен-6-карбоновой кислоты (0,35 г) т.пл. 254-255°.
Найдено, %: С 61,37 Н 4,60; К 10,19 . ,.,,5
Рассчитано, %: С 61,74; Н 4,44; - М 10,20
Пример 2. 3-метил-2-(3-пи- ридилметил/бензо(в)тиофен-6-карбоновая кислота (1)6-бром-3-метилбензо (в)тиен-2-ил-пирид-З-ил-кетон.
Раствор н-бутил-лития в гексане (16,3 мл 1,55 М раствора) добавляют к перемешиваемому раствору 2,6-ди- бром-3-метилбензотиофена (7,65 г) в сухом эфире (159 мл) при -70 в атмосфере сухого азота. Смесь перемешивают в течение 30 мин при -70°, после чего на протяжении 5 мин каплями добавляют 3-циано-пиридин (2,60 г) в сухом эфире (50 мл). Результирующую смесь перемешивают при -70° в течение 3 ч, а затем при комнатной температуре в течение еще 2 ч. Каплями добавляют при перемешивании концентрированную хлористоводородную кислоту (40 мл) и слои разделяют. Эфирный слой экстрагируют концентрированной хлористоводородной кислотой
6 S
(20 мл), кислотные экстракты комбинируют и подогревают для завершения гидролиза промежуточной кетиминовой соли. Раствор охлаждают и подщела- чивают раствором гидроокиси натрия. Смесь несколько раз экстрагируют этилацетатом и скомбинированные экстракты промывают водой и-осушают (). Отгонка растворителя дает
твердое вещество, которое хроматогра- фирует на силикагеле. Элюирование хлороформом бензином (т.кип. 40-60 (2:1) дает твердое вещество, которое перекристаллизовывают из этилацетата/бензина (т,кип.40-60 ) с получением 6-бром-3-метилбензо(в)тиен-2- ил -пирид-3-ил-кетона (4,70 г), т.пл. 110-Г11°.
Найдено, %: С 53,93, Н 3,17;
N 4,29
C,5H,
Рассчитано, %: С 54,22; Н 3,03; N 4,22
(()6-бром-З-метил-З-(3-пиридилметил)бензо(в)тиофен
Смесь 6-бром-3-метилбензо(в)тиен- 2-ил-пирид-З-ил-кетона (4,30 г) и гидразин-гидрата (2,60 г) в этилен- гликоле (30 мл) нагревают с обратным холодильником в течение 2 ч, а затем охлаждают. Добавляют гидроокись калия (2,80 г) и температуру постепенно повьшают до кипения с обратным холодильником. После нагревания с обратным холодильником в течение еще 3 ч раствор охлаждают и выливают в воду. Смесь несколько раз экстрагируют этилацетатом и комбинированные экстракты промывают водои и осушают (). Отгонка растворителя дает твердое вещество, которое хроматографируют на силикаге- ле. Элюирование хлороформом/бензи- ном (т.кип. 40-60 ) (3:1) дает 6бром-3-метил-2-(3-пиридилметил)бензо (в)тиофен (3,20 г). Проба, перекристаллизованная из бензина (т.кип. 40- 60°). имеет т.пл. 69-70°.
Найдено, %: С 56,65; Н 3,86; N 4,48.
С,бМ г 5.
Рассчитано, %: С 56,61, Н 3,80 N 4,40
(iii )3-метил-2-(3-пиридилметил) бензо(в)тиофен-6-карбоннтрил
Обработка 6-бром-3-метил-2-(3- пиридилметил)бензо(в)тиофен цианидом меди (1) в М ,N-диметилформамиде
по методике примера 1 (;у)дает 3- метил-2-(3-пиридилметил)-бензоен) тиофен-6-карбонитрила, т.пл. 115- 116 (из этилацетата/бензина, т,кип, 40-60°).
Найдено, %: С 72,66; Н 4,60; N 10,80
C,H,2N25
Рассчитано, %: С 82,59; Н 4,58; N 10,60
(1Y)З-метил-2-(3-пиридилметил) (бензо(в)тиофен-б-карбоновая кислота
Гидролиз 3-метил(2)3-пиридилме- тил/бензо(в)тиофен-6-карбонитрила по методике примера 1 (v) дает 3- метил-2-(3 пиридилметил)бензо(в) тиофен-6 карбоновую кислоту, т.пл. 248-249°. .
Найдено, %: С 68,12; Н 4,63; N 4,96
C,H,,NO,
Рассчитано, %: С 67,82; Н 4,6г2; N 4,94
Пример 3. 2-метил-2-(3-пиридилметил) бензо (в) тиофен-5-карбо- новая кислота.
(i)2,5-дибром-3-метилбензо(в)тио фен
Раствор брома (3,20 г)- в хлороформе (10 мл) добавляют каплями к перемешиваемому раствору 5-бром-З- метилбензо(в)тиофена (4,54 г) в хлороформе (40 мл) и раствор перемешивают при комнатной температуре в течение 1,5 ч. Затем его промываю разбавленным раствором гидроокиси натрия, водой и осушают (. Отгонка растворителя дает твердое вещество, которое перекристаллизо- вывают из бензина (т.кип, 80-100 ) с получением 2,5-дибром-З-метилбен- зо(в)тиофена (5,45 г), т.пл. 118- 122°
Найдено, %: С 35,53 Н 1,91
Рассчитано, %: С 35,32; Н 1,98
(ii)5-бром-3-метилбензо(в)тиен- 2 ил-пирид-3-ил-кетон
Последовательная обработка 2,5- дибром-3-метилбензо(в)тиофена н-бу- тил-литием и 3-цианопиридином по методике примера 2 (Одает 5 бром-3- метилбензо(в)тиен-2-ил-пирид-3-ил- кетон, характеризуемый в виде хлористоводородной соли, т.пл, 193- 195°.
Найдено,%: С 48,50; Н 3,00; N 3,94
C,5H| Br -tt55HCe
5 .Рассчитано, %: С 48,86; Н 3,01; N 3,80
(til) 5-бром-3-метил-2-(3-пиридилметил) бензо(в)тиофен
Последовательная обработка 5-бром- 0 метилбензо(в)тиен-2-ил-пирид-3-ил- кетон гидразин-гидратом и гидроокисью калия в этиленгликоле по методике примера 2 (J}-) дает 5-бром-З-метил- 2-(3-пиридилметил )бен зо (в )тиофен, 5 характеризуемый в виде хлористоводородной соли, т.пл. 201-203 .
Найдено, %: С 60,89; Н 3,46; N 4,23
Ci H Bt /fSHCE
0 Рассчитано, %: С 50,79, Н 3,69; N 3,95
(у) З-метил-2-(З-пиридилметил) Сензо(в)тиофен-5-карбонитрил
Обработка 5-бром-3-метил-2-(З-пири- 5 дилметил)бензо(в)тиофена цианидом меди (1) в N,М ДИметилформамиде по методике примера 1(п)дает З-метил-2- (3-пиридилметил)бензо(в)тиофен-5-кар- бонитрил, т.пл. 149-152° из этилаце- 0 тата/бензина, т.кип. 60-80 .
Найдено, %: С 72,56-, Н 4,52; М 10,61
C,,H,,N,5
Рассчитано, %: С 72,69; Н 4,58; 5 N 10,60 .
(v) З-метил-2-(3-пиридилметил)бен- зо(в)тиофен-5-карбоновая кислота
Гидролиз З-метил-2-(3-пиридилметил) бензо (в) тиофен-5-карбонитрила по методике примера 1 (V ) дает 3-ме- тил-2-(3-пиридилметил)бензо(в)тио- фен-5-карбоно5вую кислоту, т.пл. 230- 232°.
Найдено, %: С 67,69; Н 4,62; 5 N 4,90
C,Hj, NOjS
Рассчитано, %: С 67,82, Н 4,62; N 4,94
Пример 4. 2-(3-пиридилметил) бензо(в)тиофен-5-карбоновая кислота
(i)5-бромбензо(в)тиен-2-ил-пирид- 3-ил-кетон
Раствор н-бутиллития в гексане (25,8 мл 1,55 М раствора) добавляют каплями к перемешиваемому раствору З-бромбензо(в) тиофена (8,50 г) в сухом эфире (120 мл) при -20 в атмосфере азота и смесь перемешивают при
5
0 в течение 30 мин. Обработка результирующего соединения лития 3-циа нопиридином (4,50 г) при -70 по методике примера 2 (Одает 5-бромбен- зо(в)тиен-2-ил-пирид-3-Ш1-кетон (4,73 г) т.пл. 147-148 (из этилаце- тата) бензина, т.кип. 60-80°.
Найдено, %: С 53,07, Н 2,55, N4,49
C HjBrNOS
Рассчитано, %: С 52,84; Н 2,53; N 4,40
(i)5-бром-2-(3-пиридилметил)бен зо(в)тиофен
Последовательная обработка 5-бро бензо(в)тиен-2-ил-пирид-3-ил кетона гидразин-гидратом.и гидроокисью калия в зтиленгликоле по методике примера 2 (п) дает 5-бром-2-(3-пи- ридилметил) бензо(в)тиофен, т.пл. 102-103 (из этилацетата/бен- зина, т.кип. 60-80°).
Найдено, %: С 55,61; Н 3.25; N 4,75
,BrNS .
.Рассчитано, %: С 55,27; Н 3,31; К 4,60
(ii i) 2-(3-пиридилметил)бензо(в) тиофен-5-карбонитрил30
Обработка 5-бром-2-(3-пиридилме- тил)бензо(в)тиофена цианидом меди (р Б fi ,М-диметилформамиде по методике примера 1 (iv) дает 2-(3-пи- ридилметил)бензо(в)тиофен-5-карбо- 35 нитрил, т.пл. 59-62 .
Найдено, %: С 71,54; Н 3,99; К 10,65
Рассчитано, %: С 71,97; Н 4,03; 40 N11,19%
(iv) 2-(3-пиридилметил)бензо(в) тиофен-5-карбоновая кислота
Гидролиз 2-(3-пиридилметил)бен- зо(в)тиофен-5-карбонитрила по мето- 45 дике примера 1 (v) дает 2-(3-пири- дилметил)бензо(в)тиофен-5-карбоновую кислоту, т.пл. 246-249°(из этанола).
Найдено, %: С 66,84j Н 4,24; N5,13 50
C,,H,
Рассчитано, %: С 66,89, Н 4,12; К 5,20
Пример 5. 3-метил-2-(3-пиРаствор н-бутиллития в гексане (10,3 мл 1,55 М раствора) добавляют каплями к перемешиваемому раствору 2 J 5-дибром-З-метилбензо(в)тиофена (продукт примера 3 (ч) (4,90 г) в сухом эфире (175 мл) при О в атмосфере азота. Смесь перемешивают при О в течение 30 мин, а затем охлаждают до -70 . На протяжении 3 мин при перемешивании добавляют раствор 3,3-дипиридил-дисульфида (3,50 г) в сухом эфире (25 мл). Охлаждающую ванну удаляют и смеси дают возможность, прогреваться до комнатной температуры при перемешивании. Затем добавляют избыток воды и разделяют слои. Водный слой несколько раз экстрагируют эфиром и комбинированны органический слой и экстракты промывают водой и осушают (,). Отгон ка растворителя дает масло, которое хроматографируют на силикагеле. Элю- ирование толуолом дает вначале некоторое количество примесей, а затем чистый продукт. Упаривание со- держаш 1х продукт фракций дает 5- бром-3-метил-2-(3-пиридилтио)-бензо (в) тиофен (1,80 г), достаточно чис тый для последующей реакции. Перекри таллизованная из бензина (т.кип.40- 60 ) проба имеет т.кип. 86-87 .
Найдено, %: С 49,96; Н 2,92; N 4,03 С H,,5
Рассчитано, %: С 50,01; Н 3,00, N 4,17
(i|) 3-метил-2-(3-пиридилтио)бензо (в) тиофен-5-карбонитрил
Обработка 5-бром-3-метил-2-(3-пи- ридилтио)бензо(в)тиофена цианидом меди (1) в N ,N-диметилформамиде по методике примера 1 d v) дает 3-метил 2-(3-пиридилтил)бензо(в)тиофен-5- карбонитрил, т.пл. 125-128 (из МеОН/Н О).
Найдено, %: С 63,72; Н 3,71; N 9,64
Ci HioNzSa
Рассчитано, %: С 63,80; Н 3,57;
N 9,92
() 3-метил-2-(3-пиридилтио) бензо(в)тиофен-5-карбоновая кислота.
Гидролиз 3-метил-3-(2-пиридилтио)
- x J-ibi i JTi JJU/Jll J -J-ЭТС 1 fiJl- J- .llrlJ J J,rlJl 1 rHJ
римедилметил)бензо(в)тиофен-5-карбо- бензо(в)тиофен-5-карбонитрила по меновая кислота.
(О 5-бром-3-метил-2-(3)-пиридил- тио)бензо(в)тиофен
тодике примера 1 (v) дает З-метил-2- (3-пиридилтио)бензо(в)тиофен-5-кар- боновую кислоту, т.пл. 220-222 .
5
0
5
0
5
0
Раствор н-бутиллития в гексане (10,3 мл 1,55 М раствора) добавляют каплями к перемешиваемому раствору 2 J 5-дибром-З-метилбензо(в)тиофена (продукт примера 3 (ч) (4,90 г) в сухом эфире (175 мл) при О в атмосфере азота. Смесь перемешивают при О в течение 30 мин, а затем охлаждают до -70 . На протяжении 3 мин при перемешивании добавляют раствор 3,3-дипиридил-дисульфида (3,50 г) в сухом эфире (25 мл). Охлаждающую ванну удаляют и смеси дают возможность, прогреваться до комнатной температуры при перемешивании. Затем добавляют избыток воды и разделяют слои. Водный слой несколько раз экстрагируют эфиром и комбинированные органический слой и экстракты промывают водой и осушают (,). Отгонка растворителя дает масло, которое хроматографируют на силикагеле. Элю- ирование толуолом дает вначале некоторое количество примесей, а затем чистый продукт. Упаривание со- держаш 1х продукт фракций дает 5- бром-3-метил-2-(3-пиридилтио)-бензо (в) тиофен (1,80 г), достаточно чистый для последующей реакции. Перекристаллизованная из бензина (т.кип.40- 60 ) проба имеет т.кип. 86-87 .
Найдено, %: С 49,96; Н 2,92; N 4,03 С H,,5
Рассчитано, %: С 50,01; Н 3,00, N 4,17
(i|) 3-метил-2-(3-пиридилтио)бензо (в) тиофен-5-карбонитрил
Обработка 5-бром-3-метил-2-(3-пи- ридилтио)бензо(в)тиофена цианидом меди (1) в N ,N-диметилформамиде по методике примера 1 d v) дает 3-метил- 2-(3-пиридилтил)бензо(в)тиофен-5- карбонитрил, т.пл. 125-128 (из МеОН/Н О).
Найдено, %: С 63,72; Н 3,71; N 9,64
Ci HioNzSa
Рассчитано, %: С 63,80; Н 3,57;
N 9,92
() 3-метил-2-(3-пиридилтио) бензо(в)тиофен-5-карбоновая кислота.
Гидролиз 3-метил-3-(2-пиридилтио)
i JTi JJU/Jll J -J-ЭТС 1 fiJl- J- .llrlJ J J,rlJl 1 rHJ
бензо(в)тиофен-5-карбонитрила по мебензо(в)тиофен-5-карбонитрила по методике примера 1 (v) дает З-метил-2- (3-пиридилтио)бензо(в)тиофен-5-кар- боновую кислоту, т.пл. 220-222 .
Найдено, %: С 59,94; Н 3,83- N 4,80,
С,
Рассчитано, %: С 59,78, Н 3,68; N 4,65
Пример 6, 3-метил-2-(3-пи ридилметил)бензо(в)тиофен-5-карбоксиМИД.
Перекись водорода {1,6 мл 30 вес./об.% раствора) добавляют к перемешиваемому раствору 3-метил- 2-(3-пиридилметил)бензо-тиофен-5- карбонитрила (продукт примера 5 (/и) 0,30 г в этаноле (3,5 мл) с последу- (ощим добавлением 6 и.раствора гидро- окиси натрия (1,6 мл). Результирующу смесь нагревают при 50-55° с перемешванием в течение 2 ч, затем охлаждают и выпивают в воду. Твердое вещество отфильтровывают, промывают водой, и перекристаплизовывают из этанола/воды с получением 3-метил- 2-(3-пиридилметил)бензо(в)тиофен- 5-карбоксимида Э (-0,21 г), т.пл. 194-195
Найдено, %: С 67,91 Н 5,04, 9,66
Рассчитано, /;: С 68,Об , Н 5,00; 9,22.
Пример 7. 3-метил-2-(3-пири дилметил)бензофуран-5-карбоновая кислота (1) 5-бром-З-ме тилбензофуран- 2-ил пирид-3-ил кетона гидрохлорид.
Смесь 3-бромацетилпиридина гидробромида (1,50 г) и тонкопомолотого безводного карбоната калия (2,20 г) добавляют к перемешиваемому раствору 5-бром-2-гидроксиацетофенона (1,10 г) в сухом ацетоне (50 мл) при 5 . Смесь перемешивают при 5° в течение 30 мин, а затем при комнатной температуре в течение 24 ч. Ее затем фильтруют и твердое вещество промывают ацетоном. Комбинированные фильт- рат и смывка упаривают и остаток несколько раз экстрагируют эфиром. Комбинированные эфирные экстракты фильтруют и добавляют избыток эфирного хлористого водорода. Твердое вещество отфильтровывают, промывают эфиром и сушат с получением 4-5-бромЗ-метилбензофуран-2-ил пирид 3-ил кетона гидрохлорида (1,07 г), т,пл.193- 197°.
5
О 5 ,
0
5
5
0
Найдено, %: С 50,99; Н 3,09; N 4,22
C,H.BhNO,HCCI
. Рассчитано, %: С 51,09; Н 3,15; К 3,97
( rl-) 5-бром-3-метил-2-(3-пиридилметил )бензофуран
Смесь 5-бром-З-метилбензофуран- 2-ил пирид-3-ил-кетона в виде свободного основания (2,67 г) и гидразин- гидрата (1,80 г) в этиленгликоле (30 мл) нагревают при 120 в течение 2,5 ч. Смесь охлаждают, добавляют гидроокись калия (1,80 г) темпера- .туру повышают до 120 вновь, сохраняя ее на этом уровне в течение 1 ч. Разбавление водой и экстрагирование эфиром дает масло, которое хромато- графируют на силикагеле. Элюирование хлороформом дает твердое вещество, которое перекристаллизовывают из бен- зина (т.кип. 80-100°) с получением 6-бром-3-метил-2-(3-пиридилметил) бензофурана (2,00 г), т.пл. 57-58 .
Найдено, %: С 59,81;. Н 4,0lj N 4,74: 1.
С
Рассчитано, %: С 59,62, Н 4,00, К 4,64
( i) ; ) 3-метил-2-(3-пиридилметил) бензофуран-5-карбонитрил
Обработка 5-бром-3-метил-2-(3-пири. дилметил)бензофурана цианидом меди(1) по методике примера 1 («v) дает 3- метил-2-(3-пиридилметил)бензофуран- 5-карбонитрил, который непосредственно используют на следующей ста- ,дии. .
Точное измерение массы: найдено 248,0960,- рассчитано 248,09489.
(tv) З-метил-2-(3-пиридилметил) бензофуран-5-карбоновая кислота
Гидролиз 3-метш1-2-(3-пиридилметил) бензофуран-5-карбонитрила по методике примера 1 (у) даёт Д,-метил-2- (3-пиридилметш1)бензофуран-5-карбо- новую кислоту, т.пл. 219-221,
Найдено, %: С 71,б1; Н 4,65; N 5,12
C,gH,jN03
Рассчитано, %: С 71,90; Н 4,90; N 5,24
Пример 8. 3-хлор-2-(1-ими- дазолилметил)бензофуран-5-карбоно- вая кислота (i) З-хлор-2-метилбензо- фуран-5-карбонитрил,
Раствор 2-метилбензофуран-5-кар- бонитрила (1,52 г) и сульфурилхлори- да (1,49 г) в хлороформе (25 мл) нагревают при кипении с обратным хо- лодильником в течение 9 ч, затем охлаждают. Раствор последовательно промывают водой, разбавленным раствором гидроокиси натрия, водой, а затем осушают (). Упаривание растворителя дает твердое вещество, которое дважды перекристаллизовы- вают из метанола с получением 3-хлор 2-метилбензофуран-5-карбонитрила (0,45 г), т.пл. 131,5-133,5°.
Найдено, %: С 62,82; Н 3,17-, N 7,34
C gHgCeNO
Рассчитано, %: С 62,68; Н 3,16; N 7,31
( ii) 2-бромметил-З-хлорфензофуран 5-карбонитрил
Обработка З-хлор-2-метилбензофу- ран-5-карбонитрила-бромсукцинимидом и азобисизобутиронитрилом в четырех- хлористом углероде по методике примера 3( I i; ) да ет 2-бромметил-З-хлор- бензофуран-5-карбонитрИиП, т.пл. 124- 127 (из этилацетата/бензина, т.кип, 80-ЮО)..
Найдено, %: С 44,71; Н 1,94; N 5,49
qoN SrCeNO
Рассчитано, %: С 44,40; Н 1,86; N 5,18
(iJi ) 3-хлор-2-(1-имидазолилметил бензофуран-5-карбонитрил
Обработка 2-бромметил-3-хлорбензо фуран-5-карбонитрила имидазолом и бикарбонатом натрия по методике приме- pa 4 (лу) дает. 3-хлор-2-( 1-имидазо- лилметил(бензофуран-5-карбонитрил, т.пл, 231-233°(из этилацетата/бензина, т.кип. 60-80 ),
Найдено, %: С 60,65; Н 3,11; N 16,42
С H,3CEN,0
Рассчитано, %:.С 60,59; Н 3,13; N 16.31.
( iv ) 3-хлор-2-(1-имидазолилметш1 бензофуран-5-карбоновая кислота
Раствор 3-хлор-2-(1-имидазолилметил) бензофуран-5-карбонитрила (0,35 г) в концентрированной серной кислоте (5 мл) и воде (5 мл) нагре- вают при кипении с обратным холодильником в течение 1 ч, а затем охлаждают. Раствор разбавляют 5 мл воды и
подщелачивают добавлением 5 н.раствором гидроокиси натрия. Раствор фильтруют и подкисляют добавлением уксусной кислоты. Твердое вещество, выкристаллизовывающееся при стоянии, отфильтровывают 5 промывают водой и сушат с получением 3-хлор-.2-( 1-ими- дазолилметйл)бензофуран-5-карбоновой кислоты (0,20 г), т.пл. 248-250 .
НаГщено, %: С 56,27 Н 3,35; N 10,24
C H CENjOj
Рассчитано, %: С 56,43; Н 3,28; N 10,13
Пример 9. 3-бром-2-(1-имидазолилметил) бензофуран-5-карбоновая кислота
( 1 ) 3-бром-2-метилбензофуран-5- карбонитрил
Бром (3,20 г) каплями добавляют к перемешиваемой смеси 2-метилбензо- фуран-5-карбонитрила (3,04 г) и безводного ацетата натрия (2,0 г) в уксусной кислоте (30 мл), и смесь перемешивают при комнатной температуре в течение 1 ч, а затем выпивают в воду (около 200 мл). Смесь несколько раз экстрагируют хлороформом и скомбинированные экстракты промывают последовательно водой, разбав- |Ленным раствором гидроокиси натрия, водой и осушают (). Отгонка растворителя дает резино- подобное твердое вещество, которое растирают с несколькими миллилитрами метанола и фильтруют. Твердое вещество промывают небольшим количеством метанола и сушат с получением 3-бром 3-метилбензофуран-5-карбонитрила (3,44 г), т.пл. 163-165 , повышающаяся до 164-166° после перекристаллизации из изопропанола/бензина (т.кип. 60-80°).
Найдено, %: С 50,98; Н 2,62; N 6,09
С, N О
Рассчитано, %: С 50,87 Н 2,56, N 5,93
( ч ) З-бром-2-бромметштбензофу- ран-5-карбонитрил
Обработка З-бром-2-метилбензофу- ран-5-карбонитрила - бромсукцинимидом и азобисбутиронитрилом в четыреххлористом углероде по методике примера 3 ( ( м ) дает З-бром-2-броммвтил- бензофуран-5-карбонитрил, т.пл.129- 131 (из этилацетата)бензина, т.кип. 80-100.
Найдено %: С 38,31; Н 1,57; К А,60
С,Н
Рассчитано, %: С 38,13; Н 1,60; К 4,45
(((О 3-бром-2-(1гимидазолил- метил)бензофуран-5-карбонитрил
Обработка З-бром-2-бромметилбензо фуран-5-карбонитрила имидазолом и бикарбонатом натрия по методике примера. 4 (ду) дает 3-бром-2-(1-имида- золилметил)бензофуран-5-карбонитрил, т,пл. 119-122 (из этилацетата/бен- зина, т.кип. 80-100 ).
Найдено, %: С 51,59; Н 2,69; N 14,09.
C,HgBr N ,0
Рассчитано, %: С 51,68; Н 2,67; N 13,91
( IV ) 3-бром-2-(1-имидазолилме- тил)бензофуран -5-карбоновая кислота
Обработка 3-бром-2-(1-имидазолил- метил)бензофуран-5-карбонитрила серной кислотой / водой (I) по методике примера 8 ( Iv) дает 3-бром-2-(1-ими- дазолилметил)бензофуран-5-карбоно- вую кислоту, т.пл. 249-251 .
Найдено, %: С 48,58; Н 2,80 М 8,72
C,,H,,BrN20,
Рассчитано, %: С 48,61; Н 2,83; N .8,72
Пример 10. 1-метил-2-(3-пи- ридилметил)нафталин-7-карбоновая кислота.
( 1 ) 7-бром-2-(3-пиридилметилен)- 1-твтралон
Смесь 7-бром-1-тетралон(11,25 г), пиридин-3-карбоксальдегида(5,35 г), уксусной кислоты (5 мл) и пиперидина (6 мл) нагревают на паровой бане 6 ч, а затем оставляют стоять 18 ч. Отгоняют летучий материал.и остаток растворяют в этилацетате. Раствор несколько раз экстрагируют разбавленной соляной кислотой и комбинированные экстракты подщелачивают разбавленным раствором гидроокиси натрия. Твердое вещество отфильтровывают, промывают водой и перекристаллизовы- вают из метанола с получением 7-бром 2-(3-пиридилметилен)-1-тетралона (12,8 г), т.пл. 124-125.
Найдено, %: С 60,87; Н 3,86 N 4,46
C,(.H|jBhN О
Рассчитано, %: С 61,16; Н 3,85,- N 4,46
( ) 6-бром-2-(3-пиридилметил)-1- 5 те.тралон
Раствор 7-бром-2-(3-пиридилметилен) 1 -тетралона (13,9 г) в этаноле (150 мл), содержащий 5%-ный палладий на угле (0,50 г), гидрогенизуют при
10 25° и давлении 4 атм до отбора теоретического количества водорода. Катализатор отфильтровывают и фильтрат упаривают. Остаток дистиллируют с получением масла (12,0 г), т.кип.20015 240 при 1,0 мм рт.ст., содержащего около 40% дебромированного материала. Продукт очищают .жидкостной хроматографией под высоким давлением, используя колонку с силикагелем и
20 смесь гексан/этилацетат (45:55) в, качестве элюента. Вначале элюируют дебромированный Продукт, а затем чистый 7-бром-2-(3-пиридилметил)-1- тетралон, т.пл. 63-67 .
25 ( lii ) 7-бром-1-гидрокси-1-метил- 2-(3-пиридилметил)-1,2,3,4-тетрагид-, ронафталин
Метилмагнийбромид (15 мл ЗМ раствора в эфире) добавляют каплями на
30 протяжении 5 мин к перемешиваемому раствору 6-бром-2-(3-пиридилметил)- 1-тетралона (3,20 г) в сухом тетра- гидрофуране (50 мл). Результирующую смесь нагревают с обратным холодиль5 НИКОМ при перемешивании в течение 10 ч, затем охлаждают. Добавляют избыток водного раствора хлористого аммония и смесь несколько раз экстрагируют эфиром. Комбинированные эфир0 ные экстракты осушают () и упаг ривают. Остаток хроматографируют на силикагеле. Элюирование хлороформом дает 7-бром-1-гидрокси-1-метил- 2-(3-пиридйлметил)-1,2,3,4-тетрагидро5 нафталин (2,87 г) в виде смеси изомеров, которую непосредственно используют на следующей стадии.
( t v) 7-бром-1-метил-2-(3-пиридилметил ) нафталин
0 7-бром-1-гидрокси-1-метш:-2-(3пиридилметил)-1,2,3,4-тетрагидронафта- лин (2,87 г) растворяют в муравьиной кислоте (30 мл) и раствор оставляют стоять при в течение 6ч, после
5 чего упаривают при 35 . Остаток растворяют в этилацетате и раствор промывают раствором бикарбоната натрия, водой и осушают (). Упаривание
растворителя дает масло, которое хро- матографируют на силикагеле, Элюиро- вание хлороформом дает дегидратированный продукт в виде масла (2,11 г).
Смесь масла (2,00 г) и серы (0,35 г) нагревают при 200 в течение 2 ч, затем охлаждают. Остаток отбирают в нескольких миллилитрах этилацетата и смесь фильтруют. Фильтрат упаривают и остаток хроматогра- фируют на силикагеле. Элюирование хлороформом дает вначале некоторые примеси, а затем чистьй продукт. Упаривание содержащих продукт фракций дает твердое вещество, которое пере- кристаллизовывают из бензина (т.кип. 80-100 ) с получением 7-бром- 1-метш1-2-(3-пиридилметил)нафталина (1,42 г), т.пл. I0l-t04°.
Найдено, %: С 65,52; Н 4,60; N 4,42
С,Н|,ВгМ
Рассчитано, %: С 65,40; Н 4,52; N4,49
(V) 1-метил-2-(3-пиридилметил) нафталин-7-карбонитрил
Обработка 7-бром-1-метил-2-(3- пиридилметил)нафталина цианидом меди (1) по методике примера 1 (v) дает 1-метил-2-(3-пиридилметил)на- фталин-7-карбонитрил, т.пл. 110-112 (из бензина, т.кип. 80-100 ).
Найдено, %: С 84,05; Н 5,56; N 10,93
N
Рассчитано, %: С 83,69; Н 5,46; М 10,84
(:V( ) 1-метил-2-(3-пиридилметил) ;нафталин-7-карбоновая кислота
Гидролиз 1-метил-2-(3-пиридилме- тил)нафталин-7-карбонитрила по методике примера 1 () дает 1-метш1-2- (3-пиpидилмeтил)нaфтaлин-7-кapбoнo- вyю кислоту, т.пл. 210-211 .
Найдено,.%: С 77,95; Н 5,47; N 5,38.
C|aH|5 N Oj .
Рассчитано, % С 77,96, Н 5,45; N 5,05
Пример 11. 3-хлор-2-(1-ими- дазолилметил)бензо(в)тиофен-6-кар- боновая кислота.
(л) Хлорангидрид 6-бром-З-хлор- бензо(в)тиофен-2-карбоновой кислоты
Смесь пара-бромкоричной кислоты (49,95 г), тионилхлор1ща(79,80 мл), пиридина (1,77 мл) и хлорбензола
(220 мл) нагревают с обратным холодильником в течение 72 ч, затем охлаждают и фильтруют. Фильтрат упарива- 5 ют и остаток растирают с бензином. Твердое вещество отфильтровывают и перекристаллизовывают из толуола/бензина с получением хлорангид- рида 6-бром-3-хлорбензо(в)тиофен0 2-карбоновой кислоты (26,6 г), т.пл. 126-127°.
Найдено, %: С 35,00; Н 1,15
C H Br-CE OS Рассчитано, %: С 34,87; Н 0,98
5 (ч) 6-бром-3-хлор-2- гидроксиме- тилбензо(в)тиофен
Раствор хлорангидрида 6-бром- 3-хлорбензо(в)тиофен-2-карбоновой кислоты (6,20 г) в сухом эфире
0 (50 мл) и сухом тетрагидрофуране (50 мл) каплями добавляют к перемешиваемой суспензии литий-алюминий- гидрида (0,58 г) в сухом эфире (250 мл) при О в атмосфере сухого
5 азота. Смесь перемешивают при комнат- ной температуре 30 мин, а затем при кипении с обратным холодильником в течение 2,5 ч до охлаждения и оставляют стоять 18 ч. Затем охлажда0 ют и избыток литий-алюминий-гидрида разлагают осторожным добавлением воды (1,0 мм), затем 5 н. гидроокиси натрия (1,0 мл), воды (2,0 мл) при интенсивном перемешивании. Смесь фильтруют и фильтрат упаривают с получением твердого вещества, которое хроматографируют на силикагеле. Элюирование хлороформом вначале дает некоторое количество примесей,
- а затем чистый продукт. Содержащие продукты фракции комбинируют и упаривают с получением твердого вещества, которое перекристаллизовывают из хлороформа с получением 6-бром- 3-хлор-2-гидроксиметилбензо(в)тио- фена (2,22 г), т.пл. 117-118°.
Найдено, %: С 39,03; Н 2,18
c,HgBr сео5
Рассчитано, %: С 38,94} Н 2,19. ( |1() 6-бром-3-хлор-2-хлорметил- - бензо(в)тиофен.
5
5
0
Обработка 6-бром-3-хлор-2-гидрок- симетил-бензо(Б)тиофена тионилхло- РИДОМ и, пиридином по методике примера 1 (i i) дает 6-бром-3-хлор-2-хлор- метилбензо(в)тиофен, т.пл.95-9б (из бензина, т.кип. 40-60).
Найдено, %: С 36,12; Н 1,66 .,5
Рассчитано, %: С 36,52; Н 1,70.
(iv) 6-бром-3-хлор-2-(1-имида- золилметил)бензо(в)тиофен
Обработка 6-бром-3-хлор-2-хлор- метилбензо(в)тиофена имидазолом и бикарбонатом натрия по методике примера 4 (iv), указанной в Евро- пейской заявке, дает 6-бром-З-хлор- 2(1-имидазолилметил)бензо(в)тиофен, т.пл. 123-124 (из этилацетата/бен- зина).
Найдено, %: С 43,99; Н 2,46; IN 8,55
BrCeNS
Рассчитано, %: С 44,18; Н 2,47; N 8,72.
( V) 3-хлор-2-(1-имидазолилме- тил) (в)тиофен-6-карбонитрил
Обработка 6-бром-3-хлор-2-(1-имидазолилметил )бензо-тиофена цианидом меди (I) по методике примера 1 (fl v) дает 3-хлор-2-(1-имидазолилметил) беизо(в)тиофен-6-карбонитрил, т.пл. 158-159°.
Найдено, %: С 56,63; Н 2,97; N 15,03
C,HgCfN,5Рассчитано, %: С 57,04; Н 2,95; N 15,35
( vi ) 3-хлор-2-(1-имидазолилметил бензо(в)тиофен-6-карбоновая кислота
Гидролиз 3-хлор-2-(1-имидазолил) бензо(в)тиофен-6-карбонитрила по методике примера 8 (iv) .дает 3-хлор 2-(1-имидазолилметил)бензо(в)тиофен 6-карбоновую кислоту, т.пл, 256-257
Найдено, %: С 53,24; Н 3,15;- tJ 9,70
Рассчитано, %: С 53,33; Н 3,10; N 9,57
Пример 12. 2-(3-пиридил- 1метил)бензофуран-5-карбоновая кисло iTa.
I (i) 5-бромбензофуран-2-ил пирид- 3-ил кетон
Смесь 5-бромсалицилальдегида (17,7 г), 3-бромацетилпиридина гидробромида (25,3 г) и безводного карбоната калия (60:8 г), в 2-бутано- не (200 мл) нагревают с обратным холодильником при перемепивании в течение 5 ч. Смесь фильтруют и твердое вещество промьшают 2-бутаноном. Комбинированные фильтрат и смывки
упаривают и остаток перекристалли- зовывают из метанола с «получением 5-бром-бензофуран-2-ил пирил-3-ил- кетона (19,2 г), т.пл. 144-145 .
Найдено, %: С 55,56; И 2,79; N 4,72
С| Н ВгНОг
Рассчитано, %: С 56,65, Н 2,67; N 4,63
(ii) 5-бром-3-(3-пиридилметил) бензофуран
Восстановление 5-бромиберзофуран 2-ил пирид-3- ил кетойа по методике примера 7 (/(г) дает 5-бром-2-(3-пи- ридметил)бензофуран, т.пл. 72-74 (из бензина, т.кип. 60-80).
Найдено, %: С 58,01; Н 3,51; N 5,09
C,,H,BrNO
Рассчитано, %: С 58,35;.Н 3,50; N 4,86
( fli ) 2-(3-пиридилметш1)бензофу- ран-5-карбонитрил
Обработка 5-бром-(3-пиридилметил бензофурана цианидом меди (I) по методике примера 1 (iv) дает 2-(3- пиридилметил)бензофуран-5-карбони- трил, т.пл. 59-61 .
Найдено, %: С 76,44; Н 4,27; N 12,38
С„Н,,НгО
Рассчитано, %: С 76,90; Н 4,28; N 11,96 .
(1 у) 2-(3-пиридилметил)бензофура 5-карбоновая кислота
Гидролиз 2-(3-пиридилметил)бензо фуран-5-карбонитрила по методике прмера 1 (v) дает 2-(3-пиридилметил) бензофуран-5-карбоновую кислоту, т.пл. 197-198.
Найдено, %: С 71,3t; Н 4,51-, N 5,58
C,5H,,N05
Рассчитано, %: С 71, Н 4,38; N 5,32.
Пример 13. 5-карбокси-З-ме тилбензо(в)тиен-2-ил пирид 3-ил ке- тон
( 1 ) 5-циано-3-метилбензо(в)ти- ен-2-ил-пирид-2-ил кетон
Обработка 5-бром-3-метилбензо(в) тиен-2-ил-пирид-З-ил кетона (продук примера 2 (JO цианидом меди (Т) по методике примера .1 (IV) дает 5-циан 3 метилбензо(в)тиен-2-ил пирид-3-ил кетон, т.пл. 138-139° (из этилацета та/бензина, т.кип. 6Q-80°).
Найдено, %: С 69,08- Н 3,70; N 9,87.
C,gH, Рассчитано, %: С 69,04; Н 3,62;
:N 10,07
( ) 5-карбокси-3-метилбензо(в) тиен-2-ил пирид-3-ил кетон
1 Гидролиз 5-циано-3-метилбензо(в) тиен-2-ил пирид-3-ил кетона по мето- дике примера 8 (IV) дает 5-карбокси- 3-метилбензотиен-2-ил-пирид-3-ш1 кетон, J.пл. 253-265 .
Найдено, %: С б4,00; Н 3,81; Ц. 4,60
C,,H,,NO,5
Рассчитано, %: С 64,63; Н 3,73; N 4,71
Пример 14. 3-метил-2-(1-ими
дазолиЛметил)бензофуран-.5-К| р|боновая кислота 1) 5-б ром-З-этилбензофуран- 2-карбонйтрил.
Смесь 5-бром-2-оксипропиофенона (t3,74 г), хлорацетонитрила (4,62мл) безводного карбоната калия (49,8 г) в безводном диметилформамиде (140 мл нагревали при температуре дефлегмации в течение 1 ч при перемешивании. Растворитель выпарили и остаток разделили между .водой И простым диэти- ловым эфиром. Слои отделили друг от друга и водньй слой несколько раз экстрагировали простым диэтиловым эфиром. Смесь органического слоя с экстрактом тщательно промыли водой и высушили (над Na,SO). После выпаривания растворителя получили твердый остаток, который подвергли хроматографии на силикагеле. В результате элюирования смесью хлороформа с бен- зином(3:1) получили 5-бром-З-этил- бензофуран-2-карбонитрил (8,90 г) с т.пл. 68-69 после кристаллизации из смеси метанола с водой.
Найдено, %: С 53,14j Н 3,24; N 5,71
C,,HgBrNO
Рассчитано, %: С 52,83 Н 3,22; N 5,60
II) 5-бром-3-этилбензофуран-2- карбоновая кислота
Смесь 5-бром-3-этилбензофуран-2 карбонитрила (2,00 г), гидроокиси калия (1,00 г), воды (Ю мл) и этанола (0,5 мл) нагревали при температу- ре дефлегмации в течение 48 ч и затем вьтаривали растворитель. Остаток растворили в воде и раствор профильт5
О
5
0
0
ровали и подкислили 2 Н.Соляной кислотой. Твердые частицы отфильтровали, промыли водой, высушили и получили 5-6ром-3-этилбензофуран-2-карбоновую кислоту (2,01 г) с т.пл. 240-242 после кристаллизации из смеси метанола с водой.
Найдено, %: С 49,27; н з,51 С„н;Вг О,
Рассчитано, %: С 49,10; Н 3,37
fll) 5-бром-3-этил-2-оксиметил- бензофуран
В перемешиваемый раствор 5-бром- З-этилбензофуран-2-карбоновой кислоты (1,91 г) в безводном тетрагидрофура- не (70 мл) при О в атмосфере СУХого ( азота по каплям добавили боран-тетра- гидрофурановый комплекс (25 мл 1М раствора). Раствор перемешивали при О в течение часа и затем при комнатной температуре в течение 24 ч. Для того, чтобы разложить избыток боранового комплекса, непрерывно добавляли метанол и затем раствор выпарили. Остаток растворили в простом диэтиловом эфире, раствор промьши водой и высушили (над ). Эфир выпарили и получили твердый остаток, который хроматографировали на сили-. кагеле. В результате элюирования хлороформом получили твердое вещество, которое кристаллизовали из смеси . этилацетата с бензином и получили 5-бром-3-этил-2-оксиметилбензофуран (1,05 г) т.пл. 93-94°.
Найдено, %: С 51,71; И 4,36 С,,Н„ВгОг
Рассчитано, %: С 51,79; И 4,35
V) 5-бром-2-хлорметил-3-этш1- бензофуран
Обработка 5-бром-3-этш1-2-окси- метилбензофуран тионилхлоридом и пиридином по способу, описанному в примере 1 (П), получили 5-бром-2-хлор- метил-3-этилбензофуран, т.пл. 58-60 .
Найдено, %: С 48,41;- Н 3,89 C,,HjgBrCeo
Рассчитано, %: С 48,30; И 3,68
V) 5-бром-3-этил-2-(1-имидазолил- метил)бензофуран
Обработав 5-бром-3-этш1-2-оксиме- тилбензофуран имидазолом и бикарбонатом натрия по способу, описанному в примере 4 (14) указанной Европейской патентной заявки, получили 5-бром-З этил-2-(1-имидазолилметил)бензофу- , ран, т.пл. 140-141.
х
Найдено, %: С 55,10; Н 4,29, W 9,18
СцН„ВгНр
Рассчитано, %: С 55,12; Н 4,45; N 9,29
Vr) 3-этил-2-(1-нмидазолилметил) бензофуран-5 карбонитрил
Обработав 5--бром-3-эти.п-2-( 1-ими- дазолилметил)бензофуран цианидом меди (1) по способу, описанному в примере Г( IV), получили 3-этил-2--( дaзoлил) бензофуран-5-карбонитрил, ТЛ1Л. 88-89°,
Найдено, %: С 70,99; Н 5,28; N 16,46
с,,п,о
Рассчитано, %: С 71,70, Н 5,21; N16,72
11Г) 3-этил-2(1-имиДазолилметил) бензофуран-5-карбоновая кислота
Осуществив гидролиэ З-этил-2- (1-имидазолилметил)бензофуран-5-кар бонитрила по способу, описанному в примере iCV), получили 3-этил-2-{1- имидазолилметил)бензофуран 5-карбо- новую кислоту, . 215-217°.
Найдено, %: С 66,05; Н 5,29; Н 10,31
С,5 иНгОэ Рассчитано, %: С 66,66; Н 5,22;
К 10,36 ,
Пример 15,- 2-(1-имидазолилметил)-1-метил нафталин-7-карбоновая кислота.
1) 7 бром-2-диметиламин,ометил-1 - тетралон
Смесь 7-бром 1-тетралона (4,50 г хлоргидрата диметиламина (2,50 г)„ параформальдегида (1,0 г) этанола (6 мл) и концентрированной соляной кислоты (4 капли) нагревали при температуре дефлегмации в течение 2 ч и охлаждали. Смесь разбавили несколькими миллилитрами ацетона, отфильтровали твердые частицы, промыли их небольшим количеством ацетона высушили и получили хлоргидрат 7- бром-2-диметиламинометил-1-тетралона, имеющий т.пл 169-171 и достаточно чистый для использования в следующей реакции.
Образец, кристаллизованный из см си метанола с этилацетатом, имел т.пл. 176-178°.
Найдено, %: С 48,99- Н 5,26; N 4,72
,gBrNOHC
Рассчитано, %: С 49,00,- Н 5,38; N 4,40
Хлоргидрат превратили в свободное
основание путем растворения в небольшом объеме воды и добавив незначительный избыток насыщенного водного раствора бикарбоната натрия. После экстрагирования простым диэтиловым
эфиром получили свободное основание в виде масла.
II) 7-бром-2-(1-имидазолилметил)- 1-тетралон
Раствор 7-бром-2-диметиламинометил-1-тетралонового свободного основания (6,,0 г) и имидазола (2,5 г) в ксилоле (ЗО мл) нагревали при температуре дефлегмации в течение 1,5 ч и затем выпарили. Остаток растворили
в простом дизтиловом эфире и раствор про(-№ши водой, а затем разбавленной соляной кислотой. Кислый зкстракт сделали щелочным разбавленным раствором едкого натра. Смесь экстрагирозалп хлороформом, экстракт промыли водой и высушили (над Na2S04). После выпаривания растворителя получили твердый остаток, который подвергли кристаллизации из этилацетата; и
получили 7-бром 2-(1-имидазолилметил)- -тетралон 3 т.пл. 129-131.
Найдено, I: С 54,86; Н 4,30; N 9,34
Рассчитано, %: С 55,10, Н 4,29 N 9,13
( in ) 7--бром-1-оксо-1-метил 2- (1-имидазолилметил)-1,2,354-тетра- гиброфталин
Обработав 7-бром-2-(1-имидазолилметил) - 1-тетрадон бромметилмагнием по способу, описанному в примере 10 (iri)j, получили 7-бромокси-1-метил-2- (1-:;-1мидазопилметил)-1, 54-тетрагидронафталин в виде смеси изомеров, которую непосредственно использовали на следующей стадии,
ly) 7 бром-2-(1-имидазолилметил)- 1 метилнафталин
Раствор 7-бром-1-окси-1-метил-2- (1 имидазолилметил)-1,2,3 54-тетра- гидронафталина (1,95 г) и трифенилме- танола (2,37 г) в трифторуксусной кислоте (30 мл) нагревали при температуре дефлегмации в течение 4 сут, затем добавили еще 2,37 г трифенил- метанола и, нагревали раствор при температуре дефлегмации еще 5 сут. Раствор выпарили и остаток превратили в основание разбавленным раствором едкого натра. Смесь несколько раз экстрагировали этилацетатом, экстракт промыли водой и высушили (над ) После выпаривания растворителя получили масло, которое затем хроматогра- фировали на силикагеле. В результате элюирования хлороформом получили трифенилметан, некоторое количество трифенилметанола и чистый продукт, Содержащие продукт фракции выпарили и получили 7-бром-2-(1-имидазолилме- тил)-1-метилнафталин (1,38 г). Обра- зец, кристаллизованный из смеси этил- ацетата с бензином (т.к. 70-80 ), имел т.пл. 112-113 .
Найдено, %: С 59,82; Н 4,32; N 9,10
С Н,Вг N 2
Рассчитано, %: С 59,8,2; Н 4,35,- N 9,30С
У ) 2-(1-имидазолилметил)-1-метил- нафталин-7-карбонитрил
Обработав 7-бром-2-(1-имидазолил- метил)-1-метилнафталин цианидом меди по способу, описанному в примере 1 (tV), получили 2-(1-имидaзoлилмeтил)- 1-мeтилнaфтaлин-7-кapбoнитpил, т.пл. 141-143 , достаточно чистый для использования в следующей реакции.
VI) 2-(1-имидазолилметил)-1-метил нафталин-7-карбоновая кислота
Осуществив гидролиз 2-(1-имидазо- лилметил)-1-метилнафталин-7-карбоно- вая по способу, описанному в примере 1 (V), получили 2-(1-имидазолилметил) 1-метилнафталин-7-карбоновую кислоту т.пл. 300 .
Найдено, %: С 71,77; Н 5,27; N 10,44
С,Н,
Рассчитано, %: С 72,17; Н 5,30; N 10,52
Соединения формулы (1) и их фармацевтически допустимые соли избирательно ингибируют действие фермента тромбоксан-синтетазы, не оказывая существенного неблагоприятного влияния на действие ферментов простатциклин- синтетазы или циклоксигеназы. Тем самым, соединения представляют ценность для лечения множества клинических состояний, которые характеризу- ются дисбалансом простайциклин/тром- боксан А. По рассмотренным причинам 1 эти состояния включают тромбозы, ишемическую болезнь сердца, сердечные приступы, преходящие ишемические приступы, мигрень, болезни периферических сосудов, рак, сосудистые осложнения диабета и эндотоксиновог шока.
Исследования показали, что в болшинстве тканей основным продуктом мтаболизма аразидоновой кислоты является одно из двух неустойчивых веществ, тромбоксан Aj(TxAj) или простациклин (PGIj)
В большинстве случаев простаглан дины PGEg, PGD оказываются сравнительно менее важными побочными продуктами при таком направлении процессов биосинтеза. Обнаружение тромбоксана Aj и простациклина существенно расширило понимание процессов гомеостаза сосудов. Например, простациклин является мощ- ньгм вазодиллататором и ингибитором агрегации тромбоцитов, и в этом отношении является наиболее мощным из выявленных до сих пор эндогенных веществ. Фермент простациклин-син- тетаза располагается в эндотелиаль- ном слое сосудистой сети, и может снабжаться эндоперекисями, высвобождаемыми тромбоцитами крови, соприкасающимися со стенками сосудов. Продуцируемый таким путем простациклин весьма важен для предотвращения отложения тромбоцитов на стенки сосудов.
Тромбоксан А синтезируется с помощью фермента тромбоксансинтета- зы, который имеется, например, в тромбоцитах крови. Тромбоксан А является мпщным вазоконстриктором и про-агрегирующим веществом. Его действие, как таковое, прямо противоположно действию простациклина. Если, по какой-либо причине, ухудшается выр аботка простациклина сосудистой сетью, продуцируемые контактирующими со стенкой сосудов тромбоцитами эндоперекиси преобразуются в тромбоксан, а не преобразуются эффективным путем в простациклин. Изменение равновесия простациклин/ тромбоксан в сторону последнего вещества может приводить к агрегации тромбоцитов, т.е. вазоспазу и к повышенной чувствительности к атеро- тромбозу. Известно также, что в экспериментальном атеросклерозе подавляется выработка простациклина и усиливается производство тромбокса ка АЛС Тем самым, тромбоксан Aj признан как основной причинный агент в различных разновидностях стенокардии, инфаркта миокар/ла внезапного смертельного исхода на почве сердеч- недостаточности и приступов. Исследования на кроликах показали, что ЭКГ-изменения, характерные для Э 1 их состояний, возникают в случае, кс гдд свежеприготовленный тромбоксан A,j зпрыски:вают непосредственно в сардг1е животного. Эта методология считается уникальной животной моделью сердечных приступов пациентов с коронарной недостаточностью и использована для демонстрации того, что введение соединения, предполо- л ительно являющегося антагонистом эффектов тромбоксана А, защищает кроликов от фатальных последствий инъекп,ин тромбоксана Aj,«
Другой областью, где дисбаланс PG1, /ТхА считается важным составным фактором, является мигрень.
Головная боль при мигрени связана с изменениями внутри- и внемозго- зого кровотока5 в частности пред- шс;ству ощим 1 оловной боли уменьше нием мозгового кровотока с последу-- ю;цим распространением на обе сосудистые области на протяжении фазы 1 оловной боли,
Перед развитием головной боли повышается уровень содержания 5-гид рокситрипамина в крови и это свидетельствует о существовании аг ре- гаи.ии in vivo и высвобождении ами- нав из тр(7мбоцитных запасов. Известно, что тромбоциты крови пациентов 5 склонных к мигрени, более подверже- нь; агрегации 3 чем у нормальных индивидов« Кроме того5 в последкее вре мя постулировано, что аномалия функ- г;,ии тромбоцитов является не просто глазным фактором в автогенезе присту пов мигрени,, но фактически оказывается их основной причиной о Таким образом, препарат, который избирательно иодифицирует функцию тромбо- ц;итав в направлении ингибирования образования тромбоксана мог бы дать значительный положительный эфф жт в терапии мигрени.
Аномалии поведения тромбоцитов обнаружены у пациентов с сахарньм
диабетом. Известно, что больные диабетом особенно чувствительны к микрососудистым осложнениям, атероскле- розу и тромбозу, и тромбоцитная ги- пер-реактивность считается причиной подобной ангиопатии. Диабетические тромбоциты продуцируют повышенные количества ТхВ и малонового диальдегида. Кроме того, показано что у крыс с экспериментальным диабетом выработка сосудистого простациклина ухудшена и усиливается синтез ТхА, из тромбоцитов. Таким образом, считается, что дисбаланс между простациклином и ТхА ответственен за микрососудистА1е осложнения диабета„ Поэтому, ингибитор ТхА - синтетазы был бы весьма клинически
полезен для профилактики этих сосу- дистьух осложнений.
Аспирин и большинство других нестероидных противовоспалительных препаратов ингибируют фермент циклооксигеназу. Эффектом этого оказы- . вается прекращение выработки зндоперекисей и снижение в резуль- . этого уровня содержания и простациклина и тромбоксана А. Ас
пкрин и аспиринрподобные препараты оценивались клинически с точки зрения предотвраще1Ш я сердечных приступов .
Несмотря на то, что при использовании этих препаратов были получены некоторые обнадеживающие результаты, для лечения подобных клинических состояний более ценным бьшо
бы соединение, которое обеспечивает специфическое ингибирование образования тромбоксана А, оставляя в неприкосновенности биосинтеза простациклина.
Способность первичных новообразований давать метастазы является основной причиной неудач в лeчeн и рака у человека. Предполагалось, что метастатические опухоли клетки могут
изменять критическое равновесие PGI ТхА., благоприятствуя тромбозу. Про- стациклин является мощным антиметастатическим агентом благодаря своему , тромбоцит-антиагрегационному дейст- вию„ Этот результат говорит о том, что ингибитор ТхА,- синтетазы может действовать как антиметастатический агент.
Шок, вызываемый бактериальными эндотоксинами, связан с тромбоцито- пенией, рассеянным внутрисосудистым свертыванием, лизосомной лабилиза- цией и высококонстрикцией легочной и брыжеечной артерий. Кроме того, заметно повышается уровень содержания тромбоксана в плазме. Введение имидазольных ингибиторов TxAg- синтетазы экспериментальным животным до эндотоксина приводило к снижению симптоматики шока и существенному повышению нормы выживания. i
Воздействие соединений формулы (I) на фермент тромбоксансинтета- зу, и ферменты простациклин-синте- тазу и циклооксигеназу измеряют с помощью следующих ферментных анализов .
1.Циклооксигеназа.
Микросомы семенных пузырьков барана инкубируют с аразидоновой кислотой (1%% мкмоль, 1 мин при 22 С) для получения 7СНу и пробы реакцион ной смеси вливают в поток бикарбоната по Кребсу при 37 , содержащего смесь антагонистов и индометацина, который используют для перфузии вырезанной по спирапи полоски аорты кролика. Способность соединения ин- гибировать фермент измеряют сравнением увеличения изометрического напряжения, создаваемого РСН в отсутствии испытуемого соединения, и вслед за предварительным инкубированием фермента с испытуемым соединением в течение 5 мин.
2.Простациклин (РС12)-синтетазы
Микросомы аорты свиньи инкубируют (30 с, -22) с nCHg, полученным и в П.1, и реакцию прекращают, используя 5 объемов этанола. Выработку РСЕ оценивают путем измерения его стабильного продукта распада, 6-кето РСГ., используя специфичный радио- иммуноанализ.
РС.1д -производство может быть полностью ингибировано предварительным инкубированием фермента с избирал тельным ингибитором PCI -синтетазы, 15-гидроперексиарахидоновой кислотой . Испытуемое соединение предварительно инкубируют с ферментом в течение 5 мин и измеряют его способность предотвращать выработку РСГ(6-кето РСГ,).
3.Тромбоксан А2.(ТхА2)синтетаза
Предварительно обработанные индо- метацином микросомы человеческих тромбоцитов инкубируют (2 мин, О в РСНл, полученным аналогично п.1) и реакцию прекращают с помощью 5 объемов этанола. Выработку ТхА оценивают путем измерения его стабильного метаболита ТхВ2, используя специфический радиоиммуноанализ.
Испытуемое соединение предварительно инкубируют с ферментом в течение 5 мин, и его способность инги- бировать фермент тромбоксан-синте- тазу измеряют как снижение выработки
ТхА2 (TxBj).
Показано, что испытанные рассмотренным путем соединения формулы (I) способны избирательно ин- гибировать фермент тромбоксансин- татазу.
В дополнение указанному описан анализ для измерения ингибирования агрегации тромбоцитов человеческой
крови, и он может считаться прогнозным для оценки клинической анти- тромбической эффективности. В этом испытании оба клинически эффективных препарата, аспирин и сульфинпиразон,
проявляют ингибирующую активность в отношении множества агрегирующих агентов.
Описан также ряд тестов in vivo
«на животных для оценки потенциальных анти-тромбических лекарственных препаратов.
Методика Петроно и соавторов приспособлена для изучения выработки ТхВ в образцах цельной крови,
взятой у животных перед обработкой лекарственным препаратом и после неё. Образцы крови отбирают в стеклянные пробирки и оставляют при 37 для свертывания. Сыворотку отделяют центрифугированием и образцы хранят при до проведения анализа на TxBg, когда подходящие разбавления депротеинизированных этанолом образцов анализируют с
помощью радиоиммуноанализа. Эта методика используется в экспериментах с испытуемыми соединениями для определения силы действия при внутривенном введении анестезированным
кроликам.
Анестезированные кролики. Белые кролики-самцы New Lealand (2,6-5,6 кг) использованы для анестезии пентобарбитоном натрия (30 мг/кг внутривенно), а затем уретаном (500 мг/кг внутрибрюшинно) После канюлирования трахеи сонную артерию катетеризируют для сбора образцов крови. Катетер оставляют незакрытым путем медленной инфузии (0,2 мл/мин) стерильного солевого раствора. Контрольные пробы сонно- артериальной крови отбирают за 30 и 5 мин до введения испытуемого соединения или среды (0,9 % вес./об О,- мл/кг) через краевую уашую вену,, Используьэт три группы кроликов Первая группа получает 0,03 мг/кг. Аналогично, вторая группа получает 0,3 МГ/КГ , затем 1 мг-/кг. Третья группа получает среду-носитель, с последующей еще одной инъекцией средьг-носителя спустя 1 ч. Пробы сонноартериальной крови отбирают спустя 15 и 45 мин после введения любых доз, В момент отбора в стекляную пробирку отбирают 1 мл образца KpoBi, без антикоагулянта, для определения TxBj . С Зтой целью, пробе крови дают возможность свернуться на протяхсении двухчасового инкубирования при 37°(для этого времени предварительные эксперименты показали максимальную выработку TxB,g) и сыворотку получают центрифугированием. Образцы сыворотки затем обрабатывают методом радиоиммуноана- л лза на ТхВ,., после депротенизации этанолом и разбавления буфером Изогель-Трис.
Внутривенное вливание арахидоно- вой кислоты вызывает смерть кроликов в результате агглютинации тромбоцитов и эмболизации в легких. И ;вновь5 клинически эффективные аспирин и сулъфинпиразон защищают кролика от летального действия ин.ъек- ции. Показано также, что сульфинпир зон препятствует агрегации тромбопи ТОО 3 экстракорпоральном контуре абдоминальной аорты крыс.
Соединения могут быть введены орально в виде таблеток или капсул, содержащих единичную дозу соединени вместе с такими индифферентньпчи составляющими, как кукурузньш крахмал карбонат кальция, дикальцЕйфосфат альгрновая кислота, лактоза, стеара магния, Примогель (торговая марка или тальк. Таблетки обычно готовят
,; о 5 С 5 p
,.
CS ;
5
U
совместным гранулированием ингре- дтиентов и прессованием результирующей смеси с получением таблеток требуемого размера. Капсулы обычно готовят совместным гранулированием ингредиентов и наполнением ими; желатиновых капсул подходящего размера с заполнением требуемой дозой.
Соединения могут быть введены также парзнтерально, например, с помощью внутримышечной, внутривенной или подкожной инъекции. Для парэнте- рального введения их лучше всего использовать в виде стерильного водного раствора, который может содержать и другие растворенные вещества, такие, как регухшторы тонического давления и рН. Соединения могут быгь добавлены в дистиллированную воду и рН доводят до 3-6,, используя кислоту, такую как лимонная,, молочная или хлористоводородная. Для обеспечения изотонического характера раствора могут быть добавлены достаточные количества растворенных веществ, таких как декстроза или соль. Результирующий раствор может затем стерилизован и наполнен в стерильньш стеклянные ампулы по,д- ходящего размера, содержащие требуемый объем раствора. Соединения согласно изобретению могут быть также Бвед€ ны инфузией парэнтералы-:ого состава, описанного выше, в вену.
Для орального приема людьми суточная дозировка соединения формулы (I) составляет 0,1-20 мг/кг в сутки для -ипичного взрослого пациента (70 кг). Для парэнтерального введения, суточная дозировка соединения формулы (I) составляет 0,01-0,5 мг/кг в сутки, для типичного взрослого и,ациента. Так, таблетки или капсулы содержат 5-150 мг активного соединения для орального приема до 3 раз 3 сутки, ,Дозы для парэнтерального введения содержат О,5-0,35 мг активного соединения. Типичная ампула представляет собой ампулу на 10 мл, содержащую 5 мг активного соединения в 6;-10 мл раствора.
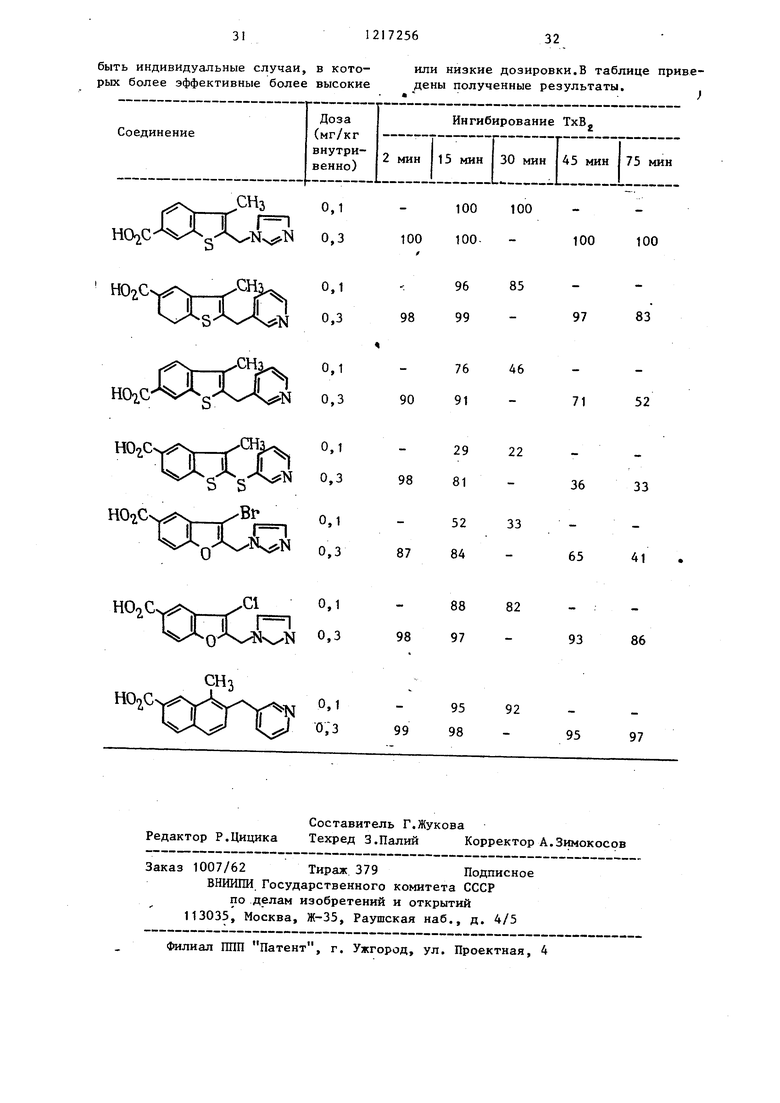
Естественно, следует иметь в виду, что Е любом случае врач сам определяет фактическую дозировку, наиболее подходящую для пациента с учетом возраста, веса и его реакции. Указанные дозировки являются усреднен- ньми примерами: естественно могут
быть индивидуальные случаи, в кото- или низкие дозировки.В таблице приве- рых более эффективные более высокие дены полученные результаты.
Заказ 1007/62 Тираж 379 Подписное ВНИИПИ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб., д. 4/5
Филиал ПГШ Патент, г. Ужгород, ул. Проектная, 4
- 














Способ получения бензофуранбен- зо(в)тиофен- или нафталинкарбоновых кислот общей формулы I .А IB X где У, которьй присоединен к кольцу А, означает СООН или X - О, 5 или ДI присоединен к атомУ углерода кольца В, означает водород, галоид, С|-С4-алкил или 5 (.-алкил); R, который присоединен к атому углерода кольца В, означает - 1 или (3-пиридил)-, где 7, - группа CHj, СО или 5 , или их фармацевтически приемлемых солей, о т л и ч а ю щ и и с я тем, что соединение общей формулы П С € (Л где R , R и X имеют указанные значения, а нитрильная группа присоединена к кольцу А соединения формулы 1, подвергают гидролизу с использованием гидроокиси натрия или серной кислоты в виде их водных растворов с выделением целевого продукта, где У-СООН, или с использованием перекиси водорода и гидроокиси натрия с выделением целевого продукта, где y-CONH.
| Бюлер К,, Пирсон Д | |||
| Органические синтезы, ч | |||
| II , М.: Мир, 1973, с | |||
| Приспособление для нагрузки тендеров дровами | 1920 |
|
SU228A1 |
Авторы
Даты
1986-03-07—Публикация
1982-08-25—Подача