Изобретение относится к производным новых гетероциклических систем дигидропирроло[1,2,3-e,d]пиримидо[4,5-b]пиразина или дигидропирроло[1,2,3-е,d] пиримидо[4,5-b]диазепина и способу их получения.
Производные новых гетероциклических систем дигидропирроло[1,2,3-e,d]пиримидо[4,5-b]пиразина или дигидропирроло[1,2,3-e,d]пиримидо(4,5-b)диазепина, и новый способ получения систем могут быть использованы в синтезе биологически активных веществ.
П р и м е р. Получение 8-хлор-6-метил-4,5-дигидропирроло[1,2,3-e,d]птеридина(1а).
1. Получение исходного соединения 5-нитро-2,4-диэтокси-6-( β-диметиламиновинил)пиримидина.
Раствор 16,0 г (0,07 моль) 5-нитро-6-метил-2,4-диэтоксипиримидина и 16,6 г (0,09 моль) 80%-ного диэтилацетата диметилформамида нагревают до 75-80оС и выдерживают при этой температуре с перемешиванием 3 ч. Реакционную смесь выливают в 80 мл воды, выпавший осадок отфильтровывают, промывают 15 мл воды, перекристаллизовывают из 250 мл этанола.
Получают 17,6 г (89%) целевого продукта в виде кристаллов ярко-желтого цвета, растворимых в низших спиртах, нерастворимых в воде, т.пл. 135-137оС.
ИК-спектр, см-1: 1625 (C=C), 1550, 1320, 875 (C-NO2).
Масс-спектр: M+ 282.
ПМР-спектр, δ в СDCl3, м. д. 1,38 и 1,41 (3Н т СН3СН2О), 2,99 (6Н с N(CH3)2, 4,39 и 4,46 (2Н кв СН3СН2О), 5,30 (Н д Cα Н), 8,00 (Н д C β Н).
Найдено, C 50,92; H 6,40; N 19,71.
С12Н18N4O4
Вычислено, C 51,06; H 6,43; N 19,85.
УФ-спектр (С2Н5ОН), λмакс (lg ε), нм: 213 (4,42), 248 (4,20), 292 (4,28).
2. Получение 2,4-диэтоксипирроло[3,2-d]пиримидина.
К раствору 1,8 г (0,006 моль) 5-нитро-2,4-диэтокси-6-( β -диметиламиновинил)пиримидина в 25 мл ледяной уксусной кислоты при 70-80оС небольшими порциями прибавляют 5,0 г (0,077 моль) цинковой пыли. Реакционную смесь нагревают до 100оС и выдерживают при этой температуре 2 ч. Смесь охлаждают, неорганический осадок отфильтровывают, промывают 10 мл уксусной кислоты. Маточный раствор упаривают досуха, остаток обрабатывают холодной водой (5-10оС), выпавший осадок отфильтровывают, промывают 10 мл воды, перекристаллизовывают из 35 мл 50%-ного водного раствора этанола.
Получают 1,1 г (83%) порошка в виде кристаллов светло-кремового цвета, растворимых в низких спиртах, нерастворимых в воде, т.пл. 194-196оС.
ИК-спектр, см-1: 3080 (NH).
Масс-спектр: М+ 207.
Найдено, C 57,84; H 6,50; N 20,58.
С10Н13N3O2
Вычислено, C 57,96; H 6,32; N 20,28.
УФ-спектр (С2Н5ОН), λмакс (lg ε ), нм: 220 (4,45), 265 (3,98).
3. Получение 2,4-диэтокси-5-( β-диметиламиноэтил)пирроло[3,2-d]пиримидина дигидрохлорида.
Смесь 6,0 г (0,03 моль) 2,4-диэтоксипирроло[3,2-d]пиримидина, 6,0 г (0,04 моль) β-диметиламиноэтилхлорида гидрохлорида, 1,0 г (0,004 моль) триэтилбензиламмонийхлорида и 60 мл 40%-ного водного раствора едкого натра выдерживают при 40-45оС в течение 5 ч, затем добавляют 60 мл воды и 60 мл хлористого метилена и перемешивают при 20-25оС в течение 10 мин. Органический слой отделяют, водный экстрагируют хлористым метиленом (3х50) мл. Полученный экстракт сушат безводным сульфатом натрия, осушитель отфильтровывают, хлористый метилен отгоняют. Маслянистый остаток растворяют в 50 мл абсолютного этанола, добавляют 9%-ный спиртовой раствор хлористого водорода до рН 1,0. Смесь охлаждают до 0оС, выпавший осадок отфильтровывают, промывают 20 мл этилацетата, перекристаллизовывают из 70 мл этанола.
Получают 8,0 г (77%) продукта в виде кристаллов белого цвета, растворимых в воде, низших спиртах, нерастворимых в неполярных растворителях, т.пл. 144-145оС.
Масс-спектр: M+ 278.
ПМР-спектр, δ в D-ДМСО, м.д. 1,41 и 1,50 (3Н тр СН3СН2О), 2,80 (6Н с N(CH3)2] 3,53 (2H тр CH2N), 4,55 и 4,71 (2Н кв СН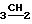 О), 4,81 (2Н тр -СН2N-), 6,51 (H д C6H), 8,03 (Н д С7Н).
О), 4,81 (2Н тр -СН2N-), 6,51 (H д C6H), 8,03 (Н д С7Н).
Найдено, C 47,71; H 7,12; N 16,03; Cl 20,49.
C14H22N4O2 · 2HCl
Вычислено, C 47,86; H 6,88; N 16,95; Cl 20,18.
4. Получение 2,4-диоксо-5-( β-диметиламиноэтил)-1,2,3,4-тетрагидропирроло[3,2- d]пиримидина гидрохлорида.
Раствор 10,0 г (0,03 моль) 2,4-диэтокси-5- (β-диметиламиноэтил)пирроло[3,2-d] пи- римидина дигидрохлорида в 150 мл концентрированной соляной кислоты кипятят в течение 10 ч. Раствор упаривают досуха, остаток обрабатывают 130 мл этанола, выпавший осадок отфильтровывают, промывают 25 мл этанола и перекристаллизовывают из 220 мл 90%-ного водного раствора этанола.
Получают 7,3 г (99%) продукта в виде кристаллов белого цвета, растворимых в воде, слабо растворимых в низших спиртах, нерастворимых в неполярных растворителях, т.пл. 270-272оС.
ИК-спектр, см-1: 3100 (NH) 1700 (C=O)
Масс-спектр: M+ 222.
Найдено, C 46,13; H 5,59; N 21,66; Cl 13,77.
С10Н13N4O2 · HCl
Вычислено, C 46,43; H 5,84; N 21,66; Cl 13,70.
5. Получение целевого продукта (1а).
Смесь 5,0 г (0,02 моль) 2,4-диоксо-5-(β -диметиламиноэтил)-1,2,3,4-тетрагидропир- роло[3,2-d]пиримидина гидрохлорида и 350 мл хлорокиси фосфора кипятят в течение 7 ч. Раствор упаривают досуха, остаток выливают в смесь льда с 25%-ным водным раствором аммиака. Полученный водный раствор (рН 8,0) охлаждают до 0оС, выпавший осадок отфильтровывают, промывают 15 мл воды, перекристаллизовывают из 50 мл этанола.
Получают 2,2 г (55%) целевого продукта в виде кристаллов светло-бежевого цвета, растворимых в низших спиртах, бензоле, нерастворимых в воде, устойчивых на воздухе, т.пл. 206-208оС.
Масс-спектр: М+ 208,5.
ПМР-спектр, δ в D-ДМСО, м.д. 3,10 (3H c N=CH3), 3,73 и 4,23 (2Н тр -СН2-СН2), 6,32 (Н д С2Н), 7,48 (Н д С1Н).
Найдено, C 51,92; H 1,44; N 26,81; Cl 17,02
С9Н9N4Cl
Вычислено, C 51,81; H 4,35; N 26,85; Cl 16,99
УФ-спектр (С2Н5ОН), λ макс (lg ε), нм: 216 (4,26) 250 (3,99), 293 (4,03).
П р и м е р 2. Получение 9-хлор-7-метил-4Н-5,6-дигидропирроло[1,2,3-e,d] пиримидо [4,5-b]диазепина (1б).
1. Получение 2,4-диэтокси-5-(γ -диметиламинопропил)пирроло[3,2-d]-пиримидина дигидрохлорида.
Смесь 4,4 г (0,021 моль) 2,4-диэтоксипирроло[3,2-d]пиримидина, полученного в условиях примера 1, 4,5 г (0,028 моль) γ -диметиламинопропилхлорида гидрохлорида, 1,0 г (0,004 моль) триэтилбензиламмоний-хлорида и 45 мл водного раствора едкого натра выдерживают при 40-45оС в течение 5 ч, затем добавляют 50 мл воды и 50 мл хлористого метилена. Смесь перемешивают при 20-25оС в течение 10 мин. Органический слой отделяют, водный экстрагируют хлористым метиленом (3х40 мл). Полученный экстракт сушат безводным сульфатом натрия, осушитель отфильтровывают, хлористый метилен отгоняют. Маслянистый остаток растворяют в 60 мл абсолютного этанола, добавляют 9%-ный спиртовой раствор хлористого водорода до рН 1,0, охлаждают до 0оС, выпавший осадок отфильтровывают, промывают 20 мл этилацетата, перекристаллизовывают из 90 мл этанола.
Получают 5,2 (67%) продукта в виде кристаллов белого цвета, растворимых в воде, низших спиртах, не растворимых в неполярных растворителях, устойчивых на воздухе, т.пл. 135-137оС.
Масс-спектр: M+ 292.
ПМР-спектр, δ, в D-ДМСО, м.д. 1,41 и 1,50 (3Н тр 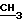 СН2О), 2,24 [2H мульт. СН2-N(CH3)2] 2,69 и 2,71 [3H c N(CH3)2] 2,99 (2Н мульт. СН2СН2-СН2), 4,45 (2Н тр СН2-N), 4,56 и 4,71 (2Н кв СН
СН2О), 2,24 [2H мульт. СН2-N(CH3)2] 2,69 и 2,71 [3H c N(CH3)2] 2,99 (2Н мульт. СН2СН2-СН2), 4,45 (2Н тр СН2-N), 4,56 и 4,71 (2Н кв СН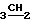 О), 6,48 (Н д С6Н), 7,99 (Н д С7Н).
О), 6,48 (Н д С6Н), 7,99 (Н д С7Н).
Найдено, C 49,27; H 7,46; N 15,25; Cl 19,49.
C15H24N4O2·2HCl
Вычислено, С 48,32; Н 7,18; N 15,34; Cl 19,41.
2. Получение 2,4-диоксо-5-(γ -диметиламинопропил)-1,2,3,4-тетрагидропиролло[3,2-d]пиримидина гидрохлорида.
Раствор 6,0 г (0,016 моль) 2,4-диэтокси-5-(γ -диметиламинопропил)пирроло[3,2-d]пиримидина дигидрохлорида в 60 мл концентрированной соляной кислоты кипятят в течение 10 ч, затем упаривают досуха.
Остаток обрабатывают 100 мл этанола, выпавший осадок отфильтровывают, промывают 20 мл этанола, перекристаллизовывают из 160 мл 90%-ного водного раствора этанола. Получают 4,4 г (98%) продукта в виде кристаллов белого цвета, растворимых в воде, слабо растворимых в низших спиртах, нерастворимых в неполярных растворителях, устойчивых на воздухе, т.пл. 246-248оС.
ИК-спектр, см-1: 3140 (NH), 1680 (C=O).
Масс-спектр: М+ 236.
Найдено, C 48,53; H 6,31; N 20,03; Cl 12,96.
C11H15N4O2 ·HCl
Вычислено, C 48,44; H 6,28; N 20,54; Cl 13,00.
Получение целевого продукта (1б).
Смесь 4,4 г (0,016 моль) 2,4-диоксо-5-(γ диметиламинопропил)-1,2,3,4-тетрагидро- пирроло[3,2-d]пиримидина гидрохлорида и 270 мл хлорокиси фосфора кипят в течение 7 ч. Хлорокись фосфора отгоняют, остаток выливают в смесь льда с 25%-ным водным раствором аммиака. Полученный раствор (рН 8,0) охлаждают до 0оС, выпавший осадок отфильтровывают, промывают 15 мл воды, перекристаллизовывают из 65 мл этанола.
Получают 2,0 г (55%) целевого продукта (1б) в виде кристаллов светло-бежевого цвета, растворимых в низших спиртах, бензоле, нерастворимых в воде, устойчивых на воздухе, т.пл. 190-192oC.
Масс-спектр: М+ 222.
ПМР-спектр, δ, в D-ДМСО, м.д. 2,22 (2Н квинт, СН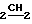 СН2), 3,22 (3Н с СН3), 3,65 и 4,21 (2Н тр
СН2), 3,22 (3Н с СН3), 3,65 и 4,21 (2Н тр 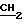 -СН2-СН2), 6,35 (Н д С2Н), 7,57 (Н д С1Н).
-СН2-СН2), 6,35 (Н д С2Н), 7,57 (Н д С1Н).
Найдено, C 54,10; H 5,03; N 25,41; Cl 15,96.
C10H11N4Cl
Вычислено, C 53,94; H 4,98; N 25,16; Cl 15,92.
УФ-спектр (С2Н5ОН), λ макс (lg ε ) нм: 220 (4,18), 250 (4,11), 302 (4,05).
1. Производные дигидропирроло[1,2,3, -e,d]пиримидо[4,5-b]пиразина или дигидропирроло[1,2,3-e,d]пиримидо[4,5-b]диазепина общей формулы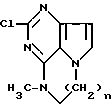
где n = 1 или 2.
2. Способ получения дигидропирроло[1,2,3-e, d]пиримидо [4,5-b]пиразина или дигидропирроло[1,2,3-e,d] пиримидо[4,5-b]диазепина общей формулы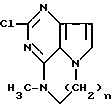
где n = 1 или 2,
отличающийся тем, что 5-нитро-2,4-диэтокси-6- (β -диметиламиновинил)пиримидин восстанавливают в кислой среде при 70 - 100oС, полученный 2,4-диэтоксипирроло[3,2-d]пиримидин обрабатывают соединением формулы (CH3)2N -CH2 (CH2)n Cl • HCl, где n = 1 или 2, в присутствии триэтилбензиламмонийхлорида в щелочной среде при 40 - 45oС, выделенный гидрохлорид соответствующего производного пирроло[3,2-d]пиримидина подвергают кислотному гидролизу при кипячении, полученное 2,4-диоксипроизводное пирроло[3,2-d]пиримидина кипятят с хлорокисью фосфора.
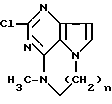
где n = 1 или 2.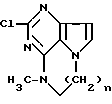
где n = 1 или 2,
отличающийся тем, что 5-нитро-2,4-диэтокси-6- (β -диметиламиновинил)пиримидин восстанавливают в кислой среде при 70 - 100oС, полученный 2,4-диэтоксипирроло[3,2-d]пиримидин обрабатывают соединением формулы (CH3)2N -CH2 (CH2)n Cl • HCl, где n = 1 или 2, в присутствии триэтилбензиламмонийхлорида в щелочной среде при 40 - 45oС, выделенный гидрохлорид соответствующего производного пирроло[3,2-d]пиримидина подвергают кислотному гидролизу при кипячении, полученное 2,4-диоксипроизводное пирроло[3,2-d]пиримидина кипятят с хлорокисью фосфора.
| Taulor E.C., Duman D.I | |||
| "Pteriolines, 49, Sunthesis of 2,4 - Diamino - 6,8 - dihudro -7-arul 1 - 8 - oxopurrolo[3,4-g] pteridines" J.Org | |||
| Chem | |||
| Устройство для видения на расстоянии | 1915 |
|
SU1982A1 |
| Способ очищения сернокислого глинозема от железа | 1920 |
|
SU47A1 |
| Hori M | |||
| eal | |||
| Ring Transformation Reaction Of Novel Xanthinium Jlides | |||
| Heterocucles, 1982, v.19, N 10, p.1845. | |||
Авторы
Даты
1996-03-20—Публикация
1984-10-05—Подача