Изобретение относится к новой спирогетероциклической системе, представленной 1'-бензил-5,7-диметил-6-оксоспиро-(1,3-ди- азаадамантан-2,4'-пиперидином) формулы у которого обнаружена избирательная α -адреноблокирующая активность.
у которого обнаружена избирательная α -адреноблокирующая активность.
Указанное свойство позволяет предполагать возможность его использования в медицине.
Целью изобретения является новая спирогетероциклическая система, содержащая диазаадамантановый и пиперидиновый циклы, на основе которой могут быть по- лучены биологически активные вещества.
П р и м е р. 1'-Бензил-5,7-диметил-6-оксоспиро-(1,3-диазаадамантан-2,4'-пипери- дин).
К раствору 4,2 г (0,025 моль) 1,5-диметил-3,7-диазабицикло[3,3,1]нонан-9-она в 50 мл абсолютная этанола прибавляют 4,2 г (0,024 моль) 1-бензил-4-пиперидона и кипятят в течение 4 ч. Растворитель отгоняют, к остатку прибавляют 30 мл воды и фильтруют. Осадок промывают водой, сушат и перекристаллизовывают из изопропилового спирта, выход 5,4 г (66,7%), т.пл. 163-164оС (изопропиловый спирт) Rf 0,63 (силуфол УФ-254, бутанол триэтиламин, 3: 1, проявитель нингидрин).
Найдено, C 74,74; Н 8,70; N 11,83.
С21Н29N3O
Вычислено, С 74,34; Н 8,55; N 12,39.
ИК-спектр, ν, см-1: 1580, 1600 (С=С аром), 1705 (С=0 кетон).
ПМР-спектр (СDCl-ГМДС), δ, м.д. 0,8 с (6Н, 2СН3); 2,0-,25 м (8Н, 2',3', 5', 6'-CH2); 2,7 д (4Н, J=14 Гц; 4,8,9,10-СН, ах), 3,45 с (2Н, СН2-С6Н5); 3,55 д (4Н, J=14 Гц, 4,8,9,10-СН, ep), 7,15 с (5Н, С6Н5).
УФ-спектр (96%-ный этанол), λмакс, нм (ε):207 (9569), 252 (1914).
Масс-спектр, м. е. (относительная интенсивность,): 339 (М+, 33); 338 (25), 323 (3, 5); 311 (14); 309 (12); 201 (20); 200 (100); 199 (21); 187 (18); 186 (23); 176 (12); 173 (14); 172 (77г), 149 (5); 138 (7); 134 (8); 124 (12).
Биологические свойства 1'-бензил-5,7-диметил-6-гоксоспиро(1,3-диазаадамантан-2,4'-пиперидина) (соединение 1) изучали в опытах на изолированных семявыносящих протоках белых крыс породы Вистар (массой 180-220 г). Опыты проведены на 41 семявыносящем протоке крысы.
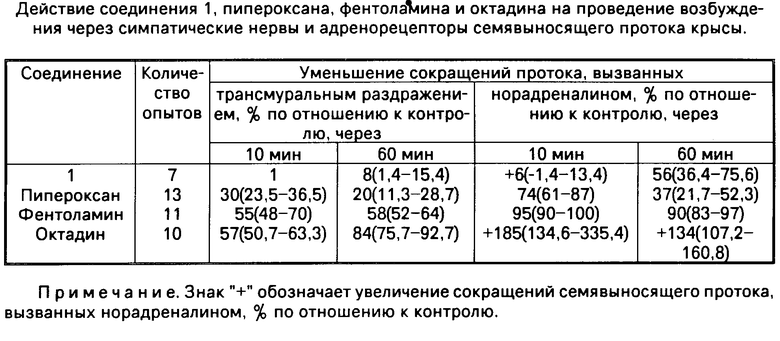
Изучали действие этого соединения на α -адренорецепторы и на проведение возбуждения через постганглионарные симпатические нервы. Об этих свойствах судили по уменьшению сокращений семявыносящего протока, вызванных трансмуральным электрическим раздражением (прямоугольными электрическими импульсами длительностью 0,1 мс с супрамаксимальным напряжением частотой 80 имп/c в течение 3 с через каждые 1,5 мин) в норадреналином в концентрации 1 10-5 г/мл. В качестве контрольных препаратов использованы α -адреноблокаторы пипероксан и фентоламин и симпатолитик октадин. Все соединения испытаны в концентрациях 0,05 мм. Обобщенные данные приведены в таблице.
Как видно из таблицы соединение 1 в первые минуты воздействия не проявляет существенного влияния на сокращение семявыносящего протока, вызванного норадреналином. Однако постепенно проявляется блокирующее действие и на 60-й минуте соединение 1 приводит к 50%-ному уменьшению реакции. Адреноблокирующее действие пипероксана и фентоламина развивается очень быстро, после чего на 60-й минуте эффект пипероксана уменьшается наполовину, а фентоламина держится на исходном уровне. Соединение 1 отличается от известных адренолитиков не только медленным развитием α -адреноблокирующего эффекта, но и тем, что не влияет на сокращения протока, вызванного трансмуральным электрическим раздражением, т.е. не обладает симпатолитической активностью. Таким образом, в опытах на семяновыносящих протоках крысы соединение 1 проявляет постепенно нарастающую и избирательную α -адреноблокирующую активность.
1′ -Бензил-5,7-диметил-6-оксоспиро-(1,3-диазаадамантан- 2,4′ -пиперидин) формулы
обладающий α -адреноблокирующей активностью.
| Авакян О.М | |||
| Фармакологическая регуляция высвобождения и захвата норадреналина | |||
| Ереван | |||
| Изд | |||
| АН АрмССР, 1973, с.20. |
Авторы
Даты
1995-08-27—Публикация
1984-08-17—Подача