Изобретение относится к химии фосфоpоpганических соединений, а именно к улучшенному способу получения 2-фенокси-5,7-диметил-2,6-диоксо-1,3-диаза-2-фосфа- адамантана формулы I который обладает противоопухолевой активностью и может найти применение в качестве лекарственного препарата.
который обладает противоопухолевой активностью и может найти применение в качестве лекарственного препарата.
Целью изобретения является упрощение процесса и повышение выхода соединения формулы I.
П р и м е р 1. Получение 2-фенокси-5,7-диметил-2,6-диоксо-1,3-диаза-2-фосфаада- мантана при молярном соотношении диазаадамантана, дихлорангидрида фенилфосфорной кислоты и триэтиламина, равном 1:1:2.
К раствору 0,45 г (0,0025 моль) 5,7-диметил-6-оксо-1,3-диазаадамантана в 50 мл бензола прибавляют 0,7 мл (0,005 моль) триэтиламина, затем при перемешивании 0,53 г (0,0025 моль) дихлорангидрида фенилового эфира фосфорной кислоты и продолжают перемешивание в течение 4 ч. Фильтруют, фильтрат промывают водой и упаривают под вакуумом. Остаток перекристаллизовывают из этанола. Выход 0,57 г (75%), т.пл. 193-194оС (этанол), Rf 0,60 (силуфол УФ-254, пропанол вода, 1:4, проявление нингидрином).
Найдено, C 58,91; H 6,24; N 9,08.
C15H19N2O3P
Вычислено, C 58,62; H 6,21; N 9,15.
П р и м е р 2. Молярное соотношение реагентов равно 1:1,5:4,8. Процесс проводят аналогично примеру 1, только берут 0,45 г (0,0025 моль) 5,7-диметил-6-оксо-1,3-диазаадамантана, 1,7 мл (0,012 моль) триэтиламина и 0,8 г (0,0038 моль) дихлорангидрида фенилового эфира фосфорной кислоты, выход 0,60 г (80%), т.пл. 193-194оС, Rf 0,60.
Найдено, C 58,65; H 6,30; N 9,25.
C15H19N2O3P
Вычислено, C 58,62; H 6,21; N 9,15.
П р и м е р 3. Молярное соотношение реагентов равно 1:0,8:2,4. Процесс проводят аналогично примеру 1, только берут 0,45 г (0,0025 моль) 5,7-диметил-6-оксо-1,3-диазаадамантана, 0,84 мл (0,006 моль) триэтиламина и 0,45 г (0,002 моль) дихлорангидрида фенилового эфира фосфорной кислоты, выход 0,45 г (60%), т.пл. 193-194оС, Rf 0,60.
Найдено, C 58,75; H 6,30; N 9,00.
C15H19N2O3P
Вычислено, C 58,62; H 6,21; N 9,15.
П р и м е р 4. Молярное соотношение реагентов равно 1:1,2:6,0. Процесс проводят аналогично примеру 1, только берут 0,45 г (0,0025 моль) 5,7-диметил-6-оксо-1,3-диазаадамантана, 2,1 мл (0,015 моль) триэтиламина и 0,63 г (0,003 моль) дихлорангидрида фенилового эфира фосфорной кислоты, выход 0,62 г (82%), т.пл. 193-194оС, Rf 0,60.
Найдено, C 58,45; H 6,11; N 8,85.
C15H19N2O3P
Вычислено, C 58,62; H 6,21; N 9,15.
П р и м е р 5. К раствору 0,45 г (0,0025 моль) 5,7-диметил-6-оксо-1,3-диазаадамантана в 50 мл бензола прибавляют 0,94 г (0,009 моль) триэтиламина, затем при перемешивании 0,63 г (0,003 моль) дихлорангидрида фенилового эфира фосфорной кислоты и продолжают перемешивание в течение 4 ч. Фильтруют, фильтрат промывают водой и упаривают под вакуумом. Остаток перекристаллизовывают из этанола, выход 0,64 г (83,6%), т.пл. 193-194оС (этанол), Rf 0,60 (силуфол УФ 254, пропанол-вода, 1:4, проявление нингидрином).
Найдено, C 58,63; H 6,20; N 8,95.
C15H19N2O3P
Вычислено, C 58,62; H 6,21; N 9,15.
ИК-спектр, ν, см-1: 1280 (Р-О-С), 1330 (Р=О), 1495, 1600 (С=С аром), 1710 (С=О кетон).
ПМР (CDCl3), δ, м.д. 0,9 с (6Н, 2СН3); 2,9-4,4 м (8Н, 4СН2), 7,4 с (5Н, аром).
Мол.м. 306 (масс-спектрометрически).
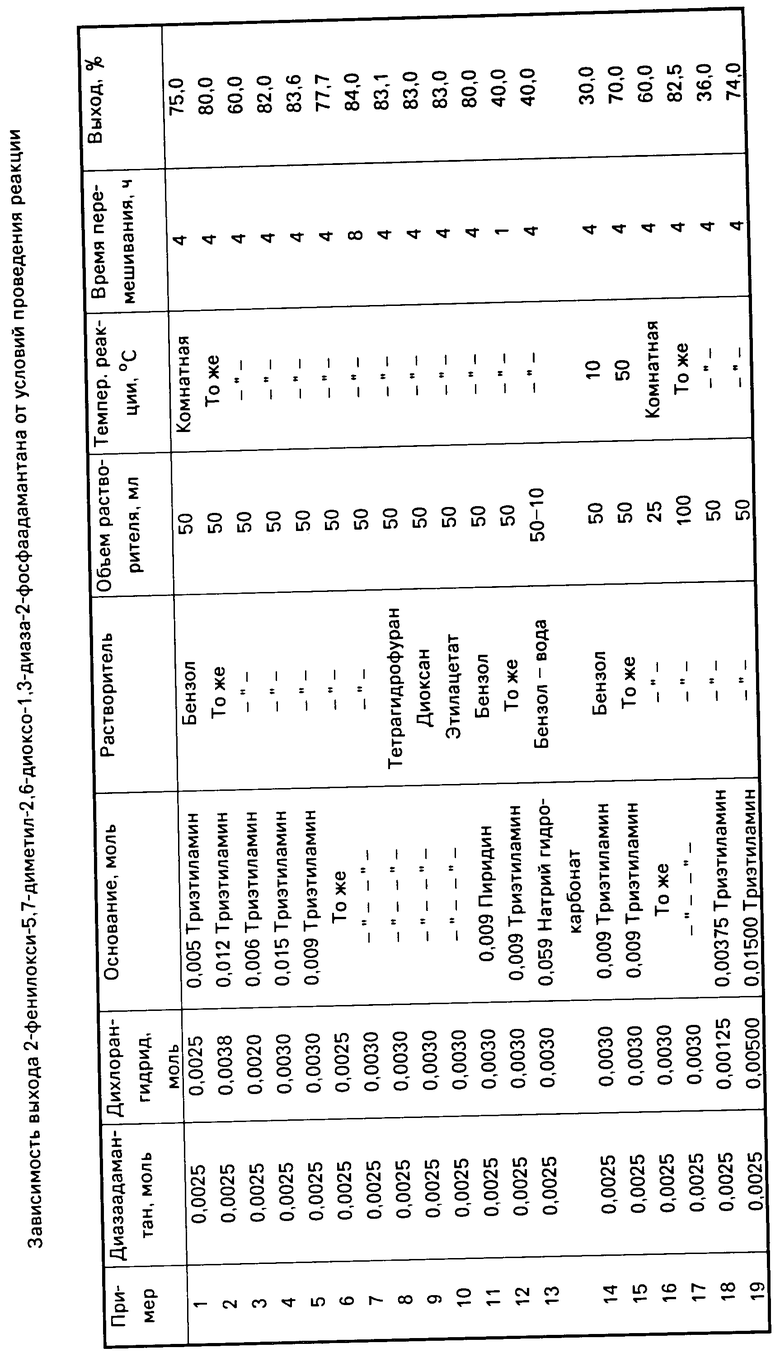
П р и м е р ы 6-19, показывающие зависимость выхода соединения формулы I от условий проведения процесса (различное соотношение реагирующих веществ, различные растворители и различные условия реакции с учетом объема растворителя, температуры реакции и длительности процесса), приведены в таблице.
Таким образом, при стехиометрическом соотношении 5,7-диметил-6-оксо-1,3-диазаадамантана, дихлорангидрида фенилового эфира фосфорной кислоты и триэтиламина, равном 1:1:2, выход целевого продукта составляет 75% (пример 1), увеличение количества триэтиламина практически не влияет на выход при соотношении 1:1:3,6 выход составляет 77,7% (пример 6). Одновременное увеличение количеств дихлорангидрида и триэтиламина (1:1,2:3,6-6) приводит к целевому продукту с выходами соответственно 82,0 и 83,6% (примеры 4 и 5). Еще большее увеличение количеств дихлорангидрида и триэтиламина 1:1,5-2:5-6, а также уменьшение количества дихлорангидрида 1:0,8:2,4, приводит к целевому продукту с выходами 74-80 и 60% (соответственно примеры 2, 19 и 3, 18). При удлинении времени перемешивания до 8 ч, замене бензола тетрагидрофураном, диоксаном или этилацетатом, а триэтиламина пиридином выход колеблется в пределах 77,7-84% (примеры 7-11). Уменьшение времени перемешивания до 1 ч, а также замена триэтиламина бикарбонатом натрия в смеси бензол вода, взятых в объемном соотношении 50:10 (мл), приводят к понижению выхода до 40% (примеры 12 и 13). Проведение реакции при температуре 10 или 50оС приводит к понижению выхода до 30 и 70% соответственно (примеры 14 и 15). Одновременное уменьшение количеств дихлорангидрида и триэтиламина приводит к резкому падению выхода до 36% (пример 18). Уменьшение объема бензола до 25 мл приводит к понижению выхода (60%), а увеличение объема до 100 мл практически не влияет на выход (82,5%) (примеры 16 и 17).
Таким образом, оптимальным является проведение реакции при избытке дихлорангидрида по отношению к диазаадамантану в присутствии триэтиламина или пиридина, взятого в трехкратном избытке по отношению к дихлорангидриду, в органическом растворителе при комнатной температуре в течение 4 ч (выход 80-83,6% ), что позволяет упростить процесс получения и повысить до 80-83,6% выход целевого продукта.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-БИС-( β -ХЛОРЭТИЛ)АМИНО-ИЛИ 2-ФЕНОКСИ-5,7-ДИМЕТИЛ -2,6-ДИОКСО-1,3-ДИАЗА -2-ФОСФААДАМАНТАНЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 1985 |
|
SU1282521A1 |
| 2′, 2′, 5,7 -ТЕТРАМЕТИЛ-6-ОКСОСПИРО-(1,3-ДИАЗААДАМАНТАН- 2,4′ -ТЕТРАГИДРОПИРАН) | 1984 |
|
SU1162195A1 |
| 2`,2`,5,7-ТЕТРАМЕТИЛ-6-ОКСОСПИРО-(1,3-ДИАЗААДАМАНТАН- 2,4′ -ТЕТРАГИДРОТИОПИРАН), ОБЛАДАЮЩИЙ ПРОТИВОСТАФИЛОКОККОВОЙ АКТИВНОСТЬЮ | 1984 |
|
SU1246568A1 |
| Способ получения дихлорангидридов хлорсодержащих 1,3-бутадиен-2-фосфоновых кислот | 1976 |
|
SU681066A1 |
| I′ -БЕНЗИЛ-5,7-ДИМЕТИЛ-6-ОКСОСПИРО-(1,3-ДИАЗААДАМАНТАН- 2,4′ -ПИПЕРИДИН), ОБЛАДАЮЩИЙ α -АДРЕНОБЛОКИРУЮЩЕЙ АКТИВНОСТЬЮ | 1984 |
|
SU1221878A1 |
| 1,3-Двузамещенные (2-тио) мочевины,обладающие активностью при мнезических процессах | 1978 |
|
SU1097622A1 |
| Способ получения монометинцианиновых красителей ряда 1,3-диметил-1,3-дигидропиримидона-2 | 1982 |
|
SU1004426A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 1(2)-БЕНЗИЛ-5-R-ТЕТРАЗОЛОВ | 1991 |
|
RU2030407C1 |
| Способ получения бензоморфанов или их солей или рацемической смеси или их оптических изомеров | 1975 |
|
SU721002A3 |
| Способ получения производных бензоксазин-2-она | 1983 |
|
SU1138025A3 |
Изобретение относится к фосфорорганическим веществам, в частности к способам получения 2-фенокси-5,7 -диметил-2,6-диоксо -1,3-диаза-2 -фосфаадамантана, который обладает противоопухолевой активностью и может найти применение в фармацевтике. Цель упрощение процесса и повышение выхода целевого продукта. Его синтез ведут реакцией 5,7- диметил -6-оксо-1,3 -диазаадамантана с дихлорангидридом фенилфосфорной кислоты в присутствии триэтиламина при их молярном соотношении 1,0 0,8-1,5 2,0-6,0 при комнатной температуре в среде органического растворителя в течение 4 ч при перемешивании. Выход 80 83,2% т.пл. 193-194 °С, брутто-формула C15H19N2O3P. Способ позволяет повысить выход целевого продукта на 23-41% и упростить процесс за счет уменьшения числа стадий. 1 табл.
Способ получения 2-фенокси-5,7-диметил-2,6-диоксо-1,3 -диаза-2-фосфаадамантана формулы
взаимодействием замещенного циклического диазакетона с дихлорангидридом фенилфосфорной кислоты и триэтиламином в среде огранического растворителя, отличающийся тем, что с целью упрощения процесса и повышения выхода целевого продукта, в качестве замещенного циклического диазакетона используют 5,7-диметил-6-оксо-1,3-диазаадамантан и процесс ведут при молярном соотношении реагентов 1 0,8 1,5 2 6.
| 2-БИС-( β -ХЛОРЭТИЛ)АМИНО-ИЛИ 2-ФЕНОКСИ-5,7-ДИМЕТИЛ -2,6-ДИОКСО-1,3-ДИАЗА -2-ФОСФААДАМАНТАНЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 1985 |
|
SU1282521A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-08-20—Публикация
1988-01-25—Подача