Изобретение относится к новым соединениям группы замещенных арилалкиламинов общей формулы: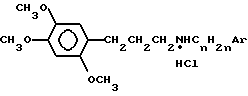 где CnH2n A r= -CH(CH3)CH2C6H5 I или -CH2CH2CH(C6H5)2 II, проявляющим блокирующее действие на захват катехоламинов.
где CnH2n A r= -CH(CH3)CH2C6H5 I или -CH2CH2CH(C6H5)2 II, проявляющим блокирующее действие на захват катехоламинов.
Структурными аналогами описываемых соединений являются гидрохлориды N-(арилалкил)-3-(2,4-диметоксифенил)-1-пропил-аминов, проявляющие блокирующее действие на нейрональный и экстранейрональный захват катехоламинов.
Наиболее излученными аналогами по биологическому действию являются метанефрин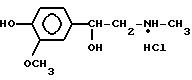
и мелипрамин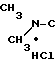 H2-CH2-CH2-N
H2-CH2-CH2-N [1]
[1]
Метанефрин оказывает выраженное блокирующее действие на экстранейрональный захват катехоламинов и практически не влияет на их нейрональный захват. Мелипрамин, наоборот, оказывает выраженное действие на нейрональный захват катехоламинов и мало влияет на экстранейрональный захват.
Цель изобретения расширение ассортимента средств, проявляющих блокирующее действие на захват катехоламинов нейрональный и экстранейрональный одновременно, обладающих меньшей токсичностью.
Поставленная цель достигается новыми гидрохлоридами замещенных арилалкиламинов вышеуказанной формулы I.
Описываемые соединения получают гидрированием соответствующих амидов алюмогидридом лития с последующим осаждением гидрохлоридов эфирным раствором хлористого водорода.
П р и м е р 1. Гидрохлорид N-(1-метил-2-фенил)этил-3-(2,4,5-триметоксифенил)-1- пропиламина [1]
К раствору 0,68 г (0,02 моль) алюмогидрида лития в 100 мл абсолютного тетрагидрофурана прибавляют по каплям раствор 3,6 г (0,01 моль) N-(1-метил-2-фенил)этиламида 3-(2,4,5-триметоксифенил)пропионовой кислоты в 50 мл тетрагидрофурана. Затем реакционную массу кипятят в течение 7-8 ч. После охлаждения до комнатной температуры комплекс разлагают 10 мл воды. Осадок отфильтровывают и промывают горячим тетрагидрофураном. Фильтрат высушивают над сернокислым магнием. После отгонки растворителя маслообразный продукт растворяют в абсолютном эфире и действием эфирного раствора хлористого водорода переводят в гидрохлорид N-(1-метил-2-фенил)этил-3- (2,4,5-триметоксифенил)-1-пропиламина, который пере- кристаллизовывают из смеси спирт-эфир (1: 10). Выход 2,58 г (68%), белые кристаллы с т.пл. 157-159оС, Rf 0,78. Найдено, N 3,71; Cl 9,50. C21H30NO3Cl. Вычислено, N 3,68; Cl 9,34. Аналогично получают гидрохлорид N-(3,3-дифенил)-пропил-3-(2,4,5-триметок-сифенил)-1-пропиламина (2). Из 4,3 г (0,01 моль) N-(3,3-дифенил)пропиламида 3-(2,4,5-триметоксифенил)пропионовой кислоты. Выход 3,4 г (75%), т.пл. 151-152оС, Rf 0,68. Найдено, N 2,87; Cl 7,56. C27H34NO3Cl. Вычислено, N 3,07; Cl 7,78.
Аналогично получен гидрохлорид соединения 2, т.пл. 151-152оС, Rf 0,68.
Изучено влияние описываемых соединений на нейрональный и экстранейрональный захват катехоламинов-норад- реналина-Н3 с удельной активностью 5 кюри/ммоль и адреналина-Н3 с удельной активностью 14 кюри/ммоль. В качестве сравнительных препаратов использованы блокатор нейронального захвата катехоламинов мелипрамин и блокатор экстранейронального захвата катехоламинов метанефрин. Опыты проводились на белых крысах породы Вистар весом 180-200 г. Крыс оглушали электрическим током и декапитировали. Влияние описываемых соединений на нейрональный захват катехоламинов изучено в опытах на семявыносящих протоках крысы. Семявыносящие протоки помещали в 5 мл камеры, содержащие насыщенный кислородом раствор Тироде при 37оС на 30 мин. Затем органы инкубировали с описываемыми соединениями в течение 30 мин. После этого семявыносящие протоки в течение 30 мин инкубировали в свежем растворе Тироде, в присутствии описываемых соединений и норадреналина-Н3 в концентрации 0,2 мккюри/мл. По окончании инкубации проводили пятикратную промывку органов раствором Тироде. Затем органы помещали в сцинтилляционные кюветы, заливали 1 мл этилового спирта и оставляли на 16-18 ч, после чего добавляли 10 мл сцинтилляционной жидкости.
Влияние описываемых соединений на экстранейрональный захват катехоламинов изучают на срезах стенки левого желудочка сердца крысы в несколько измененных условиях опыта:
вместо норадреналина-Н3 использовали адреналин-Н3
увеличили количество добавляемого в инкубационную среду адреналина за счет разбавления адреналина-Н3 немеченным адреналином в концентрации 2,5 ˙ 10-6 моль. В опытах был использован адреналин-Н3 в концентрации 0,2 мккюри/мл
сократили инкубацию с адреналином-Н3 до 5 мин, так как для полного осуществления экстранейронального захвата катехоламинов в опытах с перфузией сердца достаточно 2-3 мин.
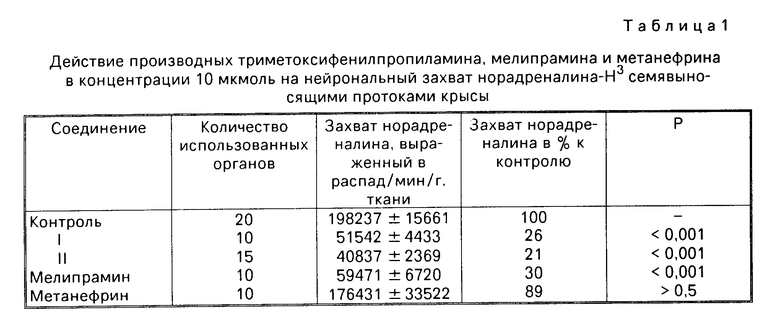
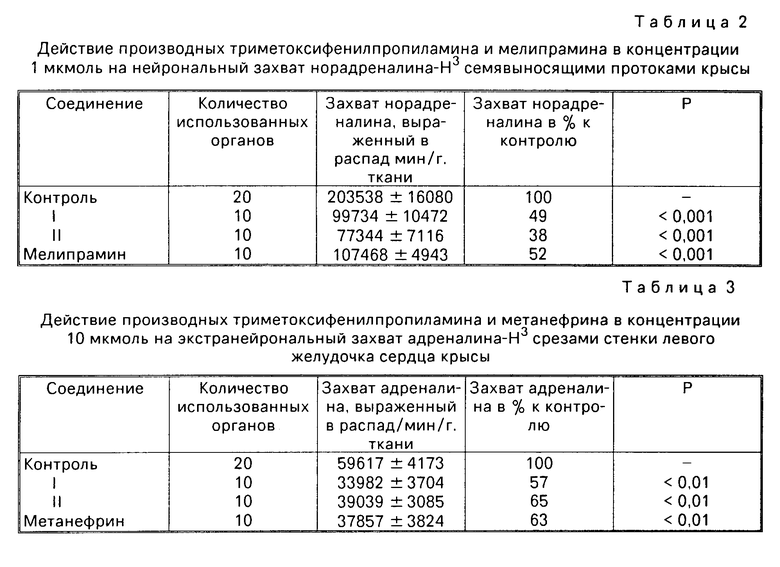
Исследования показали, что соединения в соответствии с настоящим изобретением в концентрации 10 мкмоль обладают наиболее выраженной блокирующей активностью, однако достоверно блокируют захват норадреналина-Н3 также при концентрации 1 мкмоль (таблицы 1 и 2). Статистическая обработка полученных результатов показала, что по блокирующей активности описываемые соединения не отличаются от мелипрамина (Р>0,5). Как и следовало ожидать метанефрин не оказывает достоверного влияния на нейрональный захват норадреналина-Н3 (Р>0,5).
Данные опытов по изучению действия соединений на экстранейрональный захват катехоламинов представлены в табл. 3, из которой видно, что по этому показателю описываемые соединения не отличаются от метанефрина (43-34%).
Определяли острую токсичность описываемых соединений и статистическую достоверность разницы в токсичности вышеуказанных соединений и мелипрамина, а также наиболее активных известных N-(арилалкил)-3-(2,4-диметоксифенил)-1- пропиламинов. Опыты проводили на белых мышах обоего пола весом 18-23 г. Соединения вводили внутрибрюшинно. Каждую дозу вводили шести животным. Число погибших животных регистрировали через 24 ч после введения. Среднюю смертельную дозу подсчитывали по Литчфильду и Уилкоксону. LD50 соединения (I) равна 187(166,7-209,4) мг/кг, соединения II равна 200(144,9-276) мгкг и мелипрамина 91(84-98,7) мг/кг.
Описываемые соединения менее токсичны (Р=0,05), чем и гидрохлориды N-(3-фениолпропил)-3-(2,4-диметоксифенил)-1-про- пиламина в N-(3,3-дифенилпропил)-3-(2,4-диметоксифенил)-1-пропиламина (I).
Таким образом описываемые соединения обладают выраженным блокирующим действием на нейрональный и экстранейрональный захват катехоламинов и менее токсичны, чем известные соединения.
Гидрохлориды N-(арилалкил)-3-(2,4,5-триметоксифенил)-1-пропиламинов общей формулы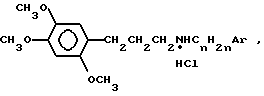
где CnH2nAr -CH(CH3)CH2C6H5 или -CH2CH2CH(C6H5)2,
проявляющие блокирующее действие на нейрональный и экстранейрональный захват катехоламинов.
Авторы
Даты
1995-10-27—Публикация
1982-02-05—Подача