Изобретение относится к электрохимии и неорганической химии, в частности к электрохимическим способам получения отрицательных ионов металлов, и может применяться в аналитической химии для разработки способов количественного определения и отделения рения и в металлургии для получения nopoDiKOB металлического рения.
Целью изобретения является увеличение выхода продукта.
П р и м е р 1. В анодную камеру ячейки вводят 100 г 155%-ной амальгамы натрия, в катодную камеру двухкамерной ячейки - 100 г х.ч. ртути. Далее в катодную и анодную камеры вводят по 50 мл 0,1 М раствора гидроксида натрия, очищенного от кислорода путем обработки его в течение 1 мин 1,5%-ной амальгамой натрия, и в катодное отделение раствор рения (УП) ,в виде перрената натрия до его концентрации 1,25 мг/50 мл (1,34к м). Закрывают камеры ячейки . пришлифованными крышками с отверстиями для ввода двух микроэлектродов и электрохимических ключей, замыкают цепь через миллиамперметр и ведут электролиз при и перемешивании раствора и катода без наложения внешней ЭДС до достижения равенства потенциалов двух микроэлектродов величины - 1,1В (нас. к.э.) и резкого сдвига потенциала ртутного катода при разомкнутой цепи в этот момент до Е -1,8 В. Потенциал 1,1 В достигается за мин электролиза. До момента окончания процесса потенциал ртутного катода при разомкнутой цепи также равен - 1,1 В и отражает процесс образования отрицательных ионов рения - ренида.
После окончания процесса определяют количество ренида в растворе оксидиметрическим методом, вводя в катодную камеру избыток сульфата железа (Ш), подкисленного серной кислотой до 1М (катодную ртуть предварительно сливают). Расчет количества ренида ведут по формуле
MYRe
™fie 1000.8
-количество содержания рения
m в титруемом растворе, г;
NV Re
-нормальность и объем ШпО ;
-атомная масса рения.
Количество реиида равно 1,2ДЗ мг/ /50 мл, что составляет ,6% от исходного количества перрената.
П р и м е р 2. Процесс ведут аналогично примеру 1, но при концентрации перрената 1 ,875 мг/50 мл (2,0.10 м), концентрации ,2 М. Найдено ренида 1,864 мг, что составляет 99,4% от исходного количества рения (УП).
П р и м е р 3. Процесс ведут аналогично примеру 1, но при концентрации перрената 0,625 мг/50 мл (б,7х к 10 м), концентрации NaOH 0,3 М. Найдено ренида 0,607 мг, что составляет 97,2% от исходного количества перрената.
П р и м е р 4. Процесс ведут аналогично примеру 1, но при концентрации перрената - 2,50 мг/50 мл (2,68.10 м), концентрации NaOH 0,1 Н. Найдено ренида 1,820 мг, что составляет 72,8% от исходного количества перрената.
П р и м е р 5. Процесс ведут аналогично примеру 1, но при концентрации перрената 1,25 мг/50 мл (1 ,34. 10 м), концентрации М аОН . 0,05 М. Найдено ренида 0,72 мг, что составляет 58,3% от исходного количества перрената.
П р и м е р 6. Процесс ведут аналогично примеру 1, но при концентрации перрената 1,25 мг/50 мл (1 ,34.), концентрации NaOH 0,37 М. Найдено ренида 1,148 мг, что составляет 91,8% от исходного количества перрената.
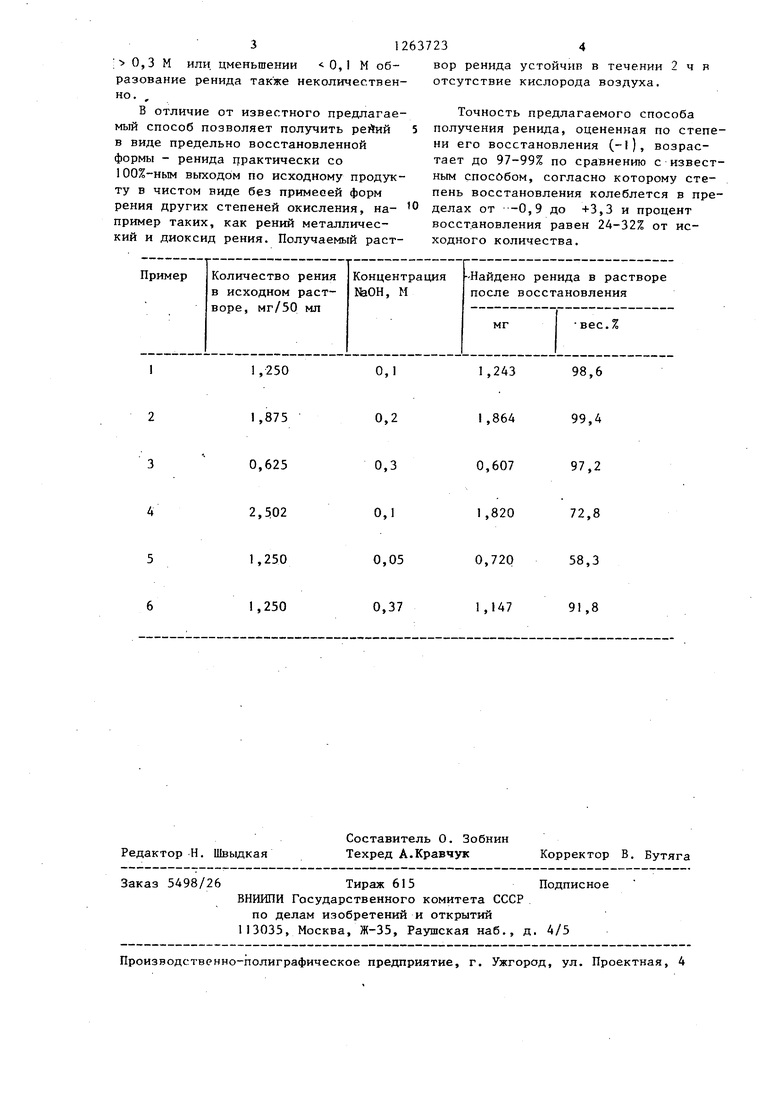
Результаты получения ренида в щелочных растворах ( 18±2С) приведены в таблице.
Как видно из таблицы для количественного получения электролизом щелрчного раствора перрената натрия в
двухкамерной ячейке оптимальными ус ловиями ведения процесса являются 0,1-0,3 М раствора NaOH и концентрация перрената натрия не более 5. 2. ( ;S 2,0 мг/50 мл ).
Ведение процесса при. концентрации перрената 2.10 М нецелесообразно ввиду неколичественного получения ренида, а при концентрации 5.10 М трудно оценить полноту превращения
рения (УП) в ренид ввиду низкой чувствительности оксидиметрического метода определения количеств ренида. При увеличении концентрации NaOH
31
: 0,3 М или цменьшении 0,1 М образование ренида также неколичествен но. ,
В отличие от известного предлагае мый способ позволяет получить рейий в виде предельно восстановленной формы - ренида практически со 100%-ным выходом по исходному продук ту в чистом виде без примесей форм рения других степеней окисления, например таких, как рений металлический и диоксид рения. Получаемый раст637234
вор ренида устойчив в течении 2 ч Р отсутствие кислорода воздуха.
Точность предлагаемого способа 5 получения ренида, оцененная по степени его восстановления (-1), возрастает до 97-99% по сравнению с известным способом, согласно которому степень восстановления колеблется в пре0 делах от -0,9 до +3,3 и процент восстановления равен 24-32% от исходного количества.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения соединений трехвалентного рения | 1980 |
|
SU966118A1 |
| Способ получения триселенида натрия | 1983 |
|
SU1113427A1 |
| Способ получения гексателлурида натрия | 1983 |
|
SU1117339A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РЕНИЯ КИНЕТИЧЕСКИМ ИНВЕРСИОННО-ВОЛЬТАМПЕРОМЕТРИЧЕСКИМ МЕТОДОМ В ПОРОДАХ И РУДАХ | 2012 |
|
RU2506580C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РЕНИЯ В РУДАХ И РУДНЫХ КОНЦЕНТРАТАХ МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2004 |
|
RU2247369C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РЕНИЯ КИНЕТИЧЕСКИМ ИНВЕРСИОННО-ВОЛЬТАМПЕРОМЕТРИЧЕСКИМ МЕТОДОМ В ВОДНЫХ РАСТВОРАХ ПРИРОДНОГО И ТЕХНОГЕННОГО ПРОИСХОЖДЕНИЯ | 2012 |
|
RU2490625C1 |
| Способ получения соединений двухвалентного молибдена | 1981 |
|
SU968100A1 |
| Катализатор для получения соединений азота | 1974 |
|
SU545373A1 |
| Электрохимический способ определения рения в присутствии элементов YI группы | 1989 |
|
SU1684654A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РЕНИЯ И РЕНИЯ В ПРИСУТСТВИИ МОЛИБДЕНА МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2003 |
|
RU2241983C1 |
СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА РЕНИДА Е1АТРИЯ путем восстановления перрената натрия в водном растворе с использованием амальгамы натрия, отличающийся тем,, что, с целью- увеличения выхода продукта, восстановление ведут электрохимически в Диафрагменном электролизере с ртутным катодом и амальгамой натрия в качестве анода в водном растворе гидроксида натрия концентрацией 0,10,3 М перрената натрия 5.10 2.10 моль/л до значения редокс- потенциала в объеме раствора 1,05 -(-1,15) В относительно насьщенного с S каломельного электрода. (Л

| Сперанская Е.Ф., Беленко И.А | |||
| Электроосаждение рения и его сплавов на ртутном катоде | |||
| - В сб.: Рений, Труды 1У Всесоюзного совещания по проблеме рения | |||
| М.: Наука, 1976, с | |||
| Облицовка комнатных печей | 1918 |
|
SU100A1 |
| Карпова Л.А., Беленко И.А., Сперанская Е.Ф | |||
| Восстановление рения (ХУТ амальгамами шелочных металлов.Известия вузов | |||
| Химия и химическая ;технология, 1976, т | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Паровая машина | 1919 |
|
SU1327A1 |
Авторы
Даты
1986-10-15—Публикация
1984-08-21—Подача