Изобретение относится к улучшенному способу получения замещенных амидов аргинина и может быть использовано в различных областях синтетической органической химии, в частности при синтезе хромогенных субстратов для определения активности ферментов, например сериновых протеиназ.
Целью изобретения является увеличение выхода целевого продукта и расширение ассортимента.
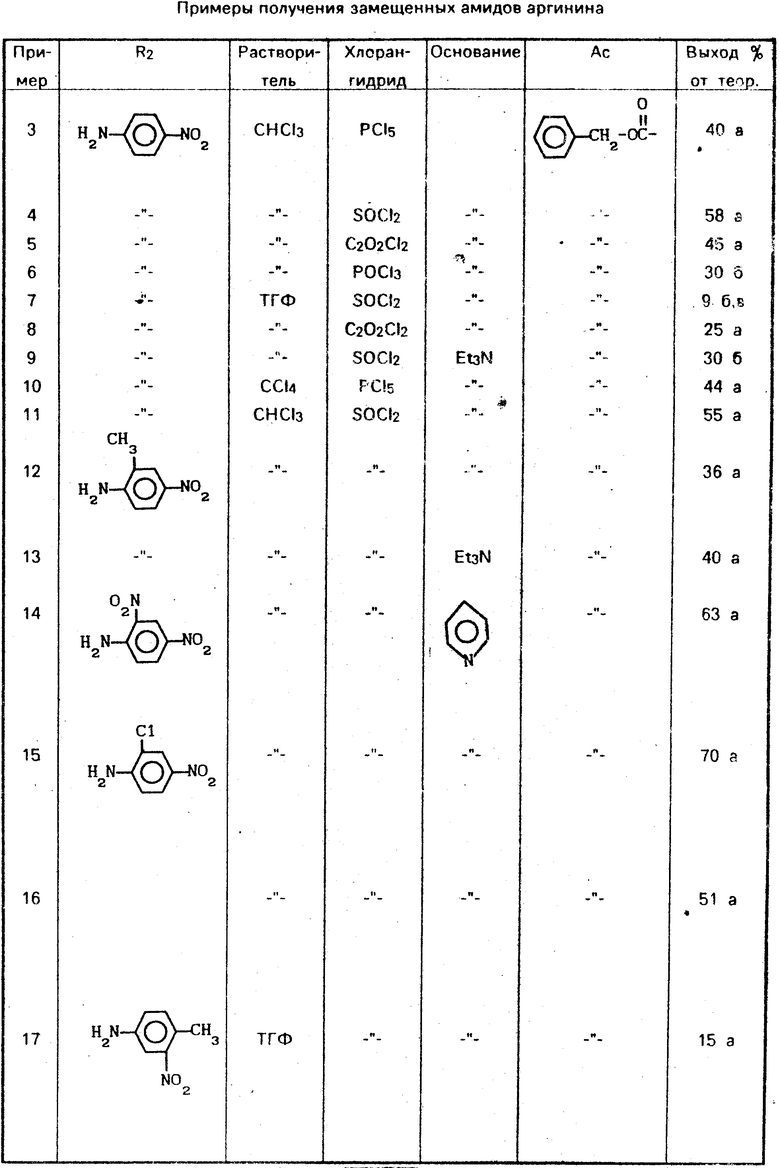
Изобретение иллюстрируется следующими примерами.
П р и м е р 1. К раствору 0,005 моль абс. диметилформамида в 10 мл сухого тетрагидрофурана прибавили по каплям раствор 0,005 моль хлористого тионила в 5 мл тетрагидрофурана при размешивании и охлаждении до (-5)-(-10)оС. К образовавшейся смеси добавили при охлаждении до 0о по каплям раствор 0,005 моль Z Arg в 10 мл ДМФ, полученного кратковременным нагреванием до 85оС и охлаждении до комнатной температуры. Затем к реакционной смеси добавили раствор 0,005 моль п-нитроанилина в 5 мл тетрагидрофурана, содержащего 0,005 моль пиридина. Смесь выдерживали еще 1 ч при комнатной температуре, отгоняли тетрагидрофуран при пониженном давлении и добавили к остатку сначала 2-кратный объем этилацетата, а затем такой же объем гексана. Выпавшее масло растворили в 30 мл смеси ЭA: бутанол (2: 1). Раствор промыли водой, органический слой сушили безводной Na2SO4, отфильтровали и упарили. Остаток затвердел при добавлении сухого эфира. После перекристаллизации из ацетона получили 0,92 г гидрохлорида п-нитроанилида Z-карбобензоксиаргинина (40% от теоретического). Т. пл. 182-3оС; Rf 0,76 (ЭА: ацетон: 50% уксусная кислота - 2: 1: 1), Rf - 0,54 (хлороформ: метанол: конц. NH4OH= 6: 4: 1); λ max этанол= 316 нм, ε max= 1,4 x x 104, [ α ] 20D= -11,6оС (С= 0,2 этанол).
0,5 г гидрохлорида Arg pNA обрабатывали 2 мл 2 н HBr в ледяной уксусной кислоте в течение 45 мин, затем все залили сухим эфиром. Выпавший осадок промыли несколько раз эфиром и высушили в вакуум-эксикаторе над твердым КОН. Выход 2HBr x x Arg pNA 0,47 г (96% от теоретического). Rf - 0,22 (н-бутанол : уксусная кислота : вода= 5: 1: 2), Rf - 0,45 (н-бутанол : уксусная кислота : пиридин : H2O 30,6: 20: 24); λ max этанол= 316 нм, ε max= 1,34 x 104, [ α ] 20D = = -20oC (C= 0,6 H2O).
П р и м е р 2. К суспензии 2,1 г PCl5 в 6 мл CCl4 при перемешивании и охлаждении до -5оС добавлен раствор 1 мл ДМФА в 5 мл CCl4, и через 10 мин при t= 0о раствор 3,1 г карбобензоксиаргинина в 13 мл ДМФА. Через 20 мин к полученному раствору добавлено 1,7 г п-нитроанилина и 5 мл пиридина; смесь перемешивалась 1,5 ч при 20оС и оставлялась "до утра" без перемешивания. К полученной суспензии при перемешивании добавляли 30 мл воды, низший слой отделяли и добавляли к нему 40 мл гексана. Выпавшее масло смешивали с водным слоем и 40 мл бутанола. Бутанольный слой отделяли, водный дважды экстрагировали (10+20 мл) бутанолом, объединенные бутанольные вытяжки упаривали при пониженном давлении до 15 мм, смешивали с 30 мл гексана, масло промывали гексаном, высушивали в вакууме. Добавляли 10 мл 2 М HBr в уксусной кислоте, перемешивали 1,5 ч, добавляли 30 мл сухого эфира, растворитель декантировали, остаток промывали эфиром, растворяли в этаноле и нейтрализовали водн. NH3. Выпадающие при охлаждении кристаллы монобромида нитроанилида аргинина перекристаллизовывали из этанола. Дополнительную порцию продукта можно получить упариванием маточных растворов, растворением остатка в воде, экстракцией бутанолом, упариванием бутанольных вытяжек досуха и кристаллизацией продукта из этанола. Выход 2,92 г (78% от теор. ), спектральные характеристики соответствуют пр. 1.
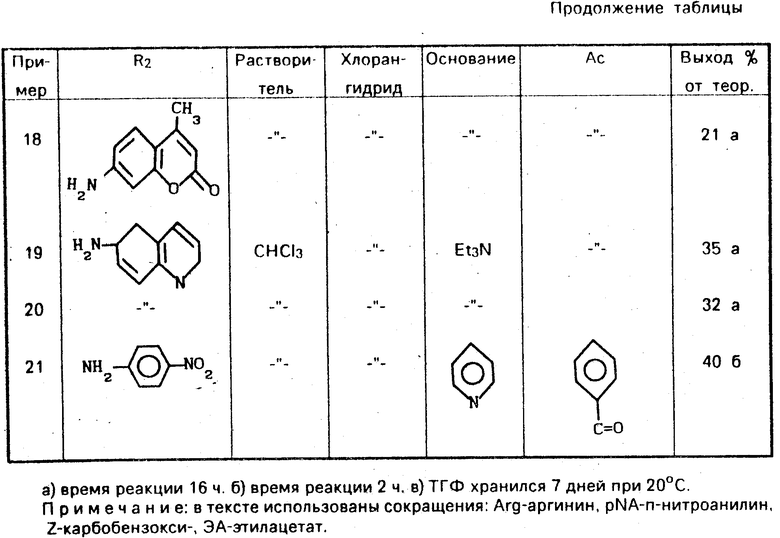
В связи с тем, что при проведении синтеза последовательность операций практически не меняется, другие примеры собраны в таблице.
(56) N. Nishi, S. Tokura, I. Noqucki. Bull. Chem. Soc. Japan, 43(9) z 900-7 (1970).
O. Somorin, N. Nishi, I. Noquchi, Bull. Chem. Soc. Japan, 51(4), 1255-6 (1978).
J. Jacquot - Armend. M. Hill, FEBS Letters, 11,249-53 (1970).
СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ АМИДОВ АРГИНИНА общей формулы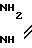 C-
C-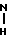 -(CH2)3-
-(CH2)3-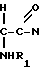 HR2/
HR2/
где R1 - H, C6H5CH2OCO, C6H5CO;
R2 - моно- или дизамещенный Cl-, NO2- или CH3-группой фенил, или 5-хинолил или 6(3-метилкумарин)ил,
или их солей, включающий стадии активирования Nα -ациларгинина или его соли и ацилирования им аминов формулы NH2R2, где R2 имеет указанное значение, в среде органического растворителя в присутствии основания и последующее выделение целевого продукта или его декарбобензоксилирование, отличающийся тем, что, с целью увеличения выхода и расширения ассортимента целевых продуктов, в качестве активирующего агента используют диметилформамидинийхлорид.
Авторы
Даты
1994-03-15—Публикация
1984-07-03—Подача