11280007;
Изобретение относится к микробио- Пример 1. Исходные данные: рН логической промышленности, а именно к основам для питательных сред и способам их получения.
среды 0)2; продолжительность гидролиза 25 мрш; темпера- ура гидролиза
123 С.
Целью изобретения является увеличение выхода целевого продукта, улучшение физических и ростовых свойств питательных сред, приготовленных на предлагаемой основе.
Способ заключается в том, что для 10 та в смеси до гидролиза 100,48 мг%. приготовления основы питательных сред Химические показатели кислотного используют биомассу слизистых бацилл, которые подвергаются комбинированному способу гидролиза, включающему две стадии:15
кислотньй гидролиз, который разлагает белок слизистых бацилл на 20-30% с получением прозрачного гидролизата;
ферментативньй гидролиз как более мягкий и щадящий, который дорас- 20 щепляет остатки биомассы на 55-60%.
Предварительный кислотный гидролиз необходим потому, что биомасса
гидролизата:
Аминеазот, мг% Общий азот,, мг% Степень расщепления, % Хлориды, % Цвет
262,38 1020.0
26
2,08 Темно-корич
незый
Содержание аминсазота увеличивает ся в 2,6 раза.
Данный пример подтверлодает получе .ние кислотного гидролизата с необхослизистых бацилл не может разложиться до нужной степени под действием фермента, ввиду чего получаемый продукт гидролиза (основа для питательной г среды) очень мутен и не пригоден для конструирования питательных сред. Деструкция белка бацилл происходит только под действием кислот, в результате чего получается .прозрачный гидролизат.
Наилучшими условиями получения кислотного гидролизата биомассы слизистых бацилл, используемого в качестве основы для питательных сред, являются: рН среды, в которой приводится гидролиз, 0,45-0,65; t 120- 123°С; время 40-60 мин.
Если при кислотном гидролизе рН среды брать выше 0,45 (0,2-0,3), то ведение гидролиза при такой же температуре (120-123 С) обеспечит необходимую степень расщепления.(20-30%) . за более короткое время (25-35 мин) но гидролизат будет содержать большое количество хпоридов и, как следствие этого, питательные среды приг
25
Данный пример подтверлодает получе- .ние кислотного гидролизата с необходимой степенью расшепления, но он содержит завьшгенное количество хлоридов и имеет плохие физические свойства - темный цветр поэтому недопустимо его применение в качестве осно30 вы для питательных сред.
Если же кислотный гидролиз проводить при рН ниже 0,65 (0,75-150)5 то ведение гидролиза при той же температуре (120-123 С) обеспечит необхо35 димую степень расщепления (20-30%) за более длительный период времени (более 2ч), За этот период времени произойдет так же .деструкция многихС. аминокиспот, необходимых для роста
40 и размножения микроорганизмов. Кроме того, гидролизат будет иметь физическ:: е свойства (темно-коричне- вьй цвет)о
П р и м е р 2 о Исходные данные:
45 рН среды 1,0; продолжительность гидролиза 2 ч 10 мин, t l20°Co
100,0 г С ухой биомассы заливают 4,0 л воды, добавляют 165 мл концентрированной соляной кислоты, гидролиз
готовленные на его основе, будут так- 50 сырья проводят при t°120°C в течение
зйе содержать избыточное количество 2 ч 10 M-IH. Содержание аминоазота в
NaCl, количественное содержание кото- смеси до гидролиза 92,4 мг%.
рого в питательных средах строго ли- Химические показатели кислотного
митировано. Кроме того, произойдет де- гидролизата
струкция многих выделившихся амино- 55 Аминоазот, мг% 130,0
кислот (тирозина, серина, аланина , Общий азот, мг% 690,0
и др.), необходимых для роста микро-- Степень расщеапе 19,8
организмов.
Пример 1. Исходные данные: рН
среды 0)2; продолжительность гидролиза 25 мрш; темпера- ура гидролиза
Пример 1. Исходные данные: рН
123 С.
100,0 г сухой бргомассы заливают 4,0 л воды, добавль ют 300,0 мч концентрированной соляной кислоты, гидролиз сырья проводят при t°123°C в течение 25 мин. Содержание аминоазоа в смеси до гидролиза 100,48 мг%. Химические показатели кислотного
идролизата:
Аминеазот, мг% Общий азот,, мг% Степень расщепления, % Хлориды, % Цвет
262,38 1020.0
26
2,08 Темно-коричнезый
20
25
Содержание аминсазота увеличивается в 2,6 раза.
Данный пример подтверлодает получе- .ние кислотного гидролизата с необходимой степенью расшепления, но он содержит завьшгенное количество хлоридов и имеет плохие физические свойства - темный цветр поэтому недопустимо его применение в качестве осно30 вы для питательных сред.
Если же кислотный гидролиз проводить при рН ниже 0,65 (0,75-150)5 то ведение гидролиза при той же температуре (120-123 С) обеспечит необхо35 димую степень расщепления (20-30%) за более длительный период времени (более 2ч), За этот период времени произойдет так же .деструкция многихС. аминокиспот, необходимых для роста
40 и размножения микроорганизмов. Кроме того, гидролизат будет иметь физическ:: е свойства (темно-коричне- вьй цвет)о
П р и м е р 2 о Исходные данные:
45 рН среды 1,0; продолжительность гидролиза 2 ч 10 мин, t l20°Co
100,0 г С ухой биомассы заливают 4,0 л воды, добавляют 165 мл концентрированной соляной кислоты, гидролиз
Степень расщеапения,
19,8
Хлориды, %0,7ОД
ЦветТемно-коричневый
Данный пример подтверждает получение кислотного гидролизата с необходимой степенью расщепления. Но время гидролиза увеличивается и, как следствие этого, ухудшаются физические свойства гидролизата (темно-ко- ричневйй цвет), что затрудняет его применение как основы для питатель- ных сред.
При еще более низком рН (ниже 2,0) и температуре достигается расщепление биомассы за еще более длительный период времени (более 6 ч) и продукт гидролиза будет иметь плохие физические свойства (темный цвет)
При ведении кислотного гидролиза биомассы при рН 0,45-0,65 в течение 30 мин и менее получается кислотный гидролизат с плохими физическими свойствами и с малой степенью расщепления (до 8%), что приведет к удлинению стадии ферментативного гидролиза (до 4 недель).
Если же проводить гидролиз при рН 0,45-0,65 в течение 30-40 мин при пониженной температуре (60-80 0, то, как и в вьшеприведенном примере, получается кислотньш гидролизат с еще более малой степенью расщепления (до 3-4%) и плохими физическими свойствами (мутный). Гидролиз биомассы соляной кислотой при рН 0,45-0,65, при 120-123°С в течение 40-60 мин деструктирует белок биомассы на 20- 30%, в результате чего продукты гидролиза содержат: смесь разнообразных частиц распада белка и некоторые необходимые для роста микробов амино- кислоты, не подвергшиеся деструкции; минимальное количество хлоридов, которые оказывают отрицательное влияние на ростовые свойства питательных сред; и имеют хорошие физические свойства (по прозрачности и цвету), что позволяет использовать как составную часть основы для питательных сред.
Самостоятельного применения кис- лотный гидролизат иметь не может, так как имеет малую степень расщепления, недостаточную для применения его в качестве основы для питательных сред.
П р и м е р 3. Исходные данные: рН среды 0,45; продоллштельность гидролиза 40 мин при 120 С.
100,0 г сухой биомассы заливают 4,0л в оды, добавляют 260,0 мл концентрированной соляной кислоты, гидролиз проводят при 120°с в течение 40 мин. Содержание аминоазота в смеси до гидролиза 78,6 мг.
Химические показатели кислотного гидролизата:
Аминоазот, мг% 151,2 Общий азот, мг% 750,0 Хлориды, %1,281
Степень расщепления, %%20 Цвет Слабо-коричневы Содержание аминного азота увеличилось почти вдвое.
Получено 3,0 л прозрачного кислотного гидролизата, которьй декантируют и 1,2 л осадка.
Данный пример подтверждает пол.уче ние кислотного гидролизата с необходимыми химическими показателями и хорошими физическими свойствами, что позволяет использовать его как составную часть основы для питательных сред.
П р и м е р 4. Исходные данные: р среды 0,65; продолжительность гидролиза 60 мин при 123°С.
100,0 г сухой биомассы заливают 4,0 л воды, добавляют 220,0 мл концентрированной соляной кислоты, гидролиз сырья проводят при 123°С в течение 60 мин.
Содержание аминоазота в смеси до гидролиза 128,8 мг%.
Химические показатели кислотного гидролизата:
Аминоазот, мг% 240,55 Общий азот, мг% 750,0 Хлориды, %0,980
Степень расщепления, Цвет Слабо-коричневый Получено 3,2 л прозрачного кислотного гидролизата, который декантируют, и 1,0л осадка.
Данный пример подтверждает получение кислотного гидролизата с необ ходимыми химическими показателями и хорошими физическими свойствами, что позволяет использовать его как составную часть основы для питательных сред.
В случае проведения только кислотного гидролиза с применением соляной кислоты для получения гидролизата с необходимой степенью расщепления, применяемого в качестве с)сно- вы для питательных сред, нeoбxo r,имo подействовать на биомассу слизистых бацилл очень крепкой соляной кислотой при рН среды 0,1-0,15, продоллси- тельности более 4,5 ч и 110-120°С,
Как следствие этого , продукты гидролиза будут иметь плохие физические свойства (темно-коричневый), произойдет деструкция многих аминокислотj необходимых для роста микроорганизмов (триптофан, тирозин, аланин, се- рин, метионин и др.) кроме того, продукты гидролиза будут содержать большое количество кислоты, которую необходимо удалить или нейтрализовать. При нейтрализации произойдет образование большого количества хлоридов, т.е. основа будет иметь большую зольность, что недопустимо иметь в основе питательных сред.
Установлено, что хорошие ростовые свойства питательньк сред, приготовленных на основе из гидролизатов биомассы, будут в этом случав; если ос 25 в количестве 1% о объема смеси
среды,, которая оСеспечивает мак мальную активно сть подделудочно лезы при заданной температуре А находится в пределах 7,8-8,0 рН
g регулировать рН среды до требуе пррделсв в процессе гидролиза м ;oбaвлeниeм раствора щелочи или лоты.
Для хорошего роста большинст
10 роорганизмов необходимо, чтобы тельнык средах содержалось опре ное количественное и видовое со ние свободных аминокислот, кото будут освобождаться по мере воз
ВИЯ по,ал елудочной железы на кисл ный остаток биомассы.
П р и м е р 5. Исходные данн среды SjO; температура гидролиз время ри.цролиза 1Э дн.
20 Кислотн)1;й осадэк }. количеств заливают 2,5 л , добавляют фарша лоджелудочнэй нелезы, дов 20%-HbD i раствором NaOH до рН 8, .сервируют хлорофоэмом, добавляя
в
нова будет иметь степень расщепления белков 40-45%. Поэтому для достилсе- НИН этого и для увеличения выхода цв левого продукта с единицы биомассы осадок после кислотного гидролиза до- полнительно подвергают ферментативному гидролизу, как более мягкому и ш;а- дящему, который проводят с применением по;:ркелудочной железы в течение 10- 14 сут, так как в дальнейшем нараста- ет аминоазот в гидролизате крайне незначительно.
Для этого кислотные осадки заливают водой, доводят рН смесидо758 8,0, добавлением 20% NaOH. Фарша под желудочной железы берут из расчета 100 г на 1л жидкости, консервируют хлороформом в количестве 1-1,3% от объема жидкости и термостатирую г при 40-42 - С. Длительность ферментатизно- го гидролиза 10-14 дн. обеспечивает необходимое накопление в гидролизате и нужную степень расщепления сырья pasHjao 53--60%. При меньшем времени воздействия подаелудочной железы (5- 7 Дн) на кислотный остаток биомассы степень расщегшения последнего уменьшается (30-33%) и в гидролизате будут преобладать в основном высокомо-. лекулярные пептиды и пептоны. Ан;шо- гично величина рН среды устанавливается таким образом, чтобы это обеспечивало максимальную активность применяемого фермента. Оптима1: :ьная реакция
в количестве 1% о объема смеси
среды,, которая оСеспечивает максимальную активно сть подделудочной железы при заданной температуре АО-42 С, находится в пределах 7,8-8,0 рН. 0трегулировать рН среды до требуемых пррделсв в процессе гидролиза можно ;oбaвлeниeм раствора щелочи или кис-- лоты.
Для хорошего роста большинства микроорганизмов необходимо, чтобы в пиога- тельнык средах содержалось определенное количественное и видовое содержание свободных аминокислот, которые будут освобождаться по мере воздейстВИЯ по,ал елудочной железы на кислотный остаток биомассы.
П р и м е р 5. Исходные данные: рН среды SjO; температура гидролиза 42°С,. время ри.цролиза 1Э дн.
Кислотн)1;й осадэк }. количестве 1,0л заливают 2,5 л , добавляют 330,ОГ фарша лоджелудочнэй нелезы, доводят 20%-HbD i раствором NaOH до рН 8,0; кон- .сервируют хлорофоэмом, добавляя его
в количестве 1% о объема смеси
гид42 С в течение 10 дн в
в
рОЛИ3уют при термостате,
Сод(ержание амилоазота в смеси до термос гатирования 128,8 мг%,
Химические показатели ферментативного гпдролизата:
мг
644,42 1150
56
Аминоазот Обгл.ий азот5 м: % Степень расще ше- ния %
Получено 3s3 л прозрачного оЬерме тативного гидролизата с необходимой ;Д.ая основы питательньк сред степенью расщепления з минимально короткий срок „
П р 7Л м е р 6, Исходные да:-п-1ые: рН среды 7,8„ тймлература гидролиза ,, зфемя гидролиза 14 дн,
KHCJiOTHbM гидр1:1лязат в количестве 1,0 л заливают 2,) л воды, добавляют 350-., О г фарша поджелудочной жеде зы5добавляют 20% p sствор; МаОН до рН 7, консернируют хлорооЬормом в количестве 1% объема жидкоетИр гидролиз ведут npi-i 40 С в течение 14 дн в термостате ,
Содефжак ие ажиюазота в смеси до термостатирования 88,4 мг.
Хим-1-(ческие покг1затели ферментативного Г1-;дролизата
/iMHHoasoT, мг/о
06пц-:й азот,, мгл
Стег{ень расщеги;е
НИ.Я „ %
638..4
51
Получено 3,2л прозрачного ферментативного гидролизата с необходимой для основы питательных сред степенью расщепления в максимально короткий срок.
Для хорошего роста большинства микробов необходимо, чтобы в питательной среде в среднем количество аминоазота было в пределах 25-30% от общего азота.
Смешив ание ферментативного и кислотного гидролизатов в соотношении 1:1,17-1:1,3 позволяет получить основу с необходимой степенью расщепления (40-45%) и, как следствие, из такой основы можно приготовить питательные среды с необходимым содержанием аминного и общего азота (содержание аминоазота 395-470%, а общего белка 100-1100 мг%).
С повьшением ферментативного гидролизата в этом объеме смеси увеличивается степень расщепления основы (до 55%), но ростовые свойства основы от этого не улучшаются
2800078
ние нерационально и экономически невыгодно, так как это должно привести к увеличению расхода ферментативного гидролизата, более дорогостоя2 щего, чем кислотный.
Выбранные оптимальные соотношения прозрачных фракций ферментативного и кислотного гидролизатов биомассы слизистых бацилл способствуют
JO достижению цели изобретения. .
Смесь вьщерживают при 5-7°С 4- 5 дней для вьтадения нерасщепленных белков ферментативного гидролизата, инактивации ферментов, установления
15 стабильности рН и содержания аминного азота. За этот срок происходят аналогичные пр оцессы.
Фракции могут храниться длительное время в холодильной камере или
20 бытовом холодильнике. Кислотная
фракция, имеклдая рН 0,45-0,65, хранится до 2-х лет при 5-8 С,Ферментативная фракция хранится при этой же температуре до одного года. Консерван- Следова- 25 том для нее является хлороформ,
который добавляется согласно литературным данным из расчета 0,1%.
тельно, увеличение ферментативного гидролизата нерационально и экономически не выгодно, так как себестоимость его гораздо выше кислотного гидролизата ввиду длительности процесса первого и, следовательно, требует больших энергозатрат.
С понижением содержания ферментативного гидролизата уменьшается степень расщепления основы (до 30%) и, как следствие, ростовые свойства пи- тательньк сред резко ухудшаются.
С повышением содержания кислотного гидролизата в этом объеме смеси степень расщепления основы незначитель- 40 основе, по сравнению с питательными но повышается (до 48%), но одновре- средами, приготовленными на основе менно происходит и повьипение содержания Nad (1,0-1,3), что недопустимо.
С понижением содержания кислотного
Смесь ферментативного и кислотно- 30 го гидролизатов хранится при той же температуре до одного года. Добавка консерванта и его количество такие же, что у ферментативного гидролизата.
35 П р и м е р 7. Из данной основы готовили питательные среды для контроля стерильности и плотные питательные среды. Причем чувствительность сред, приготовленных на этой
казеина, одинакова, а в некоторых случаях превосходит при значительно меньшем содержании аминоазота.
гидролизата в смеси степень.расщепле- 45 расход основы на 1 л питательния основы повьш1ается (до 50%), содержание NaCl в ней уменьшается, но ростовые свойства питательных сред, приготовленных из этой основы, не улучшаются, следовательно, уменьше40 основе, по сравнению с питательными средами, приготовленными на основе
Смесь ферментативного и кислотно- 30 го гидролизатов хранится при той же температуре до одного года. Добавка консерванта и его количество такие же, что у ферментативного гидролизата.
35 П р и м е р 7. Из данной основы готовили питательные среды для контроля стерильности и плотные питательные среды. Причем чувствительность сред, приготовленных на этой
основе, по сравнению с питательными средами, приготовленными на основе
казеина, одинакова, а в некоторых случаях превосходит при значительно меньшем содержании аминоазота.
50
ных сред, приготовленных из гидролизата Bacillus micilagenosus, меньше расхода гидролизата казеина.
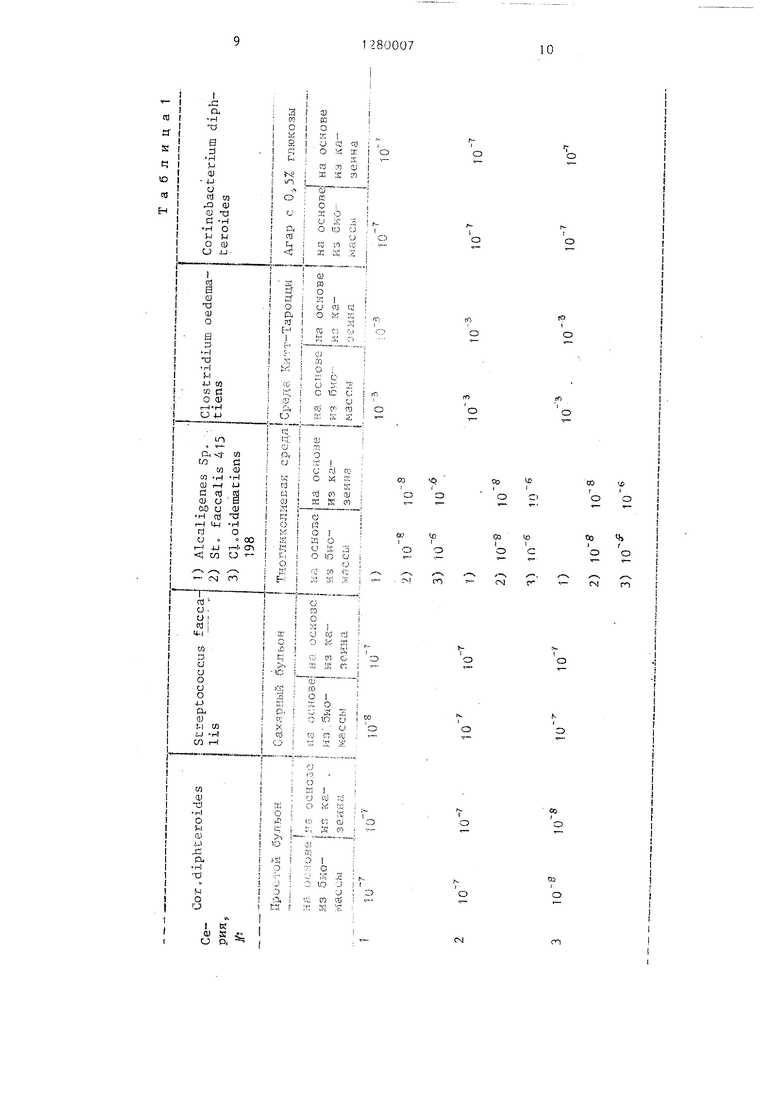
Сравнительные ростовые свойства представлены.в табл.1.
I ts;
Щ Я ii о о,
t о
о
о
f9 О
О
О
со
о
о
Преимуществом пре,, соба Получения основы бацилл является заме:; го дефицитного птпево: са и др. (казеина), о ходимости ЕВеде.ПИЯ е щие полученную оснотзу: фоста, так как она с обходимые компоненты ния и вьзделения иршроор а
1 кг СЬфЬЯ (биомасс,; С Л КЗ ЦИЛЛ) можно ПрИГО Г Т; .U
за больше питатель -ьгк сое и той же концентрацией аь: та (120 мг%)з чем кз новы,, полученной кз (pecj.:e гидролизатов дровкей,
Формула 3 о б i Способ приготовления а
микробиологических ;-,. Э:
0007)4
,7У :--1йтриваюи ий ферментативный гид ол1:з нсходлЪй биомассы микроорга- низмо; ноджелу,ОЧНОЙ железой, о т- . - и q -о щ и 11 с я теМ; что, с целью увеличер ия вьгхода целевого продукта к улучшег:ия физических и росто- выу свойс Г в гштательных сред в качестве ИСХОДНО1 биомассы использ пот слизистые бацилль;,; которые предвари- - TejibHc псдвергггот гидролизу в раство- ое соляной кислоты при рН 0,45-0,65
12 О- -12 5 С в течение MJ мин,, затем декантации, а ти в н о -лу г и,цр ОЛИ з у п од в а р - -:енньш декантации :оН 7,8-8; О в течение от 10 , лиозрачмые фракции фермен- л KHc,i;ovi:oro гидролизатов ::; еоо Ц-готепни 1;1.17 при Ь-7 С в тече





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения белкового гидролизата из коллагенсодержащих отходов производства белковой колбасной оболочки | 1982 |
|
SU1074901A1 |
| Способ получения питательной среды для производства биомассы @ @ | 1983 |
|
SU1124029A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПАНКРЕАТИЧЕСКОГО БЕЛКОВОГО ГИДРОЛИЗАТА И ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ БИФИДОБАКТЕРИЙ С ЕГО ИСПОЛЬЗОВАНИЕМ | 2002 |
|
RU2253673C2 |
| Питательная среда для получения рестриктирующих эндонуклеаз из бактерий рода НаеморнILUS | 1987 |
|
SU1479507A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИТАТЕЛЬНОЙ ОСНОВЫ И ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ МИКРООРГАНИЗМОВ РОДА YERSINIA И VIBRIO | 2007 |
|
RU2360962C2 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ГЛУБИННОГО КУЛЬТИВИРОВАНИЯ ХОЛЕРНОГО ВИБРИОНА | 2010 |
|
RU2425866C1 |
| "Питательная среда "Церебробакт" для культивирования лактобацилл" | 1991 |
|
SU1808008A3 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ БИФИДОБАКТЕРИЙ И ЛАКТОБАЦИЛЛ"ЭПИДЕРМАТ" | 1992 |
|
RU2039814C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕЛКОВОГО ГИДРОЛИЗАТА | 1994 |
|
RU2061039C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫРАЩИВАНИЯ ВОЗБУДИТЕЛЯ ТУЛЯРЕМИИ | 2006 |
|
RU2333948C2 |
Изобретение относится к микробиологической промышленности, а именно к основам для питательных сред и способам их получения. С целью увеличения выхода целевого продукта, улучшения физических и ростовых свойств питательных сред в качестве основы используют биомассу слизистых бацилл, которую сначала подвергают гидролизу в растворе соляной кислоты при рН 0,45-0,65: 120-123 с в течение 30- 40 мин, а затем полученный после декантации прозрачной фазы осадок подвергают ферментативному гидролизу поджелудочной железой при рН 7,8-8,0; 40-42°С в течение 10-14 дней. Прозрачные фракции ферментативного и кислотного гидролизатов смешивают в соотношении 1:1,17-1:1,3 и выдерживают при 5-7°С в течение 4-5 дней. Полученная основа имеет необходимое содержание общего и аминного азота 1000-1100 и 393-470 мг Соответственно, полностью удовлетворяет потребность в углероде, который содержится в аминокислотах(всего 17 аминокислот из них 10 незаменимых) иполисахарХнах и не требует добавления ростовых факто-. ров, так как содержит витамины группы В и А и микроэлементы. 3 табл. i (Л 1C с

| Методические указания по использованию утративших срок годности кровезаменителей для конструирования микробиологических питательных сред | |||
| М., 1980 | |||
| Способ получения питательной основы | 1978 |
|
SU742463A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
1986-12-30—Публикация
1985-03-12—Подача