(21)4292496/28-13
(22)30.07.87
(46) 15.05.89. Бюл. N 18
(71)Центральный научно-исследовательский институт вакцин и сывороток им. И.И.Мечникова
(72)В.М.Поляченко, В.А.Мельникова, И.М.Грубер, Э.-Л.Ю.Кюдулене, В.М.Раскин и Г.А.Смирнова
(53)577.14(088.8)
(56)Kilan М., The prokariotes. A. handboo R. on habiotats isolation and indentification of bacteria/
ed. M.P.Starr e.a. Springer. Verlag, 1982, v. 2, pp. 1371-1382.
M.Takanatai, Methods in Molecular Biology, ed. R.B.Wickner, 1974, v. 7, pp. 113-124.
(54)ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ПОЛУЧЕНИЯ РЕСТРИКТИРУ70ЩИХ ЭНДОНУКЛЕАЗ ИЗ БАКТЕРИЙ РОДА HAEMOPHILUS
(57)Изобретение относится к области микробиологии и молекулярной биологии, в частности к получению рестрикционных эндонуклеаз. Целью изобретения является повышение выхода целевого продукта. Питательная среда состоит из ингредиентов, включающих источник азота, источник витаминов НАД, ГЕМИН и соль. В качестве азотного питания используют аминопептид - ферментативный гидролизат крови животных, и кислотный гидролизат казеина средней степени расщепления, а в качестве витаминного препарата - экстракт кормовых дрожжей (ЭКД). Питательная среда имеет следующий состав, мас.%: аминопептид 0,35-0,45; гидролизат казеина 0,35-0,45; ЭКД 0,1-0,2; НАД 0,0002; гемин 0,001; хлористый натрий 0,1-0,15; дистиллированная вода остальное. Предлагаемая среда позволяет повысить выход ферментов рестрикции более чем в 10 раз по сравнению с известной средой. 4 табл.
с
Ј

| название | год | авторы | номер документа |
|---|---|---|---|
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ АНАЭРОБОВ | 1992 |
|
RU2086646C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫРАЩИВАНИЯ БАКТЕРИЙ РОДА HAEMOPHILUS | 2006 |
|
RU2320714C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ И ВЫДЕЛЕНИЯ ВОЗБУДИТЕЛЕЙ ГНОЙНЫХ БАКТЕРИАЛЬНЫХ МЕНИНГИТОВ, СУХАЯ (ВАРИАНТЫ) | 2011 |
|
RU2471865C1 |
| Способ получения эндонуклеаз-рестриктаз, обладающих способностью узнавать и расщеплять последовательности нуклеотидов 5 @ -GPUCGPYC-3 @ и 5 @ -CATG-3 @ | 1987 |
|
SU1458388A1 |
| Штамм гетеротрофных бактерий Klebsiella pneumonia - ассоциант для получения микробной белковой массы | 2018 |
|
RU2687137C1 |
| Штамм бактерий BacILLUS LIснеNI FоRмIS - продуцент рестриктазы В @ 13I | 1989 |
|
SU1650697A1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ ЛЕЙШМАНИЙ | 1992 |
|
RU2086644C1 |
| Питательная среда для культивирования MIcRococcUS LUтеUS ВКПМ В-2836 - продуцента сайт-специфической эндонуклеазы MLU1 | 1989 |
|
SU1693041A1 |
| Способ получения эндонуклеазы рестрикции, узнающей и расщепляющей последовательность нуклеотидов 5 @ - TGATCA-3 @ | 1990 |
|
SU1724689A1 |
| Штамм бактерий BacILLUS aLVeI - продуцент рестриктазы BaV В II | 1990 |
|
SU1761803A1 |
Изобретение относится к микробиологии и молекулярной биологии, в частности к получению рестрикционных эндонуклеаз. Целью изобретения является повышение выхода целевого продукта. Питательная среда состоит из ингредиентов, включаюших источник азота, источник витаминов НАД, гемин и соль. В качестве азотного питания используют аминопептид - ферментативный гидролизат крови животных, и кислотный гидролизат казеина средней степени расщепления, α в качестве витаминного препарата - экстракт кормовых дрожжей (ЭКД). Питательная среда имеет следующий состав, мас.%: аминопептид 0,35-0,45
гидролизат казеина 0,35-0,45
ЭКД 0,1-0,2
НАД 0,0002
гемин 0,001
хлористый натрий 0,1-0,15
дистиллированная вода остальное. Предлагаемая среда позволяет повысить выход ферментов рестрикции более чем в 10 раз по сравнению с известной средой. 3 табл.
Изобретение относится к биотехнологии, молекулярной биологии, в частности к получению рестрикционных эндонуклеаз.
Цель изобретения - повышение выхода целевого продукта.
Изобретение заключается в том, что в известной питательной среде, содержащей источник азотного питания, источник витаминов, НАД, гемин и соль, в качестве источника азота (используют ферментативный гидролизат |крови животных (аминопептьд) в сочетанин с гидролизатом казеина средней степени расщепления, в качестве источника витаминов - экстракт кормовых дрожжей.
Используемый аминопептид представляет собой Ферментативный гидролизат, полученный из крови крупного рогатого скота с помощью гидролиза поджелудочной железой. Гидролизат казеина средней степени расщепления изготавливается из казеина путем гидролиза соляной кисчотой.
со ел о vl
Питательную среду приготавливают следующим образом.
Ишредиенты смешивают в заданном соотношении, добавляют дистиллирован ную воду до 1 л, нагревают до кипения, устанавливают рН 7,2-7,4, разливают в бутыли и стерилизуют при 121СС в течение 15 мин. В среду добавляют необходимые для гемофилов факторы роста НАД и гемин в количестве 2 и 10 мг/л.
Культивирование штаммов гемофиль- ньк бактерий, продуцентов ферментов рестрикции осуществляют в ферментере с рабочим объемом 2л, а также в бутылях объемом 5 л на аппарате для встряхивания при 60-70 качаний в 1 мин Сбор биомассы проводят в конце фазы экспоненциального роста - начале ста ционарной фазы.
Рестриктирующую эндонуклеазу получают следующим образом.
Бактериальные клетки собирают и разрушают ультразвуком с последующим центрифугированием при 48 OOOg в течение 1 ч для получения бесклеточного экстракта, из которого выделяют ферменты рестрикции методом ионообменной хроматографии на колонке с фосфоцеллкшозой Р 11 фирмы Ватман. Все процедуры по получению бесклеточного экстракта и выделению ферментов проводят при 4°С.
Рестриктазную активность определя ют общепринятым методом разделения фрагментов ДНК фага / в 1%-ном ага- розном геле.
Пример 1 (оптимальный). Готовят питательную среду следующего состава, мас.%:
Аминопептид0,4
Гидролизат казеина 0,4 Экстракт кормовых
дрожжей (ЭКД) 0,15 НАД0,0002
Гемин0,001
Хлористый натрий 0,12 Дистиллированная вода Остальное Пример 2 (минимальный). Гото
вят питательную среду следующего тава, мас.%:
Аминопепгид0,35
Гидропичат казеина0,35 Экстракт кормовых
дрожжей0,1
НАД0,0002
Гемин0,001
Хлористый натрий0,1
5 0
5 0
5
0
5
0
5
Дистиллированная вода Остальное Пример 3 (максимальный). Го товят питательную среду следующего состава, мас.%:
Аминопептид0,45
Гидролизат казеина 0,45 Экстракт кормовых др ожжей0,2
НАД0,0001
Гемин0,002
Хлористый натрий 0,15 Дистиллированная вода Остальное Данные по выходу клеточной биомассы и удельной рестриктазной активности на предлагаемой и известной среде для штамма Н. influenzae Re B-2297 приведены в табл. 1.
Аналогичные данные для штамма-продуцента рестриктаз Hind II, III H. influenzae Rd В-2072 приведены втабл.2.
Аналогичные результаты получены также при исследовании следующих штаммов: Н. influenzae Rf B-2296 (продуцент рестриктазы Hinf I), Н. haemoliticus B-1 841 (продуцент рестриктаз Hha I, Hha II) и H.aegyp- tius B-2709 (продуцент рестриктазы Пае III).
Таким образом, используемая среда может применяться для выращивания различных видов рода Haemophilus.
Используемая среда обеспечивает выход биомассы, сравнимый с выходом на известной среде, однако содержание ферментов рестрикции в культуре продуцента, полученной на предлагаемой среде, превышает более чем в 10 раз.
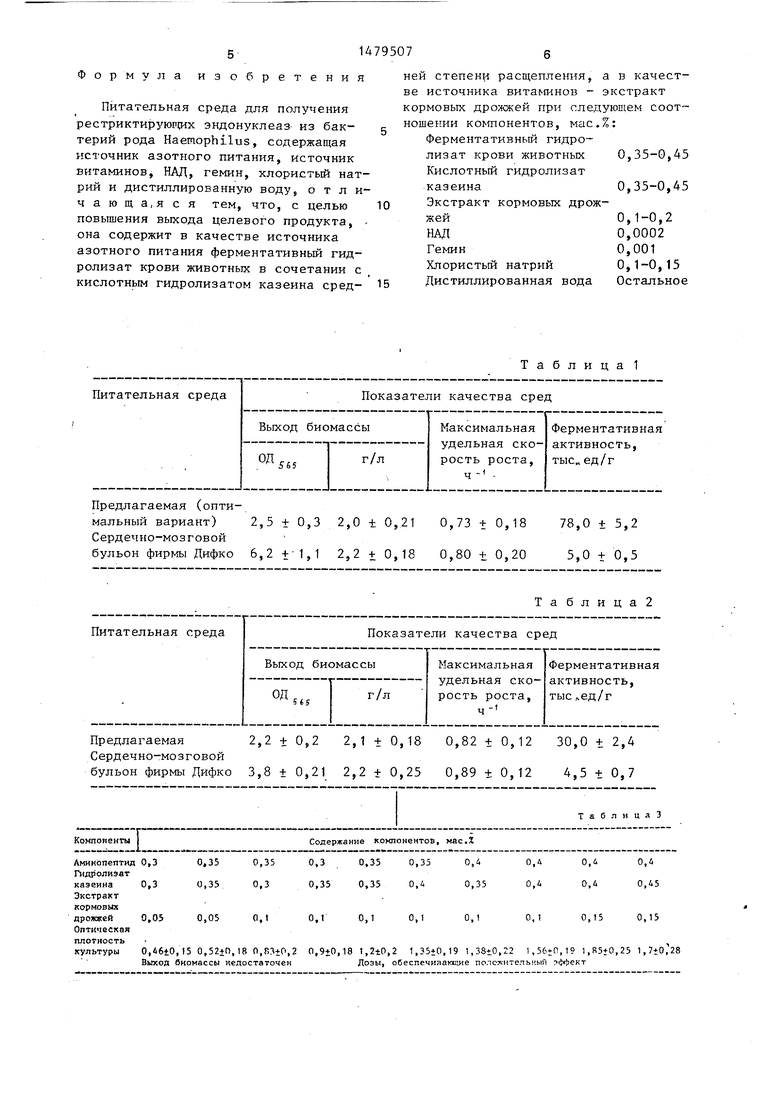
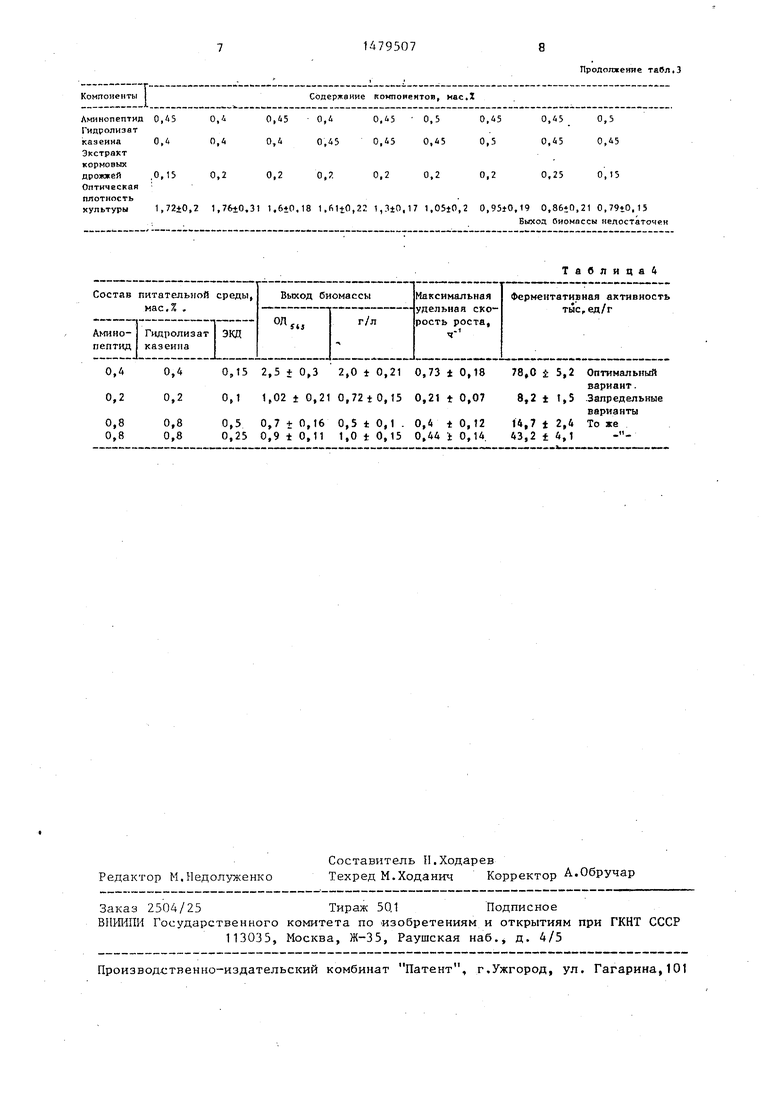
Изменение содержания компонентов используемой среды по сравнению с оптимальным вариантом как в сторону уменьшения, так и увеличения, приводит к снижению выхода биомассы. Данные представлены в табл. 3. В табл. 4 приведены данные, характеризующие ростовые свойства предлагаемой питательной среды в зависимости от величины навесок используемых ингредиентов и содержание ферментов рестрикции в полученных на этих средах культурах штамма-продуцента Н. influenzae Re B-2297. Среда, приготовленная по примеру 1, является оптимальным вариантом и обеспечивает не только максимальную продуктивность по выходу биомассы, но также и максимальную ферментную активность культуры продуцента.
51479507
ормула изобретения
не ве ко но
Питательная среда для получения рестриктирующих эндонуклеаз из бак- терий рода Haemophilus, содержащая источник азотного питания, источник витаминов, НАД, гемин, хлористый натрий и дистиллированную воду, о т л и- чающа.яся тем, что, с целью повышения выхода целевого продукта, - она содержит в качестве источника азотного питания ферментативный гид- ролизат крови животных в сочетании с кислотным гидролизатом казеина сред-
Таблица 1 Питательная средаПоказатели качества сред
Выход биомассы Максимальная Ферментативная
1 удельная ско- активность,
г/л рость роста, тыс„ед/г
ч Предлагаемая (оптимальный вариант) 2,5 + 0,3 2,0 + 0,21 0,73 + 0,18 78,0 ± 5,2 Сердечно-моз говой бульон фирмы Дифко 6,2 + 1,1 2,2 ± 0,18 0,80 ± 0,20 5,0 + 0,5
Таблица2 Питательная средаПоказатели качества сред
Выход биомассы Максимальная Ферментативная
удельная ско- активность,
ОД г/л рость роста, тыс„ед/г
a 15.
Ч
Предлагаемая 2,2 + 0,2 2,1 ± 0,18 0,82 ± 0,12 30,0 ± 2,4
Сердечно-мозговой
бульон фирмы Дифко 3,8 ±0,21 2,2+0,25 0,89+0,12 4,5 ±0,7
ТаблнцаЗ
Компоненты IСодержание компонентов, мас.%
Аминопептид 0,3 0.35 0,35 0,3 0,35 0,35 0,4 0,4 0,4 0,4 Гидролиза
казеина 0,3 0,35 0,3 0,35 0,35 0,4 0,35 0,4 0,4 0,45 Экстракт кормовых
дрожжей 0,05 0,05 0,1 0,1 0,1 0,1 0,1 0,1 0,15 0,15 Оптическая
плотность ,
культуры 0,46+0,15 0,52+0,18 0,81+0,2 0,9+0,18 1,2±0,2 1,35+0,19 1,38+0,22 1,56+0,19 1,85+0,25 1,7±0,28 Выход биомассы недостаточенЛозы, обеспечилающие по-тсм1те1Ь ыГ - ффект
ней степени расщепления, а в качестве источника витаминов - экстракт кормовых дрожжей при следующем соотношении компонентов, мас.%:
Ферментативный гидролизат крови животных 0,35-0,45
Кислотный гидролизат
казеина0,35-0,45
Экстракт кормовых дрожжей
НАД
Гемин
Хлористый натрий
0,1-0,2 0,0002 0,001 0,1-0,15
Дистиллированная вода Остальное
Экстракт
кормовых
дрожжей ,0,15 0,2 0,2 0,7 0,2 0,2 0,2 0,25 0,15
Оптическая
плотность
культуры1,72±0,2 1,76+0.31 1,6+0.18 1,fi1tO,22 1,3±0,17 1,05±0,2 0,,19 0,86+0,21 0,79+0,15
Выход Оиомассы недостаточен
0,40,40,152,5 ± 0,32,0 ± 0,210,73 ± 0,18
0,20,20,11,02 ± 0,210,72t0,150,21 t 0,07
0,80,80,50,7 t 0,to0,5 t 0,1 .0,4 0,12
0,80,80,250,9 ± 0,111,0 t 0,150,44 3t 0,14
Продолжение табл.З
Тавлица4
i 5,2 Оптимальный
вариант.
t 1,5 Запредельные варианты
t 2,4 To же
t 4,1
eti-
Авторы
Даты
1989-05-15—Публикация
1987-07-30—Подача