Изобретение относится к получению конъюгатов биологически активных соединений и аминоэтилсефарозы,- которые могут быть использованы в медицине для фоторадиационной терапии опухолей и для диагностики онкологических заболеваний.
Цель изобретения - получение водорастворимых конъюгатов, обладающих радиозащитным действием и способностью локализоваться в опухолевых клетках
Пример 1. Ди-(глицил)-амид- мезопорфирин 1Х-агарозао
Раствор 68 мг (0,1 ммоль) ди- (глицил)-амид-меяопорфирина IX (1) в 10 мл 50%-ного водного диметилфор- мамида (ДМФА) смешивают с 5 мл раствора 100 мг 1-этнл-3-(3-диэтиламино- пропил)карбодиимида (ЭДК) в воде, рН смеси доводят до 5 с помощью 6 н. соляной кислоты, добавляют 10 мл объема аминоэткпсефарозы и суспензию перемешивают 16 ч при О С в темноте.
3
Гель отделяют на пористом стеклянном фильтре, проминают смесью Д№А - вода (1:2, 1:1) (по 50 мл), водой (50 мл) и нагревают в течение 2 ч при 75°С в 50 мл 50%-ной уксусной кислоты. Полученный красный раствор упаривают несколько раз с водой для удаления АсОН, остаток растворяют в 5 мл воды
684289&
НС1, лиофилизуют и получают 120 мг водорастворимого конъюгата, содержащего 0,10 мг (III) на 1 мг сухой массы конъюгата спектрофотометрический метод; для порфирина (III): А1Д07 500; А4Дв0 138.
П р и м е р За (см. табл.1).
П р и м е р 4. Гематопорфирин




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения -сульфоната в-цепи инсулина человека | 1977 |
|
SU696011A1 |
| ПОЛИМЕРНЫЙ КОНЪЮГАТ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2130462C1 |
| СПОСОБ ИММОБИЛИЗАЦИИ БИОЛОГИЧЕСКИ АКТИВНОГО ВЕЩЕСТВА (БАВ) НА НОСИТЕЛЬ (ВАРИАНТЫ) И КОНЪЮГАТ БАВ-НОСИТЕЛЬ, ПОЛУЧЕННЫЙ ДАННЫМИ СПОСОБАМИ | 2008 |
|
RU2409669C9 |
| Способ получения пептидов с последовательностью актг-человека,содержащих в -конечном положении аминооксикислоту | 1973 |
|
SU490284A3 |
| Способ получения пептидов | 1976 |
|
SU639446A3 |
| Способ получения пептидов | 1971 |
|
SU454736A3 |
| Способ получения ариламидов @ -защищенных аминокислот и пептидов | 1982 |
|
SU1051062A1 |
| СОЛИ 2,7,12,18-ТЕТРАМЕТИЛ-3,8-ДИЭТИЛ-13,17-ДИ-(3-ДИМЕТИЛАМИНОПРОПИЛ)-ПОРФИРИНА, ОБЛАДАЮЩИЕ ПРОТИВОЛУЧЕВОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1985 |
|
SU1287521A1 |
| Способ получения тетрапептидов или их кислотно-аддитивных солей | 1981 |
|
SU1082319A3 |
| Способ получения гидрохлорида @ -6-аминогексилгликозида-N-ацетилмурамоил-L-аланил-Д-изоглутамина | 1988 |
|
SU1558927A1 |
Изобретение относится к получению конъюгатов биологически активных соединений и аминоэтилсефарозы, которые могут быть использованы в медицине для фоторадиапионной терапии опухолей и для диагностики онкологических заболеваний. Изобретение позволяет получить водорастворимые конъюгаты, обладающие радиоэащитным действием и способностью локализоваться в опухолевых клетках за счет того, что производные порфиринов, выбранные из группы, содержащей ди-(глицил)-амид- мезопорфирин IX, ди-(фенилаланил)- амидмезопорфирин IX, ди-(аланил)- амид-мезопорфирин IX, гематопорфирин и 1,3-диметоксиэтилгематопорфирин, ковалентно присоединяют к аминоэтил- сефарозе и полученный иммобилизованный лиганд нагревают в течение 1-3 ч при 75-80вС в 0,1-0,5 н. соляной кислоте, 50-80/Ј-ной уксусной кислоте или в 0,1-0,3 н. растворе едкого натра, содержащем 0,1-0,15 мас.% бор- гидрида натрия. 3 табл. « IB
и лиофилизуют. Выход водорастворимо
конъюгата 100 мг. Здесь и в других примерах для определения содержания порфирина в конъюгате последний (45 мг) нагревают в 5 мл 1 н. НС1 в течение 2 ч при 80 С. и определяют поглощение полученного раствора при 547 и 590 нм, считая поглопение исходного порфирина (I): Т5 ° 500Ч
А 1ТО 4 Ч О
А 590- Jt
Пример 1а. Осуществляют аналогично примеру 1, лишь вместо 50%- ной АсОН используют 65% АсОН.
П р и м е р 2 о Ди-(фенилаланил)- амид-мезопорфирин 1Х-агароза.
Суспензию 86 мг (0,1 ммоль) ди- (фенилаланил)-амид-мезопорфирина IX (II) в смеси (13:6) ДМФА - вода, содержащую 100 мг водорастворимого ЭДК, перемешивают 16 ч при 20 С с 10 мл аминоэтилсефарозы, поддерживая рН 5,5 с помощью 6 н. НС1. Гель промывают 100 мл смеси (2:1) ДМФА - вода, 100 мл воды, солюбилизируют 3 ч при 80°С в 50 мл 0,1 н. НС1, лифилизуют и получают 140 мг водораст
воримого конъюгата. Содержание порфи рина в полученном конъюгате (0,2мг/м сухой массы) определяют спектрофото- метрически, принимая поглощение порфирина (II): .
П р и м е р 2а. Осуществляют аналогично примеру 2, но вместо 0,1 н. НС1 используют 0,3 нс НС10
Приме р 3. Ди-(аланил)-амид- мезопорфирин 1Х-агароза.
Раствор 70,8 мг (0,1 ммоль) ди- (аланил)-амид-мезопорфирина IX (III) в 15 мл ДМФА смешивают с 5 мл ъодкого раствора 100 мг ЭДК и 7 мл аминоэтилсефарозы. Суспензию перемешивают 2,5 ч при 20°С (рН 4,7-5,0), гель отфильтровывают, промывают на фильтре 100 мл смеси (1:1) ДКФА - вода, 100 мл смеси (2:1) ДМФА - вода и окончательно водой (200 мл) до отсутствия порфирина в промывных водах (контроль по поглощению при 400 нм). Яркоокрашенный гель солюбилизируют 1 ч при 75°С в 60 мл 0,5 н.
JQ агароза.
20
25
Раствор 67,1 мг (0,1 ммоль) гема- топорфирина (IV) в 10 мл ДМФА добавляют пррциями за 3 раза к суспензии 10 мл аминоэтилсефарозы в 12 мл воды и одновременно добавляют 100 мл твердого ЭДК, поддерживая рН 4,7-5 (с помощью 0,1 н. NaOH), смесь перемешивают 2 ч при 20°С и через 16 ч при О С гель фильтруют, промывают до отсутствия порфирина в промывных водах смесями ДМФА - вода (1:1 - 1:2) по 50 мл и окончательно водой (100 мл). Твердый остаток солюбилизируют 2 ч при 7Ь°С в 100 мл 0,1 н. NaOH, содержащем 0,1%-ную NaBH4. Полученный раствор диализуют против 2 л дистиллированной воды в течение 16 ч и лиофилизуют. Выход водорастворимого конъюгата 80 мг. Содержание 30 гематопорфирина (IV) 0,1 мг/кг сухой массы, считая поглощение порфирина (IV): , ,27.
П р и м е р 4а. Осуществляют аналогично примеру 4 (измерения см. в табл.1).
П р и м е р 4б. Гематопорфирин- агароза.
Методом, описанным в примерах 4 и 4а, из 67,1 мг (0,1 ммоль) гематопорфирина (IV) и 10 мл аминоэтилсефарозы получили окрашенный гель, для солюбилизации которого (после удаления несвязавшегося (IV) промыванием геля) использовали 100 мл 0,5 н. Д5 NaOH в присутствии 0,2%-ной NaBH.. Полученный красный раствор диализова- ли 16 ч против 2 л дистиллированной воды и лиофилизовали. Выход водорастворимого конъюгата 70 мл, а содержание гематопорфирина 0,06 мг/мг сухой массы (метйд анализа по примеру 4).
П р и м е р 5. 1,3-Диметоксиэтил- гематопорфирин-агароза (V).
К суспензии 10 мл аминоэтилсефарозы в 15 мл воды добавляют за 3 раза раствор 70 мг (0,1 ммоль) 1,3-димет- оксиэтил-гематопорфирина (V) в 10 мл ДМФА и твердый ЭДК (150 мг), поддерживая рН 4,7-5,0 с помощью 0,1 н.
35
40
50
NaOH. Суспензию перемешивают 2 ч при - 20° С и 16 ч при О С, фильтруют, гель на фильтре промывают смесью ДМФА - вода (1,5:1) до отсутствия поглощения при 400 нм в фильтрате (100 мл) и водой, солюбилизируют 2 ч при 75°С в 50 мл 0,1 нс НС1. Выход водорастворимого конъюгата 100 мг, содержание порфиринл (V) 0,2 мг/1 мг сухой массы конъюгата, принимая поглощение порфирина (V): АКа°..,5, AWo
II р и м е р 5а. Осуществляют аналогично примеру 5 (изменения см. в табл.1)о
П р и м е р 6. Ди-(фенилаланил)- амид-мезопорфирин 1Х-агароза,
Раствор 7 мл упакованного объема аминоэтилсефарозы в 20 мл обрабатывают 2 ч при 20 С раствором 40 мг (0, ммоль) ди-(фенилаланил)-амида- мезопорфирина IX в 30 мл ДМФА, в присутствии пиридина добавляют порциями 1 г твердого дициклогексилкарбо- диимида и через 10 ч при 20 С смесь концентрируют до 20 мл, фильтруют и фильтрат хроматографируют на колонке с сефадексом С-25, уравновешенной ДМФА, окрашенную фракцию, выходящую с исключающимся объемом, упаривают досуха, остаток солюбилизируют 2 ч при 75°С в АО мл 80%-ной уксусной кислоты, диализуют против воды и лио- филиэуют. Выход конъюгата 60 мг. Содержание порфирина 0,2 мг/мг сухой массы (см. пример 2).
П р и м е р 7. Холостой опыт (в отсутствие конденсирующего агента- ЭДК).
Суспензию 10 мл аминоэтилсефароэы в 15 мл воды перемешивают 2 ч при 20°С 16 ч при 0°С с раствором 70 мг 1,3-диметоксигематопорфирина
10
15
полисахариде при осуществлении реакции присоединения бея конденсирующег агента - ЭДК; 2) при гельхроматогра- фии на сефадексе С 25 окрашенный , конъюгат выходит с колонки с исключающимся объемом (пример 6); 3) при центрифугировании образцов всех кот югатов в пробирках через мембранный фильтр, пропускающий вещества с моле кулярной массой менее 10 кДа, проход менее 10% нанесенного образца конъюгата,
Пример8. Ди-(глицил)-амид- мезопорфирин 1Х-агароза.
Полученный в примере 1 ярко-красный гель (условия конденсации и коли чества исходного порфирина (I) и ами ноэтилсефарозы те же, что и в приме- 20 ре 1) нагревают 1 ч при 75 С в 50 мл 65%-ной уксусной кислоты, упаривают несколько раз с водой для удаления уксусной кислоты, остаток растворяют в 5 мл воды и лиофилизуют. Выход 25 водорастворимого конъюгата 100 мг, содержание порфирина 9,5 мг (определено по примеру 1)о
П р и м е р 9. Ди-фенилаланил)- амид-мезопорфирин 1Х-агароза.
Методом, описанным в примере 2, из 86 мг порфирина (II) и 10 мл амин этилсефарозы получают окрашенный в красный цвет гель, который солюбили- зируют 2 ч при 80°С в 50 мл 0,3 н. НС1, лиофилизуют и получают 130 мг водорастворимого конъюгата, содержащего 14 мг (II) исходного порфирина (спектрофотометрический метод анализ как в примере 2).
30
35
40
Пример -10 (ср.). Ди-(аланил) амид-мезопорфирин 1Х-агароза.
Из 70,8 мг ди-(аланил)-амид-мезо- порфирина (III) и 7 мл аминоэтилсефа
(V) в 10 мл ДМФА (рН 4,7-5,0). Далее, 45 розы мет°Д°м описанным в примере 3,
получают красный гель, для солюбилиз ции которого используют 50 мл 0,5 н. НС1 (нагревание 3 ч при 85°С). Солюб лизированный продукт лиофилиэуют, ра
как описано в примере 5, гель промывают на стеклянном фильтре смесью ДМФА - вода (1,5:1) до отсутствия поглощения при 400 нм в фильтрате (100 мл), затем водой (200 мл). Фильтрат упаривают, сушат и выделяют 69,5 мг исходного порфирина (V). Остающийся на фильтре гель бесцветный.
Наличие ковалентных связей биологчески активного вещества с полисаха- ридным носителем доказано следующими фактами:
1) при проведении холостого опыта (пример 7) отсутствует порфирин на
5
полисахариде при осуществлении реакции присоединения бея конденсирующего агента - ЭДК; 2) при гельхроматогра- фии на сефадексе С 25 окрашенный , конъюгат выходит с колонки с исключающимся объемом (пример 6); 3) при центрифугировании образцов всех югатов в пробирках через мембранный фильтр, пропускающий вещества с молекулярной массой менее 10 кДа, проходит менее 10% нанесенного образца конъюгата,
Пример8. Ди-(глицил)-амид- мезопорфирин 1Х-агароза.
Полученный в примере 1 ярко-красный гель (условия конденсации и количества исходного порфирина (I) и аминоэтилсефарозы те же, что и в приме- 0 ре 1) нагревают 1 ч при 75 С в 50 мл 65%-ной уксусной кислоты, упаривают несколько раз с водой для удаления уксусной кислоты, остаток растворяют в 5 мл воды и лиофилизуют. Выход 5 водорастворимого конъюгата 100 мг, содержание порфирина 9,5 мг (определено по примеру 1)о
П р и м е р 9. Ди-фенилаланил)- амид-мезопорфирин 1Х-агароза.
Методом, описанным в примере 2, из 86 мг порфирина (II) и 10 мл аминоэтилсефарозы получают окрашенный в красный цвет гель, который солюбили- зируют 2 ч при 80°С в 50 мл 0,3 н. НС1, лиофилизуют и получают 130 мг водорастворимого конъюгата, содержащего 14 мг (II) исходного порфирина (спектрофотометрический метод анализа как в примере 2).
0
5
Пример -10 (ср.). Ди-(аланил)- амид-мезопорфирин 1Х-агароза.
Из 70,8 мг ди-(аланил)-амид-мезо- порфирина (III) и 7 мл аминоэтилсефарозы мет°Д°м описанным в примере 3,
получают красный гель, для солюбилиза- ции которого используют 50 мл 0,5 н. НС1 (нагревание 3 ч при 85°С). Солюби- лизированный продукт лиофилиэуют, растворяют в 10 мл воды, выпавший красный осадок отщепившегося от полисаха- ридного носителя порфирина отделяют . на фильтре, фильтрат диализуют против 1,5 л дистиллированной воды (16 ч)
и снова лиофилизуют. Выход водорастворимого продукта 80 мг, содержание исходного порфирина (III) 7,5 мг.
П р и м е р 11. Гематопорфирии- агароза.
71684289
Раствор 67,1 мг (0,1 ммоль) гема- топорфирина (IV) в 10 мл диметилфор- мамида () постепенно добавляют к суспензии 10 мл аминоэтилсефарозы в 12 мл воды, одновременно добавляют 100 мг твердого ЭДК (рН 4,7-5,0) с помощью 0,1 н. NaOH, смесь перемеши8
вают 2 ч при 20°С и 16 ч при , гель фильтруют, промывают до отсутствия порфирина в промывных водах смесями ДМФА - вода (1:1) и (1:2) (по 50 мл) и окончательно водой (100 мл). Твердый остаток нагревают 2 ч при
Ю
нетоксичных для интактных клеток дозах вносили в инкубационную среду через 3-5 мин после облучения на рентгеновской установке РУМ-7 в дозе 4 г при мощности дозы 0,4 г/мин и фильтре 0,47 мм А1.
Из табл.3 видно, что лечебное действие ди-(фе нилала нил)-амидме з опорфи- рина IX-агароза, гематопорфирина- агароза и 1,3-диметоксиэтилгематопор- фирин-агароза сопоставимо с терапевтическим действием некоторых биополимеров, таких как ДНК и РКК, но отли75 С в 100 мл 0,1 н. NaOH, содержаще- ., чается от них стабильностью результат
го 0,15%-ной NaBH4. Полученный красный раствор диализуют против 2 л дистиллированной воды (16 ч) и лиофшшзуют. Выход водорастворимого конъюгата 75 мг, содержание иматопорфирина (IV) 7,6 мг (спектрофотометрическое определение) .
Пример 12(ср.) 1,3-Диметокси- этилгематопорфирин-агароза.
Методом, описанным в примере 5, из 70 мг 1,3-диметоксиэтилгематопор- фирина (V) и 10 мл аминоэтилсефарозы получают гель, который при нагревании в 50 мл 0,1 н. НС& за 0,5 ч при 77°С растворился не полностью, красный фильтрат лиофилизуют и получают 60 мг конъюгата, содержащего 0,15 мг исходного порфирина (V) на 1 мг сухой массы конъюгатао
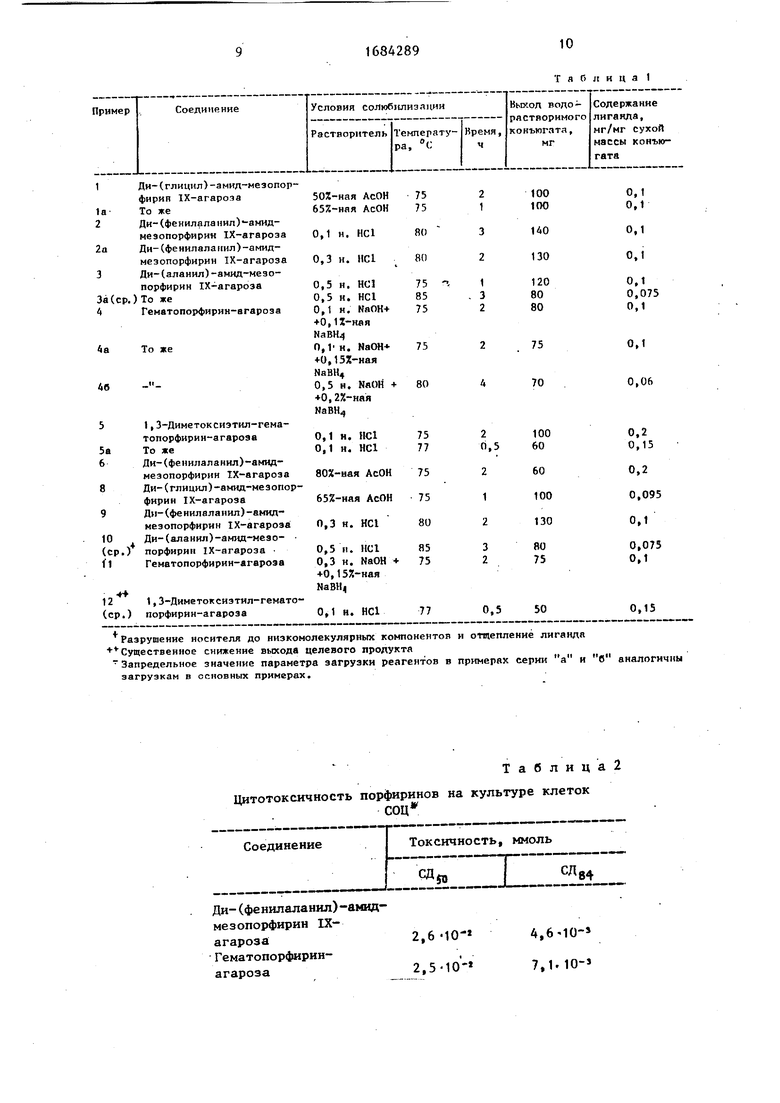
Данные примеров приведены в табл.1.
В табл.2 представлены результаты изучения токсических свойств получаемых конъюгатов . Из табл.2 видно, что полученные соединения относятся к группе низкотоксичных веществ.
Радиозащитное действие полученных соединений были изучены in vitro.
Эксперименты in vitro проводили на асинхронной культуре клеток сердца обезьяны циномольгус (СОЦ), выживаемость клеток оценивали по методике Пака и Маркуса. Порфирины и ДНК в
20
25
30
тов, а также близки по значению с ранее изученным биологически активным порфирином-дикалиевой солью 2,4 ди(оЈ-метоксиэтил)дейтеропорфирина-1Х.
Формула изо бретения
Способ получения конъюгатов на основе производного сефарозы, включающий ковалентное присоединение лиган- дов к производному сефарозы с последующей химической модификацией иммобилизованного лиганда, отличающийся тем, что, с целью получения водорастворимых конъюгатов, обладающих радиозащитным действием и способностью локализоваться в опухолевых клетках, в качестве лигандов используют производные порфирина, выбранные из группы, включающей ди- (глицил)-амид-мез опорфирин IX, ди- (фенилаланил)амид-мезопорфирин IX, ди-(аланил)-амид-мезопорфирин IX, гематопорфирин и 1,3-диметоксиэтил- гематопорфирин, в качестве производного сефарозы - аминоэтилсефарозу, а химическую модификацию осуществляют нагреванием иммобилизованного лиганда в течение 1-3 ч при 75-80°С в 0,1- 4,j 0,5 н. соляной кислоте или в 50-80%- ной уксусной кислоте, или в 0,1-0,3 н. растворе едкого натра, содержащем 0,1-0,15 мас.% боргидрида натрия.
35
40
8
нетоксичных для интактных клеток дозах вносили в инкубационную среду через 3-5 мин после облучения на рентгеновской установке РУМ-7 в дозе 4 г при мощности дозы 0,4 г/мин и фильтре 0,47 мм А1.
Из табл.3 видно, что лечебное действие ди-(фе нилала нил)-амидме з опорфи- рина IX-агароза, гематопорфирина- агароза и 1,3-диметоксиэтилгематопор- фирин-агароза сопоставимо с терапевтическим действием некоторых биополимеров, таких как ДНК и РКК, но отли0
5
0
тов, а также близки по значению с ранее изученным биологически активным порфирином-дикалиевой солью 2,4 ди(оЈ-метоксиэтил)дейтеропорфирина-1Х.
Формула изо бретения
Способ получения конъюгатов на основе производного сефарозы, включающий ковалентное присоединение лиган- дов к производному сефарозы с последующей химической модификацией иммобилизованного лиганда, отличающийся тем, что, с целью получения водорастворимых конъюгатов, обладающих радиозащитным действием и способностью локализоваться в опухолевых клетках, в качестве лигандов используют производные порфирина, выбранные из группы, включающей ди- (глицил)-амид-мез опорфирин IX, ди- (фенилаланил)амид-мезопорфирин IX, ди-(аланил)-амид-мезопорфирин IX, гематопорфирин и 1,3-диметоксиэтил- гематопорфирин, в качестве производного сефарозы - аминоэтилсефарозу, а химическую модификацию осуществляют нагреванием иммобилизованного лиганда в течение 1-3 ч при 75-80°С в 0,1- ,j 0,5 н. соляной кислоте или в 50-80%- ной уксусной кислоте, или в 0,1-0,3 н. растворе едкого натра, содержащем 0,1-0,15 мас.% боргидрида натрия.
5
0
загрузкам в сгионных примерах.
Таблица
Цитотоксичность порфиринов на культуре клеток
СОЦ
Соединение
Ди-(фенилаланил)-амидмезопорфирин IXагароза2,6-10-
Гематопорфиринагароза2,5-10-
Таблиц. 1
Токсичность, ммоль СД,
5U5L1684289
СоединениеТоксичность, ммоль
СД 50
t 3-Диметоксиэтилгематопорфирин-агароза 1, 3,
Дикалиевая соль
2,4-ди-(б6-метоксиэтил)дейтеропорфирина-IX1,9-10- 3,8.10-3
1,3,5,8-тетраметил2,4-диэтил-6,7-ди(диметилпропиламМоний)-порфириндиметансульфонат1,6 3,
СОЦ - сердце обезьян циномольгус.
Таблиц аЗ
Радиозащитное действие конъюгатов на культуре клеток СОЦ
Соединение Эффективная Противолучевая доза соедине- эффективность, ния, ммоль/мл %
ПРД при ЛД70
Ди-(фенилаланил)-амидмезопорфирин 1Х-агароза1 52,3± 3,9
Гематопорфиринагароза1,,7±7,4
1,3-Диметоксиэтилгематопорфиринагароза1,8 И ,7 ±5,2
ДНК0,1 мг/мл 53,4±3,4
Дикалиевая соль 2,4ди-(ot-метоксиэтил)дейтеропорфирина-IX1 10 67,3+3,9
U
Различия с контролем при Р 0,05 достоверны
Составитель О.Рокачевская Редактор М.Келемеш Техред М.Дидык Корректор М.Шароши
Заказ 3483ТиражПодписное
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР 113035, Москва, Ж-35, Раушская наб., д. 4/5
Производственно-издательский комбинат Патент, г.Ужгород, ул. Гагарина,101
12
Продолжение табл.2
| Lipson R, e.a | |||
| The use a derivative of hematoporphyrin irt fumoz detection - J« Na tl | |||
| Судно | 1925 |
|
SU1961A1 |
| Evensen J0F | |||
| e.a | |||
| Photodynamic therapy of C,jH mouse mammary carcinoma with hematoporphyrin di - ethers es Sentitizers | |||
| - Br0 J0 Cancer, v.55(b), T981, p | |||
| Способ генерирования переменного тока | 1923 |
|
SU483A1 |
| Тужилкова Т.Н | |||
| и др | |||
| Радиозащитные свойства порфириноВо - Радиобиология, т.17, 1977, выл.2, с | |||
| Арматура для железобетонных свай и стоек | 1916 |
|
SU259A1 |
| Способ получения адсорбентов,содержащих аминогруппы | 1982 |
|
SU1054353A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
Авторы
Даты
1991-10-15—Публикация
1988-08-16—Подача