Изобретение относится к способу получения солей мурамилпептидов - новых биологических активных соединений, которые могут найти применение в медицине.
Цель изобретения - получение новых производных в ряду мурамилпептидов, обладающих более высокой антивирусной активностью и низкой токсичностью.
Пример 1. 3,60 г(5,66 моль (Со1-)-п-бутилового эфира N-ацетилму- рамил-Ь-аланил-Б-глютаминовой кислоты, 0,6 моль воды и 0,88 г(7,54ммоль) N-оксисукцинимида при непрерывном перемешивании растворяют в 20 мл сме- си хлороформа и метанола при объемном соотношении 4:К В смесь вводят 1,6 г (7,54 ммоль) твердого дициклогексил- карбодиимида и по каплям в течение 4 ч при комнатной температуре добавляют раствор 3,7 (4,72 ммоль) натриевой соли Ь-аланил-2-(1,2-дипальмито- ил-глицеро-3-оксифосфорил-окси)-этил- -амида в 40 мл хлороформа. Смесь вы держивают 1 ч, упаривают на роторном иоплрителе, к остатку добавляют 200 мл диоксана, раствор лиофилизуют
Продукт суспендируют в 100 мл хло- роформа, добавляют 600 мл эфира уксусной кислоты, смесь при непрерывном перемешивании охлаждают в ледяной бане в течение 1 ч. Нерастворившиеся частичци дициклогексилкарбодиимида отфильтровьшают, фильтрат упаривают Остаток растворяют в 14 мл смеси хлороформа-метанола и воды 70:30:5 (объемное соотношение) и очищают на колонке (диаметр 4,5 см, длина 80 см) запол14,енную 700 г геля кремневой кислоты 60 (Мерк, 70-230 Меш, ASTM) в указанной смеси растворителей. Прого- ;Няют 500мл указанной смеси, затем этой же смесьюэлюируют продукт, собирая фракции объемом 10 мл № 133-152 и 153- 236, их раздельно подвергают диофильт- радии. Процент основной фракции растворяют в 300 мл бидистиллированной воды, быстро нагревают до 40 С, после охлаждения центрифугируют, удаляя нерастворившиеся частички дицикло- гексилмочевины.
Надосадочную жидкость подают в диализатор (Амикон Корпорейшн, Дан- вер, Массачуает, 01932 США, модель Ц02, ультрафильтр РМ, 10176 мм диаметр, инертный, неонный полимер на основе полисульфона, средняя ве
0
5
личина пор 10 А) ц, подвергают диализу при 4 атм техн. против ,5 л бидистиллированной воды, 0,5 л буферного раствора фосфата-хлорида натрия (по 0,1 М, 1:1, рН 7) и 1,5 л воды полного вымывания хлоридов.
Полученный продукт диализа ( 70 мл) стерильно фильтруют на фильтре с милипорами (0,2 мкм) и лиофилизируют. ;Ползгчают натриевую соль N-ацетшт- -мурамил-Ь-аланил-Б-глютамил-(Cd) - -н-бутилэфир-(сг)-Ь-аланин-2-(1,2- -дипалмитоил-Зп-глицеро-З-окси-фос- форилокси)-этиламида (3,4 моль Н О) в виде бесцветного порошка в количестве 4,13 г (67% от теории):
+ 14 + °с (с 0,44; вода);
Rf 0,37 (хлороформ:метанол:во- да 70 : 30 : 5);
Rf 0,64 (этиловый эфир уксусной кислоты : н-бутанол-пиридин:уксусная кислота:вода - 42:21:21:6:10)
Рассчитано, %: С 54,77; Н 8,94; N 5,07; Р 2,24; Н ,0 4,71
СбьН issOjoNsPIIa 0,41 Н20(1381,63)
Найдено, %: С 54,3; Н 9,1; N 5,6; 2,3, H,jO 4,7.
Рассчитано: Na 1,75
.s (1316,59)
Найдено;: Na 1 ,57 .
Исходный продукт получают следующим образом.
5,5 г (8,1 ммоль) (с)-п-бутил-(с)- -бензилэфир-4,б-О-изопропилиден-N- -ацетил-мурамил-Ь-аланил-П-глютами- новой кислоты растворяют в 60 мл 60%-ной уксусной кислоты и оставляют на ночь при комнатной температуре. Желтоватый раствор выпаривают приблизительно наполовину на роторном ис-, парителе при , лиофилизуют.
4,8 г (7,5 ммоль) полученного продукта растворяют в 100 мл смеси диметоксиэтана и воды (9:1), смешивают с 0,8 г катализатора, состоящего из окиси палладия на угле (10%--ный) и в течение 4 ч обрабатывают водородом, катализатор отфильтровьшают. Фильтрат упаривают, остаток чистят дважды хроматографией на геле кремневой кислоты 60 (Мерк, 1:200, фракции 10 и 5 мл) в системе хлороформ: метанол: вода 70:30:5. Фракции, содержашие.продукт, объединяют, упаривают.
Полученный продукт частично представленный в В1оде натриевой соли
5
0
5
31
(из геля кремневой кислоты) растворяют в АО мл бндистйллата и пропускают через 50 мл хорошо очищенного ионо- обменника (Dowex 50w х 8 50/100 меш, форма Н) колонку промьгоагот 100 мл бидистиллата, элюат фильтруют через фильтр с миллипорами 0,2 МкМ и ли- офилизуют. Получают 3,7 г (697, от теории) (Со1)-п-6-утиленэфира-Ы-аце- тил-мурамил-Ь-аланил -В-глютаминовой кислоты в виде бесцветного порошка, содержащего 0,6 моль воды.
Сс З +45 j ГС (с 1,142, метанол) ;
Rf 0,23 (хлороформ:метанол:вода 70:30:5);
Rf 0,40 (Н-бутанол:уксусная кис- лота:вода 75:7,5:21),
Исходный материал получают следующим образом.
4,4 г (11 ммоль) натриевой соли К-ацетил-4,6-0-изопропилиден-мура- миловой кислоты (2,5 моль, 1 г) суспендируют в 60 мл диметилформамида. При интенсивном перемешивании после- довательно добавляют 4,4 г (П моль) хлоргидрата (Со(.)-п-бутиловый эфир- (Сс.)-бензш1овый эфир Ь-аланил-В-глю таминовой кислоты, 2,53 г (22 ммоль N-оксисукцинимида и 2,5 г (12,1 ммол дициклогексилкарбодиимида , смесь перемешивают в течение ночи при комнатной температуре.
Для переработки суспензии последнюю разбавляют 100 мл этилового зфи- ра уксусной кислоты и после получасового размешивания при О С отфильт- ровьгоают нерастворившиеся частички (дициклогексамочевина, хлорид натрия Фильтрат упаривают в вакууме при 30°С, остаток вводят в 400 мл уксусного эфира и экстрагируют биди тил- лированной водой (10x50 мл)о После сушки органической фазы и упаривания растворителя остается 5,6 г (Cot)-п- -бутилэфира-( Col)-бензилэфира N-аце- ТШ1-4,6,О-изопрополиден-Ъ-аланил-В- -глютаминовой кислоты в виде аморфного порошка (75% от теории).
/ot/ +30 + 1°С (с 0,732; мета- нол);
Rf 0,87 (хлороформ:метанол:во- да 70:30:5);
Rf 0,83 (h-бутанол:уксусная кис лота:вода /5:7,5:21).
Исходный продукт получают следующим обраэом.
5 O
5
0
0
5 -
0
164
5,6 г (12,1 ммоль) ()-п-бутил- эфир-(су)-бензилэфира N-третичн. бу- тилоксикарбонил-Ь-аланил-В-глютами- новой кислоты растворяют в 20 мл абс, этилэфира уксусной кислоты, при ин тенсивном перемешивании и исключении попадания влаги по каплям вводят 50 мл 4,5 н. соляной кислоты в абс. уксусном эфире и смесь оставляют стоять в течение часа при 0°С. Желтоватый раствор упаривают при комнатной температуре приблизительно до 20 мл, смешивают с 150 мл диоксана и лиофилизируют.. Получают 4,75 г (97% от теории) гидрохлорида (Сс)-п-бу- тилэфир-(С J )-бензилэфир-Ь-аланил-В- -глтотаминовой кислоты в виде бесцветного масла
+19 + (С 0,313; метанол) ;
Rf 0,58 (хлороформ:метанол:вода 70:30:5);
Rf 0,56 (этил-эфир уксусной кислоты: п -бутанол:пиридин:вода 42:21:6:10).
Исходный продукт получают следующим образом.
К 8,5 г (25,8 ммоль) гидрохлорида- (Cct)-п-бутилэфир-(С у) -бензилэфир-D- -глютаминовой кислоты и 7,4 г (25,8 ммоль) N-трет.бутилоксикарбо- нил-Ь-аланин-К-оксисукцинимидэфира. растворенных в 150 мл диметилформамида, добавляют 2,6 г (25,7 ммоль) N- метилморфолина и смесь оставляют стоять в течение 20 ч при комнатной температуре. Прозрачный желтый раствор выпаривают в вакууме при 30 С, полутвердый остаток вводят в 500 мл этилового эфира уксусной кислоты и экстрагируют семь раз безводным сульфатом натрия. Остаток после выпаривания уксусного эфира чистят на 600 г геля кремневой кислоты 60 (Мерк, размер зерна 70-230, меш ASTM) в системе хлороформ:метанол 98:2. Продукт в-фракциях 36-82 собирают и высушивают. Получают (Col)- -бутил- эфир- (С 4)-бензилэфир-К-трет. -бутнлок- сика рбонил-Ь-аланин-В-глютаминовой кислоты в виде бесцветного масла (6 г, 50% от теории).
oLl. - 1°С (с 0,315; ди- метилформамид);
. .Rf 0,73 (хлороформ:изопропанол: :уксусная кислота 70:8:2);
Rf 0,75 (п-бутанол:уксусная кислота: вода 75:7,5:21).
Исходный продукт получают следующим образом.
К 11,0 г (30 ммоль) (Сы)-п-бутил- эфир-(С3)-бензилэфира Ы-трет.-бути - локсикарбонил-В-глютаминовой кислоты растворенного в 25 мл абс, этилового эфира уксусной кислоты, добавляют на холоде при постоянном помешивании и исключении попадания влаги 25 мл 4 н.соляной кислоты в абс. этиловом эфире уксусной кислоты и оставляют все это стоять в течение часа. Легколетучие составляющие упаривают при , масляный остаток вводят в 150 мл абс. диэтилового эфира и смес упаривают снова (3 мл). Масляный остаток высушивают над натровым асбестом при полувакууме. Получают гидрохлорид (Со.)-п-бутиловый эфир-(су)- -бензилового эфира D-глютаминовой кислоты (8,5 г; 92,4% от теории).
9 + ГС (с 0,646; метанол) ;
Rf 0,82 (хлороформ:метанол:вода 70:30:5);
Rf 0,68 (этил-эфир уксусной кислоты : п-бутанол: пиридин: уксусная кислота:вода 42: 21 : 21:6:10).
Исходный продукт получают .следующим образом.
20,0 г (64,6 ммоль) (сУ)-бензилового эфира N-трет.-бутилоксикарбонил -D-глютаминовой кислоты растворяют в 750 мл абс.тетрагидрофурана, 25,05 г (64,6 ммоль) карбоната цезия (Флука, чистый), растворенных в 80 мл воды вводят по каплям и всю смесь улари- вают в вакууме. Остаток растворяют в 200 мл абс.диметилформамида, раство- рител% упаривают и всю операцию повторяют. Кристаллический остаток, полученный после сушки в высоком вакууме, растворяют в 1 л абс. диметил- формамида и при постоянном перемешивании по каплям вводят 13,3 г (97 ммоль) п-бутилбромида.
Суспензию, полученную после 18-ча сового перемешивания при комнатной температуре, фильтруют, фильтрат упаривают наполовину и после добавления 1 л этилового эфира уксусной кислоты э сстрагируют водой (10x100 мл). Органическую фазу сушат над сульфатом натрия и упаривают. Масляньш остаток вводят в 100 мл диэтилового эфира и кристаллизуют благодаря добавке 1800 мл петролейного эфира и вьщерж- ке при . Кристаллическую массу
5
0
5
0
5
0
5
0
5
отсасывают, промьтвают и высушивают. Получают (Сы)-п-бутил эфир-(с dL)-6eH- зилэфир N-трет.-бутилоксикарбонил-D- -глютаминовой кислоты в виде бесцветных игл (21 г; 89% от теории). То 70-71°С;
20-И°С (с 1,149, мета- . .0 -
Rf 0,77 (хлороформгизопропанол: :уксусная кислота 30:8:2);
Rf 0,92 (этил-эфир уксусной кислоты:1-бутанол:пиридин:уксусная кислота:вода 42:21:21:6:10)о
Ь-аланин-2-(1,2-дипалмитоил-Зп- -глицеро-3-оксифосфорилокси)-этил- амид, служащий в качестве исходного продукта, получают следующим образом.
13,25 г (14,9 ммоль) N-трет.-бу- тршоксикарбонил-Ъ-аланин-2-(1,2-ди- палмитоил-Бп-глицеро-З-оксифосфорил- окси)-этил-,амид вводят при постоянном перемешивании вводят в 170 мл охлажденного до 0°С смеси из три- фторуксусной кислоты и хлористого метилена при соотношении 1:3 (V:V), причем получают прозрачный раствор. После выдержки в течение 2 1/2 ч при ко мнатной температуре раствор упаривают на роторном испарителе при . Полутвердый остаток для удаления избыточной трифторуксусной кислоты смешивают неоднократно каждый раз со 100 мл хлорида метилена и затем выпаривают.
После пятикратного перетирания остатка каждый раз со 100 мл абс. диэтилового эфира и отстаивания полученного продукта получают хорошо фильтруемую суспензию. Ее фильтруют на нутч-фильтре, промывают твердый продукт диэтиловым эфиром, затем дважды раз 100 мл горячего ацетона и сушат в вакууме при 60- 70°С. Получают 10,9 г Ь-аланин-2- -(1,2-дипальмитоил-Бп-глицеро-З-ок- сифосфорилокси)-этиламид в виде бесцветных кристаллов с Тп 138-147 °С (95,6% от теории).
+30 + I C (с 1, хлоро-. форм:метанол:вода 70:30:5);
Rf 0,14 (хлороформ:метанол 7:3);
Rf 0,40 (хлороформ:метанол:вода 70:30:5).
Полученньй таким образом продукт переводят в натриевую соль следующим образом,
3,82 г (5 ммоль) Ъ-аланин-2-(1,2- -дипальмитоил-Зп-глицеро-З-оксифосфо рилокси)-этиламида растворяют в 100 мл смеси хлороформ:метанол 7:3 при кратковременном нагревании до 35 С. Охлаждают и осторожно добавляют по каплям 5 мл IN натрового щелока. Прозрачный раствор выпаривают приблизительно до 1/3. первоначального объема и после добавления 200 мл диоксана лиофилизируют. Получают натриевую соль Ь-аланин-2-(1,2-дипaльми тoил-Sn-глш epo-3-oкcифocфopилoкcи)- -этилaмидa в виде рыхлого порошка (0,41 г).
Пример 2. 3,5гСб,9 ммоль -(СсЛ)-метилового эфира N-ацетил-му- рамил-Ь-этенил-Б-глутаминовой кислоты и 1,2 г N-оксисукцинимида растворяют в 50 мл смеси, состоящей, из ди- метилформамида, изопропанола и хлороформа (-1:3:6; V:V:V), добавляют 2,10 г (10,35 ммоль) дициклогексил- карбодиимида и при исключении попадания вЛаги при помепшвании выдерживаю 1 ч при комнатной температуре. Суспензию смешивают с 50 мл этилового эфира уксусной кислоты, 30 мин вьщер живают при перемешивании в ледяной ванне-и затем отфильтровывают нераст воримые частицы дициклогексилмочеви- ны. Фильтрат упаривают на роторном испарителе приблизительно до 40 мл, в результате добавления 150 абс. ди- этилового эфира выпадает сложный активный эфир (дважды), фильтруют и высушивают, в результате получают эфир с N-окси-сукцинимидом с Rf 0,43 (хлороформ:метанол:вода 70:30:5) - сырьевой продукт в ко- личестве 5,1 .г.
3,43 г (4,4 ммоль) Ъ-аланин-2- -(1,2-дипалмитоил-Зп-глицеро-3-окси- фосфорилокси)-этиламида суспендируют в 45 мл хлороформа и при 40°С в те- чение 5 мин по каплям вводят 0,86 мл (6,1 ммоль) триэтиламина, растворенного в 5 мл хлороформа, при этом получают прозрачный раствор. К нему по каплям при интенсивном метании при исключении попадания влаги в течение 5 мин добавляют раствор указанного активного сложного эфнра в 100 Мл смеси, состоящей из диметил фбрмамида, хлороформа и диоксана (1:14:6; V:V:V).
После 2 1/2 ч перемешивания при комнатной температуре несколько мутный раствор упаривают на роторном испарителе до сухого состояния (30° Полученный продукт очищают на геле кремневой кислоты 60 (Мерк, размер зерен 70-230 Меш, ASTM) в системе хлороформ:метанол:вода 70:30:5 (5 мл фракций). Фракции содержащие продукт, собирают (ДС). Остаток после вьтаривания растворителя растворяют в 250 мл дважды дистиллированной воды и очищают аналогично тому, как это описано в примере 1, путем ди- фильтрации (AMICON-мешалка, тип 402 ультрафильтр 0.30/76 мм). Раствор, остающийся в мешалке, фильтруют через фильтр с миллипорами (0,2 МКм) и лиофилизируют. Получают натриевую соль Ш-ацети.п-мурамил-Ь-аланил-В- -глютамид-(Со.)-метилэфир-(С 5: )-1-ала- нин-2-(1,2-дипальмитоил-5п-глицеро- -3-оксифосфорилокси)-этил-амида, 2,96 моль Но в виде бесцветного порошка .
ы. +11 j Гс (с 0,285; 10%-ная уксусная кислота);
Rf 0,25 (хлороформ:метанол:во- да 70:30:5);
Rf 0,39 (этиловый эфир уксусной кислоты: п -бутанол-пиридин:уксусная кислота:вода 42:21:21:6:10) (в кол-ве 3,1 г; 55% от теории).
Исходные соединения получают, следующим образом.
7,7 г (21,2 ммоль) гидрохлорида (CoL} -метилэфира- (С V) -бензил эфира Ъ-аланил-В-глютаминовой кислоты и 8,96 г (23,3 ммоль) натриевой соли К-ацетил-4,6-0-изопропйлиден-мурами- новой кислоты соединяют аналогично примеру 1 по методу дициклогексикар- бодиимид): N-окси-суксинимид. Полученный продукт без дальнейшей очистки расщепляют в 100 мл 60%-ной уксусной кислоты. После 5 1/2 ч меша- ния при комнатной температуре раствор упаривают, смешивают с водой, вновь упаривают и после добавки 100 мл диоксана лиофилизируют.-Остаток чистят на 60 мл геля кремневой кислоты в системе хлороформ:метанол: . :вода 70:30:5 (7 мл фракций), процесс проводится дважды.
Фракции, содержание необходимый продукт, объединяют, растворитель упаривают. В остатке (Со(.)-метилэфир- (С)-бензилэфир N-aцeтил-мypaмил-L- -аланил-В-глютаминовой кислоты в ви- де бесцветной пены с Rf 0,63 хлореформ:метанол:вода 70:30:5) в количестве 6,9 г.
6,0 г (10 ммоль) (Со()-метилэфир- -(СУ)-бензилэфир N-ацетил-мурамилхроматографе на 550 г геля кремневой кислоты 60„
Получаемьп продукт собирают, сме шивают с 200 мл бидистиллированной
fO
условиях (о,45 мкм) и лиофилизируют Получают натриевую соль N-ацетил-му рамил-Ъ-ал анил-Б-глютамил- (Cot) -трет -бутилэфир-(су)-Ь-аланин-2-(1,2-ди- палмитоил-8п-глицеро-3-оксифосфорил окси)-этил-амида в виде бесцветного порошка, содержащего 3,4 моль воды.
j° -1-14 1°С (С 0,817; .10%-ная уксусная кислота);
f5
-Ъ аланил-Б-глютаминовой кислоты, ра- воды (), фильтруют в стерильных створенного в смеси 1,2 диметоксиэта- на и воды 95,5 (V:V), гидрируют в присутствии 0,6 г катализатора палладий на угле (10%-ный) в течение 1 1/2 ч при нормальном давлении. Катализатор отфильтровывают и фильтрат упаривают при комнатной температуре при повышенном давлении. Остаток чистят на 400 г геля кремневой кислоты 60 в системе хлороформ:метанол:вода 70:30:5 (10 мл фракций), как было указано вьше.
Фракции, содержащие продукт, объединяют, растворитель упаривают. Остаток в форме соли натрия чистят от солей, как описано в примере 1, на 50 мл Dowex 50 WX 8 (50/100 Меш, форма Н, сильнокислотный катионооб- менник). Фильтрат пропускают через фильтр с миллипорами (0,45 мкм) и . лиофилизируют. Получают (Cot)-метиловый эфир Н-ацетил-мурамил-Ь-аланил- -Б глютаминовой кислоты (1,27 моль
20
25
Rf 0,29 (хлороформ:метанол:вода 70:30:5);
Rf 0,53 (этиловый эфир уксусной кислоты: П -бутанол:пиридин:уксусная кислота:вода 42:21:21:6:10). Выход натриевой соли 8,39 г 78% от теории Пептидпроизводное, используемое в качестве исходного продукта, получают следующим образом.
38,3 г (63,5 ммоль) (Со()-трет.- -бутилэфир-(С У)-бензилэфира (4- -бифенилил)-пропилоксикарбонил -Ь- -аланил-Б-глютаминовой кислоты растворяют в 700 м смеси из трифторэтана 30 и воды 9:1 (V/V) и в результате до бавления по каплям 1,23 н.соляной кислоты в такой же смеси растворителей (1 об. ч. концентрированной соля ной кислоты и 9 об. ч. трифторэтано- 35 ла) значение рН уменьшается до 1,5 ( 2 1/2 ч, расход 51,66 мл, т.е. 81% от теории).
Н„0) в виде бесцветного порошка с +47 - 1°С (С 1,249; мета -
(58%
от тенол) в количестве 3,1 г ории).
Rf - 0,80 (хлороформ:метанол:вода 70:30:5);
Rf 0,30 (ацетоннитрил:вода 3:1);
Rf rr 0,43 (этиловый эфир уксусной кислоты:уксусная кислота:вода:метанол 67:10:23:12)о
38,3 г (63,5 ммоль) (Со()-трет.- -бутилэфир-(С У)-бензилэфира (4- -бифенилил)-пропилоксикарбонил -Ь- -аланил-Б-глютаминовой кислоты растворяют в 700 м смеси из трифторэтана 30 и воды 9:1 (V/V) и в результате до бавления по каплям 1,23 н.соляной кислоты в такой же смеси растворителей (1 об. ч. концентрированной соля ной кислоты и 9 об. ч. трифторэтано- 35 ла) значение рН уменьшается до 1,5 ( 2 1/2 ч, расход 51,66 мл, т.е. 81% от теории).
Светложелтоватый раствор на ротор
ном испарителе в вакууме, создаваеП р и м е р 3. 9,4 г (11,1 ммоль)0 мом водоструйным насосом, при ЗО с (Cot)-Трет.-бутилэфира N-ацетил-мура- упаривают почти до 100 мл, затем до- мил-Ь-аланил-Б-глютаминовой кислоты переводят аналогично примеру 2 в активный эфир и затем, как описано. соединяют с 6.48 г (8,2 ммолй) L- -аланин-2-(1,2-дипалмитоил-Зп-глице- ро-3-оксифосфорилокси)-этиламида в присутствии триэтиламина. Полученный продукт суспендируют в 250 мл бидисбавляют 200 мл диоксана, смесь высушивают на холоде.
Полутвердый остаток растворяют в 30 мл абс. диэтилового эфира и при 0-5°С при постоянном перемешивании, и продукт осаждают 150 мл петролей- ного.эфира. Вьщерживают на холоде (-2б°С), декантируют и повторяют эту
( процедуру дважды. Масляный остаток затем вводят в 100 мл. трет.-бутанотиллата воды и быстро нагревают до 37°С, перемешивают 15 мин в ледяной ванне, отфильтровьгеают нерастворимые частички дициклогексилмочевины и фильтрат подвергают диафильтрации.
( процедуру дважды. Масляный остаток затем вводят в 100 мл. трет.-бутанола, лиофилизируют и остаток высушивают над натровым асбестом в высоком вакууме. Получают гидрохлорид
как описано в ripHMepe 1 (AMICON - ме--5-5 (СоО-трет.-бутилэфира (СУ)-бензил- шалка 402, ультрафильтр РМ И 30/76 мм эфира Ь-аланил-В-глютаминовой кисло- Остающийся в мешалке раствор (120 мл) ты в виде сильно гигроскопич юго по- лиофилизируют и продукт чистят на рошка.
хроматографе на 550 г геля кремневой кислоты 60„
Получаемьп продукт собирают, смешивают с 200 мл бидистиллированной
условиях (о,45 мкм) и лиофилизируют. Получают натриевую соль N-ацетил-му- рамил-Ъ-ал анил-Б-глютамил- (Cot) -трет- -бутилэфир-(су)-Ь-аланин-2-(1,2-ди- палмитоил-8п-глицеро-3-оксифосфорил- окси)-этил-амида в виде бесцветного порошка, содержащего 3,4 моль воды.
j° -1-14 1°С (С 0,817; .10%-ная уксусная кислота);
воды (), фильтруют в стерильных
f5
воды (), фильтруют в стерильных
0
5
Rf 0,29 (хлороформ:метанол:вода 70:30:5);
Rf 0,53 (этиловый эфир уксусной кислоты: П -бутанол:пиридин:уксусная кислота:вода 42:21:21:6:10). Выход натриевой соли 8,39 г 78% от теории. Пептидпроизводное, используемое в качестве исходного продукта, получают следующим образом.
38,3 г (63,5 ммоль) (Со()-трет.- -бутилэфир-(С У)-бензилэфира (4- -бифенилил)-пропилоксикарбонил -Ь- -аланил-Б-глютаминовой кислоты растворяют в 700 м смеси из трифторэтана 0 и воды 9:1 (V/V) и в результате добавления по каплям 1,23 н.соляной кислоты в такой же смеси растворителей (1 об. ч. концентрированной соляной кислоты и 9 об. ч. трифторэтано- 5 ла) значение рН уменьшается до 1,5 ( 2 1/2 ч, расход 51,66 мл, т.е. 81% от теории).
Светложелтоватый раствор на ротор)0 мом водоструйным насосом, при ЗО с упаривают почти до 100 мл, затем до-
бавляют 200 мл диоксана, смесь высушивают на холоде.
Полутвердый остаток растворяют в 30 мл абс. диэтилового эфира и при 0-5°С при постоянном перемешивании, и продукт осаждают 150 мл петролей- ного.эфира. Вьщерживают на холоде (-2б°С), декантируют и повторяют эту
( процедуру дважды. Масляный остаток затем вводят в 100 мл. трет.-бутано11
20
Cdl-j j: 1°C (C 1,630; хлороформ);
Rf 0,60 (хлороформ:метанол:вода 70:30:5);
Rf 0,45 (п-бу,танол:уксусная кис- лота:вода 10:1:2:8) 19,25 г (76,5% от теории).
fO
К охлажденному до 0°С раствору, состоящему из 65,96 г (0,2 моль) гидрохлорида (Сы)-трет.-бутилэфира- -(СУ)-бензилэфира D-глютаминовой кислоты и 65,47 г (0,2 моль) (4-бифенилил)-пропилркси-кар6онилЗ- -L-аланина в 650 мл абс. диметилформ- амида, добавляют при постоянном помешивании 22 мл (0,24 моль) И-метил- формалина и затем 59,11 г (0,24 моль) 2-этокси-Н-этокси-карбонил-1,2-дигид- , рохинолина. После 10-часового разме- шивания при комнатной температуре желтый раствор упаривают на роторном испарителе при 30°С. Остаток вводят в 1 л этилового эфира уксусной кислоты, экстрагируют водой (5x200 мл), водную фазу экстрагируют 0,5 л уксусного -эфира и собранные органические фазы высушивают.
Продукт, полученный после упари- вания растворителя (продукта 150 мл) чистят многократно на хроматографе на геле кремневой кислоты 60 (1:20) с уксусным эфиром. Получают (Coi)- -трет. -бутилэфир- (с If -бензилэфир-NПример 4. К раствору 4,62 г (6,05 ммоль) 1,-аланин-2-( 1 ,2-дипaлми- тoил-Sn-глицepo-3-oкcифocфopилoкcи)- -этилaмидa в 100 м смеси хлороформ: :изопропанол:вода 70:30:2 при помешивании при 15 С в течение 10 мин по каплям добавляют 14,52 г (7,26 ммоль) 0,5 М раствора триэтил- амина в смеси хлороформ:изопропанол: :вода 70:30:-2. Затем в течение |20 мин добавляют 4-мя порциями.по 1,5 г в твердом виде 6,0 г (7,26 ммоль) (Со1)-метилэфир-(С)-К- -гидрооксисуксинимидэфира N-пропио- нил-дезметилмурамил-Ь-аланил-В-глю- таминовой кислоты, содержащий еще ди- циклогексилмочевину, причем раствор мутнеет на глазах.
Затем после 15-минутного помешивания при 15°С охлаждение прекращают и продолжают перемешивание еще 2 1/2 ч при комнатной температуре. Затем полученный таким образом мутньй раствор упаривают в вакууме при ЗО С. Остаток (10,75 г) суспендируют в 170 мл бидистиллированной воды (рН 5,5), суспензию путем добавки 0,3 мл триэтиламина доводят до рН 6,0; отфильтровывают нерастворимые частицы (дициклогексилмочевины) и
25
(4-бифенилил)-пропш10ксикарбонил- 5 фильтрат лиофилизируют в высоком ва-Ь-аланил-В-глютаминовой кислоты в виде бесцветного масла, oi. -14 + 1°С (С 1,625; эти- ловьй эфир уксусной кислоты) (100 г, 83% от теории);
Rf 0,73 (хлороформ:изопропанол: :уксусная кислота 70:8:2);
Rf 0,51 (толуол:уксусный эфир 1:1).
Используемый в качестве исходного продукта гидрохлорид (Сс/.)-трет.-бу- тилэфира-(СУ)-бензш1эфира D-глютаминовой кислоты получают путем проведения реакции между (су)-бензиловым эфиром D-глютаминовой кислоты и изо- бутанолом в смеси, состоящей из 1,4- -диоксана и серной кислоты, выделяют продукт в виде бесцветных игл с Т;, 108-109°С.
10
-16 + (с 1,235;
этанол);
Rf 0,84 (хлороформ-метанол:вода 70:30:5);
- 5
fO
- 29951612
Rf 0,64 (этиловьш эфир уксусной кислоты:h-бутанол:пиридин:уксусная кислота:вода 42:21:21:6:10) в количестве 61% от теории).
Пример 4. К раствору 4,62 г (6,05 ммоль) 1,-аланин-2-( 1 ,2-дипaлми- тoил-Sn-глицepo-3-oкcифocфopилoкcи)- -этилaмидa в 100 м смеси хлороформ: :изопропанол:вода 70:30:2 при помешивании при 15 С в течение 10 мин по каплям добавляют 14,52 г (7,26 ммоль) 0,5 М раствора триэтил- амина в смеси хлороформ:изопропанол: :вода 70:30:-2. Затем в течение |20 мин добавляют 4-мя порциями.по 1,5 г в твердом виде 6,0 г (7,26 ммоль) (Со1)-метилэфир-(С)-К- -гидрооксисуксинимидэфира N-пропио- нил-дезметилмурамил-Ь-аланил-В-глю- таминовой кислоты, содержащий еще ди- циклогексилмочевину, причем раствор мутнеет на глазах.
Затем после 15-минутного помешивания при 15°С охлаждение прекращают и продолжают перемешивание еще 2 1/2 ч при комнатной температуре. Затем полученный таким образом мутньй раствор упаривают в вакууме при ЗО С. Остаток (10,75 г) суспендируют в 170 мл бидистиллированной воды (рН 5,5), суспензию путем добавки 0,3 мл триэтиламина доводят до рН 6,0; отфильтровывают нерастворимые частицы (дициклогексилмочевины) и
25
0
5
кууме.
Полученный таким образом лиофили- зат растворяют в 300 мл, затем лиофилизируют в глубоком вакууме.
Получают натриевую соль N-пропио- нил-дезметилмурамил-Ъ-аланил-В-глю- тамил-(Со1)-метилэфир-(с)-Ь-аланин- -2-(1,2-дипалмитоил-8п-глицеро-3-ок- сифосфорилокси)-этиламида в виде бесцветного порошка, содержащего 1,90 моль воды.
3,7 + О,ГС (С 0,672; хлороформ);
0 ° +1,7 Т О, ГС-(С 1,044; вода);
Rf 0,42 (хлороформ:метанол:вода 70:30:5);
Rf 0,62 (уксусный эфир:п-бута- нол:пиридин:уксусная кислота:вода 42:21:21:6:10) в количестве 5,64 г (71,2% от теории).
Исходный продукт получают следующим образом.
5
5,12 г (10,1 ммоль) dL-метилового эфира М-пропионилдезметилмурамил-Ъ- -аланил -В-глютаминовой кислоты полностью растворяют в то мл смеси хлороформ:изопропанол 7:3 и в результате добавления 10 мл диметил- формамида.
К этому раствору добавляют 2,68 г (13 ммоль) дициклогексилкарбодиимида и 1,50 г (13 ммоль) N-оксисукциними- да и полученный в результате этого прозрачный бесцветный раствор мешают в течение 1 1/2 ч при комнатной температуре и затем вьщерживают 17 ч при 4° С..
Полученную таким образом суспензию смешивают с 400 мл диэтилового эфира и затем перемешивают еще в течение 1 ч при комнатной температуре.
Затем кристаллизат отсасьшают, промывают диэтиловым эфиром и высушивают в вакууме над пятиокисью фосфора.
Получают сьгрой (CdO-метилэфир-. . -4с у) -К-оксисукцинимидэфир-М-пропио- ннп-дезметилмурамил-Ь-аланил-О-глюта миновой кислоты в виде бесцветных кристаллов, содержащий в виде примеси дициклогексилмочевину и используемый без последующей очистки.
Rf 0,46 (хлороформ:метанол 5:1);
Rf 0,72 (хлороформ:метанол 7:3) Выход сложного эфира 8,34 г,
Исходный продукт получают следующим образом.
Раствор 13,0 г (21,75 ммоль) (Cot) -метилэфир-(С)-бензилэфира N-пропио нил-д зметилмурамил-Ъ-аланил-Б-глю- тамииовой кислоты в 250 мл смеси ди- метоксиэтан:вода 20:1 гидрируется 2,5 г катализатора палладий на угле (10%-ный) в течение 1 ч при комнатной температуре и нормальном давлении.
Затем катализатор отфильтровьшают фильтрат упаривают в вакууме до сухого состояния и полученньй остаток трижды смешивают с водой в количестве по 50 мл и снова упаривают.
Осадок растворяют в приблизительно 100 мл бидистиллированной вода, фильтруют этот раствор через фильтр с миллипорами (NAL GENES: 0,2 мкм) и лиофилизируют в глубоком вакууме. Получают ot-метиловый эфир N-пропио- нил-дезметилмурамил-Ъ-аланил-Б-глю
0
5
0
5
0
5
0
5
0
5
таминовой кислоты (0,68 моль воды) в виде бесцветного лиоЛилизата +14,9 4. 0,°С (с 1,067; метанол), в количестве 11,0 г(96% от теории).
Rf 0,78 (хлороформ:метанол:вода 7,:30:5);
Rf 0,57 (уксусный эфир:п-бута- нол:пиридин:уксусная кислота:вода 42:21:.21:6:10).
Исходный продукт получают следующим образом.
Раствор 20,7 г (32/46 ммоль) (СЫ)- -метилэфир-(С)-бензилэфира 4,6-0- -изопропиллиден-И-пропионил-дезме- тилмурамил-Ь-аланил-Б-глютаминовой кислоты в 400 мл 60%-ной уксусной кислоте мешают в течение 21 ч при комнатной температуре, затем упаривают в вакууме при 30°С и полученный остаток последовательно трижды смешивают каждый раз со .100 мл воды и снова упаривают. Полученный сырой продукт очишают путем хроматографии на колонне на 1000 г геля кремневой кислоты 60 (Мерк, 0,063-0,200 мм) в системе метиленхлорид:метанол 85: :15 (15 мл фракции) Фракции 207-290 собираются и вьтариваются в вакууме при 30°С. Получают (Сс1)-метилэфир- -(с)-бензилэфир N-пропионил-дезме- тилмурамил-Ъ-аланил-Б-глютаминовой кислоты, содержащей 0,24 моль воды
+16 + 0,1 С (С 1,463;. метанол);
Rf 0,24 (хлороформ:метанол 9:1);
Rf 0,53 (хлороформ:метанол 5:1);
Rf 0,94 (хлороформ:метанол:вода 70:30:5) в количестве 13,7 г (70,1% от теории).
Исходньй продукт получают следующим образом,
В суспензию из 13,2 г (35,77 ммоль) натриевой соли 4,6-0 изопропилиден- -Н-пропиони,п-дезметилмураминовой кислоты в 200 мл диметилформамида добавляют при комнатной температуре при мешании 9,6 г (46,5 ммоль) дициклогексилкарбодиимида, 5,35 г (46,5 ммоль) N-оксисукцинимида и 12,8 г (35,77 ммоль) гидрохлорида (СсА)метилэфир-(С11)-бе:нзилэфира L- аланин-Б-глютаминовой кислоты и все мешают в течение 21.ч при комнатной температуре,
Полученную таким образом белую суспензию смешивают с 200 мл уксус151
ного эфира, перемешивают в течение 1 ч при , отделяют от кристаллизатора (дит иклогексилмочевины), на нутч-фильтре, промьшают ледяным уксусным эфиром и фильтрат упаривают в вакууме при 30 С. Полученный таким образом остаток вводят в 300 мл уксусного эфира и дважды последовательно промьшают 50 мл 2 н. лийонной кислоты, водой, 10%-ным раствором гидро карбоната натрия и снова водой.
Эфирные слои объединяют, высушивают над сульфатом натрия, фильтруют и упаривают в вакууме.
Получают (Сс)1)-метилэфир-(С }1)-бен- зилэфир 4,6-0-изопропилиден-М-пропио нил-дезметилмурамил-Ь-аланил-В-глю- таминовой кислоты.
Rf 0,65 (хлороформ:метанол 9:1);.
Rf 0,86 (хлороформ:метанол 5:1) в количестве 21,3 г (93,3% от теории).
Оба исходных продзпста получают следующим образом.
К раствору 20,3 г (48,0 ммоль) (Сс)-метилэфир-(су)-бензш1эфира N- -трет.-бутилоксикарбонила-Ъ-аланил- -D-глютаминовой кислоты в 100 мл абсолютного уксусного эфира добавляют при 0°С 100 мл приблизительно 5 N соляной кислоты в абсолютном эфире и мешают 2 ч при 0°С.
Желтоватьй раствор упаривают в вакууме, полученный остаток дважды сме шивают каждый раз со 100 мл абсолютного эфира и снова упаривают. После дигерирования с абсолютным диэтиловы
эфиром (2x100 мл) остаток высушивают
в вакууме и получают гидрохлорид
(Сс1)-метилэфир-(С} )-бензилэфира L- -аланил-В-глютаминовой кислоты, соде р «гашэ1й 0,31 моль воды.
(с 0,043
метанол);
Rf 0,72 (хлороформ:метанол:вода 70:30:5);
Rf 0,44 (хлороформ:метанол 5:1);
Rf 0,31 (хлороформ: метанол 9:1) в количестве 1,7 г (94,8% от теории).
Раствор 34,4 г (73,8 ммоль, 2,14 ммоль), содержащий хлорид натрия натриевой соли 1оС-О-бензил-4,6- -0-изопропилиден N-пропионил-дезме- тилмураминовой кислоты в 340 мл воды гидрируют при постоянном значении
1616
рН 7,1 6,0 г 10%-ного катализатора палладий на угле в течение 23 ч при комнатной температуре и нормальном давлении. Затем катализатор отфильтровывают, фильтрат упаривают в вакууме при ЗО С и при рН 7,1; и полученный таким образом остаток высушивают в высоком вакууме над пятиоки- сью фосфора. Получают натриевую соль 4,6-0-изопропилиден-Ы-пропионил-дез- метилмураминовой кислоты (16,6 г, 94,8% от теории)
Rf 0,50 (хлороформ:метанол:вода 70:30:5);.
Rf 0,66 (ацетонитрил:вода 3:1).
Исходньй продукт получают следующим образом.
Раствор 14,3 г (32,7 ммоль) метилового эфира 1 с.-0-бензил-4,6-0-изо- пропилиден-М-пропионил-дезметилмура- миновой кислоты в 130 мл метанола смешивают с 24,4 мл (48,7 ммоль) 2 н натрового щелока и перемешивают в течение 1 1/2 ч при комнатной температуре .
Затем полученный таким образом прозрачный желтоватьй раствор с помощью 1 н. соляной кислоты доводят до значения рН 7,0 и упаривают в вакууме при 30 С.
После сушки над пятиокисью фосфора получают натриевую соль I -0- г-бензил-4,6-0-изoпpoпилидeн-N-пpoпиo нил-дезметилмураминовой кислоты в виде бесцветных кристаллов в количеств 27,2 г.
Rf 0,67 (хлороформ:метанол:вода 70:30:5);
Rf « 0,74 (ацетонитрил:вода 3:1
Исходный продукт получают следующим образом.
К суспензии из 6,75 г (224,7 ммол гидрида натрия в 120 мл абсолютного тетрагидрофурана добавляют по каплям при 5 С в атмосфере азота при постоянном помешивании в течение 5 мин раствор 31,3 г (85,65 ммоль) 1Ы.-0- -бензил-2-дезокси-4,6-0-изопропили- ден-2-пропионамид-Ы-В-глюкопиранози- да в 200 мл абсол)отного тетрагидрофурана, причем температура повышается до 20°С.
Полученную таким образом суспензию перемешивают еще 2 ч при 40°С, затем охлаждают до 0°и добавляют по каплям в атмосфере азота и непрерывном помешивании в течение 30 мин
171
к охлажденному до -15°С раствору 20,7 г (135,77 ммоль) метилового эфира бромуксусной кислоты в 95 мл абс. тетрагидрофурана. Полученную таким образом суспензию размешивают еще в течение 3 ч при 0-5°С, затем добавляется 20 мл метанола и 20 мл тетрагидрофурана . С помощью 4,5 мл ледяной уксусной кислоты устанавливают значение рН-6 и раствор упаривают в ва- кууме при .
Остаток растворяют 200 мл метилен хлорида и промывают полученный раствор водой (3x125 мл). Собранные ме- тиленхлоридные фракции высушивают над сульфатом натрия, фильтруют и упаривают в вакууме при 30 С.
Получают сьфой продукт в виде желтоватых кристаллов, которые затем очищают хромотографией на колонне на 500 г нейтральной окиси алюминия (Йоелм N, супер 1), используя эфир в качестве. элюента (Ю мл фракций). Фракции 14-36 объединяют и упаривают в вакууме.
Получают метиловый эфир 1ot-0- -бензил-4,б-О-изопропилиден-N-npo- пионил-дезметилмураминовой кислоты в виде бесцветных кристаллов с Тп 121-123° (диэтилэфир:нефтяной эфир 1:2).
+147,9 + 0,1°С (С 0,849; хлороформ) - 32,2 г (86,2% от теории).
Rf 0,67 (хлороформ:метанол 9:1).
Пример 5. Аналогично примеру 4 получают из 5,525 г (6,43 ммоль) сырого (содержит еще , незначительное количество дициклогек силмочевины) (СЫ.)-трет-бутилэфир- -(СУ)-И-окси-сукцинимидэфира N-npo- пионил-дезметилмурамил-Ъ-аланил-Б- -глютаминовой кислоты и 3,78 г (4,95 ммоль) Ь-аланин-2-(1,2-дипаль- митоил-5п-глицерр-3-оксифосфорилок- си)-этиламида натриевую соль N-npo- пионил-дезметилмурамил-Ь-аланил-Б- -глютамил-(Сd) -трет.-бутилэфир-(С у) - -Ь-аланин-2-( 1 ,2-дипальмитоил-5п.- -глицеро-3-оксифосфорилокси)-этил- амида в виде бесцветного порошка, содержащего 2,64 моль воды.
LuLl ° +2,5 + 0,1°С (с 0,649; .вода);
+5,8 ;+ 0,1°С (С 0,694; хлороформ);
1618
Rf 0,60 (хлороформ:метанол:во- да 70:30:5), в количестве 4,32 г (64,0% от теории).
Ис лодный продукт получают следующим образом.
Аналогично примеру 3 из 3,44 г (6,15 ммоль) cat-трет.-бутилэфира Н-пропионил-дезметилмурам ил-Ъ-аланил -D-глютаминовой Кислоты, 1,68 г (8,14 ммоль) дициклогексилкарбодими- да и 0,94 г (8,14 ммоль) N-оксисук- цинимида получают сырой ()-трет.- -бутилэфир-(су)-К-оксисукцинимидэфир N-пропионил-дeзмeтилмypaмил-L-aлaнил -D-глютaминoвoй кислоты в количестве 5,38 г в виде бесцветных кристаллов, содержащих дициклогексилмочевину, и используемьпс без дальнейшей очистки.
Rf 0,61 (хлороформ:метанол:во- да 70:30:5).
Исходньй продукт получают следующим образом.
Раствор 5,1 г (7 ммоль) (СсА)-трет -бутилэфир-(Су)-бензилэфира d -0- -бензил-К-пропионил-дезметилмурамш1- -Ь-аланил-В-глютаминовой кислоты в 100 мл смеси диметоксиэтан:вода 9:1 гидрируют с 1,5 г 5%-ного катализатора палладий на угле (Е 101N, Дегусса) в течение 20 ч при комнатной температуре и нормальном давлении Через 20 ч катализатор отфильт- ровьгоают и снова производят гидрирование с 1,5 г свежего катализатора в течение 26 ч как указано. Затем катализатор отфильтровьшают и фильтрат упаривают в вакууме до сухого состояния при 30°С.
Полученный таким образом остаток растворяют в смеси, состоящей из 100 мл метиленхлорида и 5 мл изопро- панола, раствор смешивают с 500 мл смеси из дизтилового н петролейного эфира 3:2 и перемешивают еще 1 ч при комнатной температуре. Затем от- сасьшают вьшавший в осадок продукт и промьюают его диэтиловым эфиром. Получают с -трет- бутилэфир N-npo- пионилдезметилмурамил-1-алканил-D- -глютаминовой кислоты в виде бесцветг ного порошка, содержащего 0,52 моль воды (3,7 г, 94,7,от теории).
+20,2 + 0,1°С (С 0,902; вода);
Rf 0,32 (хлороформ:метанол:вода 70:30:5);
Rf 0,54 (ацетонитрил:вода 3:1).
191
Получают исходный продукт следу- кнцим образом.
Аналогично примеру 4 получают из 7,3 г (9,5 ммоль) (Cdl)-трет.-бутил- эфир-(С у)-бензил эфир-1 oL-0-бензил- -4,6-0-изопропш1иден-пропионил-дез- метилмурамил-1-аланил-Б-глютаминовой кислоты и 150 мл 60%-ной уксусной кислоты (Cot.) -трет. -бутилэфи р- f С у) - -бензилэфир 1оС-О-бензил-К-пропно- нил-дезметилмурамил-Ъ-аланил-В-глю- таминовой кислоты в виде бесцветных кристаллов с Т 152-153 С (метанол: :вода 1:5).
Со. +68,9 J- 0,ГС (с 0,991; метанол);
Rf 0,40 (хлороформ:метанол 9:1);
Rf 0,70 (анетонитрил:вода 3:1), количество кислоты 5,9 г (85,3% от теории).
Исходный продукт получают следующим образом.
Аналогично примеру 4 из 4,65 г (9,62 ммоль, 2,066 ммоль/г, содержит еще хлорид натрия) натриевой соли 1с.-0-бензил-4, б-О-изопропилиден-N- -пропионил-де зме тилмураминов ой кис- лоты, 2,38 г (11,54 ммоль) дицикло- гексилкарбодиимида, 1,33 г (11,54 ммоль) N-оксисукцинимида и 3,86, г (9,62 ммоль) гидрохлорида (Cot) -трет. -бутилэфир- (С %) -бензилэфи- ра Ъ-аланил-Б-глютаминовой кислоты получают (Сct)-трет.-бутилэфир-(СV)- -бензилэфир 1с«.-0-бензил-4,6-0-изo- пpoпилидeн-N-пpoпиoнил-дeзмeтилмypa- мил-aлaнил-D-глютaминoвoй кислоты, содержащей О, 31 моль воды.
+38,4 + 0,1°С (С 1,086 метиленхлорид); ,86 (ацетонитрил : вода 3 : 1)
Rf 0,83 (хлороформ:метанол 9:1), выход кислоты 7,3 г (97,9% от теории).
Пример 6. Аналогично примеру 4 из 3,07 г (4 ммоль) сырого (еще содержит дициклогексилмочевину) (Cot) -п-бутилэфир-()-М-оксисук11инимид- эфира Ш-пропионил-дезмётилмурамил- -Ь-апанил-Б-глютаминовой кислоты и 2,37 г (3,1 ммоль) Ь-аланил-2-(1,2- -дипалмитоил-Зп-глицеро-З-оксифосфо- рилокси)-этиламида получают натриевую соль N-пропионил-дезметилмурамил
-Ъ-аланил-Б-глютамил- (Col) -h -бутил- эфир-(С 4)-Ъ-аланин-2-( 1,2-дипальми- тоил-Бп-глицеро-3--оксифосфорилокси)1620
-этиламид в виде бесцветного порошка, содержащего 2,93 моль воды.
20- +6,9 -f (с 0,504; метиленхлорид);
Rf 0,65 (хлороформ:метанол:вода 70:30:5);
Rf 0,63 (хлороформ:метанол 7:3), выход порошка 2,93 г (70,9%)
Исходный продукт получают следующим образом.
Аналогично примеру 4 из 2,2 г (3,9 ммоль) dt--п-бутилэфира N-npo- пион ил-д е зм е тилмур амил-L-аланил-D- -глютаминовой -кислоты, 1,2 г (5,8 ммоль) дициклогексилкарбодиими- да и 0,69 г (5,8 ммоль) N-оксисукцинимида получают сырой (СЫ)-п-бутил- эфир-(сУ)-И-оксисукцинимидзфир N- -пропионил-дезметилмурамил-Ъ-аланил- -D-глютаминовой кислоты в виде бесцветных кристаллов, содержащих дициклогексилмочевину и используемых без дополнительной очистки (количество кристаллов 3,07 г).
Rf 0,66 (хлороформ:метанол:вЬ- да 70:30:5).
Исходный продукт получают следующим образом.
Аналогично примеру 5 (продолжительность гидрирования 20 мин) из 7,3 г (11,3 ммоль) (Со(.)-п-бутил-эфир- -(су)-бензилэфира TJ-пропионил-дезме- тилмурамил-Ъ-аланил-Л-глютаминовой кислоты получают oL-n-бутилэфир N- -пропионил-дезметилмурамил-L-аланил- -D-глютаминовой кислоты в виде бес,- цветного порощка, содержащего 0,88 моль воды, с выходом кислоты 5,8 гС90,9% от теории).
+16,4 j 0,Гс (с 0,959; вода);
Rf 0,61 (метиленхлорид:метанол: :вода 70:30:5);
Rf 0,52 (ацетонитрил:вода 3:1).
Исходный продукт получают следующим образом.
Аналогично примеру 4 из 9,5 г ((3,97 ммоль) (Со1)-п-бутилэфир-(С)- -бензилэфир 4,б-О-изопропилиден-N- -пропионил-дезметил-мурамил-Ъ-аланил -D-глютаминовои кислоты и 120 мл 60%-ной уксусной кислоты получают (С.о(.) -г-п-бутилэфир- (С у) -бензг-лэфир К-пропионил-дезметилмурамил-Ъ-ала- нил-Б-глютаминовой кислоты, содержащий 0,41 моль воды, (7,5 г, 83%).
+15,7 + n,l«C (С 1,019; метанол);.
Rf 0,23 (метиленхлорид:метанол 9:1);
Rf 0,Д5 (метиленхлорид:метанол 5:1);
R.f 0,82 (метиленхлорид:метанол: :вода 70:30:5).
Исходньй продукт получают следующим образом.
Аналогично примеру 4 из 3,81 г (10,76 ммоль V 2,72 ммоль/г, содержит еще хлорид натрия) натриевой соли 4,б-0-изопропилиден-К-пропионил- -дезметилмураминовой кислоты, 2,44 г (11,83 ммоль) дициклокарбодиимида, 1,36 г (11,83 ммоль) N-оксисукииними да (10,76 ммоль) гидрохлорида (СЯ)- -п-бутилэфира-(Со(,)-бензил-Ъ-аланнл- -D-глютаминовой кислоты получают (CoL) -п-бутилзфир-( С V) -бензилэфир, 4,6-0-изопропилиден-К-пропионил-дес- метилмурамил-Ь-аланил-Б-глютаминовой кислоты (4,1 г, 56,2%).
Coi.° +10,,1 С (С 0,928; метанол).;
Rf 0,81 (метиленхлорид:метанол: :вода 70:30:5);
Rf 0,57 (метиленхлорид:метанол 5:1).
Пример 7. К раствору, состоящему из 2,85 г (2,09 ммоль) полученной согласно примеру 5 натриевой соли N-пропионил-десметилмурамил -L-аланил-Б-глютамил-( Col.)-трет.-бу- тилэфир-(С у)-Ъ-аланин-2-(1,2-дипал- митоил-Зп-глицеро-З-оксифосфорилок- си) этиламида и 112 мл абс, метилен- хлорида, добавляют трифторуксусной кислоты и все перемешивают в течение 3 ч при комнатной температуре. Затем бесцветный прозрачный раствор упаривают в вакууме при 30°С и полученный таким образом остаток несколько раз вводят в метиленхлорид и снова упаривают.
Получают 3,0 г бесцветного масла, растворенного в 350 мл смеси фосфат- буферного раствора хлорида натрия
(по 0,1 М, 1:1, рН 7), фильтруют в AMICON-диализаторе (модель 402, ультрафильтр РМ 0 30/76 мм) при 3 атм. Затем фильтруют для удаления хлоридов в противотоке з общей слож- ности 2,1 л бидистиллированной БОДЫ. Раствор, оставшийся в диализаторе (приблизительно 50 мл) лиофилизируют в высоком вакууме. Получают бесцвет
0
5
,
п
д г
л
г
ный лиофилизлт, который очищают методом хроматографии на колонне на 260 г геля кремневой кислоты (60, 0,063-0,200 мм) в системе хлороформ: :метанол:вода 70:30:5 (10 мл фракций) .
Фракции 90-260 объединяют и упаривают в глубоком вакууме без нагрева (охла дение) до сухого состояния. Остаток вводят в 250 мл бидистиллированной воды и затем в AMICON-диализаторе (модель 402, ультрафильтр ПМ 0 30/76 мм) упаривают при 3 атм до ;приблизительно 50 мл, затем последовательно фильтруют для удаления хлоридов в противотоке 250 мл фосфатного буферного раствора - хлорид натрия (по 0,1 М 1:1, ) и 175 мл бидистиллированной воды. Раствор, оставшийся в диализаторе, стерильно, фильтруют, затем;пропускают через два фильтра с миллипорами (NAL GENES, 0,45 мкм соответственно 0,2 мкм) и лиофилизируют в высоком вакууме.
Получают динатриевую соль (Cii)-L- -аланин-2-(1,2-дипальмитоил-8п-глице- ро-3-оксифосфорилокси)-этиламида Н-пропионилдезметилмурамил-Ь-аланил- D-глютаминовой кислоты в виде бесцветного гидроскопического порощка, со- деркап.его 4,8 моль воды.
ы-
40
-6,1 + 1°С (с 0,489;
метиленхлорид:этанол 1:1);
Rf 0,28 (уксусный эфир:и-бута- нол:пиридин:уксусная кислота:вода 41:21:21:6:10);
Rf 0,62 (ацетонитрил:вода 3:1), выход соли 1,04 г (36,4%).
Пример 8. 4,5 г(ммоль) натриевой соли N-aцeтил-мypaмил-L-aлa- нил-В-глютамил-(С Ы) -трет.-бутилзфир- -(С1)-Ь-аланин-2-( 1 ,2-дипалмитоил- -Sn-глицеро-З-оксифосфорилокси)-этил- амида, высушенной в высоком вакууме над пятиокисью фосфора, растворяют в 75 мл сухого дихлорметана. Охлаждают до 0°С и при помешивании в абсолютных условиях вводят 25 мл безводной трифторуксусно КИСЛОТЫ И за- тем нагревают до комнатной температуры. Через 2 1/2 ч прозрачный бесцветный раствор упаривают в роторном испарителе при комнатной температуре (приблизительно до 10 мл), многократно смешивают с дихлорметаном в количестве по 100 мл и наконец снова упаривают.
23
Сырой продукт дважды очищают путем хроматографии на 400 г геля коем- невой кислоты 60 (для каждого раза 400 г) в системе хлороформ:метанол: :вода 70:30:5. Продукт, содержащийся во фракциях 9-172,-растворяют в 100 мл дважды дистиллированной воды и чистят путем фильтрации (AMICON - мешалка 402, ультрафильтр РМ 10/76 мм) аналогична примеру 1. Раствор фильтруют с помощью фильтра с миллипорами (0,2 мкм) и лиофилизи- руют. Получают ..динатриевую соль ( -Ь-аланин-2-(1,2-дипалмитоил-Бп-гли- церо-3-оксифосфорилокси)-этиламида К-ацетил-мурамил-Ь-аланил-В-глютами- новой кислоты, содержащую 4,89 моль воды, в виде бесцветного рыхлого порошка.
2.О
Ccilj, 10+1 С°(С 0,675; мета нол), выход соли 1,1 г (25%);
Rf 0,08 (хлороформ:метанол:во- да 70:30:5);
Rf 0,15 (этиловый эфир уксусной кислоты:h-бутанол:пиридин:уксусная кислота:вода 42:21:21:6:10);
Rf 0,30 (хлороформ:метанол:вода :уксусная кислота 70:40:9:1).
Проведены биологические испытания полученных предложенным способом солей мурамилпептидов.
Альвеолярные макрофаги крыс,полу- ченные при промывке легких, инкубируют 24 ч ли бо с липосомами, включающими активное вещество, либо в физи ологическом растворе с активным веще ством. Вводят опухолевые клетки, мар Кированные I. Инкубируют 72 ч. По гибшие опухолевые клетки отмывают, определяют число живых клеток по их радиоактивности. Активность макрофагов оценивают на основе клеточной токсичности., т.е. по числу животных, погибщих при опытах. Удельная клеточ ная токсичность (%) рассчитьшалась следующим образом:
100
срм в опухолевых клетках, ин кубированных макрофаги актив ным началом
срм в опухолевых клетках, ин кубированных макрофаги и PBS Опыты проведены со следующими соединениями:
I - натриевая соль N-ацетил-му рамил-Ь-аланил-В-глютамил -(СУ)-Ъ-аланил-2-(1,2-ди- палмитоил-Бп-глииеро-З-ок- сифосфорилокси)-этиламида;
15
25
9951624
11 - натриевая соль N-пропионил-нормурамил-11-аланил-В-. -глютамил (Сс)1)-п-бутиловьпт эфир-(СУ)-Ь-аланил-2-( 1 ,2- 5-дипальмитоил-Зп-глицеро-3-оксифосфорилокси)-этил- амида, (пример 5); III - натриевая соль N-пропионил-нормурамил-Ь-аланил-В -глютамил ( COL)-п-метил эфир- -(С)-Ь-аланил-2-(1 ,2-ди- пальмитоил-Бп-глицеро-З- -оксифосфорилокси)-этил- амида (пример 4); IV - натриевая соль N-ацетил- -мурамил-Ь-аланил-Б-глю- тамил-(Cd) -трет.-бутилэфир -(су) -Ь-аланин-2-(1,2-ди- пальмитоил-Зп-глицеро-З- 20 -оксифосфорилокси)-этил- амида (пример 3); V - натриевая соль N-ацетил-г -мурамил-Ь-аланил-р-глюта- мил-(Со1.)метш10вый сложный эфир (СУ)-Ь-аланин-2-(1 ,2- -дипaльмитoил-Sn-глицepo- -3-oкcифocфopилoкcи)-этил- амида (пример 2); VI - натриевая соль N-пропионил-нормурамил-Ъ-аланил-Б--глютамил-(Col)-сложный трет.-бутиловый эфир-(су)- -аланин-2-(I,2-дипальмит- тоил-8п-глицеро-3-оксифос- 35 форилокси)- этиламида (пример 6).
Полученные результаты сведены в табл. 1.
40
Проведено сравнение производных
мурамилпептидов обшей формулы I с известным соедийением.
Испытание на пирогенность проведе- но на кроликах и показало, что при подкожном введении высоких доз, как 30 мг/кг К-ацетил-мурамил-Ь-аланил- -D-глютамил- (Cd.) -м-Путил эфир- (C,V} -L- -аланин-2-(1,2-дипальмитоил-5п-гли- Q церр-3-оксифосфорилокси)-этиламид- -соль натрия (соединение II) не наблюдается пирогенного эффекта.
В противоположность этому при тех же дозах натриевой соли N-ацетил- j -мурамил-Ь-аланил-В-изоглютаминил-Ь- -аланин-2-(1,2-дипалмитоил-Зп-глице- ро-3-оксифосфорилокси)-этиламида (VIl) наблюдается сильное повьш1ение температуры.
30
25
Результаты испытания на пироген- ность при внутривенном введении испытуемых соединений в дозе 1 мг./кг показаны в табл. 2.
Результаты показьшают, что измен ние температуры ( лТ С) в случае предложенных соединений примерно в 2-4 раза ниже, чем в случае известнго соединения уНо Кроме того, мура илпептиды формулы I могут успешно применяться для профилактики и лечения заболеваний, вызьшаемых ДНК - врусами с кубической симметрией и ну леокапсидом без оболочки, ДНК - вирусами с вирионом в оболочке, а также РНК - вирусами с кубической сим- метрией капсида и РНК - вирусами со спиральной симметрией капсида.
Соединения формулы I предпочтительно использовать в случае ДНК- вирусов с вирионом в оболочке и кубческой симметрией капсида, в случае РНК-вирусов с кубической симметрией капсида и варионом без оболочки, а также в случае РНК-вирусов со спиральной симметрией капсида, в котор нуклеокапсидная оболочка расположен у наружной поверхности мембраны, и, кроме того, в случае Adenoviridae, Poxvirides, Coronaviridae, в частности, при человеческих Coronaviren.
В первую очередь соединения сЬор- fyлы I применяют в случае Herpesvir dae, picornaviridae, Myxoviren, a
также в сл. учае masfadenviren, в час
ности человеческих заболеваний, причем сильное действие проявляется не только в случае бактериальных возбудителей, но и против вирусных возбудителей. Эти-соединения проявляют длительное профилактическое или терпевтическое действие, длящееся от многих дней до нескольких недель после однократного приема соединений формулы I, получаемых предложенным способом, а такхе эффективное воздействие на широкий спектр вирусных возбудителейо
Проведены испытания антивирусной активности предложенных соединений.
А натриевая соль N-ацетилмура- мил-Ъ-аланил-С-глютаминовой кислоты -(СУ)-Ъ-аланил-2-(1,2-дипальмитоил- -сн глицеро-3-оксифосфорш1окси) - -этиламид.
В натриевая соль N-ацетилмура- мил-Ъ-аланил-Б-глютамил-(Су)- -бутил овьй сложный эфир-(Сс1-)-Ь-аланин
26
0
15
5
35 фдр
-2-(1,2-дипальмитоил-сн-глицеро-З- -оксифосфорилокси)-этиламид.
С натриевая соль N-ацетилмура- мил-Ьаланил-В-глютамил-(G У)-метиловый сложный эфир-(Сс1)-Ь-аланин-2- (1,2-дипальмитош1-сн-глицеро-3-окси- фосфорилокси)-этиламидо Каждую из 20 и 30 самок мышей - MF-2f SPP весом каждая по 1А-16 г заражают через нос, применяя легкую анастезию и используя смесь из равных частей ди- этилового эфира, этанола и хлороформа, образующих пластинки единицами вирусовых штамов Influenza А(Texas) 1/77 (адаптирующихся мьппами) в количестве 1- в виде 0,05 мл взвеси вирусов .
В указанный срок для заражения в организм каждой их мышей вводят единожды (единичная доза) согласно табл. 1 количестт о активного ингредиента в 0,2 мл 0,005%-ного по весу раствора натрий-карбоксиметилцеллюло- уе зы В дважды дистиллированной воде через нос или через рот.
Остальные из числа указанных мышей, т.е. 10 или 20 животных служат в качестве контрольных: им вводят плацебо (0,005%-ный по массе раствор натрий-карбоксиметилцеллюлозы)„
Через нос активный ингредиент вводят, применяя легкую анестезию с использованием смеси из равных частей диэтилового эфира, этанола и хлоро0
30
0
5
0
5
Процентное количество мьш1ей, оставшихся в живых через 24 дн. после заражения, приведено в табл. 3.
Проведено сравнение с известным антивирусным агентом (действует на вирусы Influenza А) - амантадином. Действие амантадина начинается только при дозе в несколько мг/кг, значение ЛДдд для мыгаей составляет 700 мг/кг.
Предложенное соединения действуют уже при дозе 0,1 мг/кг, в определенных случаях уже при 0,01 мг/кг, в то время как значения для мышей составляет более 3000 мг/кг. Это значит, что диапазон терапевтического действия предложенных соединений по сравнению с амантадином значительно шире. К тому же, предложенные соединения проявляют антивирусное действие уже после их однократного применения не более чем за 7 дн, до зара27
жения или после него, в то время как амантадип необходимо вводить уже до заражения, например за 24ч до заражения, и продолжать ежедневное введение в течение не менее 5дн., т.е. предложенные соединения проявляют как терапевтическое, так и профилактическоедействие, в то время как амантадин проявляет только поофилактическое действие.
Ш20Н
29951628
Кроме того, производные мурамил- пептидов обпей (Формулы I малотоксичны. В табл. А показана острая токсичность, определ енная на мышах.
Формула изобретения
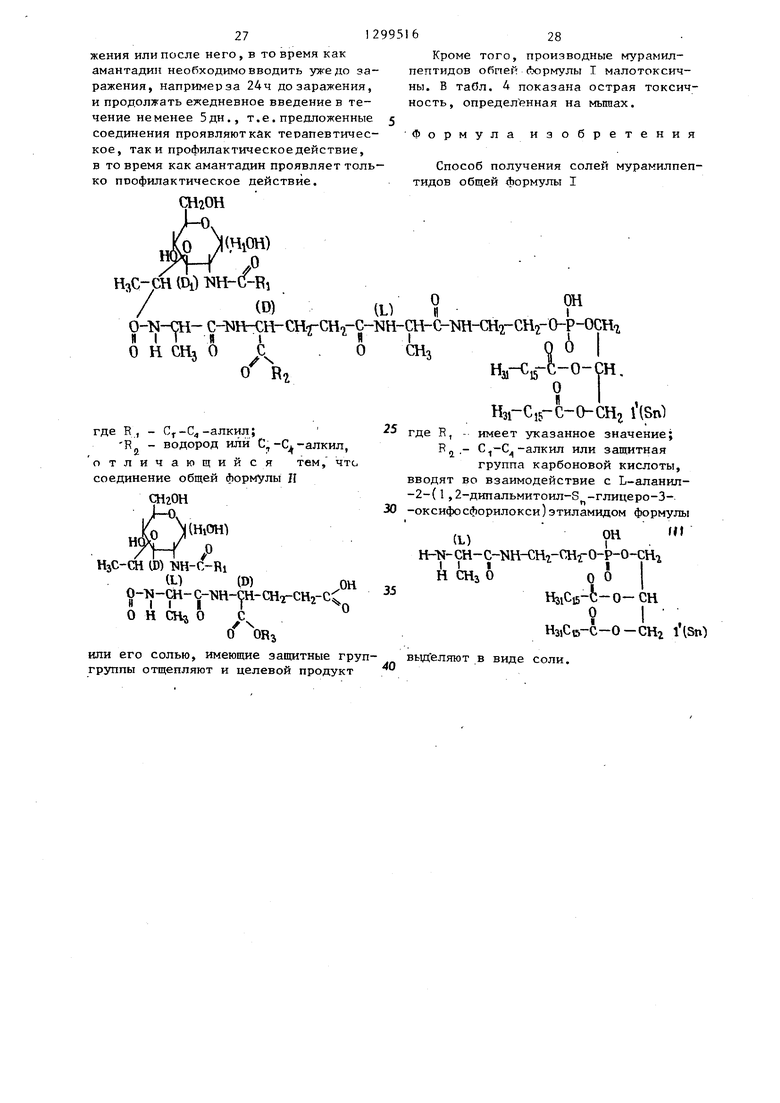
Способ получения солей мурамилпеп- тидов общей формулы I
)
дС-ш (DI) TQH-ef-Bi
/(D)
а)
O-TSJ-CH- C- IH-CH-CH CH -C-NH- II I 1 я и с . о
/
о R
п .п
о Н СН.З о
где R, - С -С -алкил;
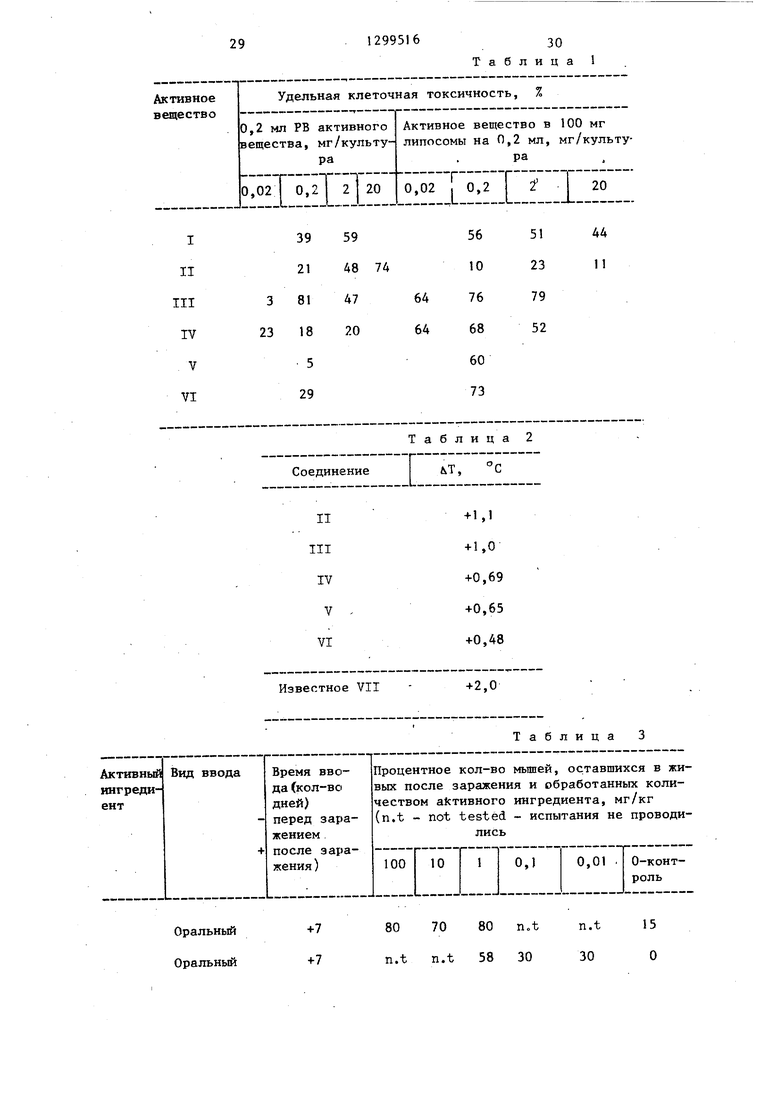
E - водород или с,-С -алкил, отличающийся тем, чтс. соединение общей формулы Л
снгОН
(HiOH)
/
НзС-Ш Ш) -NH-C-Ri
а) (D)он
O- -N-CH- C-TQH-CH-CHr-CHz-C
f IT rvr
0 H CHa 0
/Ч 0 ORj
о
он
-CH-C-Ml-CH -CHj-Q-p-OCH
снзQ
HM
:-o-CH
0
n I
Hsi-Cjs-C-O-CHj l (Stv)
где R, - имеет указанное значение; RJ.- С,-С,-алкил или защитная
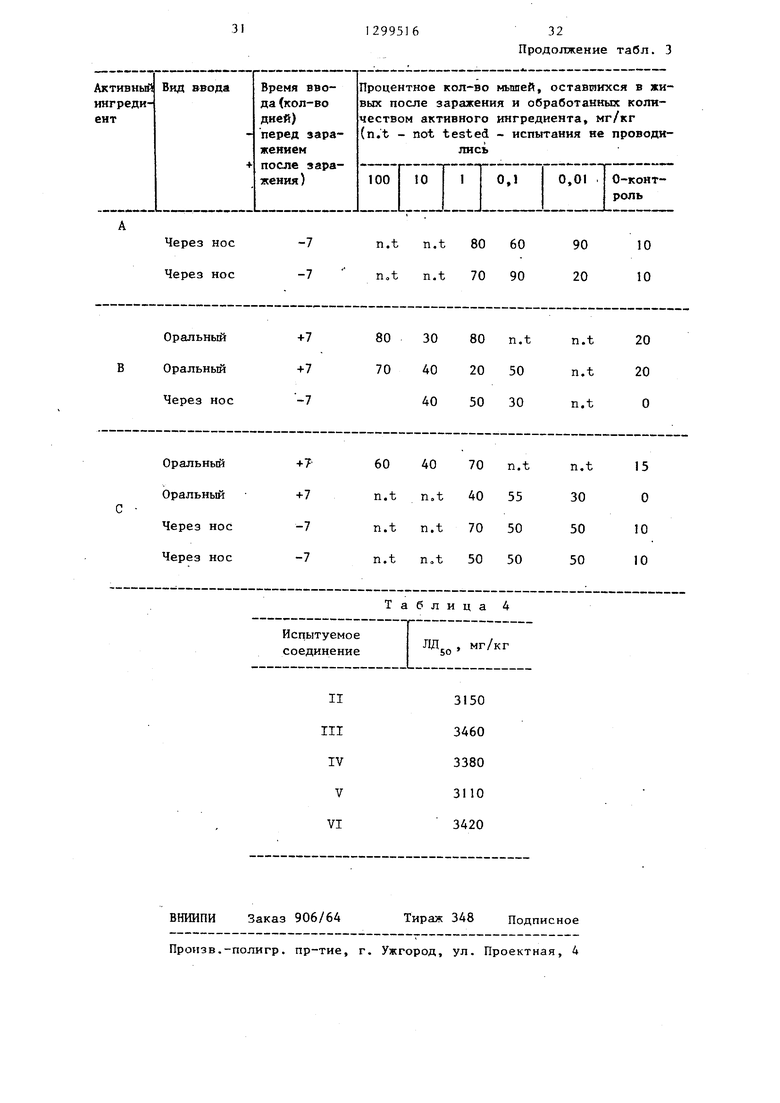
группа карбоновой кислоты, вводят во взаимодействие с L-аланил- -2-(1,2-дипальмитоил-3 -глицеро-3- -оксифосфорилокси)этиламидом формулы
(L) Н И H- N-CH-C-ИН-СНг-ШгО-Р-О-СНг
н снз О о о I
4iiCi5-l -0-СН
V I .
H3iCe-C-0-CH2 llSn)
или его солью, имеющие защитные груп- вьщ еляют в виде соли.
группы отщепляют и целевой продукт
40
29
Активное вещество
Удельная клеточная токсичность, %
0,2 мл РВ активного вещества, мг/культура
0,021 0, 2
3 23
39 21 81 18 5 29
Таблица2 СоединениеМ, °С
II+1,1
III+1,0
IV+0,69
V, +0,65
VI+0,48
Известное VII -+2,0
Таблица 3
Активный Вид ввода Время вво-Процентное кол-во мьшей, оставшихся в жиингреди- да(кол-вовых после заражения и обработанных колиент дней)чеством активного ингредиента, мг/кг
перед зара-(n.t - not tested - испытания не проводи- жениемлись + после заражения)100 10 I 1 0,1 0,01 . 0-контроль
Оральный Оральный
+7
+7
129951630
Таблица i
Активное вещество в 100 мг липосомы на 0,2 мл, мг/культу- ра
20
0,02 0,2 1 2 J
20
74
64 64
56 10 76 68 60 73
51 23 79 52
44 11
80 70 80 n.t n.t 15 n.t n.t 58 30 30 О












Изобретение касается замещенных пептидов, в частности натриевых солей мурамилпептидов: N-ацетил-мура- мил-Ъ-аланил-Б-глютамил-(С 1)-L-ала нил-2-(1,2-дипалмитоил-Зп-глицеро-3- -оксифосфорилокси)-этилс1мида (l); N- -аце тил-мурамил-L-аланил-В-глютамил- -(Cot)-алкиловый эфир ( )-(CV)-L- -аланил-2-(I,2-дипальмитош1-5п-глицеро-3-оксифосфорилокс-О-этиламида (и), которые обладают антивирусной активностью и могут быть использованы в медицине. Для выявления активности ; среди замещенных пептидов были получены новые соли I и II. Синтез ведут из N-ацетил-мурамил-L-аланил-D-глю- таминовой кислоты или ее С( алкило- вого () эфира, который в среде смеси растворителей (СН 01 + ) в присутствии N-оксисукцинимида и ди- циклогексилкарбодиимида конденсируют с натриевой солью Ь-аланил-2-(1,2- -дипальмитоил-8п-глицеро-3-оксифос- форилокси)-этиламида при комнатной температуре. Испытания I и II показывают, что они обладают лучшей антивирусной активностью, чем известньп Н-ацетил-мурамил-Ь-аланил-2-(1,2-ди- пальмитоил-8п-глицеро-3-оксифосфорил- окси)-зтенсламид (пирогенность в лТ °С, .составляет 0,48-1,1 против 2). Кроме того, I и II можно использовать против вирусных и бактериальных воз- ,будителей и для профилактики заболеваний. 4 табл. СО ьо со со СЛ О5 СМ

| Шредер Э | |||
| Любке К | |||
| Пептиды, М.; Мир, 1967, ч | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ получения бензидиновых оснований | 1921 |
|
SU116A1 |
| Распределительный золотник к паровой копровой бабе | 1930 |
|
SU25495A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Приспособление для изготовления в грунте бетонных свай с употреблением обсадных труб | 1915 |
|
SU1981A1 |
Авторы
Даты
1987-03-23—Публикация
1983-07-22—Подача