Изобретение относится к новым про- изводньм митомицина С, а именно к 7- замещенным 9а-метоксимитозана общей формулы
О
о
I СНоОС-В
t-t
осн
(i)
где А - амино-, метокси- или. группа общей формулы
Ь
R R N - 4
В - амино- или амидиновая группа общей формулы
. R,R 4
где R, - водород, формил или метил;
R - водород или метил; R и R - каждый в отдельности метил
3
или изопропил или вместе с атомом азота,к которому они присоединены, образуют пиперидин или морфолин, обладающим противоопухолевой активностью.
Целью изобретения является поиск в ряду производных митомицина С соединений, обладающих более высокой противоопухолевой активностью.
Пример 1. 7- (Диметиламино) метилен амино-N (диметиламино)-ме- тилен-9а-метоксимитозан (соединение I ).
7-(Дйметиламино)метилен амино- N . -(диметиламино)-метш1ен-формил- 9а-метоксимитозан (соединение II).
К суспензии 500 мг (1,50 мМ) митомицина С в 25 мл хлороформа добавля- ют в целом 9,6 мл (2,4 мл порциями через О, 18, 21 и 23ч) N, N-диметил- формамид диметштацеталя и суспензию перемешивают при 50°С в течение 41 ч После выпаривания растворителя и из- бытка реагента при пониженном давлении получают темно-зеленьй остаток; ТХС (хлористый метилен/метанол 20:1) показывает отсутствие митомицина С при наличии двух новых зеленых ком- понентов (R f 0,16 и 0,22). Основной компонент (R f 0,16) вьщеляют хроматографией мгновенного испарения используя смесь хлористый метилен
5
0
5
0
0
5 Q
(метанол 20:1) в качестве элюента, в виде зеленого твердого вещества (340 мг 51,5%), который после растворения в диэтиловом эфире с последующим добавлением гексана дает соединение I в виде темно-зеленого аморфного порошка.
Вычислено
Найдено,%: С 56,20; Н 6,28; N 17,88.
.
Вычислено,%: С 56,71; Н 6,08; N 18,90.
Второстепенный компонент (R f 0,22) вьщеляют (180 мг, 25,35%) в в виде аморфного твердого вещества, которое после осаждения из диэтило- вого эфира и гексана идентифицируют как соединение II,
. Найдено,%: С 55,41; Н 5,96; N 16,99.
C.,.
Вычислено,%: С 55,89; Н 5,93; N 17,78.
В растворах соединений I и II либо в этилацетате, либо в Ы,Ы-диметил- формамид диметилацетале при стоянии при комнатной температуре более 10 ч происходит превращение соединения II (R f 0,22) с соединение I (R f 0,16), что удостоверяется ТСХ, с получением раствора с повышенным содержанием соединения I.
Примеры 2-7 выполняют аналогично примеру 1 с модификациями, указанными ниже, с получением различных дополнительных соединений предлагаемо- . го изобретения,
П р и м е р 2. 7-(Диизопропилами7 но)метилен амино-N (диизопропилами- но)метилен-9а-метоксимитозан (соединение III ).
Суспензию митомицина С (200 мг, 0,6 мМ) в Ы,К-диизопропилформамид диэтилацетале (3 мл) нагревают при перемешивании в течение 15 ч при53°С. Реакционную смесь выливают в 50 мл воды и экстрагируют этилацетатом (3 30 мл). Объединенньш органический экстракт сушат (Na , SO) и выпаривают с получением темно-зеленого сиропа, ТСХ (хлористьш метилен/метанол 10:1) показывает наличие основного зеленого компонента с R f 0,43 и примесей,, движущихся быстрее (R f 0,45-0,50). Основной компонент III вьщеляют в виде темно-зеленого твердого вещества (156 мг, 46,8%) с по-.
313
мощью двукратной хроматографии мгновенного испарения с использованием . смеси хлористый метилен/метанол 20:1 в качестве элюента.
Найдено,%: С 62,03; Н 7,80; Г N 14,60.
Вычислено,%: С 62,55; Н 7,91; N 15,10.
Пример 3. 7-(Диметиламино) метилен амино-Н ° -(диметиламино)- мeтилeн-9a-мeтoкcи-N -метилмитозан (соединение IV );
В этом примере порфиромицин (N - метилмитомицин С), 130 мг (0,37 мМ) замещают в качестве исходного соединения в реакции с 0,8 мл (1,5 мМ) К,М-диметилформамид диметилацеталя, используя 10 мл хлороформа и 2 мл метанола в качестве реакционного растворителя, время реакции 50 мин при 50°С. Соединение IV получают в виде сиропа после выпаривания реакционного растворителя. Это соединени затем очищают хроматографией мгновен ного испарения, используя 20 г сили- кагеля и смесь хлористый метилен/метанол (20:1) в качестве элюента.
Найдено,%: С 57,11; Н 6,11; N 17,49.
СааНзо бО,,.
Вычислено,%: С 57,60; Н 6,55;
N 18,33.
Эта методика дает соединение V : 7-амино- М -диметиламино-метилен-9а- метокси-N.-метилмитозан, в качестве побочного продукта с выходом 30%, тех : R f 0,40 (хлористый метилен/ /метанол 9:1).
Найдено,%: С 54,68; Н 6,13; - N 16,59.
.
вычислено,%: С 56,53; Н 6,20;
N 17,38.
П р и м е р 4. 9а-Метокси-7-(1- пиперидиниламино) метилен амино- N -(1-пиперидинилметилен) митозан (соединение VI).
Ы-(диэтоксиметил) пиперидин (3 мл) и митомицин С (200 мг) взаимодействуют при в течение 2,5 ч в хлороформе (3 мл). Продукт получают с выходом 27,6%, тех : R f 0,20 (хлористый метилен/метанол 20:1).
Найдено,%: С 61,01; Н 6,85; N 15,34.
C,,H,,.
14
Вычислено,%: С 61,79; Н 6,87; N 16,02.
Ы -формил производное предыдущего вещества, N -формил-9а-метокси- 7-(1-пиперидиниламино)метиленУами- ( 1-пиперидинилметилен) митозан получают в качестве основного компонента, выход 43%, ТСХ : R f 0,25 (хлористый метилен/метанол 20:1).
Найдено,%: С 59,99; Н 6,17; N 15,07.
C gHseN G.
Вычислено,%: 60,08; Н 6,52; N 15,21.
П р и м е р 5. 9а-Метокси-7-11( 1- морфолино) метилен амино-N (l-MOp- фолино-метилен митозан (соединение VIlX
Перемешиваемую суспензию митоми- цина С (200 мг, 0,6 мМ), в хлороформе (10 мл) и N-диэтокси метилморфо- лнна (4 мл) нагревают при 53 С в течение 42 ч. Реакционную смесь концентрируют до консистенции сиропа под высоким вакуумом. С помощью сырой хроматографии мгновенного испарения (crude flash Chromatogra- phy) (хлористый метилен/метанол 25:1 отделяют зеленые компоненты от избытка реагентов. Объединенные зеленые реагенты растворяют в 20 мл этилаце- тата и промьгоают водой (3 20 мл). Объединенные промывки реэкстрагируют этилацетатом (3 15 мп). Все этилаце татные фракции объединяют, сушат (Na 80 ) и вьшаривают до темно-зеленого сиропа, ТСХ (хлористый метилен/ /метанол 10:1) которого свидетельствует о наличии отдельного компонента с R f 0,33 и нескольких зеленых примесей (R f 0,35-0,40). С помощью хроматографии мгновенного испарения компонент cRf 0,33 вьщеляют (130 мг, 56,8%) в виде темно-зеленого аморфного твердого вещества, которое характеризуется как соединение VII).
Найдено,%: С 53,07; Н 6,03; N 15,37. -. ,,N,0,.
Вычислено,%: С 56,78; Н 6,06; N 15,90.
Пример 6. 7-Амино-Ы -диме- тиламинометилен-9а-метоксимитозан (соединение VIII).
200 г митомицина С (0,6 мМ) растворяют в 10 МП хлороформа и 2 мл метанола, добаЬляют N,N-димeтилфopмa МИД диметилацеталь (0,64 мл,4,8 мМ) и раствор перемешивают при 50 С в течение 50 мин. Тонкослойная хроматография (хлористый метилен/метанол 90:10) показывает следы непрореагировавшего митомицина С (R f 0,22) и два новых компонента (R f 0,42 и 0,33 соответственно). Раствор концентрируют при пониженном давлении до консистенции сиропа, этот сироп подвергают хроматографии мгновенного испарения (25 г силикагеля), используя хлористый метилен/метанол (20:1) в качестве элюента.
Быстрый компонент (R f 0,42) выделяют в виде зеленого аморфного твердого вещества (60 мг, 22,5%) и идентифицируют как соединение I с помощью его ЯМР-спектра (пиридин d).
Основной синий компонент (R f 0,33) выделяют в виде аморфного твердого вещества (148 мг, 63,3%) и характеризуют как соединение VIII.
амино)этилиден 9-метоксимитозан (соединение X).
600 мг суспензии (1,79 ммоль) митомицина С в 2 мл метанола обра5 батывают 3 мл Ы,М-диметилацетамид диметилацеталя. Затем суспензию нагревают до 75-80°С и перемешивают в течение 2 ч. На этой стадии ТСХ (хлористый метилен/метанол 10:1) показыfO вает, что почти весь митомицин С израсходован в процессе реакции. На хроматографе полученный продукт проявляется в виде зеленой полосы.Растворитель и летучие вещества удаляют
)5 концентрированием реакционной смеси досуха при пониженном давлении с получением сиропа, который растворяют в хпористом метилене и наносят на колонку с 40 г .силикагеля, после че20 го колонку элюируют 200 мл 1%-ного метанола в хлористом метилене,200 мл 2%-ного метанола в хлористом метилене и 400 мл 5%-ного метанола в хлористом метилене. Фракции, содержащие
Аналитический образец получают осаж 25- зеленую полосу, представляющую собой
продукт, объединяют и концентрируют до аморфного твердого вещества, весящего 110 мг. Выход 13%. Это вещество растворяют в 2 мл ацетона и осаж- 30 дают из раствора добавлением гексана. Продукт собирают фильтрацией. Найдено,%;: С 58,89; Н 6,89; 17,64.
дением из хлористого метилена и н - пентана.
Найдено,%: С 54,70; Н 6,14; N 17,95.
C..Oj.
Вычислено,%: С 55,48; Н 5,91; N 17,98.
N
,10
35
Пример 7. 7,9а-Диметокси- N -диметиламинометиленмитозан (соединение IX ).
Вместо митомицина С (пример 1) берут митомицин А (170 мг) и подвергают взаимодействию с Ы,К-диметилфор-,.,, мамиддиметилацеталем (0,6 мл) в растворе хлороформ/метанол (10:1) при 50°С в течение 1 ч. Целевой продукт получают с выходом 48%, ТСХ : R f 0,50 (смесь хлористый метилен/метанол 9:1).
Найдено,%: С 56,51; Н 5,92;
N
С з з вО Вычислено,%: С 58,46; Н 6,83;
17,79.
Противоопухолевая активность по отношению к Р-388 Murine лейкемии. В табл. 1 приведены результаты лабораторных исследований на CDF, мышах-самках, которым внутрибрюшинно имплантировали опухолевый прививочный материал, содержащий Ю асцитны
клеток Р-388 murine лейк емии, и кото 45 рым вводили различные дозы тестируемого соединения формулы I или митомицина С.
С,а «a.N.Oe
N 13,71.
Соединения вводили путем внутри„ брюшинной инъекции. На каждую дозу брали группу из шести мышей, которые получали одну единственную дозу соединения в первый после заражения день. В каждую серию экспериментов
с г включали группу из десяти мьш1ей, которым вводили физиологический раствор. Группы, обработанные митомициВычислено,%: С 56,39; Н 5,94; N 13,85.
N -формил производное соединение IX получают в виде соединения 1Ха, 7, 9а-диметокси-М ° -диметиламиномети- лен-N 1а-формилмитозана с выходом 16,5%, тех : R f 0,61 (хлористый метилен/метанол 9:1).
Примере. 7- 1-(Диметилами10
но)этилиден1 амино-N - 1-(диметилном .с, были включены в качестве положительного контроля. Для каждой
амино)этилиден 9-метоксимитозан (соединение X).
600 мг суспензии (1,79 ммоль) митомицина С в 2 мл метанола обрабатывают 3 мл Ы,М-диметилацетамид диметилацеталя. Затем суспензию нагревают до 75-80°С и перемешивают в течение 2 ч. На этой стадии ТСХ (хлористый метилен/метанол 10:1) показывает, что почти весь митомицин С израсходован в процессе реакции. На хроматографе полученный продукт проявляется в виде зеленой полосы.Растворитель и летучие вещества удаляют
концентрированием реакционной смеси досуха при пониженном давлении с получением сиропа, который растворяют в хпористом метилене и наносят на колонку с 40 г .силикагеля, после чего колонку элюируют 200 мл 1%-ного метанола в хлористом метилене,200 мл 2%-ного метанола в хлористом метилене и 400 мл 5%-ного метанола в хлористом метилене. Фракции, содержащие
зеленую полосу, представляющую собой
пр до ся во да
N
35
С з з вО Вычислено,%: С 58,46; Н 6,83;
N
17,79.
Противоопухолевая активность по отношению к Р-388 Murine лейкемии. В табл. 1 приведены результаты лабораторных исследований на CDF, мышах-самках, которым внутрибрюшинно имплантировали опухолевый прививочный материал, содержащий Ю асцитных
клеток Р-388 murine лейк емии, и кото- рым вводили различные дозы тестируемого соединения формулы I или митомицина С.
ном .с, были включены в качестве положительного контроля. Для каждой
713018318
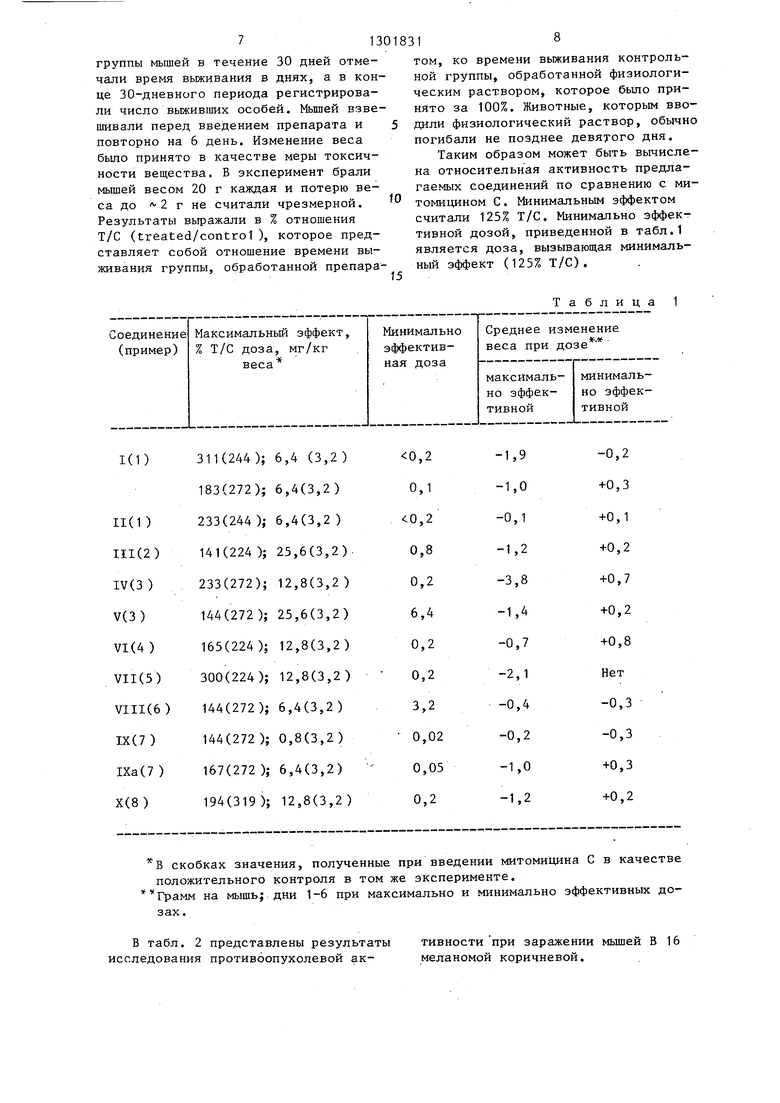
группы мышей в течение 30 дней отме-том, ко времени выживания контрольчали время выживания в днях, а в кон-ной группы, обработанной физиологице 30-дневного периода регистрирова-ческим раствором, которое было прили число выживших особей. Мышей взве-нято за 100%, Животные, которым ввошивали перед введением препарата и 5дили физиологический раствор, обычно
повторно на 6 день. Изменение весапогибали не позднее девятого дня. было принято в качестве меры токсич- Таким образом может быть вычислености вещества, В эксперимент бралина относительная активность предламышей весом 20 г каждая и потерю ве-гаемых соединений по сравнению с миса до Л 2 г не считали чрезмерной. томицином С. Минимальным эффектом
Результаты вьфажали в % отношениясчитали 125% Т/С. Минимально эффекТ/С (treated/control ), которое пред-тивной дозой, приведенной в табл.1
ставляет собой отношение времени вы-является доза, вызывающая минимальживания группы, обработанной препара-ньш эффект (125% Т/С),
15
В скобках значения, полученные при введении митомицина С в качестве
положительного контроля в том же эксперименте.
Грамм на мышь; дни 1-6 при максимально и минимально эффективных дозах .
В табл. 2 представлены результаты тивности при заражении мьш1ей В 16 исследования противоопухолевой ак- меланомой коричневой.
15
Таблица 1
Эксперименты проводили на В DF мышах, которым внутрибрюшинно ино- кулировали опухолевый имплантант. Прот5шенность эксперимента 60 дней. На каждую дозу тестируемого соединения брали группу из 10 мышей и для каждой группы определяли время выживания. У контрольных животных,ино- кулированных так же, как и опытные животные, и инъекцированных растворителем без препарата, время выживания составляло 21 день. Отношение времени вьокивания опытных животных ко времени выживания контрольных (.% Т/С) использовали в качестве меры
В скобках значения контроля с митомицином С,
Соединения исследовали на противоопухолевую активность по отношению К В 16 Murine меланоме при подкожном введении опухолевого имплантанта и внутривенном введении препарата,График введения препарата и значения времени выживания (исследования проводили в течение 40 дней) определяли как указано. На 12-й день измеряли изменение веса. Максимально эффективная доза соединения I была 30 мг/кг. Эта доза вызывала эффект , 156% Т/С и прирост веса 1,5 г. В группы брали по шесть животных, и при этой дозе мыши выживали в течение всех 40 дней Минимально эффективная доза была 0,25 мг/кг, при этой дозе на 12-й день изменение веса равнялось 1,0 г
Минимально эффективную дозу мито мицина С не определяли.
В кратком токсикологическом исследовании группам из пяти белых В DF мьшей на дозу внутрибрюшинно вводили
„
эффективности и для каждого тестируемого соединения определяли максимально эффективную и минимально эффективную дозы. За минимально эффективную дозу принимали такую дозу, которая вызывала 125% Т/С эффект. Для каждой дозы опытным животным внутрибрюшинно вводили тестируемое соединение на 1-й, 5-й и 9-й день. Среднее изменение веса в день, отмеченное при максимально эффективной дозе и при минимально эффективной дозе, использовали в качестве меры токсичности. Потеря веса в 2 г для 20 г мыши не считалась чрезмерной.
Таблица 2
40
45
50
55
однократную дозу соединения. В результате при оптимально эффективной дозе вводимого соединения не наблюдалось значительного уменьшения числа лимфоцитов. При этой дозе также не отмечалось значительного повьппе- ния азота мочевины крови (В un) или сывороточной глютаматфосфотрансфера- зы (SIPT), что указывает на отсутствие неблагоприятного воздействия на функцию почек или печени, а также на то, что препарат не подавляет активность лимфоцитов.
Ввиду высокой противоопухолевой активности, выявленное в экспериментах на животных, а также пониженной токсичности в сравнении с митомицином С данное изобретение включает использование соединений общей фор- гyлы I для подавления опухолевого роста у млекопитающих. В этих целях они применяются системно (по всему организму) у млекопитающих, имеюищх
П 130183112
опухоли, в основном в нетоксичных 1
противоопухолевых эффективных дозах.R R N-C NФормула изобретенияВ- амино- или амидиновая группа
5общей формулы
7-Замещенные 9а-метоксимитозанаRj
общей формулы ,R R
водород, формил или метил;
Q 0Rj - водород или метил;
АХ, лртд 3 4 каждый в отдельности метил
| |Г IxJ ri iили изопропил или вместе с
CH iIi { TST -nатомом азота, к которому
Q 1L 1они присоединены, образуют
5пиперидин или морфолин,
где А - амино-, метокси- или группаобладающее противоопухолевой актив- общей формулыностью.




Изобретение касается производных мнтомизина С, в частности соединений общей формулы I CHj -С СА - С(0)-С« -0(0, сн- -сн,-о - с (о)-в, -c-N-c(ocH,) - сн. CHjСН;NR. м НА, ных ий о)-в, ;NR. где А - OCHj; R R N-CCR) N-; В - (R,,)N-; , CH, формил; R -H; CH.j; каждый в отдельности метил или изопропил или вместе с N -пиперидин или мор- фолин, которые как обладающие противоопухолевой активностью могут быть использованы в медицине. Для выявления лучшей активности у соединений указанного класса бьши получены новые I, Синтез их ведут из митомицина С или митомицина А или их N-алкилпро- изводных с соответствующим амидоаце- талем в безводной среде органического растворителя (хлороформ, дихлор- метан, а также смесь хлороформа и метанола) при 50-65 С до получения соединения, где В или А+В представляют собой группу )N-, с последующим хроматографическим вьщелением целевого I, Активность последнего по отношению времени выживания группы, обработанной препаратом, ко времени выживания контрольной группы составляет 141-311% при дозе 25,6-6,4 мг/кг массы(для Р 388 Murin лейкомии). 2 табл. to (Л со о оо 00

| Патент США № 3121084, кл | |||
| Прибор для периодического прерывания электрической цепи в случае ее перегрузки | 1921 |
|
SU260A1 |
Авторы
Даты
1987-04-07—Публикация
1983-10-18—Подача