сд i
;с



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения гликозида | 1987 |
|
SU1590045A3 |
| Способ получения антрациклиновых гликозидов | 1986 |
|
SU1553015A3 |
| Способ получения 6-деоксиантрациклингликозидов | 1984 |
|
SU1429935A3 |
| Способ получения антрациклингликозидов | 1983 |
|
SU1378784A3 |
| АНТРАЦИКЛИН ГЛИКОЗИДЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВЫМИ СВОЙСТВАМИ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1990 |
|
RU2043360C1 |
| АНТРАЦИКЛИН ГЛИКОЗИД И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1992 |
|
RU2081878C1 |
| Способ получения 4-йодпроизводных антрациклингликозидов | 1982 |
|
SU1181550A3 |
| Способ получения антрациклиновых гликозидов | 1988 |
|
SU1614764A3 |
| Способ получения 4 @ -дезокси-13(S)-дигидро-4 @ -йододоксорубицина | 1988 |
|
SU1760986A3 |
| Способ получения рацемических аглюконов | 1983 |
|
SU1311616A3 |
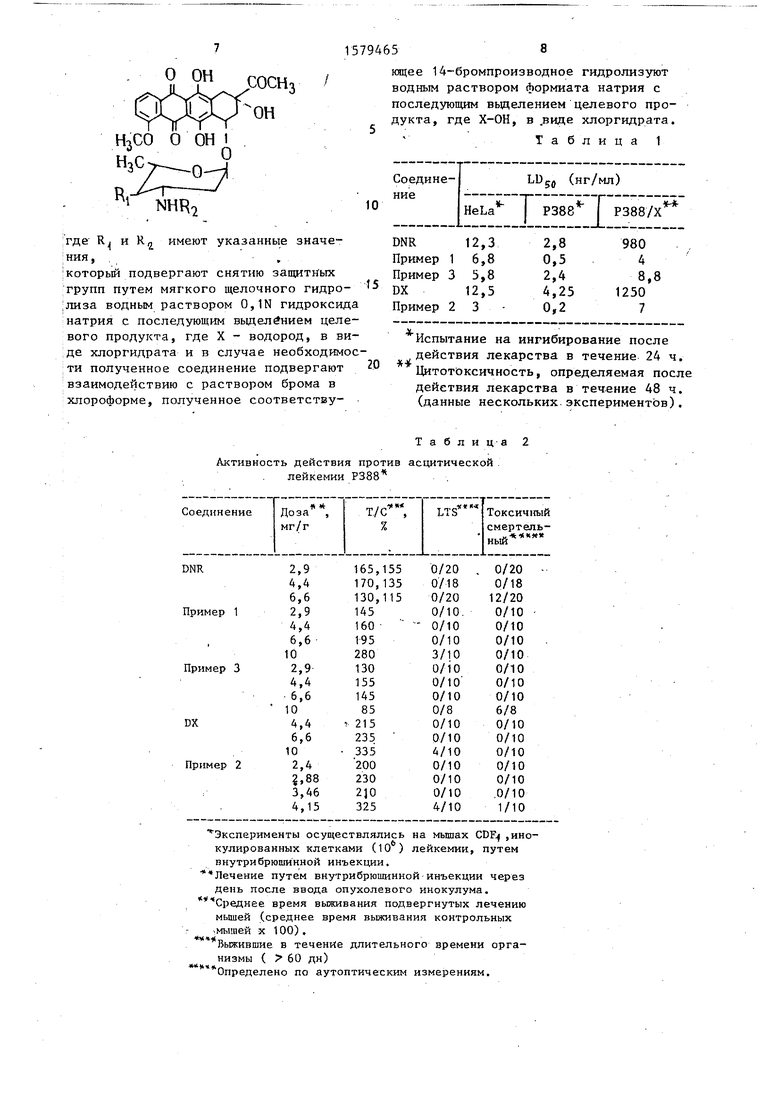
Изобретение касается гликозидов, в частности получения 4-деокси-4-бромдаунорубицина или 4-деокси-4-бромдоксорубицина, или 4-деокси-4-хлордаупорубицина, или 4-деокси-4-хлордоксорубицина, обладающих противоопухолевой активностью, что может быть использовано в медицине. Цель - создание новых более активных веществ указанного класса. Синтез ведут реакцией 4 1-эпи-4 1-0-трифторметансульфонил-N-трифторацетилзамещенного даупорубицина в водном CH 2CL 2 с тетра(N-бутил)аммоний бромидом (хлоридом) при комнатной температуре с последующим снятием защитных групп в полученном веществе с помощью мягкого щелочного гидролиза водным раствором 0,1N. NAOH. Целевой продукт выделяют в виде хлоргидрата или, при необходимости, его подвергают реакции с раствором брома в CHCL 3 с последующим гидролизом водным раствором формиата натрия. Новые вещества эффективны против общей лейкомии. 4 табл.
Изобретение относится к способу получения новых производных 4 -гало- ид-антрациклингликозидов общей формулы
0 он ,сосн2х
Н3СО О ОН
нз Ь-0-7
Ri NH2
где X - водород или гидроксильная
группа;
R( - бром или хлор,
обладающих противоопухолевой активностью.
Цель изобретения - получение новых 4 -галоид-антрациклингликозидов, обладающих большей активностью по сравнению с родоначальниками данного ряда соединений - доксорубицином и да- унорубицином и ближайшим структурным аналогом-соответствующпм 4 -йодпро- изводным.
СЛ
О
Поставленная цель достигается путем взаимодействия 4 -эпи-4 -0-три- фторметансульфонил-Ы-замещенного да- унорубицина в водном метиленхлориде с тетра (н-бутил)аммоний бромидом или тетра (н-бутил)аммоний хлоридом с-получением соответствующих 4 -бром- или 4 -хлорпроизводных, которые подвергают мягкому щелочному гидролизу с це- лью снятия зардитных групп, и полученный 4 -галоиддаунорубицин в случае необходимости переводят в соответствующее 4 -галоидпроизводное доксоруби- цина.( f
Пример 1. 4 -Деокси-4 -бром- даунорубицин (Х-Н, R4-OCH3, ), 2 г бромида тетра (н-бутил)аммония вводят в раствор 4,0 г 4 -эпи-4 -О-трифторметансульфонил-И-трифтор- ацетилдаунорубицина (2:R -OCHj, R -COCFj) в 80 мл водного метилен- хлорида. Через 1.ч при комнатной температуре реакционную смесь промывают водой и органическую фазу выпаривают в вакууме. Остаточный продукт выпаривания очищают на силикагеле, используя смесь метиленхлорид: ацетон в качестве элюента, в результате чего получают 3,5 г 4 -деокси-4 -бром-N- -трифторацетилдаунорубицина с т.пл. 130°С; FD, MS 685 (М). Тонкослойная хроматография на пластинках Kiesel- gel (Merck F 254) с использованием системы растворителя метиленхлорид: ацетон (в объемном отношении 10:1), Rf 0,5.,
В раствор 3 г 4 -деокси-4 -бром- -N-трифторацетилдаунорубицина в 20 мл ацетона вводят 160 мл 0,1 N водного раствора гидрата окиси натрия. Через 4 ч при комнатной температуре величину рН раствора доводят до 8,6 пос- редством 0,1 N кислоты и экстрагируют раствор метиленхлоридом. Растворитель выпаривают и остаточный продукт выпаривания подвергают обработке мета- нольным раствором хлористого водорода, в результате чего получают хлор- гидрат целевого продукта (2,2 г, т.пл. 180°С с одновременным разложением) ; тонкослойная хроматография на пластинках Kieselgel (Merck F 254) с использованием системы растворителей метиленхлорид: метанол: вода: уксусная кислота в объемном отношении 80: :20:7:3, Rf - 0,32.
Пример 2. 4 -Деокси-4 -бром- доксорубицин (Х-ОН, Rf-Br).
JQк
94654
2 г 4 -деокси-4 -бромдаунорубици- на, полученного как описано в примере 1, растворяют в смеси метанола с ди- оксаном. Раствор подвергают обработке обычным образом сначала бромом, в результате чего получается 14-бром
Q 5
5
0
5
0
5
0
результате обработки 4 -эпи-4 производное, а затем - водным раствором формиата натрия, в результате чего получают 4 -деокси-4 -бромдоксору- бицин. Это соединение превращают в его хлоргидрат путем обработки мета- нольным раствором хлористого водорода. Т.пл. этого продукта Составляет 170°С (с разложением), FD, MS 605 (М), тонкослойная хроматография на пластинках Kieselgel (Merck F 254) с использованием системы растворителя метиленхлорид: метанол: вода: уксусная кислота в объемном отношении 80:20:7:3, Rf 0,20.
ПримерЗ. 4 -Деокси-4 -хлор- даунорубицин (Х-Н, ).
В
-0-трифторметансульфонил-М-трифтор- ацетилдаунорубицина (2, R -OCHj, R -COCF) хлоридом тетра (н-бутил)аммония, как описано в примере 1, получают 4 -деокси-4 -хлордаунорубицин, т.пл. 175 С с разложением, FD, MS 545 (М), тонкослойная хроматография на пластинках Kieselgel (Merck F 254) с использованием системы растворителя метиленхлорид: метанол: вода: уксусная кислота в объемном отношении 8:20:7:3, Rf 0,32.
П р и м е р 4. 4J-Деокси-4 -хлор- доксорубицин (X - ОН, Rj- C1).
По методике примера 2 4 -деокси-4 - -хлордаунорубицин превращают в 4 -деокси-4 -хлордоксорубицин и выделяют его в виде хлоргидрата: т.пл. 180°С с разложением; FQ масс-спектр 551 (М+). Тонкослойная хроматография на пластинках Kieselgel (Merr-k F 254) с использованием системы растворителя хлористый метилен: метанол: вода: уксусная кислота в объемном отношении 80:20:7:3 Rf 0,2.
Испытания на биологическую активность .
Соединения примеров 1,2 и 3 подвергались испытанию в условиях in vitro в сопоставлении с даунсрубици- ном (DNR) и доксорубицином (DX) на действие против клеток HeLa, клеток Р388 чувствительных и стойких и пу (Р388(ПХ).
Результаты цитотоксической активности соединений примеров 4,3 и 2 представлены в табл. 1.
Все новые производные показали себя более цитотоксичными, чем их родоначальные соединения против клеток HeLa и Р388, чувствительных к ДХ. Однако эта повышенная цитотоксич- ность является более явно выраженной, если рассматривать активность данных соединений против Р 388 10 . В данном случае эти новые производные показывают 100-250-кратное увеличение цитотоксичности по сравнению с родоначальным препаратом. Данные соединения подвергались испытанию в условиях in vivo против трех различных видов экспериментальной лейкемии.
Противоопухолевое действие на ас- цитическую лейкемию Р388 приведено в табл. 2.
Как видно из табл. 2, активность действия, проявленная соединениями примера 3 равна активности DNR, в то время как другое производное DNR (соединение примера 1) проявляет активность противоопухолевого действия явно более высокую, чем DNR.
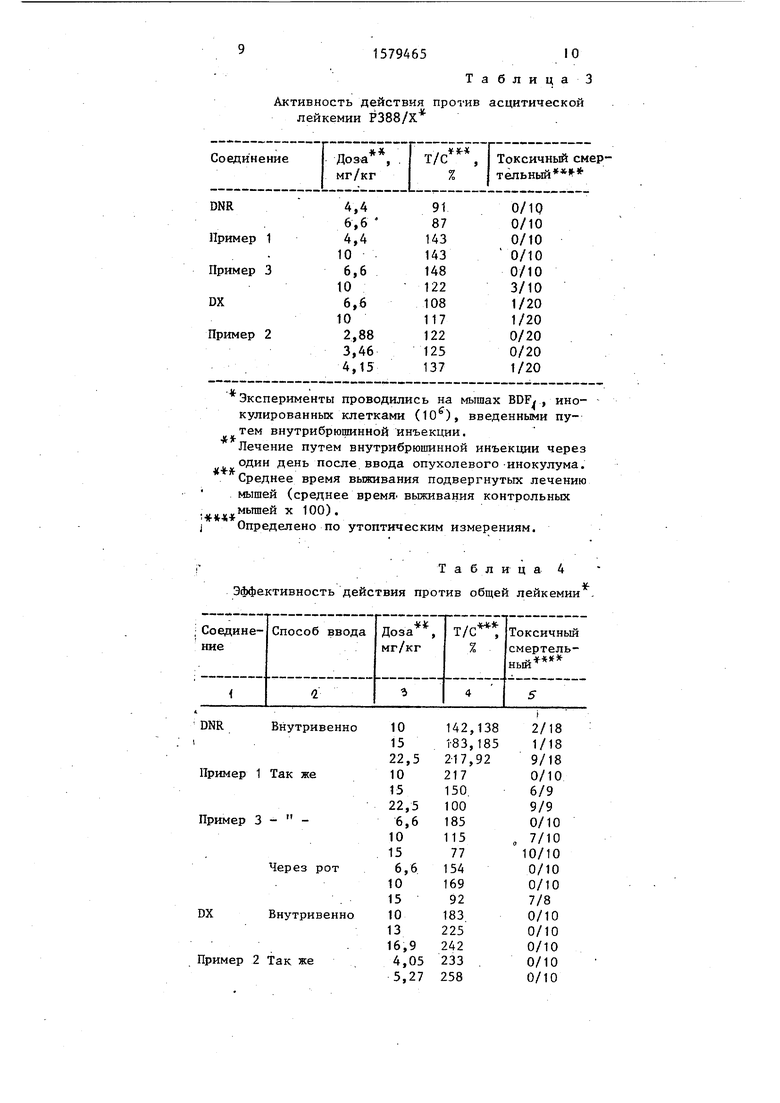
Соединение примера 2 при максимально допустимой дозе (4,15 мг/кг) имеет примерно такую же активность действия, как и DX. Все эти новые соединения проявляют активность действия против лейкемии P388/DX (см. табл. 3), в то время как DNR и DX неэффективны.
Эти три новых соединения подвергали испытанию после их внутривенной инъекции на действие их против рассеянной общей лейкемии (Gross heuke- mia), результаты испытания приведены в табл. 4.
В данной системе соединение 3 является таким же активным, как и DNR, в то время как соединение примера 1 является более активным, чем родона- чальное соединение. Соединение примера 2 показывает примерно такую же эффективность, как и соединение DX. Оба эти соединения подвергались испытанию после ввода в организм через рот и показали значительную активност действия, в то время как DNR и 1)Х не были активны при вводе таким же образом.
, Цитотоксическое действие на клетки HeLa сопоставимо (3 нг/мл) для 4 - бромдоксорубицина и структурного ана
лога - 4 -иодоксорубицина, в то время как действие in -vitro против Р 388 опухолевых клеток, 4 -бромдоксоруби- цин намного более активно (0,2 нг/мл) по сравнению со структурным аналогом (5+2 нг/мл).
Аналогичным образом (по отношению к действию .in vivo против Гросс - лейкемии) был найден показатель Т/С 258% для 4 -бромдоксорубицина при дозе 5,27 мг/кг; 4 -иодоксорубицин имеет показатель Т/С 150-183% при дозе 6,0 мг/кг.
Кроме того, смертельные случаи от отравления составляют 2/17 для 4 -иод- доксорубицина и 0/20 для аналогичного бромпроизводного.
5
20Формула изобретения
Способ получения 4 -галоид-антра- циклингликозидов общей формулы
25
СОСН2Х
ОН
/
Н3СО О ОН X нзс ---О-/
ч Mh
где X - водород NH2 или гидроксильная
группа;
R(- бром или хлор, отличающийся тем, что 41-эпи-4 -О-трифторметансульфонил-N- -замещенный даунорубицин общей формулы
о
so CFjSop где R - трифторацетил, растворенный в водном метиленхлориде, при комнатной температуре подвергают взаимодействию с тетра (.н-бутил)аммоний бромидом или тетра (н-бутил)аммоний хлоридом, получая N-защищенный гликозид общей формулы
О ОН
Н3СО О ОН I Н3С-°
1
-0- NHR2
где R, и R имеют указанные значения,
который подвергают снятию защитных групп путем мягкого щелочного гидролиза водным раствором 0,Ш гидроксида натрия с последующим выделением целевого продукта, где X - водород, в виде хлоргидрата и в случае необходимости полученное соединение подвергают взаимодействию с раствором брома в хлороформе, полученное соответствуТаблица 2
Активность действия против асцитической лейкемии Р388
ер 1
ер 3
ер 2
2,9
4,4
6,6
2,9
4,4
6,6 10
2,9
4,4
6,6 10
4,4
6,6 10
2,4
2,88
3,46
4,15
Эксперименты осуществлялись на мышах CDF , ино кулированных клетками (10 ) лейкемии, путем внутрибрюшинной инъекции.
Лечение путем внутрибрюшинной инъекции через день после ввода опухолевого инокулума.
Среднее время выживания подвергнутых лечению мышей (среднее время выживания контрольных мышей х 100).
Выжившие в течение длительного времени организмы ( 60 дн)
«
Определено по аутоптическим измерениям.
ющее 14-бромпроизводное гидролизуют водным раствором формиата натрия с последующим выделением целевого продукта, где Х-ОН, в .виде хлоргидрата.
Таблица 1
#
Испытание на ингибирование после действия лекарства в течение 24 ч. Цитотоксичность, определяемая после действия лекарства в течение 48 ч. (данные нескольких экспериментов).
155 135 115
0/20
0/18
0/20
0/10
0/10
0/10
3/10
0/10
0/10
0/10
0/8
0/10
0/10
4/10
0/10
0/10
0/10
4/10
0/20 0/18 12/20 0/10 0/10 0/10 0/10 0/10 0/10 0/10 6/8 0/10 0/10 0/10 0/10 0/10 0/10 1/10
157946510
Таблица 3
Активность действия против асцитической лейкемии Р388/Х
Эксперименты проводились на мышах BDF,, ино- кулированных клетками (10), введенными путем внутрибрюшинной инъекции. Лечение путем внутрибрюшинной инъекции через один день после ввода опухолевого инокулума. Среднее время выживания подвергнутых лечению мышей (среднее время выживания контрольных мышей х 100). Определено по утоптическим измерениям.
Таблица 4 Эффективность действия против общей лейкемии
DNR
Внутривенно
Пример 1 Так же Пример 3 - Через рот
DX
Внутривенно
Пример 2 Так же
11
157946512
Продолжение табл.4
Через рот
Эксперименты осуществляли на мышах СЭН, иноку- лированных клетками лейкемии (2x10 ), путем
внутривенной инъекции.
Лечение путем ввода препарата путем внутривеной инъекции или через рот через день после ввода опухолевого инокулума.
Среднее время выживания подвергнутых лечению мышей (ср.еднее время выживания контрольных .мышей х 100).
Определено по аутентическим измерениям.
Редактор М. Келемеш
Составитель Г. Коннова
Техред Л.Олийнык Корректор В. Гирняк
Заказ 1925
Тираж 302
ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР 113035, Москва, Ж-35, Раушская наб., д. 4/5
Производственно-издательский комбинат Патент, г.Ужгород, ул. Гагарина,101
242 114 157
3/10 0/10 0/10
Подписное
| Патент США У 3803124, кл | |||
| Прибор для периодического прерывания электрической цепи в случае ее перегрузки | 1921 |
|
SU260A1 |
| Способ получения антрациклингликозидов | 1983 |
|
SU1378784A3 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Способ получения 4-йодпроизводных антрациклингликозидов | 1982 |
|
SU1181550A3 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1990-07-15—Публикация
1984-08-07—Подача