Изобретение птиосится к способу получения новых замещенных хиназоли- ионов-2 общей формулы
где R - низший алкил,
которые обладают кардиотонической активностью и могут найти прикене ние в медицине.
Цель изобретения - получение новых замещенных хиназолинонов,являющихся промежуточными для получения соединений , обладающих почечной сосудорасширяющей активностью и проявляющих более высотую кардиотоничес- кую активность по сравнению со структурным аналогом.
Пример 1. Получение исходного соединения 2,3-диметокси-6-нитро- бензальдегида.
К взвеси NaH (16,0 г, 50% дисперсия в масле, 33/ ммоль в дйме- тилформамиде (ДМФ) (200 мл) по каплям добавляют раствор 2-окси-З-ме- токси-6-нитробензальдегида (49,0 г, 248 ммоль) в ДМФ (300 мл) с такой скоростью, чтобы температура не превышала 35°С. Смесь выдерживают при комнатной температуре в течение 1 ч, затем к ней по каплям добавляют большой избыток йодистого метила (100 мл) После слабой экзотермической реакции смесь энергично перемешивают в течение 19 ч при комнатной, температуре. После удаления йодистого метила реакционную смесь выливают в ледяную воду (1 л).Сырой продукт - коричневое твердое вещество отфильтровывают промывают водой (холодной) и затем перекристаллизовывают из изопропило- вого спирта (700 мл). Получают продукт в виде желтовато-коричневого твердого вещества, выход 27,9 г (53,3%), т.пл. Юб-Юб С.
О р и м е р 2. Получение целевого продукта 5,6-диметокси-4-метил-2- -(1Н)-хиназолинона.
Стадия 1. 2,З-Диметокси-6-нитро- бензальдегидгзтиленкеталь.
Смесь 2,З-диметокси-6-нитробен- зальдегида (16,0 i-, 75 ммоль), зти- ленгликоля (64 г, 103 ммоль) и п-то- луолсульфокислоты моггогидрата (О, 2 г
в бензоле (750 мл) нагревают при температуре дефлегмации в аппарате Дина-Старка в течение 48 ч. Раствор выливают в ледяную воду (1 л).Органическую фазу промывают насьщ1ен- ным водным раствором NaHCG (2x20 мл), сушат над Na2S04 , отфильтровывают растворитель удаляют в вакууме.
Сырой продукт перекристаллизовывают из н-гексана (2л), выход 15,2 г (78,2%), т.пл. 74-76 0.
Стадия 2. 2,3-Диметокси-6-амино- бензальдегидэтиленкеталь.
Раствор 2,3-диметокси-6-нитробен- зальдегидэтиленкеталя (12,1 г,
62.7ммоль) в этилацетате (350 мл), содержащем ацетат натрия (0,5 г),обрабатывают окисью платины (1,0 г)
и смесь гидрируют в течение
24 ч при давлении примерно 50 фунтов на KB.дюйм.Катализатор отфильтровывают, растворитель удаляют в вакууме. Получают светло-коричневое
масло. После кристаллизации из н- гексана получают продукт в виде желтовато-коричневого твердого вещества,вьгход 12,8 г (85,1%),т.пл.78- 80°С.
Стадия 3. 2,3-Диметокси-6-этокси- карбониламинобензальде гидэтиленке-. таль.
Этилхлорформиат (1,9 г 17,5 ммоль) добавляют при перемешивании к 6-амино-2 5 3-диметоксибензальдегидэтилвн- кеталю (1,6 г, 7,1 ммоль),растворенному в тетрагидрофуране (50 мл), добавляют раствор гидроокиси натрия в воде (0,72 г в 3,5 мл ) и полученньй раствор перемешивают в течение 2 ч при комнатной температуре. Тетрагидрофуран удаляют в вакууме и остаток экстрагируют CHClj (2х X 100 мл).Экстракты сушат над )
отфильтровывают и растворитель удаляют в вакууме.Сырой продукт кристаллизуют из н-гексана,вьгход 1,2 г (57,1%), т.пл. 95-96°С.
Стадия 4. 2,З-Диметокси-6-этоксикарбониламинобензальдегид.
2,З-Диметокси-6-этоксикарбонил- аминобензальдегидэтиленкеталь (5,0 г,
16.8ммоль) растворяют в смеси ацетона (36 мл) и водного раствора НС1
(3 мл, 1н. раствора). Смесь перемешивают при комнатной температуре в течение 4 ч. Растворитель удаляют в вакууме и получают желтое твердое вещество (3,9 г).После перекристал
лизации из н-гексана получают чистый продукт в виде желтого твердого вещества, выход 3,6 г (84,7%),т.пл.86- .
Стадия 5. 5,6-Диметокси-2(1Н)-хи- назолинон.
Поток сухого газообразного аммиака пропускают через раствор 2,3-диобъема примерно 250 мл получают гря но-белого цвета осадок, который отфильтровывают, кристаллизируют из изопропанола (200 мл) и получают продукт в виде бесцветного твердого вещества, выход 9,7 г (87,8%), т.пл. 210-212°С.
Стадия 7. 5,6-Диметокси-4-метилметокси-6-этоксикарбониламинобензаль- ю -2(1Н)-хиназолинон.
дегида (12,4 г, 48,9 ммоль) в ацетате аммония (95 г), температуру которого поддерживают на уровне 155- в течение 3 ч.Реакционную смесь
Перманганат калия (25,6 г,162,38 ммоль) добавляют в раствор 3,4-ди- гидро-5,6-диметокси-4-метил-2(1Н)- -хиназолинона (18,04 г, 81,19 ммоль)
охлаждают и выливают в смесь 15 в ацетоне (5,0 л) и смесь перемешиводы со льдом. Образуется коричневато-желтое твердое вещество.Водную смесь обрабатывают NaCl (50 г) и затем экстрагируют CHClj (3x200 млХ Экстракты объединяют, растворитель удаляют в вакууме и получают 9,2 г бледно-коричневого масла. После растирания этого масла с ацетоном (горячим) получают продукт в виде желтого твердого вещества, выход 2,1 г (20,8%), т.пл. 242-244 с.
Стадия 6. 3,4-Дигидpo-5,6-димeтoк cи-4-мeтил-2 (1Н)-хиназолинон.
В суспензию 5,6-диметокси-2(1Н)- -хиназолинона (10,0 г, 48,5 ммоль) в безводном тетрагидрофуране (1100мл в атмосфере азота при в течение 20 мин добавляют избыточное количество бромметилмагния в диэтиловом эфире (62,60 мл, 3,1 М раствор в диэтиловом эфире, 194,06 ммоль).Затем реакционную смесь извлекают из охлаждающей бани, дают ей нагреться до комнатной температуры и перемешивают при комнатной температуре в течение 16 ч.Добавляют дополнительное.количество бромметилмагния (15,65 мл, 3,1 М раствор в диэтиловом эфире, 48,52 ммоль) и реакционную смесь нагревают при температуре дефлегмации в течение 2 ч. Охлаждают в ледяной бане и при перемешивании добавляют водный раствор Ш4С1(100мл насыщенного NH4C1 в 100 мл HjО).После э,того добавляют 10%-ную водную соляную кислоту до достижения рН Л 6,0. Слои разделяют и водный слой экстрагируют CHClj (3x250 мл).Экстракты объединяют с ранее отделенным тетрагидрофурановьгм слоем, объе-gg трахеальную трубку с манжетой,исполь- диненные органические слои промыва- зуя респиратор Гарварда. В бедренную ют насьш1енным водным {эаствором NaCl артерию и вену поместили полиэтиле- (200 мл) и сушат над Na2S04. После новые катетеры для записи среднего фильтрования и концентрирования до артериального кровяного давления
объема примерно 250 мл получают грязно-белого цвета осадок, который отфильтровывают, кристаллизируют из изопропанола (200 мл) и получают продукт в виде бесцветного твердого вещества, выход 9,7 г (87,8%), т.пл. 210-212°С.
Стадия 7. 5,6-Диметокси-4-метилПерманганат калия (25,6 г,162,38 ммоль) добавляют в раствор 3,4-ди- гидро-5,6-диметокси-4-метил-2(1Н)- -хиназолинона (18,04 г, 81,19 ммоль)
вают при комнатной температуре в атмосфере азота с защитой от света алюминиевой фольгой в течение 96 ч. Образовавшийся коричневый оса0 док отфильтровывают,промывают ацетоном (500 мл) и частично растворяют в кипящей воде (1000 мЛ).Горячий водный раствор (после фильтрования) нейтрализуют в помощью 10%-ного водно5 го раствора со хяной кислоты и затем экстрагируют CHClj (4x250 мл) и смесью 10%-ного изопропилового спирта с этилацетатом (4x250 мл).Полученные экстракты сушат над MgSO, от0 фильтровывают и концентрируют до 500 мл, образуется твердое вещество, которое отфильтровывают.Фильтрат еще раз концентрируют в вакууме и получают 3,25 г желтовато-коричневого твердого вещества, которое хрома5
0
5
0
тографируют на силикаре, приготовленном в CHClj (500 мл фракции).После элюйрования смесью 0,5% метанол/ /хлороформ получают желтое твердое вещество (1,92 г), из которого после перекристаллизации из изопропанола (75 мл) получают целевой продукт в виде желтого твердого вещества, выход 0,940 г (5,3%), т.пл. 230- 232 С.
Кардиотонические исследования.
Подготовка анестезированной собаки с открытой грудной клеткой.
Нечистокровные собаки любого пола (8-20 кг) подвергались анестезии при помощи пентобарбитала натрия (.нембутала), 45 мг/кг вводимого внут- рибрюшинно, и искусственному дыханию комнатным воздухом через эндо(MAP) и ивода лекарства.Датчик давления с катетером на конце типа Мил лар PC 370 вводился в левый желудочек через левую сонную артерию для измерения давления в левом желудочке (LVP). Импульсы давления использовались для запуска кардиотахомет- ра фирмы Бекман для определения частоты ударов сердца (НР) и форму сигналов давления, в левом желудочке дифференцируют,используя устройство связи типа 8758 фирмы Бекман для получения LV dP/dt макс (dP/dt), индекса сокращаемости миокарда. Правая тарокотомия была выполнена в четвертом межреберном пространстве
и была открыта околосердечная сумка. Дуга герметичного тензодатчика с внешней калибровкой фирмы Уолтон Броди была пришита к свободной стенке правого желудочка и она удлинялась примерно на 30% от ее замкнутого положения для измерения изменений в силе сокращения (СГ).Реакция непрерывно наблюдалась на динографе Р612 фирмы Бекман или самописце 2800 фирмы Боулд.
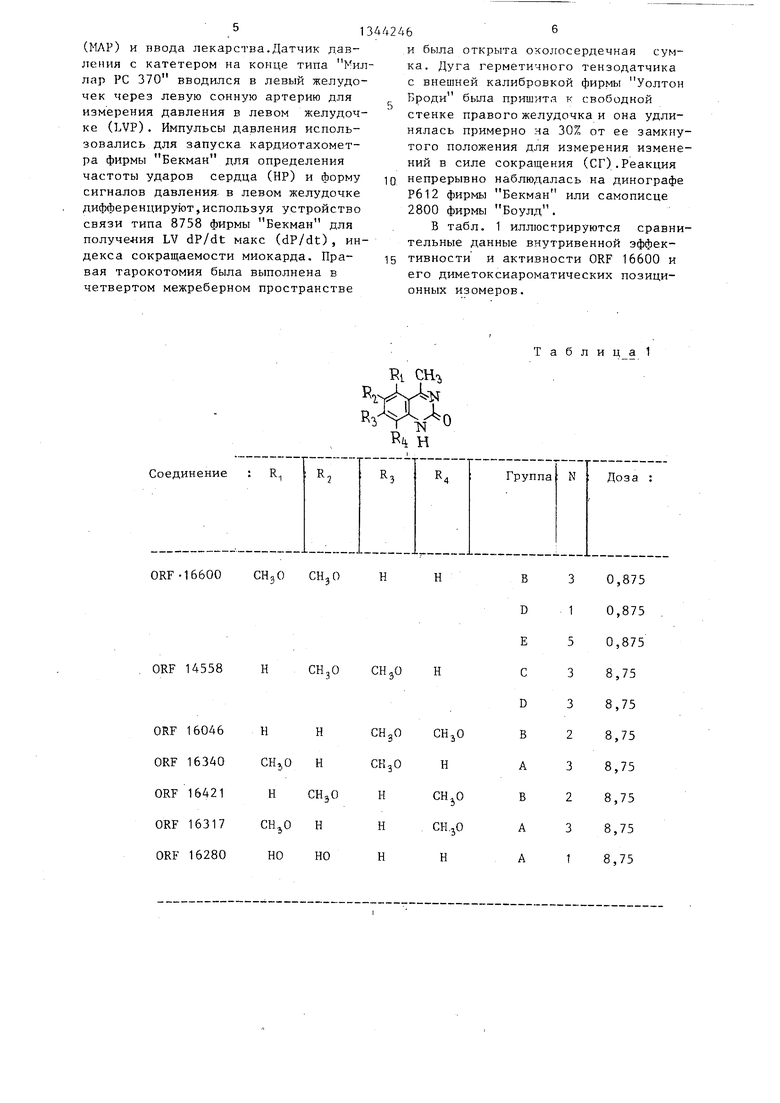
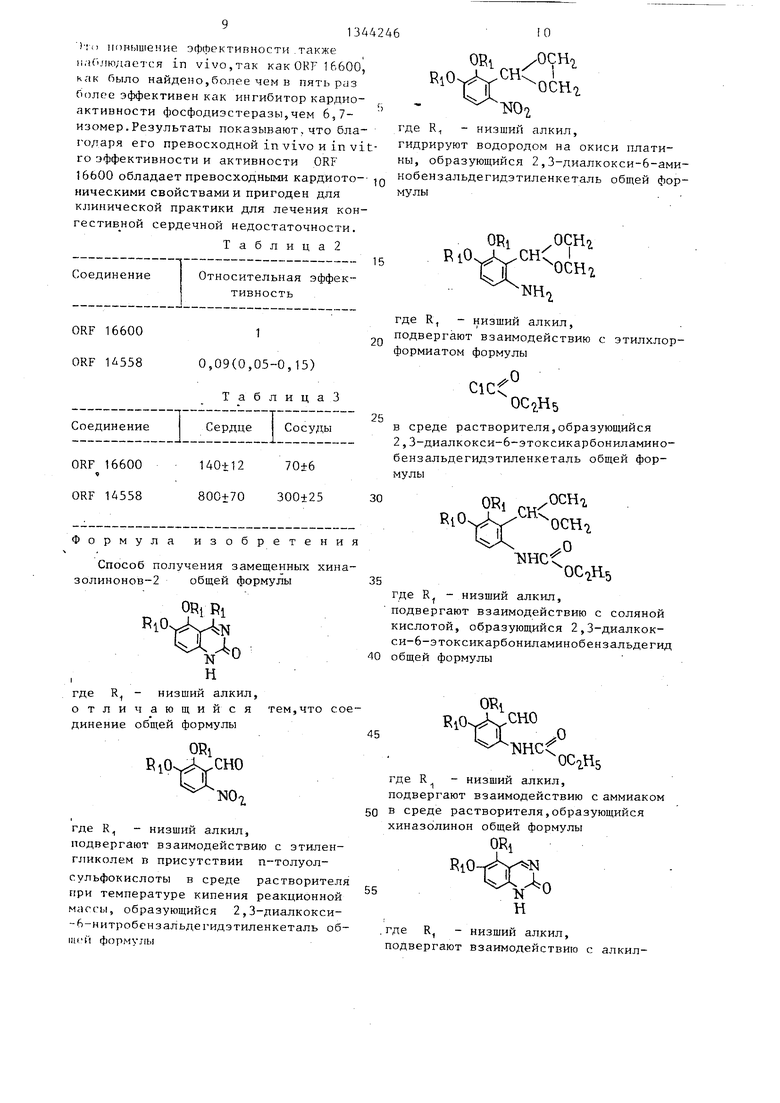
В табл. 1 иллюстрируются сравнительные данные внутривенной эффективности и активности ORF 16600 и его диметоксиароматических позиционных изомеров.
Т а б л и ц а 1


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 4-замещенных 6,7-диокси-2(1Н)-хиназолинон-1-пропионовых кислот | 1983 |
|
SU1407398A3 |
| Способ получения замещенных хиназолиндионов | 1985 |
|
SU1409129A3 |
| СУЛЬФАМАТЫ ПСЕВДОФРУКТОПИРАНОЗЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1994 |
|
RU2139875C1 |
| НОВЫЕ, СОДЕРЖАЩИЕ ГЕТЕРОАТОМ ТЕТРАЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ СЕЛЕКТИВНЫХ МОДУЛЯТОРОВ РЕЦЕПТОРОВ ЭСТРОГЕНА | 2003 |
|
RU2331645C2 |
| ТЕТРАЦИКЛИЧЕСКИЕ ГЕТЕРОСОЕДИНЕНИЯ В КАЧЕСТВЕ МОДУЛЯТОРОВ ЭСТРОГЕННЫХ РЕЦЕПТОРОВ | 2002 |
|
RU2305099C2 |
| Способ получения производных 1,8-нафтиридина или их солей | 1984 |
|
SU1482527A3 |
| ПЕПТИДИЛЬНЫЕ ГЕТЕРОЦИКЛЫ, ИСПОЛЬЗУЕМЫЕ ПРИ ЛЕЧЕНИИ ТРОМБИНАССОЦИИРОВАННЫХ ЗАБОЛЕВАНИЙ | 1996 |
|
RU2181125C2 |
| ПРОИЗВОДНЫЕ НИПЕКОТИНОВОЙ КИСЛОТЫ КАК ВЕЩЕСТВА, ПРЕПЯТСТВУЮЩИЕ ТРОМБООБРАЗОВАНИЮ | 1995 |
|
RU2135470C1 |
| КОНДЕНСИРОВАННОЕ 4-ОКСОПИРИМИДИНОВОЕ ПРОИЗВОДНОЕ | 2005 |
|
RU2358969C2 |
| ПРОИЗВОДНЫЕ АМИНОВ ИЛИ АМИДОВ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ АНТАГОНИЗИРОВАНИЯ РЕЦЕПТОРА Y5 НЕЙРОПЕПТИДА NPY | 2000 |
|
RU2228927C2 |
Изобретение касается, замещенных хиназолинонов-2, в частности соединений общей формулы: ORi ог с тян-с о где R, - низший алкил, которые обладают кардиотонической активностью и могут быть использованы в медицине. Цель - создание активных веществ указанного класса.Их синтез ведут аце- тализацией соответствующего 2,3-ди- aлкoкcи-6-N02-бензальдегида этилен- гликолем в присутствии п-толуолсуль- фокислоты в среде растворителя при кипении. Затем каталь гидрируют на окиси платины (перевод N0 - NHj), последовательно обрабатывают этил- хлорформиатом в среде растворителя, соляной кислотой, аммиаком в среде растворителя,алкилмагнийбромидомв среде растворителя и КМп04 в среде растворителя.Новые соединения показывают кардиотоническую активность в 4-6 раз вьше известного аналога. 3 табл. i О)
ORF-16600 CHjO CHjO
4558
16046 16340 16421 16317 16280
CH,,0 CHgO
H H CH,,0 H
H CHgO
CHjO H
HO
HO
CHgO
СНзО
H H H
CHgO
CHjO
СНзО
H H H
CH,0
CH.jO
Соединение Активность, % от контрольных
+88
+ 100
+ 114
+90
+95
+54
+93
+60
+54
+39
Данные табл. 1 показывают,что эффективность OPF 16600 примерно в 10 раз больше, чем у любого аналога Переход от 5,6- к 6,7- и 7,8-диме- токсиизомерам приводит как к потере эффективности,так и положительной инотропной активности. Диокси-извес ный ORF 16600 (например,16280) обладает маргинальной активностью.Даные четко показывают отличие ORF 16600 от его позиционных изомеров.
Величина LCjg показывает относительную способность соединения подавлять фермент. Чем ниже величина, тем более эффективно соединение.
В табл. 2 сопоставлены относительные эффективности ORF 16600 и ORF 14558, используя данные по силе сокращения,определенные экспериментально доза-реакция.Если ORF 16600 обладает относительной эффективностью 1, ORF 14558 - менее чем 1/10 эффективности ORF 16600.
Подавление циклофосфодиэстераз сердечно-сосудистых циклических AMP LC50им показано в табл. З.
1344246
8 Продолжение табл.1
+ 11 + 19 +20- + 19 +31 + 16 +25 + 13 + 13 О
-14
-11
-16
-35
-23
-4
-40
-6
-6
+8
Данные в табл. 3 иллюстрируют,
что ORF 16600 также более эффективен (в 4-6 раз) как ингибитор сердечнососудистой активности фосфодиэсте- разы по сравнению с ORF 14558. Поскольку подавление этой активности
фермента может представлять собой биохимический .механизм для повьппения силы сокращения сердца и понижения after load (артериального кровяного давления), эти данные в сочетании
с экспериментами in vivo демонстрируют, что ORF 16600 обладает неожиданно высокой кардиотонической ак тивностью по сравнению с его изомерами.
5,6-Диметокси-4-метил-2(1Н)-хина- золинон (ORF 16600) показал неожиданно высокую активность и эффективность in vivo по сравнению со всеми другими диметоксиароматическими
позиционными изомерами и обладает примерно в 10 раз более высокой эффективностью чем любой из его изомеров как положительный инотропный агент (увеличивает силу сокращений).
13А4246
() повышение эффективности .также н.чОяю/шется in vivo,так как ORF 16600, как было найдено,более чем в пять раз Солее эффективен как ингибитор кардио- активности фосфодиэстеразы,чем 6,7- изомер.Результаты показывают,что бла- 1-одаря его превосходной in vivo и in vitro эффективности и активности ORF
ORi
о ОСН
ошг
-N02
где RI - низший алкил, гидрируют водородом на окиси платины, образующийся 2,3-диалкокси-6-ами16600 обладает превосходными кардиото-- ,Q нобензальдегидэтиленкеталь общей форническими свойствами и пригоден для клинической практики для лечения кон- гестив ной сердечной недостаточности.
Таблица2
Соединение
Относительная эффективность
1
0,09(0,05-0,15)
ТаблицаЗ Сердде i Сосуды
Сердде
мулы
ORi
г/
ОСНг
« «Чснг
С
NH
этилхлоргде К, - низший алкил, подвергают взаимодействию с формиатом Формулы
cicC
в среде растворителя,образующийся 2,З-диалкокси-6-этоксикарбониламино- бензальдегидзтиленкеталь общей формулы
Формула изобретения
Способ получения замещенных хина- золинонов-2 общей формулы
30
RtO
ORi ,
NHC€
о
.5
где R - низший алкил, подвергают взаимодействию с соляной кислотой, образующийся 2,3-диалкок- си-6-этоксикарбониламинобензальдегид общей формулы
где R - низший алкил, отличающийся тем,что соединение общей формулы
ORi
N0-2.
где R - низший алкил, подвергают взаимодействию с этилен- гликолем в присутствии п-толуол- сульфокислоты в среде растворителя при температуре кипения реакционной массы, образующийся 2,3-диалкокси- -6-нитробонзальдегидэтиленкеталь об- пк. й формулы
ORi
11НС
:0
где R - низший алкил, подвергают взаимодействию с аммиаком 50 в среде растворителя,образующийся хиназолинон общей формулы
.где R, - низший алкил, подвергают взаимодействию с алкил111344246 2
магнийбромидом в среде растворителя, где R - низший алкил, образующийся хиназолинон общей форму- подвергают взаимодействию с пермангалынатом калия в среде растворителя.
ORi RI
RiOv sOiNH
н
Составитель Г.Жукова Редактор Н.Гунько Техред И.Попович Корректор Л.Патай
4839/58Тираж 371 Подписное
ВНИИПИ Государственного комитета СССР по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб,, д. 4/5
Производственно-полиграфическое предприятие, г. Ужгород, ул. Проектная, 4

| Общая органическая химия | |||
| - М.: Химия, 1985, т | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Устройство для отыскания металлических предметов | 1920 |
|
SU165A1 |
Авторы
Даты
1987-10-07—Публикация
1985-02-15—Подача