Изобретение относится к пищевой промышленности, в частности к способам определения пептидов в напитках, и может применяться в консервной, пи- вобезалкогольной, -винодельческой промышленности,
Целью изобретения является повышение точности анализа, сокращение его длительности и снижение расходов реактивов и материалов.
Способ осуществляют следующим.образом,
10-20 мл напитка наливают в химический стакан емкостью 50 мл, добавляют щелочь до получения рН среды 7,0 (0,5-1,2 мл 1 н, щелочи) и пропускают через стеклянную колонку (размером 1,0x20 см), заполненную
5
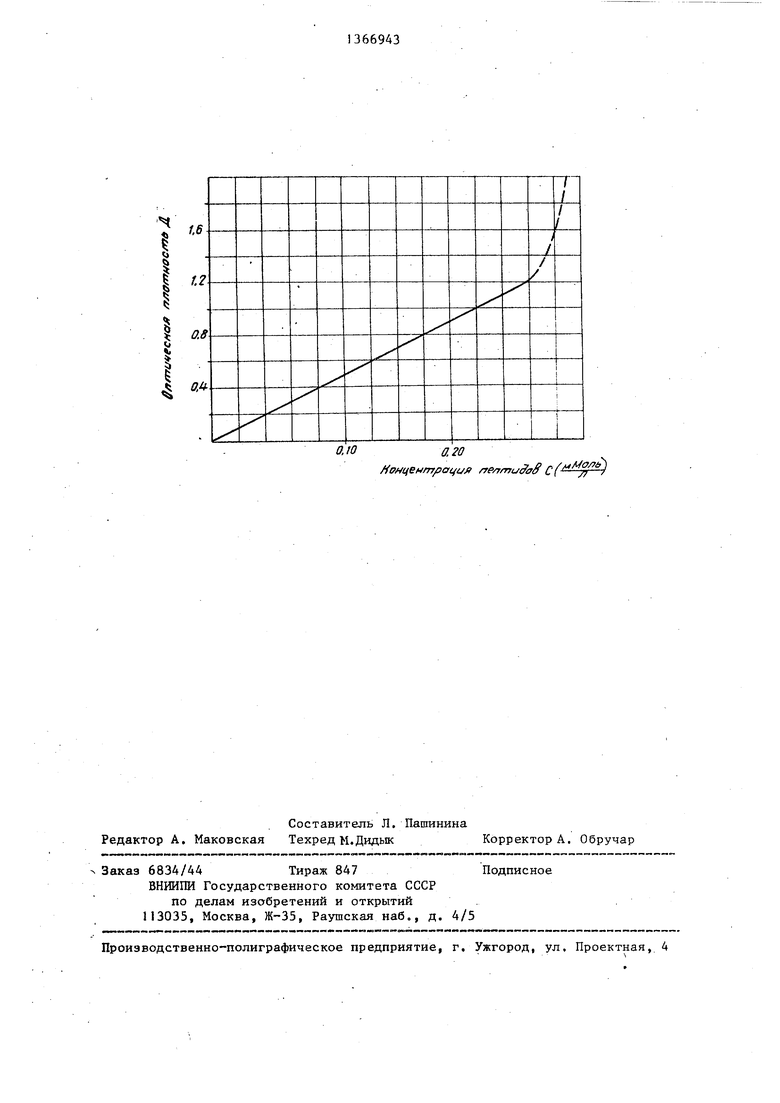
образуется продукт, имеющий максимум поглощения при Л 335 нм. Смесь выдерживают 30 мин при комнатной температуре (8-20 С), Затем в колбу приливают 1 н, раствор соляной кислоты до получения рН среды 3,0- 3,2. В колбу добавляют дистиллированную воду до метки 25 мл и тщательно перемешивают. Полученный раствор наливают в кювету слоем толщиной 1 см, после чего измеряют оптическую плотность при 335 нм. Если оптическая плотность D 1,2 и зависимость D f (С) выходит за пределы линейного участка калибровочной кривой (см. чертеж), то исследуемая проба чрезмерно концентрирована, анализ после ее соответствующего разбавле

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПЕПТИДОВ ИЛИ ИХ ПРОИЗВОДНЫХ | 1970 |
|
SU268305A1 |
| Способ получения антибиотика казугамицина | 1964 |
|
SU454749A3 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕПАРИНА | 1992 |
|
RU2042356C1 |
| СПОСОБ СИНТЕЗА АЛЬФА-КЕТОМЕТИЛСЕЛЕНОБУТИРАТА | 2021 |
|
RU2776282C1 |
| СПОСОБ ДООЧИСТКИ ХИМОПАПАИНА | 1990 |
|
RU2074891C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО БЕЛКА SAV-RGD, СПЕЦИФИЧЕСКИ УЗНАЮЩЕГО КЛЕТКИ МЕЛАНОМЫ | 2013 |
|
RU2563540C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНСУЛИНА ИЗ ПРИРОДНОГО ИСТОЧНИКА И ИНСУЛИН | 2003 |
|
RU2251426C1 |
| Способ получения антибиотиков | 1975 |
|
SU528038A3 |
| Способ получения антибиотика @ -19393 @ и/или @ -19393 @ | 1980 |
|
SU1075984A3 |
| Штамм Pichia pastoris Y-4349 - продуцент альфа-фетопротеина человека, способ получения альфа-фетопротеина и композиции его содержащей | 2024 |
|
RU2838856C1 |
Изобретение относится к пищевой промышленности. Способ сокращает длительность анализа и расход химических реактивов и материалов, а также повышает точность анализа. Согласно способу 15 мл исследуемого напитка, доведенного до нейтральной среды (рН 7), пропускают через стеклянную колонку размером (1,0 х X 20 см), заполненную ионообменной смолой КРС-2П в водородной форме, со скоростью 1,5 мл/мин. После промывания смолы дистиллированной водой в количестве 15 мл проводят элюирова- ние пептидов 30 мл 10%-ного раствора аммиака со скоростью 2,0 мл/мин. 4,0 мЛ полученного злюата, имеющего рН среды 12,5, наливают в мерную колбу емкостью 25 мл, добавляют 0,5 мл 0,1 н. раствора метилглиоксаля, смесь выдерживают 30 мин при комнатной температуре (18-20 С), приливают 1 н. раствор соляной кислоты с таким расчетом, чтобы рН среды стала равной 3,0-3,2, В колбу добавляют дистиллированную воду до метки и тщательно перемешивают, после чего проводят спектрофотометрирование продуктов реакции при 335 нм, Содержание пептидов определяют по калибровочной кривой. 1 ил,, 2 табл. сл оо О) Од СО 4 оо
считывают по формуле m -К-С М, где m
(О
ионообменной смолой КРС-2П в водород-2о ния повторяют. По калибровочной кри- ной форме, со скоростью 1,5 мл/мин. вой (фиг. 1) при оптической плотности Ионообменная смола КРС-2П - продукт D находят концентрацию пептидов С сополимеризации стирола и дивинилбен- (мМоль/л). Полученные данные С перезола (ДВБ) - характеризуется низким процентом сщитости (2% ДВБ), Пептиды 25 задерживаются на смоле вследствие ионообмена и сил адсорбции. Больщин- ство веществ, искажающих результат анализа (белки, фенольные соединения, соли, сахара, органические кислоты), зо свободно проходят через колонку, и лишь незначительная часть примесей задерживается на смоле. Для гарантированного смыва этой части примесей смолу промывают дистиллированной во35
концентрация пептидов в
мг/л;
коэффициент разбавления;
концентрация пептидов,
мМоль/л|
молекулярная масса трипептида глицил-глицил-глицин,
равная 189 г/моль. Для сравнения результатов анализа с аналогами концентрацию пептидов выражают в мг азота пептида на литр (мг N пеп/л) по зависимости:
К Р -
М, дой в объеме, равном обьему исходной пробы (10-20 мл). После промывания смолы проводят элюирование пептидов 10%-ным раствором аммиака со ского стью 2,0 мл/мин, 10%-ный раствор аммиака, имеющий рН среды 12,5 (элюент), берется в двухкратном избытке по отношению к объему исходной пробы для обеспечения полной элюации пептидов из смолы. Так как количество пептидов и аминокислот в полученном элюате весьма незначительно по сравнению с объемом элюента, то рН среды последнего практически не изменяется и остается равнымМ2,5 Для проверки полноты элюирования пептидов и аминокислот со с -юлой 1,0- 2,0 мл элюата наливают в мерную колбу емкостью 25 мл и добавляют 0,5 мл 0,1 н, раствора метилглиоксаля . Такого количества раствора метилглиоксаля с избытком достаточно для полного взаимодействия с содержащимися в элюате пептидами, в результате чет
считывают по формуле m -К-С М, где m
(О
ния повторяют. По калибровочной кри- вой (фиг. 1) при оптической плотност D находят концентрацию пептидов С (мМоль/л). Полученные данные С пере5о
5
концентрация пептидов в
мг/л;
коэффициент разбавления;
концентрация пептидов,
мМоль/л|
молекулярная масса трипептида глицил-глицил-глицин,
равная 189 г/моль. Для сравнения результатов анализа с аналогами концентрацию пептидов выражают в мг азота пептида на литр (мг N пеп/л) по зависимости:
К Р -
М,
m ,
m -
(2)
5
0
5
где т., - концентрация пептидов,
мг N пеп/л; М 1 - молекулярная масса азота,
равная 14;
п - число атомов азота входящих в состав пептида (для глицил-глицил-глицИна ). Общая продолжительность анализа составляет 65 мин.
Пример 1. 15мл яблочного сока наливают в. химический стакан емкостью 50 мл, добавляют едкий натрий до получения рН среды 7,0 (1,2 мл I н. NaOH) и пропускают через стеклянную колонку (размером 1,0 X 20 см), заполненную ионообменной смолой КРС-2П в водородной форме, со скоростью 1,5 мл/мин. Далее промьшают смолу дистиллированной водой в количестве 15 мл. После этого проводят элюирование пептидов 30 мл 10%-ного раствора аммиака (2-кратное разбавление) со скоростью .2,0 мл/мин Полученный элюат имеет рН среды 12,5 В мерную колбу емкостью 25 мл наливают 2,0 мл элюата, добавляют 0,5 мл 0,1 н, раствора метилглиоксаля, смес выдерживают 30 мин при комнатной температуре (18-20 с). Затем в колбу приливают 1 н. раствор соляной кислоты до получения рН среды 3,0-3,2. В колбу добавляют дистиллированную воду до метки 25 мл (12,5-кратное разбавление) и тщательно перемешивают. Полученный раствор наливают в кювету слоем толщиной 1 см, после чего на спектрофотометре СФ-4А измеряют оптическую плотность при Л 335 нм. По калибровочной кривой при оптической плотности D 0,850 концентрация пептидов С равна
0,172 йМоль.
JT
так как коэффициент разбавления К 25, то m 812 мг/л (по формуле 1), а азот пепетидов т 178 мг/л (по формуле 2). Общая продолжительность анализа 75 мин.
Параллельно проводят анализ исследуемого напитка по способу-прототипу, концентрация пептидов составляет 736 мг/л, а азот пептидов 164 мг/л. Продолжительность анализа по прототипу - 102 мин. .
Пример 2. 20 мл вина наливают в химический стакан емкостью 50 мл добавляют едкий натрий до получения рН среды 7,0(1,2 мл 1 н, NaOH) и пропускают через стеклянную колонку (размером 1,0 х 2 О см), заполненную ионообменной смолой КРС-2П в водородной форме, со скоростью 1,5 мл/мин. Далее промывают смолу дистиллированной водой в количестве 20 мл. После этого проводят элюирование пептидов 40 мл 10%-ного раствора ам -шака со скоростью 2,0 мл/мин/. 2,0 мл элюата,г имеющего рН среды 12,5, используют для проведения ре- .акции с метилглиоксалем, после чего подвергают спектрофотометрическому анализу , как описано в примере 1. По калибровочной кривой при оптической плотности D 0,360 находят концентрацию пептидов - 349 г/л, азот пептидов - 77 мг/л. Общая продолжительность анализа 80 мин. Аяализ исо
5
0
5
0
5
0
5
0
5
следуемого напитка по прототипу дал следующие результаты: 305 и 68 мг/л соответственно. Продолжительность анализа по прототипу 95 мин.
Пример 3. 10 мл пива наливают в химический стакан емкостью 20 мл, добавляют едкий натрий до получения рН среды 7,0 (0,5 мл 1 н. NaOH) и пропускают,через колонку (размером 1,0 х 20 см), заполненную ионообменной смолой КРС-2П в водородной форме, со скоростью 1,5 мл/мин. Далее промывают смолу Дистиллированной водой в количестве 10 шт. После этого проводят элюирование пепти- дов 20 мл 10%-ного аммиака со скоростью 2,0 мл/мин 1,0 мл элюата, имеющего рП среды 12,5, используют для проведения реакции с метилглиоксалем, после чего подвергают спектрофотомет- рическому анализу, как описано в примере 1. При оптической плотности D 0,870 концентрация пептидов равна 1658 мг/л, азот пептидов - 365 мг/л. Общая продолжительность определения 65 мин. При проведении анализа напитка по прототипу концентрация пептидов составила 1531 мг/л, а азот пептидов - 340 мг/л. Общая продолжительность анализа по прототипу - 88 мин.
Пример 4. Сравнительный анализ точности двух методов определения пептидов проводят на яблочном соке и столовом вине. Предвари-- тельно в каждом из исследуемых напитков определяют концентрацию пептидов. Из химически чистого препарата гли- цил-глицил-глицина готовят рабочий раствор с концентрацией 2000 мг/л. Рабочий раствор пептида добавляют в каждый из напитков из расчета 100 мг/л. В последующем проводят определение суммарного содержания пептидов так, как описано в прототипе и приведенных выше примерах. Критерием оценки точности методов служит процент определения добавленного пептида.
Результаты определения и матема- тической обработки приведены в табл. 1, из которой следует, что более высокая точность достигается по предлагаемому способу (% определения пептидов по предлагаемому способу составил 99,2 и 98,8, а в прототипе - 97,4 и 91,7 соответственно).
Технико-экономическая эффективность предлагаемого способа достигается сокращением продолжительности анализа и расхода химических реактивов и материалов (табл. 2).
Формула изобретения
Способ определения пептидов в напитках, предусматривающий отбор пробы, введение в нее щелочи, доведение рН раствора до 12,5, внесение метилглиоксаля, выдержку, спектрофо- тометрирование продуктов реакции и установление концентрации пептидов,
ный
736
100
вое 305
100
812 821 818 806
367 370 375 374
97,4
91,7
отличающийся тем, что, с целью повышения точности анализа, сокращения его длительности и снижения реактивов и материалов, щелочь вводят в пробу до обеспечения рН 7,0, после чего вьщёляют пептиды из пробы путем пропускания ее через ионообменную смолу КРС-2П водородной форме, промывают смолу дистиллированной водой и элюируют пептиды, при этом доведение рН раствора до 12,5 осуществляют в процессе элюирования пептидов 10%-ным раствором аммиака.
Таблица I
100
100
909 901 904 905
444 444 441 446
99,2
98,8
Продолжительность анализа, мин
Стоимость расходуемых реактивов и материалов, коп
В том числе:
Ацетат свинцд
Гидроксид натрия
Соляная кислота
Метилглиоксаль Смола КРС-2П
АммиакСтоловое вино
Яблочный сок
Пиво
73
3,312
0,010 0,010 0,040 0,600 0,012 1,440 0,600 0,600
О.Ю 0.20
Нонцентра1 с/А np/rmu crff 
| Petershater G | |||
| Prey V | |||
| Eine photometrische Methode zur analyti- schen | |||
| Bestiinmung von Peptiden neben Aminosan reu | |||
| - Aucrochimica Acta, 1969, № 5, s | |||
| Устройство для избирательного управления с одного конца однопроводной линии несколькими реле | 1918 |
|
SU981A1 |
| Способ определения пептидов в напитках | 1977 |
|
SU630582A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1988-01-15—Публикация
1986-07-28—Подача