Известен: епбсоб получения НептаДОВ М их производных взаиМоДейстбнем аминокислоты или пептида или их производных в присутствии эквивалентного количества щелочи в водной среде со смешанным ангидридом N-защищенных аминокислоты или пептида и этоксихлоругольной кислоты при температуре ниже 10°С, при рН выше 6 и при перемешивании. Для получения более длинного пептида полученный выше пептид выделяют и подвергают взаимодействию с требуемой аминокислотой в виде ее смешанного ангидрида.
Предложенный способ отличается от известного тем, что в качестве карбоксильной компоненты используют N-карбоксиангидриды или N-тиокарбоксиангидриды аминокислот или их производных, процесс ведут при защитном рН4-И с последующим декарбоксилированием или детиокарбоксилированием путем подкисления до рН ниже 3-5.
Способ позволяет упростить синтез пептидов, так как для получения более длинного пептида ранее полученный пептид не выделяют, а непосредственно в реакционную смесь вносят ангидрид требуемой N-карбокси- или N-тиокарбоксиаминокислоты. Выход дипептидов достигает 95-98%.
Смесь 420 Mi (2 ммоль) хлоргидрата аргинина в 20 мл 1 М водного раствора боратного буфера (борнокислого калия), содержащего 5 г льда, рН 11, охлаждают до температуры
около , затем добавляют 386 мг
(2,01 ммоль) твердого ангидрида N-карбоксифенилаланина при энергичном перемешиваНИИ. Смесь перемешивают в течение 1 мин,
после чего рН доводят до 3 концентрированной серной кислотой при 0°С, при пропускании азота через смесь в течение 10 мин. Полученный фенилаланиларгинин не выделяют.
Добавлением концентрированного раствора едкого кали при охлаждении до 0° рН смеси
доводят до 9,5. Затем вносят 5 г льда и 285 мг (2,02 ммоль) ангидрида N-карбоксипролина и перемешивают в течение 3 мин. Декарбоксилирование проводят так, как описано выше, полученный продукт не выделяют.
Предыдущую операцию повторяют при рН 10 с добавлением 235 мг (2,04 ммоль) ангидрида N-карбоксиаланина и перемешивают в течение 1 мин. Аланил-пролил-фенилаланиларгинин, полученный прИ декарбоксилироваНИИ по вышеописанному способу, не выделяют. Эту же операцию повторяют .при рН 10 при перемещивании в течение 1 мин, исполь зуя 235 мг (2 ммоль) ангидрида N-карбоксиаланина для образования аланил-аланил-пролил-фенилаланил-аргинина, который не выделяют.
Повторяя операцию при рН 10 с 294 мг (2,02 ммоль) ангидрида N-карбоксивалина, получают валил-аланил-аланил-пролил-фенилаланил-аргинин.
рН полученного раствора (46 мл) доводят до 7,5 водным раствором едкого натра и загружают в 30-лгл колонку со смолой 1RC 50 в кислой форме (колонка с внутренним диаметром 1,5 см) со скоростью пропускания 2 мл/мин и элюнруют 75 мл 0,25 н. серной кислоты, затем 75 мл 1,0 н. серной кислоты. Элюат, включающий аргининсодержащий пептид, собирают в погоны по 25 мл со скоростью 1 мл/мин.
Образцы всех фракций наносят на круговую бумажную хроматограмму в системе втор-бутанол - вода - уксусная кислота (в соотношении 6:3:1). При удалении фронта растворителя на 6 см фракции элюата 3, 4, 5 и 6 показывают сильную нингидринную реакцию (полосу) с Rf 0,39, что указывает на искомый гексапептид (значение Rf продукта и реагентов предварительно определяют тонкослойной хроматографией). Эти фракции объединяют, упаривают под вакуумом, водным раствором едкого натра доводят рН до 7,5 и сушат вымораживанием. Полученное твердое веш,ество экстрагируют четыре раза порциями метанола по 10 мл, после чего метанол отгоняют под вакуумом. Остаток растворяют ъ Q мл воды, водным раствором серной кислоты рН доводят до 3,0 и высаживают веш,ество добавлением 25 мл метанола и затем 55 мл этанола. Суспензию оставляют на ночь на холоду, после чего отфильтровывают. Получают заданный продукт, что устанавливают анализом аминокислот после гидролиза.
Глицил - аланил-лейцил - изолейцил - валилфенил-аланин получают вышеописанным методом. Оптимальные условия: концентрацию реагентов, рН, температуру и продолжительность реакции проверяют предварительно пробами с небольшими количествами реагентов, прежде чем проводить ее в крупном масштабе. Реакции ведут при рН от 4 до 11, как правило с избытком ангидрида, при температуре от -5 до 5°С, в аппарате с мешалкой (смесителе). Температуру поддерживают с помощью внутреннего или наружного о.члаждения либо того и другого.
Ангидриды следующих кислот используют в виде трифторацетилпроизводных: серин, треонин, р-оксилейцин, Y-оксинорвалин.
Ниже приведены кислоты, ангидриды которых применяют в виде S-бензильных производных: цистеин, р-тиолнорвалинпеницилламин.
N-карбоксиангидрид тирозина используют в форме тетрагидрофуранового производного.
ией. Прочие защитные группы также удалят в конце реакции.
Ниже приведен список принятых сокращеий:
Глицин - ГЛИ
Аланин - АЛД
Лейцин -ЛЕЙ
Изолейцин - ИЗОЛ
Валин ВАЛ
Фенилаланин - ФЕН
Тирозин - ТНР
Триптофан - ТРИ
Аргинин - АГН
Лизин - ЛИЗ
Гистидин - ГИС
Серин -СЕР
Треонин - ТР
Пролин - ПРО
Цистеин - ЦИС
Цистин - ЦИСТ
Метионин - МЕТ
Аспарагиновая кислота -АСР
Глутаминовая кислота - ГЛУ
Аспарагин - АСН
Глутамин - ГЛН
а-Аминоадипиновая - а, АД
а-Аминопимелиновая - а, ПИ
а-Аминосубериновая - а, СУ
а-Аминосебационовая - а, СЕ
р-Метиласпарагиновая - рМ, АСП
р-Метилглутаминовая - рМ, ГЛУ
Р,р-Диметиласпарагиновая - рМ, рМ, АСП
Орнитин -ОРН
а-Аминоизомасляная - а, ИВУ
а-Аминодиэтилуксусная - а, АДА
а-Аминодиизопропилуксусная - р, АДИА
а-Аминоэтилизопропилуксусная - а, АЕИА
Пеницилламнн - ПЕНМ
р-Оксинорвалин - рОН, НВАЛ
р-Тиолновалин - р, ТВАЛ
а-Аминофенилуксусная кислота - а, АРА
о-Хлорфенилаланин - о - ХЛ - ФЕ
Фурфурилаланин - ФАЛА
Тиенилаланин - ТАЛА
а-Нафтилаланин - а, НАЛА
3-Тионафтенилаланин - ТНАЛА
3-Кумаронилаланин - КОУ, АЛА
М-Л1етилглицин - NM, ГЛИ
N-метилаланин - NM, АЛА
N-Метиллейцин - NM, ЛЕИ
N-Метилтирозин - NM, ТИР
В соответствии с вышеописанной методикой олучают следуюише гексапептиды:
ГЛИ-АЛА-ИЗОЛ-ВАЛ-ФЕ-ТИР
ТРИ-АГН-ЛИЗ-ГИС-СЕР-ТР
ПРО-ЦИСТ-МЕТ-АСП-ГЛУ-АСН
ГЛН-а, а-.АД-а, ПЛ-а, СУ-а, СЕ-рМ, АСП
рМ, ГЛУ-р.М, АСП-ОРН-а, ИВУ-АДА-а, ДИА
а-АЕИА-рОН, НВАЛ-ПЕНМ-рТ, ВАЛ-а, РА-о-ХЛ-ФЕ
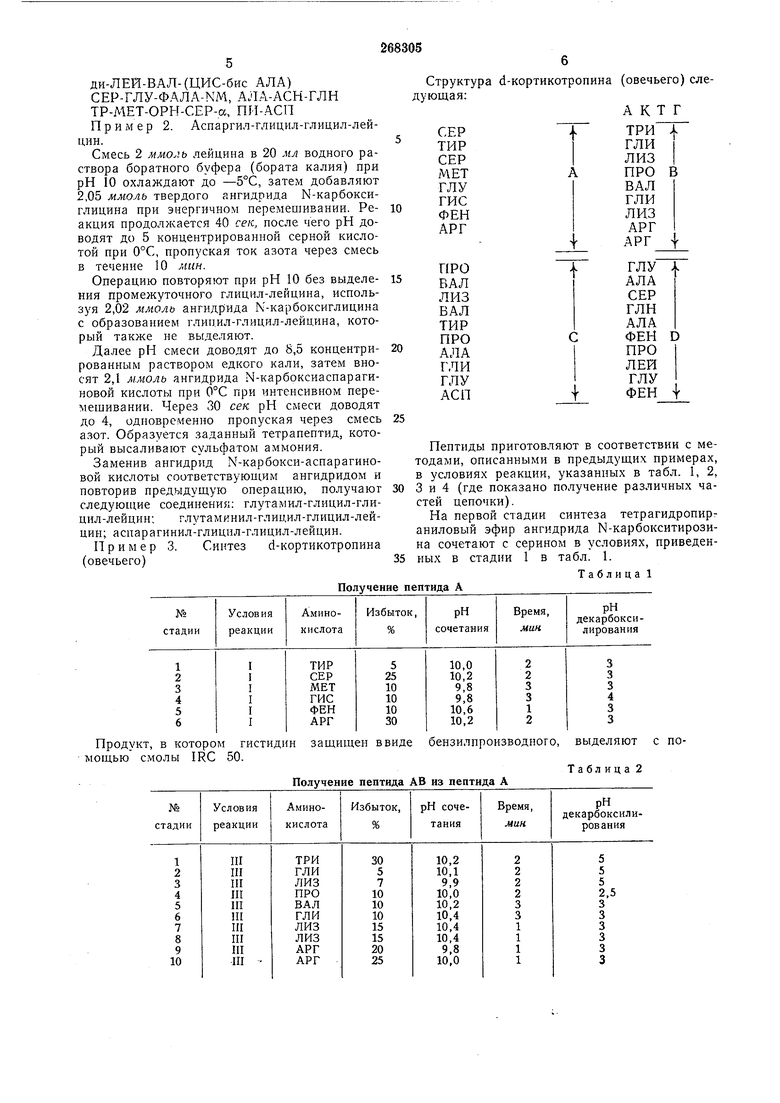
ФАЛА-ТАЛА-а, НАЛА-ТНАЛА-КОУ, АЛАM, ГЛИ ди-ЛЕЙ-ВАЛ-(ЦИС-бис АЛА) СЕР-ГЛУ-ФАЛА-NM, АЛА-АСН-ГЛН ТР-МЕТ-ОРН-СЕР-а, ПИ-АСП Пример 2. Аспаргил-глицил-глицил-лейцин. Смесь 2 ммоль лейцина в 20 мл водного раствора боратного буфера (бората калия) при рН 10 охлаждают до -5°С, затем добавляют 2,05 ммоль твердого ангидрида N-карбоксиглицина при энергичном иеремешивании. Реакция продолжается 40 сек, после чего рН доводят до 5 концентрированной серной кислотой при 0°С, пропуская ток азота через смесь в течение 10 лшн. Операцию повторяют при рН 10 без выделения промежуточного глицил-лейцина, используя 2,02 ммоль ангидрида N-карбоксиглицина с образованием глицил-глицил-лейцина, который также не выделяют. Далее рН смеси доводят до 8,5 концентрированным раствором едкого кали, затем вносят 2,1 м-моль ангидрида N-карбоксиаспарагиновой кислоты при 0°С при интенсивном перемешивании. Через 30 сек рН смеси доводят до 4, одновременно пропуская через смесь азот. Образуется заданный тетрапептид, который высаливают сульфатом аммония. Заменив ангидрид N-карбокси-аспарагиновой кислоты соответствующим ангидридом и повторив предыдущую операцию, получают следующие соединения: глутамил-глицил-глицил-лейцин; глутаминил-глицил-глицил-лейцин; аспарагинил-глицил-глицил-лейцин. Пример 3. Синтез d-кортикотропина (овечьего) Получен ептиды приготовляют в соответствии с меами, описанными в предыдущих примерах, условиях реакции, указанных в табл. 1, 2, 4 (где показано получение различных чай цепочки). а первой стадии синтеза тетрагидропириловый эфир ангидрида N-карбокситирозисочетают с серином в условиях, приведенх в стадии 1 в табл. 1. Таблица 1 да А




| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ N-КАРБОКСИАНГИДРИДОВ ОКСИАМИНОКИСЛОТ | 1969 |
|
SU257380A1 |
| СПОСОБ ПОЛУЧЕНИЯ 6-МЕТИЛЕНТЕТРАЦИКЛИНА | 1972 |
|
SU341225A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕНИЦИЛЛИНОВ | 1973 |
|
SU367605A1 |
| Способ получения пептидов с последовательностью актг-человека,содержащих в -конечном положении аминооксикислоту | 1973 |
|
SU490284A3 |
| СПОСОБ ПОЛУЧЕНИЯ З-ОКСИ-З-МЕТИЛ-7- АМИНОЦЕФАЛОСПОРИНОВ | 1973 |
|
SU361571A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ КУМЕРМИЦИНОВ | 1972 |
|
SU342339A1 |
| СПОСОБ РАЗДЕЛЕНИЯ РАЦЕМИЧЕСКОЙ СМЕСИ (ЦИС-1,2- | 1971 |
|
SU289597A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ЦЕФАЛОСПОРАНОВЫХ КИСЛОТ | 1972 |
|
SU343438A1 |
| Способ получения -сульфоната в-цепи инсулина человека | 1977 |
|
SU696011A1 |
| Способ получения -сульфоната в-цепи инсулина человека | 1972 |
|
SU487066A1 |

Продукт, в котором гистидин защищен в виде бензилпроизводного, выделяют с помощью смолы IRC 50. Получение пептида АВ из пептида А
Таблица 2
Получение пептида ABC из пептида АВ
Получение пептида АВСД из пептида ABC
Конечный продукт выделяют с помощью смолы IRC 50.
Карбобензокси- и бензильную группы удаляют путем восстановления натрием в жидком аммиаке.
Конечная аминогруппа у лизина (см. табл. 2 и 3) защищена карбобензоксигруппой. Оксигруппа у тирозина (см. табл. 3) защищена в виде тетрагидропиранильного производного. Оксигруппа у серина (табл. 4) защищена трифторадетильной группой. Обе защитные группы удаляют в процессе реакции сочетания.
Пример 4. Применение карбоксипептидазы-В.
Этот пример иллюстрирует удаление аргинина из пептида с помощью карбоксипептидазы-В.
Приготовляют три смеси:
а - 100 мл трнс-буфера (ОД моль хлористого натрия и 0,2 моль триоксиметиламипометан) при рН 7,65;
б - 8,5 мг сульфата лейцил-аланил-глицилпролил-фенилаланил-аргинина в 3,3 мл того же буфера;
в - 10 мл энзиматической смеси, разбавленной 0,015 мл смеси карбоксипептидазы-В, с содержанием 10 мг энзимов в 1 мл, в том же буфере,
Таблица 3
Таблица 4
Далее смещивают 2 мл смеси а, I мл смеси б и I мл смеси я и инкубируют в течение 1 час
при 37°С.
Смесь подвергают тонкослойной хроматографии на силикагеле, отмечают два пятнэ. Одно из них - аргинин, другое - пентапептид.
При проведении реакции в препаративных масщтабах растворы смешивают в том же соотнощении и инкубированную смесь сущат вымораживанием, экстрагируют метанолом, метанольный раствор упаривают досуха, остаток
растворяют в воде, а из водного раствора выделяют хроматографически с помощью смолы IRC 50.,
Пример 5. Валил-аланил-глицил-пролилфенилаланил-(С1) аргинин.
Этот пример иллюстрирует получение меченого пептида.
Приготовляют смесь, содержащую 0,392 мг меченого аргинина (Ci, 0,5 милликюри) в 5,0 мл 0,01 н. соляной кислоты к 421 мг немеченого аргинина в 20 мл I М буферного раствора бората калия, при рН 10,5. Отбирают 0,2 мл смеси и к ней добавляют 401 мг (5%-ный молярнйй избыток) N-карбоксиангидрида фенилаланина (сразу) при интенсивном пер(гмешивании при температуре О-2°С в течение 1 мин, поддерживая рН в интервале 10,5--10,4 5 н. едким кали. В конце реакции приливают, каплю каприлового спирта в качестве пеногасителя. Затем рН доводят до 3,5 концентрированной серной кислотой, пропускают через смесь струю азота в течение 10 мин, поднимают рН до 10,2 с помощью концентрированного (раствора) едкого кали и отбирают 0,1 мл реакционной смеси, содержащей пролнларгинин (С)..
В образовавщуюся смесь вводят 300,5 мг (6,5%-ный молярный избыток) N-карбоксиангидрида пролина при интенсивном перемешивании, при О-2°С. Реакция продолжается 1 мин, рН поддерживают в интервале 10,2- 10,1 5 н. раствором едкого кали. Декарбоксилирование ведут при рН 3,0 вышеописанным способом. Затем повышают рН до 10,2 концентрированным раствором едкого кали и отбирают на анализ 0,1 мл пробы, содержащей глицил-пролил-фенилаланил-аргинин (С).
Тетрапептид переводят в N-карбоксипептид аланил-глицил-пролил - фенилаланил - аргинина (GI) добавлением 248 мг (8%-ный молярный избыток) N-карбоксиангидрида аланина в реакционную смесь при и интенсивном перемещивании. Реакцию продолжают 1 мин, поддерживая рН в интервале 10,2-10,0 5 н. раствором едкого кали, а N-карбоксипептид декарбоксилируют при рН 3 вышеописанным способом. Далее рН повышают до 10,2 концентрированным водным раствором едкого кали и отбирают на анализ 0,1 мл пробы, содержащей нужное соединение.
Затем в реакционную смесь вносят 340 мг ангидрида N-карбоксивалина при О-2°С и интенсивном перемешивании. Реакцию продолжают 2 мин, поддерживая рН в интервале 10.3-10,0 5 н. раствором едкого кали. Далее концентрированной серной кислотой устанавливают рН 6,5 и отбирают на анализ 0,2 мл пробы, содержащей нужный радиоактивный гексапептид.
Каждую из проб хроматографируют на бумаге, применяя систему бутанол - уксусная кислота - вода в соотношении 4:1:5. Хроматограммы проявляют на радиоактивность. Результаты показывают, что свыше 85% продуктов каждой из реакции весьма загрязнены побочными продуктами.
Реакционную смесь подвергают лиофильной сушке, остаток экстрагируют трижды (по 150 мл) метанолом, экстракты объединяют и упаривают под вакуумом при 40°С досуха. Остаток растворяют в 2 мл воды, V4 часть раствора разбавляют в соотношении 1:1. Разбавленный раствор хроматографируют на колонке 200 мл с карбоксильной ионообменной смолой (С-50 фир.мы РОМ и Хасс, Филадельфия; диаметр 2,2 г.и/высота 55 слг)-в водородной форме. Через колонку пропускают раствор со скоростью 2.5 мл/мин, затем промывают водой в количестве 2 л, элюируют 0,01 н. серной кислотой. Элюент проверяют на изотоп С,
используя антраценовую колонку, с начальной скоростью 0,2 мл/мин. Затем скорость постепенно в течение 20 час повышают до 0,6 мл/мин и поддерживают ее постоянной до конца. Элюент собирают во фракции по 24 мл, а нужный продукт выделяют из фракций 25-72 установлением рН до 9,5 с помощью 50%-ного раствора едкого натра и сущат вымораживанием (лиофильная сушка). Остаток экстрагируют метанолом, экстракт упаривают под вакуумом при 40°С досуха. Остаток растворяют в небольшом количестве воды, рН доводят до 3,5 концентрированной соляной кислотой. Раствор подвергают лиофильной
сущке, после чего заданный продукт перекристаллизовывают из смеси вода - этанол. Пример 6. Брадикинин. Табл. 5 иллюстрирует получение нонапептида аргинил-пролил-пролил-глицил-фенилаланил-серил-пролил-фенилаланил-аргинина по предлагаемому способу. Таблица показывает последовательность стадий внесения N-карбоксиангидридов или М-тиокарбоксиангидр.идов с целью образования заданного продукта. Реакция начинается между 1 ммоль аргинина и 1 ммоль ангидрида N-карбоксифенилаланина в 0 мл водного буферного раствора борной кислоты при рН 10,5-рН реакционной смеси поддерживают 50%-ным водным раствоедкого натра в течение реакции.
Г ромежуточный iipo/inji-фенила ланил-аргинин выделяют с конечной декарбокснлизацией при рН 3, лиофильной сушкой смеси и растворением остатка метаполом. Метанольный раствор хроматографируют на силихагеле (колонке) и заданный трипептид элюируют 20%-ным водным метанолом, содержащим достаточное количество уксусной кислоты, чтобы поддерживать рН около 5. Трипептид превращают в заданный нонапептид последующи.ми реакциями (без выделения промежуточных продуктов). По первой реакции (стадия 3) 1 ммоль трипептида в 5 ммоль воды реагирует с эквивалентным количеством ангидрида
N-тиокарбоксисерина при рН 9 и температуре 4°С в продолжение 30 мин. Условия второй реакции (стадия 4) указаны в таблице, причем рП регулируют, используя твердую гидроокись бария. Детиокарбоксилирование проводят в конце каждой из реакций концентрированной серной кислотой. Прежде чем начинать следующую стадию реакции отфильтровывают выпавший сульфат бария. Конечным нродуктом этой серии реакций является раствор сульфата брадикинина, который переводят в свободное основание и выделяют хроматографически на ионообменной сзльфоновой смоле IRC-50 с постепенным элюированием водным раствором уксусной кислоты.
Пример 7. Серил-пролил-фенилаланиларгинин.
15,75 г хлоргидрата аргинина растворяют в 2,62 л буферного раствора тетрабората натрия, рН 10. Концентрированной серной кислочение 10 мин. Далее рН повышают до 10,2 50%-ным водным раствором едкого натра, после чего раствор охлаждают до 0°С. В смесь загружают 400 г льда и затем 82,5 ммоль ангидрида N-карбоксифенилаланина в 20 мл ацетона. Смесь интенсивно перемешивают 1 мин при указанной температуре и подкисляют концентрированной серной кислотой до рН 3, продувая азотом в течение 10 мин. Затем подщелачивают 50%-ным водным раствором едкого натра до рН 9,5 и загружают 400 г льда и 112,5 млюль ангидрида N-карбоксинролина в 150 мл ацетона. Раствор интенсивно перемешивают 1 мин при 0°С и декарбоксилируют по вынхеописанному методу. Операцию повторяют при рН 9,3 добавлением 15,0 ммоль трифторацетилангидрида N-карбоксисерина в 150 мл ацетона, затем перемешивают 1 мин, доводят рН до 7 и сушат вымораживанием. Силикагель с абсорбированным продуктом вносят в силикагелевую колонку, предварительно обработанную изопропанолом, далее проявляют, используя систему метанол : вода : : аммиак в соотношении 80 : 18 : 2, и выделяют заданный тетрапентид, не содержащий трифторацетильной группы.
Аналогично получают следующие соединения, используя трифторацетильное и трихлорацетильное производные соответствующих ангидридов N-карбокси или N-тиокарбокси-аминокислот (в каждом случае выделяют продукт, не содержащий защитной оксигрупны.
Таблица 5
При N-тиокарбоксисоединениях величина рН сочетания равна 8,8 вместо 9,3): Треонил-пролил-фенилаланил-аргинин Оксипролил-пролил-фенилаланил-аргинин р-Феннлсерил-пролил-фенилаланил-аргинин р-Оксилейцил-пролил-фенилаланил-аргинин |3-Оксинорвалил-пролил - фенилаланил-аргинин
у-Оксинорвалил-пролил - фенилаланил-арг№НИН
Предмет изобретения

Авторы
Даты
1970-01-01—Публикация