ы
Изобретение относится к способу получения новых производных пиразола общей формулы
3J -T-GN
Ч II-
iiJL- °
(IJ
где к - С,-Сб-алкил или группа фор- ю
мул
IRO
m
m
ФIR)
m
или
R и 1Ц - Н, С,-С -апкил, алкенил, С -С -цикло- алкил или С|-Сз-алкок- ;СИ 25
Или
Rj и RJ, взятые вместе с атомом азота, к которому они присоединены, образуют пи- перидиновое морфолиновое 30 или пирролидиновое кольцо; R - галоген, С -С4-алкил,
С -С -алкокси, С4-С4-га-. лоидалкил, циано; m 0..3,35
обладающих гербицидной активностью, ;соторые могут найти применение в сельском хозяйстве.
Целью изобретения является способ получения новьпс производных пиразола, 40 обладающих гербидидной активностью, превьшающей активность известных гербицидов ряда пиразола.
Пример 1. 5-Дйано-1-(2-пиридинил)-Ы-метил-1Н-пиразол-4-карбоксамид45 А- Сложный этиловый эфир 5-амино1 - (2 пиридинш1) -1 Н-пиразол-4-карбо- новой кислоты.
Раствор 21,83 г 2-гидразинпиридина и 38,2 г этил (зтоксиметилен)циано-; cjj адетата растворяют в 150 мл уксусной ьсислоты и 50 мл воды, нагревают на шаровой ванне в,течение 16 ч. Реакционную смесь охлаждают до комнатной температуры и помещают в рефрижератор для образования кристаллов. Осажденное 1 ердое вещество собирают фильтрацией ы промывают холодным 50%-ным водным этанолом, получают 23,62 г сложного
5
0
5
0
5
0
5
jj
этилового эфира 5-амино-1-(2-пириди- нил)-1Н-пиразол-4-карбоновой кислоты. Выход 50,9%. Т.пл. 89-9Гс.
B.Сложный этиловый эфир 5-ХЛОР-1- (2-пиридинил)-1Н-пиразол-4-карбоновой кислоты.
Хлористый нитразил пробулькивают в раствор 23,62 г сложного этилового эфира 5-амино-1-(2-пнридинил)-1Н-пи- разол-4-карбоиовой кислоты в 100 мл хлороформа в течение 5 мин. Реакционную смесь нагревают на паровой ванне 5 мин h летучие вещества удаляют при пониженном давлении, получают масло. Остаток охлаждают, получают твердое вещество, которое кристаллизуют, из этанола, получают 16,,3 г сложного этилового эфира 5-хлор-1-(2-пиридинил)- 1Н-пиразол-4-карбоновой кислоты. Выход 64,8%. Т.пл. .
Найдено, %: С 52,22; Н 3,75; N 16,59.
С„ H.oClNjO.
Вьгаислено, %: С 52,50; Н 4,01j N 16,70.
C.Сложный этиловый эфир 5-циано1 - (, 2-пиридинил) -1 Н-пиразол-4-карбоно- вой кислоты.
Растворяют 7,36 г сложного этилового эфира 5-хлор-1-(2-пиридинил)-1Н- пиразол-4-карбонов зй кислоты, 3,2 г цианида натрия в 25 мл ДМФ, нагрева- ,ют при 100 С в течение 3 ч. Реакционную смесь охлаждают и разбавляют 300 мл ледяной воды. Осадок твердого вещества собирают фильтрацией, получают 5,79 г твердого вещества, которое перекристаллизовывают из этанола, получают 4,72 г сложного этилового эфира 5-диано-1-(2-пиридинил)- li Н-пиразол-4-карбоновой кислоты. Т.пл о П2-114°С.
Найдено,%: С-59,43; Н 4,11; N 23,06.
C4zH,o,N402,
Вычислено, %: С 59,90; Н 4,16; N 23,13.
D.К раствору 2,5 г сложного этилового эфира 5-циано-1-(2-пиридинил)- 1 Н-пиразол-4-карбонов(й кислоты в
20 мл ДМФ добавляют избыток 40%-ного (тонометиламина таким образом, чтобы исходный пиразол не осаждался. Через 24 ч добавляют к реакционной смеси дополнительные количества монометиламина и для того, чтобы сохранить эти реактанты в растворе. Реакционную смесь нагревают, добавляют к ней
t50 мл ледяной воды. Осажденное твердое вещество собирают фильтрацией и перекристаллизовывают из метанола, получают 1,2 г 5-циано-1-(2-пиридинш1)- Н-метил-1Н-пиразол-4-карбоксамид. Т.пл. 200-202 0.
Найдено, %: С 58,87; Н 3,83; N 30,53.
С„ HqN40i
Вычислено, ,: С 58,15; Н 3,99; N 30,82.
Пример 2. 5-Циано-1- 2-(три- фторметил) -4-хлорфенил| -М-метил-1Н- пиразол-А-карбоксамид.
А. Сложный этиловый эфир 5-амино- 1 (трифторметил)-4-хлорфенил -1Н- пиразол-4-карбоновой кислоты.
Раствор 31,58 г 2-(трифторметил)- А-хлорфенилгидразина и 27,92 г этил (этоксиметилен)цианоацетата, растворенный в 225 г уксусной кислоты и 75 мл воды, нагревают н паровой ванне в течение примерно 16 ч. Реакционную смесь охлаждают до комнатной тем- 25 N 12,23.
С.Сложный этиловый эфир 5-циано-1- -- (. трифторметил) -4-хлорфенил -1Нпиразол- -карбоновой кислоты.
Раствор 3,15 г сложного этилового эфира 5-хлор-1- 2-(трифторметил)-4- хлорфенил -1Н-пиразол-4-карбоновой кислоты и 1,1 г цианида натрия в 25 м диметилформамида нагревают при 100 С в течение 4,5 ч. В реакционную смесь добавляют 3 г молекулярных с.. Реакционную смесь охлаждают и добавляют 300 мл ледяной воды. Осажденное твердое вещество собирают фильтрацией и перекристаллизовывают из этанола (древесный уголь), получают 1 г сложного этилового эфира 5-циано-1- 2- (трифторметил)-4-хлорфенил -1К-пира- зол-4-карбоновой кислоты. Т.пл. 70- 72°С.
Найдено, %: С 49,16; Н 2,39; N 11,93.
C,4H,ClF.,.i.
Вычислено, %:-С 48,93; Н 2,64;













30
ратуры и помещают в рефрижератор. Осажденное твердое вещество собирают фильтрацией и объединяют .с тверым вещество, отделенным от фильтрата, получают 43 г сложного этилового эфира 5-амино-1- 2-(грифторметил)- 4-хлорфенил -1Н-пиразол-4-карбс новой кислоты. Т.пл. 114-11 .
В. Сложный этиловый эфир 5-хло.р- (трифторметил)-4-хлорфенил -1Н- пиразол-4-карбоновой кислоты.
Газообразную соляную кислоту про- булькивают через раствор 26 г сложного этилового эфира 5-амино-1- 2- (трифторметил)-4-хлорфенш1 -1Н-пира- о N 17 20. зол-4-карбоновой кислоты, растворенного в 250 мл хлороформа в течение 1 мин. Затем хлористый нитрозил про- булькивают через раствор в течение 10 мин. Реакционную смесь нагревают а паровой ванне и летучие удаляют ри пониженном давлении. Остаток астворяют в горячем этаноле, очищат древесным углем и продукт кристал- , получают 16,6 г сложного тилового эфира 5-хлор-1- 2-(триторметил) -4-хлорфенил -1Н-пиразол- -карбоновой кислоты. Т.пл. 67-69 с.:
D. Ра вого эфи тил) -4-х новой ки мономети вают при онную см воды, ос бирают ф 35 таллизац 535 мг 5 4-хло; фе карбокса
Найде
N
С,, Hg
Вычис 17,05.
П р и 45 хлорфени боксамид
А. Сл 1-(2,4-д боновой
Раств эфира 5пйразолцианида л ДМФ, под 55 в течени добавляю рагреваю вливают твердое
50
Найдено, %: С 44,48; Н 2,33; 75,80.
C,,HqCVF,NiO.
Вычислено,%: С 44,22; Н 2,57; 7,93.
N 17 20.
D. Раствор 1,23 г сложного этилового эфира 5-5-циано- 2-(трифторметил) -4-хлорфенил -1 Н-пиразол-4-карбо- новой кислоты и 8 мл 40%-ного водного монометиламина в 20 мл ДМФ перемешивают при 25°С в течение 16 ч. Реакционную смесь вливают в 150 мл ледяной воды, осажденное твердое вещество собирают фильтрацией и очищают перёкрис- таллизацией из этанола, получают 535 мг 5-циано-1- 2-(трифторметил)- 4-хло; фенил) -N-метил-1 Н-пиразол-4-- карбоксамида. Т.пл. 162-164 С.
Найдено,%: С 47,74; Н 2,67;
о N 17 20.
N
С,, HgClFjN O.
Вычислено, %: С 47,51; Н 2,45; 17,05.
П р и м е р 3. 5-.Циано-1-(2,4-ди- 45 хлорфенил)-N-метил-1Н-пиразол-4-кар- боксамид.
А. Сложный этиловьм эфир 5-циано- 1-(2,4-дихлорфенш1)-1Н-пиразол-4-кар боновой кислоты.
Раствор 5,4 г сложного этилового эфира 5хлор-1-(2,4-дихлорфенил)-1Н- пйразол4-карбоновой кислоты и 2 г цианида лития, растворенного в 30 мл ДМФ, подвергают реакции при 55 в течение 23 ч. К реакционной смеси добавляют еще 1 г цианида лития и рагревают в течение еще 7 ч. Смесь вливают в ледяную воду, осажденное твердое вещество собирают фильтраци-
50
ей и перек ристаллизовывают из спирта (древесньй уголь), получают 3,75 г сложного этилового эфира 5-циано-1- (2,4-дихлорфенил)-1Н-пиразол-4-кар5о- новой кислоты. Выход 61%. Т.пл. 79- 8Гс.
И
Найдено, %: С 50,12; Н 3,11; 13,29.
C,jH,,Cl2N,0. Вычислено,%: С 50,35; Н 2,93;
13,55.
В. К раствору 2,5 г сложного эти- jioBoro эфира 5-циано-1-(2,4-дихлорфенил)-1Н-пиразол-4-карбоновой кис- jjioTH в 20 мл ДМФ добавляют 20 мл 40%-ного водного монометиламина. Реакционную смесь перемешивают при ком 1 атной температуре 2,5 ч, раствор вливают в ледяную воду. Осадок соби- ак)т фильтрацией и перекристаллизовы йают из метанола ri воды, получают 1,3 г 5-циано-1 - (2,4-диклорфенил) Йетил-.1 Н-пиразол-4-карбоксамид. Т.пл |82-183°С.
На йдено, %; С 48,69; Н 2,74; И 19,23.
.C,iHgCl N40.
С 48,84; Н 2,73;
Вычислено,% 18,98.
П р и м е р 4. 5-Циано-1-(4-бром- фенил)-М-метш1-1Н-пиразол-4-карбокса1Ф1Л ,
А, Сложный этиловьй эфир 5- Циано1-(4-бромфенил)-1Н-пиразол-4-карбоно™
аой кислоты
Раствор 6,6 сложного этилового эфира 5-хлор-1-(4-бромфенил)-1Н-пира эол-4-.1-:арбонов6й кислоты в-30 мл ДШ ,с 2 г, цианида натрия нагревают при в течение 3 ч. Реакционную смесь вливают в ледяную воду и осажденное твердое вещество собирают фильтраци ей. Продукт перекристаллизовывают из ЗА-спирта, получают 5,3 г сложно- го этилового эфира 5-циано-1-(4-бром- феккл)-1Н-пиразол-4-карбоновой кисло-- ты. Т.пл. 104-105 С.
Найдено, %: С 48,90; Н 2,91; N 13,23.
,o BrN,02.
Вычислено, %: С 48,77; Н 3,Т5; N13,13,.
В. Раствор 3,2 г сложного зтило- цого эфира 5-циано-1-(4-бромфенил)- 1Н-пиразол-4-карбоновой кислоты в 40 мл ЗА-спирта и 10 мл 40%-ного водного монометиламина нагревают с обратным холодильником в течение 2 ч. К реак
0
5
0
5
0
ti
ционной смеси добавляют дополнительно 10 мл 40%-ного водного монометиламина, реакционную смесь нагревают с обратным холодильником 3 ч. Смесь охлаждают и осажденное твердое вещество собирают фильтрацией, получают 1 г 5-циано-1-(4-бромфенил)-К-метил- 1Н-пиразол-4-карбоксамид. Т.пл. 240- 241°С..
Найдено, %: С 47,39; Н 3,07; N 18,49.
,BrN40.
Вычислено,%: С 47,29; Н 2,97; N 18,36.
Следующие соединения получают аналогично примерам 1-4.
П р и м е р 5. 5- Диано-1-фенил-Ы- циклопропил-1Н-пиразол- 4-карбоксамид, Т.пл. 220-222 С.
Найдено, %: С 66,47; Н 4,68; N 22,06-.
C,4H,iN40.
Вычислено,%: С 66,,66; Н 4,79; N 22,21.
П р и м е р 6. 5-Циано-1-(3-бром- фенил)-N-метил-1Н-пиразол-1-карбокса- МИД, Т.пл. 178,5-180,,5°С.
Найдено, %: С 47,33; Н 3,03; N 18,26.
.
Вычислено, %: С 47,24; Н 2,97; N 18,36.
Пример 7. 5-Циано-1-(3-бром фенил) -N-этил-1 Н-пиразол-4-карбокса°. .МИД, Т.пл. 154,5-156 С.
Найдено, %: С 48,74j Н 3,4 6; N 17,34. . C,jH«BrN40,
Вычислено, %: С 48,92; Н 3,47; N 17,55.
Пример 8. 5- иaнo-1-fЗ-(тpи- фторметил)фенилЗ -N-метил-1Н-пиразол 4-карбоксамид, т.пл. 151-153°С.
Найдено, %: С 53,29; Н 3,28; N 18,88.
C,5H,F,N4.0.
Вычислено,%:.С 53,07; К 19,04.
3,08;
Пример 9. 5-Циано- - з-(три- фторметил)фен.ил -N-этил--1 Н-пиразол- 4-карбоксамид, т.пл. 143-145 С.
Найдено,%: С 54,75; И 3,39; N 18,28.
N
0,4 И„ F,N40.
Вычислено,%: С 54,55; Н 3,60; 18,17.
Пример 10. 5-Циано-1-(2,4-ди- бромфенил)-Н-метил-1Н-пиразол-4-кар- боксамид, т.пл. 198-200 С.
Найдено, %: С 37,50; Н 2,15; N 14,47.
C,2H8B4 N40.
Вычислено,%: С 37,53; Н 2,10; N 14,59.
П р и м.е р 11. 5-Циано-1-(3-ме- тилфенил)-М-метил-1Н-пиразол-4-кар- боксамид, т.пл. 159-161°С.
Найдено,%: С 64,70; Н 5,09; N 23,18.
C,H,4N40.
Пример 17. 5-Циа 2-пиpидинил)-N-мeтил-1Hкарбоксами р, т.пл. 218-2
Найдено, %: С 50,29; N 26,53.
С,1 HgClNjO.
Вычислено, %: С 50,49 N 27,76.
10 Пример18. 5-Циа ди -ил)-Ы-этил-1Н-пиразол МИД, т.пл. 210,5-212°С.
Найдено,%: С 59,72; Н N 29,02.
Вычислено, %: С 64,99; Н 5,03; N 23,32.
Пример 12. 5-Циано-1-(3-фтор- фенил)-N-метил-1Н-пиразол-4-карбокса- мид, т.пл. 188-189,5 с.
Найдено, %: С 58,8Т; Н 3,62; N 22,70.
C,;(H,FN40.
Вычислено,%: С 59,02; Н 3,71; N 22,94.
Пример 13. 5-Циано-1-(3-фтор- фенил)-Н-этил-1Н-пиразол-4-карбокса- мид, т.пл. 163-164 С.Найдено, %: С 60,64; Н 4,11; N 21,46.
С„Н4, FN40.
Вычислено, %: С 60,46; Н 4ц29; N 21,69.;
П р и м е р 14. 5-Циано-1-(4-пири- динил)-N-метил-1Н-пиразол-4-карбокса15
С,гН„К50.
Вычислено,%: С 59,74; N 29,03.
Пример 19. 5-Циа 20 фенил)-N-нетил-1Н-пиразо амид, т.пл. Т81-183°С.
Найдено, %: С 55,56; N 21,36.
C,HqClN40.
Пример 20. 5-Циа токсифеНИЛ)-N-нетил-1Н-п карбоксамид, т.пл. 190,5 30 Найдено,%: С 60,66; Н N 21,61.
C,,H,N402.
Вычислено,%: С 60,93; N 21,86.
П р и м е р 21. 5-Циа дихлорфенил)-N-метил-1Нкарбоксамид, т.пл. 196-1
Найдено,%: С 48,54; Н N 18,89.
,
Вычислено,%: С 48,44; N 18,98.
Пример 22. 5-Циа хлорфенил) -N-этшl-1 Н-пир
35
40
МИД, т.пл. 216-218 с.
.Найдено, %: С 57,93; Н 3,86; N 30,66.
С, .
Вычислено,%: С 58,14; Н 3,99; N 30,82.
Пример 15. 5-Циано-1-(3-хлор- . .,
фенил)-N-метил-1Н-пиразол-4-карбокса- ксамид, . т.пл. 151-153 с. МИД, т.пл. 181-182°С.
Найдено,%: С 55,44; Н 3,56; N 21,63.
,ClNyO.
вычислено,%: С 55,28; Н 3,48; N 21,49.
Пример 16. 5-Циано-1-(3-хлор фенил)-N-этил-1Н-пиразол-4-карбокса- 135-136°С.
МИД, т.пл.
Найдено, %: С 56,94; Н 4,06; N 20;38.
СоН, C1N40.
Вычислено,%: С 56,84; Н 4,04; N 20,39.
Найдено,%1 С 50,72; Н N 18,27.
C,,H,Cl2N40.
Вычислено, %: С 50.51 N 18,12.
Пример 23. 5-Циа фторметил)фенил -N-метил 4-карбоксамид, т.пл. 182 Найдено,%: С 52,99; Н
; N 18,84.
,N40.
Вычислено,%: С 53,07; N 19,04.
29968
Пример 17. 5-Циано-1-(5-хлор- 2-пиpидинил)-N-мeтил-1Hпиpэзoл-4- - карбоксами р, т.пл. 218-219 С.
Найдено, %: С 50,29; Н 3,27; N 26,53.
С,1 HgClNjO.
Вычислено, %: С 50,49; Н 3,08; N 27,76.
10 Пример18. 5-Циано-1-(2-пири- ди -ил)-Ы-этил-1Н-пиразол-4-карбокса- , МИД, т.пл. 210,5-212°С.
Найдено,%: С 59,72; Н 4,54; N 29,02.
С,гН„К50.
Вычислено,%: С 59,74; Н 4,60; N 29,03.
Пример 19. 5-Циано-1-(2-хлор фенил)-N-нетил-1Н-пиразол-4-карбокс- амид, т.пл. Т81-183°С.
Найдено, %: С 55,56; Н 3,46; N 21,36.
C,HqClN40.
Вычислено,%: С 55,29; Н 3,48; N 21,49. ...
Пример 20. 5-Циано-1-(4-ме- токсифеНИЛ)-N-нетил-1Н-пиразол-4- карбоксамид, т.пл. 190,5-192°С. Найдено,%: С 60,66; Н 4,61; N 21,61.
C,,H,N402.
Вычислено,%: С 60,93; Н 4,72; N 21,86.
П р и м е р 21. 5-Циано- 1-(3,4- дихлорфенил)-N-метил-1Нпиразол-4- карбоксамид, т.пл. 196-197°С.
Найдено,%: С 48,54; Н 2,79; N 18,89.
,
Вычислено,%: С 48,44;. Н 2,73; N 18,98.
Пример 22. 5-Циано-1-(3,4-ди- хлорфенил) -N-этшl-1 Н-пиразол-4-карбо г
. .,
ксамид, . т.пл. 151-153 с.
Найдено,%1 С 50,72; Н 3,16; N 18,27.
C,,H,Cl2N40.
Вычислено, %: С 50.51; Н 3.26: N 18,12.
Пример 23. 5-Циано-1- 2-1три фторметил)фенил -N-метил-1Н-пиразол- 4-карбоксамид, т.пл. 182-184°С. Найдено,%: С 52,99; Н 3,04;
; N 18,84.
,N40.
Вычислено,%: С 53,07; Н 3,08; N 19,04.
9142299610
П р и м е р 24. 5-Циано-1-(4-фтор-П р -и м е р 31. 5--Циано-1-фенил- фенил) -N-метил- 1 Н-пиразол- 4-карбокс-N-2-пропенил-1 Н-пира:1ол-4-карбоксамид. амид, т.пл. .т.пл. 163-164 С.
Найдено, %: С 58,80; Н 3,49}Найдено, %: С 66,39; Н 4,57;
N 22,71. N 22,08.
, Р1ч 40. .
Вычислено,%: С 59,02; Н 3,71; Вычислено.%: С 66,66; Н 4,7;
N 22,94.N 22,21.
10 П р и м е р 32. 5-Циано-1-фенилПример 25. .5-Цианр-1-(4-фтор- -этил-1Н-пиразол-4-карбоксамид,
ФЕНИЛ)-N-этил-1H-пиpaзoл-4-кapбo-т.пл. 199-200 С. кЬамид, т.пл. 163-165 С.Найдено,%: С 65,18; Н 4,82;
; Найдено,%: С 60,21; Н 4,17;N 23,48. Ni21,44. .
С„Н„ FN40.Вычислено,%: С 64,99; Н 5,03;
; Вычислено,%: С 60,46; Н 4,29;N 23,32.
NJ21,69.При м е р 33. 5Н иано-1-С4-хлор: Пример 26. 5-Циано-1-(3-хлор-,Фенил)-N-метил-1Н-пиразС)л-4-карбокс:
44метилфенйл)-N-метил-1Н-пиразол-4- 20змид, т.пл.. 211-212 С. кёрбоксамид, т.пл. 186-190 с.
; Найдено; : С 57-,09; Н 3,90;Найдено.%: С 55,13; Н 3,43;
,30.N 21,32. , I C(,H C1N40. .Ct-iHqClN O.
I Вычислено, %: С 56,84; Н 4,04; 25 Вычислено,%: С.55,29; Н 3,48;
N.20,39.,N 21,49.
{Пример 27, 5-Циано-1-(2,3- П р и м е р 34. 5-Циано-1-(2,5-диДЙхлорфенил)-N-метил-1Н-пиразол-4-хлорфенил)-N-метил-1Н-пиразол-4-карка рбоксамид, т.пл. 212-214°С.боксамид, т.пл. 186-187 С.
Найдено,%: С 48,58; Н 2,61; 30 Найдено,%: С 48,73; Н 2,60;
N ,19,09. N 18,84.
C,iH8Cl,N40.C,2.HeClzN40.
Выделено, %: С 48,84; Н 2,73;Вычислено,%: С 48,84; Н 2,73;
N 18,98. N 18,98.
Пример 28. 5-Циано-1-(3,4-ди-„ Пример 35. 5-1 ано-1-(2,5-ди
метилфенил)-N-метил-1Н-пиразол-4-кар-хлорфенил)-К-этил-1Н-пиразол-4-карбобоксамид, т.пл. 195-197 с.ксамид, т.пл. 170-172 Со
.Найдено,%: С 50,67;; Н 3,27;
Яайдёно.%: С 65,86; Н 5,29;N 18,22. Н 21,75. . 40CHH,oC4N40.
C,4n,4N40. .Вычислено,%: С 50,51; Н 3,26;
Вычислено,%: С:. 66,13; Н 5,55;N18,12. N 22,03. П р и м е р 36. 5-Циано-1-(4-меПример 29. 5-Циано-1-(2-хино-тилфенил)-N-метил-1Н-пиразол-4-карболинил)-N-мeтшI-1H-пиpaзoл-4-кapбoкc- д ксамид, т-.пл. 205-207 с. ашад т.пл. 22в-227°С.Найдено,%: С 65,19; Н 4,97-;
Найдено,%; С 65,12; Н 3,80;Н 23,04. N 25,43. .
С,5Н„ N50.C,,.
Вычислено,%:. С 64,97; Н 4,00; . Вычислено, %: С 64,99; Н 5,03;
Н 25,26. 23,32.
Пример 30. 5-Циано-1-фенил- Пример 37. 5-Циано-1-(4-меН Пропш1-1Н-пиразол-4-карбоксамид,тилфенил)-Н-этш1-1Н-пиразол-4-карбот.пл. 168-169 С .жсамид, т.пл. 209-Z10°C.
Найдено,%: С 65,88; Н 5,33;Найдено,%: С 66,36; Н 5,39;
.Ш 21,85.. N 22,16.
С,4НнМ40.C 4H44N40.
Вычислено, %: С 66,13; Н 5,55; Вычислено,%: С 66,17; Н 5,55;
22,03.N 22,03.
11142299612
П р и м е р 38. 5-Циано-1-(2,4-ди- мид с последующей перекристаллизацией
хлорфенил)-М-этил-1Н.-пиразол-4-карбо- ксамид, т.пл. 140-141.
Найдено,%: С 50,68; Н 3,28; N 18,25.
Cj HioCl N O.
Вычислено,%: С 50,51; Н 3,26; N 18,12.
из этанола. Т.пл. 185-187 С.
Найдено,%: С 64,42; II 4,47; 5 N 24,88.
п. и j(
C,5H,jN,0.
Вычислено,%: С 64,51; Н 4,69; N 25,07.
Пример. 42. 5-Циано-1-(4-хлор Пример 39. 5-Циано-1-(4-хлор- to фенил)-К-циклопропил-1Н-пиразол-4феннл)-Ы-этил-1Н-пиразол-4-карбо- ксамид, т.пл. 166-168 С.
Найдено, %: С 56,92; Н 4,00; N 20,23.
C,3H,,C1N40.
Вычислено,%: С 56,84; Н 4,04; N 20,39.
П р и м е р 40. 4-Циано-1-(3-циа- нофенил)-N-метил-1Н-пиразол-4-карбо- ксамид, т.пл. 206-208 0.
Найдено,%: С 62,10; Н 3,85; N 27,60:
C HqNyO.
Вычислено,%: С 62,15; Н 3,61; N 27,87.
П р и м е р 41. 5-Циано-1-(3-циа- нофенил)-К-метил-Ы-этил-1Н-пиразол- 4-карбоксамид. .
А. 5-Циано-1-(3-цианофенил)-1Н- пиразол-4-карбоновая кислота.
7,7 г сложного этилового эфира 5-циаио-1-(3-цианофенил)-1Н-питазол- 4-кар боновой кислоты растворяют в 75 мл горячего этанола. К реакцирнкарооксамид.
А. 5-Циано-1-(4-хлорфенил)-1Н-ли- разол-4-карбоновая кислота.
Горячий раствор 5,61 г гидроокиси
15 калия, растворенного в 110 мл ЗА-эта- нола7 добавляют к горячему раствору 11,3 г сложного этилового эфира 5-ци- ано-1-(4-хлорфенил)-1Н-пиразол-4-кар- боновой кислоты, растворенной в 225 мл
20 ЗА-этанола. Полученную соль растворяют в 1 л воды и раствор подкисляют - концентрированной соляной кислотой. Осажденное твердое вещество собирают фильтрацией и перекристаллизовывают
25 из толуола, получают 8,47 г 5-циано- 1-(4-хлорфенил)-1Н-пиразол7-4-карбоно- вой кислоты, т.пл. 192-195 С.
при комнатной температуре 15 мин. К реакционной смеси добавляют 7 мл циклопропиламина и смесь перемешивают
Найдено,%: С 53,25; Н 2,50;
N 16,73. 30 C HbClNjO.
Вычислено,%: С 53,35; Н 2,24;
N 16,97.
В. Раствор 2,47 г 5-iftiaHO-1-(4хлорфенил)-1Н-пиразол-4-карбоновой ной смеси добавляют 3,2 г гидроокиси кислоты и 2,03 г карбонилдиимидазола. калия, растворенного в этаноле. Не- растворяют в 25 мп ДМФ, перемешивают большое количество воды добавляют к реакционной смеси, которую немедленно вливают в воду. Раствор подкисляют концентрированной соляной кисло- Q в течение 16 ч. Смесь вливают в 150мл той и осажденное твердое вещество ледяной воды и осажденное твердое ве- собирают фильтрацией, высушивают, по- щество собирают фильтрацией. Твердое лучают 4,3 г 5-цианог-1-(3-циано- вещество перекристаллизовывают из фенил)- Н-пиразол-4-карбоновой кисло- этанола, сушат, получают 5-циано-1- ты, т.пл. 190-192 С.Д2 (4-хлорфенил)-Я-циклопропил-1Н-пиразол-4-карбоксамид. Т.пл. 204-20б с.
В. 2 г карбонилдиимидазола добав- Найдено,%: С 58,70; Н 4,05; ляют к раствору 2,0 г 5-циано-1-(3- N 19,31. цианофенил)-1 Н-пиразол-4-карбоновой C,4H(,C1N40.
кислоты, растворенной в 50 мл даЯ). . , Вычислено.%: С 58,65; Н 3,87; Реакционную смесь перемешивают при комнатной температуре 25 мин, добавляют 740 мг N-этил-N-мeтилaминa. Реак- |дионную смесь перемешивают 24 чj после чего раствор выливают в ледяную
воду Осажденное твердое вещество со-55 щим амином. бирают фильтрацией и высушивают, по- Пример 43. 5-Циано-1-(4-хлор- лучают 1,2 г 5-циано-IT-(3-цианофенил)- фенил)-М8К-диметш1-1 Н-пиразол-4-карбс)- N-мeтшI-N-этил-1Н-пиразол-4-карбокса- ксамид, т.пл. 123-125 С.
N 19,.
Предлагаемое соединение в следун - ш;их примерах получают реакцией пирз.- золкарбоновой кислоты с соответствуюиз этанола. Т.пл. 185-187 С.
Найдено,%: С 64,42; II 4,47; N 24,88.
п. и j(
C,5H,jN,0.
Вычислено,%: С 64,51; Н 4,69 N 25,07.
карооксамид.
А. 5-Циано-1-(4-хлорфенил)-1Н-ли- разол-4-карбоновая кислота.
Горячий раствор 5,61 г гидроокиси
калия, растворенного в 110 мл ЗА-эта- нола7 добавляют к горячему раствору 11,3 г сложного этилового эфира 5-ци- ано-1-(4-хлорфенил)-1Н-пиразол-4-кар- боновой кислоты, растворенной в 225 мл
ЗА-этанола. Полученную соль растворяют в 1 л воды и раствор подкисляют - концентрированной соляной кислотой. Осажденное твердое вещество собирают фильтрацией и перекристаллизовывают
из толуола, получают 8,47 г 5-циано- 1-(4-хлорфенил)-1Н-пиразол7-4-карбоно- вой кислоты, т.пл. 192-195 С.
при комнатной температуре 15 мин. К реакционной смеси добавляют 7 мл циклопропиламина и смесь перемешивают
хлорфенил)-1Н-пиразол-4-карбоновой кислоты и 2,03 г карбонилдиимидазола. растворяют в 25 мп ДМФ, перемешивают в течение 16 ч. Смесь вливают в 150мл ледяной воды и осажденное твердое ве- щество собирают фильтрацией. Твердое вещество перекристаллизовывают из этанола, сушат, получают 5-циано-1- (4-хлорфенил)-Я-циклопропил-1Н-пира Вычислено.%: С 58,65; Н 3,87;
N 19,.
Предлагаемое соединение в следун - ш;их примерах получают реакцией пирз.- золкарбоновой кислоты с соответствуюНайдено.%: С 56,78; Н 4,08; N 20,32.
С„Н„ C1N40.
Вьгаислено,%: С 56,84; Н 4,04;
N 20,39. .,
П р и м е р 44. 5-Циано-1-(4-хлор фенил )-Н- метил-Н-этил-1Н-пиразол-4- карбоксамид, т.пл, 87-89 С.
Найдено,7.: С 57,98; Н 4,49;
,:N 19,34. ; C,4H,C1N40.
Вычислено,%: С 58,24; Н 4,54; :N 19,40.
Пример 45. 5-Циано-1-(4-хлор (фенил )-М,Ы-диэтил-1 Н-пиразол-4 -карбо ксамид, т.пл. 109-1 . ; Найдено,%: С 59,32; Н 4,79; iN 18,33.
CijH..
Вычислено,%: С 59,51; Н 4,99; 1N 18,50. .,
; П р и м е р 46. 5-Циано-1-(4-хлор |фенил) -N-этил-N-пpoпил-1 Н-пиразол-4 жарбоксамид, т.пл. 51-52°С.
Найдено,%: С 60,65; Н 5,50; J7;82... .
: C, C1N40.
Вычислено,%: С 60,66; Н 5,41; N 17,69
.Пример 47. 5-Циано-1-(4-хлор фенил)N,N-дипропил-1Н-пиразол-4-кар брксамид, т.пл. 83-84°С.
Найдено,%: С 61,61; Н 5,58; N 16,88.
С, .
Вычислено,%: С 61,72; Н 5,79; N 1 6, У 4.
.. П .р и м е р 48. (4-xлop- фэнил)4-циaнo-1H-пиpaзoл-4-илjкap- бонил -пиперидин, т.пл. 124-125°С.
Найдено,%: С 60,74; Н 4,74; N 17,60.
C.eH..
Вычислено,%: С 61,05; Н 4,80; N 17,80.
Пример 49. 5-Циано-1-(3-зспор 4-метилфенил)-N,К-диметил-1Н-пиразол 4-карбоксамид, т.пл. 109-111°С.
Найдено,%; С 57,96; Н 4,34; N 19,39.
C,4H,C1N40.
Вычислено,: С 58,24; Н 4,54; N 19,40.
П р и м е р 50. 5-Циано-1-(2,4- дихлорфенил)-N,N-диметил-1Н-пиразол 4 карбоксамид, т.пл. 117-119 С.
Найдено,%: С 50,25; Н 3,26; N 17,80.
.C,.jHioCl N40.
Вычислено,%: С 50,51; Н 3,26; N 18,12.
П р и м е р 51. 5-Циано-1-(2,4-ди хлорфенил)-N-циклопропил-1Н-пиразол- 4-карбоксамид, т,пл. 173-174 С.
Найдено,%: С 52,38; Н 3,26; N 17,41.
.
Вычислено %: С 52,36; Н 3,14; N 17,44.
Пример 52. 5-Циано-1-(2,4- дихлорфенил)-Ы-метил-Н-этил-1Н-пира- зол-4-карбоксамид, т.пл. 75-77 С.
Найдено, %: С 51,76; Н 3,74; N 17,28.
.
Вычислено,%: С 52,03; Н 3,74; N 17,34.
Пример 53. 5-Циано-1-(2,4-ди хлорфецшт)-Н,Н-диэт11п-1Н-пиразол-4- карбоксамид, т.пл. 111-112,5°С.
Найдено,%: С 53,23; Н 3,94; N 16,56.
С„Н,оС1,Н40..
Вычислено,%: С 53,43; Н 4,18; N 16,61.
Пример 54. )-Циано-1-(2,4-ди хлорфенил)-Ы-метил-Н-метокси-1Н-пира зол-4-карбоксамид, г.шт. 143-145 с.
Найдено,%: С 47,88; Н 3,09; N 17,16.
С, H,oCl,N402.
Вычислено.%: С 48,02; Н 3,10 N 17,32.
Пример 55. 5-Циано-1-(3-бром фенил)-N,N-диметил-1Н-пиразол-4-кар- боксамид, т.пл. 125 с.
Найдено,%: С 49,17; Н 3,30; N 17,29.
C,5H,,BrN40.
Вычислено,%: С 48,92; Н 3,47; N 17,55. . ,
Пример 56. 5 Циано-1-:(,3-бром фeнил)-N-мeтил-N-мeтoкcи-tН-пиразол- 4-карбоксамид, т.пл. 154-155 с.
Найдено,%: С 46,83; Н 3,45; N 16,49.
С4, Ни BrN402 .
Вычислено,%: С 46,59; Н 3,31; N 16,72.
П р и м е р 57. 5-Циано-1-ГЗ-(трй фторметил)фенил -Ы,N-диметил-1И-пира зол-4-карбОксамид, т.пл. 97-99°С.
Найдено,%: С 54,46; Н 3,88; N 18,01.
C,,H«F,N40.
Вычислено.: С 54}55; Н 3,60; N 18,17.
П p и м e p 58, 5-Циано-1- 3-(три- 5 фторметил)фенил -Н-циклопропил-1Н- пиразол-4-карбоксамид, т.пл. 180- 182 с.
Найдено,%: С 56,28; Н 3,50| N17,40.10
С,уН„ .
Вычислено,%: С 56,25; Н 3,46; N17,49.
5-Циано-1- 3-(триC,5H,5BrN40.
Вычислено,%: С 51,89; Н N 16,41.
П р и м е р 65. 5-Циано фенил)-N-циклoпpoпил-1Н-пн карбоксамид, т.пл. 217-218
Найдено,%: С 50,61; Н 3 N16,80.
C,4H,,BrN40.
Ьычислено,%: С 50,78; N16,92.
П р и м е р 66. 5-Циано метил)-N,N-димeтил-1Н-пира
ll Р И М с р ш) .7 « л Аъ««жч t 1. ...--. - . у . р,. ,- .. .п ....-
фторметил)фенил -N-мeтил-N-этил-1H- jsбоксамид, т.пл. 132-133 С.
пиразол-4-карбоксамвд, т.пл. 67-68°С.
« Найдено, X: С 55,61; Н 4,03; N 17,64.
На йдено,%: С 60,71; Н 4 N 21,70.
Ci}H,,FN40.
C,5H,,F,N40.
Ц.ычислено.%: С 55,90; Н 4,07; N 17,38.
Пример 60. 5-Циано-1-Гзфтopмeтил)фeнилЗ-N-мeтил-N-мeтoк 1Н-пиразол-4-карбоксамид, т.пл. 23°C.
Найдено.%: С 52,11; Н 3,51; N 17,35.
Вычислено,%: С 51,86; Н 3,-42; N 17,28.
Пример 61. 5-Циано-1-(4фенил)-N,N-диметил-1Н-пиразол-4 боксамид, т.пл. 131-133°С.
С 48,79; Н
Найдено,%: N 17,51.
С,5Н,, BrN40.
Вычислено,%: С 48,92; Н 3,47; N 17,55.
П р и м е р 62. 5-Циано-1-(4фeнил)-N-мeтил-N-мeтoкcи-1H-пиpa 4-карбоксамид, т.пл. 147 С.
Найдено,%: С 46,42; Н 3,24; N 16,52.
. С.„Нн BrN4 iВычислено, %: С 46,59; Н 3,31 N 16,72.
П р и м е р 63. 5-Циано-1-(4фенил)-Н-метил-М-этил-1Н-пиразол карбоксамид, т.пл. 91-93 0.
Найдено,%: С 50,41; Н 3,76; N16,63.
С,дН,,ВгЫ40.
В;ычислено,%: С 50,47; Н 3,93; N 16,82.
П ри м е р 64. 5-Циано-1-(4-бром фенил)-N-диэтил-1H-пиpaзoл-4-кapбo- .кса мщ, т.пл. 108-110 С. .
Найдено,%; С 51,83; « 4,32; Ы 16,12.
C,5H,5BrN40.
Вычислено,%: С 51,89; Н 4,35; N 16,41.
П р и м е р 65. 5-Циано-1-(4-бром фенил)-N-циклoпpoпил-1Н-пнразол-4- карбоксамид, т.пл. 217-218 С.
Найдено,%: С 50,61; Н 3,35; N16,80.
C,4H,,BrN40.
Ьычислено,%: С 50,78; Н 3,35; N16,92.
П р и м е р 66. 5-Циано-1-(3-фтор метил)-N,N-димeтил-1Н-пиразол-4-кар...--. - . у . р,. ,- .. .п ....-
боксамид, т.пл. 132-133 С.
sбоксамид, т.пл. 132-133 С.
5
Q N 19,40.
На йдено,%: С 60,71; Н 4,07; N 21,70.
Ci}H,,FN40.
Вычислено,%: С 60,46; Н 4,29; 20 N 21,69.
П р и м е р 67. 5-Циано-1-СЗ-хлор- фенил)-N,N-диметил-1Н-пиразол-4-кар- боксамид, т.пл. 110-113°С.
Найдено,%: С 56,66; Н 3,72; 5 N 20,21.
C,,H,C1N40.
Вычислено,%: С 56,84; Н 4,04; N 20,39.
П р и м е р 68. 5-Циан.о-1-(3-хлор- 3Q фенил)-N-циклопропил-1Н-пиразол-4- карбоксамид, т.пл. 178-179 с.
Найдено,%: С 58,88; Н 3,84; N 19,68.
,, C1N40.
Вычислено,%: С 58,65; Н 3,87; N 19,54.
Пример 69. 5-Циано-1-(3-хлор- фенил)-N-мeтил-N-мeтoкcи-1Н-пиразол- 4-карбоксамид, т.пл. 164-166 С.
Найдено,%: С 53,79; Н 3,81;
N 19,40.
C,jH,,ClN40.
Вьгчислено,%: С 53,71; Н 3,81; N 19,27.
П р и м е р 70. 5-Циано-1-(3-пири- динил)-N,N-диэтил-1Н-пиразол-4-карбо- ксамид, т.пл. .
Найдено, %: С 62,37; Н 5,38; , N 26,21.
,sNs-0.
Вычислено,%: С 62,44; Н 5,61; N 26,00.
Пример 71. 5-Циано-1-(2-пири- динил)-N-мeтил-N-этил-1Н-пиразап-4- карбоксамид, т.пл. 106-108 С.
с 60,91; Н 4,98;
Вычислено,%: С 61,70; Н 5,13; N 27,A3..
Пример 72. 5-Циано-1-(2-пи- ридинил) -N-циклопропил-1 1-пиразол- 4-карбоксамид, т.пл. 22t-222°C.
Найдено,%: С 61,59; Н 4,48; fi 27,55. .; .
.) Вычислено, %: С 61,65; Н 4,38; Ц 27,65.
П р и м е р 73. 5-Циано-1-(2-пиП р и м е р 79. 5-Циано-1-(3,4- диxлopфeнил)-N,N-димeтил-1H-пиpaзoл- 4-карбоксамид, т.пл. 122-124°С. 5 Найдено,%: С 50,43; Н 3,06; N 18,08.
C,,,HioCl N40.
Вычислено,%: С 50„51; Н 3,26; N 18,12. 10 П р и м е р 80. 5--Циано-1-(3,4дихлорфеншт)-N-циклопропил-1Н-пира, р ,. -. Н ,... .ow , ч. 11 зол-4-карбоксамид, т.пл. 194-19б с.
р;идинил)-Н-метил-Н-метокси-1Н-пира-Найдено,%: С. 52,57; Н 3,13;
з1ол-4-карбоксамид, т.пл. 113-116 С.N 17 50.
5С,4Н„С1гК40.
N 17,44.
П р и м е р 81. 5-Циано-1-(4-фтор- фенил;-N,N-диметил-1Н-пиразол-4-кар..-. л
Найдено,%: С 55,81; Н 4,01; 27,03.
С,Н„ NyO-j..
Вычислено,% С 56,03; Н 4,31; NJ 27,22.
I , -фенил -IN, и-диметил-1 н-пиразол Пример 74. 5- Циано-1-(2-пи-20 боксамид, т.пл. 118-120 с.
pИдинил)-N.N-димeтил-1H-пиpaзoл-4-Найдено,,: С 60,24; К 4,06,
кkDбDкcaмип. т.пл. 136-138 С. м oi лскЬрбоксамид, т.пл. 136-138°С.
1 Найдено,%: С 59,55;. Н 4,87; N128,77.
i С,, Н,. .
(2 «
Вычислено,%: С 59,75; Н 4,56; Nl29,05.
N 21,66;
CijHuFN O.
5 Вычислено,%: С 60,46; Н 4,29; N 21,69.
П р и м е р 82. 5- Циано-1-(2-хино.:j,uj.
: П р и-м е р 75. 1-{ 5-Циано-1-(2-линил)-N,N-диметил-1Н-пиразол-4-карп идинил)-1Н-пиразол-4-ил карбонил боксамид, т.пл. 167-168°Г.
i.1 IА 4 С Jt 4 П / . . - .™.,,, i
30
морфолин, Т.пл, 115-118 С.
Найдено,%: С 59,24; Н 4,79; N24,97.
С,4Н,Ы40г.
Вычислено,%: С Н 4,63; N 24,72.
Пример 76. 5-Циано-1-фенил- H- мeтил-N-этил-1H -пиpaзoл-4-кapбo- кс;.амид т.пл,. 79°С.
Найдено,%: С 65,85; Н 5,31; гГ22,80
Ci4H,,N40,Вычислено,%: С 66,13; Н 5,55; N 22,03,
35
40
Найдено,%: С 66,30; Н 4,58; N 24,03.
C..
Вьмислено,%: С 65,97; Н 4,50; N 24,04.
П р и м е р 83. 5- Диано-1-фенил- N,N-диметил-1Н-пиразол-4-карбокса- 1чид, т.пл. 109-1 .
Найдено,%: С 64,87; Н 5,03; N 23,41.
C,,H,2N40.
Вычислено,%: С 64,99; Н 5,03; ,32.
П р и м е р 84. 5- иано-1-фенил- N-(1-метилэтил i) -1 Н-пиразол-4-карбоП р и м е р 77. 5-Циано-1-(4-метoкcифeнил)-N5N-димeтил-1H-пиpaзoл- ксамид, т.пл. 208-209 с„ 4-карб6ксамид, т.пл. 113-114°С.
Найдено,%: С 62,46; Н-5,27; N 20,92. .
CuH,4N40,t.
Вычислено,%s С 62,21; Н 5,22; К 20,73.
П Р и м е р 78. 5-Циано-1-(4-ме- токсифенил)-N-этил-1Н-пиразол-4-кар
. ft
боксамид, т.пл. 121-123 с.
Найдено,%; С 63,32; Н 5,77; М 19,65,
C,5H,6N404.
Вычислено, %s С 63,37; Н 5,67; N 19,71.
Найдено,%: С 65,88,; Н 5,39; N 21,90.
C,.
..Вычислено,%; С 65/13} Н 5,55;
N 22,03.
П.р и м е р 85. 5-Циано-1-фенил- 1Н-пиразол-4-карбоксамид, т.пл. 178- 179.
Найдено,%: С 62,13; Н 3,76| N 26,36.
.
Вь1числено,%: С 62,26; Н 3,80; N 26J40.
Найдено,,: С 60,24; К 4,06,
м oi лсN 21,66;
CijHuFN O.
Вычислено,%: С 60,46; Н 4,29; N 21,69.
П р и м е р 82. 5- Циано-1-(2-хинолинил)-N,N-диметил-1Н-пиразол-4-карбоксамид, т.пл. 167-168°Г.
. . - .™.,,, i
Найдено,%: С 66,30; Н 4,58; N 24,03.
C..
Вьмислено,%: С 65,97; Н 4,50; N 24,04.
П р и м е р 83. 5- Диано-1-фенил- N,N-диметил-1Н-пиразол-4-карбокса- 1чид, т.пл. 109-1 .
Найдено,%: С 64,87; Н 5,03; N 23,41.
C,,H,2N40.
Вычислено,%: С 64,99; Н 5,03; ,32.
П р и м е р 84. 5- иано-1-фенил- N-(1-метилэтил i) -1 Н-пиразол-4-карбоксамид, т.пл. 208-209 с„
Найдено,%: С 65,88,; Н 5,39; N 21,90.
C,.
Вычислено,%; С 65/13} Н 5,55;
N 22,03.
П.р и м е р 85. 5-Циано-1-фенил- 1Н-пиразол-4-карбоксамид, т.пл. 178- 179.
Найдено,%: С 62,13; Н 3,76| N 26,36.
.
Вь1числено,%: С 62,26; Н 3,80; N 26J40.
П р и м е р 86. 5-Циано-1-фенил- К-метокси-1Н-пиразол-А-карбоксамид т.пл. 163-16А°С.
Найдено,%: С 59,63; Н 3,92; N 22,93.
CnHioN O.
Вычислено,%: С 59,50; Н 4,16; N 23,13.
Прим ер 87. 5-Циано-1-фенил- N-мeтил-N-мeтoкcи-1К-пиразол-4-карбоксамид, т.пл. 129°С.
Найдено, %: С 61,06; И 4,57; N 21,68.
C,,H,2N40.
Вычислено,%: С 60,93; Н 4,72; N 21,86.
П р и м е р 88, 5-Циано-1-фенш1- N,N-диэтил-1Н-пиразол-4-карбоксамид масло.
Найдено,%: С 66,88; Н 5,96; N 20,63.
C,,H,6N40.
Вычислено,%: С 67,15; Н 6,01;
N 20,88.
I
П р и м е р 89. 1-Г(5-Циано-1-фенил-1Н-пиразол-4-ил) карбонил -пирро лидин, т.пл. 139-140 С.
Найдено, %: С 67,87; Н 5,52; N 21,07.
С,5 Н,4 N40.
Вычислено,%: С 67,65; Н 5,30; N 21,04.;
П р и м е р 90. 5-Циано-1-фенил- N,N-дипропил-1Н-пиразол-4-карбокса- мид, масло.
Найдено,%: С 68,70; Н 6,57; N 18,89.
.
Вычислено,%: С 68,90; Н 6,80; N 18,90.
П р и м е р 91. 5-Циано-1-(4-ме- тилфенил)-N,N-диметил-1Н-пиразол-4- карбоксамид, т.пл. 149-150 С.
Найдено, %: С 65,88; Н 5,28; N 21,82.
С44Н„ 40Вычислено, %: С 66,13; Н 5,55. N 22,03.
Пример 92. 5-Циано-1-(4-фто фенил) -Н-циклопропк11-1 Н-пиразол-4- карбоксамид, т.пл. 185-187 С.
Найдено,%: С 61,95; Н 3,83; N 20,54,
С,4Н„ FN40.
Вычислено,%: С 62,22; Н 4,10; М 20,73.
П р и м е р 93. З-Циано-1-фенил- N-мeтил-N-2-пpoпeнил-1Н-пиразол-4- карбоксамид, т.пл. 47-50 С. Найдено,%: С 67,83; Н 5,09;
N 20,76.
C,,H,4N40.
Вычислено,%: С 67,65; Н 5,30; N 21,04.
Пример 94. 5-Циано-1-фенил- Н-метил-М-циклопропил-1 Н-пиразол-- - карбоксамид, т.пл. 79-81 С.
Найдено,%: С 67,44; Н 5,13; N 21 ,0(Г. ,4N40.
Вычислено,%: С 67,65; Н 5,30; N 21,04.
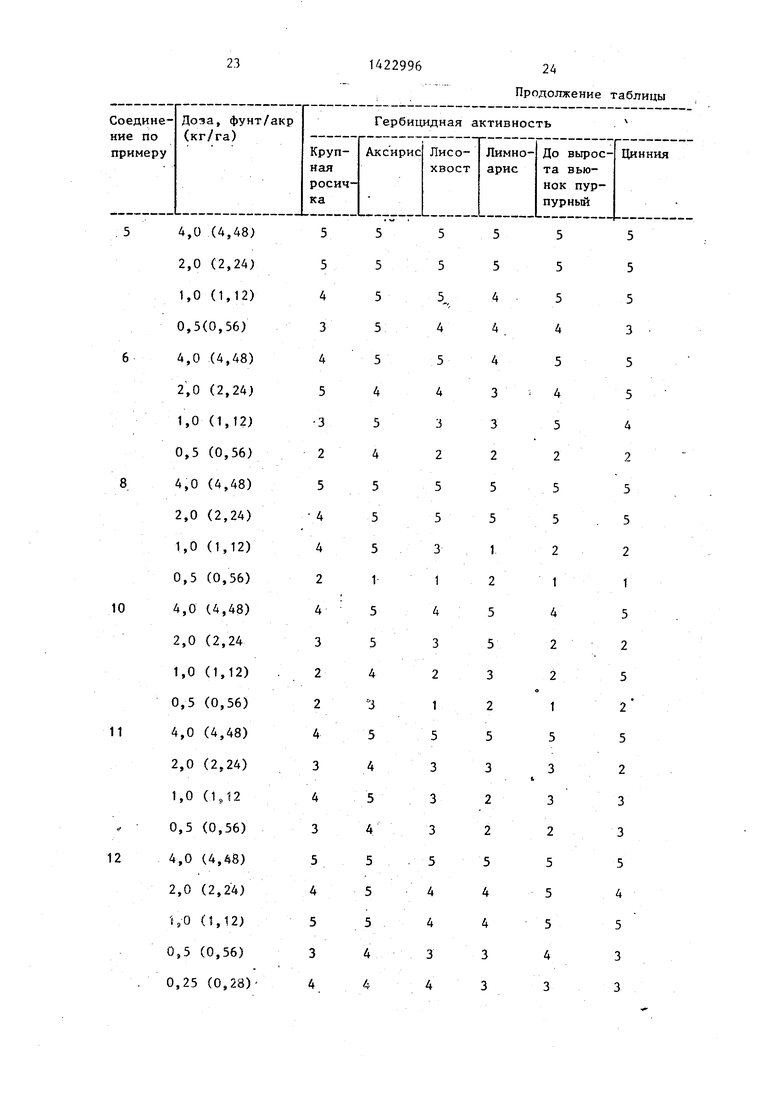
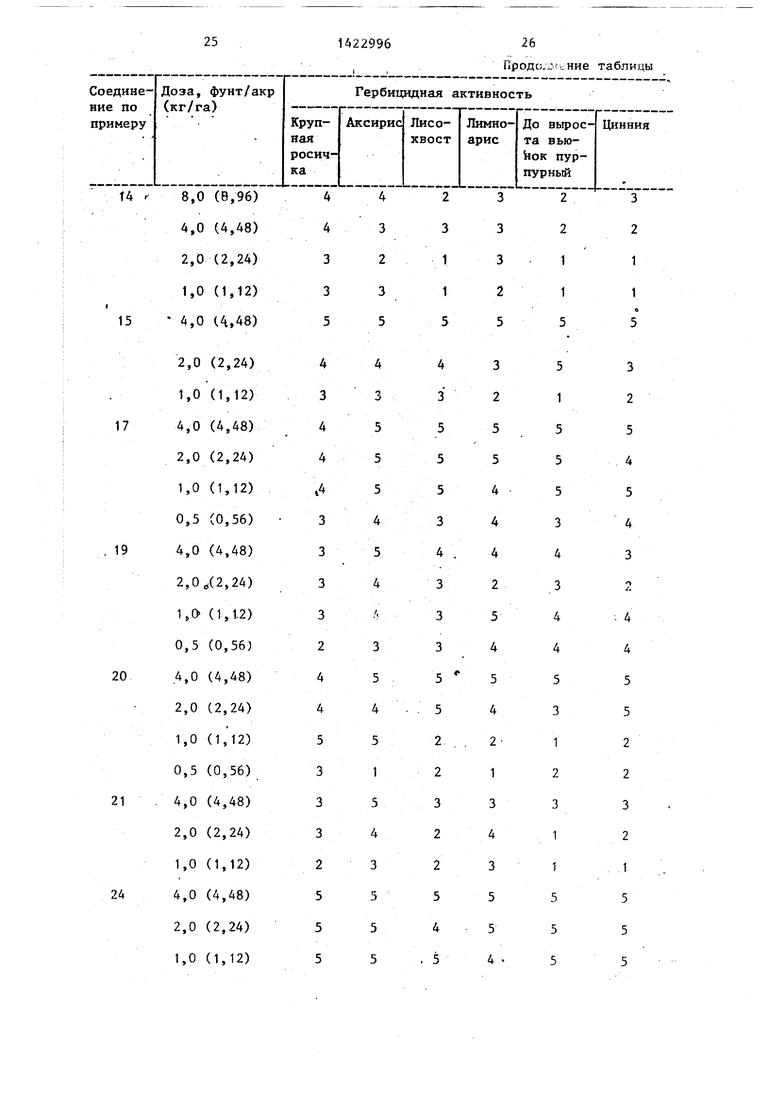
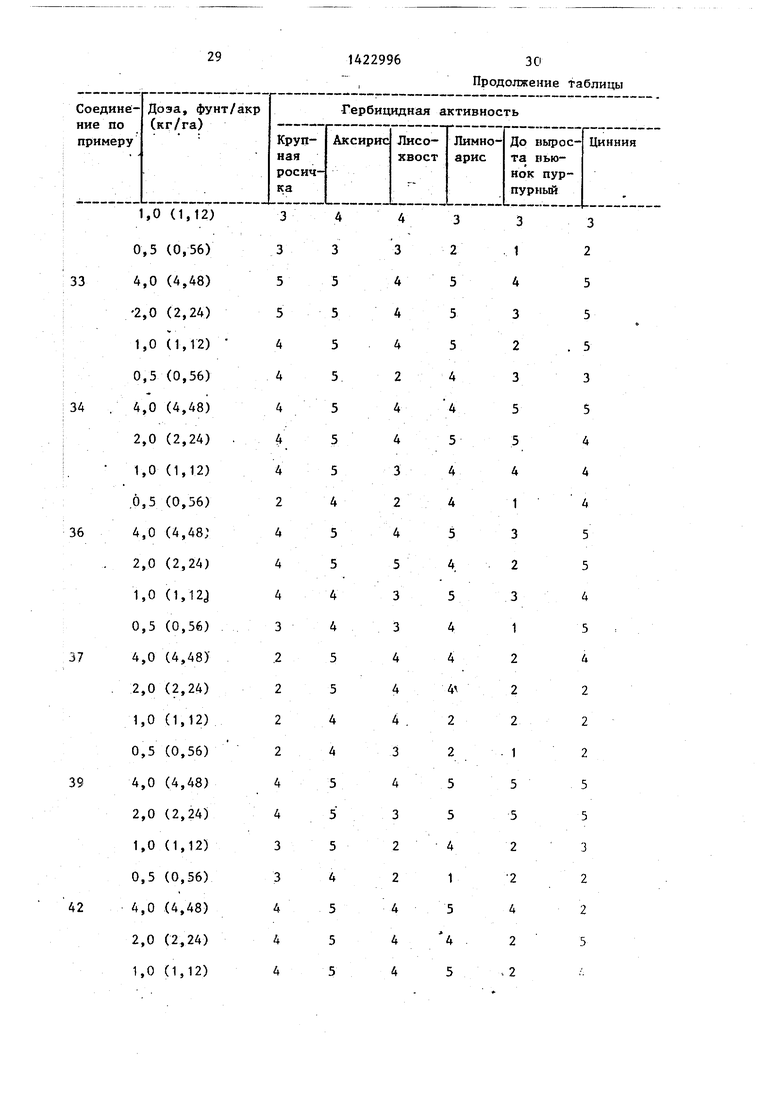
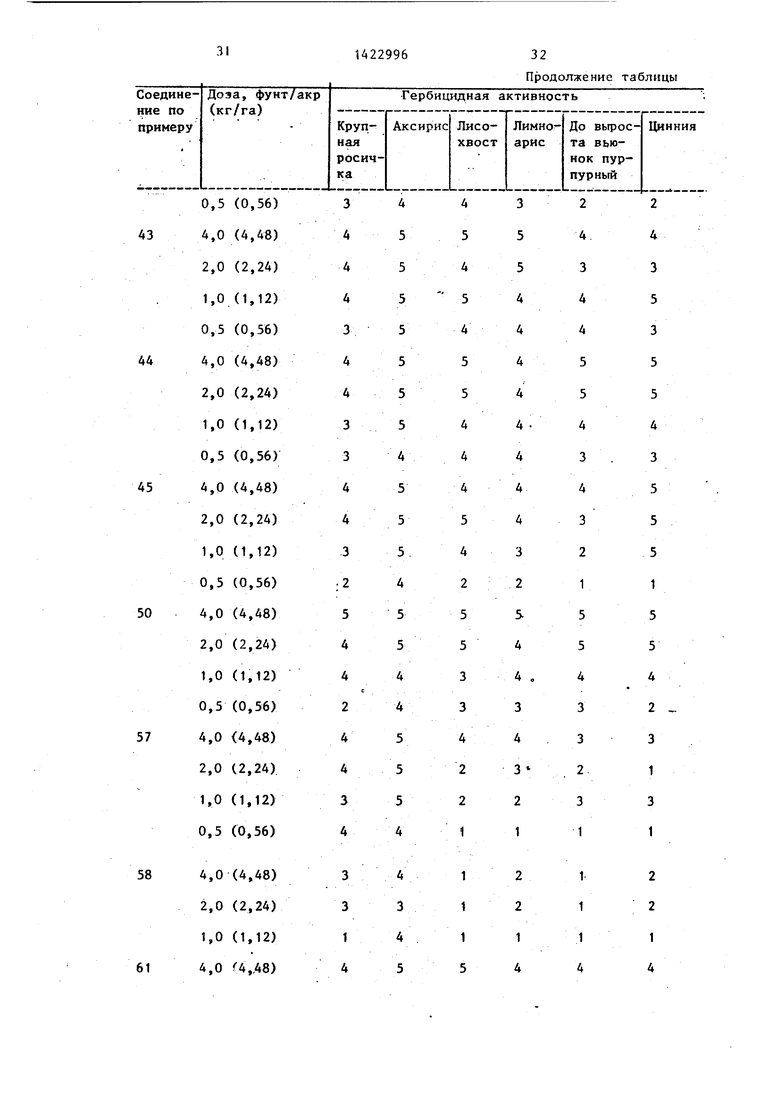
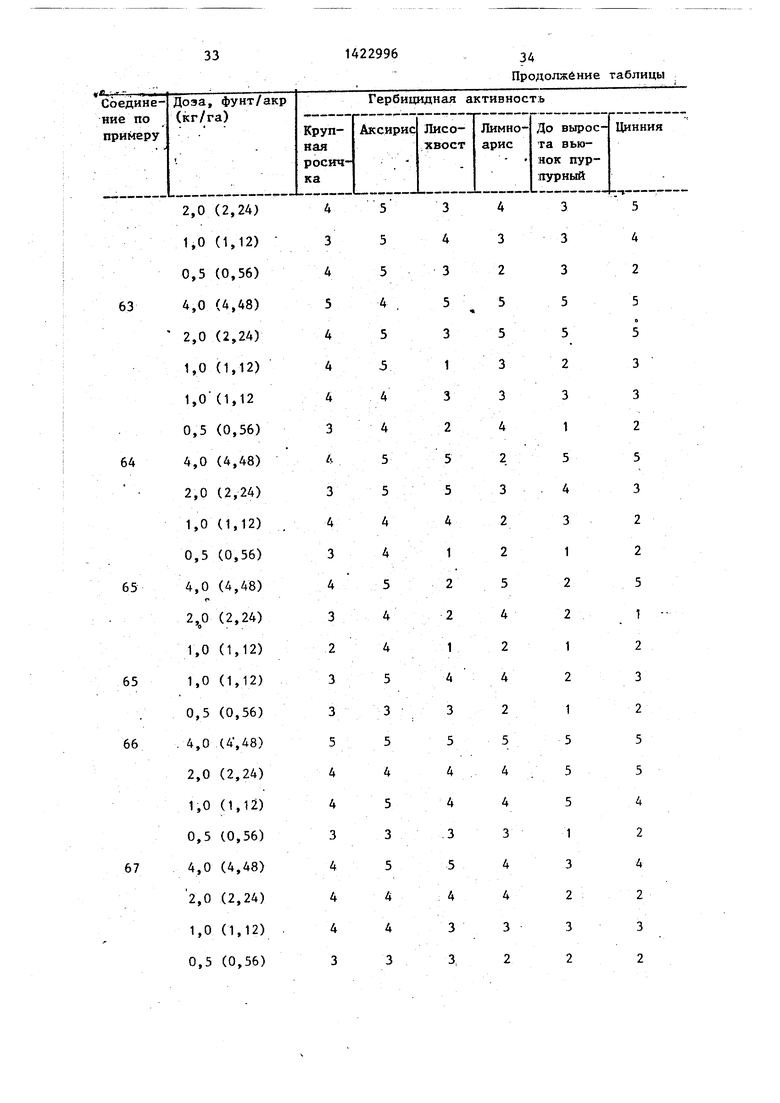
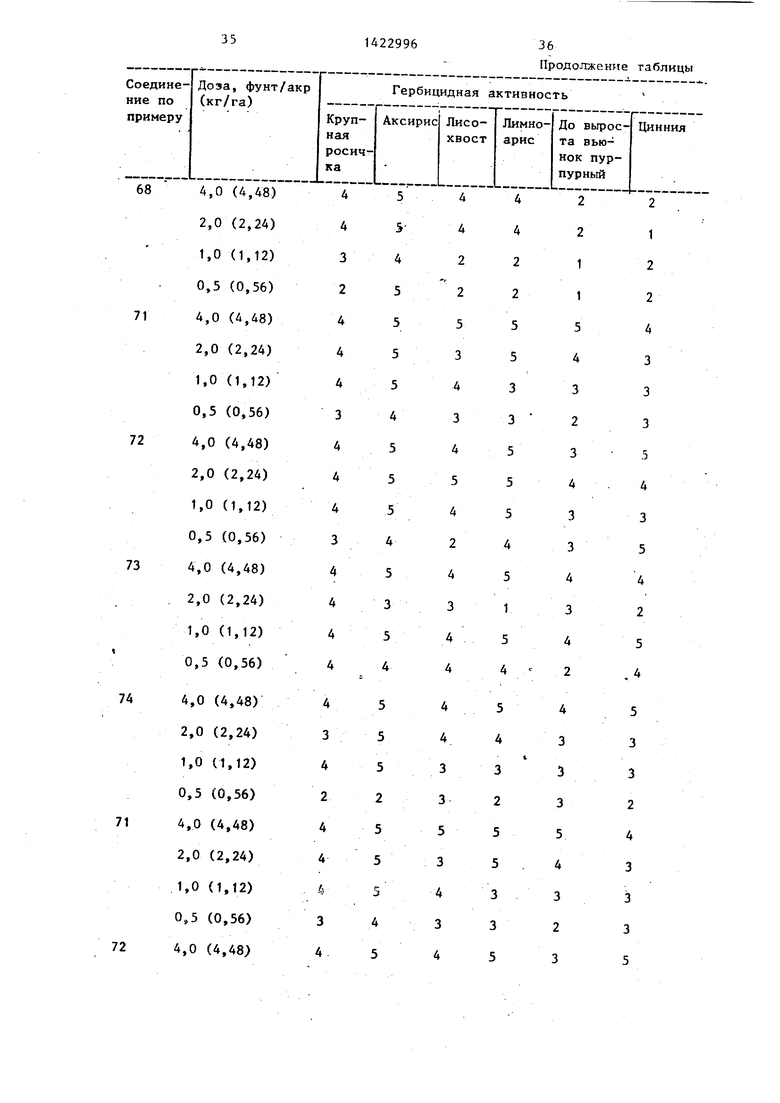
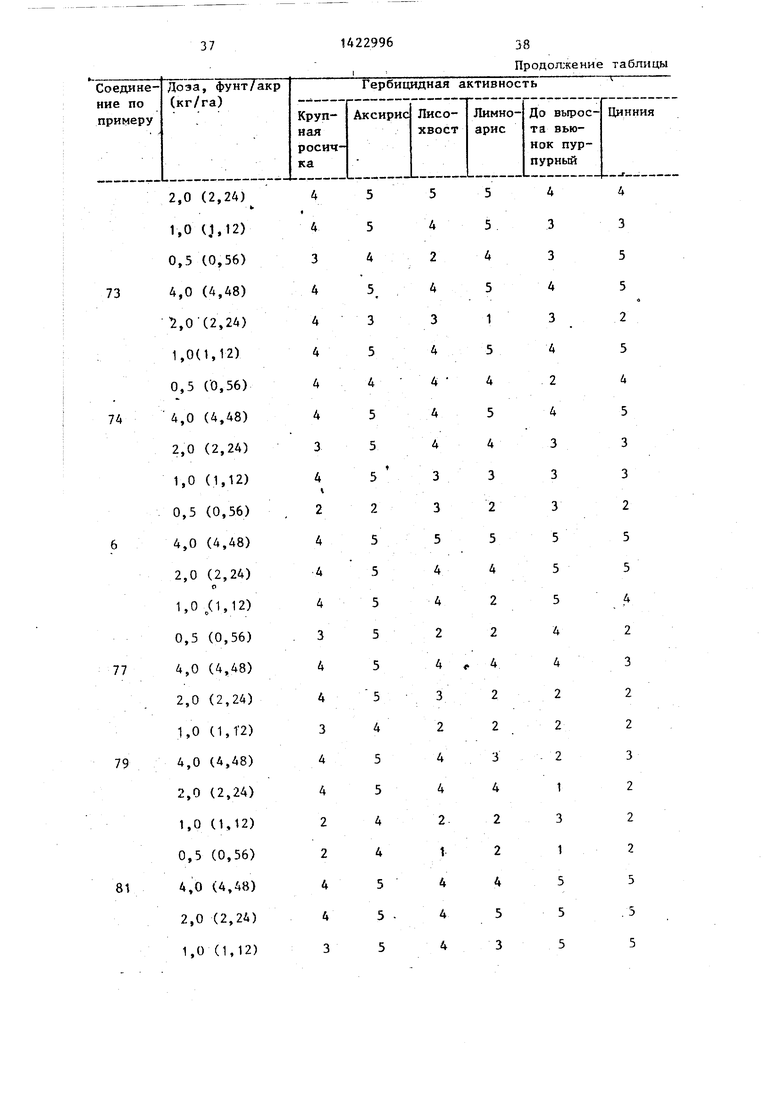
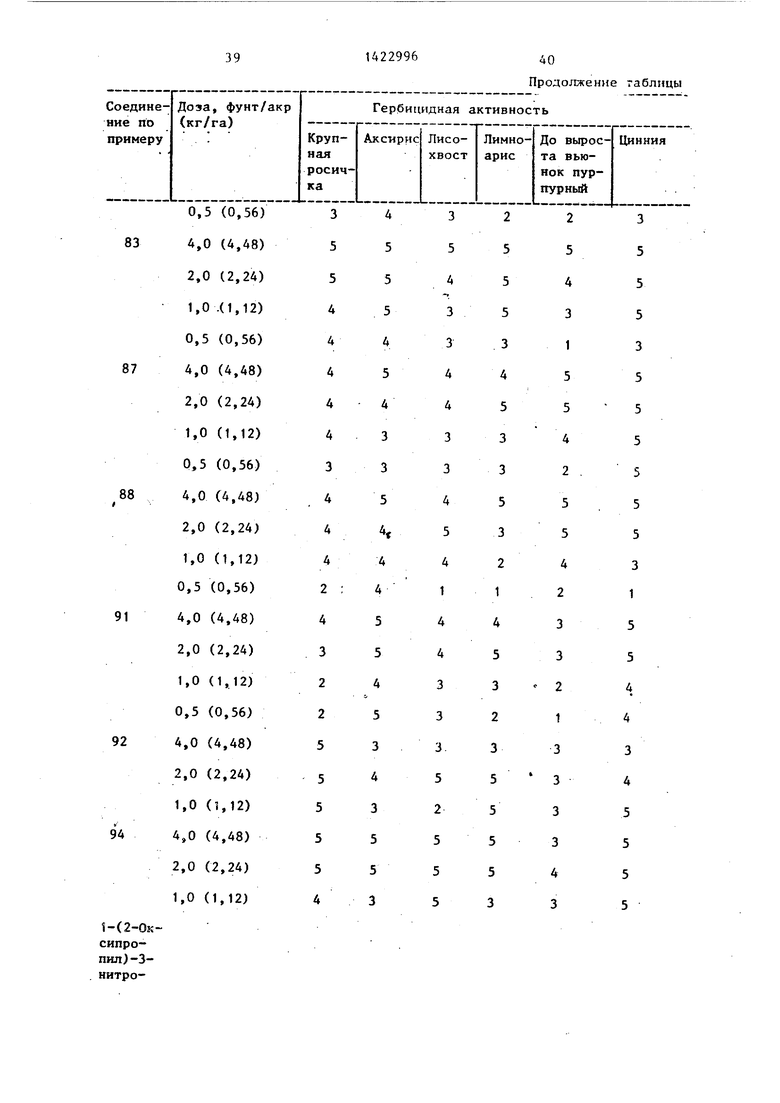
Гербицидное действие соединений. Готовят испытательные растворы для применения путем растворения соответствующего соединения в растворителе, содержащем Токсимул R и Ток- симул S (смеси анионньпс и неионных поверхностно-активньк пгентов фирмы Степан компани, Нортфилд, шт. Иллинойс), и смесь ацетона с этанолом 1:1 (об./об.). Раствор разбавляют деионизованной водой и применяют до всхода. Степень гербицидной активности определяют путем распределения обработанных растений на категории от 1 до 5(1- отсутствие повреждений, 2 - легкие повреждения, 3 - умеренные повреждения, 4 - серьезные повреждения, 5 - растения не дали всхо- да) .
Более низкие концентрации испытательных соединений получают путем последовательного растворения описанной рецептуры в смеси поверхностно- активного агента, содержащего растворитель и деионизованную воду.
В таблице приведены данные гербицидной активности соединений формулы (I) в сравнении с известным соеди нением.
Как видно из таблицы, соединения (l) превосходят известньп гербицид в отношении любого из сорняков. ТаКИМ образом, соединения (I) обладают высокой гербицидной активностью и могут быть использованы в сельском хозяйстве.
Формула изобретения
Способ получения производных пиразола общей формулы
H,l)J-Tr- N
Чг
N
R)- С -С -алкил или группа формул
4(R.)
m
m или
Rj и Rj- каждый независимо водород, С,-С -алкил, ,-алкенил,
Сз С -циклоалкил или ,
алкокси.
RJ и RJ взятые вместе с атомом азота, KJ которому они присоединены, обра- уют пиперидиновое, морфолиновое или Нирролидиновое кольцо;
0
R - каждый независимо галоген, С -С4 алкил, С(-С4 алкокси, С4-С4-галоидалкил, циано; m O.iJ при условии, что, когда R - С -С4-алкил, этот заместитель существует при ином, чем 2 или 6, положении фенилового кольца, и .когда R - Ci-Cj-алкокси, R3 иной, чем С,-С,-алкокси,
отличающийся тем, что
пиразол общей формулы
R-N-j- GN
OB 5
где R4 имеет указанные значения;
RJ - водород или низший алкил, 0 подвергают взаимодействию с амином, общей формулы
HNRgR где R, ,2. и R j имеют указанные значе™
ния,
5 с выделением целевого продукта в свободном виде.
5
Продолжение таблицы
25
1А22996
26
Пр од CL r-f;.: НИ е т а бл и Х1Ы
27
0,5(0,56) 4,-О-(4,48)
2,0(2,24)
1,0(1,12)
0,5(0,56)
4,0(4,48)
2,0(2,24)
1,0(1,12)
0,5(0,56)
4,0(4,48)
2,0(2,24)
1,0(1,12)
4,0(4,48)
2,0(2,24)
1,0(1,12)
0,5(0,56)
4,0(4,48)
2,0(2,24)
1,0(1,12)
4,0(4,48)
2,0(2,24)
1,0(t,12)
0,5(0,56)
4,0(4,48)
2,0(2,24
4 4 5 4 2 3 3 2 2 5 4 3 4 4 3 1 3 3 3 4 4 4 2 5 4
1422996
28 Продолжение таблицы
4 4 4 4 3 4 4 3 1 5 4 4 4 4 4 3 3 3 2 4 4 3 2 4 3
4 4 5 5 4 3 4 5 1 4 4 2 4 А 3 3 4 4 3 4 4 3 3 5 4
5 4 4 3 3 4 2 1 1 4 4 4 1 4 2 2 3 3 2 4 3 4 3 5 4
5 5 5 4 3 4 5 5 1 3 2 2 5 2 4 1 3 3 3 4 4 3 2 5 5
29
1422996
3
4
6
7
9
2
1,0 (1,12)
0,5 (0,56) 4,0 (4,48) -2,0 (2,24) 1,0 (1,12) 0,5 (0,56) 4,0 (4,48) 2,0 (2,24) 1,0 (1,12) ,6,5 (0,56) 4,0 (4,48; 2,0 (2,24) 1,0 (1,12j 0,5 (0,56) 4,0 (4,48) 2,0 (2,24) 1,0 (1,12) 0,5 (0,56) 4,0 (4,48) 2,0 (2,24) 1,0 (1,12) 0,5 (0,56) 4,0 (4,48) 2,0 (2,24) 1,0 (1,12)
3 3 5 5 4 4 4 4 4 2 4 4 4 3 .2 2 2 2 4 4 3 3 4 4 4
4
3
5
5
5
5
5
5
5
4
5
5
4
4
5
5
4
4
5
5
5
4
5
5
5
30 Продолжение таблицы
3
2 5 5 5 4 4 5- 4 4 5
-i. 5 4 4 4 2 2 5 5 4 1 5
Ч 5
3
1
4
3
2
3
5
5
4
1
3
2
3
1
2
2
2
. 1 5 5 2 2 4 2
. 2
3 2
5 5
. 5 3 5 4 4 4 5 5 4 5 k 2 2 2
. 5 5 3 2 2 5
31
0,5(0,56)
4,0(4,48)
2,0(2,24)
1,0(1,12)
0,5(0,56)
4,0(4,48)
2,0(2,24)
1,0(1,12)
0,5(0,56)
4,0(4,48)
2,0(2,24)
1,0(1,12)
0,5(0,56)
4,0(4,48)
2,0(2,24)
1,0(1,12)
0,5(0,56)
4,,48)
2,0(2,24)
1,0(1,12)
0,5(0,56)
4,0(4,48)
2,0(2,24)
1,0(1,12)
4,,,48)
3 4 4 4 3 4 4 3 3 4 4 3
;2
5 4 4
с
2 4 4 3 4
3 3 1 4
1А22996
32 Продолжение таблицы
4 5 4 5 4 5 5 4 4 4 5 4 2 5 5 3 3 4 2 2 1
1 1 1 5
3
5
5
4
4
4
4
4
4
4
3
2
S
4
4 ,
3
4
3
2
1
2 2 1 4
2 4 3 4 4 5 5 4 3 4 3 2 1 5 5 4 3 3 2 3 1
1 1 1 4
2
4
3
5
3
5
5
4
3
5
5
5
1
5
5
4
2
3
1
3
1
2 2 1
4
33
1422996
ЗА Продолжение таблицы
Продол;кенне таблицы
39
83
87
8
1
2
4
0,5 (0,56) А,О (4,А8) 2,0 (2,24) 1,0 .(1,12) 0,5 (0,56) 4,0 (4,48) 2,0 (2,24) 1,0 (1,12) 0,5 (0,56) 4,0 (4,48) 2,0 (2,24) 1,0 (1,12) 0,5 (0,56) 4,0 (4,48) 2,0 (2,24) 1,0 (1,12) 0,5 (0,56) 4,0 (4,48) 2,0 (2,24) 1,0 (1,12) 4,0 (4,48) 2,0 (2,24) 1,0 (1,12)
3
5 5 4 4 4 4 4 3 4 4
4
2 :
4
3
2
2
5
5 5 5 5 4
1-(2-Ок- сипро- пш1)-3- нитро1422996
iO Продолжение таблицы
3 5 4 3 3 4 4 3 3 4 5 4 1
4
4
3
3
5
2
5
5
5
2 5 5 5 3 4 5 3 3 5 3 2 1
4
5
3
2
3
5
5
5
5
3
2 5 4 3 1
5 5 4 2 5 5 4 2 3 3
2 1 3
3 3 3 4 3
3 5 5 5 3 5 5 5 5 5 5
3 1
5 5
4 4 3 4 5 5 5 5
41
1422996
4,0 (4,48) 2,0 (2,24) (1,12)
2 2 2
.42 Продолжение таблицы
2 2 2
2 2 2
1 2 2
2 2 2
| Бюлер К., Пирсон Д | |||
| Органические синтезы | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| - М.: Мир, 1973. | |||
Авторы
Даты
1988-09-07—Публикация
1984-11-06—Подача